吸着剤と逆作用薬とを含有する不正使用防止投与剤型
吸着剤及び逆作用薬、例えばオピオイドアンタゴニスト、を含有する医薬組成物及び投与剤型。1つの実施形態では、逆作用薬の少なくとも一部が吸着剤材料の表面上又はミクロ細孔構造内に存在する。吸着剤と逆作用薬とを含有する医薬組成物及び投与剤型は、活性薬剤、例えばオピオイド、を含有する投与剤型の不正使用、乱用、誤用又は転用を防止する又は阻止するために有用である。本発明はまた、そのような投与剤型で患者を治療するための方法、並びにそのような投与剤型及び患者を治療するための投与剤型の使用法を指示する説明書を含むキットに関する。本発明はさらに、そのような医薬組成物及び投与剤型を製造するための方法に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本出願は、その開示全体が全ての目的に関して明白に参照により本明細書に組み込まれる、2004年3月30日出願の米国特許仮出願第60/558,301号の優先権を主張する。
【0002】
本発明は、活性薬剤、例えばオピオイド、を含有する投与剤型の不正使用、乱用、誤用又は転用を防止する又は阻止するために有用な、吸着剤及び逆作用薬、例えばオピオイドアンタゴニスト、を含有する医薬組成物及び投与剤型に関する。本発明はまた、そのような投与剤型で患者を治療するための方法、並びにそのような剤型と患者を治療するために前記投与剤型を使用するための説明書とを含むキットに関する。本発明はさらに、そのような医薬組成物及び投与剤型を製造するための方法に関する。
【背景技術】
【0003】
毒物又は薬剤の意図されたものでない又は不法な使用の治療又は防止に多大の努力が注がれてきた。例えば過剰の薬剤又は毒物を摂取した患者のための1つの治療は、吸着剤、例えば活性炭の投与を含む(Remington's: The Science and Practice of Pharmacy 1238 (20th ed. 2000)参照)。活性炭は、薬剤又は毒物の一部を吸着し、それが循環系に入るのを防ぐことが意図されている。
【0004】
Proctorらへの米国特許第4,594,249号は、アルコール摂取の直前、摂取中又は摂取直後のアルコール消費者への活性炭の投与による、アルコール飲料の摂取の後作用を軽減するための方法を開示する。
【0005】
ニシムラ(Nishimura)への米国特許第4,761,284号は、その開示によれば、医薬組成物の崩壊を伴わずに患者の胃腸管において外因性又は内因性毒素を吸着するために有用な活性炭の球状粒子を含有する医薬組成物を開示する。
【0006】
米国特許出願公開第2002/0155103 A1号は、その開示によれば、アルコール摂取に関連する後作用の発現を予防する又は遅延させるために有用な活性炭と石灰石を含有する組成物を開示する。
【0007】
また、投与剤型、例えばオピオイド鎮痛薬剤型、の不正使用防止性を高めるための試みが当技術分野において為されてきた。不正使用防止オピオイド投与剤型の開発へのこれまでのアプローチには、オピオイドアゴニストをオピオイドアンタゴニストと組み合わせることが含まれていた。そのような組合せの特定例は、メタドンとナロキソン(Pachterらへの米国特許第3,773,955号);メタドール又はアセチルメタドールとナロキソン(Pachterらへの米国特許第3,966,940号);オキシコドンとナロキソン(Gordonらへの米国特許第4,457,933号);及びブプレノルフィンとナロキソン(Lewisらへの米国特許第4,582,835号)を含有する組成物を含む。
【0008】
Palermoらへの米国特許第6,228,863号は、アゴニストを単離するために少なくとも2つの分離工程を必要とする、オピオイドアゴニストとオピオイドアンタゴニストを組み合わせた経口投与剤型を開示する。
【0009】
Al-Razzakらへの米国特許第5,610,193号は、製薬上許容し得るHIVプロテアーゼ阻害剤と製薬上許容し得る吸着剤に吸着された溶媒を含有する医薬組成物を開示する。この参考文献は、前記組成物が、水に難溶性である活性化合物の経口バイオアベイラビリティーの改善を提供すると主張する。
【0010】
Oshlackらへの米国特許第6,696,088 B2号及び米国特許出願公開第2003/00073717 A1号、同第2003/0004177 A1号及び同第2003/0065002 A1号は、放出可能形態のオピオイドアゴニストと、投与剤型を無傷投与したときには実質的に放出されないオピオイドアンタゴニストを含有する経口投与剤型を開示する。
【発明の開示】
【発明が解決しようとする課題】
【0011】
改善された不正使用防止投与剤型及びそれらの製造のための改善された手法が、現在も当技術分野において求められている。
【課題を解決するための手段】
【0012】
本発明は、吸着剤と逆作用薬とを含有する医薬組成物及び投与剤型に関する。本発明はまた、そのような組成物及び投与剤型を製造するための方法に関する。本発明はさらに、そのような医薬組成物又は投与剤型で患者を治療するための方法、並びにそのような医薬組成物又は投与剤型と患者を治療するための前記組成物又は投与剤型の使用法を指示する説明書とを含むキットに関する。本発明に従った投与剤型は、カプセル又は錠剤、直腸坐剤及び膣坐剤を含むがこれらに限定されない、経口投与剤型を含むが、これらに限定されない。ある実施形態では、投与剤型は複数の粒子を含有し得る。
【0013】
1つの実施形態では、本発明は、吸着剤と逆作用薬を含有する投与剤型に関する。もう1つの実施形態では、本発明は、作用薬、吸着剤及び逆作用薬を含有する投与剤型に関する。
【0014】
もう1つの実施形態では、本発明は、作用薬を含む複数の第一粒子;及び吸着剤と逆作用薬とを含む複数の第二粒子を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型に関する。1つの実施形態では、本発明は、オピオイドアゴニストを含む複数の第一粒子;及び吸着剤とオピオイドアンタゴニストとを含む複数の第二粒子を含有し、前記第一粒子が、患者への経口投与時にオピオイドアゴニストの制御放出を提供する投与剤型に関する。
【0015】
もう1つの実施形態では、本発明は、吸着剤と逆作用薬とを含むコア;及び作用薬を含むシェルを含有し、前記シェルが前記コアを少なくとも部分的に覆う又は取り囲む投与剤型に関する。
【0016】
1つの実施形態では、前記逆作用薬の少なくとも一部が前記吸着剤の少なくとも一部に吸着されている。もう1つの実施形態では、前記逆作用薬の少なくとも大部分、すなわち50重量%が前記吸着剤の少なくとも一部に吸着されている。さらなる実施形態では、前記逆作用薬の基本的に全部が前記吸着剤の少なくとも一部に吸着されている。
【0017】
本発明の組成物及び投与剤型は、作用薬及び/又は逆作用薬の制御放出、即時放出又は遅延放出を提供することができる。
【0018】
本発明はまた、吸着剤と逆作用薬とを含有する投与剤型を製造するための方法に関する。1つの実施形態では、本発明は、吸着剤を提供すること;逆作用薬を含有する液体を提供すること;前記吸着剤を、逆作用薬を含有する前記液体と、逆作用薬の少なくとも一部が吸着剤に吸着するのに十分な時間接触させること;前記吸着剤を液相から分離すること;及び場合により、前記吸着剤を洗浄すること、を含む、投与剤型を製造するための方法に関する。
【0019】
もう1つの実施形態では、本発明は、吸着剤を提供すること;逆作用薬を含有する液体を提供すること;前記吸着剤を流動床に添加すること;前記吸着剤を流動化すること;前記液体を流動化した吸着剤に噴霧すること;及び場合により、前記吸着剤を乾燥すること、
を含む、投与剤型を製造するための方法に関する。
【0020】
本発明はまた、吸着剤と逆作用薬とを含有する本発明の投与剤型を患者に投与することを含む、病気又はその症状を治療する方法に関する。本発明の1つの実施形態では、疼痛を有する患者を治療する。
【0021】
本発明はまた、本発明の投与剤型をその必要のある患者に投与することを含む、疼痛を治療するための投与剤型の乱用、誤用又は転用を低減するための方法に関する。
【0022】
さらにもう1つの実施形態では、本発明は、少なくとも1つの本発明の投与剤型及び患者を治療するための投与剤型の使用法を指示する説明書のセットを含む、患者を治療するためのキットに関する。本発明の1つの実施形態では、キットは患者の疼痛を治療することを目的とする。
【0023】
本発明は、本発明の非制限的な実施形態の例示を意図する、以下の詳細な説明及び実施例を参照することにより、さらに十分に理解することができる。
【発明を実施するための最良の形態】
【0024】
5.1
定義
本明細書における何らかの薬剤、例えば作用薬、逆作用薬、オピオイドアゴニスト又はオピオイドアンタゴニストへの言及は、異なる規定がない限り、そのような薬剤の製薬上許容し得る形態、例えば遊離形態、製薬上許容し得る塩形態、製薬上許容し得る塩基形態、製薬上許容し得る水和物、製薬上許容し得る溶媒和物、立体異性体、光学異性体;並びにそのような薬剤のプロドラッグ及びそのような薬剤の製薬活性類似体、及び前記のいずれか2つ以上の混合物を包含する。
【0025】
本明細書で使用する「製薬上許容し得る塩」という語句は、作用薬又は逆作用薬の、酸性及び塩基性基、例えば窒素基から形成される塩であり得る。そのような塩の例は、硫酸塩、クエン酸塩、酢酸塩、シュウ酸塩、塩化物、臭化物、ヨウ化物、硝酸塩、重硫酸塩、リン酸塩、酸性リン酸塩、イソニコチン酸塩、乳酸塩、サリチル酸塩、酸性クエン酸塩、酒石酸塩、オレイン酸塩、タンニン酸塩、パントテン酸塩、重酒石酸塩、アスコルビン酸塩、コハク酸塩、マレイン酸塩、ゲンチジン酸塩、フマル酸塩、グルコン酸塩、グルカロン酸塩、サッカリン酸塩、ギ酸塩、安息香酸塩、グルタミン酸塩、メタンスルホン酸塩、エタンスルホン酸塩、ベンゼンスルホン酸塩、p−トルエンスルホン酸塩、グルビオナート及びパルモエート(すなわち1,1’−メチレン−ビス−(2−ヒドロキシ−3−ナフトエート))塩を含むが、これらに限定されない。「製薬上許容し得る塩」という用語は、選択的に、酸性官能基、例えばカルボン酸又はスルホン酸官能基を有する作用薬又は逆作用薬と、製薬上許容し得る無機又は有機塩基から生成される塩であり得る。そのような塩基の例は、アルカリ金属、例えばナトリウム、カリウム及びリチウムの水酸化物;アルカリ土類金属、例えばカルシウム及びマグネシウムの水酸化物;他の金属、例えばアルミニウム及び亜鉛の水酸化物;アンモニア、及び有機アミン、例えば不飽和又はヒドロキシ置換モノ−、ジ−又はトリアルキルアミン;ジシクロヘキシルアミン;トリブチルアミン;ピリジン;N−メチルアミン、N−エチルアミン;ジエチルアミン;トリエチルアミン;モノ−、ビス−又はトリス−(2−ヒドロキシ−低級アルキルアミン)、例えばモノ−、ビス−又はトリス−(2−ヒドロキシエチルアミン)、2−ヒドロキシ−tert−ブチルアミン、又はトリス−(ヒドロキシメチル)メチルアミン、N,N,−ジ−低級アルキル−N−(ヒドロキシ低級アルキル)−アミン、例えばN,N−ジメチル−N−(2−ヒドロキシエチル)アミン、又はトリ−(2−ヒドロキシエチル)アミン;N−メチル−D−グルカミン;及びアミノ酸、例えばアルギニン、リシン等を含むが、これらに限定されない。
【0026】
「患者」又は「動物」は、好ましくは哺乳動物であり、ウシ、サル、ウマ、ヒツジ、ブタ、ニワトリ、シチメンチョウ、ウズラ、ネコ、イヌ、マウス、ラット、ウサギ及びモルモット、及び最も好ましくはヒトを含むが、これらに限定されない。
【0027】
本明細書で使用する、「活性吸着剤」という語句は、その吸着能力を高めるために物理的及び/又は化学的処理を受けた吸着剤を意味する。
【0028】
本明細書で使用する、「作用薬」という語句は、患者の血流中に十分な量で吸収されたとき生物学的作用を生じさせる薬剤を指す。
【0029】
本明細書で使用する「吸着剤」という語句は、他の分子又は物質をその表面及び/又は孔及び/又はチャネルに保有する又は保持することができる大きな表面積及び/又はミクロ細孔容積を示す製薬上許容し得る物質を指す。
【0030】
本明細書で使用する、「吸着剤/逆作用薬」という用語は、逆作用薬がその表面及び/又は孔及び/又はチャネルの少なくとも一部に吸着されている吸着剤を指す。
【0031】
本明細書で使用する「逆作用薬」という語句は、投与剤型中に存在する作用薬の少なくとも1つの生物学的作用、例えば陶酔作用を部分的に又は完全に取り消す又は無効にする、あるいは患者又は動物の血流中に十分な量で吸収されたとき、1種以上の不快な生理的反応、例えば嘔吐、吐き気、下痢、まずい味を生じさせる薬剤を指す。
【0032】
本明細書で使用する、「制御放出」という用語は、長い時間にわたっての制御された方式での投与剤型からの作用薬のインビボ放出を指す。例えば制御放出経口投与剤型は、例えば5〜24時間にわたって薬剤を放出することができる。
【0033】
本明細書で使用する、「遅延放出」という語句は、作用薬が、投与後少なくとも1時間、投与剤型から実質的に放出されないインビボ放出工程を指す。一旦、遅延放出が起これば、投与剤型は制御放出又は即時放出によって作用薬を放出することができる。
【0034】
本明細書で使用する、「ラミネート」という用語は、2つ以上の層を含む構造、すなわち多層構造を指す。
【0035】
本明細書で使用する、「オピオイドアゴニスト」という語句は、場合により立体特異的に、オピオイド受容体のいくつかの亜種の1種以上に結合して、アゴニスト活性を生じさせる作用薬を指す。
【0036】
本明細書で使用する、「オピオイドアンタゴニスト」という語句は、患者又は動物の血流中に十分な量で吸収されたとき、オピオイドアゴニストの少なくとも1つの生物学的作用、例えば陶酔作用を低減する、遅延させる又は無効にする逆作用薬を指す。
【0037】
吸着剤と逆作用薬とを含有する投与剤型
本発明は、吸着剤と逆作用薬とを含有する医薬組成物及び投与剤型、及びそのような組成物及び投与剤型を製造するための方法を対象とする。ある実施形態では、本発明は、作用薬、吸着剤及び逆作用薬を含有する投与剤型に関する。
【0038】
1つの実施形態では、本発明は、作用薬を含む複数の第一粒子;及び吸着剤と逆作用薬とを含む複数の第二粒子を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型に関する。もう1つの実施形態では、本発明は、オピオイドアゴニストを含む複数の第一粒子;及び吸着剤とオピオイドアンタゴニストとを含む複数の第二粒子を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されており、及び前記第一粒子が、患者への経口投与後に前記オピオイドアゴニストの制御放出を提供する、経口投与剤型に関する。
【0039】
もう1つの実施形態では、本発明は、吸着剤と逆作用薬とを含有するコア、及び作用薬を含有するシェルを含み、前記シェルが前記コアを少なくとも部分的に覆う又は取り囲む投与剤型に関する。
【0040】
本発明の組成物及び投与剤型は、作用薬の任意の放出速度(制御放出、即時放出又は遅延放出を含むが、限定はされない。)を提供することができる。
【0041】
本発明は、少なくとも1つの吸着剤/逆作用薬を含む。ある実施形態では、逆作用薬の少なくとも一部が吸着剤の少なくとも一部に吸着されている。1つの実施形態では、逆作用薬の少なくとも大部分、すなわち少なくとも50重量%が吸着剤の少なくとも一部に吸着されている。他の実施形態では、吸着剤の少なくとも一部に吸着される逆作用薬のパーセンテージは、例えば少なくとも70重量%、少なくとも80重量%、又は少なくとも90重量%又はそれ以上であり得る。1つの実施形態では、逆作用薬の基本的に全部が吸着剤の少なくとも一部に吸着されている。
【0042】
ある実施形態では、本発明の組成物及び投与剤型は、無傷投与剤型の患者への意図された通りの投与後に逆作用薬が血流中にインビボで放出又は吸収されるのを低減する又は防止するように製剤又は製造される。そこで、ある実施形態では、投与剤型中に存在する逆作用薬の小量だけが、好ましくは約10重量%未満、より好ましくは約1重量%未満又は0%が、無傷投与剤型の患者への意図された通りの投与後にインビボで血流中に放出又は吸収される。ある実施形態では、吸着剤/逆作用薬の逆作用薬がオピオイドアンタゴニストであるとき、好ましくは約0.5mg未満、より好ましくは約0.05mg未満のオピオイドアンタゴニストが、無傷投与剤型の患者への意図された通りの投与後にインビボで放出される。
【0043】
ある実施形態では、本発明の投与剤型は、誤処置又は誤用された場合、インビボで有意の量の逆作用薬を放出するように設計される。例えば乱用者が、作用薬の即時放出を提供することが期待できる、粉末形態の組成物を得るために投与剤型を粉砕しようとすることがあり得る。この場合、製剤を粉砕することは、逆作用薬/吸着剤中に存在する逆作用薬を露出させ、それにより、投与された場合逆作用薬を放出させるはずである。あるいは、乱用者が製剤を有機溶媒、例えばエタノールに溶解して、溶液から作用薬を単離しようとすることがあり得る。この場合、エタノールなどの溶媒の存在下では逆作用薬が脱着又は溶解するので、有機溶媒による抽出工程が有意の割合の逆作用薬の放出を生じさせるはずである。
【0044】
1つの実施形態では、吸着剤と逆作用薬とを他の物質、例えば結合剤、可塑剤、加工助剤、賦形剤等、又は前記の2つ以上の組合せと共に押出することができる。
【0045】
1つの実施形態では、本発明は、作用薬、吸着剤及び逆作用薬を含有する複数の粒子を含み、前記粒子が吸着剤と逆作用薬とを含有するコアを含み、前記コアが作用薬を含有するシェルによって少なくとも部分的に取り囲まれている、固体投与剤型に関する。前記粒子は、コアとシェルとの共押出を含む工程によって作られる。好ましくは、シェルはコア成分の大部分を取り囲む。
【0046】
ある実施形態では、吸着剤及び逆作用薬はコア全体に存在し得る。1つの実施形態では、吸着剤と逆作用薬はコアとシェルとの両方に存在し得る。もう1つの実施形態では、吸着剤と逆作用薬とは多層粒子の1つ以上の内層に存在し得る。
【0047】
ある実施形態では、シェルは吸着剤/逆作用薬を全く含まない。他の実施形態では、シェルは吸着剤/逆作用薬を含み得る。1つの実施形態では、シェル中に存在する逆作用薬の量は、コア中に存在する逆作用薬の量よりも少ない。他の実施形態では、シェルは、任意の放出速度(即時放出又は制御放出を含むが、限定はされない。)を有し得る、吸着剤/逆作用薬ではない逆作用薬を含み得る。
【0048】
1つの実施形態では、吸着剤と逆作用薬はコアにのみ存在し、作用薬は多層粒子のシェルにのみ存在する。この実施形態では、少量の作用薬及び/又は逆作用薬が共押出後に他の成分又は層に移動することが許容し得る。
【0049】
他の実施形態では、本発明の投与剤型は、何らかの適切な大きさの1又はそれ以上の粒子を含み得る。1つの実施形態では、投与剤型は、複数の小さな粒子、例えば全ての寸法において約0.1mmから約5.0mm、好ましくは全ての寸法において約0.1mmから約3.0mmの大きさを有する粒子を含み得る。前記粒子は、所望に応じて、任意の形状も有することができ、例えば円柱状、球状、正方形、楕円体、又は何らかの規則的な又は不規則な形態をとり得る。
【0050】
1つの実施形態では、投与剤型は、硬又は軟ゼラチンカプセル内に作用薬を含有する有効量の溶融押出マルチ微粒子(「MEM」)を含むように製造される。例えばコア及びシェルを含む複数のMEMを、摂取されて体液と接触したとき、吸着剤/逆作用薬からの逆作用薬の有意の放出を伴わずに作用薬の有効な持続放出用量を提供するのに十分な量でゼラチンカプセル中に入れることができる。本発明の投与剤型のマルチ微粒子の粒径は、全ての寸法において約0.1mmから約5.0mm、より好ましくは全ての寸法において約0.1mmから約3.0mmである。
【0051】
本発明の投与剤型は、経口的に、例えば錠剤又はカプセルの形態で、あるいは直腸又は膣経路で、例えば坐薬の形態で投与することができる。好ましい実施形態では、本発明は経口投与剤型を対象とする。
【0052】
ある実施形態では、投与剤型は、例えば約5から8時間にわたって、好ましくは少なくとも12時間にわたって、より好ましくは少なくとも24時間、又はそれ以上にわたって、インビボで作用薬の制御放出を提供するように製剤される。
【0053】
作用薬と吸着剤/逆作用薬とを含有する無傷投与剤型を患者に投与するとき、逆作用薬の少量だけがインビボで放出され、好ましくはほとんど全く放出されず、一方作用薬は、即時放出から制御放出まで変化し得る、意図された速度で放出される。しかし、作用薬、吸着剤及び逆作用薬を含有する投与剤型が、特に高温(例えば約45℃から約50℃以上、約100℃まで又はそれ以上)の溶媒中で、不正使用される、例えば砕かれる、破砕、粉砕又は溶解されるとき、体内への吸収のために利用され得る逆作用薬の量は実質的に上昇する。逆作用薬は、その後、作用薬の少なくとも1つの作用、例えば陶酔作用を低減することによって、又は患者において1種以上の不快な作用を惹起することによってその作用を及ぼすために利用可能となる。そこで、逆作用薬が作用薬のアンタゴニストである場合、逆作用薬の作用によって作用薬の少なくとも1つの作用が、好ましくは実施的に低下するか、又はさらには排除される。例えば作用薬がオピオイドアゴニストであり、逆作用薬がオピオイドアンタゴニストである場合、投与剤型が不正使用されたとき高い量のオピオイドアンタゴニストが体内で利用可能となり、オピオイド−受容体結合を妨げ、オピオイドアゴニストの陶酔作用を低減する。従って、無傷投与剤型として意図された通りに本発明の投与剤型を服用する患者だけが、実質的に作用薬の完全な薬理作用を享受する。逆作用薬が催吐薬であり、投与剤型が不正使用される場合、催吐薬の放出及び吸収は吐き気及び/又は嘔吐を誘発して使用者が投与剤型を不正使用するのを阻止し、また、ある種の場合には、被験者の体内から作用薬を除去する。従って、投与剤型中の作用薬の乱用は、逆作用薬により引き起こされる好ましくない作用のために、より望ましくないものとなる。
【0054】
発明者は、作用薬と逆作用薬の放出速度はインビボ法又はインビトロ法によって測定することができると考える。しかし、本発明者は、2つの異なる方法によって得られる結果の間に必ずしも直接の相関があると主張するわけではない。
【0055】
意図された通りに患者に投与されたとき、無傷投与剤型からの逆作用薬のインビボ放出は、好ましくは作用薬の恩恵を実質的に低下させない又は不快な生理的反応を生じさせないように十分に低い。逆作用薬の放出速度は、主としてコア、鞘(sheath)及びシェルの組成物によって決定される。本発明の投与剤型は、典型的には無傷投与剤型の意図された通りの投与後にインビボで約10重量%未満、好ましくは約1重量%未満の逆作用薬を放出し、より好ましくは逆作用薬を実質的に全く放出しない。逆作用薬がオピオイドアンタゴニストであるとき、投与剤型は、無傷投与剤型の意図された通りの投与後にインビボで、好ましくは約0.5mg未満、より好ましくは約0.05mg未満のオピオイドアンタゴニストを放出する。例えば1つの実施形態では、逆作用薬がナルトレキソンオピオイドアンタゴニストであるとき、好ましくは0.0625mg未満のナルトレキソンが、意図された通りの無傷投与剤型の投与後にインビボで放出される。
【0056】
ある実施形態では、本発明の投与剤型は、標準インビトロ溶解試験において36時間にわたって、好ましくは約10重量%未満、より好ましくは約1重量%未満の逆作用薬を放出し、より好ましくは逆作用薬を実質的に全く放出しない。例えば経口投与剤型が5.0mgのオピオイドアンタゴニストを含有し、USPバスケット法(USP I型バスケット、100rpm;充填擬似胃液700mL、酵素なしでpH1.2;37℃で1時間、次いで擬似腸液900mL;試験期間酵素なしでpH7.5)を用いて溶解試験を実施するとき、36時間にわたって擬似胃腸液中に放出されるオピオイドアンタゴニストの量は、0.5mg未満、より好ましくは0.05mg未満であり得る。
【0057】
本発明の1つの実施形態では、固体投与剤型は、場合により化粧被覆物によって覆うことができる。医薬投与剤型のために使用されるいかなる公知の種類の化粧被覆物も、被覆された投与剤型が本発明の意図する目的を達成する限り、使用することができる。
【0058】
ある実施形態では、投与剤型は、高い安定性を達成するために長時間高温に暴露することによって硬化することができる。本明細書で使用する、「硬化」という用語は、安定化された最終投与剤型を得ることを目的とする投与剤型(又は中間生成物)の熱処理を意味する。当業者に了解されるように、本発明の製剤が疎水性遅延剤の一部又は全部としてポリマーを組み込むとき、熱処理は硬化作用を引き起こし、ポリマーはおそらくそれ自体でより安定な状態へと架橋する。本発明の製剤が疎水性物質、例えば硬化植物油又はステアリルアルコールを含むとき、熱処理は、ポリマーの硬化よりはむしろ製剤のアニーリングに近いことがある。しかし、本発明のために、「硬化」という用語の使用は、硬化及びアニーリングの両方を包含するとみなされる。疎水性材料がろう様物質だけを含む状況では、硬化は、最大の安定性を達成するのに十分な時間、例えば約5から約72時間、約35℃から約65℃の温度で達成することができる。他の実施形態では、硬化は、約40℃から約60℃の温度で約5〜約48時間又はそれ以上、好ましくは少なくとも約24時間、実施される。安定な投与剤型の意図する結果を達成する適切な硬化時間は、当業者によって決定され得る。
【0059】
吸着剤材料
本発明のために有用な吸着剤材料は、窒素を吸着質として使用するBrunauer-Emmett-Teller(BET)モデル(全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、F. S. Baker et al., "Activated Carbon" in Kirk-Othmer Encyc. of Chem. Technol., 4:1016 (4th ed. 1995)参照)などの方法によって測定したとき高い表面積を示す、水不溶性の製薬上許容し得る材料である。従って、1つの実施形態では、本発明における使用に適する吸着剤材料は、100mg/g以上のBET表面積を示す。好ましくは、吸着剤材料は500mg/g以上のBET表面積を示す。最も好ましくは、吸着剤材料は1,000mg/g以上のBET表面積を示す。
【0060】
本発明において有用な製薬上許容し得る吸着剤材料の非限定的な例は、活性炭及び活性黒鉛を含む活性炭素;カオリン、モンモリロナイト、アタパルジャイト、イライト、ベントナイト及びハロイサイトを含む活性白土;二酸化ケイ素、コロイド状二酸化ケイ素(例えばCabot Corp.より入手可能な、CAB-O-SIL)及びアルミナを含む活性無機金属酸化物及び/又は無機イオン交換樹脂;活性ケイ酸アルミニウム及び/又は無機イオン交換組成物、例えばゼオライト;有機イオン交換樹脂、例えばスルホン酸ポリスチレンを含む活性有機酸;有機高分子ベースの吸着剤、例えば微結晶セルロース、デンプン、マルトデキストリン、クロスポビドン(例えばGAF Corp.より入手可能な、POLYPLAXDONE XL又はXL10);等の1種以上の高表面積形態を含む。
【0061】
好ましくは、吸着剤材料は活性吸着剤材料である。活性吸着剤材料は、市販のものを入手し得る及び/又は使用者により、当技術分野において周知の方法によって使用の直前に活性化される。例えば無機吸着剤を活性化する方法は、真空又は不活性パージガスと組み合わせた熱を使用して、表面吸着種、例えば水、有機化合物及び硫化物を除去することを含む。
【0062】
無機イオン交換組成物及び有機イオン交換樹脂を活性化する方法は、塩のイオンをイオン交換樹脂材料の表面に吸着させ、場合により処理した樹脂又は材料を乾燥する、特定塩を含有する溶液での処理を含む。活性化した樹脂又は材料を、次に、逆作用薬の塩形態で処理すると、逆作用薬のイオンがあらかじめ吸着したイオンを置換し、それによって逆作用薬をイオン交換樹脂又は材料に付着させる。
【0063】
1つの実施形態では、吸着剤材料は、活性炭、アルミナ、ベントナイト及びカオリンからなる群より選択される。
【0064】
好ましい実施形態では、吸着剤材料は活性炭又は活性炭素であり、この2つの用語は、低レベルの不純物を含む大きな表面積及び/又はミクロ細孔容積の炭素を表すために、本明細書では交換可能に使用される(例えば米国薬局方26 404(2003)参照)。全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、F. S. Baker et al., "Activated Carbon" in Kirk-Othmer Encyc. of Chem.Techrzol., 4:1015-1022 (4th ed. 1995)は、種々のグレードの活性炭を製造するための方法を開示する。本発明において有用な活性炭は、約100m2/g以上の表面積を示す。ある実施形態では、活性炭の表面積は約300m2/gから約2,000m2/gである。
【0065】
本発明において有用化活性吸着剤はまた、水溶液からのメチレンブルー染料の吸光度(adsorbance)(「MB値」)によって測定したとき高い吸着能を示す(各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、ASTM D3860-98(活性炭の吸着能)及びASTM C837-99(白土の吸着能)参照)。1つの実施形態では、本発明における使用に適する吸着剤材料は、30mg/g以上のMB値を示す;もう1つの実施形態では、吸着剤材料は150mg/g以上のMB値を示す;及びもう1つの実施形態では、吸着剤材料は300mg/g以上のMB値を示す。
【0066】
本発明において有用な吸着剤材料の非限定的な例は、以下の表1に列挙する活性炭を含む。
【0067】
【表1】

【0068】
疎水性被覆材料
本発明の投与剤型は、吸着剤又は吸着剤/逆作用薬の表面の少なくとも一部に配置された少なくとも1つの疎水性被覆材料をさらに含み得る。理論的に制限されることなく、疎水性被覆材料は吸着剤材料の細孔及びチャネルを密封し、それによって水性液体、例えば胃液、が吸着剤材料の細孔又は格子構造に入り込むのを阻止する又は防止すると考えられる。1つの実施形態では、疎水性被覆材料は吸着剤/逆作用薬の少なくとも一部を覆う。
【0069】
1つの実施形態では、前記の少なくとも1つの疎水性材料は、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される。
【0070】
1つの実施形態では、前記の少なくとも1つの疎水性被覆材料は、例えばグリセロールのエステル;脂肪酸、例えばステアリン酸及びイソステアリン酸;アルコール、例えばステアリルアルコール、イソステアリルアルコール、セチルアルコール及びセトステアリルアルコール;蜜ろう;硬化ヒマシ油および硬化綿実油;及びそれらの混合物を含む。もう1つの実施形態では、疎水性被覆材料はステアリルアルコールである。
【0071】
疎水性マトリックス材料
ある実施形態では、本発明の投与剤型及び医薬組成物は疎水性マトリックス材料をさらに含み得る。疎水性マトリックス材料は、疎水性被覆材料と同じであるか又は異なり得る。疎水性マトリックス材料は、少なくとも部分的には、作用薬及び逆作用薬の放出特性を制御することができ;及び逆作用薬の放出をさらに防止する、阻止する又は遅延させることができる。本発明において有用な疎水性マトリックス材料は、胃腸管において不溶性であるか又は低い溶解度を有することが当技術分野で公知であるものを含む。そのような材料は、アクリル酸及びメタクリル酸のポリマー及びコポリマー、並びにアルキルセルロースからなる群より選択される疎水性材料を含むが、これらに限定されない。マトリックスはまた、付加的な疎水性材料、例えばゼイン、シェラック、硬化ヒマシ油、硬化植物油又はそれらの混合物を含有し得る。
【0072】
1つの実施形態では、疎水性マトリックス材料はアクリルポリマーを含む。適切なアクリルポリマーの例は、アクリル酸及びメタクリル酸のコポリマー、メチルメタクリレートコポリマー、エトキシエチルメタクリレート、シアノエチルメタクリレート、アミノアルキルメタクリレートコポリマー、ポリ(アクリル酸)、ポリ(メタクリル酸)、メタクリル酸アルキルアミドコポリマー、ポリ(メチルメタクリレート)、ポリメタクリレート、ポリ(メチルメタクリレート)コポリマー、ポリ(メタクリル酸)(無水物)、メチルメタクリレート、ポリアクリルアミド、アミノアルキルメタクリレートコポリマー、ポリ(メタクリル酸無水物)、並びにグリシジルメタクリレートコポリマーを含むが、これらに限定されない。適切なアクリルポリマーの付加的な例は、アクリル及びメタクリルモノマー1モル当り約0.02〜0.03モルのトリ(低級アルキル)アンモニウム基を含むアクリル酸エステル及びメタクリル酸エステルから合成されるコポリマー(例えばアクリル酸低級アルキルエステルとメタクリル酸低級アルキルエステルとのコポリマー)を含む、アクリル樹脂を含むが、これらに限定されない。
【0073】
アクリルポリマーは、1種以上のアンモニオメタクリレートコポリマーを含み得る。アンモニオメタクリレートコポリマーは当技術分野において周知であり、低含量の第四級アンモニウム基を有するアクリル酸エステル及びメタクリル酸エステルの十分に重合されたコポリマーである。所与の治療薬について望ましい溶解プロフィールを得るために、異なる物理的性質を有する2種以上のアンモニオメタクリレートコポリマーを組み込むことが必要な場合がある。例えば第四級アンモニウム基対中性アクリル(メタクリル)エステルのモル比を変化させることによって、生じる被覆物の透過特性を変化させ得ることは公知である。当業者は、所望放出速度で治療薬を放出するコポリマーを提供するためにモノマーを容易に組み合わせることができる。第四級アンモニウム基の官能性を有するアクリレート及びメタクリレートのコポリマーは、EUDRAGIT RS及びEUDRAGIT RL(Rohm Pharma, GmbH, Weiterstat, Germany)として市販されている。好ましいアンモニオメタクリレート樹脂は、全ての形態のEUDRAGIT RS、例えばEUDRAGIT RS POを含む。EUDRAGIT RSは、EA:MM:TAMのモル比が1:2:0.01である、エチルアクリレート(EA)、メチルメタクリレート(MM)及びトリメチルアンモニウムエチルメタクリレートクロリド(TAM)の水不溶性コポリマーであることが知られている;例えば米国特許第6,306,391号参照。EUDRAGIT RS POha,EUDRAGIT RSの粉末化形態であることが知られている;例えば、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、米国特許第5,492,692号参照。
【0074】
1つの実施形態では、疎水性マトリックス材料は、水不溶性セルロースポリマーを含む。ある実施形態では、セルロースポリマーは、セルロースエーテル、セルロースエステル、又はセルロースエステルエーテルである。好ましくは、セルロースポリマーは、約0から約3(3を含む)までの無水グルコース単位上の置換度(「D.S.」)を有する。本明細書で使用するD.S.という用語は、置換基によって置換されている、セルロースポリマーの無水グルコース単位上に存在するヒドロキシル基の平均数を意味する。代表的セルロースポリマーは、セルロースアシレート、セルロースジアシレート、セルローストリアシレート、セルロースアセテート、セルロースジアセテート、セルローストリアセテート、モノ−、ジ−及びトリセルロースアルカニレート、モノ−、ジ−及びトリセルロースアリーレート、及びモノ−、ジ−及びトリセルロースアルケニレートから選択されるポリマーを含むが、これらに限定されない。例示的なセルロースポリマーは、約1から約2のD.S.を有するセルロースアセテート及び約2から約3のD.S.を有するセルロースアセテートを含む。好ましくは、セルロースポリマーは、エチルセルロース、セルロースアセテート、セルロースプロピオネート(低、中又は高分子量)、セルロースアセテートプロピオネート、セルロースアセテートブチレート、セルロースアセテートフタレート、又はセルローストリアセテートである。より好ましいセルロースはエチルセルロースである。
【0075】
より特定のセルロースポリマーは、約1.8のD.S.を有するセルロースプロピオネート;約1.8のD.S.を有するセルロースアセテートブチレート;約2.9〜3のD.S.を有するセルローストリアシレート、例えばセルローストリアセテート、セルローストリバレレート、セルローストリラウレート、セルローストリパルミテート、セルローストリスクシネート及びセルローストリオクタノエート;約2.2〜2.6のD.S.を有するセルロースジアシレート、例えばセルロースジスクシネート、セルロースジパルミテート、セルロースジオクタノエート、セルロースジペンタノエート;及びセルロースのコエステル、例えばセルロースアセテートブチレート、セルロースアセテートオクタノエートブチレート及びセルロースアセテートプロピオネートを含む。
【0076】
ある実施形態では、吸着剤/逆作用薬を疎水性マトリックス材料と混合することができる。例えば吸着剤/逆作用薬を含有するコアは、約50重量%までの1種以上の疎水性マトリックス材料、好ましくは約50重量%までの1種以上の疎水性マトリックス材料、より好ましくは約25重量%までの1種以上の疎水性マトリックス材料をさらに含み得る。コア中に疎水性マトリックス材料を含むことは、吸着剤材料からの逆作用薬の放出又は脱着をさらに低減する、遅延させる又は防止することができる。
【0077】
上述したように、作用薬及び逆作用薬の放出速度は、部分的には、疎水性マトリックス材料の組成物によって制御される。製薬技術分野の当業者は、疎水性マトリックス材料の組成物を変更することによってこれらの放出速度に影響を及ぼすことができ、そのような変更は本発明の開示を考慮した常用実験によって決定される。
【0078】
作用薬
いかなる種類の作用薬も、本発明の投与剤型において使用することができる。有用な作用薬の例は、鎮痛薬、抗炎症薬、駆虫薬、抗不整脈薬、抗菌薬、抗ウイルス薬、抗凝固薬、抗うつ薬、抗糖尿病薬、抗てんかん薬、抗真菌薬、抗痛風薬、抗高血圧薬、抗マラリア薬、抗片頭痛薬、抗ムスカリン薬、抗腫瘍薬、勃起機能不全改善薬、免疫抑制剤、抗原虫薬、抗甲状腺薬、抗不安薬、鎮静薬、催眠薬、神経弛緩薬、β-遮断薬、心臓イオンチャネル薬、コルチコステロイド、利尿薬、抗パーキンソン病薬、胃腸薬、ヒスタミン受容体アンタゴニスト、角質溶解薬、脂質調節薬、抗狭心症薬、cox-2阻害剤、ロイコトリエン阻害剤、マクロライド系抗生物質、筋弛緩薬、栄養剤、オピオイド鎮痛薬、プロテアーゼ阻害剤、性ホルモン、興奮薬、筋弛緩薬、抗骨粗しょう症薬、抗肥満薬、認知増強薬、抗尿失禁薬、栄養油、抗良性前立腺肥大症薬、必須脂肪酸及び非必須脂肪酸を含むが、これらに限定されない。投与剤型は2つ以上の作用薬を含み得る。
【0079】
作用薬のより特定の例は、オピオイド、ベンゾジアゼピン、バルビツレート、及び刺激薬、例えばメチルフェニデート及びアンフェタミン、ドロナビノール、グルテチミド、メチルフェニデート、ナビロン、タンパク質同化ステロイド、メチルプリロン、エトクロルビノール、エチナメート、フェンフルラミン、メプロバメート、ペモリン、レボメタジル、ベンズフェタミン、クロルフェンテルミン、ジエチルプロピオン、フェンテルミン、メブタメート、クロルテルミン、フェニルアセトン、ドロナビノール、ナビロン、ベンフェタミン、抱水クロラール、エトクロルビノール、パラアルデヒド、ミダゾラム、及びデトロプロポキシフェンを含むが、これらに限定されない。
【0080】
ある実施形態では、作用薬はオピオイドアゴニストである。有用なオピオイドアゴニストは、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジアモルフォン、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、エトルフィン、ジヒドロエトルフィン、フェンタニル、ヒドロコドン、ヒドロモルフォン、ヒドロモルフォドン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ナルブフェン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パントポン、パパベレタム、パレゴリック、ペンタゾシン、フェナドキソン、フェンジメトラジン、フェンジメトラゾン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロポキシフェン、プロピルヘキセドリン、スフェンタニル、チリジン、トラマドール、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0081】
ある実施形態では、オピオイドアゴニストは、ヒドロコドン、モルフィン、ヒドロモルフォン、オキシコドン、コデイン、レボルファノール、メペリジン、メタドン、オキシモルフォン、ブプレノルフィン、フェンタニル及びその誘導体、ジピパノン、ヘロイン、トラマドール、エトルフィン、ジヒドロエトルフィン、ブトルファノール、レボルファノール及びそれらの混合物からなる群より選択される。1つの実施形態では、オピオイドアゴニストは、オキシコドン、ヒドロモルフォン又はヒドロコドンである。
【0082】
「ベンゾジアゼピン」という用語は、ベンゾジアゼピン及びベンゾジアゼピンの誘導体であって、中枢神経系を抑制することができる薬剤を指す。ベンゾジアゼピンは、アルプラゾラム、ブロマゼパム、クロルジアゼポキシド、クロラゼペート、ジアゼパム、エスタゾラム、フルラゼパム、ハラゼパム、ケタゾラム、ロラゼパム、ニトラゼパム、オキサゼパム、プラゼパム、クアゼパム、テマゼパム、トリアゾラム、メチルフェニデート及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0083】
バルビツレートは、バルビツール酸(2,4,6−トリオキソヘキサヒドロピリミジン)から誘導される鎮静−催眠薬を指す。バルビツレートは、アモバルビタール、アプロバルビタール、ブタバルビタール、ブタルビタール、メトヘキシタール、メフォバルビタール、メタルビタール、ペントバルビタール、フェノバルビタール、セコバルビタール及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0084】
刺激薬は、中枢神経系を刺激する薬剤を指す。刺激薬は、アンフェタミン、例えばアンフェタミン、デキストロアンフェタミン樹脂複合体、デキストロアンフェタミン、メタンフェタミン、メチルフェニデート及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0085】
作用薬は、結腸疾患、例えば過敏性腸症候群、過敏性腸疾患、クローン病、便秘、術後アトニー、胃腸感染を治療するために結腸領域で局所的に作用する薬剤、及び抗原性物質をリンパ系組織に送達する治療薬を含むが、これらに限定されない、結腸への送達を意図する薬剤であり得る。結腸疾患の治療のための作用薬は、5−ASA;ステロイド類、例えばヒドロコルチゾン及びブデゾニド;緩下薬;軟便剤;オクトレオチド;シサプリド;抗コリン作用薬;オピオイド;カルシウムチャネル遮断薬;結腸の細胞への送達のためのDNA;グルコサミン;トロンボキサンA2シンテターゼ阻害剤、例えばリドグレル;5HT3−アンタゴニスト、例えばオンダンセトロン;感染性細菌、例えばクロストリジウム・ディフィシル(Clostridium difficile)に対する抗体;及び、例えばHIVの予防のための、抗ウイルス薬を含むが、これらに限定されない。
【0086】
あるいは、作用薬は、全身的に活性であり、結腸領域において吸収が高い薬剤であり得る。そのような薬剤は、極性化合物、例えばヘパリン;インスリン;カルシトニン;ヒト成長ホルモン(HGH);成長ホルモン放出ホルモン(GHRH);インターフェロン;ソマトスタチン及び類似体、例えばオクトレオチド及びバプレオチド;エリトロポエチン(EPO);顆粒球コロニー刺激因子(GCSF);副甲状腺ホルモン(PTH);黄体化ホルモン放出ホルモン(LHRH)及びその類似体;心房性ナトリウム利尿因子(ANF);バソプレシン;デスモプレシン;カルシトニン遺伝子関連ペプチド(CGRP);及び鎮痛薬を含む。
【0087】
作用薬粒子は、疎水性材料、結合剤、可塑剤、賦形剤、及び前記のいずれか2つ以上の組合せをさらに含み得る。適切なマトリックス材料は、所望結果、例えば即時放出、持続放出又は遅延放出を達成するのに十分な速度で作用薬を放出することを可能にするものを含む。1つの実施形態では、作用薬の胃腸液への拡散放出を可能にする、透過性マトリックス材料を使用する。
【0088】
逆作用薬
逆作用薬は、作用薬の生物学的作用を少なくとも部分的に低減するか又は遮断する、あるいは動物又は患者の血流中に吸収されたとき不快な作用を作り出す、任意の医薬活性物質であり得る。逆作用薬の例は、任意の治療的に活性な作用物質のアンタゴニストを含むが、これらに限定されない。オピオイドアゴニストを本発明の投与剤型中の作用薬として使用するときは、オピオイドアンタゴニストを逆作用薬として使用することができる。同様に、ベンゾジアゼピンを本発明の投与剤型における作用薬として使用するときは、ベンゾジアゼピンアンタゴニストを逆作用薬として使用できる。バルビツレートを本発明の投与剤型中の作用薬として使用するときは、バルビツレートアンタゴニストを逆作用薬として使用することができる。アンフェタミンを本発明の投与剤型における作用薬として使用するときは、アンフェタミンアンタゴニストを逆作用薬として使用できる。作用薬が、その通常治療範囲以上の用量で投与したとき毒性であるとき、すなわち過量の重大な潜在的可能性が存在するときは、毒性作用薬の解毒薬を逆作用薬として使用することができる。
【0089】
1つの実施形態では、逆作用薬はオピオイドアンタゴニストである。本発明において有用なオピオイドアンタゴニストは、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、シクラゾシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0090】
有用なオピオイドアンタゴニスト塩は、酸とオピオイドアンタゴニストの塩基性窒素基とから形成される塩を含む。オピオイドアンタゴニスト塩の例は、硫酸塩、クエン酸塩、酢酸塩、シュウ酸塩、塩化物、臭化物、ヨウ化物、硝酸塩、重硫酸塩、リン酸塩、酸性リン酸塩、イソニコチン酸塩、乳酸塩、サリチル酸塩、酸性クエン酸塩、酒石酸塩、オレイン酸塩、タンニン酸塩、パントテン酸塩、重酒石酸塩、アスコルビン酸塩、コハク酸塩、マレイン酸塩、ゲンチジン酸塩、フマル酸塩、グルコン酸塩、グルカロン酸塩、サッカリン酸塩、ギ酸塩、安息香酸塩、グルタミン酸塩、メタンスルホン酸塩、エタンスルホン酸塩、ベンゼンスルホン酸塩、p−トルエンスルホン酸塩、及びパルモエート(すなわち1,1’−メチレン−ビス−(2−ヒドロキシ−3−ナフトエート))塩を含むが、これらに限定されない。
【0091】
他のオピオイドアンタゴニスト塩は、酸性官能基、例えばカルボン酸又はスルホン酸官能基を有するアンタゴニストと、製薬上許容し得る無機又は有機塩基から生成される塩を含む。適切な塩基は、5.1章の「製薬上許容し得る塩」という用語に言及した項において上記で特定したものを含むが、これらに限定されない。
【0092】
ある実施形態では、オピオイドアンタゴニストは、ナルメフェン、ナロキソン、ナルトレキソン、又はそれらの製薬上許容し得る塩である。もう1つの実施形態では、オピオイドアンタゴニストは、ナルトレキソン塩、例えば塩酸ナルトレキソンである。
【0093】
本発明の逆作用薬として使用できるベンゾジアゼピンアンタゴニストは、フルマゼニルを含むが、これに限定されない。
【0094】
本発明の逆作用薬として使用できるバルビツレートアンタゴニストは、本明細書で述べるようなアンフェタミンを含むが、これらに限定されない。
【0095】
本発明の逆作用薬として使用できる刺激薬アンタゴニストは、本明細書で述べるベンゾジアゼピンを含むが、これらに限定されない。
【0096】
本発明のもう1つの実施形態では、逆作用薬は、望ましくない生理的反応、例えば嘔吐を引き起こす薬剤である。このタイプの逆作用薬は、オピオイド、ベンゾジアゼピン、バルビツレート、又は刺激薬を含むいかなる種類の治療薬に関しても使用できる。本発明における逆作用薬としての使用に適する催吐薬の例は、イペカック(ipecac)及びアポモルフィンを含むがこれらに限定されない、投与後安全且つ有効に嘔吐を誘発する薬剤を含む。
【0097】
本発明の投与剤型を製造するための方法
吸着剤/逆作用薬
ある実施形態では、本発明は、吸着剤/逆作用薬を製造するための方法に関する。例えば、一部の実施形態では、本発明は、液相から逆作用薬を吸着剤材料に吸着させるための方法に関する。1つの実施形態では、本発明は、吸着剤材料を提供すること;逆作用薬を含有する液体と吸着剤材料を、逆作用薬の少なくとも一部が吸着剤に吸着するのに十分な時間接触させること;吸着剤/逆作用薬液相から分離すること;及び場合により、吸着剤/逆作用薬を洗浄すること、を含む、吸着剤/逆作用薬を製造するための方法に関する。
【0098】
1つの実施形態では、本発明は、吸着剤材料と逆作用薬とを含有する組成物を押出することを含む、本発明の投与剤型を製造するための方法に関する。
【0099】
もう1つの実施形態では、本発明は、a)i)吸着剤と逆作用薬とを含有するコア;及びii)コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む鞘、を共押出して、押出物鎖(extrudate strand)を形成すること;及びb)例えば切断によって、押出物鎖を複数の粒子にすること、を含む、投与剤型を製造するための方法に関する。
【0100】
もう1つの実施形態では、本発明は、a)i)吸着剤と逆作用薬とを含有するコア;ii)場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む鞘;及びiii)コア及び/又は場合により鞘を少なくとも部分的に取り囲む、作用薬を含有するシェル、を共押出して、押出物鎖を形成すること;及びb)例えば切断によって、押出物鎖を複数の粒子にすること、を含む、投与剤型を製造するための方法に関する。
【0101】
もう1つの実施形態では、本発明は、a)作用薬を含有する複数の第一粒子を形成すること;b)i)吸着剤と逆作用薬とを含有するコア;及びii)コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、疎水性マトリックス材料を含有する鞘、を含む複数の第二粒子を共押出すること;及びc)第一及び第二粒子を投与剤型に添加すること、を含む、投与剤型を製造するための方法に関する。
【0102】
もう1つの実施形態では、本発明は、a)i)吸着剤と逆作用薬とを含有するコア;ii)場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、より好ましくはコアを実質的に又は完全に取り囲む鞘;及びiii)鞘を少なくとも部分的に取り囲む、好ましくは鞘の大部分を取り囲む、より好ましくは鞘を実質的に又は完全に取り囲む、作用薬を含有するシェル、を共押出して、多層押出物シート又はラミネートを形成すること;及びb)多層押出物シートを投与剤型、例えば錠剤、カプレット又は複数の粒子に成形すること、を含む、投与剤型を製造するための方法に関する。
【0103】
吸着(又は収着)過程及び吸着の速度と程度に影響を及ぼす因子は当技術分野において周知である(例えば、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、Perry's Chemical Engineer's Handbook, 16: 1-48 (6th ed. 1984); D. M. Ruthven, "Adsorption" in Kirk-Othmer Encyc.of Clzem. Technol., 4: 493-528 (4th ed. 1995); and S. A. Gembicki et al., "Adsorption, Liquid Separation" in Kirk-Othmer Encyc. of Chem. Technol., 4:573-600 (4th ed. 1995)参照)。
【0104】
1つの実施形態では、吸着工程は、吸着剤と液相とを含む反応容器内で、場合により混合しながら、実施する。もう1つの実施形態では、吸着剤はカラム内に含まれ、液相が吸着剤材料を通って循環する。吸着剤の速度及び/又は程度は、例えば液相中の逆作用薬の濃度変化を経時的に観測することによって、監視できる。
【0105】
液相からの吸着を含む工程のための適切な溶媒は、逆作用薬を溶解することができるが、一旦逆作用薬が吸着剤材料に吸着された後は逆作用薬を再溶解する傾向が低いものである。適切な溶媒の非限定的な例は、水、水溶液、例えば擬似胃液(pH1.2)、擬似腸液(pH6.8)、0.1N塩酸溶液及び0.1Nリン酸溶液を含む。
【0106】
1つの実施形態では、約1から約7のpHを有する水性溶媒を溶液吸着工程において使用する。より好ましくは、水性溶媒のpHは約1から約4である。より好ましくは水性溶媒のpHは約1であり得る。
【0107】
ある実施形態では、溶液吸着工程において使用する液相の温度は、吸着の速度と程度に影響を及ぼすように変化させ得る。当業者は常用実験によって最適反応温度を決定することができる。
【0108】
本発明はまた、逆作用薬を含む液相を吸着剤材料に噴霧することによって吸着剤/逆作用薬を製造するための方法に関する。1つの実施形態では、本発明は、吸着剤材料を提供すること;逆作用薬を含有する液相を提供すること;吸着剤材料を流動床に添加すること;吸着剤材料を流動化すること;流動化した材料に液相を噴霧すること;及び場合により、吸着剤/逆作用薬を乾燥すること、を含む、吸着剤/逆作用薬を製造するための方法に関する。1つの実施形態では、噴霧した粒子を乾燥する方法は、強制通気、減圧、熱及び前記のいずれか2つ以上の混合物からなる群より選択される。
【0109】
噴霧適用工程は、外側表面は乾燥しているように見えるが、まだ内側表面は液相で「湿潤」である吸着剤を提供する。溶媒の溶媒和力に依存して、逆作用薬が吸着剤材料の表面に吸着されてもよく又は吸着されなくてもよい。しかし、例えば、場合により熱を伴う、減圧蒸発による溶媒の除去は、液体ビヒクルが蒸発するので吸着剤材料の表面への逆作用薬の沈着を生じさせる。噴霧工程は、逆作用薬を別に脱着させる溶媒の使用を可能にする。
【0110】
噴霧乾燥工程のために有用な溶媒の非限定的な例は、上述したような水;メタノール、エタノール、n−プロパノール及びi−プロパノールを含むアルコール;ジエチルエーテル、ジ−プロピルエーテル及びd−ブチルエーテルを含むジアルキルエーテル;及び環状エーテル、例えばテトラヒドロフラン、及び前記のいずれか2つ以上の混合物を含む。
【0111】
ある実施形態では、吸着剤/逆作用薬は、疎水性被覆材料をさらに含む。被覆材料は、吸着剤/逆作用薬の細孔及びチャネルを密封し、それによって逆作用薬の放出をさらに遅延させる、低減する又は排除する。疎水性被覆材料は、適用方法が吸着剤/逆作用薬からの逆作用薬の有意の脱着を引き起こさないことを条件として、従来の任意の被覆手段を使用して適用することができる。
【0112】
1つの実施形態では、疎水性被覆材料を適用するための方法は、疎水性被覆材料を含む液相を提供すること;及び吸着剤/逆作用薬に液相を噴霧すること、を含む。
【0113】
もう1つの実施形態では、疎水性被覆材料を適用するための方法は、疎水性被覆材料の溶融物を提供すること;及びその溶融物を吸着剤/逆作用薬に適用すること、を含む。1つの実施形態では、固体を溶融物に浸漬被覆することによって疎水性被覆材料を吸着剤/逆作用薬に適用する。
【0114】
本発明はまた、溶融押出又は造粒の間に疎水性被覆材料を吸着剤/逆作用薬に適用するための方法に関する。この実施形態では、吸着剤/逆作用薬と疎水性被覆材料を他の成分と共にフィードホッパーに添加し、この混合物を押出する又は圧縮する。理論に縛られることなく、押出又は圧縮工程に必要なエネルギーは、疎水性被覆材料を流動化し、吸着剤/逆作用薬上に被覆物を形成するのに十分であると考えられる。
【0115】
放出可能形態のオピオイドアゴニスト及び実質的に放出されないオピオイドアンタゴニストを含有する投与剤型の製剤及び製造に関するさらなる詳細は、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、Oschlack et al.への米国特許第6,696,088 B2号に開示されている。
【0116】
5.8.2
投与剤型を押出する又は共押出するための方法
ある実施形態では、本発明はまた、吸着剤/逆作用薬を含むコアを押出することによって、例えば溶融押出することによって、吸着剤/逆作用薬を含有する医薬組成物又は投与剤型を製造するための方法に関する。1つの実施形態では、コアは疎水性材料をさらに含む。
【0117】
1つの実施形態では、本発明は、a)吸着剤/逆作用薬を含有するコア;及びコアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む鞘、を共押出して、押出物鎖を形成すること;及びb)例えば切断によって、押出物鎖を複数の吸着剤/逆作用薬粒子にすること、を含む、複数の吸着剤/逆作用薬粒子を製造するための方法に関する。
【0118】
1つの実施形態では、コアは吸着剤/逆作用薬と疎水性被覆材料とを含み、鞘は疎水性マトリックス材料を含む。
【0119】
もう1つの実施形態では、本発明は、a)作用薬を含有する複数の第一粒子を形成すること;b)吸着剤/逆作用薬、及び場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、疎水性マトリックス材料を含有する鞘、を含む複数の第二粒子を共押出すること;及びc)第一及び第二粒子を一緒にすること、を含む、投与剤型を製造するための方法に関する。
【0120】
もう1つの実施形態では、本発明は、a)吸着剤/逆作用薬を含有するコア;コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、より好ましくはコアを実質的に又は完全に取り囲む鞘;及び鞘を少なくとも部分的に取り囲む、好ましくは鞘の大部分を取り囲む、より好ましくは鞘を実質的に又は完全に取り囲む、作用薬を含有するシェル、を共押出して、押出物鎖を形成すること;及びb)例えば切断によって、押出物鎖を複数の吸着剤/逆作用薬粒子にすること、を含む、投与剤型を製造するための方法に関する。
【0121】
もう1つの実施形態では、本発明は、a)吸着剤/逆作用薬を含有するコア;場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、より好ましくはコアを実質的に又は完全に取り囲む鞘;及び鞘を少なくとも部分的に取り囲む、好ましくは鞘の大部分を取り囲む、より好ましくは鞘を実質的に又は完全に取り囲む、作用薬を含有するシェル、を共押出して、多層押出物シート又はラミネートを形成すること;及びb)多層押出物シートを投与剤型、例えば錠剤、カプレット又は複数の粒子に成形すること、を含む、投与剤型を製造するための方法に関する。1つの実施形態では、前記方法は、多層押出物シートを粒子にするためのローリングパンチの使用を含む。
【0122】
ある実施形態では、前記押出物を投与剤型において、例えば錠剤、カプレット又は複数の粒子において使用する。
【0123】
押出及び/又は共押出によって作用薬含有組成物又は粒子を製造するための方法は周知である。例えば粒子からなる投与剤型を含む、医薬投与剤型を押出し、形成するための公知の方法を開示する、各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第5,958,452号、同第5,965,161号及び同第6,335,033号参照。
【0124】
作用薬を投与するための2層組成物又は粒子を形成するための共押出方法も公知である。例えば全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、米国特許出願公開第2002/0119197 A1号参照。
【0125】
共押出によって本発明の投与剤型を形成するための方法を以下で述べる。異なる記載がない限り、コアだけを含む押出粒子を製造するための方法は、(1)コア製剤を供給するために1台のホッパーだけを使用する必要があること、及び(2)金型は1つの口だけを有することを除き、共押出に関するものと同様である。
【0126】
1つの実施形態では、共押出工程は、患者への意図された通りの無傷投与後にインビボで限られた量の逆作用薬を放出する、吸着剤/逆作用薬を含有する医薬組成物又は投与剤型を製造するために使用される。1つの実施形態では、前記組成物又は投与剤型は、好ましくは逆作用薬を全く含まない鞘により、その長さに沿って少なくとも部分的に放射状に取り囲まれた、吸着剤/逆作用薬を含有するコアを有する、共押出された吸着剤/逆作用薬円柱状粒子を含む。さらなる実施形態では、吸着剤/逆作用薬、例えばオピオイドアンタゴニストを含有する共押出粒子を、作用薬を含有する粒子と共にゼラチンカプセルに入れる。
【0127】
本発明はさらに、吸着剤/逆作用薬及び、場合により、疎水性被覆材料を含有するコア製剤を第一押出機に充填すること;作用薬を含有するシェル製剤を第二押出機に充填すること;前記製剤を第一及び第二押出機において加熱すること;前記製剤を共押出して、作用薬を含有するシェルによって放射状に取り囲まれた逆作用薬コアを含む鎖を形成すること;及び例えば切断によって、前記鎖を粒子にすること、を含む、投与剤型において有用な粒子状吸着剤/逆作用薬を製造するための方法に関する。
【0128】
もう1つの実施形態では、本発明は、吸着剤/逆作用薬及び、場合により、疎水性被覆材料を含有するコア製剤を第一押出機に充填すること;作用薬を含有するシェル製剤を第二押出機に充填すること;前記製剤を第一及び第二押出機において加熱すること;前記製剤を共押出して、多層押出物シート又はラミネートを形成すること;及び多層押出物シートを投与剤型、例えば錠剤、カプレット又は複数の粒子に成形すること、を含む、多層投与剤型を形成するための方法に関する。1つの実施形態では、前記方法は、多層押出物シートを粒子にするためのローリングパンチの使用を含む。
【0129】
本発明の共押出工程のために有用な装置の一例は、2台の粉末供給ホッパーを含み、1台は吸着剤/逆作用薬コア成分を負荷するため及び1台はシェル成分を負荷するためである。逆作用薬コア成分は、吸着剤/逆作用薬;及び場合により、疎水性被覆材料及び上述したような付加的な遅延剤、結合剤、可塑剤及び賦形剤を含むがこれらに限定されない付加的な物質を含有する。シェル成分は、作用薬、制御放出マトリックス材料及び上述したような付加的な遅延剤、結合剤、可塑剤及び賦形剤を含むがこれらに限定されない付加的な物質を含有する。各々のホッパーの内容物が押出機に充填される。各々の押出機の出口は、多数の同軸出口開口部を有する同じ同軸金型に接続されており、それによって鎖のコア中に逆作用薬を含む押出物の鎖及びコアを放射状に取り囲むシェルが形成される。
【0130】
各々の押出機は、例えば単軸又は二軸スクリューと加熱バレルを備え得る。各々のスクリュー押出機は、独立して、(i)逆方向回転(すなわち反対方向の回転で駆動される)非かみ合い型;(ii)同方向回転(すなわち同方向の回転で駆動される)非かみ合い型;(iii)逆方向回転かみ合い型;又は(iv)同方向回転かみ合い型であり得る。各々の押出機は、独立して、その架構の先端に位置する単一排出口又は放射状排出口を有し得る。各々のスクリュー押出機は、独立して、スクリューの各々の先端の駆動手段又は1つの先端にだけ存在する駆動手段を有し得る。各々のスクリュー押出機は、独立して、5から70、好ましくは20から60の長さ対直径比、又はL/D比を有し得る。当業者はそのような装置、例えば真空付属物を有するLeistritz二軸スクリュー押出機、Leistritz Micro 18/GL 40D二軸スクリュー押出機、又はWarner & Pfleiderer ZSK-30型二軸スクリュー押出機に精通する。
【0131】
各々の押出機の各々個別に調節可能なバレル区域の温度は、所与の製剤のために必要な温度に設定され、押出機は、1つの形態では約30分間、熱平衡させる。二軸スクリュー押出機の内圧は、マイナス約600から約980ミリバールに維持することができる。
【0132】
定常状態温度に達した後、各々の粉末供給ホッパーの内容物は別々の予備加熱された押出機に供給され、それによって各々の押出機内で、かみ合い型スクリュー及び混練機によって一連の区域を通って駆動されながら、加熱及び混合を通して、1つの実施形態では約30℃から約200℃の温度、好ましくは約50℃から約150℃、の緊密に混合された溶融塊を形成する。場合により、空気流通口が押出機内に存在し得る。液体成分を、粉末製剤とは独立して、溶融塊に添加することを所望する場合は、何らかの公知の手段によって、例えば容積移送式ポンプ、例えば歯車ポンプによって供給される注入口によって、液体を押出機内に注入することができる。
【0133】
各々の押出機を出てくる溶融塊は、場合により結合ブロック及び/又は主ゲートアダプターの下流にある、同軸金型内に集められ、その後金型の出口開口部を通過する。1つの実施形態では、押出物は、逆作用薬コア及びコアを少なくとも部分的に取り囲む鞘を含有する単一又は多数の押出鎖として成形される。もう1つの実施形態では、押出物は多層シート又はラミネートとして成形される。
【0134】
各々の押出機の回転速度(rpm)は、それらの結合産出量が、金型出口で、約1から約20kg/時又はそれ以上、好ましくは約6から約8kg/時であるように調節される。各々の押出機の回転速度は、各々の押出機の産出量がコア対鞘の所望比率を生じるように調節することができるパラメータの1つである。
【0135】
金型出口の寸法及び/又は横断面輪郭は、生じる鎖又はシートの厚さ及び形状を変化させるように調節することができる。例えば金型口は円形横断面形状に限定されず、楕円形、正方形、長方形、六角形、三角形、五望星等であり得る。ある実施形態では、円形横断面を有する金型口は、約0.1mmから約5.0mmの直径を有する鎖を提供するように調節することができる。鎖の形状は、数ある因子の中でも特に、金型出口開口部の形状及び鎖を粒子にする方法によって決定される。
【0136】
共押出工程から生産された鎖は、その後金型口から離れて運搬され、当業者に公知の方法によって、例えば扇冷却トンネル又はその上で鎖が冷却時に凝結して硬化する連続移動ベルトを使用して、凝固される。鎖は、当業者に公知の方法によって、例えばレーザー切断、熱線カッター又は裁断機を用いて、押出された鎖を粒子にするための適切な装置に送られる。鎖を粒子にすることは、凝結の前、凝結の間又は凝結の後に実施することができる。1つの実施形態では、共押出工程から生じる硬化した鎖はペレタイザーによって切断され、これは、ローラー、固定ナイフ、回転カッター等が利用できる。ローラー速度及びカッター速度は、所望の大きさ及び放出特性の粒子を生産するように設定される。適切な機器及びシステムは、ニュージャージー(New Jersey)のRand Castle Inc.などの配給業者から入手可能である。他の適切な装置は当業者に明白である。
【0137】
1つの実施形態では、共押出された鎖を切断して、逆作用薬含有コアが円柱の両端で露出されている、図1に示すような多数の円柱を形成する。いかなる場合も、逆作用薬含有コア及び鞘の組成物は、吸着剤/逆作用薬からの逆作用薬のインビボ放出速度を制限するように適宜製剤されるべきである。
【0138】
共押出工程からシートが生産される場合、シートは、押出物が多層シートとして形成されることを除いて、鎖に関して上述したように加工される。シートは、次に、何らかの方法によって、例えばローリングパンチを使用して、粒子又は錠剤に成形されうる。押出及び/又は共押出によって組成物又は粒子を製造するための方法は周知である。例えば、粒子からなる投与剤型を含む、医薬投与剤型を押出して形成するための公知の方法を開示する、各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第5,958,452号、同第5,965,161号及び同第6,335,033号参照。
【0139】
1つの実施形態では、共押出された多層押出物は、切断する、挟む、又は圧着することによって、多数の微粒子、例えば逆作用薬含有コアが鞘層及びシェル層によって実質的に又は完全に包まれている、図1に示すものに成形される。好都合には、好ましい実施形態では、ローリングパンチ装置の作用は、鞘がコアを実質的に又は完全に取り囲み、シェルが鞘を実質的に又は完全に取り囲むようにシェル層及び鞘層を圧着する又は挟む。いかなる場合も、コア及び鞘の組成物は、吸着剤/逆作用薬からの逆作用薬のインビボ放出速度を制限する又は妨げるように適宜製剤されるべきである。装置、例えば成形圧延機、ピンチ装置、ベルト及びローラー又は牽引ローラーを用いて押出物を粒子又は錠剤に成形するための方法は、例えば各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第6,120,802号及び同第5,073,379号に開示されている。
【0140】
加えて、粒子が、金型出口に依存して、何らかの幾何学的形状、例えばビーズ、シード、ペレット等であり得ることは了解されるべきである。1つの実施形態では、鎖から形成される微粒子は、約0.1mmから約3.0mmの直径を有する楕円体である。もう1つの実施形態では、鎖から形成される微粒子は、約0.1から約3.0mmの長さ及び約0.1から約3.0mmの直径を有する円柱状である。
【0141】
多層押出物から粒子が形成されるとき、粒子の形状は、変形円柱状(例えば上部及び/又は底部が屈曲している円柱状側面を有する;側面はある程度屈曲しており、実質的に扁平な上部及び/又は底部を有する、又はそれらの組合せ)、卵型、楕円形等、又はそれらの何らかの組合せをさらに含み得るが、この場合「円柱状」は、円形横断面だけでなく以下の横断面の1種以上も含み得る:角が少なくとも部分的に丸くなった形状を含む、三角形、四角形、菱形、ダイアモンド型、台形、五角形、六角形、八角形、星型(例えば3、4、5、6又はそれ以上の頂点を有する)、又はそれらの何らかの組合せ。1つの実施形態では、形成される微粒子は、約0.1mmから約3.0mmの寸法(高さ、長さ及び幅)を有する楕円体であり得る。もう1つの実施形態では、形成される微粒子は、類似の寸法を有する円柱状であり得る。
【0142】
同様に、押出物がシートであるとき、金型口の寸法及び/又は横断面輪郭は、生じる多層シートの厚さ及び形状を変化させるように調節することができる。例えば金型口は長方形横断面輪郭に限定されず、台形特徴(すなわち押出物の上部の幅が押出物の底部の幅より小さい場合、又はその逆の場合)を有し得るか;多層シート又はラミネートの幅及び/又は厚さに関してある程度の屈曲を有し得るか(すなわち厚みが押出物の幅に沿って変化するように、上部及び/又は底部面が凹型及び/又は凸型屈曲を有し得る;1つの実施形態では、金型口開口部は非常に扁平な卵形を有する);又はそれらの何らかの組合せを有し得る。例えば円形横断面を有する口は、約0.1mmから約50mm、あるいは約0.5mmから約20mm、例えば約1mmから約10mmの直径を有する多層シート又はラミネートを提供するように調節することができる。
【0143】
粒子に成形した後、共押出粒子を収集し、そのような固体医薬組成物が使用されるいかなる方法でも使用することができる。場合により、粒子に成形した後、粒子をNo.16 TBC(約0.054")及びNo.26 TBC(約0.031")開放スクリーンを使用する分離器に通して、収集する。好ましい実施形態では、逆作用薬を含有する共押出粒子と作用薬を含有する粒子を、患者への経口投与のための硬ゼラチンカプセル中に一緒に入れる。
【0144】
1つの実施形態では、投与剤型は、ゼラチンカプセルに入った、コア及び場合によりシェルを含む複数の粒子を含有する。
【0145】
1つの実施形態では、投与剤型は、ゼラチンカプセルに入った、コア、場合により鞘、及びシェルを含む複数の粒子を含有する。
【0146】
コア、場合により鞘、及びシェルの組成物及び寸法が、作用薬の所望放出速度を達成するように変化させ得ることは、製薬押出技術の当業者には明白である。例えば共押出金型出口寸法を変えることにより、コア、鞘及びシェルの厚さを変化させ得る。ある実施形態では、コア、鞘及びシェルの厚さは各々約0.05mmから約3.0mmであり得る;1つの実施形態では、約0.2mmから約1.0mmであり得る。鞘の所望の厚さは、例えば疎水性マトリックス材料の溶解速度及びコアの厚さによって決定され得る。ある実施形態では、鞘の厚さは約0.05mmから約3.0mmである;1つの実施形態では、約0.1mmから約1.0mmである。シェルの厚さは、例えばシェル組成物及び作用薬の所望放出速度に基づいて調節することができる。ある実施形態では、シェルの厚さは約0.05mmから約3.0mmであり得る;1つの実施形態では約0.1mmから約1.0mmであり得る。ある実施形態では、コア、任意の鞘、及びシェルの厚さは、約5.0mm以下の最大寸法;1つの実施形態では、約3.0mm以下の最大寸法、を有する粒子を提供するように調節することができる。
【0147】
1つの実施形態では、投与剤型は複数のMEMを含む。場合により、切断及び/又はパンチ後、粒子を、例えばNo.16 TBC及びNo.26 TBC開放スクリーンを使用する分離器に通して、収集することができる。1つの実施形態では、粒子を、患者への経口投与のための硬又は軟ゼラチンカプセルに入れる。
【0148】
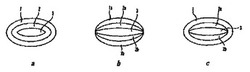
図1a、1b及び1cは、本発明の共押出粒子又は錠剤の3つの実施形態の透視図を示す。図1a、1b及び1cの各々において、コア3は逆作用薬と疎水性材料を含有する。図1aにおいて、疎水性材料を含有する鞘2は、コア3を完全に覆って取り囲む。シェル1は、作用薬と疎水性材料を含有し、鞘2を完全に覆って取り囲む。
【0149】
図1bに示す実施形態では、鞘2は、上方鞘成分2aと下方鞘成分2bを含む。鞘2はコア3の上部と底部を取り囲むが、少量のコア3を粒子の側面に沿って露出したまま残す。同様に、シェル1は、上方シェル成分1aと下方シェル成分1bを含む。シェル1は鞘2の上部と底部を取り囲むが、鞘2及び/又はコア3の小さな部分を粒子の側面に沿って露出したまま残す。
【0150】
図1cでは、鞘2は、コア3の上部と底部を取り囲み、コア3の小さな部分を側面に沿って露出したまま残す、上方鞘成分2aと下方鞘成分2bを含む。この実施形態では、シェル1は鞘2とコア3の両方を完全に覆って取り囲む。
【0151】
ある実施形態では、吸着剤/逆作用薬は、押出された粒子又は共押出された多層粒子のコア中に存在する。吸着剤/逆作用薬を含有するコアは、場合により1種以上の結合剤、付加的な遅延剤、可塑剤、及び/又は賦形剤を含み得る。結合剤は、マトリックスの完全性を維持するために有用であり、また体液中への逆作用薬の放出を防止する、阻止する又は遅延させるのに役立ち得る。結合剤の例は、天然及び合成ろう、水不溶性ろう、脂肪アルコール、例えばステアリルアルコール、脂肪酸、例えばステアリン酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、及び炭化水素骨格を有する疎水性及び親水性ポリマー、水溶性ポリマー、例えばヒドロキシセルロース、並びに前記のいずれか2つ以上の混合物を含む。
【0152】
可塑剤は、疎水性マトリックス材料がセルロースポリマー又はアクリルポリマーを含むとき有用である。適切な可塑剤の非限定的な例は、例えばアセチルトリエチルシトレート及び/又はアセチルトリブチルシトレートを含む。
【0153】
吸着剤/逆作用薬含有コアはまた、押出の間の製剤の加工性を改善するため及び/又は最終生成物の性質を改善するために添加することができる、他の賦形剤も含み得る。液体賦形剤の非限定的な例は、水及び、石油、動物、植物又は合成起源のものを含む油、例えば落花生油、ダイズ油、鉱物油、ゴマ油、ヒマシ油、トリグリセリド等を含む。固体賦形剤の例は、ステアリン酸マグネシウム、食塩水、アカシアゴム、ゼラチン、デンプンペースト、滑石、ケラチン、コロイド状シリカ、尿素等を含む。着色料もコアに添加し得る。賦型剤は吸着剤材料と同じであってもよく又は異なっていてもよい。
【0154】
ある実施形態では、本発明の投与剤型のコアは、シェルに関して5.8.2.1章で開示する物質の1種以上を含み得る。
【0155】
5.8.2.1
鞘(Sheath)
ある実施形態では、本発明の投与剤型は、吸着剤/逆作用薬を含有するコアを少なくとも部分的に取り囲む、好ましくは吸着剤/逆作用薬を含有するコアの大部分を取り囲む鞘を含み得る。ある実施形態では、鞘は、好ましくは疎水性マトリックス材料を含み、及び場合により結合剤、付加的な遅延剤、可塑剤及び賦形剤を含む。ある実施形態では、鞘は小さなパーセンテージの逆作用薬及び/又は作用薬を含有し得るが、鞘はいかなる逆作用薬又は作用薬も含有しないことが好ましい。
【0156】
1つの実施形態では、鞘の疎水性マトリックス材料は、アクリル酸及びメタクリル酸のポリマー及びコポリマー、及び疎水性被覆材料について上述した水不溶性アルキルセルロースからなる群より選択される1種以上の物質を含む。鞘は、場合により1種以上の付加的な疎水性材料、例えばコアについて上述したような、シェラック、ゼイン、硬化ヒマシ油、硬化植物油及びそれらの混合物を含有し得る。
【0157】
鞘において使用される疎水性マトリックス材料は、場合により疎水性被覆材料として使用されるものと同じであってもよく又は異なっていてもよい。鞘において使用される疎水性材料は、好ましくは胃腸管内で実質的に不溶性であるが、この材料はインビボである限られた程度まで経時的に溶解又は生分解することができ、それによって吸着剤材料からの少量の逆作用薬がコアからインビボ放出することを許容する。製薬技術の当業者は、例えば鞘の組成物を変えること、鞘の厚さを上昇させること、コアのより大きな割合を鞘で取り囲むこと、コアの大きさ及び/又は寸法を変えること、及び/又は鞘及び/又はコアの組成物を変えることによって、そのような放出の速度を変化させることができる。これらや他の方法は、当業者に公知であるか又はこの開示を考慮して常用実験によって決定され得る。
【0158】
ある実施形態では、鞘は、約10重量%から約99重量%、好ましくは約40重量%から約95重量%、より好ましくは約60重量%から約90重量%の1種以上の疎水性マトリックス材料を含有し得る。
【0159】
鞘は、1種以上の付加的な遅延剤、あるいは1種以上の結合剤又は可塑剤又は賦形剤、あるいはそれらの何らかの組合せ、例えば逆作用薬含有コアに関して5.8.2章で上述したものをさらに含有し得る。
【0160】
5.8.2.2
シェル
ある実施形態では、本発明の投与剤型は、作用薬を含有するシェルを含み得る。投与剤型は、投与後にシェルからインビボで作用薬の何らかの速度の放出、例えば即時放出、制御放出又は遅延放出を提供することができる。ある実施形態では、投与剤型は、作用薬、例えばオピオイドアゴニストの制御放出を提供する。オピオイドアゴニストの制御放出投与剤型の製剤及び製造の方法は、当技術分野において公知である。例えば、各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第5,958,452号;同第5,965,161号;同第5,968,551号;同第6,294,195号及び同第6,335,033号は、制御放出オピオイドアゴニスト投与剤型を開示する。そのような特許の1つ以上の開示は、制御放出オピオイドアゴニスト投与剤型についての詳細、例えば製剤、疎水性マトリックス材料、遅延剤、結合剤、可塑剤及び賦形剤、並びにMEMを含有する錠剤、カプレット及びカプセルを形成するための押出方法を含む。
【0161】
ある実施形態では、作用薬は、経口投与後インビボで作用薬の制御放出を提供するマトリックス中に分散し得る。医薬組成物又は投与剤型を製造するためのいかなる適切な制御放出マトリックスも使用できる。ある種の制御放出マトリックスが経口製剤に関して公知である(例えばその開示全体が全ての目的に関して参照により明白に本明細書に組み込まれる、Lee et al., "Controlled-Release Drug-Delivery Systems" in Remington's: The Science and Practice of Pharmacy 903-929 (20th ed.2000)参照)。上記で特定した特許及び出版物に開示されている制御放出投与剤型に加えて、有用な制御放出マトリックスの他の例は、各々その内容全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第6,143,328号;同第5,266,331号;同第5,549,912号;同第5,508,042号;同第5,656,295号;同第5,324,351号;同第5,356,467号及び同第5,472,712号に述べられている。
【0162】
制御放出マトリックスは、場合により親水性材料と組み合わせた、可融疎水性材料を含み得る。可融疎水性材料は、例えば約45℃から約100℃の融点、1つの実施形態では約50℃から約90℃の融点を有し得る、例えば疎水性ポリマーあるいは天然又は合成ろう又は油、例えば硬化植物油又は硬化ヒマシ油であり得る。疎水性材料は、疎水性被覆材料として使用されるものと同じであり得る。親水性材料は、親水性ポリマー、例えばヒドロキシセルロース;水溶性可融物質、例えばポリエチレングリコール;水溶性微粒子物質、例えばラクトース;又はわずかに水溶性の微粒子物質、例えばリン酸二カルシウムであり得る。
【0163】
本発明に従った制御放出投与剤型を製造するため、任意の公知の共押出方法を使用できるが、好ましい方法は、適切なマトリックス材料と成分の溶融共押出である。例えば制御放出マトリックスに分散した作用薬を含有するシェルは、例えば以下の1種以上を含むがこれらに限定されない、適切な非可融材料と共に作用薬を押出することによって製造することできる:
【0164】
(a)親水性又は疎水性ポリマー、例えばゴム、セルロースエーテル、タンパク質由来物質、ナイロン、アクリル樹脂、ポリ乳酸、ポリ塩化ビニル、デンプン、ポリビニルピロリドン、及びセルロースアセテートフタレート。これらのポリマーのうちで、セルロースエーテル、例えば置換セルロースエーテル、例えばアルキルセルロース(例えばエチルセルロース)、C1−C6ヒドロキシアルキルセルロース(例えばヒドロキシプロピルセルロース及びヒドロキシエチルセルロース)、及びアクリル樹脂(例えばメタクリレート、例えばメタクリル酸コポリマー)が使用できる。制御放出マトリックスは、好都合には約1重量%から約80重量%の疎水性及び/又は親水性ポリマーを含有し得る。
【0165】
(b)可消化、長鎖(C8−C50、1つの実施形態ではC8−C40)置換又は非置換炭化水素、例えば脂肪酸;硬化植物油;脂肪アルコール、例えばラウリル、ミリスチル、ステアリル、セチル又は、1つの実施形態ではセトステアリルアルコール;脂肪酸のグリセリルエステル、例えばモノステアリン酸グリセリル;鉱物油;及びろう、例えば蜜ろう、グリコワックス、カスターワックス、及びカルナウバろう。1つの実施形態では約25℃から約90℃の融点を有する炭化水素を使用する。これらの長鎖炭化水素物質のうちで、脂肪アルコールは1つの実施形態において有用である。制御放出マトリックスは、約60重量%までの少なくとも1つの可消化長鎖炭化水素を含有し得る。
【0166】
(c)ポリアルキレングリコール。制御放出マトリックスは、約60重量%までの少なくとも1つのポリアルキレングリコールを含有し得る。ポリアルキレングリコールは、例えばポリプロピレングリコール、又は1つの実施形態ではポリエチレングリコールであり得る。ポリアルキレングリコールの数平均分子量は、1つの実施形態では約200から約15,000ダルトンであり、もう1つの実施形態では約400から約12,000ダルトンである。
【0167】
1つの実施形態では、本発明の投与剤型における使用のための適切な制御放出マトリックスは、1種以上のセルロースエーテル又はアクリル樹脂、あるいは1種以上のC12−C36脂肪アルコール;もう1つの実施形態では、C12−C22脂肪アルコール及び/又は1種以上の硬化植物油を含み得る。1つの実施形態では、特に適切なマトリックスは、1種以上のアルキルセルロース、あるいは1種以上のC12−C36脂肪アルコール;もう1つの実施形態では、C12−C22脂肪アルコール及び、場合により、1種以上のポリアルキレングリコールを含む。もう1つの実施形態では、マトリックスは、約0.5重量%から約60重量%、もう1つの実施形態では約1重量%から約50重量%のセルロースエーテルを含有し得る。
【0168】
アクリル樹脂は、例えばメタクリレート、例えばメタクリル酸コポリマー、USNF A型(EUDRAGIT L)、B型(EUDRAGIT S)、C型(EUDRAGIT L 100-55)、EUDRAGIT NE 30 D、EUDRAGIT E、EUDRAGIT RL、又はEUDRAGIT RS(Rohm Pharma GmbH, Weiterstat, Germanyから市販されている)であり得る。1つの実施形態では、マトリックスは、約0.5重量%から約95重量%のアクリル樹脂、もう1つの実施形態では約10重量%から約50重量%のアクリル樹脂を含有する。
【0169】
ポリアルキレングリコールが存在しない場合、マトリックスは、1つの実施形態では約1重量%から約40重量%、もう1つの実施形態では約2重量%から約36重量%の脂肪アルコールを含有する。ポリアルキレングリコールが経口投与剤型中に存在するときは、脂肪アルコールとポリアルキレングリコールの合計重量は、1つの実施形態ではマトリックスの約2重量%から約40重量%、もう1つの実施形態ではマトリックスの約2重量%から約36重量%を構成する。
【0170】
ポリアルキレングリコールは、例えばポリプロピレングリコール又は、1つの実施形態ではポリエチレングリコールであり得る。ポリアルキレングリコールの数平均分子量は、1つの実施形態では約200〜約15,000ダルトン、もう1つの実施形態では約400〜約12,000ダルトンである。
【0171】
錠剤製剤を製造するための方法
上述したように、本発明はまた、吸着剤/逆作用薬を含有する錠剤又は粒子に関する。本発明の吸着剤/逆作用薬を含有する錠剤は従来の手段によって製造することができる(例えば、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、Rudnic et al., "Oral Dosage Forms" in Remington's: The Science and Practiceof Pharmacy 858-885 (20th ed. 2000)参照)。1つの実施形態では、粒子又は錠剤は、作用薬と吸着剤/逆作用薬を含有する製剤を造粒し、圧縮することによって製造される。
【0172】
もう1つの実施形態では、錠剤は、作用薬を含有する複数の第一粒子及び吸着剤/逆作用薬を含有する複数の第二粒子を圧縮することによって製造される。
【0173】
もう1つの実施形態では、粒子又は錠剤は、吸着剤/逆作用薬を含有するコア及び作用薬を含有するシェルを含み、シェルがコアを少なくとも部分的に覆う投与剤型を造粒し、圧縮することによって製造される。
【0174】
粒子又は錠剤は、何らかの幾何学的形状、例えば球、長円体、ペレット等であり得、製造の方法、作用薬及び吸着剤/逆作用薬の量及び種類、及び標的とする患者に依存していかなる寸法においても大きさが異なり得ることは了解されるべきである。ある実施形態では、本発明の錠剤は、いかなる方向でも約5mmから約75mmの寸法を有する;もう1つの実施形態では、錠剤は、いかなる方向でも約5mmから約30mmの寸法を有する;及びもう1つの実施形態では、錠剤は、いかなる方向でも約5mmから約15mmの寸法を有する。
【0175】
本発明の粒子又は錠剤は、上記5.8.2.1章で定義したような製薬上許容し得る疎水性被覆材料;賦形剤、例えば結合剤(例えばプレゼラチン化トウモロコシデンプン、ポリビニルピロリドン又はヒドロキシプロピルメチルセルロース);充填剤(例えばラクトース、微結晶セルロース又はリン酸水素カルシウム);潤滑剤(例えばステアリン酸マグネシウム、滑石又はシリカ);崩壊剤(例えばジャガイモデンプン又はグリコール酸デンプンナトリウム);湿潤剤(例えばラウリル硫酸ナトリウム);及び当技術分野で周知の他の添加物又は賦形剤をさらに含み得る。錠剤は、そのような被覆が錠剤の意図される使用を妨げないことを条件として、当技術分野で周知の方法によって被覆することができる。被覆工程の非限定的な例は、噴霧被覆である。1つの実施形態では、錠剤は浸漬被覆によって形成される。
【0176】
溶融押出組成物から錠剤を製造するための他の方法は上記に述べられている。
【0177】
投与のための方法
本発明はまた、治療の必要のある患者に本発明の投与剤型を投与することを含む、患者において病気を治療するための方法を対象とする。投与剤型は、例えば経口投与剤型、例えば錠剤又はカプセル、あるいは直腸又は膣投与剤型、例えば坐薬であり得る。1つの実施形態では、病気は疼痛であり、投与剤型はオピオイドと吸着剤/オピオイドアンタゴニストを含有する。ある実施形態では、投与剤型を1日2回患者に投与し、他の実施形態では1日1回投与する。
【0178】
投与単位当りの量
本発明の投与剤型では、投与単位当りの作用薬の量は、その特定適応症についての有効量であり、逆作用薬の量とは無関係である。例えば治療薬がオピオイドアゴニストである場合、本発明の投与剤型中のオピオイドアゴニストの量は約1mgから約800mg;1つの実施形態では約5mgから約160mgである。当業者は、過剰な実験を必要とせずに、特定適応症のために必要な治療薬の量を容易に決定することができる。
【0179】
本発明の投与剤型中の逆作用薬の量は、不正使用されたとき実質的な量の逆作用薬が直ちに投与剤型から放出され、動物の血液中に吸収された場合に、逆作用薬が意図される逆作用を与えることができる量である。投与剤型が不正使用された場合、逆作用薬が作用薬の薬理作用の1種以上、例えば陶酔作用を低減する又は排除することが意図されているとき、投与剤型中の逆作用薬の量は、少なくとも、不正使用が起こった後両方の薬剤が投与剤型から実質的に又は完全に放出されて動物の血液中に吸収されたとき、作用薬の作用を低減する又は排除するのに十分である。
【0180】
例えば、1つの実施形態では、逆作用薬がオピオイドアンタゴニスト、例えばナルトレキソン又はナルメフェンであるとき、本発明の投与剤型中に存在するオピオイドアンタゴニストの量は、約0.1mgから約50mg又はそれ以上であり得る。オピオイドアンタゴニスト、シクラゾシン及びナルトレキソンは、経口投与したとき、24時間に近い長い作用期間にわたってそれらの効果の多くを保持する。これらのオピオイドアンタゴニストの約10mg未満の量を本発明の経口製剤において使用する。
【0181】
不正使用された場合、逆作用薬が望ましくない生理的反応、例えば嘔吐を引き起こすことが意図されているとき、投与剤型中の逆作用薬の量は、少なくとも、不正使用が起こった後の放出時にそのような作用を引き起こすのに十分である。
【0182】
安全性の理由から、投与剤型中に存在する逆作用薬の量は、全部が直ちに放出された場合でもヒトに対して有害であってはならない。当業者は、過剰な実験を必要とせずに、有害性を伴わずに意図される逆作用を惹起するために必要な逆作用薬の量を容易に決定することができる。
【0183】
本発明のある実施形態では、投与剤型中の治療薬対逆作用薬の比率は、重量比で約1:1から約50:1、1つの実施形態では重量比で約1:1から約20:1であり得る。他のある実施形態では、前記比率は、重量比で約1:1から約10:1であり得る。
【0184】
オピオイドアゴニストがヒドロコドンである非限定的実施形態では、制御放出投与剤型は、投与単位当りヒドロコドン約5mgから約80mgの鎮痛用量を含有し得る。オピオイドアゴニストがヒドロモルフォンである非限定的実施形態では、投与単位当り塩酸ヒドロモルフォン約2mgから約64mgの量で含有され得る。オピオイドアゴニストがモルフィンである非限定的実施形態では、投与単位当りモルフィン約2.5mgから約800mgが投与剤型中に存在し得る。オピオイドアゴニストがオキシコドンである非限定的実施形態では、投与剤型は、投与単位当りオキシコドン約2.5mgから約160mg、もう1つの実施形態では、オキシコドン約20mgから約30mgを含有し得る。制御放出オキシコドン製剤は当技術分野において公知である。非限定的実施形態では、オピオイドアゴニストは、投与単位当り約25mgから800mgの量のトラマドールであり得る。投与剤型は1種以上のオピオイドアゴニストを含有することができ、各々の用量は適宜に調節することができる。
【0185】
「単位用量」という用語は、本発明に関して、作用薬(例えばオピオイドアゴニスト)の単回所望用量を患者に投与するために必要な投与剤型の総量と定義される。
【0186】
膣又は直腸投与のための方法
上述したように、本発明はまた、膣又は直腸を通した吸収のための坐薬の形態の、作用薬及び吸着剤/逆作用薬を含有する投与剤型の投与を対象とする。坐薬として投与するとき、組成物は、好ましくは坐薬基材を含む。微粒子を溶解しないことを条件として、いかなる坐薬基剤も使用することができる。例えばココアバターは、その融点をわずかに上昇させるためにろうの添加によって改変し得る、伝統的な坐薬基材である。1種以上の水混和性坐薬基材、例えば様々な分子量のポリエチレングリコールが含まれ得る。坐薬として投与したとき、坐薬製剤中の複数の第一及び第二粒子の合計濃度は、1つの実施形態では、組成物の約5.0重量%から約80重量%である。
【0187】
キット
本発明はまた、少なくとも1つの本発明の投与剤型を含むキットを対象とする。1つの実施形態では、投与剤型は容器、例えばビン又は箱の中に存在する。もう1つの実施形態では、キットは、例えば疼痛のために、患者を治療するための投与剤型の使用を指示する説明書のセットをさらに含む。1つの実施形態では、説明書は、容器に貼付された印刷ラベルであるか又は容器上に印刷され得る。もう1つの実施形態では、説明書は、容器中又は容器を含む包装中に挿入された印刷紙を含み得る。説明書はまた、投与剤型及び/又はその使用が投与剤型の乱用、誤用又は転用を低減するように設計されていることを言明し得る。
【0188】
本明細書において言及する全ての特許、特許出願、試験方法、文献、及び他の資料は、全ての目的に関してそれらの全体が参照により明白に本明細書に組み込まれる。
【0189】
実施例
以下の実施例は本発明の理解を助けるために提示するものであり、本明細書で説明し、特許請求する本発明を、特定して限定すると解釈されるべきではない。当業者の範囲内である、現在公知の又は今後開発される全ての等価物の置換、及び製剤の変更又は実験計画の重要でない変更を含む、本発明のそのような変法は、本発明の範囲内に属するとみなされるべきである。
【実施例1】
【0190】
炭/ナルトレキソンの製造及び性質
実施例1は、吸着剤/逆作用薬を製造するための非限定的な方法を説明する。使用した吸着剤は、Merck KGaA of Darmstadt,Germanyの系列会社であるEM Scienceより入手したDARCO活性炭であった。使用したDARCO活性炭は、活性炭についてのUSP吸収能試験(米国薬局方 26:404(2003)参照)に合格した20から40メッシュの黒色粒状炭であった。
【0191】
ナルトレキソンの吸着: 活性炭(5.02g)を、0.1N HCl(900mL)中の塩酸ナルトレキソン(504.26mg)(Mallinkrodt,St.Louis MOより入手した)の溶液に添加した。生じた混合物を37℃、100rpmで120時間攪拌し、高性能液体クロマトグラフィー(HPLC)を用いて液相中の塩酸ナルトレキソンの濃度低下を測定することにより、活性炭への塩酸ナルトレキソンの吸着(又は取込み)を観測した。そのデータを使用して、例えば2時間後の、活性炭に吸着されたナルトレキソンの量を以下のように算定した:
【0192】
吸着されたナルトレキソン
=(ナルトレキソン(初期))×〔1−(HPLCピーク面積(T=2時間)/HPLCピーク面積(T=0))〕
【0193】
吸着されたナルトレキソン
=(504.26mg)×〔1−(215860/483568)〕=279.16mg
【0194】
データを表2に示し、図2にグラフで表す。
【0195】
【表2】

【0196】
結果は、実質的に全部のナルトレキソンの吸着が約1.5時間以内に完了したことを示した。混合物を、半融ガラスフリットを用いて真空ろ過した。炭吸着剤ナルトレキソン逆作用薬を自由流動粉末(「炭/ナルトレキソン」)として与えるために、生じたろ過ケーキを動的真空下でガラスフリット上に維持した。図2のデータに基づき、工程終了時(t=2時間)の炭/ナルトレキソン中の塩酸ナルトレキソンの算定含量は5.56重量%であった。
【0197】
炭/ナルトレキソンの動的脱着: 上述したように調製した炭/ナルトレキソンを1リットル半融ガラスろ過漏斗に移し、25℃で0.1N HClの63×1Lアリコート(63 1L aliquots)によって洗浄した。洗浄ろ液中の塩酸ナルトレキソンの濃度を、上述したようにHPLCを用いて測定した。結果を表3に示し、図3にグラフで表す。
【0198】
【表3】

【0199】
結果は、塩酸ナルトレキソンの脱着の大部分が最初の18回の洗浄工程の間に生じたことを示した。
【実施例2】
【0200】
酸洗浄した炭/ナルトレキソンの製造及び性質
酸洗浄: 最後の洗浄後、実施例1から生じたケーキを、酸洗浄した炭/ナルトレキソン(「酸洗浄炭/ナルトレキソン」)の乾燥自由流動固体形態を与えるためにろ過フラスコで乾燥した。乳鉢と乳棒を用いて固体の一部を微細粉末に摩砕し、その後以下のようにメタノールで抽出することによって酸洗浄炭/ナルトレキソン中の塩酸ナルトレキソン含量を測定した。計量した摩砕酸洗浄炭/ナルトレキソンの一部(約50mg)を100mLメスフラスコに添加し、メタノール50mLを加えて、約25℃で、生じた混合物を15分間超音波処理した。超音波処理後、混合物を放置して約25℃に冷却させた。4.000mLアリコートをピペットで取り出し、250mLメスフラスコに移して、0.1N HClで250.00mLに希釈した。希釈した混合物を25℃で15〜30分間振とうし、生じた混濁液体をWhatman HXナイロンろ紙を通してろ過した。次に、ろ液中のナルトレキソンの濃度を、ナルトレキソン標準品に対してHPLCを用いて測定した。平均ナルトレキソン含量(n=摩砕した酸洗浄炭/ナルトレキソンの3試料)は3.06重量%であった。
【0201】
酸洗浄炭/ナルトレキソンの静的脱着: 上記からの酸洗浄炭/ナルトレキソンの一部(約50mg)を、37℃の温度で0.1N HCl 900mLを含むパドル付き2000mLビーカーに添加した。ビーカーの内容物を100rpmで72時間混合し、HPLCを用いて液相中のナルトレキソン濃度を観測した。静的脱着試験において得られたデータを、薬剤全部が脱着された場合のナルトレキソンの理論的濃度に基準化した。データを表4に示し、図4にグラフで表す。各々の点は酸洗浄炭/ナルトレキソンのn=6試料の平均値に相当する。
【0202】
【表4】

【0203】
結果は、脱着可能なナルトレキソンの大部分(全部ではない)が、最初の36時間以内に脱着することを示した。静的脱着の72時間後の液相中のナルトレキソンの含量に基づき、酸洗浄炭/ナルトレキソン中に残存するナルトレキソンの算定含量は、その初期値(3.06重量%)の61%又は約1.9重量%であった。
【0204】
上記脱着試験の結果は、吸着剤/逆作用薬、例えば炭/ナルトレキソンが、逆作用薬の望ましくない放出を防止するために有用であることを示した。
【実施例3】
【0205】
疎水性マトリックス材料で密封した炭/ナルトレキソンの製造及び性質
疎水性材料での炭/ナルトレキソンの密封: ステアリルアルコール(約10〜15g)を含むビーカーを高温プレート上に置き、熱を加えてアルコールを溶融し、溶融物を67℃の温度までさらに加熱した。実施例1で製造した炭/ナルトレキソンの一部(200.41mg)を100メッシュのUSP溶解バスケットに添加した。バスケットを5〜10分間前記溶融物中に完全に液浸し、炭/ナルトレキソンの被覆を助けるために往復運動で上下に動かした。バスケットを溶融物から取り出し、放置して周囲温度に冷却して、密封された炭/ナルトレキソン(「密封炭/ナルトレキソン」)(472.45mg)を、白色の陰影を伴う黒色固体として得た。密封炭/ナルトレキソン中の塩酸ナルトレキソンの含量を、炭/ナルトレキソン出発物質の重量及びそのナルトレキソン含量(3.06重量%)を密封炭/ナルトレキソン生成物の重量と共に使用して算定した。
【0206】
ナルトレキソン含量
=(3.06重量%)×〔(炭/ナルトレキソンの重量)/(密封炭/ナルトレキソンの重量)〕
【0207】
ナルトレキソン含量
=(3.06重量%)×〔(200.14mg)/(472.45mg)〕=1.30重量%
【0208】
密封炭/ナルトレキソンの静的脱着: 密封炭/ナルトレキソンの一部(約77mg)を、0.1N HCl(900mL)を含むパドル付き2000mLビーカーに添加し、内容物を37℃、100rpmで72時間混合した。HPLCを用いて液相中のナルトレキソン濃度を観測した。静的脱着試験において得られたデータを表5に示し、図5にグラフで表しており(−○−○−○−)、密封炭/ナルトレキソンのn=6試料の平均値を示す。比較として、実施例1で製造した炭/ナルトレキソン(−□−□−□−)(n=6試料)に関して同じデータを収集し、図5にグラフで表した。
【0209】
【表5】

【0210】
炭/ナルトレキソンを72時間混合した後、液相中の塩酸ナルトレキソンの濃度は約610ng/mLであった。これに対し、密封炭/ナルトレキソンを72時間混合した後、液相中の塩酸ナルトレキソンの濃度はわずかに約42ng/mLであった。結果は、炭/ナルトレキソンを適切な疎水性被覆材料で密封することは吸着剤からの逆作用薬の望ましくない放出をさらに防止することを示した。
【実施例4】
【0211】
疎水性マトリックス材料で密封した酸洗浄炭/ナルトレキソンの製造
疎水性材料での酸洗浄炭/ナルトレキソンの密封: 実施例2で製造した酸洗浄炭/ナルトレキソンを使用して、実施例3で述べたステアリルアルコール被覆手順を反復した。密封した酸洗浄炭/ナルトレキソン(「密封酸洗浄炭/ナルトレキソン」)中の塩酸ナルトレキソンの含量を、酸洗浄炭/ナルトレキソン出発物質の重量及びそのナルトレキソン含量(3.06重量%)を密封酸洗浄炭/ナルトレキソンの重量と共に使用して算定した。密封酸洗浄炭/ナルトレキソン生成物中の塩酸ナルトレキソンの平均含量(密封酸洗浄炭/ナルトレキソンのn=6試料に基づく)は1.30重量%であった。
【0212】
密封酸洗浄炭/ナルトレキソンのインビトロ脱着: 密封酸洗浄炭/ナルトレキソンの一部(約250mg)を、37℃で0.1N HCl 900mLを含む、パドル付きUSP 2型溶解容器に添加し、溶解容器の内容物を100rpmで120時間混合した。液相の分析(HPLC)は、少なくとも120時間にわたって検出可能なナルトレキソンが放出されなかったことを示した。
【実施例5】
【0213】
不正使用時の密封酸洗浄炭/ナルトレキソンからのナルトレキソンの放出
実施例4からの密封酸洗浄炭/ナルトレキソンの試料を、微細分割された粉末が形成されるまで乳鉢と乳棒を用いて破砕した。計量した試料の部分(各々約0.025g)を、脱イオン蒸留水(pH6.5)又は水中40%エタノールのいずれか10.00mLを含むシンチレーションバイアルに添加した。生じた混合物を25℃又は100℃で10分間、手で振とうすることによって抽出した。次に、試料の液相中のナルトレキソンの含量を、公知のナルトレキソン標準品に対してHPLCを用いて測定し、結果を以下の表6に示す。また表6は、水又はメタノール中25℃で抽出した破砕していない密封酸洗浄炭/ナルトレキソンについての比較データも含む。
【0214】
【表6】

【0215】
試験の結果は、不正使用、例えば破砕、に供していない密封酸洗浄炭/ナルトレキソンは有意の量のナルトレキソンを放出しない、すなわち約0mgのナルトレキソンが放出されたことを示した。結果はまた、不正使用、例えば破砕後に水又はアルコール含有溶媒による抽出、に供した密封酸洗浄炭/ナルトレキソンの試料がナルトレキソンを放出することを示した。表6のデータはさらに、密封酸洗浄炭/ナルトレキソンの破砕試料からの放出の程度が高温で上昇することを示した。結果は、密封酸洗浄炭/ナルトレキソンが不正使用防止投与剤型において有用であることを示す。
【図面の簡単な説明】
【0216】
【図1】図1a、1b及び1cは、本発明の投与剤型の3つの実施形態の透視図を示す。
【図2】塩酸ナルトレキソンの活性炭への吸着(mg)を時間の関数として示すグラフである。
【図3】活性炭からの塩酸ナルトレキソンの脱着(ng/mL洗浄液)を洗浄液リットルの関数として示すグラフである。
【図4】活性炭からの塩酸ナルトレキソンの脱着(%)を時間の関数として示すグラフである。
【図5】インビトロ刺激溶解試験におけるa)密封活性炭及びb)非密封活性炭からの塩酸ナルトレキソンの脱着(μg)を時間の関数として示す比較グラフである。
【技術分野】
【0001】
本出願は、その開示全体が全ての目的に関して明白に参照により本明細書に組み込まれる、2004年3月30日出願の米国特許仮出願第60/558,301号の優先権を主張する。
【0002】
本発明は、活性薬剤、例えばオピオイド、を含有する投与剤型の不正使用、乱用、誤用又は転用を防止する又は阻止するために有用な、吸着剤及び逆作用薬、例えばオピオイドアンタゴニスト、を含有する医薬組成物及び投与剤型に関する。本発明はまた、そのような投与剤型で患者を治療するための方法、並びにそのような剤型と患者を治療するために前記投与剤型を使用するための説明書とを含むキットに関する。本発明はさらに、そのような医薬組成物及び投与剤型を製造するための方法に関する。
【背景技術】
【0003】
毒物又は薬剤の意図されたものでない又は不法な使用の治療又は防止に多大の努力が注がれてきた。例えば過剰の薬剤又は毒物を摂取した患者のための1つの治療は、吸着剤、例えば活性炭の投与を含む(Remington's: The Science and Practice of Pharmacy 1238 (20th ed. 2000)参照)。活性炭は、薬剤又は毒物の一部を吸着し、それが循環系に入るのを防ぐことが意図されている。
【0004】
Proctorらへの米国特許第4,594,249号は、アルコール摂取の直前、摂取中又は摂取直後のアルコール消費者への活性炭の投与による、アルコール飲料の摂取の後作用を軽減するための方法を開示する。
【0005】
ニシムラ(Nishimura)への米国特許第4,761,284号は、その開示によれば、医薬組成物の崩壊を伴わずに患者の胃腸管において外因性又は内因性毒素を吸着するために有用な活性炭の球状粒子を含有する医薬組成物を開示する。
【0006】
米国特許出願公開第2002/0155103 A1号は、その開示によれば、アルコール摂取に関連する後作用の発現を予防する又は遅延させるために有用な活性炭と石灰石を含有する組成物を開示する。
【0007】
また、投与剤型、例えばオピオイド鎮痛薬剤型、の不正使用防止性を高めるための試みが当技術分野において為されてきた。不正使用防止オピオイド投与剤型の開発へのこれまでのアプローチには、オピオイドアゴニストをオピオイドアンタゴニストと組み合わせることが含まれていた。そのような組合せの特定例は、メタドンとナロキソン(Pachterらへの米国特許第3,773,955号);メタドール又はアセチルメタドールとナロキソン(Pachterらへの米国特許第3,966,940号);オキシコドンとナロキソン(Gordonらへの米国特許第4,457,933号);及びブプレノルフィンとナロキソン(Lewisらへの米国特許第4,582,835号)を含有する組成物を含む。
【0008】
Palermoらへの米国特許第6,228,863号は、アゴニストを単離するために少なくとも2つの分離工程を必要とする、オピオイドアゴニストとオピオイドアンタゴニストを組み合わせた経口投与剤型を開示する。
【0009】
Al-Razzakらへの米国特許第5,610,193号は、製薬上許容し得るHIVプロテアーゼ阻害剤と製薬上許容し得る吸着剤に吸着された溶媒を含有する医薬組成物を開示する。この参考文献は、前記組成物が、水に難溶性である活性化合物の経口バイオアベイラビリティーの改善を提供すると主張する。
【0010】
Oshlackらへの米国特許第6,696,088 B2号及び米国特許出願公開第2003/00073717 A1号、同第2003/0004177 A1号及び同第2003/0065002 A1号は、放出可能形態のオピオイドアゴニストと、投与剤型を無傷投与したときには実質的に放出されないオピオイドアンタゴニストを含有する経口投与剤型を開示する。
【発明の開示】
【発明が解決しようとする課題】
【0011】
改善された不正使用防止投与剤型及びそれらの製造のための改善された手法が、現在も当技術分野において求められている。
【課題を解決するための手段】
【0012】
本発明は、吸着剤と逆作用薬とを含有する医薬組成物及び投与剤型に関する。本発明はまた、そのような組成物及び投与剤型を製造するための方法に関する。本発明はさらに、そのような医薬組成物又は投与剤型で患者を治療するための方法、並びにそのような医薬組成物又は投与剤型と患者を治療するための前記組成物又は投与剤型の使用法を指示する説明書とを含むキットに関する。本発明に従った投与剤型は、カプセル又は錠剤、直腸坐剤及び膣坐剤を含むがこれらに限定されない、経口投与剤型を含むが、これらに限定されない。ある実施形態では、投与剤型は複数の粒子を含有し得る。
【0013】
1つの実施形態では、本発明は、吸着剤と逆作用薬を含有する投与剤型に関する。もう1つの実施形態では、本発明は、作用薬、吸着剤及び逆作用薬を含有する投与剤型に関する。
【0014】
もう1つの実施形態では、本発明は、作用薬を含む複数の第一粒子;及び吸着剤と逆作用薬とを含む複数の第二粒子を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型に関する。1つの実施形態では、本発明は、オピオイドアゴニストを含む複数の第一粒子;及び吸着剤とオピオイドアンタゴニストとを含む複数の第二粒子を含有し、前記第一粒子が、患者への経口投与時にオピオイドアゴニストの制御放出を提供する投与剤型に関する。
【0015】
もう1つの実施形態では、本発明は、吸着剤と逆作用薬とを含むコア;及び作用薬を含むシェルを含有し、前記シェルが前記コアを少なくとも部分的に覆う又は取り囲む投与剤型に関する。
【0016】
1つの実施形態では、前記逆作用薬の少なくとも一部が前記吸着剤の少なくとも一部に吸着されている。もう1つの実施形態では、前記逆作用薬の少なくとも大部分、すなわち50重量%が前記吸着剤の少なくとも一部に吸着されている。さらなる実施形態では、前記逆作用薬の基本的に全部が前記吸着剤の少なくとも一部に吸着されている。
【0017】
本発明の組成物及び投与剤型は、作用薬及び/又は逆作用薬の制御放出、即時放出又は遅延放出を提供することができる。
【0018】
本発明はまた、吸着剤と逆作用薬とを含有する投与剤型を製造するための方法に関する。1つの実施形態では、本発明は、吸着剤を提供すること;逆作用薬を含有する液体を提供すること;前記吸着剤を、逆作用薬を含有する前記液体と、逆作用薬の少なくとも一部が吸着剤に吸着するのに十分な時間接触させること;前記吸着剤を液相から分離すること;及び場合により、前記吸着剤を洗浄すること、を含む、投与剤型を製造するための方法に関する。
【0019】
もう1つの実施形態では、本発明は、吸着剤を提供すること;逆作用薬を含有する液体を提供すること;前記吸着剤を流動床に添加すること;前記吸着剤を流動化すること;前記液体を流動化した吸着剤に噴霧すること;及び場合により、前記吸着剤を乾燥すること、
を含む、投与剤型を製造するための方法に関する。
【0020】
本発明はまた、吸着剤と逆作用薬とを含有する本発明の投与剤型を患者に投与することを含む、病気又はその症状を治療する方法に関する。本発明の1つの実施形態では、疼痛を有する患者を治療する。
【0021】
本発明はまた、本発明の投与剤型をその必要のある患者に投与することを含む、疼痛を治療するための投与剤型の乱用、誤用又は転用を低減するための方法に関する。
【0022】
さらにもう1つの実施形態では、本発明は、少なくとも1つの本発明の投与剤型及び患者を治療するための投与剤型の使用法を指示する説明書のセットを含む、患者を治療するためのキットに関する。本発明の1つの実施形態では、キットは患者の疼痛を治療することを目的とする。
【0023】
本発明は、本発明の非制限的な実施形態の例示を意図する、以下の詳細な説明及び実施例を参照することにより、さらに十分に理解することができる。
【発明を実施するための最良の形態】
【0024】
5.1
定義
本明細書における何らかの薬剤、例えば作用薬、逆作用薬、オピオイドアゴニスト又はオピオイドアンタゴニストへの言及は、異なる規定がない限り、そのような薬剤の製薬上許容し得る形態、例えば遊離形態、製薬上許容し得る塩形態、製薬上許容し得る塩基形態、製薬上許容し得る水和物、製薬上許容し得る溶媒和物、立体異性体、光学異性体;並びにそのような薬剤のプロドラッグ及びそのような薬剤の製薬活性類似体、及び前記のいずれか2つ以上の混合物を包含する。
【0025】
本明細書で使用する「製薬上許容し得る塩」という語句は、作用薬又は逆作用薬の、酸性及び塩基性基、例えば窒素基から形成される塩であり得る。そのような塩の例は、硫酸塩、クエン酸塩、酢酸塩、シュウ酸塩、塩化物、臭化物、ヨウ化物、硝酸塩、重硫酸塩、リン酸塩、酸性リン酸塩、イソニコチン酸塩、乳酸塩、サリチル酸塩、酸性クエン酸塩、酒石酸塩、オレイン酸塩、タンニン酸塩、パントテン酸塩、重酒石酸塩、アスコルビン酸塩、コハク酸塩、マレイン酸塩、ゲンチジン酸塩、フマル酸塩、グルコン酸塩、グルカロン酸塩、サッカリン酸塩、ギ酸塩、安息香酸塩、グルタミン酸塩、メタンスルホン酸塩、エタンスルホン酸塩、ベンゼンスルホン酸塩、p−トルエンスルホン酸塩、グルビオナート及びパルモエート(すなわち1,1’−メチレン−ビス−(2−ヒドロキシ−3−ナフトエート))塩を含むが、これらに限定されない。「製薬上許容し得る塩」という用語は、選択的に、酸性官能基、例えばカルボン酸又はスルホン酸官能基を有する作用薬又は逆作用薬と、製薬上許容し得る無機又は有機塩基から生成される塩であり得る。そのような塩基の例は、アルカリ金属、例えばナトリウム、カリウム及びリチウムの水酸化物;アルカリ土類金属、例えばカルシウム及びマグネシウムの水酸化物;他の金属、例えばアルミニウム及び亜鉛の水酸化物;アンモニア、及び有機アミン、例えば不飽和又はヒドロキシ置換モノ−、ジ−又はトリアルキルアミン;ジシクロヘキシルアミン;トリブチルアミン;ピリジン;N−メチルアミン、N−エチルアミン;ジエチルアミン;トリエチルアミン;モノ−、ビス−又はトリス−(2−ヒドロキシ−低級アルキルアミン)、例えばモノ−、ビス−又はトリス−(2−ヒドロキシエチルアミン)、2−ヒドロキシ−tert−ブチルアミン、又はトリス−(ヒドロキシメチル)メチルアミン、N,N,−ジ−低級アルキル−N−(ヒドロキシ低級アルキル)−アミン、例えばN,N−ジメチル−N−(2−ヒドロキシエチル)アミン、又はトリ−(2−ヒドロキシエチル)アミン;N−メチル−D−グルカミン;及びアミノ酸、例えばアルギニン、リシン等を含むが、これらに限定されない。
【0026】
「患者」又は「動物」は、好ましくは哺乳動物であり、ウシ、サル、ウマ、ヒツジ、ブタ、ニワトリ、シチメンチョウ、ウズラ、ネコ、イヌ、マウス、ラット、ウサギ及びモルモット、及び最も好ましくはヒトを含むが、これらに限定されない。
【0027】
本明細書で使用する、「活性吸着剤」という語句は、その吸着能力を高めるために物理的及び/又は化学的処理を受けた吸着剤を意味する。
【0028】
本明細書で使用する、「作用薬」という語句は、患者の血流中に十分な量で吸収されたとき生物学的作用を生じさせる薬剤を指す。
【0029】
本明細書で使用する「吸着剤」という語句は、他の分子又は物質をその表面及び/又は孔及び/又はチャネルに保有する又は保持することができる大きな表面積及び/又はミクロ細孔容積を示す製薬上許容し得る物質を指す。
【0030】
本明細書で使用する、「吸着剤/逆作用薬」という用語は、逆作用薬がその表面及び/又は孔及び/又はチャネルの少なくとも一部に吸着されている吸着剤を指す。
【0031】
本明細書で使用する「逆作用薬」という語句は、投与剤型中に存在する作用薬の少なくとも1つの生物学的作用、例えば陶酔作用を部分的に又は完全に取り消す又は無効にする、あるいは患者又は動物の血流中に十分な量で吸収されたとき、1種以上の不快な生理的反応、例えば嘔吐、吐き気、下痢、まずい味を生じさせる薬剤を指す。
【0032】
本明細書で使用する、「制御放出」という用語は、長い時間にわたっての制御された方式での投与剤型からの作用薬のインビボ放出を指す。例えば制御放出経口投与剤型は、例えば5〜24時間にわたって薬剤を放出することができる。
【0033】
本明細書で使用する、「遅延放出」という語句は、作用薬が、投与後少なくとも1時間、投与剤型から実質的に放出されないインビボ放出工程を指す。一旦、遅延放出が起これば、投与剤型は制御放出又は即時放出によって作用薬を放出することができる。
【0034】
本明細書で使用する、「ラミネート」という用語は、2つ以上の層を含む構造、すなわち多層構造を指す。
【0035】
本明細書で使用する、「オピオイドアゴニスト」という語句は、場合により立体特異的に、オピオイド受容体のいくつかの亜種の1種以上に結合して、アゴニスト活性を生じさせる作用薬を指す。
【0036】
本明細書で使用する、「オピオイドアンタゴニスト」という語句は、患者又は動物の血流中に十分な量で吸収されたとき、オピオイドアゴニストの少なくとも1つの生物学的作用、例えば陶酔作用を低減する、遅延させる又は無効にする逆作用薬を指す。
【0037】
吸着剤と逆作用薬とを含有する投与剤型
本発明は、吸着剤と逆作用薬とを含有する医薬組成物及び投与剤型、及びそのような組成物及び投与剤型を製造するための方法を対象とする。ある実施形態では、本発明は、作用薬、吸着剤及び逆作用薬を含有する投与剤型に関する。
【0038】
1つの実施形態では、本発明は、作用薬を含む複数の第一粒子;及び吸着剤と逆作用薬とを含む複数の第二粒子を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型に関する。もう1つの実施形態では、本発明は、オピオイドアゴニストを含む複数の第一粒子;及び吸着剤とオピオイドアンタゴニストとを含む複数の第二粒子を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されており、及び前記第一粒子が、患者への経口投与後に前記オピオイドアゴニストの制御放出を提供する、経口投与剤型に関する。
【0039】
もう1つの実施形態では、本発明は、吸着剤と逆作用薬とを含有するコア、及び作用薬を含有するシェルを含み、前記シェルが前記コアを少なくとも部分的に覆う又は取り囲む投与剤型に関する。
【0040】
本発明の組成物及び投与剤型は、作用薬の任意の放出速度(制御放出、即時放出又は遅延放出を含むが、限定はされない。)を提供することができる。
【0041】
本発明は、少なくとも1つの吸着剤/逆作用薬を含む。ある実施形態では、逆作用薬の少なくとも一部が吸着剤の少なくとも一部に吸着されている。1つの実施形態では、逆作用薬の少なくとも大部分、すなわち少なくとも50重量%が吸着剤の少なくとも一部に吸着されている。他の実施形態では、吸着剤の少なくとも一部に吸着される逆作用薬のパーセンテージは、例えば少なくとも70重量%、少なくとも80重量%、又は少なくとも90重量%又はそれ以上であり得る。1つの実施形態では、逆作用薬の基本的に全部が吸着剤の少なくとも一部に吸着されている。
【0042】
ある実施形態では、本発明の組成物及び投与剤型は、無傷投与剤型の患者への意図された通りの投与後に逆作用薬が血流中にインビボで放出又は吸収されるのを低減する又は防止するように製剤又は製造される。そこで、ある実施形態では、投与剤型中に存在する逆作用薬の小量だけが、好ましくは約10重量%未満、より好ましくは約1重量%未満又は0%が、無傷投与剤型の患者への意図された通りの投与後にインビボで血流中に放出又は吸収される。ある実施形態では、吸着剤/逆作用薬の逆作用薬がオピオイドアンタゴニストであるとき、好ましくは約0.5mg未満、より好ましくは約0.05mg未満のオピオイドアンタゴニストが、無傷投与剤型の患者への意図された通りの投与後にインビボで放出される。
【0043】
ある実施形態では、本発明の投与剤型は、誤処置又は誤用された場合、インビボで有意の量の逆作用薬を放出するように設計される。例えば乱用者が、作用薬の即時放出を提供することが期待できる、粉末形態の組成物を得るために投与剤型を粉砕しようとすることがあり得る。この場合、製剤を粉砕することは、逆作用薬/吸着剤中に存在する逆作用薬を露出させ、それにより、投与された場合逆作用薬を放出させるはずである。あるいは、乱用者が製剤を有機溶媒、例えばエタノールに溶解して、溶液から作用薬を単離しようとすることがあり得る。この場合、エタノールなどの溶媒の存在下では逆作用薬が脱着又は溶解するので、有機溶媒による抽出工程が有意の割合の逆作用薬の放出を生じさせるはずである。
【0044】
1つの実施形態では、吸着剤と逆作用薬とを他の物質、例えば結合剤、可塑剤、加工助剤、賦形剤等、又は前記の2つ以上の組合せと共に押出することができる。
【0045】
1つの実施形態では、本発明は、作用薬、吸着剤及び逆作用薬を含有する複数の粒子を含み、前記粒子が吸着剤と逆作用薬とを含有するコアを含み、前記コアが作用薬を含有するシェルによって少なくとも部分的に取り囲まれている、固体投与剤型に関する。前記粒子は、コアとシェルとの共押出を含む工程によって作られる。好ましくは、シェルはコア成分の大部分を取り囲む。
【0046】
ある実施形態では、吸着剤及び逆作用薬はコア全体に存在し得る。1つの実施形態では、吸着剤と逆作用薬はコアとシェルとの両方に存在し得る。もう1つの実施形態では、吸着剤と逆作用薬とは多層粒子の1つ以上の内層に存在し得る。
【0047】
ある実施形態では、シェルは吸着剤/逆作用薬を全く含まない。他の実施形態では、シェルは吸着剤/逆作用薬を含み得る。1つの実施形態では、シェル中に存在する逆作用薬の量は、コア中に存在する逆作用薬の量よりも少ない。他の実施形態では、シェルは、任意の放出速度(即時放出又は制御放出を含むが、限定はされない。)を有し得る、吸着剤/逆作用薬ではない逆作用薬を含み得る。
【0048】
1つの実施形態では、吸着剤と逆作用薬はコアにのみ存在し、作用薬は多層粒子のシェルにのみ存在する。この実施形態では、少量の作用薬及び/又は逆作用薬が共押出後に他の成分又は層に移動することが許容し得る。
【0049】
他の実施形態では、本発明の投与剤型は、何らかの適切な大きさの1又はそれ以上の粒子を含み得る。1つの実施形態では、投与剤型は、複数の小さな粒子、例えば全ての寸法において約0.1mmから約5.0mm、好ましくは全ての寸法において約0.1mmから約3.0mmの大きさを有する粒子を含み得る。前記粒子は、所望に応じて、任意の形状も有することができ、例えば円柱状、球状、正方形、楕円体、又は何らかの規則的な又は不規則な形態をとり得る。
【0050】
1つの実施形態では、投与剤型は、硬又は軟ゼラチンカプセル内に作用薬を含有する有効量の溶融押出マルチ微粒子(「MEM」)を含むように製造される。例えばコア及びシェルを含む複数のMEMを、摂取されて体液と接触したとき、吸着剤/逆作用薬からの逆作用薬の有意の放出を伴わずに作用薬の有効な持続放出用量を提供するのに十分な量でゼラチンカプセル中に入れることができる。本発明の投与剤型のマルチ微粒子の粒径は、全ての寸法において約0.1mmから約5.0mm、より好ましくは全ての寸法において約0.1mmから約3.0mmである。
【0051】
本発明の投与剤型は、経口的に、例えば錠剤又はカプセルの形態で、あるいは直腸又は膣経路で、例えば坐薬の形態で投与することができる。好ましい実施形態では、本発明は経口投与剤型を対象とする。
【0052】
ある実施形態では、投与剤型は、例えば約5から8時間にわたって、好ましくは少なくとも12時間にわたって、より好ましくは少なくとも24時間、又はそれ以上にわたって、インビボで作用薬の制御放出を提供するように製剤される。
【0053】
作用薬と吸着剤/逆作用薬とを含有する無傷投与剤型を患者に投与するとき、逆作用薬の少量だけがインビボで放出され、好ましくはほとんど全く放出されず、一方作用薬は、即時放出から制御放出まで変化し得る、意図された速度で放出される。しかし、作用薬、吸着剤及び逆作用薬を含有する投与剤型が、特に高温(例えば約45℃から約50℃以上、約100℃まで又はそれ以上)の溶媒中で、不正使用される、例えば砕かれる、破砕、粉砕又は溶解されるとき、体内への吸収のために利用され得る逆作用薬の量は実質的に上昇する。逆作用薬は、その後、作用薬の少なくとも1つの作用、例えば陶酔作用を低減することによって、又は患者において1種以上の不快な作用を惹起することによってその作用を及ぼすために利用可能となる。そこで、逆作用薬が作用薬のアンタゴニストである場合、逆作用薬の作用によって作用薬の少なくとも1つの作用が、好ましくは実施的に低下するか、又はさらには排除される。例えば作用薬がオピオイドアゴニストであり、逆作用薬がオピオイドアンタゴニストである場合、投与剤型が不正使用されたとき高い量のオピオイドアンタゴニストが体内で利用可能となり、オピオイド−受容体結合を妨げ、オピオイドアゴニストの陶酔作用を低減する。従って、無傷投与剤型として意図された通りに本発明の投与剤型を服用する患者だけが、実質的に作用薬の完全な薬理作用を享受する。逆作用薬が催吐薬であり、投与剤型が不正使用される場合、催吐薬の放出及び吸収は吐き気及び/又は嘔吐を誘発して使用者が投与剤型を不正使用するのを阻止し、また、ある種の場合には、被験者の体内から作用薬を除去する。従って、投与剤型中の作用薬の乱用は、逆作用薬により引き起こされる好ましくない作用のために、より望ましくないものとなる。
【0054】
発明者は、作用薬と逆作用薬の放出速度はインビボ法又はインビトロ法によって測定することができると考える。しかし、本発明者は、2つの異なる方法によって得られる結果の間に必ずしも直接の相関があると主張するわけではない。
【0055】
意図された通りに患者に投与されたとき、無傷投与剤型からの逆作用薬のインビボ放出は、好ましくは作用薬の恩恵を実質的に低下させない又は不快な生理的反応を生じさせないように十分に低い。逆作用薬の放出速度は、主としてコア、鞘(sheath)及びシェルの組成物によって決定される。本発明の投与剤型は、典型的には無傷投与剤型の意図された通りの投与後にインビボで約10重量%未満、好ましくは約1重量%未満の逆作用薬を放出し、より好ましくは逆作用薬を実質的に全く放出しない。逆作用薬がオピオイドアンタゴニストであるとき、投与剤型は、無傷投与剤型の意図された通りの投与後にインビボで、好ましくは約0.5mg未満、より好ましくは約0.05mg未満のオピオイドアンタゴニストを放出する。例えば1つの実施形態では、逆作用薬がナルトレキソンオピオイドアンタゴニストであるとき、好ましくは0.0625mg未満のナルトレキソンが、意図された通りの無傷投与剤型の投与後にインビボで放出される。
【0056】
ある実施形態では、本発明の投与剤型は、標準インビトロ溶解試験において36時間にわたって、好ましくは約10重量%未満、より好ましくは約1重量%未満の逆作用薬を放出し、より好ましくは逆作用薬を実質的に全く放出しない。例えば経口投与剤型が5.0mgのオピオイドアンタゴニストを含有し、USPバスケット法(USP I型バスケット、100rpm;充填擬似胃液700mL、酵素なしでpH1.2;37℃で1時間、次いで擬似腸液900mL;試験期間酵素なしでpH7.5)を用いて溶解試験を実施するとき、36時間にわたって擬似胃腸液中に放出されるオピオイドアンタゴニストの量は、0.5mg未満、より好ましくは0.05mg未満であり得る。
【0057】
本発明の1つの実施形態では、固体投与剤型は、場合により化粧被覆物によって覆うことができる。医薬投与剤型のために使用されるいかなる公知の種類の化粧被覆物も、被覆された投与剤型が本発明の意図する目的を達成する限り、使用することができる。
【0058】
ある実施形態では、投与剤型は、高い安定性を達成するために長時間高温に暴露することによって硬化することができる。本明細書で使用する、「硬化」という用語は、安定化された最終投与剤型を得ることを目的とする投与剤型(又は中間生成物)の熱処理を意味する。当業者に了解されるように、本発明の製剤が疎水性遅延剤の一部又は全部としてポリマーを組み込むとき、熱処理は硬化作用を引き起こし、ポリマーはおそらくそれ自体でより安定な状態へと架橋する。本発明の製剤が疎水性物質、例えば硬化植物油又はステアリルアルコールを含むとき、熱処理は、ポリマーの硬化よりはむしろ製剤のアニーリングに近いことがある。しかし、本発明のために、「硬化」という用語の使用は、硬化及びアニーリングの両方を包含するとみなされる。疎水性材料がろう様物質だけを含む状況では、硬化は、最大の安定性を達成するのに十分な時間、例えば約5から約72時間、約35℃から約65℃の温度で達成することができる。他の実施形態では、硬化は、約40℃から約60℃の温度で約5〜約48時間又はそれ以上、好ましくは少なくとも約24時間、実施される。安定な投与剤型の意図する結果を達成する適切な硬化時間は、当業者によって決定され得る。
【0059】
吸着剤材料
本発明のために有用な吸着剤材料は、窒素を吸着質として使用するBrunauer-Emmett-Teller(BET)モデル(全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、F. S. Baker et al., "Activated Carbon" in Kirk-Othmer Encyc. of Chem. Technol., 4:1016 (4th ed. 1995)参照)などの方法によって測定したとき高い表面積を示す、水不溶性の製薬上許容し得る材料である。従って、1つの実施形態では、本発明における使用に適する吸着剤材料は、100mg/g以上のBET表面積を示す。好ましくは、吸着剤材料は500mg/g以上のBET表面積を示す。最も好ましくは、吸着剤材料は1,000mg/g以上のBET表面積を示す。
【0060】
本発明において有用な製薬上許容し得る吸着剤材料の非限定的な例は、活性炭及び活性黒鉛を含む活性炭素;カオリン、モンモリロナイト、アタパルジャイト、イライト、ベントナイト及びハロイサイトを含む活性白土;二酸化ケイ素、コロイド状二酸化ケイ素(例えばCabot Corp.より入手可能な、CAB-O-SIL)及びアルミナを含む活性無機金属酸化物及び/又は無機イオン交換樹脂;活性ケイ酸アルミニウム及び/又は無機イオン交換組成物、例えばゼオライト;有機イオン交換樹脂、例えばスルホン酸ポリスチレンを含む活性有機酸;有機高分子ベースの吸着剤、例えば微結晶セルロース、デンプン、マルトデキストリン、クロスポビドン(例えばGAF Corp.より入手可能な、POLYPLAXDONE XL又はXL10);等の1種以上の高表面積形態を含む。
【0061】
好ましくは、吸着剤材料は活性吸着剤材料である。活性吸着剤材料は、市販のものを入手し得る及び/又は使用者により、当技術分野において周知の方法によって使用の直前に活性化される。例えば無機吸着剤を活性化する方法は、真空又は不活性パージガスと組み合わせた熱を使用して、表面吸着種、例えば水、有機化合物及び硫化物を除去することを含む。
【0062】
無機イオン交換組成物及び有機イオン交換樹脂を活性化する方法は、塩のイオンをイオン交換樹脂材料の表面に吸着させ、場合により処理した樹脂又は材料を乾燥する、特定塩を含有する溶液での処理を含む。活性化した樹脂又は材料を、次に、逆作用薬の塩形態で処理すると、逆作用薬のイオンがあらかじめ吸着したイオンを置換し、それによって逆作用薬をイオン交換樹脂又は材料に付着させる。
【0063】
1つの実施形態では、吸着剤材料は、活性炭、アルミナ、ベントナイト及びカオリンからなる群より選択される。
【0064】
好ましい実施形態では、吸着剤材料は活性炭又は活性炭素であり、この2つの用語は、低レベルの不純物を含む大きな表面積及び/又はミクロ細孔容積の炭素を表すために、本明細書では交換可能に使用される(例えば米国薬局方26 404(2003)参照)。全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、F. S. Baker et al., "Activated Carbon" in Kirk-Othmer Encyc. of Chem.Techrzol., 4:1015-1022 (4th ed. 1995)は、種々のグレードの活性炭を製造するための方法を開示する。本発明において有用な活性炭は、約100m2/g以上の表面積を示す。ある実施形態では、活性炭の表面積は約300m2/gから約2,000m2/gである。
【0065】
本発明において有用化活性吸着剤はまた、水溶液からのメチレンブルー染料の吸光度(adsorbance)(「MB値」)によって測定したとき高い吸着能を示す(各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、ASTM D3860-98(活性炭の吸着能)及びASTM C837-99(白土の吸着能)参照)。1つの実施形態では、本発明における使用に適する吸着剤材料は、30mg/g以上のMB値を示す;もう1つの実施形態では、吸着剤材料は150mg/g以上のMB値を示す;及びもう1つの実施形態では、吸着剤材料は300mg/g以上のMB値を示す。
【0066】
本発明において有用な吸着剤材料の非限定的な例は、以下の表1に列挙する活性炭を含む。
【0067】
【表1】

【0068】
疎水性被覆材料
本発明の投与剤型は、吸着剤又は吸着剤/逆作用薬の表面の少なくとも一部に配置された少なくとも1つの疎水性被覆材料をさらに含み得る。理論的に制限されることなく、疎水性被覆材料は吸着剤材料の細孔及びチャネルを密封し、それによって水性液体、例えば胃液、が吸着剤材料の細孔又は格子構造に入り込むのを阻止する又は防止すると考えられる。1つの実施形態では、疎水性被覆材料は吸着剤/逆作用薬の少なくとも一部を覆う。
【0069】
1つの実施形態では、前記の少なくとも1つの疎水性材料は、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される。
【0070】
1つの実施形態では、前記の少なくとも1つの疎水性被覆材料は、例えばグリセロールのエステル;脂肪酸、例えばステアリン酸及びイソステアリン酸;アルコール、例えばステアリルアルコール、イソステアリルアルコール、セチルアルコール及びセトステアリルアルコール;蜜ろう;硬化ヒマシ油および硬化綿実油;及びそれらの混合物を含む。もう1つの実施形態では、疎水性被覆材料はステアリルアルコールである。
【0071】
疎水性マトリックス材料
ある実施形態では、本発明の投与剤型及び医薬組成物は疎水性マトリックス材料をさらに含み得る。疎水性マトリックス材料は、疎水性被覆材料と同じであるか又は異なり得る。疎水性マトリックス材料は、少なくとも部分的には、作用薬及び逆作用薬の放出特性を制御することができ;及び逆作用薬の放出をさらに防止する、阻止する又は遅延させることができる。本発明において有用な疎水性マトリックス材料は、胃腸管において不溶性であるか又は低い溶解度を有することが当技術分野で公知であるものを含む。そのような材料は、アクリル酸及びメタクリル酸のポリマー及びコポリマー、並びにアルキルセルロースからなる群より選択される疎水性材料を含むが、これらに限定されない。マトリックスはまた、付加的な疎水性材料、例えばゼイン、シェラック、硬化ヒマシ油、硬化植物油又はそれらの混合物を含有し得る。
【0072】
1つの実施形態では、疎水性マトリックス材料はアクリルポリマーを含む。適切なアクリルポリマーの例は、アクリル酸及びメタクリル酸のコポリマー、メチルメタクリレートコポリマー、エトキシエチルメタクリレート、シアノエチルメタクリレート、アミノアルキルメタクリレートコポリマー、ポリ(アクリル酸)、ポリ(メタクリル酸)、メタクリル酸アルキルアミドコポリマー、ポリ(メチルメタクリレート)、ポリメタクリレート、ポリ(メチルメタクリレート)コポリマー、ポリ(メタクリル酸)(無水物)、メチルメタクリレート、ポリアクリルアミド、アミノアルキルメタクリレートコポリマー、ポリ(メタクリル酸無水物)、並びにグリシジルメタクリレートコポリマーを含むが、これらに限定されない。適切なアクリルポリマーの付加的な例は、アクリル及びメタクリルモノマー1モル当り約0.02〜0.03モルのトリ(低級アルキル)アンモニウム基を含むアクリル酸エステル及びメタクリル酸エステルから合成されるコポリマー(例えばアクリル酸低級アルキルエステルとメタクリル酸低級アルキルエステルとのコポリマー)を含む、アクリル樹脂を含むが、これらに限定されない。
【0073】
アクリルポリマーは、1種以上のアンモニオメタクリレートコポリマーを含み得る。アンモニオメタクリレートコポリマーは当技術分野において周知であり、低含量の第四級アンモニウム基を有するアクリル酸エステル及びメタクリル酸エステルの十分に重合されたコポリマーである。所与の治療薬について望ましい溶解プロフィールを得るために、異なる物理的性質を有する2種以上のアンモニオメタクリレートコポリマーを組み込むことが必要な場合がある。例えば第四級アンモニウム基対中性アクリル(メタクリル)エステルのモル比を変化させることによって、生じる被覆物の透過特性を変化させ得ることは公知である。当業者は、所望放出速度で治療薬を放出するコポリマーを提供するためにモノマーを容易に組み合わせることができる。第四級アンモニウム基の官能性を有するアクリレート及びメタクリレートのコポリマーは、EUDRAGIT RS及びEUDRAGIT RL(Rohm Pharma, GmbH, Weiterstat, Germany)として市販されている。好ましいアンモニオメタクリレート樹脂は、全ての形態のEUDRAGIT RS、例えばEUDRAGIT RS POを含む。EUDRAGIT RSは、EA:MM:TAMのモル比が1:2:0.01である、エチルアクリレート(EA)、メチルメタクリレート(MM)及びトリメチルアンモニウムエチルメタクリレートクロリド(TAM)の水不溶性コポリマーであることが知られている;例えば米国特許第6,306,391号参照。EUDRAGIT RS POha,EUDRAGIT RSの粉末化形態であることが知られている;例えば、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、米国特許第5,492,692号参照。
【0074】
1つの実施形態では、疎水性マトリックス材料は、水不溶性セルロースポリマーを含む。ある実施形態では、セルロースポリマーは、セルロースエーテル、セルロースエステル、又はセルロースエステルエーテルである。好ましくは、セルロースポリマーは、約0から約3(3を含む)までの無水グルコース単位上の置換度(「D.S.」)を有する。本明細書で使用するD.S.という用語は、置換基によって置換されている、セルロースポリマーの無水グルコース単位上に存在するヒドロキシル基の平均数を意味する。代表的セルロースポリマーは、セルロースアシレート、セルロースジアシレート、セルローストリアシレート、セルロースアセテート、セルロースジアセテート、セルローストリアセテート、モノ−、ジ−及びトリセルロースアルカニレート、モノ−、ジ−及びトリセルロースアリーレート、及びモノ−、ジ−及びトリセルロースアルケニレートから選択されるポリマーを含むが、これらに限定されない。例示的なセルロースポリマーは、約1から約2のD.S.を有するセルロースアセテート及び約2から約3のD.S.を有するセルロースアセテートを含む。好ましくは、セルロースポリマーは、エチルセルロース、セルロースアセテート、セルロースプロピオネート(低、中又は高分子量)、セルロースアセテートプロピオネート、セルロースアセテートブチレート、セルロースアセテートフタレート、又はセルローストリアセテートである。より好ましいセルロースはエチルセルロースである。
【0075】
より特定のセルロースポリマーは、約1.8のD.S.を有するセルロースプロピオネート;約1.8のD.S.を有するセルロースアセテートブチレート;約2.9〜3のD.S.を有するセルローストリアシレート、例えばセルローストリアセテート、セルローストリバレレート、セルローストリラウレート、セルローストリパルミテート、セルローストリスクシネート及びセルローストリオクタノエート;約2.2〜2.6のD.S.を有するセルロースジアシレート、例えばセルロースジスクシネート、セルロースジパルミテート、セルロースジオクタノエート、セルロースジペンタノエート;及びセルロースのコエステル、例えばセルロースアセテートブチレート、セルロースアセテートオクタノエートブチレート及びセルロースアセテートプロピオネートを含む。
【0076】
ある実施形態では、吸着剤/逆作用薬を疎水性マトリックス材料と混合することができる。例えば吸着剤/逆作用薬を含有するコアは、約50重量%までの1種以上の疎水性マトリックス材料、好ましくは約50重量%までの1種以上の疎水性マトリックス材料、より好ましくは約25重量%までの1種以上の疎水性マトリックス材料をさらに含み得る。コア中に疎水性マトリックス材料を含むことは、吸着剤材料からの逆作用薬の放出又は脱着をさらに低減する、遅延させる又は防止することができる。
【0077】
上述したように、作用薬及び逆作用薬の放出速度は、部分的には、疎水性マトリックス材料の組成物によって制御される。製薬技術分野の当業者は、疎水性マトリックス材料の組成物を変更することによってこれらの放出速度に影響を及ぼすことができ、そのような変更は本発明の開示を考慮した常用実験によって決定される。
【0078】
作用薬
いかなる種類の作用薬も、本発明の投与剤型において使用することができる。有用な作用薬の例は、鎮痛薬、抗炎症薬、駆虫薬、抗不整脈薬、抗菌薬、抗ウイルス薬、抗凝固薬、抗うつ薬、抗糖尿病薬、抗てんかん薬、抗真菌薬、抗痛風薬、抗高血圧薬、抗マラリア薬、抗片頭痛薬、抗ムスカリン薬、抗腫瘍薬、勃起機能不全改善薬、免疫抑制剤、抗原虫薬、抗甲状腺薬、抗不安薬、鎮静薬、催眠薬、神経弛緩薬、β-遮断薬、心臓イオンチャネル薬、コルチコステロイド、利尿薬、抗パーキンソン病薬、胃腸薬、ヒスタミン受容体アンタゴニスト、角質溶解薬、脂質調節薬、抗狭心症薬、cox-2阻害剤、ロイコトリエン阻害剤、マクロライド系抗生物質、筋弛緩薬、栄養剤、オピオイド鎮痛薬、プロテアーゼ阻害剤、性ホルモン、興奮薬、筋弛緩薬、抗骨粗しょう症薬、抗肥満薬、認知増強薬、抗尿失禁薬、栄養油、抗良性前立腺肥大症薬、必須脂肪酸及び非必須脂肪酸を含むが、これらに限定されない。投与剤型は2つ以上の作用薬を含み得る。
【0079】
作用薬のより特定の例は、オピオイド、ベンゾジアゼピン、バルビツレート、及び刺激薬、例えばメチルフェニデート及びアンフェタミン、ドロナビノール、グルテチミド、メチルフェニデート、ナビロン、タンパク質同化ステロイド、メチルプリロン、エトクロルビノール、エチナメート、フェンフルラミン、メプロバメート、ペモリン、レボメタジル、ベンズフェタミン、クロルフェンテルミン、ジエチルプロピオン、フェンテルミン、メブタメート、クロルテルミン、フェニルアセトン、ドロナビノール、ナビロン、ベンフェタミン、抱水クロラール、エトクロルビノール、パラアルデヒド、ミダゾラム、及びデトロプロポキシフェンを含むが、これらに限定されない。
【0080】
ある実施形態では、作用薬はオピオイドアゴニストである。有用なオピオイドアゴニストは、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジアモルフォン、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、エトルフィン、ジヒドロエトルフィン、フェンタニル、ヒドロコドン、ヒドロモルフォン、ヒドロモルフォドン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ナルブフェン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パントポン、パパベレタム、パレゴリック、ペンタゾシン、フェナドキソン、フェンジメトラジン、フェンジメトラゾン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロポキシフェン、プロピルヘキセドリン、スフェンタニル、チリジン、トラマドール、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0081】
ある実施形態では、オピオイドアゴニストは、ヒドロコドン、モルフィン、ヒドロモルフォン、オキシコドン、コデイン、レボルファノール、メペリジン、メタドン、オキシモルフォン、ブプレノルフィン、フェンタニル及びその誘導体、ジピパノン、ヘロイン、トラマドール、エトルフィン、ジヒドロエトルフィン、ブトルファノール、レボルファノール及びそれらの混合物からなる群より選択される。1つの実施形態では、オピオイドアゴニストは、オキシコドン、ヒドロモルフォン又はヒドロコドンである。
【0082】
「ベンゾジアゼピン」という用語は、ベンゾジアゼピン及びベンゾジアゼピンの誘導体であって、中枢神経系を抑制することができる薬剤を指す。ベンゾジアゼピンは、アルプラゾラム、ブロマゼパム、クロルジアゼポキシド、クロラゼペート、ジアゼパム、エスタゾラム、フルラゼパム、ハラゼパム、ケタゾラム、ロラゼパム、ニトラゼパム、オキサゼパム、プラゼパム、クアゼパム、テマゼパム、トリアゾラム、メチルフェニデート及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0083】
バルビツレートは、バルビツール酸(2,4,6−トリオキソヘキサヒドロピリミジン)から誘導される鎮静−催眠薬を指す。バルビツレートは、アモバルビタール、アプロバルビタール、ブタバルビタール、ブタルビタール、メトヘキシタール、メフォバルビタール、メタルビタール、ペントバルビタール、フェノバルビタール、セコバルビタール及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0084】
刺激薬は、中枢神経系を刺激する薬剤を指す。刺激薬は、アンフェタミン、例えばアンフェタミン、デキストロアンフェタミン樹脂複合体、デキストロアンフェタミン、メタンフェタミン、メチルフェニデート及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0085】
作用薬は、結腸疾患、例えば過敏性腸症候群、過敏性腸疾患、クローン病、便秘、術後アトニー、胃腸感染を治療するために結腸領域で局所的に作用する薬剤、及び抗原性物質をリンパ系組織に送達する治療薬を含むが、これらに限定されない、結腸への送達を意図する薬剤であり得る。結腸疾患の治療のための作用薬は、5−ASA;ステロイド類、例えばヒドロコルチゾン及びブデゾニド;緩下薬;軟便剤;オクトレオチド;シサプリド;抗コリン作用薬;オピオイド;カルシウムチャネル遮断薬;結腸の細胞への送達のためのDNA;グルコサミン;トロンボキサンA2シンテターゼ阻害剤、例えばリドグレル;5HT3−アンタゴニスト、例えばオンダンセトロン;感染性細菌、例えばクロストリジウム・ディフィシル(Clostridium difficile)に対する抗体;及び、例えばHIVの予防のための、抗ウイルス薬を含むが、これらに限定されない。
【0086】
あるいは、作用薬は、全身的に活性であり、結腸領域において吸収が高い薬剤であり得る。そのような薬剤は、極性化合物、例えばヘパリン;インスリン;カルシトニン;ヒト成長ホルモン(HGH);成長ホルモン放出ホルモン(GHRH);インターフェロン;ソマトスタチン及び類似体、例えばオクトレオチド及びバプレオチド;エリトロポエチン(EPO);顆粒球コロニー刺激因子(GCSF);副甲状腺ホルモン(PTH);黄体化ホルモン放出ホルモン(LHRH)及びその類似体;心房性ナトリウム利尿因子(ANF);バソプレシン;デスモプレシン;カルシトニン遺伝子関連ペプチド(CGRP);及び鎮痛薬を含む。
【0087】
作用薬粒子は、疎水性材料、結合剤、可塑剤、賦形剤、及び前記のいずれか2つ以上の組合せをさらに含み得る。適切なマトリックス材料は、所望結果、例えば即時放出、持続放出又は遅延放出を達成するのに十分な速度で作用薬を放出することを可能にするものを含む。1つの実施形態では、作用薬の胃腸液への拡散放出を可能にする、透過性マトリックス材料を使用する。
【0088】
逆作用薬
逆作用薬は、作用薬の生物学的作用を少なくとも部分的に低減するか又は遮断する、あるいは動物又は患者の血流中に吸収されたとき不快な作用を作り出す、任意の医薬活性物質であり得る。逆作用薬の例は、任意の治療的に活性な作用物質のアンタゴニストを含むが、これらに限定されない。オピオイドアゴニストを本発明の投与剤型中の作用薬として使用するときは、オピオイドアンタゴニストを逆作用薬として使用することができる。同様に、ベンゾジアゼピンを本発明の投与剤型における作用薬として使用するときは、ベンゾジアゼピンアンタゴニストを逆作用薬として使用できる。バルビツレートを本発明の投与剤型中の作用薬として使用するときは、バルビツレートアンタゴニストを逆作用薬として使用することができる。アンフェタミンを本発明の投与剤型における作用薬として使用するときは、アンフェタミンアンタゴニストを逆作用薬として使用できる。作用薬が、その通常治療範囲以上の用量で投与したとき毒性であるとき、すなわち過量の重大な潜在的可能性が存在するときは、毒性作用薬の解毒薬を逆作用薬として使用することができる。
【0089】
1つの実施形態では、逆作用薬はオピオイドアンタゴニストである。本発明において有用なオピオイドアンタゴニストは、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、シクラゾシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物を含むが、これらに限定されない。
【0090】
有用なオピオイドアンタゴニスト塩は、酸とオピオイドアンタゴニストの塩基性窒素基とから形成される塩を含む。オピオイドアンタゴニスト塩の例は、硫酸塩、クエン酸塩、酢酸塩、シュウ酸塩、塩化物、臭化物、ヨウ化物、硝酸塩、重硫酸塩、リン酸塩、酸性リン酸塩、イソニコチン酸塩、乳酸塩、サリチル酸塩、酸性クエン酸塩、酒石酸塩、オレイン酸塩、タンニン酸塩、パントテン酸塩、重酒石酸塩、アスコルビン酸塩、コハク酸塩、マレイン酸塩、ゲンチジン酸塩、フマル酸塩、グルコン酸塩、グルカロン酸塩、サッカリン酸塩、ギ酸塩、安息香酸塩、グルタミン酸塩、メタンスルホン酸塩、エタンスルホン酸塩、ベンゼンスルホン酸塩、p−トルエンスルホン酸塩、及びパルモエート(すなわち1,1’−メチレン−ビス−(2−ヒドロキシ−3−ナフトエート))塩を含むが、これらに限定されない。
【0091】
他のオピオイドアンタゴニスト塩は、酸性官能基、例えばカルボン酸又はスルホン酸官能基を有するアンタゴニストと、製薬上許容し得る無機又は有機塩基から生成される塩を含む。適切な塩基は、5.1章の「製薬上許容し得る塩」という用語に言及した項において上記で特定したものを含むが、これらに限定されない。
【0092】
ある実施形態では、オピオイドアンタゴニストは、ナルメフェン、ナロキソン、ナルトレキソン、又はそれらの製薬上許容し得る塩である。もう1つの実施形態では、オピオイドアンタゴニストは、ナルトレキソン塩、例えば塩酸ナルトレキソンである。
【0093】
本発明の逆作用薬として使用できるベンゾジアゼピンアンタゴニストは、フルマゼニルを含むが、これに限定されない。
【0094】
本発明の逆作用薬として使用できるバルビツレートアンタゴニストは、本明細書で述べるようなアンフェタミンを含むが、これらに限定されない。
【0095】
本発明の逆作用薬として使用できる刺激薬アンタゴニストは、本明細書で述べるベンゾジアゼピンを含むが、これらに限定されない。
【0096】
本発明のもう1つの実施形態では、逆作用薬は、望ましくない生理的反応、例えば嘔吐を引き起こす薬剤である。このタイプの逆作用薬は、オピオイド、ベンゾジアゼピン、バルビツレート、又は刺激薬を含むいかなる種類の治療薬に関しても使用できる。本発明における逆作用薬としての使用に適する催吐薬の例は、イペカック(ipecac)及びアポモルフィンを含むがこれらに限定されない、投与後安全且つ有効に嘔吐を誘発する薬剤を含む。
【0097】
本発明の投与剤型を製造するための方法
吸着剤/逆作用薬
ある実施形態では、本発明は、吸着剤/逆作用薬を製造するための方法に関する。例えば、一部の実施形態では、本発明は、液相から逆作用薬を吸着剤材料に吸着させるための方法に関する。1つの実施形態では、本発明は、吸着剤材料を提供すること;逆作用薬を含有する液体と吸着剤材料を、逆作用薬の少なくとも一部が吸着剤に吸着するのに十分な時間接触させること;吸着剤/逆作用薬液相から分離すること;及び場合により、吸着剤/逆作用薬を洗浄すること、を含む、吸着剤/逆作用薬を製造するための方法に関する。
【0098】
1つの実施形態では、本発明は、吸着剤材料と逆作用薬とを含有する組成物を押出することを含む、本発明の投与剤型を製造するための方法に関する。
【0099】
もう1つの実施形態では、本発明は、a)i)吸着剤と逆作用薬とを含有するコア;及びii)コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む鞘、を共押出して、押出物鎖(extrudate strand)を形成すること;及びb)例えば切断によって、押出物鎖を複数の粒子にすること、を含む、投与剤型を製造するための方法に関する。
【0100】
もう1つの実施形態では、本発明は、a)i)吸着剤と逆作用薬とを含有するコア;ii)場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む鞘;及びiii)コア及び/又は場合により鞘を少なくとも部分的に取り囲む、作用薬を含有するシェル、を共押出して、押出物鎖を形成すること;及びb)例えば切断によって、押出物鎖を複数の粒子にすること、を含む、投与剤型を製造するための方法に関する。
【0101】
もう1つの実施形態では、本発明は、a)作用薬を含有する複数の第一粒子を形成すること;b)i)吸着剤と逆作用薬とを含有するコア;及びii)コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、疎水性マトリックス材料を含有する鞘、を含む複数の第二粒子を共押出すること;及びc)第一及び第二粒子を投与剤型に添加すること、を含む、投与剤型を製造するための方法に関する。
【0102】
もう1つの実施形態では、本発明は、a)i)吸着剤と逆作用薬とを含有するコア;ii)場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、より好ましくはコアを実質的に又は完全に取り囲む鞘;及びiii)鞘を少なくとも部分的に取り囲む、好ましくは鞘の大部分を取り囲む、より好ましくは鞘を実質的に又は完全に取り囲む、作用薬を含有するシェル、を共押出して、多層押出物シート又はラミネートを形成すること;及びb)多層押出物シートを投与剤型、例えば錠剤、カプレット又は複数の粒子に成形すること、を含む、投与剤型を製造するための方法に関する。
【0103】
吸着(又は収着)過程及び吸着の速度と程度に影響を及ぼす因子は当技術分野において周知である(例えば、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、Perry's Chemical Engineer's Handbook, 16: 1-48 (6th ed. 1984); D. M. Ruthven, "Adsorption" in Kirk-Othmer Encyc.of Clzem. Technol., 4: 493-528 (4th ed. 1995); and S. A. Gembicki et al., "Adsorption, Liquid Separation" in Kirk-Othmer Encyc. of Chem. Technol., 4:573-600 (4th ed. 1995)参照)。
【0104】
1つの実施形態では、吸着工程は、吸着剤と液相とを含む反応容器内で、場合により混合しながら、実施する。もう1つの実施形態では、吸着剤はカラム内に含まれ、液相が吸着剤材料を通って循環する。吸着剤の速度及び/又は程度は、例えば液相中の逆作用薬の濃度変化を経時的に観測することによって、監視できる。
【0105】
液相からの吸着を含む工程のための適切な溶媒は、逆作用薬を溶解することができるが、一旦逆作用薬が吸着剤材料に吸着された後は逆作用薬を再溶解する傾向が低いものである。適切な溶媒の非限定的な例は、水、水溶液、例えば擬似胃液(pH1.2)、擬似腸液(pH6.8)、0.1N塩酸溶液及び0.1Nリン酸溶液を含む。
【0106】
1つの実施形態では、約1から約7のpHを有する水性溶媒を溶液吸着工程において使用する。より好ましくは、水性溶媒のpHは約1から約4である。より好ましくは水性溶媒のpHは約1であり得る。
【0107】
ある実施形態では、溶液吸着工程において使用する液相の温度は、吸着の速度と程度に影響を及ぼすように変化させ得る。当業者は常用実験によって最適反応温度を決定することができる。
【0108】
本発明はまた、逆作用薬を含む液相を吸着剤材料に噴霧することによって吸着剤/逆作用薬を製造するための方法に関する。1つの実施形態では、本発明は、吸着剤材料を提供すること;逆作用薬を含有する液相を提供すること;吸着剤材料を流動床に添加すること;吸着剤材料を流動化すること;流動化した材料に液相を噴霧すること;及び場合により、吸着剤/逆作用薬を乾燥すること、を含む、吸着剤/逆作用薬を製造するための方法に関する。1つの実施形態では、噴霧した粒子を乾燥する方法は、強制通気、減圧、熱及び前記のいずれか2つ以上の混合物からなる群より選択される。
【0109】
噴霧適用工程は、外側表面は乾燥しているように見えるが、まだ内側表面は液相で「湿潤」である吸着剤を提供する。溶媒の溶媒和力に依存して、逆作用薬が吸着剤材料の表面に吸着されてもよく又は吸着されなくてもよい。しかし、例えば、場合により熱を伴う、減圧蒸発による溶媒の除去は、液体ビヒクルが蒸発するので吸着剤材料の表面への逆作用薬の沈着を生じさせる。噴霧工程は、逆作用薬を別に脱着させる溶媒の使用を可能にする。
【0110】
噴霧乾燥工程のために有用な溶媒の非限定的な例は、上述したような水;メタノール、エタノール、n−プロパノール及びi−プロパノールを含むアルコール;ジエチルエーテル、ジ−プロピルエーテル及びd−ブチルエーテルを含むジアルキルエーテル;及び環状エーテル、例えばテトラヒドロフラン、及び前記のいずれか2つ以上の混合物を含む。
【0111】
ある実施形態では、吸着剤/逆作用薬は、疎水性被覆材料をさらに含む。被覆材料は、吸着剤/逆作用薬の細孔及びチャネルを密封し、それによって逆作用薬の放出をさらに遅延させる、低減する又は排除する。疎水性被覆材料は、適用方法が吸着剤/逆作用薬からの逆作用薬の有意の脱着を引き起こさないことを条件として、従来の任意の被覆手段を使用して適用することができる。
【0112】
1つの実施形態では、疎水性被覆材料を適用するための方法は、疎水性被覆材料を含む液相を提供すること;及び吸着剤/逆作用薬に液相を噴霧すること、を含む。
【0113】
もう1つの実施形態では、疎水性被覆材料を適用するための方法は、疎水性被覆材料の溶融物を提供すること;及びその溶融物を吸着剤/逆作用薬に適用すること、を含む。1つの実施形態では、固体を溶融物に浸漬被覆することによって疎水性被覆材料を吸着剤/逆作用薬に適用する。
【0114】
本発明はまた、溶融押出又は造粒の間に疎水性被覆材料を吸着剤/逆作用薬に適用するための方法に関する。この実施形態では、吸着剤/逆作用薬と疎水性被覆材料を他の成分と共にフィードホッパーに添加し、この混合物を押出する又は圧縮する。理論に縛られることなく、押出又は圧縮工程に必要なエネルギーは、疎水性被覆材料を流動化し、吸着剤/逆作用薬上に被覆物を形成するのに十分であると考えられる。
【0115】
放出可能形態のオピオイドアゴニスト及び実質的に放出されないオピオイドアンタゴニストを含有する投与剤型の製剤及び製造に関するさらなる詳細は、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、Oschlack et al.への米国特許第6,696,088 B2号に開示されている。
【0116】
5.8.2
投与剤型を押出する又は共押出するための方法
ある実施形態では、本発明はまた、吸着剤/逆作用薬を含むコアを押出することによって、例えば溶融押出することによって、吸着剤/逆作用薬を含有する医薬組成物又は投与剤型を製造するための方法に関する。1つの実施形態では、コアは疎水性材料をさらに含む。
【0117】
1つの実施形態では、本発明は、a)吸着剤/逆作用薬を含有するコア;及びコアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む鞘、を共押出して、押出物鎖を形成すること;及びb)例えば切断によって、押出物鎖を複数の吸着剤/逆作用薬粒子にすること、を含む、複数の吸着剤/逆作用薬粒子を製造するための方法に関する。
【0118】
1つの実施形態では、コアは吸着剤/逆作用薬と疎水性被覆材料とを含み、鞘は疎水性マトリックス材料を含む。
【0119】
もう1つの実施形態では、本発明は、a)作用薬を含有する複数の第一粒子を形成すること;b)吸着剤/逆作用薬、及び場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、疎水性マトリックス材料を含有する鞘、を含む複数の第二粒子を共押出すること;及びc)第一及び第二粒子を一緒にすること、を含む、投与剤型を製造するための方法に関する。
【0120】
もう1つの実施形態では、本発明は、a)吸着剤/逆作用薬を含有するコア;コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、より好ましくはコアを実質的に又は完全に取り囲む鞘;及び鞘を少なくとも部分的に取り囲む、好ましくは鞘の大部分を取り囲む、より好ましくは鞘を実質的に又は完全に取り囲む、作用薬を含有するシェル、を共押出して、押出物鎖を形成すること;及びb)例えば切断によって、押出物鎖を複数の吸着剤/逆作用薬粒子にすること、を含む、投与剤型を製造するための方法に関する。
【0121】
もう1つの実施形態では、本発明は、a)吸着剤/逆作用薬を含有するコア;場合により、コアを少なくとも部分的に取り囲む、好ましくはコアの大部分を取り囲む、より好ましくはコアを実質的に又は完全に取り囲む鞘;及び鞘を少なくとも部分的に取り囲む、好ましくは鞘の大部分を取り囲む、より好ましくは鞘を実質的に又は完全に取り囲む、作用薬を含有するシェル、を共押出して、多層押出物シート又はラミネートを形成すること;及びb)多層押出物シートを投与剤型、例えば錠剤、カプレット又は複数の粒子に成形すること、を含む、投与剤型を製造するための方法に関する。1つの実施形態では、前記方法は、多層押出物シートを粒子にするためのローリングパンチの使用を含む。
【0122】
ある実施形態では、前記押出物を投与剤型において、例えば錠剤、カプレット又は複数の粒子において使用する。
【0123】
押出及び/又は共押出によって作用薬含有組成物又は粒子を製造するための方法は周知である。例えば粒子からなる投与剤型を含む、医薬投与剤型を押出し、形成するための公知の方法を開示する、各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第5,958,452号、同第5,965,161号及び同第6,335,033号参照。
【0124】
作用薬を投与するための2層組成物又は粒子を形成するための共押出方法も公知である。例えば全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、米国特許出願公開第2002/0119197 A1号参照。
【0125】
共押出によって本発明の投与剤型を形成するための方法を以下で述べる。異なる記載がない限り、コアだけを含む押出粒子を製造するための方法は、(1)コア製剤を供給するために1台のホッパーだけを使用する必要があること、及び(2)金型は1つの口だけを有することを除き、共押出に関するものと同様である。
【0126】
1つの実施形態では、共押出工程は、患者への意図された通りの無傷投与後にインビボで限られた量の逆作用薬を放出する、吸着剤/逆作用薬を含有する医薬組成物又は投与剤型を製造するために使用される。1つの実施形態では、前記組成物又は投与剤型は、好ましくは逆作用薬を全く含まない鞘により、その長さに沿って少なくとも部分的に放射状に取り囲まれた、吸着剤/逆作用薬を含有するコアを有する、共押出された吸着剤/逆作用薬円柱状粒子を含む。さらなる実施形態では、吸着剤/逆作用薬、例えばオピオイドアンタゴニストを含有する共押出粒子を、作用薬を含有する粒子と共にゼラチンカプセルに入れる。
【0127】
本発明はさらに、吸着剤/逆作用薬及び、場合により、疎水性被覆材料を含有するコア製剤を第一押出機に充填すること;作用薬を含有するシェル製剤を第二押出機に充填すること;前記製剤を第一及び第二押出機において加熱すること;前記製剤を共押出して、作用薬を含有するシェルによって放射状に取り囲まれた逆作用薬コアを含む鎖を形成すること;及び例えば切断によって、前記鎖を粒子にすること、を含む、投与剤型において有用な粒子状吸着剤/逆作用薬を製造するための方法に関する。
【0128】
もう1つの実施形態では、本発明は、吸着剤/逆作用薬及び、場合により、疎水性被覆材料を含有するコア製剤を第一押出機に充填すること;作用薬を含有するシェル製剤を第二押出機に充填すること;前記製剤を第一及び第二押出機において加熱すること;前記製剤を共押出して、多層押出物シート又はラミネートを形成すること;及び多層押出物シートを投与剤型、例えば錠剤、カプレット又は複数の粒子に成形すること、を含む、多層投与剤型を形成するための方法に関する。1つの実施形態では、前記方法は、多層押出物シートを粒子にするためのローリングパンチの使用を含む。
【0129】
本発明の共押出工程のために有用な装置の一例は、2台の粉末供給ホッパーを含み、1台は吸着剤/逆作用薬コア成分を負荷するため及び1台はシェル成分を負荷するためである。逆作用薬コア成分は、吸着剤/逆作用薬;及び場合により、疎水性被覆材料及び上述したような付加的な遅延剤、結合剤、可塑剤及び賦形剤を含むがこれらに限定されない付加的な物質を含有する。シェル成分は、作用薬、制御放出マトリックス材料及び上述したような付加的な遅延剤、結合剤、可塑剤及び賦形剤を含むがこれらに限定されない付加的な物質を含有する。各々のホッパーの内容物が押出機に充填される。各々の押出機の出口は、多数の同軸出口開口部を有する同じ同軸金型に接続されており、それによって鎖のコア中に逆作用薬を含む押出物の鎖及びコアを放射状に取り囲むシェルが形成される。
【0130】
各々の押出機は、例えば単軸又は二軸スクリューと加熱バレルを備え得る。各々のスクリュー押出機は、独立して、(i)逆方向回転(すなわち反対方向の回転で駆動される)非かみ合い型;(ii)同方向回転(すなわち同方向の回転で駆動される)非かみ合い型;(iii)逆方向回転かみ合い型;又は(iv)同方向回転かみ合い型であり得る。各々の押出機は、独立して、その架構の先端に位置する単一排出口又は放射状排出口を有し得る。各々のスクリュー押出機は、独立して、スクリューの各々の先端の駆動手段又は1つの先端にだけ存在する駆動手段を有し得る。各々のスクリュー押出機は、独立して、5から70、好ましくは20から60の長さ対直径比、又はL/D比を有し得る。当業者はそのような装置、例えば真空付属物を有するLeistritz二軸スクリュー押出機、Leistritz Micro 18/GL 40D二軸スクリュー押出機、又はWarner & Pfleiderer ZSK-30型二軸スクリュー押出機に精通する。
【0131】
各々の押出機の各々個別に調節可能なバレル区域の温度は、所与の製剤のために必要な温度に設定され、押出機は、1つの形態では約30分間、熱平衡させる。二軸スクリュー押出機の内圧は、マイナス約600から約980ミリバールに維持することができる。
【0132】
定常状態温度に達した後、各々の粉末供給ホッパーの内容物は別々の予備加熱された押出機に供給され、それによって各々の押出機内で、かみ合い型スクリュー及び混練機によって一連の区域を通って駆動されながら、加熱及び混合を通して、1つの実施形態では約30℃から約200℃の温度、好ましくは約50℃から約150℃、の緊密に混合された溶融塊を形成する。場合により、空気流通口が押出機内に存在し得る。液体成分を、粉末製剤とは独立して、溶融塊に添加することを所望する場合は、何らかの公知の手段によって、例えば容積移送式ポンプ、例えば歯車ポンプによって供給される注入口によって、液体を押出機内に注入することができる。
【0133】
各々の押出機を出てくる溶融塊は、場合により結合ブロック及び/又は主ゲートアダプターの下流にある、同軸金型内に集められ、その後金型の出口開口部を通過する。1つの実施形態では、押出物は、逆作用薬コア及びコアを少なくとも部分的に取り囲む鞘を含有する単一又は多数の押出鎖として成形される。もう1つの実施形態では、押出物は多層シート又はラミネートとして成形される。
【0134】
各々の押出機の回転速度(rpm)は、それらの結合産出量が、金型出口で、約1から約20kg/時又はそれ以上、好ましくは約6から約8kg/時であるように調節される。各々の押出機の回転速度は、各々の押出機の産出量がコア対鞘の所望比率を生じるように調節することができるパラメータの1つである。
【0135】
金型出口の寸法及び/又は横断面輪郭は、生じる鎖又はシートの厚さ及び形状を変化させるように調節することができる。例えば金型口は円形横断面形状に限定されず、楕円形、正方形、長方形、六角形、三角形、五望星等であり得る。ある実施形態では、円形横断面を有する金型口は、約0.1mmから約5.0mmの直径を有する鎖を提供するように調節することができる。鎖の形状は、数ある因子の中でも特に、金型出口開口部の形状及び鎖を粒子にする方法によって決定される。
【0136】
共押出工程から生産された鎖は、その後金型口から離れて運搬され、当業者に公知の方法によって、例えば扇冷却トンネル又はその上で鎖が冷却時に凝結して硬化する連続移動ベルトを使用して、凝固される。鎖は、当業者に公知の方法によって、例えばレーザー切断、熱線カッター又は裁断機を用いて、押出された鎖を粒子にするための適切な装置に送られる。鎖を粒子にすることは、凝結の前、凝結の間又は凝結の後に実施することができる。1つの実施形態では、共押出工程から生じる硬化した鎖はペレタイザーによって切断され、これは、ローラー、固定ナイフ、回転カッター等が利用できる。ローラー速度及びカッター速度は、所望の大きさ及び放出特性の粒子を生産するように設定される。適切な機器及びシステムは、ニュージャージー(New Jersey)のRand Castle Inc.などの配給業者から入手可能である。他の適切な装置は当業者に明白である。
【0137】
1つの実施形態では、共押出された鎖を切断して、逆作用薬含有コアが円柱の両端で露出されている、図1に示すような多数の円柱を形成する。いかなる場合も、逆作用薬含有コア及び鞘の組成物は、吸着剤/逆作用薬からの逆作用薬のインビボ放出速度を制限するように適宜製剤されるべきである。
【0138】
共押出工程からシートが生産される場合、シートは、押出物が多層シートとして形成されることを除いて、鎖に関して上述したように加工される。シートは、次に、何らかの方法によって、例えばローリングパンチを使用して、粒子又は錠剤に成形されうる。押出及び/又は共押出によって組成物又は粒子を製造するための方法は周知である。例えば、粒子からなる投与剤型を含む、医薬投与剤型を押出して形成するための公知の方法を開示する、各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第5,958,452号、同第5,965,161号及び同第6,335,033号参照。
【0139】
1つの実施形態では、共押出された多層押出物は、切断する、挟む、又は圧着することによって、多数の微粒子、例えば逆作用薬含有コアが鞘層及びシェル層によって実質的に又は完全に包まれている、図1に示すものに成形される。好都合には、好ましい実施形態では、ローリングパンチ装置の作用は、鞘がコアを実質的に又は完全に取り囲み、シェルが鞘を実質的に又は完全に取り囲むようにシェル層及び鞘層を圧着する又は挟む。いかなる場合も、コア及び鞘の組成物は、吸着剤/逆作用薬からの逆作用薬のインビボ放出速度を制限する又は妨げるように適宜製剤されるべきである。装置、例えば成形圧延機、ピンチ装置、ベルト及びローラー又は牽引ローラーを用いて押出物を粒子又は錠剤に成形するための方法は、例えば各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第6,120,802号及び同第5,073,379号に開示されている。
【0140】
加えて、粒子が、金型出口に依存して、何らかの幾何学的形状、例えばビーズ、シード、ペレット等であり得ることは了解されるべきである。1つの実施形態では、鎖から形成される微粒子は、約0.1mmから約3.0mmの直径を有する楕円体である。もう1つの実施形態では、鎖から形成される微粒子は、約0.1から約3.0mmの長さ及び約0.1から約3.0mmの直径を有する円柱状である。
【0141】
多層押出物から粒子が形成されるとき、粒子の形状は、変形円柱状(例えば上部及び/又は底部が屈曲している円柱状側面を有する;側面はある程度屈曲しており、実質的に扁平な上部及び/又は底部を有する、又はそれらの組合せ)、卵型、楕円形等、又はそれらの何らかの組合せをさらに含み得るが、この場合「円柱状」は、円形横断面だけでなく以下の横断面の1種以上も含み得る:角が少なくとも部分的に丸くなった形状を含む、三角形、四角形、菱形、ダイアモンド型、台形、五角形、六角形、八角形、星型(例えば3、4、5、6又はそれ以上の頂点を有する)、又はそれらの何らかの組合せ。1つの実施形態では、形成される微粒子は、約0.1mmから約3.0mmの寸法(高さ、長さ及び幅)を有する楕円体であり得る。もう1つの実施形態では、形成される微粒子は、類似の寸法を有する円柱状であり得る。
【0142】
同様に、押出物がシートであるとき、金型口の寸法及び/又は横断面輪郭は、生じる多層シートの厚さ及び形状を変化させるように調節することができる。例えば金型口は長方形横断面輪郭に限定されず、台形特徴(すなわち押出物の上部の幅が押出物の底部の幅より小さい場合、又はその逆の場合)を有し得るか;多層シート又はラミネートの幅及び/又は厚さに関してある程度の屈曲を有し得るか(すなわち厚みが押出物の幅に沿って変化するように、上部及び/又は底部面が凹型及び/又は凸型屈曲を有し得る;1つの実施形態では、金型口開口部は非常に扁平な卵形を有する);又はそれらの何らかの組合せを有し得る。例えば円形横断面を有する口は、約0.1mmから約50mm、あるいは約0.5mmから約20mm、例えば約1mmから約10mmの直径を有する多層シート又はラミネートを提供するように調節することができる。
【0143】
粒子に成形した後、共押出粒子を収集し、そのような固体医薬組成物が使用されるいかなる方法でも使用することができる。場合により、粒子に成形した後、粒子をNo.16 TBC(約0.054")及びNo.26 TBC(約0.031")開放スクリーンを使用する分離器に通して、収集する。好ましい実施形態では、逆作用薬を含有する共押出粒子と作用薬を含有する粒子を、患者への経口投与のための硬ゼラチンカプセル中に一緒に入れる。
【0144】
1つの実施形態では、投与剤型は、ゼラチンカプセルに入った、コア及び場合によりシェルを含む複数の粒子を含有する。
【0145】
1つの実施形態では、投与剤型は、ゼラチンカプセルに入った、コア、場合により鞘、及びシェルを含む複数の粒子を含有する。
【0146】
コア、場合により鞘、及びシェルの組成物及び寸法が、作用薬の所望放出速度を達成するように変化させ得ることは、製薬押出技術の当業者には明白である。例えば共押出金型出口寸法を変えることにより、コア、鞘及びシェルの厚さを変化させ得る。ある実施形態では、コア、鞘及びシェルの厚さは各々約0.05mmから約3.0mmであり得る;1つの実施形態では、約0.2mmから約1.0mmであり得る。鞘の所望の厚さは、例えば疎水性マトリックス材料の溶解速度及びコアの厚さによって決定され得る。ある実施形態では、鞘の厚さは約0.05mmから約3.0mmである;1つの実施形態では、約0.1mmから約1.0mmである。シェルの厚さは、例えばシェル組成物及び作用薬の所望放出速度に基づいて調節することができる。ある実施形態では、シェルの厚さは約0.05mmから約3.0mmであり得る;1つの実施形態では約0.1mmから約1.0mmであり得る。ある実施形態では、コア、任意の鞘、及びシェルの厚さは、約5.0mm以下の最大寸法;1つの実施形態では、約3.0mm以下の最大寸法、を有する粒子を提供するように調節することができる。
【0147】
1つの実施形態では、投与剤型は複数のMEMを含む。場合により、切断及び/又はパンチ後、粒子を、例えばNo.16 TBC及びNo.26 TBC開放スクリーンを使用する分離器に通して、収集することができる。1つの実施形態では、粒子を、患者への経口投与のための硬又は軟ゼラチンカプセルに入れる。
【0148】
図1a、1b及び1cは、本発明の共押出粒子又は錠剤の3つの実施形態の透視図を示す。図1a、1b及び1cの各々において、コア3は逆作用薬と疎水性材料を含有する。図1aにおいて、疎水性材料を含有する鞘2は、コア3を完全に覆って取り囲む。シェル1は、作用薬と疎水性材料を含有し、鞘2を完全に覆って取り囲む。
【0149】
図1bに示す実施形態では、鞘2は、上方鞘成分2aと下方鞘成分2bを含む。鞘2はコア3の上部と底部を取り囲むが、少量のコア3を粒子の側面に沿って露出したまま残す。同様に、シェル1は、上方シェル成分1aと下方シェル成分1bを含む。シェル1は鞘2の上部と底部を取り囲むが、鞘2及び/又はコア3の小さな部分を粒子の側面に沿って露出したまま残す。
【0150】
図1cでは、鞘2は、コア3の上部と底部を取り囲み、コア3の小さな部分を側面に沿って露出したまま残す、上方鞘成分2aと下方鞘成分2bを含む。この実施形態では、シェル1は鞘2とコア3の両方を完全に覆って取り囲む。
【0151】
ある実施形態では、吸着剤/逆作用薬は、押出された粒子又は共押出された多層粒子のコア中に存在する。吸着剤/逆作用薬を含有するコアは、場合により1種以上の結合剤、付加的な遅延剤、可塑剤、及び/又は賦形剤を含み得る。結合剤は、マトリックスの完全性を維持するために有用であり、また体液中への逆作用薬の放出を防止する、阻止する又は遅延させるのに役立ち得る。結合剤の例は、天然及び合成ろう、水不溶性ろう、脂肪アルコール、例えばステアリルアルコール、脂肪酸、例えばステアリン酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、及び炭化水素骨格を有する疎水性及び親水性ポリマー、水溶性ポリマー、例えばヒドロキシセルロース、並びに前記のいずれか2つ以上の混合物を含む。
【0152】
可塑剤は、疎水性マトリックス材料がセルロースポリマー又はアクリルポリマーを含むとき有用である。適切な可塑剤の非限定的な例は、例えばアセチルトリエチルシトレート及び/又はアセチルトリブチルシトレートを含む。
【0153】
吸着剤/逆作用薬含有コアはまた、押出の間の製剤の加工性を改善するため及び/又は最終生成物の性質を改善するために添加することができる、他の賦形剤も含み得る。液体賦形剤の非限定的な例は、水及び、石油、動物、植物又は合成起源のものを含む油、例えば落花生油、ダイズ油、鉱物油、ゴマ油、ヒマシ油、トリグリセリド等を含む。固体賦形剤の例は、ステアリン酸マグネシウム、食塩水、アカシアゴム、ゼラチン、デンプンペースト、滑石、ケラチン、コロイド状シリカ、尿素等を含む。着色料もコアに添加し得る。賦型剤は吸着剤材料と同じであってもよく又は異なっていてもよい。
【0154】
ある実施形態では、本発明の投与剤型のコアは、シェルに関して5.8.2.1章で開示する物質の1種以上を含み得る。
【0155】
5.8.2.1
鞘(Sheath)
ある実施形態では、本発明の投与剤型は、吸着剤/逆作用薬を含有するコアを少なくとも部分的に取り囲む、好ましくは吸着剤/逆作用薬を含有するコアの大部分を取り囲む鞘を含み得る。ある実施形態では、鞘は、好ましくは疎水性マトリックス材料を含み、及び場合により結合剤、付加的な遅延剤、可塑剤及び賦形剤を含む。ある実施形態では、鞘は小さなパーセンテージの逆作用薬及び/又は作用薬を含有し得るが、鞘はいかなる逆作用薬又は作用薬も含有しないことが好ましい。
【0156】
1つの実施形態では、鞘の疎水性マトリックス材料は、アクリル酸及びメタクリル酸のポリマー及びコポリマー、及び疎水性被覆材料について上述した水不溶性アルキルセルロースからなる群より選択される1種以上の物質を含む。鞘は、場合により1種以上の付加的な疎水性材料、例えばコアについて上述したような、シェラック、ゼイン、硬化ヒマシ油、硬化植物油及びそれらの混合物を含有し得る。
【0157】
鞘において使用される疎水性マトリックス材料は、場合により疎水性被覆材料として使用されるものと同じであってもよく又は異なっていてもよい。鞘において使用される疎水性材料は、好ましくは胃腸管内で実質的に不溶性であるが、この材料はインビボである限られた程度まで経時的に溶解又は生分解することができ、それによって吸着剤材料からの少量の逆作用薬がコアからインビボ放出することを許容する。製薬技術の当業者は、例えば鞘の組成物を変えること、鞘の厚さを上昇させること、コアのより大きな割合を鞘で取り囲むこと、コアの大きさ及び/又は寸法を変えること、及び/又は鞘及び/又はコアの組成物を変えることによって、そのような放出の速度を変化させることができる。これらや他の方法は、当業者に公知であるか又はこの開示を考慮して常用実験によって決定され得る。
【0158】
ある実施形態では、鞘は、約10重量%から約99重量%、好ましくは約40重量%から約95重量%、より好ましくは約60重量%から約90重量%の1種以上の疎水性マトリックス材料を含有し得る。
【0159】
鞘は、1種以上の付加的な遅延剤、あるいは1種以上の結合剤又は可塑剤又は賦形剤、あるいはそれらの何らかの組合せ、例えば逆作用薬含有コアに関して5.8.2章で上述したものをさらに含有し得る。
【0160】
5.8.2.2
シェル
ある実施形態では、本発明の投与剤型は、作用薬を含有するシェルを含み得る。投与剤型は、投与後にシェルからインビボで作用薬の何らかの速度の放出、例えば即時放出、制御放出又は遅延放出を提供することができる。ある実施形態では、投与剤型は、作用薬、例えばオピオイドアゴニストの制御放出を提供する。オピオイドアゴニストの制御放出投与剤型の製剤及び製造の方法は、当技術分野において公知である。例えば、各々その全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第5,958,452号;同第5,965,161号;同第5,968,551号;同第6,294,195号及び同第6,335,033号は、制御放出オピオイドアゴニスト投与剤型を開示する。そのような特許の1つ以上の開示は、制御放出オピオイドアゴニスト投与剤型についての詳細、例えば製剤、疎水性マトリックス材料、遅延剤、結合剤、可塑剤及び賦形剤、並びにMEMを含有する錠剤、カプレット及びカプセルを形成するための押出方法を含む。
【0161】
ある実施形態では、作用薬は、経口投与後インビボで作用薬の制御放出を提供するマトリックス中に分散し得る。医薬組成物又は投与剤型を製造するためのいかなる適切な制御放出マトリックスも使用できる。ある種の制御放出マトリックスが経口製剤に関して公知である(例えばその開示全体が全ての目的に関して参照により明白に本明細書に組み込まれる、Lee et al., "Controlled-Release Drug-Delivery Systems" in Remington's: The Science and Practice of Pharmacy 903-929 (20th ed.2000)参照)。上記で特定した特許及び出版物に開示されている制御放出投与剤型に加えて、有用な制御放出マトリックスの他の例は、各々その内容全体が全ての目的に関して参照により明白に本明細書に組み込まれる、米国特許第6,143,328号;同第5,266,331号;同第5,549,912号;同第5,508,042号;同第5,656,295号;同第5,324,351号;同第5,356,467号及び同第5,472,712号に述べられている。
【0162】
制御放出マトリックスは、場合により親水性材料と組み合わせた、可融疎水性材料を含み得る。可融疎水性材料は、例えば約45℃から約100℃の融点、1つの実施形態では約50℃から約90℃の融点を有し得る、例えば疎水性ポリマーあるいは天然又は合成ろう又は油、例えば硬化植物油又は硬化ヒマシ油であり得る。疎水性材料は、疎水性被覆材料として使用されるものと同じであり得る。親水性材料は、親水性ポリマー、例えばヒドロキシセルロース;水溶性可融物質、例えばポリエチレングリコール;水溶性微粒子物質、例えばラクトース;又はわずかに水溶性の微粒子物質、例えばリン酸二カルシウムであり得る。
【0163】
本発明に従った制御放出投与剤型を製造するため、任意の公知の共押出方法を使用できるが、好ましい方法は、適切なマトリックス材料と成分の溶融共押出である。例えば制御放出マトリックスに分散した作用薬を含有するシェルは、例えば以下の1種以上を含むがこれらに限定されない、適切な非可融材料と共に作用薬を押出することによって製造することできる:
【0164】
(a)親水性又は疎水性ポリマー、例えばゴム、セルロースエーテル、タンパク質由来物質、ナイロン、アクリル樹脂、ポリ乳酸、ポリ塩化ビニル、デンプン、ポリビニルピロリドン、及びセルロースアセテートフタレート。これらのポリマーのうちで、セルロースエーテル、例えば置換セルロースエーテル、例えばアルキルセルロース(例えばエチルセルロース)、C1−C6ヒドロキシアルキルセルロース(例えばヒドロキシプロピルセルロース及びヒドロキシエチルセルロース)、及びアクリル樹脂(例えばメタクリレート、例えばメタクリル酸コポリマー)が使用できる。制御放出マトリックスは、好都合には約1重量%から約80重量%の疎水性及び/又は親水性ポリマーを含有し得る。
【0165】
(b)可消化、長鎖(C8−C50、1つの実施形態ではC8−C40)置換又は非置換炭化水素、例えば脂肪酸;硬化植物油;脂肪アルコール、例えばラウリル、ミリスチル、ステアリル、セチル又は、1つの実施形態ではセトステアリルアルコール;脂肪酸のグリセリルエステル、例えばモノステアリン酸グリセリル;鉱物油;及びろう、例えば蜜ろう、グリコワックス、カスターワックス、及びカルナウバろう。1つの実施形態では約25℃から約90℃の融点を有する炭化水素を使用する。これらの長鎖炭化水素物質のうちで、脂肪アルコールは1つの実施形態において有用である。制御放出マトリックスは、約60重量%までの少なくとも1つの可消化長鎖炭化水素を含有し得る。
【0166】
(c)ポリアルキレングリコール。制御放出マトリックスは、約60重量%までの少なくとも1つのポリアルキレングリコールを含有し得る。ポリアルキレングリコールは、例えばポリプロピレングリコール、又は1つの実施形態ではポリエチレングリコールであり得る。ポリアルキレングリコールの数平均分子量は、1つの実施形態では約200から約15,000ダルトンであり、もう1つの実施形態では約400から約12,000ダルトンである。
【0167】
1つの実施形態では、本発明の投与剤型における使用のための適切な制御放出マトリックスは、1種以上のセルロースエーテル又はアクリル樹脂、あるいは1種以上のC12−C36脂肪アルコール;もう1つの実施形態では、C12−C22脂肪アルコール及び/又は1種以上の硬化植物油を含み得る。1つの実施形態では、特に適切なマトリックスは、1種以上のアルキルセルロース、あるいは1種以上のC12−C36脂肪アルコール;もう1つの実施形態では、C12−C22脂肪アルコール及び、場合により、1種以上のポリアルキレングリコールを含む。もう1つの実施形態では、マトリックスは、約0.5重量%から約60重量%、もう1つの実施形態では約1重量%から約50重量%のセルロースエーテルを含有し得る。
【0168】
アクリル樹脂は、例えばメタクリレート、例えばメタクリル酸コポリマー、USNF A型(EUDRAGIT L)、B型(EUDRAGIT S)、C型(EUDRAGIT L 100-55)、EUDRAGIT NE 30 D、EUDRAGIT E、EUDRAGIT RL、又はEUDRAGIT RS(Rohm Pharma GmbH, Weiterstat, Germanyから市販されている)であり得る。1つの実施形態では、マトリックスは、約0.5重量%から約95重量%のアクリル樹脂、もう1つの実施形態では約10重量%から約50重量%のアクリル樹脂を含有する。
【0169】
ポリアルキレングリコールが存在しない場合、マトリックスは、1つの実施形態では約1重量%から約40重量%、もう1つの実施形態では約2重量%から約36重量%の脂肪アルコールを含有する。ポリアルキレングリコールが経口投与剤型中に存在するときは、脂肪アルコールとポリアルキレングリコールの合計重量は、1つの実施形態ではマトリックスの約2重量%から約40重量%、もう1つの実施形態ではマトリックスの約2重量%から約36重量%を構成する。
【0170】
ポリアルキレングリコールは、例えばポリプロピレングリコール又は、1つの実施形態ではポリエチレングリコールであり得る。ポリアルキレングリコールの数平均分子量は、1つの実施形態では約200〜約15,000ダルトン、もう1つの実施形態では約400〜約12,000ダルトンである。
【0171】
錠剤製剤を製造するための方法
上述したように、本発明はまた、吸着剤/逆作用薬を含有する錠剤又は粒子に関する。本発明の吸着剤/逆作用薬を含有する錠剤は従来の手段によって製造することができる(例えば、全ての目的に関してその全体が参照により明白に本明細書に組み込まれる、Rudnic et al., "Oral Dosage Forms" in Remington's: The Science and Practiceof Pharmacy 858-885 (20th ed. 2000)参照)。1つの実施形態では、粒子又は錠剤は、作用薬と吸着剤/逆作用薬を含有する製剤を造粒し、圧縮することによって製造される。
【0172】
もう1つの実施形態では、錠剤は、作用薬を含有する複数の第一粒子及び吸着剤/逆作用薬を含有する複数の第二粒子を圧縮することによって製造される。
【0173】
もう1つの実施形態では、粒子又は錠剤は、吸着剤/逆作用薬を含有するコア及び作用薬を含有するシェルを含み、シェルがコアを少なくとも部分的に覆う投与剤型を造粒し、圧縮することによって製造される。
【0174】
粒子又は錠剤は、何らかの幾何学的形状、例えば球、長円体、ペレット等であり得、製造の方法、作用薬及び吸着剤/逆作用薬の量及び種類、及び標的とする患者に依存していかなる寸法においても大きさが異なり得ることは了解されるべきである。ある実施形態では、本発明の錠剤は、いかなる方向でも約5mmから約75mmの寸法を有する;もう1つの実施形態では、錠剤は、いかなる方向でも約5mmから約30mmの寸法を有する;及びもう1つの実施形態では、錠剤は、いかなる方向でも約5mmから約15mmの寸法を有する。
【0175】
本発明の粒子又は錠剤は、上記5.8.2.1章で定義したような製薬上許容し得る疎水性被覆材料;賦形剤、例えば結合剤(例えばプレゼラチン化トウモロコシデンプン、ポリビニルピロリドン又はヒドロキシプロピルメチルセルロース);充填剤(例えばラクトース、微結晶セルロース又はリン酸水素カルシウム);潤滑剤(例えばステアリン酸マグネシウム、滑石又はシリカ);崩壊剤(例えばジャガイモデンプン又はグリコール酸デンプンナトリウム);湿潤剤(例えばラウリル硫酸ナトリウム);及び当技術分野で周知の他の添加物又は賦形剤をさらに含み得る。錠剤は、そのような被覆が錠剤の意図される使用を妨げないことを条件として、当技術分野で周知の方法によって被覆することができる。被覆工程の非限定的な例は、噴霧被覆である。1つの実施形態では、錠剤は浸漬被覆によって形成される。
【0176】
溶融押出組成物から錠剤を製造するための他の方法は上記に述べられている。
【0177】
投与のための方法
本発明はまた、治療の必要のある患者に本発明の投与剤型を投与することを含む、患者において病気を治療するための方法を対象とする。投与剤型は、例えば経口投与剤型、例えば錠剤又はカプセル、あるいは直腸又は膣投与剤型、例えば坐薬であり得る。1つの実施形態では、病気は疼痛であり、投与剤型はオピオイドと吸着剤/オピオイドアンタゴニストを含有する。ある実施形態では、投与剤型を1日2回患者に投与し、他の実施形態では1日1回投与する。
【0178】
投与単位当りの量
本発明の投与剤型では、投与単位当りの作用薬の量は、その特定適応症についての有効量であり、逆作用薬の量とは無関係である。例えば治療薬がオピオイドアゴニストである場合、本発明の投与剤型中のオピオイドアゴニストの量は約1mgから約800mg;1つの実施形態では約5mgから約160mgである。当業者は、過剰な実験を必要とせずに、特定適応症のために必要な治療薬の量を容易に決定することができる。
【0179】
本発明の投与剤型中の逆作用薬の量は、不正使用されたとき実質的な量の逆作用薬が直ちに投与剤型から放出され、動物の血液中に吸収された場合に、逆作用薬が意図される逆作用を与えることができる量である。投与剤型が不正使用された場合、逆作用薬が作用薬の薬理作用の1種以上、例えば陶酔作用を低減する又は排除することが意図されているとき、投与剤型中の逆作用薬の量は、少なくとも、不正使用が起こった後両方の薬剤が投与剤型から実質的に又は完全に放出されて動物の血液中に吸収されたとき、作用薬の作用を低減する又は排除するのに十分である。
【0180】
例えば、1つの実施形態では、逆作用薬がオピオイドアンタゴニスト、例えばナルトレキソン又はナルメフェンであるとき、本発明の投与剤型中に存在するオピオイドアンタゴニストの量は、約0.1mgから約50mg又はそれ以上であり得る。オピオイドアンタゴニスト、シクラゾシン及びナルトレキソンは、経口投与したとき、24時間に近い長い作用期間にわたってそれらの効果の多くを保持する。これらのオピオイドアンタゴニストの約10mg未満の量を本発明の経口製剤において使用する。
【0181】
不正使用された場合、逆作用薬が望ましくない生理的反応、例えば嘔吐を引き起こすことが意図されているとき、投与剤型中の逆作用薬の量は、少なくとも、不正使用が起こった後の放出時にそのような作用を引き起こすのに十分である。
【0182】
安全性の理由から、投与剤型中に存在する逆作用薬の量は、全部が直ちに放出された場合でもヒトに対して有害であってはならない。当業者は、過剰な実験を必要とせずに、有害性を伴わずに意図される逆作用を惹起するために必要な逆作用薬の量を容易に決定することができる。
【0183】
本発明のある実施形態では、投与剤型中の治療薬対逆作用薬の比率は、重量比で約1:1から約50:1、1つの実施形態では重量比で約1:1から約20:1であり得る。他のある実施形態では、前記比率は、重量比で約1:1から約10:1であり得る。
【0184】
オピオイドアゴニストがヒドロコドンである非限定的実施形態では、制御放出投与剤型は、投与単位当りヒドロコドン約5mgから約80mgの鎮痛用量を含有し得る。オピオイドアゴニストがヒドロモルフォンである非限定的実施形態では、投与単位当り塩酸ヒドロモルフォン約2mgから約64mgの量で含有され得る。オピオイドアゴニストがモルフィンである非限定的実施形態では、投与単位当りモルフィン約2.5mgから約800mgが投与剤型中に存在し得る。オピオイドアゴニストがオキシコドンである非限定的実施形態では、投与剤型は、投与単位当りオキシコドン約2.5mgから約160mg、もう1つの実施形態では、オキシコドン約20mgから約30mgを含有し得る。制御放出オキシコドン製剤は当技術分野において公知である。非限定的実施形態では、オピオイドアゴニストは、投与単位当り約25mgから800mgの量のトラマドールであり得る。投与剤型は1種以上のオピオイドアゴニストを含有することができ、各々の用量は適宜に調節することができる。
【0185】
「単位用量」という用語は、本発明に関して、作用薬(例えばオピオイドアゴニスト)の単回所望用量を患者に投与するために必要な投与剤型の総量と定義される。
【0186】
膣又は直腸投与のための方法
上述したように、本発明はまた、膣又は直腸を通した吸収のための坐薬の形態の、作用薬及び吸着剤/逆作用薬を含有する投与剤型の投与を対象とする。坐薬として投与するとき、組成物は、好ましくは坐薬基材を含む。微粒子を溶解しないことを条件として、いかなる坐薬基剤も使用することができる。例えばココアバターは、その融点をわずかに上昇させるためにろうの添加によって改変し得る、伝統的な坐薬基材である。1種以上の水混和性坐薬基材、例えば様々な分子量のポリエチレングリコールが含まれ得る。坐薬として投与したとき、坐薬製剤中の複数の第一及び第二粒子の合計濃度は、1つの実施形態では、組成物の約5.0重量%から約80重量%である。
【0187】
キット
本発明はまた、少なくとも1つの本発明の投与剤型を含むキットを対象とする。1つの実施形態では、投与剤型は容器、例えばビン又は箱の中に存在する。もう1つの実施形態では、キットは、例えば疼痛のために、患者を治療するための投与剤型の使用を指示する説明書のセットをさらに含む。1つの実施形態では、説明書は、容器に貼付された印刷ラベルであるか又は容器上に印刷され得る。もう1つの実施形態では、説明書は、容器中又は容器を含む包装中に挿入された印刷紙を含み得る。説明書はまた、投与剤型及び/又はその使用が投与剤型の乱用、誤用又は転用を低減するように設計されていることを言明し得る。
【0188】
本明細書において言及する全ての特許、特許出願、試験方法、文献、及び他の資料は、全ての目的に関してそれらの全体が参照により明白に本明細書に組み込まれる。
【0189】
実施例
以下の実施例は本発明の理解を助けるために提示するものであり、本明細書で説明し、特許請求する本発明を、特定して限定すると解釈されるべきではない。当業者の範囲内である、現在公知の又は今後開発される全ての等価物の置換、及び製剤の変更又は実験計画の重要でない変更を含む、本発明のそのような変法は、本発明の範囲内に属するとみなされるべきである。
【実施例1】
【0190】
炭/ナルトレキソンの製造及び性質
実施例1は、吸着剤/逆作用薬を製造するための非限定的な方法を説明する。使用した吸着剤は、Merck KGaA of Darmstadt,Germanyの系列会社であるEM Scienceより入手したDARCO活性炭であった。使用したDARCO活性炭は、活性炭についてのUSP吸収能試験(米国薬局方 26:404(2003)参照)に合格した20から40メッシュの黒色粒状炭であった。
【0191】
ナルトレキソンの吸着: 活性炭(5.02g)を、0.1N HCl(900mL)中の塩酸ナルトレキソン(504.26mg)(Mallinkrodt,St.Louis MOより入手した)の溶液に添加した。生じた混合物を37℃、100rpmで120時間攪拌し、高性能液体クロマトグラフィー(HPLC)を用いて液相中の塩酸ナルトレキソンの濃度低下を測定することにより、活性炭への塩酸ナルトレキソンの吸着(又は取込み)を観測した。そのデータを使用して、例えば2時間後の、活性炭に吸着されたナルトレキソンの量を以下のように算定した:
【0192】
吸着されたナルトレキソン
=(ナルトレキソン(初期))×〔1−(HPLCピーク面積(T=2時間)/HPLCピーク面積(T=0))〕
【0193】
吸着されたナルトレキソン
=(504.26mg)×〔1−(215860/483568)〕=279.16mg
【0194】
データを表2に示し、図2にグラフで表す。
【0195】
【表2】

【0196】
結果は、実質的に全部のナルトレキソンの吸着が約1.5時間以内に完了したことを示した。混合物を、半融ガラスフリットを用いて真空ろ過した。炭吸着剤ナルトレキソン逆作用薬を自由流動粉末(「炭/ナルトレキソン」)として与えるために、生じたろ過ケーキを動的真空下でガラスフリット上に維持した。図2のデータに基づき、工程終了時(t=2時間)の炭/ナルトレキソン中の塩酸ナルトレキソンの算定含量は5.56重量%であった。
【0197】
炭/ナルトレキソンの動的脱着: 上述したように調製した炭/ナルトレキソンを1リットル半融ガラスろ過漏斗に移し、25℃で0.1N HClの63×1Lアリコート(63 1L aliquots)によって洗浄した。洗浄ろ液中の塩酸ナルトレキソンの濃度を、上述したようにHPLCを用いて測定した。結果を表3に示し、図3にグラフで表す。
【0198】
【表3】

【0199】
結果は、塩酸ナルトレキソンの脱着の大部分が最初の18回の洗浄工程の間に生じたことを示した。
【実施例2】
【0200】
酸洗浄した炭/ナルトレキソンの製造及び性質
酸洗浄: 最後の洗浄後、実施例1から生じたケーキを、酸洗浄した炭/ナルトレキソン(「酸洗浄炭/ナルトレキソン」)の乾燥自由流動固体形態を与えるためにろ過フラスコで乾燥した。乳鉢と乳棒を用いて固体の一部を微細粉末に摩砕し、その後以下のようにメタノールで抽出することによって酸洗浄炭/ナルトレキソン中の塩酸ナルトレキソン含量を測定した。計量した摩砕酸洗浄炭/ナルトレキソンの一部(約50mg)を100mLメスフラスコに添加し、メタノール50mLを加えて、約25℃で、生じた混合物を15分間超音波処理した。超音波処理後、混合物を放置して約25℃に冷却させた。4.000mLアリコートをピペットで取り出し、250mLメスフラスコに移して、0.1N HClで250.00mLに希釈した。希釈した混合物を25℃で15〜30分間振とうし、生じた混濁液体をWhatman HXナイロンろ紙を通してろ過した。次に、ろ液中のナルトレキソンの濃度を、ナルトレキソン標準品に対してHPLCを用いて測定した。平均ナルトレキソン含量(n=摩砕した酸洗浄炭/ナルトレキソンの3試料)は3.06重量%であった。
【0201】
酸洗浄炭/ナルトレキソンの静的脱着: 上記からの酸洗浄炭/ナルトレキソンの一部(約50mg)を、37℃の温度で0.1N HCl 900mLを含むパドル付き2000mLビーカーに添加した。ビーカーの内容物を100rpmで72時間混合し、HPLCを用いて液相中のナルトレキソン濃度を観測した。静的脱着試験において得られたデータを、薬剤全部が脱着された場合のナルトレキソンの理論的濃度に基準化した。データを表4に示し、図4にグラフで表す。各々の点は酸洗浄炭/ナルトレキソンのn=6試料の平均値に相当する。
【0202】
【表4】

【0203】
結果は、脱着可能なナルトレキソンの大部分(全部ではない)が、最初の36時間以内に脱着することを示した。静的脱着の72時間後の液相中のナルトレキソンの含量に基づき、酸洗浄炭/ナルトレキソン中に残存するナルトレキソンの算定含量は、その初期値(3.06重量%)の61%又は約1.9重量%であった。
【0204】
上記脱着試験の結果は、吸着剤/逆作用薬、例えば炭/ナルトレキソンが、逆作用薬の望ましくない放出を防止するために有用であることを示した。
【実施例3】
【0205】
疎水性マトリックス材料で密封した炭/ナルトレキソンの製造及び性質
疎水性材料での炭/ナルトレキソンの密封: ステアリルアルコール(約10〜15g)を含むビーカーを高温プレート上に置き、熱を加えてアルコールを溶融し、溶融物を67℃の温度までさらに加熱した。実施例1で製造した炭/ナルトレキソンの一部(200.41mg)を100メッシュのUSP溶解バスケットに添加した。バスケットを5〜10分間前記溶融物中に完全に液浸し、炭/ナルトレキソンの被覆を助けるために往復運動で上下に動かした。バスケットを溶融物から取り出し、放置して周囲温度に冷却して、密封された炭/ナルトレキソン(「密封炭/ナルトレキソン」)(472.45mg)を、白色の陰影を伴う黒色固体として得た。密封炭/ナルトレキソン中の塩酸ナルトレキソンの含量を、炭/ナルトレキソン出発物質の重量及びそのナルトレキソン含量(3.06重量%)を密封炭/ナルトレキソン生成物の重量と共に使用して算定した。
【0206】
ナルトレキソン含量
=(3.06重量%)×〔(炭/ナルトレキソンの重量)/(密封炭/ナルトレキソンの重量)〕
【0207】
ナルトレキソン含量
=(3.06重量%)×〔(200.14mg)/(472.45mg)〕=1.30重量%
【0208】
密封炭/ナルトレキソンの静的脱着: 密封炭/ナルトレキソンの一部(約77mg)を、0.1N HCl(900mL)を含むパドル付き2000mLビーカーに添加し、内容物を37℃、100rpmで72時間混合した。HPLCを用いて液相中のナルトレキソン濃度を観測した。静的脱着試験において得られたデータを表5に示し、図5にグラフで表しており(−○−○−○−)、密封炭/ナルトレキソンのn=6試料の平均値を示す。比較として、実施例1で製造した炭/ナルトレキソン(−□−□−□−)(n=6試料)に関して同じデータを収集し、図5にグラフで表した。
【0209】
【表5】

【0210】
炭/ナルトレキソンを72時間混合した後、液相中の塩酸ナルトレキソンの濃度は約610ng/mLであった。これに対し、密封炭/ナルトレキソンを72時間混合した後、液相中の塩酸ナルトレキソンの濃度はわずかに約42ng/mLであった。結果は、炭/ナルトレキソンを適切な疎水性被覆材料で密封することは吸着剤からの逆作用薬の望ましくない放出をさらに防止することを示した。
【実施例4】
【0211】
疎水性マトリックス材料で密封した酸洗浄炭/ナルトレキソンの製造
疎水性材料での酸洗浄炭/ナルトレキソンの密封: 実施例2で製造した酸洗浄炭/ナルトレキソンを使用して、実施例3で述べたステアリルアルコール被覆手順を反復した。密封した酸洗浄炭/ナルトレキソン(「密封酸洗浄炭/ナルトレキソン」)中の塩酸ナルトレキソンの含量を、酸洗浄炭/ナルトレキソン出発物質の重量及びそのナルトレキソン含量(3.06重量%)を密封酸洗浄炭/ナルトレキソンの重量と共に使用して算定した。密封酸洗浄炭/ナルトレキソン生成物中の塩酸ナルトレキソンの平均含量(密封酸洗浄炭/ナルトレキソンのn=6試料に基づく)は1.30重量%であった。
【0212】
密封酸洗浄炭/ナルトレキソンのインビトロ脱着: 密封酸洗浄炭/ナルトレキソンの一部(約250mg)を、37℃で0.1N HCl 900mLを含む、パドル付きUSP 2型溶解容器に添加し、溶解容器の内容物を100rpmで120時間混合した。液相の分析(HPLC)は、少なくとも120時間にわたって検出可能なナルトレキソンが放出されなかったことを示した。
【実施例5】
【0213】
不正使用時の密封酸洗浄炭/ナルトレキソンからのナルトレキソンの放出
実施例4からの密封酸洗浄炭/ナルトレキソンの試料を、微細分割された粉末が形成されるまで乳鉢と乳棒を用いて破砕した。計量した試料の部分(各々約0.025g)を、脱イオン蒸留水(pH6.5)又は水中40%エタノールのいずれか10.00mLを含むシンチレーションバイアルに添加した。生じた混合物を25℃又は100℃で10分間、手で振とうすることによって抽出した。次に、試料の液相中のナルトレキソンの含量を、公知のナルトレキソン標準品に対してHPLCを用いて測定し、結果を以下の表6に示す。また表6は、水又はメタノール中25℃で抽出した破砕していない密封酸洗浄炭/ナルトレキソンについての比較データも含む。
【0214】
【表6】

【0215】
試験の結果は、不正使用、例えば破砕、に供していない密封酸洗浄炭/ナルトレキソンは有意の量のナルトレキソンを放出しない、すなわち約0mgのナルトレキソンが放出されたことを示した。結果はまた、不正使用、例えば破砕後に水又はアルコール含有溶媒による抽出、に供した密封酸洗浄炭/ナルトレキソンの試料がナルトレキソンを放出することを示した。表6のデータはさらに、密封酸洗浄炭/ナルトレキソンの破砕試料からの放出の程度が高温で上昇することを示した。結果は、密封酸洗浄炭/ナルトレキソンが不正使用防止投与剤型において有用であることを示す。
【図面の簡単な説明】
【0216】
【図1】図1a、1b及び1cは、本発明の投与剤型の3つの実施形態の透視図を示す。
【図2】塩酸ナルトレキソンの活性炭への吸着(mg)を時間の関数として示すグラフである。
【図3】活性炭からの塩酸ナルトレキソンの脱着(ng/mL洗浄液)を洗浄液リットルの関数として示すグラフである。
【図4】活性炭からの塩酸ナルトレキソンの脱着(%)を時間の関数として示すグラフである。
【図5】インビトロ刺激溶解試験におけるa)密封活性炭及びb)非密封活性炭からの塩酸ナルトレキソンの脱着(μg)を時間の関数として示す比較グラフである。
【特許請求の範囲】
【請求項1】
吸着剤と逆作用薬とを含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型。
【請求項2】
前記逆作用薬の少なくとも80重量%が前記吸着剤に吸着されている、請求項1記載の投与剤型。
【請求項3】
前記逆作用薬の少なくとも90重量%が前記吸着剤に吸着されている、請求項2記載の投与剤型。
【請求項4】
前記吸着剤が、活性炭、アルミナ、二酸化ケイ素ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項1記載の投与剤型。
【請求項5】
前記吸着剤が活性炭である、請求項4記載の投与剤型。
【請求項6】
前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料をさらに含む、請求項1記載の投与剤型。
【請求項7】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項6記載の経口投与剤型。
【請求項8】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項7記載の経口投与剤型。
【請求項9】
前記投与剤型が経口投与剤型である、請求項1記載の投与剤型。
【請求項10】
前記投与剤型が、無傷投与後にインビボで約0.5mg以下の前記逆作用薬を放出する、請求項1記載の投与剤型。
【請求項11】
前記投与剤型が、無傷投与後にインビボで約0.05mg以下の前記逆作用薬を放出する、請求項1記載の投与剤型。
【請求項12】
作用薬を含む複数の第一粒子;及び
吸着剤と逆作用薬を含む複数の第二粒子
を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型。
【請求項13】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項12記載の投与剤型。
【請求項14】
前記吸着剤が活性炭である、請求項13記載の投与剤型。
【請求項15】
前記の複数の第二粒子が、前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料をさらに含む、請求項12記載の投与剤型。
【請求項16】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項15記載の経口投与剤型。
【請求項17】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項16記載の経口投与剤型。
【請求項18】
前記作用薬がオピオイドアゴニストであり、前記逆作用薬がオピオイドアンタゴニストである、請求項12記載の投与剤型。
【請求項19】
前記オピオイドアゴニストが、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、フェンタニル、ヘロイン、ヒドロコドン、ヒドロモルフォン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レバロルファン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルブフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パパベレタム、ペンタゾシン、フェナドキソン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロピラム、プロポキシフェン、スフェンタニル、トラマドール、チリジン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項18記載の投与剤型。
【請求項20】
前記オピオイドアゴニストが、モルフィン、コデイン、ヒドロモルフォン、ヒドロコドン、オキシコドン、オキシモルフォン、ジヒドロコデイン、ジヒドロモルフィン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項19記載の投与剤型。
【請求項21】
前記オピオイドアンタゴニストが、シクラゾシン、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項18記載の投与剤型。
【請求項22】
前記オピオイドアンタゴニストが、ナルメフェン、ナロキソン、ナルトレキソン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項21記載の投与剤型。
【請求項23】
前記投与剤型が経口投与剤型である、請求項12記載の投与剤型。
【請求項24】
前記投与剤型が、前記第一粒子と前記第二粒子とを含有するカプセルを含む、請求項23記載の投与剤型。
【請求項25】
前記投与剤型が、無傷投与後にインビボで約0.5mg以下の前記逆作用薬を放出する、請求項12記載の投与剤型。
【請求項26】
前記投与剤型が、無傷投与後にインビボで約0.05mg以下の前記逆作用薬を放出する、請求項25記載の投与剤型。
【請求項27】
オピオイドアゴニストを含む複数の第一粒子;及び
吸着剤とオピオイドアンタゴニストを含む複数の第二粒子
を含有し、
前記オピオイドアゴニストの少なくとも大部分が前記吸着剤に吸着されており、かつ
前記第一粒子が、患者への経口投与後に前記オピオイドアゴニストの制御放出を提供する、経口投与剤型。
【請求項28】
前記第一粒子及び前記第二粒子が各々、全ての寸法において約0.1mmから約3.0mmの大きさを有する、請求項27記載の経口投与剤型。
【請求項29】
前記第二粒子の各々が、前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料を含む、請求項27記載の経口投与剤型。
【請求項30】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項29記載の経口投与剤型。
【請求項31】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項30記載の経口投与剤型。
【請求項32】
前記オピオイドアゴニストが、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、フェンタニル、ヘロイン、ヒドロコドン、ヒドロモルフォン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レバロルファン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルブフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パパベレタム、ペンタゾシン、フェナドキソン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロピラム、プロポキシフェン、スフェンタニル、トラマドール、チリジン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項27記載の経口投与剤型。
【請求項33】
前記オピオイドアゴニストが、モルフィン、コデイン、ヒドロモルフォン、ヒドロコドン、オキシコドン、オキシモルフォン、ジヒドロコデイン、ジヒドロモルフィン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項32記載の経口投与剤型。
【請求項34】
前記オピオイドアンタゴニストが、シクラゾシン、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項27記載の経口投与剤型。
【請求項35】
前記オピオイドアンタゴニストが、ナロキソン、ナルトレキソン及びナルメフェン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項34記載の経口投与剤型。
【請求項36】
前記投与剤型が、前記第一粒子と前記第二粒子とを含有する錠剤を含む、請求項27記載の経口投与剤型。
【請求項37】
前記投与剤型が、前記第一粒子と前記第二粒子とを含有するカプセルを含む、請求項27記載の経口投与剤型。
【請求項38】
前記第二粒子が、無傷経口投与後にインビボで約0.5mg以下の前記オピオイドアンタゴニストを放出する、請求項27記載の経口投与剤型。
【請求項39】
前記第二粒子が、無傷経口投与後にインビボで約0.05mg以下の前記オピオイドアンタゴニストを放出する、請求項38記載の経口投与剤型。
【請求項40】
作用薬;
吸着剤;及び
逆作用薬
を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型。
【請求項41】
前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料をさらに含む、請求項40記載の投与剤型。
【請求項42】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項41記載の経口投与剤型。
【請求項43】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項42記載の投与剤型。
【請求項44】
前記作用薬がオピオイドアゴニストであり、前記逆作用薬がオピオイドアンタゴニストである、請求項40記載の投与剤型。
【請求項45】
前記オピオイドアゴニストが、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、フェンタニル、ヘロイン、ヒドロコドン、ヒドロモルフォン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レバロルファン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルブフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パパベレタム、ペンタゾシン、フェナドキソン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロピラム、プロポキシフェン、スフェンタニル、トラマドール、チリジン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項44記載の投与剤型。
【請求項46】
前記オピオイドアゴニストが、モルフィン、コデイン、ヒドロモルフォン、ヒドロコドン、オキシコドン、オキシモルフォン、ジヒドロコデイン、ジヒドロモルフィン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項45記載の投与剤型。
【請求項47】
前記オピオイドアンタゴニストが、シクラゾシン、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項44記載の投与剤型。
【請求項48】
前記オピオイドアンタゴニストが、ナルメフェン、ナロキソン、ナルトレキソン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項47記載の投与剤型。
【請求項49】
前記投与剤型が経口投与剤型である、請求項44記載の投与剤型。
【請求項50】
前記投与剤型が、複数の粒子を含有するカプセルを含む、請求項44記載の投与剤型。
【請求項51】
前記投与剤型が錠剤を含む、請求項44記載の投与剤型。
【請求項52】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項40記載の投与剤型。
【請求項53】
前記吸着剤が活性炭である、請求項52記載の投与剤型。
【請求項54】
前記投与剤型が、無傷経口投与後にインビボで約0.5mg以下の前記逆作用薬を放出する、請求項40記載の経口投与剤型。
【請求項55】
前記投与剤型が、無傷経口投与後にインビボで約0.05mg以下の前記逆作用薬を放出する、請求項54記載の経口投与剤型。
【請求項56】
前記投与剤型が、
前記吸着剤及び前記逆作用薬を含有するコア、及び
前記作用薬を含有するシェル
をさらに含み、前記シェルが前記コアの大部分を取り囲む、請求項40記載の投与剤型。
【請求項57】
吸着剤を提供すること;
逆作用薬を含有する液体を提供すること;
前記吸着剤を、前記逆作用薬を含有する前記液体と、前記逆作用薬の少なくとも一部が前記吸着剤に吸着するのに十分な時間接触させること
を含む、投与剤型を製造する方法。
【請求項58】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項57記載の方法。
【請求項59】
前記液相から前記吸着剤を除去した後、少なくとも1つの疎水性材料を前記吸着剤の外側表面に適用することをさらに含む、請求項57記載の方法。
【請求項60】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項59記載の方法。
【請求項61】
前記逆作用薬がオピオイドアンタゴニストである、請求項57記載の方法。
【請求項62】
前記吸着剤及びオピオイドアゴニストを投与剤型に添加することをさらに含む、請求項61記載の方法。
【請求項63】
吸着剤を提供すること;
逆作用薬を含有する液体を提供すること;
前記吸着剤を流動床に添加すること;
前記吸着剤を流動化すること;
前記液体を流動化した吸着剤に噴霧すること;及び
場合により、前記吸着剤を乾燥すること
を含む、投与剤型を製造する方法。
【請求項64】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項63記載の方法。
【請求項65】
前記液相から前記吸着剤を除去した後、少なくとも1つの疎水性材料を前記吸着剤の外側表面に適用することをさらに含む、請求項63記載の方法。
【請求項66】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項65記載の方法。
【請求項67】
前記逆作用薬がオピオイドアンタゴニストである、請求項63記載の方法。
【請求項68】
前記吸着剤及びオピオイドアゴニストを投与剤型に添加することをさらに含む、請求項63記載の方法。
【請求項69】
請求項40記載の投与剤型を患者に投与することを含む、患者の病気又はその症状を治療する方法。
【請求項70】
請求項27記載の投与剤型を患者に投与することを含む、疼痛を有する患者を治療する方法。
【請求項71】
請求項27記載の投与剤型、及び疼痛の治療のために前記投与剤型の投与を患者に指示する説明書を含む、疼痛を有する患者を治療するためのキット。
【請求項1】
吸着剤と逆作用薬とを含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型。
【請求項2】
前記逆作用薬の少なくとも80重量%が前記吸着剤に吸着されている、請求項1記載の投与剤型。
【請求項3】
前記逆作用薬の少なくとも90重量%が前記吸着剤に吸着されている、請求項2記載の投与剤型。
【請求項4】
前記吸着剤が、活性炭、アルミナ、二酸化ケイ素ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項1記載の投与剤型。
【請求項5】
前記吸着剤が活性炭である、請求項4記載の投与剤型。
【請求項6】
前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料をさらに含む、請求項1記載の投与剤型。
【請求項7】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項6記載の経口投与剤型。
【請求項8】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項7記載の経口投与剤型。
【請求項9】
前記投与剤型が経口投与剤型である、請求項1記載の投与剤型。
【請求項10】
前記投与剤型が、無傷投与後にインビボで約0.5mg以下の前記逆作用薬を放出する、請求項1記載の投与剤型。
【請求項11】
前記投与剤型が、無傷投与後にインビボで約0.05mg以下の前記逆作用薬を放出する、請求項1記載の投与剤型。
【請求項12】
作用薬を含む複数の第一粒子;及び
吸着剤と逆作用薬を含む複数の第二粒子
を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型。
【請求項13】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項12記載の投与剤型。
【請求項14】
前記吸着剤が活性炭である、請求項13記載の投与剤型。
【請求項15】
前記の複数の第二粒子が、前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料をさらに含む、請求項12記載の投与剤型。
【請求項16】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項15記載の経口投与剤型。
【請求項17】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項16記載の経口投与剤型。
【請求項18】
前記作用薬がオピオイドアゴニストであり、前記逆作用薬がオピオイドアンタゴニストである、請求項12記載の投与剤型。
【請求項19】
前記オピオイドアゴニストが、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、フェンタニル、ヘロイン、ヒドロコドン、ヒドロモルフォン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レバロルファン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルブフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パパベレタム、ペンタゾシン、フェナドキソン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロピラム、プロポキシフェン、スフェンタニル、トラマドール、チリジン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項18記載の投与剤型。
【請求項20】
前記オピオイドアゴニストが、モルフィン、コデイン、ヒドロモルフォン、ヒドロコドン、オキシコドン、オキシモルフォン、ジヒドロコデイン、ジヒドロモルフィン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項19記載の投与剤型。
【請求項21】
前記オピオイドアンタゴニストが、シクラゾシン、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項18記載の投与剤型。
【請求項22】
前記オピオイドアンタゴニストが、ナルメフェン、ナロキソン、ナルトレキソン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項21記載の投与剤型。
【請求項23】
前記投与剤型が経口投与剤型である、請求項12記載の投与剤型。
【請求項24】
前記投与剤型が、前記第一粒子と前記第二粒子とを含有するカプセルを含む、請求項23記載の投与剤型。
【請求項25】
前記投与剤型が、無傷投与後にインビボで約0.5mg以下の前記逆作用薬を放出する、請求項12記載の投与剤型。
【請求項26】
前記投与剤型が、無傷投与後にインビボで約0.05mg以下の前記逆作用薬を放出する、請求項25記載の投与剤型。
【請求項27】
オピオイドアゴニストを含む複数の第一粒子;及び
吸着剤とオピオイドアンタゴニストを含む複数の第二粒子
を含有し、
前記オピオイドアゴニストの少なくとも大部分が前記吸着剤に吸着されており、かつ
前記第一粒子が、患者への経口投与後に前記オピオイドアゴニストの制御放出を提供する、経口投与剤型。
【請求項28】
前記第一粒子及び前記第二粒子が各々、全ての寸法において約0.1mmから約3.0mmの大きさを有する、請求項27記載の経口投与剤型。
【請求項29】
前記第二粒子の各々が、前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料を含む、請求項27記載の経口投与剤型。
【請求項30】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項29記載の経口投与剤型。
【請求項31】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項30記載の経口投与剤型。
【請求項32】
前記オピオイドアゴニストが、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、フェンタニル、ヘロイン、ヒドロコドン、ヒドロモルフォン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レバロルファン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルブフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パパベレタム、ペンタゾシン、フェナドキソン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロピラム、プロポキシフェン、スフェンタニル、トラマドール、チリジン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項27記載の経口投与剤型。
【請求項33】
前記オピオイドアゴニストが、モルフィン、コデイン、ヒドロモルフォン、ヒドロコドン、オキシコドン、オキシモルフォン、ジヒドロコデイン、ジヒドロモルフィン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項32記載の経口投与剤型。
【請求項34】
前記オピオイドアンタゴニストが、シクラゾシン、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項27記載の経口投与剤型。
【請求項35】
前記オピオイドアンタゴニストが、ナロキソン、ナルトレキソン及びナルメフェン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項34記載の経口投与剤型。
【請求項36】
前記投与剤型が、前記第一粒子と前記第二粒子とを含有する錠剤を含む、請求項27記載の経口投与剤型。
【請求項37】
前記投与剤型が、前記第一粒子と前記第二粒子とを含有するカプセルを含む、請求項27記載の経口投与剤型。
【請求項38】
前記第二粒子が、無傷経口投与後にインビボで約0.5mg以下の前記オピオイドアンタゴニストを放出する、請求項27記載の経口投与剤型。
【請求項39】
前記第二粒子が、無傷経口投与後にインビボで約0.05mg以下の前記オピオイドアンタゴニストを放出する、請求項38記載の経口投与剤型。
【請求項40】
作用薬;
吸着剤;及び
逆作用薬
を含有し、前記逆作用薬の少なくとも大部分が前記吸着剤に吸着されている投与剤型。
【請求項41】
前記吸着剤の外側表面の少なくとも一部に配置された少なくとも1つの疎水性材料をさらに含む、請求項40記載の投与剤型。
【請求項42】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項41記載の経口投与剤型。
【請求項43】
前記の少なくとも1つの疎水性材料が、モノステアリン酸グリセリル;蜜ろう;セチルアルコール;ステアリルアルコール;硬化ヒマシ油;硬化綿実油;ステアリルアルコール;ステアリン酸;及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項42記載の投与剤型。
【請求項44】
前記作用薬がオピオイドアゴニストであり、前記逆作用薬がオピオイドアンタゴニストである、請求項40記載の投与剤型。
【請求項45】
前記オピオイドアゴニストが、アルフェンタニル、アリルプロジン、アルファプロジン、アニレリジン、ベンジルモルフィン、ベジトラミド、ブプレノルフィン、ブトルファノール、クロニタゼン、コデイン、デソモルフィン、デキストロモラミド、デゾシン、ジアンプロミド、ジヒドロコデイン、ジヒドロモルフィン、ジメノキサドール、ジメフェプタノール、ジメチルチアンブテン、ジオキサフェチルブチレート、ジピパノン、エプタゾシン、エトヘプタジン、エチルメチルチアンブテン、エチルモルフィン、エトニタゼン、フェンタニル、ヘロイン、ヒドロコドン、ヒドロモルフォン、ヒドロキシペチジン、イソメタドン、ケトベミドン、レバロルファン、レボルファノール、レボフェナシルモルファン、ロフェンタニル、メペリジン、メプタジノール、メタゾシン、メタドン、メトフォン、モルフィン、ミロフィン、ナルブフィン、ナルセイン、ニコモルフィン、ノルレボルファノール、ノルメタドン、ナロルフィン、ノルモルフィン、ノルピパノン、アヘン、オキシコドン、オキシモルフォン、パパベレタム、ペンタゾシン、フェナドキソン、フェノモルファン、フェナゾシン、フェノペリジン、ピミノジン、ピリトラミド、プロヘプタジン、プロメドール、プロペリジン、プロピラム、プロポキシフェン、スフェンタニル、トラマドール、チリジン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項44記載の投与剤型。
【請求項46】
前記オピオイドアゴニストが、モルフィン、コデイン、ヒドロモルフォン、ヒドロコドン、オキシコドン、オキシモルフォン、ジヒドロコデイン、ジヒドロモルフィン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項45記載の投与剤型。
【請求項47】
前記オピオイドアンタゴニストが、シクラゾシン、ナロキソン、ナルトレキソン、ナルメフェン、ナルブフィン、ナロルフィン、シクラザシン、レバロルファン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項44記載の投与剤型。
【請求項48】
前記オピオイドアンタゴニストが、ナルメフェン、ナロキソン、ナルトレキソン、それらの製薬上許容し得る塩、及び前記のいずれか2つ以上の混合物からなる群より選択される、請求項47記載の投与剤型。
【請求項49】
前記投与剤型が経口投与剤型である、請求項44記載の投与剤型。
【請求項50】
前記投与剤型が、複数の粒子を含有するカプセルを含む、請求項44記載の投与剤型。
【請求項51】
前記投与剤型が錠剤を含む、請求項44記載の投与剤型。
【請求項52】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項40記載の投与剤型。
【請求項53】
前記吸着剤が活性炭である、請求項52記載の投与剤型。
【請求項54】
前記投与剤型が、無傷経口投与後にインビボで約0.5mg以下の前記逆作用薬を放出する、請求項40記載の経口投与剤型。
【請求項55】
前記投与剤型が、無傷経口投与後にインビボで約0.05mg以下の前記逆作用薬を放出する、請求項54記載の経口投与剤型。
【請求項56】
前記投与剤型が、
前記吸着剤及び前記逆作用薬を含有するコア、及び
前記作用薬を含有するシェル
をさらに含み、前記シェルが前記コアの大部分を取り囲む、請求項40記載の投与剤型。
【請求項57】
吸着剤を提供すること;
逆作用薬を含有する液体を提供すること;
前記吸着剤を、前記逆作用薬を含有する前記液体と、前記逆作用薬の少なくとも一部が前記吸着剤に吸着するのに十分な時間接触させること
を含む、投与剤型を製造する方法。
【請求項58】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項57記載の方法。
【請求項59】
前記液相から前記吸着剤を除去した後、少なくとも1つの疎水性材料を前記吸着剤の外側表面に適用することをさらに含む、請求項57記載の方法。
【請求項60】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項59記載の方法。
【請求項61】
前記逆作用薬がオピオイドアンタゴニストである、請求項57記載の方法。
【請求項62】
前記吸着剤及びオピオイドアゴニストを投与剤型に添加することをさらに含む、請求項61記載の方法。
【請求項63】
吸着剤を提供すること;
逆作用薬を含有する液体を提供すること;
前記吸着剤を流動床に添加すること;
前記吸着剤を流動化すること;
前記液体を流動化した吸着剤に噴霧すること;及び
場合により、前記吸着剤を乾燥すること
を含む、投与剤型を製造する方法。
【請求項64】
前記吸着剤が、活性炭、アルミナ、ベントナイト、カオリン、及び前記のいずれか2つ以上の混合物からなる群より選択される少なくとも1つの材料を含む、請求項63記載の方法。
【請求項65】
前記液相から前記吸着剤を除去した後、少なくとも1つの疎水性材料を前記吸着剤の外側表面に適用することをさらに含む、請求項63記載の方法。
【請求項66】
前記の少なくとも1つの疎水性材料が、アクリル酸及びメタクリル酸のポリマー及びコポリマー、アルキルセルロース、天然及び合成ろう、水不溶性ろう、脂肪アルコール、脂肪酸、硬化脂肪、脂肪酸エステル、脂肪酸グリセリド、炭化水素、炭化水素骨格を有する疎水性及び親水性ポリマー、並びに前記のいずれか2つ以上の混合物からなる群より選択される、請求項65記載の方法。
【請求項67】
前記逆作用薬がオピオイドアンタゴニストである、請求項63記載の方法。
【請求項68】
前記吸着剤及びオピオイドアゴニストを投与剤型に添加することをさらに含む、請求項63記載の方法。
【請求項69】
請求項40記載の投与剤型を患者に投与することを含む、患者の病気又はその症状を治療する方法。
【請求項70】
請求項27記載の投与剤型を患者に投与することを含む、疼痛を有する患者を治療する方法。
【請求項71】
請求項27記載の投与剤型、及び疼痛の治療のために前記投与剤型の投与を患者に指示する説明書を含む、疼痛を有する患者を治療するためのキット。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公表番号】特表2007−530684(P2007−530684A)
【公表日】平成19年11月1日(2007.11.1)
【国際特許分類】
【出願番号】特願2007−506256(P2007−506256)
【出願日】平成17年3月23日(2005.3.23)
【国際出願番号】PCT/US2005/009734
【国際公開番号】WO2005/097075
【国際公開日】平成17年10月20日(2005.10.20)
【出願人】(599108792)ユーロ−セルティーク エス.エイ. (134)
【Fターム(参考)】
【公表日】平成19年11月1日(2007.11.1)
【国際特許分類】
【出願日】平成17年3月23日(2005.3.23)
【国際出願番号】PCT/US2005/009734
【国際公開番号】WO2005/097075
【国際公開日】平成17年10月20日(2005.10.20)
【出願人】(599108792)ユーロ−セルティーク エス.エイ. (134)
【Fターム(参考)】
[ Back to top ]

