固体酸化物型電池の発電方法及び該発電方法を使用して発電する固体酸化物型電池
【課題】連続的に燃料電池反応を継続させることのできる新規な固体酸化物型電池の発電方法を提供すること。
【解決手段】複合金属酸化物を含むアノード材料を有するアノード11、カソード材料を有するカソード31、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質21、発電の際に燃料として使用される固体炭素2、及び該固体炭素が格納された燃料室1を少なくとも有する固体酸化物型電池における発電方法であって、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電することを特徴とする固体酸化物型電池の発電方法。
【解決手段】複合金属酸化物を含むアノード材料を有するアノード11、カソード材料を有するカソード31、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質21、発電の際に燃料として使用される固体炭素2、及び該固体炭素が格納された燃料室1を少なくとも有する固体酸化物型電池における発電方法であって、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電することを特徴とする固体酸化物型電池の発電方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、アノード材料に供給される固体炭素を燃料として用いて発電する固体酸化物型電池の発電方法、及び、該発電方法を使用して発電する固体酸化物型電池に関する。
【背景技術】
【0002】
イオン伝導性の固体酸化物(酸化物イオン伝導体)からなる電解質層(固体電解質層)をカソード(空気極)とアノード(燃料極)との間に配置した積層構造を有する固体酸化物型電池(SOFC)は、第三世代の燃料電池として期待され、その開発が進んでいる。
【0003】
固体酸化物型電池は、アノードに還元剤、例えば、水素(H2)、一酸化炭素(CO)、メタン(CH4)等のガス(燃料ガス)を供給し、カソードに酸化剤、例えば、酸素(O2)等を含むガス(例えば空気)を供給することにより発電するデバイスである(例えば、下記特許文献1参照)。
【0004】
従来の固体酸化物型電池(SOFC)では電極活物質はガス状であったが、電極活物質としてエネルギー密度の非常に高い固体炭素を用いることが提案された(特許文献2)。特許文献2は、アノード材料に担持させた固体炭素を二酸化炭素(CO2)と反応させて気体の一酸化炭素(CO)に変換し、当該気体の一酸化炭素(CO)を酸化することにより発電することを特徴としている。また、電気化学リアクター(電気化学的な反応場を提供する装置)としての利用も可能であると提案している。
【0005】
しかしながら、上記の固体酸化物型電池は、炭化水素等の有機化合物を導入し、熱分解反応を進行させて、一旦固体炭素をアノードに担持させる賦活工程等を必須工程として含み、あらかじめ燃料となる固体炭素をアノードに担持させておくことが必要であり、発電途中で固体炭素を補充することができないため、連続的に燃料電池反応を継続することができず、連続的な作動が求められる発電システムや電気化学リアクターにはそのまま適用することは難しく、実用化の観点からするとその技術価値を十分に発揮させることができなかった。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開平9−129256号公報
【特許文献2】特開2008−198585号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明は上記背景技術に鑑みてなされたものであり、その課題は、アノードに炭化水素等の有機化合物を導入して熱分解反応を進行させて、固体炭素をアノードに一旦担持させる工程を必要とせず、連続的に燃料電池反応を継続させることのできる新規の固体酸化物型電池の発電方法を提供することにある。
【課題を解決するための手段】
【0008】
本発明者らは上記課題を解決すべく鋭意検討を行った結果、固体酸化物型電池の装置構成として少なくとも固体炭素を格納するための燃料室を設け、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電させる発電方法を採れば、固体炭素がアノードに担持されていないで燃料室に格納されていても、すなわち固体炭素がアノードから離れていても、該固体炭素が燃料として消費され、結果として連続的な発電が可能であることを見出し、本発明に到った。
【0009】
すなわち、本発明の第1の要旨は、複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池における発電方法であって、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電することを特徴とする固体酸化物型電池の発電方法に存する。
【0010】
第2の要旨は、上記アノードに固体炭素を担持させて用いる上記の固体酸化物型電池の発電方法に存する。
【0011】
第3の要旨は、上記燃料室の固体炭素に一酸化炭素又は二酸化炭素を供給することで発電を開始させる上記の固体酸化物型電池の発電方法に存する。
【0012】
第4の要旨は、発電開始時に発電開始剤を供給するための発電開始剤導入管の先端が、燃料室とアノードの間に配置されている上記の固体酸化物型電池の発電方法に存する。
【0013】
第5の要旨は、発電開始直後、電流密度をその初期値から増加させながら運転させることを特徴とする上記の固体酸化物型電池の発電方法に存する。
【0014】
第6の要旨は、発電開始時に、アノードへ電気化学的に酸素源を注入することを特徴とする上記の固体酸化物型電池の発電方法に存する。
【0015】
第7の要旨は、発電時に下記反応式(1)及び(2)を利用して発電することを特徴とする上記の固体酸化物型電池の発電方法に存する。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【0016】
第8の要旨は、上記固体炭素の炭素含有率が50質量%以上である上記の固体酸化物型電池の発電方法に存する。
【0017】
第9の要旨は、上記固体炭素が排気ガス中の炭素微粒子である上記の固体酸化物型電池の発電方法に存する。
【0018】
第10の要旨は、複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池に存する。
【0019】
第11の要旨は、発電開始時に発電開始剤を供給するための発電開始剤導入管を有し、該発電開始剤導入管の先端が燃料室とアノードの間に配置されている上記の固体酸化物型電池に存する。
【0020】
第12の要旨は、発電時に下記反応式(1)及び(2)を利用して発電する上記の固体酸化物型電池に存する。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【0021】
第13の要旨は、上記の固体酸化物型電池の発電方法を使用して発電することを特徴とする固体酸化物型電池に存する。
【発明の効果】
【0022】
本発明によれば、あらかじめアノードに、炭化水素等の有機化合物を導入し、熱分解反応で一旦固体炭素を担持させておく必要がないため、連続的に燃料電池反応を継続することができることから、連続的な作動を要する発電システムや電気化学リアクターへの適用を容易ならしめ、実用化を促進し得る。
【0023】
特に、後述する実施例2のように、アノードに固体炭素を直接担持しなくても発電しており、このことは燃料室に格納した固体炭素が消費されていることを意味している。すなわち、従来のように、炭化水素等の有機化合物を導入し熱分解反応を進行させて、固体炭素をアノードに直接担持させる賦活工程を必要とすることなく、燃料室に固体炭素を供給しさえすれば連続的に燃料電池を運転することが可能となるため、実用性の高い運転方法が可能となる。
【0024】
また、燃料である固体炭素がアノードに接していなくても、近傍に存在する燃料室に格納又は充填されていれば作動することから、燃料の供給方法に幅が広がり、システムの設計面でも幅が広がる。特に、内燃機関から排出される排ガス中に含まれる粒子状物質(Particulate Matter、以下、「PM」と略記する。)を除去する浄化装置に適用した場合、PM捕集部と固体酸化物型電池部とを独立させて配置することが可能なため、連続的なPM除去と同時に発電が可能な、いわゆる外部電源等を必要としない自己完結型の電気化学的PM浄化システムの構築が容易となり、実用的な浄化装置を提供することができる。
【図面の簡単な説明】
【0025】
【図1】本発明の固体酸化物型電池の実施形態の基本構成の一例を示す模式断面図である。
【図2】本発明の固体酸化物型電池であって、アノード材料にも固体炭素が担持されている実施形態の基本構成の一例を示す模式断面図である。
【図3】本発明の固体酸化物型電池であって、発電開始剤導入管を備えた実施形態の基本構成を示す模式断面図である。
【図4】本発明の固体酸化物型電池であって、発電開始剤導入管が燃料室内を貫通している実施形態の基本構成の一例を示す模式断面図である。
【図5】本発明の固体酸化物型電池であって、発電開始剤導入管の先端が燃料室内に位置するように配置されている実施形態の基本構成の一例を示す模式断面図である。
【図6】本発明の固体酸化物型電池であって、電流密度を制御するための外部制御回路を有している実施形態の基本構成の一例を示す模式断面図である。
【図7】本発明の固体酸化物型電池であって、アノードへ電気化学的に酸素源を注入するための電気回路を有している実施形態の基本構成の一例を示す模式断面図である。
【図8】本発明の固体酸化物型電池であって、円筒形状をしたものの基本構成の一例を示す模式断面図である。
【図9】本発明の固体酸化物型電池であって、円筒形状をしたものの基本構成の一例を示す模式断面図である。
【図10】本発明の固体酸化物型電池であって、円筒形をした燃料電池セルの片末端が封じられているものの基本構成の一例を示す模式縦断面図と、模式横(C−d)断面図である。
【図11】本発明の固体酸化物型電池であって、円筒形状をしたものの基本構成の一例を示す模式断面図である。
【図12】図11に示した本発明の固体酸化物型電池の模式斜視図である。
【図13】本発明の固体酸化物型電池であって、燃料電池セル1が積層されているものの基本構成の一例を示す模式断面図である。
【発明を実施するための形態】
【0026】
以下、図面を参照しながら本発明の好適な実施形態について詳細に説明するが、本発明は以下の実施の形態に限定されるものではなく、その技術的思想の範囲内で種々変形することができる。
【0027】
<固体酸化物型電池の形態>
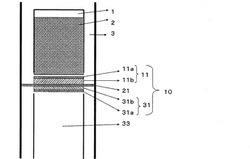
図1は、本発明の固体酸化物型電池の好適な一実施形態の基本構成を示す模式断面図である。図1に示す固体酸化物型電池は、少なくとも、燃料電池セル10、燃料室1及び「酸化剤を含むガス導入口」33を有している。そして、燃料電池セル10は、主として、アノード11、カソード31、及び、アノード11とカソード31との間に配置された電解質21とから構成されている。図1に示すアノード11は、アノード材料11b及びアノード集電体11aを有している。また、図1に示すカソード31は、カソード材料31b及びカソード集電体31aを有している。
【0028】
また、本発明の固体酸化物型電池は、燃料である固体炭素2を格納でき、該固体炭素2を燃料電池セル10に供給するための燃料室1を具備している。ここで燃料室1とは、アノード11側に設けられた発電のための固体炭素2を格納する空間であり、そこに格納される固体炭素2はアノード11に接している必要はないが、該固体炭素2の少なくとも一部はアノード11に接していることも好ましい。より具体的には、燃料室1は、そこに格納される固体炭素2が、アノード集電体11aやアノード材料11bと接触するようになっている必要はないが、接触するようになっていることも好ましい。本発明では、アノード11に、後述するように発電開始時に、また、上記したように発電中にも、固体炭素2を担持させて用いることが好ましい。発電中に担持させる固体炭素2は、前述の有機化合物の熱分解反応で生じるものではなく、外部から燃料室1に供給したものである。
【0029】
限定はされないが、例えば図1においては、燃料室1のうち下約90%に固体炭素2が格納されている。発電中でも、燃料室1に燃料である固体炭素2を追加することによって、発電を継続することができる。
【0030】
アノード11側への酸素の混入は、発電効率の観点からできるだけ軽減した方が好ましい。酸素除去のために、窒素(N2)や二酸化炭素(CO2)等の不活性ガスで置換した固体炭素2を格納することも好ましい。
【0031】
燃料室1に固体炭素2があり、発電により生じたCO2が、例えば500〜1000℃で存在すれば、CO生成反応が進行し、燃料電池セル10により発電が継続される。本発明は、この意外な事実の新しい発見に基づいてなされたものである。
【0032】
更に、図1に示す固体酸化物型電池は、アノード11側にCO2を排出するための二酸化炭素(CO2)排出口3、カソード31側に酸素(O2)等の酸化剤を供給するための「酸化剤を含むガス導入口」33を有している。
【0033】
図2も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した形態と異なる点は、燃料室1内の固体炭素2以外に、アノード材料11bにも、固体炭素15が担持されていることであり、それ以外は図1に示す固体酸化物型電池と同じ構成である。特に、発電開始時に、アノード材料11bに固体炭素15を担持させておくことが、初期発電特性の安定化の観点から好ましい。アノード11に担持される固体炭素15は、燃料室1内に格納される後述する固体炭素2と同じものでもよいし、異なるものでもよい。
【0034】
図3も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した基本構成に加えて、二酸化炭素(CO2)排出口3の燃料室1を除くスペースに、発電開始剤導入管13を備え、発電開始剤導入管13の先端が、燃料室1とアノード11(具体的には、アノード集電体11a)との間に配置されている。発電開始剤導入管の先端が、燃料室1とアノード11の間に配置されていることによって、発電開始剤がアノード材料11bの近傍に供給され、その結果、初期の発電特性が安定し易い。
【0035】
図4に示す固体酸化物型電池は、図3に示した固体酸化物型電池と基本構成は同じであるが、発電開始剤導入管13の配置が異なる。すなわち、発電開始剤導入管13は燃料室1内を貫通し、発電開始剤導入管13の先端が、燃料室1とアノード11との間に配置されている。より詳しくは、燃料室1とアノード集電体11aの間に位置するように配置されている。効果は上記と同様である。
【0036】
図5に示す固体酸化物型電池は、図3と図4に示した固体酸化物型電池と基本構成は同じであるが、発電開始剤導入管13の先端の位置が異なる。すなわち、発電開始剤導入管13の先端が燃料室1内に位置するように配置されている。これでも、発電開始剤は徐々にアノード11に供給されるため、上記と同様の効果が得られる。
【0037】
図6も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した固体酸化物型電池の基本構成に加えて、固体酸化物型電池の電流密度を制御するための外部制御回路22を有している。
【0038】
図7も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した固体酸化物型電池の基本構成に加えて、アノード11へ電気化学的に酸素源を注入するための電気回路23を有している。本発明の固体酸化物型電池の発電方法においては、発電開始時に、アノード11へ電気化学的に酸素源を注入することが、初期の発電特性を安定化させる点で好ましい。酸素源は特に限定はないが、具体的には、例えば、空気や酸素等が挙げられる。酸素源の電気化学的な注入方法については特に限定はされないが、具体的には、例えば、アノード11とカソード31との間に、電池セルの持つネルンスト電位を利用し、電流密度0.01mA/cm2〜5mA/cm2で流し、カソード31で酸素が電子を取り込んで酸化物イオン(O2−)となり、このO2−が電解質を移動してアノード11で燃料と反応して電子を放出させ、電極反応を開始させることが好ましい。発電開始時に、アノード11へ電気化学的に酸素源を注入しないと、発電の初期段階で安定した発電が得られない場合がある。
【0039】
図8も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、アノード11の外周側に燃料室1、カソード31の内周側に「酸化剤を含むガス導入口」33を配した構成となっている。
【0040】
図9も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、アノード11の内周側に燃料室1、カソード31の外周側に「酸化剤を含むガス導入口」33を配した構成となっている。
【0041】
図10も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、燃料電池セル10が円筒形をしており、円筒形をした燃料電池セル10の片末端は封じられている。燃料電池セル10の円筒の外部に燃料室1、内部に「酸化剤を含むガス導入口」33を配した構成となっている。
【0042】
図11も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、燃料室1を貫通するように円筒形をした燃料電池セル10が配されている。また、燃料室1に二酸化炭素(CO2)排出口3が設けられており、貫通型の円筒形の燃料電池セル10の円筒内部に、空気等の酸素含有ガスを供給するための「酸化剤を含むガス導入口」33を設けた構成となっている。
【0043】
図12は、図11に示した本発明の固体酸化物型電池を立体的に示した模式斜視図である。
【0044】
図13は、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21を有する燃料電池セル10が積層しており、2つのアノード11で挟まれたスペースに燃料室1が設けられ、カソード31で挟まれたスペースに空気等の酸素含有ガス等を供給するための「酸化剤を含むガス導入口」33が設けられた構成となっている。
【0045】
<アノード>
アノード11のアノード材料11bは複合金属酸化物を含む。すなわち、アノード材料11bは、複合金属酸化物を含むものであってもよいし、サーメットを含むものであってもよい。ここで「サーメット」とは、金属と金属酸化物粉末が混合され焼結されたものをいう。複合金属酸化物又はサーメットは多孔質であることが好ましい。複合金属酸化物又はサーメットとしては、公知の固体酸化物型燃料電池にアノード活物質として一般に用いられているものが好適に使用できる。
【0046】
[複合金属酸化物]
自身がアノード材料11bの成分として、また、アノード材料11bの成分であるサーメットの原料としても用いられる複合金属酸化物としては、固体酸化物型燃料電池にアノード活物質として一般に用いられているものであれば特に限定はない。発電の際に、十分な出力特性、耐久性等を確実に得る点からは、イットリアが配合された安定化ジルコニア(Y2O3−ZrO2)(以下、「YSZ」と略記する);Gd、La、Y、Sm、Nd、Ca、Mg、Sr、Ba、Dy及びYbからなる群より選ばれる少なくとも1種がドープされたCeO2[このうち特に、GdがドープされたCeO2(以下、「GDC」と略記する)、SmがドープされたCeO2が好ましい];Sc2O3−ZrO2(以下、「ScSZ」と略記する);Sm2O3−CeO2(以下、「SDC」と略記する)等が特に好ましい。
【0047】
ここで、上記YSZの場合、Y2O3の割合(Y2O3の含有量)は、Y2O3−ZrO2に対して8〜10モル%であることが好ましい。また、上記GDCの場合、Gdの割合(Gdの含有量)は、ドープされたCeO2に対して3〜40モル%が好ましく、8〜40モル%がより好ましく、10〜40モル%が更に好ましく、15〜40モル%であることが特に好ましい。更に、上記SmがドープされたCeO2の場合、Smの割合(Smの含有量)は、ドープされたCeO2に対して15〜40モル%であることが好ましい。また、特に好ましいセリア系固溶体としては、Ce0.8Gd0.2O2−δ(式中、δは酸素欠損量を示す)、Ce0.67Gd0.33O2−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0048】
また、発電の際に、十分な出力特性を得る観点からは、電気伝導性を有する複合金属酸化物を用いることが好ましい。複合金属酸化物の導電率は、1000℃において、0.01〜10Scm−1であることが特に好ましい。
【0049】
[[サーメット]]
本発明の効果をより確実に得るとともに、優れた出力特性をより確実に得る観点から、アノード材料11bはサーメットであることが好ましい。サーメットとしては、固体酸化物型燃料電池にアノード活物質として一般に用いられているものであれば特に限定はないが、Ni、Pt、Au、Cu、Fe、W及びTaからなる群より選ばれる少なくとも1種の金属と複合金属酸化物(特に上記複合金属酸化物)とのサーメットが好ましい。発電の際に、十分な出力特性を確実に得る点等からは、ニッケルと複合金属酸化物のサーメット等が好ましいものとして挙げられ、特に、ニッケルと上記した複合金属酸化物とのサーメット等が好ましいものとして挙げられる。
【0050】
特に好ましくは、出力特性の点で、ニッケルとYSZとのサーメット(以下、「Ni/YSZ」と略記する)、ニッケルとGDCとのサーメット(以下、「Ni/GDC」と略記する)、ニッケルとScSZとのサーメット(以下、「Ni/ScSZ」と略記する)又はニッケルとSDCとのサーメット(以下、「Ni/SDC」と略記する)である。
【0051】
また、サーメットにおける金属の体積分率V1と、複合金属酸化物の体積分率V2とが下記式で表される条件を満たしていることが、電子伝導性確保の点で好ましい。
0.2≦[V1/(V1+V2)]≦0.8
【0052】
ここで、[V1/(V1+V2)]が0.2未満となると、アノード材料11b中の電子伝導性が十分に確保できなくなり、固体酸化物型電池の出力特性が不十分となる場合がある。また、[V1/(V1+V2)]が0.8を超えると、アノード材料11b中のイオン伝導性が十分に確保できなくなり、固体酸化物型電池1の出力特性が不十分となる場合がある。アノード材料11b中の電子伝導性とイオン伝導性を共に十分に確保する観点から、[V1/(V1+V2)]は0.2〜0.8であることが好ましく、0.3〜0.7であることが特に好ましく、0.4〜0.6が更に好ましい。
【0053】
具体的には、Ni/YSZ、Ni/GDC、Ni/ScSZ、又はNi/SDCにおいて、体積分率の比としてNi/(かかる複合金属酸化物+Ni)の値が、上記値の範囲に入っているものが好ましい。
【0054】
[[電気伝導性を有する複合金属酸化物]]
ここで、アノード材料11bがサーメットのような金属粒子若しくは合金粒子を含む材料であると、アノード中の金属が、カーバイドやカーボンウィスカーを生成させる原因になり、長期的な電極劣化の要因となる場合がある。すなわち、金属に溶解した炭素が析出して成長する際に金属粒子を電極のフレーム構造から脱落させてしまい、それが電極劣化の要因となる場合がある。また、酸化還元サイクル時の金属粒子の体積膨張・収縮により、それが電極劣化の要因となる場合がある。したがって、アノード材料11bとして、上記サーメットに代えて、電気伝導性を有する複合金属酸化物を用いることも好ましい。
【0055】
電極劣化の原因となる金属粒子若しくは合金粒子を含むサーメットに代えて、アノード材料11bのうちの少なくとも1種のアノード材料に電気伝導性を有する複合金属酸化物を用いることによって、上記電極劣化の要因が解消され、RDCFCの運転時にアノードの劣化を抑制し、酸化還元サイクル特性を向上させ、高出力を安定的に維持させることができる。アノード材料11bに電気伝導性を有する複合金属酸化物を含むことが好ましい。ここで、「電気伝導性を有する」とは、運転温度において電気伝導度が10−4Scm−1以上であることを意味する。
【0056】
ここで、前記した電極劣化を生じない範囲においては金属を含有していてもよく、本発明は、アノード材料11bの組成から、少量の「金属粒子若しくは合金粒子」の含有を排除するものではない。アノード材料11b全体中に含有される「金属粒子若しくは合金粒子」は合計で10質量%以下が好ましく、5質量%以下がより好ましく、2質量%以下が特に好ましく、金属粒子も合金粒子も含まれていないことが更に好ましい。
【0057】
上記の「電気伝導性を有する複合金属酸化物」の電気伝導度は、運転温度において10−2Scm−1以上であることが好ましく、10−1Scm−1以上であることが特に好ましい。ここで、「電気伝導」とは、電子伝導、ホール伝導、酸化物イオン伝導及びプロトン伝導のうちの少なくとも1つからなる電気伝導、すなわち、それらのうちの1つ又は2つ以上が組み合わされた電気伝導を意味する。電気伝導度が低過ぎると、十分な出力特性が得られない場合がある。
【0058】
本発明の固体酸化物型電池のアノードは、金属粒子も合金粒子も含有していないか、又は、それらによる3次元的ネットワークが形成されない範囲を上限として金属粒子若しくは合金粒子を含有していることが好ましい。「3次元的ネットワーク」とは、アノードの厚さ方向にそれのみを通して電気伝導が可能の状態(通じる状態)をいう。金属粒子若しくは合金粒子による3次元的ネットワークが形成されていると、酸化と還元の繰り返しで、アノード材料が体積膨張と体積収縮を繰り返す結果、アノードが劣化する場合がある。
【0059】
また、本発明の固体酸化物型電池のアノード材料11bに用いられる電気伝導性を有する複合金属酸化物は、それ自体で、3次元的ネットワークを形成していること、すなわち複合金属酸化物自体で、電子伝導可能な3次元的ネットワークを形成していることが、良好な電気伝導性を実現し、結果として十分な出力特性が得られる点で好ましい。
【0060】
本発明の固体酸化物型電池のアノード材料11bに用いられる電気伝導性を有する複合金属酸化物は、少なくともそのうちの1種は、ペロブスカイト型結晶構造、パイロクロア型結晶構造又はフルオライト型結晶構造を有する複合金属酸化物よりなることが好ましい。
【0061】
ペロブスカイト型結晶構造を有する複合金属酸化物とは、いわゆるペロブスカイト型の結晶構造をとる複合金属酸化物をいい、下記一般式(G)で表わされる複合金属酸化物が好ましい。
A1±aB1±bO3−δ (G)
[組成式(G)中、Aは、La、Sr、Ca、Y、Ba、Pr、Ce、K、Na、Sm、Pb、Nd、Gd、Bi、Ag、Cs、Rb、Tl、Cd、Eu、Mg、Dy、Li及びHoからなる群より選ばれる少なくとも1種を示し、Bは、Co、Cr、Mn、Ni、Ce、Gd、Al、Ti、Zr、Sc、Mg、Ga、Cu、Fe、Yb、Y、Nb、I、Ni、Sr、Bi、In、Ca、Sn、Ta、W、Th、U、Hf、Mo、Lu、Tm、Tb、Dy、Ho、Os、Rh、Ag、Tr、Sb、Zn、Pa、In、Re及びErからなる群より選ばれる少なくとも1種を示し、0≦a≦0.2、0≦b≦0.2であり、δは酸素欠損量である。]
【0062】
このうち、LaMnO3、LaCoO3、LaCrO3等を母体とする物質がより好ましく、例えば、(LaSr)MnO3系の複合金属酸化物(本発明では、これを「LSM」と略記する)、(LaSr)CoO3系の複合金属酸化物(本発明では、これを「LSC」と略記する)が特に好ましいものとして挙げられる。
【0063】
また、組成式(G)において、Bが、MnをB全体に対して50モル%以上含有するものであることが、前記効果をより奏するために好ましい。また、組成式(G)において、Bが、CoをB全体に対して50モル%以上含有するものであること、又は、Bが、CoとFeを、それらの合計でB全体に対して50モル%以上含有するものであることが、前記効果を奏するために好ましい。
【0064】
そのほかのペロブスカイト型結晶構造を有する複合金属酸化物は、一般式、A(B1−xMx)1±aO3−δ[式中、0≦x≦0.8、0≦a≦0.2である]において、AはBa、Sr、Ca等の2価のカチオンから少なくとも1種が選ばれ、BはCe、Zr、Ti等の4価のカチオンから少なくとも1種が選ばれ、Mは3価の希土類、Y、Sc、In、Yb、Nd、Gd、Al、Ga等から少なくとも1種が選ばれる。
【0065】
例えば、Ba(Ce1−xGdx)1±aO3[式中、0≦x≦0.8、0≦a≦0.2である]、Ca(Al1−xTix)1±aO3[式中、0≦x≦0.8、0≦a≦0.2である]、Sr(Ce1−xYbx)1±aO3(式中、0≦x≦0.8、0≦a≦0.2である)、Sr(Zr1−xYx)1±aO3(式中、0≦x≦0.8、0≦a≦0.2である)、Sr(Zr1−xScx)1±aO3(式中、0≦x≦0.8、0≦a≦0.2である)等で表されるものも好ましい。具体的には、BaCe0.9Gd0.1O3、CaAl0.7Ti0.3O3、SrCe0.95Yb0.05O3、SrZr0.95Y0.05O3、SrZr0.9Sc0.1O3等が挙げられる。
【0066】
一般式、La1−xSrxGa1−y−zMgyMzO3[式中、Mは、Co、Fe、Ni又はCuの何れか1種以上の元素を示し、x=0.05〜0.3、y=0〜0.29、z=0.01〜0.3、y+z=0.025〜0.3の範囲である。]で表されるランタンガレートも好ましい。具体的には、La0.8Sr0.2Ga0.8Mg0.15Co0.05O3−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0067】
好ましい電気伝導性を有する複合金属酸化物としては、具体的には、例えば、La0.8Sr0.2MnO3、La0.85Sr0.15MnO3、La0.95Sr0.05MnO3等の、La1−bSrbMnO[bは、0≦b≦0.5]で表わされる化合物;La0.8Sr0.2CoO3、La0.85Sr0.15CoO3、La0.95Sr0.05CoO3等の、La1−dSrdMnO3[dは、0≦d≦0.5]で表わされる化合物;La0.6Sr0.4Fe0.8Co0.2O3、La0.6Sr0.4Fe0.2Co0.8O3等のLa1−eSreFefCo1−fO3[eは0≦e≦0.5、fは0≦f≦1]で表わされる化合物;La0.75Sr0.2Cr0.5Mn0.5O3等のLa1−gSrgCr1−hMnhO3[gは0≦g≦0.5、hは0≦h≦1]で表わされる化合物;等が挙げられる。
【0068】
パイロクロア型結晶構造を有する複合金属酸化物とは、いわゆるパイロクロア型の結晶構造をとる複合金属酸化物をいい、Ln2((Zr1−xTix)2)1±aO7(式中、LnはSc、Y、La及び他のランタノイドからなる群より選ばれた1種以上の元素を示し、0≦x≦0.5、0≦a≦0.2である)が好ましいものとして挙げられる。具体的には例えば、Gd2((Zr1−xTix)2)1±aO7(式中、0≦x≦0.5、0≦a≦0.2である)、Y2((Zr1−xTix)2)1±aO7(式中、0≦x≦0.5、0≦a≦0.2である)等が挙げられる。
【0069】
フルオライト型結晶構造を有する複合金属酸化物とは、いわゆるフルオライト型の結晶構造をとる複合金属酸化物をいい、その中で好ましいものはセリア系複合金属酸化物で、Ce1−xMxO2(式中、MはGd、La、Y、Sc、Sm、Pr、Nd、Ca、Mg、Sr、Ba、Dy、Yb、Tb及び他の2価または3価のランタノイドからなる群から選ばれた1種以上の元素を示し、0≦x≦0.5である)で表されるものである。特に好ましいセリア系複合金属酸化物として、Ce0.8Gd0.2O2−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0070】
本発明の固体酸化物型電池のアノード材料11bに用いられる電気伝導性を有する複合金属酸化物としては、ペロブスカイト型結晶構造を有する複合金属酸化物が、金属粒子若しくは合金粒子を含有しなくても高い電気伝導性を有し、前記した本発明の効果をより奏する点で特に好ましい。
【0071】
上記アノード材料11bが2種以上のアノード材料よりなる複合材料である場合には、上記以外のアノード材料も複合金属酸化物であることが好ましい。更に、アノードにおいては、少なくとも電子伝導性とホール伝導性のどちらかを有する複合金属酸化物、及び、少なくとも酸化物イオン伝導性とプロトン伝導性のどちらかを有する複合金属酸化物の2種類以上のアノード材料を含有することが好ましい。ここで、「少なくとも電子伝導性とホール伝導性のどちらかを有する」とは、その両方を合わせた電気伝導度が10−4Scm−1以上であることをいい、「少なくとも酸化物イオン伝導性とプロトン伝導性のどちらかを有する」とは、その両方を合わせた電気伝導度が10−4Scm−1以上であることをいう。
【0072】
本発明における好ましいアノード材料11bとしては、比較的高い電子伝導性と酸化物イオン伝導性の両方を有するという点で、LSMとGDCの複合材料であるLSM/GDC、LSC単独、LSCとGDCの複合材料であるLSC/GDC等が挙げられる。また、電子伝導性とプロトン伝導性の両方を有するという点で、LSMとSrCe1−iYbiO3(iは、0≦i≦1)(以下、「SCYb」と略記する)の複合材料であるLSM/SCYb、LSCとSCYbの複合材料であるLSC/SCYb等が挙げられる。また、電子伝導性と酸化物イオン伝導性に加えてプロトン伝導性を有するという点で、LSCとGDCとSCYbの複合材料であるLSM/GDC/SCYb等が挙げられる。
【0073】
[膜厚]
アノード材料11bの膜厚は特に限定はないが、通常10μm〜5mmであり、好ましくは20μm〜1mm、より好ましくは30μm〜700μm、更に好ましくは40μm〜400μm、最も好ましくは50μm〜150μmである。膜厚は、触針タイプの表面粗さ計、又はSEMによる断面観察で測定してもよい。
【0074】
なお、ここで言及したアノード11(燃料極)の最適な厚さは、空孔度によって変わる。すなわち、空孔度はアノード11への気体の拡散のしやすさや、発生した一酸化炭素(CO)ガスの実効反応サイトへの移動しやすさに影響するため、空孔度が変わると厚さの最適条件は変わることがある。したがって、得られたアノード11の空孔度に合わせて適宜アノード11の膜厚は決定することが好ましい。
【0075】
[発電開始剤]
本発明の固体酸化物型電池の使用に際しては、発電開始剤導入時(以下、「発電開始剤導入工程」ということもある)と発電時(以下、「発電工程」ということもある)が少なくとも存在する。発電開始剤導入時には、アノード11に発電開始剤を供給することで発電を開始させることが、初期の発電特性が安定し易い点で好ましい。ここで、「発電開始剤」とは、一酸化炭素又は二酸化炭素をいう。発電開始剤導入工程においては、発電開始剤を供給し、一酸化炭素又は二酸化炭素を燃料室1の固体炭素2に接触させる。
【0076】
発電開始剤の導入手段として、例えば、図3、4、5に示したように、発電開始時に発電開始剤を供給する発電開始剤導入管13を設置することが好ましい。発電開始剤導入管13の先端は、発電開始剤がアノード11に到達すれば、どの位置に配置されていてもよいが、図3又は図4に示したように、燃料室1とアノード11の間に配置されていることが、発電開始剤をアノード11に迅速かつ確実に供給できる点で好ましい。
【0077】
[アノードの機構、構造、物性等]
発電時には(発電工程では)、燃料室1に供給した固体炭素2を使用し、少なくとも後記する反応式(1)及び反応式(2)により電子を発生させる。また同時に、カソード31では、酸化性ガスに電子を供与し、イオン化した酸化物イオン(O2−)を電解質21に注入する。
【0078】
本発明の固体酸化物型電池の大きさは特に限定はないが、1cm3〜500m3であることが好ましく、1000cm3〜50000cm3であることが特に好ましい。
【0079】
本発明の固体酸化物型電池の発電時の出力は特に限定はないが、0.001kW〜500kWが好ましく、0.01kW〜100kWであることが特に好ましく、0.01kW〜10kWであることが更に好ましい。本発明の固体酸化物型電池は、上記大きさの場合に上記出力を発生できる。
【0080】
アノード11のアノード集電体11aの構成材料は電子伝導性を有し、かつ固体酸化物型電池の作動温度領域において化学的及び物理的に安定であるものであればその形状及び構成材料は特に限定されず、公知の固体酸化物型燃料電池に備えられているものと同様のものを使用することができる。600℃〜1200℃で化学的及び物理的に安定であるものが好ましい。
【0081】
このアノード集電体11aは、燃料電池セル10を複数積層して使用する場合には、各単位セル間に配置されるセパレータとしての機能をも果たすものである。
【0082】
また、アノード11には、ガスの供給口(図示せず)及び放出口(図示せず)、並びに、これらの供給口と放出口とに接続されたガスの内部流路(図示せず)が設けられていてもよい。本発明の固体酸化物型電池は、一般の公知の燃料電池とは燃料の種類、使用方法、発電原理等は全く異なるが、ガスの供給口及び放出口並びにこれらの供給口と放出口とに接続されたガスの内部流路等の機械的外部構造については、一般の公知の燃料電池の構造と同様のものが使用できる。
【0083】
本発明の固体酸化物型電池では、発電時に、アノード11に対し反応生成ガスを外部に放出させるためのキャリアガスを実質的に導入しないことが好ましい。後述するように、キャリアガスを実質的に導入しないと、アノード11において反応式(1)で示される反応がより効率的に起こるので好ましい。またこれにより、発電時には装置構成をより極めてコンパクトにできる。
【0084】
<カソード>
発電時には、カソード31には、「酸化剤(例えば酸素)を含むガス」(例えば空気)が供給され、カソード材料31bは、酸化剤の還元反応が進行する反応場となるものである。カソード材料31bの組成や形状については特に限定されず、公知の固体酸化物型燃料電池に備えられているカソード31に一般に使用されているものと同様のものを使用することができる。例えば、(LaSr)MnO3系、(LaSr)CoO3系の複合金属酸化物からなる材料等を好ましく使用することができる。特に好ましくは、例えば、La0.85Sr0.15MnO3 等が挙げられる。
【0085】
カソード31のカソード集電体31aの構成は、先に述べたアノード11のアノード集電体11aと同様であり、構成材料及び形状については特に限定されず、公知の固体酸化物型燃料電池に備えられているものと同様のものを使用することができる。なお、カソード集電体31aには、空気等の酸化剤を含むガスをカソード材料31bに供給するためのガス流路(図示せず)が形成されている。また、このカソード集電体31aは、燃料電池セル10を複数積層して使用する場合には、各単位セル間に配置されるセパレータとしての機能をも果たすものである。
【0086】
<電解質>
電解質21は、イオン伝導性の固体酸化物を含む。電解質21は、酸化物イオン(O2−)の移動媒体であると同時に、還元剤(先に述べた固体炭素2)と酸化剤を含むガス(例えば空気)を直接接触させないための隔壁としても機能し、ガス不透過性の緻密な構造を有している。この電解質21の構成材料は特に限定されず、公知の固体酸化物型燃料電池に用いられる材料を使用することができるが、酸化物イオンの伝導性が高く、カソード31側の酸化性雰囲気からアノード11側の還元性雰囲気までの条件下で、化学的に安定で、熱衝撃に強い材料から構成することが好ましい。
【0087】
かかる要件を満たす材料としては、例えば、イットリア安定化ジルコニア(YSZ)、
スカンジア安定化ジルコニア(ScSZ)等の安定化ジルコニア;ランタンガレート;セリア系固溶体等が好ましいものとして挙げられる。
【0088】
安定化ジルコニアは特に限定はないが、下記一般式
(ZrO2)1−x(M2O3)x
[式中、MはY、Sc、Sm、Al、Nd、Gd、Yb及びCeからなる群より選ばれた1種以上の元素を示す。ただしここで、MがCeの場合はM2O3の代わりにCeO2である。]、又は、下記一般式
(ZrO2)1−x(MO)x
[式中、MはCa及びMgからなる群より選ばれた1種以上の元素を示す]における、xが0<x≦0.3である固溶体が好ましい。特に好ましいものとしては、例えば、(ZrO2)1−x(Y2O3)x(式中、0<x≦0.3)等が挙げられ、より好ましくは、式中、0.08≦x≦0.1である。また、更に好ましいものとしては(ZrO2)0.92(Y2O3)0.08等が挙げられる。
【0089】
なお、例えば「式中、Aは、Q、R及びTからなる群から選ばれた1種以上の元素を示す」という表現は、式中、AがQである固容体とAがRである固溶体の混合でもよいことを示すだけではなく、AとしてQとRとを同時に結晶サイトに有する固溶体をも示すものとする。以下、同様である。
【0090】
ランタンガレートは特に限定はないが、一般式、La1−xSrxGa1−y−zMgyAzO3(式中、AはCo、Fe、Ni又はCuの何れか1種以上の元素を示し、x=0.05〜0.3、y=0〜0.29、z=0.01〜0.3、y+z=0.025〜0.3の範囲である)で表される固溶体が好ましい。具体的には、La0.8Sr0.2Ga0.8Mg0.15Co0.05O3−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0091】
セリア系固溶体は特に限定はないが、Ce1−xMxO2(式中、MはGd、La、Y、Sc、Sm、Al、Pr、Nd、Ca、Mg、Sr、Ba、Dy、Yb、Tb、及び他の2価又は3価のランタノイドからなる群から選ばれた1種以上の元素を示す)における、xが0<x≦0.5である固溶体が好ましい。中でも、MがGdであるCe1−xGdxO2(式中、0<x≦0.5)、又は、MがSmであるCe1−xSmxO2(式中、0<x≦0.5)がより好ましく、何れの式においても、式中、0.03≦x≦0.4が特に好ましく、0.08≦x≦0.4が更に好ましく、0.1≦x≦0.4が最も好ましい。また、特に好ましいセリア系固溶体としては、Ce0.8Gd0.2O2−δ(式中、δは酸素欠損量を示す)、Ce0.67Gd0.33O2−δ(式中、δは酸素欠損量を示す)、Ce0.9Gd0.1O2−δ(式中、δは酸素欠損量を示す)等が挙げられる。特に、GDCを電解質21の材料として用いると、発電時の温度が750℃以下であっても、出力密度を充分大きくできるので好ましい。
【0092】
また、発電の際に、十分な出力特性を得る観点からは、かかる複合金属酸化物の導電率は、1000℃において、0.01〜10Scm−1であることが好ましい。
【0093】
<固体酸化物型電池の製造方法>
本発明の固体酸化物型電池の製造方法は特に限定されず、公知の固体酸化物燃料電池の製造に適用されている公知の薄膜製造技術等を使用することができる。例えば、スキージ法、スクリーンプリンティング法、真空蒸着法、スパッタ法、イオンプレーティング法等のPVD法、熱CVD法、プラズマCVD法、レーザーCVD法等のCVD法、溶射法等が挙げられる。
【0094】
例えば、電解質21を形成する方法としては、例えば、公知のセラミックプロセスであるシート成形焼結法を例示することができる。より具体的には、原料及び溶媒を混合することによって得たスラリーをシート状に延ばし、乾燥させた後に、必要に応じてカッターナイフ等を用いて成形し焼成する。スラリーには、必要に応じて、バインダー、可塑剤、分散剤等の公知の添加剤を配合させてもよい。成形、焼成等の条件は、原料の組成に応じて適宜設定することができる。また、先に述べたPVD法、CVD法、溶射法等の薄膜形成法により、例えば、アノード11又はカソード31上に電解質21の層を形成することもできる。
【0095】
<運転方法>
本発明の固体酸化物型電池の運転方法は、前記した一酸化炭素等の発電開始剤を燃料室1の固体炭素2に供給して電池反応を開始させる工程後、カソード31に空気等の酸化剤を含むガスを供給し、連続的に供給される固体炭素2を還元剤として発電する発電工程とを少なくとも含む方法であれば特に限定されない。通常、発電開始剤を導入して電池反応が開始され、固体炭素2が供給され続ける限り、連続的な運転が可能である。
【0096】
発電開始剤導入方法については、特に限定されるものではなく、燃料室1の固体炭素2へ極少量の一酸化炭素又は二酸化炭素を瞬間的に流せばよい。反応開始剤の流入量は、電池反応が開始するのに十分量であればよく特に限定されない。
【0097】
燃料として供給される固体炭素2は炭素を含有するものをいい、ここで「炭素」とは無定形炭素、グラファイト等の単体炭素をいう。固体炭素2は、具体的には特に限定はないが、天然黒鉛、人造黒鉛、カーボンブラック(ファーネスブラック、チャンネルブラック、アセチレンブラック、ランプブラック等)、グラファイトチョーク、フラーレン等の結晶性炭素;木炭、竹炭、墨等の動植物由来の炭素;煙突煤;コークス;排気ガスに含まれるPM中の炭素微粒子;等が挙げられる。
【0098】
固体炭素2の形態は、粉末、顆粒、ペレット、芯状等、何れの形態であってもよいが、固体炭素2の充填部をガスが透過する必要がある。ペレット、芯状等、バルクの場合は、バルク自体に多孔性を持たせる、あるいは貫通孔や溝を設ける等してガス流路を確保することが好ましい。
【0099】
また、固体炭素2の種類については、上記したように内燃機関等から排出される排気ガス中のPM等でも燃料として使用可能である。PM中の炭素微粒子が燃料である固体炭素2となる。すなわち、本発明の固体酸化物型電池においては、固体炭素2が排気ガス中の炭素微粒子であることも好ましい。
【0100】
固体炭素2中の炭素の含有率は、発電特性の観点からは高い方が良く、固体炭素2全体に対して50質量%以上であることが好ましく、70質量%以上であることがより好ましく、90質量%以上であることが特に好ましい。
【0101】
固体炭素2の供給方法については、上記形態の固体炭素2を直接的に燃料室1に格納すればよく、従来の公知文献2に記載されているような賦活工程が不要なため、非常に簡便である。また、PM浄化装置へ適用する場合は、排ガス中のPMを捕集して蓄積させる機構を固体酸化物型電池に併設することで、連続的に供給することができる。
【0102】
本発明の固体酸化物型電池の発電方法においては、発電開始直後、電流密度をその初期値から増加させながら運転させることが、安定した発電のために好ましい。発電開始直後、徐々に電流密度を上げることが、安定した発電のために特に好ましい。「徐々に電流密度を上げる」とは、通常、毎分当り0.008mA/cm2〜2mA/cm2で増加させることをいい、特に好ましくは、毎分当り0.016mA/cm2〜1mA/cm2である。かかる範囲を外れると、初期の発電特性が安定しない場合がある。
【0103】
以上、本発明の好適な実施形態について説明したが、本発明は上記実施形態に限定されるものではない。例えば、本発明の固体酸化物型電池は、例えば、図に示した固体酸化物型電池を複数積層した形態を有していてもよい。
【0104】
本発明においては、燃料室1中の固体炭素2を、発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電する。特に、発電時にアノード11において、少なくとも、下記の反応式(1)及び(2)を利用して発電を行う。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【0105】
反応式(1)を利用することで、アノード11の近傍に供給される固体炭素2を、気体のCOに変換して燃料として消費するので、発電時において固体炭素2の存在位置の影響を極めて小さくすることが可能になる。つまり、固体酸化物型電池では、一般的に電解質21の表面に近いところでの電極反応ほど発電への寄与が大きいので、電解質21の表面から遠いところに分布する固体炭素2は消費されにくい。そのため、反応式(1)で示される反応が起きない場合と比べて高い燃料利用率が得られ、アノード11から離れた位置に固体炭素2が供給されても発電が可能になる。
【0106】
加えて、反応式(2)によるCOの酸化反応は、下記反応式(3)又は反応式(4)による固体炭素2の酸化反応よりも反応速度が大きいため、高い出力密度が得られる。反応式(2)を支配的に起こすには、例えば、反応生成ガスによる圧力上昇分以上はアノード11外部に反応生成ガスを放出させないようにして、反応式(1)や反応式(3)で生成した一酸化炭素(CO)をアノード11に滞留する時間を長くすることや、系外から流入する酸素によって起こる一酸化炭素(CO)の酸化による消費を抑えること等が挙げられる。
C+O2− → CO+2e− (3)
C+2O2− → CO2+4e− (4)
【0107】
本発明の固体酸化物型電池の発電方法においては、反応式(2)で消費される一酸化炭素(CO)の50モル%以上が反応式(1)で生成されることが好ましい。すなわち、発電時に消費される一酸化炭素の50モル%以上が、固体炭素2と二酸化炭素との反応により生じた一酸化炭素であることが好ましい。特に好ましくは60モル%以上、更に好ましくは70モル%以上である。
【0108】
また、本発明の固体酸化物型電池の発電方法においては、電荷移動量の50%以上が、固体炭素2と二酸化炭素との反応により得られた一酸化炭素の酸化に起因することが好ましい。
【0109】
反応式(2)を支配的に起こす手段としては、反応式(1)や反応式(3)で生成したCOをアノード11に滞留する時間を長くさせることや、系外から流入する酸素によって起こるCOの酸化による消費を抑えるために、酸素の流入を遮断すること等が挙げられる。常法のようにアノード11にキャリアガスを流すと、反応式(2)は殆ど起こらない。
【0110】
アノード11において反応式(1)で示される反応を起こすためには、電極反応(2)及び/又は(4)で生成したCO2をアノード11中に長く滞留させることが大事であり、そのために発電時のキャリアガスの導入を無くすことが好ましい。キャリアガスの導入を無くすためには、系外からの空気つまりは酸素の漏れこみを、シール性能を向上する等して、極力少なくし、酸素分圧の上昇による電圧低下を防ぐことが好ましい。
【0111】
発電工程において、カソード31に供給する酸化剤を含むガスは、入手容易性から空気であることが好ましい。また、同様の観点から、酸化剤は酸素であることが好ましい。
【0112】
また、発電時における固体酸化物型電池の電荷移動量や出力密度を向上させる観点から、アノード11に、該アノード11における反応生成ガスを外部に放出させるためのキャリアガスを供給しないことが好ましい。
【0113】
本発明の固体酸化物型電池において、発電工程での温度は400〜1000℃が好ましく、450〜900℃がより好ましく、500〜750℃が特に好ましい。温度が低すぎると反応式(1)が進行しにくくなることや、セル(電極及び電解質)の抵抗が大きくなるために、出力密度が低下する場合がある。一方、高すぎると、セルや周辺部材の劣化が早まる場合がある。
【0114】
本発明の固体酸化物型電池は、発電時の温度750℃以下で、出力密度が50(mW/cm2)以上にすることができる。また、出力密度が50(mW/cm2)以上になるように、組成、構造、設定等が調整された固体酸化物型電池が好ましい。特に、電解質21としてGDCを用いることによって、発電時の温度が750℃以下であっても、出力密度を50(mW/cm2)以上にすることができる。
【0115】
また、本発明の固体酸化物型電池は、電流密度9.3mA/cm2で発電したときの燃料利用効率を60%以上にできる。また、燃料利用効率60%以上になるように、組成、構造、設定等が調整された固体酸化物型電池が好ましい。ここで「燃料利用効率」とは、アノード材料11b近傍に供給した固体炭素2中の炭素に対する、反応式(4)を仮定し電荷移動量から計算した消費炭素量の割合である。
【0116】
また、本発明の固体酸化物型電池は、電流密度80mA/cm2で発電したときの燃料利用効率を20%以上にできる。また、燃料利用効率20%以上になるように、組成、構造、設定等が調整された固体酸化物型電池が好ましい。特に好ましくは30%以上、更に好ましくは40%以上である。
【0117】
具体的には、上記したように、系外からの空気すなわち酸素の漏れこみを、シール性能を向上する等して極力少なくしたり、アノード11の大気への開口径を小さくしたりして大気からアノード11への酸素の流入を抑制して、反応式(1)及び/又は反応式(2)における一酸化炭素(CO)について損失を軽減することによって実現される。
【0118】
本発明の固体酸化物型電池の構造は特に限定されるものではなく、例えば、図13のように、平板状の電解質21の層の一方の面にアノード11、他方の面にカソード31を形成した構造を有し、セパレータを介して順次積層したスタックからなる平板型の固体酸化物型電池の構成を有しているものであってもよく、あるいは図8〜12のように、円筒状の支持管の円筒面上にカソード31、電解質21の層及びアノード11を順次形成し、積層させた構造を有する円筒型の固体酸化物型電池の構成を有しているものであってもよい。
【0119】
上記は本願発明を主として燃料電池として利用する際の最良の形態の一例を示したものであるが、本願発明は、二次電池、水素発生装置、排ガス除去等への応用、すなわち、電気化学リアクターとしての利用も可能であり、この場合も上記に準じて適宜実施可能である。
【実施例】
【0120】
以下、本発明を実施例により更に詳細に説明するが、本発明はこれら実施例に限定されるものではない。
【0121】
<実施例1>
電解質として、厚さ0.3mmのScSZ(10モル%のSc2O3と1モル%のCeO2がドープされたZrO2)ディスクを使用し、アノード材料には、Ni/GDC(GdがドープされたCeO2)多孔質サーメットを、カソード材料にはLa0.85Sr0.15MnO3多孔質膜を用いた。アノードの厚さは50μmであった。なお、構成と製造方法は、一般的な固体酸化物型燃料電池の構成と製造方法に従った。すなわち、アノード材料及びカソード材料の粉体を溶媒に分散し、有機バインダー等を添加してスラリーを調製した。次いで、当該スラリーをドクターブレード法でディスクに塗布し、焼成して固体酸化物型燃料電池を作成した。
【0122】
アノード材料への固体炭素の担持は以下の手順でおこなった。すなわち、カーボンブラック(三菱化学社製「MA7」)(以下、「CB」と略記する)をエタノールに分散させた溶液を調製し、このCB分散溶液をアノードに滴下、浸透させ、1.0mgのCBをアノードに担持させた。
【0123】
集電体を介して、アノードと反対側のスペース(燃料室)に28.3mgのCBを充填した。なお、燃料として用いた固体炭素であるCBの炭素含有率は96.5質量%〜100質量%(揮発成分3.5質量%含有)であった。このようにして、図2に示したような固体酸化物型電池を作製した。
【0124】
アノードに純アルゴン(Ar)を202STPmL/分で約1時間供給し、O2等の残留ガスを十分排気した。
【0125】
発電中はカソード側に純酸素を酸化剤として供給し、アノード側はアルゴン(Ar)ガスをフローしなかった。セルのシールを確実にし、アノードから3.5mの1/8インチステンレス管をつなぎ、ガスクロマトグラフ装置を挟んで5mのビニルチューブ(内径8mm)で外に排気することで、大気からの空気の逆拡散を抑制した。
【0126】
900℃で、電流をある一定電流密度に調整した場合の発電をおこない、それぞれの電量密度における端子電圧の経時変化をモニターした。その時の最大出力密度(mW/cm2)と電流密度(mA/cm2)を表1に示す。
【0127】
<実施例2>
アノードにCBを担持しないこと、及び燃料室へのCBの充填量が21.0mgであること以外は、実施例1と同様に固体酸化物型電池を作製し、900℃での電流変化時の発電特性を調べた。その時の電流密度(mA/cm2)と最大出力密度(mW/cm2)を表1に示す。
【0128】
【表1】

【0129】
表1より、実施例1、2ともに固体炭素を消費して発電していることが判った。例えば、表1に示すように、実施例1では電流が58.4mAの時に24.6mW/cm2の出力密度が得られ、実施例2では電流が33.0mAの時に20.3mW/cm2の出力密度が得られた。
【0130】
特に、実施例2のようにアノードに固体炭素を直接担持しなくても発電しており、このことは燃料室に充填、格納した固体炭素が消費されていることを意味している。すなわち、特許文献2に開示されている従来のような賦活工程を必要とすることなく、燃料室に固体炭素を供給しさえすれば連続的に燃料電池を運転することが可能となるため、実用性の高い発電方法が提供される。
【0131】
また、ディーゼル車等の内燃機関から排出されるPMのように、飛散してくる固体炭素に対しても、捕集した後に燃料室に供給する、あるいは直接燃料室でPMを捕集する仕組みさえ導入すれば、本発明の固体酸化物型電池の運転方法が適用できるため、有害物質であるPMを除去(消費)し、発電することが可能である。
【産業上の利用可能性】
【0132】
本発明は、従来のような賦活工程を必要とすることなく、燃料室に固体炭素を供給しさえすれば連続的に燃料電池を運転することが可能なため、より実用性の高い運転方法が提供でき、燃料電池応用分野に広く利用できるものである。また、この固体炭素を酸化させる作用を応用すれば、ディーゼルエンジン等の内燃機関から排出される排ガス中に含まれるPMの除去も可能であり、電気化学リアクター(電気化学的な反応場を提供する装置)としての利用も可能である。
【符号の説明】
【0133】
1 燃料室
2 固体炭素
3 二酸化炭素(CO2)排出口
10 燃料電池セル
11 アノード
11a アノード集電体
11b アノード材料
13 発電開始剤導入管
15 アノードに担持された固体炭素
21 電解質
22 外部制御回路
23 電気回路
31 カソード
31a カソード集電体
31b カソード材料
33 酸化剤を含むガス導入口
【技術分野】
【0001】
本発明は、アノード材料に供給される固体炭素を燃料として用いて発電する固体酸化物型電池の発電方法、及び、該発電方法を使用して発電する固体酸化物型電池に関する。
【背景技術】
【0002】
イオン伝導性の固体酸化物(酸化物イオン伝導体)からなる電解質層(固体電解質層)をカソード(空気極)とアノード(燃料極)との間に配置した積層構造を有する固体酸化物型電池(SOFC)は、第三世代の燃料電池として期待され、その開発が進んでいる。
【0003】
固体酸化物型電池は、アノードに還元剤、例えば、水素(H2)、一酸化炭素(CO)、メタン(CH4)等のガス(燃料ガス)を供給し、カソードに酸化剤、例えば、酸素(O2)等を含むガス(例えば空気)を供給することにより発電するデバイスである(例えば、下記特許文献1参照)。
【0004】
従来の固体酸化物型電池(SOFC)では電極活物質はガス状であったが、電極活物質としてエネルギー密度の非常に高い固体炭素を用いることが提案された(特許文献2)。特許文献2は、アノード材料に担持させた固体炭素を二酸化炭素(CO2)と反応させて気体の一酸化炭素(CO)に変換し、当該気体の一酸化炭素(CO)を酸化することにより発電することを特徴としている。また、電気化学リアクター(電気化学的な反応場を提供する装置)としての利用も可能であると提案している。
【0005】
しかしながら、上記の固体酸化物型電池は、炭化水素等の有機化合物を導入し、熱分解反応を進行させて、一旦固体炭素をアノードに担持させる賦活工程等を必須工程として含み、あらかじめ燃料となる固体炭素をアノードに担持させておくことが必要であり、発電途中で固体炭素を補充することができないため、連続的に燃料電池反応を継続することができず、連続的な作動が求められる発電システムや電気化学リアクターにはそのまま適用することは難しく、実用化の観点からするとその技術価値を十分に発揮させることができなかった。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開平9−129256号公報
【特許文献2】特開2008−198585号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明は上記背景技術に鑑みてなされたものであり、その課題は、アノードに炭化水素等の有機化合物を導入して熱分解反応を進行させて、固体炭素をアノードに一旦担持させる工程を必要とせず、連続的に燃料電池反応を継続させることのできる新規の固体酸化物型電池の発電方法を提供することにある。
【課題を解決するための手段】
【0008】
本発明者らは上記課題を解決すべく鋭意検討を行った結果、固体酸化物型電池の装置構成として少なくとも固体炭素を格納するための燃料室を設け、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電させる発電方法を採れば、固体炭素がアノードに担持されていないで燃料室に格納されていても、すなわち固体炭素がアノードから離れていても、該固体炭素が燃料として消費され、結果として連続的な発電が可能であることを見出し、本発明に到った。
【0009】
すなわち、本発明の第1の要旨は、複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池における発電方法であって、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電することを特徴とする固体酸化物型電池の発電方法に存する。
【0010】
第2の要旨は、上記アノードに固体炭素を担持させて用いる上記の固体酸化物型電池の発電方法に存する。
【0011】
第3の要旨は、上記燃料室の固体炭素に一酸化炭素又は二酸化炭素を供給することで発電を開始させる上記の固体酸化物型電池の発電方法に存する。
【0012】
第4の要旨は、発電開始時に発電開始剤を供給するための発電開始剤導入管の先端が、燃料室とアノードの間に配置されている上記の固体酸化物型電池の発電方法に存する。
【0013】
第5の要旨は、発電開始直後、電流密度をその初期値から増加させながら運転させることを特徴とする上記の固体酸化物型電池の発電方法に存する。
【0014】
第6の要旨は、発電開始時に、アノードへ電気化学的に酸素源を注入することを特徴とする上記の固体酸化物型電池の発電方法に存する。
【0015】
第7の要旨は、発電時に下記反応式(1)及び(2)を利用して発電することを特徴とする上記の固体酸化物型電池の発電方法に存する。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【0016】
第8の要旨は、上記固体炭素の炭素含有率が50質量%以上である上記の固体酸化物型電池の発電方法に存する。
【0017】
第9の要旨は、上記固体炭素が排気ガス中の炭素微粒子である上記の固体酸化物型電池の発電方法に存する。
【0018】
第10の要旨は、複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池に存する。
【0019】
第11の要旨は、発電開始時に発電開始剤を供給するための発電開始剤導入管を有し、該発電開始剤導入管の先端が燃料室とアノードの間に配置されている上記の固体酸化物型電池に存する。
【0020】
第12の要旨は、発電時に下記反応式(1)及び(2)を利用して発電する上記の固体酸化物型電池に存する。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【0021】
第13の要旨は、上記の固体酸化物型電池の発電方法を使用して発電することを特徴とする固体酸化物型電池に存する。
【発明の効果】
【0022】
本発明によれば、あらかじめアノードに、炭化水素等の有機化合物を導入し、熱分解反応で一旦固体炭素を担持させておく必要がないため、連続的に燃料電池反応を継続することができることから、連続的な作動を要する発電システムや電気化学リアクターへの適用を容易ならしめ、実用化を促進し得る。
【0023】
特に、後述する実施例2のように、アノードに固体炭素を直接担持しなくても発電しており、このことは燃料室に格納した固体炭素が消費されていることを意味している。すなわち、従来のように、炭化水素等の有機化合物を導入し熱分解反応を進行させて、固体炭素をアノードに直接担持させる賦活工程を必要とすることなく、燃料室に固体炭素を供給しさえすれば連続的に燃料電池を運転することが可能となるため、実用性の高い運転方法が可能となる。
【0024】
また、燃料である固体炭素がアノードに接していなくても、近傍に存在する燃料室に格納又は充填されていれば作動することから、燃料の供給方法に幅が広がり、システムの設計面でも幅が広がる。特に、内燃機関から排出される排ガス中に含まれる粒子状物質(Particulate Matter、以下、「PM」と略記する。)を除去する浄化装置に適用した場合、PM捕集部と固体酸化物型電池部とを独立させて配置することが可能なため、連続的なPM除去と同時に発電が可能な、いわゆる外部電源等を必要としない自己完結型の電気化学的PM浄化システムの構築が容易となり、実用的な浄化装置を提供することができる。
【図面の簡単な説明】
【0025】
【図1】本発明の固体酸化物型電池の実施形態の基本構成の一例を示す模式断面図である。
【図2】本発明の固体酸化物型電池であって、アノード材料にも固体炭素が担持されている実施形態の基本構成の一例を示す模式断面図である。
【図3】本発明の固体酸化物型電池であって、発電開始剤導入管を備えた実施形態の基本構成を示す模式断面図である。
【図4】本発明の固体酸化物型電池であって、発電開始剤導入管が燃料室内を貫通している実施形態の基本構成の一例を示す模式断面図である。
【図5】本発明の固体酸化物型電池であって、発電開始剤導入管の先端が燃料室内に位置するように配置されている実施形態の基本構成の一例を示す模式断面図である。
【図6】本発明の固体酸化物型電池であって、電流密度を制御するための外部制御回路を有している実施形態の基本構成の一例を示す模式断面図である。
【図7】本発明の固体酸化物型電池であって、アノードへ電気化学的に酸素源を注入するための電気回路を有している実施形態の基本構成の一例を示す模式断面図である。
【図8】本発明の固体酸化物型電池であって、円筒形状をしたものの基本構成の一例を示す模式断面図である。
【図9】本発明の固体酸化物型電池であって、円筒形状をしたものの基本構成の一例を示す模式断面図である。
【図10】本発明の固体酸化物型電池であって、円筒形をした燃料電池セルの片末端が封じられているものの基本構成の一例を示す模式縦断面図と、模式横(C−d)断面図である。
【図11】本発明の固体酸化物型電池であって、円筒形状をしたものの基本構成の一例を示す模式断面図である。
【図12】図11に示した本発明の固体酸化物型電池の模式斜視図である。
【図13】本発明の固体酸化物型電池であって、燃料電池セル1が積層されているものの基本構成の一例を示す模式断面図である。
【発明を実施するための形態】
【0026】
以下、図面を参照しながら本発明の好適な実施形態について詳細に説明するが、本発明は以下の実施の形態に限定されるものではなく、その技術的思想の範囲内で種々変形することができる。
【0027】
<固体酸化物型電池の形態>
図1は、本発明の固体酸化物型電池の好適な一実施形態の基本構成を示す模式断面図である。図1に示す固体酸化物型電池は、少なくとも、燃料電池セル10、燃料室1及び「酸化剤を含むガス導入口」33を有している。そして、燃料電池セル10は、主として、アノード11、カソード31、及び、アノード11とカソード31との間に配置された電解質21とから構成されている。図1に示すアノード11は、アノード材料11b及びアノード集電体11aを有している。また、図1に示すカソード31は、カソード材料31b及びカソード集電体31aを有している。
【0028】
また、本発明の固体酸化物型電池は、燃料である固体炭素2を格納でき、該固体炭素2を燃料電池セル10に供給するための燃料室1を具備している。ここで燃料室1とは、アノード11側に設けられた発電のための固体炭素2を格納する空間であり、そこに格納される固体炭素2はアノード11に接している必要はないが、該固体炭素2の少なくとも一部はアノード11に接していることも好ましい。より具体的には、燃料室1は、そこに格納される固体炭素2が、アノード集電体11aやアノード材料11bと接触するようになっている必要はないが、接触するようになっていることも好ましい。本発明では、アノード11に、後述するように発電開始時に、また、上記したように発電中にも、固体炭素2を担持させて用いることが好ましい。発電中に担持させる固体炭素2は、前述の有機化合物の熱分解反応で生じるものではなく、外部から燃料室1に供給したものである。
【0029】
限定はされないが、例えば図1においては、燃料室1のうち下約90%に固体炭素2が格納されている。発電中でも、燃料室1に燃料である固体炭素2を追加することによって、発電を継続することができる。
【0030】
アノード11側への酸素の混入は、発電効率の観点からできるだけ軽減した方が好ましい。酸素除去のために、窒素(N2)や二酸化炭素(CO2)等の不活性ガスで置換した固体炭素2を格納することも好ましい。
【0031】
燃料室1に固体炭素2があり、発電により生じたCO2が、例えば500〜1000℃で存在すれば、CO生成反応が進行し、燃料電池セル10により発電が継続される。本発明は、この意外な事実の新しい発見に基づいてなされたものである。
【0032】
更に、図1に示す固体酸化物型電池は、アノード11側にCO2を排出するための二酸化炭素(CO2)排出口3、カソード31側に酸素(O2)等の酸化剤を供給するための「酸化剤を含むガス導入口」33を有している。
【0033】
図2も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した形態と異なる点は、燃料室1内の固体炭素2以外に、アノード材料11bにも、固体炭素15が担持されていることであり、それ以外は図1に示す固体酸化物型電池と同じ構成である。特に、発電開始時に、アノード材料11bに固体炭素15を担持させておくことが、初期発電特性の安定化の観点から好ましい。アノード11に担持される固体炭素15は、燃料室1内に格納される後述する固体炭素2と同じものでもよいし、異なるものでもよい。
【0034】
図3も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した基本構成に加えて、二酸化炭素(CO2)排出口3の燃料室1を除くスペースに、発電開始剤導入管13を備え、発電開始剤導入管13の先端が、燃料室1とアノード11(具体的には、アノード集電体11a)との間に配置されている。発電開始剤導入管の先端が、燃料室1とアノード11の間に配置されていることによって、発電開始剤がアノード材料11bの近傍に供給され、その結果、初期の発電特性が安定し易い。
【0035】
図4に示す固体酸化物型電池は、図3に示した固体酸化物型電池と基本構成は同じであるが、発電開始剤導入管13の配置が異なる。すなわち、発電開始剤導入管13は燃料室1内を貫通し、発電開始剤導入管13の先端が、燃料室1とアノード11との間に配置されている。より詳しくは、燃料室1とアノード集電体11aの間に位置するように配置されている。効果は上記と同様である。
【0036】
図5に示す固体酸化物型電池は、図3と図4に示した固体酸化物型電池と基本構成は同じであるが、発電開始剤導入管13の先端の位置が異なる。すなわち、発電開始剤導入管13の先端が燃料室1内に位置するように配置されている。これでも、発電開始剤は徐々にアノード11に供給されるため、上記と同様の効果が得られる。
【0037】
図6も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した固体酸化物型電池の基本構成に加えて、固体酸化物型電池の電流密度を制御するための外部制御回路22を有している。
【0038】
図7も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。図1に示した固体酸化物型電池の基本構成に加えて、アノード11へ電気化学的に酸素源を注入するための電気回路23を有している。本発明の固体酸化物型電池の発電方法においては、発電開始時に、アノード11へ電気化学的に酸素源を注入することが、初期の発電特性を安定化させる点で好ましい。酸素源は特に限定はないが、具体的には、例えば、空気や酸素等が挙げられる。酸素源の電気化学的な注入方法については特に限定はされないが、具体的には、例えば、アノード11とカソード31との間に、電池セルの持つネルンスト電位を利用し、電流密度0.01mA/cm2〜5mA/cm2で流し、カソード31で酸素が電子を取り込んで酸化物イオン(O2−)となり、このO2−が電解質を移動してアノード11で燃料と反応して電子を放出させ、電極反応を開始させることが好ましい。発電開始時に、アノード11へ電気化学的に酸素源を注入しないと、発電の初期段階で安定した発電が得られない場合がある。
【0039】
図8も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、アノード11の外周側に燃料室1、カソード31の内周側に「酸化剤を含むガス導入口」33を配した構成となっている。
【0040】
図9も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、アノード11の内周側に燃料室1、カソード31の外周側に「酸化剤を含むガス導入口」33を配した構成となっている。
【0041】
図10も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、燃料電池セル10が円筒形をしており、円筒形をした燃料電池セル10の片末端は封じられている。燃料電池セル10の円筒の外部に燃料室1、内部に「酸化剤を含むガス導入口」33を配した構成となっている。
【0042】
図11も、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21が円筒形状である固体酸化物型電池であり、燃料室1を貫通するように円筒形をした燃料電池セル10が配されている。また、燃料室1に二酸化炭素(CO2)排出口3が設けられており、貫通型の円筒形の燃料電池セル10の円筒内部に、空気等の酸素含有ガスを供給するための「酸化剤を含むガス導入口」33を設けた構成となっている。
【0043】
図12は、図11に示した本発明の固体酸化物型電池を立体的に示した模式斜視図である。
【0044】
図13は、本発明の固体酸化物型電池の基本構成を示す模式断面図である。アノード11、カソード31及び電解質21を有する燃料電池セル10が積層しており、2つのアノード11で挟まれたスペースに燃料室1が設けられ、カソード31で挟まれたスペースに空気等の酸素含有ガス等を供給するための「酸化剤を含むガス導入口」33が設けられた構成となっている。
【0045】
<アノード>
アノード11のアノード材料11bは複合金属酸化物を含む。すなわち、アノード材料11bは、複合金属酸化物を含むものであってもよいし、サーメットを含むものであってもよい。ここで「サーメット」とは、金属と金属酸化物粉末が混合され焼結されたものをいう。複合金属酸化物又はサーメットは多孔質であることが好ましい。複合金属酸化物又はサーメットとしては、公知の固体酸化物型燃料電池にアノード活物質として一般に用いられているものが好適に使用できる。
【0046】
[複合金属酸化物]
自身がアノード材料11bの成分として、また、アノード材料11bの成分であるサーメットの原料としても用いられる複合金属酸化物としては、固体酸化物型燃料電池にアノード活物質として一般に用いられているものであれば特に限定はない。発電の際に、十分な出力特性、耐久性等を確実に得る点からは、イットリアが配合された安定化ジルコニア(Y2O3−ZrO2)(以下、「YSZ」と略記する);Gd、La、Y、Sm、Nd、Ca、Mg、Sr、Ba、Dy及びYbからなる群より選ばれる少なくとも1種がドープされたCeO2[このうち特に、GdがドープされたCeO2(以下、「GDC」と略記する)、SmがドープされたCeO2が好ましい];Sc2O3−ZrO2(以下、「ScSZ」と略記する);Sm2O3−CeO2(以下、「SDC」と略記する)等が特に好ましい。
【0047】
ここで、上記YSZの場合、Y2O3の割合(Y2O3の含有量)は、Y2O3−ZrO2に対して8〜10モル%であることが好ましい。また、上記GDCの場合、Gdの割合(Gdの含有量)は、ドープされたCeO2に対して3〜40モル%が好ましく、8〜40モル%がより好ましく、10〜40モル%が更に好ましく、15〜40モル%であることが特に好ましい。更に、上記SmがドープされたCeO2の場合、Smの割合(Smの含有量)は、ドープされたCeO2に対して15〜40モル%であることが好ましい。また、特に好ましいセリア系固溶体としては、Ce0.8Gd0.2O2−δ(式中、δは酸素欠損量を示す)、Ce0.67Gd0.33O2−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0048】
また、発電の際に、十分な出力特性を得る観点からは、電気伝導性を有する複合金属酸化物を用いることが好ましい。複合金属酸化物の導電率は、1000℃において、0.01〜10Scm−1であることが特に好ましい。
【0049】
[[サーメット]]
本発明の効果をより確実に得るとともに、優れた出力特性をより確実に得る観点から、アノード材料11bはサーメットであることが好ましい。サーメットとしては、固体酸化物型燃料電池にアノード活物質として一般に用いられているものであれば特に限定はないが、Ni、Pt、Au、Cu、Fe、W及びTaからなる群より選ばれる少なくとも1種の金属と複合金属酸化物(特に上記複合金属酸化物)とのサーメットが好ましい。発電の際に、十分な出力特性を確実に得る点等からは、ニッケルと複合金属酸化物のサーメット等が好ましいものとして挙げられ、特に、ニッケルと上記した複合金属酸化物とのサーメット等が好ましいものとして挙げられる。
【0050】
特に好ましくは、出力特性の点で、ニッケルとYSZとのサーメット(以下、「Ni/YSZ」と略記する)、ニッケルとGDCとのサーメット(以下、「Ni/GDC」と略記する)、ニッケルとScSZとのサーメット(以下、「Ni/ScSZ」と略記する)又はニッケルとSDCとのサーメット(以下、「Ni/SDC」と略記する)である。
【0051】
また、サーメットにおける金属の体積分率V1と、複合金属酸化物の体積分率V2とが下記式で表される条件を満たしていることが、電子伝導性確保の点で好ましい。
0.2≦[V1/(V1+V2)]≦0.8
【0052】
ここで、[V1/(V1+V2)]が0.2未満となると、アノード材料11b中の電子伝導性が十分に確保できなくなり、固体酸化物型電池の出力特性が不十分となる場合がある。また、[V1/(V1+V2)]が0.8を超えると、アノード材料11b中のイオン伝導性が十分に確保できなくなり、固体酸化物型電池1の出力特性が不十分となる場合がある。アノード材料11b中の電子伝導性とイオン伝導性を共に十分に確保する観点から、[V1/(V1+V2)]は0.2〜0.8であることが好ましく、0.3〜0.7であることが特に好ましく、0.4〜0.6が更に好ましい。
【0053】
具体的には、Ni/YSZ、Ni/GDC、Ni/ScSZ、又はNi/SDCにおいて、体積分率の比としてNi/(かかる複合金属酸化物+Ni)の値が、上記値の範囲に入っているものが好ましい。
【0054】
[[電気伝導性を有する複合金属酸化物]]
ここで、アノード材料11bがサーメットのような金属粒子若しくは合金粒子を含む材料であると、アノード中の金属が、カーバイドやカーボンウィスカーを生成させる原因になり、長期的な電極劣化の要因となる場合がある。すなわち、金属に溶解した炭素が析出して成長する際に金属粒子を電極のフレーム構造から脱落させてしまい、それが電極劣化の要因となる場合がある。また、酸化還元サイクル時の金属粒子の体積膨張・収縮により、それが電極劣化の要因となる場合がある。したがって、アノード材料11bとして、上記サーメットに代えて、電気伝導性を有する複合金属酸化物を用いることも好ましい。
【0055】
電極劣化の原因となる金属粒子若しくは合金粒子を含むサーメットに代えて、アノード材料11bのうちの少なくとも1種のアノード材料に電気伝導性を有する複合金属酸化物を用いることによって、上記電極劣化の要因が解消され、RDCFCの運転時にアノードの劣化を抑制し、酸化還元サイクル特性を向上させ、高出力を安定的に維持させることができる。アノード材料11bに電気伝導性を有する複合金属酸化物を含むことが好ましい。ここで、「電気伝導性を有する」とは、運転温度において電気伝導度が10−4Scm−1以上であることを意味する。
【0056】
ここで、前記した電極劣化を生じない範囲においては金属を含有していてもよく、本発明は、アノード材料11bの組成から、少量の「金属粒子若しくは合金粒子」の含有を排除するものではない。アノード材料11b全体中に含有される「金属粒子若しくは合金粒子」は合計で10質量%以下が好ましく、5質量%以下がより好ましく、2質量%以下が特に好ましく、金属粒子も合金粒子も含まれていないことが更に好ましい。
【0057】
上記の「電気伝導性を有する複合金属酸化物」の電気伝導度は、運転温度において10−2Scm−1以上であることが好ましく、10−1Scm−1以上であることが特に好ましい。ここで、「電気伝導」とは、電子伝導、ホール伝導、酸化物イオン伝導及びプロトン伝導のうちの少なくとも1つからなる電気伝導、すなわち、それらのうちの1つ又は2つ以上が組み合わされた電気伝導を意味する。電気伝導度が低過ぎると、十分な出力特性が得られない場合がある。
【0058】
本発明の固体酸化物型電池のアノードは、金属粒子も合金粒子も含有していないか、又は、それらによる3次元的ネットワークが形成されない範囲を上限として金属粒子若しくは合金粒子を含有していることが好ましい。「3次元的ネットワーク」とは、アノードの厚さ方向にそれのみを通して電気伝導が可能の状態(通じる状態)をいう。金属粒子若しくは合金粒子による3次元的ネットワークが形成されていると、酸化と還元の繰り返しで、アノード材料が体積膨張と体積収縮を繰り返す結果、アノードが劣化する場合がある。
【0059】
また、本発明の固体酸化物型電池のアノード材料11bに用いられる電気伝導性を有する複合金属酸化物は、それ自体で、3次元的ネットワークを形成していること、すなわち複合金属酸化物自体で、電子伝導可能な3次元的ネットワークを形成していることが、良好な電気伝導性を実現し、結果として十分な出力特性が得られる点で好ましい。
【0060】
本発明の固体酸化物型電池のアノード材料11bに用いられる電気伝導性を有する複合金属酸化物は、少なくともそのうちの1種は、ペロブスカイト型結晶構造、パイロクロア型結晶構造又はフルオライト型結晶構造を有する複合金属酸化物よりなることが好ましい。
【0061】
ペロブスカイト型結晶構造を有する複合金属酸化物とは、いわゆるペロブスカイト型の結晶構造をとる複合金属酸化物をいい、下記一般式(G)で表わされる複合金属酸化物が好ましい。
A1±aB1±bO3−δ (G)
[組成式(G)中、Aは、La、Sr、Ca、Y、Ba、Pr、Ce、K、Na、Sm、Pb、Nd、Gd、Bi、Ag、Cs、Rb、Tl、Cd、Eu、Mg、Dy、Li及びHoからなる群より選ばれる少なくとも1種を示し、Bは、Co、Cr、Mn、Ni、Ce、Gd、Al、Ti、Zr、Sc、Mg、Ga、Cu、Fe、Yb、Y、Nb、I、Ni、Sr、Bi、In、Ca、Sn、Ta、W、Th、U、Hf、Mo、Lu、Tm、Tb、Dy、Ho、Os、Rh、Ag、Tr、Sb、Zn、Pa、In、Re及びErからなる群より選ばれる少なくとも1種を示し、0≦a≦0.2、0≦b≦0.2であり、δは酸素欠損量である。]
【0062】
このうち、LaMnO3、LaCoO3、LaCrO3等を母体とする物質がより好ましく、例えば、(LaSr)MnO3系の複合金属酸化物(本発明では、これを「LSM」と略記する)、(LaSr)CoO3系の複合金属酸化物(本発明では、これを「LSC」と略記する)が特に好ましいものとして挙げられる。
【0063】
また、組成式(G)において、Bが、MnをB全体に対して50モル%以上含有するものであることが、前記効果をより奏するために好ましい。また、組成式(G)において、Bが、CoをB全体に対して50モル%以上含有するものであること、又は、Bが、CoとFeを、それらの合計でB全体に対して50モル%以上含有するものであることが、前記効果を奏するために好ましい。
【0064】
そのほかのペロブスカイト型結晶構造を有する複合金属酸化物は、一般式、A(B1−xMx)1±aO3−δ[式中、0≦x≦0.8、0≦a≦0.2である]において、AはBa、Sr、Ca等の2価のカチオンから少なくとも1種が選ばれ、BはCe、Zr、Ti等の4価のカチオンから少なくとも1種が選ばれ、Mは3価の希土類、Y、Sc、In、Yb、Nd、Gd、Al、Ga等から少なくとも1種が選ばれる。
【0065】
例えば、Ba(Ce1−xGdx)1±aO3[式中、0≦x≦0.8、0≦a≦0.2である]、Ca(Al1−xTix)1±aO3[式中、0≦x≦0.8、0≦a≦0.2である]、Sr(Ce1−xYbx)1±aO3(式中、0≦x≦0.8、0≦a≦0.2である)、Sr(Zr1−xYx)1±aO3(式中、0≦x≦0.8、0≦a≦0.2である)、Sr(Zr1−xScx)1±aO3(式中、0≦x≦0.8、0≦a≦0.2である)等で表されるものも好ましい。具体的には、BaCe0.9Gd0.1O3、CaAl0.7Ti0.3O3、SrCe0.95Yb0.05O3、SrZr0.95Y0.05O3、SrZr0.9Sc0.1O3等が挙げられる。
【0066】
一般式、La1−xSrxGa1−y−zMgyMzO3[式中、Mは、Co、Fe、Ni又はCuの何れか1種以上の元素を示し、x=0.05〜0.3、y=0〜0.29、z=0.01〜0.3、y+z=0.025〜0.3の範囲である。]で表されるランタンガレートも好ましい。具体的には、La0.8Sr0.2Ga0.8Mg0.15Co0.05O3−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0067】
好ましい電気伝導性を有する複合金属酸化物としては、具体的には、例えば、La0.8Sr0.2MnO3、La0.85Sr0.15MnO3、La0.95Sr0.05MnO3等の、La1−bSrbMnO[bは、0≦b≦0.5]で表わされる化合物;La0.8Sr0.2CoO3、La0.85Sr0.15CoO3、La0.95Sr0.05CoO3等の、La1−dSrdMnO3[dは、0≦d≦0.5]で表わされる化合物;La0.6Sr0.4Fe0.8Co0.2O3、La0.6Sr0.4Fe0.2Co0.8O3等のLa1−eSreFefCo1−fO3[eは0≦e≦0.5、fは0≦f≦1]で表わされる化合物;La0.75Sr0.2Cr0.5Mn0.5O3等のLa1−gSrgCr1−hMnhO3[gは0≦g≦0.5、hは0≦h≦1]で表わされる化合物;等が挙げられる。
【0068】
パイロクロア型結晶構造を有する複合金属酸化物とは、いわゆるパイロクロア型の結晶構造をとる複合金属酸化物をいい、Ln2((Zr1−xTix)2)1±aO7(式中、LnはSc、Y、La及び他のランタノイドからなる群より選ばれた1種以上の元素を示し、0≦x≦0.5、0≦a≦0.2である)が好ましいものとして挙げられる。具体的には例えば、Gd2((Zr1−xTix)2)1±aO7(式中、0≦x≦0.5、0≦a≦0.2である)、Y2((Zr1−xTix)2)1±aO7(式中、0≦x≦0.5、0≦a≦0.2である)等が挙げられる。
【0069】
フルオライト型結晶構造を有する複合金属酸化物とは、いわゆるフルオライト型の結晶構造をとる複合金属酸化物をいい、その中で好ましいものはセリア系複合金属酸化物で、Ce1−xMxO2(式中、MはGd、La、Y、Sc、Sm、Pr、Nd、Ca、Mg、Sr、Ba、Dy、Yb、Tb及び他の2価または3価のランタノイドからなる群から選ばれた1種以上の元素を示し、0≦x≦0.5である)で表されるものである。特に好ましいセリア系複合金属酸化物として、Ce0.8Gd0.2O2−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0070】
本発明の固体酸化物型電池のアノード材料11bに用いられる電気伝導性を有する複合金属酸化物としては、ペロブスカイト型結晶構造を有する複合金属酸化物が、金属粒子若しくは合金粒子を含有しなくても高い電気伝導性を有し、前記した本発明の効果をより奏する点で特に好ましい。
【0071】
上記アノード材料11bが2種以上のアノード材料よりなる複合材料である場合には、上記以外のアノード材料も複合金属酸化物であることが好ましい。更に、アノードにおいては、少なくとも電子伝導性とホール伝導性のどちらかを有する複合金属酸化物、及び、少なくとも酸化物イオン伝導性とプロトン伝導性のどちらかを有する複合金属酸化物の2種類以上のアノード材料を含有することが好ましい。ここで、「少なくとも電子伝導性とホール伝導性のどちらかを有する」とは、その両方を合わせた電気伝導度が10−4Scm−1以上であることをいい、「少なくとも酸化物イオン伝導性とプロトン伝導性のどちらかを有する」とは、その両方を合わせた電気伝導度が10−4Scm−1以上であることをいう。
【0072】
本発明における好ましいアノード材料11bとしては、比較的高い電子伝導性と酸化物イオン伝導性の両方を有するという点で、LSMとGDCの複合材料であるLSM/GDC、LSC単独、LSCとGDCの複合材料であるLSC/GDC等が挙げられる。また、電子伝導性とプロトン伝導性の両方を有するという点で、LSMとSrCe1−iYbiO3(iは、0≦i≦1)(以下、「SCYb」と略記する)の複合材料であるLSM/SCYb、LSCとSCYbの複合材料であるLSC/SCYb等が挙げられる。また、電子伝導性と酸化物イオン伝導性に加えてプロトン伝導性を有するという点で、LSCとGDCとSCYbの複合材料であるLSM/GDC/SCYb等が挙げられる。
【0073】
[膜厚]
アノード材料11bの膜厚は特に限定はないが、通常10μm〜5mmであり、好ましくは20μm〜1mm、より好ましくは30μm〜700μm、更に好ましくは40μm〜400μm、最も好ましくは50μm〜150μmである。膜厚は、触針タイプの表面粗さ計、又はSEMによる断面観察で測定してもよい。
【0074】
なお、ここで言及したアノード11(燃料極)の最適な厚さは、空孔度によって変わる。すなわち、空孔度はアノード11への気体の拡散のしやすさや、発生した一酸化炭素(CO)ガスの実効反応サイトへの移動しやすさに影響するため、空孔度が変わると厚さの最適条件は変わることがある。したがって、得られたアノード11の空孔度に合わせて適宜アノード11の膜厚は決定することが好ましい。
【0075】
[発電開始剤]
本発明の固体酸化物型電池の使用に際しては、発電開始剤導入時(以下、「発電開始剤導入工程」ということもある)と発電時(以下、「発電工程」ということもある)が少なくとも存在する。発電開始剤導入時には、アノード11に発電開始剤を供給することで発電を開始させることが、初期の発電特性が安定し易い点で好ましい。ここで、「発電開始剤」とは、一酸化炭素又は二酸化炭素をいう。発電開始剤導入工程においては、発電開始剤を供給し、一酸化炭素又は二酸化炭素を燃料室1の固体炭素2に接触させる。
【0076】
発電開始剤の導入手段として、例えば、図3、4、5に示したように、発電開始時に発電開始剤を供給する発電開始剤導入管13を設置することが好ましい。発電開始剤導入管13の先端は、発電開始剤がアノード11に到達すれば、どの位置に配置されていてもよいが、図3又は図4に示したように、燃料室1とアノード11の間に配置されていることが、発電開始剤をアノード11に迅速かつ確実に供給できる点で好ましい。
【0077】
[アノードの機構、構造、物性等]
発電時には(発電工程では)、燃料室1に供給した固体炭素2を使用し、少なくとも後記する反応式(1)及び反応式(2)により電子を発生させる。また同時に、カソード31では、酸化性ガスに電子を供与し、イオン化した酸化物イオン(O2−)を電解質21に注入する。
【0078】
本発明の固体酸化物型電池の大きさは特に限定はないが、1cm3〜500m3であることが好ましく、1000cm3〜50000cm3であることが特に好ましい。
【0079】
本発明の固体酸化物型電池の発電時の出力は特に限定はないが、0.001kW〜500kWが好ましく、0.01kW〜100kWであることが特に好ましく、0.01kW〜10kWであることが更に好ましい。本発明の固体酸化物型電池は、上記大きさの場合に上記出力を発生できる。
【0080】
アノード11のアノード集電体11aの構成材料は電子伝導性を有し、かつ固体酸化物型電池の作動温度領域において化学的及び物理的に安定であるものであればその形状及び構成材料は特に限定されず、公知の固体酸化物型燃料電池に備えられているものと同様のものを使用することができる。600℃〜1200℃で化学的及び物理的に安定であるものが好ましい。
【0081】
このアノード集電体11aは、燃料電池セル10を複数積層して使用する場合には、各単位セル間に配置されるセパレータとしての機能をも果たすものである。
【0082】
また、アノード11には、ガスの供給口(図示せず)及び放出口(図示せず)、並びに、これらの供給口と放出口とに接続されたガスの内部流路(図示せず)が設けられていてもよい。本発明の固体酸化物型電池は、一般の公知の燃料電池とは燃料の種類、使用方法、発電原理等は全く異なるが、ガスの供給口及び放出口並びにこれらの供給口と放出口とに接続されたガスの内部流路等の機械的外部構造については、一般の公知の燃料電池の構造と同様のものが使用できる。
【0083】
本発明の固体酸化物型電池では、発電時に、アノード11に対し反応生成ガスを外部に放出させるためのキャリアガスを実質的に導入しないことが好ましい。後述するように、キャリアガスを実質的に導入しないと、アノード11において反応式(1)で示される反応がより効率的に起こるので好ましい。またこれにより、発電時には装置構成をより極めてコンパクトにできる。
【0084】
<カソード>
発電時には、カソード31には、「酸化剤(例えば酸素)を含むガス」(例えば空気)が供給され、カソード材料31bは、酸化剤の還元反応が進行する反応場となるものである。カソード材料31bの組成や形状については特に限定されず、公知の固体酸化物型燃料電池に備えられているカソード31に一般に使用されているものと同様のものを使用することができる。例えば、(LaSr)MnO3系、(LaSr)CoO3系の複合金属酸化物からなる材料等を好ましく使用することができる。特に好ましくは、例えば、La0.85Sr0.15MnO3 等が挙げられる。
【0085】
カソード31のカソード集電体31aの構成は、先に述べたアノード11のアノード集電体11aと同様であり、構成材料及び形状については特に限定されず、公知の固体酸化物型燃料電池に備えられているものと同様のものを使用することができる。なお、カソード集電体31aには、空気等の酸化剤を含むガスをカソード材料31bに供給するためのガス流路(図示せず)が形成されている。また、このカソード集電体31aは、燃料電池セル10を複数積層して使用する場合には、各単位セル間に配置されるセパレータとしての機能をも果たすものである。
【0086】
<電解質>
電解質21は、イオン伝導性の固体酸化物を含む。電解質21は、酸化物イオン(O2−)の移動媒体であると同時に、還元剤(先に述べた固体炭素2)と酸化剤を含むガス(例えば空気)を直接接触させないための隔壁としても機能し、ガス不透過性の緻密な構造を有している。この電解質21の構成材料は特に限定されず、公知の固体酸化物型燃料電池に用いられる材料を使用することができるが、酸化物イオンの伝導性が高く、カソード31側の酸化性雰囲気からアノード11側の還元性雰囲気までの条件下で、化学的に安定で、熱衝撃に強い材料から構成することが好ましい。
【0087】
かかる要件を満たす材料としては、例えば、イットリア安定化ジルコニア(YSZ)、
スカンジア安定化ジルコニア(ScSZ)等の安定化ジルコニア;ランタンガレート;セリア系固溶体等が好ましいものとして挙げられる。
【0088】
安定化ジルコニアは特に限定はないが、下記一般式
(ZrO2)1−x(M2O3)x
[式中、MはY、Sc、Sm、Al、Nd、Gd、Yb及びCeからなる群より選ばれた1種以上の元素を示す。ただしここで、MがCeの場合はM2O3の代わりにCeO2である。]、又は、下記一般式
(ZrO2)1−x(MO)x
[式中、MはCa及びMgからなる群より選ばれた1種以上の元素を示す]における、xが0<x≦0.3である固溶体が好ましい。特に好ましいものとしては、例えば、(ZrO2)1−x(Y2O3)x(式中、0<x≦0.3)等が挙げられ、より好ましくは、式中、0.08≦x≦0.1である。また、更に好ましいものとしては(ZrO2)0.92(Y2O3)0.08等が挙げられる。
【0089】
なお、例えば「式中、Aは、Q、R及びTからなる群から選ばれた1種以上の元素を示す」という表現は、式中、AがQである固容体とAがRである固溶体の混合でもよいことを示すだけではなく、AとしてQとRとを同時に結晶サイトに有する固溶体をも示すものとする。以下、同様である。
【0090】
ランタンガレートは特に限定はないが、一般式、La1−xSrxGa1−y−zMgyAzO3(式中、AはCo、Fe、Ni又はCuの何れか1種以上の元素を示し、x=0.05〜0.3、y=0〜0.29、z=0.01〜0.3、y+z=0.025〜0.3の範囲である)で表される固溶体が好ましい。具体的には、La0.8Sr0.2Ga0.8Mg0.15Co0.05O3−δ(式中、δは酸素欠損量を示す)等が挙げられる。
【0091】
セリア系固溶体は特に限定はないが、Ce1−xMxO2(式中、MはGd、La、Y、Sc、Sm、Al、Pr、Nd、Ca、Mg、Sr、Ba、Dy、Yb、Tb、及び他の2価又は3価のランタノイドからなる群から選ばれた1種以上の元素を示す)における、xが0<x≦0.5である固溶体が好ましい。中でも、MがGdであるCe1−xGdxO2(式中、0<x≦0.5)、又は、MがSmであるCe1−xSmxO2(式中、0<x≦0.5)がより好ましく、何れの式においても、式中、0.03≦x≦0.4が特に好ましく、0.08≦x≦0.4が更に好ましく、0.1≦x≦0.4が最も好ましい。また、特に好ましいセリア系固溶体としては、Ce0.8Gd0.2O2−δ(式中、δは酸素欠損量を示す)、Ce0.67Gd0.33O2−δ(式中、δは酸素欠損量を示す)、Ce0.9Gd0.1O2−δ(式中、δは酸素欠損量を示す)等が挙げられる。特に、GDCを電解質21の材料として用いると、発電時の温度が750℃以下であっても、出力密度を充分大きくできるので好ましい。
【0092】
また、発電の際に、十分な出力特性を得る観点からは、かかる複合金属酸化物の導電率は、1000℃において、0.01〜10Scm−1であることが好ましい。
【0093】
<固体酸化物型電池の製造方法>
本発明の固体酸化物型電池の製造方法は特に限定されず、公知の固体酸化物燃料電池の製造に適用されている公知の薄膜製造技術等を使用することができる。例えば、スキージ法、スクリーンプリンティング法、真空蒸着法、スパッタ法、イオンプレーティング法等のPVD法、熱CVD法、プラズマCVD法、レーザーCVD法等のCVD法、溶射法等が挙げられる。
【0094】
例えば、電解質21を形成する方法としては、例えば、公知のセラミックプロセスであるシート成形焼結法を例示することができる。より具体的には、原料及び溶媒を混合することによって得たスラリーをシート状に延ばし、乾燥させた後に、必要に応じてカッターナイフ等を用いて成形し焼成する。スラリーには、必要に応じて、バインダー、可塑剤、分散剤等の公知の添加剤を配合させてもよい。成形、焼成等の条件は、原料の組成に応じて適宜設定することができる。また、先に述べたPVD法、CVD法、溶射法等の薄膜形成法により、例えば、アノード11又はカソード31上に電解質21の層を形成することもできる。
【0095】
<運転方法>
本発明の固体酸化物型電池の運転方法は、前記した一酸化炭素等の発電開始剤を燃料室1の固体炭素2に供給して電池反応を開始させる工程後、カソード31に空気等の酸化剤を含むガスを供給し、連続的に供給される固体炭素2を還元剤として発電する発電工程とを少なくとも含む方法であれば特に限定されない。通常、発電開始剤を導入して電池反応が開始され、固体炭素2が供給され続ける限り、連続的な運転が可能である。
【0096】
発電開始剤導入方法については、特に限定されるものではなく、燃料室1の固体炭素2へ極少量の一酸化炭素又は二酸化炭素を瞬間的に流せばよい。反応開始剤の流入量は、電池反応が開始するのに十分量であればよく特に限定されない。
【0097】
燃料として供給される固体炭素2は炭素を含有するものをいい、ここで「炭素」とは無定形炭素、グラファイト等の単体炭素をいう。固体炭素2は、具体的には特に限定はないが、天然黒鉛、人造黒鉛、カーボンブラック(ファーネスブラック、チャンネルブラック、アセチレンブラック、ランプブラック等)、グラファイトチョーク、フラーレン等の結晶性炭素;木炭、竹炭、墨等の動植物由来の炭素;煙突煤;コークス;排気ガスに含まれるPM中の炭素微粒子;等が挙げられる。
【0098】
固体炭素2の形態は、粉末、顆粒、ペレット、芯状等、何れの形態であってもよいが、固体炭素2の充填部をガスが透過する必要がある。ペレット、芯状等、バルクの場合は、バルク自体に多孔性を持たせる、あるいは貫通孔や溝を設ける等してガス流路を確保することが好ましい。
【0099】
また、固体炭素2の種類については、上記したように内燃機関等から排出される排気ガス中のPM等でも燃料として使用可能である。PM中の炭素微粒子が燃料である固体炭素2となる。すなわち、本発明の固体酸化物型電池においては、固体炭素2が排気ガス中の炭素微粒子であることも好ましい。
【0100】
固体炭素2中の炭素の含有率は、発電特性の観点からは高い方が良く、固体炭素2全体に対して50質量%以上であることが好ましく、70質量%以上であることがより好ましく、90質量%以上であることが特に好ましい。
【0101】
固体炭素2の供給方法については、上記形態の固体炭素2を直接的に燃料室1に格納すればよく、従来の公知文献2に記載されているような賦活工程が不要なため、非常に簡便である。また、PM浄化装置へ適用する場合は、排ガス中のPMを捕集して蓄積させる機構を固体酸化物型電池に併設することで、連続的に供給することができる。
【0102】
本発明の固体酸化物型電池の発電方法においては、発電開始直後、電流密度をその初期値から増加させながら運転させることが、安定した発電のために好ましい。発電開始直後、徐々に電流密度を上げることが、安定した発電のために特に好ましい。「徐々に電流密度を上げる」とは、通常、毎分当り0.008mA/cm2〜2mA/cm2で増加させることをいい、特に好ましくは、毎分当り0.016mA/cm2〜1mA/cm2である。かかる範囲を外れると、初期の発電特性が安定しない場合がある。
【0103】
以上、本発明の好適な実施形態について説明したが、本発明は上記実施形態に限定されるものではない。例えば、本発明の固体酸化物型電池は、例えば、図に示した固体酸化物型電池を複数積層した形態を有していてもよい。
【0104】
本発明においては、燃料室1中の固体炭素2を、発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電する。特に、発電時にアノード11において、少なくとも、下記の反応式(1)及び(2)を利用して発電を行う。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【0105】
反応式(1)を利用することで、アノード11の近傍に供給される固体炭素2を、気体のCOに変換して燃料として消費するので、発電時において固体炭素2の存在位置の影響を極めて小さくすることが可能になる。つまり、固体酸化物型電池では、一般的に電解質21の表面に近いところでの電極反応ほど発電への寄与が大きいので、電解質21の表面から遠いところに分布する固体炭素2は消費されにくい。そのため、反応式(1)で示される反応が起きない場合と比べて高い燃料利用率が得られ、アノード11から離れた位置に固体炭素2が供給されても発電が可能になる。
【0106】
加えて、反応式(2)によるCOの酸化反応は、下記反応式(3)又は反応式(4)による固体炭素2の酸化反応よりも反応速度が大きいため、高い出力密度が得られる。反応式(2)を支配的に起こすには、例えば、反応生成ガスによる圧力上昇分以上はアノード11外部に反応生成ガスを放出させないようにして、反応式(1)や反応式(3)で生成した一酸化炭素(CO)をアノード11に滞留する時間を長くすることや、系外から流入する酸素によって起こる一酸化炭素(CO)の酸化による消費を抑えること等が挙げられる。
C+O2− → CO+2e− (3)
C+2O2− → CO2+4e− (4)
【0107】
本発明の固体酸化物型電池の発電方法においては、反応式(2)で消費される一酸化炭素(CO)の50モル%以上が反応式(1)で生成されることが好ましい。すなわち、発電時に消費される一酸化炭素の50モル%以上が、固体炭素2と二酸化炭素との反応により生じた一酸化炭素であることが好ましい。特に好ましくは60モル%以上、更に好ましくは70モル%以上である。
【0108】
また、本発明の固体酸化物型電池の発電方法においては、電荷移動量の50%以上が、固体炭素2と二酸化炭素との反応により得られた一酸化炭素の酸化に起因することが好ましい。
【0109】
反応式(2)を支配的に起こす手段としては、反応式(1)や反応式(3)で生成したCOをアノード11に滞留する時間を長くさせることや、系外から流入する酸素によって起こるCOの酸化による消費を抑えるために、酸素の流入を遮断すること等が挙げられる。常法のようにアノード11にキャリアガスを流すと、反応式(2)は殆ど起こらない。
【0110】
アノード11において反応式(1)で示される反応を起こすためには、電極反応(2)及び/又は(4)で生成したCO2をアノード11中に長く滞留させることが大事であり、そのために発電時のキャリアガスの導入を無くすことが好ましい。キャリアガスの導入を無くすためには、系外からの空気つまりは酸素の漏れこみを、シール性能を向上する等して、極力少なくし、酸素分圧の上昇による電圧低下を防ぐことが好ましい。
【0111】
発電工程において、カソード31に供給する酸化剤を含むガスは、入手容易性から空気であることが好ましい。また、同様の観点から、酸化剤は酸素であることが好ましい。
【0112】
また、発電時における固体酸化物型電池の電荷移動量や出力密度を向上させる観点から、アノード11に、該アノード11における反応生成ガスを外部に放出させるためのキャリアガスを供給しないことが好ましい。
【0113】
本発明の固体酸化物型電池において、発電工程での温度は400〜1000℃が好ましく、450〜900℃がより好ましく、500〜750℃が特に好ましい。温度が低すぎると反応式(1)が進行しにくくなることや、セル(電極及び電解質)の抵抗が大きくなるために、出力密度が低下する場合がある。一方、高すぎると、セルや周辺部材の劣化が早まる場合がある。
【0114】
本発明の固体酸化物型電池は、発電時の温度750℃以下で、出力密度が50(mW/cm2)以上にすることができる。また、出力密度が50(mW/cm2)以上になるように、組成、構造、設定等が調整された固体酸化物型電池が好ましい。特に、電解質21としてGDCを用いることによって、発電時の温度が750℃以下であっても、出力密度を50(mW/cm2)以上にすることができる。
【0115】
また、本発明の固体酸化物型電池は、電流密度9.3mA/cm2で発電したときの燃料利用効率を60%以上にできる。また、燃料利用効率60%以上になるように、組成、構造、設定等が調整された固体酸化物型電池が好ましい。ここで「燃料利用効率」とは、アノード材料11b近傍に供給した固体炭素2中の炭素に対する、反応式(4)を仮定し電荷移動量から計算した消費炭素量の割合である。
【0116】
また、本発明の固体酸化物型電池は、電流密度80mA/cm2で発電したときの燃料利用効率を20%以上にできる。また、燃料利用効率20%以上になるように、組成、構造、設定等が調整された固体酸化物型電池が好ましい。特に好ましくは30%以上、更に好ましくは40%以上である。
【0117】
具体的には、上記したように、系外からの空気すなわち酸素の漏れこみを、シール性能を向上する等して極力少なくしたり、アノード11の大気への開口径を小さくしたりして大気からアノード11への酸素の流入を抑制して、反応式(1)及び/又は反応式(2)における一酸化炭素(CO)について損失を軽減することによって実現される。
【0118】
本発明の固体酸化物型電池の構造は特に限定されるものではなく、例えば、図13のように、平板状の電解質21の層の一方の面にアノード11、他方の面にカソード31を形成した構造を有し、セパレータを介して順次積層したスタックからなる平板型の固体酸化物型電池の構成を有しているものであってもよく、あるいは図8〜12のように、円筒状の支持管の円筒面上にカソード31、電解質21の層及びアノード11を順次形成し、積層させた構造を有する円筒型の固体酸化物型電池の構成を有しているものであってもよい。
【0119】
上記は本願発明を主として燃料電池として利用する際の最良の形態の一例を示したものであるが、本願発明は、二次電池、水素発生装置、排ガス除去等への応用、すなわち、電気化学リアクターとしての利用も可能であり、この場合も上記に準じて適宜実施可能である。
【実施例】
【0120】
以下、本発明を実施例により更に詳細に説明するが、本発明はこれら実施例に限定されるものではない。
【0121】
<実施例1>
電解質として、厚さ0.3mmのScSZ(10モル%のSc2O3と1モル%のCeO2がドープされたZrO2)ディスクを使用し、アノード材料には、Ni/GDC(GdがドープされたCeO2)多孔質サーメットを、カソード材料にはLa0.85Sr0.15MnO3多孔質膜を用いた。アノードの厚さは50μmであった。なお、構成と製造方法は、一般的な固体酸化物型燃料電池の構成と製造方法に従った。すなわち、アノード材料及びカソード材料の粉体を溶媒に分散し、有機バインダー等を添加してスラリーを調製した。次いで、当該スラリーをドクターブレード法でディスクに塗布し、焼成して固体酸化物型燃料電池を作成した。
【0122】
アノード材料への固体炭素の担持は以下の手順でおこなった。すなわち、カーボンブラック(三菱化学社製「MA7」)(以下、「CB」と略記する)をエタノールに分散させた溶液を調製し、このCB分散溶液をアノードに滴下、浸透させ、1.0mgのCBをアノードに担持させた。
【0123】
集電体を介して、アノードと反対側のスペース(燃料室)に28.3mgのCBを充填した。なお、燃料として用いた固体炭素であるCBの炭素含有率は96.5質量%〜100質量%(揮発成分3.5質量%含有)であった。このようにして、図2に示したような固体酸化物型電池を作製した。
【0124】
アノードに純アルゴン(Ar)を202STPmL/分で約1時間供給し、O2等の残留ガスを十分排気した。
【0125】
発電中はカソード側に純酸素を酸化剤として供給し、アノード側はアルゴン(Ar)ガスをフローしなかった。セルのシールを確実にし、アノードから3.5mの1/8インチステンレス管をつなぎ、ガスクロマトグラフ装置を挟んで5mのビニルチューブ(内径8mm)で外に排気することで、大気からの空気の逆拡散を抑制した。
【0126】
900℃で、電流をある一定電流密度に調整した場合の発電をおこない、それぞれの電量密度における端子電圧の経時変化をモニターした。その時の最大出力密度(mW/cm2)と電流密度(mA/cm2)を表1に示す。
【0127】
<実施例2>
アノードにCBを担持しないこと、及び燃料室へのCBの充填量が21.0mgであること以外は、実施例1と同様に固体酸化物型電池を作製し、900℃での電流変化時の発電特性を調べた。その時の電流密度(mA/cm2)と最大出力密度(mW/cm2)を表1に示す。
【0128】
【表1】

【0129】
表1より、実施例1、2ともに固体炭素を消費して発電していることが判った。例えば、表1に示すように、実施例1では電流が58.4mAの時に24.6mW/cm2の出力密度が得られ、実施例2では電流が33.0mAの時に20.3mW/cm2の出力密度が得られた。
【0130】
特に、実施例2のようにアノードに固体炭素を直接担持しなくても発電しており、このことは燃料室に充填、格納した固体炭素が消費されていることを意味している。すなわち、特許文献2に開示されている従来のような賦活工程を必要とすることなく、燃料室に固体炭素を供給しさえすれば連続的に燃料電池を運転することが可能となるため、実用性の高い発電方法が提供される。
【0131】
また、ディーゼル車等の内燃機関から排出されるPMのように、飛散してくる固体炭素に対しても、捕集した後に燃料室に供給する、あるいは直接燃料室でPMを捕集する仕組みさえ導入すれば、本発明の固体酸化物型電池の運転方法が適用できるため、有害物質であるPMを除去(消費)し、発電することが可能である。
【産業上の利用可能性】
【0132】
本発明は、従来のような賦活工程を必要とすることなく、燃料室に固体炭素を供給しさえすれば連続的に燃料電池を運転することが可能なため、より実用性の高い運転方法が提供でき、燃料電池応用分野に広く利用できるものである。また、この固体炭素を酸化させる作用を応用すれば、ディーゼルエンジン等の内燃機関から排出される排ガス中に含まれるPMの除去も可能であり、電気化学リアクター(電気化学的な反応場を提供する装置)としての利用も可能である。
【符号の説明】
【0133】
1 燃料室
2 固体炭素
3 二酸化炭素(CO2)排出口
10 燃料電池セル
11 アノード
11a アノード集電体
11b アノード材料
13 発電開始剤導入管
15 アノードに担持された固体炭素
21 電解質
22 外部制御回路
23 電気回路
31 カソード
31a カソード集電体
31b カソード材料
33 酸化剤を含むガス導入口
【特許請求の範囲】
【請求項1】
複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池における発電方法であって、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電することを特徴とする固体酸化物型電池の発電方法。
【請求項2】
上記アノードに固体炭素を担持させて用いる請求項1記載の固体酸化物型電池の発電方法。
【請求項3】
上記燃料室の固体炭素に一酸化炭素又は二酸化炭素を供給することで発電を開始させる請求項1又は請求項2に記載の固体酸化物型電池の発電方法。
【請求項4】
発電開始時に発電開始剤を供給するための発電開始剤導入管の先端が、燃料室とアノードの間に配置されている請求項3に記載の固体酸化物型電池の発電方法。
【請求項5】
発電開始直後、電流密度をその初期値から増加させながら運転させることを特徴とする請求項1ないし請求項4の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項6】
発電開始時に、アノードへ電気化学的に酸素源を注入することを特徴とする請求項1ないし請求項5の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項7】
発電時に下記反応式(1)及び(2)を利用して発電することを特徴とする請求項1ないし請求項6の何れか1項に記載の固体酸化物型電池の発電方法。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【請求項8】
上記固体炭素の炭素含有率が50質量%以上である請求項1ないし請求項7の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項9】
上記固体炭素が排気ガス中の炭素微粒子である請求項1ないし請求項8の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項10】
複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池。
【請求項11】
発電開始時に発電開始剤を供給するための発電開始剤導入管を有し、該発電開始剤導入管の先端が燃料室とアノードの間に配置されている請求項10に記載の固体酸化物型電池。
【請求項12】
発電時に下記反応式(1)及び(2)を利用して発電する請求項10又は請求項11に記載の固体酸化物型電池。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【請求項13】
請求項1ないし請求項9の何れか1項に記載の固体酸化物型電池の発電方法を使用して発電することを特徴とする固体酸化物型電池。
【請求項1】
複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池における発電方法であって、該燃料室中の固体炭素を発電によって発生した二酸化炭素と反応させて一酸化炭素に変換し、当該一酸化炭素を酸化することにより発電することを特徴とする固体酸化物型電池の発電方法。
【請求項2】
上記アノードに固体炭素を担持させて用いる請求項1記載の固体酸化物型電池の発電方法。
【請求項3】
上記燃料室の固体炭素に一酸化炭素又は二酸化炭素を供給することで発電を開始させる請求項1又は請求項2に記載の固体酸化物型電池の発電方法。
【請求項4】
発電開始時に発電開始剤を供給するための発電開始剤導入管の先端が、燃料室とアノードの間に配置されている請求項3に記載の固体酸化物型電池の発電方法。
【請求項5】
発電開始直後、電流密度をその初期値から増加させながら運転させることを特徴とする請求項1ないし請求項4の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項6】
発電開始時に、アノードへ電気化学的に酸素源を注入することを特徴とする請求項1ないし請求項5の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項7】
発電時に下記反応式(1)及び(2)を利用して発電することを特徴とする請求項1ないし請求項6の何れか1項に記載の固体酸化物型電池の発電方法。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【請求項8】
上記固体炭素の炭素含有率が50質量%以上である請求項1ないし請求項7の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項9】
上記固体炭素が排気ガス中の炭素微粒子である請求項1ないし請求項8の何れか1項に記載の固体酸化物型電池の発電方法。
【請求項10】
複合金属酸化物を含むアノード材料を有するアノード、カソード材料を有するカソード、アノードとカソードとの間に配置されたイオン伝導性の固体酸化物を含む電解質、発電の際に燃料として使用される固体炭素、及び該固体炭素が格納された燃料室を少なくとも有する固体酸化物型電池。
【請求項11】
発電開始時に発電開始剤を供給するための発電開始剤導入管を有し、該発電開始剤導入管の先端が燃料室とアノードの間に配置されている請求項10に記載の固体酸化物型電池。
【請求項12】
発電時に下記反応式(1)及び(2)を利用して発電する請求項10又は請求項11に記載の固体酸化物型電池。
CO2+C → 2CO (1)
CO+O2− → CO2+2e− (2)
【請求項13】
請求項1ないし請求項9の何れか1項に記載の固体酸化物型電池の発電方法を使用して発電することを特徴とする固体酸化物型電池。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2011−40285(P2011−40285A)
【公開日】平成23年2月24日(2011.2.24)
【国際特許分類】
【出願番号】特願2009−186932(P2009−186932)
【出願日】平成21年8月11日(2009.8.11)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【出願人】(000005968)三菱化学株式会社 (4,356)
【Fターム(参考)】
【公開日】平成23年2月24日(2011.2.24)
【国際特許分類】
【出願日】平成21年8月11日(2009.8.11)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【出願人】(000005968)三菱化学株式会社 (4,356)
【Fターム(参考)】
[ Back to top ]

