固形組織内の検体の光音響検出法及び検出システム
生体外でインタクトなリンパ節などの固形組織(12)内の検体を検出するために好ましいシステムは、完全にインタクトなリンパ節などの固形組織に向けてパルス状レーザービームを発生するために配置されたレーザー(22)を含む。このリンパ節内で生じた光音響信号を検出するために、音響検知器、好ましくは、少なくとも3つの音響検知器(20a,20b,20c)が、XYZ座標系などで三次元空間を測るために異なる位置に配置されている。少なくとも1つのコンピューター(28)が音響検知器からの信号を受け取る。コンピューターは、信号及び信号のタイミングから、検体の有無、好ましくは、検体の位置を決定する。生体外でリンパ節内の検体を検出するための好ましい方法は、抽出したリンパ節をパルス状レーザービームに被曝させることを含む。このとき、音響信号が検知される。音響信号は、リンパ節内の検体の有無を確認するため解析される。好ましくは、三次元空間を測る複数の検知器から複数の光音響信号が検知され、検体の位置も決定される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明の分野は、固形組織内での検体検出法及び組織解析システムである。本発明の好ましい用途は、インタクトなまま切除されたセンチネルリンパ節での黒色腫微小転移巣の生体外検出であり、本発明の好ましいシステムは、抽出したリンパ節において黒色腫微小転移巣の存在と位置との両方を検出できる光音響システムである。
【背景技術】
【0002】
センチネルリンパ節は、がん性腫瘍からリンパ系を介して移動してきた転移がん細胞が最初にたどり着くリンパ節群に由来するリンパ節である。センチネルリンパ節のマッピングは、センチネルリンパ節の典型的には染料注入による検出、及び、生検で転移がん細胞の有無を決定するための該センチネルリンパ節の切除を含む。リンパ節マッピング法は、皮膚黒色腫及びその他のがんの位置が特異的なリンパ節分布パターンを有しており、1つ以上のリンパ節があるリンパ節流域内の転移性疾患にまず関与するという理解に基づいている。もしこれらの最初のリンパ節又はセンチネルリンパ節が関与していないのであれば、流域全体は腫瘍がないはずである。この種の処置が、センチネルリンパ節マッピングにより検出することのできる2種のがん、悪性黒色腫及び乳がん、の診断及び治療に現在使用されている。転移性疾患の検出と監視は、これらのがん及び他の形態のがんの治療において正の臨床転帰を得るために不可欠である。所属リンパ節の状態を知ることは、予後診断のみならず、治療法を決定するためにも重要である。
【0003】
黒色腫は、皮膚がんの最も致命的な形態であり、全てのがん型の中で最も速い増殖率を有している。米国では、黒色腫を発症する生涯リスクは、55人中に1人であり、世界の他の国々では、その割合はさらに高い。黒色腫の早期の外科的切除が最善の治療手段である。一方、転移性疾患の検出と監視も、正の臨床転帰を得るために不可欠である。
【0004】
センチネルリンパ節マッピング技術の弱点は、抽出したセンチネルリンパ節が転移がん細胞を有しているか否かを決定するために生検を用いる点にある。このことは、センチネルリンパ節が僅かな数の微小転移巣細胞のみを有している可能性のある初期段階において、特に当てはまる。こうした細胞は、リンパ節のほんの僅かを占めるに過ぎないので、生検でリンパ節から切片を作成する場合には、検出が困難である。典型的な生検では、8から10の切片を採取するのみであるため、こうした微小転移巣細胞を検出できる可能性は極めて僅かである。リンパ節を部分的に検査するだけでは、高い偽陰性率が予期され得る。リンパ節が切除されると、典型的には、6から10個の約6μmの厚さの切片が採取され、転移がんの検査に用いられる。そのため、1cm長の典型的なリンパ節では、リンパ節のほんの僅かな部分(時として1%未満)のみが検査に供される。非現実的ではあるが、たとえ切片の数を大きく増やしたとしても、それでもまだ、微小転移巣細胞の検出は、大きく運に左右されるだろう。黒色腫マーカーの免疫組織化学的染色は感度をさらに高めるものの、それでもまだ、相応の割合の生検で、たとえ最良の手法を用いた場合でも、偽陰性が検出される可能性が高い。数々の研究によれば、センチネルリンパ節の偽陰性率は10%を超えることが判明している。非特許文献1及び非特許文献2を参照のこと。
【0005】
センチネルリンパ節及び転移がんの検出を改善するためにさまざまな努力がなされてきた。例えば、センチネルリンパ節の生検で黒色腫前駆細胞を検出するため逆転写ポリメラーゼ連鎖反応(RTーPCR)が用いられてきた。しかし、臨床検査におけるRT−PCRの有用性は明らかではない。非特許文献3を参照のこと。Wang等は、センチネルリンパ節で黒色腫や乳がんを検出するために超音波変調光学的断層撮影法を使用することを提唱している。しかし、この技術は、微小転移巣を検出できない可能性が高い(非特許文献4)。また、関連する生体内の技術ではセンチネルリンパ節の位置の特定が行われる。Wang等は、生体内でセンチネルリンパ節の位置を特定するために非侵襲的光音響同定システムを介した非侵襲的な技術を使用することを提唱している。しかし、この技術は、メチレンブルーを注入した後にセンチネルリンパ節に集積したメチレンブルーを検出することにより、生体内のセンチネルリンパ節の位置を同定するものである。非特許文献5を参照のこと。Wang等の方法では、原発性腫瘍を切除した後の組織にメチレンブルーを注入しセンチネルリンパ節を同定する。この染料は、腫瘍を吸い込み且つセンチネルリンパ節(Sentinel Lymph Node;SLN)につながるリンパ管により吸い上げられる。この青色染料は光音響の対象として用いられ、この染料を検出することで腋窩を切り進まずとも細針吸引を用いて生検を得ることが可能となる。この技術は、潜在的には、SLN検査の侵襲性を減少し得る。染料検出感度を試験するために、生体外の検査が行われた。この技術は、生体内でSLNを見つけるために外因性の染料を用いるため、抽出したリンパ節での微小転移巣の位置の特定には適合しない。また、この染料はSLNを非選択的に着色する。さらに、センチネルリンパ節での転移がんの検出するために超音波を用いる別の試みでも、61%もの偽陽性率が示された(非特許文献6)。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】Jansen,L.,Nieweg,O.,Peterse,J.,Hoefnagel,C,Olmos,R.,Kroon,B.,“Reliability of Sentinel Lymph Node Biopsy for Staging Melanoma”,Br.J.Surg.,2000年,第87巻,484−489頁
【非特許文献2】Yu,L.,Flotte,T.,Tanabe,K.,Gadd,M.,Cosimi,A.,Sober,A.,Mihm,M.,Jr.,Duncan,L.,“Detection of Microscopic Melanoma Metastasesin Sentinel Lymph Nodes”,Cancer,1999年,第86巻,617−627頁
【非特許文献3】Hauschild,A.,Christophers,E.,“Sentinel Node Biopsy in Melanoma”,Virchows Arch.,2001年,第438号,99−106頁
【非特許文献4】Wang,et al.,“Sentinel Lymph Node Detection ex vivo Using Ultrasound−Modulated Optical Tomography”,J.Biomed.Opt.,2008年,第13巻
【非特許文献5】Wang et al.,“Noninvasive Photoacoustic Identification of Sentinel Lymph Nodes Containing Methylene Blue in vivo in a Rat Model”,Journal of Biomedical Optics,2008年9/10月,第13巻,第5号,054033頁
【非特許文献6】Rossi et al.,“The Role of Preoperative Ultrasound Scan in Detecting Lymph Node Metastasis Before Sentinel Node Biopsy in Melanoma Patients”,J.Surg.Oncol.,第83巻,80−84頁
【発明の概要】
【0007】
生体外でインタクトなリンパ節などの固形組織内の検体を検出するために好ましいシステムは、完全にインタクトなリンパ節などの固形組織に向けてパルス状レーザービームを発生するために配置されたレーザーを含む。このリンパ節内で生じた光音響信号を検出するために、音響検知器、好ましくは、少なくとも3つの音響検知器が、XYZ座標系などで三次元空間を測るために異なる位置に配置されている。少なくとも1つのコンピューターが音響検知器からの信号を受け取る。コンピューターは、信号及び信号のタイミングから、検体の有無、好ましくは、検体の位置を決定する。
【0008】
生体外でリンパ節内の検体を検出するための好ましい方法は、抽出したリンパ節をパルス状レーザービームに被曝させることを含む。このとき、音響信号が検知される。音響信号は、リンパ節内の検体の有無を確認するため解析される。好ましくは、三次元空間を測る複数の検知器から複数の光音響信号が検知され、検体の位置も決定される。
【図面の簡単な説明】
【0009】
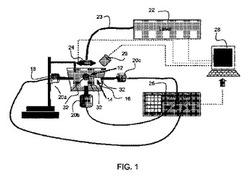
【図1】固形組織内の検体を検出するための光音響検出システムの好ましい実施形態を示す模式図。
【図2A】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節から得られた光音響応答のプロット図。
【図2B】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節から得られた光音響応答のプロット図。
【図2C】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節から得られた光音響応答のプロット図。
【図2D】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節にメラニン細胞を注入した後の光音響応答を示すプロット図。
【図2E】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節にメラニン細胞を注入した後の光音響応答を示すプロット図。
【図2F】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節にメラニン細胞を注入した後の光音響応答を示すプロット図。
【図3】図1に係る3つの検知器を用いた実験系におけるブタリンパ節検査の信号強度のプロット図。
【発明を実施するための形態】
【0010】
本発明は、センチネルリンパ節などの抽出した固形組織内の検体の光音響検出のための方法及びシステムを提供する。本発明の方法及びシステムでは、リンパ節内の微小検体の検出及び位置の特定が可能となる。光吸収体である任意の検体を固形組織内で検出することができる。しかし、本発明の方法及びシステムは、リンパ節内の微小転移巣の存在及び位置を検出するために特に有用である。本発明の方法及びシステムでは、例えば、従来のセンチネルリンパ節生検の代替又は補助として、抽出したセンチネルリンパ節内の微小転移巣の有無を検出し、三次元空間における位置を特定することができる。
【0011】
生体外でインタクトなリンパ節などの固形組織内の検体を検出するために好ましいシステムは、完全にインタクトなリンパ節などの固形組織に向けてパルス状レーザービームを発生するために配置されたレーザーを含む。このリンパ節内で生じた光音響信号を検出するために、音響検知器、好ましくは、少なくとも3つの音響検知器が、XYZ座標系などで三次元空間を測るために異なる位置に配置されている。少なくとも1つのコンピューターが音響検知器からの信号を受け取る。コンピューターは、信号及び信号のタイミングから、検体の有無、好ましくは、検体の位置を決定する。
【0012】
生体外でリンパ節内の検体を検出するための方法は、抽出したリンパ節をパルス状レーザービームに被曝させることを含む。このとき、音響信号が検知される。音響信号は、リンパ節内の検体の有無を確認するため解析される。好ましくは、三次元空間を測る複数の検知器から複数の光音響信号が検出され、検体の位置も決定される。本発明の好ましい方法及びシステムでは、抽出したリンパ節を音響媒体中に配置し、その後、音響媒体からの光音響応答を検知する。好ましい音響媒体は脱イオン水である。音響媒体として、ゲル、及び、油、例えば、ミネラルオイルを用いてもよい。空気も同様に音響媒体ではあるものの、液体、ゲル、及び、油などの媒体が好ましい。別の実施形態では、リンパ節は空気中に(ピンや他の支持手段により)つるされ、そして、光音響変換器がリンパ節そのものに、好ましくは、音響調節ゲルを用いて、物理的に接触している。
【0013】
本発明の好ましい実施形態のシステム及び方法では、抽出したリンパ節の黒色腫微小転移巣を検出する。この場合、検体は微小転移巣そのものである。これらの本発明の好ましい方法及びシステムでは、黒色腫特有の光吸収特性を用いてSLNを切除した後転移がんを見つける。黒色腫細胞の光吸収特性が検出に必要な光音響応答を生成するために用いられる。これにより、黒色腫微小転移の検出のための極めて強力な技術が提供される。
【0014】
別の好ましい実施形態では、他種のがん細胞を検出することができる。乳がん又は他種のがん細胞を、別の実施形態では、検出することができる。この場合、外因性の吸収体が導入される。外因性の吸収体は、対象のがん細胞に特異的に誘引されるものである。外因性の吸収体の例としては、がん細胞に対する既知の抗原(ある種の乳がんではHER−2、また、エストロゲン陽性乳がん細胞ではエストロゲン受容体など)に官能化されるナノ粒子などが挙げられる。こうしたナノ粒子は、金、銀、又は、他種のナノ粒子であってもよい。また、官能化される量子ドット又はマイクロスフィアを用いてもよい。対象のがん細胞を特異的に染色する組織化学的染料を、がん細胞を特異的に対象とし吸収体として機能し得る別種の外因性受容器として用いることもできる。
【0015】
以下、本発明の好ましい実施形態について、図面を参照しながら説明する。図面は模式図を含むかもしれないが、これら模式図の意味するところは、当業者であれば周知技術と以下の記載を参考に理解できるだろう。強調のため図面では特徴が誇張されているかもしれないし、また、特徴は縮尺通りではないかもしれない。以下では実験系について論ずるが、当業者であればこれら実験系及び試験結果からより上位概念化された本発明の特徴を理解できるだろう。
【0016】
図1は、生体外でインタクトなリンパ節などの固形組織内の検体を検出するための例示的システム10を示す。インタクトなリンパ節12又はインタクトなリンパ節の要部の形態の固形組織が、試料保持器16内に収容された音響媒体14内に所定のサンプルボリューム位置で配置されている。試料保持器は、外部の機械的振動を隔離することができるスタンド18によりつるされている。ただし、通常であれば、検知信号が数十メガヘルツの範囲であるため、振動は計測結果に影響を与えないだろう。
【0017】
インタクトなリンパ節12内で生じた音響信号を検知するため、音響検知器20a,20b及び20cがXYZ座標系内の3箇所の異なる位置に配置されている。この好ましいシステムは、検体の有無と位置との両方の決定を可能とするために独立した信号を発生するよう3つの検知器20a,20b,20cを有しているが、光吸収性の検体の有無を検出するのであれば1つの信号検知器のみで十分である。好ましい音響検知器は圧電検知器である。圧電式以外の検知器としては、例えば、試料内又はリンパ節を囲むキャリア流体内の光学的振動を測定する検出器などが挙げられる。
【0018】
光音響信号はレーザー22により発生されたパルス状レーザービームにより誘起される。レーザーのビームは、光ファイバー23を介して伝達され、そして、リンパ節12を向くようレンズ24によりコリメートされてもよい。コリメーションは好ましいが必須ではない。コリメーションは、望ましい高レーザー強度(laser fluence)を維持するための役には立つものの、光ファイバーから十分に収束されたビームが提供されるため不可欠ではない。ある実施形態では、レンズ24はリンパ節12の全体を網羅するビームを形成する。別の実施形態では、レンズ24は、リンパ節12全体を『イメージング』するようなパターンで走査される細く収束されたビームを形成する。細く収束されたビームを走査する場合、リンパ節12及びリンパ節12に存在する微小転移巣を通過する光子の伝播が増加する。しかし、いずれの実施形態でも、効果的に、XYZ座標系などの三次元空間におけるリンパ節12内の微小転移巣の位置を特定することができる。走査することで、レーザー光が微小転移巣に近接するリンパ節の不透明な媒質内に進入することが可能となり、光音響応答が増加する。走査型マイクロモーター25は、コリメーションレンズ24を動かすことで、試料リンパ節12とレーザービームとの間の相対的移動を生じることができる。該走査型マイクロモーター25は、コンピューター28により制御してもよい。全リンパ節12を走査パターンで照射するためにファイバーレンズが走査されるが、リンパ節を平行移動させたりレーザービームを操縦するなど他の方法で走査を実行してもよい。レーザー22に付随させた光検知器をコンピューター28及び波形検知器26をトリガーするために用いてもよい。微小転移巣は、波形分析器26により検知されコンピューター28により解析される異なる音波により明らかとなる。例えばXYZ座標系などで三次元空間を測るよう特徴的な位置に配置されている3つの検知器20a,20b及び20cを用いて、コンピューター28は検知器20a,20b及び20cのそれぞれが受け取った音波のタイミングによりリンパ節12内の微小転移巣の位置を決定することができる。3つの検知器20a,20b及び20cは直交するべきだが、同一直線上に配置されるのでなければ、検体の位置を決定するために逆投影法を用いてもよい。特に、検知器20a,20b及び20cの向きにより決定される3つのベクトルが三次元空間を測る限り、逆投影の計算を行うことで十分な情報を得ることができるだろう。検知器とリンパ節との間の距離は、多くの場合、重要ではないが、距離を長くし過ぎると装置が大きくなるため結合流体の不要な粘弾性減衰を招く虞がある。普通、検知器20a,20b及び20cとリンパ節12との間の距離は約1cm以下であることが好ましい。
【0019】
コンピューター28は、検知器20a,20b及び20cの位置と、リンパ節及び該リンパ節を囲む音響媒体14内を信号が移動する速度とを知っており、これにより、リンパ節内の黒色腫の位置を決定することが可能となる。コンピューター28は、検体に関する位置情報の自動的な走査及び出力又は蓄積を実行することができる。出力又は蓄積された情報は、例えば、リンパ節を三次元にマップし検体の位置を示すようなマップの形態をとってもよい。こうした光音響情報は、検体の位置のマップ、例えば、検出された黒色腫のマップを用意するために用いられてもよい。この情報は、リンパ節内の黒色腫の位置を示すために、例えばカメラ又は他種の光学的検知器29による標準的な撮像などにより得られたリンパ節の画像に重ね合わせてもよい。
【0020】
3つより多くの検知器を用いてもよく、例を挙げれば、5個,7個,10個,さらには、12個などがありうる。リンパ節に対する検知器の相対的位置、及び、信号がそれぞれの検知器により検出される相対的時間を知ることは有用である。第1及び第2の検知器での信号の受信の間に相対的な差を定められるように、全ての検知器を共通の時間的尺度上に配置してもよい。普通、検知器の数を多くすると、黒色腫の位置を推定する際の精度が高くなる。しかし、また、検知器の数を多くすると、複雑さや費用も嵩むようになる虞がある。また、多くの用途では、黒色腫の位置を推定する際の精度は、3個,4個,5個,6個,又は、7個より多くの検知器を必要とするほど高くはないかもしれない。
【0021】
試料保持器16は、液性の音響媒体14を収容するよう構成された検査室であり得、また、さまざまな形状を有し得る。音響媒体14は、それ自身が吸収体として機能しないよう、用いられるレーザー波長に対して透明であるべきである。多くのレーザー波長について適切な媒体の例として、食塩水が挙げられる。好ましくは、音響媒体は、検査対象の組織と実質的に同一の音響インピーダンスを有する。試料保持器は、透明であってもよいし、又は、レーザービームを受け入れるための透明部を有してもよい。リンパ節は、検知器の検出結果が該リンパ節の位置と相関し得るように、試料保持器内の既知の位置に配置されるべきである。好ましい実施形態では、用いられるレーザー波長に対して透明なピン32又は他種の要素を、リンパ節を挿すために又は保持するために、用いることができる。ピンは、リンパ節を所定の位置に保持することに加えて、三次元空間上の位置基準を設けることができる。試料保持器16は、好ましくは、この検査室に対するリンパ節の相対的位置を知るための他の目印を含む。三次元空間での既知の位置(例えば、X、Y及びZ軸)を定めるために、試料保持器内の座標系のマーキングは有用であり得る。こうしたマーキングは、リンパ節を後で精密に切り分けるために、既知の位置に対するリンパ節内の検出検体の推定位置の座標を獲得できるので有用であり得る。試料保持器の座標系に対する検知器20a,20b及び20cの相対位置は、コンピューター28に提供される。本システムは、好ましくは、リンパ節12及び目印を撮像するカメラ又は他の形態の光学的検知器29を含む。この画像を用いることで、コンピューターは、光音響信号から生成された検体位置のマップと組み合わせることができるようなリンパ節の三次元マップを生成することができる。別の実施形態では、本システムは、リンパ節12を光音響的に撮像するためにレーザー22とは異なる波長を用いることができる。例えば、用いられる波長はリンパ節内の水分を吸収される対象とすることができるだろう。この場合、音響媒体は水であってはならず、適切なゲル又は油を用いることができるだろう。
【0022】
リンパ節の位置を測る目印として働き得るマーキングの例としては、リンパ節を配置する際の相対位置の基準となり得、且つ、三次元のXYZ座標系及び位置を定めるために有用であり得るような第1及び第2の平面に沿って配置されたグリッド又は他の基準のマーキング又は指標要素が挙げられる。指標要素の他の例としては、ピン、支柱、若しくは、試料保持器の床面から垂直に伸びた他の構造的要素、マーキングを付された垂直の壁面若しくは隆起部、側壁から試料保持器内に水平に伸びる支柱若しくはピン、又は、リンパ節を配置する際の試料保持器内での三次元の相対位置の基準となり得るような他の物理的指標要素などが挙げられる。レーザー光を吸収しないため、ナイロンピンが一例として挙げられる。光を吸収しない素材、例を挙げればポリマーなど、からなる他の保持要素を用いることもできる。ピン32のそれぞれが座標を定めてもよいし、又は、検知器20a,20b,20cがX,Y及びZ座標をなすように複数のピン32が用いられてもよい。
【0023】
検知器20a,20b,20cは、試料保持器の側壁、床面、天上に沿って配置されてもよく、また、そうでなければ、流体の圧力波を検出するために、キャリア流体と流体接触して配置されてもよい。また、光線の偏向を介して光音響的事象を検出する他種の検知器を用いてもよい。このとき、流体接触は不要である。これらは、検査資料保持器の外側に配置してもよい。
【0024】
あるシステムは、黒色腫の推定位置でリンパ節を精密に切り分けるための第2のステーションを含んでもよい。これは、リンパ節を高度に精密に切り分けることがリンパ節内の黒色腫の特定の位置でのみ可能であった先行技術に対して、顕著に有利である。これにより、労力及び費用の著しい節約が達成される。
【0025】
図1に係る実験系を構築し試験を行った。以下に論ずる実験は本発明の好ましいシステム及び方法のさらなる特徴を明らかにするものであるが、当業者であれば、本発明に基づく商業的システムを、性能、小型性、及び、従来の最適化などの利点を得るために特別に加工した部品を用いて構築できることを理解するだろう。実験及び好ましい実施形態は黒色腫の検出に向けられているが、当業者であれば、光電子エネルギーの吸収体である他のリンパ節及び他の検体も本発明の方法及びシステムにより解析できることを理解するだろう。
【実施例】
【0026】
(実験系及びデータ)
本実験では、僅か500個程度の黒色腫細胞を有するリンパ節からの光音響応答を正確に検出し、リンパ節の三次元空間内におけるリンパ節内でのこれら細胞の位置を決定することができるようにするため、複数の検知器により情報を獲得した。正常なリンパ節は応答を示さなかった。このように、本発明の検出方法及びシステムは、完全にインタクトなリンパ節内の微小転移巣の存在を検出するために用いることができる。また、リンパ節のさらなる組織学的観察の指針として用いることもでき、これにより、センチネルリンパ節生検の精度は向上する。今回の観察では偽陽性又は偽陰性の結果は観察されなかった。
【0027】
大部分の黒色腫は全く黒色で、メラニン欠乏黒色腫の推計は5%未満又は1.8〜8.1%であった。なお、後者の値は、部分的に色素を有する黒色腫を含むものである。このように、黒色腫の極めて大部分は、光音響発生及び検出に活用できる天然の光吸収体を含んでいる。光音響効果は、光子の光エネルギーが機械的撹乱に変換され音波が生じる際に起きる。
【0028】
(実験に用いた検出システム)
周波数三倍化QスイッチNd:YAGレーザー(Vibrant355II、Opotek製、米国カルフォルニア州カールズバッド)を光学パラメーター式発振器をパンプするために用いた。このシステムは、410−2400nmの波長範囲を有していた。実験では、このシステムを、532nmの波長に設定し、図1に示すようにリンパ節を照射するため、直径600μmの光ファイバーを用いて焦点を合わせた。レーザーエネルギーは4−6mJの範囲であり、レーザーパルス持続時間は5n秒であった。レーザーシステムの繰り返し率は10Hzであった。リンパ節内で生じた光音響信号は、ポリフッ化ビニリデン(Polyvinylidene Fluoride;PVDF)のフィルム(Ketech社、米国ニューメキシコ州アルバカーキ)から作られた3つの圧電音響検知器により受信された。この信号は、レーザー出力を監視する光ダイオード(DETIOA、Thorlabs製、米国ニュージャージー州ニュートン)によりトリガーされたオシロスコープ(TDS024、Tektronix製、米国オレゴン州ウィルソンヴィル)に送信された。光ファイバーは、リンパ節上約1cmに配置された。音響検知器は、リンパ節に対して直角に、各検知器のリンパ節表面から最も近い所での位置が1−3mmの間となるよう、配置された。光音響波の時間と組織内での音速(約1.5mm/μs)との積を求めることにより、それぞれの波形から、より正確な位置を推定することができる。変換器は、約10cm長の半剛体の同軸ケーブル(Micor−coax製、米国ペンシルベニア州ポットタウン)のセグメントから作られた。PVDFと同軸ケーブルとから音響検知器を作成する手順は、J.Viator等,“Clinical Testing of a Photoacoustic Probe for Port Wine Stain Depth Determination”,2002年,第30巻,141−148頁に記載されている。本実験では、外部導体の直径は3.6mm、内部導体の直径は0.9mmであり、両導体は誘電体により絶縁された。25μm厚のPVDFフィルムは同軸ケーブルの露出研磨面に取り付けられた。
【0029】
<リンパ節の準備及び試験>
イヌのリンパ節を、該リンパ節の周囲の結合組織及びその他の組織から分離し、その後、リンパ節内部又は周囲の血液を取り除くため脱イオン水中に一晩浸けた。このリンパ節はライマメの形状をしており約1cmの長さであった。リンパ節全体を音響媒体内に配置した。音響媒体は脱イオン水槽であった。これにより、検知器までの音波伝達が保証された。532nmの波長を直径600μmの光ファイバーを通してリンパ節の上面に向けた。検知信号は350MHzの計装用増幅器(SR445、Stanford Research Systems製、米国カリフォルニア州サニーベール)を用いて5倍に増幅され、その後、平均を128回取った。10Hzのレーザー繰り返し率で、128回の平均をとるのに12.8秒かかった。
【0030】
<大きな黒色腫塊を注入したイヌリンパ節>
本システムの黒色腫を検出する能力を試験するため、リンパ節に黒色腫細胞を注入した。ヒト悪性黒色腫細胞系列HS936を培養したものを黒色腫細胞源として用いた。黒色腫がペレットを形成するまで、高濃度黒色腫懸濁液を遠心機にかけた。上澄みを取り除き、高濃度の黒色腫をピペットにより吸い上げた。黒色腫細胞の総数は約1x106であった。この細胞塊の直径は約1mmであった。リンパ節に照射したレーザースポットの直径は約1.5mmであった。レーザービームをリンパ節全体に照射するよう走査した。1.5mmのスポットはリンパ節のより広い区域に拡散するが、リンパ節全体に照射するためにレーザービームの走査を用いた。微小転移巣を模倣するため、リンパ節の側面に小さな切開部を設け、黒色腫をピペットを用いてその切開部に注入した。黒色腫を移植しない対照リンパ節においても、切開部の形成を含む試験を繰り返した。
【0031】
<小さな黒色腫塊を注入したブタリンパ節>
かなり少ない数の黒色腫細胞から球体を形成した。上述した遠心からこの手順は異なる。具体的には、黒色腫細胞はアクリルアミド溶液内に懸濁物として集められた。このアクリルアミド溶液は、過硫酸アンモニウム及びテトラメチルエチレンジアミン(Tetramethylethylenediamine;TEMED)(共に米国ミズーリ州セントルイス所在のSigma Aldrich製)を用いて、直径約1mmの球体に凝固された。浮遊細胞を含有する重合開始前のアクリルアミド溶液をミネラルオイル中に滴下すると、過硫酸アンモニウム及びTEMEDにより1分以内に硬化し、球体が形成された。この技術により形成された球体のそれぞれは、約500個の黒色腫細胞を含有しており、健康なブタのリンパ節に移植された。健康なブタ由来のリンパ節はイヌのリンパ節と同程度の大きさと形状であった。『陽性』のリンパ節にそれぞれ黒色腫細胞を移植した。
【0032】
測定では、検知信号をより高倍率で増幅した(125倍)。光ファイバーは、リンパ節の上約1mmに配置され、直径約600μmのスポットが形成された。このようにして、ブタのリンパ節表面でのレーザー強度はイヌのリンパ節表面での強度の約6倍となった。
【0033】
<結果と考察>
図2A−2Cは、イヌリンパ節への照射後黒色腫細胞の注入前に得られた3つの検知器のそれぞれからの光音響波形を示す。図2D−2Fは、黒色腫細胞の注入後の検知器のそれぞれからの波形を示す。1μ秒以内に生じる最初の波形はレーザーからの電気的ノイズによるものである。黒色腫細胞を添加していないリンパ節では、図2A−2Cから分かるように、光音響信号は見られない。信号は、約100μVのベースラインのノイズ値の平坦な直線を示すのみである。黒色腫細胞が存在するリンパ節では、図2D−2Fから分かるように、かなりの光音響信号が見られる。検出器1では、図2Dから分かるように、約0.5mVのピーク振幅のピークを有する約9μ秒の信号が生じた。検出器2では、図2Eから分かるように、約0.4mVの振幅で約4.5μ秒の信号が生じた。検出器3では、図2Fから分かるように、約0.6mVの振幅で約4.2μ秒の信号が生じた。検出器3からの波長は音波回折のため逆転している。しかし、検出のために必要なのは波の存在のみであり、また、位置の決定に必要なのは波のタイミングのみであって、波の形状は問題とならない。
【0034】
ブタのリンパ節からの信号強度を図3に示す。それぞれのリンパ節の信号は8回の測定の平均である。黒色腫を移植しなかった対照リンパ節は、図3に示した対照波形と同様の信号を示した。ブタのリンパ節からの結果は、ナノ秒の持続期間のレーザー光を照射された際に、少数の黒色腫細胞が光音響信号を発生することを明確に示した。ブタのリンパ節には、約500個の黒色腫細胞があった。こうした微小転移巣の直径は、細胞の平均直径を約20μmとしたとき、約100−200μmであった。こうした数の細胞が、染色切片を顕微鏡で観察して初めて見つかるような微小塊を構成する。このような微小転移巣は、1cm長のリンパ節の組織切片上では容易に見過ごされてしまう可能性がある。強く明瞭な信号は、より少ない数の細胞でも検出可能であることを示している。
【0035】
(正確な位置特定のための光音響逆投影法)
リンパ節内の微小転移巣の特定の位置を決定するための技術の1つとして、光音響逆投影法が挙げられる。この方法は、組織学的検査の指針として用いることが可能であり、これにより、偽陽性の画面を減らすことができる。逆投影法による再構築を用いることで、転移がんの位置を特定しリンパ節内のその位置を決定することができ、これにより、組織学的検査のために検出確率が最も高い組織切片を選択することが可能となる。逆投影法は、異なる位置を用いて信号を三角測量するのと類似した数学的方法である。さらに、フィルター処理及びノイズ除去処理を行なってもよい。適切な逆投影法は、『Iterative Reconstruction Algorithm for Optoacoustic Imaging』,J.Acoust.Soc.Am.,2002年10月,第112巻,第4号,1536−1544頁に開示されている。
【0036】
(検出感度の最適化)
本実験では、偽陽性率は観察されなかった。しかし、実際的には、リンパ節のリンスが不完全であるため、リンパ節内に血液が残存している可能性があった。血液の寄与による不要な光音響応答を避けるために、レーザー波長を、赤色、例えば、630nmに変更してもよく、これにより、脱酸素化ヘモグロビン由来の光音響応答は約8分の1に、酸素化ヘモグロビン由来の応答は約50分の1未満に減少する。一方、メラニン由来の応答は約2分の1程度にしか減少しないだろう。このようにして、ノイズを制限しつつ、感度は改善される。
【0037】
別の選択肢として、2つの波長を用い、この2つの波長の相対感度を解析することが考えられる。例えば、532nm及び630nmの波長への応答を取得し、光音響波をヘモグロビン又はメラニン由来のものに分類することができる。凝固した血液と未変性のヘモグロビンとを熱的に区別するために、統計的分類法が用いられてきた。Viator等,“Photoacoustic Discrimination of Viable and Thermally Coagulated Blood Using a Two− Wavelength Method for Burn Injury Monitoring”,Phys.Med.Biol.,2007年,第52巻,1815−1829頁を参照のこと。血液とメラニンとを区別するために、同様に、2つの波長の使用を用いてもよい。メラニンが単純な吸収スペクトルを示すのに対して、ヘモグロビンは特徴的な吸収スペクトルを示すため、このような分類が可能となる。
【0038】
上記の実験では、イヌのリンパ節と比較してブタリンパ節の実験条件では検出が増幅されることが示された。両実験条件には、増幅倍率が5倍に対して125倍であった点、及び、組織表面に光ファイバーをより近接して配置することでレーザー強度が増加していた点で差があった。さらに、ブタリンパ節用に作られた検知器は、音波への感度が数倍高かった。ブタ用の検知器は、基本構成こそイヌ用の検知器と同様であったものの、より感度良く構築された。こうした改善の結果、感度はおよそ3桁も増加した。
【0039】
信号対ノイズ比を増加するために、ウェーブレットノイズ除去及び検出中の走査を用いてもよい。適切なノイズ除去法及び走査法は、Viator等,“Automated Wavelet Denoising of Photoacoustic Signals for Circulating Melanoma Cell Detection and Burn Image Reconstruction”,Phys.Med.Biol.,2008年5月21日,N227−N236頁に記載されている。
【0040】
本願発明の具体的な実施形態を示し記載してきたが、当業者であれば、他の変形例、置換例、及び、代替例が容易であることを理解するだろう。こうした変形例、置換例、及び、代替例は、添付の請求項に定められた本発明の精神と範囲を超えずになすことができる。本発明のさまざまな特徴が添付の請求項において規定する。
【0041】
(関連出願の相互参照)
本願は、合衆国法典第35巻第119条に基づき、2009年4月20日に出願の米国特許仮出願第61/170,880号の優先権を主張する。
【技術分野】
【0001】
本発明の分野は、固形組織内での検体検出法及び組織解析システムである。本発明の好ましい用途は、インタクトなまま切除されたセンチネルリンパ節での黒色腫微小転移巣の生体外検出であり、本発明の好ましいシステムは、抽出したリンパ節において黒色腫微小転移巣の存在と位置との両方を検出できる光音響システムである。
【背景技術】
【0002】
センチネルリンパ節は、がん性腫瘍からリンパ系を介して移動してきた転移がん細胞が最初にたどり着くリンパ節群に由来するリンパ節である。センチネルリンパ節のマッピングは、センチネルリンパ節の典型的には染料注入による検出、及び、生検で転移がん細胞の有無を決定するための該センチネルリンパ節の切除を含む。リンパ節マッピング法は、皮膚黒色腫及びその他のがんの位置が特異的なリンパ節分布パターンを有しており、1つ以上のリンパ節があるリンパ節流域内の転移性疾患にまず関与するという理解に基づいている。もしこれらの最初のリンパ節又はセンチネルリンパ節が関与していないのであれば、流域全体は腫瘍がないはずである。この種の処置が、センチネルリンパ節マッピングにより検出することのできる2種のがん、悪性黒色腫及び乳がん、の診断及び治療に現在使用されている。転移性疾患の検出と監視は、これらのがん及び他の形態のがんの治療において正の臨床転帰を得るために不可欠である。所属リンパ節の状態を知ることは、予後診断のみならず、治療法を決定するためにも重要である。
【0003】
黒色腫は、皮膚がんの最も致命的な形態であり、全てのがん型の中で最も速い増殖率を有している。米国では、黒色腫を発症する生涯リスクは、55人中に1人であり、世界の他の国々では、その割合はさらに高い。黒色腫の早期の外科的切除が最善の治療手段である。一方、転移性疾患の検出と監視も、正の臨床転帰を得るために不可欠である。
【0004】
センチネルリンパ節マッピング技術の弱点は、抽出したセンチネルリンパ節が転移がん細胞を有しているか否かを決定するために生検を用いる点にある。このことは、センチネルリンパ節が僅かな数の微小転移巣細胞のみを有している可能性のある初期段階において、特に当てはまる。こうした細胞は、リンパ節のほんの僅かを占めるに過ぎないので、生検でリンパ節から切片を作成する場合には、検出が困難である。典型的な生検では、8から10の切片を採取するのみであるため、こうした微小転移巣細胞を検出できる可能性は極めて僅かである。リンパ節を部分的に検査するだけでは、高い偽陰性率が予期され得る。リンパ節が切除されると、典型的には、6から10個の約6μmの厚さの切片が採取され、転移がんの検査に用いられる。そのため、1cm長の典型的なリンパ節では、リンパ節のほんの僅かな部分(時として1%未満)のみが検査に供される。非現実的ではあるが、たとえ切片の数を大きく増やしたとしても、それでもまだ、微小転移巣細胞の検出は、大きく運に左右されるだろう。黒色腫マーカーの免疫組織化学的染色は感度をさらに高めるものの、それでもまだ、相応の割合の生検で、たとえ最良の手法を用いた場合でも、偽陰性が検出される可能性が高い。数々の研究によれば、センチネルリンパ節の偽陰性率は10%を超えることが判明している。非特許文献1及び非特許文献2を参照のこと。
【0005】
センチネルリンパ節及び転移がんの検出を改善するためにさまざまな努力がなされてきた。例えば、センチネルリンパ節の生検で黒色腫前駆細胞を検出するため逆転写ポリメラーゼ連鎖反応(RTーPCR)が用いられてきた。しかし、臨床検査におけるRT−PCRの有用性は明らかではない。非特許文献3を参照のこと。Wang等は、センチネルリンパ節で黒色腫や乳がんを検出するために超音波変調光学的断層撮影法を使用することを提唱している。しかし、この技術は、微小転移巣を検出できない可能性が高い(非特許文献4)。また、関連する生体内の技術ではセンチネルリンパ節の位置の特定が行われる。Wang等は、生体内でセンチネルリンパ節の位置を特定するために非侵襲的光音響同定システムを介した非侵襲的な技術を使用することを提唱している。しかし、この技術は、メチレンブルーを注入した後にセンチネルリンパ節に集積したメチレンブルーを検出することにより、生体内のセンチネルリンパ節の位置を同定するものである。非特許文献5を参照のこと。Wang等の方法では、原発性腫瘍を切除した後の組織にメチレンブルーを注入しセンチネルリンパ節を同定する。この染料は、腫瘍を吸い込み且つセンチネルリンパ節(Sentinel Lymph Node;SLN)につながるリンパ管により吸い上げられる。この青色染料は光音響の対象として用いられ、この染料を検出することで腋窩を切り進まずとも細針吸引を用いて生検を得ることが可能となる。この技術は、潜在的には、SLN検査の侵襲性を減少し得る。染料検出感度を試験するために、生体外の検査が行われた。この技術は、生体内でSLNを見つけるために外因性の染料を用いるため、抽出したリンパ節での微小転移巣の位置の特定には適合しない。また、この染料はSLNを非選択的に着色する。さらに、センチネルリンパ節での転移がんの検出するために超音波を用いる別の試みでも、61%もの偽陽性率が示された(非特許文献6)。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】Jansen,L.,Nieweg,O.,Peterse,J.,Hoefnagel,C,Olmos,R.,Kroon,B.,“Reliability of Sentinel Lymph Node Biopsy for Staging Melanoma”,Br.J.Surg.,2000年,第87巻,484−489頁
【非特許文献2】Yu,L.,Flotte,T.,Tanabe,K.,Gadd,M.,Cosimi,A.,Sober,A.,Mihm,M.,Jr.,Duncan,L.,“Detection of Microscopic Melanoma Metastasesin Sentinel Lymph Nodes”,Cancer,1999年,第86巻,617−627頁
【非特許文献3】Hauschild,A.,Christophers,E.,“Sentinel Node Biopsy in Melanoma”,Virchows Arch.,2001年,第438号,99−106頁
【非特許文献4】Wang,et al.,“Sentinel Lymph Node Detection ex vivo Using Ultrasound−Modulated Optical Tomography”,J.Biomed.Opt.,2008年,第13巻
【非特許文献5】Wang et al.,“Noninvasive Photoacoustic Identification of Sentinel Lymph Nodes Containing Methylene Blue in vivo in a Rat Model”,Journal of Biomedical Optics,2008年9/10月,第13巻,第5号,054033頁
【非特許文献6】Rossi et al.,“The Role of Preoperative Ultrasound Scan in Detecting Lymph Node Metastasis Before Sentinel Node Biopsy in Melanoma Patients”,J.Surg.Oncol.,第83巻,80−84頁
【発明の概要】
【0007】
生体外でインタクトなリンパ節などの固形組織内の検体を検出するために好ましいシステムは、完全にインタクトなリンパ節などの固形組織に向けてパルス状レーザービームを発生するために配置されたレーザーを含む。このリンパ節内で生じた光音響信号を検出するために、音響検知器、好ましくは、少なくとも3つの音響検知器が、XYZ座標系などで三次元空間を測るために異なる位置に配置されている。少なくとも1つのコンピューターが音響検知器からの信号を受け取る。コンピューターは、信号及び信号のタイミングから、検体の有無、好ましくは、検体の位置を決定する。
【0008】
生体外でリンパ節内の検体を検出するための好ましい方法は、抽出したリンパ節をパルス状レーザービームに被曝させることを含む。このとき、音響信号が検知される。音響信号は、リンパ節内の検体の有無を確認するため解析される。好ましくは、三次元空間を測る複数の検知器から複数の光音響信号が検知され、検体の位置も決定される。
【図面の簡単な説明】
【0009】
【図1】固形組織内の検体を検出するための光音響検出システムの好ましい実施形態を示す模式図。
【図2A】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節から得られた光音響応答のプロット図。
【図2B】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節から得られた光音響応答のプロット図。
【図2C】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節から得られた光音響応答のプロット図。
【図2D】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節にメラニン細胞を注入した後の光音響応答を示すプロット図。
【図2E】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節にメラニン細胞を注入した後の光音響応答を示すプロット図。
【図2F】図1に係る3つの検知器を用いた実験系における健康なイヌのリンパ節にメラニン細胞を注入した後の光音響応答を示すプロット図。
【図3】図1に係る3つの検知器を用いた実験系におけるブタリンパ節検査の信号強度のプロット図。
【発明を実施するための形態】
【0010】
本発明は、センチネルリンパ節などの抽出した固形組織内の検体の光音響検出のための方法及びシステムを提供する。本発明の方法及びシステムでは、リンパ節内の微小検体の検出及び位置の特定が可能となる。光吸収体である任意の検体を固形組織内で検出することができる。しかし、本発明の方法及びシステムは、リンパ節内の微小転移巣の存在及び位置を検出するために特に有用である。本発明の方法及びシステムでは、例えば、従来のセンチネルリンパ節生検の代替又は補助として、抽出したセンチネルリンパ節内の微小転移巣の有無を検出し、三次元空間における位置を特定することができる。
【0011】
生体外でインタクトなリンパ節などの固形組織内の検体を検出するために好ましいシステムは、完全にインタクトなリンパ節などの固形組織に向けてパルス状レーザービームを発生するために配置されたレーザーを含む。このリンパ節内で生じた光音響信号を検出するために、音響検知器、好ましくは、少なくとも3つの音響検知器が、XYZ座標系などで三次元空間を測るために異なる位置に配置されている。少なくとも1つのコンピューターが音響検知器からの信号を受け取る。コンピューターは、信号及び信号のタイミングから、検体の有無、好ましくは、検体の位置を決定する。
【0012】
生体外でリンパ節内の検体を検出するための方法は、抽出したリンパ節をパルス状レーザービームに被曝させることを含む。このとき、音響信号が検知される。音響信号は、リンパ節内の検体の有無を確認するため解析される。好ましくは、三次元空間を測る複数の検知器から複数の光音響信号が検出され、検体の位置も決定される。本発明の好ましい方法及びシステムでは、抽出したリンパ節を音響媒体中に配置し、その後、音響媒体からの光音響応答を検知する。好ましい音響媒体は脱イオン水である。音響媒体として、ゲル、及び、油、例えば、ミネラルオイルを用いてもよい。空気も同様に音響媒体ではあるものの、液体、ゲル、及び、油などの媒体が好ましい。別の実施形態では、リンパ節は空気中に(ピンや他の支持手段により)つるされ、そして、光音響変換器がリンパ節そのものに、好ましくは、音響調節ゲルを用いて、物理的に接触している。
【0013】
本発明の好ましい実施形態のシステム及び方法では、抽出したリンパ節の黒色腫微小転移巣を検出する。この場合、検体は微小転移巣そのものである。これらの本発明の好ましい方法及びシステムでは、黒色腫特有の光吸収特性を用いてSLNを切除した後転移がんを見つける。黒色腫細胞の光吸収特性が検出に必要な光音響応答を生成するために用いられる。これにより、黒色腫微小転移の検出のための極めて強力な技術が提供される。
【0014】
別の好ましい実施形態では、他種のがん細胞を検出することができる。乳がん又は他種のがん細胞を、別の実施形態では、検出することができる。この場合、外因性の吸収体が導入される。外因性の吸収体は、対象のがん細胞に特異的に誘引されるものである。外因性の吸収体の例としては、がん細胞に対する既知の抗原(ある種の乳がんではHER−2、また、エストロゲン陽性乳がん細胞ではエストロゲン受容体など)に官能化されるナノ粒子などが挙げられる。こうしたナノ粒子は、金、銀、又は、他種のナノ粒子であってもよい。また、官能化される量子ドット又はマイクロスフィアを用いてもよい。対象のがん細胞を特異的に染色する組織化学的染料を、がん細胞を特異的に対象とし吸収体として機能し得る別種の外因性受容器として用いることもできる。
【0015】
以下、本発明の好ましい実施形態について、図面を参照しながら説明する。図面は模式図を含むかもしれないが、これら模式図の意味するところは、当業者であれば周知技術と以下の記載を参考に理解できるだろう。強調のため図面では特徴が誇張されているかもしれないし、また、特徴は縮尺通りではないかもしれない。以下では実験系について論ずるが、当業者であればこれら実験系及び試験結果からより上位概念化された本発明の特徴を理解できるだろう。
【0016】
図1は、生体外でインタクトなリンパ節などの固形組織内の検体を検出するための例示的システム10を示す。インタクトなリンパ節12又はインタクトなリンパ節の要部の形態の固形組織が、試料保持器16内に収容された音響媒体14内に所定のサンプルボリューム位置で配置されている。試料保持器は、外部の機械的振動を隔離することができるスタンド18によりつるされている。ただし、通常であれば、検知信号が数十メガヘルツの範囲であるため、振動は計測結果に影響を与えないだろう。
【0017】
インタクトなリンパ節12内で生じた音響信号を検知するため、音響検知器20a,20b及び20cがXYZ座標系内の3箇所の異なる位置に配置されている。この好ましいシステムは、検体の有無と位置との両方の決定を可能とするために独立した信号を発生するよう3つの検知器20a,20b,20cを有しているが、光吸収性の検体の有無を検出するのであれば1つの信号検知器のみで十分である。好ましい音響検知器は圧電検知器である。圧電式以外の検知器としては、例えば、試料内又はリンパ節を囲むキャリア流体内の光学的振動を測定する検出器などが挙げられる。
【0018】
光音響信号はレーザー22により発生されたパルス状レーザービームにより誘起される。レーザーのビームは、光ファイバー23を介して伝達され、そして、リンパ節12を向くようレンズ24によりコリメートされてもよい。コリメーションは好ましいが必須ではない。コリメーションは、望ましい高レーザー強度(laser fluence)を維持するための役には立つものの、光ファイバーから十分に収束されたビームが提供されるため不可欠ではない。ある実施形態では、レンズ24はリンパ節12の全体を網羅するビームを形成する。別の実施形態では、レンズ24は、リンパ節12全体を『イメージング』するようなパターンで走査される細く収束されたビームを形成する。細く収束されたビームを走査する場合、リンパ節12及びリンパ節12に存在する微小転移巣を通過する光子の伝播が増加する。しかし、いずれの実施形態でも、効果的に、XYZ座標系などの三次元空間におけるリンパ節12内の微小転移巣の位置を特定することができる。走査することで、レーザー光が微小転移巣に近接するリンパ節の不透明な媒質内に進入することが可能となり、光音響応答が増加する。走査型マイクロモーター25は、コリメーションレンズ24を動かすことで、試料リンパ節12とレーザービームとの間の相対的移動を生じることができる。該走査型マイクロモーター25は、コンピューター28により制御してもよい。全リンパ節12を走査パターンで照射するためにファイバーレンズが走査されるが、リンパ節を平行移動させたりレーザービームを操縦するなど他の方法で走査を実行してもよい。レーザー22に付随させた光検知器をコンピューター28及び波形検知器26をトリガーするために用いてもよい。微小転移巣は、波形分析器26により検知されコンピューター28により解析される異なる音波により明らかとなる。例えばXYZ座標系などで三次元空間を測るよう特徴的な位置に配置されている3つの検知器20a,20b及び20cを用いて、コンピューター28は検知器20a,20b及び20cのそれぞれが受け取った音波のタイミングによりリンパ節12内の微小転移巣の位置を決定することができる。3つの検知器20a,20b及び20cは直交するべきだが、同一直線上に配置されるのでなければ、検体の位置を決定するために逆投影法を用いてもよい。特に、検知器20a,20b及び20cの向きにより決定される3つのベクトルが三次元空間を測る限り、逆投影の計算を行うことで十分な情報を得ることができるだろう。検知器とリンパ節との間の距離は、多くの場合、重要ではないが、距離を長くし過ぎると装置が大きくなるため結合流体の不要な粘弾性減衰を招く虞がある。普通、検知器20a,20b及び20cとリンパ節12との間の距離は約1cm以下であることが好ましい。
【0019】
コンピューター28は、検知器20a,20b及び20cの位置と、リンパ節及び該リンパ節を囲む音響媒体14内を信号が移動する速度とを知っており、これにより、リンパ節内の黒色腫の位置を決定することが可能となる。コンピューター28は、検体に関する位置情報の自動的な走査及び出力又は蓄積を実行することができる。出力又は蓄積された情報は、例えば、リンパ節を三次元にマップし検体の位置を示すようなマップの形態をとってもよい。こうした光音響情報は、検体の位置のマップ、例えば、検出された黒色腫のマップを用意するために用いられてもよい。この情報は、リンパ節内の黒色腫の位置を示すために、例えばカメラ又は他種の光学的検知器29による標準的な撮像などにより得られたリンパ節の画像に重ね合わせてもよい。
【0020】
3つより多くの検知器を用いてもよく、例を挙げれば、5個,7個,10個,さらには、12個などがありうる。リンパ節に対する検知器の相対的位置、及び、信号がそれぞれの検知器により検出される相対的時間を知ることは有用である。第1及び第2の検知器での信号の受信の間に相対的な差を定められるように、全ての検知器を共通の時間的尺度上に配置してもよい。普通、検知器の数を多くすると、黒色腫の位置を推定する際の精度が高くなる。しかし、また、検知器の数を多くすると、複雑さや費用も嵩むようになる虞がある。また、多くの用途では、黒色腫の位置を推定する際の精度は、3個,4個,5個,6個,又は、7個より多くの検知器を必要とするほど高くはないかもしれない。
【0021】
試料保持器16は、液性の音響媒体14を収容するよう構成された検査室であり得、また、さまざまな形状を有し得る。音響媒体14は、それ自身が吸収体として機能しないよう、用いられるレーザー波長に対して透明であるべきである。多くのレーザー波長について適切な媒体の例として、食塩水が挙げられる。好ましくは、音響媒体は、検査対象の組織と実質的に同一の音響インピーダンスを有する。試料保持器は、透明であってもよいし、又は、レーザービームを受け入れるための透明部を有してもよい。リンパ節は、検知器の検出結果が該リンパ節の位置と相関し得るように、試料保持器内の既知の位置に配置されるべきである。好ましい実施形態では、用いられるレーザー波長に対して透明なピン32又は他種の要素を、リンパ節を挿すために又は保持するために、用いることができる。ピンは、リンパ節を所定の位置に保持することに加えて、三次元空間上の位置基準を設けることができる。試料保持器16は、好ましくは、この検査室に対するリンパ節の相対的位置を知るための他の目印を含む。三次元空間での既知の位置(例えば、X、Y及びZ軸)を定めるために、試料保持器内の座標系のマーキングは有用であり得る。こうしたマーキングは、リンパ節を後で精密に切り分けるために、既知の位置に対するリンパ節内の検出検体の推定位置の座標を獲得できるので有用であり得る。試料保持器の座標系に対する検知器20a,20b及び20cの相対位置は、コンピューター28に提供される。本システムは、好ましくは、リンパ節12及び目印を撮像するカメラ又は他の形態の光学的検知器29を含む。この画像を用いることで、コンピューターは、光音響信号から生成された検体位置のマップと組み合わせることができるようなリンパ節の三次元マップを生成することができる。別の実施形態では、本システムは、リンパ節12を光音響的に撮像するためにレーザー22とは異なる波長を用いることができる。例えば、用いられる波長はリンパ節内の水分を吸収される対象とすることができるだろう。この場合、音響媒体は水であってはならず、適切なゲル又は油を用いることができるだろう。
【0022】
リンパ節の位置を測る目印として働き得るマーキングの例としては、リンパ節を配置する際の相対位置の基準となり得、且つ、三次元のXYZ座標系及び位置を定めるために有用であり得るような第1及び第2の平面に沿って配置されたグリッド又は他の基準のマーキング又は指標要素が挙げられる。指標要素の他の例としては、ピン、支柱、若しくは、試料保持器の床面から垂直に伸びた他の構造的要素、マーキングを付された垂直の壁面若しくは隆起部、側壁から試料保持器内に水平に伸びる支柱若しくはピン、又は、リンパ節を配置する際の試料保持器内での三次元の相対位置の基準となり得るような他の物理的指標要素などが挙げられる。レーザー光を吸収しないため、ナイロンピンが一例として挙げられる。光を吸収しない素材、例を挙げればポリマーなど、からなる他の保持要素を用いることもできる。ピン32のそれぞれが座標を定めてもよいし、又は、検知器20a,20b,20cがX,Y及びZ座標をなすように複数のピン32が用いられてもよい。
【0023】
検知器20a,20b,20cは、試料保持器の側壁、床面、天上に沿って配置されてもよく、また、そうでなければ、流体の圧力波を検出するために、キャリア流体と流体接触して配置されてもよい。また、光線の偏向を介して光音響的事象を検出する他種の検知器を用いてもよい。このとき、流体接触は不要である。これらは、検査資料保持器の外側に配置してもよい。
【0024】
あるシステムは、黒色腫の推定位置でリンパ節を精密に切り分けるための第2のステーションを含んでもよい。これは、リンパ節を高度に精密に切り分けることがリンパ節内の黒色腫の特定の位置でのみ可能であった先行技術に対して、顕著に有利である。これにより、労力及び費用の著しい節約が達成される。
【0025】
図1に係る実験系を構築し試験を行った。以下に論ずる実験は本発明の好ましいシステム及び方法のさらなる特徴を明らかにするものであるが、当業者であれば、本発明に基づく商業的システムを、性能、小型性、及び、従来の最適化などの利点を得るために特別に加工した部品を用いて構築できることを理解するだろう。実験及び好ましい実施形態は黒色腫の検出に向けられているが、当業者であれば、光電子エネルギーの吸収体である他のリンパ節及び他の検体も本発明の方法及びシステムにより解析できることを理解するだろう。
【実施例】
【0026】
(実験系及びデータ)
本実験では、僅か500個程度の黒色腫細胞を有するリンパ節からの光音響応答を正確に検出し、リンパ節の三次元空間内におけるリンパ節内でのこれら細胞の位置を決定することができるようにするため、複数の検知器により情報を獲得した。正常なリンパ節は応答を示さなかった。このように、本発明の検出方法及びシステムは、完全にインタクトなリンパ節内の微小転移巣の存在を検出するために用いることができる。また、リンパ節のさらなる組織学的観察の指針として用いることもでき、これにより、センチネルリンパ節生検の精度は向上する。今回の観察では偽陽性又は偽陰性の結果は観察されなかった。
【0027】
大部分の黒色腫は全く黒色で、メラニン欠乏黒色腫の推計は5%未満又は1.8〜8.1%であった。なお、後者の値は、部分的に色素を有する黒色腫を含むものである。このように、黒色腫の極めて大部分は、光音響発生及び検出に活用できる天然の光吸収体を含んでいる。光音響効果は、光子の光エネルギーが機械的撹乱に変換され音波が生じる際に起きる。
【0028】
(実験に用いた検出システム)
周波数三倍化QスイッチNd:YAGレーザー(Vibrant355II、Opotek製、米国カルフォルニア州カールズバッド)を光学パラメーター式発振器をパンプするために用いた。このシステムは、410−2400nmの波長範囲を有していた。実験では、このシステムを、532nmの波長に設定し、図1に示すようにリンパ節を照射するため、直径600μmの光ファイバーを用いて焦点を合わせた。レーザーエネルギーは4−6mJの範囲であり、レーザーパルス持続時間は5n秒であった。レーザーシステムの繰り返し率は10Hzであった。リンパ節内で生じた光音響信号は、ポリフッ化ビニリデン(Polyvinylidene Fluoride;PVDF)のフィルム(Ketech社、米国ニューメキシコ州アルバカーキ)から作られた3つの圧電音響検知器により受信された。この信号は、レーザー出力を監視する光ダイオード(DETIOA、Thorlabs製、米国ニュージャージー州ニュートン)によりトリガーされたオシロスコープ(TDS024、Tektronix製、米国オレゴン州ウィルソンヴィル)に送信された。光ファイバーは、リンパ節上約1cmに配置された。音響検知器は、リンパ節に対して直角に、各検知器のリンパ節表面から最も近い所での位置が1−3mmの間となるよう、配置された。光音響波の時間と組織内での音速(約1.5mm/μs)との積を求めることにより、それぞれの波形から、より正確な位置を推定することができる。変換器は、約10cm長の半剛体の同軸ケーブル(Micor−coax製、米国ペンシルベニア州ポットタウン)のセグメントから作られた。PVDFと同軸ケーブルとから音響検知器を作成する手順は、J.Viator等,“Clinical Testing of a Photoacoustic Probe for Port Wine Stain Depth Determination”,2002年,第30巻,141−148頁に記載されている。本実験では、外部導体の直径は3.6mm、内部導体の直径は0.9mmであり、両導体は誘電体により絶縁された。25μm厚のPVDFフィルムは同軸ケーブルの露出研磨面に取り付けられた。
【0029】
<リンパ節の準備及び試験>
イヌのリンパ節を、該リンパ節の周囲の結合組織及びその他の組織から分離し、その後、リンパ節内部又は周囲の血液を取り除くため脱イオン水中に一晩浸けた。このリンパ節はライマメの形状をしており約1cmの長さであった。リンパ節全体を音響媒体内に配置した。音響媒体は脱イオン水槽であった。これにより、検知器までの音波伝達が保証された。532nmの波長を直径600μmの光ファイバーを通してリンパ節の上面に向けた。検知信号は350MHzの計装用増幅器(SR445、Stanford Research Systems製、米国カリフォルニア州サニーベール)を用いて5倍に増幅され、その後、平均を128回取った。10Hzのレーザー繰り返し率で、128回の平均をとるのに12.8秒かかった。
【0030】
<大きな黒色腫塊を注入したイヌリンパ節>
本システムの黒色腫を検出する能力を試験するため、リンパ節に黒色腫細胞を注入した。ヒト悪性黒色腫細胞系列HS936を培養したものを黒色腫細胞源として用いた。黒色腫がペレットを形成するまで、高濃度黒色腫懸濁液を遠心機にかけた。上澄みを取り除き、高濃度の黒色腫をピペットにより吸い上げた。黒色腫細胞の総数は約1x106であった。この細胞塊の直径は約1mmであった。リンパ節に照射したレーザースポットの直径は約1.5mmであった。レーザービームをリンパ節全体に照射するよう走査した。1.5mmのスポットはリンパ節のより広い区域に拡散するが、リンパ節全体に照射するためにレーザービームの走査を用いた。微小転移巣を模倣するため、リンパ節の側面に小さな切開部を設け、黒色腫をピペットを用いてその切開部に注入した。黒色腫を移植しない対照リンパ節においても、切開部の形成を含む試験を繰り返した。
【0031】
<小さな黒色腫塊を注入したブタリンパ節>
かなり少ない数の黒色腫細胞から球体を形成した。上述した遠心からこの手順は異なる。具体的には、黒色腫細胞はアクリルアミド溶液内に懸濁物として集められた。このアクリルアミド溶液は、過硫酸アンモニウム及びテトラメチルエチレンジアミン(Tetramethylethylenediamine;TEMED)(共に米国ミズーリ州セントルイス所在のSigma Aldrich製)を用いて、直径約1mmの球体に凝固された。浮遊細胞を含有する重合開始前のアクリルアミド溶液をミネラルオイル中に滴下すると、過硫酸アンモニウム及びTEMEDにより1分以内に硬化し、球体が形成された。この技術により形成された球体のそれぞれは、約500個の黒色腫細胞を含有しており、健康なブタのリンパ節に移植された。健康なブタ由来のリンパ節はイヌのリンパ節と同程度の大きさと形状であった。『陽性』のリンパ節にそれぞれ黒色腫細胞を移植した。
【0032】
測定では、検知信号をより高倍率で増幅した(125倍)。光ファイバーは、リンパ節の上約1mmに配置され、直径約600μmのスポットが形成された。このようにして、ブタのリンパ節表面でのレーザー強度はイヌのリンパ節表面での強度の約6倍となった。
【0033】
<結果と考察>
図2A−2Cは、イヌリンパ節への照射後黒色腫細胞の注入前に得られた3つの検知器のそれぞれからの光音響波形を示す。図2D−2Fは、黒色腫細胞の注入後の検知器のそれぞれからの波形を示す。1μ秒以内に生じる最初の波形はレーザーからの電気的ノイズによるものである。黒色腫細胞を添加していないリンパ節では、図2A−2Cから分かるように、光音響信号は見られない。信号は、約100μVのベースラインのノイズ値の平坦な直線を示すのみである。黒色腫細胞が存在するリンパ節では、図2D−2Fから分かるように、かなりの光音響信号が見られる。検出器1では、図2Dから分かるように、約0.5mVのピーク振幅のピークを有する約9μ秒の信号が生じた。検出器2では、図2Eから分かるように、約0.4mVの振幅で約4.5μ秒の信号が生じた。検出器3では、図2Fから分かるように、約0.6mVの振幅で約4.2μ秒の信号が生じた。検出器3からの波長は音波回折のため逆転している。しかし、検出のために必要なのは波の存在のみであり、また、位置の決定に必要なのは波のタイミングのみであって、波の形状は問題とならない。
【0034】
ブタのリンパ節からの信号強度を図3に示す。それぞれのリンパ節の信号は8回の測定の平均である。黒色腫を移植しなかった対照リンパ節は、図3に示した対照波形と同様の信号を示した。ブタのリンパ節からの結果は、ナノ秒の持続期間のレーザー光を照射された際に、少数の黒色腫細胞が光音響信号を発生することを明確に示した。ブタのリンパ節には、約500個の黒色腫細胞があった。こうした微小転移巣の直径は、細胞の平均直径を約20μmとしたとき、約100−200μmであった。こうした数の細胞が、染色切片を顕微鏡で観察して初めて見つかるような微小塊を構成する。このような微小転移巣は、1cm長のリンパ節の組織切片上では容易に見過ごされてしまう可能性がある。強く明瞭な信号は、より少ない数の細胞でも検出可能であることを示している。
【0035】
(正確な位置特定のための光音響逆投影法)
リンパ節内の微小転移巣の特定の位置を決定するための技術の1つとして、光音響逆投影法が挙げられる。この方法は、組織学的検査の指針として用いることが可能であり、これにより、偽陽性の画面を減らすことができる。逆投影法による再構築を用いることで、転移がんの位置を特定しリンパ節内のその位置を決定することができ、これにより、組織学的検査のために検出確率が最も高い組織切片を選択することが可能となる。逆投影法は、異なる位置を用いて信号を三角測量するのと類似した数学的方法である。さらに、フィルター処理及びノイズ除去処理を行なってもよい。適切な逆投影法は、『Iterative Reconstruction Algorithm for Optoacoustic Imaging』,J.Acoust.Soc.Am.,2002年10月,第112巻,第4号,1536−1544頁に開示されている。
【0036】
(検出感度の最適化)
本実験では、偽陽性率は観察されなかった。しかし、実際的には、リンパ節のリンスが不完全であるため、リンパ節内に血液が残存している可能性があった。血液の寄与による不要な光音響応答を避けるために、レーザー波長を、赤色、例えば、630nmに変更してもよく、これにより、脱酸素化ヘモグロビン由来の光音響応答は約8分の1に、酸素化ヘモグロビン由来の応答は約50分の1未満に減少する。一方、メラニン由来の応答は約2分の1程度にしか減少しないだろう。このようにして、ノイズを制限しつつ、感度は改善される。
【0037】
別の選択肢として、2つの波長を用い、この2つの波長の相対感度を解析することが考えられる。例えば、532nm及び630nmの波長への応答を取得し、光音響波をヘモグロビン又はメラニン由来のものに分類することができる。凝固した血液と未変性のヘモグロビンとを熱的に区別するために、統計的分類法が用いられてきた。Viator等,“Photoacoustic Discrimination of Viable and Thermally Coagulated Blood Using a Two− Wavelength Method for Burn Injury Monitoring”,Phys.Med.Biol.,2007年,第52巻,1815−1829頁を参照のこと。血液とメラニンとを区別するために、同様に、2つの波長の使用を用いてもよい。メラニンが単純な吸収スペクトルを示すのに対して、ヘモグロビンは特徴的な吸収スペクトルを示すため、このような分類が可能となる。
【0038】
上記の実験では、イヌのリンパ節と比較してブタリンパ節の実験条件では検出が増幅されることが示された。両実験条件には、増幅倍率が5倍に対して125倍であった点、及び、組織表面に光ファイバーをより近接して配置することでレーザー強度が増加していた点で差があった。さらに、ブタリンパ節用に作られた検知器は、音波への感度が数倍高かった。ブタ用の検知器は、基本構成こそイヌ用の検知器と同様であったものの、より感度良く構築された。こうした改善の結果、感度はおよそ3桁も増加した。
【0039】
信号対ノイズ比を増加するために、ウェーブレットノイズ除去及び検出中の走査を用いてもよい。適切なノイズ除去法及び走査法は、Viator等,“Automated Wavelet Denoising of Photoacoustic Signals for Circulating Melanoma Cell Detection and Burn Image Reconstruction”,Phys.Med.Biol.,2008年5月21日,N227−N236頁に記載されている。
【0040】
本願発明の具体的な実施形態を示し記載してきたが、当業者であれば、他の変形例、置換例、及び、代替例が容易であることを理解するだろう。こうした変形例、置換例、及び、代替例は、添付の請求項に定められた本発明の精神と範囲を超えずになすことができる。本発明のさまざまな特徴が添付の請求項において規定する。
【0041】
(関連出願の相互参照)
本願は、合衆国法典第35巻第119条に基づき、2009年4月20日に出願の米国特許仮出願第61/170,880号の優先権を主張する。
【特許請求の範囲】
【請求項1】
生体外で固形組織内の検体を検出する方法であって、
前記固形組織(12)を所定の位置に配置する工程、
前記固形組織をわずかにしか吸収されずに通過し、前記検体に少なくとも部分的に吸収されるように選択された光のパルス状波長を前記固形組織に照射する工程、
光音響波形を得るためにある期間の間、前記照射工程により発生した光音響応答を音響学的に検知する工程、
前記光音響波形を解析する工程、及び、
検出した応答ピークを前記検体の存在に起因させる工程、
からなる方法。
【請求項2】
前記配置工程は、前記固形組織を音響媒体(14)中の所定の位置に配置することを含み、及び、
前記音響学的検知工程は、前記音響媒体を介して前記光音響応答を検知することを含む、請求項1に記載の方法。
【請求項3】
前記音響媒体は脱イオン水からなる、請求項2に記載の方法。
【請求項4】
前記音響媒体は油又はゲルからなる、請求項2に記載の方法。
【請求項5】
前記解析工程は、検出した応答ピークのタイミングに基づいて、検出した任意の検体の位置を決定することを含む、請求項1に記載の方法。
【請求項6】
前記音響学的検知工程は、複数の特徴的光音響応答を獲得することを含み、及び、
前記解析工程は、検出した任意の検体の位置を決定することに加えて、前記検体の有無を決定する、請求項1に記載の方法。
【請求項7】
前記照射工程は、前記固形組織の全体を覆うようにレーザービームを走査することを含む、請求項1に記載の方法。
【請求項8】
前記照射工程は、前記固形組織上にレーザービームの焦点を合わせることを含む、請求項1に記載の方法。
【請求項9】
前記レーザービームは、赤色波長域で放射されるパルス状レーザービームからなる、請求項5に記載の方法。
【請求項10】
前記焦点合わせは、前記レーザービームを光ファイバー(23)を介して1から数マイクロメーターの前記固形組織内に放射することを含む、請求項5に記載の方法。
【請求項11】
前記固形組織は、インタクトなリンパ節又はインタクトなリンパ節の要部を含む、請求項1に記載の方法。
【請求項12】
前記検体はメラニンを含む、請求項8に記載の方法。
【請求項13】
前記照射工程は、複数の光のパルス状波長を前記固形組織に照射することを含む、請求項1に記載の方法。
【請求項14】
固形組織(12)を所定のボリュームでその内部に保持するよう構成されている試料保持器(16)、
パルス状レーザービームを発生することのできるレーザー(22)、
前記パルス状レーザービームを前記固形組織内に向けるための光フォーカサー(23,24)、
固形組織内に収容された検体の光音響応答を検出するために配置されている音響検知器(20a)、及び、
前記光音響応答を解析し且つ前記光音響応答に基づいて前記固形組織内の検体の有無を決定するためのコンピューター(28)を備える、生体外で固形組織内の検体を検出するためのシステム。
【請求項15】
前記試料保持器(16)は、固形組織を前記所定のボリュームで保持するための1つ以上のピン(32)を含み、及び、
前記1つ以上のピンは、前記パルス状レーザービームに対して実質的に透明である、請求項12に記載のシステム。
【請求項16】
前記試料保持器(16)は、音響媒体(14)を収容し且つ前記固形組織を前記所定のボリュームで前記音響媒体内に保持するよう構成されており、及び、
前記音響検知器は、前記試料保持器により保持された音響媒体と音響学的に接触するように配置されている、請求項15に記載のシステム。
【請求項17】
前記音響検知器は、同一直線上に配置されていない少なくとも3つの音響検知器(20a,20b,20c)を含み、及び、
前記コンピューターは、前記少なくとも3つの音響検知器から独立した信号を受け取り、且つ、前記独立した信号を用いて、該信号及び該信号のタイミングから検体の有無及び位置を決定する、請求項14に記載のシステム。
【請求項18】
前記音響検知器は、三次元空間を測るように配置されている少なくとも3つの音響検知器(20a,20b,20c)を含み、及び、
前記コンピューターは、前記少なくとも3つの音響検知器から独立した信号を受け取り、且つ、前記独立した信号を用いて、該信号及び該信号のタイミングから検体の有無及び位置を決定する、請求項14に記載のシステム。
【請求項19】
前記少なくとも3つの音響検知器は、XYZ座標系に沿って異なる位置に配置されている、請求項18に記載のシステム。
【請求項20】
前記試料保持器は、三次元座標系を定める指標要素を備え、
前記固形組織は、前記三次元座標系内の既知の位置に配置され、
前記少なくとも3つの検知器は、定められた前記三次元座標系に対して既知の位置に配置される、請求項14に記載のシステム。
【請求項21】
前記固形組織を撮像するためのカメラ又は光学的検知器(29)をさらに備え、
前記コンピューターは、前記固形組織の画像と前記光音響応答とを前記固形組織と前記固形組織内の検体の位置とのマップを生成するために用いる、請求項20に記載のシステム。
【請求項22】
前記光フォーカサーは、前記所定のボリュームで1から数マイクロメーター内に前記パルス状レーザービームを放射する光ファイバー(23)を含む、請求項14に記載のシステム。
【請求項23】
前記所定のボリュームに対して前記パルス状レーザービームを走査するための走査モーターをさらに備える、請求項22に記載のシステム。
【請求項24】
前記音響検知器は、誘電体により絶縁され、且つ、薄い音響学的に感度の高いフィルムにより覆われた露出研磨面で終始する複数の同軸導体を含む、請求項23に記載のシステム。
【請求項25】
前記音響学的に感度の高いフィルムは、ポリフッ化ビニリデンからなる、請求項24に記載のシステム。
【請求項26】
抽出した固形組織(12)をパルス状レーザービームに被曝させる工程、
前記被曝工程により生じた光音響信号を検出する工程、及び、
前記固形組織内の検体の有無を確かめるために前記光音響信号を解析する工程、
からなる生体外で固形組織内の検体を検出する方法。
【請求項27】
前記固形組織内の前記検体の位置を推定するために前記光音響信号を解析する工程をさらに備える、請求項26に記載の方法。
【請求項28】
前記検出工程は、前記固形組織内の前記検体の位置を推定するために、同一直線上にない異なる位置に配置されている複数の音響検知器(20a,20b,20c)を備え、該各検知器からの検出時間及び該各検知器の相対的位置を用い検出することを含む、請求項26に記載の方法。
【請求項29】
前記音響検知器の数は、少なくとも3つであり、及び、
前記少なくとも3つの音響検知器は、前記固形組織に対して異なる直交位置に配置されている、請求項26に記載の方法。
【請求項30】
前記固形組織は完全にインタクトなリンパ節である、請求項26に記載の方法。
【請求項31】
被験者からリンパ節を抽出する予備工程をさらに含む、請求項30に記載の方法。
【請求項1】
生体外で固形組織内の検体を検出する方法であって、
前記固形組織(12)を所定の位置に配置する工程、
前記固形組織をわずかにしか吸収されずに通過し、前記検体に少なくとも部分的に吸収されるように選択された光のパルス状波長を前記固形組織に照射する工程、
光音響波形を得るためにある期間の間、前記照射工程により発生した光音響応答を音響学的に検知する工程、
前記光音響波形を解析する工程、及び、
検出した応答ピークを前記検体の存在に起因させる工程、
からなる方法。
【請求項2】
前記配置工程は、前記固形組織を音響媒体(14)中の所定の位置に配置することを含み、及び、
前記音響学的検知工程は、前記音響媒体を介して前記光音響応答を検知することを含む、請求項1に記載の方法。
【請求項3】
前記音響媒体は脱イオン水からなる、請求項2に記載の方法。
【請求項4】
前記音響媒体は油又はゲルからなる、請求項2に記載の方法。
【請求項5】
前記解析工程は、検出した応答ピークのタイミングに基づいて、検出した任意の検体の位置を決定することを含む、請求項1に記載の方法。
【請求項6】
前記音響学的検知工程は、複数の特徴的光音響応答を獲得することを含み、及び、
前記解析工程は、検出した任意の検体の位置を決定することに加えて、前記検体の有無を決定する、請求項1に記載の方法。
【請求項7】
前記照射工程は、前記固形組織の全体を覆うようにレーザービームを走査することを含む、請求項1に記載の方法。
【請求項8】
前記照射工程は、前記固形組織上にレーザービームの焦点を合わせることを含む、請求項1に記載の方法。
【請求項9】
前記レーザービームは、赤色波長域で放射されるパルス状レーザービームからなる、請求項5に記載の方法。
【請求項10】
前記焦点合わせは、前記レーザービームを光ファイバー(23)を介して1から数マイクロメーターの前記固形組織内に放射することを含む、請求項5に記載の方法。
【請求項11】
前記固形組織は、インタクトなリンパ節又はインタクトなリンパ節の要部を含む、請求項1に記載の方法。
【請求項12】
前記検体はメラニンを含む、請求項8に記載の方法。
【請求項13】
前記照射工程は、複数の光のパルス状波長を前記固形組織に照射することを含む、請求項1に記載の方法。
【請求項14】
固形組織(12)を所定のボリュームでその内部に保持するよう構成されている試料保持器(16)、
パルス状レーザービームを発生することのできるレーザー(22)、
前記パルス状レーザービームを前記固形組織内に向けるための光フォーカサー(23,24)、
固形組織内に収容された検体の光音響応答を検出するために配置されている音響検知器(20a)、及び、
前記光音響応答を解析し且つ前記光音響応答に基づいて前記固形組織内の検体の有無を決定するためのコンピューター(28)を備える、生体外で固形組織内の検体を検出するためのシステム。
【請求項15】
前記試料保持器(16)は、固形組織を前記所定のボリュームで保持するための1つ以上のピン(32)を含み、及び、
前記1つ以上のピンは、前記パルス状レーザービームに対して実質的に透明である、請求項12に記載のシステム。
【請求項16】
前記試料保持器(16)は、音響媒体(14)を収容し且つ前記固形組織を前記所定のボリュームで前記音響媒体内に保持するよう構成されており、及び、
前記音響検知器は、前記試料保持器により保持された音響媒体と音響学的に接触するように配置されている、請求項15に記載のシステム。
【請求項17】
前記音響検知器は、同一直線上に配置されていない少なくとも3つの音響検知器(20a,20b,20c)を含み、及び、
前記コンピューターは、前記少なくとも3つの音響検知器から独立した信号を受け取り、且つ、前記独立した信号を用いて、該信号及び該信号のタイミングから検体の有無及び位置を決定する、請求項14に記載のシステム。
【請求項18】
前記音響検知器は、三次元空間を測るように配置されている少なくとも3つの音響検知器(20a,20b,20c)を含み、及び、
前記コンピューターは、前記少なくとも3つの音響検知器から独立した信号を受け取り、且つ、前記独立した信号を用いて、該信号及び該信号のタイミングから検体の有無及び位置を決定する、請求項14に記載のシステム。
【請求項19】
前記少なくとも3つの音響検知器は、XYZ座標系に沿って異なる位置に配置されている、請求項18に記載のシステム。
【請求項20】
前記試料保持器は、三次元座標系を定める指標要素を備え、
前記固形組織は、前記三次元座標系内の既知の位置に配置され、
前記少なくとも3つの検知器は、定められた前記三次元座標系に対して既知の位置に配置される、請求項14に記載のシステム。
【請求項21】
前記固形組織を撮像するためのカメラ又は光学的検知器(29)をさらに備え、
前記コンピューターは、前記固形組織の画像と前記光音響応答とを前記固形組織と前記固形組織内の検体の位置とのマップを生成するために用いる、請求項20に記載のシステム。
【請求項22】
前記光フォーカサーは、前記所定のボリュームで1から数マイクロメーター内に前記パルス状レーザービームを放射する光ファイバー(23)を含む、請求項14に記載のシステム。
【請求項23】
前記所定のボリュームに対して前記パルス状レーザービームを走査するための走査モーターをさらに備える、請求項22に記載のシステム。
【請求項24】
前記音響検知器は、誘電体により絶縁され、且つ、薄い音響学的に感度の高いフィルムにより覆われた露出研磨面で終始する複数の同軸導体を含む、請求項23に記載のシステム。
【請求項25】
前記音響学的に感度の高いフィルムは、ポリフッ化ビニリデンからなる、請求項24に記載のシステム。
【請求項26】
抽出した固形組織(12)をパルス状レーザービームに被曝させる工程、
前記被曝工程により生じた光音響信号を検出する工程、及び、
前記固形組織内の検体の有無を確かめるために前記光音響信号を解析する工程、
からなる生体外で固形組織内の検体を検出する方法。
【請求項27】
前記固形組織内の前記検体の位置を推定するために前記光音響信号を解析する工程をさらに備える、請求項26に記載の方法。
【請求項28】
前記検出工程は、前記固形組織内の前記検体の位置を推定するために、同一直線上にない異なる位置に配置されている複数の音響検知器(20a,20b,20c)を備え、該各検知器からの検出時間及び該各検知器の相対的位置を用い検出することを含む、請求項26に記載の方法。
【請求項29】
前記音響検知器の数は、少なくとも3つであり、及び、
前記少なくとも3つの音響検知器は、前記固形組織に対して異なる直交位置に配置されている、請求項26に記載の方法。
【請求項30】
前記固形組織は完全にインタクトなリンパ節である、請求項26に記載の方法。
【請求項31】
被験者からリンパ節を抽出する予備工程をさらに含む、請求項30に記載の方法。
【図1】


【図2A】


【図2B】


【図2C】


【図2D】


【図2E】


【図2F】


【図3】




【図2A】


【図2B】


【図2C】


【図2D】


【図2E】


【図2F】


【図3】


【公表番号】特表2012−524285(P2012−524285A)
【公表日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願番号】特願2012−507309(P2012−507309)
【出願日】平成22年4月20日(2010.4.20)
【国際出願番号】PCT/US2010/031731
【国際公開番号】WO2010/123883
【国際公開日】平成22年10月28日(2010.10.28)
【出願人】(504238378)ザ キュレイターズ オブ ザ ユニバーシティ オブ ミズーリ (3)
【Fターム(参考)】
【公表日】平成24年10月11日(2012.10.11)
【国際特許分類】
【出願日】平成22年4月20日(2010.4.20)
【国際出願番号】PCT/US2010/031731
【国際公開番号】WO2010/123883
【国際公開日】平成22年10月28日(2010.10.28)
【出願人】(504238378)ザ キュレイターズ オブ ザ ユニバーシティ オブ ミズーリ (3)
【Fターム(参考)】
[ Back to top ]

