塩酸リトドリン注射製剤
【課題】
特定の濃度の塩酸リトドリンと特定の濃度の亜硫酸塩類を含有し、特定のpHに調製した、トレオ体と亜硫酸付加物の生成を抑制する塩酸リトドリン注射製剤を提供する。
【解決手段】
塩酸リトドリン5〜15mg/mLおよび亜硫酸塩類0.3〜0.7mg/mLを含有し、pHが4.7〜5.5である注射液をプラスチック製容器に充填し、脱酸素剤と共に酸素難透過性包材に封入されてなることを特徴とする塩酸リトドリン注射製剤。
特定の濃度の塩酸リトドリンと特定の濃度の亜硫酸塩類を含有し、特定のpHに調製した、トレオ体と亜硫酸付加物の生成を抑制する塩酸リトドリン注射製剤を提供する。
【解決手段】
塩酸リトドリン5〜15mg/mLおよび亜硫酸塩類0.3〜0.7mg/mLを含有し、pHが4.7〜5.5である注射液をプラスチック製容器に充填し、脱酸素剤と共に酸素難透過性包材に封入されてなることを特徴とする塩酸リトドリン注射製剤。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、塩酸リトドリンが溶解された液状の薬剤に関する。
【背景技術】
【0002】
塩酸リトドリンは、切迫流産・早産治療剤として使用されている医薬品であり、ブドウ糖またはマルトース注射液に希釈したかたちで点滴静注することにより投与されるものである。
一般的に、塩酸リトドリン注射液は、熱により酸化分解物や異性化物(トレオ体)の生成が起こるため、室温保存は困難である。そのため、市販の塩酸リトドリン注射液は、5℃以下の冷蔵保存を要するガラスアンプル充填製剤であり、酸化防止剤として亜硫酸塩類が配合されている。
しかし、亜硫酸塩類を配合すると、酸化分解物の生成が抑制される代わりに、塩酸リトドリンの亜硫酸付加物(S1:スレオ−1−(4−ヒドロキシフェニル)−2−〔2−(4−ヒドロキシフェニル)エチルアミノ〕−1−プロパンスルフォン酸、S2 :エリスロ−1−(4−ヒドロキシフェニル)−2−〔2−(4−ヒドロキシフェニル)エチルアミノ〕−1−プロパンスルフォン酸)の生成が起こるという問題がある。特に、製造工程中に高圧蒸気滅菌を行った場合、トレオ体、亜硫酸付加物の生成が増加することが報告されている(非特許文献1)。
このように、塩酸リトドリンは、冷蔵保存であれば問題ないが、熱の影響により、トレオ体や亜硫酸付加物が生成するため、加熱滅菌を行ったり、室温保存に変更したりすることは非常に困難である。
【先行技術文献】
【非特許文献】
【0003】
【非特許文献1】リンドルフ点滴静注50mgの純度試験 日医工株式会社HP
【発明の概要】
【発明が解決しようとする課題】
【0004】
塩酸リトドリン注射液は、上述したように類縁物質の生成を抑えるために、5℃以下の冷蔵保存を要するガラスアンプル充填製剤であった。この注射液を医療現場により安全に提供していくためには、ガラスアンプルに充填されたものではなく、シリンジ、特にプラスチック性のシリンジに充填したプレフィルドシリンジ製剤が求められている。しかし、プレフィルドシリンジ化すると、従来のアンプル・バイアルとは形状が異なるため、一般にアンプル・バイアルの保存に適したレイアウトがなされている冷蔵庫での保管が煩雑となることから、そのような制限のない室温下にて保存可能なプラスチック製のプレフィルドシリンジ製剤が提供されることが医療現場では望まれている。
室温保存にするためには、トレオ体の生成を抑えることが重要となるが、そのために安定化剤として加える亜硫酸塩類が過剰であると、塩酸リトドリンの亜硫酸付加物が多量に生成する。従って本発明は、トレオ体の生成とともに亜硫酸付加物の生成も抑えることで、長期間にわたって室温保存可能で、安全な塩酸リトドリン注射製剤を提供することを目的とするものである。
【0005】
上記課題に鑑み、塩酸リトドリンを含有し、亜硫酸塩類を含有する注射液につき、鋭意検討を重ねた結果、亜硫酸塩類の配合量を特定の範囲に設定することにより上記問題を解決できることを究明し、本発明に到達した。
【0006】
上記課題は以下の本発明により解決される。
【0007】
(1)塩酸リトドリン5〜15mg/mLおよび亜硫酸塩類0.3〜0.7mg/mLを含有し、pHが4.7〜5.5である塩酸リトドリン注射製剤。
【0008】
(2)プラスチック製容器に充填された(1)に記載の塩酸リトドリン注射製剤。
【0009】
(3)前記プラスチック製容器が注射器である請求項(2)に記載の塩酸リトドリン注射製剤。
【0010】
(4)脱酸素剤と共に酸素難透過性包材に封入されてなることを特徴とする(2)または(3)に記載の塩酸リトドリン注射製剤。
【0011】
(5)前記酸素難透過性包材は遮光性を有するものである(4)に記載の塩酸リトドリン注射製剤。
【0012】
(6)高圧蒸気滅菌されたものである(1)〜(5)のいずれかに記載の塩酸リトドリン注射製剤。
【発明の効果】
【0013】
本発明は、塩酸リトドリン水溶液が特定の濃度の亜硫酸塩類を含有し、特定のpHに調整した、トレオ体と亜硫酸付加物の生成が抑制された塩酸リトドリン注射製剤である。また、容器がプラスチック製であるので、破損のおそれもなく、ガラスフレークが注射液に混入するおそれもない。また、容器をシリンジ等の注射器とすることによって、ブドウ糖注射液やマルトース注射液等の希釈液に短時間で容易かつ確実に混注することができるようになったため、医療現場に更なる安全と安心を提供するものである。
【図面の簡単な説明】
【0014】
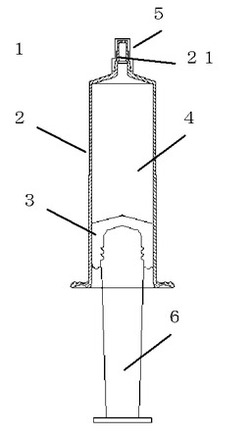
【図1】図1は、本発明の医療用容器の実施例の断面図である。
【発明を実施するための形態】
【0015】
本発明の塩酸リトドリン注射製剤は、特定の濃度の塩酸リトドリンと特定の濃度の亜硫酸塩類を含有する水溶液を特定のpHに調整した塩酸リトドリン注射液をプラスチック製容器に充填し、脱酸素剤とともに酸素難透過性包材に封入したもので、トレオ体と亜硫酸付加物の生成が抑制された安定な注射液製剤である。
【0016】
上記注射液中の塩酸リトドリンの濃度は、5〜15mg/mLであり、亜硫酸塩類の濃度は、0.3〜0.7mg/mLである。亜硫酸塩類としては、たとえば、亜硫酸水素ナトリウム、ピロ亜硫酸ナトリウムおよび亜硫酸ナトリウムなどの亜硫酸アルカリ金属塩類を用いるのが好ましい。注射液には、塩化ナトリウム、ブドウ糖、マルトース、マンニトール、ソルビトール、マンノース、クエン酸ナトリウム、酢酸ナトリウム、リン酸二水素ナトリウム、または乳酸ナトリウム等の等張化剤を適宜配合することができる。また、この注射剤は、酢酸、氷酢酸、塩酸、クエン酸、乳酸、硫酸、コハク酸、L−アスパラギン酸、L−グルタミン酸、安息香酸、リン酸、リンゴ酸、アスコルビン酸、グルコン酸、またはニコチン酸等の酸性物質、水酸化ナトリウム、酢酸ナトリウム、クエン酸ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸水素ナトリウム、乳酸ナトリウム、リン酸二カリウム、リン酸三ナトリウム、リン酸水素二ナトリウム、または酢酸アンモニウム等の塩基性物質を添加することができる。
【0017】
本発明のプラスチック製容器としては、水蒸気透過性の少ない材料が望ましい。これらの観点から、ポリプロピレン、ポリエチレン、ポリスチレン、ポリアミド、ポリ(4−メチルペンテン−1)、アクリル樹脂、アクリロニトリルーブタジエン−スチレン共重合体、ポリエチレンテレフタレート、ポリエチレンナフタレート、環状オレフィンポリマーや環状オレフィンコポリマー等の環状ポリオレフィン、非晶性ポリアリレートなどのポリオレフィン、ポリエステルで光学的に透明な材料で形成されることが好ましい。特に環状ポリオレフィン、ポリプロピレン、ポリエチレンが望ましい。
【0018】
容器は、プラスチックアンプル、プラスチックバイアル等の形態とすることができるが、注射器の形態であることが好ましい。注射器としては、先端に注射針が取り付けられているか、注射針の取り付け部を有する外筒、該外筒の内側面と密接し外筒内部空間の後端開口側を密封するとともに外筒内を摺動可能なガスケット、該ガスケット後端に取り付けられるプランジャーとで構成されるシリンジ形態のものが好ましい。この場合、注射液は上記内部空間に密封されている。ガスケットとしては上記した機能を有するものであれば良いが、ブチルゴム、イソプレンゴム等の合成ゴムや、スチレン系エラストマーやオレフィン系エラストマーを主成分としたエラストマー組成物などが形成材料として例示される。なお、注射器としては、容器自体を外部から押圧することにより充填された注射液が取り付けられた注射針から吐出するよう構成されているスポイト形状など、公知の種々の注射器の形状を採用することができる。
【0019】
本発明において使用される包材は酸素難透過性を有するものである。該包材を形成する材料は、酸素透過性が無いか、あっても極めて低いものであり、例えば、アルミニウム箔、アルミ蒸着フィルム、酸化アルミ蒸着フィルム、酸化珪素蒸着フィルム、ポリビニルアルコール、エチレンビニルアルコール共重合体、ポリエチレンテレフタレート、ポリエチレンナフタレート、ポリ塩化ビニリデン、等をガスバリア層として有するラミネートフィルムが挙げられる。包装体としたとき包材の外から内部を視認する必要がある場合は、酸化アルミ蒸着フィルム、酸化珪素蒸着フィルム、ポリビニルアルコール、エチレンビニルアルコール共重合体、ポリエチレンテレフタレート、ポリエチレンナフタレート、ポリ塩化ビニリデン、等の透明性の高いガスバリア層を採用することが好ましいが、必要に応じアルミニウム箔やアルミ蒸着フィルム等を採用して遮光包材とすることもできる。
【0020】
脱酸素剤としては、水酸化鉄、酸化鉄、炭化鉄などの鉄化合物を有効成分とするもの等を利用できる。その市販品としては、エージレス(登録商標:三菱ガス化学(株)製)、モジュラン(日本化薬(株)製)およびセキュール(登録商標:日本曹達(株)製)等が挙げられる。
【0021】
本発明では、プラスチック製容器を使用するため、保存中にプラスチックを透過してくる酸素により、亜硫酸塩類が消費され、亜硫酸塩類による類縁物質の生成の抑制効果が損なわれる恐れがある。そのため、容器の酸素透過性を積極的に利用し、脱酸素剤と共に塩酸リトドリン注射液を充填したプラスチック容器を酸素難透過性包材で密封することで、室温下であっても長期にわたる保存安定化を可能としている。また、注射液中や容器内の空間部に存在する酸素による酸化を防ぐために、容器空間部および薬液中のガスを窒素などの不活性ガスで置換することが望ましい。例えば、注射液を窒素バブリングし、容器への充填を窒素雰囲気下で行うことなどによって行われる。
【実施例】
【0022】
以下に本発明について具体的に説明するが、本発明は以下の例により何ら限定されない。
【0023】
(調製例1)
注射用水450mLに塩酸リトドリン5.0g及び塩化ナトリウム1.45gを入れ、ピロ亜硫酸ナトリウム0、0.05、0.15、0.25、0.35、0.50gを入れ、攪拌溶解させた。塩酸リトドリン及び塩化ナトリウムが完全に溶解した後、氷酢酸2.175gを加え、水酸化ナトリウムを加えてpH5.25に調整した。注射用水を加えて全量を500mLとし、塩酸リトドリン注射液(10mg/mL)を調製した。この液を0.2μmの酢酸セルロースフィルターにより無菌ろ過後、溶存酸素を窒素バブリングによって窒素置換してから、容器として先端ノズル部を封止してなる容量5mLのポリプロピレン製シリンジ外筒に5mL充填し、空間部を窒素置換した後、注射液の充填口として用いたシリンジ後端開口からスチレン系エラストマー組成物製のガスケットを挿入し、空間部が極力小さくなるようにして該ガスケットによる施栓を行い、塩酸リトドリン注射液充填プレフィルドシリンジを製造した。
【0024】
ついで、該塩酸リトドリン注射液充填プレフィルドシリンジを115℃15分間高圧蒸気滅菌し、脱酸素剤(商品名:エージレス、三菱瓦斯化学社製)と共にアルミ蒸着フィルム製ガスバリア層を有するラミネートフィルムからなる酸素難透過性包材に開口をヒートシールすることにより密封包装して、塩酸リトドリン注射液充填プレフィルドシリンジ包装体とした。
【0025】
(試験例1)
調製例1により得られた塩酸リトドリン注射液充填プレフィルドシリンジ包装体をそれぞれ、40℃にて保存し、3箇月経過後の塩酸リトドリン含量、トレオ体及び亜硫酸付加物の含量をHPLCにて測定し、その結果を表1に示した(表中、値はn=3の平均値,単位は%)。
【0026】
測定にあたっては日局塩酸リトドリン純度試験を準用し、内標準法にて試験を実施した。塩酸リトドリンの含量は、標準溶液中の内標準物質のピーク面積を100として、試料溶液中の内標準物質のピーク面積に対するリトドリンのピーク面積から、その割合を塩酸リトドリン含量として算出した。トレオ体及び亜硫酸付加物の含量は、試料溶液中のリトドリンのピーク面積に対するトレオ体及び亜硫酸付加物のピーク面積の割合として算出した。
【0027】
【表1】

【0028】
測定の結果、試験例1の製剤は、保存条件下3箇月にわたって有意な含量低下は認められなかった。しかし、ピロ亜硫酸ナトリウム0.1mg/mL以下においては3箇月経過後にトレオ体の増加が認められ、0.3〜0.7mg/mLの範囲では、トレオ体の生成が抑制された。また、亜硫酸付加物はピロ亜硫酸ナトリウムの量とともに増加する傾向があり、1.0mg/mL以上では顕著な増加が認められた。
【0029】
(調製例2)
注射用水450mLに塩酸リトドリン5.0g及び塩化ナトリウム1.45gを入れ、ピロ亜硫酸ナトリウム0.15gを入れ、攪拌溶解させた。塩酸リトドリン及び塩化ナトリウムが完全に溶解した後、氷酢酸2.175gおよび、氷酢酸又は水酸化ナトリウムを加えてpH5.50、4.70、4.00、3.00に調整した。注射用水を加えて全量を500mLとし、塩酸リトドリン注射液(10mg/mL)を調製した。この液を0.2μmの酢酸セルロースフィルターにより無菌ろ過後、溶存酸素を窒素バブリングによって窒素置換してから、容器として先端ノズル部を封止してなる容量5mLのポリプロピレン製シリンジ外筒に5mL充填し、空間部を窒素置換した後、注射液の充填口として用いたシリンジ後端開口からスチレン系エラストマー組成物製のガスケットを挿入し、空間部が極力小さくなるようにして該ガスケットによる施栓を行い、塩酸リトドリン注射液充填プレフィルドシリンジを製造した。
【0030】
ついで、該塩酸リトドリン注射液充填プレフィルドシリンジを115℃15分間高圧蒸気滅菌し、脱酸素剤(商品名:エージレス、三菱瓦斯化学社製)と共にアルミ蒸着フィルム製ガスバリア層を有するラミネートフィルムからなる酸素難透過性包材に開口をヒートシールすることにより密封包装して、塩酸リトドリン注射液充填プレフィルドシリンジ包装体とした。
【0031】
(試験例2)
調製例2により得られた塩酸リトドリン注射液充填プレフィルドシリンジ包装体をそれぞれ、40℃にて保存し、3箇月経過後の塩酸リトドリン含量、トレオ体及び亜硫酸付加物の含量をHPLCにて測定し、その結果を表2に示した(表中、値はn=3の平均値,単位は%)。
【0032】
【表2】

【0033】
測定の結果、試験例2の製剤は、保存条件下3箇月にわたって塩酸リトドリンの含量低下はほとんど認められなかった。しかし、pH4.00以下においては3箇月経過後にトレオ体の増加が認められた。
【0034】
(調製例3)
注射用水450mLに塩酸リトドリン2.5、7.5g及び塩化ナトリウム1.45gを入れ、ピロ亜硫酸ナトリウム0.15gを入れ、攪拌溶解させた。塩酸リトドリン及び塩化ナトリウムが完全に溶解した後、氷酢酸2.175gを加え、水酸化ナトリウムを加えてpH5.25に調製した。注射用水を加えて全量を500mLとし、塩酸リトドリン注射液(5mg/mL、15mg/mL)を調製した。この液を0.2μmの酢酸セルロースフィルターにより無菌ろ過後、溶存酸素を窒素バブリングによって窒素置換してから、容器として先端ノズル部を封止してなる容量5mLのポリプロピレン製シリンジ外筒に5mL充填し、空間部を窒素置換した後、注射液の充填口として用いたシリンジ後端開口からスチレン系エラストマー組成物製のガスケットを挿入し、空間部が極力小さくなるようにして該ガスケットによる施栓を行い、塩酸リトドリン注射液充填プレフィルドシリンジを製造した。
【0035】
ついで、該塩酸リトドリン注射液充填プレフィルドシリンジを115℃15分間高圧蒸気滅菌し、脱酸素剤(商品名:エージレス、三菱瓦斯化学社製)と共にアルミ蒸着フィルム製ガスバリア層を有するラミネートフィルムからなる酸素難透過性包材に開口をヒートシールすることにより密封包装して、塩酸リトドリン注射液充填プレフィルドシリンジ包装体とした。
【0036】
(試験例3)
上記により得られた塩酸リトドリン注射液充填プレフィルドシリンジ包装体をそれぞれ、40℃にて保存し、3箇月経過後の塩酸リトドリン含量、トレオ体及び亜硫酸付加物の含量をHPLCにて測定したが、試験例1のピロ亜硫酸ナトリウム0.3mg/mLの場合と同様、トレオ体および亜硫酸付加物の生成量の増加は見られなかった。
【符号の説明】
【0037】
1 プレフィルドシリンジ
2 外筒
21 先端開口
22 後端開口
3 ガスケット
4 薬剤
5 封止部材
6 プランジャー
【技術分野】
【0001】
本発明は、塩酸リトドリンが溶解された液状の薬剤に関する。
【背景技術】
【0002】
塩酸リトドリンは、切迫流産・早産治療剤として使用されている医薬品であり、ブドウ糖またはマルトース注射液に希釈したかたちで点滴静注することにより投与されるものである。
一般的に、塩酸リトドリン注射液は、熱により酸化分解物や異性化物(トレオ体)の生成が起こるため、室温保存は困難である。そのため、市販の塩酸リトドリン注射液は、5℃以下の冷蔵保存を要するガラスアンプル充填製剤であり、酸化防止剤として亜硫酸塩類が配合されている。
しかし、亜硫酸塩類を配合すると、酸化分解物の生成が抑制される代わりに、塩酸リトドリンの亜硫酸付加物(S1:スレオ−1−(4−ヒドロキシフェニル)−2−〔2−(4−ヒドロキシフェニル)エチルアミノ〕−1−プロパンスルフォン酸、S2 :エリスロ−1−(4−ヒドロキシフェニル)−2−〔2−(4−ヒドロキシフェニル)エチルアミノ〕−1−プロパンスルフォン酸)の生成が起こるという問題がある。特に、製造工程中に高圧蒸気滅菌を行った場合、トレオ体、亜硫酸付加物の生成が増加することが報告されている(非特許文献1)。
このように、塩酸リトドリンは、冷蔵保存であれば問題ないが、熱の影響により、トレオ体や亜硫酸付加物が生成するため、加熱滅菌を行ったり、室温保存に変更したりすることは非常に困難である。
【先行技術文献】
【非特許文献】
【0003】
【非特許文献1】リンドルフ点滴静注50mgの純度試験 日医工株式会社HP
【発明の概要】
【発明が解決しようとする課題】
【0004】
塩酸リトドリン注射液は、上述したように類縁物質の生成を抑えるために、5℃以下の冷蔵保存を要するガラスアンプル充填製剤であった。この注射液を医療現場により安全に提供していくためには、ガラスアンプルに充填されたものではなく、シリンジ、特にプラスチック性のシリンジに充填したプレフィルドシリンジ製剤が求められている。しかし、プレフィルドシリンジ化すると、従来のアンプル・バイアルとは形状が異なるため、一般にアンプル・バイアルの保存に適したレイアウトがなされている冷蔵庫での保管が煩雑となることから、そのような制限のない室温下にて保存可能なプラスチック製のプレフィルドシリンジ製剤が提供されることが医療現場では望まれている。
室温保存にするためには、トレオ体の生成を抑えることが重要となるが、そのために安定化剤として加える亜硫酸塩類が過剰であると、塩酸リトドリンの亜硫酸付加物が多量に生成する。従って本発明は、トレオ体の生成とともに亜硫酸付加物の生成も抑えることで、長期間にわたって室温保存可能で、安全な塩酸リトドリン注射製剤を提供することを目的とするものである。
【0005】
上記課題に鑑み、塩酸リトドリンを含有し、亜硫酸塩類を含有する注射液につき、鋭意検討を重ねた結果、亜硫酸塩類の配合量を特定の範囲に設定することにより上記問題を解決できることを究明し、本発明に到達した。
【0006】
上記課題は以下の本発明により解決される。
【0007】
(1)塩酸リトドリン5〜15mg/mLおよび亜硫酸塩類0.3〜0.7mg/mLを含有し、pHが4.7〜5.5である塩酸リトドリン注射製剤。
【0008】
(2)プラスチック製容器に充填された(1)に記載の塩酸リトドリン注射製剤。
【0009】
(3)前記プラスチック製容器が注射器である請求項(2)に記載の塩酸リトドリン注射製剤。
【0010】
(4)脱酸素剤と共に酸素難透過性包材に封入されてなることを特徴とする(2)または(3)に記載の塩酸リトドリン注射製剤。
【0011】
(5)前記酸素難透過性包材は遮光性を有するものである(4)に記載の塩酸リトドリン注射製剤。
【0012】
(6)高圧蒸気滅菌されたものである(1)〜(5)のいずれかに記載の塩酸リトドリン注射製剤。
【発明の効果】
【0013】
本発明は、塩酸リトドリン水溶液が特定の濃度の亜硫酸塩類を含有し、特定のpHに調整した、トレオ体と亜硫酸付加物の生成が抑制された塩酸リトドリン注射製剤である。また、容器がプラスチック製であるので、破損のおそれもなく、ガラスフレークが注射液に混入するおそれもない。また、容器をシリンジ等の注射器とすることによって、ブドウ糖注射液やマルトース注射液等の希釈液に短時間で容易かつ確実に混注することができるようになったため、医療現場に更なる安全と安心を提供するものである。
【図面の簡単な説明】
【0014】
【図1】図1は、本発明の医療用容器の実施例の断面図である。
【発明を実施するための形態】
【0015】
本発明の塩酸リトドリン注射製剤は、特定の濃度の塩酸リトドリンと特定の濃度の亜硫酸塩類を含有する水溶液を特定のpHに調整した塩酸リトドリン注射液をプラスチック製容器に充填し、脱酸素剤とともに酸素難透過性包材に封入したもので、トレオ体と亜硫酸付加物の生成が抑制された安定な注射液製剤である。
【0016】
上記注射液中の塩酸リトドリンの濃度は、5〜15mg/mLであり、亜硫酸塩類の濃度は、0.3〜0.7mg/mLである。亜硫酸塩類としては、たとえば、亜硫酸水素ナトリウム、ピロ亜硫酸ナトリウムおよび亜硫酸ナトリウムなどの亜硫酸アルカリ金属塩類を用いるのが好ましい。注射液には、塩化ナトリウム、ブドウ糖、マルトース、マンニトール、ソルビトール、マンノース、クエン酸ナトリウム、酢酸ナトリウム、リン酸二水素ナトリウム、または乳酸ナトリウム等の等張化剤を適宜配合することができる。また、この注射剤は、酢酸、氷酢酸、塩酸、クエン酸、乳酸、硫酸、コハク酸、L−アスパラギン酸、L−グルタミン酸、安息香酸、リン酸、リンゴ酸、アスコルビン酸、グルコン酸、またはニコチン酸等の酸性物質、水酸化ナトリウム、酢酸ナトリウム、クエン酸ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸水素ナトリウム、乳酸ナトリウム、リン酸二カリウム、リン酸三ナトリウム、リン酸水素二ナトリウム、または酢酸アンモニウム等の塩基性物質を添加することができる。
【0017】
本発明のプラスチック製容器としては、水蒸気透過性の少ない材料が望ましい。これらの観点から、ポリプロピレン、ポリエチレン、ポリスチレン、ポリアミド、ポリ(4−メチルペンテン−1)、アクリル樹脂、アクリロニトリルーブタジエン−スチレン共重合体、ポリエチレンテレフタレート、ポリエチレンナフタレート、環状オレフィンポリマーや環状オレフィンコポリマー等の環状ポリオレフィン、非晶性ポリアリレートなどのポリオレフィン、ポリエステルで光学的に透明な材料で形成されることが好ましい。特に環状ポリオレフィン、ポリプロピレン、ポリエチレンが望ましい。
【0018】
容器は、プラスチックアンプル、プラスチックバイアル等の形態とすることができるが、注射器の形態であることが好ましい。注射器としては、先端に注射針が取り付けられているか、注射針の取り付け部を有する外筒、該外筒の内側面と密接し外筒内部空間の後端開口側を密封するとともに外筒内を摺動可能なガスケット、該ガスケット後端に取り付けられるプランジャーとで構成されるシリンジ形態のものが好ましい。この場合、注射液は上記内部空間に密封されている。ガスケットとしては上記した機能を有するものであれば良いが、ブチルゴム、イソプレンゴム等の合成ゴムや、スチレン系エラストマーやオレフィン系エラストマーを主成分としたエラストマー組成物などが形成材料として例示される。なお、注射器としては、容器自体を外部から押圧することにより充填された注射液が取り付けられた注射針から吐出するよう構成されているスポイト形状など、公知の種々の注射器の形状を採用することができる。
【0019】
本発明において使用される包材は酸素難透過性を有するものである。該包材を形成する材料は、酸素透過性が無いか、あっても極めて低いものであり、例えば、アルミニウム箔、アルミ蒸着フィルム、酸化アルミ蒸着フィルム、酸化珪素蒸着フィルム、ポリビニルアルコール、エチレンビニルアルコール共重合体、ポリエチレンテレフタレート、ポリエチレンナフタレート、ポリ塩化ビニリデン、等をガスバリア層として有するラミネートフィルムが挙げられる。包装体としたとき包材の外から内部を視認する必要がある場合は、酸化アルミ蒸着フィルム、酸化珪素蒸着フィルム、ポリビニルアルコール、エチレンビニルアルコール共重合体、ポリエチレンテレフタレート、ポリエチレンナフタレート、ポリ塩化ビニリデン、等の透明性の高いガスバリア層を採用することが好ましいが、必要に応じアルミニウム箔やアルミ蒸着フィルム等を採用して遮光包材とすることもできる。
【0020】
脱酸素剤としては、水酸化鉄、酸化鉄、炭化鉄などの鉄化合物を有効成分とするもの等を利用できる。その市販品としては、エージレス(登録商標:三菱ガス化学(株)製)、モジュラン(日本化薬(株)製)およびセキュール(登録商標:日本曹達(株)製)等が挙げられる。
【0021】
本発明では、プラスチック製容器を使用するため、保存中にプラスチックを透過してくる酸素により、亜硫酸塩類が消費され、亜硫酸塩類による類縁物質の生成の抑制効果が損なわれる恐れがある。そのため、容器の酸素透過性を積極的に利用し、脱酸素剤と共に塩酸リトドリン注射液を充填したプラスチック容器を酸素難透過性包材で密封することで、室温下であっても長期にわたる保存安定化を可能としている。また、注射液中や容器内の空間部に存在する酸素による酸化を防ぐために、容器空間部および薬液中のガスを窒素などの不活性ガスで置換することが望ましい。例えば、注射液を窒素バブリングし、容器への充填を窒素雰囲気下で行うことなどによって行われる。
【実施例】
【0022】
以下に本発明について具体的に説明するが、本発明は以下の例により何ら限定されない。
【0023】
(調製例1)
注射用水450mLに塩酸リトドリン5.0g及び塩化ナトリウム1.45gを入れ、ピロ亜硫酸ナトリウム0、0.05、0.15、0.25、0.35、0.50gを入れ、攪拌溶解させた。塩酸リトドリン及び塩化ナトリウムが完全に溶解した後、氷酢酸2.175gを加え、水酸化ナトリウムを加えてpH5.25に調整した。注射用水を加えて全量を500mLとし、塩酸リトドリン注射液(10mg/mL)を調製した。この液を0.2μmの酢酸セルロースフィルターにより無菌ろ過後、溶存酸素を窒素バブリングによって窒素置換してから、容器として先端ノズル部を封止してなる容量5mLのポリプロピレン製シリンジ外筒に5mL充填し、空間部を窒素置換した後、注射液の充填口として用いたシリンジ後端開口からスチレン系エラストマー組成物製のガスケットを挿入し、空間部が極力小さくなるようにして該ガスケットによる施栓を行い、塩酸リトドリン注射液充填プレフィルドシリンジを製造した。
【0024】
ついで、該塩酸リトドリン注射液充填プレフィルドシリンジを115℃15分間高圧蒸気滅菌し、脱酸素剤(商品名:エージレス、三菱瓦斯化学社製)と共にアルミ蒸着フィルム製ガスバリア層を有するラミネートフィルムからなる酸素難透過性包材に開口をヒートシールすることにより密封包装して、塩酸リトドリン注射液充填プレフィルドシリンジ包装体とした。
【0025】
(試験例1)
調製例1により得られた塩酸リトドリン注射液充填プレフィルドシリンジ包装体をそれぞれ、40℃にて保存し、3箇月経過後の塩酸リトドリン含量、トレオ体及び亜硫酸付加物の含量をHPLCにて測定し、その結果を表1に示した(表中、値はn=3の平均値,単位は%)。
【0026】
測定にあたっては日局塩酸リトドリン純度試験を準用し、内標準法にて試験を実施した。塩酸リトドリンの含量は、標準溶液中の内標準物質のピーク面積を100として、試料溶液中の内標準物質のピーク面積に対するリトドリンのピーク面積から、その割合を塩酸リトドリン含量として算出した。トレオ体及び亜硫酸付加物の含量は、試料溶液中のリトドリンのピーク面積に対するトレオ体及び亜硫酸付加物のピーク面積の割合として算出した。
【0027】
【表1】

【0028】
測定の結果、試験例1の製剤は、保存条件下3箇月にわたって有意な含量低下は認められなかった。しかし、ピロ亜硫酸ナトリウム0.1mg/mL以下においては3箇月経過後にトレオ体の増加が認められ、0.3〜0.7mg/mLの範囲では、トレオ体の生成が抑制された。また、亜硫酸付加物はピロ亜硫酸ナトリウムの量とともに増加する傾向があり、1.0mg/mL以上では顕著な増加が認められた。
【0029】
(調製例2)
注射用水450mLに塩酸リトドリン5.0g及び塩化ナトリウム1.45gを入れ、ピロ亜硫酸ナトリウム0.15gを入れ、攪拌溶解させた。塩酸リトドリン及び塩化ナトリウムが完全に溶解した後、氷酢酸2.175gおよび、氷酢酸又は水酸化ナトリウムを加えてpH5.50、4.70、4.00、3.00に調整した。注射用水を加えて全量を500mLとし、塩酸リトドリン注射液(10mg/mL)を調製した。この液を0.2μmの酢酸セルロースフィルターにより無菌ろ過後、溶存酸素を窒素バブリングによって窒素置換してから、容器として先端ノズル部を封止してなる容量5mLのポリプロピレン製シリンジ外筒に5mL充填し、空間部を窒素置換した後、注射液の充填口として用いたシリンジ後端開口からスチレン系エラストマー組成物製のガスケットを挿入し、空間部が極力小さくなるようにして該ガスケットによる施栓を行い、塩酸リトドリン注射液充填プレフィルドシリンジを製造した。
【0030】
ついで、該塩酸リトドリン注射液充填プレフィルドシリンジを115℃15分間高圧蒸気滅菌し、脱酸素剤(商品名:エージレス、三菱瓦斯化学社製)と共にアルミ蒸着フィルム製ガスバリア層を有するラミネートフィルムからなる酸素難透過性包材に開口をヒートシールすることにより密封包装して、塩酸リトドリン注射液充填プレフィルドシリンジ包装体とした。
【0031】
(試験例2)
調製例2により得られた塩酸リトドリン注射液充填プレフィルドシリンジ包装体をそれぞれ、40℃にて保存し、3箇月経過後の塩酸リトドリン含量、トレオ体及び亜硫酸付加物の含量をHPLCにて測定し、その結果を表2に示した(表中、値はn=3の平均値,単位は%)。
【0032】
【表2】

【0033】
測定の結果、試験例2の製剤は、保存条件下3箇月にわたって塩酸リトドリンの含量低下はほとんど認められなかった。しかし、pH4.00以下においては3箇月経過後にトレオ体の増加が認められた。
【0034】
(調製例3)
注射用水450mLに塩酸リトドリン2.5、7.5g及び塩化ナトリウム1.45gを入れ、ピロ亜硫酸ナトリウム0.15gを入れ、攪拌溶解させた。塩酸リトドリン及び塩化ナトリウムが完全に溶解した後、氷酢酸2.175gを加え、水酸化ナトリウムを加えてpH5.25に調製した。注射用水を加えて全量を500mLとし、塩酸リトドリン注射液(5mg/mL、15mg/mL)を調製した。この液を0.2μmの酢酸セルロースフィルターにより無菌ろ過後、溶存酸素を窒素バブリングによって窒素置換してから、容器として先端ノズル部を封止してなる容量5mLのポリプロピレン製シリンジ外筒に5mL充填し、空間部を窒素置換した後、注射液の充填口として用いたシリンジ後端開口からスチレン系エラストマー組成物製のガスケットを挿入し、空間部が極力小さくなるようにして該ガスケットによる施栓を行い、塩酸リトドリン注射液充填プレフィルドシリンジを製造した。
【0035】
ついで、該塩酸リトドリン注射液充填プレフィルドシリンジを115℃15分間高圧蒸気滅菌し、脱酸素剤(商品名:エージレス、三菱瓦斯化学社製)と共にアルミ蒸着フィルム製ガスバリア層を有するラミネートフィルムからなる酸素難透過性包材に開口をヒートシールすることにより密封包装して、塩酸リトドリン注射液充填プレフィルドシリンジ包装体とした。
【0036】
(試験例3)
上記により得られた塩酸リトドリン注射液充填プレフィルドシリンジ包装体をそれぞれ、40℃にて保存し、3箇月経過後の塩酸リトドリン含量、トレオ体及び亜硫酸付加物の含量をHPLCにて測定したが、試験例1のピロ亜硫酸ナトリウム0.3mg/mLの場合と同様、トレオ体および亜硫酸付加物の生成量の増加は見られなかった。
【符号の説明】
【0037】
1 プレフィルドシリンジ
2 外筒
21 先端開口
22 後端開口
3 ガスケット
4 薬剤
5 封止部材
6 プランジャー
【特許請求の範囲】
【請求項1】
塩酸リトドリン5〜15mg/mLおよび亜硫酸塩類0.3〜0.7mg/mLを含有し、pHが4.7〜5.5である塩酸リトドリン注射製剤。
【請求項2】
プラスチック製容器に充填された請求項1に記載の塩酸リトドリン注射製剤。
【請求項3】
前記プラスチック製容器が注射器である請求項2に記載の塩酸リトドリン注射製剤。
【請求項4】
脱酸素剤と共に酸素難透過性包材に封入されてなることを特徴とする請求項2または3に記載の塩酸リトドリン注射製剤。
【請求項5】
前記酸素難透過性包材は遮光性を有するものである請求項4に記載の塩酸リトドリン注射液製剤。
【請求項6】
高圧蒸気滅菌されたものである請求項1〜5のいずれかに記載の塩酸リトドリン注射製剤。
【請求項1】
塩酸リトドリン5〜15mg/mLおよび亜硫酸塩類0.3〜0.7mg/mLを含有し、pHが4.7〜5.5である塩酸リトドリン注射製剤。
【請求項2】
プラスチック製容器に充填された請求項1に記載の塩酸リトドリン注射製剤。
【請求項3】
前記プラスチック製容器が注射器である請求項2に記載の塩酸リトドリン注射製剤。
【請求項4】
脱酸素剤と共に酸素難透過性包材に封入されてなることを特徴とする請求項2または3に記載の塩酸リトドリン注射製剤。
【請求項5】
前記酸素難透過性包材は遮光性を有するものである請求項4に記載の塩酸リトドリン注射液製剤。
【請求項6】
高圧蒸気滅菌されたものである請求項1〜5のいずれかに記載の塩酸リトドリン注射製剤。
【図1】




【公開番号】特開2012−1493(P2012−1493A)
【公開日】平成24年1月5日(2012.1.5)
【国際特許分類】
【出願番号】特願2010−138229(P2010−138229)
【出願日】平成22年6月17日(2010.6.17)
【出願人】(000109543)テルモ株式会社 (2,232)
【Fターム(参考)】
【公開日】平成24年1月5日(2012.1.5)
【国際特許分類】
【出願日】平成22年6月17日(2010.6.17)
【出願人】(000109543)テルモ株式会社 (2,232)
【Fターム(参考)】
[ Back to top ]

