変異トリコデルマ属微生物及びこれを用いたタンパク質の製造方法
【課題】トリコデルマ属微生物を宿主として目的のタンパク質を分泌生産できる変異トリコデルマ属微生物を提供し、上記目的のタンパク質の製造方法を提供する。
【解決手段】本発明に係る変異トリコデルマ属微生物は、トウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドでトリコデルマ属微生物を形質転換してなる。
【解決手段】本発明に係る変異トリコデルマ属微生物は、トウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドでトリコデルマ属微生物を形質転換してなる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、所定のタンパク質をコードするポリヌクレオチドで形質転換した変異トリコデルマ属微生物及びこれを用いたタンパク質の製造方法に関する。
【背景技術】
【0002】
トリコデルマ・リーセイ(Trichoderma reesei)を含むトリコデルマ属微生物は、セルラーゼ等の分解酵素を分泌生産することから、植物バイオマスを原料としたバイオ燃料の製造に有用であることが知られている。また、トリコデルマ属微生物におけるセルラーゼ生産能を強化したり、種々の遺伝子発現を可能とするような高機能な変異トリコデルマ属微生物の開発も精力的に取り組まれている。
【0003】
具体的に、特許文献1には、CBH1シグナルペプチドとCBH1活性ドメインの下流にスオレニン(swollenin)遺伝子を結合して、トリコデルマ属やアスペルギルス属等の糸状菌に当該スオレニン遺伝子を発現させ、スオレニンを分泌生産する方法が開示されている。なお、CBH1シグナルペプチドとは、セロビオヒドロラーゼ1(Cellobiohydrolase 1)のシグナルペプチドである。特許文献1に開示された方法によれば、トリコデルマ属微生物を宿主とし、目的タンパク質を分泌生産させるにはCBH1シグナルペプチドが有効であると理解できる。
【0004】
しかし、特許文献1に記載される方法は、如何なる遺伝子の分泌発現を可能とする方法ではなく、例えば、植物由来のタンパク質を分泌生産できないといった問題があった。植物由来タンパク質等の種々のタンパク質を分泌生産した実例は少なく、例えば非特許文献1が知られている程度である。非特許文献1には、トリコデルマ・リーセイを宿主とし、大麦由来のエンドペプチダーゼを発現させたことが開示されている。
【0005】
トリコデルマ属微生物を宿主とした場合に、種々のタンパク質を分泌生産できる手法の開発が望まれていた。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】WO2007/115723
【非特許文献】
【0007】
【非特許文献1】Applied and Environmental Microbiology, 1997, 63(12), p.4938-4940
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は、上述した実情に鑑み、トリコデルマ属微生物を宿主として目的のタンパク質を分泌生産できる変異トリコデルマ属微生物を提供すること、また、当該変異トリコデルマ属微生物を使用する上記目的のタンパク質の製造方法を提供することを目的とする。
【課題を解決するための手段】
【0009】
上述した目的を達成するため、本発明者等が鋭意検討した結果、トウモロコシ由来のエクスパンシン遺伝子に含まれるシグナルペプチドを使用することで、トリコデルマ属微生物において遺伝子産物を分泌生産できることを見いだし本発明を完成するに至った。
【0010】
本発明は以下を包含する。
(1)トウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドでトリコデルマ属微生物を形質転換した変異トリコデルマ属微生物。
(2)トリコデルマ属微生物がトリコデルマ・リーセイであることを特徴とする(1)記載の変異トリコデルマ属微生物。
(3)上記シグナルペプチドは、配列番号1に示すアミノ酸配列を含むことを特徴とする(1)記載の変異トリコデルマ属微生物。
(4)上記目的タンパク質がトウモロコシ由来エクスパンシンであることを特徴とする(1)記載の変異トリコデルマ属微生物。
(5)上記目的タンパク質がセルロース鎖の非還元性末端からセロビオース単位で切断するセロビオハイドロラーゼであることを特徴とする(1)記載の変異トリコデルマ属微生物。
(6)上記目的タンパク質が抗体であることを特徴とする(1)記載の変異トリコデルマ属微生物。
(7)上記(1)乃至(6)いずれか記載の変異トリコデルマ属微生物を培地にて培養し、目的タンパク質を分泌生産する、目的タンパク質の製造方法。
【発明の効果】
【0011】
本発明によれば、トウモロコシ由来エクスパンシンのシグナルペプチドを使用することで、トリコデルマ属微生物を宿主として種々のタンパク質の分泌生産が可能となる。すなわち、本発明に係る変異トリコデルマ属微生物は、トウモロコシ由来エクスパンシンのシグナルペプチドの機能により、目的タンパク質を分泌生産できる。このため、本発明に係る変異トリコデルマ属微生物を使用することで、生産効率に優れたタンパク質の製造方法を提供することができる。
【図面の簡単な説明】
【0012】
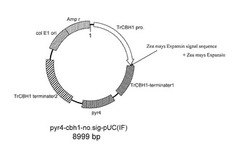
【図1】本実施例1で作製した発現ベクターの概略構成図である。
【図2】本実施例1で作製した形質転換体の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図3】比較例1として作製した形質転換体の菌体粉砕液及び培養上清のWestern blottingの結果を示す写真である。
【図4】比較例2として作製した形質転換体の菌体粉砕液及び培養上清のWestern blottingの結果を示す写真である。
【図5】本実施例1で作製した形質転換体の糖化能を評価した結果を示す特性図である。
【図6】本実施例1で作製した形質転換体(トリコデルマ・リーセイTU6株)の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図7】本実施例2で作製した形質転換体(トリコデルマ・リーセイPC3-7株)の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図8】本実施例3で作製した形質転換体(トリコデルマ・リーセイTU6株)の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図9】本実施例3で作製した形質転換体(トリコデルマ・リーセイTU6株)の培養上清を用いたELISAの結果を示す写真である。
【発明を実施するための形態】
【0013】
以下、本発明に係る変異トリコデルマ属微生物及びこれを用いたタンパク質の製造方法について詳細に説明する。
【0014】
本発明に係る変異トリコデルマ属微生物は、宿主となるトリコデルマ属微生物にトウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドを導入したものである。
【0015】
トリコデルマ属微生物
ここで、トリコデルマ属微生物とは、糸状菌のなかでトリコデルマ属に分類される全ての微生物を包含する意味である。本発明において宿主となるトリコデルマ属微生物は、従来公知のトリコデルマ属微生物の野生株でもよいし、当該野生株から派生した変異株であっても良い。変異株としては、遺伝子導入や遺伝子破壊等の変異が導入された株でも良いし、UV照射やニトロソ化合物処理等の変異原処理により突然変異が導入された株であっても良い。
【0016】
トリコデルマ属微生物としては、例えば、Trichoderma aggressivum、Trichoderma asperellum、Trichoderma atroviride、Trichoderma aureoviride、Trichoderma austrokoningii、Trichoderma brevicompactum、Trichoderma candidum、Trichoderma caribbaeum var. aequatoriale、Trichoderma caribbaeum var. Caribbaeum、Trichoderma catoptron、Trichoderma cremeum、Trichoderma ceramicum、Trichoderma cerinum、Trichoderma chlorosporum、Trichoderma chromospermum、Trichoderma cinnamomeum、Trichoderma citrinoviride、Trichoderma crassum、Trichoderma cremeum、Trichoderma dingleyeae、Trichoderma dorotheae、Trichoderma effusum、Trichoderma erinaceum、Trichoderma estonicum、Trichoderma fertile、Trichoderma gelatinosus、Trichoderma ghanense、Trichoderma hamatum、Trichoderma harzianum、Trichoderma helicum、Trichoderma intricatum、Trichoderma konilangbra、Trichoderma koningii、Trichoderma koningiopsis、Trichoderma longibrachiatum、Trichoderma longipile、Trichoderma minutisporum、Trichoderma oblongisporum、Trichoderma ovalisporum、Trichoderma petersenii、Trichoderma phyllostahydis、Trichoderma piluliferum、Trichoderma pleuroticola、Trichoderma pleurotum、Trichoderma polysporum、Trichoderma pseudokoningii、Trichoderma pubescens、Trichoderma reesei、Trichoderma rogersonii、Trichoderma rossicum、Trichoderma saturnisporum、Trichoderma sinensis、Trichoderma sinuosum、Trichoderma sp. MA 3642、Trichoderma sp. PPRI 3559、Trichoderma spirale、Trichoderma stramineum、Trichoderma strigosum、Trichoderma stromaticum、Trichoderma surrotundum、Trichoderma taiwanense、Trichoderma thailandicum、Trichoderma thelephoricolum、Trichoderma theobromicola、Trichoderma tomentosum、Trichoderma velutinum、Trichoderma virens、Trichoderma viride及びTrichoderma viridescensが挙げられる。なかでも、トリコデルマ属微生物としては、セルラーゼの分泌生産能が高いものを宿主として使用することが好ましい。セルラーゼの分泌生産能が高いトリコデルマ属微生物としては、例えば、トリコデルマ・リーセイ(Trichoderma reesei)が挙げられる。すなわち、本発明において宿主としては、トリコデルマ・リーセイ(Trichoderma reesei)を使用することが好ましい。
【0017】
シグナルペプチド
本発明では、目的タンパク質を菌体外に分泌させる機能を有するシグナルペプチドとして、トウモロコシ由来エクスパンシンのシグナルペプチドを使用する。トウモロコシ由来のエクスパンシン遺伝子については、米国特許公開公報2002/0103355に開示されている。トウモロコシ由来エクスパンシンのシグナルペプチドのアミノ酸配列を配列番号1に示す。なお、配列番号1に示すアミノ酸配列をコードするポリヌクレオチドの塩基配列は適宜設計することができる。特に、トリコデルマ属微生物における翻訳効率を高めることを企図してトリコデルマ属微生物において使用頻度の高いコドンを利用し、配列番号1に示すアミノ酸配列をコードするポリヌクレオチドの塩基配列を設計することが好ましい。
【0018】
目的タンパク質
本発明では、上述したシグナルペプチドに目的タンパク質を連結することで、当該目的タンパク質を菌体外に分泌生産することができる。ここで、目的タンパク質としては、何ら限定されず、如何なる分子量、如何なる生物種由来、如何なる等電点、如何なるアミノ酸配列のタンパク質であっても良い。目的タンパク質がトウモロコシ以外の生物由来である場合、上述したシグナルペプチドと目的タンパク質との融合タンパク質をコードするポリヌクレオチドをトリコデルマ属微生物に導入する。
【0019】
また、目的タンパク質はトウモロコシ由来エクスパンシンでもよい。目的タンパク質がトウモロコシ由来エクスパンシンである場合、トウモロコシ由来のエクスパンシン遺伝子を、そのシグナルペプチドをコードする領域を含む形でトリコデルマ属微生物に導入する。
【0020】
特に、目的タンパク質としては、一例として植物バイオマスの糖化処理に関与する酵素を挙げることができる。トリコデルマ属微生物は、菌体外にセルラーゼを分泌生産することができるため、植物バイオマスの糖化処理に既に利用されてきた。よって、この糖化処理に関与する酵素を目的タンパク質としてトリコデルマ属微生物に導入することによって、植物バイオマスの糖化効率を向上させることができる。なお、エクスパンシンは、植物セルロースとマトリックスとの水素結合を切断する活性を有する酵素である。
【0021】
さらに、バイオマスの糖化に関与する酵素としては、エクスパンシンに限定されず、例えばセロビオハイドロラーゼ、エンドグルカナーゼ及びβ-グルコシダーゼを挙げることができる。すなわち、目的タンパク質として、セロビオハイドロラーゼ、エンドグルカナーゼ及びβ-グルコシダーゼを挙げることができる。なお、セロビオハイドロラーゼには、セルロースの還元末端からセロビオース単位で切断するセロビオハイドロラーゼI及びセルロースの非還元末端からセロビオース単位で切断するセロビオハイドロラーゼIIが存在する。目的タンパク質としては、これらセロビオハイドロラーゼI及びIIのいずれであっても良い。
【0022】
一方、目的タンパク質の由来としては、ウイルス、古細菌、細菌、真菌、放線菌、藻類、原生動物、昆虫、植物及び動物といった如何なる生物種由来のタンパク質であってもよい。目的タンパク質としては一例として抗体を挙げることができる。この場合、上述したトリコデルマ属微生物を用いて、抗体を生産するシステムを構築することができる。
【0023】
ベクター
上述したシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドは、一般的に利用されている発現ベクターの形でトリコデルマ属微生物に導入することができる。ベクターは典型的には、選択可能マーカー遺伝子、クローニング部位及び制御領域(プロモーター及びターミネーター)を有している。このベクターは、本技術分野においてよく知られており商業的に入手可能である。
【0024】
ベクターに含まれるプロモーターは、トリコデルマ属微生物において機能しうるならば、構成的発現プロモーター及び誘導型プロモーターのいずれでも良い。プロモーターが機能しうるとは、宿主微生物(この場合はトリコデルマ属微生物)内において下流遺伝子の転写が可能であることを意味する。プロモーターとしては、例えば、アスペルギウスニガー(Aspergillus niger)等のアスペルギルス属微生物由来のグルコアミラーゼ、アルファ-アミラーゼ、又はアルファ-グルコシダーゼをコードしている遺伝子のプロモーターを挙げることができる。また、A.ニドゥランス(A.nidulans)のgpdA遺伝子、oliC遺伝子又はtrpC遺伝子のプロモーター、ニューロスポラクラッサ(Neurospora crassa)のcbh1又はtrp1遺伝子のプロモーター、A. ニガー(A.niger 又はリゾムコアミエヘイ(Rhizomucor miehei)のアスパラギン酸プロテイナーゼエンコード遺伝子のプロモーター、トリコデルマ・リーセイ由来のcbh1遺伝子、cbh2遺伝子、egl1遺伝子、egl2遺伝子又は他のセルラーゼをコードしている遺伝子のプロモーターを使用することができる。特に、宿主となるトリコデルマ属微生物がトリコデルマ・リーセイである場合、プロモーターとしては、トリコデルマ・リーセイ由来のcbh1遺伝子、cbh2遺伝子、egl1遺伝子、egl2遺伝子又は他のセルラーゼをコードしている遺伝子のプロモーターを使用することが好ましく、特にcbh1遺伝子のプロモーターを使用することがより好ましい。
【0025】
目的タンパク質の生産
本発明では、上述したシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドを組み込んだ発現ベクターを定法に従ってトリコデルマ属微生物に導入し、目的タンパク質を菌体外に分泌生産させる。従って、トリコデルマ属微生物の菌体外がら目的タンパク質を回収する事が出来る。目的タンパク質は、細胞溶解物又は培地の上清サンプルを直接、当該技術分野で知られているドデシルナトリウム硫酸ポリアクリルアミドゲル電気泳動(SDS-PAGE)及びWestern blottingで解析することにより測定できる。細胞培養中に生産された目的タンパク質は培地の中に分泌され、そして、例えば細胞培地から不要な成分を取り除くことにより、精製、又は、単離される。目的タンパク質の精製には、例えば、アフィニティークロマトグラフィー、イオン交換クロマトグラフィー、疎水性相互作用クロマトグラフィー、エタノール沈殿、逆相HPLC、シリカ上またはDEAEなどの陽イオン交換樹脂によるクロマトグラフィー、クロマトフォーカシング、 SDS-PAGE、硫酸アンモニュウム沈殿法、ゲルろ過等の手法を単独で又は組み合わせて使用できる。
【実施例】
【0026】
以下、実施例により本発明をより詳細に説明するが、本発明の技術的範囲は以下の実施例に限定されるものではない。
【0027】
〔実施例1〕
本実施例では、トウモロコシ由来のエクスパンシン遺伝子をトリコデルマ・リーセイに導入した。
【0028】
本例では、トウモロコシ由来のエクスパンシン遺伝子を組み込んだベクターを構築した(図1)。本例では、基本となるベクターとして、pUC19ベクターのKpnI、AatIIサイトにCBH1プロモーターを含むCBH1遺伝子の上流領域を組み込み、KpnI、SphIサイトにCBH1ターミネーターを含むCBH1遺伝子の下流領域を組み込み、EcoRV,、BamHIサイトにpyr4配列を組み込んだものを使用した。
【0029】
また、本例では、トウモロコシ由来のエクスパンシン遺伝子を、そのシグナルペプチドをコードする領域を含む全領域を化学合成した。このとき、トウモロコシ由来のエクスパンシン遺伝子の塩基配列は、宿主となるトリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した。設計したトウモロコシ由来のエクスパンシン遺伝子のうち、シグナルペプチド領域をコードする領域の塩基配列を配列番号2に示した。なお、トウモロコシ由来のエクスパンシンのうち、シグナルペプチド領域を除いた領域のアミノ酸配列を配列番号3に示した。
【0030】
上述した基本となるベクターのKpnI、SpeIサイトに、化学合成したトウモロコシ由来のエクスパンシン遺伝子を組み込み、Sse8387Iで制限酵素処理を行い線状ベクターにしてトリコデルマ・リーセイを形質転換した。本例では、宿主となるトリコデルマ・リーセイとして、トリコデルマ・リーセイPC3-7株を使用した。トリコデルマ・リーセイの形質転換は、定法に従ってトリコデルマ・リーセイのプロトプラストを調製し、上記線状ベクター及びPEG Bufferをこの順で添加する方法により行った。得られた形質転換体は、コロニーPCRによりトウモロコシ由来エクスパンシン遺伝子が導入されたことを確認した。その後、セルラーゼ生産用培地にて形質転換体を120rpm、28℃で5日間培養し、SDS-PAGE及びWestern blottingにて目的とするエクスパンシンが分泌生産されていることを確認した。
【0031】
また、本例では、比較のために、トウモロコシ由来エクスパンシンのシグナルペプチドに変えて、CBH1のシグナルペプチド(配列番号4)を用いてトウモロコシ由来エクスパンシン遺伝子の分泌生産を試みた。すなわち、CBH1のシグナルペプチドとトウモロコシ由来エクスパンシンとからなる融合タンパク質をコードするポリヌクレオチドで、トリコデルマ・リーセイを形質転換し比較例の形質転換体を作製した(比較例1)。CBH1 のシグナルペプチドとCBH1活性ドメインの下流にトウモロコシ由来エクスパンシンを結合した融合タンパク質をコードするポリヌクレオチドで、トリコデルマ・リーセイを形質転換し比較例の形質転換体を作製した(比較例2)。
【0032】
本実施例で作製した形質転換体の培養上清をSDS-PAGEにより分析した結果及びこれをWestern blottingにて分析した結果を図2に示す。なお、図2に示したWestern blotting分析はHis6タグ抗体によるものである。また、図2においてWとは野生型トリコデルマ・リーセイの培養上清の結果である。
【0033】
また、比較例1の形質転換体の培養菌体とその培養上清をWestern blottingによって評価した結果を図3に示した。同様に比較例2の形質転換体の培養菌体とその培養上清をWestern blottingによって評価した結果を図4に示した。図3及び4に示すように、比較例1及び2の形質転換体の破砕液において目的タンパク質の位置にバンドが確認できるが、培養上清には目的タンパク質が含まれていないことが判った。この結果から、比較例1及び2の形質転換体では、菌体内に目的タンパク質を発現するものの分泌できていないことが示され、CBH1のシグナルペプチドが機能していないことが示唆された。
【0034】
これらと比較して、本実施例で作製した形質転換体では、培養上清中に目的タンパク質を検出することができた(図2中の矢印)。この結果から、トウモロコシ由来エクスパンシンのシグナルペプチドは、トリコデルマ・リーセイ等のトリコデルマ属微生物における目的タンパク質の分泌生産に有効に利用できることが明らかとなった。
【0035】
また、本実施例で作製した形質転換体は、菌体外にエクスパンシンを分泌生産できることから、植物バイオマスを糖化する糖化能が野生型に比して優れるものと期待される。そこで、本実施例で作製した形質転換体の糖化能を、野生型のトリコデルマ・リーセイ及び市販酵素を使用した場合と比較して検討した。具体的には、先ず、1%アビセルに、タンパク質が6.7mg/g-バイオマスになるように培養上清を添加しNovo188を各5μLずつ追加添加して、糖化した(50mM酢酸Naバッファー、32℃、120rpm)。各時間毎にサンプリングしバイオセンサー(王子計測機器(株))、でグルコース量を定量した。その結果を図5に示す。図5に示すように、本実施例で作製した形質転換体は、野生型のトリコデルマ・リーセイと比較して優れた糖化能を示すことが明らかとなった。この結果から、本実施例で作製した形質転換体は、エクスパンシンを分泌生産でき優れた糖化能を示すことから、野生型のトリコデルマ・リーセイよりも糖化処理に好適であることが明らかとなった。
【0036】
また、本例では、宿主となるトリコデルマ・リーセイとして、トリコデルマ・リーセイTU6株を使用して、同様にトウモロコシ由来エクスパンシンの分泌生産を試みた。なお、宿主としてトリコデルマ・リーセイTU6株を使用した以外は、同様に実験を行った。結果を図6に示す。図6に示すように、トリコデルマ・リーセイTU6株においても、トウモロコシ由来エクスパンシンに含まれるシグナルペプチドは、分泌シグナルとして十分に機能することが明らかとなった。
【0037】
〔実施例2〕
本実施例では、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチドを利用して、目的タンパク質の分泌生産を検討した。具体的に本実施例では、目的タンパク質として白色腐朽菌(Phanerochaete chrysosporium)由来のCBH2の分泌生産を検討した。
【0038】
先ず、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチド(配列番号1)と、CBH2のうちシグナルペプチドを除く領域とを融合した融合タンパク質をコードするポリヌクレオチドを化学合成した。このとき、合成したポリヌクレオチドの塩基配列は、宿主となるトリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した。なお、トウモロコシ由来のエクスパンシンのシグナルペプチド領域をコードする領域の塩基配列は、実施例1と同様に配列番号2に示す塩基配列とした。また、Phanerochaete chrysosporium由来のCBH2遺伝子のうち、シグナルペプチド領域を除いた領域をトリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した塩基配列を配列番号5に示した。なお、Phanerochaete chrysosporium由来のCBH2のうち、シグナルペプチド領域を除いた領域のアミノ酸配列を配列番号6に示した。なお、配列番号6に示すアミノ酸配列のうちN末端側のHisの6残基は、いわゆるHis6タグである。
【0039】
また本実施例では、実施例1と同様に、pUC19ベクターのKpnI、AatIIサイトにCBH1プロモーターを含むCBH1遺伝子の上流領域を組み込み、KpnI、SphIサイトにCBH1ターミネーターを含むCBH1遺伝子の下流領域を組み込み、EcoRV,、BamHIサイトにpyr4配列を組み込んだものを基本ベクターとして使用した。この基本となるベクターのKpnI、SpeIサイトに、化学合成した上記融合タンパク質をコードするポリヌクレオチドを組み込み、実施例1と同様にして、Sse8387Iで制限酵素処理を行い線状ベクターにしてトリコデルマ・リーセイPC3-7株を形質転換した。
【0040】
また、本例では、比較のために、トウモロコシ由来エクスパンシンのシグナルペプチドに変えて、Phanerochaete chrysosporium由来のCBH2のシグナルペプチド(配列番号7)を用いてPhanerochaete chrysosporium由来のCBH2遺伝子の分泌生産を試みた。すなわち、シグナルペプチドを含むPhanerochaete chrysosporium由来のCBH2をコードし、トリコデルマ・リーセイにおける使用頻度の高いコドンとなるようにPhanerochaete chrysosporium由来のCBH2遺伝子を設計した。Phanerochaete chrysosporium由来のCBH2のシグナルペプチド(配列番号7)をコードする、トリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した塩基配列を配列番号8に示した。
【0041】
そして、実施例1と同様にして形質転換トリコデルマ・リーセイを培養し、培養上清をSDS-PAGEにより分析したWestern blottingにて分析した結果を図7に示す。なお、図7に示したWestern blotting分析はHis6タグ抗体によるものである。また、図7においてレーン1はマーカーであり、レーン2が本実施例で作製した形質転換トリコデルマ・リーセイの培養上清の結果であり、レーン3は比較のために作製した形質転換トリコデルマ・リーセイの培養上清の結果である。
【0042】
図7に示すように、比較のために作製した形質転換体の培養上清には、Phanerochaete chrysosporium由来のCBH2が含まれていないことが判った。この結果から、Phanerochaete chrysosporium由来のCBH2に含まれるシグナルペプチドは、宿主であるトリコデルマ・リーセイにおいて分泌シグナルとして機能しないことが示唆された。これに対して、本実施例で作製した形質転換トリコデルマ・リーセイの培養上清には、Phanerochaete chrysosporium由来のCBH2が含まれていた。この結果から、トウモロコシ由来エクスパンシンに含まれるシグナルペプチドは、宿主であるトリコデルマ・リーセイ等のトリコデルマ属微生物において分泌シグナルとして十分に機能することが明らかとなった。
【0043】
〔実施例3〕
本実施例では、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチドを利用して、目的タンパク質の分泌生産を検討した。具体的に本実施例では、目的タンパク質として抗卵白リゾチームラクダVHH抗体(1ZV5)の分泌生産を検討した。
【0044】
抗卵白リゾチームラクダVHH抗体(1ZV5)についても同様に、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチド(配列番号1)と、抗卵白リゾチームラクダVHH抗体とを融合した融合タンパク質をコードするポリヌクレオチドを化学合成した。本例で使用した抗卵白リゾチームラクダVHH抗体をコードする塩基配列及びアミノ酸配列をそれぞれ配列番号9及び10に示した。なお、本例で使用した抗卵白リゾチームラクダVHH抗体についてはGenst, ED. et, (2005), PNAS, 103(12), p.4586-4591を参照している。
【0045】
また本例でも、実施例1及び2と同様に、pUC19ベクターのKpnI、AatIIサイトにCBH1プロモーターを含むCBH1遺伝子の上流領域を組み込み、KpnI、SphIサイトにCBH1ターミネーターを含むCBH1遺伝子の下流領域を組み込み、EcoRV,、BamHIサイトにpyr4配列を組み込んだものを基本ベクターとして使用した。この基本となるベクターのKpnI、SpeIサイトに、化学合成した上記融合タンパク質をコードするポリヌクレオチドを組み込み、実施例1と同様にして、Sse8387Iで制限酵素処理を行い線状ベクターにしてトリコデルマ・リーセイを形質転換した。ただし、本例では、宿主となるトリコデルマ・リーセイとして、トリコデルマ・リーセイTU6株を使用した。
【0046】
そして、実施例1及び2と同様にして形質転換トリコデルマ・リーセイを培養し、培養上清をSDS-PAGEにより分析したWestern blottingにて分析した結果を図8に示す。なお、図8に示したWestern blotting分析には、一次抗体として抗His6 Rabbit抗体を使用し、二次抗体として抗Rabbit Goat抗体を使用した。また、図8においてWild typeとしたレーンは形質転換していないトリコデルマ・リーセイの培養上清であり、変異体としたレーンは形質転換トリコデルマ・リーセイの培養上清である。
【0047】
図8に示すように、本実施例で作製した形質転換トリコデルマ・リーセイの培養上清には、抗卵白リゾチームラクダVHH抗体(1ZV5)が含まれていた。この結果から、トウモロコシ由来エクスパンシンに含まれるシグナルペプチドは、宿主であるトリコデルマ・リーセイ等のトリコデルマ属微生物において分泌シグナルとして十分に機能し、ほ乳類由来のタンパク質であっても分泌生産が可能であることが明らかとなった。
【0048】
また、本例では、形質転換トリコデルマ・リーセイの培養上清を用いてELISAを行った。ELISAにて分析した結果を図9に示す。なお、図9に示したELISA分析には、ウェルを卵白リゾチームでコーティングし、一次抗体として抗His6 Rabbit抗体を使用し、二次抗体として抗Rabbit Goat抗体を使用した。また、図9において、Wtとしたウェルは形質転換していないトリコデルマ・リーセイの培養上清を使用したときの結果であり、変異体としたウェルは形質転換トリコデルマ・リーセイの培養上清を使用したときの結果である。
【0049】
図9に示すように、本実施例で作製した形質転換トリコデルマ・リーセイの培養上清に分泌された抗卵白リゾチームラクダVHH抗体(1ZV5)は、抗原のエピトープを認識して結合するよう機能しており、立体構造が完璧な状態であることが示唆された。この結果から、宿主であるトリコデルマ・リーセイ等のトリコデルマ属微生物を利用して、ほ乳類由来のタンパク質を機能しうるかたちで分泌生産できることが明らかとなった。
【技術分野】
【0001】
本発明は、所定のタンパク質をコードするポリヌクレオチドで形質転換した変異トリコデルマ属微生物及びこれを用いたタンパク質の製造方法に関する。
【背景技術】
【0002】
トリコデルマ・リーセイ(Trichoderma reesei)を含むトリコデルマ属微生物は、セルラーゼ等の分解酵素を分泌生産することから、植物バイオマスを原料としたバイオ燃料の製造に有用であることが知られている。また、トリコデルマ属微生物におけるセルラーゼ生産能を強化したり、種々の遺伝子発現を可能とするような高機能な変異トリコデルマ属微生物の開発も精力的に取り組まれている。
【0003】
具体的に、特許文献1には、CBH1シグナルペプチドとCBH1活性ドメインの下流にスオレニン(swollenin)遺伝子を結合して、トリコデルマ属やアスペルギルス属等の糸状菌に当該スオレニン遺伝子を発現させ、スオレニンを分泌生産する方法が開示されている。なお、CBH1シグナルペプチドとは、セロビオヒドロラーゼ1(Cellobiohydrolase 1)のシグナルペプチドである。特許文献1に開示された方法によれば、トリコデルマ属微生物を宿主とし、目的タンパク質を分泌生産させるにはCBH1シグナルペプチドが有効であると理解できる。
【0004】
しかし、特許文献1に記載される方法は、如何なる遺伝子の分泌発現を可能とする方法ではなく、例えば、植物由来のタンパク質を分泌生産できないといった問題があった。植物由来タンパク質等の種々のタンパク質を分泌生産した実例は少なく、例えば非特許文献1が知られている程度である。非特許文献1には、トリコデルマ・リーセイを宿主とし、大麦由来のエンドペプチダーゼを発現させたことが開示されている。
【0005】
トリコデルマ属微生物を宿主とした場合に、種々のタンパク質を分泌生産できる手法の開発が望まれていた。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】WO2007/115723
【非特許文献】
【0007】
【非特許文献1】Applied and Environmental Microbiology, 1997, 63(12), p.4938-4940
【発明の概要】
【発明が解決しようとする課題】
【0008】
本発明は、上述した実情に鑑み、トリコデルマ属微生物を宿主として目的のタンパク質を分泌生産できる変異トリコデルマ属微生物を提供すること、また、当該変異トリコデルマ属微生物を使用する上記目的のタンパク質の製造方法を提供することを目的とする。
【課題を解決するための手段】
【0009】
上述した目的を達成するため、本発明者等が鋭意検討した結果、トウモロコシ由来のエクスパンシン遺伝子に含まれるシグナルペプチドを使用することで、トリコデルマ属微生物において遺伝子産物を分泌生産できることを見いだし本発明を完成するに至った。
【0010】
本発明は以下を包含する。
(1)トウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドでトリコデルマ属微生物を形質転換した変異トリコデルマ属微生物。
(2)トリコデルマ属微生物がトリコデルマ・リーセイであることを特徴とする(1)記載の変異トリコデルマ属微生物。
(3)上記シグナルペプチドは、配列番号1に示すアミノ酸配列を含むことを特徴とする(1)記載の変異トリコデルマ属微生物。
(4)上記目的タンパク質がトウモロコシ由来エクスパンシンであることを特徴とする(1)記載の変異トリコデルマ属微生物。
(5)上記目的タンパク質がセルロース鎖の非還元性末端からセロビオース単位で切断するセロビオハイドロラーゼであることを特徴とする(1)記載の変異トリコデルマ属微生物。
(6)上記目的タンパク質が抗体であることを特徴とする(1)記載の変異トリコデルマ属微生物。
(7)上記(1)乃至(6)いずれか記載の変異トリコデルマ属微生物を培地にて培養し、目的タンパク質を分泌生産する、目的タンパク質の製造方法。
【発明の効果】
【0011】
本発明によれば、トウモロコシ由来エクスパンシンのシグナルペプチドを使用することで、トリコデルマ属微生物を宿主として種々のタンパク質の分泌生産が可能となる。すなわち、本発明に係る変異トリコデルマ属微生物は、トウモロコシ由来エクスパンシンのシグナルペプチドの機能により、目的タンパク質を分泌生産できる。このため、本発明に係る変異トリコデルマ属微生物を使用することで、生産効率に優れたタンパク質の製造方法を提供することができる。
【図面の簡単な説明】
【0012】
【図1】本実施例1で作製した発現ベクターの概略構成図である。
【図2】本実施例1で作製した形質転換体の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図3】比較例1として作製した形質転換体の菌体粉砕液及び培養上清のWestern blottingの結果を示す写真である。
【図4】比較例2として作製した形質転換体の菌体粉砕液及び培養上清のWestern blottingの結果を示す写真である。
【図5】本実施例1で作製した形質転換体の糖化能を評価した結果を示す特性図である。
【図6】本実施例1で作製した形質転換体(トリコデルマ・リーセイTU6株)の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図7】本実施例2で作製した形質転換体(トリコデルマ・リーセイPC3-7株)の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図8】本実施例3で作製した形質転換体(トリコデルマ・リーセイTU6株)の培養上清のSDS-PAGEの結果及びWestern blottingの結果を示す写真である。
【図9】本実施例3で作製した形質転換体(トリコデルマ・リーセイTU6株)の培養上清を用いたELISAの結果を示す写真である。
【発明を実施するための形態】
【0013】
以下、本発明に係る変異トリコデルマ属微生物及びこれを用いたタンパク質の製造方法について詳細に説明する。
【0014】
本発明に係る変異トリコデルマ属微生物は、宿主となるトリコデルマ属微生物にトウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドを導入したものである。
【0015】
トリコデルマ属微生物
ここで、トリコデルマ属微生物とは、糸状菌のなかでトリコデルマ属に分類される全ての微生物を包含する意味である。本発明において宿主となるトリコデルマ属微生物は、従来公知のトリコデルマ属微生物の野生株でもよいし、当該野生株から派生した変異株であっても良い。変異株としては、遺伝子導入や遺伝子破壊等の変異が導入された株でも良いし、UV照射やニトロソ化合物処理等の変異原処理により突然変異が導入された株であっても良い。
【0016】
トリコデルマ属微生物としては、例えば、Trichoderma aggressivum、Trichoderma asperellum、Trichoderma atroviride、Trichoderma aureoviride、Trichoderma austrokoningii、Trichoderma brevicompactum、Trichoderma candidum、Trichoderma caribbaeum var. aequatoriale、Trichoderma caribbaeum var. Caribbaeum、Trichoderma catoptron、Trichoderma cremeum、Trichoderma ceramicum、Trichoderma cerinum、Trichoderma chlorosporum、Trichoderma chromospermum、Trichoderma cinnamomeum、Trichoderma citrinoviride、Trichoderma crassum、Trichoderma cremeum、Trichoderma dingleyeae、Trichoderma dorotheae、Trichoderma effusum、Trichoderma erinaceum、Trichoderma estonicum、Trichoderma fertile、Trichoderma gelatinosus、Trichoderma ghanense、Trichoderma hamatum、Trichoderma harzianum、Trichoderma helicum、Trichoderma intricatum、Trichoderma konilangbra、Trichoderma koningii、Trichoderma koningiopsis、Trichoderma longibrachiatum、Trichoderma longipile、Trichoderma minutisporum、Trichoderma oblongisporum、Trichoderma ovalisporum、Trichoderma petersenii、Trichoderma phyllostahydis、Trichoderma piluliferum、Trichoderma pleuroticola、Trichoderma pleurotum、Trichoderma polysporum、Trichoderma pseudokoningii、Trichoderma pubescens、Trichoderma reesei、Trichoderma rogersonii、Trichoderma rossicum、Trichoderma saturnisporum、Trichoderma sinensis、Trichoderma sinuosum、Trichoderma sp. MA 3642、Trichoderma sp. PPRI 3559、Trichoderma spirale、Trichoderma stramineum、Trichoderma strigosum、Trichoderma stromaticum、Trichoderma surrotundum、Trichoderma taiwanense、Trichoderma thailandicum、Trichoderma thelephoricolum、Trichoderma theobromicola、Trichoderma tomentosum、Trichoderma velutinum、Trichoderma virens、Trichoderma viride及びTrichoderma viridescensが挙げられる。なかでも、トリコデルマ属微生物としては、セルラーゼの分泌生産能が高いものを宿主として使用することが好ましい。セルラーゼの分泌生産能が高いトリコデルマ属微生物としては、例えば、トリコデルマ・リーセイ(Trichoderma reesei)が挙げられる。すなわち、本発明において宿主としては、トリコデルマ・リーセイ(Trichoderma reesei)を使用することが好ましい。
【0017】
シグナルペプチド
本発明では、目的タンパク質を菌体外に分泌させる機能を有するシグナルペプチドとして、トウモロコシ由来エクスパンシンのシグナルペプチドを使用する。トウモロコシ由来のエクスパンシン遺伝子については、米国特許公開公報2002/0103355に開示されている。トウモロコシ由来エクスパンシンのシグナルペプチドのアミノ酸配列を配列番号1に示す。なお、配列番号1に示すアミノ酸配列をコードするポリヌクレオチドの塩基配列は適宜設計することができる。特に、トリコデルマ属微生物における翻訳効率を高めることを企図してトリコデルマ属微生物において使用頻度の高いコドンを利用し、配列番号1に示すアミノ酸配列をコードするポリヌクレオチドの塩基配列を設計することが好ましい。
【0018】
目的タンパク質
本発明では、上述したシグナルペプチドに目的タンパク質を連結することで、当該目的タンパク質を菌体外に分泌生産することができる。ここで、目的タンパク質としては、何ら限定されず、如何なる分子量、如何なる生物種由来、如何なる等電点、如何なるアミノ酸配列のタンパク質であっても良い。目的タンパク質がトウモロコシ以外の生物由来である場合、上述したシグナルペプチドと目的タンパク質との融合タンパク質をコードするポリヌクレオチドをトリコデルマ属微生物に導入する。
【0019】
また、目的タンパク質はトウモロコシ由来エクスパンシンでもよい。目的タンパク質がトウモロコシ由来エクスパンシンである場合、トウモロコシ由来のエクスパンシン遺伝子を、そのシグナルペプチドをコードする領域を含む形でトリコデルマ属微生物に導入する。
【0020】
特に、目的タンパク質としては、一例として植物バイオマスの糖化処理に関与する酵素を挙げることができる。トリコデルマ属微生物は、菌体外にセルラーゼを分泌生産することができるため、植物バイオマスの糖化処理に既に利用されてきた。よって、この糖化処理に関与する酵素を目的タンパク質としてトリコデルマ属微生物に導入することによって、植物バイオマスの糖化効率を向上させることができる。なお、エクスパンシンは、植物セルロースとマトリックスとの水素結合を切断する活性を有する酵素である。
【0021】
さらに、バイオマスの糖化に関与する酵素としては、エクスパンシンに限定されず、例えばセロビオハイドロラーゼ、エンドグルカナーゼ及びβ-グルコシダーゼを挙げることができる。すなわち、目的タンパク質として、セロビオハイドロラーゼ、エンドグルカナーゼ及びβ-グルコシダーゼを挙げることができる。なお、セロビオハイドロラーゼには、セルロースの還元末端からセロビオース単位で切断するセロビオハイドロラーゼI及びセルロースの非還元末端からセロビオース単位で切断するセロビオハイドロラーゼIIが存在する。目的タンパク質としては、これらセロビオハイドロラーゼI及びIIのいずれであっても良い。
【0022】
一方、目的タンパク質の由来としては、ウイルス、古細菌、細菌、真菌、放線菌、藻類、原生動物、昆虫、植物及び動物といった如何なる生物種由来のタンパク質であってもよい。目的タンパク質としては一例として抗体を挙げることができる。この場合、上述したトリコデルマ属微生物を用いて、抗体を生産するシステムを構築することができる。
【0023】
ベクター
上述したシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドは、一般的に利用されている発現ベクターの形でトリコデルマ属微生物に導入することができる。ベクターは典型的には、選択可能マーカー遺伝子、クローニング部位及び制御領域(プロモーター及びターミネーター)を有している。このベクターは、本技術分野においてよく知られており商業的に入手可能である。
【0024】
ベクターに含まれるプロモーターは、トリコデルマ属微生物において機能しうるならば、構成的発現プロモーター及び誘導型プロモーターのいずれでも良い。プロモーターが機能しうるとは、宿主微生物(この場合はトリコデルマ属微生物)内において下流遺伝子の転写が可能であることを意味する。プロモーターとしては、例えば、アスペルギウスニガー(Aspergillus niger)等のアスペルギルス属微生物由来のグルコアミラーゼ、アルファ-アミラーゼ、又はアルファ-グルコシダーゼをコードしている遺伝子のプロモーターを挙げることができる。また、A.ニドゥランス(A.nidulans)のgpdA遺伝子、oliC遺伝子又はtrpC遺伝子のプロモーター、ニューロスポラクラッサ(Neurospora crassa)のcbh1又はtrp1遺伝子のプロモーター、A. ニガー(A.niger 又はリゾムコアミエヘイ(Rhizomucor miehei)のアスパラギン酸プロテイナーゼエンコード遺伝子のプロモーター、トリコデルマ・リーセイ由来のcbh1遺伝子、cbh2遺伝子、egl1遺伝子、egl2遺伝子又は他のセルラーゼをコードしている遺伝子のプロモーターを使用することができる。特に、宿主となるトリコデルマ属微生物がトリコデルマ・リーセイである場合、プロモーターとしては、トリコデルマ・リーセイ由来のcbh1遺伝子、cbh2遺伝子、egl1遺伝子、egl2遺伝子又は他のセルラーゼをコードしている遺伝子のプロモーターを使用することが好ましく、特にcbh1遺伝子のプロモーターを使用することがより好ましい。
【0025】
目的タンパク質の生産
本発明では、上述したシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドを組み込んだ発現ベクターを定法に従ってトリコデルマ属微生物に導入し、目的タンパク質を菌体外に分泌生産させる。従って、トリコデルマ属微生物の菌体外がら目的タンパク質を回収する事が出来る。目的タンパク質は、細胞溶解物又は培地の上清サンプルを直接、当該技術分野で知られているドデシルナトリウム硫酸ポリアクリルアミドゲル電気泳動(SDS-PAGE)及びWestern blottingで解析することにより測定できる。細胞培養中に生産された目的タンパク質は培地の中に分泌され、そして、例えば細胞培地から不要な成分を取り除くことにより、精製、又は、単離される。目的タンパク質の精製には、例えば、アフィニティークロマトグラフィー、イオン交換クロマトグラフィー、疎水性相互作用クロマトグラフィー、エタノール沈殿、逆相HPLC、シリカ上またはDEAEなどの陽イオン交換樹脂によるクロマトグラフィー、クロマトフォーカシング、 SDS-PAGE、硫酸アンモニュウム沈殿法、ゲルろ過等の手法を単独で又は組み合わせて使用できる。
【実施例】
【0026】
以下、実施例により本発明をより詳細に説明するが、本発明の技術的範囲は以下の実施例に限定されるものではない。
【0027】
〔実施例1〕
本実施例では、トウモロコシ由来のエクスパンシン遺伝子をトリコデルマ・リーセイに導入した。
【0028】
本例では、トウモロコシ由来のエクスパンシン遺伝子を組み込んだベクターを構築した(図1)。本例では、基本となるベクターとして、pUC19ベクターのKpnI、AatIIサイトにCBH1プロモーターを含むCBH1遺伝子の上流領域を組み込み、KpnI、SphIサイトにCBH1ターミネーターを含むCBH1遺伝子の下流領域を組み込み、EcoRV,、BamHIサイトにpyr4配列を組み込んだものを使用した。
【0029】
また、本例では、トウモロコシ由来のエクスパンシン遺伝子を、そのシグナルペプチドをコードする領域を含む全領域を化学合成した。このとき、トウモロコシ由来のエクスパンシン遺伝子の塩基配列は、宿主となるトリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した。設計したトウモロコシ由来のエクスパンシン遺伝子のうち、シグナルペプチド領域をコードする領域の塩基配列を配列番号2に示した。なお、トウモロコシ由来のエクスパンシンのうち、シグナルペプチド領域を除いた領域のアミノ酸配列を配列番号3に示した。
【0030】
上述した基本となるベクターのKpnI、SpeIサイトに、化学合成したトウモロコシ由来のエクスパンシン遺伝子を組み込み、Sse8387Iで制限酵素処理を行い線状ベクターにしてトリコデルマ・リーセイを形質転換した。本例では、宿主となるトリコデルマ・リーセイとして、トリコデルマ・リーセイPC3-7株を使用した。トリコデルマ・リーセイの形質転換は、定法に従ってトリコデルマ・リーセイのプロトプラストを調製し、上記線状ベクター及びPEG Bufferをこの順で添加する方法により行った。得られた形質転換体は、コロニーPCRによりトウモロコシ由来エクスパンシン遺伝子が導入されたことを確認した。その後、セルラーゼ生産用培地にて形質転換体を120rpm、28℃で5日間培養し、SDS-PAGE及びWestern blottingにて目的とするエクスパンシンが分泌生産されていることを確認した。
【0031】
また、本例では、比較のために、トウモロコシ由来エクスパンシンのシグナルペプチドに変えて、CBH1のシグナルペプチド(配列番号4)を用いてトウモロコシ由来エクスパンシン遺伝子の分泌生産を試みた。すなわち、CBH1のシグナルペプチドとトウモロコシ由来エクスパンシンとからなる融合タンパク質をコードするポリヌクレオチドで、トリコデルマ・リーセイを形質転換し比較例の形質転換体を作製した(比較例1)。CBH1 のシグナルペプチドとCBH1活性ドメインの下流にトウモロコシ由来エクスパンシンを結合した融合タンパク質をコードするポリヌクレオチドで、トリコデルマ・リーセイを形質転換し比較例の形質転換体を作製した(比較例2)。
【0032】
本実施例で作製した形質転換体の培養上清をSDS-PAGEにより分析した結果及びこれをWestern blottingにて分析した結果を図2に示す。なお、図2に示したWestern blotting分析はHis6タグ抗体によるものである。また、図2においてWとは野生型トリコデルマ・リーセイの培養上清の結果である。
【0033】
また、比較例1の形質転換体の培養菌体とその培養上清をWestern blottingによって評価した結果を図3に示した。同様に比較例2の形質転換体の培養菌体とその培養上清をWestern blottingによって評価した結果を図4に示した。図3及び4に示すように、比較例1及び2の形質転換体の破砕液において目的タンパク質の位置にバンドが確認できるが、培養上清には目的タンパク質が含まれていないことが判った。この結果から、比較例1及び2の形質転換体では、菌体内に目的タンパク質を発現するものの分泌できていないことが示され、CBH1のシグナルペプチドが機能していないことが示唆された。
【0034】
これらと比較して、本実施例で作製した形質転換体では、培養上清中に目的タンパク質を検出することができた(図2中の矢印)。この結果から、トウモロコシ由来エクスパンシンのシグナルペプチドは、トリコデルマ・リーセイ等のトリコデルマ属微生物における目的タンパク質の分泌生産に有効に利用できることが明らかとなった。
【0035】
また、本実施例で作製した形質転換体は、菌体外にエクスパンシンを分泌生産できることから、植物バイオマスを糖化する糖化能が野生型に比して優れるものと期待される。そこで、本実施例で作製した形質転換体の糖化能を、野生型のトリコデルマ・リーセイ及び市販酵素を使用した場合と比較して検討した。具体的には、先ず、1%アビセルに、タンパク質が6.7mg/g-バイオマスになるように培養上清を添加しNovo188を各5μLずつ追加添加して、糖化した(50mM酢酸Naバッファー、32℃、120rpm)。各時間毎にサンプリングしバイオセンサー(王子計測機器(株))、でグルコース量を定量した。その結果を図5に示す。図5に示すように、本実施例で作製した形質転換体は、野生型のトリコデルマ・リーセイと比較して優れた糖化能を示すことが明らかとなった。この結果から、本実施例で作製した形質転換体は、エクスパンシンを分泌生産でき優れた糖化能を示すことから、野生型のトリコデルマ・リーセイよりも糖化処理に好適であることが明らかとなった。
【0036】
また、本例では、宿主となるトリコデルマ・リーセイとして、トリコデルマ・リーセイTU6株を使用して、同様にトウモロコシ由来エクスパンシンの分泌生産を試みた。なお、宿主としてトリコデルマ・リーセイTU6株を使用した以外は、同様に実験を行った。結果を図6に示す。図6に示すように、トリコデルマ・リーセイTU6株においても、トウモロコシ由来エクスパンシンに含まれるシグナルペプチドは、分泌シグナルとして十分に機能することが明らかとなった。
【0037】
〔実施例2〕
本実施例では、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチドを利用して、目的タンパク質の分泌生産を検討した。具体的に本実施例では、目的タンパク質として白色腐朽菌(Phanerochaete chrysosporium)由来のCBH2の分泌生産を検討した。
【0038】
先ず、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチド(配列番号1)と、CBH2のうちシグナルペプチドを除く領域とを融合した融合タンパク質をコードするポリヌクレオチドを化学合成した。このとき、合成したポリヌクレオチドの塩基配列は、宿主となるトリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した。なお、トウモロコシ由来のエクスパンシンのシグナルペプチド領域をコードする領域の塩基配列は、実施例1と同様に配列番号2に示す塩基配列とした。また、Phanerochaete chrysosporium由来のCBH2遺伝子のうち、シグナルペプチド領域を除いた領域をトリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した塩基配列を配列番号5に示した。なお、Phanerochaete chrysosporium由来のCBH2のうち、シグナルペプチド領域を除いた領域のアミノ酸配列を配列番号6に示した。なお、配列番号6に示すアミノ酸配列のうちN末端側のHisの6残基は、いわゆるHis6タグである。
【0039】
また本実施例では、実施例1と同様に、pUC19ベクターのKpnI、AatIIサイトにCBH1プロモーターを含むCBH1遺伝子の上流領域を組み込み、KpnI、SphIサイトにCBH1ターミネーターを含むCBH1遺伝子の下流領域を組み込み、EcoRV,、BamHIサイトにpyr4配列を組み込んだものを基本ベクターとして使用した。この基本となるベクターのKpnI、SpeIサイトに、化学合成した上記融合タンパク質をコードするポリヌクレオチドを組み込み、実施例1と同様にして、Sse8387Iで制限酵素処理を行い線状ベクターにしてトリコデルマ・リーセイPC3-7株を形質転換した。
【0040】
また、本例では、比較のために、トウモロコシ由来エクスパンシンのシグナルペプチドに変えて、Phanerochaete chrysosporium由来のCBH2のシグナルペプチド(配列番号7)を用いてPhanerochaete chrysosporium由来のCBH2遺伝子の分泌生産を試みた。すなわち、シグナルペプチドを含むPhanerochaete chrysosporium由来のCBH2をコードし、トリコデルマ・リーセイにおける使用頻度の高いコドンとなるようにPhanerochaete chrysosporium由来のCBH2遺伝子を設計した。Phanerochaete chrysosporium由来のCBH2のシグナルペプチド(配列番号7)をコードする、トリコデルマ・リーセイにおける使用頻度の高いコドンとなるように設計した塩基配列を配列番号8に示した。
【0041】
そして、実施例1と同様にして形質転換トリコデルマ・リーセイを培養し、培養上清をSDS-PAGEにより分析したWestern blottingにて分析した結果を図7に示す。なお、図7に示したWestern blotting分析はHis6タグ抗体によるものである。また、図7においてレーン1はマーカーであり、レーン2が本実施例で作製した形質転換トリコデルマ・リーセイの培養上清の結果であり、レーン3は比較のために作製した形質転換トリコデルマ・リーセイの培養上清の結果である。
【0042】
図7に示すように、比較のために作製した形質転換体の培養上清には、Phanerochaete chrysosporium由来のCBH2が含まれていないことが判った。この結果から、Phanerochaete chrysosporium由来のCBH2に含まれるシグナルペプチドは、宿主であるトリコデルマ・リーセイにおいて分泌シグナルとして機能しないことが示唆された。これに対して、本実施例で作製した形質転換トリコデルマ・リーセイの培養上清には、Phanerochaete chrysosporium由来のCBH2が含まれていた。この結果から、トウモロコシ由来エクスパンシンに含まれるシグナルペプチドは、宿主であるトリコデルマ・リーセイ等のトリコデルマ属微生物において分泌シグナルとして十分に機能することが明らかとなった。
【0043】
〔実施例3〕
本実施例では、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチドを利用して、目的タンパク質の分泌生産を検討した。具体的に本実施例では、目的タンパク質として抗卵白リゾチームラクダVHH抗体(1ZV5)の分泌生産を検討した。
【0044】
抗卵白リゾチームラクダVHH抗体(1ZV5)についても同様に、トウモロコシ由来のエクスパンシンに含まれるシグナルペプチド(配列番号1)と、抗卵白リゾチームラクダVHH抗体とを融合した融合タンパク質をコードするポリヌクレオチドを化学合成した。本例で使用した抗卵白リゾチームラクダVHH抗体をコードする塩基配列及びアミノ酸配列をそれぞれ配列番号9及び10に示した。なお、本例で使用した抗卵白リゾチームラクダVHH抗体についてはGenst, ED. et, (2005), PNAS, 103(12), p.4586-4591を参照している。
【0045】
また本例でも、実施例1及び2と同様に、pUC19ベクターのKpnI、AatIIサイトにCBH1プロモーターを含むCBH1遺伝子の上流領域を組み込み、KpnI、SphIサイトにCBH1ターミネーターを含むCBH1遺伝子の下流領域を組み込み、EcoRV,、BamHIサイトにpyr4配列を組み込んだものを基本ベクターとして使用した。この基本となるベクターのKpnI、SpeIサイトに、化学合成した上記融合タンパク質をコードするポリヌクレオチドを組み込み、実施例1と同様にして、Sse8387Iで制限酵素処理を行い線状ベクターにしてトリコデルマ・リーセイを形質転換した。ただし、本例では、宿主となるトリコデルマ・リーセイとして、トリコデルマ・リーセイTU6株を使用した。
【0046】
そして、実施例1及び2と同様にして形質転換トリコデルマ・リーセイを培養し、培養上清をSDS-PAGEにより分析したWestern blottingにて分析した結果を図8に示す。なお、図8に示したWestern blotting分析には、一次抗体として抗His6 Rabbit抗体を使用し、二次抗体として抗Rabbit Goat抗体を使用した。また、図8においてWild typeとしたレーンは形質転換していないトリコデルマ・リーセイの培養上清であり、変異体としたレーンは形質転換トリコデルマ・リーセイの培養上清である。
【0047】
図8に示すように、本実施例で作製した形質転換トリコデルマ・リーセイの培養上清には、抗卵白リゾチームラクダVHH抗体(1ZV5)が含まれていた。この結果から、トウモロコシ由来エクスパンシンに含まれるシグナルペプチドは、宿主であるトリコデルマ・リーセイ等のトリコデルマ属微生物において分泌シグナルとして十分に機能し、ほ乳類由来のタンパク質であっても分泌生産が可能であることが明らかとなった。
【0048】
また、本例では、形質転換トリコデルマ・リーセイの培養上清を用いてELISAを行った。ELISAにて分析した結果を図9に示す。なお、図9に示したELISA分析には、ウェルを卵白リゾチームでコーティングし、一次抗体として抗His6 Rabbit抗体を使用し、二次抗体として抗Rabbit Goat抗体を使用した。また、図9において、Wtとしたウェルは形質転換していないトリコデルマ・リーセイの培養上清を使用したときの結果であり、変異体としたウェルは形質転換トリコデルマ・リーセイの培養上清を使用したときの結果である。
【0049】
図9に示すように、本実施例で作製した形質転換トリコデルマ・リーセイの培養上清に分泌された抗卵白リゾチームラクダVHH抗体(1ZV5)は、抗原のエピトープを認識して結合するよう機能しており、立体構造が完璧な状態であることが示唆された。この結果から、宿主であるトリコデルマ・リーセイ等のトリコデルマ属微生物を利用して、ほ乳類由来のタンパク質を機能しうるかたちで分泌生産できることが明らかとなった。
【特許請求の範囲】
【請求項1】
トウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドでトリコデルマ属微生物を形質転換した変異トリコデルマ属微生物。
【請求項2】
トリコデルマ属微生物がトリコデルマ・リーセイであることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項3】
上記シグナルペプチドは、配列番号1に示すアミノ酸配列を含むことを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項4】
上記目的タンパク質がトウモロコシ由来エクスパンシンであることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項5】
上記目的タンパク質がセルロース鎖の非還元性末端からセロビオース単位で切断するセロビオハイドロラーゼであることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項6】
上記目的タンパク質が抗体であることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項7】
請求項1乃至6いずれか一項記載の変異トリコデルマ属微生物を培地にて培養し、目的タンパク質を分泌生産する、目的タンパク質の製造方法。
【請求項1】
トウモロコシ由来エクスパンシンのシグナルペプチドと目的タンパク質とをコードするポリヌクレオチドでトリコデルマ属微生物を形質転換した変異トリコデルマ属微生物。
【請求項2】
トリコデルマ属微生物がトリコデルマ・リーセイであることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項3】
上記シグナルペプチドは、配列番号1に示すアミノ酸配列を含むことを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項4】
上記目的タンパク質がトウモロコシ由来エクスパンシンであることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項5】
上記目的タンパク質がセルロース鎖の非還元性末端からセロビオース単位で切断するセロビオハイドロラーゼであることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項6】
上記目的タンパク質が抗体であることを特徴とする請求項1記載の変異トリコデルマ属微生物。
【請求項7】
請求項1乃至6いずれか一項記載の変異トリコデルマ属微生物を培地にて培養し、目的タンパク質を分泌生産する、目的タンパク質の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2012−235767(P2012−235767A)
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願番号】特願2011−252004(P2011−252004)
【出願日】平成23年11月17日(2011.11.17)
【出願人】(000003207)トヨタ自動車株式会社 (59,920)
【出願人】(304021288)国立大学法人長岡技術科学大学 (458)
【出願人】(000003609)株式会社豊田中央研究所 (4,200)
【Fターム(参考)】
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願日】平成23年11月17日(2011.11.17)
【出願人】(000003207)トヨタ自動車株式会社 (59,920)
【出願人】(304021288)国立大学法人長岡技術科学大学 (458)
【出願人】(000003609)株式会社豊田中央研究所 (4,200)
【Fターム(参考)】
[ Back to top ]

