多血小板血漿および/または少血小板血漿のゲル化促進方法、並びにそれに使用するキット、凝固促進材および骨補填材
【課題】多血小板血漿および/または少血小板血漿を短時間で、かつ簡単に所望の形状にゲル化させることができる方法、並びにそれに使用するキット、凝固促進材および骨補填材を提供すること。
【解決手段】多血小板血漿および/または少血小板血漿にゲル化剤を添加し、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させる、多血小板血漿および/または少血小板血漿のゲル化促進方法であり、この方法に使用するキットおよび凝固促進材である。前記凝固促進材に一時的に接触させた後の多血小板血漿および/または少血小板血漿に骨修復材を添加することによって、骨補填材として使用することもできる。
【解決手段】多血小板血漿および/または少血小板血漿にゲル化剤を添加し、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させる、多血小板血漿および/または少血小板血漿のゲル化促進方法であり、この方法に使用するキットおよび凝固促進材である。前記凝固促進材に一時的に接触させた後の多血小板血漿および/または少血小板血漿に骨修復材を添加することによって、骨補填材として使用することもできる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、多血小板血漿および/または少血小板血漿のゲル化を促進させる方法、並びにそれに使用するキット、凝固促進材および骨補填材に関する。
【背景技術】
【0002】
近年、歯科領域や整形外科領域等において、自己の血液成分を用いて創傷治癒や骨再生を早めるという治療法として、多血小板血漿(Platelet Rich Plasma:以下、「PRP」と言うことがある。)や、少血小板血漿(Platelet Poor Plasma:以下、「PPP」と言うことがある。)を用いる治療法が広まってきている。
【0003】
PRPおよびPPPのうち、PRPは、全血よりも血小板濃度の高い血漿であり、創傷治癒を促進するために使用されている。また、骨折等の外傷や骨腫瘍の摘出等によって生じる骨欠損部への補填材として、ハイドロキシアパタイトやβ−リン酸三カルシウム(以下、「β−TCP」と言うことがある。)を主成分としたブロック状または顆粒状の骨修復材が広く使用されているが(例えば、特許文献1参照)、PRPは、このような骨修復材と混合されることによって、骨欠損や軟骨下骨欠損等の骨補填材としても使用されている。
【0004】
一方、PPPは、全血よりも血小板濃度の低い血漿であり、再生医療等の分野で使用されている。上述したPRPおよびPPPは、通常、採取した血液を遠心分離することによって得られ、所望の形状にゲル化させて使用することが多い。
【0005】
PRP等をゲル化させる際には、通常、ゲル化剤が使用される。特許文献2には、PRPおよびβ−TCPの混合物をゲル化させる際に使用するゲル化剤として、トロンビンおよび塩化カルシウムが記載されている。
しかし、トロンビンは、ウシまたはヒト由来のものが一般的であり、それゆえ感染等に対する安全性の問題がある。
【0006】
この問題を解決するため、非特許文献1には、塩化カルシウムのみでPRPのゲル化を行うことが記載されている。
しかし、塩化カルシウムのみでPRP等のゲル化を行うと、ゲル化に要する時間が長く、操作性に劣るという問題がある。
【0007】
特許文献3には、血液にガラスを加えて血液のゲル化を促進させる方法が記載されている。
しかし、特許文献3に記載されているゲル化促進方法は、全血に対する方法である。また、ガラスを加えて血液をゲル化させると、ゲル化物とガラスとの分離が難しいという問題もある。
【先行技術文献】
【特許文献】
【0008】
【特許文献1】特開2001−137328号公報
【特許文献2】国際公開第2002/040071号パンフレット
【特許文献3】特公昭58−027933号公報
【非特許文献】
【0009】
【非特許文献1】冨山高史、外7名、「多血小板血漿(Platelet-Rich Plasma;PRP)と自家骨移植を併用した歯周組織再生療法の評価」、日歯周誌、2007年、49(1)、p.71−76
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明の課題は、多血小板血漿および/または少血小板血漿を短時間で、かつ簡単に所望の形状にゲル化させることができる方法、並びにそれに使用するキット、凝固促進材および骨補填材を提供することである。
【課題を解決するための手段】
【0011】
本発明者らは、上記課題を解決すべく鋭意研究を重ねた結果、以下の知見を見出した。すなわち、PRPやPPPのゲル化をガラス製容器内で行うと、短時間でゲル化を完了させることができる。
【0012】
しかし、PRP等のゲル化をガラス製容器内で完了させると、次の問題がある。すなわち、PRP等は、使用する用途に応じて所望の形状にゲル化させる必要がある。例えばPRPを上述した骨補填材として使用する場合には、骨欠損に応じた形状にPRPをゲル化させる必要がある。このような形状にPRPをゲル化させるには、ガラス製容器を骨欠損に応じた形状に成形する必要がある。
【0013】
しかし、骨欠損形状は複雑な場合が多く、そのような形状にガラス製容器を成形するのは困難であり、それゆえガラス製容器ではPRP等を所望の形状にゲル化させ難い。また、症例に応じた個別の形状毎に容器を準備する必要があるが、ガラス製容器は量産性に劣り、個別の形状への対応が困難である。
【0014】
ガラス製容器に代えて、成形性や量産性に優れるプラスチック製容器を採用すれば、上述したガラス製容器による問題を解決できるとも考えられるが、プラスチック製容器内でPRP等のゲル化を行うと、ガラス製容器よりもゲル化に要する時間が長くなり、操作性に劣る。
【0015】
一方、本発明者らは、PRP等のゲル化をガラス製容器内で行うとゲル化が促進される理由について検討を重ねた。その結果、PRP等をガラス等に接触させることがゲル化反応の引き金となっており、ゲル化完了までPRP等をガラス等に接触させる必要はないという知見を得た。そして、この知見に基づき、さらに鋭意研究を重ねた結果、PRP等を一時的にガラス等に接触させ、その後、汎用性の高いプラスチック製容器内に収容し、このプラスチック製容器内でゲル化を完了させれば、短時間で、かつ簡単に所望の形状にゲル化させることができることを見出し、本発明を完成するに至った。
【0016】
すなわち、本発明の多血小板血漿および/または少血小板血漿のゲル化促進方法は、以下の構成からなる。
(1)多血小板血漿および/または少血小板血漿にゲル化剤を添加し、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させることを特徴とする、多血小板血漿および/または少血小板血漿のゲル化促進方法。
(2)前記ゲル化剤が、塩化カルシウムである前記(1)記載のゲル化促進方法。
(3)前記凝固促進材が、ガラスである前記(1)または(2)記載のゲル化促進方法。
(4)前記凝固促進材に一時的に接触させた後の多血小板血漿および/または少血小板血漿に骨修復材を添加し、プラスチック製容器内に収容してゲル化させる前記(1)〜(3)のいずれかに記載のゲル化促進方法。
(5)前記骨修復材が、β−リン酸三カルシウムである前記(4)記載のゲル化促進方法。
(6)(骨修復材)/(多血小板血漿および/または少血小板血漿)の体積比が、0.05〜2.0である前記(4)または(5)記載のゲル化促進方法。
【0017】
本発明のキットは、以下の構成からなる。
(7)凝固促進材と、プラスチック製容器と、を備え、前記(1)〜(6)のいずれかに記載のゲル化促進方法に使用することを特徴とするキット。
(8)前記凝固促進材の形状が、容器状、フィルター状、棒状、繊維状またはビーズ状である前記(7)記載のキット。
【0018】
本発明の凝固促進材は、以下の構成からなる。
(9)前記(1)〜(6)のいずれかに記載のゲル化促進方法に使用することを特徴とする凝固促進材。
本発明の骨補填材は、以下の構成からなる。
(10)前記(4)〜(6)のいずれかに記載のゲル化促進方法を用いて作製された骨補填材。
【発明の効果】
【0019】
本発明によれば、PRPやPPPを短時間でゲル化させて操作性を向上させることができるという効果がある。また、ゲル化を完了させる容器に汎用性の高いプラスチック製容器を採用するので、骨欠損等の症例に応じた個別の形状に対応する容器の作製が簡単になり、それゆえPRPやPPPを簡単に所望の形状にゲル化させることができる。しかも、プラスチック製容器は、ガラス製容器よりも量産性に優れるので、経済的にも有利になる。さらに、塩化カルシウムのみでPRPやPPPのゲル化を行っても短時間でゲル化を完了させることができる。したがって、ゲル化剤に塩化カルシウムを採用すれば、トロンビンによる感染等に対する安全性の問題を回避することができ、安全性を向上させることができる。
【図面の簡単な説明】
【0020】
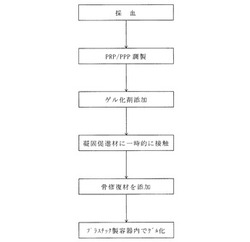
【図1】本発明の一実施形態に係る多血小板血漿および/または少血小板血漿のゲル化促進方法の工程を示すフローチャートである。
【発明を実施するための形態】
【0021】
以下、本発明の一実施形態に係る多血小板血漿および/または少血小板血漿のゲル化促進方法、並びにそれに使用するキット、凝固促進材および骨補填材について、図1を参照して詳細に説明する。同図に示すように、本実施形態のゲル化促進方法では、まず、採血を行う。採取した血液には、凝固防止剤を添加するのが好ましい。これにより、PRPおよびPPPを抗凝固化することができる。凝固防止剤としては、例えばクエン酸ナトリウム等が挙げられる。
【0022】
次に、採取した血液を遠心分離し、PRPおよびPPPを調製する。具体的に説明すると、まず、1回目の遠心分離を行い、採取した血液を上層および下層の2層に分離させる。分離した上層および下層のうち、下層が赤血球層である。1回目の遠心分離の条件としては、300〜1,000G程度で1分〜20分程度が適当である。
【0023】
赤血球層である下層を除去した後、上層に対して2回目の遠心分離を行い、これにより血小板を実質的に多く含む下層の画分、すなわちPRPを採取する。また、血小板が比較的少ない上層の画分、すなわちPPPを採取する。2回目の遠心分離の条件としては、1000〜3000G程度で2分〜20分程度が適当である。なお、PRPおよびPPPの調製方法としては、PRPおよびPPPを調製可能な限り、上述した遠心分離の条件に限定されるものではない。
【0024】
得られたPRPおよび/またはPPPに、ゲル化剤を添加する。ゲル化剤としては、例えば塩化カルシウム、グルコン酸カルシウム等が挙げられ、特に塩化カルシウムが好適である。ゲル化剤は、単独で添加してもよいし、予め水性媒体等で溶解または希釈した溶液としてから添加してもよい。水性媒体としては、例えば水等が挙げられる。ゲル化剤の添加量としては、特に限定されないが、例えば塩化カルシウムを添加する場合には、(塩化カルシウム)/(PRPおよび/またはPPP)=0.2〜2mg/ml程度が適当である。
【0025】
次に、ゲル化剤を添加したPRPおよび/またはPPPを、凝固促進材に一時的に接触させる。これにより、PRPおよび/またはPPPのゲル化を促進させることができる。本明細書において「凝固促進材に一時的に接触させる」とは、PRPおよび/またはPPPを凝固促進材に接触させるという操作を、ゲル化剤添加と同時か、または直後から、ゲル化が完了する前まで、すなわちPRPおよび/またはPPPがまだ流動性を保っている期間にのみ行う、ことをいう。PRPおよび/またはPPPを凝固促進材に接触させる時間としては、PRPおよび/またはPPPの量等にもよるが、通常、1分〜10分程度が適当である。
【0026】
凝固促進材としては、ガラス(ケイ酸塩ガラス)、カオリン、ベントナイト、珪藻土、珪藻珪土、珪砂等が挙げられ、特にガラスが好適である。凝固促進材の形状としては、例えば容器状、(多孔質)フィルター状、(細い)棒状、繊維状、ビーズ状等が挙げられる。
【0027】
PRPおよび/またはPPPを凝固促進材に接触させる方法としては、例えばPRPおよび/またはPPPを、容器状の凝固促進材に収容する方法、フィルター状の凝固促進材を通過させる方法、棒状、繊維状またはビーズ状等の凝固促進材を添加し、その後、分離する方法等が挙げられる。PRPおよび/またはPPPを凝固促進材に接触させる際には、これらを揺動させた状態で接触させるのが好ましい。これにより、PRPおよび/またはPPPと凝固促進材との接触面積を向上させることができる。
【0028】
本実施形態では、凝固促進材に一時的に接触させた後のPRPおよび/またはPPPに骨修復材を添加する。骨修復材としては、例えばβ−TCP、α−リン酸三カルシウム、リン酸四カルシウム、リン酸八カルシウム、非結晶質リン酸カルシウム、ハイドロキシアパタイト、炭酸アパタイト等が挙げられ、これらは1種または2種以上を混合して用いてもよく、特にβ−TCPが好適である。
【0029】
骨修復材は、平均直径が3mm以下の顆粒状であるのが好ましく、平均直径が1.5mm以下の顆粒状であるのがより好ましい。平均直径が小さいほど、ゲル化物の表面が滑らかになることで密着性が向上し、かつ骨修復材の充填量を増加させて骨再生を早めることができる。
【0030】
骨修復材の添加量としては、(骨修復材)/(PRPおよび/またはPPP)=0.05〜1.0g/mlとなる割合が好ましく、0.2〜0.8g/mlとなる割合がより好ましい。骨修復材の充填量が少ないと、骨再生が遅くなるおそれがあるので好ましくない。また、骨修復材の充填量があまり大きいと、ゲル化物の強度が低下し、ゲル化物の取り扱い性が低下するおそれがあるので好ましくない。
【0031】
最後に、骨修復材が添加されたPRPおよび/またはPPPをプラスチック製容器内に収容し、このプラスチック製容器内でゲル化を完了させて骨補填材を得る。本実施形態では、上述したように、PRPおよび/またはPPPを凝固促進材に一時的に接触させているので、PRPおよび/またはPPPを短時間でゲル化させることができる。また、本実施形態では、汎用性の高いプラスチック製容器内でゲル化を完了させるので、骨欠損等の症例に応じた個別の形状に対応する容器の作製が簡単になり、それゆえPRPおよび/またはPPPを簡単に所望の形状にゲル化させることができる。
【0032】
プラスチック製容器の構成材料としては、例えばポリプロピレン樹脂、ポリエチレン樹脂、ポリカーボネート樹脂、ポリスチレン樹脂、光硬化性樹脂等が挙げられ、また、シリコーンゴムや熱可塑性エラストマー、天然ゴム、合成ゴム等のゴム弾性を示すプラスチック材料であってもよい。プラスチック製容器は、例えば汎用のディスポーザブル容器であってもよいし、骨欠損等の症例に応じた個別の形状を光造形法等で作製したものであってもよく、その形状は、単なるプレート状でもよいし、チューブ状でもよい。ゲル化は、通常、室温(23℃)で静置することによって行えばよい。
【0033】
以下、実施例を挙げて本発明を詳細に説明するが、本発明は以下の実施例のみに限定されるものではない。
【実施例】
【0034】
まず、採血を行うとともに、採取した血液をテルモ(株)製の血液バッグ内に収容した。この血液バッグ内には、CPDA液が28mlの割合で含有されている。CPDA液の成分(W/V%)は、以下の通りである。
・クエン酸ナトリウム水和物 2.630
・クエン酸水和物 0.327
・ブドウ糖 2.900
・リン酸二水素ナトリウム 0.251
・アデニン 0.0275
【0035】
次に、血液バッグ内からポリエチレン樹脂製のシリンジを介して血液を取出し、シリンジ毎、遠心分離してPPPを採取した。遠心分離の条件としては、2,000Gで10分間とした。
【0036】
得られたPPPに、2重量%の塩化カルシウム溶液を添加混合し、混合液を得た。塩化カルシウム溶液の添加量は、(塩化カルシウム溶液)/(PPP)=0.05ml/mlにした。次に、得られた混合液を凝固促進材であるガラス製容器内に収容し、手で適度に3分間揺動させた。
【0037】
一方、平均直径が0.1mmである顆粒状のβ−TCPを、(β−TCP)/(PPP)の体積比が0.8となる割合で、プラスチック製容器であるポリエチレン樹脂製の容器内に予め収容した。そして、このポリエチレン樹脂製の容器内に上述の混合液を加えて攪拌し、室温(23℃)で静置し、ゲル化完了に要する時間、すなわちゲル化時間を測定した。その結果を、表1に示す。
【0038】
なお、ゲル化したか否かの判断は、目視観察によって行った。また、ゲル化時間とは、ポリエチレン樹脂製の容器内で塩化カルシウム溶液を添加してからゲル化が完了するまでの時間のことを意味する。
【0039】
[比較例]
まず、上述した実施例と同様にしてPPPを採取し、塩化カルシウム溶液との混合液を得た。次に、得られた混合液をガラス製容器内に収容しなかった以外は、上述した実施例と同様にしてβ−TCPが収容されているポリエチレン樹脂製の容器内に加えて攪拌し、室温(23℃)で静置してゲル化時間を測定した。その結果を、表1に示す。
【0040】
【表1】

【0041】
表1から明らかなように、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させた実施例は、凝固促進材に一時的に接触させなかった比較例よりも、ゲル化時間が短く、操作性に優れているのがわかる。
【技術分野】
【0001】
本発明は、多血小板血漿および/または少血小板血漿のゲル化を促進させる方法、並びにそれに使用するキット、凝固促進材および骨補填材に関する。
【背景技術】
【0002】
近年、歯科領域や整形外科領域等において、自己の血液成分を用いて創傷治癒や骨再生を早めるという治療法として、多血小板血漿(Platelet Rich Plasma:以下、「PRP」と言うことがある。)や、少血小板血漿(Platelet Poor Plasma:以下、「PPP」と言うことがある。)を用いる治療法が広まってきている。
【0003】
PRPおよびPPPのうち、PRPは、全血よりも血小板濃度の高い血漿であり、創傷治癒を促進するために使用されている。また、骨折等の外傷や骨腫瘍の摘出等によって生じる骨欠損部への補填材として、ハイドロキシアパタイトやβ−リン酸三カルシウム(以下、「β−TCP」と言うことがある。)を主成分としたブロック状または顆粒状の骨修復材が広く使用されているが(例えば、特許文献1参照)、PRPは、このような骨修復材と混合されることによって、骨欠損や軟骨下骨欠損等の骨補填材としても使用されている。
【0004】
一方、PPPは、全血よりも血小板濃度の低い血漿であり、再生医療等の分野で使用されている。上述したPRPおよびPPPは、通常、採取した血液を遠心分離することによって得られ、所望の形状にゲル化させて使用することが多い。
【0005】
PRP等をゲル化させる際には、通常、ゲル化剤が使用される。特許文献2には、PRPおよびβ−TCPの混合物をゲル化させる際に使用するゲル化剤として、トロンビンおよび塩化カルシウムが記載されている。
しかし、トロンビンは、ウシまたはヒト由来のものが一般的であり、それゆえ感染等に対する安全性の問題がある。
【0006】
この問題を解決するため、非特許文献1には、塩化カルシウムのみでPRPのゲル化を行うことが記載されている。
しかし、塩化カルシウムのみでPRP等のゲル化を行うと、ゲル化に要する時間が長く、操作性に劣るという問題がある。
【0007】
特許文献3には、血液にガラスを加えて血液のゲル化を促進させる方法が記載されている。
しかし、特許文献3に記載されているゲル化促進方法は、全血に対する方法である。また、ガラスを加えて血液をゲル化させると、ゲル化物とガラスとの分離が難しいという問題もある。
【先行技術文献】
【特許文献】
【0008】
【特許文献1】特開2001−137328号公報
【特許文献2】国際公開第2002/040071号パンフレット
【特許文献3】特公昭58−027933号公報
【非特許文献】
【0009】
【非特許文献1】冨山高史、外7名、「多血小板血漿(Platelet-Rich Plasma;PRP)と自家骨移植を併用した歯周組織再生療法の評価」、日歯周誌、2007年、49(1)、p.71−76
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明の課題は、多血小板血漿および/または少血小板血漿を短時間で、かつ簡単に所望の形状にゲル化させることができる方法、並びにそれに使用するキット、凝固促進材および骨補填材を提供することである。
【課題を解決するための手段】
【0011】
本発明者らは、上記課題を解決すべく鋭意研究を重ねた結果、以下の知見を見出した。すなわち、PRPやPPPのゲル化をガラス製容器内で行うと、短時間でゲル化を完了させることができる。
【0012】
しかし、PRP等のゲル化をガラス製容器内で完了させると、次の問題がある。すなわち、PRP等は、使用する用途に応じて所望の形状にゲル化させる必要がある。例えばPRPを上述した骨補填材として使用する場合には、骨欠損に応じた形状にPRPをゲル化させる必要がある。このような形状にPRPをゲル化させるには、ガラス製容器を骨欠損に応じた形状に成形する必要がある。
【0013】
しかし、骨欠損形状は複雑な場合が多く、そのような形状にガラス製容器を成形するのは困難であり、それゆえガラス製容器ではPRP等を所望の形状にゲル化させ難い。また、症例に応じた個別の形状毎に容器を準備する必要があるが、ガラス製容器は量産性に劣り、個別の形状への対応が困難である。
【0014】
ガラス製容器に代えて、成形性や量産性に優れるプラスチック製容器を採用すれば、上述したガラス製容器による問題を解決できるとも考えられるが、プラスチック製容器内でPRP等のゲル化を行うと、ガラス製容器よりもゲル化に要する時間が長くなり、操作性に劣る。
【0015】
一方、本発明者らは、PRP等のゲル化をガラス製容器内で行うとゲル化が促進される理由について検討を重ねた。その結果、PRP等をガラス等に接触させることがゲル化反応の引き金となっており、ゲル化完了までPRP等をガラス等に接触させる必要はないという知見を得た。そして、この知見に基づき、さらに鋭意研究を重ねた結果、PRP等を一時的にガラス等に接触させ、その後、汎用性の高いプラスチック製容器内に収容し、このプラスチック製容器内でゲル化を完了させれば、短時間で、かつ簡単に所望の形状にゲル化させることができることを見出し、本発明を完成するに至った。
【0016】
すなわち、本発明の多血小板血漿および/または少血小板血漿のゲル化促進方法は、以下の構成からなる。
(1)多血小板血漿および/または少血小板血漿にゲル化剤を添加し、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させることを特徴とする、多血小板血漿および/または少血小板血漿のゲル化促進方法。
(2)前記ゲル化剤が、塩化カルシウムである前記(1)記載のゲル化促進方法。
(3)前記凝固促進材が、ガラスである前記(1)または(2)記載のゲル化促進方法。
(4)前記凝固促進材に一時的に接触させた後の多血小板血漿および/または少血小板血漿に骨修復材を添加し、プラスチック製容器内に収容してゲル化させる前記(1)〜(3)のいずれかに記載のゲル化促進方法。
(5)前記骨修復材が、β−リン酸三カルシウムである前記(4)記載のゲル化促進方法。
(6)(骨修復材)/(多血小板血漿および/または少血小板血漿)の体積比が、0.05〜2.0である前記(4)または(5)記載のゲル化促進方法。
【0017】
本発明のキットは、以下の構成からなる。
(7)凝固促進材と、プラスチック製容器と、を備え、前記(1)〜(6)のいずれかに記載のゲル化促進方法に使用することを特徴とするキット。
(8)前記凝固促進材の形状が、容器状、フィルター状、棒状、繊維状またはビーズ状である前記(7)記載のキット。
【0018】
本発明の凝固促進材は、以下の構成からなる。
(9)前記(1)〜(6)のいずれかに記載のゲル化促進方法に使用することを特徴とする凝固促進材。
本発明の骨補填材は、以下の構成からなる。
(10)前記(4)〜(6)のいずれかに記載のゲル化促進方法を用いて作製された骨補填材。
【発明の効果】
【0019】
本発明によれば、PRPやPPPを短時間でゲル化させて操作性を向上させることができるという効果がある。また、ゲル化を完了させる容器に汎用性の高いプラスチック製容器を採用するので、骨欠損等の症例に応じた個別の形状に対応する容器の作製が簡単になり、それゆえPRPやPPPを簡単に所望の形状にゲル化させることができる。しかも、プラスチック製容器は、ガラス製容器よりも量産性に優れるので、経済的にも有利になる。さらに、塩化カルシウムのみでPRPやPPPのゲル化を行っても短時間でゲル化を完了させることができる。したがって、ゲル化剤に塩化カルシウムを採用すれば、トロンビンによる感染等に対する安全性の問題を回避することができ、安全性を向上させることができる。
【図面の簡単な説明】
【0020】
【図1】本発明の一実施形態に係る多血小板血漿および/または少血小板血漿のゲル化促進方法の工程を示すフローチャートである。
【発明を実施するための形態】
【0021】
以下、本発明の一実施形態に係る多血小板血漿および/または少血小板血漿のゲル化促進方法、並びにそれに使用するキット、凝固促進材および骨補填材について、図1を参照して詳細に説明する。同図に示すように、本実施形態のゲル化促進方法では、まず、採血を行う。採取した血液には、凝固防止剤を添加するのが好ましい。これにより、PRPおよびPPPを抗凝固化することができる。凝固防止剤としては、例えばクエン酸ナトリウム等が挙げられる。
【0022】
次に、採取した血液を遠心分離し、PRPおよびPPPを調製する。具体的に説明すると、まず、1回目の遠心分離を行い、採取した血液を上層および下層の2層に分離させる。分離した上層および下層のうち、下層が赤血球層である。1回目の遠心分離の条件としては、300〜1,000G程度で1分〜20分程度が適当である。
【0023】
赤血球層である下層を除去した後、上層に対して2回目の遠心分離を行い、これにより血小板を実質的に多く含む下層の画分、すなわちPRPを採取する。また、血小板が比較的少ない上層の画分、すなわちPPPを採取する。2回目の遠心分離の条件としては、1000〜3000G程度で2分〜20分程度が適当である。なお、PRPおよびPPPの調製方法としては、PRPおよびPPPを調製可能な限り、上述した遠心分離の条件に限定されるものではない。
【0024】
得られたPRPおよび/またはPPPに、ゲル化剤を添加する。ゲル化剤としては、例えば塩化カルシウム、グルコン酸カルシウム等が挙げられ、特に塩化カルシウムが好適である。ゲル化剤は、単独で添加してもよいし、予め水性媒体等で溶解または希釈した溶液としてから添加してもよい。水性媒体としては、例えば水等が挙げられる。ゲル化剤の添加量としては、特に限定されないが、例えば塩化カルシウムを添加する場合には、(塩化カルシウム)/(PRPおよび/またはPPP)=0.2〜2mg/ml程度が適当である。
【0025】
次に、ゲル化剤を添加したPRPおよび/またはPPPを、凝固促進材に一時的に接触させる。これにより、PRPおよび/またはPPPのゲル化を促進させることができる。本明細書において「凝固促進材に一時的に接触させる」とは、PRPおよび/またはPPPを凝固促進材に接触させるという操作を、ゲル化剤添加と同時か、または直後から、ゲル化が完了する前まで、すなわちPRPおよび/またはPPPがまだ流動性を保っている期間にのみ行う、ことをいう。PRPおよび/またはPPPを凝固促進材に接触させる時間としては、PRPおよび/またはPPPの量等にもよるが、通常、1分〜10分程度が適当である。
【0026】
凝固促進材としては、ガラス(ケイ酸塩ガラス)、カオリン、ベントナイト、珪藻土、珪藻珪土、珪砂等が挙げられ、特にガラスが好適である。凝固促進材の形状としては、例えば容器状、(多孔質)フィルター状、(細い)棒状、繊維状、ビーズ状等が挙げられる。
【0027】
PRPおよび/またはPPPを凝固促進材に接触させる方法としては、例えばPRPおよび/またはPPPを、容器状の凝固促進材に収容する方法、フィルター状の凝固促進材を通過させる方法、棒状、繊維状またはビーズ状等の凝固促進材を添加し、その後、分離する方法等が挙げられる。PRPおよび/またはPPPを凝固促進材に接触させる際には、これらを揺動させた状態で接触させるのが好ましい。これにより、PRPおよび/またはPPPと凝固促進材との接触面積を向上させることができる。
【0028】
本実施形態では、凝固促進材に一時的に接触させた後のPRPおよび/またはPPPに骨修復材を添加する。骨修復材としては、例えばβ−TCP、α−リン酸三カルシウム、リン酸四カルシウム、リン酸八カルシウム、非結晶質リン酸カルシウム、ハイドロキシアパタイト、炭酸アパタイト等が挙げられ、これらは1種または2種以上を混合して用いてもよく、特にβ−TCPが好適である。
【0029】
骨修復材は、平均直径が3mm以下の顆粒状であるのが好ましく、平均直径が1.5mm以下の顆粒状であるのがより好ましい。平均直径が小さいほど、ゲル化物の表面が滑らかになることで密着性が向上し、かつ骨修復材の充填量を増加させて骨再生を早めることができる。
【0030】
骨修復材の添加量としては、(骨修復材)/(PRPおよび/またはPPP)=0.05〜1.0g/mlとなる割合が好ましく、0.2〜0.8g/mlとなる割合がより好ましい。骨修復材の充填量が少ないと、骨再生が遅くなるおそれがあるので好ましくない。また、骨修復材の充填量があまり大きいと、ゲル化物の強度が低下し、ゲル化物の取り扱い性が低下するおそれがあるので好ましくない。
【0031】
最後に、骨修復材が添加されたPRPおよび/またはPPPをプラスチック製容器内に収容し、このプラスチック製容器内でゲル化を完了させて骨補填材を得る。本実施形態では、上述したように、PRPおよび/またはPPPを凝固促進材に一時的に接触させているので、PRPおよび/またはPPPを短時間でゲル化させることができる。また、本実施形態では、汎用性の高いプラスチック製容器内でゲル化を完了させるので、骨欠損等の症例に応じた個別の形状に対応する容器の作製が簡単になり、それゆえPRPおよび/またはPPPを簡単に所望の形状にゲル化させることができる。
【0032】
プラスチック製容器の構成材料としては、例えばポリプロピレン樹脂、ポリエチレン樹脂、ポリカーボネート樹脂、ポリスチレン樹脂、光硬化性樹脂等が挙げられ、また、シリコーンゴムや熱可塑性エラストマー、天然ゴム、合成ゴム等のゴム弾性を示すプラスチック材料であってもよい。プラスチック製容器は、例えば汎用のディスポーザブル容器であってもよいし、骨欠損等の症例に応じた個別の形状を光造形法等で作製したものであってもよく、その形状は、単なるプレート状でもよいし、チューブ状でもよい。ゲル化は、通常、室温(23℃)で静置することによって行えばよい。
【0033】
以下、実施例を挙げて本発明を詳細に説明するが、本発明は以下の実施例のみに限定されるものではない。
【実施例】
【0034】
まず、採血を行うとともに、採取した血液をテルモ(株)製の血液バッグ内に収容した。この血液バッグ内には、CPDA液が28mlの割合で含有されている。CPDA液の成分(W/V%)は、以下の通りである。
・クエン酸ナトリウム水和物 2.630
・クエン酸水和物 0.327
・ブドウ糖 2.900
・リン酸二水素ナトリウム 0.251
・アデニン 0.0275
【0035】
次に、血液バッグ内からポリエチレン樹脂製のシリンジを介して血液を取出し、シリンジ毎、遠心分離してPPPを採取した。遠心分離の条件としては、2,000Gで10分間とした。
【0036】
得られたPPPに、2重量%の塩化カルシウム溶液を添加混合し、混合液を得た。塩化カルシウム溶液の添加量は、(塩化カルシウム溶液)/(PPP)=0.05ml/mlにした。次に、得られた混合液を凝固促進材であるガラス製容器内に収容し、手で適度に3分間揺動させた。
【0037】
一方、平均直径が0.1mmである顆粒状のβ−TCPを、(β−TCP)/(PPP)の体積比が0.8となる割合で、プラスチック製容器であるポリエチレン樹脂製の容器内に予め収容した。そして、このポリエチレン樹脂製の容器内に上述の混合液を加えて攪拌し、室温(23℃)で静置し、ゲル化完了に要する時間、すなわちゲル化時間を測定した。その結果を、表1に示す。
【0038】
なお、ゲル化したか否かの判断は、目視観察によって行った。また、ゲル化時間とは、ポリエチレン樹脂製の容器内で塩化カルシウム溶液を添加してからゲル化が完了するまでの時間のことを意味する。
【0039】
[比較例]
まず、上述した実施例と同様にしてPPPを採取し、塩化カルシウム溶液との混合液を得た。次に、得られた混合液をガラス製容器内に収容しなかった以外は、上述した実施例と同様にしてβ−TCPが収容されているポリエチレン樹脂製の容器内に加えて攪拌し、室温(23℃)で静置してゲル化時間を測定した。その結果を、表1に示す。
【0040】
【表1】

【0041】
表1から明らかなように、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させた実施例は、凝固促進材に一時的に接触させなかった比較例よりも、ゲル化時間が短く、操作性に優れているのがわかる。
【特許請求の範囲】
【請求項1】
多血小板血漿および/または少血小板血漿にゲル化剤を添加し、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させることを特徴とする、多血小板血漿および/または少血小板血漿のゲル化促進方法。
【請求項2】
前記ゲル化剤が、塩化カルシウムである請求項1記載のゲル化促進方法。
【請求項3】
前記凝固促進材が、ガラスである請求項1または2記載のゲル化促進方法。
【請求項4】
前記凝固促進材に一時的に接触させた後の多血小板血漿および/または少血小板血漿に骨修復材を添加し、プラスチック製容器内に収容してゲル化させる請求項1〜3のいずれかに記載のゲル化促進方法。
【請求項5】
前記骨修復材が、β−リン酸三カルシウムである請求項4記載のゲル化促進方法。
【請求項6】
(骨修復材)/(多血小板血漿および/または少血小板血漿)の体積比が、0.05〜2.0である請求項4または5記載のゲル化促進方法。
【請求項7】
凝固促進材と、プラスチック製容器と、を備え、請求項1〜6のいずれかに記載のゲル化促進方法に使用することを特徴とするキット。
【請求項8】
前記凝固促進材の形状が、容器状、フィルター状、棒状、繊維状またはビーズ状である請求項7記載のキット。
【請求項9】
請求項1〜6のいずれかに記載のゲル化促進方法に使用することを特徴とする凝固促進材。
【請求項10】
請求項4〜6のいずれかに記載のゲル化促進方法を用いて作製された骨補填材。
【請求項1】
多血小板血漿および/または少血小板血漿にゲル化剤を添加し、凝固促進材に一時的に接触させ、その後プラスチック製容器内に収容してゲル化させることを特徴とする、多血小板血漿および/または少血小板血漿のゲル化促進方法。
【請求項2】
前記ゲル化剤が、塩化カルシウムである請求項1記載のゲル化促進方法。
【請求項3】
前記凝固促進材が、ガラスである請求項1または2記載のゲル化促進方法。
【請求項4】
前記凝固促進材に一時的に接触させた後の多血小板血漿および/または少血小板血漿に骨修復材を添加し、プラスチック製容器内に収容してゲル化させる請求項1〜3のいずれかに記載のゲル化促進方法。
【請求項5】
前記骨修復材が、β−リン酸三カルシウムである請求項4記載のゲル化促進方法。
【請求項6】
(骨修復材)/(多血小板血漿および/または少血小板血漿)の体積比が、0.05〜2.0である請求項4または5記載のゲル化促進方法。
【請求項7】
凝固促進材と、プラスチック製容器と、を備え、請求項1〜6のいずれかに記載のゲル化促進方法に使用することを特徴とするキット。
【請求項8】
前記凝固促進材の形状が、容器状、フィルター状、棒状、繊維状またはビーズ状である請求項7記載のキット。
【請求項9】
請求項1〜6のいずれかに記載のゲル化促進方法に使用することを特徴とする凝固促進材。
【請求項10】
請求項4〜6のいずれかに記載のゲル化促進方法を用いて作製された骨補填材。
【図1】




【公開番号】特開2013−63924(P2013−63924A)
【公開日】平成25年4月11日(2013.4.11)
【国際特許分類】
【出願番号】特願2011−202906(P2011−202906)
【出願日】平成23年9月16日(2011.9.16)
【出願人】(504418084)京セラメディカル株式会社 (106)
【出願人】(504176911)国立大学法人大阪大学 (1,536)
【Fターム(参考)】
【公開日】平成25年4月11日(2013.4.11)
【国際特許分類】
【出願日】平成23年9月16日(2011.9.16)
【出願人】(504418084)京セラメディカル株式会社 (106)
【出願人】(504176911)国立大学法人大阪大学 (1,536)
【Fターム(参考)】
[ Back to top ]

