大容量微粒子サンプル中の病原体検出
【課題】食品サンプル等のサンプル中の微生物を検出するための方法及びフィルターシステムを開示する。
【解決手段】フィルターは、例えば静電荷により、微生物を引きつけるように構成される。微生物の検出を可能にするために、微生物を含有するフィルターをインキュベートして、微生物を増殖させる。フィルターは分解性であってもよく、かつ検出は、微生物又は微生物の分子マーカーを検出用フィルターから抽出することを含んでよい。微生物をマイクロビーズの間を通過させながら、サンプルから汚れや他の混在物質を捕捉するように選択された多孔質マイクロビーズ要素を、フィルターシステムは含んでもよい。このフィルターシステムを使用して、サンプル中の微生物を検出する方法。この方法は、ポリマー及び/又は微生物検出試薬をフィルターに添加して、微生物の増殖を局在化させるとともに、試薬の蒸発を防止するステップも含んで良い。
【解決手段】フィルターは、例えば静電荷により、微生物を引きつけるように構成される。微生物の検出を可能にするために、微生物を含有するフィルターをインキュベートして、微生物を増殖させる。フィルターは分解性であってもよく、かつ検出は、微生物又は微生物の分子マーカーを検出用フィルターから抽出することを含んでよい。微生物をマイクロビーズの間を通過させながら、サンプルから汚れや他の混在物質を捕捉するように選択された多孔質マイクロビーズ要素を、フィルターシステムは含んでもよい。このフィルターシステムを使用して、サンプル中の微生物を検出する方法。この方法は、ポリマー及び/又は微生物検出試薬をフィルターに添加して、微生物の増殖を局在化させるとともに、試薬の蒸発を防止するステップも含んで良い。
【発明の詳細な説明】
【技術分野】
【0001】
関連出願
本出願は、2007年8月1日提出の米国仮出願第60/953422号、2007年11月1日提出の米国仮出願第60/984624号、2007年12月31日提出の米国仮出願第61/018079号、及び2008年5月21日提出の米国仮出願第61/055099号の優先権を主張する。これら関連出願の全ては、ここに引用することにより本明細書の記載の一部をなすものとする。
【0002】
発明の分野
本開示は、大容量の微粒子サンプル中の病原体を検出するための試薬、方法及び装置に関する。
【背景技術】
【0003】
関連技術の説明
疾病予防管理センター(CDC)による最近の評価によれば、米国内で、各年だけで、7600万の食品媒介疾病(food-borne illness)の例、32万5千の入院例、及び5000の死亡例の原因が、食品媒介病原体(food-borne pathogen)である。ヒトへの有害
な医学的影響に加えて、これらの食品媒介事例の大発生は、医療費増大、生産性低下、商品回収、及び輸出差し止めによって、経済に悪影響をもたらす。米国農務省(USDA)は、特定の食品媒介病原体が少量でも生き残り、食中毒又は大発生を引き起こし得るので、その病原体に対してゼロトレランス政策を推奨している。そのため、食品サンプル中の1個の病原体でも検出できる高精度の病原体検出技術の開発が必要である。
【0004】
現在、多数の検出技術及び製品が、食品媒介病原体の検出に利用できるが、数グラムの食品サンプルを汚染する1個の病原体を、24時間という時間枠内で検出することは、今もなお困難である。一般に、病原体は、希釈及び均質化により食品サンプルから抽出され、これらは数百mLほどの又はそれ以上のサンプル容積を生じる。大容量のサンプル中にある少数の病原体を検出するためには、病原体濃度が病原体検出アッセイに適するレベルに達するまで、細胞を培養することが必要である。必要な前増菌(pre-enrichment)時間は、標的病原体の倍加時間、生存能力、及び検出に要する病原体濃度に依存する。前増菌は、通常少なくとも12〜48時間かかる。そのため、ポリメラーゼ連鎖反応(PCR)や酵素結合免疫吸着法(ELISA)などの高感度検出アッセイを用いても、食品サンプル中の病原体混入の検出は、依然として1日又は2日を必要とする。更に、これらのアッセイは、一般に、高価であり、熟練の検査技師を必要とする。
【0005】
更に、前増菌培養を用いる食品病原体アッセイは、増菌した病原体の取り扱いを要し、これは、試験所及び検査技師の二次汚染を生じ得る。従って、これらのアッセイは、食品製造プラントでの現場検査には適切ではなく、その代わりに現場の外、例えば委託試験所(reference laboratories)で行う必要がある。また、混入病原体の生存能力及び食品サンプルの成分が、病原体増殖速度に影響を与え得るという理由から、及びサンプルが細胞増殖の静止期又は衰退期にどれほど迅速に到達するかどうかは、病原体汚染レベルに依存し得るという理由から、前増菌培養によって、混入食品病原体に関する定量的情報が失われてしまう。そのため、前増菌を用いる食品病原体アッセイは、非定量的であり、食品の病原体汚染レベルの評価は難しい。
【0006】
前増菌を伴う病原体アッセイの上記欠点を克服するために、病原体濃度を増すために、大容量のサンプルの遠心分離又は濾過などの他の増菌手順が必要となろう。しかしながら
、遠心分離は、遠心分離機が必要であり、特に、多数の大容量サンプルを検査する必要がある場合、一般に、厄介なプロセスである。
【0007】
濾過は、より高い処理能力で遂行でき、かつ大容量サンプル中に存在する少ない数の病原体でも濃縮することができる。病原体を濃縮するために、濾過法は、通常、標的病原体より小さい孔径を有する精密濾過(MF)膜フィルターを、一般に利用する。こうして、病原体は、そのようなフィルターで濃縮でき、いくつかの検出法、例えばコロニー形成及びDNAプローブハイブリダイゼーションにより検出することができる。しかしながら、これらの膜フィルターは、粒子捕捉能力(dirt-holding capacity)が非常に低く、その
小さい孔径のために、微粒状の食品抽出物により容易に目詰まりを起こす傾向がある。これらのフィルターは、飲料水や環境水などの微粒子をほとんど含有しないサンプル、又は非常に小容量の微粒子のサンプルに適する。適切な保持率を備えたデプスフィルターも、病原体の捕捉に使用されるが、しかしながら、そのようなデプスフィルターに捕捉された病原体の検出は、その3次元マトリックス構造及びフィルター厚さのため、より面倒である。
【発明の概要】
【0008】
本発明は、その実施形態として、以下のステップの1つ又は複数によってサンプル中の微生物を検出する方法に関する。
濾過中の目詰まりを防ぐように構成された孔を有し、かつ微生物を引きつけるように構成されたフィルターでサンプルを濾過して、微生物をフィルターに収集するステップ。
微生物の増殖を局在化させ及び/又は微生物検出試薬の蒸発を防止するように構成されるポリマーと、微生物検出試薬とをフィルターに添加するステップ。
検出できるレベルまで微生物を増殖させるのに十分な時間にわたりフィルターをインキュベートするステップ。
サンプル中に微生物の存在を検出するステップ。
【0009】
好ましい実施形態では、前記ポリマーはヒドロゲルである。好ましくは、ヒドロゲルは、環境感受性ヒドロゲルである。環境感受性ヒドロゲルは、環境的変化を受ける前は、少なくとも部分的にゾル形態であって、低粘度を有するが、環境的変化を受けると、粘度が増加し、少なくとも部分的にゲル形態となる。好ましい実施形態では、環境的変化は、温度、pH、入射光量、イオン濃度、圧力、磁場、電場、音波照射又は生化学的分子の濃度である。好ましい実施形態では、フィルターへの環境感受性ヒドロゲルの添加は、少なくとも部分的にゾル形態の環境感受性ヒドロゲルを有する溶液をフィルターに添加するステップと、環境的変化を起こして、この溶液をゲル化するステップとを含む。
【0010】
好ましい実施形態では、ヒドロゲルは、ヒドロゲル粒子である。好ましくは、ヒドロゲル粒子は、ヒドロゲル粒子の懸濁液を吸収、吸引、濾過又は浸漬及びスプレーするなどの方法により添加される。好ましい実施形態では、ヒドロゲル粒子は、フィルター孔より小さく、そのため、フィルター孔を効率的に塞ぐ。
【0011】
好ましい実施形態では、ヒドロゲルは、脱水形態でフィルター孔に添加され、次いでフィルター孔の内側で水和させる。好ましくは、脱水ヒドロゲルの水和は、1分から6時間の時間がかかる。好ましくは、脱水ヒドロゲルは、溶液の形態でフィルター孔に添加され、1分から6時間にわたるインキュベーションにより、孔の内側で水和させる。
【0012】
好ましい実施形態では、フィルターに加工されるポリマーは、粘着性ポリマー溶液である。粘着性ポリマー溶液は、フィルターに流入して、孔を満たし、微生物の増殖を効果的に局在化させる。好ましくは、粘着性ポリマー溶液には、水溶性ポリマー又はヒドロゲル懸濁液がある
【0013】
好ましい実施形態では、フィルターに加工される微生物検出試薬は、微生物の増殖を選択的に促進するように構成された増殖培地を含有する。好ましくは、増殖培地は、検出すべき微生物は耐性を持つが、他の生物は耐性を持たない選択的な試薬又は抗生物質を含むか、検出すべき微生物は迅速に増殖し及び/又は他の生物の増殖は緩慢もしくは阻害するように選択されたpH及び温度を含むか、又は検出すべき微生物によって容易に代謝されるが、他の生物によっては容易に代謝されない栄養素を含む。一部の好ましい実施形態では、増殖培地は、好気性菌の増殖に十分な量の酸素を含むか、又は嫌気性菌の増殖のために十分な量の酸素を含まない。
【0014】
好ましい実施形態では、検出ステップは、微生物の存在下でシグナルを生じるように構成されたシグナリング試薬からのシグナルを検出し、これにより微生物を検出することを含む。好ましくは、シグナリング試薬は、微生物に特異的な酵素のための基質、微生物に特異的な酵素のための発色性もしくは発蛍光性の基質、又は微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性もしくは発蛍光性の指示薬との組合せである。
【0015】
一部の好ましい実施形態では、シグナリング試薬は、検出すべき微生物又はこの微生物の細胞成分を認識する薬剤、例えば、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物である。好ましくは、この薬剤は、例えば染料分子、金属コロイド、ポリマー粒子、磁性粒子、半導体粒子、リポソーム、ポリマーソーム、タンパク質、酵素又は核酸からの標識を有する。
【0016】
本発明は、別の実施形態として、濾過中の目詰まりを防ぐように構成された孔と、微生物を引きつけるように構成されたフィルターとを有し、更に多孔質で球状のマイクロビーズの層も含む層状フィルター複合体を用いて、微粒子サンプルを濾過することにより、この微粒子サンプルから微生物を分離するステップを含む方法に関する。好ましくは、この方法は、フィルター中に固定化された微生物を検出するステップを含む。
【0017】
本発明の実施形態では、前記方法の濾過ステップ後に、微生物の検出又は増殖を阻害する物質を除去するのに十分な時間にわたりフィルターを洗浄するステップを含んでもよい。
【0018】
好ましい実施形態では、前記方法でのフィルターは、繊維状物質を有するデプスフィルターである。好ましくは、繊維状物質は、セルロース繊維又はガラスマイクロファイバーである。
【0019】
好ましくは、フィルターは、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、又は生物的相互作用などの相互作用によって微生物を引きつけるように構成されている。好ましい実施形態では、微生物を認識する薬剤は、フィルターマトリックス上に特異的に又は非特異的に固定化される。薬剤は、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物であってよい。
【0020】
好ましい実施形態では、前記方法におけるフィルターは、更に、多孔質で球状のマイクロビーズの層を含む。一部の好ましい実施形態では、この多孔質球状マイクロビーズの層は、フィルターの上流側の面に配置される。一部の好ましい実施形態では、多孔質球状マイクロビーズの層は、メッシュ支持体の上流側の面に配置される。メッシュ支持体は、フィルター上に又はフィルターの上流側に配置される。
【0021】
好ましい実施形態では、多孔質球状マイクロビーズの層は、均等又はグレーデッド(graded)層を形成する。好ましくは、多孔質球状マイクロビーズの層表面は、極めて不活性で
あり、微生物に対する非特異的な結合が低い。
【0022】
好ましい実施形態では、マイクロビーズの直径は1〜1000μmであり、より好ましくは、マイクロビーズの直径は15〜600μmであり、更により好ましくは、マイクロビーズの直径は50〜300μmである。好ましくは、マイクロビーズの孔径は、微生物のサイズより小さく、微生物は、濾過ステップの間、マイクロビーズの間を通過する。一部の好ましい実施形態では、マイクロビーズは、架橋された親水性ポリマーを含む。
【0023】
一部の好ましい実施形態では、濾過ステップの後に、洗浄液を添加することにより多孔質球状マイクロビーズ層を破壊し、その後、マイクロビーズを懸濁させ、洗浄液をフィルターで濾過する。
【0024】
本発明は、その実施形態として、以下の構成要素のうち1つ又は複数を含む微生物検出キットに関する。
濾過中の目詰まりを防ぐように構成された孔を有し、かつ微生物を引きつけるように構成されたフィルター。
微生物の存在を検出するように構成された微生物検出試薬。
微生物の増殖を局在化するように及び/又は微生物検出試薬の蒸発を防止するように構成されたポリマー。
【0025】
好ましい実施形態では、フィルターは、繊維状物質を有するデプスフィルターである。好ましくは、繊維状物質は、セルロース繊維及びガラスマイクロファイバーから選択される。
【0026】
好ましくは、フィルターは、例えば静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物相互作用などの相互作用によって微生物を引きつけるように構成されている。
【0027】
好ましい実施形態では、微生物を認識する検出試薬は、フィルターマトリックス上に特異的に又は非特異的に固定化される。薬剤は、好ましくは、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物である。
【0028】
好ましい実施形態では、キットのポリマー成分はヒドロゲルである。好ましくは、ヒドロゲルは、環境感受性ヒドロゲルであり、これは、少なくとも部分的にゾル形態である。環境感受性ヒドロゲルは、環境的変化を受ける前は低粘度を有し、環境的変化を受けると、粘度が増加し、少なくとも部分的にゲル形態になる。好ましくは、環境的変化は、温度、pH、入射光量、イオン濃度、圧力、磁場、電場、音波照射又は生化学的分子濃度の変化である。
【0029】
好ましい実施形態では、ヒドロゲルは、ヒドロゲル粒子である。好ましくは、ヒドロゲル粒子は、フィルター孔より小さく、そのため、フィルター孔を効率的に塞ぐ。更に好ましくは、ヒドロゲルは、脱水形態であってよい。
【0030】
好ましい実施形態では、キット中のフィルターは、多孔質で球状のマイクロビーズの層も含む。一部の好ましい実施形態では、この多孔質球状マイクロビーズの層は、フィルターの上流側の面に配置される。一部の好ましい実施形態では、多孔質球状マイクロビーズの層は、メッシュ支持体の上流側の面に配置され、メッシュ支持体は、フィルター上に又はフィルターの上流側に配置される。
【0031】
好ましい実施形態では、多孔質球状マイクロビーズ層は、均等な又はグレーデッドな層
を形成する。好ましい実施形態では、多孔質球状マイクロビーズ層の表面は、極めて不活性であり、微生物に対する非特異的な結合が低い。
【0032】
好ましい実施形態では、マイクロビーズの直径は1〜1000μmであり、更に好ましくは、マイクロビーズの直径は15〜600μmであり、更になお好ましくは、マイクロビーズの直径は50〜300μmである。
【0033】
好ましい実施形態では、マイクロビーズの孔径は、微生物のサイズより小さく、そのため微生物は、濾過ステップの間、マイクロビーズの間を通過する。一部の好ましい実施形態では、マイクロビーズは、架橋された親水性ポリマーを含む。
【0034】
好ましい実施形態では、キット中の微生物検出試薬は、微生物の増殖を選択的に促進するように構成された増殖培地を含有する。好ましくは、増殖培地は、検出すべき微生物は耐性を持つが、他の生物は耐性を持たない選択的な試薬又は抗生物質を含むか、検出すべき微生物を迅速に増殖し及び/又は他の生物の増殖は緩慢にもしくは阻害するように選択されたpH及び温度を含むか、又は検出すべき微生物によって容易に代謝されるが、他の生物によっては容易に代謝されない栄養素を含む。一部の好ましい実施形態では、増殖培地は、好気性菌の増殖に十分な量の酸素を含むか、又は嫌気性菌の増殖のために十分な量の酸素を含まない。
【0035】
好ましい実施形態では、増殖培地は、微生物の存在下でシグナルを生じることにより、微生物を検出するように構成されたシグナリング試薬を含む。好ましくは、シグナリング試薬は、微生物に特異的な酵素、微生物に特異的な酵素のための発色性もしくは発蛍光性の基質、又は微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性もしくは発蛍光性の指示薬との組合せである。
【0036】
一部の好ましい実施形態では、シグナリング試薬は、検出すべき微生物又はこの微生物の細胞成分を認識する薬剤であり、例えば、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物であり、好ましくは、薬剤は、例えば染料分子、金属コロイド、ポリマー粒子、磁性粒子、半導体粒子、リポソーム、ポリマーソーム、タンパク質、酵素及び核酸等の標識を含む。
【0037】
本発明は、その実施形態として、濾過中の目詰まりを防ぐように構成された孔を有するとともに微生物を引きつけるように構成された濾過媒体(filter medium)と、多孔質で
球状のマイクロビーズ層とを含む微生物検出用の層状フィルター複合体に関する。
【0038】
好ましい実施形態では、層状フィルター複合体中の濾過媒体は、繊維状物質を有するデプスフィルターである。好ましくは、繊維状物質は、セルロース繊維又はガラスマイクロファイバーである。
【0039】
好ましい実施形態では、層状フィルター複合体の濾過媒体は、例えば静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物的相互作用などの相互作用によって微生物を引きつけるように構成されている。好ましい実施形態では、微生物を認識する薬剤は、フィルターマトリックス上に特異的に又は非特異的に固定化され、薬剤は、抗体、抗原、アプタマー、タンパク質、核酸及び炭水化物から選択される。
【0040】
好ましい実施形態では、層状フィルター複合体中の多孔質球状マイクロビーズの層は、フィルターの上流側の面に配置される。他の好ましい実施形態では、多孔質球状マイクロビーズの層は、メッシュ支持体の上流側の面に配置され、メッシュ支持体は、フィルター上に又はフィルターの上流側に配置される。好ましくは、多孔質球状マイクロビーズ層は
、均等な又はグレーデッドな層を形成する。好ましくは、多孔質球状マイクロビーズ層の表面は、極めて不活性であり、微生物への非特異的な結合が低い。
【0041】
好ましい実施形態では、マイクロビーズの直径は1〜1000μmであり、更に好ましくは、マイクロビーズの直径は15〜600μmであり、更になお好ましくは、マイクロビーズの直径は50〜300μmである。好ましい実施形態では、マイクロビーズの孔径は、微生物のサイズより小さく、そのため微生物は、濾過ステップの間、マイクロビーズの間を通過する。一部の実施形態では、マイクロビーズは、架橋した親水性ポリマーを含む。
【0042】
本発明は、その実施形態として、多孔質フィルターに関し、これは、膨潤し得るが、水に溶解しない3次元高分子網目構造体であるヒドロゲルと、濾過中の目詰まりを防ぐように構成された孔を有するとともに微生物を引きつけるように構成されたフィルターとを含む。
【0043】
好ましい実施形態では、多孔質フィルターのヒドロゲルは、脱水形態である。
【0044】
好ましい実施形態では、フィルターは、繊維状物質を含むフィルターマトリックスを有する。
【0045】
好ましい実施形態では、ヒドロゲルの3次元高分子網目構造体には、例えば、寒天、キトサン、セルロース、カラギーナン、アルギネート、アクリレートポリマー及びコポリマー、ポリエチレングリコール、ポリグリコール酸、ポリ乳酸、ペクチン、ローカストビーンガム、ポリヒドロキシブチレート(PHB)、ポリヒドロキシバレレート(PHV)、ポリカプロラクトン、ポリジオキサノン、ポリアンヒドリド、ポリシアノアクリレート、ポリアミノ酸、ポリオルトエステル、ポリホスファゼン、ポリプロピレンフマレート、ポリアルキレンオキサレート、シリコーンポリマー、コラーゲン、フィブリノゲン、フィブリン、ゼラチン、デンプン、アミロース、デキストラン、シルク、ケラチン、エラスチン、アクチン、ミオシン、グリコサミノグリカン又はポリビニルアルコール等のポリマーがある。
【0046】
好ましい実施形態では、フィルターは、例えば、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物的相互作用などの相互作用によって微生物を引きつけるように構成されている。
【0047】
好ましい実施形態では、微生物を認識する薬剤は、フィルターマトリックス上に特異的に又は非特異的に固定化される。好ましくは、前記薬剤は、金属水酸化物又は金属酸化物、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物から選択される。好ましくは、金属水酸化物又は金属酸化物は、水酸化ジルコニウム、水酸化チタン、酸化ハフニウム、ヒドロキシアパタイト、酸化鉄、酸化チタン又は酸化アルミニウムである。
【0048】
好ましい実施形態では、フィルターは、微生物検出試薬を含有し、かつ微生物含有サンプルの濾過の間にわたりこの微生物検出試薬を保持する。好ましくは、微生物検出試薬は、検出すべき微生物の増殖を選択的に促進するように構成された増殖培地と、微生物の存在下でシグナルを生じるように構成されたシグナリング試薬とを含む。好ましくは、増殖培地は、検出すべき微生物は耐性を持つが、他の生物は耐性を持たない選択的な試薬又は抗生物質を含むか、検出すべき微生物は迅速に増殖し及び/又は他の生物の増殖は緩慢にもしくは阻害するように選択されたpH及び温度を含むか、又は検出すべき微生物によって容易に代謝されるが、他の生物によっては容易に代謝されない栄養素を含む。一部の好ましい実施形態では、増殖培地は、好気性菌の増殖に十分な量の酸素を含むか、又は嫌気
性菌の増殖のために十分な酸素を含まない。
【0049】
好ましい実施形態では、シグナリング試薬は、微生物に特異的な酵素のための基質、微生物に特異的な酵素のための発色性又は発蛍光性の基質、及び微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性又は発蛍光性の指示薬との組合せから選択される。
【0050】
好ましい実施形態では、シグナリング試薬は、検出すべき微生物又はこの微生物の細胞成分を認識する薬剤であり、例えば抗体、抗原、アプタマー、タンパク質、核酸及び炭水化物等である。好ましくは、この薬剤は、例えば染料分子、金属コロイド、ポリマー粒子、磁性粒子、半導体粒子、リポソーム、ポリマーソーム、タンパク質、酵素又は核酸等の標識を含む。
【0051】
本発明は、その実施形態として、以下のステップのうちの1つ又は複数のステップを含むサンプル中の微生物を検出する方法における前記多孔質フィルターの使用に関する。
サンプルを前記多孔質フィルターにより濾過して、微生物を固定化するステップ。
微生物を検出可能なレベルまで増殖させるのに十分な時間にわたりフィルターをインキュベートするステップ。
シグナリング試薬を使用して微生物を検出するステップ。
【0052】
一部の好ましい実施形態では、濾過後に、多孔質フィルターは溶解する。例えば、多孔質フィルターは、分解性ポリマーを含んでよい。好ましくは、分解性ポリマーは、例えば繊維、表面コーティング、ビーズ、粒子、シート又は層などの形状で提供される。一部の好ましい実施形態では、分解性ポリマーは、加水分解、酸化又は酵素機構を介して、溶液となる。
【0053】
一部の実施形態では、この分解性多孔質フィルターは、以下のステップのうちの1つ又は複数によりサンプル中の微生物を検出する方法に使用される。
(a)サンプルをフィルターで濾過して、微生物を固定化するステップ。
(b)分解性フィルターを分解して溶液にするステップ。
(c)この溶液から、微生物又は微生物に特異的な分子マーカーを抽出するステップ。
(d)微生物又は微生物に特異的な分子マーカーを検出して、サンプル中の微生物の存在を確認するステップ。
【0054】
本発明の他の態様、特徴及び利点は、後述する好ましい実施形態の詳細な説明から明らかとなろう。
【0055】
以下に、図面を参照して、本発明の上述した特徴及び他の特徴を説明するが、この図面の好ましい実施形態は、本発明を図解することを意図するものであり、本発明を限定するものではない。
【図面の簡単な説明】
【0056】
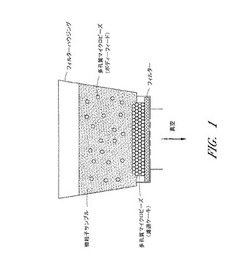
【図1】多孔質の球状ビーズを用いた濾過の概略図を示す。
【図2】環境感受性ヒドロゲルを使用する病原体検出アッセイ手順のステップの概略図を示す。
【図3】ヒドロゲルマイクロビーズを使用する病原体検出アッセイ手順のステップの概略図を示す。
【図4】ヒドロゲル複合フィルターの種々の構造を示す。図4Aは、ヒドロゲルがフィルターマトリックス層の間に位置する実施形態を示す。図4Bは、ヒドロゲル粒子がフィルターマトリックス層の間に位置する実施形態を示す。図4Cは、ヒドロゲル粒子がフィルターマトリックス全体にわたり分散している実施形態を示す。図4Dは、ヒドロゲル繊維がフィルターマトリックスを形成している実施形態を示す。
【図5】病原体検出試薬が装入されたスマートヒドロゲル粒子を含む複合ヒドロゲルフィルターを示す。
【図6】分解性フィルターの種々の構造を示す。図6Aは、フィルター膜が分解性粒子からできている実施形態を示す。図6Bは、フィルター膜が分解性繊維からできている実施形態を示す。図6Cは、フィルター膜が分解性コーティングを備えた水溶性粒子からできている実施形態を示す。
【図7】分解性フィルターを使用して病原体を収集かつ検出するアッセイを図解する。
【図8】ガラスファイバーデプスフィルターで濾過した10%全乳サンプル250mLについての病原体検出アッセイの結果を示す。図8A及び8Bは、リステリア細胞200cfuを接種した乳サンプルの30℃で40時間インキュベートした後の結果を示す。図8C及び8Dは、リステリア細胞を含まない乳サンプルの30℃で40時間インキュベートした後の結果を示す。
【図9】ヒドロゲル微粒子の顕微鏡画像を示す。微粒子は、より高いコントラストをつけるため、トリパンブルーで染色した。
【図10】陽電荷フィルターで濾過した病原体検出アッセイの結果を示し、図10A〜図10Eは、BHIブロス10mL当たりリステリア細胞235、23.5、2.35、0.235及び0cfuについての結果である。
【図11】10%デリ・ミート(A)及び10%スティックチーズホモジネート(B)に関して、多孔質マイクロビーズ2gと共に陽電荷デプスフィルターを使用する濾過速度(黒丸)、無孔ガラスビーズ15gと共に陽電荷デプスフィルターを使用する濾過速度(黒四角)及び濾過補助材無しで陽電荷デプスフィルターを使用する濾過速度(黒三角)を示す。
【図12】幾つかのグレードの多孔質球状マイクロビーズ濾過補助材:架橋ポリメタクリレートマイクロビーズ(直径45〜90μm:0.5g(白丸)、1.0g(黒丸))、及び架橋デキストランマイクロビーズ(直径17〜70μm:0.5g(白四角)、直径35〜140μm:0.5g(ひし形)、直径86〜258μm:0.5g(白三角)、1.0g(黒三角)、直径170〜520μm:0.5g(×))と共にガラスファイバーデプスフィルターを使用して、10%デリ・ミート(A)及び10%フランクフルトソーセージホモジネート(B)を濾過する速度を示す。
【図13】ガラスファイバーデプスフィルター及び多孔質マイクロビーズ濾過補助材により濾過された、10%デリ・ミートホモジネートの〜225mL(デリ・ミート25g)当たりリステリア細胞220cfu(図13A、13B)、22cfu(図13C、13D)及び0cfu(図13E、13F)に関する病原体検出アッセイの結果を示す。図13A、13C及び13Eは、30℃で24時間のインキュベーション後の結果を示し、図13B、13D及び13Fは、30℃で40時間のインキュベーション後の結果を示す。
【図14】ガラスファイバーデプスフィルター及び多孔質マイクロビーズ濾過補助材により濾過された10%デリ・ミートホモジネート〜225mL(デリ・ミート25g)中の病原体検出アッセイの結果を示す。図14Aの表は、フィルターの上流側(上部)及び下流側(底部)から観察される着色スポットの数をまとめたものである。図14Bは、観察された着色スポットの総数を、接種された病原体濃度に対してプロットしたものである。黒丸及び白丸は、リステリア・モノサイトゲネスとリステリア・イノキュアをそれぞれ示す。
【図15】加工フィルターによるアッセイの結果を示し、インキュベーション後にフィルター上に見出されるリステリア細胞を示す。
【図16】スマートヒドロゲルにより固定化された病原体検出試薬を有する複合フィルターについてのアッセイの結果を示す。
【図17】病原体検出のための分解性フィルターについてのアッセイのPCR結果を示す。サイクルは、PCRサイクル数を示し、ΔRNは、基準強度を控除した後の各反応における規格化相対蛍光強度を示す。
【発明を実施するための形態】
【0057】
ここに記載する実施形態は本発明の好ましい実施形態であるが、当然ながら、本発明の精神から逸脱しない範囲で種々の改変が当業者によって行われるであろう。したがって、本発明の範囲は、添付の特許請求の範囲のみによって決定されるべきである。
【0058】
本開示は、低コストで且つ短い実践時間で、大容量の微粒子サンプル中の病原体を高感度で検出することを可能にする方法、この方法で使用されるフィルターの製作、及びこの方法における多孔質球状マイクロビーズの濾過補助材の使用に関する。
【0059】
超多孔質のフィルター、多孔質球状マイクロビーズ濾過補助材及びヒドロゲル材料を使用する病原体検出濾過アッセイ
本開示の方法は、一実施形態として、大容量の微粒子サンプルから病原体を効率よく濃縮するために、病原体吸着能力及び高い粒子捕捉能力を有する超多孔質のフィルターを利用するものである。本開示の方法の実施形態に有用な超多孔質のフィルターは、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、又は生物的相互作用により標的病原体を引きつけることができ、また微粒子サンプルによるフィルターの目詰まりを十分に防止できる多孔質なものがよい。特定の実施形態では、配置されたフィルターは、高い粒子捕捉能力及び病原体捕捉能力を提供する3次元マトリックスを備えたデプスフィルターである。有用なデプスフィルターは、例えばガラスファイバー及びニトロセルロース繊維などの繊維状物質から製造されていてよく、単層又は同じか若しくは異なる粒子保持率を有する多層のフィルターからなる。フィルターは、病原体を効果的に捕捉し、かつサンプル中の粒子によるフィルター目詰まりを回避するのに適切である粒子保持率及び厚さを有する。例えば、長さ0.5〜2μm、直径0.4〜0.5μmである病原体、例えばリステリア等をデプスフィルターに捕捉するためには、デプスフィルターの適切な粒子保持率は、0.1〜10μm、好ましくは0.7〜2.4μmであろう。また、フィルターは、濾過の間にかけられる真空力又は圧力に耐えるのに十分な機械的強度を有する。
【0060】
他の実施形態では、病原体表面が、通常、その中に含有されるリポ多糖類、テイコ酸及び表面タンパク質のために正味の陰電荷を有するので、フィルターは、陽性電荷を使用して病原体を引きつけるデプスフィルターである。病原体は、フィルターマトリックによってではなく、フィルター上の陽性電荷により固定化され得、従って、フィルター多孔度を更に増し、かつより高い粒子捕捉能力を得て、フィルターの目詰まりを更に効果的に回避することができる。陽性電荷は、フィルターマトリックスをカチオン性分子で表面コーティングすることにより、又は陽性物質から製造された陽性コロイド、粒子もしくは繊維を組み入れることにより提供することができる。陽性物質の例は、金属水酸化物及び金属酸化物、例えば、水酸化ジルコニウム、水酸化チタン、酸化ハフニウム、酸化鉄、酸化チタン、酸化アルミニウム及びヒドロキシアパタイト、である。好ましくは、金属水酸化物又は金属酸化物の等電点は、サンプルと検出試薬のpH値より高くあって良い。ステノトロホモナス・マルトフィリア(Stenotrophomonas maltophilia)などの正電気を帯びたバクテリアの例が、ごく稀にある。そのような微生物は、陽性電荷ではなく陰性電荷を使用して、前記の陽電荷フィルターと同様にして製造できる陰性電荷を有するフィルターにより一層容易に保持することができる。
【0061】
他の実施形態では、フィルターは、病原体認識剤、例えば、抗体、抗原、タンパク質、核酸、炭水化物、アプタマー、又はバクテリオファージを含む。これらの病原体認識剤は、サンプル中に発見される他の病原体に対して、病原体を選択的又は非選択的に認識でき
、かつ化学結合、物理結合又は他の標準固定法により、フィルターマトリックス上に固定化することができる。特定の実施形態では、病原体認識剤は、トール様受容体(TLR)であり、これは、種々の微生物の表面に存在する構造的に保存された分子を認識する。TLR2は、グラム陽性ペプチドグリカン及びリポテイコ酸を認識でき、かつTLR4は、グラム陰性バクテリア上のリポ多糖類を認識できる。
【0062】
フィルターの他に、本開示は、検査すべきサンプル中の微粒子によるフィルター目詰まりを防止するための多孔質球状マイクロビーズ濾過補助材の使用に関する(図1)。有用なマイクロビーズは、小さいサイズで分布する球状の、回転楕円体形状の又は楕円体形状の多孔質マイクロビーズであってよい。このマイクロビーズは立方最密構造や六方細密構造などの最密構造又はそれに近い構造をとることができる。検査すべき病原体が、サンプル濾過時に、マイクロビーズの間を通過するために、マイクロビーズは、通常は、直径を1〜1000μm、好ましくは15〜600μm、更に好ましくは50〜300μmにしてもよい。有用なマイクロビーズは、水、緩衝液、増殖培養液又はサンプル溶液に、浮くのではなく、懸濁するのに適切な比重を有する。マイクロビーズは、通常、標的病原体より小さい孔を有することで、サンプル濾過時に病原体が多孔質球状マイクロビーズの孔の内側に留まるのを阻むことができる。好ましくは、マイクロビーズは、不活性表面、好ましくは親水性表面を有してよく、かつタンパク質、核酸、炭水化物、バクテリア、ウィルス及び細胞を含む生体分子及び微生物への非特異的な結合は低い。特定の実施形態では、マイクロビーズ濾過補助材は、例えばポリメタクリレートやデキストランなどの架橋ポリマーから製造されている。場合により、マイクロビーズは、その多孔質構造のため、後段の検出を阻害し得る物質を除去できる。
【0063】
大容量の微粒子サンプルを少なくとも次の手法又はその組合せの1つで濾過するのを支援するために、多孔質球状マイクロビーズの濾過補助材を使用することができる。濾過補助材の配置としては、サンプルの濾過前に、病原体吸着能力を有する超多孔質のフィルターの上流側の面上に、多孔質球状マイクロビーズの均等な又はグレーデッドな層を配置することができる。又は、濾過前に、微粒子サンプルに濾過補助材を添加して、サンプル濾過時に多孔質球状マイクロビーズ層を形成することにより、マイクロビーズの新層を連続的に設け、濾過を更に改良することができる。サンプル濾過後に、濾過補助材層を容易に除去するために、超多孔質のフィルターと濾過補助材層の間にメッシュ支持体を配置できる。場合により、マイクロビーズ表面への病原体の結合を最小にするために、使用前に、多孔質マイクロビーズ濾過補助材は、ペプチド又はタンパク質などのブロッキング試薬含有溶液中に懸濁させるか又はプレインキュベートする。
【0064】
検出すべき病原体は、マイクロビーズの間を通過し、マイクロビーズの表面上又は孔中に捕捉されることはない。他方で、濾過補助材層を含まないフィルターを通常目詰まりさせるサンプル中の粒子は、マイクロビーズ表面上及び多孔質球状マイクロビーズ間の間隙に捕捉されるであろう。マイクロビーズの多孔質構造のために、濾過時のサンプル流は、ビーズの間を通過するだけでなく、マイクロビーズ自体にも浸透し、そのため、サンプル粒子は、ビーズ間の間隙よりもビーズ表面に捕捉される傾向があり、そのことにより多孔質球状濾過補助材層は、高い粒子捕捉能力をもたらし、大容量微粒子サンプルの濾過の際のフィルターの目詰まりを防止できる。サンプルの完全な濾過後に、濾過補助材層を崩壊させて、マイクロビーズを洗浄溶液中に懸濁させることができる。この洗浄溶液を濾過して、微粒子サンプルの最初の濾過の間に濾過補助材層に捕捉される病原体を収集できることにより、フィルターへの病原体固定化収量を改良することができる。この洗浄プロセスを数回繰り返して、フィルターへの病原体の回収量を最大にすることができる。洗浄溶液は、一般に、病原体に悪影響を及ぼさない緩衝溶液又は増殖培養液である。
【0065】
フィルターと濾過補助材に加え、本開示は、病原体検出反応の間の病原体検出試薬の蒸
発を防ぎ、フィルター中で病原体の増殖を局在化させるために、ポリマー材料を使用することにも関する。有用なポリマー材料には、多糖類及びタンパク質などの天然又は合成ポリマーがある。ポリマー材料の幾つかの例には、寒天、アルギネート、カラギーナン、セルロース、キトサン、デキストラン、ペクチン、コラーゲン、フィブリノゲン、アクリレートポリマー、ポリエチレングリコール、ポリビニルアルコール並びにこれらの誘導体及びコポリマーがあるが、これらに限定はされない。ポリマー材料は、分子内及び/又は分
子間架橋によりヒドロゲルを形成することが望ましい。ヒドロゲルは、膨潤し得るが水に不溶であり、かつ一定の期間、蒸発せずに水又は溶液を保持し得る3次元高分子網目構造体である。
【0066】
特定の実施形態では、ヒドロゲルは、環境感受性ヒドロゲルである。有用な環境感受性ヒドロゲルは、環境からの刺激、例えば、温度、pH、光、イオン、圧力、磁場、電場、音波照射又は生化学的分子の1つ又は複数に応答し得る。環境感受性ヒドロゲルが、ゾル形態である場合、物質は水溶性ポリマーの形状であるが、刺激を与えた結果として、物質はゲル形態(ヒドロゲル)に変換され、不水溶性となり、分子内又は分子間架橋される。ゾル形態とゲル形態の間の変換は完全に又は部分的に起こり得る。特定の実施形態では、環境感受性ヒドロゲル及び環境的刺激は、特に生存病原体を検出すべき場合、病原体に有害ではない。特定の実施形態では、ゾル形態は、孔を容易に充填するためには、フィルター孔に容易に流入できないほど高粘性であってはならない。ゲル形態は、病原体検出試薬の蒸発を防止し、病原体の増殖を効果的に局在化させる。環境感受性ヒドロゲルの幾つかの例には、アガロース、低融点アガロース、カラギーナン、ペクチン、メチルセルロース及びPluronic F127があるが、これらに限定はされない。アガロースは、〜45℃でゾル形態であり、〜37℃まで冷却するとゲルとなる。低融点アガロースは、〜37℃でゾル形態であり、〜20℃でゲル形態である。カラギーナン及びペクチンは、カリウム及びカルシウムなどの特定のイオンの不在下でゾル形態であり、これらのイオンを添加するとゲルとなる。メチルセルロース及びPluronic F127は、〜4℃でゾル形態であり、〜37℃まで加温後にゲル形態となる。特定の実施形態では、適切なヒドロゲルの濃度は、種々のヒドロゲルに応じて変化し得る。特定の実施形態では、アガロース又は低融点アガロースの適切な濃度は、0.01%〜30%、好ましくは0.1%〜10%、更に好ましくは0.5%〜5%である。特定の実施形態では、サンプルの濾過後に、吸収、吸引、毛管作用、濾過、浸漬、スプレー又は他の技術によりゾル形態をデプスフィルター孔に添加することができ、環境からの刺激によりゲル形態に変換することができる。
【0067】
特定の実施形態では、サンプル濾過後に、フィルター孔はヒドロゲル粒子で充填される。ヒドロゲル粒子は、単分散系又は多分散系であって良い。ヒドロゲル粒子の有用な形状は、球形、四面体、六面体、多面体又は円柱形であるが、これらに限定はされない。しかしながら、任意の規則的又は不規則的な形状を使用することもできる。フィルター孔をヒドロゲル粒子で効果的に充填するために、ヒドロゲル粒子は、フィルター孔より小さく、フィルター孔に入り込むことができる。場合により、ヒドロゲル粒子は、フィルター中に保持されるのに十分なほどに大きく、かつ超多孔質のフィルターの保持率より大きくて良い。フィルター孔へのヒドロゲル粒子の加工は、吸収、吸引、毛管作用、濾過、浸漬、スプレー又は他の技術により遂行できる。有用なヒドロゲル粒子は、幾つかの慣用技術、例えば鋳造、乳化重合/ゲル化、沈殿重合、膜乳化、切断、スライス及び破砕などにより合成又は調製することができる。一部の実施形態では、ヒドロゲル粒子は、アガロースゲルから製造され、適切なアガロース濃度は、0.01%〜10%(w/v)、更に好ましくは0.1%〜5%(w/v)である。
【0068】
特定の実施形態では、フィルター孔は、脱水ヒドロゲルの水和作用によって満たされる。脱水ヒドロゲルが水和の際に膨潤すると、ヒドロゲル容積は劇的に増加する。脱水ヒド
ロゲルは、吸収、吸引、毛管作用、濾過、浸漬、スプレー又は他の技術により、フィルター孔に加工でき、脱水ヒドロゲルの水和は、例えば、水、緩衝液又は増殖培養液などの溶液により加工した後に行うことができる。特定の実施形態では、脱水ヒドロゲルは、単分散又は多分散粒子であり、脱水ヒドロゲル粒子のサイズは、フィルター孔に効果的に入るのに十分な小ささで良い。脱水ヒドロゲル粒子は、加熱、乾燥、凍結乾燥及び任意の他の技術によってヒドロゲル粒子を脱水することにより、調製することができる。特定の実施形態では、脱水ヒドロゲル粒子の水和作用は、10秒〜6時間、更に有利には1〜30分に及ぶ一定の時間がかかり、そのため、水和前に、溶液に懸濁する脱水ヒドロゲル粒子を前記技術によりフィルター孔に添加し、次いで孔内部をインキュベーションにより水和させることができる。
【0069】
特定の実施形態では、フィルター孔は、高粘性ポリマー溶液で充填される。この溶液は、フィルター孔に容易に流入し、孔を容易に充填することができないほど粘性が高くはないが、病原体の増殖を効果的に局在化するのに十分なほどの粘性がある。ポリマー溶液として、水溶性ポリマー又はヒドロゲル懸濁液を挙げることができる。
【0070】
特定の実施形態では、病原体検出試薬は、病原体の増殖培地を含有する。増殖培地は、通常、病原体増殖のための種々の塩、炭素源、窒素源及びアミノ酸の1つ又は複数を含む。特定の実施形態では、増殖培地は、選択的培地であり、抗菌作用/抗真菌効果、温度もしくはpH耐性又は特定の代謝産物の合成能力により、選択的に特定の病原体の増殖を促進し、そうして病原体を、他の競合バクテリア又は微生物に対し選択的に増殖させることができる。一部の実施形態では、病原体検出試薬は、増殖培地の酸素濃度を減らすことにより、特定の病原体の増殖を促進するか又は損傷した病原体の蘇生を促進する化合物、例えばL−システイン及びOxyrase(Oxyrase Inc.,Mansfield,OH)、を含有することができる。
【0071】
一部の実施形態では、病原体検出試薬は、他のバクテリア又は微生物から病原体を識別するシグナリング試薬を含有してよい。前記シグナリング試薬の一例は、病原体に特異的な酵素のための発色性又は発蛍光性の基質である。前記基質の例には、X−、ラピス(Lapis)−、マゼンタ(Magenta)−、サーモン(Salmon)−、グリーン(Green)−、ON
P−及びMU−結合基質、例えばβ−D−グルクロニド、β−D−ガラクト−ピラノシド、β−D−グルコ−ピラノシド、N−アセチル−β−D−ガラクトサミニド、N−アセチル−β−D−グルコサミニド、カプリレート−ノナノエート、ブチレート、myo−イノシトール−1−ホスフェート及びホスフェートがある。前記シグナリング試薬の別の例は、フェノールレッドなどのpH指示薬とキシロースなどの病原体特異的酵素用基質との組合せである。基質の代謝は、検出試薬のpHを変え、かつpH指示薬は比色法でpH変化を示す。前記シグナリング試薬の他の例は、病原体もしくは病原体特異的細胞成分を認識するDNA、RNA、LNA、PNAを含む核酸もしくは他の核酸、抗体、抗原、又はアプタマーである。これらのプローブ分子を、シグナル生成のため、蛍光染料分子、金又は銀コロイド、ポリマー粒子、磁性粒子、半導体粒子、量子ドット、フォトニック結晶粒子、リポソーム、ポリマーソーム、酵素、タンパク質及び核酸により標識化することができる。
【0072】
特定の実施形態では、環境感受性ヒドロゲルを使用する大容量の微粒子サンプル中の病原体の検出は、以下のステップを含む(図2)。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、超多孔質のフィルターと多孔質マイクロビーズ濾過補助材とを含む層状フィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)もし必要な場合は、フィルターへの病原体の回収率を最大にし、かつ病原体検出アッセイの潜在的な阻害剤を除去するために、フィルターと多孔質マイクロビーズ濾過補助
材を洗浄するステップ。
(3)フィルターを回収し、病原体検出試薬を含有する環境感受性ヒドロゲルのゾル形態を用いて、吸収、浸漬、スプレー又は他の技術によりフィルター孔に充填するステップ。(4)環境的刺激を与えて、環境感受性ヒドロゲルのゾル形態をゲル形態に変換するステップ。
(5)病原体を検出可能にするために病原体の増殖に十分な時間、ヒドロゲルを含有するフィルターをインキュベートするステップ。
(6)シグナリング試薬を使用して増殖病原体を検出するステップ。
【0073】
特定の実施形態では、ヒドロゲル粒子を使用する、大容量微粒子サンプル中の病原体の検出は、以下のステップを含む(図3)。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、超多孔質のフィルターと多孔質マイクロビーズ濾過補助材とを含む層状フィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)もし必要な場合は、フィルターへの病原体の回収率を最大にし、かつ病原体検出アッセイの潜在的な阻害剤を除去するために、フィルター及び/又は多孔質マイクロビーズ濾過補助材を洗浄するステップ。
(3)フィルターを回収し、病原体検出試薬を含有するヒドロゲル粒子を用いて、フィルター孔に充填するステップ。
(4)ヒドロゲル及び粒子を含有するフィルターを、病原体を検出可能にするために病原体の増殖に十分な時間、インキュベートするステップ。
(5)シグナリング試薬を使用して増殖病原体を検出するステップ。
【0074】
場合により、損傷した病原体の蘇生及び検出のために、サンプルの濾過及び病原体検出の前に、損傷した病原体の蘇生を可能にする増殖培地又は溶液中で微粒子サンプルを調製し、かつインキュベートできる。或いは、損傷した病原体は、サンプル濾過後に、インキュベーション(損傷した病原体の蘇生を可能にする増殖培地、溶液又は環境中で行なわれ得る)によりフィルター中で蘇生させ、病原体検出試薬により検出することができる。或いは、病原体検出試薬は、損傷した病原体を蘇生させるように構成され、かつ本明細書に記載のヒドロゲル物質を含有する又は含有しない状態で、追加の試薬、例えば抗生物質、の補充により、病原体検出試薬の濃度、成分又はpHをインキュベーションの間に変化させることができ、これにより、損傷病原体を蘇生させ、かつ検出することができる。
【0075】
微粒子サンプルの濾過及びヒドロゲル含有検出試薬の適用は、手作業を必要とし、これらのプロセスは、1時間以内に終了することができる。これらのプロセスは、標準的な自動化装置を使用して、容易に自動化することができる。病原体増殖及び検出のために必要なインキュベーション時間は、病原体の倍加時間と、シグナリング試薬の感度に依存する。フィルター中の1個の病原体を検出するのに必要とされるインキュベーション時間を、表1に示す。感度の低い発色基質を使用して、病原体を確認した場合ですら、全アッセイは、非常に短い実践時間で、24時間以内に終了することができる。
【0076】
【表1】

【0077】
特定の実施形態では、病原体を超多孔質フィルターへ固定後に、代替の病原体検出アッセイを使用することができる。1つの有用な病原体検出法は、ヒドロゲルを含まずに、病原体に特異的な酵素基質を含む選択的な培地中におけるフィルターインキュベーションである。発色性もしくは発蛍光性の酵素基質、又はフェノールレッドなどのpH指示薬とキシロースなどの病原体特異的酵素用基質との組合せを使用して、病原体を検出できる。培地の光学密度、光吸収、又は蛍光強度は、インキュベーション後に又はインキュベーションの間にわたり、測定又はモニターして、病原体の存在を検出することができる。又は培地中で増殖された病原体を慣用の病原体検出アッセイ、例えばポリメラーゼ連鎖反応(PCR)、逆転写ポリメラーゼ連鎖反応(RT−PCR)、核酸配列ベース増幅法(NASBA)、ループ媒介等温増幅法(LAMP)、その他の等温核酸増幅法、酵素結合免疫吸着法(ELISA)、免疫クロマトグラフィー、バイオセンサー又は核酸プローブなどにより検出することができる。或いは、病原体、又は特定の病原体の存在を指示する病原体の細胞成分、例えばゲノムDNA、リボソームRNA、トランスファーRNA、メッセンジャーRNA又はタンパク質などは、界面活性剤、カオトロピック試薬、有機溶剤又は電気泳動法を使用して、フィルター構造を破壊するか又は破壊せずにフィルターから抽出でき、かつ慣用の病原体検出法を使用して検出できる。或いは、フィルターに固定化された病原体は、フィルターに検知剤(sensing agent)を加工して検出することができる。有
用な検知剤は、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、又は生物的相互作用により、フィルター内部に固定化することができる。検知剤の例は、米国特許第6087114号及びRider et al.,“AB Cell−Based
Sensor for Rapid Identification of Pathogens”,Science,301,213−15(2003)に開示されている病原体特異的抗体固定化B−細胞である。
【0078】
検出できる病原体の例には、ヒト、動物、植物、環境及び/又は産業に伝染性又は有害
である病原菌及び他の微生物がある。病原菌の例には、エシェリキア(Escherichia)、
サルモネラ、リステリア、カンピロバクター(Campylobacter)、シゲラ(Shigella)、
ブルセラ(Brucella)、ヘリコバクター(Helicobactor)、マイコバクテリウム(Mycobacterium)、ストレプトコッカス(Streptococcus)及びシュードモナス(Pseudomonas)
があるが、これらに限定はされない。病原性ウィルスは、本明細書に開示されるように、慣用の病原体検出法を併用して検出できる。病原性ウィルス科の例には、アデノウィルス科、ピコルナウィルス科、ヘルペスウィルス科、ヘパドナウィルス科、フラビウィルス科、レトロウィルス科、オルトミクソウィルス科、パラミクソウィルス科、パポバウィルス科、ラブドウィルス科及びトガウィルス科があるが、これらに限定されない。更に、開示
された濾過システムは、大容量の微粒子サンプル中の病原性及び非病原性微生物の両方の検出に有用である。
【0079】
検査できる微粒子サンプルの例には、食品サンプル、食品サンプルホモジネート、食品サンプルの洗浄溶液、飲料水、海/河川水、環境水、泥及び土があるが、これらに限定されない。更に、種々の環境表面を拭うスワブ、スポンジ及びタオルも検査することができる。更に、開示された濾過システムは、ヒトの体液、尿、血液及び製造用水/溶液を含む他の大容量の微粒子サンプルを検査するのに役立つ。サンプル、特に固体形、は、より効率良く濾過するために、サンプルの濾過前に、50〜1000μm孔を有するメッシュにより希釈、均質化及び/又は濾過することができる。
【0080】
病原体検出のための複合ヒドロゲルフィルター
特定の実施形態では、ヒドロゲルは、病原体認識能力を備えた超多孔質のフィルターに含まれて、複合ヒドロゲルフィルターを形成する。複合ヒドロゲルフィルターは、さまざまな手法で製造することができる。一実施形態では、ヒドロゲル又はヒドロゲル粒子は、ガラスファイバー又はニトロセルロース繊維などの繊維物質を含むフィルターマトリックスの上部、底部、又は内部に配置することができる。他の実施形態では、フィルターマトリックスは、ヒドロゲル繊維から形成される。ヒドロゲルは3次元高分子網目構造体なので、その脱水状態では超多孔質である。多孔度は、ヒドロゲルの生成に使用する重合方法に依存して調整することができる。一実施形態では、濾過の間、サンプル溶液は、ヒドロゲル内側の孔を通って浸透することができる。別の実施形態では、溶液は、ヒドロゲル粒子の間の間隙を通って濾過することができる。このように、複合ヒドロゲルフィルターでは、濾過の間、目詰まりが起こり得ない。複合ヒドロゲルフィルターの多種多様な実施形態を図4A〜4Dに示す。
【0081】
一実施形態では、複合ヒドロゲルフィルターは、ヒドロゲルの内側又は表面上に病原体検出試薬を含有し、検査すべきサンプル溶液の濾過後でも、効果的に試薬を保持する。別の実施形態では、サンプル濾過の間に病原体検出試薬が溶出するのを防止するために、環境感受性ヒドロゲル(スマートヒドロゲル)を使用して、病原体検出試薬を保持及び放出する。スマートヒドロゲルは、小さい物理的、生物学的又は化学的刺激に応答でき、縮小、膨潤及びゾル形態−ゲル形態間の変換等の大きな特性の変化を起こす。この実施形態では、膨潤している間は、病原体検出試薬がスマートヒドロゲル中に取り込まれた状態にある。スマートヒドロゲルは、サンプル濾過の間は、病原体検出試薬を放出しない。濾過後に環境的刺激を与えて、スマートヒドロゲルを縮まらせると、病原体検出試薬がスマートヒドロゲルから放出され、フィルターに分散する(図5)。病原体検出剤含有スマートヒドロゲル又はヒドロゲル粒子は、図4A〜4Cに示されるように、フィルターマトリックスの上部、その間、又は全体にわたって組み込むことができる。別の実施形態では、病原体検出試薬は、スマートヒドロゲルがゾル形態である間は、そこに取り込まれた状態にある。ゲル形態のスマートヒドロゲルは、サンプル濾過の間、病原体検出試薬を放出しない。濾過後に環境的刺激を与えて、スマートヒドロゲルをゾル形態に変換させると、病原体検出試薬が、スマートヒドロゲルから放出され、フィルター全体にわたり分散する。
【0082】
病原体検出試薬を含有する複合ヒドロゲルフィルターを使用する大容量微粒子サンプル中の病原体検出は、以下のステップを含み、図3に示される方法よりステップ数を少なくできる。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、複合ヒドロゲルフィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)もし必要な場合は、病原体検出アッセイ又は病原体増殖の潜在的な阻害剤を除去するために、フィルターを洗浄するステップ。
(3)病原体を検出可能にするために、病原体の増殖に十分な時間、フィルターをインキ
ュベートするステップ。
(4)シグナリング試薬を使用して増殖病原体を検出するステップ。
【0083】
分解性フィルター膜
特定の実施形態では、病原体認識能力を有する超多孔質のフィルターは、サンプル濾過後に、溶媒に分解又は溶解させ、固定化された病原体を効率よく収集する。分解性フィルターは、濾過の前又は間は、保全されるが、簡易処理により分解させることができる。このフィルターは、例えば合成の分解性もしくは腐食性ポリマー、又は天然の分解性もしくは腐食性ポリマー、又はこれらのコポリマーなどの分解性材料から製造される。合成分解性ポリマーには、ポリグリコール酸、ポリ乳酸、ポリヒドロキシブチレート(PHB)、ポリヒドロキシバレレート(PHV)、ポリカプロラクトン、ポリジオキサノン、ポリアンヒドリド、ポリシアノアクリレート、ポリアミノ酸、ポリオルトエステル、ポリホスファゼン、ポリプロピレンフマレート及びこれらのコポリマーがある。天然ポリマーには、コラーゲン、フィブリノゲン、フィブリン、ゼラチン、セルロース、キトサン、デンプン、アミロース、アルギネート、デキストラン、シルク、ケラチン、エラスチン、アクチン、ミオシン、グリコサミノグリカン、カラギーナン及びこれらのコポリマーがある。フィルターの分解は、加水分解、酸化又は酵素機構を介して行うことができる。
【0084】
分解性フィルターはさまざまな手法で製造することができる。一実施形態では、フィルターは、分解性ポリマーから構成されるので、サンプル溶液は、濾過の間、多孔質分解性ポリマー内側の孔を通って浸透することができる。別の実施形態では、フィルター膜は、多数の分解性ポリマー粒子から構成されるので、溶液は、分解性ポリマー粒子間の間隙を抜けて濾過することができる。従って、複合分解性フィルターが、濾過の間に詰まることはありえない。もう1つ別の実施形態では、フィルターは、分解性ポリマーコーティングが施された水溶性ポリマーから構成される。別の実施形態では、フィルターは、分解性ポリマーコーティングが施された多数の水溶性ポリマー粒子から構成される。複合ヒドロゲルフィルターの種々の実施形態が、図6A〜6Cに図示される。
【0085】
病原体検出試薬を含有する分解性フィルターを使用する大容量微粒子サンプルの病原体検出は、以下のステップを含む(図7)。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、分解性フィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)刺激を与えて、フィルターを溶液にするステップ。
(3)分解溶液から病原体又は病原体特異的分子マーカーを収集するステップ。
(4)病原体又は病原体特異的分子マーカーを検出するステップ。
【実施例】
【0086】
例1:環境感受性ヒドロゲルを使用する10%全乳での病原体検出アッセイ
病原体検出アッセイは、種々の用量のリステリア細胞を接種した10%全乳250mLに行った。
【0087】
リステリア・イノキュア(Listeria innocua)を、BHIブロス中で、37℃で一晩培養した。リステリア濃度は、1/106希釈後に、コロニーを数えて評価した。10%全乳は、全乳25mLを滅菌PBS緩衝液(pH7.4)225mLで希釈して調製した。リステリア検出試薬は、以下のようにして調製した。
(1)Fraser broth base(Oxoid,UK)11.5g及びBacto agarose2gを蒸留水200mL中に溶解させ、120℃で20分間滅菌し、45℃でゾル形態に保持した。
(2)Fraser supplement(Oxoid,UK)1vial/500mLとX−グルコシド(Sigma,MO)50mg/Lを溶液に追加した。
【0088】
病原体検出アッセイは、以下のようにして行った。
(1)リステリア(200cfu)接種サンプル又はリステリア−ネガティブサンプルを、GMF150 1μm(Whatman,NJ)で、真空濾過により濾過した。
(2)GMF150 1μm濾過媒体を滅菌容器に移し、45℃で5分間保持した。
(3)フィルターをリステリア検出試薬5mLに45℃で5分間浸漬し、リステリア検出試薬を室温まで冷却することでゲル形態に変換した。
(4)フィルターを、30℃で一晩インキュベートしてリステリア細胞の増殖を検出した。
【0089】
24時間のインキュベーション後、リステリア−ポジティブサンプルについてはリステリア細胞によるX−グルコシドの代謝のため、フィルター中にコロニー様着色スポットが観察された。これらの着色は、24時間より40時間で非常に濃くなり、このことは、リステリア細胞の増殖を示す(図8A、8B)。これとは対照的に、リステリアネガティブサンプルは、何ら着色を示さなかった(図8C、8D)。
【0090】
例2:ヒドロゲル粒子の調製
ヒドロゲル粒子を、油中水(W/O)乳化法を使用して調製した。低融点(LMP)アガロース(Invitrogen,Carlsbad,CA)溶液を、水に溶解し、濃度3%(w/v)にし、55℃に保持した。LMPアガロース溶液1mLを鉱油40mLに1滴づつ混合し、55℃に保持し、磁気撹拌機で強力に撹拌し、W/O乳液を形成した。撹拌しながら温度を4℃まで減じて、LMPアガロース含有乳液をゲル化して、LMPアガロース粒子を形成した。アガロース粒子を滅菌水で3度洗浄し、使用まで4℃に保持した。顕微鏡分析により、得られたアガロース粒子が、直径5〜50μmの球形であることを確認した(図9)。
【0091】
例3:ヒドロゲルマイクロビーズを使用する病原体検出アッセイ
新たに、リステリア・イノキュアを、BHIブロス中で、37℃で一晩培養した。アガロース粒子(250μL当量)を、X−グルコシド50mg/L、LiCl28g/L及びRapid L.Mono Supplement2(Biorad,CA)66.4μL/mLを含有する滅菌BHIブロス5mL中に、室温で少なくとも1時間懸濁させた。
【0092】
一連の希釈したリステリア細胞を含有するサンプルを、真空吸引を使用して、Nanoceramフィルター(直径47−mm,Argonide,FL)で濾過した。懸濁アガロース粒子を含有する溶液をフィルター上部に添加し、1分間インキュベートし、かつ真空吸引を使用して濾過した。アガロース粒子含有フィルターを37℃で最長2日までインキュベートした。17〜24時間のインキュベーション後に、リステリアの増殖を示すブルースポットが、裸眼で観察された。ブルースポットの数は、サンプル中に接種されたリステリア細胞の量によく相関した(図10)。
【0093】
例4:食品ホモジネートの濾過
多孔質球状マイクロビーズ(架橋ポリメタクリレート、EG50OH、日立化成、日本)0.5〜1g、多孔質マイクロビーズ(架橋デキストラン、Sephadex G25,GE Healthcare,NJ)0.5〜2g、無孔濾過補助材(ガラスビーズ、直径40μm、Filter aid 400,3M,MN)15gを使用するか又は濾過補助材を使用しないで、Nanocream filter(直径47−mm,Argonide,FL)又はGMF150 1μm(Whatman,NJ)について、食品ホモジネートの濾過速度を比較した。食品ホモジネートの濾過前に、濾過補助材を、ナノセーラムフィルター(Nanoceramfilter)又はGMF150 1μmフィルターの上流側
の面に置いた。
【0094】
食品ホモジネートは、以下のようにして調製した。
(1)食品サンプル(デリ・ミート、フランクフルトソーセージ又はスティックチーズ)25gを蒸留水225mLと混合した。
(2)食品サンプルを手動又はストマッカー(stomacher;Seward,UK)で、2
30rpmで2分間、粉砕消化(stomach)した。
(3)ストマッカー袋(Nasco,WI)付属のフィルターを使用して、食品ホモジネートを分離した。
【0095】
10%デリ・ミートホモジネートにおいて、濾過補助材無しのナノセーラムフィルター(黒三角)は、ホモジネート100mLより少量で目詰まりをおこした(図11A)。しかしながら、ガラスビーズ(黒四角)又は多孔質マイクロビーズ濾過補助材(架橋デキストラン2g、86〜258μm)(黒丸)を使用すると、フィルターの目詰まりを起こさずに、ホモジネートサンプル225mL全部を濾過することが可能であった。多孔質マイクロビーズ濾過補助材を用いる濾過は、5分以内に完了し、ガラスビーズ濾過補助材を用いる濾過よりはるかに迅速であった。
【0096】
10%チーズホモジネートにおいて、濾過補助材無し(黒三角)及びガラスビーズ濾過補助材有り(黒四角)のナノセーラムフィルターは、それぞれホモジネート5及び75mLより少量で目詰まりをおこした(図11B)。しかしながら、多孔質マイクロビーズ濾過補助材(架橋デキストラン、2g、86〜258μm)(黒丸)を使用すると、ホモジネート225mL全部を5分以内に濾過することができた。
【0097】
様々なグレードの多孔質球状マイクロビーズ濾過補助材の濾過性能を、10%デリ・ミートホモジネートを使用して比較した。架橋ポリメタクリレートマイクロビーズ(直径45〜90μm:0.5g(白丸)、1.0g(黒丸))及び架橋デキストランマイクロビーズ(直径17〜70μm:0.5g(白四角)、直径35〜140μm:0.5g(ひし形)、直径86〜258μm:0.5g(白三角)、1.0g(黒三角)、直径170〜520μm:0.5g(×))を、GMF150 1μmフィルターについて評価した(図12A)。直径170〜520μmの架橋デキストランマイクロビーズを除き、ホモジネート225mL全部は5分以内に完全に濾過された。
【0098】
様々なグレードの多孔質球状マイクロビーズ濾過補助材の濾過性能を、10%フランクフルトソーセージホモジネートを使用して同様に比較した。架橋ポリメタクリレートマイクロビーズ(直径45〜90μm:0.5g(白丸))及び架橋デキストランマイクロビーズ(直径17〜70μm:0.5g(白四角)、直径35〜140μm:0.5g(ひし形)、直径86〜258μm:0.5g(白三角)、直径170〜520μm:0.5g(×))を、GMF150 1μmフィルターについて評価した(図12B)。ホモジネート225mL全部は5分以内に完全に濾過された。これらの実験により、多孔質マイクロビーズ濾過補助材が慣用の無孔濾過補助材より、優れた粒子捕捉能力及び濾過能力を有することが説明される。
【0099】
実験5:10%デリ・ミートホモジネート225mLでの病原体検出アッセイ
病原体検出アッセイは、種々の用量のリステリア細胞を接種した10%デリ・ミートホモジネート225mLを用いて行った。
【0100】
リステリア・モノサイトゲネス(Listeria monocytogenes)及びリステリア・イノキュアを、BHIブロス中で、37℃で一晩培養した。リステリア濃度は、1/106希釈後に、コロニーを数えて評価した。10%デリ・ミートホモジネートは、以下のようにして
調製した。
(1)デリ・ミート25gを滅菌PBS緩衝液(pH7.4)225mLと混合した。
(2)デリ・ミートサンプルをストマッカー(Seward,UK)により、230rpmで2分間、粉砕消化した。
(3)ストマッカー袋(Nasco,WI)付属のフィルターを使用して、デリ・ミートホモジネートを分離した。
濾過の前に、デリ・ミートホモジネートに、種々の用量のリステリア細胞を接種した。多孔質マイクロビーズ濾過補助材(架橋デキストラン、直径86〜258μm、Sephadex G25,GE Healthcare,NJ)は、BHIブロスに懸濁させ(50g/L)、120℃で20分間滅菌した。リステリア検出試薬は以下のようにして調製した。
(1)フレーザーブロス基礎培地(Fraser broth base;Oxoid,UK)11.5g
及びバクトアガロース(Bacto agarose)2gを蒸留水200mL中に溶解させ、120
℃で20分間滅菌し、45℃でゾル形態に保持した。
(2)フレーザーサプリメント(Fraser supplement)(Oxoid,UK)1vial
/500mlとX−グルコシド(Sigma,MO)50mg/Lを溶液に追加した。
【0101】
病原体検出アッセイは、以下のようにして行った。
(1)多孔質マイクロビーズ濾過補助材0.5gを、GMF150 1μm濾過媒体(直径47mm:Whatman,NJ)及びポリエチレンメッシュセパレーター(穴:直径330μm)の上部に置いた。
(2)多孔質マイクロビーズ濾過補助材0.5gを、リステリア接種デリ・ミートホモジネートと混合した。
(3)デリ・ミートホモジネートを真空濾過により濾過した。
(4)多孔質マイクロビーズを滅菌PBS溶液(pH7.4)20mLで徹底的に3回洗浄した。
(5)GMF150 1μm濾過媒体を滅菌容器に移し、45℃で5分間保持した。
(6)フィルターをリステリア検出試薬5mLに45℃で5分間浸漬し、リステリア検出試薬を室温まで冷却することでゲル形態に変換した。
(7)フィルターを、30℃で一晩インキュベートしてリステリア細胞の増殖を検出した。
【0102】
24時間のインキュベーション後、リステリア細胞によるX−グルコシドの代謝のため、フィルター中にコロニー様着色スポットが観察された(図13A、13C)。これらの着色は、24時間より40時間で更に濃くなり、このことは、リステリア細胞の増殖を示す(図13B、13D)。これとは対照的に、リステリアネガティブサンプルは、3日間のインキュベーション後ですら何ら着色を示さなかった(図13E、13F)。着色スポットの数は、接種リステリア細胞の数に密接に相関し、10%デリ・ミートホモジネート〜225mL(デリ・ミート25g)から接種リステリア細胞の約60%が濾過媒体に収集された(図14A、図14B)。
【0103】
例6:複合ヒドロゲルフィルター
複合ヒドロゲルフィルターの製作のために、アルミナナノ繊維(病原体認識試薬)を含むナノセーラムフィルター(直径47−mm,Argonide,FL)を、ヒドロゲルを担持するマトリックスとして使用した。費用が安いため、寒天ヒドロゲルを使用した。ナノセーラムフィルターで寒天ゲルを濾過して、新しいフィルターを製作した。病原体認識試薬、ここではアルミナナノ繊維、が、ヒドロゲルで被覆されると、これらは、病原体との静電相互作用の損失のため、通常、機能不全になり得るが、ここで、ナノセーラムフィルターは、多層から構成されるデプスフィルターであり、この問題が起こるのを防ぐために最上層を、寒天ヒドロゲルで被覆した。
【0104】
製作手順は、以下に説明する。ナノセーラムフィルターの最上層を、バルク膜から剥がし、1%寒天溶液を最上層に注いだ。次いで、寒天溶液は、真空下に最上層を通って濾過され、最上層のもともとの多孔性を保持した。その後、最上層を室温で空気乾燥させ、少量の水をその上にスプレーし、かつコンプレッサーを使用して、層を一緒に圧縮して、再びバルク膜へ取り付けた。最終的に組立てられたフィルター膜は、室温で乾燥させた。
【0105】
製造されたフィルター膜を、以下の手順により、病原体溶液を使用して検査した。
(1)フィルター膜を滅菌水150mLで洗浄した。
(2)BHIブロス10mL中リステリア細胞約103cfuをフィルターに添加し、真空下で濾過した。
(3)濾過後に、BHIブロス5mL及びX−グルコシド(発色基質)50mg/Lをフィルター膜に添加した。
(4)フィルター膜を37℃で15時間インキュベートした。
【0106】
図15は、その結果を示す。着色は、インキュベーション後にフィルター上に発見されたリステリア細胞の存在を示す
【0107】
例7:スマートヒドロゲルにより固定化された病原体検出試薬を有する複合ヒドロゲルフィルター
温度が37℃(インキュベーション温度)に達すると、縮む能力を有するので、感熱性ヒドロゲル、ポリ(N−イソプロピルアクリルアミド)/キトサンを使用した。合成は、以下のステップを含む。
(1)キトサン(0.03g)、酢酸(240μl)及びNIPAm(1.6g)を蒸留水(20mL)に溶解させた。
(2)架橋剤、N,N’−メチレンビスアクリルアミド(0.06g)、開始剤2,2−ジメトキシ−2−フェニルアセトフェノン(0.01g)及び触媒N,N,N’,N’−テトラメチルエチレンジアミン(200μl)を溶液に添加し、窒素下に40分間脱気した。
(3)溶液を、ペトリ皿中で、365nmUV光下で2時間光重合させた。
(4)ヒドロゲルを、毎日水を換えながら、蒸留水に3日間浸漬した。
生成されたスマートヒドロゲルを粉砕して、小粒子にし、X−グルコシド(発色基質)200mg/Lを有するBHIブロスに浸漬し、37℃と25℃との間で数回、加熱/冷却した。次いで粒子を集め、ヒドロゲル複合ナノセーラムフィルター(例6に示される)を使用して、図5に図示されるように、スマートヒドロゲル粒子を最上層とバルク層との間に添加することにより組み立てた。
【0108】
乾燥フィルター膜は、病原体溶液を使用して、以下の手順に従い、検査した。
(1)フィルター膜を滅菌水150mLで洗浄した。
(2)BHIブロス中のリステリア細胞(〜104cfu/mL)5mLを濾過した。
(3)フィルターを、密閉容器中で37℃で15時間インキュベートした。
【0109】
図16は、その結果を示す。検出すべきサンプルの濾過後に、なんら発色基質溶液を添加することなく、着色がフィルター上に見られた。
【0110】
例8:分解性フィルター膜
k−カラギーナン及びアルギン酸ナトリウムを使用して、分解性フィルターを製作した。アルギン酸ナトリウム0.4g、k−カラギーナン0.2g及びPluronic F127(界面活性剤)0.2gを蒸留水30mlに90℃で溶解させ、次いで酢酸100μlを溶液に添加した。重炭酸ナトリウム0.2gを溶液に移し、気泡を発生させた。泡
状溶液を形成後、溶液の10mLを直径60mmのペトリ皿に注いだ。ペトリ皿の溶液を室温まで冷却すると、多孔質ゲルが形成された。次いでゲル膜を0.5MCaCl2と0.5MKCl溶液に1時間浸漬して、架橋ヒドロゲル構造体を形成した。その後、架橋ヒドロゲル構造体を、真空下に凍結乾燥し、分解性ヒドロゲルフィルターを製造した。
【0111】
分解性フィルターを使用する病原体検出アッセイを行った。リステリア・イノキュア〜109cfuを接種したPBS緩衝液50mLを、真空吸引で、分解性ヒドロゲルフィルターに通して濾過させた。次いで、フィルターを100mMEDTA溶液10mL中で80℃で15分間インキュベートして、ヒドロゲルフィルターを完全に溶解させた。取扱説明書に従い、DNA Clean&Concentrator−5キット(Zymo research,CA)を使用して、フィルター溶解溶液240μLから、リステリアゲノムDNAを抽出した。抽出されたリステリアゲノムDNAは、ABI7900(Applied biosystem,CA)を用いるリアルタイムPCRにより検出し、閾値サイクル(Ct)値は23〜24.5である(図17)。他方、リステリアゲノムDNAは、ネガティブ対照、リステリアネガティブPBS緩衝液10mL、では検出されなかった。
【0112】
本発明の精神から逸脱せずに多数かつ種々の変更をなし得ることは当業者であれば理解するであろう。よって、上述した本発明の態様は、一例にすぎず、本発明の範囲を限定する意図はないことが、明確に理解されるべきである。
【技術分野】
【0001】
関連出願
本出願は、2007年8月1日提出の米国仮出願第60/953422号、2007年11月1日提出の米国仮出願第60/984624号、2007年12月31日提出の米国仮出願第61/018079号、及び2008年5月21日提出の米国仮出願第61/055099号の優先権を主張する。これら関連出願の全ては、ここに引用することにより本明細書の記載の一部をなすものとする。
【0002】
発明の分野
本開示は、大容量の微粒子サンプル中の病原体を検出するための試薬、方法及び装置に関する。
【背景技術】
【0003】
関連技術の説明
疾病予防管理センター(CDC)による最近の評価によれば、米国内で、各年だけで、7600万の食品媒介疾病(food-borne illness)の例、32万5千の入院例、及び5000の死亡例の原因が、食品媒介病原体(food-borne pathogen)である。ヒトへの有害
な医学的影響に加えて、これらの食品媒介事例の大発生は、医療費増大、生産性低下、商品回収、及び輸出差し止めによって、経済に悪影響をもたらす。米国農務省(USDA)は、特定の食品媒介病原体が少量でも生き残り、食中毒又は大発生を引き起こし得るので、その病原体に対してゼロトレランス政策を推奨している。そのため、食品サンプル中の1個の病原体でも検出できる高精度の病原体検出技術の開発が必要である。
【0004】
現在、多数の検出技術及び製品が、食品媒介病原体の検出に利用できるが、数グラムの食品サンプルを汚染する1個の病原体を、24時間という時間枠内で検出することは、今もなお困難である。一般に、病原体は、希釈及び均質化により食品サンプルから抽出され、これらは数百mLほどの又はそれ以上のサンプル容積を生じる。大容量のサンプル中にある少数の病原体を検出するためには、病原体濃度が病原体検出アッセイに適するレベルに達するまで、細胞を培養することが必要である。必要な前増菌(pre-enrichment)時間は、標的病原体の倍加時間、生存能力、及び検出に要する病原体濃度に依存する。前増菌は、通常少なくとも12〜48時間かかる。そのため、ポリメラーゼ連鎖反応(PCR)や酵素結合免疫吸着法(ELISA)などの高感度検出アッセイを用いても、食品サンプル中の病原体混入の検出は、依然として1日又は2日を必要とする。更に、これらのアッセイは、一般に、高価であり、熟練の検査技師を必要とする。
【0005】
更に、前増菌培養を用いる食品病原体アッセイは、増菌した病原体の取り扱いを要し、これは、試験所及び検査技師の二次汚染を生じ得る。従って、これらのアッセイは、食品製造プラントでの現場検査には適切ではなく、その代わりに現場の外、例えば委託試験所(reference laboratories)で行う必要がある。また、混入病原体の生存能力及び食品サンプルの成分が、病原体増殖速度に影響を与え得るという理由から、及びサンプルが細胞増殖の静止期又は衰退期にどれほど迅速に到達するかどうかは、病原体汚染レベルに依存し得るという理由から、前増菌培養によって、混入食品病原体に関する定量的情報が失われてしまう。そのため、前増菌を用いる食品病原体アッセイは、非定量的であり、食品の病原体汚染レベルの評価は難しい。
【0006】
前増菌を伴う病原体アッセイの上記欠点を克服するために、病原体濃度を増すために、大容量のサンプルの遠心分離又は濾過などの他の増菌手順が必要となろう。しかしながら
、遠心分離は、遠心分離機が必要であり、特に、多数の大容量サンプルを検査する必要がある場合、一般に、厄介なプロセスである。
【0007】
濾過は、より高い処理能力で遂行でき、かつ大容量サンプル中に存在する少ない数の病原体でも濃縮することができる。病原体を濃縮するために、濾過法は、通常、標的病原体より小さい孔径を有する精密濾過(MF)膜フィルターを、一般に利用する。こうして、病原体は、そのようなフィルターで濃縮でき、いくつかの検出法、例えばコロニー形成及びDNAプローブハイブリダイゼーションにより検出することができる。しかしながら、これらの膜フィルターは、粒子捕捉能力(dirt-holding capacity)が非常に低く、その
小さい孔径のために、微粒状の食品抽出物により容易に目詰まりを起こす傾向がある。これらのフィルターは、飲料水や環境水などの微粒子をほとんど含有しないサンプル、又は非常に小容量の微粒子のサンプルに適する。適切な保持率を備えたデプスフィルターも、病原体の捕捉に使用されるが、しかしながら、そのようなデプスフィルターに捕捉された病原体の検出は、その3次元マトリックス構造及びフィルター厚さのため、より面倒である。
【発明の概要】
【0008】
本発明は、その実施形態として、以下のステップの1つ又は複数によってサンプル中の微生物を検出する方法に関する。
濾過中の目詰まりを防ぐように構成された孔を有し、かつ微生物を引きつけるように構成されたフィルターでサンプルを濾過して、微生物をフィルターに収集するステップ。
微生物の増殖を局在化させ及び/又は微生物検出試薬の蒸発を防止するように構成されるポリマーと、微生物検出試薬とをフィルターに添加するステップ。
検出できるレベルまで微生物を増殖させるのに十分な時間にわたりフィルターをインキュベートするステップ。
サンプル中に微生物の存在を検出するステップ。
【0009】
好ましい実施形態では、前記ポリマーはヒドロゲルである。好ましくは、ヒドロゲルは、環境感受性ヒドロゲルである。環境感受性ヒドロゲルは、環境的変化を受ける前は、少なくとも部分的にゾル形態であって、低粘度を有するが、環境的変化を受けると、粘度が増加し、少なくとも部分的にゲル形態となる。好ましい実施形態では、環境的変化は、温度、pH、入射光量、イオン濃度、圧力、磁場、電場、音波照射又は生化学的分子の濃度である。好ましい実施形態では、フィルターへの環境感受性ヒドロゲルの添加は、少なくとも部分的にゾル形態の環境感受性ヒドロゲルを有する溶液をフィルターに添加するステップと、環境的変化を起こして、この溶液をゲル化するステップとを含む。
【0010】
好ましい実施形態では、ヒドロゲルは、ヒドロゲル粒子である。好ましくは、ヒドロゲル粒子は、ヒドロゲル粒子の懸濁液を吸収、吸引、濾過又は浸漬及びスプレーするなどの方法により添加される。好ましい実施形態では、ヒドロゲル粒子は、フィルター孔より小さく、そのため、フィルター孔を効率的に塞ぐ。
【0011】
好ましい実施形態では、ヒドロゲルは、脱水形態でフィルター孔に添加され、次いでフィルター孔の内側で水和させる。好ましくは、脱水ヒドロゲルの水和は、1分から6時間の時間がかかる。好ましくは、脱水ヒドロゲルは、溶液の形態でフィルター孔に添加され、1分から6時間にわたるインキュベーションにより、孔の内側で水和させる。
【0012】
好ましい実施形態では、フィルターに加工されるポリマーは、粘着性ポリマー溶液である。粘着性ポリマー溶液は、フィルターに流入して、孔を満たし、微生物の増殖を効果的に局在化させる。好ましくは、粘着性ポリマー溶液には、水溶性ポリマー又はヒドロゲル懸濁液がある
【0013】
好ましい実施形態では、フィルターに加工される微生物検出試薬は、微生物の増殖を選択的に促進するように構成された増殖培地を含有する。好ましくは、増殖培地は、検出すべき微生物は耐性を持つが、他の生物は耐性を持たない選択的な試薬又は抗生物質を含むか、検出すべき微生物は迅速に増殖し及び/又は他の生物の増殖は緩慢もしくは阻害するように選択されたpH及び温度を含むか、又は検出すべき微生物によって容易に代謝されるが、他の生物によっては容易に代謝されない栄養素を含む。一部の好ましい実施形態では、増殖培地は、好気性菌の増殖に十分な量の酸素を含むか、又は嫌気性菌の増殖のために十分な量の酸素を含まない。
【0014】
好ましい実施形態では、検出ステップは、微生物の存在下でシグナルを生じるように構成されたシグナリング試薬からのシグナルを検出し、これにより微生物を検出することを含む。好ましくは、シグナリング試薬は、微生物に特異的な酵素のための基質、微生物に特異的な酵素のための発色性もしくは発蛍光性の基質、又は微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性もしくは発蛍光性の指示薬との組合せである。
【0015】
一部の好ましい実施形態では、シグナリング試薬は、検出すべき微生物又はこの微生物の細胞成分を認識する薬剤、例えば、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物である。好ましくは、この薬剤は、例えば染料分子、金属コロイド、ポリマー粒子、磁性粒子、半導体粒子、リポソーム、ポリマーソーム、タンパク質、酵素又は核酸からの標識を有する。
【0016】
本発明は、別の実施形態として、濾過中の目詰まりを防ぐように構成された孔と、微生物を引きつけるように構成されたフィルターとを有し、更に多孔質で球状のマイクロビーズの層も含む層状フィルター複合体を用いて、微粒子サンプルを濾過することにより、この微粒子サンプルから微生物を分離するステップを含む方法に関する。好ましくは、この方法は、フィルター中に固定化された微生物を検出するステップを含む。
【0017】
本発明の実施形態では、前記方法の濾過ステップ後に、微生物の検出又は増殖を阻害する物質を除去するのに十分な時間にわたりフィルターを洗浄するステップを含んでもよい。
【0018】
好ましい実施形態では、前記方法でのフィルターは、繊維状物質を有するデプスフィルターである。好ましくは、繊維状物質は、セルロース繊維又はガラスマイクロファイバーである。
【0019】
好ましくは、フィルターは、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、又は生物的相互作用などの相互作用によって微生物を引きつけるように構成されている。好ましい実施形態では、微生物を認識する薬剤は、フィルターマトリックス上に特異的に又は非特異的に固定化される。薬剤は、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物であってよい。
【0020】
好ましい実施形態では、前記方法におけるフィルターは、更に、多孔質で球状のマイクロビーズの層を含む。一部の好ましい実施形態では、この多孔質球状マイクロビーズの層は、フィルターの上流側の面に配置される。一部の好ましい実施形態では、多孔質球状マイクロビーズの層は、メッシュ支持体の上流側の面に配置される。メッシュ支持体は、フィルター上に又はフィルターの上流側に配置される。
【0021】
好ましい実施形態では、多孔質球状マイクロビーズの層は、均等又はグレーデッド(graded)層を形成する。好ましくは、多孔質球状マイクロビーズの層表面は、極めて不活性で
あり、微生物に対する非特異的な結合が低い。
【0022】
好ましい実施形態では、マイクロビーズの直径は1〜1000μmであり、より好ましくは、マイクロビーズの直径は15〜600μmであり、更により好ましくは、マイクロビーズの直径は50〜300μmである。好ましくは、マイクロビーズの孔径は、微生物のサイズより小さく、微生物は、濾過ステップの間、マイクロビーズの間を通過する。一部の好ましい実施形態では、マイクロビーズは、架橋された親水性ポリマーを含む。
【0023】
一部の好ましい実施形態では、濾過ステップの後に、洗浄液を添加することにより多孔質球状マイクロビーズ層を破壊し、その後、マイクロビーズを懸濁させ、洗浄液をフィルターで濾過する。
【0024】
本発明は、その実施形態として、以下の構成要素のうち1つ又は複数を含む微生物検出キットに関する。
濾過中の目詰まりを防ぐように構成された孔を有し、かつ微生物を引きつけるように構成されたフィルター。
微生物の存在を検出するように構成された微生物検出試薬。
微生物の増殖を局在化するように及び/又は微生物検出試薬の蒸発を防止するように構成されたポリマー。
【0025】
好ましい実施形態では、フィルターは、繊維状物質を有するデプスフィルターである。好ましくは、繊維状物質は、セルロース繊維及びガラスマイクロファイバーから選択される。
【0026】
好ましくは、フィルターは、例えば静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物相互作用などの相互作用によって微生物を引きつけるように構成されている。
【0027】
好ましい実施形態では、微生物を認識する検出試薬は、フィルターマトリックス上に特異的に又は非特異的に固定化される。薬剤は、好ましくは、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物である。
【0028】
好ましい実施形態では、キットのポリマー成分はヒドロゲルである。好ましくは、ヒドロゲルは、環境感受性ヒドロゲルであり、これは、少なくとも部分的にゾル形態である。環境感受性ヒドロゲルは、環境的変化を受ける前は低粘度を有し、環境的変化を受けると、粘度が増加し、少なくとも部分的にゲル形態になる。好ましくは、環境的変化は、温度、pH、入射光量、イオン濃度、圧力、磁場、電場、音波照射又は生化学的分子濃度の変化である。
【0029】
好ましい実施形態では、ヒドロゲルは、ヒドロゲル粒子である。好ましくは、ヒドロゲル粒子は、フィルター孔より小さく、そのため、フィルター孔を効率的に塞ぐ。更に好ましくは、ヒドロゲルは、脱水形態であってよい。
【0030】
好ましい実施形態では、キット中のフィルターは、多孔質で球状のマイクロビーズの層も含む。一部の好ましい実施形態では、この多孔質球状マイクロビーズの層は、フィルターの上流側の面に配置される。一部の好ましい実施形態では、多孔質球状マイクロビーズの層は、メッシュ支持体の上流側の面に配置され、メッシュ支持体は、フィルター上に又はフィルターの上流側に配置される。
【0031】
好ましい実施形態では、多孔質球状マイクロビーズ層は、均等な又はグレーデッドな層
を形成する。好ましい実施形態では、多孔質球状マイクロビーズ層の表面は、極めて不活性であり、微生物に対する非特異的な結合が低い。
【0032】
好ましい実施形態では、マイクロビーズの直径は1〜1000μmであり、更に好ましくは、マイクロビーズの直径は15〜600μmであり、更になお好ましくは、マイクロビーズの直径は50〜300μmである。
【0033】
好ましい実施形態では、マイクロビーズの孔径は、微生物のサイズより小さく、そのため微生物は、濾過ステップの間、マイクロビーズの間を通過する。一部の好ましい実施形態では、マイクロビーズは、架橋された親水性ポリマーを含む。
【0034】
好ましい実施形態では、キット中の微生物検出試薬は、微生物の増殖を選択的に促進するように構成された増殖培地を含有する。好ましくは、増殖培地は、検出すべき微生物は耐性を持つが、他の生物は耐性を持たない選択的な試薬又は抗生物質を含むか、検出すべき微生物を迅速に増殖し及び/又は他の生物の増殖は緩慢にもしくは阻害するように選択されたpH及び温度を含むか、又は検出すべき微生物によって容易に代謝されるが、他の生物によっては容易に代謝されない栄養素を含む。一部の好ましい実施形態では、増殖培地は、好気性菌の増殖に十分な量の酸素を含むか、又は嫌気性菌の増殖のために十分な量の酸素を含まない。
【0035】
好ましい実施形態では、増殖培地は、微生物の存在下でシグナルを生じることにより、微生物を検出するように構成されたシグナリング試薬を含む。好ましくは、シグナリング試薬は、微生物に特異的な酵素、微生物に特異的な酵素のための発色性もしくは発蛍光性の基質、又は微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性もしくは発蛍光性の指示薬との組合せである。
【0036】
一部の好ましい実施形態では、シグナリング試薬は、検出すべき微生物又はこの微生物の細胞成分を認識する薬剤であり、例えば、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物であり、好ましくは、薬剤は、例えば染料分子、金属コロイド、ポリマー粒子、磁性粒子、半導体粒子、リポソーム、ポリマーソーム、タンパク質、酵素及び核酸等の標識を含む。
【0037】
本発明は、その実施形態として、濾過中の目詰まりを防ぐように構成された孔を有するとともに微生物を引きつけるように構成された濾過媒体(filter medium)と、多孔質で
球状のマイクロビーズ層とを含む微生物検出用の層状フィルター複合体に関する。
【0038】
好ましい実施形態では、層状フィルター複合体中の濾過媒体は、繊維状物質を有するデプスフィルターである。好ましくは、繊維状物質は、セルロース繊維又はガラスマイクロファイバーである。
【0039】
好ましい実施形態では、層状フィルター複合体の濾過媒体は、例えば静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物的相互作用などの相互作用によって微生物を引きつけるように構成されている。好ましい実施形態では、微生物を認識する薬剤は、フィルターマトリックス上に特異的に又は非特異的に固定化され、薬剤は、抗体、抗原、アプタマー、タンパク質、核酸及び炭水化物から選択される。
【0040】
好ましい実施形態では、層状フィルター複合体中の多孔質球状マイクロビーズの層は、フィルターの上流側の面に配置される。他の好ましい実施形態では、多孔質球状マイクロビーズの層は、メッシュ支持体の上流側の面に配置され、メッシュ支持体は、フィルター上に又はフィルターの上流側に配置される。好ましくは、多孔質球状マイクロビーズ層は
、均等な又はグレーデッドな層を形成する。好ましくは、多孔質球状マイクロビーズ層の表面は、極めて不活性であり、微生物への非特異的な結合が低い。
【0041】
好ましい実施形態では、マイクロビーズの直径は1〜1000μmであり、更に好ましくは、マイクロビーズの直径は15〜600μmであり、更になお好ましくは、マイクロビーズの直径は50〜300μmである。好ましい実施形態では、マイクロビーズの孔径は、微生物のサイズより小さく、そのため微生物は、濾過ステップの間、マイクロビーズの間を通過する。一部の実施形態では、マイクロビーズは、架橋した親水性ポリマーを含む。
【0042】
本発明は、その実施形態として、多孔質フィルターに関し、これは、膨潤し得るが、水に溶解しない3次元高分子網目構造体であるヒドロゲルと、濾過中の目詰まりを防ぐように構成された孔を有するとともに微生物を引きつけるように構成されたフィルターとを含む。
【0043】
好ましい実施形態では、多孔質フィルターのヒドロゲルは、脱水形態である。
【0044】
好ましい実施形態では、フィルターは、繊維状物質を含むフィルターマトリックスを有する。
【0045】
好ましい実施形態では、ヒドロゲルの3次元高分子網目構造体には、例えば、寒天、キトサン、セルロース、カラギーナン、アルギネート、アクリレートポリマー及びコポリマー、ポリエチレングリコール、ポリグリコール酸、ポリ乳酸、ペクチン、ローカストビーンガム、ポリヒドロキシブチレート(PHB)、ポリヒドロキシバレレート(PHV)、ポリカプロラクトン、ポリジオキサノン、ポリアンヒドリド、ポリシアノアクリレート、ポリアミノ酸、ポリオルトエステル、ポリホスファゼン、ポリプロピレンフマレート、ポリアルキレンオキサレート、シリコーンポリマー、コラーゲン、フィブリノゲン、フィブリン、ゼラチン、デンプン、アミロース、デキストラン、シルク、ケラチン、エラスチン、アクチン、ミオシン、グリコサミノグリカン又はポリビニルアルコール等のポリマーがある。
【0046】
好ましい実施形態では、フィルターは、例えば、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物的相互作用などの相互作用によって微生物を引きつけるように構成されている。
【0047】
好ましい実施形態では、微生物を認識する薬剤は、フィルターマトリックス上に特異的に又は非特異的に固定化される。好ましくは、前記薬剤は、金属水酸化物又は金属酸化物、抗体、抗原、アプタマー、タンパク質、核酸又は炭水化物から選択される。好ましくは、金属水酸化物又は金属酸化物は、水酸化ジルコニウム、水酸化チタン、酸化ハフニウム、ヒドロキシアパタイト、酸化鉄、酸化チタン又は酸化アルミニウムである。
【0048】
好ましい実施形態では、フィルターは、微生物検出試薬を含有し、かつ微生物含有サンプルの濾過の間にわたりこの微生物検出試薬を保持する。好ましくは、微生物検出試薬は、検出すべき微生物の増殖を選択的に促進するように構成された増殖培地と、微生物の存在下でシグナルを生じるように構成されたシグナリング試薬とを含む。好ましくは、増殖培地は、検出すべき微生物は耐性を持つが、他の生物は耐性を持たない選択的な試薬又は抗生物質を含むか、検出すべき微生物は迅速に増殖し及び/又は他の生物の増殖は緩慢にもしくは阻害するように選択されたpH及び温度を含むか、又は検出すべき微生物によって容易に代謝されるが、他の生物によっては容易に代謝されない栄養素を含む。一部の好ましい実施形態では、増殖培地は、好気性菌の増殖に十分な量の酸素を含むか、又は嫌気
性菌の増殖のために十分な酸素を含まない。
【0049】
好ましい実施形態では、シグナリング試薬は、微生物に特異的な酵素のための基質、微生物に特異的な酵素のための発色性又は発蛍光性の基質、及び微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性又は発蛍光性の指示薬との組合せから選択される。
【0050】
好ましい実施形態では、シグナリング試薬は、検出すべき微生物又はこの微生物の細胞成分を認識する薬剤であり、例えば抗体、抗原、アプタマー、タンパク質、核酸及び炭水化物等である。好ましくは、この薬剤は、例えば染料分子、金属コロイド、ポリマー粒子、磁性粒子、半導体粒子、リポソーム、ポリマーソーム、タンパク質、酵素又は核酸等の標識を含む。
【0051】
本発明は、その実施形態として、以下のステップのうちの1つ又は複数のステップを含むサンプル中の微生物を検出する方法における前記多孔質フィルターの使用に関する。
サンプルを前記多孔質フィルターにより濾過して、微生物を固定化するステップ。
微生物を検出可能なレベルまで増殖させるのに十分な時間にわたりフィルターをインキュベートするステップ。
シグナリング試薬を使用して微生物を検出するステップ。
【0052】
一部の好ましい実施形態では、濾過後に、多孔質フィルターは溶解する。例えば、多孔質フィルターは、分解性ポリマーを含んでよい。好ましくは、分解性ポリマーは、例えば繊維、表面コーティング、ビーズ、粒子、シート又は層などの形状で提供される。一部の好ましい実施形態では、分解性ポリマーは、加水分解、酸化又は酵素機構を介して、溶液となる。
【0053】
一部の実施形態では、この分解性多孔質フィルターは、以下のステップのうちの1つ又は複数によりサンプル中の微生物を検出する方法に使用される。
(a)サンプルをフィルターで濾過して、微生物を固定化するステップ。
(b)分解性フィルターを分解して溶液にするステップ。
(c)この溶液から、微生物又は微生物に特異的な分子マーカーを抽出するステップ。
(d)微生物又は微生物に特異的な分子マーカーを検出して、サンプル中の微生物の存在を確認するステップ。
【0054】
本発明の他の態様、特徴及び利点は、後述する好ましい実施形態の詳細な説明から明らかとなろう。
【0055】
以下に、図面を参照して、本発明の上述した特徴及び他の特徴を説明するが、この図面の好ましい実施形態は、本発明を図解することを意図するものであり、本発明を限定するものではない。
【図面の簡単な説明】
【0056】
【図1】多孔質の球状ビーズを用いた濾過の概略図を示す。
【図2】環境感受性ヒドロゲルを使用する病原体検出アッセイ手順のステップの概略図を示す。
【図3】ヒドロゲルマイクロビーズを使用する病原体検出アッセイ手順のステップの概略図を示す。
【図4】ヒドロゲル複合フィルターの種々の構造を示す。図4Aは、ヒドロゲルがフィルターマトリックス層の間に位置する実施形態を示す。図4Bは、ヒドロゲル粒子がフィルターマトリックス層の間に位置する実施形態を示す。図4Cは、ヒドロゲル粒子がフィルターマトリックス全体にわたり分散している実施形態を示す。図4Dは、ヒドロゲル繊維がフィルターマトリックスを形成している実施形態を示す。
【図5】病原体検出試薬が装入されたスマートヒドロゲル粒子を含む複合ヒドロゲルフィルターを示す。
【図6】分解性フィルターの種々の構造を示す。図6Aは、フィルター膜が分解性粒子からできている実施形態を示す。図6Bは、フィルター膜が分解性繊維からできている実施形態を示す。図6Cは、フィルター膜が分解性コーティングを備えた水溶性粒子からできている実施形態を示す。
【図7】分解性フィルターを使用して病原体を収集かつ検出するアッセイを図解する。
【図8】ガラスファイバーデプスフィルターで濾過した10%全乳サンプル250mLについての病原体検出アッセイの結果を示す。図8A及び8Bは、リステリア細胞200cfuを接種した乳サンプルの30℃で40時間インキュベートした後の結果を示す。図8C及び8Dは、リステリア細胞を含まない乳サンプルの30℃で40時間インキュベートした後の結果を示す。
【図9】ヒドロゲル微粒子の顕微鏡画像を示す。微粒子は、より高いコントラストをつけるため、トリパンブルーで染色した。
【図10】陽電荷フィルターで濾過した病原体検出アッセイの結果を示し、図10A〜図10Eは、BHIブロス10mL当たりリステリア細胞235、23.5、2.35、0.235及び0cfuについての結果である。
【図11】10%デリ・ミート(A)及び10%スティックチーズホモジネート(B)に関して、多孔質マイクロビーズ2gと共に陽電荷デプスフィルターを使用する濾過速度(黒丸)、無孔ガラスビーズ15gと共に陽電荷デプスフィルターを使用する濾過速度(黒四角)及び濾過補助材無しで陽電荷デプスフィルターを使用する濾過速度(黒三角)を示す。
【図12】幾つかのグレードの多孔質球状マイクロビーズ濾過補助材:架橋ポリメタクリレートマイクロビーズ(直径45〜90μm:0.5g(白丸)、1.0g(黒丸))、及び架橋デキストランマイクロビーズ(直径17〜70μm:0.5g(白四角)、直径35〜140μm:0.5g(ひし形)、直径86〜258μm:0.5g(白三角)、1.0g(黒三角)、直径170〜520μm:0.5g(×))と共にガラスファイバーデプスフィルターを使用して、10%デリ・ミート(A)及び10%フランクフルトソーセージホモジネート(B)を濾過する速度を示す。
【図13】ガラスファイバーデプスフィルター及び多孔質マイクロビーズ濾過補助材により濾過された、10%デリ・ミートホモジネートの〜225mL(デリ・ミート25g)当たりリステリア細胞220cfu(図13A、13B)、22cfu(図13C、13D)及び0cfu(図13E、13F)に関する病原体検出アッセイの結果を示す。図13A、13C及び13Eは、30℃で24時間のインキュベーション後の結果を示し、図13B、13D及び13Fは、30℃で40時間のインキュベーション後の結果を示す。
【図14】ガラスファイバーデプスフィルター及び多孔質マイクロビーズ濾過補助材により濾過された10%デリ・ミートホモジネート〜225mL(デリ・ミート25g)中の病原体検出アッセイの結果を示す。図14Aの表は、フィルターの上流側(上部)及び下流側(底部)から観察される着色スポットの数をまとめたものである。図14Bは、観察された着色スポットの総数を、接種された病原体濃度に対してプロットしたものである。黒丸及び白丸は、リステリア・モノサイトゲネスとリステリア・イノキュアをそれぞれ示す。
【図15】加工フィルターによるアッセイの結果を示し、インキュベーション後にフィルター上に見出されるリステリア細胞を示す。
【図16】スマートヒドロゲルにより固定化された病原体検出試薬を有する複合フィルターについてのアッセイの結果を示す。
【図17】病原体検出のための分解性フィルターについてのアッセイのPCR結果を示す。サイクルは、PCRサイクル数を示し、ΔRNは、基準強度を控除した後の各反応における規格化相対蛍光強度を示す。
【発明を実施するための形態】
【0057】
ここに記載する実施形態は本発明の好ましい実施形態であるが、当然ながら、本発明の精神から逸脱しない範囲で種々の改変が当業者によって行われるであろう。したがって、本発明の範囲は、添付の特許請求の範囲のみによって決定されるべきである。
【0058】
本開示は、低コストで且つ短い実践時間で、大容量の微粒子サンプル中の病原体を高感度で検出することを可能にする方法、この方法で使用されるフィルターの製作、及びこの方法における多孔質球状マイクロビーズの濾過補助材の使用に関する。
【0059】
超多孔質のフィルター、多孔質球状マイクロビーズ濾過補助材及びヒドロゲル材料を使用する病原体検出濾過アッセイ
本開示の方法は、一実施形態として、大容量の微粒子サンプルから病原体を効率よく濃縮するために、病原体吸着能力及び高い粒子捕捉能力を有する超多孔質のフィルターを利用するものである。本開示の方法の実施形態に有用な超多孔質のフィルターは、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、又は生物的相互作用により標的病原体を引きつけることができ、また微粒子サンプルによるフィルターの目詰まりを十分に防止できる多孔質なものがよい。特定の実施形態では、配置されたフィルターは、高い粒子捕捉能力及び病原体捕捉能力を提供する3次元マトリックスを備えたデプスフィルターである。有用なデプスフィルターは、例えばガラスファイバー及びニトロセルロース繊維などの繊維状物質から製造されていてよく、単層又は同じか若しくは異なる粒子保持率を有する多層のフィルターからなる。フィルターは、病原体を効果的に捕捉し、かつサンプル中の粒子によるフィルター目詰まりを回避するのに適切である粒子保持率及び厚さを有する。例えば、長さ0.5〜2μm、直径0.4〜0.5μmである病原体、例えばリステリア等をデプスフィルターに捕捉するためには、デプスフィルターの適切な粒子保持率は、0.1〜10μm、好ましくは0.7〜2.4μmであろう。また、フィルターは、濾過の間にかけられる真空力又は圧力に耐えるのに十分な機械的強度を有する。
【0060】
他の実施形態では、病原体表面が、通常、その中に含有されるリポ多糖類、テイコ酸及び表面タンパク質のために正味の陰電荷を有するので、フィルターは、陽性電荷を使用して病原体を引きつけるデプスフィルターである。病原体は、フィルターマトリックによってではなく、フィルター上の陽性電荷により固定化され得、従って、フィルター多孔度を更に増し、かつより高い粒子捕捉能力を得て、フィルターの目詰まりを更に効果的に回避することができる。陽性電荷は、フィルターマトリックスをカチオン性分子で表面コーティングすることにより、又は陽性物質から製造された陽性コロイド、粒子もしくは繊維を組み入れることにより提供することができる。陽性物質の例は、金属水酸化物及び金属酸化物、例えば、水酸化ジルコニウム、水酸化チタン、酸化ハフニウム、酸化鉄、酸化チタン、酸化アルミニウム及びヒドロキシアパタイト、である。好ましくは、金属水酸化物又は金属酸化物の等電点は、サンプルと検出試薬のpH値より高くあって良い。ステノトロホモナス・マルトフィリア(Stenotrophomonas maltophilia)などの正電気を帯びたバクテリアの例が、ごく稀にある。そのような微生物は、陽性電荷ではなく陰性電荷を使用して、前記の陽電荷フィルターと同様にして製造できる陰性電荷を有するフィルターにより一層容易に保持することができる。
【0061】
他の実施形態では、フィルターは、病原体認識剤、例えば、抗体、抗原、タンパク質、核酸、炭水化物、アプタマー、又はバクテリオファージを含む。これらの病原体認識剤は、サンプル中に発見される他の病原体に対して、病原体を選択的又は非選択的に認識でき
、かつ化学結合、物理結合又は他の標準固定法により、フィルターマトリックス上に固定化することができる。特定の実施形態では、病原体認識剤は、トール様受容体(TLR)であり、これは、種々の微生物の表面に存在する構造的に保存された分子を認識する。TLR2は、グラム陽性ペプチドグリカン及びリポテイコ酸を認識でき、かつTLR4は、グラム陰性バクテリア上のリポ多糖類を認識できる。
【0062】
フィルターの他に、本開示は、検査すべきサンプル中の微粒子によるフィルター目詰まりを防止するための多孔質球状マイクロビーズ濾過補助材の使用に関する(図1)。有用なマイクロビーズは、小さいサイズで分布する球状の、回転楕円体形状の又は楕円体形状の多孔質マイクロビーズであってよい。このマイクロビーズは立方最密構造や六方細密構造などの最密構造又はそれに近い構造をとることができる。検査すべき病原体が、サンプル濾過時に、マイクロビーズの間を通過するために、マイクロビーズは、通常は、直径を1〜1000μm、好ましくは15〜600μm、更に好ましくは50〜300μmにしてもよい。有用なマイクロビーズは、水、緩衝液、増殖培養液又はサンプル溶液に、浮くのではなく、懸濁するのに適切な比重を有する。マイクロビーズは、通常、標的病原体より小さい孔を有することで、サンプル濾過時に病原体が多孔質球状マイクロビーズの孔の内側に留まるのを阻むことができる。好ましくは、マイクロビーズは、不活性表面、好ましくは親水性表面を有してよく、かつタンパク質、核酸、炭水化物、バクテリア、ウィルス及び細胞を含む生体分子及び微生物への非特異的な結合は低い。特定の実施形態では、マイクロビーズ濾過補助材は、例えばポリメタクリレートやデキストランなどの架橋ポリマーから製造されている。場合により、マイクロビーズは、その多孔質構造のため、後段の検出を阻害し得る物質を除去できる。
【0063】
大容量の微粒子サンプルを少なくとも次の手法又はその組合せの1つで濾過するのを支援するために、多孔質球状マイクロビーズの濾過補助材を使用することができる。濾過補助材の配置としては、サンプルの濾過前に、病原体吸着能力を有する超多孔質のフィルターの上流側の面上に、多孔質球状マイクロビーズの均等な又はグレーデッドな層を配置することができる。又は、濾過前に、微粒子サンプルに濾過補助材を添加して、サンプル濾過時に多孔質球状マイクロビーズ層を形成することにより、マイクロビーズの新層を連続的に設け、濾過を更に改良することができる。サンプル濾過後に、濾過補助材層を容易に除去するために、超多孔質のフィルターと濾過補助材層の間にメッシュ支持体を配置できる。場合により、マイクロビーズ表面への病原体の結合を最小にするために、使用前に、多孔質マイクロビーズ濾過補助材は、ペプチド又はタンパク質などのブロッキング試薬含有溶液中に懸濁させるか又はプレインキュベートする。
【0064】
検出すべき病原体は、マイクロビーズの間を通過し、マイクロビーズの表面上又は孔中に捕捉されることはない。他方で、濾過補助材層を含まないフィルターを通常目詰まりさせるサンプル中の粒子は、マイクロビーズ表面上及び多孔質球状マイクロビーズ間の間隙に捕捉されるであろう。マイクロビーズの多孔質構造のために、濾過時のサンプル流は、ビーズの間を通過するだけでなく、マイクロビーズ自体にも浸透し、そのため、サンプル粒子は、ビーズ間の間隙よりもビーズ表面に捕捉される傾向があり、そのことにより多孔質球状濾過補助材層は、高い粒子捕捉能力をもたらし、大容量微粒子サンプルの濾過の際のフィルターの目詰まりを防止できる。サンプルの完全な濾過後に、濾過補助材層を崩壊させて、マイクロビーズを洗浄溶液中に懸濁させることができる。この洗浄溶液を濾過して、微粒子サンプルの最初の濾過の間に濾過補助材層に捕捉される病原体を収集できることにより、フィルターへの病原体固定化収量を改良することができる。この洗浄プロセスを数回繰り返して、フィルターへの病原体の回収量を最大にすることができる。洗浄溶液は、一般に、病原体に悪影響を及ぼさない緩衝溶液又は増殖培養液である。
【0065】
フィルターと濾過補助材に加え、本開示は、病原体検出反応の間の病原体検出試薬の蒸
発を防ぎ、フィルター中で病原体の増殖を局在化させるために、ポリマー材料を使用することにも関する。有用なポリマー材料には、多糖類及びタンパク質などの天然又は合成ポリマーがある。ポリマー材料の幾つかの例には、寒天、アルギネート、カラギーナン、セルロース、キトサン、デキストラン、ペクチン、コラーゲン、フィブリノゲン、アクリレートポリマー、ポリエチレングリコール、ポリビニルアルコール並びにこれらの誘導体及びコポリマーがあるが、これらに限定はされない。ポリマー材料は、分子内及び/又は分
子間架橋によりヒドロゲルを形成することが望ましい。ヒドロゲルは、膨潤し得るが水に不溶であり、かつ一定の期間、蒸発せずに水又は溶液を保持し得る3次元高分子網目構造体である。
【0066】
特定の実施形態では、ヒドロゲルは、環境感受性ヒドロゲルである。有用な環境感受性ヒドロゲルは、環境からの刺激、例えば、温度、pH、光、イオン、圧力、磁場、電場、音波照射又は生化学的分子の1つ又は複数に応答し得る。環境感受性ヒドロゲルが、ゾル形態である場合、物質は水溶性ポリマーの形状であるが、刺激を与えた結果として、物質はゲル形態(ヒドロゲル)に変換され、不水溶性となり、分子内又は分子間架橋される。ゾル形態とゲル形態の間の変換は完全に又は部分的に起こり得る。特定の実施形態では、環境感受性ヒドロゲル及び環境的刺激は、特に生存病原体を検出すべき場合、病原体に有害ではない。特定の実施形態では、ゾル形態は、孔を容易に充填するためには、フィルター孔に容易に流入できないほど高粘性であってはならない。ゲル形態は、病原体検出試薬の蒸発を防止し、病原体の増殖を効果的に局在化させる。環境感受性ヒドロゲルの幾つかの例には、アガロース、低融点アガロース、カラギーナン、ペクチン、メチルセルロース及びPluronic F127があるが、これらに限定はされない。アガロースは、〜45℃でゾル形態であり、〜37℃まで冷却するとゲルとなる。低融点アガロースは、〜37℃でゾル形態であり、〜20℃でゲル形態である。カラギーナン及びペクチンは、カリウム及びカルシウムなどの特定のイオンの不在下でゾル形態であり、これらのイオンを添加するとゲルとなる。メチルセルロース及びPluronic F127は、〜4℃でゾル形態であり、〜37℃まで加温後にゲル形態となる。特定の実施形態では、適切なヒドロゲルの濃度は、種々のヒドロゲルに応じて変化し得る。特定の実施形態では、アガロース又は低融点アガロースの適切な濃度は、0.01%〜30%、好ましくは0.1%〜10%、更に好ましくは0.5%〜5%である。特定の実施形態では、サンプルの濾過後に、吸収、吸引、毛管作用、濾過、浸漬、スプレー又は他の技術によりゾル形態をデプスフィルター孔に添加することができ、環境からの刺激によりゲル形態に変換することができる。
【0067】
特定の実施形態では、サンプル濾過後に、フィルター孔はヒドロゲル粒子で充填される。ヒドロゲル粒子は、単分散系又は多分散系であって良い。ヒドロゲル粒子の有用な形状は、球形、四面体、六面体、多面体又は円柱形であるが、これらに限定はされない。しかしながら、任意の規則的又は不規則的な形状を使用することもできる。フィルター孔をヒドロゲル粒子で効果的に充填するために、ヒドロゲル粒子は、フィルター孔より小さく、フィルター孔に入り込むことができる。場合により、ヒドロゲル粒子は、フィルター中に保持されるのに十分なほどに大きく、かつ超多孔質のフィルターの保持率より大きくて良い。フィルター孔へのヒドロゲル粒子の加工は、吸収、吸引、毛管作用、濾過、浸漬、スプレー又は他の技術により遂行できる。有用なヒドロゲル粒子は、幾つかの慣用技術、例えば鋳造、乳化重合/ゲル化、沈殿重合、膜乳化、切断、スライス及び破砕などにより合成又は調製することができる。一部の実施形態では、ヒドロゲル粒子は、アガロースゲルから製造され、適切なアガロース濃度は、0.01%〜10%(w/v)、更に好ましくは0.1%〜5%(w/v)である。
【0068】
特定の実施形態では、フィルター孔は、脱水ヒドロゲルの水和作用によって満たされる。脱水ヒドロゲルが水和の際に膨潤すると、ヒドロゲル容積は劇的に増加する。脱水ヒド
ロゲルは、吸収、吸引、毛管作用、濾過、浸漬、スプレー又は他の技術により、フィルター孔に加工でき、脱水ヒドロゲルの水和は、例えば、水、緩衝液又は増殖培養液などの溶液により加工した後に行うことができる。特定の実施形態では、脱水ヒドロゲルは、単分散又は多分散粒子であり、脱水ヒドロゲル粒子のサイズは、フィルター孔に効果的に入るのに十分な小ささで良い。脱水ヒドロゲル粒子は、加熱、乾燥、凍結乾燥及び任意の他の技術によってヒドロゲル粒子を脱水することにより、調製することができる。特定の実施形態では、脱水ヒドロゲル粒子の水和作用は、10秒〜6時間、更に有利には1〜30分に及ぶ一定の時間がかかり、そのため、水和前に、溶液に懸濁する脱水ヒドロゲル粒子を前記技術によりフィルター孔に添加し、次いで孔内部をインキュベーションにより水和させることができる。
【0069】
特定の実施形態では、フィルター孔は、高粘性ポリマー溶液で充填される。この溶液は、フィルター孔に容易に流入し、孔を容易に充填することができないほど粘性が高くはないが、病原体の増殖を効果的に局在化するのに十分なほどの粘性がある。ポリマー溶液として、水溶性ポリマー又はヒドロゲル懸濁液を挙げることができる。
【0070】
特定の実施形態では、病原体検出試薬は、病原体の増殖培地を含有する。増殖培地は、通常、病原体増殖のための種々の塩、炭素源、窒素源及びアミノ酸の1つ又は複数を含む。特定の実施形態では、増殖培地は、選択的培地であり、抗菌作用/抗真菌効果、温度もしくはpH耐性又は特定の代謝産物の合成能力により、選択的に特定の病原体の増殖を促進し、そうして病原体を、他の競合バクテリア又は微生物に対し選択的に増殖させることができる。一部の実施形態では、病原体検出試薬は、増殖培地の酸素濃度を減らすことにより、特定の病原体の増殖を促進するか又は損傷した病原体の蘇生を促進する化合物、例えばL−システイン及びOxyrase(Oxyrase Inc.,Mansfield,OH)、を含有することができる。
【0071】
一部の実施形態では、病原体検出試薬は、他のバクテリア又は微生物から病原体を識別するシグナリング試薬を含有してよい。前記シグナリング試薬の一例は、病原体に特異的な酵素のための発色性又は発蛍光性の基質である。前記基質の例には、X−、ラピス(Lapis)−、マゼンタ(Magenta)−、サーモン(Salmon)−、グリーン(Green)−、ON
P−及びMU−結合基質、例えばβ−D−グルクロニド、β−D−ガラクト−ピラノシド、β−D−グルコ−ピラノシド、N−アセチル−β−D−ガラクトサミニド、N−アセチル−β−D−グルコサミニド、カプリレート−ノナノエート、ブチレート、myo−イノシトール−1−ホスフェート及びホスフェートがある。前記シグナリング試薬の別の例は、フェノールレッドなどのpH指示薬とキシロースなどの病原体特異的酵素用基質との組合せである。基質の代謝は、検出試薬のpHを変え、かつpH指示薬は比色法でpH変化を示す。前記シグナリング試薬の他の例は、病原体もしくは病原体特異的細胞成分を認識するDNA、RNA、LNA、PNAを含む核酸もしくは他の核酸、抗体、抗原、又はアプタマーである。これらのプローブ分子を、シグナル生成のため、蛍光染料分子、金又は銀コロイド、ポリマー粒子、磁性粒子、半導体粒子、量子ドット、フォトニック結晶粒子、リポソーム、ポリマーソーム、酵素、タンパク質及び核酸により標識化することができる。
【0072】
特定の実施形態では、環境感受性ヒドロゲルを使用する大容量の微粒子サンプル中の病原体の検出は、以下のステップを含む(図2)。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、超多孔質のフィルターと多孔質マイクロビーズ濾過補助材とを含む層状フィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)もし必要な場合は、フィルターへの病原体の回収率を最大にし、かつ病原体検出アッセイの潜在的な阻害剤を除去するために、フィルターと多孔質マイクロビーズ濾過補助
材を洗浄するステップ。
(3)フィルターを回収し、病原体検出試薬を含有する環境感受性ヒドロゲルのゾル形態を用いて、吸収、浸漬、スプレー又は他の技術によりフィルター孔に充填するステップ。(4)環境的刺激を与えて、環境感受性ヒドロゲルのゾル形態をゲル形態に変換するステップ。
(5)病原体を検出可能にするために病原体の増殖に十分な時間、ヒドロゲルを含有するフィルターをインキュベートするステップ。
(6)シグナリング試薬を使用して増殖病原体を検出するステップ。
【0073】
特定の実施形態では、ヒドロゲル粒子を使用する、大容量微粒子サンプル中の病原体の検出は、以下のステップを含む(図3)。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、超多孔質のフィルターと多孔質マイクロビーズ濾過補助材とを含む層状フィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)もし必要な場合は、フィルターへの病原体の回収率を最大にし、かつ病原体検出アッセイの潜在的な阻害剤を除去するために、フィルター及び/又は多孔質マイクロビーズ濾過補助材を洗浄するステップ。
(3)フィルターを回収し、病原体検出試薬を含有するヒドロゲル粒子を用いて、フィルター孔に充填するステップ。
(4)ヒドロゲル及び粒子を含有するフィルターを、病原体を検出可能にするために病原体の増殖に十分な時間、インキュベートするステップ。
(5)シグナリング試薬を使用して増殖病原体を検出するステップ。
【0074】
場合により、損傷した病原体の蘇生及び検出のために、サンプルの濾過及び病原体検出の前に、損傷した病原体の蘇生を可能にする増殖培地又は溶液中で微粒子サンプルを調製し、かつインキュベートできる。或いは、損傷した病原体は、サンプル濾過後に、インキュベーション(損傷した病原体の蘇生を可能にする増殖培地、溶液又は環境中で行なわれ得る)によりフィルター中で蘇生させ、病原体検出試薬により検出することができる。或いは、病原体検出試薬は、損傷した病原体を蘇生させるように構成され、かつ本明細書に記載のヒドロゲル物質を含有する又は含有しない状態で、追加の試薬、例えば抗生物質、の補充により、病原体検出試薬の濃度、成分又はpHをインキュベーションの間に変化させることができ、これにより、損傷病原体を蘇生させ、かつ検出することができる。
【0075】
微粒子サンプルの濾過及びヒドロゲル含有検出試薬の適用は、手作業を必要とし、これらのプロセスは、1時間以内に終了することができる。これらのプロセスは、標準的な自動化装置を使用して、容易に自動化することができる。病原体増殖及び検出のために必要なインキュベーション時間は、病原体の倍加時間と、シグナリング試薬の感度に依存する。フィルター中の1個の病原体を検出するのに必要とされるインキュベーション時間を、表1に示す。感度の低い発色基質を使用して、病原体を確認した場合ですら、全アッセイは、非常に短い実践時間で、24時間以内に終了することができる。
【0076】
【表1】

【0077】
特定の実施形態では、病原体を超多孔質フィルターへ固定後に、代替の病原体検出アッセイを使用することができる。1つの有用な病原体検出法は、ヒドロゲルを含まずに、病原体に特異的な酵素基質を含む選択的な培地中におけるフィルターインキュベーションである。発色性もしくは発蛍光性の酵素基質、又はフェノールレッドなどのpH指示薬とキシロースなどの病原体特異的酵素用基質との組合せを使用して、病原体を検出できる。培地の光学密度、光吸収、又は蛍光強度は、インキュベーション後に又はインキュベーションの間にわたり、測定又はモニターして、病原体の存在を検出することができる。又は培地中で増殖された病原体を慣用の病原体検出アッセイ、例えばポリメラーゼ連鎖反応(PCR)、逆転写ポリメラーゼ連鎖反応(RT−PCR)、核酸配列ベース増幅法(NASBA)、ループ媒介等温増幅法(LAMP)、その他の等温核酸増幅法、酵素結合免疫吸着法(ELISA)、免疫クロマトグラフィー、バイオセンサー又は核酸プローブなどにより検出することができる。或いは、病原体、又は特定の病原体の存在を指示する病原体の細胞成分、例えばゲノムDNA、リボソームRNA、トランスファーRNA、メッセンジャーRNA又はタンパク質などは、界面活性剤、カオトロピック試薬、有機溶剤又は電気泳動法を使用して、フィルター構造を破壊するか又は破壊せずにフィルターから抽出でき、かつ慣用の病原体検出法を使用して検出できる。或いは、フィルターに固定化された病原体は、フィルターに検知剤(sensing agent)を加工して検出することができる。有
用な検知剤は、静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、又は生物的相互作用により、フィルター内部に固定化することができる。検知剤の例は、米国特許第6087114号及びRider et al.,“AB Cell−Based
Sensor for Rapid Identification of Pathogens”,Science,301,213−15(2003)に開示されている病原体特異的抗体固定化B−細胞である。
【0078】
検出できる病原体の例には、ヒト、動物、植物、環境及び/又は産業に伝染性又は有害
である病原菌及び他の微生物がある。病原菌の例には、エシェリキア(Escherichia)、
サルモネラ、リステリア、カンピロバクター(Campylobacter)、シゲラ(Shigella)、
ブルセラ(Brucella)、ヘリコバクター(Helicobactor)、マイコバクテリウム(Mycobacterium)、ストレプトコッカス(Streptococcus)及びシュードモナス(Pseudomonas)
があるが、これらに限定はされない。病原性ウィルスは、本明細書に開示されるように、慣用の病原体検出法を併用して検出できる。病原性ウィルス科の例には、アデノウィルス科、ピコルナウィルス科、ヘルペスウィルス科、ヘパドナウィルス科、フラビウィルス科、レトロウィルス科、オルトミクソウィルス科、パラミクソウィルス科、パポバウィルス科、ラブドウィルス科及びトガウィルス科があるが、これらに限定されない。更に、開示
された濾過システムは、大容量の微粒子サンプル中の病原性及び非病原性微生物の両方の検出に有用である。
【0079】
検査できる微粒子サンプルの例には、食品サンプル、食品サンプルホモジネート、食品サンプルの洗浄溶液、飲料水、海/河川水、環境水、泥及び土があるが、これらに限定されない。更に、種々の環境表面を拭うスワブ、スポンジ及びタオルも検査することができる。更に、開示された濾過システムは、ヒトの体液、尿、血液及び製造用水/溶液を含む他の大容量の微粒子サンプルを検査するのに役立つ。サンプル、特に固体形、は、より効率良く濾過するために、サンプルの濾過前に、50〜1000μm孔を有するメッシュにより希釈、均質化及び/又は濾過することができる。
【0080】
病原体検出のための複合ヒドロゲルフィルター
特定の実施形態では、ヒドロゲルは、病原体認識能力を備えた超多孔質のフィルターに含まれて、複合ヒドロゲルフィルターを形成する。複合ヒドロゲルフィルターは、さまざまな手法で製造することができる。一実施形態では、ヒドロゲル又はヒドロゲル粒子は、ガラスファイバー又はニトロセルロース繊維などの繊維物質を含むフィルターマトリックスの上部、底部、又は内部に配置することができる。他の実施形態では、フィルターマトリックスは、ヒドロゲル繊維から形成される。ヒドロゲルは3次元高分子網目構造体なので、その脱水状態では超多孔質である。多孔度は、ヒドロゲルの生成に使用する重合方法に依存して調整することができる。一実施形態では、濾過の間、サンプル溶液は、ヒドロゲル内側の孔を通って浸透することができる。別の実施形態では、溶液は、ヒドロゲル粒子の間の間隙を通って濾過することができる。このように、複合ヒドロゲルフィルターでは、濾過の間、目詰まりが起こり得ない。複合ヒドロゲルフィルターの多種多様な実施形態を図4A〜4Dに示す。
【0081】
一実施形態では、複合ヒドロゲルフィルターは、ヒドロゲルの内側又は表面上に病原体検出試薬を含有し、検査すべきサンプル溶液の濾過後でも、効果的に試薬を保持する。別の実施形態では、サンプル濾過の間に病原体検出試薬が溶出するのを防止するために、環境感受性ヒドロゲル(スマートヒドロゲル)を使用して、病原体検出試薬を保持及び放出する。スマートヒドロゲルは、小さい物理的、生物学的又は化学的刺激に応答でき、縮小、膨潤及びゾル形態−ゲル形態間の変換等の大きな特性の変化を起こす。この実施形態では、膨潤している間は、病原体検出試薬がスマートヒドロゲル中に取り込まれた状態にある。スマートヒドロゲルは、サンプル濾過の間は、病原体検出試薬を放出しない。濾過後に環境的刺激を与えて、スマートヒドロゲルを縮まらせると、病原体検出試薬がスマートヒドロゲルから放出され、フィルターに分散する(図5)。病原体検出剤含有スマートヒドロゲル又はヒドロゲル粒子は、図4A〜4Cに示されるように、フィルターマトリックスの上部、その間、又は全体にわたって組み込むことができる。別の実施形態では、病原体検出試薬は、スマートヒドロゲルがゾル形態である間は、そこに取り込まれた状態にある。ゲル形態のスマートヒドロゲルは、サンプル濾過の間、病原体検出試薬を放出しない。濾過後に環境的刺激を与えて、スマートヒドロゲルをゾル形態に変換させると、病原体検出試薬が、スマートヒドロゲルから放出され、フィルター全体にわたり分散する。
【0082】
病原体検出試薬を含有する複合ヒドロゲルフィルターを使用する大容量微粒子サンプル中の病原体検出は、以下のステップを含み、図3に示される方法よりステップ数を少なくできる。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、複合ヒドロゲルフィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)もし必要な場合は、病原体検出アッセイ又は病原体増殖の潜在的な阻害剤を除去するために、フィルターを洗浄するステップ。
(3)病原体を検出可能にするために、病原体の増殖に十分な時間、フィルターをインキ
ュベートするステップ。
(4)シグナリング試薬を使用して増殖病原体を検出するステップ。
【0083】
分解性フィルター膜
特定の実施形態では、病原体認識能力を有する超多孔質のフィルターは、サンプル濾過後に、溶媒に分解又は溶解させ、固定化された病原体を効率よく収集する。分解性フィルターは、濾過の前又は間は、保全されるが、簡易処理により分解させることができる。このフィルターは、例えば合成の分解性もしくは腐食性ポリマー、又は天然の分解性もしくは腐食性ポリマー、又はこれらのコポリマーなどの分解性材料から製造される。合成分解性ポリマーには、ポリグリコール酸、ポリ乳酸、ポリヒドロキシブチレート(PHB)、ポリヒドロキシバレレート(PHV)、ポリカプロラクトン、ポリジオキサノン、ポリアンヒドリド、ポリシアノアクリレート、ポリアミノ酸、ポリオルトエステル、ポリホスファゼン、ポリプロピレンフマレート及びこれらのコポリマーがある。天然ポリマーには、コラーゲン、フィブリノゲン、フィブリン、ゼラチン、セルロース、キトサン、デンプン、アミロース、アルギネート、デキストラン、シルク、ケラチン、エラスチン、アクチン、ミオシン、グリコサミノグリカン、カラギーナン及びこれらのコポリマーがある。フィルターの分解は、加水分解、酸化又は酵素機構を介して行うことができる。
【0084】
分解性フィルターはさまざまな手法で製造することができる。一実施形態では、フィルターは、分解性ポリマーから構成されるので、サンプル溶液は、濾過の間、多孔質分解性ポリマー内側の孔を通って浸透することができる。別の実施形態では、フィルター膜は、多数の分解性ポリマー粒子から構成されるので、溶液は、分解性ポリマー粒子間の間隙を抜けて濾過することができる。従って、複合分解性フィルターが、濾過の間に詰まることはありえない。もう1つ別の実施形態では、フィルターは、分解性ポリマーコーティングが施された水溶性ポリマーから構成される。別の実施形態では、フィルターは、分解性ポリマーコーティングが施された多数の水溶性ポリマー粒子から構成される。複合ヒドロゲルフィルターの種々の実施形態が、図6A〜6Cに図示される。
【0085】
病原体検出試薬を含有する分解性フィルターを使用する大容量微粒子サンプルの病原体検出は、以下のステップを含む(図7)。
(1)検出すべき病原体を含有し得る大容量の微粒子サンプルを、分解性フィルターで濾過して、標的病原体をフィルターに収集するステップ。
(2)刺激を与えて、フィルターを溶液にするステップ。
(3)分解溶液から病原体又は病原体特異的分子マーカーを収集するステップ。
(4)病原体又は病原体特異的分子マーカーを検出するステップ。
【実施例】
【0086】
例1:環境感受性ヒドロゲルを使用する10%全乳での病原体検出アッセイ
病原体検出アッセイは、種々の用量のリステリア細胞を接種した10%全乳250mLに行った。
【0087】
リステリア・イノキュア(Listeria innocua)を、BHIブロス中で、37℃で一晩培養した。リステリア濃度は、1/106希釈後に、コロニーを数えて評価した。10%全乳は、全乳25mLを滅菌PBS緩衝液(pH7.4)225mLで希釈して調製した。リステリア検出試薬は、以下のようにして調製した。
(1)Fraser broth base(Oxoid,UK)11.5g及びBacto agarose2gを蒸留水200mL中に溶解させ、120℃で20分間滅菌し、45℃でゾル形態に保持した。
(2)Fraser supplement(Oxoid,UK)1vial/500mLとX−グルコシド(Sigma,MO)50mg/Lを溶液に追加した。
【0088】
病原体検出アッセイは、以下のようにして行った。
(1)リステリア(200cfu)接種サンプル又はリステリア−ネガティブサンプルを、GMF150 1μm(Whatman,NJ)で、真空濾過により濾過した。
(2)GMF150 1μm濾過媒体を滅菌容器に移し、45℃で5分間保持した。
(3)フィルターをリステリア検出試薬5mLに45℃で5分間浸漬し、リステリア検出試薬を室温まで冷却することでゲル形態に変換した。
(4)フィルターを、30℃で一晩インキュベートしてリステリア細胞の増殖を検出した。
【0089】
24時間のインキュベーション後、リステリア−ポジティブサンプルについてはリステリア細胞によるX−グルコシドの代謝のため、フィルター中にコロニー様着色スポットが観察された。これらの着色は、24時間より40時間で非常に濃くなり、このことは、リステリア細胞の増殖を示す(図8A、8B)。これとは対照的に、リステリアネガティブサンプルは、何ら着色を示さなかった(図8C、8D)。
【0090】
例2:ヒドロゲル粒子の調製
ヒドロゲル粒子を、油中水(W/O)乳化法を使用して調製した。低融点(LMP)アガロース(Invitrogen,Carlsbad,CA)溶液を、水に溶解し、濃度3%(w/v)にし、55℃に保持した。LMPアガロース溶液1mLを鉱油40mLに1滴づつ混合し、55℃に保持し、磁気撹拌機で強力に撹拌し、W/O乳液を形成した。撹拌しながら温度を4℃まで減じて、LMPアガロース含有乳液をゲル化して、LMPアガロース粒子を形成した。アガロース粒子を滅菌水で3度洗浄し、使用まで4℃に保持した。顕微鏡分析により、得られたアガロース粒子が、直径5〜50μmの球形であることを確認した(図9)。
【0091】
例3:ヒドロゲルマイクロビーズを使用する病原体検出アッセイ
新たに、リステリア・イノキュアを、BHIブロス中で、37℃で一晩培養した。アガロース粒子(250μL当量)を、X−グルコシド50mg/L、LiCl28g/L及びRapid L.Mono Supplement2(Biorad,CA)66.4μL/mLを含有する滅菌BHIブロス5mL中に、室温で少なくとも1時間懸濁させた。
【0092】
一連の希釈したリステリア細胞を含有するサンプルを、真空吸引を使用して、Nanoceramフィルター(直径47−mm,Argonide,FL)で濾過した。懸濁アガロース粒子を含有する溶液をフィルター上部に添加し、1分間インキュベートし、かつ真空吸引を使用して濾過した。アガロース粒子含有フィルターを37℃で最長2日までインキュベートした。17〜24時間のインキュベーション後に、リステリアの増殖を示すブルースポットが、裸眼で観察された。ブルースポットの数は、サンプル中に接種されたリステリア細胞の量によく相関した(図10)。
【0093】
例4:食品ホモジネートの濾過
多孔質球状マイクロビーズ(架橋ポリメタクリレート、EG50OH、日立化成、日本)0.5〜1g、多孔質マイクロビーズ(架橋デキストラン、Sephadex G25,GE Healthcare,NJ)0.5〜2g、無孔濾過補助材(ガラスビーズ、直径40μm、Filter aid 400,3M,MN)15gを使用するか又は濾過補助材を使用しないで、Nanocream filter(直径47−mm,Argonide,FL)又はGMF150 1μm(Whatman,NJ)について、食品ホモジネートの濾過速度を比較した。食品ホモジネートの濾過前に、濾過補助材を、ナノセーラムフィルター(Nanoceramfilter)又はGMF150 1μmフィルターの上流側
の面に置いた。
【0094】
食品ホモジネートは、以下のようにして調製した。
(1)食品サンプル(デリ・ミート、フランクフルトソーセージ又はスティックチーズ)25gを蒸留水225mLと混合した。
(2)食品サンプルを手動又はストマッカー(stomacher;Seward,UK)で、2
30rpmで2分間、粉砕消化(stomach)した。
(3)ストマッカー袋(Nasco,WI)付属のフィルターを使用して、食品ホモジネートを分離した。
【0095】
10%デリ・ミートホモジネートにおいて、濾過補助材無しのナノセーラムフィルター(黒三角)は、ホモジネート100mLより少量で目詰まりをおこした(図11A)。しかしながら、ガラスビーズ(黒四角)又は多孔質マイクロビーズ濾過補助材(架橋デキストラン2g、86〜258μm)(黒丸)を使用すると、フィルターの目詰まりを起こさずに、ホモジネートサンプル225mL全部を濾過することが可能であった。多孔質マイクロビーズ濾過補助材を用いる濾過は、5分以内に完了し、ガラスビーズ濾過補助材を用いる濾過よりはるかに迅速であった。
【0096】
10%チーズホモジネートにおいて、濾過補助材無し(黒三角)及びガラスビーズ濾過補助材有り(黒四角)のナノセーラムフィルターは、それぞれホモジネート5及び75mLより少量で目詰まりをおこした(図11B)。しかしながら、多孔質マイクロビーズ濾過補助材(架橋デキストラン、2g、86〜258μm)(黒丸)を使用すると、ホモジネート225mL全部を5分以内に濾過することができた。
【0097】
様々なグレードの多孔質球状マイクロビーズ濾過補助材の濾過性能を、10%デリ・ミートホモジネートを使用して比較した。架橋ポリメタクリレートマイクロビーズ(直径45〜90μm:0.5g(白丸)、1.0g(黒丸))及び架橋デキストランマイクロビーズ(直径17〜70μm:0.5g(白四角)、直径35〜140μm:0.5g(ひし形)、直径86〜258μm:0.5g(白三角)、1.0g(黒三角)、直径170〜520μm:0.5g(×))を、GMF150 1μmフィルターについて評価した(図12A)。直径170〜520μmの架橋デキストランマイクロビーズを除き、ホモジネート225mL全部は5分以内に完全に濾過された。
【0098】
様々なグレードの多孔質球状マイクロビーズ濾過補助材の濾過性能を、10%フランクフルトソーセージホモジネートを使用して同様に比較した。架橋ポリメタクリレートマイクロビーズ(直径45〜90μm:0.5g(白丸))及び架橋デキストランマイクロビーズ(直径17〜70μm:0.5g(白四角)、直径35〜140μm:0.5g(ひし形)、直径86〜258μm:0.5g(白三角)、直径170〜520μm:0.5g(×))を、GMF150 1μmフィルターについて評価した(図12B)。ホモジネート225mL全部は5分以内に完全に濾過された。これらの実験により、多孔質マイクロビーズ濾過補助材が慣用の無孔濾過補助材より、優れた粒子捕捉能力及び濾過能力を有することが説明される。
【0099】
実験5:10%デリ・ミートホモジネート225mLでの病原体検出アッセイ
病原体検出アッセイは、種々の用量のリステリア細胞を接種した10%デリ・ミートホモジネート225mLを用いて行った。
【0100】
リステリア・モノサイトゲネス(Listeria monocytogenes)及びリステリア・イノキュアを、BHIブロス中で、37℃で一晩培養した。リステリア濃度は、1/106希釈後に、コロニーを数えて評価した。10%デリ・ミートホモジネートは、以下のようにして
調製した。
(1)デリ・ミート25gを滅菌PBS緩衝液(pH7.4)225mLと混合した。
(2)デリ・ミートサンプルをストマッカー(Seward,UK)により、230rpmで2分間、粉砕消化した。
(3)ストマッカー袋(Nasco,WI)付属のフィルターを使用して、デリ・ミートホモジネートを分離した。
濾過の前に、デリ・ミートホモジネートに、種々の用量のリステリア細胞を接種した。多孔質マイクロビーズ濾過補助材(架橋デキストラン、直径86〜258μm、Sephadex G25,GE Healthcare,NJ)は、BHIブロスに懸濁させ(50g/L)、120℃で20分間滅菌した。リステリア検出試薬は以下のようにして調製した。
(1)フレーザーブロス基礎培地(Fraser broth base;Oxoid,UK)11.5g
及びバクトアガロース(Bacto agarose)2gを蒸留水200mL中に溶解させ、120
℃で20分間滅菌し、45℃でゾル形態に保持した。
(2)フレーザーサプリメント(Fraser supplement)(Oxoid,UK)1vial
/500mlとX−グルコシド(Sigma,MO)50mg/Lを溶液に追加した。
【0101】
病原体検出アッセイは、以下のようにして行った。
(1)多孔質マイクロビーズ濾過補助材0.5gを、GMF150 1μm濾過媒体(直径47mm:Whatman,NJ)及びポリエチレンメッシュセパレーター(穴:直径330μm)の上部に置いた。
(2)多孔質マイクロビーズ濾過補助材0.5gを、リステリア接種デリ・ミートホモジネートと混合した。
(3)デリ・ミートホモジネートを真空濾過により濾過した。
(4)多孔質マイクロビーズを滅菌PBS溶液(pH7.4)20mLで徹底的に3回洗浄した。
(5)GMF150 1μm濾過媒体を滅菌容器に移し、45℃で5分間保持した。
(6)フィルターをリステリア検出試薬5mLに45℃で5分間浸漬し、リステリア検出試薬を室温まで冷却することでゲル形態に変換した。
(7)フィルターを、30℃で一晩インキュベートしてリステリア細胞の増殖を検出した。
【0102】
24時間のインキュベーション後、リステリア細胞によるX−グルコシドの代謝のため、フィルター中にコロニー様着色スポットが観察された(図13A、13C)。これらの着色は、24時間より40時間で更に濃くなり、このことは、リステリア細胞の増殖を示す(図13B、13D)。これとは対照的に、リステリアネガティブサンプルは、3日間のインキュベーション後ですら何ら着色を示さなかった(図13E、13F)。着色スポットの数は、接種リステリア細胞の数に密接に相関し、10%デリ・ミートホモジネート〜225mL(デリ・ミート25g)から接種リステリア細胞の約60%が濾過媒体に収集された(図14A、図14B)。
【0103】
例6:複合ヒドロゲルフィルター
複合ヒドロゲルフィルターの製作のために、アルミナナノ繊維(病原体認識試薬)を含むナノセーラムフィルター(直径47−mm,Argonide,FL)を、ヒドロゲルを担持するマトリックスとして使用した。費用が安いため、寒天ヒドロゲルを使用した。ナノセーラムフィルターで寒天ゲルを濾過して、新しいフィルターを製作した。病原体認識試薬、ここではアルミナナノ繊維、が、ヒドロゲルで被覆されると、これらは、病原体との静電相互作用の損失のため、通常、機能不全になり得るが、ここで、ナノセーラムフィルターは、多層から構成されるデプスフィルターであり、この問題が起こるのを防ぐために最上層を、寒天ヒドロゲルで被覆した。
【0104】
製作手順は、以下に説明する。ナノセーラムフィルターの最上層を、バルク膜から剥がし、1%寒天溶液を最上層に注いだ。次いで、寒天溶液は、真空下に最上層を通って濾過され、最上層のもともとの多孔性を保持した。その後、最上層を室温で空気乾燥させ、少量の水をその上にスプレーし、かつコンプレッサーを使用して、層を一緒に圧縮して、再びバルク膜へ取り付けた。最終的に組立てられたフィルター膜は、室温で乾燥させた。
【0105】
製造されたフィルター膜を、以下の手順により、病原体溶液を使用して検査した。
(1)フィルター膜を滅菌水150mLで洗浄した。
(2)BHIブロス10mL中リステリア細胞約103cfuをフィルターに添加し、真空下で濾過した。
(3)濾過後に、BHIブロス5mL及びX−グルコシド(発色基質)50mg/Lをフィルター膜に添加した。
(4)フィルター膜を37℃で15時間インキュベートした。
【0106】
図15は、その結果を示す。着色は、インキュベーション後にフィルター上に発見されたリステリア細胞の存在を示す
【0107】
例7:スマートヒドロゲルにより固定化された病原体検出試薬を有する複合ヒドロゲルフィルター
温度が37℃(インキュベーション温度)に達すると、縮む能力を有するので、感熱性ヒドロゲル、ポリ(N−イソプロピルアクリルアミド)/キトサンを使用した。合成は、以下のステップを含む。
(1)キトサン(0.03g)、酢酸(240μl)及びNIPAm(1.6g)を蒸留水(20mL)に溶解させた。
(2)架橋剤、N,N’−メチレンビスアクリルアミド(0.06g)、開始剤2,2−ジメトキシ−2−フェニルアセトフェノン(0.01g)及び触媒N,N,N’,N’−テトラメチルエチレンジアミン(200μl)を溶液に添加し、窒素下に40分間脱気した。
(3)溶液を、ペトリ皿中で、365nmUV光下で2時間光重合させた。
(4)ヒドロゲルを、毎日水を換えながら、蒸留水に3日間浸漬した。
生成されたスマートヒドロゲルを粉砕して、小粒子にし、X−グルコシド(発色基質)200mg/Lを有するBHIブロスに浸漬し、37℃と25℃との間で数回、加熱/冷却した。次いで粒子を集め、ヒドロゲル複合ナノセーラムフィルター(例6に示される)を使用して、図5に図示されるように、スマートヒドロゲル粒子を最上層とバルク層との間に添加することにより組み立てた。
【0108】
乾燥フィルター膜は、病原体溶液を使用して、以下の手順に従い、検査した。
(1)フィルター膜を滅菌水150mLで洗浄した。
(2)BHIブロス中のリステリア細胞(〜104cfu/mL)5mLを濾過した。
(3)フィルターを、密閉容器中で37℃で15時間インキュベートした。
【0109】
図16は、その結果を示す。検出すべきサンプルの濾過後に、なんら発色基質溶液を添加することなく、着色がフィルター上に見られた。
【0110】
例8:分解性フィルター膜
k−カラギーナン及びアルギン酸ナトリウムを使用して、分解性フィルターを製作した。アルギン酸ナトリウム0.4g、k−カラギーナン0.2g及びPluronic F127(界面活性剤)0.2gを蒸留水30mlに90℃で溶解させ、次いで酢酸100μlを溶液に添加した。重炭酸ナトリウム0.2gを溶液に移し、気泡を発生させた。泡
状溶液を形成後、溶液の10mLを直径60mmのペトリ皿に注いだ。ペトリ皿の溶液を室温まで冷却すると、多孔質ゲルが形成された。次いでゲル膜を0.5MCaCl2と0.5MKCl溶液に1時間浸漬して、架橋ヒドロゲル構造体を形成した。その後、架橋ヒドロゲル構造体を、真空下に凍結乾燥し、分解性ヒドロゲルフィルターを製造した。
【0111】
分解性フィルターを使用する病原体検出アッセイを行った。リステリア・イノキュア〜109cfuを接種したPBS緩衝液50mLを、真空吸引で、分解性ヒドロゲルフィルターに通して濾過させた。次いで、フィルターを100mMEDTA溶液10mL中で80℃で15分間インキュベートして、ヒドロゲルフィルターを完全に溶解させた。取扱説明書に従い、DNA Clean&Concentrator−5キット(Zymo research,CA)を使用して、フィルター溶解溶液240μLから、リステリアゲノムDNAを抽出した。抽出されたリステリアゲノムDNAは、ABI7900(Applied biosystem,CA)を用いるリアルタイムPCRにより検出し、閾値サイクル(Ct)値は23〜24.5である(図17)。他方、リステリアゲノムDNAは、ネガティブ対照、リステリアネガティブPBS緩衝液10mL、では検出されなかった。
【0112】
本発明の精神から逸脱せずに多数かつ種々の変更をなし得ることは当業者であれば理解するであろう。よって、上述した本発明の態様は、一例にすぎず、本発明の範囲を限定する意図はないことが、明確に理解されるべきである。
【特許請求の範囲】
【請求項1】
サンプル中の微生物を検出する方法であって、
濾過中の目詰まりが防止された孔を有し、かつ静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物相互作用からなる群から選択される相互作用により、微生物を引きつける繊維状物質を有するデプスフィルターであるフィルター媒体でサンプルを濾過することにより、微生物をフィルターに収集するステップと、
微生物の増殖を局在化させ及び/又は微生物検出試薬の蒸発を防止するポリマーと、微生物検出試薬とをフィルターに加工するステップと、
前記フィルターをインキュベートして、微生物を検出できるレベルに増殖させるステップと、
サンプル中の微生物の存在を検出するステップと
を含む方法。
【請求項2】
前記濾過ステップ後に、フィルターを洗浄して、微生物の検出又は増殖を阻害する物質を除去するステップを更に含む請求項1に記載の方法。
【請求項3】
前記繊維状物質が、セルロース繊維、ガラスマイクロファイバー又はヒドロゲル繊維を含む請求項1に記載の方法。
【請求項4】
微生物を認識する薬剤が、前記フィルターのマトリックス上に特異的又は非特異的に固定化されており、この薬剤が、抗体、抗原、アプタマー、タンパク質、核酸及び炭水化物からなる群から選択される請求項1に記載の方法。
【請求項5】
前記ポリマーが、環境感受性ヒドロゲルであり、この環境感受性ヒドロゲルが、温度、pH、入射光量、イオン濃度、圧力、磁場、電場、音波照射及び生化学的分子濃度といった環境的変化を受ける前は、少なくとも部分的にゾル形態であって、低粘度を有しているが、環境的変化を受けると、粘度が増加し、少なくとも部分的にゲル形態となる請求項1に記載の方法。
【請求項6】
前記フィルターへの前記環境感受性ヒドロゲルの加工が、
少なくとも部分的にゾル形態である環境感受性ヒドロゲルを含む溶液を前記フィルターに加工するステップと、
環境的変化を与えて、前記溶液をゲル化するステップと
を含む請求項5に記載の方法。
【請求項7】
前記ポリマーがヒドロゲル粒子である請求項1に記載の方法。
【請求項8】
前記ヒドロゲル粒子を含む懸濁液の吸収、吸引、濾過、浸漬及びスプレーからなる群から選択される手法により、前記ヒドロゲル粒子を加工するステップを更に含む請求項7に記載の方法。
【請求項9】
前記ヒドロゲル粒子が、前記フィルターの孔より小さく、よって、前記フィルターの孔を効率的に塞ぐ請求項7に記載の方法。
【請求項10】
前記フィルターが、多孔質で球状のマイクロビーズの層を更に備える請求項1に記載の方法。
【請求項11】
前記微生物検出試薬が、微生物の増殖を選択的に促進する増殖培地を備える請求項1に記載の方法。
【請求項12】
前記増殖培地が、微生物は耐性を持つが、他の有機体は耐性を持たない選択的な試薬又は抗生物質を含むか、微生物は迅速に増殖し及び/又は他の有機体の増殖は緩慢に若しくは阻害するように選択されたpH及び温度を含むか、又は微生物により容易に代謝されるが、他の有機体によっては容易に代謝されない栄養素を含む請求項11に記載の方法。
【請求項13】
前記検出ステップが、微生物の存在下でシグナルを生じるシグナリング試薬からのシグナルを検知し、それによって微生物を検出することを含む請求項11に記載の方法。
【請求項14】
前記シグナリング試薬が、微生物に特異的な酵素のための基質、微生物に特異的な酵素のための発色性又は発蛍光性の基質、及び微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性又は発蛍光性の指示薬との組合せからなる群から選択される請求項13に記載の方法。
【請求項1】
サンプル中の微生物を検出する方法であって、
濾過中の目詰まりが防止された孔を有し、かつ静電相互作用、親水性相互作用、疎水性相互作用、物理的相互作用、及び生物相互作用からなる群から選択される相互作用により、微生物を引きつける繊維状物質を有するデプスフィルターであるフィルター媒体でサンプルを濾過することにより、微生物をフィルターに収集するステップと、
微生物の増殖を局在化させ及び/又は微生物検出試薬の蒸発を防止するポリマーと、微生物検出試薬とをフィルターに加工するステップと、
前記フィルターをインキュベートして、微生物を検出できるレベルに増殖させるステップと、
サンプル中の微生物の存在を検出するステップと
を含む方法。
【請求項2】
前記濾過ステップ後に、フィルターを洗浄して、微生物の検出又は増殖を阻害する物質を除去するステップを更に含む請求項1に記載の方法。
【請求項3】
前記繊維状物質が、セルロース繊維、ガラスマイクロファイバー又はヒドロゲル繊維を含む請求項1に記載の方法。
【請求項4】
微生物を認識する薬剤が、前記フィルターのマトリックス上に特異的又は非特異的に固定化されており、この薬剤が、抗体、抗原、アプタマー、タンパク質、核酸及び炭水化物からなる群から選択される請求項1に記載の方法。
【請求項5】
前記ポリマーが、環境感受性ヒドロゲルであり、この環境感受性ヒドロゲルが、温度、pH、入射光量、イオン濃度、圧力、磁場、電場、音波照射及び生化学的分子濃度といった環境的変化を受ける前は、少なくとも部分的にゾル形態であって、低粘度を有しているが、環境的変化を受けると、粘度が増加し、少なくとも部分的にゲル形態となる請求項1に記載の方法。
【請求項6】
前記フィルターへの前記環境感受性ヒドロゲルの加工が、
少なくとも部分的にゾル形態である環境感受性ヒドロゲルを含む溶液を前記フィルターに加工するステップと、
環境的変化を与えて、前記溶液をゲル化するステップと
を含む請求項5に記載の方法。
【請求項7】
前記ポリマーがヒドロゲル粒子である請求項1に記載の方法。
【請求項8】
前記ヒドロゲル粒子を含む懸濁液の吸収、吸引、濾過、浸漬及びスプレーからなる群から選択される手法により、前記ヒドロゲル粒子を加工するステップを更に含む請求項7に記載の方法。
【請求項9】
前記ヒドロゲル粒子が、前記フィルターの孔より小さく、よって、前記フィルターの孔を効率的に塞ぐ請求項7に記載の方法。
【請求項10】
前記フィルターが、多孔質で球状のマイクロビーズの層を更に備える請求項1に記載の方法。
【請求項11】
前記微生物検出試薬が、微生物の増殖を選択的に促進する増殖培地を備える請求項1に記載の方法。
【請求項12】
前記増殖培地が、微生物は耐性を持つが、他の有機体は耐性を持たない選択的な試薬又は抗生物質を含むか、微生物は迅速に増殖し及び/又は他の有機体の増殖は緩慢に若しくは阻害するように選択されたpH及び温度を含むか、又は微生物により容易に代謝されるが、他の有機体によっては容易に代謝されない栄養素を含む請求項11に記載の方法。
【請求項13】
前記検出ステップが、微生物の存在下でシグナルを生じるシグナリング試薬からのシグナルを検知し、それによって微生物を検出することを含む請求項11に記載の方法。
【請求項14】
前記シグナリング試薬が、微生物に特異的な酵素のための基質、微生物に特異的な酵素のための発色性又は発蛍光性の基質、及び微生物に特異的な酵素のための基質とこの基質の消化を検出する発色性又は発蛍光性の指示薬との組合せからなる群から選択される請求項13に記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図11】


【図12】


【図14】


【図17】


【図8】


【図9】


【図10】


【図13】


【図15】


【図16】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図11】


【図12】


【図14】


【図17】


【図8】


【図9】


【図10】


【図13】


【図15】


【図16】


【公開番号】特開2013−9674(P2013−9674A)
【公開日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願番号】特願2012−163534(P2012−163534)
【出願日】平成24年7月24日(2012.7.24)
【分割の表示】特願2010−519256(P2010−519256)の分割
【原出願日】平成20年8月1日(2008.8.1)
【出願人】(000004455)日立化成工業株式会社 (4,649)
【出願人】(500294958)ヒタチ ケミカル リサーチ センター インコーポレイテッド (27)
【Fターム(参考)】
【公開日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願日】平成24年7月24日(2012.7.24)
【分割の表示】特願2010−519256(P2010−519256)の分割
【原出願日】平成20年8月1日(2008.8.1)
【出願人】(000004455)日立化成工業株式会社 (4,649)
【出願人】(500294958)ヒタチ ケミカル リサーチ センター インコーポレイテッド (27)
【Fターム(参考)】
[ Back to top ]

