小豆煮汁抽出物を含む脂質代謝改善剤
【課題】新規な脂質代謝改善剤を提供する。
【解決手段】小豆煮汁を、デンプン質、タンパク質又はペクチン質を分解する少なくとも1種の酵素で処理し、当該処理後の上澄み液を濃縮することにより得られ、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分として含む。この脂質代謝改善剤は、脂質の吸収を阻害し、血清中の中性脂肪や低密度コレステロール濃度を低下させると共に、脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症の発症を予防又は治療するために有用である。
【解決手段】小豆煮汁を、デンプン質、タンパク質又はペクチン質を分解する少なくとも1種の酵素で処理し、当該処理後の上澄み液を濃縮することにより得られ、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分として含む。この脂質代謝改善剤は、脂質の吸収を阻害し、血清中の中性脂肪や低密度コレステロール濃度を低下させると共に、脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症の発症を予防又は治療するために有用である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、特定の小豆煮汁抽出物を有効成分として含む脂質代謝改善剤に関し、より詳細には、小豆の餡を製造する際の副産物として生成する小豆煮汁抽出物を酵素処理し、さらに濃縮することにより得られ、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分とする脂質代謝改善剤及びその脂質代謝改善剤を含有する食品等に関するものである。
【背景技術】
【0002】
十勝の特産物である小豆には、様々な機能性物質があることが知られている。例えば、小豆餡を製造する際に排出される煮汁は、これまで廃棄処分されてきたが、この煮汁には、カテキンやアントシアニンのようなポリフェノールが含まれている。小豆煮汁のポリフェノール成分とその抗酸化作用については多くの報告がある。例えば、鮮やかな赤色を呈する天然の色付け剤(特許文献1)や、小豆種皮を有効成分として含有する血圧上昇抑制剤及び動脈硬化症予防改善剤(特許文献2)、小豆ポリフェノールによる膵リパーゼ活性抑制作用と高脂肪食雌マウスの体重増加抑制作用(非特許文献1)及び小豆の廃液から得られる有用材料のラジカル消化能、抗酸化作用、高脂血症改善予防作用等(特許文献3)などが報告されている。
【0003】
上記の特許文献1は、従来は廃棄されていた小豆の煮汁を有効利用する技術に関するものである。小豆の煮汁を酵素処理、膜濃縮という簡単な操作で処理することにより、小豆由来の色素成分を含み、炭水化物、ミネラル及びポリフェノールを主成分とする濃縮物を得ることができる。製造コストも安く、実用的であり、自然由来の色素を主成分としていることから、市場での人気も高く天然色素として市場に出回っているが、その薬理作用については全く記載していない。
【0004】
特許文献2には、小豆種皮に含まれる有効成分が、ラットを用いた動物実験で、血圧の上昇、血管内皮における活性酸素の産生、NAD(P)Hオキシダーゼのサブユニットの発現及び炎症性サイトカイン(MCP−1)の産生を抑制し、アテローム性動脈硬化症を予防改善しうることが記載されている。また、非特許文献1には、小豆煮汁から糖やタンパク質を除去して抽出したポリフェノールが、膵リパーゼの活性を阻害し、これによって高脂肪食を与えた雌マウスにおける食餌性脂肪の消化、吸収を抑制し、脂肪が糞中に排泄されて体重増加が抑制されている可能性について報告している。
【0005】
特許文献3は、小豆餡又は煮小豆の製造工程中に得られる廃液から不溶物を除去した後減圧下で濃縮した濃縮物が、ラジカル消化能、抗酸化作用にすぐれ、さらに、高脂血症改善予防作用、癌抑制・アレルギー疾患改善などの免疫能を高める作用、糖尿病予防改善作用、内臓脂肪蓄積予防抑制作用及びメタボリックシンドロームの予防改善作用を有することが記載されている。
【0006】
しかしながら、上記先行技術文献はいずれも小豆由来の成分の有用性を示唆するものであるが、活性が十分とはいえず、かつその活性成分や脂質代謝改善作用のメカニズムについての詳細な検討は行われていないのが現状である。そのため、小豆由来の資源を有効利用すると共にその機能をさらに高め、あるいは作用メカニズムの解明を通じて効果的な使用方法を明らかにする必要がある。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−295365号公報
【特許文献2】特開2010−229069号公報
【特許文献3】特開2007−151537号公報
【非特許文献】
【0008】
【非特許文献1】日本食品科学工学会誌、第54巻、第5号、229−232頁、2007年
【発明の概要】
【発明が解決しようとする課題】
【0009】
近年、日本において食生活の欧米化による脂肪の取りすぎと、多忙な生活による慢性的な運動不足から引き起こされる肥満は、高血圧、心臓病、糖尿病等の生活習慣病の危険因子として問題となっている。本発明は、このような問題に関連してなされたものであって、上記特許文献1に記載の小豆煮汁抽出物が、食物繊維やポリフェノール等が含まれている複合物であることから、様々な相互作用により、新しい機能が見出せるのではないかと考え、その生体への効果とメカニズムを探索することにより、新規な脂質代謝改善剤を見出すことを課題とする。
【課題を解決するための手段】
【0010】
上記課題を解決するために本発明者らは鋭意検討を重ねた結果、小豆煮汁の抽出物、特に、特定の処理により得られた抽出物に脂質代謝改善作用があることを見出し、かかる知見に基づいて本発明を完成した。
【0011】
すなわち、本発明の脂質代謝改善剤は、小豆煮汁を、デンプン質、タンパク質、又はペクチン質を分解する少なくとも1種の酵素で処理し、当該処理後の上澄み液を濃縮することにより得られ、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分として含むことを特徴とする。また、前記ポリフェノールの含有量が、小豆煮汁抽出物に対する固形分換算で少なくとも15重量%であることが好ましい。
【0012】
1つの実施形態において、本発明の脂質代謝改善剤は、食事中の脂質吸収を抑制するために用いられることを特徴とする。他の1つの実施形態では、血清中の中性脂肪濃度;低密度、中密度及び超低密度コレステロールの総濃度;並びに内臓脂肪の蓄積量からなる群から選択される1つ以上を減少させるための脂質代謝改善剤が提供される。さらに異なる1つの実施形態において、本発明の脂質代謝改善剤は、脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症の発症を予防又は治療するために用いられることを特徴とする。
【0013】
本発明の他の視点では、上記脂質代謝改善剤の有効量を含み、脂質代謝改善機能を有する食品、又は脂質代謝を改善する必要のある対象者のための健康食品、機能性食品又は特定保健用食品が提供される。さらに異なる視点において、脂質含有食品に、上記脂質代謝改善剤の有効量を添加してなる、当該食品中の脂質の吸収及び/又は代謝を抑制するための食品が提供される。
【発明の効果】
【0014】
本発明の脂質代謝改善剤は、動物実験において膵リパーゼ活性の抑制作用により脂質の吸収を阻害することが示された。また、血清中の中性脂肪や低密度コレステロール濃度を低下させることも分かった。さらに、脂肪細胞の成熟化段階において脂肪滴の蓄積やIL−6、PAI−1及びMCP−1のような炎症性又は血液凝固系のアディポサイトカインの分泌を抑制することから、脂質代謝の異常及びこれに伴う種々の疾患を改善、予防するために有用であると考えられる。
【図面の簡単な説明】
【0015】
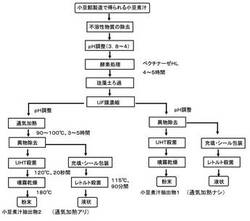
【図1】本発明の脂質代謝改善剤に含まれる小豆煮汁抽出物の製造方法の概略を示す工程図である。
【図2】実施例1で本発明の脂質代謝改善剤を含む実験食を投与したラットの血清中の総コレステロール及びHDL−コレステロール濃度の経時変化を示すグラフである。
【図3】実施例1で本発明の脂質代謝改善剤を含む実験食を投与したラットの血清中の中性脂肪及び低密度+中密度+超低密度コレステロール濃度の経時変化を示すグラフである。
【図4】実施例1で本発明の脂質代謝改善剤を含む実験食を4週間投与したラット糞便中の総脂質排出量を示すグラフである。
【図5】実施例1で本発明の脂質代謝改善剤を含む実験食を4週間投与したラット肝臓中の総脂質量を示すグラフである。
【図6】実施例1で本発明の脂質代謝改善剤のブタ膵リパーゼ活性に与える影響を調べた結果である。
【図7】実施例1で本発明の脂質代謝改善剤を含む実験食を4週間投与したラットの血漿中のレジスチン濃度を示すグラフである。
【図8】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるトリグリセリドの蓄積量を測定した結果である。
【図9】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるGPDH活性を測定した結果である。
【図10】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるIL−6の分泌量を測定した結果である。
【図11】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるPAI−1の分泌量を測定した結果である。
【図12】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるMCP−1の分泌量を測定した結果である。
【発明を実施するための形態】
【0016】
[本発明の脂質代謝改善剤及びその製造方法]
本発明の脂質代謝改善剤は、小豆煮汁を処理して得られ、鮮やかなアズキ色を呈した溶液状又は粉体状の抽出物を有効成分として含む。その製造方法は、例えば、特許文献1に記載された方法又はそれと類似する方法を用いることができ、その典型的な製造方法の概要を図1に示す。以下に、図1を参照しながら、本発明の脂質代謝改善剤に有効成分として含まれる小豆煮汁抽出物の製造方法について簡単に説明する。
【0017】
まず、出発原料として用いる小豆煮汁は、製餡工場における小豆の渋切工程で回収される小豆煮汁が好ましい。小豆の渋切り工程で生じる煮汁には、渋み成分であるポリフェノールの他にデンプン質、タンパク質、脂質、無機塩類などが含まれている。この小豆煮汁に、デンプン質、タンパク質、ペクチン質等の高分子成分を分解するために必要な酵素を添加し、例えば、20〜60℃で1〜6時間、好ましくは30〜50℃で4〜5時間攪拌しながら酵素反応を行う。添加する酵素は、デンプン質分解酵素としてはアミラーゼ等が、タンパク質分解酵素としてはプロテアーゼ等が、及びペクチン質分解酵素としてはペクチナーゼ等を用いることができ、これらの中から選択される1種以上の酵素であれば得に制限されるものではないが、好ましくはこれらの1種又は2種以上の混合物として市販されている酵素を使用することができる。例えば、ヤクルト薬品工業製の品名ペクチナーゼHLなどが挙げられる。これにより、煮汁に含まれているデンプン質、タンパク質、及びペクチン質などの高分子成分を分解し、後続する膜濃縮工程における膜の目詰まりを防止する作用もある。また、液体食品に添加した場合のオリ(沈殿)の発生を防止することもできる。
【0018】
その後、静置して小豆煮汁に含まれている未分解のデンプン質、繊維質、タンパク質、脂質などの成分を沈殿させ、ろ過による上澄み液を取り出す。この上澄み液を限外ろ過膜装置などにより10〜20倍の濃縮を行う。この膜濃縮工程により、有効成分である小豆のポリフェノールを濃縮し、さらにミネラルや食物繊維とのバランスを調整することができる。水分や余分のミネラル、糖質等の低分子成分を除去することができれば濃縮方法は問わないが、限外ろ過膜による濃縮が好ましい。この目的のための限外ろ過膜は通常分画分子量が3,000〜50,000のものを用いる。このようにして得られた濃縮液はさらに加工することができる。第1に、濃縮液をpH8〜9に調整した後、90〜100℃の温度で、空気を吹き込みながら3〜5時間通気加熱を行う。これにより、小豆色が強くなり、着色性がよりいっそう増強された小豆煮汁抽出物を製造することができる。さらに、これを高温短時間殺菌後、噴霧乾燥して粉末にするか、あるいは液状のままレトルト殺菌等で殺菌する工程により保存性にすぐれた製品(通気加熱アリ)が得られる。第2に、濃縮液をpHを8〜9に調整した後、通気加熱工程を行わずに上記と同様の乾燥、殺菌工程を経て粉末状又は液状の製品(通気加熱ナシ)とする。
【0019】
このようにして得られた小豆煮汁抽出物は、食物繊維、ミネラル、ポリフェノールを含み、ポリフェノールは、小豆煮汁抽出物全量に対して固形分換算で15〜25重量%程度含有されている。ミネラル成分の含有量は、小豆煮汁抽出物全量に対して固形分換算で10〜25重量%程度含まれていることが好ましく、食物繊維としては30〜60重量%程度である。上記製造方法により得られた小豆煮汁抽出物粉末の組成の一例は以下の表1に、またそのミネラル成分の組成を表2に示されるが、好ましい範囲内においてこれらの含有量は適宜調整することができる。
【0020】
本発明に係る小豆煮汁抽出物は、一般に使用されている担体、助剤、添加剤等とともに製剤化することができ、例えば、医薬製剤の形態で脂質代謝改善剤として用いることができる。本発明の脂質代謝改善剤は、例えば、錠剤、コーティング錠、糖衣錠、硬及び軟ゼラチンカプセル、溶液、エマルジョン又は懸濁液の剤形で、経口投与することができる。しかし、投与は、例えば坐薬の剤形で腸内にも、又は例えばオイルパック剤等の経皮的の剤形で非経口的に行うこともできる。
【0021】
上記の錠剤、コーティング剤、糖衣錠及び硬ゼラチンカプセルを製造するために、薬学的に不活性な無機又は有機賦形剤と共に加工することができる。乳糖、トウモロコシデンプン又はそれらの誘導体、タルク、ステアリン酸又はその塩等は、例えば錠剤、糖衣錠及び硬ゼラチンカプセルのそうした賦形剤として用いることができる。
【0022】
さらに、本発明の脂質代謝改善剤は、保存剤、可溶化剤、安定化剤、湿潤剤、乳化剤、甘味料、着色剤、香料、浸透圧を変化させるための塩、緩衝剤、マスキング剤又は酸化防止剤を含有することができる。本発明の脂質代謝改善剤は、治療に価値があるさらに他の物質も含有することができる。本発明の脂質代謝改善剤は、食品の形態にあってもよい。
【0023】
[脂質代謝改善剤としての用途]
本発明の脂質代謝改善剤は、哺乳動物(例えば、ヒト、マウス、ラット、ウサギ、イヌ、ネコ、ウシ、ウマ、ブタ、サル等)の脂質代謝を改善する必要のある対象者のために用いるものであって、具体的には、以下のような用途に使用される。
(1)食事中の脂質吸収を抑制する用途:
本発明の脂質代謝改善剤は、膵リパーゼ活性を阻害して消化管からの脂肪の吸収を抑制するから、脂肪の取りすぎと、慢性的な運動不足から引き起こされる肥満を抑制する必要のある対象者にとって脂質代謝が改善されると考えられる。
(2)血清中の中性脂肪濃度、低密度、中密度及び超低密度コレステロールの総濃度を低下させる用途:
中性脂肪や、低密度、中密度及び超低密度コレステロールは、高血圧や動脈硬化を引き起こす素因となることから、これらの脂質成分の血中濃度が高い対象者にとって脂質代謝の改善作用を有すると考えられる。
(3)内臓脂肪の蓄積を減少させる用途:
後述する実施例に示すように、本発明の脂質代謝改善剤は、膵リパーゼ活性を阻害することにより、消化管からの脂肪の吸収を抑制するとともに、肝臓に蓄積する脂質量を低下させる働きがある。内臓脂肪の蓄積は種々の慢性疾患の素因となるから、このような対象者にとって脂質代謝の改善作用を有すると考えられる。
【0024】
(4)脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症を予防又は治療する用途:
生体内の脂肪細胞は、エネルギーを備蓄する働きだけでなく、さまざまな生理活性物質(アディポサイトカイン)を分泌する細胞であることが分かっている。アディポサイトカインにはさまざまな種類が存在する。インスリンの働きを阻害して糖尿病を引き起こす腫瘍壊死因子(TNF−α)をはじめ、高血圧と関連するアンジオテンシノーゲン、血栓の形成に関係し心筋梗塞や脳卒中の原因となるプラスミノーゲン活性化抑制因子(PAI―1)などで、脂肪細胞から大量に分泌されて動脈硬化などの発症に強く関連している。これらのいわゆる悪玉アディポサイトカインは内臓脂肪の増加によってさらにその合成・分泌量が増えるという性質がある。そのため内臓脂肪が蓄積するに従い高血圧や糖尿病、高脂血症が進展し、脳卒中や心疾患を発症させやすくなる。したがって、本発明において、脂質代謝の異常とは、肥満の原因となる脂肪細胞の肥大化や過形成、内臓脂肪の蓄積、及び脂肪細胞からのアディポサイトカインの分泌異常などの状態を含み、合併症とは、脂質代謝の異常に伴って発症する高血圧や糖尿病、高脂血症などをいうがこれらに限定されない。
【0025】
正常な、肥満していない、小型の脂肪細胞からはアディポネクチンなどの善玉アディポサイトカインが活発に分泌されて、悪玉アディポサイトカインはほとんど分泌されない。逆に、肥満して肥大化した脂肪細胞からは善玉アディポサイトカインは出なくなり、悪玉アディポサイトカインの分泌が活発になることが分かっている。従って、本発明の脂質代謝改善剤は、脂質代謝異常の原因である悪玉アディポサイトカインの分泌を抑制し、これによって脂肪細胞の肥満を抑制するから、ヒト脂肪細胞からのアディポサイトカインの分泌調節剤、又はヒト脂肪細胞の肥大化抑制剤として用いることができる。
【0026】
「脂質代謝改善剤の有効量」という用語は、ある個人の脂質代謝の状態を改善するのに必要な量を意味する。用量は、それぞれの脂質代謝の状態における個々の要求に適用させることができる。用量は、改善すべき脂質代謝の重篤度、対象者の年齢及び全般的な健康状態、投与経路及び剤形、並びに医師の経験のような多数の要因に応じて広い範囲内で変化させることができる。本発明の脂質代謝改善剤の有効成分である小豆煮汁抽出物は、成人1人当たり0.5〜100mg/kg体重(好ましくは1〜50mg/kg体重)、非経口的に投与する場合は0.05〜50mg/kg体重(好ましくは0.5〜50mg/kg体重)の範囲で一日1〜3回に分けて投与することができる。
【0027】
[食品及び健康食品としての用途]
本発明の脂質代謝改善剤は、飲食品に配合し、脂質代謝改善機能を有する食品として用いることができる。このためには、その有効成分である小豆煮汁抽出物の有効量を飲食品の製造原料段階、製造の中間工程段階又は最終製品の段階で添加、配合する。ここで、「小豆煮汁抽出物の有効量」とは、個々の飲食品において通常喫食される量を摂取した場合に、上述したような範囲で有効成分が摂取されるような含有量をいう。より具体的には、本発明による食品は、上述した小豆煮汁抽出物をそのまま飲食品として調製したもの、各種タンパク質、糖類、脂肪、微量元素、ビタミン類等を更に配合したもの、液状、半液体状若しくは固体状にしたもの、一般の飲食品へ添加したものであってもよい。
【0028】
本発明において「食品」とは、健康食品、機能性食品、及び特定保健用食品を含む意味で用いられる。また「食品」の形態は特に限定されるものではなく、例えば、飲料の形態であってもよい。本発明の健康食品は、好ましくは単位用量剤形である。単位用量剤形とは、有効成分の適切な1回投与量に分割された製剤をいう。この単位用量剤形は、包装された調剤であってよく、錠剤、カプセル剤、散剤及び顆粒剤それ自体でも、あるいは適切な数のそれらのいずれかが包装された形であってもよい。1つの実施形態において、本発明の健康食品、機能性食品、特定保健用食品は、脂質代謝を改善する必要のある対象者のために用いられることが好ましい。このような対象者を特定するためには、食品の包装や添付文書にその旨を記載することができる。
【0029】
その他の飲食品として具体的には、ジュース類、清涼飲料水、茶類、乳酸菌飲料、発酵乳、冷菓、乳製品(バター、チーズ、ヨーグルト、加工乳、脱脂乳等)、畜肉製品(ハム、ソーセージ、ハンバーグ等)、魚肉練り製品(蒲鉾、竹輪、さつま揚げ等)、卵製品(だし巻き、卵豆腐等)、菓子類(クッキー、ゼリー、スナック菓子)、パン類、麺類、漬物類、燻製品、干物、佃煮、塩蔵品、スープ類、調味料などを例示することができるが、これらに制限されない。1つの実施形態において、本発明の脂質代謝改善剤は、脂質含有食品に添加されることが好ましく、当該食品を摂取した者にとって食品中の脂質の吸収及び/又は代謝を抑制して肥満や成人病を予防することができる。
【0030】
本発明に係る健康食品及び食品は、ヒトが飲食品として長年摂取してきた小豆抽出成分であることから、毒性も低く、哺乳動物に対し安全に用いられる。食品として摂取する場合には、成人1人1日当たり30〜6000mgの範囲、好ましくは60〜3000mgの範囲の摂取量となるよう本発明による有効成分を食品に配合することができる。
【実施例】
【0031】
以下に本発明を、実施例によりさらに詳細に説明するが、本発明は実施例に限定されるものではなく、種々の変更例が可能である。
【0032】
製造例1:小豆煮汁抽出物の製造
出発原料として用いる小豆煮汁は、製餡工場における小豆の渋切工程で回収される小豆煮汁を用いた。不溶性物質を除去した後、pHを3.8〜4に調整した小豆煮汁に、あらかじめ所定量を水に溶かして調製したペクチナーゼHL(ヤクルト薬品工業製)を0.005〜0.001重量%となるように添加し、50℃で4〜5時間攪拌しながら酵素反応を行った。その後、静置して小豆煮汁に含まれている未分解のデンプン質、繊維質、タンパク質、脂質などの成分を沈殿させ、ろ過による上澄み液を取り出した。この上澄み液を限外ろ過膜装置により濃縮した後に、苛性ソーダ(水酸化ナトリウム)を加えて上澄み液のpHを8〜9に調整した。50メッシュのストレーナーで異物を除去した後、超高温殺菌装置で120℃、20秒間の殺菌(UHT)処理を行った。殺菌した濃縮液のうち、粉末製品用の400Lをスプレードライヤーに供給し、180℃の熱風により乾燥させて、40kgの粉末状製品(小豆煮汁抽出物1(通気加熱ナシ))を得た。また、液状製品用としては、同様に製造した濃縮発色液400Lをレトルト用パックに100〜150mlずつ入れ、シールした後、レトルト装置で115℃90分間殺菌して約400kgの液状製品を製造した。
【0033】
一方、通気加熱した小豆煮汁抽出物2を製造するために、上述した限外ろ過膜濃縮後、pHを8〜9に調製した濃縮液を、噴霧装置を付けたタンクに投入し、タンクの底部から上部のスプレー口に濃縮液を送り込んで噴霧循環させ、90〜100℃に維持しつつ3〜5時間噴霧して濃縮液に空気を送り込んだ後、タンクの壁に冷却水を循環させ、約20℃まで冷却した。この濃縮液を2つに分け、上記と同様の方法により噴霧乾燥した粉末状製品(小豆煮汁抽出物2、(通気加熱アリ)と、液状製品を得た。上記製造方法により得られた小豆煮汁抽出物粉末の組成を以下の表1に、またそのミネラル成分の組成を表2に示す。なお、これらの分析方法は、日本食品標準成分分析マニュアルに記載の方法に基づく。例えば、ポリフェノールの分析は、Foline-Denis法、ミネラル成分中のリンは、バナドモリブデン酸吸光光度法、リン以外のミネラル成分は原子吸光光度計法を用いた。
【0034】
【表1】

【0035】
【表2】

【0036】
実施例1:動物実験
[実験動物及び飼育条件]
実験動物は8週齢のFischer系雄ラット20匹を日本チャールズ・リバー株式会社から購入した。飼育条件は23±1℃、湿度60±5%とし、明暗周期12時間(明07:00/暗19:00)とした。ラットはプラスチックケースを用いて1個体ずつ飼育した。ラットの取り扱いは、Guide of the Care and Use of Laboratory Animalsに従って行った。
【0037】
[実験食]
標準食にはAIN93G(オリエンタル酵母株式会社製)を使用し、その群を標準食群(C)とした。そして標準食に表1で示した小豆煮汁抽出物2(通気加熱アリ)を1%添加したものを小豆煮汁抽出物投与群(A)とした。また、AIN93G(オリエンタル酵母株式会社製)にラード15%を添加したものを高脂肪食対照群(CF)、高脂肪食対照群に1%の小豆煮汁抽出物2(通気加熱アリ)を添加したものを小豆煮汁抽出部添加高脂肪食対照群(AF)とした。これら実験食の組成を表3に示した。
【0038】
【表3】

【0039】
[投与実験]
8週齢雄ラット20匹に市販のラット用粉末飼料を与えた1週間の予備飼育後、各投与群で体重に有意差が出ないように3つの投与群に各群5匹ずつ群分けを行った。投与期間は4週間とし、1匹のラットに1日あたり25gの実験食を投与、食餌と水は自由摂取とした。1週毎に体重・摂食量の計測を行った。摂食量は給与量と残量の差から算出した。また毎週、頸静脈から採血を行った。採血は一晩絶食させた後、空腹時に行い、得られた血液はエッペンチューブに入れて2時間室温放置後、15分間7000rpmで遠心分離し、血清画分を分画し、分析まで−30℃で保存した。また、投与期間最後の3日間の糞を採取し、分析まで−30℃で保存した。投与期間終了後、ラットにネンブタール麻酔をかけ解剖、心臓採血、肝臓の摘出を行った。摘出した肝臓は冷生理食塩水(9gNaCl/L)で洗浄し、乾燥したろ紙で水分を除去してから重量測定後、液体窒素で冷凍し、−80℃で保存した。
【0040】
[血清の生化学的成分の分析]
総コレステロール、高密度アポリポタンパク質コレステロール(HDLコレステロール)、中性脂肪、遊離脂肪酸の4項目の測定は酵素法により行った。総コレステロール濃度と高密度アポリポタンパク質コレステロール濃度の差を超低密度アポリポタンパク質コレステロール+中密度アポリポタンパク質コレステロール+低密度アポリポタンパク質コレステロール(VLDL+IDL+LDLコレステロール)濃度とした。その結果を図2及び3に示した。なお、以下に示すそれぞれのデータは平均値±標準偏差で表わした。データ間の有意差検定はt−検定を行い、p<0.05を有意とした。
【0041】
図2に示したように、血清中の総コレステロール量は、3週目から4週目において標準食群(C)と、小豆煮汁抽出物投与群(A)とで有意な差が認められ、高脂肪食群においても小豆煮汁抽出物の添加により低下する傾向が見られた。一方、図3に示したように、血清中性脂肪(TG)については、標準食群において、小豆煮汁抽出物を添加した方が有意に低下しており、高脂肪食群においても低下する傾向がみられた。
【0042】
[糞中の全脂質量の測定]
約0.5gの糞をネジ付試験管(φ15)に量り取り、凍結乾燥機(東京理科機器社製FDU−830型)により凍結乾燥させた。これに4%酢酸を加えたクロロホルム−メタノール混合液(2:1,v/v;C−M)を2ml加え、超音波発生装置(ブランソン社製5510J−MT型)で10分間処理して脂溶性物質の抽出を行い、冷却多本架遠心機(コクサン社製80R型、4℃)を用い10分間2000rpmで遠心分離することによりC−M層と残渣に分離し、上層であるC−M層を別のネジ付試験管(φ18)に移した。この残渣に同様の操作を2回繰り返し、得られたC−M層に1.5mlの1%塩化バリウム溶液を加え、試験管ミキサー(IWAKI社製251型)で撹拌した後、10分間2000rpmで遠心分離することで、クロロホルム層と水層に分離した。上層である水層を除去し、残ったクロロホルム層にメタノールを適当量加えロータリーエバポレーター(SHIBATA社製RE111型)で減圧濃縮し、さらにC−M(2:1)を加え減圧濃縮することで全脂質を得て重量を測定した。これにC−M(2:1)を1ml加え−30℃で保管した。その結果を図4に示した。
【0043】
図4に示したように、ラット糞中の脂質排出量は、高脂肪食の両方の群において、小豆煮汁抽出物を添加した方が有意に多いことが分かった。
【0044】
[肝臓中総脂質の定量]
上記の方法と同様に肝臓中の全脂質を抽出し、肝臓中の総脂質量を測定した。その結果を図5に示した。肝臓中の脂質量は、高脂肪食群において有意な差が認められ、小豆煮汁抽出物の添加により脂肪の蓄積が抑制されると考えられる。
【0045】
[膵リパーゼ活性抑制試験]
基質液の作成
Hanらの方法に従って、トリオレイン240mg、レシチン30mg、胆汁酸15mg、0,1Mトリス塩酸緩衝液で溶解し、超音波発生装置で10分間処理したものを基質液とした。
膵リパーゼ
基質液0.2mlを、シンフレックス用マルチブロック付き恒温槽を用いて400rpmで30℃になるまで温め、その後ブタ由来膵リパーゼ(50μg/ml)0.1ml、及び検体液(50μg/ml)0.2mlを加え、700rpm 37℃で反応させた。今回は(1)反応時間を30分に保ち、用いた小豆煮汁抽出物の濃度を変えた場合、(2)濃度を一定に保ち、反応時間を変えた場合との2種類の実験行った。
遊離オレイン酸量の測定
遊離したオレイン酸量は、NEFA−HAテストワコー(和光純薬工業株式会社)を用いて測定した。
(1)では活性値は検体無添加の値を100%とし、(2)では遊離脂肪酸基準液を用いて濃度を算出することによって、活性値を算出した。
【0046】
図6に示したように、小豆煮汁抽出物の用量依存的にリパーゼ活性が低下し、50%阻害を示す濃度は12.5μg/mlであった。経時的に測定した遊離オレイン酸濃度も小豆煮汁抽出物の添加により生成が抑制されることが分かる。
【0047】
[血清レジスチン濃度の測定]
表4に示したキットを用い、後述する実施例2に記載した方法に従って、4週間経過後のラット血清中のレジスチン濃度を測定した結果を図7に示した。標準食及び高脂肪食のいずれの群においても血清レジスチン濃度の低下傾向が見られ、高脂肪食群では有意に低下していることが分かった。なお、レジスチンは肥大した脂肪細胞で産生され、骨格筋や肝臓でインスリン伝達を傷害し、インスリン抵抗性を誘導すると考えられている。
【0048】
実施例2:ヒト脂肪細胞を用いた実験
[使用細胞、試薬]
ヒト内臓前駆脂肪細胞はプライマリーセル株式会社より購入した。培養に使用した24ウェルプラスチックプレートは旭硝子株式会社より購入した。通常培地の内臓脂肪分化メディウム Ver.2、0.01%コラーゲン、HBSS(−)バッファーはプライマリーセル株式会社より、増殖促進培地に添加したFibroblast Growth Factor(basic)は和光純薬工業(株)より購入した。分化促進培地に添加したDexamethazone、TroglitazoneはSIGMA-ALDRICH Japan Lidより、Isobutyl-1-methylxanthine、試薬調製のためのジメチルスルホキシドは和光純薬工業株式会社より購入した。
【0049】
[細胞培養]
実験材料としてプライマリーセルより購入したヒト内臓脂肪細胞Human Preadipocyte (3.5×105 cell)(ScienCell Research Laboratoties )の3継代の細胞を用いて、培養には24ウエルプレートを使用した。増殖培地は終濃度10ng/mlとなるように FGF(Fibroblast Growth Factor(basic)を添加した内蔵脂肪分化メディウムVer.2を使用。分化誘導培地にはそれぞれ終濃度1μM Dexamethazone、0.05mM IBMX、10μM Troglitazoneを添加した内蔵脂肪分化メディウムVer.2を使用した。
【0050】
培養方法は、まず、24ウェルプレートに500μlずつ0.01%コラーゲンを添加し、ウェル全体にコラーゲンをコーティングした後、余分なコラーゲンを吸引し、HBSS(−)バッファーで2度洗浄した。他方、25mlの増殖培地に1mlの前駆内臓脂肪細胞を混合しておいた。これを1mlずつコラーゲンコートされたプレートのウェルに細胞を播種してった。定法に従い室温37℃、湿度95%、CO2 5%条件でヒト内臓脂肪細胞を増殖培地で3日間培養した。コンフルエントになったところで分化誘導培地に交換した。4日間この分化誘導培地で分化させた後、通常培地の内蔵脂肪分化メディウムVer.2へ交換、その3日後に250〜750μg/mlの小豆煮汁抽出物1(通気加熱ナシ)又は小豆煮汁抽出物2(通気加熱アリ)を添加した。培養計14日後に細胞を回収しトリグリセライド量、GPDH活性、それらを補正するためのDNA量をそれぞれ測定した。また、14日目の培地を回収し、遠心分離により沈殿物を取り除いた上澄み液を用い、イライザ法によりアディポサイトカインの発現量を測定した。また、回収した細胞からトータルRNAを抽出し、cDNAを合成した。
【0051】
[分析方法]
TG測定はトリグリセライドE−テストワコー(和光純薬工業株式会社:Lot No.KJ677)GPDH活性測定(GPDH Assay Kit, Code No.AK01 プライマリーセル株式会社Lot. ILU)DNA量の定量は超微量分光光度計 ナノドロップ NanoDrop ND−2000 (Thermo Fisher Scientific社)を使用した。なお、以下の測定データにおいて、それぞれのデータは平均値±標準誤差(S.E.)で表した。データ間の有意差検定は、一元分散分析の後Turkey-Kramer testで事後比較を行った。P<0.05を有意とした。
【0052】
[TG蓄積量の測定]
脂肪細胞のトリグリセライドの定量はトリグリセライドE−テストワコー(和光純薬工業株式会社)を使用し、添付の使用説明書の方法に従って定量を行った。すなわち、試薬は発色剤1瓶を緩衝液1瓶で溶解しておいた。検体は14日間培養後の細胞プレートを500μlのPBSバッファーで全てのウェルを2回洗浄した後、0.4μlのPBSバッファーを加え、超音波処理機で細胞を磨砕したものを使用した。各濃度のサンプルとスタンダードを150μlに発色試薬3mlを加えよく混合しウォーターバスで37℃、5分間保温し、600nmで吸光度を測定した。計算法は以下の通りである。
トリグリセライド濃度(mg/dl)=検体吸光度/スタンダード吸光度×300
この値をDNA量で補正したものをTG蓄積量とした。
【0053】
その結果を図8に示した。通気加熱アリ/ナシともに、用量依存的に脂肪細胞内のTG蓄積量を減少させることが分かった。
【0054】
[GPDH活性測定]
GPDH活性の測定はGPDH Assay Kit (プライマリーセル株式会社)を使用し、添付の使用説明書の方法に従って定量を行った。すなわち、反応基質溶液は、反応基質のバイアル1本に対し精製水4.2mlで溶解した。酵素抽出溶液は酵素抽出試薬を精製水200mlで溶解した。検体は14日間培養後の細胞プレートを500μlのPBSバッファーで全てのウェルを2回洗浄した後、酵素抽出溶液を1ウェルあたり700μlを加えた。このプレートを超音波処理機を用いて細胞を磨砕した溶液を回収し、冷却遠心分離(4℃、12800g、5分間)で分離した上清を検体として使用した。測定方法は、反応基質溶液80μlを96マイクロプレートに加え25℃に5分間加温した。また検体も25℃で保温した。その後、マイクロプレート内に検体40μlを加え、よく攪拌した後、波長340nmにおける吸光度減少率を経時測定し、1分間あたりの吸光度の変化量(ΔO.D.)を10分間求めた。計算方法は以下の通り。
光路長(cm)=反応総量/プレートのウェル底面積=0.12/0.25=0.48
GPDH活性(U/ml)
=(ΔO.D./NADHのミリモル分子吸光係数)×(反応総量ml/検体量ml)
×(検体希釈率/光路長cm)
=(ΔO.D./6.22)×(0.12/0.04)×(5/0.48)
この値をDNA量で補正したものをGPDH活性値とした。
【0055】
その結果を図9に示した。ジヒドロキシアセトンリン酸からTGの合成に必要なグリセロール3リン酸を生成する酵素であるGPDH活性も、本発明の脂質代謝改善剤の添加により有意に減少していることが明らかとなった。このことから、本発明の脂質代謝改善剤は、脂肪細胞の成熟段階におけるGPDH活性の抑制及びそれによるTGの蓄積抑制効果があることが示された。
【0056】
[アディポサイトカインの定量]
アディポサイトカインはELISA法を用いて定量を行った。検体は培養14日目の培地を回収し、14000rpmで5分間遠心分離し、分離した上清を−80℃で保存したものを使用した。使用したELISAキットは、表4の通りであり、各キットに添付されている使用説明書の方法に従って定量を行った。すなわち、ヒトアディポネクチンELISAキット(大塚製薬株式会社)の方法であれば、まず検体前処理液を蒸留水で5倍希釈した後、献体である培養上清10μlを希釈した見地前処理液90μlと混和し、ヒートブロックを用いて100℃で5分間加熱した。これに献体希釈液を900μl加え混和し、100倍希釈検体とした。
【0057】
【表4】

【0058】
希釈した洗浄液を抗体プレートの各ウェルに約350μlずつ加えた後、ウェルの液を完全に除去した。各濃度の標準液及び前処理済みの抗体を各ウェルに100μlずつ加え、室温で1時間静置反応させた。ウェルの液を完全に除去し、洗浄液を各ウェルに300μlずつ加え、再度速やかに吸引除去した。この洗浄と吸引の操作をさらに2回繰り返した後、ウェルに残った洗浄液を除去した。第一抗体液を抗体プレートの各ウェルに100μlずつ加え室温で1時間静置反応させた。再びウェルの液を完全に除去し、洗浄液を各ウェルに300μlずつ加え、再度速やかに吸引除去した。この洗浄と吸引の操作をさらに2回繰り返した後、ウェルに残った洗浄液を除去した。抗体標識抗体液を抗体プレートの各ウェルに100μlずつ加え、室温で1時間静置反応させた。再びウェルの液を完全に除去し、洗浄液を各ウェルに300μlずつ加え、再度速やかに吸引除去した。この洗浄と吸引の操作をさらに2回繰り返した後、ウェルに残った洗浄液を除去した。基質液を抗体プレートの各ウェルに100μlずつ加え、室温で15分間静置反応させた後、反応停止液を抗体プレートの各ウェルに100μlずつ加えた。プレートリーダーで各ウェルの450nmと対照波長の650nmの吸高度を測定した。
【0059】
以上の測定結果を図10〜図12に示した。脂質代謝系のアディポサイトカインであるレプチンやレジスチンのみならず。炎症性サイトカインであるIL−6や血液凝固系サイトカインであるPAI−1、血管内皮の炎症を引き起こすMCP−1の分泌も抑制することが分かった。したがって、本発明の脂質代謝改善剤は、肥大化した脂肪細胞から分泌されるサイトカインによって誘導される生体内における炎症状態又は炎症性疾患に対して有効であると考えられる。
【0060】
試作例1:ソーセージの製造
牛肉(赤身)525gをミンチ状とした後、豚脂225g及び氷水250gと均一に混練した。これに、食塩15g、脱脂粉乳20g、カラーミン10Nを1g、ウィンナーWを5g、砂糖5g、ブラックペッパー3g、ホワイトペッパー3g、コリアンダー1.5g、オールスパイス1g、ベイローレル0.5g、ナツメグ0.5g及び小豆煮汁抽出物2(粉末)3gを添加し、カッターキュアリングを行った。この原料肉を定法に従ってケーシング(腸詰)、スモーク(乾燥・燻煙)した後、製品の種類に応じて、湯煮または蒸煮により加熱処理を行い冷却後に包装した。
【0061】
試作例2:ハンバーグの製造
合い挽肉400gをミンチ状にし、たまねぎ(小)1個、サラダ油少々、食パン1枚、牛乳大さじ3杯、卵(小)1個、塩少々、こしょう少々、ナツメグ少々及び小豆煮汁抽出物2(粉末)を全量に対して1%となるように添加した。これらの原料をミキサーにかけてよく混合した後、成型、製品の種類に応じて加熱し、包装して冷凍した。
【0062】
試作例3:ジャーキーの製造
牛肉(赤身)1kgを整形し、これにたまねぎ(小)1個、にんにく3かけ、しょうゆ1カップ、日本酒0.5カップ、みりん0.5カップ、砂糖30g、塩30g、唐辛子少々、荒挽きこしょう少々及び小豆煮汁抽出物1(粉末)2gを添加して塩漬けした。これをスライス、乾燥、場合により熟成した後、製品として包装した。
【0063】
試作例4:天ぷら衣の製造
小麦粉10g、溶き卵1/2個分及び水大さじ1.5杯を混合し、その全量に対して小豆煮汁抽出物1(粉末)を1%添加混合して作成した。
【技術分野】
【0001】
本発明は、特定の小豆煮汁抽出物を有効成分として含む脂質代謝改善剤に関し、より詳細には、小豆の餡を製造する際の副産物として生成する小豆煮汁抽出物を酵素処理し、さらに濃縮することにより得られ、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分とする脂質代謝改善剤及びその脂質代謝改善剤を含有する食品等に関するものである。
【背景技術】
【0002】
十勝の特産物である小豆には、様々な機能性物質があることが知られている。例えば、小豆餡を製造する際に排出される煮汁は、これまで廃棄処分されてきたが、この煮汁には、カテキンやアントシアニンのようなポリフェノールが含まれている。小豆煮汁のポリフェノール成分とその抗酸化作用については多くの報告がある。例えば、鮮やかな赤色を呈する天然の色付け剤(特許文献1)や、小豆種皮を有効成分として含有する血圧上昇抑制剤及び動脈硬化症予防改善剤(特許文献2)、小豆ポリフェノールによる膵リパーゼ活性抑制作用と高脂肪食雌マウスの体重増加抑制作用(非特許文献1)及び小豆の廃液から得られる有用材料のラジカル消化能、抗酸化作用、高脂血症改善予防作用等(特許文献3)などが報告されている。
【0003】
上記の特許文献1は、従来は廃棄されていた小豆の煮汁を有効利用する技術に関するものである。小豆の煮汁を酵素処理、膜濃縮という簡単な操作で処理することにより、小豆由来の色素成分を含み、炭水化物、ミネラル及びポリフェノールを主成分とする濃縮物を得ることができる。製造コストも安く、実用的であり、自然由来の色素を主成分としていることから、市場での人気も高く天然色素として市場に出回っているが、その薬理作用については全く記載していない。
【0004】
特許文献2には、小豆種皮に含まれる有効成分が、ラットを用いた動物実験で、血圧の上昇、血管内皮における活性酸素の産生、NAD(P)Hオキシダーゼのサブユニットの発現及び炎症性サイトカイン(MCP−1)の産生を抑制し、アテローム性動脈硬化症を予防改善しうることが記載されている。また、非特許文献1には、小豆煮汁から糖やタンパク質を除去して抽出したポリフェノールが、膵リパーゼの活性を阻害し、これによって高脂肪食を与えた雌マウスにおける食餌性脂肪の消化、吸収を抑制し、脂肪が糞中に排泄されて体重増加が抑制されている可能性について報告している。
【0005】
特許文献3は、小豆餡又は煮小豆の製造工程中に得られる廃液から不溶物を除去した後減圧下で濃縮した濃縮物が、ラジカル消化能、抗酸化作用にすぐれ、さらに、高脂血症改善予防作用、癌抑制・アレルギー疾患改善などの免疫能を高める作用、糖尿病予防改善作用、内臓脂肪蓄積予防抑制作用及びメタボリックシンドロームの予防改善作用を有することが記載されている。
【0006】
しかしながら、上記先行技術文献はいずれも小豆由来の成分の有用性を示唆するものであるが、活性が十分とはいえず、かつその活性成分や脂質代謝改善作用のメカニズムについての詳細な検討は行われていないのが現状である。そのため、小豆由来の資源を有効利用すると共にその機能をさらに高め、あるいは作用メカニズムの解明を通じて効果的な使用方法を明らかにする必要がある。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特開2008−295365号公報
【特許文献2】特開2010−229069号公報
【特許文献3】特開2007−151537号公報
【非特許文献】
【0008】
【非特許文献1】日本食品科学工学会誌、第54巻、第5号、229−232頁、2007年
【発明の概要】
【発明が解決しようとする課題】
【0009】
近年、日本において食生活の欧米化による脂肪の取りすぎと、多忙な生活による慢性的な運動不足から引き起こされる肥満は、高血圧、心臓病、糖尿病等の生活習慣病の危険因子として問題となっている。本発明は、このような問題に関連してなされたものであって、上記特許文献1に記載の小豆煮汁抽出物が、食物繊維やポリフェノール等が含まれている複合物であることから、様々な相互作用により、新しい機能が見出せるのではないかと考え、その生体への効果とメカニズムを探索することにより、新規な脂質代謝改善剤を見出すことを課題とする。
【課題を解決するための手段】
【0010】
上記課題を解決するために本発明者らは鋭意検討を重ねた結果、小豆煮汁の抽出物、特に、特定の処理により得られた抽出物に脂質代謝改善作用があることを見出し、かかる知見に基づいて本発明を完成した。
【0011】
すなわち、本発明の脂質代謝改善剤は、小豆煮汁を、デンプン質、タンパク質、又はペクチン質を分解する少なくとも1種の酵素で処理し、当該処理後の上澄み液を濃縮することにより得られ、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分として含むことを特徴とする。また、前記ポリフェノールの含有量が、小豆煮汁抽出物に対する固形分換算で少なくとも15重量%であることが好ましい。
【0012】
1つの実施形態において、本発明の脂質代謝改善剤は、食事中の脂質吸収を抑制するために用いられることを特徴とする。他の1つの実施形態では、血清中の中性脂肪濃度;低密度、中密度及び超低密度コレステロールの総濃度;並びに内臓脂肪の蓄積量からなる群から選択される1つ以上を減少させるための脂質代謝改善剤が提供される。さらに異なる1つの実施形態において、本発明の脂質代謝改善剤は、脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症の発症を予防又は治療するために用いられることを特徴とする。
【0013】
本発明の他の視点では、上記脂質代謝改善剤の有効量を含み、脂質代謝改善機能を有する食品、又は脂質代謝を改善する必要のある対象者のための健康食品、機能性食品又は特定保健用食品が提供される。さらに異なる視点において、脂質含有食品に、上記脂質代謝改善剤の有効量を添加してなる、当該食品中の脂質の吸収及び/又は代謝を抑制するための食品が提供される。
【発明の効果】
【0014】
本発明の脂質代謝改善剤は、動物実験において膵リパーゼ活性の抑制作用により脂質の吸収を阻害することが示された。また、血清中の中性脂肪や低密度コレステロール濃度を低下させることも分かった。さらに、脂肪細胞の成熟化段階において脂肪滴の蓄積やIL−6、PAI−1及びMCP−1のような炎症性又は血液凝固系のアディポサイトカインの分泌を抑制することから、脂質代謝の異常及びこれに伴う種々の疾患を改善、予防するために有用であると考えられる。
【図面の簡単な説明】
【0015】
【図1】本発明の脂質代謝改善剤に含まれる小豆煮汁抽出物の製造方法の概略を示す工程図である。
【図2】実施例1で本発明の脂質代謝改善剤を含む実験食を投与したラットの血清中の総コレステロール及びHDL−コレステロール濃度の経時変化を示すグラフである。
【図3】実施例1で本発明の脂質代謝改善剤を含む実験食を投与したラットの血清中の中性脂肪及び低密度+中密度+超低密度コレステロール濃度の経時変化を示すグラフである。
【図4】実施例1で本発明の脂質代謝改善剤を含む実験食を4週間投与したラット糞便中の総脂質排出量を示すグラフである。
【図5】実施例1で本発明の脂質代謝改善剤を含む実験食を4週間投与したラット肝臓中の総脂質量を示すグラフである。
【図6】実施例1で本発明の脂質代謝改善剤のブタ膵リパーゼ活性に与える影響を調べた結果である。
【図7】実施例1で本発明の脂質代謝改善剤を含む実験食を4週間投与したラットの血漿中のレジスチン濃度を示すグラフである。
【図8】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるトリグリセリドの蓄積量を測定した結果である。
【図9】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるGPDH活性を測定した結果である。
【図10】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるIL−6の分泌量を測定した結果である。
【図11】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるPAI−1の分泌量を測定した結果である。
【図12】実施例2で本発明の脂質代謝改善剤を含む培地中で培養した成熟化ヒト脂肪細胞におけるMCP−1の分泌量を測定した結果である。
【発明を実施するための形態】
【0016】
[本発明の脂質代謝改善剤及びその製造方法]
本発明の脂質代謝改善剤は、小豆煮汁を処理して得られ、鮮やかなアズキ色を呈した溶液状又は粉体状の抽出物を有効成分として含む。その製造方法は、例えば、特許文献1に記載された方法又はそれと類似する方法を用いることができ、その典型的な製造方法の概要を図1に示す。以下に、図1を参照しながら、本発明の脂質代謝改善剤に有効成分として含まれる小豆煮汁抽出物の製造方法について簡単に説明する。
【0017】
まず、出発原料として用いる小豆煮汁は、製餡工場における小豆の渋切工程で回収される小豆煮汁が好ましい。小豆の渋切り工程で生じる煮汁には、渋み成分であるポリフェノールの他にデンプン質、タンパク質、脂質、無機塩類などが含まれている。この小豆煮汁に、デンプン質、タンパク質、ペクチン質等の高分子成分を分解するために必要な酵素を添加し、例えば、20〜60℃で1〜6時間、好ましくは30〜50℃で4〜5時間攪拌しながら酵素反応を行う。添加する酵素は、デンプン質分解酵素としてはアミラーゼ等が、タンパク質分解酵素としてはプロテアーゼ等が、及びペクチン質分解酵素としてはペクチナーゼ等を用いることができ、これらの中から選択される1種以上の酵素であれば得に制限されるものではないが、好ましくはこれらの1種又は2種以上の混合物として市販されている酵素を使用することができる。例えば、ヤクルト薬品工業製の品名ペクチナーゼHLなどが挙げられる。これにより、煮汁に含まれているデンプン質、タンパク質、及びペクチン質などの高分子成分を分解し、後続する膜濃縮工程における膜の目詰まりを防止する作用もある。また、液体食品に添加した場合のオリ(沈殿)の発生を防止することもできる。
【0018】
その後、静置して小豆煮汁に含まれている未分解のデンプン質、繊維質、タンパク質、脂質などの成分を沈殿させ、ろ過による上澄み液を取り出す。この上澄み液を限外ろ過膜装置などにより10〜20倍の濃縮を行う。この膜濃縮工程により、有効成分である小豆のポリフェノールを濃縮し、さらにミネラルや食物繊維とのバランスを調整することができる。水分や余分のミネラル、糖質等の低分子成分を除去することができれば濃縮方法は問わないが、限外ろ過膜による濃縮が好ましい。この目的のための限外ろ過膜は通常分画分子量が3,000〜50,000のものを用いる。このようにして得られた濃縮液はさらに加工することができる。第1に、濃縮液をpH8〜9に調整した後、90〜100℃の温度で、空気を吹き込みながら3〜5時間通気加熱を行う。これにより、小豆色が強くなり、着色性がよりいっそう増強された小豆煮汁抽出物を製造することができる。さらに、これを高温短時間殺菌後、噴霧乾燥して粉末にするか、あるいは液状のままレトルト殺菌等で殺菌する工程により保存性にすぐれた製品(通気加熱アリ)が得られる。第2に、濃縮液をpHを8〜9に調整した後、通気加熱工程を行わずに上記と同様の乾燥、殺菌工程を経て粉末状又は液状の製品(通気加熱ナシ)とする。
【0019】
このようにして得られた小豆煮汁抽出物は、食物繊維、ミネラル、ポリフェノールを含み、ポリフェノールは、小豆煮汁抽出物全量に対して固形分換算で15〜25重量%程度含有されている。ミネラル成分の含有量は、小豆煮汁抽出物全量に対して固形分換算で10〜25重量%程度含まれていることが好ましく、食物繊維としては30〜60重量%程度である。上記製造方法により得られた小豆煮汁抽出物粉末の組成の一例は以下の表1に、またそのミネラル成分の組成を表2に示されるが、好ましい範囲内においてこれらの含有量は適宜調整することができる。
【0020】
本発明に係る小豆煮汁抽出物は、一般に使用されている担体、助剤、添加剤等とともに製剤化することができ、例えば、医薬製剤の形態で脂質代謝改善剤として用いることができる。本発明の脂質代謝改善剤は、例えば、錠剤、コーティング錠、糖衣錠、硬及び軟ゼラチンカプセル、溶液、エマルジョン又は懸濁液の剤形で、経口投与することができる。しかし、投与は、例えば坐薬の剤形で腸内にも、又は例えばオイルパック剤等の経皮的の剤形で非経口的に行うこともできる。
【0021】
上記の錠剤、コーティング剤、糖衣錠及び硬ゼラチンカプセルを製造するために、薬学的に不活性な無機又は有機賦形剤と共に加工することができる。乳糖、トウモロコシデンプン又はそれらの誘導体、タルク、ステアリン酸又はその塩等は、例えば錠剤、糖衣錠及び硬ゼラチンカプセルのそうした賦形剤として用いることができる。
【0022】
さらに、本発明の脂質代謝改善剤は、保存剤、可溶化剤、安定化剤、湿潤剤、乳化剤、甘味料、着色剤、香料、浸透圧を変化させるための塩、緩衝剤、マスキング剤又は酸化防止剤を含有することができる。本発明の脂質代謝改善剤は、治療に価値があるさらに他の物質も含有することができる。本発明の脂質代謝改善剤は、食品の形態にあってもよい。
【0023】
[脂質代謝改善剤としての用途]
本発明の脂質代謝改善剤は、哺乳動物(例えば、ヒト、マウス、ラット、ウサギ、イヌ、ネコ、ウシ、ウマ、ブタ、サル等)の脂質代謝を改善する必要のある対象者のために用いるものであって、具体的には、以下のような用途に使用される。
(1)食事中の脂質吸収を抑制する用途:
本発明の脂質代謝改善剤は、膵リパーゼ活性を阻害して消化管からの脂肪の吸収を抑制するから、脂肪の取りすぎと、慢性的な運動不足から引き起こされる肥満を抑制する必要のある対象者にとって脂質代謝が改善されると考えられる。
(2)血清中の中性脂肪濃度、低密度、中密度及び超低密度コレステロールの総濃度を低下させる用途:
中性脂肪や、低密度、中密度及び超低密度コレステロールは、高血圧や動脈硬化を引き起こす素因となることから、これらの脂質成分の血中濃度が高い対象者にとって脂質代謝の改善作用を有すると考えられる。
(3)内臓脂肪の蓄積を減少させる用途:
後述する実施例に示すように、本発明の脂質代謝改善剤は、膵リパーゼ活性を阻害することにより、消化管からの脂肪の吸収を抑制するとともに、肝臓に蓄積する脂質量を低下させる働きがある。内臓脂肪の蓄積は種々の慢性疾患の素因となるから、このような対象者にとって脂質代謝の改善作用を有すると考えられる。
【0024】
(4)脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症を予防又は治療する用途:
生体内の脂肪細胞は、エネルギーを備蓄する働きだけでなく、さまざまな生理活性物質(アディポサイトカイン)を分泌する細胞であることが分かっている。アディポサイトカインにはさまざまな種類が存在する。インスリンの働きを阻害して糖尿病を引き起こす腫瘍壊死因子(TNF−α)をはじめ、高血圧と関連するアンジオテンシノーゲン、血栓の形成に関係し心筋梗塞や脳卒中の原因となるプラスミノーゲン活性化抑制因子(PAI―1)などで、脂肪細胞から大量に分泌されて動脈硬化などの発症に強く関連している。これらのいわゆる悪玉アディポサイトカインは内臓脂肪の増加によってさらにその合成・分泌量が増えるという性質がある。そのため内臓脂肪が蓄積するに従い高血圧や糖尿病、高脂血症が進展し、脳卒中や心疾患を発症させやすくなる。したがって、本発明において、脂質代謝の異常とは、肥満の原因となる脂肪細胞の肥大化や過形成、内臓脂肪の蓄積、及び脂肪細胞からのアディポサイトカインの分泌異常などの状態を含み、合併症とは、脂質代謝の異常に伴って発症する高血圧や糖尿病、高脂血症などをいうがこれらに限定されない。
【0025】
正常な、肥満していない、小型の脂肪細胞からはアディポネクチンなどの善玉アディポサイトカインが活発に分泌されて、悪玉アディポサイトカインはほとんど分泌されない。逆に、肥満して肥大化した脂肪細胞からは善玉アディポサイトカインは出なくなり、悪玉アディポサイトカインの分泌が活発になることが分かっている。従って、本発明の脂質代謝改善剤は、脂質代謝異常の原因である悪玉アディポサイトカインの分泌を抑制し、これによって脂肪細胞の肥満を抑制するから、ヒト脂肪細胞からのアディポサイトカインの分泌調節剤、又はヒト脂肪細胞の肥大化抑制剤として用いることができる。
【0026】
「脂質代謝改善剤の有効量」という用語は、ある個人の脂質代謝の状態を改善するのに必要な量を意味する。用量は、それぞれの脂質代謝の状態における個々の要求に適用させることができる。用量は、改善すべき脂質代謝の重篤度、対象者の年齢及び全般的な健康状態、投与経路及び剤形、並びに医師の経験のような多数の要因に応じて広い範囲内で変化させることができる。本発明の脂質代謝改善剤の有効成分である小豆煮汁抽出物は、成人1人当たり0.5〜100mg/kg体重(好ましくは1〜50mg/kg体重)、非経口的に投与する場合は0.05〜50mg/kg体重(好ましくは0.5〜50mg/kg体重)の範囲で一日1〜3回に分けて投与することができる。
【0027】
[食品及び健康食品としての用途]
本発明の脂質代謝改善剤は、飲食品に配合し、脂質代謝改善機能を有する食品として用いることができる。このためには、その有効成分である小豆煮汁抽出物の有効量を飲食品の製造原料段階、製造の中間工程段階又は最終製品の段階で添加、配合する。ここで、「小豆煮汁抽出物の有効量」とは、個々の飲食品において通常喫食される量を摂取した場合に、上述したような範囲で有効成分が摂取されるような含有量をいう。より具体的には、本発明による食品は、上述した小豆煮汁抽出物をそのまま飲食品として調製したもの、各種タンパク質、糖類、脂肪、微量元素、ビタミン類等を更に配合したもの、液状、半液体状若しくは固体状にしたもの、一般の飲食品へ添加したものであってもよい。
【0028】
本発明において「食品」とは、健康食品、機能性食品、及び特定保健用食品を含む意味で用いられる。また「食品」の形態は特に限定されるものではなく、例えば、飲料の形態であってもよい。本発明の健康食品は、好ましくは単位用量剤形である。単位用量剤形とは、有効成分の適切な1回投与量に分割された製剤をいう。この単位用量剤形は、包装された調剤であってよく、錠剤、カプセル剤、散剤及び顆粒剤それ自体でも、あるいは適切な数のそれらのいずれかが包装された形であってもよい。1つの実施形態において、本発明の健康食品、機能性食品、特定保健用食品は、脂質代謝を改善する必要のある対象者のために用いられることが好ましい。このような対象者を特定するためには、食品の包装や添付文書にその旨を記載することができる。
【0029】
その他の飲食品として具体的には、ジュース類、清涼飲料水、茶類、乳酸菌飲料、発酵乳、冷菓、乳製品(バター、チーズ、ヨーグルト、加工乳、脱脂乳等)、畜肉製品(ハム、ソーセージ、ハンバーグ等)、魚肉練り製品(蒲鉾、竹輪、さつま揚げ等)、卵製品(だし巻き、卵豆腐等)、菓子類(クッキー、ゼリー、スナック菓子)、パン類、麺類、漬物類、燻製品、干物、佃煮、塩蔵品、スープ類、調味料などを例示することができるが、これらに制限されない。1つの実施形態において、本発明の脂質代謝改善剤は、脂質含有食品に添加されることが好ましく、当該食品を摂取した者にとって食品中の脂質の吸収及び/又は代謝を抑制して肥満や成人病を予防することができる。
【0030】
本発明に係る健康食品及び食品は、ヒトが飲食品として長年摂取してきた小豆抽出成分であることから、毒性も低く、哺乳動物に対し安全に用いられる。食品として摂取する場合には、成人1人1日当たり30〜6000mgの範囲、好ましくは60〜3000mgの範囲の摂取量となるよう本発明による有効成分を食品に配合することができる。
【実施例】
【0031】
以下に本発明を、実施例によりさらに詳細に説明するが、本発明は実施例に限定されるものではなく、種々の変更例が可能である。
【0032】
製造例1:小豆煮汁抽出物の製造
出発原料として用いる小豆煮汁は、製餡工場における小豆の渋切工程で回収される小豆煮汁を用いた。不溶性物質を除去した後、pHを3.8〜4に調整した小豆煮汁に、あらかじめ所定量を水に溶かして調製したペクチナーゼHL(ヤクルト薬品工業製)を0.005〜0.001重量%となるように添加し、50℃で4〜5時間攪拌しながら酵素反応を行った。その後、静置して小豆煮汁に含まれている未分解のデンプン質、繊維質、タンパク質、脂質などの成分を沈殿させ、ろ過による上澄み液を取り出した。この上澄み液を限外ろ過膜装置により濃縮した後に、苛性ソーダ(水酸化ナトリウム)を加えて上澄み液のpHを8〜9に調整した。50メッシュのストレーナーで異物を除去した後、超高温殺菌装置で120℃、20秒間の殺菌(UHT)処理を行った。殺菌した濃縮液のうち、粉末製品用の400Lをスプレードライヤーに供給し、180℃の熱風により乾燥させて、40kgの粉末状製品(小豆煮汁抽出物1(通気加熱ナシ))を得た。また、液状製品用としては、同様に製造した濃縮発色液400Lをレトルト用パックに100〜150mlずつ入れ、シールした後、レトルト装置で115℃90分間殺菌して約400kgの液状製品を製造した。
【0033】
一方、通気加熱した小豆煮汁抽出物2を製造するために、上述した限外ろ過膜濃縮後、pHを8〜9に調製した濃縮液を、噴霧装置を付けたタンクに投入し、タンクの底部から上部のスプレー口に濃縮液を送り込んで噴霧循環させ、90〜100℃に維持しつつ3〜5時間噴霧して濃縮液に空気を送り込んだ後、タンクの壁に冷却水を循環させ、約20℃まで冷却した。この濃縮液を2つに分け、上記と同様の方法により噴霧乾燥した粉末状製品(小豆煮汁抽出物2、(通気加熱アリ)と、液状製品を得た。上記製造方法により得られた小豆煮汁抽出物粉末の組成を以下の表1に、またそのミネラル成分の組成を表2に示す。なお、これらの分析方法は、日本食品標準成分分析マニュアルに記載の方法に基づく。例えば、ポリフェノールの分析は、Foline-Denis法、ミネラル成分中のリンは、バナドモリブデン酸吸光光度法、リン以外のミネラル成分は原子吸光光度計法を用いた。
【0034】
【表1】

【0035】
【表2】

【0036】
実施例1:動物実験
[実験動物及び飼育条件]
実験動物は8週齢のFischer系雄ラット20匹を日本チャールズ・リバー株式会社から購入した。飼育条件は23±1℃、湿度60±5%とし、明暗周期12時間(明07:00/暗19:00)とした。ラットはプラスチックケースを用いて1個体ずつ飼育した。ラットの取り扱いは、Guide of the Care and Use of Laboratory Animalsに従って行った。
【0037】
[実験食]
標準食にはAIN93G(オリエンタル酵母株式会社製)を使用し、その群を標準食群(C)とした。そして標準食に表1で示した小豆煮汁抽出物2(通気加熱アリ)を1%添加したものを小豆煮汁抽出物投与群(A)とした。また、AIN93G(オリエンタル酵母株式会社製)にラード15%を添加したものを高脂肪食対照群(CF)、高脂肪食対照群に1%の小豆煮汁抽出物2(通気加熱アリ)を添加したものを小豆煮汁抽出部添加高脂肪食対照群(AF)とした。これら実験食の組成を表3に示した。
【0038】
【表3】

【0039】
[投与実験]
8週齢雄ラット20匹に市販のラット用粉末飼料を与えた1週間の予備飼育後、各投与群で体重に有意差が出ないように3つの投与群に各群5匹ずつ群分けを行った。投与期間は4週間とし、1匹のラットに1日あたり25gの実験食を投与、食餌と水は自由摂取とした。1週毎に体重・摂食量の計測を行った。摂食量は給与量と残量の差から算出した。また毎週、頸静脈から採血を行った。採血は一晩絶食させた後、空腹時に行い、得られた血液はエッペンチューブに入れて2時間室温放置後、15分間7000rpmで遠心分離し、血清画分を分画し、分析まで−30℃で保存した。また、投与期間最後の3日間の糞を採取し、分析まで−30℃で保存した。投与期間終了後、ラットにネンブタール麻酔をかけ解剖、心臓採血、肝臓の摘出を行った。摘出した肝臓は冷生理食塩水(9gNaCl/L)で洗浄し、乾燥したろ紙で水分を除去してから重量測定後、液体窒素で冷凍し、−80℃で保存した。
【0040】
[血清の生化学的成分の分析]
総コレステロール、高密度アポリポタンパク質コレステロール(HDLコレステロール)、中性脂肪、遊離脂肪酸の4項目の測定は酵素法により行った。総コレステロール濃度と高密度アポリポタンパク質コレステロール濃度の差を超低密度アポリポタンパク質コレステロール+中密度アポリポタンパク質コレステロール+低密度アポリポタンパク質コレステロール(VLDL+IDL+LDLコレステロール)濃度とした。その結果を図2及び3に示した。なお、以下に示すそれぞれのデータは平均値±標準偏差で表わした。データ間の有意差検定はt−検定を行い、p<0.05を有意とした。
【0041】
図2に示したように、血清中の総コレステロール量は、3週目から4週目において標準食群(C)と、小豆煮汁抽出物投与群(A)とで有意な差が認められ、高脂肪食群においても小豆煮汁抽出物の添加により低下する傾向が見られた。一方、図3に示したように、血清中性脂肪(TG)については、標準食群において、小豆煮汁抽出物を添加した方が有意に低下しており、高脂肪食群においても低下する傾向がみられた。
【0042】
[糞中の全脂質量の測定]
約0.5gの糞をネジ付試験管(φ15)に量り取り、凍結乾燥機(東京理科機器社製FDU−830型)により凍結乾燥させた。これに4%酢酸を加えたクロロホルム−メタノール混合液(2:1,v/v;C−M)を2ml加え、超音波発生装置(ブランソン社製5510J−MT型)で10分間処理して脂溶性物質の抽出を行い、冷却多本架遠心機(コクサン社製80R型、4℃)を用い10分間2000rpmで遠心分離することによりC−M層と残渣に分離し、上層であるC−M層を別のネジ付試験管(φ18)に移した。この残渣に同様の操作を2回繰り返し、得られたC−M層に1.5mlの1%塩化バリウム溶液を加え、試験管ミキサー(IWAKI社製251型)で撹拌した後、10分間2000rpmで遠心分離することで、クロロホルム層と水層に分離した。上層である水層を除去し、残ったクロロホルム層にメタノールを適当量加えロータリーエバポレーター(SHIBATA社製RE111型)で減圧濃縮し、さらにC−M(2:1)を加え減圧濃縮することで全脂質を得て重量を測定した。これにC−M(2:1)を1ml加え−30℃で保管した。その結果を図4に示した。
【0043】
図4に示したように、ラット糞中の脂質排出量は、高脂肪食の両方の群において、小豆煮汁抽出物を添加した方が有意に多いことが分かった。
【0044】
[肝臓中総脂質の定量]
上記の方法と同様に肝臓中の全脂質を抽出し、肝臓中の総脂質量を測定した。その結果を図5に示した。肝臓中の脂質量は、高脂肪食群において有意な差が認められ、小豆煮汁抽出物の添加により脂肪の蓄積が抑制されると考えられる。
【0045】
[膵リパーゼ活性抑制試験]
基質液の作成
Hanらの方法に従って、トリオレイン240mg、レシチン30mg、胆汁酸15mg、0,1Mトリス塩酸緩衝液で溶解し、超音波発生装置で10分間処理したものを基質液とした。
膵リパーゼ
基質液0.2mlを、シンフレックス用マルチブロック付き恒温槽を用いて400rpmで30℃になるまで温め、その後ブタ由来膵リパーゼ(50μg/ml)0.1ml、及び検体液(50μg/ml)0.2mlを加え、700rpm 37℃で反応させた。今回は(1)反応時間を30分に保ち、用いた小豆煮汁抽出物の濃度を変えた場合、(2)濃度を一定に保ち、反応時間を変えた場合との2種類の実験行った。
遊離オレイン酸量の測定
遊離したオレイン酸量は、NEFA−HAテストワコー(和光純薬工業株式会社)を用いて測定した。
(1)では活性値は検体無添加の値を100%とし、(2)では遊離脂肪酸基準液を用いて濃度を算出することによって、活性値を算出した。
【0046】
図6に示したように、小豆煮汁抽出物の用量依存的にリパーゼ活性が低下し、50%阻害を示す濃度は12.5μg/mlであった。経時的に測定した遊離オレイン酸濃度も小豆煮汁抽出物の添加により生成が抑制されることが分かる。
【0047】
[血清レジスチン濃度の測定]
表4に示したキットを用い、後述する実施例2に記載した方法に従って、4週間経過後のラット血清中のレジスチン濃度を測定した結果を図7に示した。標準食及び高脂肪食のいずれの群においても血清レジスチン濃度の低下傾向が見られ、高脂肪食群では有意に低下していることが分かった。なお、レジスチンは肥大した脂肪細胞で産生され、骨格筋や肝臓でインスリン伝達を傷害し、インスリン抵抗性を誘導すると考えられている。
【0048】
実施例2:ヒト脂肪細胞を用いた実験
[使用細胞、試薬]
ヒト内臓前駆脂肪細胞はプライマリーセル株式会社より購入した。培養に使用した24ウェルプラスチックプレートは旭硝子株式会社より購入した。通常培地の内臓脂肪分化メディウム Ver.2、0.01%コラーゲン、HBSS(−)バッファーはプライマリーセル株式会社より、増殖促進培地に添加したFibroblast Growth Factor(basic)は和光純薬工業(株)より購入した。分化促進培地に添加したDexamethazone、TroglitazoneはSIGMA-ALDRICH Japan Lidより、Isobutyl-1-methylxanthine、試薬調製のためのジメチルスルホキシドは和光純薬工業株式会社より購入した。
【0049】
[細胞培養]
実験材料としてプライマリーセルより購入したヒト内臓脂肪細胞Human Preadipocyte (3.5×105 cell)(ScienCell Research Laboratoties )の3継代の細胞を用いて、培養には24ウエルプレートを使用した。増殖培地は終濃度10ng/mlとなるように FGF(Fibroblast Growth Factor(basic)を添加した内蔵脂肪分化メディウムVer.2を使用。分化誘導培地にはそれぞれ終濃度1μM Dexamethazone、0.05mM IBMX、10μM Troglitazoneを添加した内蔵脂肪分化メディウムVer.2を使用した。
【0050】
培養方法は、まず、24ウェルプレートに500μlずつ0.01%コラーゲンを添加し、ウェル全体にコラーゲンをコーティングした後、余分なコラーゲンを吸引し、HBSS(−)バッファーで2度洗浄した。他方、25mlの増殖培地に1mlの前駆内臓脂肪細胞を混合しておいた。これを1mlずつコラーゲンコートされたプレートのウェルに細胞を播種してった。定法に従い室温37℃、湿度95%、CO2 5%条件でヒト内臓脂肪細胞を増殖培地で3日間培養した。コンフルエントになったところで分化誘導培地に交換した。4日間この分化誘導培地で分化させた後、通常培地の内蔵脂肪分化メディウムVer.2へ交換、その3日後に250〜750μg/mlの小豆煮汁抽出物1(通気加熱ナシ)又は小豆煮汁抽出物2(通気加熱アリ)を添加した。培養計14日後に細胞を回収しトリグリセライド量、GPDH活性、それらを補正するためのDNA量をそれぞれ測定した。また、14日目の培地を回収し、遠心分離により沈殿物を取り除いた上澄み液を用い、イライザ法によりアディポサイトカインの発現量を測定した。また、回収した細胞からトータルRNAを抽出し、cDNAを合成した。
【0051】
[分析方法]
TG測定はトリグリセライドE−テストワコー(和光純薬工業株式会社:Lot No.KJ677)GPDH活性測定(GPDH Assay Kit, Code No.AK01 プライマリーセル株式会社Lot. ILU)DNA量の定量は超微量分光光度計 ナノドロップ NanoDrop ND−2000 (Thermo Fisher Scientific社)を使用した。なお、以下の測定データにおいて、それぞれのデータは平均値±標準誤差(S.E.)で表した。データ間の有意差検定は、一元分散分析の後Turkey-Kramer testで事後比較を行った。P<0.05を有意とした。
【0052】
[TG蓄積量の測定]
脂肪細胞のトリグリセライドの定量はトリグリセライドE−テストワコー(和光純薬工業株式会社)を使用し、添付の使用説明書の方法に従って定量を行った。すなわち、試薬は発色剤1瓶を緩衝液1瓶で溶解しておいた。検体は14日間培養後の細胞プレートを500μlのPBSバッファーで全てのウェルを2回洗浄した後、0.4μlのPBSバッファーを加え、超音波処理機で細胞を磨砕したものを使用した。各濃度のサンプルとスタンダードを150μlに発色試薬3mlを加えよく混合しウォーターバスで37℃、5分間保温し、600nmで吸光度を測定した。計算法は以下の通りである。
トリグリセライド濃度(mg/dl)=検体吸光度/スタンダード吸光度×300
この値をDNA量で補正したものをTG蓄積量とした。
【0053】
その結果を図8に示した。通気加熱アリ/ナシともに、用量依存的に脂肪細胞内のTG蓄積量を減少させることが分かった。
【0054】
[GPDH活性測定]
GPDH活性の測定はGPDH Assay Kit (プライマリーセル株式会社)を使用し、添付の使用説明書の方法に従って定量を行った。すなわち、反応基質溶液は、反応基質のバイアル1本に対し精製水4.2mlで溶解した。酵素抽出溶液は酵素抽出試薬を精製水200mlで溶解した。検体は14日間培養後の細胞プレートを500μlのPBSバッファーで全てのウェルを2回洗浄した後、酵素抽出溶液を1ウェルあたり700μlを加えた。このプレートを超音波処理機を用いて細胞を磨砕した溶液を回収し、冷却遠心分離(4℃、12800g、5分間)で分離した上清を検体として使用した。測定方法は、反応基質溶液80μlを96マイクロプレートに加え25℃に5分間加温した。また検体も25℃で保温した。その後、マイクロプレート内に検体40μlを加え、よく攪拌した後、波長340nmにおける吸光度減少率を経時測定し、1分間あたりの吸光度の変化量(ΔO.D.)を10分間求めた。計算方法は以下の通り。
光路長(cm)=反応総量/プレートのウェル底面積=0.12/0.25=0.48
GPDH活性(U/ml)
=(ΔO.D./NADHのミリモル分子吸光係数)×(反応総量ml/検体量ml)
×(検体希釈率/光路長cm)
=(ΔO.D./6.22)×(0.12/0.04)×(5/0.48)
この値をDNA量で補正したものをGPDH活性値とした。
【0055】
その結果を図9に示した。ジヒドロキシアセトンリン酸からTGの合成に必要なグリセロール3リン酸を生成する酵素であるGPDH活性も、本発明の脂質代謝改善剤の添加により有意に減少していることが明らかとなった。このことから、本発明の脂質代謝改善剤は、脂肪細胞の成熟段階におけるGPDH活性の抑制及びそれによるTGの蓄積抑制効果があることが示された。
【0056】
[アディポサイトカインの定量]
アディポサイトカインはELISA法を用いて定量を行った。検体は培養14日目の培地を回収し、14000rpmで5分間遠心分離し、分離した上清を−80℃で保存したものを使用した。使用したELISAキットは、表4の通りであり、各キットに添付されている使用説明書の方法に従って定量を行った。すなわち、ヒトアディポネクチンELISAキット(大塚製薬株式会社)の方法であれば、まず検体前処理液を蒸留水で5倍希釈した後、献体である培養上清10μlを希釈した見地前処理液90μlと混和し、ヒートブロックを用いて100℃で5分間加熱した。これに献体希釈液を900μl加え混和し、100倍希釈検体とした。
【0057】
【表4】

【0058】
希釈した洗浄液を抗体プレートの各ウェルに約350μlずつ加えた後、ウェルの液を完全に除去した。各濃度の標準液及び前処理済みの抗体を各ウェルに100μlずつ加え、室温で1時間静置反応させた。ウェルの液を完全に除去し、洗浄液を各ウェルに300μlずつ加え、再度速やかに吸引除去した。この洗浄と吸引の操作をさらに2回繰り返した後、ウェルに残った洗浄液を除去した。第一抗体液を抗体プレートの各ウェルに100μlずつ加え室温で1時間静置反応させた。再びウェルの液を完全に除去し、洗浄液を各ウェルに300μlずつ加え、再度速やかに吸引除去した。この洗浄と吸引の操作をさらに2回繰り返した後、ウェルに残った洗浄液を除去した。抗体標識抗体液を抗体プレートの各ウェルに100μlずつ加え、室温で1時間静置反応させた。再びウェルの液を完全に除去し、洗浄液を各ウェルに300μlずつ加え、再度速やかに吸引除去した。この洗浄と吸引の操作をさらに2回繰り返した後、ウェルに残った洗浄液を除去した。基質液を抗体プレートの各ウェルに100μlずつ加え、室温で15分間静置反応させた後、反応停止液を抗体プレートの各ウェルに100μlずつ加えた。プレートリーダーで各ウェルの450nmと対照波長の650nmの吸高度を測定した。
【0059】
以上の測定結果を図10〜図12に示した。脂質代謝系のアディポサイトカインであるレプチンやレジスチンのみならず。炎症性サイトカインであるIL−6や血液凝固系サイトカインであるPAI−1、血管内皮の炎症を引き起こすMCP−1の分泌も抑制することが分かった。したがって、本発明の脂質代謝改善剤は、肥大化した脂肪細胞から分泌されるサイトカインによって誘導される生体内における炎症状態又は炎症性疾患に対して有効であると考えられる。
【0060】
試作例1:ソーセージの製造
牛肉(赤身)525gをミンチ状とした後、豚脂225g及び氷水250gと均一に混練した。これに、食塩15g、脱脂粉乳20g、カラーミン10Nを1g、ウィンナーWを5g、砂糖5g、ブラックペッパー3g、ホワイトペッパー3g、コリアンダー1.5g、オールスパイス1g、ベイローレル0.5g、ナツメグ0.5g及び小豆煮汁抽出物2(粉末)3gを添加し、カッターキュアリングを行った。この原料肉を定法に従ってケーシング(腸詰)、スモーク(乾燥・燻煙)した後、製品の種類に応じて、湯煮または蒸煮により加熱処理を行い冷却後に包装した。
【0061】
試作例2:ハンバーグの製造
合い挽肉400gをミンチ状にし、たまねぎ(小)1個、サラダ油少々、食パン1枚、牛乳大さじ3杯、卵(小)1個、塩少々、こしょう少々、ナツメグ少々及び小豆煮汁抽出物2(粉末)を全量に対して1%となるように添加した。これらの原料をミキサーにかけてよく混合した後、成型、製品の種類に応じて加熱し、包装して冷凍した。
【0062】
試作例3:ジャーキーの製造
牛肉(赤身)1kgを整形し、これにたまねぎ(小)1個、にんにく3かけ、しょうゆ1カップ、日本酒0.5カップ、みりん0.5カップ、砂糖30g、塩30g、唐辛子少々、荒挽きこしょう少々及び小豆煮汁抽出物1(粉末)2gを添加して塩漬けした。これをスライス、乾燥、場合により熟成した後、製品として包装した。
【0063】
試作例4:天ぷら衣の製造
小麦粉10g、溶き卵1/2個分及び水大さじ1.5杯を混合し、その全量に対して小豆煮汁抽出物1(粉末)を1%添加混合して作成した。
【特許請求の範囲】
【請求項1】
小豆煮汁を、デンプン質、タンパク質、又はペクチン質を分解する少なくとも1種の酵素で処理し、当該処理後の上澄み液を濃縮することにより得られる、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分として含む脂質代謝改善剤。
【請求項2】
小豆煮汁抽出物が、前記上澄み液の濃縮物をさらに通気加熱したものである請求項1に記載の脂質代謝改善剤。
【請求項3】
前記ポリフェノールの含有量が、小豆煮汁抽出物に対する固形分換算で少なくとも15重量%である請求項1又は2に記載の脂質代謝改善剤。
【請求項4】
食事中の脂質吸収を抑制するための、請求項1〜3のいずれか1項に記載の脂質代謝改善剤。
【請求項5】
血清中の中性脂肪濃度;低密度、中密度及び超低密度コレステロールの総濃度;並びに内臓脂肪の蓄積量からなる群から選択される1つ以上を減少させるための請求項1〜4のいずれか1項に記載の脂質代謝改善剤。
【請求項6】
脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症の発症を予防又は治療するための請求項1〜5のいずれか1項に記載の脂質代謝改善剤。
【請求項7】
請求項1〜6のいずれか1項に記載の脂質代謝改善剤の有効量を含み、脂質代謝改善機能を有する食品。
【請求項8】
請求項1〜6のいずれか1項に記載の脂質代謝改善剤の有効量を含み、脂質代謝を改善する必要のある対象者のための健康食品、機能性食品、又は特定保健用食品。
【請求項9】
脂質含有食品に、請求項1〜6のいずれか1項に記載の脂質代謝改善剤の有効量を添加してなる、当該食品中の脂質の吸収及び/又は代謝を抑制するための食品。
【請求項1】
小豆煮汁を、デンプン質、タンパク質、又はペクチン質を分解する少なくとも1種の酵素で処理し、当該処理後の上澄み液を濃縮することにより得られる、ポリフェノール、ミネラル及び食物繊維を含む小豆煮汁抽出物を有効成分として含む脂質代謝改善剤。
【請求項2】
小豆煮汁抽出物が、前記上澄み液の濃縮物をさらに通気加熱したものである請求項1に記載の脂質代謝改善剤。
【請求項3】
前記ポリフェノールの含有量が、小豆煮汁抽出物に対する固形分換算で少なくとも15重量%である請求項1又は2に記載の脂質代謝改善剤。
【請求項4】
食事中の脂質吸収を抑制するための、請求項1〜3のいずれか1項に記載の脂質代謝改善剤。
【請求項5】
血清中の中性脂肪濃度;低密度、中密度及び超低密度コレステロールの総濃度;並びに内臓脂肪の蓄積量からなる群から選択される1つ以上を減少させるための請求項1〜4のいずれか1項に記載の脂質代謝改善剤。
【請求項6】
脂質代謝の異常を有し、糖尿病、動脈硬化及び炎症性疾患を含む合併症の発症が予想される対象者の、当該合併症の発症を予防又は治療するための請求項1〜5のいずれか1項に記載の脂質代謝改善剤。
【請求項7】
請求項1〜6のいずれか1項に記載の脂質代謝改善剤の有効量を含み、脂質代謝改善機能を有する食品。
【請求項8】
請求項1〜6のいずれか1項に記載の脂質代謝改善剤の有効量を含み、脂質代謝を改善する必要のある対象者のための健康食品、機能性食品、又は特定保健用食品。
【請求項9】
脂質含有食品に、請求項1〜6のいずれか1項に記載の脂質代謝改善剤の有効量を添加してなる、当該食品中の脂質の吸収及び/又は代謝を抑制するための食品。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2012−224601(P2012−224601A)
【公開日】平成24年11月15日(2012.11.15)
【国際特許分類】
【出願番号】特願2011−95946(P2011−95946)
【出願日】平成23年4月22日(2011.4.22)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成22年10月24日 日本栄養・食糧学会北海道支部発行の「第40回 日本栄養・食糧学会北海道支部会 講演要旨集 2010」に発表 平成22年11月21日 第15回日本食物繊維学会学術集会 学術集会長 原 博 発行の「第15回日本食物繊維学会学術集会講演要旨集」に発表
【出願人】(393017535)コスモ食品株式会社 (18)
【出願人】(596075417)財団法人十勝圏振興機構 (20)
【Fターム(参考)】
【公開日】平成24年11月15日(2012.11.15)
【国際特許分類】
【出願日】平成23年4月22日(2011.4.22)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成22年10月24日 日本栄養・食糧学会北海道支部発行の「第40回 日本栄養・食糧学会北海道支部会 講演要旨集 2010」に発表 平成22年11月21日 第15回日本食物繊維学会学術集会 学術集会長 原 博 発行の「第15回日本食物繊維学会学術集会講演要旨集」に発表
【出願人】(393017535)コスモ食品株式会社 (18)
【出願人】(596075417)財団法人十勝圏振興機構 (20)
【Fターム(参考)】
[ Back to top ]

