少数のヌクレイン酸鎖を直接証明する方法
【課題】 ヌクレイン酸鎖を迅速かつ確実に直接証明することのできる方法を提供する。
【解決手段】 調査溶液内で所定の対象配列(10)の少数の、好ましくは個々のヌクレイン酸鎖を直接証明する方法が、次のステップ、すなわち、証明すべきヌクレイン酸鎖の少なくともいくつかを、多数の色素分子(16)でマークされ、かつ対象配列(10)全体またはほぼ全体に対して相補的であるそれぞれ長いアンチセンス鎖(17)でハイブリッド化するステップと、アンチセンス鎖(17)がハイブリッド化されている、証明すべきヌクレイン酸鎖の少数、好ましくは1つを判別するように構成されている光学分析用の装置(20)によって対象配列(10)を同定するステップを有する。
【解決手段】 調査溶液内で所定の対象配列(10)の少数の、好ましくは個々のヌクレイン酸鎖を直接証明する方法が、次のステップ、すなわち、証明すべきヌクレイン酸鎖の少なくともいくつかを、多数の色素分子(16)でマークされ、かつ対象配列(10)全体またはほぼ全体に対して相補的であるそれぞれ長いアンチセンス鎖(17)でハイブリッド化するステップと、アンチセンス鎖(17)がハイブリッド化されている、証明すべきヌクレイン酸鎖の少数、好ましくは1つを判別するように構成されている光学分析用の装置(20)によって対象配列(10)を同定するステップを有する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、調査溶液内で所定の対象配列の少数の、好ましくは個別のヌクレイン酸の鎖を直接検出する方法に関するものである。
【0002】
本発明はさらに、この方法を実施する装置並びにその際に使用される試験溶液に関するものである。
【背景技術】
【0003】
一般に、既知の、部分的に既知の、かつ/または未知の配列のDNA/RNA分子を証明できることが望まれている。それに関する用途例は、例えば発生進化的バイオテクノロジーの枠内での遺伝学上の調査、実験室実験の分析、あるいは特にウィスル診断学である。これらすべての用途例において最初から存在する調査溶液内に多くは所定の対象配列の少数のまたは全く個別のヌクレイン酸の鎖があって、それが調査溶液内で好ましくは定量的に検出される。
【0004】
現在ではウィルス感染の証明は間接的な方法、すなわち取り付かれた宿主の免疫反応を介して行われる。テストは、これら間接的な方法に付随する一連の困難と結び付いている。それに数えられるのは遅延された免疫反応の長い潜伏期間、例えばエリザ・テストの時間のかかる分析、並びに偽陽性ないし偽陰性の免疫反応の可能性である。
【0005】
従ってウィルスを極めて専門的に証明することのできる直接試験を行うことが望まれている。この直接証明の困難性は特に、大きな感度が要求されることにある。すなわち、ボーダーラインのケースにおいては、細胞抽出物内ないしは血清内で唯一のウィルス粒子を証明することができなくてはならない。その場合に証明すべきヌクレイン酸の鎖の濃度は10マイナス12乗から10マイナス18乗分子濃度の範囲にある。
【0006】
数年前に開発された方法は、個別のあるいは少数のヌクレイン酸の鎖を、例えばゲル電気泳動などの従来の方法、温度勾配ゲル、配列決定の方法、例えばサンガー(Sanger)方法またはマクサム・ギルバート法に従って接近し得る濃度水準まで高濃縮することにある。この高濃縮には、ポリメラーゼ連鎖反応法(PCR)または証明すべきヌクレイン酸部分の固有の複製に基づく同様な方法が使用される。その場合に、短い1本鎖領域がプライマーとして供給される場合に、1本鎖を2本鎖に重合化するDNAポリメラーゼの特性が利用される。その場合に増強すべき配列を有するヌクレイン酸の鎖に、増強すべき配列の端縁領域に基づく鎖固有の、すなわち両DNA鎖の一方に対して相補的な2つの化学的に合成されたオリゴヌクレオチドが過剰に加えられる。
【0007】
まず、この種の方法は非常に時間がかかり、この方法はPCR反応を実施することが必要であるだけでなく、その後他の分析を行って、調査溶液中に求める配列が存在することを少なくとも定性的に結論づけられるようにしなければならない。さらにここでは、求める配列の対応する部分に対して正確に相補的な、約15−20ヌクレオチドの長さを有する所定の短い鎖のヌクレイン酸配列が用意されることが必要である。この種の正確に相補的な短い鎖のヌクレイン酸部分を一般に「アンチセンス配列(Antisense−Sequenz)」または「プライマー」とも称する。
【0008】
時間がかかる他に、この方法においてはさらに、両端部において配列順序の少なくとも1つの短い部分がわかっており、それによって対応するプライマーを用意できるヌクレイン酸配列しか証明できないという欠点がある。証明すべきヌクレイン酸の鎖がRNA分子である場合には、これをまずさらにRNA依存性のDNAポリメラーゼを用いてDNAコピーに書き換えてから、PCR技術を使用することが可能になる。
【0009】
場合によっては異なる処理ステップが多数あるので、この方法は多数の誤りの原因を有する。というのは個々のポリメラーゼは重合化の際にある確率でしか「正しい」相補的なヌクレオチドを組み込めないので、ここでも偽陽性と偽陰性のテスト結果がもたらされることを排除できない。
【0010】
他の方法は、求める配列を直接視認できるようにすることであって、このことは当然のことながらまずその配列が他の配列から明らかに区別できなくてはならないことを意味している。個々の分子を同定して計数する新しく開発された方法が、WO94/16313に記載されている相関蛍光分光法であって、以下においてはFCSと略称する。上述の公報には、測定体積内で証明すべき分子が他の分子から明白に区別されるかあるいは分離されて存在している限りにおいて、FCSを用いて0.1から10flの範囲の極めて少量の測定体積内で色素でマーキングされた個々のDNA/RNA分子を証明できることが記載されている。
【0011】
すでに述べたPCR法においては2つのプライマー配列が必要であって、その一方はプラス鎖の鎖始端に対して相補的であって、他方はマイナス鎖の始端に対して相補的である。両プライマー配列の位置間の配列部分がその後濃縮される。それに対してPCS証明の場合には蛍光色素でマーキングされた1つの固有のプライマー配列しか必要とされない。そのプライマー配列が検出すべき(1本鎖の)RNA配列または完全に溶融されたDNA配列の鎖に直接付加される。この形においてマークされたプライマーはその電荷特性においてもその移動度においても結合されていないプライマーから明白に区別され、それ以上濃縮しないでもFCS法によって直接検出することができる。
【0012】
FCSの測定原理は、溶液の比較的少量の体積要素がレーザの強い励起光にさらされることによって、極めて薄い溶液内の蛍光団分子が測定されることに基づいている。この測定体積内に存在する、分子に対応する励起スペクトルがレーザによって励起される。この体積要素から放出される蛍光がその後光電子増倍管上に結像される。希釈された溶液である場合には、それぞれの体積要素内の分子の濃度が明らかに変動する。
【0013】
一度体積要素内に拡散された分子は、固有の拡散速度に従って、該当する分子の固有の平均時間経つと再び体積要素から分離して、その後はもはや観察されない。
【0014】
同一の一つの分子のルミネッセンスがその分子が測定体積内に滞留する平均的な滞留時間の間に多数回励起される場合には、この分子から多数の信号が検出される。従って希釈された溶液の場合には、一度測定体積内に拡散された分子が再び出て行く前に再度励起される確率は、新しく入ってくる分子の場合よりもずっと大きい。
【0015】
上述のWO94/16313には、この測定原理に基づいて希釈溶液内で個々の分子を検出することが可能であると記載されている。証明すべき分子がヌクレイン酸鎖である場合には、証明すべき分子の所定の部分配列に対して相補的なプライマーが付加され、その結合されない状態における拡散特性が対象分子に結合された状態から区別される。
【0016】
関与する分子の拡散速度に関係する、現在では比較的長い測定時間を短縮するために、上述の文献には、測定体積内の証明すべき分子を濃縮することのできる種々の方法が記載されている。これらの方法は原理的に、結合されないプライマーとプライマー・ヌクレイン酸鎖複合体の電荷の違いを利用して、整流された電場において結合されないプライマーを複合体から分離し、あるいは異なる拡散速度を利用することに基づいている。
【0017】
証明の特異性を向上させる他の方法は、異なるようにマークされた2つの異なるプライマーを使用することにある。異なるようにマークされたプライマーに基づく蛍光信号の時間的相関によって、電子的な信号処理の方法で非相関の、従って遊離されたプライマーの信号が効果的に抑圧される。
【0018】
さらに、例えば4Hzの低周波の交流電場によって帯電された分子が測定体積によって振動され、それによって分子がほぼ合焦されるので、測定体積内で単一の分子または少数の分子だけを定量的に検出することが可能になると記載されている。
【0019】
上述の公報はFCSの多数の使用方法を記載しているが、正確には装置と、光学系と種々の分子沈澱を扱っている。もちろん特に、FCS装置を用いてプライマーを使用して個々のDNA/RNA鎖を計数できることが記載されている。このPCT出願は物理的パラメータの測定にも大いに注目しており、そのために特に異なるようにマークされた配位子が使用されるが、しかしこれは測定信号の強度を改良するためではなく、特異性を向上させるために行われる。すなわち、例えば証明すべき分子の回転速度など他のパラメータを定めることができるようにするために、この種の異なるようにマークされたゾンデにおいてクロス相関技術が使用される。
【0020】
一般的に、関与する分子の拡散速度にドリフト速度を重畳させるために、電気泳動法、毛細管、直流電場などを使用できることが記載されている。その場合にプライマーと対象分子は、それらが異なる電荷を有し、従って電場において異なるように移動するように選択することができる。
【0021】
従ってFCS法はPCR法または類似の方法に比較して一連の利点を有する。まず、FCS法は1本鎖のヌクレイン酸分子も2本鎖のそれにも直接使用することができる。多数の病原が1本鎖のRNAウィルスであるので、これらはFCS法ではまずDNAに複製する必要はなく、そのことが分析にかかる時間の中で前向きに評価される。さらにFCS法はより直接的であり、従って個々のヌクレイン酸を証明することができ、このヌクレイン酸はPCR法の場合にはまず複製しなければならず、そのことも同様にかかる時間の差をもたらす。
【0022】
さらに濃縮プロセスがある物質によってじゃまされ、あるいは阻止されることがあるので、天然の試料についてはPCR法は必ずしも信頼できない。
【0023】
しかしPCR法とまったく同様にFCS法も特異性に関しては障害が生じ易い。すなわちプライマー配列は例えば一部において、対象配列に偶然に類似している配列に対しても相補的になる場合がある。従って、結合の際に十分な特異性を得るために、15から20ヌクレオチドの長さのプライマー配列が選択される。しかしその場合には、部分的にのみ相補的な配列の融点が作業温度以下にあって、従って測定技術的に検出されないことが保証されなければならない。
【0024】
PCR法の場合には2つのプライマー配列が使用され、その場合に2つの配列が誤結合を有する確率はわずかである。しかしその代わりにここではプライマーはずっと高い濃度で使用しなければならない。というのはプライマーが反応によって消費されるからである。
【0025】
それに対してFCS法の場合にはプライマー濃度は、証明すべきヌクレイン酸鎖への添加が測定時間内で行われる程度の高さでよい。
【0026】
これらの条件がこれらの方法の使用をわずかな絶対量に厳しく制限する。
【特許文献1】WO94/16313
【発明の開示】
【発明が解決しようとする課題】
【0027】
それに基づいて本発明の課題は、上述の欠点と困難を克服し、かつヌクレイン酸鎖を迅速かつ確実に直接証明することのできる冒頭で述べた種類の方法を提供することである。
【課題を解決するための手段】
【0028】
本発明によればこの課題は、次のステップを有する冒頭で述べた種類の方法によって解決される。すなわち、a)それぞれ対象配列の部分に対して相補的な、いわゆるアンチセンス配列を有し、かつ1つまたは多数の色素分子でマークされた種々の短いプライマーの混合物を有する試験溶液を用意し、b)この試験溶液を調査溶液と混合し、この混合された溶液を、証明すべきヌクレイン酸鎖によるプライマーのハイブリッド化を許容する周辺条件の下で温置し、その後、c)温置された溶液内で光学分析装置を用いて対象配列を同定し、この装置は1つまたは多数のプライマーがハイブリッド化されている証明すべきヌクレイン酸鎖の少数、好ましくは1つをハイブリッド化されていないプライマーを背景として判別するように構成されている。
【0029】
本発明の課題は、このようにして完全に解決される。すなわち、対象配列によって多数のプライマーをハイブリッド化することによって、付加されたプライマーを有する対象配列が測定体積内へ拡散し、それが記録される蛍光信号内で「閃光」として見られる場合に、例えばFCS技術において測定体積内でプライマーの局部的な濃度が著しく増大される。すなわち、本発明の発明者は、この種のプライマーの「カクテル」を利用できることを認識した。というのは、個々のヌクレイン酸鎖を証明する場合に、蛍光信号を増強することのみが重要となるからである。ほぼ「偶然に」プライマーが付加された配列は信号が極めてわずかであるので、公知のFCS法とは異なりもはや偽陽性表示されない。
【0030】
プライマーと対象配列間のハイブリッド化の速度定数は一般に10の6乗Mマイナス1乗Sマイナス1乗より低いので、プライマー濃度が10のマイナス9乗Mですでに反応時間千秒を越える。対象配列自体がわずかな複製でしか、例えばマイクロリットル当り1つの鎖でしか存在しない場合には、直接の証明は不可能である。というのは上述の例においては結合されていないプライマーが例えば百万倍過剰に存在することになるからである。FCS法に従って記録できるようにするためには、結合された蛍光マーカーは少なすぎて貢献できない。
【0031】
しかしこの問題は本発明によれば、対象分子の種々の部位に対して相補的なプライマー配列のカクテルを用意することによって解決される。各プライマー配列の中央に、すべて同一の等しい、あるいはまた場合によっては種々の発蛍光団からなる蛍光マークを設けることができる。このカクテルは例えば約10のマイナス9乗Mの濃度で提供され、これはフェムトリットル当り1分子を意味する。従ってレーザ光線の「光トラップ」が約0.2flの体積を有するFCS法においては、時間の約20%における蛍光マークの存在に相当する「背景ノイズ」が記録されてしまう。対象分子が光または分子トラップ内に達すると、その対象分子が蛍光の突然の「輝き」をもたらす。というのは例えば20から100の蛍光マーカーが光トラップ内に同時に存在することになるからである。平均の強度のマークされた対象分子が完全に消えて行く間、この対象分子はFCSの揺らぎ記録においてほぼ「照明弾」として現れる。
【0032】
原理的にはこの考えを腫瘍細胞に使用して、迅速な直接の腫瘍証明を可能にすることもできる。ここでは、各腫瘍細胞が抗体に関する数千の抗体決定素を有するという事実を利用することができる。抗体を色素でマークすれば、抗体が結合されている腫瘍細胞は上述のFCS法では「閃光」として証明される。ここでも色素でマークされた抗体を腫瘍細胞に付加させることによって濃縮する効果が利用される。この考えに基づく腫瘍証明は、本発明による考えの他の利用例であって、色素でマークされた多数の異なるゾンデが、これらゾンデが多数結合することのできる目標対象に対して使用される。ゾンデの濃度を低く抑えて、観察される測定体積内でそのゾンデが、目標対象に平均して結合されたゾンデの数よりずっと少ない統計的確率で浮上するようにする場合には、結合されたゾンデを有する目標対象が測定体積内に進入した場合に、測定体積内のゾンデの濃縮を測定することができる。
【0033】
またこの課題は、冒頭で述べた種類の方法において次のステップによって解決される。すなわち、1)証明すべきヌクレイン酸鎖の少なくともいくつかを、多数の色素分子でマークされ、対象配列全体またはほぼ全体に対して相補的であるそれぞれ長いアンチセンス鎖でハイブリッド化し、そして、2)対象配列を、アンチセンス鎖がハイブリッド化されている証明すべきヌクレイン酸鎖の少数、好ましくは1つを判別するように構成された光学分析装置を用いて同定する。
【0034】
このことによっても本発明の課題は完全に解決される。蛍光信号の増大は、アンチセンス鎖を非常に多数の色素分子でマークすることによって行われるので、この種の2本鎖も同様に記録された蛍光信号において「閃光」として認識される。
【0035】
証明すべきヌクレイン酸鎖とアンチセンス鎖間のハイブリッド化はまず、アンチセンス鎖が別に形成され、短いプライマーを調査溶液へ付加する方法の場合と同様に適当に温度処理することによって行うことができる。
【0036】
あるいはまた、証明すべきヌクレイン酸鎖とアンチセンス鎖からなる色素でマークされた2本鎖を、証明すべきヌクレイン酸鎖を直接重合化することによって形成することも可能であって、その場合に色素でマークされたヌクレイン酸(または類似の)構成要素が使用される。好ましくはここではマークされたUTPsが使用される。このようにして得られた、極めて多数の色素分子でマークされた2本鎖が同様にマークされた自由な構成要素を背景として証明できない場合には、マークされた2本鎖を含む溶液を例えばFCS装置へ供給する前に、前段で適当な分離処理を行わなければならず、これについては後述する。
【0037】
本発明による第1の方法の実施例においては、ステップa)で対象配列の種々の、好ましくは重なり合わない部分に対して相補的なプライマー配列が形成され、その場合に種々のプライマー配列はヌクレイン酸(または類似の)構成要素の配列順序内で互いに区別される。
【0038】
ここでは、対象配列に結合されるプライマー配列の数が非常に多いので、測定体積内でプライマー配列の高度の濃縮が行われ、それが偶然に通過する個々のプライマーによる偽陽性の測定結果に対するより大きい安全性を保証するという利点がある。
【0039】
その場合に好ましくは、ステップa)において、プライマー当り周波数長さ(配列長さ)が異なる、従ってヌクレイン酸(または類似の)構成要素の数の異なるプライマーが形成され、その場合にプライマーは10から50、好ましくは15から20構成要素の配列長さを有する。
【0040】
プライマー長さが異なることによって、証明すべきヌクレイン酸の二次構造を効果的に計算に入れることができる。その場合に鎖の短いプライマーはヌクレイン酸鎖の1本鎖で存在する領域に対して使用され、長いプライマー配列は例えばまず適当な温度を選択することによって溶融しなければならない2本鎖で存在する領域に対して使用され、その場合にプライマーはその後二次構造の形成に対抗する。構成要素が比較的多数であることによって、この場合には長い鎖のプライマーと対象配列の対応する部分との結合が非常に大きく、それによってプライマーの結合が二次構造の新たな形成に優先する。15から20構成要素を有するプライマーはまず対象配列の相補的領域と十分に特異的な結合を行い、さらに偶然の非特異的な結合を許容しないことが明らかにされている。
【0041】
ある実施形態においては、10から200、好ましくは20から100の異なる配列を有するプライマーが用意されると効果的である。
【0042】
このようにして300から2000の相補的な構成要素が、ウィルスRNAとして例えば4000から10000構成要素の配列長さを有する対象配列に付加されるので、この対象配列はこの種のハイブリッド化においては平均して最大数の付加すべきプライマーを収容する。その場合に好ましくは、対象分子とプライマーとからなるこの種の複合体が測定体積内へ移動すると、プライマーの極めて激しい濃縮と、それに伴って変動する蛍光信号の著しい増大がもたらされ、それが測定の確実性をさらに向上させる。
【0043】
一般に、プライマーが例えばヌクレイン酸合成材を用いて直接的な合成によって形成されると効果的である。
【0044】
ここで、種々のオリゴヌクレオチド(プライマー)を形成する絶対に確実な方法を説明しておいた方がよいと思われる。この方法は時間がかかるが、提供された「カクテル」の内部に場合によっては対象配列全体が存在することと、それに伴って対象配列が誤って表示されることを排除する。さらに重なり合うプライマー配列が防止され、それによって所望のマーキングが可能になる。もちろん対象配列は正確にわかっていなければならない。
【0045】
あるいはまた、プライマーが色素分子でマークされたヌクレイン酸(あるいは類似の)構成要素が存在するところで対象配列の複製または転写によって形成されると効果的であって、その場合に複製または転写生成物は次に部分配列に切断されて、その後プライマーとして使用される。
【0046】
この方法は、明らかに迅速に進行するという利点を有し、もちろんカクテルはこの方法の最初にまだ対象配列を含んでいるが、それは必ずしも正確にわかっている必要はない。従って、切断する際にどんな場合でも対象配列が分解され、それによって誤った表示が防止されることが保証されなければならない。複製または転写生成物のこの切断は、例えば生成物を砕く剪断力を行使する、機械的な方法で行うことができる。
【0047】
あるいはまた、複写または転写生成物を所定の期間の間特異的および/または非特異的に切断するヌクレアーゼの作用にさらして、それによって生成物をプライマーに切断することができる。
【0048】
その場合には、この切断を時間的に制御して、所望の平均長さを有するプライマーが発生するようにできる利点が得られる。
【0049】
全体として、複写または転写生成物がポリメラーゼ連鎖反応技術、同様な方法を使用することによって、あるいは他の特異的なRNAないしDNAポリメラー
ゼを用いて形成されると効果的である。
【0050】
この方法は良好に導入される方法であって、対象配列からプライマーを形成するために効果的に使用することができる。好ましくはここではプライマーは、その配列順序が部分的にしか、あるいは全く分かっていない対象配列に対して形成することができる。ただ、対象配列の端部が分かっていること、または分かっている配列部分がまったくわかならい対象配列に付くように合成され、それによってPCR方に必要なプライマーが用意できるようにすることだけが必要である。対象配列の2つのプライマー間にある領域の順序は必ずしもわかっている必要はなく、分析用のプライマーはいわば「自動的に」正しく発生されるので、例えば新しいウィルスを探すことができる。
【0051】
さらに好ましくは、DNA合成材を用いて短いDNA鎖が形成され、このDNA鎖は、このDNA鎖がその後例えばT7ポリメラーザによって転写されて、転写生成物がプライマーとして使用される場合には、対象配列の部分を有する。
【0052】
この場合に好ましくは、公知の方法でRNAプライマーを形成することができ、このプライマーはその後本発明によって証明すべきRNA対象配列に対してカクテルとして使用することができ、その場合にさらに対象配列の配列順序全体がわかっている必要はない。
【0053】
一般に、プライマーとしてDNA、RNAまたはPNA配列が使用されると効果的である。
【0054】
その場合には、DNAとRNA対象配列が証明できると効果的であって、その場合に、ペプチド類似の脊柱を有し、従って(RNAとDNAのように)マイナスに帯電されていない、場合によってはプラスに帯電されたPNA配列を使用することによって、自由なプライマーと複合されたプライマーとを電気泳動で分離することが可能になる。プラスの残留グループの付着によってPNAsがプラスの帯電を有する場合があり、それが分離をさらに容易にする。
【0055】
さらに好ましくは、ステップb)において、混合された溶液が、対象配列の三次及び二次構造が完全に溶融されるだけ高く、プライマーと対象配列との間の特異的な結合は溶融しないだけ十分に低く、さらにプライマーと対象配列間の非特異的な結合が溶融されるだけ十分に高い温度で温置される。
【0056】
それによって好ましくはマーキングの際の重要な問題が解決される。すなわち、プライマー配列を付加するための速度定数は一般に10の6乗Mマイナス1乗Sマイナス1乗より低いので、10のマイナス9乗Mマイナス9乗のプライマー濃縮を使用する場合にすでに1000秒より多い反応時間が発生する。しかしこの値は著しく温度に関係する。というのは対象配列の二次構造が溶融しないと、プライマー配列を付加できないからである。しかしまた、プライマー結合の融点より低い温度で作業しなければならず、その場合に非特異的な誤った付加を排除するためには温度はこの融点のすぐ下でなければならない。
【0057】
すべてのことから、プライマーカクテルによる対象配列のマーキングは好ましくは、前述の融点を定量的に考慮した正確に決定された温度プロセスによってもたらされなければならないことが明らかになる。
【0058】
ある実施形態においては、好ましくはそのためにプライマーは対象配列に比較して極めて過剰に使用され、その場合に温置が行われた後に、結合されていないプライマーをハイブリッド化された対象配列から分離することができる。
【0059】
この場合に好ましくは、まずより高いプライマー濃度でハイブリッド化の飽和を行い、次に反応しなかったプライマーを分離することができる。
【0060】
このことは特に、プライマーとしてプラスに帯電されたPNA配列が使用される場合に、簡単な電気泳動方法によって可能となる。
【0061】
プライマーによってハイブリッド化された対象配列のステップc)における同定は、任意の時間分解された蛍光分光法を用いて行うことができ、この蛍光分光法は非常に少量の体積エレメント内で極めてわずかな蛍光信号を単独光子計数にいたるまで検出することができる。その場合に重要なことは、時間分解によって自由なプライマーに基づく信号を対象配列によっていわば濃縮されたプライマーに基づく信号から明確に区別できることである。
【0062】
好ましくはこれは相関蛍光分光法を用いて行われ、この方法においては温置された溶液の極めてわずかな体積単位、好ましくは0.1から20flがレーザの励起光にさらされ、励起光が測定体積内にあるプライマーを励起して蛍光光を放出させ、その場合に測定体積から放出された蛍光光は光電検出器を用いて測定され、かつ測定された放出の時間的な変化と関与する分子の相対的な拡散速度との相関が形成されるので、然るべく激しく希釈した場合には測定体積内で個々の分子が同定される。その場合に好ましくは、電場が使用され、それによってプライマーによってハイブリッド化された対象配列のドリフト速度が拡散速度を越えて増大される。
【0063】
大きなRNAまたはDNA分子は比較的低速で拡散するので、特殊な方法を用いて光トラップで濃縮しなければならない。通常の拡散の場合には、M13ファージについて測定されたように、拡散係数が5×10のマイナス8乗平方センチメートル/sであると仮定して、直径0.5μmの光トラップへの対象配列の拡散にかかる平均時間は約10のマイナス10乗Cマイナス1乗であって、その場合にcは対象配列のモル濃度である。c=10のマイナス15乗Mですでに、一日の拡散時間が得られる。
【0064】
拡散時間の短縮は、光トラップの空間要素を拡大することによっても達成させるが、その場合には狭い限界がもたらされる。というのはノイズ背景が空間要素の半径の3乗で上昇するからである。
【0065】
効果的な方法は、上述したように電場を用いてドリフト速度を増大させることであって、それによって効果的に測定時間を著しく短縮することができる。
【0066】
その場合に好ましくは、結合されていないプライマーとプライマーによってハイブリッド化された対象配列との毛管電気泳動分離が行われ、その場合に毛管の0.01mmより小さい尖端開口部が測定体積の前に位置決めされて、毛管内で直流電場が発生され、その電場がプライマーでハイブリッド化され、マイナスに帯電された対象配列を測定体積の方向へ移動させる。
【0067】
好ましくはここでは引き出された毛管、いわゆるネーエル毛管が使用され、これは例えばネーエルとサクマン(E.Neher、B.Sakmann)のサイエンティフィック・アメリカンの論文「The Patch Clamp Technique」1992年3月、第44ページから第51ページに記載されている。冒頭で述べたWO94/16313からは、この種の毛管において約1kV/cmの場を発生させ、それによって約1mm/sの移動速度がもたらされることがすでに知られている。
【0068】
毛管の代わりに4極子またはラジアルのイオントラップを使用することができ、その場合に後者が特に効果的である。後者は「点状の」尖端からなり(例えばネーエル毛管)、この尖端が例えば1cmの直径を有する環状電極によって包囲されている。この場合には場は直流場であって、プラスに帯電された毛管の尖端が設けられる。マイナスに帯電された対象構造が非均質の場内で尖端で濃縮される。そこでは場内の移動による到着移送と拡散による搬出移送との間に均衡が存在する。低速で拡散する対象構造はその低分子のプライマーよりも10の3乗倍まで強く濃縮される。
【0069】
あるいはまた、好ましくはステップc)において高周波の非均質な交流電場が使用され、この電場が対象配列内に双極子モーメントを誘導し、その双極子モーメントが非均質の場内で双極子モーメントとして移動する。
【0070】
この場合には好ましい方法で、毛管電気泳動分離またはラジアルイオントラップの主要な欠点が除去される。というのはマークされていないプライマーが一緒に濃縮されることが防止されるからである。
【0071】
アイゲン(M.Eigen)とシュヴァルツ(G.Schwarz)の「電解質(Electrolytes)」、ペルガモン プレス(Pergamon Press)1962年の論文「電場における緩和現象から決定される、溶液内の高分子電解質の構造と運動特性(Structure and kinetic properties of polyelectrolytes in solution、determined from relaxation phenomena in electric fields)」には、小さい棒状の電解質と特にヌクレイン酸が、電場内でイオン雰囲気が高電荷イオンに対して移動することによってもたらされる電気的な分極率を有することが記載されている。特にDNAの場合には、非常に大きな誘導双極子が得られ、この双極子は10の3乗ボルト/cmの場の強さにおいてすでに場内の完全な整合をもたらす。分極化の緩和時間はマイクロ秒であるので、高周波の交流電場を用いて約10の5乗から10の6乗Hzで作業を行うことができる。整合はミリ秒から秒のうちに行われる。
【0072】
換言すると、高周波の交流電場がヌクレイン酸内に強い双極子モーメントを誘導し、それをこのように供給されたヌクレイン酸を有する溶液の導電性の変化によって示すことができる。しかしこのことは、非均質の高周波の交流電場においてはヌクレイン酸はより場の強い方向へ移動することを意味し、本発明はそれを利用して、測定体積内でマークされた対象配列を濃縮するために用いている。というのは双極子は非均質な場においては場の強さが大きい方向へ移動するからであって、より強い場をそれが測定体積内に位置するように設けることができる。
【0073】
そのために、ラジアルの電極装置が使用され、この電極装置は光トラップ内に配置された電極尖端と環状の相手側電極から形成される。
【実施例】
【0074】
本発明の実施例を図面に示し、以下で詳細に説明する。
【0075】
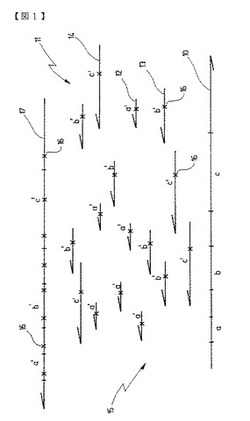
図1においてヌクレイン酸鎖が対象配列10の形状で図示されており、対象配列には選択された個々の配列部分が符号a、b及びcで記載されている。
【0076】
対象配列10の他に、対象配列10と共に温置溶液15内に存在するプライマー12、13、14の混合物11が図示されている。
【0077】
プライマーまたはオリゴヌクレオチド12は部分aに対して相補的な配列a’を有し、プライマー13と14は部分bないしcに対して相補的な配列を有する。
【0078】
プライマー12、13、14はそれぞれ然るべく励起された場合に蛍光光を発する1つまたは多数の色素分子16でマークされている。色素分子16は図1ではクロスで象徴されている。
【0079】
多数のプライマー12、13、14の代わりに、多数の色素分子16によってマークされ、かつ対象配列10に対して相補的な、多かれ少なかれ全部揃ったアンチセンス鎖17を使用し、あるいは対象配列10を2本鎖に重合化することによって発生させることもできる。
【0080】
溶液15が、対象配列10の二次構造が発生してもそれが完全に溶融される高さであるが、プライマー12、13、14と対応する部分a、b、cとの間の固有結合を溶融しないだけ十分に低い温度で温置された場合に、プライマー12、13、14が対象配列10に付加される。その場合に温置温度は、プライマー12、13、14と対象配列10との間の非固有の結合が再び溶融されるように、十分に高くなければならない。
【0081】
このようにして得られた溶液15内では1つの対象配列10または少数の対象配列10がそれぞれ多数のプライマー12、13、14を有し、その場合にプライマーは15から20構成要素の対象長さを有し、全体で20から100の異なるプライマー12、13、14が用意される。
【0082】
プライマー12、13、14は例えばヌクレイン酸合成材による直接的な合成によって形成することができ、その場合にDNA合成材を使用すると対象配列10の部分a、b、cを有する色素でマークされた短いDNA鎖が形成される。このDNA鎖はその後例えばT7ポリメラーゼで転写されて、転写生成物がプライマー12、13、14として使用される。「カクテル」と称される混合物11を形成するこの製造方法は、配列内で部分a、b、cがわかっていることが前提となる。
【0083】
それに対して配列内で部分的に、あるいはまったく分かっていないヌクレイン酸鎖10を対象配列として使用しようとする場合には、プライマー12、13、14は色素分子でマークされたヌクレイン酸構成要素の存在するところで対象配列を複製または転写することによって形成される。これは例えばポリメラーゼ連鎖反応技術、類似の方法を使用して、あるいは例えばT7ポリメラーゼなどのDNAないしRNAポリメラーゼ、逆の転写酵素などによって行われる。
【0084】
複製または転写生成物はその後部分配列に切断され、その場合に生成物をプライマーに切断するために、機械的方法または固有および/または非固有に切断するヌクレアーゼが使用される。もちろんここでは、偽陽性の表示を防止するために、転写/複写の原型として最初に使用される対象配列のどれもが混合物11内にもはや含まれていないことが保証されなければならない。
【0085】
対象配列10とプライマー12、13、14としてRNA分子もDNA分子も使用することができる。さらに、プライマー12、13、14として、正の電荷を有することが可能ないわゆるPNA分子を使用することができるので、結合されたプライマー12、13、14を有する対象配列10から電気泳動法で自由なプライマー12、13、14が分離される。
【0086】
アンチセンス鎖17を使用する場合には、これを調査溶液に付加することができ、その後然るべき温度処理によって2本鎖形成が行われるように配慮される。あるいはまた、対象配列10に色素でマークされたヌクレイン酸構成要素を付加して、ポリメラーゼを用いて対象配列10を対象配列10とアンチセンス鎖17とからなる2本鎖に重合することも可能である。証明すべき対象配列10に関する特異性は、対象配列10にまず、対象配列10の鎖始端と共に、後にポリメラーゼ用のプライマーとして用いられる2本鎖部分を形成する固有のオリゴヌクレオチドを付加しなければならないことによって得られる。このようにして種々の対象配列10をポリメラーゼ用の異なるプライマーによって選択することができる。このようにして対象配列が多数の色素分子でマークされた2本鎖に重合される。
【0087】
温置溶液15の一部はその後、図2に概略図示され符号20で示される光学分析装置へ供給され、この分析装置は1つまたは多数のプライマーがハイブリッド化されている証明すべきヌクレイン酸鎖のいくつか、好ましくは1つをハイブリッド化されていないプライマーを背景として判別するように構成されている。
【0088】
図2に示される装置20はFCS装置であって、例えば冒頭で述べたWO94/16313から知られている。このFCS装置21の構造と機能の詳細な説明は、この公報とそれに記載された引例を参照することができる。
【0089】
簡単に説明すると、FCS装置21はレーザ22を有し、このレーザはビームスプリッター23並びに共焦のイメージ光学系24を介して、0.1から10flの範囲にある少量の測定体積25を照射する。この測定体積25は共焦の光学系24を介して光電検出器26上に結像され、光電検出器はこれ以上詳しく図示しないFCS分析用の評価電子装置と接続されている。
【0090】
測定体積25は、図2では概観性を考えて図示していない温置溶液15の小部分を覆っている。
【0091】
温置溶液15が色素でマークされた上述の2本鎖を含む場合には、温置溶液15を装置20に供給する前に、場合によってはさらに色素でマークされた自由なヌクレイン酸構成要素を場合によっては電気泳動で分離しなければならない。2本鎖内に多数の色素分子が存在するので、測定体積25内へ移動するこの種の2本鎖は閃光として現れ、従ってそのままで同定可能である。供給される、あるいは発生されるアンチセンス鎖17は対象配列10に固有に「合っている」だけなので、この種の閃光は、証明すべきヌクレイン酸鎖が実際に対象配列10を有することを意味している。
【0092】
プライマー12、13、14でハイブリッド化された対象配列10を拡散管理されるより速く測定体積25内へ移動させるために、電気的な分子トラップ27が設けられており、これは図示の実施例においては環状電極28とネーエル毛管9を有し、その毛管の引き出された尖端が環状電極28に対して中央に位置している。
【0093】
環状電極28とネーエル毛管29の間に電圧が印加されると、測定体積25内への対象配列10のドリフトが行われる。プライマー12、13、14と対象配列10が異なる電気量を有する場合には、同時に電気泳動分離が得られる。
【0094】
しかし図示の実施例においては電圧30は交流電圧31であって、環状電極28とネーエル毛管29との間に非均質の高周波の交流電場を発生させる。その場合にこの交流電場の周波数は、好ましくは数百kHzの範囲にある。
【0095】
この交流電場によって特にDNAにおいては非常に大きな誘導双極子モーメントが発生し、この双極子モーメントは10マイナス3乗ボルト/cmの場の強さにおいてすでに場内での完全な整合をもたらす。分極の緩和時間はマイクロ秒である。従って約10の5乗から10の6乗Hzの高周波の交流場で作業をすることができ、その場合に整合はミリ秒から秒で行われる。この効果が、測定体積25内でマークされた対象配列を濃縮するために利用される。
【0096】
その場合に電気的な分子トラップ27は測定体積25内に配置されたネーエル
毛管29の電極尖端を使用し、その場合に電極尖端は1μmの直径を有する。それに対して環状の相手側電極25は1cmの直径を有する。
【0097】
図2では概観を考慮して図示していない温置溶液15が電極29、28間の空間を満たす。この空間内に電圧30、31が印加されると非均質のラジアル場が発生し、その場の強さは1/rに比例する。従って電極電圧が10ボルトである場合には、r=1μmの尖端で10の5乗ボルト/cmの場の強さが得られる。
【0098】
対象配列10内に誘導される双極子は、この非均質の場においては最高の場の強さの領域に、従って測定体積25の領域に引き込まれる。
【0099】
到達し得る双極子モーメントは長さの2乗に比例し、DNAの場合には等価長さが見積もられるので、マークされた長いヌクレイン酸鎖は応答するが鎖の短いプライマー配列は応答しない場の強さが選択される。高周波の交流場が印加されるので、例えばプロテイン分子などの大きな剛性の双極子も電気的トラップ27に応答しない。
【0100】
従ってこのようにして、カクテルを用いることによってマークされたプライマー配列12、13、14を対象配列10に付加して、この対象配列10をハイブリッド化されたプライマー12、13、14と共に装置20の測定体積25内へ移動させることができる。その場合にカクテルの使用によって測定された信号の強度が増大し、電気的な分子トラップ27の使用によって必要な測定時間が著しく削減される。というのは拡散速度にドリフト速度が重畳されるからである。
【0101】
従って新しい方法と、新しい混合物11並びに新しい装置20によって、容認できる測定時間内に既知および/または未知の配列の個々のヌクレイン酸鎖を証明することが可能になる。
【0102】
後述するように、測定体積25内に発生する熱効果は無視することができる:
導電性σと電場の強さEにおいて散逸するエネルギは、長さlで直径dの毛管が均質な場合には次のようになる。
【数1】

【0103】
Qel=σE2 ld2 π/4
その場合に電気的な熱等価は約0.2cal/Wsとなる。Qelを熱の消散によって液体から除去するためには、定常的な温度勾配dT/drが必要であって、その場合に媒体は次に示すように熱伝導度λを有すると仮定される。
【数2】

【0104】
0.2σE2 ld2 π/4=λldπ・dT/dr
あるいは、
【数3】

【0105】
dT/dr=σE2 ・d/λ・20
水に関するλが10のマイナス3乗cal/(cm度秒)と仮定し、その場合にσ<10マイナス3乗シーメンスでE=10ボルト/cmである代表的な例においては、毛管が0.1cmの直径を有する場合には、0.5度/cmより小さい温度勾配が得られる。従って、主要な熱停滞が水中で行われ、毛管壁では行われないと仮定して、血清を過度に希釈せずに直接調査することができる。
【0106】
同様なことがラジアルの分子トラップ27についても観察される。ネーエル毛管29の電極尖端の領域で場の強さは10マイナス5乗ボルト/cmであるので、μmの領域では10の5乗度/cmの温度勾配が発生するが、これはマイクロメータの領域の10度の過熱に相当する。
【0107】
最後に述べておきたいことは、何回も述べたWO94/16313からすでに一般的な形で知られているように、2つまたは多数の蛍光色素を使用して、クロス相関を実施することによって、測定方法の感度をさらに上昇させることが可能であることである。
【図面の簡単な説明】
【0108】
【図1】対象配列とプライマーとからなる温置溶液の簡略化した概略図である。
【図2】高周波、非均質の電気的交流場を使用する、寸法を無視して記載された電気的な分子沈澱装置を有する光学分析装置を簡略化して示す概略図である。
【符号の説明】
【0109】
10 対象配列
11 混合物
12,13,14 プライマー
15 温置溶液
16 色素分子
17 アンチセンス鎖
21 FCS装置
22 レーザ
23 ビームスプリッター
24 イメージ光学系
25 測定体積
26 光電検出器
27 分子トラップ
28 環状電極
29 ネーエル毛管
30 電圧
31 交流電圧
【技術分野】
【0001】
本発明は、調査溶液内で所定の対象配列の少数の、好ましくは個別のヌクレイン酸の鎖を直接検出する方法に関するものである。
【0002】
本発明はさらに、この方法を実施する装置並びにその際に使用される試験溶液に関するものである。
【背景技術】
【0003】
一般に、既知の、部分的に既知の、かつ/または未知の配列のDNA/RNA分子を証明できることが望まれている。それに関する用途例は、例えば発生進化的バイオテクノロジーの枠内での遺伝学上の調査、実験室実験の分析、あるいは特にウィスル診断学である。これらすべての用途例において最初から存在する調査溶液内に多くは所定の対象配列の少数のまたは全く個別のヌクレイン酸の鎖があって、それが調査溶液内で好ましくは定量的に検出される。
【0004】
現在ではウィルス感染の証明は間接的な方法、すなわち取り付かれた宿主の免疫反応を介して行われる。テストは、これら間接的な方法に付随する一連の困難と結び付いている。それに数えられるのは遅延された免疫反応の長い潜伏期間、例えばエリザ・テストの時間のかかる分析、並びに偽陽性ないし偽陰性の免疫反応の可能性である。
【0005】
従ってウィルスを極めて専門的に証明することのできる直接試験を行うことが望まれている。この直接証明の困難性は特に、大きな感度が要求されることにある。すなわち、ボーダーラインのケースにおいては、細胞抽出物内ないしは血清内で唯一のウィルス粒子を証明することができなくてはならない。その場合に証明すべきヌクレイン酸の鎖の濃度は10マイナス12乗から10マイナス18乗分子濃度の範囲にある。
【0006】
数年前に開発された方法は、個別のあるいは少数のヌクレイン酸の鎖を、例えばゲル電気泳動などの従来の方法、温度勾配ゲル、配列決定の方法、例えばサンガー(Sanger)方法またはマクサム・ギルバート法に従って接近し得る濃度水準まで高濃縮することにある。この高濃縮には、ポリメラーゼ連鎖反応法(PCR)または証明すべきヌクレイン酸部分の固有の複製に基づく同様な方法が使用される。その場合に、短い1本鎖領域がプライマーとして供給される場合に、1本鎖を2本鎖に重合化するDNAポリメラーゼの特性が利用される。その場合に増強すべき配列を有するヌクレイン酸の鎖に、増強すべき配列の端縁領域に基づく鎖固有の、すなわち両DNA鎖の一方に対して相補的な2つの化学的に合成されたオリゴヌクレオチドが過剰に加えられる。
【0007】
まず、この種の方法は非常に時間がかかり、この方法はPCR反応を実施することが必要であるだけでなく、その後他の分析を行って、調査溶液中に求める配列が存在することを少なくとも定性的に結論づけられるようにしなければならない。さらにここでは、求める配列の対応する部分に対して正確に相補的な、約15−20ヌクレオチドの長さを有する所定の短い鎖のヌクレイン酸配列が用意されることが必要である。この種の正確に相補的な短い鎖のヌクレイン酸部分を一般に「アンチセンス配列(Antisense−Sequenz)」または「プライマー」とも称する。
【0008】
時間がかかる他に、この方法においてはさらに、両端部において配列順序の少なくとも1つの短い部分がわかっており、それによって対応するプライマーを用意できるヌクレイン酸配列しか証明できないという欠点がある。証明すべきヌクレイン酸の鎖がRNA分子である場合には、これをまずさらにRNA依存性のDNAポリメラーゼを用いてDNAコピーに書き換えてから、PCR技術を使用することが可能になる。
【0009】
場合によっては異なる処理ステップが多数あるので、この方法は多数の誤りの原因を有する。というのは個々のポリメラーゼは重合化の際にある確率でしか「正しい」相補的なヌクレオチドを組み込めないので、ここでも偽陽性と偽陰性のテスト結果がもたらされることを排除できない。
【0010】
他の方法は、求める配列を直接視認できるようにすることであって、このことは当然のことながらまずその配列が他の配列から明らかに区別できなくてはならないことを意味している。個々の分子を同定して計数する新しく開発された方法が、WO94/16313に記載されている相関蛍光分光法であって、以下においてはFCSと略称する。上述の公報には、測定体積内で証明すべき分子が他の分子から明白に区別されるかあるいは分離されて存在している限りにおいて、FCSを用いて0.1から10flの範囲の極めて少量の測定体積内で色素でマーキングされた個々のDNA/RNA分子を証明できることが記載されている。
【0011】
すでに述べたPCR法においては2つのプライマー配列が必要であって、その一方はプラス鎖の鎖始端に対して相補的であって、他方はマイナス鎖の始端に対して相補的である。両プライマー配列の位置間の配列部分がその後濃縮される。それに対してPCS証明の場合には蛍光色素でマーキングされた1つの固有のプライマー配列しか必要とされない。そのプライマー配列が検出すべき(1本鎖の)RNA配列または完全に溶融されたDNA配列の鎖に直接付加される。この形においてマークされたプライマーはその電荷特性においてもその移動度においても結合されていないプライマーから明白に区別され、それ以上濃縮しないでもFCS法によって直接検出することができる。
【0012】
FCSの測定原理は、溶液の比較的少量の体積要素がレーザの強い励起光にさらされることによって、極めて薄い溶液内の蛍光団分子が測定されることに基づいている。この測定体積内に存在する、分子に対応する励起スペクトルがレーザによって励起される。この体積要素から放出される蛍光がその後光電子増倍管上に結像される。希釈された溶液である場合には、それぞれの体積要素内の分子の濃度が明らかに変動する。
【0013】
一度体積要素内に拡散された分子は、固有の拡散速度に従って、該当する分子の固有の平均時間経つと再び体積要素から分離して、その後はもはや観察されない。
【0014】
同一の一つの分子のルミネッセンスがその分子が測定体積内に滞留する平均的な滞留時間の間に多数回励起される場合には、この分子から多数の信号が検出される。従って希釈された溶液の場合には、一度測定体積内に拡散された分子が再び出て行く前に再度励起される確率は、新しく入ってくる分子の場合よりもずっと大きい。
【0015】
上述のWO94/16313には、この測定原理に基づいて希釈溶液内で個々の分子を検出することが可能であると記載されている。証明すべき分子がヌクレイン酸鎖である場合には、証明すべき分子の所定の部分配列に対して相補的なプライマーが付加され、その結合されない状態における拡散特性が対象分子に結合された状態から区別される。
【0016】
関与する分子の拡散速度に関係する、現在では比較的長い測定時間を短縮するために、上述の文献には、測定体積内の証明すべき分子を濃縮することのできる種々の方法が記載されている。これらの方法は原理的に、結合されないプライマーとプライマー・ヌクレイン酸鎖複合体の電荷の違いを利用して、整流された電場において結合されないプライマーを複合体から分離し、あるいは異なる拡散速度を利用することに基づいている。
【0017】
証明の特異性を向上させる他の方法は、異なるようにマークされた2つの異なるプライマーを使用することにある。異なるようにマークされたプライマーに基づく蛍光信号の時間的相関によって、電子的な信号処理の方法で非相関の、従って遊離されたプライマーの信号が効果的に抑圧される。
【0018】
さらに、例えば4Hzの低周波の交流電場によって帯電された分子が測定体積によって振動され、それによって分子がほぼ合焦されるので、測定体積内で単一の分子または少数の分子だけを定量的に検出することが可能になると記載されている。
【0019】
上述の公報はFCSの多数の使用方法を記載しているが、正確には装置と、光学系と種々の分子沈澱を扱っている。もちろん特に、FCS装置を用いてプライマーを使用して個々のDNA/RNA鎖を計数できることが記載されている。このPCT出願は物理的パラメータの測定にも大いに注目しており、そのために特に異なるようにマークされた配位子が使用されるが、しかしこれは測定信号の強度を改良するためではなく、特異性を向上させるために行われる。すなわち、例えば証明すべき分子の回転速度など他のパラメータを定めることができるようにするために、この種の異なるようにマークされたゾンデにおいてクロス相関技術が使用される。
【0020】
一般的に、関与する分子の拡散速度にドリフト速度を重畳させるために、電気泳動法、毛細管、直流電場などを使用できることが記載されている。その場合にプライマーと対象分子は、それらが異なる電荷を有し、従って電場において異なるように移動するように選択することができる。
【0021】
従ってFCS法はPCR法または類似の方法に比較して一連の利点を有する。まず、FCS法は1本鎖のヌクレイン酸分子も2本鎖のそれにも直接使用することができる。多数の病原が1本鎖のRNAウィルスであるので、これらはFCS法ではまずDNAに複製する必要はなく、そのことが分析にかかる時間の中で前向きに評価される。さらにFCS法はより直接的であり、従って個々のヌクレイン酸を証明することができ、このヌクレイン酸はPCR法の場合にはまず複製しなければならず、そのことも同様にかかる時間の差をもたらす。
【0022】
さらに濃縮プロセスがある物質によってじゃまされ、あるいは阻止されることがあるので、天然の試料についてはPCR法は必ずしも信頼できない。
【0023】
しかしPCR法とまったく同様にFCS法も特異性に関しては障害が生じ易い。すなわちプライマー配列は例えば一部において、対象配列に偶然に類似している配列に対しても相補的になる場合がある。従って、結合の際に十分な特異性を得るために、15から20ヌクレオチドの長さのプライマー配列が選択される。しかしその場合には、部分的にのみ相補的な配列の融点が作業温度以下にあって、従って測定技術的に検出されないことが保証されなければならない。
【0024】
PCR法の場合には2つのプライマー配列が使用され、その場合に2つの配列が誤結合を有する確率はわずかである。しかしその代わりにここではプライマーはずっと高い濃度で使用しなければならない。というのはプライマーが反応によって消費されるからである。
【0025】
それに対してFCS法の場合にはプライマー濃度は、証明すべきヌクレイン酸鎖への添加が測定時間内で行われる程度の高さでよい。
【0026】
これらの条件がこれらの方法の使用をわずかな絶対量に厳しく制限する。
【特許文献1】WO94/16313
【発明の開示】
【発明が解決しようとする課題】
【0027】
それに基づいて本発明の課題は、上述の欠点と困難を克服し、かつヌクレイン酸鎖を迅速かつ確実に直接証明することのできる冒頭で述べた種類の方法を提供することである。
【課題を解決するための手段】
【0028】
本発明によればこの課題は、次のステップを有する冒頭で述べた種類の方法によって解決される。すなわち、a)それぞれ対象配列の部分に対して相補的な、いわゆるアンチセンス配列を有し、かつ1つまたは多数の色素分子でマークされた種々の短いプライマーの混合物を有する試験溶液を用意し、b)この試験溶液を調査溶液と混合し、この混合された溶液を、証明すべきヌクレイン酸鎖によるプライマーのハイブリッド化を許容する周辺条件の下で温置し、その後、c)温置された溶液内で光学分析装置を用いて対象配列を同定し、この装置は1つまたは多数のプライマーがハイブリッド化されている証明すべきヌクレイン酸鎖の少数、好ましくは1つをハイブリッド化されていないプライマーを背景として判別するように構成されている。
【0029】
本発明の課題は、このようにして完全に解決される。すなわち、対象配列によって多数のプライマーをハイブリッド化することによって、付加されたプライマーを有する対象配列が測定体積内へ拡散し、それが記録される蛍光信号内で「閃光」として見られる場合に、例えばFCS技術において測定体積内でプライマーの局部的な濃度が著しく増大される。すなわち、本発明の発明者は、この種のプライマーの「カクテル」を利用できることを認識した。というのは、個々のヌクレイン酸鎖を証明する場合に、蛍光信号を増強することのみが重要となるからである。ほぼ「偶然に」プライマーが付加された配列は信号が極めてわずかであるので、公知のFCS法とは異なりもはや偽陽性表示されない。
【0030】
プライマーと対象配列間のハイブリッド化の速度定数は一般に10の6乗Mマイナス1乗Sマイナス1乗より低いので、プライマー濃度が10のマイナス9乗Mですでに反応時間千秒を越える。対象配列自体がわずかな複製でしか、例えばマイクロリットル当り1つの鎖でしか存在しない場合には、直接の証明は不可能である。というのは上述の例においては結合されていないプライマーが例えば百万倍過剰に存在することになるからである。FCS法に従って記録できるようにするためには、結合された蛍光マーカーは少なすぎて貢献できない。
【0031】
しかしこの問題は本発明によれば、対象分子の種々の部位に対して相補的なプライマー配列のカクテルを用意することによって解決される。各プライマー配列の中央に、すべて同一の等しい、あるいはまた場合によっては種々の発蛍光団からなる蛍光マークを設けることができる。このカクテルは例えば約10のマイナス9乗Mの濃度で提供され、これはフェムトリットル当り1分子を意味する。従ってレーザ光線の「光トラップ」が約0.2flの体積を有するFCS法においては、時間の約20%における蛍光マークの存在に相当する「背景ノイズ」が記録されてしまう。対象分子が光または分子トラップ内に達すると、その対象分子が蛍光の突然の「輝き」をもたらす。というのは例えば20から100の蛍光マーカーが光トラップ内に同時に存在することになるからである。平均の強度のマークされた対象分子が完全に消えて行く間、この対象分子はFCSの揺らぎ記録においてほぼ「照明弾」として現れる。
【0032】
原理的にはこの考えを腫瘍細胞に使用して、迅速な直接の腫瘍証明を可能にすることもできる。ここでは、各腫瘍細胞が抗体に関する数千の抗体決定素を有するという事実を利用することができる。抗体を色素でマークすれば、抗体が結合されている腫瘍細胞は上述のFCS法では「閃光」として証明される。ここでも色素でマークされた抗体を腫瘍細胞に付加させることによって濃縮する効果が利用される。この考えに基づく腫瘍証明は、本発明による考えの他の利用例であって、色素でマークされた多数の異なるゾンデが、これらゾンデが多数結合することのできる目標対象に対して使用される。ゾンデの濃度を低く抑えて、観察される測定体積内でそのゾンデが、目標対象に平均して結合されたゾンデの数よりずっと少ない統計的確率で浮上するようにする場合には、結合されたゾンデを有する目標対象が測定体積内に進入した場合に、測定体積内のゾンデの濃縮を測定することができる。
【0033】
またこの課題は、冒頭で述べた種類の方法において次のステップによって解決される。すなわち、1)証明すべきヌクレイン酸鎖の少なくともいくつかを、多数の色素分子でマークされ、対象配列全体またはほぼ全体に対して相補的であるそれぞれ長いアンチセンス鎖でハイブリッド化し、そして、2)対象配列を、アンチセンス鎖がハイブリッド化されている証明すべきヌクレイン酸鎖の少数、好ましくは1つを判別するように構成された光学分析装置を用いて同定する。
【0034】
このことによっても本発明の課題は完全に解決される。蛍光信号の増大は、アンチセンス鎖を非常に多数の色素分子でマークすることによって行われるので、この種の2本鎖も同様に記録された蛍光信号において「閃光」として認識される。
【0035】
証明すべきヌクレイン酸鎖とアンチセンス鎖間のハイブリッド化はまず、アンチセンス鎖が別に形成され、短いプライマーを調査溶液へ付加する方法の場合と同様に適当に温度処理することによって行うことができる。
【0036】
あるいはまた、証明すべきヌクレイン酸鎖とアンチセンス鎖からなる色素でマークされた2本鎖を、証明すべきヌクレイン酸鎖を直接重合化することによって形成することも可能であって、その場合に色素でマークされたヌクレイン酸(または類似の)構成要素が使用される。好ましくはここではマークされたUTPsが使用される。このようにして得られた、極めて多数の色素分子でマークされた2本鎖が同様にマークされた自由な構成要素を背景として証明できない場合には、マークされた2本鎖を含む溶液を例えばFCS装置へ供給する前に、前段で適当な分離処理を行わなければならず、これについては後述する。
【0037】
本発明による第1の方法の実施例においては、ステップa)で対象配列の種々の、好ましくは重なり合わない部分に対して相補的なプライマー配列が形成され、その場合に種々のプライマー配列はヌクレイン酸(または類似の)構成要素の配列順序内で互いに区別される。
【0038】
ここでは、対象配列に結合されるプライマー配列の数が非常に多いので、測定体積内でプライマー配列の高度の濃縮が行われ、それが偶然に通過する個々のプライマーによる偽陽性の測定結果に対するより大きい安全性を保証するという利点がある。
【0039】
その場合に好ましくは、ステップa)において、プライマー当り周波数長さ(配列長さ)が異なる、従ってヌクレイン酸(または類似の)構成要素の数の異なるプライマーが形成され、その場合にプライマーは10から50、好ましくは15から20構成要素の配列長さを有する。
【0040】
プライマー長さが異なることによって、証明すべきヌクレイン酸の二次構造を効果的に計算に入れることができる。その場合に鎖の短いプライマーはヌクレイン酸鎖の1本鎖で存在する領域に対して使用され、長いプライマー配列は例えばまず適当な温度を選択することによって溶融しなければならない2本鎖で存在する領域に対して使用され、その場合にプライマーはその後二次構造の形成に対抗する。構成要素が比較的多数であることによって、この場合には長い鎖のプライマーと対象配列の対応する部分との結合が非常に大きく、それによってプライマーの結合が二次構造の新たな形成に優先する。15から20構成要素を有するプライマーはまず対象配列の相補的領域と十分に特異的な結合を行い、さらに偶然の非特異的な結合を許容しないことが明らかにされている。
【0041】
ある実施形態においては、10から200、好ましくは20から100の異なる配列を有するプライマーが用意されると効果的である。
【0042】
このようにして300から2000の相補的な構成要素が、ウィルスRNAとして例えば4000から10000構成要素の配列長さを有する対象配列に付加されるので、この対象配列はこの種のハイブリッド化においては平均して最大数の付加すべきプライマーを収容する。その場合に好ましくは、対象分子とプライマーとからなるこの種の複合体が測定体積内へ移動すると、プライマーの極めて激しい濃縮と、それに伴って変動する蛍光信号の著しい増大がもたらされ、それが測定の確実性をさらに向上させる。
【0043】
一般に、プライマーが例えばヌクレイン酸合成材を用いて直接的な合成によって形成されると効果的である。
【0044】
ここで、種々のオリゴヌクレオチド(プライマー)を形成する絶対に確実な方法を説明しておいた方がよいと思われる。この方法は時間がかかるが、提供された「カクテル」の内部に場合によっては対象配列全体が存在することと、それに伴って対象配列が誤って表示されることを排除する。さらに重なり合うプライマー配列が防止され、それによって所望のマーキングが可能になる。もちろん対象配列は正確にわかっていなければならない。
【0045】
あるいはまた、プライマーが色素分子でマークされたヌクレイン酸(あるいは類似の)構成要素が存在するところで対象配列の複製または転写によって形成されると効果的であって、その場合に複製または転写生成物は次に部分配列に切断されて、その後プライマーとして使用される。
【0046】
この方法は、明らかに迅速に進行するという利点を有し、もちろんカクテルはこの方法の最初にまだ対象配列を含んでいるが、それは必ずしも正確にわかっている必要はない。従って、切断する際にどんな場合でも対象配列が分解され、それによって誤った表示が防止されることが保証されなければならない。複製または転写生成物のこの切断は、例えば生成物を砕く剪断力を行使する、機械的な方法で行うことができる。
【0047】
あるいはまた、複写または転写生成物を所定の期間の間特異的および/または非特異的に切断するヌクレアーゼの作用にさらして、それによって生成物をプライマーに切断することができる。
【0048】
その場合には、この切断を時間的に制御して、所望の平均長さを有するプライマーが発生するようにできる利点が得られる。
【0049】
全体として、複写または転写生成物がポリメラーゼ連鎖反応技術、同様な方法を使用することによって、あるいは他の特異的なRNAないしDNAポリメラー
ゼを用いて形成されると効果的である。
【0050】
この方法は良好に導入される方法であって、対象配列からプライマーを形成するために効果的に使用することができる。好ましくはここではプライマーは、その配列順序が部分的にしか、あるいは全く分かっていない対象配列に対して形成することができる。ただ、対象配列の端部が分かっていること、または分かっている配列部分がまったくわかならい対象配列に付くように合成され、それによってPCR方に必要なプライマーが用意できるようにすることだけが必要である。対象配列の2つのプライマー間にある領域の順序は必ずしもわかっている必要はなく、分析用のプライマーはいわば「自動的に」正しく発生されるので、例えば新しいウィルスを探すことができる。
【0051】
さらに好ましくは、DNA合成材を用いて短いDNA鎖が形成され、このDNA鎖は、このDNA鎖がその後例えばT7ポリメラーザによって転写されて、転写生成物がプライマーとして使用される場合には、対象配列の部分を有する。
【0052】
この場合に好ましくは、公知の方法でRNAプライマーを形成することができ、このプライマーはその後本発明によって証明すべきRNA対象配列に対してカクテルとして使用することができ、その場合にさらに対象配列の配列順序全体がわかっている必要はない。
【0053】
一般に、プライマーとしてDNA、RNAまたはPNA配列が使用されると効果的である。
【0054】
その場合には、DNAとRNA対象配列が証明できると効果的であって、その場合に、ペプチド類似の脊柱を有し、従って(RNAとDNAのように)マイナスに帯電されていない、場合によってはプラスに帯電されたPNA配列を使用することによって、自由なプライマーと複合されたプライマーとを電気泳動で分離することが可能になる。プラスの残留グループの付着によってPNAsがプラスの帯電を有する場合があり、それが分離をさらに容易にする。
【0055】
さらに好ましくは、ステップb)において、混合された溶液が、対象配列の三次及び二次構造が完全に溶融されるだけ高く、プライマーと対象配列との間の特異的な結合は溶融しないだけ十分に低く、さらにプライマーと対象配列間の非特異的な結合が溶融されるだけ十分に高い温度で温置される。
【0056】
それによって好ましくはマーキングの際の重要な問題が解決される。すなわち、プライマー配列を付加するための速度定数は一般に10の6乗Mマイナス1乗Sマイナス1乗より低いので、10のマイナス9乗Mマイナス9乗のプライマー濃縮を使用する場合にすでに1000秒より多い反応時間が発生する。しかしこの値は著しく温度に関係する。というのは対象配列の二次構造が溶融しないと、プライマー配列を付加できないからである。しかしまた、プライマー結合の融点より低い温度で作業しなければならず、その場合に非特異的な誤った付加を排除するためには温度はこの融点のすぐ下でなければならない。
【0057】
すべてのことから、プライマーカクテルによる対象配列のマーキングは好ましくは、前述の融点を定量的に考慮した正確に決定された温度プロセスによってもたらされなければならないことが明らかになる。
【0058】
ある実施形態においては、好ましくはそのためにプライマーは対象配列に比較して極めて過剰に使用され、その場合に温置が行われた後に、結合されていないプライマーをハイブリッド化された対象配列から分離することができる。
【0059】
この場合に好ましくは、まずより高いプライマー濃度でハイブリッド化の飽和を行い、次に反応しなかったプライマーを分離することができる。
【0060】
このことは特に、プライマーとしてプラスに帯電されたPNA配列が使用される場合に、簡単な電気泳動方法によって可能となる。
【0061】
プライマーによってハイブリッド化された対象配列のステップc)における同定は、任意の時間分解された蛍光分光法を用いて行うことができ、この蛍光分光法は非常に少量の体積エレメント内で極めてわずかな蛍光信号を単独光子計数にいたるまで検出することができる。その場合に重要なことは、時間分解によって自由なプライマーに基づく信号を対象配列によっていわば濃縮されたプライマーに基づく信号から明確に区別できることである。
【0062】
好ましくはこれは相関蛍光分光法を用いて行われ、この方法においては温置された溶液の極めてわずかな体積単位、好ましくは0.1から20flがレーザの励起光にさらされ、励起光が測定体積内にあるプライマーを励起して蛍光光を放出させ、その場合に測定体積から放出された蛍光光は光電検出器を用いて測定され、かつ測定された放出の時間的な変化と関与する分子の相対的な拡散速度との相関が形成されるので、然るべく激しく希釈した場合には測定体積内で個々の分子が同定される。その場合に好ましくは、電場が使用され、それによってプライマーによってハイブリッド化された対象配列のドリフト速度が拡散速度を越えて増大される。
【0063】
大きなRNAまたはDNA分子は比較的低速で拡散するので、特殊な方法を用いて光トラップで濃縮しなければならない。通常の拡散の場合には、M13ファージについて測定されたように、拡散係数が5×10のマイナス8乗平方センチメートル/sであると仮定して、直径0.5μmの光トラップへの対象配列の拡散にかかる平均時間は約10のマイナス10乗Cマイナス1乗であって、その場合にcは対象配列のモル濃度である。c=10のマイナス15乗Mですでに、一日の拡散時間が得られる。
【0064】
拡散時間の短縮は、光トラップの空間要素を拡大することによっても達成させるが、その場合には狭い限界がもたらされる。というのはノイズ背景が空間要素の半径の3乗で上昇するからである。
【0065】
効果的な方法は、上述したように電場を用いてドリフト速度を増大させることであって、それによって効果的に測定時間を著しく短縮することができる。
【0066】
その場合に好ましくは、結合されていないプライマーとプライマーによってハイブリッド化された対象配列との毛管電気泳動分離が行われ、その場合に毛管の0.01mmより小さい尖端開口部が測定体積の前に位置決めされて、毛管内で直流電場が発生され、その電場がプライマーでハイブリッド化され、マイナスに帯電された対象配列を測定体積の方向へ移動させる。
【0067】
好ましくはここでは引き出された毛管、いわゆるネーエル毛管が使用され、これは例えばネーエルとサクマン(E.Neher、B.Sakmann)のサイエンティフィック・アメリカンの論文「The Patch Clamp Technique」1992年3月、第44ページから第51ページに記載されている。冒頭で述べたWO94/16313からは、この種の毛管において約1kV/cmの場を発生させ、それによって約1mm/sの移動速度がもたらされることがすでに知られている。
【0068】
毛管の代わりに4極子またはラジアルのイオントラップを使用することができ、その場合に後者が特に効果的である。後者は「点状の」尖端からなり(例えばネーエル毛管)、この尖端が例えば1cmの直径を有する環状電極によって包囲されている。この場合には場は直流場であって、プラスに帯電された毛管の尖端が設けられる。マイナスに帯電された対象構造が非均質の場内で尖端で濃縮される。そこでは場内の移動による到着移送と拡散による搬出移送との間に均衡が存在する。低速で拡散する対象構造はその低分子のプライマーよりも10の3乗倍まで強く濃縮される。
【0069】
あるいはまた、好ましくはステップc)において高周波の非均質な交流電場が使用され、この電場が対象配列内に双極子モーメントを誘導し、その双極子モーメントが非均質の場内で双極子モーメントとして移動する。
【0070】
この場合には好ましい方法で、毛管電気泳動分離またはラジアルイオントラップの主要な欠点が除去される。というのはマークされていないプライマーが一緒に濃縮されることが防止されるからである。
【0071】
アイゲン(M.Eigen)とシュヴァルツ(G.Schwarz)の「電解質(Electrolytes)」、ペルガモン プレス(Pergamon Press)1962年の論文「電場における緩和現象から決定される、溶液内の高分子電解質の構造と運動特性(Structure and kinetic properties of polyelectrolytes in solution、determined from relaxation phenomena in electric fields)」には、小さい棒状の電解質と特にヌクレイン酸が、電場内でイオン雰囲気が高電荷イオンに対して移動することによってもたらされる電気的な分極率を有することが記載されている。特にDNAの場合には、非常に大きな誘導双極子が得られ、この双極子は10の3乗ボルト/cmの場の強さにおいてすでに場内の完全な整合をもたらす。分極化の緩和時間はマイクロ秒であるので、高周波の交流電場を用いて約10の5乗から10の6乗Hzで作業を行うことができる。整合はミリ秒から秒のうちに行われる。
【0072】
換言すると、高周波の交流電場がヌクレイン酸内に強い双極子モーメントを誘導し、それをこのように供給されたヌクレイン酸を有する溶液の導電性の変化によって示すことができる。しかしこのことは、非均質の高周波の交流電場においてはヌクレイン酸はより場の強い方向へ移動することを意味し、本発明はそれを利用して、測定体積内でマークされた対象配列を濃縮するために用いている。というのは双極子は非均質な場においては場の強さが大きい方向へ移動するからであって、より強い場をそれが測定体積内に位置するように設けることができる。
【0073】
そのために、ラジアルの電極装置が使用され、この電極装置は光トラップ内に配置された電極尖端と環状の相手側電極から形成される。
【実施例】
【0074】
本発明の実施例を図面に示し、以下で詳細に説明する。
【0075】
図1においてヌクレイン酸鎖が対象配列10の形状で図示されており、対象配列には選択された個々の配列部分が符号a、b及びcで記載されている。
【0076】
対象配列10の他に、対象配列10と共に温置溶液15内に存在するプライマー12、13、14の混合物11が図示されている。
【0077】
プライマーまたはオリゴヌクレオチド12は部分aに対して相補的な配列a’を有し、プライマー13と14は部分bないしcに対して相補的な配列を有する。
【0078】
プライマー12、13、14はそれぞれ然るべく励起された場合に蛍光光を発する1つまたは多数の色素分子16でマークされている。色素分子16は図1ではクロスで象徴されている。
【0079】
多数のプライマー12、13、14の代わりに、多数の色素分子16によってマークされ、かつ対象配列10に対して相補的な、多かれ少なかれ全部揃ったアンチセンス鎖17を使用し、あるいは対象配列10を2本鎖に重合化することによって発生させることもできる。
【0080】
溶液15が、対象配列10の二次構造が発生してもそれが完全に溶融される高さであるが、プライマー12、13、14と対応する部分a、b、cとの間の固有結合を溶融しないだけ十分に低い温度で温置された場合に、プライマー12、13、14が対象配列10に付加される。その場合に温置温度は、プライマー12、13、14と対象配列10との間の非固有の結合が再び溶融されるように、十分に高くなければならない。
【0081】
このようにして得られた溶液15内では1つの対象配列10または少数の対象配列10がそれぞれ多数のプライマー12、13、14を有し、その場合にプライマーは15から20構成要素の対象長さを有し、全体で20から100の異なるプライマー12、13、14が用意される。
【0082】
プライマー12、13、14は例えばヌクレイン酸合成材による直接的な合成によって形成することができ、その場合にDNA合成材を使用すると対象配列10の部分a、b、cを有する色素でマークされた短いDNA鎖が形成される。このDNA鎖はその後例えばT7ポリメラーゼで転写されて、転写生成物がプライマー12、13、14として使用される。「カクテル」と称される混合物11を形成するこの製造方法は、配列内で部分a、b、cがわかっていることが前提となる。
【0083】
それに対して配列内で部分的に、あるいはまったく分かっていないヌクレイン酸鎖10を対象配列として使用しようとする場合には、プライマー12、13、14は色素分子でマークされたヌクレイン酸構成要素の存在するところで対象配列を複製または転写することによって形成される。これは例えばポリメラーゼ連鎖反応技術、類似の方法を使用して、あるいは例えばT7ポリメラーゼなどのDNAないしRNAポリメラーゼ、逆の転写酵素などによって行われる。
【0084】
複製または転写生成物はその後部分配列に切断され、その場合に生成物をプライマーに切断するために、機械的方法または固有および/または非固有に切断するヌクレアーゼが使用される。もちろんここでは、偽陽性の表示を防止するために、転写/複写の原型として最初に使用される対象配列のどれもが混合物11内にもはや含まれていないことが保証されなければならない。
【0085】
対象配列10とプライマー12、13、14としてRNA分子もDNA分子も使用することができる。さらに、プライマー12、13、14として、正の電荷を有することが可能ないわゆるPNA分子を使用することができるので、結合されたプライマー12、13、14を有する対象配列10から電気泳動法で自由なプライマー12、13、14が分離される。
【0086】
アンチセンス鎖17を使用する場合には、これを調査溶液に付加することができ、その後然るべき温度処理によって2本鎖形成が行われるように配慮される。あるいはまた、対象配列10に色素でマークされたヌクレイン酸構成要素を付加して、ポリメラーゼを用いて対象配列10を対象配列10とアンチセンス鎖17とからなる2本鎖に重合することも可能である。証明すべき対象配列10に関する特異性は、対象配列10にまず、対象配列10の鎖始端と共に、後にポリメラーゼ用のプライマーとして用いられる2本鎖部分を形成する固有のオリゴヌクレオチドを付加しなければならないことによって得られる。このようにして種々の対象配列10をポリメラーゼ用の異なるプライマーによって選択することができる。このようにして対象配列が多数の色素分子でマークされた2本鎖に重合される。
【0087】
温置溶液15の一部はその後、図2に概略図示され符号20で示される光学分析装置へ供給され、この分析装置は1つまたは多数のプライマーがハイブリッド化されている証明すべきヌクレイン酸鎖のいくつか、好ましくは1つをハイブリッド化されていないプライマーを背景として判別するように構成されている。
【0088】
図2に示される装置20はFCS装置であって、例えば冒頭で述べたWO94/16313から知られている。このFCS装置21の構造と機能の詳細な説明は、この公報とそれに記載された引例を参照することができる。
【0089】
簡単に説明すると、FCS装置21はレーザ22を有し、このレーザはビームスプリッター23並びに共焦のイメージ光学系24を介して、0.1から10flの範囲にある少量の測定体積25を照射する。この測定体積25は共焦の光学系24を介して光電検出器26上に結像され、光電検出器はこれ以上詳しく図示しないFCS分析用の評価電子装置と接続されている。
【0090】
測定体積25は、図2では概観性を考えて図示していない温置溶液15の小部分を覆っている。
【0091】
温置溶液15が色素でマークされた上述の2本鎖を含む場合には、温置溶液15を装置20に供給する前に、場合によってはさらに色素でマークされた自由なヌクレイン酸構成要素を場合によっては電気泳動で分離しなければならない。2本鎖内に多数の色素分子が存在するので、測定体積25内へ移動するこの種の2本鎖は閃光として現れ、従ってそのままで同定可能である。供給される、あるいは発生されるアンチセンス鎖17は対象配列10に固有に「合っている」だけなので、この種の閃光は、証明すべきヌクレイン酸鎖が実際に対象配列10を有することを意味している。
【0092】
プライマー12、13、14でハイブリッド化された対象配列10を拡散管理されるより速く測定体積25内へ移動させるために、電気的な分子トラップ27が設けられており、これは図示の実施例においては環状電極28とネーエル毛管9を有し、その毛管の引き出された尖端が環状電極28に対して中央に位置している。
【0093】
環状電極28とネーエル毛管29の間に電圧が印加されると、測定体積25内への対象配列10のドリフトが行われる。プライマー12、13、14と対象配列10が異なる電気量を有する場合には、同時に電気泳動分離が得られる。
【0094】
しかし図示の実施例においては電圧30は交流電圧31であって、環状電極28とネーエル毛管29との間に非均質の高周波の交流電場を発生させる。その場合にこの交流電場の周波数は、好ましくは数百kHzの範囲にある。
【0095】
この交流電場によって特にDNAにおいては非常に大きな誘導双極子モーメントが発生し、この双極子モーメントは10マイナス3乗ボルト/cmの場の強さにおいてすでに場内での完全な整合をもたらす。分極の緩和時間はマイクロ秒である。従って約10の5乗から10の6乗Hzの高周波の交流場で作業をすることができ、その場合に整合はミリ秒から秒で行われる。この効果が、測定体積25内でマークされた対象配列を濃縮するために利用される。
【0096】
その場合に電気的な分子トラップ27は測定体積25内に配置されたネーエル
毛管29の電極尖端を使用し、その場合に電極尖端は1μmの直径を有する。それに対して環状の相手側電極25は1cmの直径を有する。
【0097】
図2では概観を考慮して図示していない温置溶液15が電極29、28間の空間を満たす。この空間内に電圧30、31が印加されると非均質のラジアル場が発生し、その場の強さは1/rに比例する。従って電極電圧が10ボルトである場合には、r=1μmの尖端で10の5乗ボルト/cmの場の強さが得られる。
【0098】
対象配列10内に誘導される双極子は、この非均質の場においては最高の場の強さの領域に、従って測定体積25の領域に引き込まれる。
【0099】
到達し得る双極子モーメントは長さの2乗に比例し、DNAの場合には等価長さが見積もられるので、マークされた長いヌクレイン酸鎖は応答するが鎖の短いプライマー配列は応答しない場の強さが選択される。高周波の交流場が印加されるので、例えばプロテイン分子などの大きな剛性の双極子も電気的トラップ27に応答しない。
【0100】
従ってこのようにして、カクテルを用いることによってマークされたプライマー配列12、13、14を対象配列10に付加して、この対象配列10をハイブリッド化されたプライマー12、13、14と共に装置20の測定体積25内へ移動させることができる。その場合にカクテルの使用によって測定された信号の強度が増大し、電気的な分子トラップ27の使用によって必要な測定時間が著しく削減される。というのは拡散速度にドリフト速度が重畳されるからである。
【0101】
従って新しい方法と、新しい混合物11並びに新しい装置20によって、容認できる測定時間内に既知および/または未知の配列の個々のヌクレイン酸鎖を証明することが可能になる。
【0102】
後述するように、測定体積25内に発生する熱効果は無視することができる:
導電性σと電場の強さEにおいて散逸するエネルギは、長さlで直径dの毛管が均質な場合には次のようになる。
【数1】

【0103】
Qel=σE2 ld2 π/4
その場合に電気的な熱等価は約0.2cal/Wsとなる。Qelを熱の消散によって液体から除去するためには、定常的な温度勾配dT/drが必要であって、その場合に媒体は次に示すように熱伝導度λを有すると仮定される。
【数2】

【0104】
0.2σE2 ld2 π/4=λldπ・dT/dr
あるいは、
【数3】

【0105】
dT/dr=σE2 ・d/λ・20
水に関するλが10のマイナス3乗cal/(cm度秒)と仮定し、その場合にσ<10マイナス3乗シーメンスでE=10ボルト/cmである代表的な例においては、毛管が0.1cmの直径を有する場合には、0.5度/cmより小さい温度勾配が得られる。従って、主要な熱停滞が水中で行われ、毛管壁では行われないと仮定して、血清を過度に希釈せずに直接調査することができる。
【0106】
同様なことがラジアルの分子トラップ27についても観察される。ネーエル毛管29の電極尖端の領域で場の強さは10マイナス5乗ボルト/cmであるので、μmの領域では10の5乗度/cmの温度勾配が発生するが、これはマイクロメータの領域の10度の過熱に相当する。
【0107】
最後に述べておきたいことは、何回も述べたWO94/16313からすでに一般的な形で知られているように、2つまたは多数の蛍光色素を使用して、クロス相関を実施することによって、測定方法の感度をさらに上昇させることが可能であることである。
【図面の簡単な説明】
【0108】
【図1】対象配列とプライマーとからなる温置溶液の簡略化した概略図である。
【図2】高周波、非均質の電気的交流場を使用する、寸法を無視して記載された電気的な分子沈澱装置を有する光学分析装置を簡略化して示す概略図である。
【符号の説明】
【0109】
10 対象配列
11 混合物
12,13,14 プライマー
15 温置溶液
16 色素分子
17 アンチセンス鎖
21 FCS装置
22 レーザ
23 ビームスプリッター
24 イメージ光学系
25 測定体積
26 光電検出器
27 分子トラップ
28 環状電極
29 ネーエル毛管
30 電圧
31 交流電圧
【特許請求の範囲】
【請求項1】
調査溶液内で所定の対象配列(10)の少数の、好ましくは個々のヌクレイン酸鎖を直接証明する方法であって、次のステップを有する、すなわち、
1)証明すべきヌクレイン酸鎖の少なくともいくつかを、多数の色素分子(16)でマークされ、かつ対象配列(10)全体またはほぼ全体に対して相補的であるそれぞれ長いアンチセンス鎖(17)でハイブリッド化し、かつ、
2)アンチセンス鎖(17)がハイブリッド化されている、証明すべきヌクレイン酸鎖の少数、好ましくは1つを判別するように構成されている光学分析用の装置(20)によって対象配列(10)を同定する、
ヌクレイン酸鎖を直接証明する方法。
【請求項2】
前記ステップ1)において、証明すべきヌクレイン酸鎖とアンチセンス鎖(17)間のハイブリッド化が、色素でマークされたヌクレイン酸(または類似の)構成要素を使用する場合に、証明すべきヌクレイン酸鎖を証明すべきヌクレイン酸鎖とアンチセンス鎖(17)からなる2本鎖に直接重合化することによって行われることを特徴とする、請求項1に記載の方法。
【請求項1】
調査溶液内で所定の対象配列(10)の少数の、好ましくは個々のヌクレイン酸鎖を直接証明する方法であって、次のステップを有する、すなわち、
1)証明すべきヌクレイン酸鎖の少なくともいくつかを、多数の色素分子(16)でマークされ、かつ対象配列(10)全体またはほぼ全体に対して相補的であるそれぞれ長いアンチセンス鎖(17)でハイブリッド化し、かつ、
2)アンチセンス鎖(17)がハイブリッド化されている、証明すべきヌクレイン酸鎖の少数、好ましくは1つを判別するように構成されている光学分析用の装置(20)によって対象配列(10)を同定する、
ヌクレイン酸鎖を直接証明する方法。
【請求項2】
前記ステップ1)において、証明すべきヌクレイン酸鎖とアンチセンス鎖(17)間のハイブリッド化が、色素でマークされたヌクレイン酸(または類似の)構成要素を使用する場合に、証明すべきヌクレイン酸鎖を証明すべきヌクレイン酸鎖とアンチセンス鎖(17)からなる2本鎖に直接重合化することによって行われることを特徴とする、請求項1に記載の方法。
【図1】


【図2】




【図2】


【公開番号】特開2009−39131(P2009−39131A)
【公開日】平成21年2月26日(2009.2.26)
【国際特許分類】
【出願番号】特願2008−260476(P2008−260476)
【出願日】平成20年10月7日(2008.10.7)
【分割の表示】特願平7−348201の分割
【原出願日】平成7年12月19日(1995.12.19)
【出願人】(597142114)エボテク バイオシステム ゲーエムベーハー (1)
【Fターム(参考)】
【公開日】平成21年2月26日(2009.2.26)
【国際特許分類】
【出願日】平成20年10月7日(2008.10.7)
【分割の表示】特願平7−348201の分割
【原出願日】平成7年12月19日(1995.12.19)
【出願人】(597142114)エボテク バイオシステム ゲーエムベーハー (1)
【Fターム(参考)】
[ Back to top ]

