少量の体液試料中のマーカーを判定する方法
本発明は、少量の体液試料中のマーカーを検出する方法に関し、当該方法は:複数の機能領域(3、4、5、6、7)を有する流動試験要素(flow test element)を提供する工程であり、当該複数の機能領域(3、4、5、6、7)が、少なくとも部分的には流体により連結しており、そして適用領域(3)及び当該適用領域(3)と連結し、かつ体液及び/又は当該体液中の成分中のマーカーを検出するように設定された試験領域(5)を有する、当該工程;少量の液体試料を前記流動試験要素の試料適用領域(3)に適用する工程;適正な試験の進行(correct test performance)を判定する工程であり、ここで、当該適正な試験の進行を判定する工程が、1つ以上の機能領域(3、4、5、6、7)において1つ以上の光学的パラメーターを測定する工程、当該測定された1つ以上の光学的パラメーターと、1つ以上の機能領域(3、4、5、6、7)に割り当てられた所定の光学的パラメーターとを比較する工程、そして前記適正な試験の進行が判定された場合、前記試験領域(5)を読み取ることにより、前記液体試料中のマーカーを判定する工程を含む、当該工程;を含む。また、流動試験要素において適正な試験の進行を判定する方法も、提供される。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、少量の体液試料中のマーカーを判定する方法に関する。
【背景技術】
【0002】
発明の背景
そのような方法は、少量の体液中の1つ以上のマーカーの存在を迅速に判定するのに使用される。公知の方法及び装置は、例えば、以下の文献に開示されている: WO 2004/033101 A1、WO 2007/000048 A1、及びWO 2009/14360 A1。
【0003】
WO 2007/000048 A1は、全血からマーカーを同定するのに有用な、少量の流体から1つ以上のマーカーを検出するのに使用される3つ以上の多孔質の膜を有するポイントオブケア装置を記載する。当該アレイは、以下:赤血球細胞の遅延剤(retardant)であって、検出試薬を含有する第一工程膜、及び前記第一工程膜と比較して試料の溶血が最小となる更なる赤血球細胞の遅延剤である、多孔性の第二工程膜、及び第二工程膜と比較して多孔性が低く、捕捉プローブを含有する、第三工程膜を有する。
【0004】
文献US 2005/0244986 A1は、妊娠検査等に有用な分析試験装置を開示する。操作において、液体試料が、試験装置の下端に適用される。試験装置上に、機能領域が提供される。円形の領域は対照として作用し得て、適用された液体試料が判定されるべき解析対象を含有するか否かに関わらず、発色シグナルをもたらす。解析対象の検出は、もう一つの円形の領域で行われる。使用者は、2つの領域中に生じたシグナルを比較することにより、適用された液体試料中に解析対象が存在するか否かを判定できる。
【0005】
文献WO 2007/149043 A1は、抗原に結合可能で、標識を含有する、検出コンジュゲートを使用して、液体試料に対してアッセイを実施する、アッセイ装置を開示する。
【0006】
文献US 2009/0253119 A1は、試験ストリップを含み、細胞や体液を含有する試料等の試料中の解析対象を検出及び定量するための、側方流動アッセイ及びシステムに関する。
【0007】
文献EP 1 975 619 A1は、第一の血液細胞分離メンバー、第二の血液細胞分離メンバー、及びクロマトグラフィー担体を、上流から試料を展開する方向にこの順序で配列されて有する、クロマトグラフィー試験装置を提供する。
【発明の概要】
【課題を解決するための手段】
【0008】
発明の概要
本発明の目的は、少量の体液試料中のマーカーを判定する改良された方法を提供することであり、ここで、当該マーカーの判定に使用される流動試験要素(flow test element)の不適正な使用が回避される。
【0009】
この目的は、請求項1に記載の少量の体液試料中のマーカーを判定する方法により解決される。更に、請求項1に記載の試験流動要素における適正な試験の進行(correct test performance)を判定する方法が提供される。本発明の有利な発達は、従属項に開示されている。
【0010】
光学的判定の過程で、吸光度、蛍光、反射、緩和(remission)及び透過から選択される1つ以上の分光的パラメーターが測定され得る。
【0011】
前記流動試験要素上の1つ以上の機能領域には、2つ以上の機能サブ領域が提供されてもよい。例えば、複数の試験サブ領域が、1つの流動試験要素上に位置してもよい。
【0012】
例えば、適正な試験の進行を判定することにより、液体試料が、その液体試料のために設定されていない流動試験要素に適用されるのを回避する。当該流動試験要素は、体液及び/又は体液の成分のために設計されてもよい。本明細書中で使用されるとき、「成分」という用語は、後から体液に添加される物質とは区別される。添加された物質も、混合物、又は混合された物質等と称されてもよい。体液の場合、そのような物質は、例えば、それが患者から回収された後に体液に添加されてもよく、例えば抗体が添加され得る。対照的に、ここで規定される成分は、体液自体の部分である。全血試料の成分の例は、血清及び血漿である。
【0013】
例えば、もし液体試料が、その液体試料のために設定されていない流動試験要素に適用されると、誤った結果がもたらされ得る。提案される方法は、液体試料中のマーカーの判定が正しく実施されることを保証する。なぜならば、使用者に適正な試験の進行が提供されているか否か、例えば正しい液体が流動試験要素にアプライされたか否か等の情報を与える、適正な試験の進行を判定する工程が存在するからである。
【0014】
好ましくは、試験領域の読み取りによる液体試料中のマーカーの判定は、1つ以上の試験波長を用いた光学的試験により実施される。好ましい態様において、適正な試験の進行を判定する工程は、試験波長と異なる1つ以上の波長を用いた光学的判定により実施される。例えば、蛍光及び/又は吸収は超は、試験波長と異なるものが選択される。
【0015】
本明細書中で使用されるとき、「流体により連結」とは、流体、例えば試料が、本発明の装置の1つの区画又は部分から本質的に障害無く移動することを意味する。そのような特徴は、好ましくは、液体試料の実際の存在から独立している。
【0016】
適正な試験の進行、特に適正な試料の使用を判定する工程は、1回目の判定の後、1回、又は数回、流動試験要素への試料の液体の適用と、マーカーの判定との間の時間に、反復されてもよい。マーカーの判定の後であっても、好ましくは判定の追加工程として、適正な試験の進行の試験が実施されてもよい。当該工程は、適正な試験の進行、特に1つ以上の機能領域における適正な試料の使用を判定する目的で実施されてもよい。
【0017】
適正な試験の進行を判定する工程は、適用された液体の一部が機能領域に到達した後に、当該機能領域の1つで実施されてもよい。この場合、当該1つの機能領域において測定された1つ以上の光学的パラメーターが、当該1つの機能領域に割り当てられた1つ以上の所定の光学的パラメーターと比較される。
【0018】
一般に、本明細書中で使用されるとき、「1つの機能領域において測定」とは、1つの機能領域を特徴付けるためにパラメーターが測定されたことを意味する。当該1つの機能領域の内側の箇所、及び/又は当該1つの機能領域の外側に位置する箇所で、光学的測定が実施される。
【0019】
1つの試験領域又は複数の試験サブ領域が、1つ以上のマーカーの判定のために設定されてもよい。提供される方法により判定され得るマーカーの例は、以下に記載されている。
【0020】
プロカルシトニン(PCT)は、敗血症の診断のための周知のバイオマーカーとされている。PCTは、細菌感染の重症度を反映し、特に、感染の進行が、敗血症、重症の敗血症、又は敗血性ショックに至ることをモニタリングするのに使用される。PCTを、全身的な炎症応答の活性の測定、治療の成功の調整、及び予後の推定に使用することができる(Assicot M et al.: Lancet 1993, 341 :515-8; Clec'h C et al: Diagnostic and prognostic value of procalcitonin in patients with septic shock. Crit Care Med 2004;32:1166-9; Lee YJ et al, Yonsei Med J 2004, 45, 29-37; Meisner M Curr Opin Crit Care 2005, 11, 473-480; Wunder C et al. Inflamm Res 2004, 53, 158-163)。敗血症患者におけるPCTレベルの増大は、死亡率と相関する(Oberhoffer M et al. Clin Chem Lab Med 1999;37:363-368)。
【0021】
アドレノメデュリン(ADM)ペプチドは、ヒト褐色細胞腫から分離された52アミノ酸を含む新規血圧降下ペプチドとして1993年に初めて記載された(Kitamura et al. (1993), Bio-chem. Biophys. Res. Commun. 192:553-560)。同年、185アミノ酸を含む前駆ペプチドをコードするcDNA及びこの前駆ペプチドの全アミノ酸配列も記載された(Kitamura et al. (1993), Biochem. Biophys. Res. Commun. 194:720-725)。特にN末端に21アミノ酸のシグナル配列を含む前駆ペプチドは、「プレプロアドレノメデュリン」(プレプロADM)と称される。当該ADMペプチドは、プレプロADMの95〜146アミノ酸を含み、そこでタンパク質開裂が起こることにより形成される。プレプロADMの開裂において形成される幾つかのペプチド断片、特に、生理的に活性のアドレノメデュリン(ADM)ペプチド及び「PAMP」、プレプロADMのシグナルペプチドの21アミノ酸に続いて20アミノ酸(22〜41)を有するペプチドは、詳細に特定されている。機能が不明で体外での高度の安定性を有する他のフラグメントとして、中部プロアドレノメデュリン(MR-proADM) (Struck et al. (2004), Peptides 25(8): 1369-72)があり、これを利用した信頼できる定量法が開発されている(Morgenthaler et al. (2005), Clin. Chem. 51(10):1823-9)。ADMは、効果的な血管拡張剤である。
【0022】
降圧降下は、特に、ADMのC末端部分のペプチド断片と関連していた。一方、ADMのN末端のペプチド配列は、昇圧降下を呈した(Kitamura et al. (2001), Peptides 22, 1713-1718)。
【0023】
エンドセリン(ET)-1は、強力な内皮由来の内在性血管収縮因子である(Yanagisawa M, Kurihara H, Kimura S, Goto, Masaki T, J Hypertens Suppl 1988; 6:S 188-91.)。ET-1は、平滑筋に存在するET(A)及びET(B)を活性化して細胞内のカルシウムの増大を引き起こすことにより血管に対する作用をもたらす(Yanagisawa et al, J Hypertens Suppl 1988;6:S188-91)。成熟エンドセリン-1は、プロエンドセリン-1というより大きな前駆体から生じる。プロエンドセリン1は、文献(Struck J, Morgenthaler NG, Bergmann Peptides. 2005 Dec;26(12):2482-6.)に記載されるように、タンパク質分解により複数の断片にプロセシングされる。これらの断片は、血液循環中でタンパク質分解に供され、当該分解は、断片の種類、並びに当該循環中に存在するプロテアーゼの種類及び濃度/活性に依存して、迅速に又は緩慢に行われる。これらの断片の一例として、C末端プロエンドセリン1(CT-proET-1)が挙げられ、これは、サンドイッチ免疫アッセイにより測定可能である(Papassotiriou J, Morgenthaler NG, Struck J, Alonso C, Bergmann A. Clin Chem. 2006 Jun;52(6): 1144-51.)。
【0024】
B型ナトリウム利尿ペプチド(BNP)は、心不全の定量マーカーである。B型ナトリウム利尿ペプチド(BNP)及びそのアミノ末端断片であるN末端プロB方ナトリウム利尿ペプチド(NT-proBNP)は、EDにおける診断精度を顕著に増大させ[Januzzi, J.L., Jr., et al., Am J Cardiol, 2005. 95(8): p. 948-54; Maisel, A.S., et al., N Engl J Med, 2002. 347(3): p. 161-7]ることにより、患者の評価及び処置を改善する[Moe, G.W., et al., Circulation, 2007. 115(24): p. 3103-10; 8.Mueller, C, et al., N Engl J Med, 2004. 350(7): p. 647-54.]。循環中の心房性ナトリウム利尿ペプチドの濃度は、BNPの約50〜100倍高い[Pandey, K.N., Peptides, 2005. 26(6): p. 901-32]。故に、ANPの増大に反映される生物学的シグナルは、病態生理学的に、かつ診断的に、BNPのシグナルよりも重要である。しかしながら、APN及びその前駆体の診断的性能については殆ど知られていない[Cowie, M.R., et al., Lancet, 1997. 350(9088): p. 1349-53]。成熟ANPは、循環中で、成熟ペプチドよりも顕著に安定であるためより妥当な解析対象と考えられる前駆N末端プロANP(NT-proANP)に由来する[Vesely, D.L., IUBMB Life, 2002. 53(3): p. 153- Pandey, K.N., Peptides, 2005. 26(6): p. 901-32]。
【0025】
心房性ナトリウム利尿ペプチド(ANP)は、ナトリウム利尿ペプチドのメンバーであり、利尿及びナトリウム利尿、並びに動脈の血圧(BP)の低下等の幾つかの生理的パラメーターを制御する。ANPは大半が心臓の心房で生産され、循環中のナトリウム利尿ペプチドの98%を占める(Vesely DL.Life 2002;53:153-159)。ANPは、循環中で成熟ペプチドよりも顕著に安定な前駆プロホルモンの開裂により生じる。前駆ホルモンの中部断片(NT-proANPの53〜90アミノ酸)は、中部プロANP(MR-proANP)といい、従来の免疫アッセイで使用されるプロANPのN又はC末端のエピトープと異なり、エキソプロテアーゼによる分解に比較的耐性である.(Morgenthaler NG et al. Clin Chem 2004;50:234-236; Gerszten RE et al. Am J Physiol Lung Cell Mol Physiol 2008)。
【0026】
ミオグロブリンは、153アミノ酸の単鎖球状タンパク質で、中心部にヘム(鉄含有ポルフィリン)補欠分子族を含有し、その周りがアポタンパク質で覆われている。ミオグロブリンは、筋肉の創傷の高精度のマーカーであり、胸部の疼痛を有する患者の心臓発作における潜在的なマーカーである(M. Weber, M. Rau, K. Madlener, A. Elsaesser, D. Bankovic, V. Mitrovic and C. Hamm (2005) Clinical Biochemistry 38: 1027)。C-MB及び心臓トロポニンT(cTnT)は、ECGと組み合わせて使用され急性心筋梗塞(AMI)を診断する臨床的サインである。心臓トロポニンは、3つのサブユニットT (cTcT)、I(cTcI)及びCからなるタンパク質複合体であり、T及びIは心筋組織にのみ局在しており、診断用マーカーとして使用される(Rottbauer W et al., Eur Heart J 1996; 17:3-8)。
【0027】
アルギニンバソプレシン(AVP)は、バソプレシン、アルギプレシン又は抗利尿ホルモン(ADH)としても知られ、ヒトを含む大半の哺乳類において見出されているホルモンである(Caldwell HK, Young WS III (2006) in Lajtha A, Lim R. Handbook of Neurochemistry and Molecular Neurobiology: Neuro-active Proteins and Peptides (3rd edition ed.). Berlin: Springer, pp. 573-607. ISBN 0-387-30348-0)。バソプレシンはペプチドホルモンである。視床下部で合成され、下垂体後葉の小胞で保存されるプレプロホルモン前駆体から形成される。バソプレシンの放出の低下、又はバソプレシンに対する腎臓の感受性の低下は、高ナトリウム血(血中ナトリウム濃度の増大)、多尿症(過剰な尿生産)、及び多渇症(のどの渇き)を特徴とする、尿崩症を引き起こす。
【0028】
本明細書中で使用されるとき、「マーカーの判定」等の用語は、試料中のマーカーの存否、及び/又はその量の定量、及び/又はその濃度を検出することを含む。故に、存否は、マーカーの検出可能な存在量、即ち本アッセイの検出限界を考慮して理解されるべきである。
【0029】
「マーカー」は、生理的又は病理的指標となる物質である。それらは、例えば、心臓組織の劣化により循環中に心筋細胞から放出されるタンパク質である心臓系の解析対象、予後の指標となるホルモン、糖尿病の症状をモニタリングするのに用いられるグルコース、及び感染により生じる様々なタンパク質及び毒素である。
【0030】
幾つかの態様において、マーカーは、本発明のアレイ、装置、方法及び使用により検出及び/又は定量されるべき、タンパク質又はペプチドである。12アミノ酸以上、好ましくは15アミノ酸以上の長さの前記タンパク質又はペプチドの断片も含まれる。本発明に係るそのようなタンパク質又はペプチドの具体例として、ミオグロビン、トロポニンT(cTnT)及びI(cTnI)、クレアチンキナーゼMB(CK-MB)、FABP、GDF-15、ST-2、プロカルシトニン(PCT)、C-反応性タンパク質(CRB)、プロアドレノメデュリン及びその断片、例えば中部プロアドレノメデュリン(MR-proADM)、アドレノメデュリン、PAMP、C末端プロアドレノメデュリン(CT-proADM)、プロエンドセリン1及びその断片、例えばC末端プロエンドセリン1(CT-proET-1)、大エンドセリン1、エンドセリン1、NT-プロエンドセリン1、プロANP及びその断片、例えば中部プロ心房性利尿ペプチド(MR-proANP)、N末端プロANP(NT-proANP)、ANP、プロバソプレシン及びその断片、例えばC末端プロアルギニンバソプレシンペプチド(CT-proAVP、「コペプチン」)、バソプレシン、ニューロフィシンII、プロBNP及びN末端プロBNP(NT-proBNP)等の、心臓血管事象の診断及び/又は予後診断に関連するマーカーである。
【0031】
本明細書中に記載されるマーカータンパク質及び/又はペプチドが、当該タンパク質のマーカータンパク質及び/又はペプチドの、12アミノ酸以上、好ましくは15アミノ酸以上の長さの断片が、マーカーとして想定されることを理解されたい。
【0032】
更に、ヒト絨毛性ゴナドトロピン(hCG)及び黄体形成ホルモン(LH)等の妊娠又は排卵に関連するホルモンも、本方法又はその様々な態様において検出され得る。癌等の疾患に対する他の抗原、特に前立腺癌抗原(前立腺血清抗原、PSA)が、本発明を使用して検出され得ることも、本発明の範囲内である。本発明の更なる応用として、肝炎、細菌及び真菌感染、例えば消化管の潰瘍におけるヘリコバクター・ピロリ(Helicobacter pylori)、バチルス・アントラキス(Bacillus anthracis)、ペディクルス・ヒューマニス(Pediculus humanis)、シフォナプテラ(Siphonaptera)及びグラム陽性細菌、例えばストレプトコッカス・パイオニエス(Streptococcus pyognes)、ストレプトコッカス・ニューモニアエ(Streptococcus pneumoniae)及びストレプトコッカス・ファエカリ(Streptococcus faecalis)等に関連するマーカーの認識が含まれ、これらは全て非限定的な例示である。また、本発明は、薬物の乱用を含む薬物の検出にも有用であり得る。血中グルコースのレベルを判定するもの等の酵素アッセイも、本発明に想定される。当該装置の使用が、これらの特定のマーカー、又は全血に限定されず、例えば上記で示したような他の解析手順に等しく応用可能であることを認識されたい。
【0033】
好ましい態様において、適正な試験の進行を判定する工程は、適用された液体試料が体液であるか若しくは体液の成分であるか、又は試験流動要素が体液若しくは体液の成分中のマーカーを判定するために設定されたものであるかを光学的に判定することにより、適正な試料の使用を判定する工程を含む。
【0034】
好ましい態様において、本発明は、更に、少量の全血試料を適用し、そして当該全血試料が溶血しているか否かを光学的に判定する工程を含む。好ましい態様において、前記光学的判定は、流動試験要素上の興味のある領域内に照射された光の緩和シグナルを測定する工程を含む。測定された緩和シグナルは、血液が溶血したか否かを判定するための参照シグナルと比較され得る。本明細書中で使用されるとき、「全血試料」とは、未処理又は本質的に未処理の血液試料を特定する。
【0035】
他の好ましい態様において、前記測定の工程は、試験領域及び対照領域と流体により連結され、そしてそれらの間に位置する領域を光学的に測定する工程を含む。この場合に調査される領域は試験領域の下流に位置するので、当該光学的測定は、既に試験領域に浸入した液体試料の一部についての情報を提供する。
【0036】
好ましい態様において、流動試験要素を提供する工程は、適用領域及び試験領域の間に位置し、それらと流体により連結された橋領域、並びに試験領域の上流にあってこれと流体により連結された対照領域を有する、流動試験要素を提供する工程を含む。当該橋領域は、適用領域及び試験領域と流体により連結された橋膜(bridge membrane)により適用され得る。当該橋膜の平均の孔の寸法は、8.0μm±2μmであり、血漿又は血清のキャピラリーフローは、2cmを30秒以内、及び/又は4cmを180秒以内で移動し、ここで、当該橋膜中の血清又は血漿のキャピラリーフローは、第一の多孔質膜よりも低く、そして試験領域よりも高い。また、当該試験領域及び対照領域は、1つ以上の膜により実行され得る。好ましくは、当該膜は、多孔質材料により形成され得る。
【0037】
更なる態様において、適正な試験の進行を判定する工程は、適用領域、橋領域、検出領域及び対照領域から選択される機能領域の1つ以上で光学的測定が行われる工程を含む。
【0038】
更なる態様において、適正な試験の進行を判定する工程は、複数の機能領域の外側に位置する流動試験要素の領域を光学的に測定する工程を含む。そのような測定は、機能領域の1つの中での測定の代わりに、又はこれに加えて実施されてもよい。例えば、前記光学的測定は、2つの機能領域の間に位置する流動試験要素の領域において実施されてもよい。機能領域の1つにおける適正な液体に関する光学的測定は、興味のある機能領域の上流及び/又は下流に位置する領域において行われる。
【0039】
好ましい態様において、本方法は、更に、少量の全血試料を適用し、流動試験要素上の興味のある領域への赤血球の浸入を光学的に判定する工程を含む。例えばマーカーが全血試料中に検出される場合、通常、試験領域自体に赤血球が浸入するは避けられるべきである。上記態様により、そのような浸入が起こったか否かをチェックすることができる。適正な試験の進行を判定する工程でそのような浸入が起こったことが示されたとき、当該工程は、そのような状況で取得された測定結果が適正でないことを使用者に伝える。
【0040】
更なる態様において、適正な試験の進行を判定する工程は、異なる時点で複数の光学的測定を実施する工程を含む。当該複数の光学的測定は、流動試験要素上の興味のある単一の又は複数の領域で実施されうる。
【0041】
他の態様において、マーカーを判定する工程は、液体試料中のマーカーの存在を判定し、当該液体試料中のマーカーの濃度を判定する、1つ以上の工程を含む。
【0042】
尚も他の好ましい態様において、適正な試験の進行を判定する工程において、適用された液体試料が、全血試料、血清試料、血漿試料、尿試料、脳脊髄液試料、便試料、唾液試料及びリンパ液試料から選択される、体液又は体液の成分であるか否かを光学的に判定する工程を含む。
【0043】
本発明の他の態様において、流動試験要素において適正な試験の進行を判定する方法が提供され、当該方法は
-複数の機能領域を有する流動試験要素を提供する工程であり、当該複数の機能領域が、少なくとも部分的には流体により連結しており、そして適用領域、及び当該適用領域と流体により連結し、かつ体液及び/又は当該体液中の成分中のマーカーを検出するように設定された試験領域を有する、当該工程;
・少量の液体試料を前記流動試験要素の試料適用領域に適用する工程;
・適正な試験の進行を判定する工程であり、ここで、当該適正な試験の進行を判定する工程が、前記機能領域において1つ以上の光学的パラメーターを測定する工程、及び当該測定された1つ以上の光学的パラメーターと、1つ以上の機能領域に割り当てられた所定の光学的パラメーターとを比較する工程;
を含む当該工程;
を含む。
【0044】
前記適正な試験の進行を判定する工程において、不適正な試験の進行が検出された場合、解析システムの更なる解析が中断されてもよい。例えば、当該解析システムは、液体試料が適用された流動試験要素の更なる使用をブロックする。好ましい態様において、当該解析システムの使用者に、警告シグナルが提示される。当該警告シグナルは、音響信号及び映像信号の1つ以上を含み得る。
【0045】
発明の好ましい態様の説明
以下で、様々な態様を参照した例示を用いて、本発明を更に詳細に記載する。
【図面の簡単な説明】
【0046】
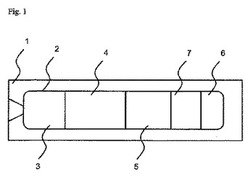
【図1】図1は、流動試験要素を上から見た模式図を示す。
【0047】
【図2】図2は、様々な時間インキュベーションした全血試料を適用した試験流動要素上の測定位置(相対的単位)と、分光緩和シグナル(相対的単位)との関連性を示す。
【実施例】
【0048】
以下の実施例は例示のみを目的として記載され、本発明の範囲の限定を意図しない。同等のものへの変更又は置換は、状況に応じて想定される。本明細書で特定の用語が採用されているが、それらは、記述的な意味で使用されており、限定を目的としない。
【0049】
図1は、上から見た流動試験要素の模式図である。ポイントオブケア装置ともいう当該流動試験要素は、複数の機能領域が配置された膜体2を有する装置体1を含む。それらの機能領域は、流体により連結されており、適用領域3、橋領域4、試験領域5、及び対照領域6を有する。
【0050】
「ポイントオブケア(POC)」試験は、患者をケアする場所又はその付近で実施される何らかの診断試験として定義される(Kost, Goals, guidelines and principles for point-of-care testing. In: ost GJ, ed. Principles and practice of point-of-care testing. Philadelphia: Lippincott Williams and Wilkins. 2002, Chapter 1, pp 3-12)。患者のより近くで解析を行うことにより、幾つかのプロセス段階が省略され、結果が出るまでの時間の短縮及びその結果に応じた迅速な管理がなされる。POC試験の長所は、迅速な回転時間(turn-around-time、TAT)、迅速な医学的決定、試料の長距離移動の回避及び必要とされる検体の体積の縮小である(Heinschink et al., Point-of-care testing. Laboratoriums Medizin 2002. 26 (1-2): 61-67.)。
【0051】
適用領域3は、少量の体液を受容し、それが、少なくとも部分的に、膜体2に流れ込み、やがてそれぞれ試験領域5及び対照領域6に至るように設定されている。本明細書中で使用されるとき、「試料適用領域」という用語は、試料が例えば試料内に試料適用領域が浸漬され、又はシリンジ若しくはピペット等の試料輸送手段を用いて試料を適用すること等により、試料が適用される、装置上の部分を特定する。当該試料適用領域は、ゆえに、試料がそれを通って第一の多孔質材料に適用されるようなポケット又は切り込み(indentation)の形態であってもよい、装置中の開口である。
【0052】
前記流れは、適用領域3及び対照領域5との間に形成される試料流動チャンネルに沿って起こる。膜体2には、1つ以上の膜要素が設けられてもよく、一つの態様において膜が重ねられる。多孔質膜材料により提供される流動チャンネルは、キャピラリーフローを起こす特徴を有する。
【0053】
1つの態様において、試験領域4は、全血試料中のマーカーの存在を判定するように設定されている。流動試験要素は、下記のように使用され得る。
【0054】
明らかなように、適用領域3の内側及び/又はこれに隣接して設けられた第一の多孔質材料と接触すると、適用された試料の赤血球細胞は、血漿から分離し始め、その流れの過程で、マーカーは検出試薬と出会う。当該検出試薬は、限定されないが、典型的には、当該マーカーのエピトープに対する標識された抗体であり、マーカー-検出試薬複合体を形成する。記載された態様において、マーカー-検出試薬複合体は、橋膜を有する橋領域4に移動し、そこで、赤血球細胞の移動は、更に、阻害/遅延させられる。そして、マーカー-検出試薬複合体は、試験膜を有する試験領域5に達し、不動化された捕捉プローブ、限定されないが、典型的には、マーカーの別個のエピとー部又は検出試薬のエピトープに対する抗体と出会う。マーカー-検出試薬複合体と不動化された捕捉プローブとの反応は、裸眼又は適切な装置を用いて認識できる、濃縮された捕捉スポットを形成する。任意の対照領域6は、試験領域5の捕捉スポットの下流に位置し、対照試薬を含有する。好ましい態様において、対照試薬は、抗動物IgGであってもよい。あるいは、対照領域6の代わりに、試験装置の膜の上を覆う透明なカバーテープの長さの違いは、試験膜の末端に試料が到達したとき、当該試料を、迅速に検出が可能なシグナルを明らかにする調整された様式で蒸発させることができる。
【0055】
液体試料中の1つのマーカー、又は複数のマーカーを一度に検出することは、本発明の範囲内である。故に、1つ以上の検出試薬及び/又は1つ以上の捕捉プローブが、本発明のポイントオブケア装置に蓄積され得ることは、当業者により認識され得ることである。
【0056】
原則として、本アッセイ、即ち検出試薬とマーカーの検出に使用される捕捉プローブとの組合せは、診断の分野において採用されるいずれの形式に基づいてもよい。当該アッセイは、非競合的アッセイ、即ちサンドイッチアッセイ、又は競合的アッセイであってもよい(The Immunoassay Handbook, Ed. David Wild, Elsevier LTD, Oxford; 3rd ed. (May 2005), ISBN-13: 978-0080445267; Hultschig C et al., Curr Opin Chem Biol. 2006 Feb;10(l):4-10. PMID: 16376134)。
【0057】
本明細書中で使用されるとき、捕捉プローブは、核酸分子、糖質分子、PNA分子、アプタマー、タンパク質、抗体、ペプチド又は糖タンパク質から成る群から選択されてもよく、好ましくは抗体である。
【0058】
当業者が利用可能な試験装置における捕捉プローブ及び対応する検出システムの標識として、様々なものを利用することが出来る。限定されないが、公知の標識、例えば金属、蛍光、電子化学発光、及び酵素標識が挙げられる。金属標識は顕著な高感度を有するため、特に好ましい。金属の中でも、金は、この種類の反応に広く使用されており、そしてその特性が良く理解されているので、最も好ましい。
【0059】
幾つかの態様において、前記第一の多孔質材料は、全血試料中で判定されるべきマーカーに結合する、抗体-金粒子コンジュゲートを含有する。従って、抗体-金粒子コンジュゲートが第一の多孔質材料中に存在し、そして当該抗体-金粒子コンジュゲートが試料と接触して当該試料中に懸濁し、そして当該試料と共に移動する。故に、当該抗体-金粒子コンジュゲートは、前記第一の多孔質材料中に不可逆的に不動化されていなくてもよい。しかしながら、試料との結合の後に転換し得る、例えば加水分解を受ける、前記第一の多孔質材料上の抗体-金粒子コンジュゲートの不動化が、幾つかの態様において想定されてもよい。
【0060】
採用される金標識抗体の好ましいサイズは、約20〜60nmであるが、マーカーの臨床的カットオフや反応物の親和性等の周知の要素に依存して、かなりのバリエーションが許容される。加えて、金シグナルは、可視産物を沈殿させる還元性銀塩を使用することにより、容易に可視化を促進できる。典型的な反応性塩は乳酸銀で、これは還元性銀イオンの供給源とされ、還元剤としてヒドロキノンが採用される。金属銀は、金の各粒子の周囲に容易に認識できる黒色の沈着物を形成する。あるいは、ホースラディッシュペルオキシダーゼ等の抗体標識が採用される場合、当該反応は、標準的な手順に従い、過酸化水素やCISオルソフェニレンジアミン等の色素を添加することにより検出され得る。より強いマーカー検出感度を有する米国特許6,046,585(その全体を本明細書中に参照により援用する)に記載のような常磁性標識等の追加の標識も、本発明の範囲内で使用され得る。
【0061】
本出願の文脈において、「検出試薬」は、材料であり、しばしば液体試料中の検出されるべきマーカーに対する抗体である。幾つかの態様において、当該検出試薬は、液体試料を適用する地点、又はその下流の第一の多孔質材料担体に放出可能に結合している。最も免疫化学的な解析において、当該検出試薬は、コロイド金等の検出可能な標識で標識され、検出されるべきマーカーと複合体を形成する。
【0062】
橋膜の血清のキャピラリーフローの文脈において、「水平変化」という用語は、血清の流動の方向における流速の変化を指す。
【0063】
本明細書中で使用されるとき、「血球細胞からの血清の分離」とは、血球細胞を特に保持しつつ、血清を前記装置の隣接する区画又は部分、例えば次の膜に透過させることを意味する。従って、好ましくは95%以上、より好ましくは99%以上、なおもより好ましくは99.5%以上、最も好ましくはほぼ100% の赤血球細胞が保持される。
【0064】
上記非限定的態様を参照して記載される体液中のマーカーの存在を判定する方法は、適正な試料の使用を判定する工程を含む。当該工程は、(a)分光光度計を用いた測定により行われる。吸光度、蛍光、透過、反射及び緩和を含む群から選択される1つ以上のパラメーターが検出及び解析されて、適用領域3に適用され、流動試験要素上の一定の機能領域に到達した液体試料の一部が、当該流動試験要素が判定の対象とする体液の一つ及び体液の成分であるか否かを判定する。好ましくは、領域6において、適正な試料の使用を判定するための光学的調査が行われる。例えば、試験領域5及び対照領域6の間に位置する領域7は、試験領域5及び/又は対照領域6に達した液体の種類が何であるかを判定するために、光学的に調査される。例えば、光学的パラメーターの緩和が、領域7において解析されてもよい。
【0065】
好ましい態様において、上記方法は、少量の全血試料を適用する工程、及び流動試験要素上の興味のある領域への赤血球の浸入を光学的に判定する工程を含む。例えば全血試料中のマーカーを判定しようとする場合、通常、試験領域5自体への赤血球の浸入は避けるべきである。上記態様により、そのような浸入が起こったか否かをチェックすることができる。適正な試料の使用を判定する工程がそのような浸入が起こったことを示した場合、これは、そのような状況で回収された測定結果が適正ではないことを、使用者に教示する。
【0066】
図2は、様々な時間インキュベーションした全血試料の分光的緩和シグナル(相対的単位)と、流動試験要素1上の相対的位置(相対的単位)との関連性を示す。当該流動試験要素1(図1参照)は、対照領域6、領域7及び試験領域5を少なくともカバーするように、左から右にスキャンされた。左側に、対照領域6の緩和シグナルに割り当てられたいわゆる対照バンドがあり、これは全ての時間で変化が無い。左側の緩和シグナルの増大は、流動試験要素1上の試験領域5への赤血球の浸入を示す。
【0067】
本願明細書、特許請求の範囲及び図面の1つ以上に開示される特徴は、単独で又は複数のものが組み合わされて、様々な態様における本発明の実現の材料となり得る。
【技術分野】
【0001】
本発明は、少量の体液試料中のマーカーを判定する方法に関する。
【背景技術】
【0002】
発明の背景
そのような方法は、少量の体液中の1つ以上のマーカーの存在を迅速に判定するのに使用される。公知の方法及び装置は、例えば、以下の文献に開示されている: WO 2004/033101 A1、WO 2007/000048 A1、及びWO 2009/14360 A1。
【0003】
WO 2007/000048 A1は、全血からマーカーを同定するのに有用な、少量の流体から1つ以上のマーカーを検出するのに使用される3つ以上の多孔質の膜を有するポイントオブケア装置を記載する。当該アレイは、以下:赤血球細胞の遅延剤(retardant)であって、検出試薬を含有する第一工程膜、及び前記第一工程膜と比較して試料の溶血が最小となる更なる赤血球細胞の遅延剤である、多孔性の第二工程膜、及び第二工程膜と比較して多孔性が低く、捕捉プローブを含有する、第三工程膜を有する。
【0004】
文献US 2005/0244986 A1は、妊娠検査等に有用な分析試験装置を開示する。操作において、液体試料が、試験装置の下端に適用される。試験装置上に、機能領域が提供される。円形の領域は対照として作用し得て、適用された液体試料が判定されるべき解析対象を含有するか否かに関わらず、発色シグナルをもたらす。解析対象の検出は、もう一つの円形の領域で行われる。使用者は、2つの領域中に生じたシグナルを比較することにより、適用された液体試料中に解析対象が存在するか否かを判定できる。
【0005】
文献WO 2007/149043 A1は、抗原に結合可能で、標識を含有する、検出コンジュゲートを使用して、液体試料に対してアッセイを実施する、アッセイ装置を開示する。
【0006】
文献US 2009/0253119 A1は、試験ストリップを含み、細胞や体液を含有する試料等の試料中の解析対象を検出及び定量するための、側方流動アッセイ及びシステムに関する。
【0007】
文献EP 1 975 619 A1は、第一の血液細胞分離メンバー、第二の血液細胞分離メンバー、及びクロマトグラフィー担体を、上流から試料を展開する方向にこの順序で配列されて有する、クロマトグラフィー試験装置を提供する。
【発明の概要】
【課題を解決するための手段】
【0008】
発明の概要
本発明の目的は、少量の体液試料中のマーカーを判定する改良された方法を提供することであり、ここで、当該マーカーの判定に使用される流動試験要素(flow test element)の不適正な使用が回避される。
【0009】
この目的は、請求項1に記載の少量の体液試料中のマーカーを判定する方法により解決される。更に、請求項1に記載の試験流動要素における適正な試験の進行(correct test performance)を判定する方法が提供される。本発明の有利な発達は、従属項に開示されている。
【0010】
光学的判定の過程で、吸光度、蛍光、反射、緩和(remission)及び透過から選択される1つ以上の分光的パラメーターが測定され得る。
【0011】
前記流動試験要素上の1つ以上の機能領域には、2つ以上の機能サブ領域が提供されてもよい。例えば、複数の試験サブ領域が、1つの流動試験要素上に位置してもよい。
【0012】
例えば、適正な試験の進行を判定することにより、液体試料が、その液体試料のために設定されていない流動試験要素に適用されるのを回避する。当該流動試験要素は、体液及び/又は体液の成分のために設計されてもよい。本明細書中で使用されるとき、「成分」という用語は、後から体液に添加される物質とは区別される。添加された物質も、混合物、又は混合された物質等と称されてもよい。体液の場合、そのような物質は、例えば、それが患者から回収された後に体液に添加されてもよく、例えば抗体が添加され得る。対照的に、ここで規定される成分は、体液自体の部分である。全血試料の成分の例は、血清及び血漿である。
【0013】
例えば、もし液体試料が、その液体試料のために設定されていない流動試験要素に適用されると、誤った結果がもたらされ得る。提案される方法は、液体試料中のマーカーの判定が正しく実施されることを保証する。なぜならば、使用者に適正な試験の進行が提供されているか否か、例えば正しい液体が流動試験要素にアプライされたか否か等の情報を与える、適正な試験の進行を判定する工程が存在するからである。
【0014】
好ましくは、試験領域の読み取りによる液体試料中のマーカーの判定は、1つ以上の試験波長を用いた光学的試験により実施される。好ましい態様において、適正な試験の進行を判定する工程は、試験波長と異なる1つ以上の波長を用いた光学的判定により実施される。例えば、蛍光及び/又は吸収は超は、試験波長と異なるものが選択される。
【0015】
本明細書中で使用されるとき、「流体により連結」とは、流体、例えば試料が、本発明の装置の1つの区画又は部分から本質的に障害無く移動することを意味する。そのような特徴は、好ましくは、液体試料の実際の存在から独立している。
【0016】
適正な試験の進行、特に適正な試料の使用を判定する工程は、1回目の判定の後、1回、又は数回、流動試験要素への試料の液体の適用と、マーカーの判定との間の時間に、反復されてもよい。マーカーの判定の後であっても、好ましくは判定の追加工程として、適正な試験の進行の試験が実施されてもよい。当該工程は、適正な試験の進行、特に1つ以上の機能領域における適正な試料の使用を判定する目的で実施されてもよい。
【0017】
適正な試験の進行を判定する工程は、適用された液体の一部が機能領域に到達した後に、当該機能領域の1つで実施されてもよい。この場合、当該1つの機能領域において測定された1つ以上の光学的パラメーターが、当該1つの機能領域に割り当てられた1つ以上の所定の光学的パラメーターと比較される。
【0018】
一般に、本明細書中で使用されるとき、「1つの機能領域において測定」とは、1つの機能領域を特徴付けるためにパラメーターが測定されたことを意味する。当該1つの機能領域の内側の箇所、及び/又は当該1つの機能領域の外側に位置する箇所で、光学的測定が実施される。
【0019】
1つの試験領域又は複数の試験サブ領域が、1つ以上のマーカーの判定のために設定されてもよい。提供される方法により判定され得るマーカーの例は、以下に記載されている。
【0020】
プロカルシトニン(PCT)は、敗血症の診断のための周知のバイオマーカーとされている。PCTは、細菌感染の重症度を反映し、特に、感染の進行が、敗血症、重症の敗血症、又は敗血性ショックに至ることをモニタリングするのに使用される。PCTを、全身的な炎症応答の活性の測定、治療の成功の調整、及び予後の推定に使用することができる(Assicot M et al.: Lancet 1993, 341 :515-8; Clec'h C et al: Diagnostic and prognostic value of procalcitonin in patients with septic shock. Crit Care Med 2004;32:1166-9; Lee YJ et al, Yonsei Med J 2004, 45, 29-37; Meisner M Curr Opin Crit Care 2005, 11, 473-480; Wunder C et al. Inflamm Res 2004, 53, 158-163)。敗血症患者におけるPCTレベルの増大は、死亡率と相関する(Oberhoffer M et al. Clin Chem Lab Med 1999;37:363-368)。
【0021】
アドレノメデュリン(ADM)ペプチドは、ヒト褐色細胞腫から分離された52アミノ酸を含む新規血圧降下ペプチドとして1993年に初めて記載された(Kitamura et al. (1993), Bio-chem. Biophys. Res. Commun. 192:553-560)。同年、185アミノ酸を含む前駆ペプチドをコードするcDNA及びこの前駆ペプチドの全アミノ酸配列も記載された(Kitamura et al. (1993), Biochem. Biophys. Res. Commun. 194:720-725)。特にN末端に21アミノ酸のシグナル配列を含む前駆ペプチドは、「プレプロアドレノメデュリン」(プレプロADM)と称される。当該ADMペプチドは、プレプロADMの95〜146アミノ酸を含み、そこでタンパク質開裂が起こることにより形成される。プレプロADMの開裂において形成される幾つかのペプチド断片、特に、生理的に活性のアドレノメデュリン(ADM)ペプチド及び「PAMP」、プレプロADMのシグナルペプチドの21アミノ酸に続いて20アミノ酸(22〜41)を有するペプチドは、詳細に特定されている。機能が不明で体外での高度の安定性を有する他のフラグメントとして、中部プロアドレノメデュリン(MR-proADM) (Struck et al. (2004), Peptides 25(8): 1369-72)があり、これを利用した信頼できる定量法が開発されている(Morgenthaler et al. (2005), Clin. Chem. 51(10):1823-9)。ADMは、効果的な血管拡張剤である。
【0022】
降圧降下は、特に、ADMのC末端部分のペプチド断片と関連していた。一方、ADMのN末端のペプチド配列は、昇圧降下を呈した(Kitamura et al. (2001), Peptides 22, 1713-1718)。
【0023】
エンドセリン(ET)-1は、強力な内皮由来の内在性血管収縮因子である(Yanagisawa M, Kurihara H, Kimura S, Goto, Masaki T, J Hypertens Suppl 1988; 6:S 188-91.)。ET-1は、平滑筋に存在するET(A)及びET(B)を活性化して細胞内のカルシウムの増大を引き起こすことにより血管に対する作用をもたらす(Yanagisawa et al, J Hypertens Suppl 1988;6:S188-91)。成熟エンドセリン-1は、プロエンドセリン-1というより大きな前駆体から生じる。プロエンドセリン1は、文献(Struck J, Morgenthaler NG, Bergmann Peptides. 2005 Dec;26(12):2482-6.)に記載されるように、タンパク質分解により複数の断片にプロセシングされる。これらの断片は、血液循環中でタンパク質分解に供され、当該分解は、断片の種類、並びに当該循環中に存在するプロテアーゼの種類及び濃度/活性に依存して、迅速に又は緩慢に行われる。これらの断片の一例として、C末端プロエンドセリン1(CT-proET-1)が挙げられ、これは、サンドイッチ免疫アッセイにより測定可能である(Papassotiriou J, Morgenthaler NG, Struck J, Alonso C, Bergmann A. Clin Chem. 2006 Jun;52(6): 1144-51.)。
【0024】
B型ナトリウム利尿ペプチド(BNP)は、心不全の定量マーカーである。B型ナトリウム利尿ペプチド(BNP)及びそのアミノ末端断片であるN末端プロB方ナトリウム利尿ペプチド(NT-proBNP)は、EDにおける診断精度を顕著に増大させ[Januzzi, J.L., Jr., et al., Am J Cardiol, 2005. 95(8): p. 948-54; Maisel, A.S., et al., N Engl J Med, 2002. 347(3): p. 161-7]ることにより、患者の評価及び処置を改善する[Moe, G.W., et al., Circulation, 2007. 115(24): p. 3103-10; 8.Mueller, C, et al., N Engl J Med, 2004. 350(7): p. 647-54.]。循環中の心房性ナトリウム利尿ペプチドの濃度は、BNPの約50〜100倍高い[Pandey, K.N., Peptides, 2005. 26(6): p. 901-32]。故に、ANPの増大に反映される生物学的シグナルは、病態生理学的に、かつ診断的に、BNPのシグナルよりも重要である。しかしながら、APN及びその前駆体の診断的性能については殆ど知られていない[Cowie, M.R., et al., Lancet, 1997. 350(9088): p. 1349-53]。成熟ANPは、循環中で、成熟ペプチドよりも顕著に安定であるためより妥当な解析対象と考えられる前駆N末端プロANP(NT-proANP)に由来する[Vesely, D.L., IUBMB Life, 2002. 53(3): p. 153- Pandey, K.N., Peptides, 2005. 26(6): p. 901-32]。
【0025】
心房性ナトリウム利尿ペプチド(ANP)は、ナトリウム利尿ペプチドのメンバーであり、利尿及びナトリウム利尿、並びに動脈の血圧(BP)の低下等の幾つかの生理的パラメーターを制御する。ANPは大半が心臓の心房で生産され、循環中のナトリウム利尿ペプチドの98%を占める(Vesely DL.Life 2002;53:153-159)。ANPは、循環中で成熟ペプチドよりも顕著に安定な前駆プロホルモンの開裂により生じる。前駆ホルモンの中部断片(NT-proANPの53〜90アミノ酸)は、中部プロANP(MR-proANP)といい、従来の免疫アッセイで使用されるプロANPのN又はC末端のエピトープと異なり、エキソプロテアーゼによる分解に比較的耐性である.(Morgenthaler NG et al. Clin Chem 2004;50:234-236; Gerszten RE et al. Am J Physiol Lung Cell Mol Physiol 2008)。
【0026】
ミオグロブリンは、153アミノ酸の単鎖球状タンパク質で、中心部にヘム(鉄含有ポルフィリン)補欠分子族を含有し、その周りがアポタンパク質で覆われている。ミオグロブリンは、筋肉の創傷の高精度のマーカーであり、胸部の疼痛を有する患者の心臓発作における潜在的なマーカーである(M. Weber, M. Rau, K. Madlener, A. Elsaesser, D. Bankovic, V. Mitrovic and C. Hamm (2005) Clinical Biochemistry 38: 1027)。C-MB及び心臓トロポニンT(cTnT)は、ECGと組み合わせて使用され急性心筋梗塞(AMI)を診断する臨床的サインである。心臓トロポニンは、3つのサブユニットT (cTcT)、I(cTcI)及びCからなるタンパク質複合体であり、T及びIは心筋組織にのみ局在しており、診断用マーカーとして使用される(Rottbauer W et al., Eur Heart J 1996; 17:3-8)。
【0027】
アルギニンバソプレシン(AVP)は、バソプレシン、アルギプレシン又は抗利尿ホルモン(ADH)としても知られ、ヒトを含む大半の哺乳類において見出されているホルモンである(Caldwell HK, Young WS III (2006) in Lajtha A, Lim R. Handbook of Neurochemistry and Molecular Neurobiology: Neuro-active Proteins and Peptides (3rd edition ed.). Berlin: Springer, pp. 573-607. ISBN 0-387-30348-0)。バソプレシンはペプチドホルモンである。視床下部で合成され、下垂体後葉の小胞で保存されるプレプロホルモン前駆体から形成される。バソプレシンの放出の低下、又はバソプレシンに対する腎臓の感受性の低下は、高ナトリウム血(血中ナトリウム濃度の増大)、多尿症(過剰な尿生産)、及び多渇症(のどの渇き)を特徴とする、尿崩症を引き起こす。
【0028】
本明細書中で使用されるとき、「マーカーの判定」等の用語は、試料中のマーカーの存否、及び/又はその量の定量、及び/又はその濃度を検出することを含む。故に、存否は、マーカーの検出可能な存在量、即ち本アッセイの検出限界を考慮して理解されるべきである。
【0029】
「マーカー」は、生理的又は病理的指標となる物質である。それらは、例えば、心臓組織の劣化により循環中に心筋細胞から放出されるタンパク質である心臓系の解析対象、予後の指標となるホルモン、糖尿病の症状をモニタリングするのに用いられるグルコース、及び感染により生じる様々なタンパク質及び毒素である。
【0030】
幾つかの態様において、マーカーは、本発明のアレイ、装置、方法及び使用により検出及び/又は定量されるべき、タンパク質又はペプチドである。12アミノ酸以上、好ましくは15アミノ酸以上の長さの前記タンパク質又はペプチドの断片も含まれる。本発明に係るそのようなタンパク質又はペプチドの具体例として、ミオグロビン、トロポニンT(cTnT)及びI(cTnI)、クレアチンキナーゼMB(CK-MB)、FABP、GDF-15、ST-2、プロカルシトニン(PCT)、C-反応性タンパク質(CRB)、プロアドレノメデュリン及びその断片、例えば中部プロアドレノメデュリン(MR-proADM)、アドレノメデュリン、PAMP、C末端プロアドレノメデュリン(CT-proADM)、プロエンドセリン1及びその断片、例えばC末端プロエンドセリン1(CT-proET-1)、大エンドセリン1、エンドセリン1、NT-プロエンドセリン1、プロANP及びその断片、例えば中部プロ心房性利尿ペプチド(MR-proANP)、N末端プロANP(NT-proANP)、ANP、プロバソプレシン及びその断片、例えばC末端プロアルギニンバソプレシンペプチド(CT-proAVP、「コペプチン」)、バソプレシン、ニューロフィシンII、プロBNP及びN末端プロBNP(NT-proBNP)等の、心臓血管事象の診断及び/又は予後診断に関連するマーカーである。
【0031】
本明細書中に記載されるマーカータンパク質及び/又はペプチドが、当該タンパク質のマーカータンパク質及び/又はペプチドの、12アミノ酸以上、好ましくは15アミノ酸以上の長さの断片が、マーカーとして想定されることを理解されたい。
【0032】
更に、ヒト絨毛性ゴナドトロピン(hCG)及び黄体形成ホルモン(LH)等の妊娠又は排卵に関連するホルモンも、本方法又はその様々な態様において検出され得る。癌等の疾患に対する他の抗原、特に前立腺癌抗原(前立腺血清抗原、PSA)が、本発明を使用して検出され得ることも、本発明の範囲内である。本発明の更なる応用として、肝炎、細菌及び真菌感染、例えば消化管の潰瘍におけるヘリコバクター・ピロリ(Helicobacter pylori)、バチルス・アントラキス(Bacillus anthracis)、ペディクルス・ヒューマニス(Pediculus humanis)、シフォナプテラ(Siphonaptera)及びグラム陽性細菌、例えばストレプトコッカス・パイオニエス(Streptococcus pyognes)、ストレプトコッカス・ニューモニアエ(Streptococcus pneumoniae)及びストレプトコッカス・ファエカリ(Streptococcus faecalis)等に関連するマーカーの認識が含まれ、これらは全て非限定的な例示である。また、本発明は、薬物の乱用を含む薬物の検出にも有用であり得る。血中グルコースのレベルを判定するもの等の酵素アッセイも、本発明に想定される。当該装置の使用が、これらの特定のマーカー、又は全血に限定されず、例えば上記で示したような他の解析手順に等しく応用可能であることを認識されたい。
【0033】
好ましい態様において、適正な試験の進行を判定する工程は、適用された液体試料が体液であるか若しくは体液の成分であるか、又は試験流動要素が体液若しくは体液の成分中のマーカーを判定するために設定されたものであるかを光学的に判定することにより、適正な試料の使用を判定する工程を含む。
【0034】
好ましい態様において、本発明は、更に、少量の全血試料を適用し、そして当該全血試料が溶血しているか否かを光学的に判定する工程を含む。好ましい態様において、前記光学的判定は、流動試験要素上の興味のある領域内に照射された光の緩和シグナルを測定する工程を含む。測定された緩和シグナルは、血液が溶血したか否かを判定するための参照シグナルと比較され得る。本明細書中で使用されるとき、「全血試料」とは、未処理又は本質的に未処理の血液試料を特定する。
【0035】
他の好ましい態様において、前記測定の工程は、試験領域及び対照領域と流体により連結され、そしてそれらの間に位置する領域を光学的に測定する工程を含む。この場合に調査される領域は試験領域の下流に位置するので、当該光学的測定は、既に試験領域に浸入した液体試料の一部についての情報を提供する。
【0036】
好ましい態様において、流動試験要素を提供する工程は、適用領域及び試験領域の間に位置し、それらと流体により連結された橋領域、並びに試験領域の上流にあってこれと流体により連結された対照領域を有する、流動試験要素を提供する工程を含む。当該橋領域は、適用領域及び試験領域と流体により連結された橋膜(bridge membrane)により適用され得る。当該橋膜の平均の孔の寸法は、8.0μm±2μmであり、血漿又は血清のキャピラリーフローは、2cmを30秒以内、及び/又は4cmを180秒以内で移動し、ここで、当該橋膜中の血清又は血漿のキャピラリーフローは、第一の多孔質膜よりも低く、そして試験領域よりも高い。また、当該試験領域及び対照領域は、1つ以上の膜により実行され得る。好ましくは、当該膜は、多孔質材料により形成され得る。
【0037】
更なる態様において、適正な試験の進行を判定する工程は、適用領域、橋領域、検出領域及び対照領域から選択される機能領域の1つ以上で光学的測定が行われる工程を含む。
【0038】
更なる態様において、適正な試験の進行を判定する工程は、複数の機能領域の外側に位置する流動試験要素の領域を光学的に測定する工程を含む。そのような測定は、機能領域の1つの中での測定の代わりに、又はこれに加えて実施されてもよい。例えば、前記光学的測定は、2つの機能領域の間に位置する流動試験要素の領域において実施されてもよい。機能領域の1つにおける適正な液体に関する光学的測定は、興味のある機能領域の上流及び/又は下流に位置する領域において行われる。
【0039】
好ましい態様において、本方法は、更に、少量の全血試料を適用し、流動試験要素上の興味のある領域への赤血球の浸入を光学的に判定する工程を含む。例えばマーカーが全血試料中に検出される場合、通常、試験領域自体に赤血球が浸入するは避けられるべきである。上記態様により、そのような浸入が起こったか否かをチェックすることができる。適正な試験の進行を判定する工程でそのような浸入が起こったことが示されたとき、当該工程は、そのような状況で取得された測定結果が適正でないことを使用者に伝える。
【0040】
更なる態様において、適正な試験の進行を判定する工程は、異なる時点で複数の光学的測定を実施する工程を含む。当該複数の光学的測定は、流動試験要素上の興味のある単一の又は複数の領域で実施されうる。
【0041】
他の態様において、マーカーを判定する工程は、液体試料中のマーカーの存在を判定し、当該液体試料中のマーカーの濃度を判定する、1つ以上の工程を含む。
【0042】
尚も他の好ましい態様において、適正な試験の進行を判定する工程において、適用された液体試料が、全血試料、血清試料、血漿試料、尿試料、脳脊髄液試料、便試料、唾液試料及びリンパ液試料から選択される、体液又は体液の成分であるか否かを光学的に判定する工程を含む。
【0043】
本発明の他の態様において、流動試験要素において適正な試験の進行を判定する方法が提供され、当該方法は
-複数の機能領域を有する流動試験要素を提供する工程であり、当該複数の機能領域が、少なくとも部分的には流体により連結しており、そして適用領域、及び当該適用領域と流体により連結し、かつ体液及び/又は当該体液中の成分中のマーカーを検出するように設定された試験領域を有する、当該工程;
・少量の液体試料を前記流動試験要素の試料適用領域に適用する工程;
・適正な試験の進行を判定する工程であり、ここで、当該適正な試験の進行を判定する工程が、前記機能領域において1つ以上の光学的パラメーターを測定する工程、及び当該測定された1つ以上の光学的パラメーターと、1つ以上の機能領域に割り当てられた所定の光学的パラメーターとを比較する工程;
を含む当該工程;
を含む。
【0044】
前記適正な試験の進行を判定する工程において、不適正な試験の進行が検出された場合、解析システムの更なる解析が中断されてもよい。例えば、当該解析システムは、液体試料が適用された流動試験要素の更なる使用をブロックする。好ましい態様において、当該解析システムの使用者に、警告シグナルが提示される。当該警告シグナルは、音響信号及び映像信号の1つ以上を含み得る。
【0045】
発明の好ましい態様の説明
以下で、様々な態様を参照した例示を用いて、本発明を更に詳細に記載する。
【図面の簡単な説明】
【0046】
【図1】図1は、流動試験要素を上から見た模式図を示す。
【0047】
【図2】図2は、様々な時間インキュベーションした全血試料を適用した試験流動要素上の測定位置(相対的単位)と、分光緩和シグナル(相対的単位)との関連性を示す。
【実施例】
【0048】
以下の実施例は例示のみを目的として記載され、本発明の範囲の限定を意図しない。同等のものへの変更又は置換は、状況に応じて想定される。本明細書で特定の用語が採用されているが、それらは、記述的な意味で使用されており、限定を目的としない。
【0049】
図1は、上から見た流動試験要素の模式図である。ポイントオブケア装置ともいう当該流動試験要素は、複数の機能領域が配置された膜体2を有する装置体1を含む。それらの機能領域は、流体により連結されており、適用領域3、橋領域4、試験領域5、及び対照領域6を有する。
【0050】
「ポイントオブケア(POC)」試験は、患者をケアする場所又はその付近で実施される何らかの診断試験として定義される(Kost, Goals, guidelines and principles for point-of-care testing. In: ost GJ, ed. Principles and practice of point-of-care testing. Philadelphia: Lippincott Williams and Wilkins. 2002, Chapter 1, pp 3-12)。患者のより近くで解析を行うことにより、幾つかのプロセス段階が省略され、結果が出るまでの時間の短縮及びその結果に応じた迅速な管理がなされる。POC試験の長所は、迅速な回転時間(turn-around-time、TAT)、迅速な医学的決定、試料の長距離移動の回避及び必要とされる検体の体積の縮小である(Heinschink et al., Point-of-care testing. Laboratoriums Medizin 2002. 26 (1-2): 61-67.)。
【0051】
適用領域3は、少量の体液を受容し、それが、少なくとも部分的に、膜体2に流れ込み、やがてそれぞれ試験領域5及び対照領域6に至るように設定されている。本明細書中で使用されるとき、「試料適用領域」という用語は、試料が例えば試料内に試料適用領域が浸漬され、又はシリンジ若しくはピペット等の試料輸送手段を用いて試料を適用すること等により、試料が適用される、装置上の部分を特定する。当該試料適用領域は、ゆえに、試料がそれを通って第一の多孔質材料に適用されるようなポケット又は切り込み(indentation)の形態であってもよい、装置中の開口である。
【0052】
前記流れは、適用領域3及び対照領域5との間に形成される試料流動チャンネルに沿って起こる。膜体2には、1つ以上の膜要素が設けられてもよく、一つの態様において膜が重ねられる。多孔質膜材料により提供される流動チャンネルは、キャピラリーフローを起こす特徴を有する。
【0053】
1つの態様において、試験領域4は、全血試料中のマーカーの存在を判定するように設定されている。流動試験要素は、下記のように使用され得る。
【0054】
明らかなように、適用領域3の内側及び/又はこれに隣接して設けられた第一の多孔質材料と接触すると、適用された試料の赤血球細胞は、血漿から分離し始め、その流れの過程で、マーカーは検出試薬と出会う。当該検出試薬は、限定されないが、典型的には、当該マーカーのエピトープに対する標識された抗体であり、マーカー-検出試薬複合体を形成する。記載された態様において、マーカー-検出試薬複合体は、橋膜を有する橋領域4に移動し、そこで、赤血球細胞の移動は、更に、阻害/遅延させられる。そして、マーカー-検出試薬複合体は、試験膜を有する試験領域5に達し、不動化された捕捉プローブ、限定されないが、典型的には、マーカーの別個のエピとー部又は検出試薬のエピトープに対する抗体と出会う。マーカー-検出試薬複合体と不動化された捕捉プローブとの反応は、裸眼又は適切な装置を用いて認識できる、濃縮された捕捉スポットを形成する。任意の対照領域6は、試験領域5の捕捉スポットの下流に位置し、対照試薬を含有する。好ましい態様において、対照試薬は、抗動物IgGであってもよい。あるいは、対照領域6の代わりに、試験装置の膜の上を覆う透明なカバーテープの長さの違いは、試験膜の末端に試料が到達したとき、当該試料を、迅速に検出が可能なシグナルを明らかにする調整された様式で蒸発させることができる。
【0055】
液体試料中の1つのマーカー、又は複数のマーカーを一度に検出することは、本発明の範囲内である。故に、1つ以上の検出試薬及び/又は1つ以上の捕捉プローブが、本発明のポイントオブケア装置に蓄積され得ることは、当業者により認識され得ることである。
【0056】
原則として、本アッセイ、即ち検出試薬とマーカーの検出に使用される捕捉プローブとの組合せは、診断の分野において採用されるいずれの形式に基づいてもよい。当該アッセイは、非競合的アッセイ、即ちサンドイッチアッセイ、又は競合的アッセイであってもよい(The Immunoassay Handbook, Ed. David Wild, Elsevier LTD, Oxford; 3rd ed. (May 2005), ISBN-13: 978-0080445267; Hultschig C et al., Curr Opin Chem Biol. 2006 Feb;10(l):4-10. PMID: 16376134)。
【0057】
本明細書中で使用されるとき、捕捉プローブは、核酸分子、糖質分子、PNA分子、アプタマー、タンパク質、抗体、ペプチド又は糖タンパク質から成る群から選択されてもよく、好ましくは抗体である。
【0058】
当業者が利用可能な試験装置における捕捉プローブ及び対応する検出システムの標識として、様々なものを利用することが出来る。限定されないが、公知の標識、例えば金属、蛍光、電子化学発光、及び酵素標識が挙げられる。金属標識は顕著な高感度を有するため、特に好ましい。金属の中でも、金は、この種類の反応に広く使用されており、そしてその特性が良く理解されているので、最も好ましい。
【0059】
幾つかの態様において、前記第一の多孔質材料は、全血試料中で判定されるべきマーカーに結合する、抗体-金粒子コンジュゲートを含有する。従って、抗体-金粒子コンジュゲートが第一の多孔質材料中に存在し、そして当該抗体-金粒子コンジュゲートが試料と接触して当該試料中に懸濁し、そして当該試料と共に移動する。故に、当該抗体-金粒子コンジュゲートは、前記第一の多孔質材料中に不可逆的に不動化されていなくてもよい。しかしながら、試料との結合の後に転換し得る、例えば加水分解を受ける、前記第一の多孔質材料上の抗体-金粒子コンジュゲートの不動化が、幾つかの態様において想定されてもよい。
【0060】
採用される金標識抗体の好ましいサイズは、約20〜60nmであるが、マーカーの臨床的カットオフや反応物の親和性等の周知の要素に依存して、かなりのバリエーションが許容される。加えて、金シグナルは、可視産物を沈殿させる還元性銀塩を使用することにより、容易に可視化を促進できる。典型的な反応性塩は乳酸銀で、これは還元性銀イオンの供給源とされ、還元剤としてヒドロキノンが採用される。金属銀は、金の各粒子の周囲に容易に認識できる黒色の沈着物を形成する。あるいは、ホースラディッシュペルオキシダーゼ等の抗体標識が採用される場合、当該反応は、標準的な手順に従い、過酸化水素やCISオルソフェニレンジアミン等の色素を添加することにより検出され得る。より強いマーカー検出感度を有する米国特許6,046,585(その全体を本明細書中に参照により援用する)に記載のような常磁性標識等の追加の標識も、本発明の範囲内で使用され得る。
【0061】
本出願の文脈において、「検出試薬」は、材料であり、しばしば液体試料中の検出されるべきマーカーに対する抗体である。幾つかの態様において、当該検出試薬は、液体試料を適用する地点、又はその下流の第一の多孔質材料担体に放出可能に結合している。最も免疫化学的な解析において、当該検出試薬は、コロイド金等の検出可能な標識で標識され、検出されるべきマーカーと複合体を形成する。
【0062】
橋膜の血清のキャピラリーフローの文脈において、「水平変化」という用語は、血清の流動の方向における流速の変化を指す。
【0063】
本明細書中で使用されるとき、「血球細胞からの血清の分離」とは、血球細胞を特に保持しつつ、血清を前記装置の隣接する区画又は部分、例えば次の膜に透過させることを意味する。従って、好ましくは95%以上、より好ましくは99%以上、なおもより好ましくは99.5%以上、最も好ましくはほぼ100% の赤血球細胞が保持される。
【0064】
上記非限定的態様を参照して記載される体液中のマーカーの存在を判定する方法は、適正な試料の使用を判定する工程を含む。当該工程は、(a)分光光度計を用いた測定により行われる。吸光度、蛍光、透過、反射及び緩和を含む群から選択される1つ以上のパラメーターが検出及び解析されて、適用領域3に適用され、流動試験要素上の一定の機能領域に到達した液体試料の一部が、当該流動試験要素が判定の対象とする体液の一つ及び体液の成分であるか否かを判定する。好ましくは、領域6において、適正な試料の使用を判定するための光学的調査が行われる。例えば、試験領域5及び対照領域6の間に位置する領域7は、試験領域5及び/又は対照領域6に達した液体の種類が何であるかを判定するために、光学的に調査される。例えば、光学的パラメーターの緩和が、領域7において解析されてもよい。
【0065】
好ましい態様において、上記方法は、少量の全血試料を適用する工程、及び流動試験要素上の興味のある領域への赤血球の浸入を光学的に判定する工程を含む。例えば全血試料中のマーカーを判定しようとする場合、通常、試験領域5自体への赤血球の浸入は避けるべきである。上記態様により、そのような浸入が起こったか否かをチェックすることができる。適正な試料の使用を判定する工程がそのような浸入が起こったことを示した場合、これは、そのような状況で回収された測定結果が適正ではないことを、使用者に教示する。
【0066】
図2は、様々な時間インキュベーションした全血試料の分光的緩和シグナル(相対的単位)と、流動試験要素1上の相対的位置(相対的単位)との関連性を示す。当該流動試験要素1(図1参照)は、対照領域6、領域7及び試験領域5を少なくともカバーするように、左から右にスキャンされた。左側に、対照領域6の緩和シグナルに割り当てられたいわゆる対照バンドがあり、これは全ての時間で変化が無い。左側の緩和シグナルの増大は、流動試験要素1上の試験領域5への赤血球の浸入を示す。
【0067】
本願明細書、特許請求の範囲及び図面の1つ以上に開示される特徴は、単独で又は複数のものが組み合わされて、様々な態様における本発明の実現の材料となり得る。
【特許請求の範囲】
【請求項1】
流動試験要素(flow test element)における適正な試験の進行(correct test performance)を判定する方法であり:
・複数の機能領域(3、4、5、6、7)を有する流動試験要素を提供する工程であり、当該複数の機能領域(3、4、5、6、7)が、少なくとも部分的には流体により連結しており、そして適用領域(3)、及び当該適用領域(3)と流体により連結し、かつ体液及び/又は当該体液中の成分中のマーカーを検出するように設定された試験領域(5)を有する、当該工程、及び
・少量の液体試料を前記流動試験要素の試料適用領域(3)に適用する工程
を含み、
前記流動試験要素における適正な試料の使用を、1つ以上の機能領域(3、4、5、6、7)において1つ以上の光学的パラメーターを測定することにより判定し、そして当該測定された1つ以上の光学的パラメーターと、1つ以上の機能領域(3、4、5、6、7)に割り当てられた1つ以上の所定の光学的パラメーターとを比較することにより、前記複数の機能領域(3、4、5、6、7)の1つの領域に到達した適用された液体試料の一部が、体液又は体液の成分であるか否かを光学的に判定する工程を特徴とする、当該方法。
【請求項2】
更に、
・少量の全血試料を適用する工程、及び
・試験領域(5)に到達した当該全血試料の一部が溶血しているか否かを光学的に判定する工程
を含む、請求項1に記載の方法。
【請求項3】
前記測定工程が、試験領域(5)及び対照領域(6)に流体により連結し、それらの間に位置する領域を光学的に測定する工程を含む、請求項1又は2のいずれかに記載の方法。
【請求項4】
前記流動試験要素を提供する工程が、適用領域(3)及び試験領域(5)との間に位置し、それらと流体により連結する1つ以上の橋領域(4)、並びに試験領域(5)の上流に位置し、それと流体により連結する対照領域(6)を有する、流動試験要素を提供する工程を含む、請求項1〜3のいずれか1項に記載の方法。
【請求項5】
前記適正な試験の進行を判定する工程が:適用領域(3)、橋領域(4)、検出領域(5)、及び対照領域(6)からなる機能領域の群から選択される1つ以上の機能領域(3、4、5、6、7)を光学的に測定する工程を含む、請求項1〜4のいずれか1項に記載の方法。
【請求項6】
前記適正な試験の進行を判定する工程が、複数の機能領域(3、4、5、6、7)の外側に位置する流動試験要素の領域を光学的に測定する工程を含む、請求項1〜5のいずれか1項に記載の方法。
【請求項7】
更に:
・少量の全血試料を適用する工程、及び
・流動試験要素上の興味のある領域への赤血球の浸入を光学的に判定する工程
を含む、請求項1〜6のいずれか1項に記載の方法。
【請求項8】
前記適正な試験の進行を判定する工程が、異なる時点で複数の光学的測定を実施する工程を含む、請求項1〜7のいずれか1項に記載の方法。
【請求項9】
前記マーカーを検出する工程が:
・液体試料中のマーカーの存在を判定する工程、及び
・液体試料中のマーカーの濃度を判定する工程
の1つ以上を含む、請求項1〜8のいずれか1項に記載の方法。
【請求項10】
前記適正な試料の使用を判定する工程が、1つの機能領域(3、4、5、6、7)に到達した適用された液体試料の一部が、全血試料、血清試料、血漿試料、尿試料、脳脊髄液試料、便試料、唾液試料、及びリンパ液試料から成る群から選択される体液又は体液の成分であるか否かを光学的に判定する工程を含む、請求項1〜9のいずれか1項に記載の方法。
【請求項11】
前記適正な試験の進行が判定された場合、更に試験領域(5)を読み取ることにより液体試料中のマーカーを判定する工程が実施される、請求項1〜10のいずれか1項に記載の方法。
【請求項1】
流動試験要素(flow test element)における適正な試験の進行(correct test performance)を判定する方法であり:
・複数の機能領域(3、4、5、6、7)を有する流動試験要素を提供する工程であり、当該複数の機能領域(3、4、5、6、7)が、少なくとも部分的には流体により連結しており、そして適用領域(3)、及び当該適用領域(3)と流体により連結し、かつ体液及び/又は当該体液中の成分中のマーカーを検出するように設定された試験領域(5)を有する、当該工程、及び
・少量の液体試料を前記流動試験要素の試料適用領域(3)に適用する工程
を含み、
前記流動試験要素における適正な試料の使用を、1つ以上の機能領域(3、4、5、6、7)において1つ以上の光学的パラメーターを測定することにより判定し、そして当該測定された1つ以上の光学的パラメーターと、1つ以上の機能領域(3、4、5、6、7)に割り当てられた1つ以上の所定の光学的パラメーターとを比較することにより、前記複数の機能領域(3、4、5、6、7)の1つの領域に到達した適用された液体試料の一部が、体液又は体液の成分であるか否かを光学的に判定する工程を特徴とする、当該方法。
【請求項2】
更に、
・少量の全血試料を適用する工程、及び
・試験領域(5)に到達した当該全血試料の一部が溶血しているか否かを光学的に判定する工程
を含む、請求項1に記載の方法。
【請求項3】
前記測定工程が、試験領域(5)及び対照領域(6)に流体により連結し、それらの間に位置する領域を光学的に測定する工程を含む、請求項1又は2のいずれかに記載の方法。
【請求項4】
前記流動試験要素を提供する工程が、適用領域(3)及び試験領域(5)との間に位置し、それらと流体により連結する1つ以上の橋領域(4)、並びに試験領域(5)の上流に位置し、それと流体により連結する対照領域(6)を有する、流動試験要素を提供する工程を含む、請求項1〜3のいずれか1項に記載の方法。
【請求項5】
前記適正な試験の進行を判定する工程が:適用領域(3)、橋領域(4)、検出領域(5)、及び対照領域(6)からなる機能領域の群から選択される1つ以上の機能領域(3、4、5、6、7)を光学的に測定する工程を含む、請求項1〜4のいずれか1項に記載の方法。
【請求項6】
前記適正な試験の進行を判定する工程が、複数の機能領域(3、4、5、6、7)の外側に位置する流動試験要素の領域を光学的に測定する工程を含む、請求項1〜5のいずれか1項に記載の方法。
【請求項7】
更に:
・少量の全血試料を適用する工程、及び
・流動試験要素上の興味のある領域への赤血球の浸入を光学的に判定する工程
を含む、請求項1〜6のいずれか1項に記載の方法。
【請求項8】
前記適正な試験の進行を判定する工程が、異なる時点で複数の光学的測定を実施する工程を含む、請求項1〜7のいずれか1項に記載の方法。
【請求項9】
前記マーカーを検出する工程が:
・液体試料中のマーカーの存在を判定する工程、及び
・液体試料中のマーカーの濃度を判定する工程
の1つ以上を含む、請求項1〜8のいずれか1項に記載の方法。
【請求項10】
前記適正な試料の使用を判定する工程が、1つの機能領域(3、4、5、6、7)に到達した適用された液体試料の一部が、全血試料、血清試料、血漿試料、尿試料、脳脊髄液試料、便試料、唾液試料、及びリンパ液試料から成る群から選択される体液又は体液の成分であるか否かを光学的に判定する工程を含む、請求項1〜9のいずれか1項に記載の方法。
【請求項11】
前記適正な試験の進行が判定された場合、更に試験領域(5)を読み取ることにより液体試料中のマーカーを判定する工程が実施される、請求項1〜10のいずれか1項に記載の方法。
【図1】


【図2】




【図2】


【公表番号】特表2013−520644(P2013−520644A)
【公表日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願番号】特願2012−553351(P2012−553351)
【出願日】平成23年2月22日(2011.2.22)
【国際出願番号】PCT/EP2011/052613
【国際公開番号】WO2011/104238
【国際公開日】平成23年9月1日(2011.9.1)
【出願人】(508093584)ベー.エル.アー.ハー.エム.エス ゲゼルシャフト ミット ベシュレンクテル ハフツング (27)
【Fターム(参考)】
【公表日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願日】平成23年2月22日(2011.2.22)
【国際出願番号】PCT/EP2011/052613
【国際公開番号】WO2011/104238
【国際公開日】平成23年9月1日(2011.9.1)
【出願人】(508093584)ベー.エル.アー.ハー.エム.エス ゲゼルシャフト ミット ベシュレンクテル ハフツング (27)
【Fターム(参考)】
[ Back to top ]

