幹細胞増殖用組成物
【課題】幹細胞の効率的な増殖に利用しうる製剤の提供。
【解決手段】以下の(a)または(b)に記載のポリペプチドまたはその誘導体を含んでなる幹細胞増殖用組成物(a)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列からなるポリペプチド、(b)特定の配列で表されるアミノ酸配列において1個または数個のアミノ酸が、欠失、置換、欠失、挿入または付加したアミノ酸配列からなり、幹細胞増殖活性を有する、ポリペプチド。
【解決手段】以下の(a)または(b)に記載のポリペプチドまたはその誘導体を含んでなる幹細胞増殖用組成物(a)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列からなるポリペプチド、(b)特定の配列で表されるアミノ酸配列において1個または数個のアミノ酸が、欠失、置換、欠失、挿入または付加したアミノ酸配列からなり、幹細胞増殖活性を有する、ポリペプチド。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、幹細胞の効率的な増殖に用いうる、新規幹細胞増殖用組成物に関する。
【背景技術】
【0002】
幹細胞は、その優れた分化能に着目され、細胞療法や再生医療におけるその利用が従前期待されている。実際の組織再生等に利用する場合、大量の幹細胞を取得することが前提となる。しかしながら、幹細胞自体の取得はしばしば困難であり、その増殖効率も再生医療に用いるレベルに至らない場合が少なくない。
【0003】
例えば、間充織幹細胞(Mesenchymal stem cells;MSC)は非造血性の多能性幹細胞であり、通常、イン・ビトロにおいて3つの細胞系、骨芽細胞、脂肪細胞および軟骨細胞への分化能を示すことが知られている。MSCは、骨髄、臍帯血、脂肪組織、胎児肺、羊水、骨格筋から単離することが可能であるが、その取得量は少量である。しかしながら、イン・ビトロやエクス・ビボにおけるMSCの増殖率はいずれも満足なレベルには至らず、医療への応用は制限されている。
このように、幹細胞を効率的に増殖させる技術が依然として求められているといえる。
【0004】
一方、WO2006/025580号公報(特許文献1)において、本発明者らの一部は、免疫抑制剤として有用な抗ヒストンH1モノクローナル抗体と、ヒストンH1との結合を阻害するペプチドとして、SSVLYGGPPSAAで表されるアミノ酸配列を有するポリペプチドを開示し、このポリペプチドが免疫抑制剤として利用しうることが報告している。しかしながら、上記ポリペプチドの幹細胞に対する生理作用は何ら記載されていない。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】WO2006/025580号公報
【発明の概要】
【0006】
本発明者らは、今般、SSVLYGGPPSAAで表されるアミノ酸配列を有するペプチドまたはその誘導体が、優れた幹細胞増殖活性を有することを見出した。本発明は、かかる知見に基づくものである。
【0007】
したがって、本発明は、優れた幹細胞増殖活性を有する新規製剤を提供することをその目的とする。
【0008】
そして、本発明による幹細胞増殖用組成物は、以下の(a)または(b)に記載のポリペプチドまたはその誘導体を含んでなるものである:
(a)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列からなるポリペプチド、
(b)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列において1個または数個のアミノ酸が、欠失、置換、欠失、挿入または付加したアミノ酸配列からなり、幹細胞増殖活性を有する、ポリペプチド。
【0009】
また、本発明による幹細胞の増殖方法は、幹細胞と、上記ポリペプチドまたはその誘導体とを接触させて、幹細胞を増殖させることを含んでなる方法である。
【発明の効果】
【0010】
本発明による組成物によれば、幹細胞の増殖活性を効果的に増強することが可能となる。また、本発明による組成物は、幹細胞の表現型および分化能を安定に維持する上でも有利である。よって、本発明による幹細胞増殖用組成物は、細胞療法や再生医療において有利に利用しうる。
【図面の簡単な説明】
【0011】
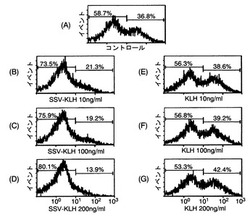
【図1】脂肪由来幹細胞(ADSC)の増殖アッセイにおけるフローサイトメトリーの結果を示す。図1Aはコントロールであり、図1B〜DはSSV−KLH処理群であり、図1E〜GはKLH単独処理群である。また、図1における縦軸は細胞数を示し、横軸は経口強度を示す。
【図2】ADSCの表面抗原(CD29、CD44、 CD90、CD34およびCD45)の発現をフローサイトメトリーによって測定した結果を示す。図2Aはコントロールを示し、図2BはSSV−KLH処理群(SSV−KLH投与量:10ng/mL)を示し、図2CはKLH単独処理群(KLH投与量:10ng/mL)を示す。また、図2における縦軸は細胞数を示し、横軸は経口強度を示す。
【図3】Aは、CFSEで処理した脾臓細胞をフローサイトメトリーで測定した結果である。 Bは、CFSE処理の後、ConAが添加された脾臓細胞をフローサイトメトリーで測定した結果である。 Cは、CFSE処理の後、ConAおよび間充織幹細胞(MSC)が添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Dは、CFSE処理の後、ConA、およびSSV−KLH(10ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Eは、CFSE処理の後、ConA、およびSSV−KLH(100ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Fは、CFSE処理の後、ConA、およびSSV−KLH(200ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Gは、CFSE処理の後、ConA、およびKLH(10ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Hは、CFSE処理の後、ConA、およびKLH(100ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Iは、CFSE処理の後、ConA、およびKLH(200ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。
【発明を実施するための形態】
【0012】
定義
本明細書において、「幹細胞」とは、分裂に伴って自己再生能を示すとともに、同時に性質の異なる細胞を生じる分化能を有する細胞をいう。
【0013】
また、本明細書において、「幹細胞増殖活性を有する」とは、下記の試験例1と実質的に同一の条件で幹細胞の増殖アッセイを行ったとき、試験例1と同一の統計比較方法において、幹細胞数が試験例1のコントロールに示されたレベルよりも有意に多いこと、好ましくはコントロールの約120%以上であることをいう。
【0014】
また、本明細書において、ポリペプチドの「誘導体」とは、ポリペプチドのアミノ末端(N末端)のアミノ基、および/または、ポリペプチドのカルボキシル末端(C末端)のカルボキシル基、および/または、ポリペプチドの各アミノ酸の側鎖の官能基(例えば、水素基、水酸基等)の一部もしくは全部が、適当な他の置換基によって修飾を受けたものをいう。適当な他の置換基による修飾は、例えば、ポリペプチド中に存在する官能基の保護、ポリペプチドの安全性および組織移行性の向上、またはポリペプチドの活性の増強等を目的として行われる。
【0015】
幹細胞増殖用組成物
本発明による幹細胞増殖用組成物は、幹細胞増殖活性を有する上記(a)または(b)に記載のポリペプチドを有効成分とすることを一つの特徴とする。(a)または(b)に記載のポリペプチドまたはその誘導体が、優れた幹細胞の増殖活性を示すことは意外な事実である。したがって、本発明の一つの態様によれば、幹細胞増殖剤の製造における、(a)または(b)に記載のポリペプチドまたはその誘導体の使用が提供される。
【0016】
(a)または(b)に記載のポリペプチドのうち、(b)に記載のポリペプチドにおいて、「1もしくは数個」の範囲は、好ましくは1〜3個、より好ましくは1〜2個程度を意味する。
【0017】
また、アミノ酸の保存的置換は、(b)に記載のポリペプチドを得るための好ましい手段のひとつである。ここで、保存的置換は、ポリペプチドの活性機能的同等性を確保し、かつ一般に交換された2つの残基の側鎖が化学的類似性を有することにより特徴付けられる。例えば、酸性残基は他の酸性残基により、塩基性残基は塩基性残基により、疎水性残基は疎水性残基により、バルキーな残基はバルキーな残基により、保存的に置き換えられることが好ましい。保存的置換としては、例えば、以下のグループ内での置換を包含する:セリンに対する置換としてスレオニン;バリンに対する置換としてロイシンまたはイソロイシン;ロイシンに対する置換としてイソロイシン、バリン、;チロシンに対する置換としてフェニルアラニン、トリプトファン;アラニンに対する置換としてグリシン。
【0018】
また、上記(a)または(b)に記載のポリペプチドは、上述の通り、幹細胞増殖活性を保持する限り、誘導体としてもよい。本発明に用いられるポリペプチドの誘導体としては、上記(a)または(b)に記載のポリペプチドにおいて、そのアミノ酸側鎖またはアミノ末端またはカルボキシル末端が修飾され、かつ所望の活性が保持されたポリペプチドが含まれる。好ましい態様によれば、上記誘導体は、ポリペプチドのアミノ末端がアシル化、アミド化もしくは糖修飾されたポリペプチドであるか、または前記ポリペプチドのカルボキシル末端がアミド化、エステル化もしくは糖修飾されたポリペプチドである。より好ましい態様によれば、上記誘導体は、ポリペプチドのアミノ末端がアシル化もしくはアミド化されたポリペプチドであるか、または前記ポリペプチドのカルボキシル末端がアミド化もしくはエステル化されたポリペプチドである。
【0019】
より具体的には、上記誘導体としては、例えば、(1)ポリペプチドのアミノ末端(N末端)のアミノ基が、置換または非置換のアルキル基(直鎖、分岐鎖または環状であってもよい)(例えば、メチル基、エチル基、プロピル基、イソプロピル基、イソブチル基、ブチル基、t−ブチル基、シクロプロピル基、シクロヘキシル基、ベンジル基)、置換または非置換のアシル基(例えば、ホルミル基、アセチル基、カプロイル基、シクロヘキシルカルボニル基、ベンゾイル基、フタロイル基、トシル基、ニコチノイル基、ピペリジンカルボニル基)、ウレタン型保護基(例えば、p−ニトロベンジルオキシカルボニル基、p−メトキシベンジルオキシカルボニル基、t−ブトキシカルボニル基)またはウレア型置換基(例えば、メチルアミノカルボニル基、フェニルカルボニル基、シクロヘキシルアミノカルボニル基)、糖(例えば、グルコース、ラクトース、マルトース)、リン脂質(例えば、ミリストイル基、パルミトイル基)、ポリエチレングリコール基等によって置換されたもの、並びに(2)ポリペプチドのカルボキシル末端(C末端)のカルボキシル基が、エステル化されているもの(例えば、その水素原子が、メチル、エチル、イソプロピル、シクロヘキシル、フェニル、ベンジル、t−ブチル、4−ピコリルにより置き換えられたもの)、アミド型の修飾を受けているもの(例えば、非置換アミド、C1〜C6アルキルアミド(メチルアミド、エチルアミド、イソプロピルアミド)を形成しているもの)、並びに(3)ポリペプチドのアミノ酸の側鎖の官能基(例えば、水素基、水酸基等)の一部もしくは全部が、上述のアミノ基と同様の置換基あるいはトリチル基等で修飾されたもの等が挙げられる。
【0020】
また、上記誘導体の他の好適な例としては、(a)または(b)に記載のポリペプチドと、薬学的に許容可能な担体との結合体が挙げられる。したがって、本発明の好ましい態様によれば、免疫アジュバントにおける誘導体は、薬学的に許容可能な担体を構成成分としてさらに含んでなる。上記担体としては、好ましくは、キーホールリンペットヘモシアニン(Keyhole limpet hemocyanin;KLH)、オボアルブミン(Ovalbumin;OVA)またはウシ血清アルブミン(Bovine Serum Albumin;BSA)であり、より好ましくはKLHである。(a)または(b)に記載のペプチドを、上述のような薬学的に許容可能な担体を用いて誘導化することは、幹細胞増殖活性を効果的に増強する上で有利である。
【0021】
また、本発明による組成物は、幹細胞増殖活性を有するポリペプチドまたはその誘導体と、その活性を実質的に阻害しない任意の成分とを含有する組成物として提供さすることができる。かかる任意の成分としては、例えば、結合剤、着色剤、乾燥剤、防腐剤、湿潤剤、安定剤、賦形剤、接着剤、可塑剤、粘着付与剤、増粘剤、パッチ材料、軟膏基材、角質除去剤、塩基性物質、吸収促進剤、脂肪酸、脂肪酸エステル、高級アルコール、界面活性剤、水、緩衝剤等が挙げられるが、好ましくは緩衝剤、軟膏基材、脂肪酸、防腐剤、塩基性物質または界面活性剤である。
【0022】
本発明による組成物において、上記(a)または(b)に記載のポリペプチドまたはその誘導体の含有量は、幹細胞の必要量、幹細胞の増殖能、投与形態等を勘案して適宜決定してよく、例えば、1〜100重量%である。
【0023】
また、本発明の幹細胞増殖用組成物は、任意の形状であり得る。本発明の造血幹細胞増殖用組成物は、例えば、錠剤、丸剤、カプセル剤、顆粒剤のような固体;または水溶液および懸濁液のような液体;またはゲル剤のような半固形としてもよい。また、後述する治療用途において、本発明の幹細胞増殖用組成物は、好ましくはRemington’s PharmaceuticalSciences, Mack Publishing社(Easton、PA)に記載されているような従来のポリペプチドの処方物の形で投与され得る。
【0024】
本発明による組成物の製造において、(a)または(b)に記載のポリペプチドは、人為的に合成してもよいが、人為的に合成する場合には、例えば、ペプチド固相合成法、ペプチド液相合成法等の公知のペプチド合成技術を使用することが可能である。
【0025】
また、(a)または(b)に記載のポリペプチドの誘導化は、例えば、Greene’s Protective Groups in Organic Synthesis, 4 th Edition, Peter G.M. Wuts et al, John Wiley & Sons, 2006等に記載の公知手法に基づき、(a)または(b)に記載のペプチドと、各種官能基導入剤を用いて製造することができる。
とりわけ、(a)または(b)に記載のポリペプチドと、薬学的に許容可能な担体とを結合する手法としては、例えば、公知のリンカーを用いる手法が挙げられる。このようなリンカーとしては、EDC(Ethylenedichloride)、カルボジイミド(DCC(dicyclohexyl carbodiimide)、DIC(1,3-diisopropyl carbodiimide))等の脱水縮合剤、グルタルアルデヒド、マレイミド、マレイミドベンゾイルオキシコハク酸等の架橋剤、PEG、リンカーペプチド等が挙げられるが、好ましくはカルボジイミドまたはグルタルアルデヒド等である。ペプチドと、担体とを結合する具体的な手法は、「ペプチド合成の基礎と実験」泉屋 信夫他著、丸善株式会社)に記載の方法等を参照されたい。
【0026】
本発明による組成物は、上述のようにして得られる(a)または(b)に記載のペプチドまたはその誘導体と、その剤形等に応じた各種成分とを適宜混合する等公知の手法により製造することができる。
【0027】
幹細胞の増殖方法
本発明のポリペプチドまたはその誘導体を用いると、上述の通り、幹細胞を効率的に増殖させることが可能である。したがって、一つの態様によれば、幹細胞と、本発明のポリペプチドまたはその誘導体とを接触させて、幹細胞を増殖させることを含んでなる、幹細胞の増殖方法が提供される。
【0028】
上記接触工程に用いられる具体的な手法は、幹細胞を増殖しうる限り特に限定されないが、好ましくは、インビトロにて行われる。好ましい態様によれば、上記接触は、幹細胞を本発明のポリペプチドまたはその誘導体を含む培地中で培養することを含んでなる。
【0029】
また、本発明のポリペプチドまたはその誘導体の有効量、および幹細胞の培養および回収の条件などは、幹細胞の種類、性質等に応じて、当業者により適宜選択され得る。
【0030】
治療用途
また、本発明による組成物は、幹細胞の増加が所望される対象の治療において、医薬として投与することができる。したがって、別の態様によれば、本発明のポリペプチドまたはその誘導体の有効量を患者に投与することを含んでなる、対象における幹細胞の増殖方法が提供される。
【0031】
本発明のポリペプチドまたはその誘導体は、例えば、経口投与、静脈投与、筋肉注射、腹腔内注射、および皮下注射のような非経口投与により対象に投与してもよい。本発明のポリペプチドまたはその誘導体を羊水中へ補充することも可能である。好ましくは、本発明のポリペプチドまたはその誘導体は注射によって対象に投与される。
【0032】
本発明のポリペプチドまたはその誘導体を投与する対象としては、それを必要とする限り特に限定されないが、哺乳動物であり、より好ましくはヒトである。
【0033】
本発明のポリペプチドまたはその誘導体の有効量は、当業者によって適宜決定される。例えば、ヒトに投与する場合、1日あたりの用量は、通常、患者の症状、重篤度、感受性に対する個体差、体重、年齢などを考慮して、当業者によって適切に決定され得る。本発明の造血幹細胞増殖剤は、1日1回投与されてもよいし、1日数回に分けて投与されてもよい。
【0034】
また、幹細胞は、本発明のポリペプチドまたはその誘導体により増殖しうる限り特に限定されず、好ましくは、前記幹細胞が、単能性幹細胞、複能性幹細胞、多能性幹細胞、胚性幹細胞(ES細胞)、体性幹細胞、臍帯血幹細胞または人工多能性幹細胞(iPS細胞)であり、より好ましくは、造血幹細胞、表皮基底膜の幹細胞、小腸粘膜上皮の幹細胞、間充織幹細胞(MSC)、脂肪由来幹細胞(ADSC)、骨髄由来細胞、臍帯血液由来幹細胞、胎児肺由来幹細胞、羊水由来幹細胞、骨格筋由来細胞、胚性幹細胞または人工多能性幹細胞等であり、さらに好ましくは間充織幹細胞(MSC)、脂肪由来幹細胞(ADSC)である。
また、幹細胞の由来する種としては、好ましくは哺乳動物であり、より好ましくはヒトである。
【0035】
なお、遺伝子治療においては、目的の遺伝子の導入効率は、遺伝子を細胞に導入工程で、どれだけ多数の細胞が分裂を行なっているかに左右されることが知られている。したがって、本発明のポリペプチドまたは誘導体を用いて幹細胞を増殖させつつ遺伝子を導入することにより、非常に高い遺伝子導入効率を得ることが可能である。したがって、本発明の別の好ましい態様によれば、上記いずれかの方法において、幹細胞に外来遺伝子が導入する工程を含んでなる。
【0036】
導入される外来遺伝子は、幹細胞の増殖を妨げない限り特に限定されず、プラスミドなどの公知のベクター等を用いて、幹細胞に導入することができる。
導入方法は、当該技術分野において公知の手法を用いることが可能であり、エレクトロポレーション、マイクロインジェクション、リポフェクション等が挙げられる。かkる導入方法は、幹細胞の種類、ベクターのサイズ、導入効率等を勘案して当業者によって適宜選択される。
【実施例】
【0037】
以下、本発明を実施例によって説明するが、本発明はこれら実施例に限定されない。
例1:幹細胞増殖剤の製造
配列番号1で表されるアミノ酸配列からなるペプチド(以下、「SSV」というは、Fmocペプチド固相合成法(製造装置;ABI430型アプライバイオシステムズ社製)により合成した。次に、SSV5mg、KLH20mgおよびグルタルアルデヒド 30μg(片山化学工業株式会社)(SIGMA社製)をリン酸緩衝液(pH 8.0)中、室温で約6時間撹拌し、SSVおよびKLHの結合体(以下、「SSV−KLH」という。)を得た。このSSV―KLHをPBSに溶解した溶液を、以下の試験において幹細胞増殖剤として用いた。
【0038】
試験例1:SSV―KLHの幹細胞増殖能に対する影響の確認1
以下の試験例において、LEW (RT11) ラット(オス)は、行政院国家科学委員会(台湾)から取得した。また、DA (主要組織適合複合体ハプロタイプ RT1a) ラット(オス)は、日本SLC株式会社(浜松)から取得した。実験中、総ての動物は、無菌動物施設内で飼育し、水および市販ラット用食品を不断給餌した。また、総ての動物実験は、Chang Gung Memorial Hospital-Kaohsiung Medical Center(台湾)のガイドラインに従って行った。
【0039】
また、細胞は、以下に記載の時点において収集し、PBSで連続的に適宜洗浄した。さらに、生存細胞数は、トリパンブルー染色(trypan blue exclusion method)および血球計によってカウントした。
【0040】
1−1:脂肪由来幹細胞(ADSC)の調製
LEWラット(8週齢)の腹部から脂肪組織を採取し、リン酸緩衝生理食塩水(PBS、 Sigma-Aldrich、St. Louis、MO)を含むペトリ皿に維持した。次に、脂肪組織をミンチにし、コラゲナーゼタイプII (0.25 mg/ml, Sigma-Aldrich)を含むハンクス液中で懸濁させた。次に、懸濁液がスムースで均一な状態になるまで、30−60分間、アジテーション(50 rpm)とともに37 ℃にて消化を行い、さらに、遠心分離により細胞のペレットを取得した。得られた細胞ペレットは、70μmナイロンメッシュで濾過し、赤血球溶解バッファーでインキュべートし、さらに、40μmで再度濾過した後、10%ウシ胎仔血清(FBS)、ならびにペニシリン/ストレプトマイシン 100U/ml および 100μg/ml (GIBCOTM Invitrogen Corporation, Carlsbad, CA, USA)を添加したDMEDの完全培地中で再懸濁した。得られた細胞は、約80%コンフルエンスの状態になるまで、3〜6日間、加湿された5%CO2インキュベーター中で維持し、ADSCの懸濁液を得た。
【0041】
1−2:脂肪由来幹細胞の増殖アッセイ
脂肪由来幹細胞(ADSC)は、繊維芽細胞の様な外観を有し、細胞集団形成から7日後に単層を形成した。プレートに粘着した細胞は、EDTA/トリプシン処理して取得した。取得したADSCを、2000細胞/cm2で24ウェルプレートに播種した。次に、ADSCに、50〜200ng/mlのSSV−KLH溶液またはKLH溶液を加え、15日間インキュベートした。この際、コントロールとして未処理群を用意した。
【0042】
1−3:吸光度測定
インキュベート後、各群の細胞は、細胞増殖剤WST-1 (Roche Molecular Biochemicals, Mannheim, Germany) を用いて処理し、 MRX マイクロプレートリーダー (Dynex Technologies, VA, USA) を用いて、450 nm および620 nmの吸光度を測定した。なお、以下の群間比較においては、一元配置分散分析(ANOVA)およびDuncan’s post hoc testを適宜用いた。また、記述統計学、平均、標準偏差および範囲についても適宜採用した。結果は、平均値 ± 標準偏差 (SD) を基準として、p<0.05 で有意差があるものとした。
【0043】
吸光度測定の結果、SSV−KLH処理群のADSCの数は、同投与量のKLH単独処理群またはコントロール群の約120%〜140%であった。
【0044】
試験例2:SSV―KLHの幹細胞増殖能に対する影響の確認2
2−1:フローサイトメトリー
CFSEのDMSO溶液を、間充織幹細胞(MSC;1×107細胞/mL in PBS)にCFSE終濃度5mMとなるように添加した。次に、得られた溶液を37℃で10分間インキュベートした。次に、得られた溶液に、これと等量の牛胎児血清(heat inactivated fetal bovine serum(FBS))を添加し、反応を停止した。1分後、溶液中のCFSEでラベル化されたMSCを洗浄後、得られた細胞の数をカウントした。得られたMSCを、培地(10% FBS 添加DMED、100U/mL ペニシリン および100ug/mL ストレプトマイシン)に5×105細胞/mLで播種した。さらに、MSCを24ウェルプレートに2000細胞/cm2で播種し、これに10〜200mg/mlのSSV−KLH溶液またはKLH溶液を加えた。3日後、細胞を回収し、Epics ALTA flow cytometerにて解析を行った。
【0045】
図1A〜Gは、各群のフローサイトメトリーの結果を示す図である。
ここで、図1Aはコントロール(処理なし)を示す。
また、図1BはSSV−KLH処理群(SSV−KLH投与量:10ng/mL)を示す。
また、図1CはSSV−KLH処理群(SSV−KLH投与量:100ng/mL)を示す。
また、図1DはSSV−KLH処理群(SSV−KLH投与量:200ng/mL)を示す。
また、図1EはKLH単独処理群(KLH投与量:10ng/mL)を示す。
また、図1FはKLH単独処理群(KLH投与量:100ng/mL)を示す。
また、図1GはKLH単独処理群(KLH投与量:100ng/mL)を示す。
【0046】
図1B〜Dに示される通り、SSV−KLH処理群では、蛍光強度が減少しており、全体の細胞のうち、CSFEラベルされた細胞の占める割合が低下していた。一方、図E〜Gに示される通り、KLH単独処理群ではコントロールと同様の蛍光パターンを示し、蛍光強度の変化は認められず、全体の細胞のうちCSFEラベルされた細胞の占める割合は変化しなかった。この結果から、SSV−KLH処理群では、細胞増殖が誘導されて全体の細胞数が増加し、KLH単独処理群では、細胞増殖が誘導されないことが確認された。
【0047】
1−3:ADSC特異的マーカーの確認
STEM CELLS 2007; 25:818-827に記載されている手法に準じて、増殖アッセイの前後において、SSV−KLH処理群、KLH単独処理群またはコントロールにおけるADSC特異的マーカーの発現をフローサイトメトリーによって測定した。
具体的には、増殖アッセイの前後において、各群における細胞を、ラットの、CD29、CD44、 CD90、CD45 (BD Biosciences Pharmingen, San Diego, CA, USA)、MHC I、MHC II (Serotec, Oxford, UK) およびCD34 (Santa Cruz Biotechnology, Santa Cruz, CA,USA)に対するマウスモノクローナル抗体を用いて免疫染色した。免疫染色後、coulter Epics(登録商標) ALTRA(登録商標)フローサイトメーター (Beckman Coulter, CA, USA) を用いて測定を行い、その分析にはEXP O32 ソフトウェア(Beckman Coulter)を用いた。
【0048】
ADSCの表面抗原(CD29、CD44、 CD90、CD34およびCD45)の発現を測定した結果は、図2に示される通りであった。
ここで、図2Aはコントロールを示す。また、図2BはSSV−KLH処理群を示す。また、図2CはKLH単独処理群を示す。
図2に示される通り、各群の細胞は、CD29、CD44およびCD90に対して陽性を示し、CD34およびCD45に対して陰性を示した。また、図示しなかったが、各群の細胞は、MHCIに対して陽性を示し、MHCIIに対して陰性を示した。
各群の細胞は、統計学的な比較においても、上記表面抗原の発現に関し、SSV−KLH処理群と、KLH単独処理群またはコントロールとは、有意な差は認められなかった。
この結果から、SSV−KLHによって処理した場合、ADSCの特異的マーカーの発現には変化がないことが確認された。
【0049】
試験例3:脂肪生成および骨形成分化アッセイ
SSV−KLH処理群、KLH処理群およびコントロールにおいて、以下の手順に従って、幹細胞の脂肪生成および骨形成分化能を測定した。
【0050】
3−1:脂肪生成分化アッセイ
脂肪生成分化アッセイに関しては、まず、5個のADSCを12ウェルプレートに幡種し、成長培地中でコンフルエンスになるまで維持した。コンフルエンスになった後、培地は脂肪生成培地 (DMEM,イソブチルメチルキサンチン 0.5 mM、デキサメタゾン 1 mM、インスリン10 mM、インドメタシン200 mM、10%FBS)に交換し、細胞は4週間培養した。その後、ホルムアルデヒドのリン酸バッファー 養液 (4%; pH 7) で5分間処理し、Oil Red O (Sigma-Aldrich)で染色した。
【0051】
3−2:骨形成分化アッセイ
骨形成分化アッセイに関しては、脂肪形成分化アッセイと同様に、5個のADSCを培養した。コンフルエンスになった後、培地は骨形成培地(DMEM、デキサメタゾン 0.1 mM、アスコルベート−2−フォスフェート 50 mM、 β-グリセロフォスフェート 10 mM および10% FBS)に交換し、細胞は4週間培養した。その後、細胞はメタノールで固定化し、アリザリンレッドで染色した。
【0052】
脂肪生成分化アッセイおよび骨形成分化アッセイの結果、Oil red O陽性の細胞数およびアリザリンレッド陽性の細胞の数に関し、SSV−KLH処理群と、KLH単独処理群またはコントロールとは、有意な差が認められなかった。
この結果から、SSV−KLHの処理によって、ADSCの脂肪細胞および骨細胞への分化能は変化しないことが確認された。
【0053】
試験例4:間充織幹細胞(MSC)による細胞増殖抑制活性に対するSSV―KLHの影響の確認
4−1:MSCおよび脾臓細胞の取得
MSCは、上述のADSCの取得方法と同様の方法により取得した。
また、DAラットより脾臓を摘出し、ピンセットを用いて細胞塊をかき出した。得られた細胞塊をlysis buffer(150mM NH4Cl、15mM NaHCO3、0.1mM EDTA2Na [pH7.3])で懸濁し、遠心分離(1,500rpm、5min)することにより赤血球を除いた。得られた脾臓細胞は、PBSで2回洗浄後、細胞数をカウントした。
【0054】
4−2:MSCの細胞増殖抑制活性の確認
CMSE stock solution(5mM in DMSO)を脾臓細胞(1×107細胞/mL in PBS)にCFSE終濃度5mMとなるように添加し、得られた懸濁液を37℃で10分間インキュベートした。次に、得られた懸濁液に、これと等量の牛胎児血清(heat inactivated fetal bovine serum(FBS))を添加し、反応を停止した。得られた脾臓細胞を、培地(RPMI-1640 with 10% FBS, penicillin/storeptomycin 100 U/ml and 100 mg/ml, and 2mM L-glutamine)に再懸濁し、ADSCフリーあるいはコートした6ウェルプレートに1×106細胞/wellで播種した。次に、ConAを終濃度2.5ug/mlで添加し、三日後に細胞を回収し、Epics ALTA flow cytometerにて解析を行った。
一方、コントロールには、ConAおよびADSCのいずれも添加しなかった。
得られた細胞を、FSC(Forward scatter:前方散乱光)を用いたフローサイトメトリーにより測定し、図3A〜Iのグラフを得た。図3A〜Iにおいては、横軸は蛍光強度を示し、CFSEラベル化した脾臓細胞が増殖すると、CFSEの蛍光強度は減少し、ピークは左にシフトする。
【0055】
図3Aは、ConAおよびMSCのいずれも添加していない、コントロールをフローサイトメトリーで測定した結果である。図3Aにおいて、M1領域(97.5%)、M2領域(2.2%)として確認された。
図3Bは、ConAを添加した脾臓細胞をフローサイトメトリーで測定した結果である。図3Bにおいて、M2領域(34%)は増加し、M1領域(68.6%)は減少していた。
この結果から、ConAの添加により脾臓細胞の増殖が進行してCFSEの強度が減少した結果、ピークが左側にシフトしていることが確認された。
図3Cは、ConAおよびMSCを添加した脾臓細胞をフローサイトメトリーで測定した結果である。図3Cにおいて、M1領域は95.2%であり、M2領域は4.9%であり、図3Aと同水準であった。
この結果から、MSCは、ConAによる細胞増殖を抑制する作用を有することが確認された。
【0056】
4−3:SSV―KLHの添加による影響の確認
SSV―KLH(10、100または200ng/mL)で前処理したMSCと、ConAとを、4−1と同様の手法により、脾臓細胞に添加し、フローサイトメトリー測定を行った。
結果は、図3D〜Fに示される通りであった。SSV―KLHで前処理したMSCを用いても、未処理のMSCを用いた場合(図3C)と同様に、脾臓細胞の増殖は抑制されることが確認された。この結果から、SSV―KLHの添加は、脾臓細胞の増殖抑制活性に影響を与えないことが確認された。
【0057】
4−4:KLHの添加による影響の確認
KLH(10、100または200ng/mL)で前処理したMSCと、ConAとを、4−1と同様の手法により、脾臓細胞に添加し、フローサイトメトリー測定を行った。
結果は、図G〜Hに示される通りであった。KLHで前処理したMSCを用いても、未処理のMSCを用いた場合(図3C)と同様に脾臓細胞の増殖は抑制されることが確認された。この結果から、KLHの添加は、脾臓細胞の増殖抑制活性に影響を与えないことが確認された。
【技術分野】
【0001】
本発明は、幹細胞の効率的な増殖に用いうる、新規幹細胞増殖用組成物に関する。
【背景技術】
【0002】
幹細胞は、その優れた分化能に着目され、細胞療法や再生医療におけるその利用が従前期待されている。実際の組織再生等に利用する場合、大量の幹細胞を取得することが前提となる。しかしながら、幹細胞自体の取得はしばしば困難であり、その増殖効率も再生医療に用いるレベルに至らない場合が少なくない。
【0003】
例えば、間充織幹細胞(Mesenchymal stem cells;MSC)は非造血性の多能性幹細胞であり、通常、イン・ビトロにおいて3つの細胞系、骨芽細胞、脂肪細胞および軟骨細胞への分化能を示すことが知られている。MSCは、骨髄、臍帯血、脂肪組織、胎児肺、羊水、骨格筋から単離することが可能であるが、その取得量は少量である。しかしながら、イン・ビトロやエクス・ビボにおけるMSCの増殖率はいずれも満足なレベルには至らず、医療への応用は制限されている。
このように、幹細胞を効率的に増殖させる技術が依然として求められているといえる。
【0004】
一方、WO2006/025580号公報(特許文献1)において、本発明者らの一部は、免疫抑制剤として有用な抗ヒストンH1モノクローナル抗体と、ヒストンH1との結合を阻害するペプチドとして、SSVLYGGPPSAAで表されるアミノ酸配列を有するポリペプチドを開示し、このポリペプチドが免疫抑制剤として利用しうることが報告している。しかしながら、上記ポリペプチドの幹細胞に対する生理作用は何ら記載されていない。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】WO2006/025580号公報
【発明の概要】
【0006】
本発明者らは、今般、SSVLYGGPPSAAで表されるアミノ酸配列を有するペプチドまたはその誘導体が、優れた幹細胞増殖活性を有することを見出した。本発明は、かかる知見に基づくものである。
【0007】
したがって、本発明は、優れた幹細胞増殖活性を有する新規製剤を提供することをその目的とする。
【0008】
そして、本発明による幹細胞増殖用組成物は、以下の(a)または(b)に記載のポリペプチドまたはその誘導体を含んでなるものである:
(a)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列からなるポリペプチド、
(b)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列において1個または数個のアミノ酸が、欠失、置換、欠失、挿入または付加したアミノ酸配列からなり、幹細胞増殖活性を有する、ポリペプチド。
【0009】
また、本発明による幹細胞の増殖方法は、幹細胞と、上記ポリペプチドまたはその誘導体とを接触させて、幹細胞を増殖させることを含んでなる方法である。
【発明の効果】
【0010】
本発明による組成物によれば、幹細胞の増殖活性を効果的に増強することが可能となる。また、本発明による組成物は、幹細胞の表現型および分化能を安定に維持する上でも有利である。よって、本発明による幹細胞増殖用組成物は、細胞療法や再生医療において有利に利用しうる。
【図面の簡単な説明】
【0011】
【図1】脂肪由来幹細胞(ADSC)の増殖アッセイにおけるフローサイトメトリーの結果を示す。図1Aはコントロールであり、図1B〜DはSSV−KLH処理群であり、図1E〜GはKLH単独処理群である。また、図1における縦軸は細胞数を示し、横軸は経口強度を示す。
【図2】ADSCの表面抗原(CD29、CD44、 CD90、CD34およびCD45)の発現をフローサイトメトリーによって測定した結果を示す。図2Aはコントロールを示し、図2BはSSV−KLH処理群(SSV−KLH投与量:10ng/mL)を示し、図2CはKLH単独処理群(KLH投与量:10ng/mL)を示す。また、図2における縦軸は細胞数を示し、横軸は経口強度を示す。
【図3】Aは、CFSEで処理した脾臓細胞をフローサイトメトリーで測定した結果である。 Bは、CFSE処理の後、ConAが添加された脾臓細胞をフローサイトメトリーで測定した結果である。 Cは、CFSE処理の後、ConAおよび間充織幹細胞(MSC)が添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Dは、CFSE処理の後、ConA、およびSSV−KLH(10ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Eは、CFSE処理の後、ConA、およびSSV−KLH(100ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Fは、CFSE処理の後、ConA、およびSSV−KLH(200ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Gは、CFSE処理の後、ConA、およびKLH(10ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Hは、CFSE処理の後、ConA、およびKLH(100ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。 Iは、CFSE処理の後、ConA、およびKLH(200ng/mL)で前処理したMSCが添加された、脾臓細胞をフローサイトメトリーで測定した結果である。
【発明を実施するための形態】
【0012】
定義
本明細書において、「幹細胞」とは、分裂に伴って自己再生能を示すとともに、同時に性質の異なる細胞を生じる分化能を有する細胞をいう。
【0013】
また、本明細書において、「幹細胞増殖活性を有する」とは、下記の試験例1と実質的に同一の条件で幹細胞の増殖アッセイを行ったとき、試験例1と同一の統計比較方法において、幹細胞数が試験例1のコントロールに示されたレベルよりも有意に多いこと、好ましくはコントロールの約120%以上であることをいう。
【0014】
また、本明細書において、ポリペプチドの「誘導体」とは、ポリペプチドのアミノ末端(N末端)のアミノ基、および/または、ポリペプチドのカルボキシル末端(C末端)のカルボキシル基、および/または、ポリペプチドの各アミノ酸の側鎖の官能基(例えば、水素基、水酸基等)の一部もしくは全部が、適当な他の置換基によって修飾を受けたものをいう。適当な他の置換基による修飾は、例えば、ポリペプチド中に存在する官能基の保護、ポリペプチドの安全性および組織移行性の向上、またはポリペプチドの活性の増強等を目的として行われる。
【0015】
幹細胞増殖用組成物
本発明による幹細胞増殖用組成物は、幹細胞増殖活性を有する上記(a)または(b)に記載のポリペプチドを有効成分とすることを一つの特徴とする。(a)または(b)に記載のポリペプチドまたはその誘導体が、優れた幹細胞の増殖活性を示すことは意外な事実である。したがって、本発明の一つの態様によれば、幹細胞増殖剤の製造における、(a)または(b)に記載のポリペプチドまたはその誘導体の使用が提供される。
【0016】
(a)または(b)に記載のポリペプチドのうち、(b)に記載のポリペプチドにおいて、「1もしくは数個」の範囲は、好ましくは1〜3個、より好ましくは1〜2個程度を意味する。
【0017】
また、アミノ酸の保存的置換は、(b)に記載のポリペプチドを得るための好ましい手段のひとつである。ここで、保存的置換は、ポリペプチドの活性機能的同等性を確保し、かつ一般に交換された2つの残基の側鎖が化学的類似性を有することにより特徴付けられる。例えば、酸性残基は他の酸性残基により、塩基性残基は塩基性残基により、疎水性残基は疎水性残基により、バルキーな残基はバルキーな残基により、保存的に置き換えられることが好ましい。保存的置換としては、例えば、以下のグループ内での置換を包含する:セリンに対する置換としてスレオニン;バリンに対する置換としてロイシンまたはイソロイシン;ロイシンに対する置換としてイソロイシン、バリン、;チロシンに対する置換としてフェニルアラニン、トリプトファン;アラニンに対する置換としてグリシン。
【0018】
また、上記(a)または(b)に記載のポリペプチドは、上述の通り、幹細胞増殖活性を保持する限り、誘導体としてもよい。本発明に用いられるポリペプチドの誘導体としては、上記(a)または(b)に記載のポリペプチドにおいて、そのアミノ酸側鎖またはアミノ末端またはカルボキシル末端が修飾され、かつ所望の活性が保持されたポリペプチドが含まれる。好ましい態様によれば、上記誘導体は、ポリペプチドのアミノ末端がアシル化、アミド化もしくは糖修飾されたポリペプチドであるか、または前記ポリペプチドのカルボキシル末端がアミド化、エステル化もしくは糖修飾されたポリペプチドである。より好ましい態様によれば、上記誘導体は、ポリペプチドのアミノ末端がアシル化もしくはアミド化されたポリペプチドであるか、または前記ポリペプチドのカルボキシル末端がアミド化もしくはエステル化されたポリペプチドである。
【0019】
より具体的には、上記誘導体としては、例えば、(1)ポリペプチドのアミノ末端(N末端)のアミノ基が、置換または非置換のアルキル基(直鎖、分岐鎖または環状であってもよい)(例えば、メチル基、エチル基、プロピル基、イソプロピル基、イソブチル基、ブチル基、t−ブチル基、シクロプロピル基、シクロヘキシル基、ベンジル基)、置換または非置換のアシル基(例えば、ホルミル基、アセチル基、カプロイル基、シクロヘキシルカルボニル基、ベンゾイル基、フタロイル基、トシル基、ニコチノイル基、ピペリジンカルボニル基)、ウレタン型保護基(例えば、p−ニトロベンジルオキシカルボニル基、p−メトキシベンジルオキシカルボニル基、t−ブトキシカルボニル基)またはウレア型置換基(例えば、メチルアミノカルボニル基、フェニルカルボニル基、シクロヘキシルアミノカルボニル基)、糖(例えば、グルコース、ラクトース、マルトース)、リン脂質(例えば、ミリストイル基、パルミトイル基)、ポリエチレングリコール基等によって置換されたもの、並びに(2)ポリペプチドのカルボキシル末端(C末端)のカルボキシル基が、エステル化されているもの(例えば、その水素原子が、メチル、エチル、イソプロピル、シクロヘキシル、フェニル、ベンジル、t−ブチル、4−ピコリルにより置き換えられたもの)、アミド型の修飾を受けているもの(例えば、非置換アミド、C1〜C6アルキルアミド(メチルアミド、エチルアミド、イソプロピルアミド)を形成しているもの)、並びに(3)ポリペプチドのアミノ酸の側鎖の官能基(例えば、水素基、水酸基等)の一部もしくは全部が、上述のアミノ基と同様の置換基あるいはトリチル基等で修飾されたもの等が挙げられる。
【0020】
また、上記誘導体の他の好適な例としては、(a)または(b)に記載のポリペプチドと、薬学的に許容可能な担体との結合体が挙げられる。したがって、本発明の好ましい態様によれば、免疫アジュバントにおける誘導体は、薬学的に許容可能な担体を構成成分としてさらに含んでなる。上記担体としては、好ましくは、キーホールリンペットヘモシアニン(Keyhole limpet hemocyanin;KLH)、オボアルブミン(Ovalbumin;OVA)またはウシ血清アルブミン(Bovine Serum Albumin;BSA)であり、より好ましくはKLHである。(a)または(b)に記載のペプチドを、上述のような薬学的に許容可能な担体を用いて誘導化することは、幹細胞増殖活性を効果的に増強する上で有利である。
【0021】
また、本発明による組成物は、幹細胞増殖活性を有するポリペプチドまたはその誘導体と、その活性を実質的に阻害しない任意の成分とを含有する組成物として提供さすることができる。かかる任意の成分としては、例えば、結合剤、着色剤、乾燥剤、防腐剤、湿潤剤、安定剤、賦形剤、接着剤、可塑剤、粘着付与剤、増粘剤、パッチ材料、軟膏基材、角質除去剤、塩基性物質、吸収促進剤、脂肪酸、脂肪酸エステル、高級アルコール、界面活性剤、水、緩衝剤等が挙げられるが、好ましくは緩衝剤、軟膏基材、脂肪酸、防腐剤、塩基性物質または界面活性剤である。
【0022】
本発明による組成物において、上記(a)または(b)に記載のポリペプチドまたはその誘導体の含有量は、幹細胞の必要量、幹細胞の増殖能、投与形態等を勘案して適宜決定してよく、例えば、1〜100重量%である。
【0023】
また、本発明の幹細胞増殖用組成物は、任意の形状であり得る。本発明の造血幹細胞増殖用組成物は、例えば、錠剤、丸剤、カプセル剤、顆粒剤のような固体;または水溶液および懸濁液のような液体;またはゲル剤のような半固形としてもよい。また、後述する治療用途において、本発明の幹細胞増殖用組成物は、好ましくはRemington’s PharmaceuticalSciences, Mack Publishing社(Easton、PA)に記載されているような従来のポリペプチドの処方物の形で投与され得る。
【0024】
本発明による組成物の製造において、(a)または(b)に記載のポリペプチドは、人為的に合成してもよいが、人為的に合成する場合には、例えば、ペプチド固相合成法、ペプチド液相合成法等の公知のペプチド合成技術を使用することが可能である。
【0025】
また、(a)または(b)に記載のポリペプチドの誘導化は、例えば、Greene’s Protective Groups in Organic Synthesis, 4 th Edition, Peter G.M. Wuts et al, John Wiley & Sons, 2006等に記載の公知手法に基づき、(a)または(b)に記載のペプチドと、各種官能基導入剤を用いて製造することができる。
とりわけ、(a)または(b)に記載のポリペプチドと、薬学的に許容可能な担体とを結合する手法としては、例えば、公知のリンカーを用いる手法が挙げられる。このようなリンカーとしては、EDC(Ethylenedichloride)、カルボジイミド(DCC(dicyclohexyl carbodiimide)、DIC(1,3-diisopropyl carbodiimide))等の脱水縮合剤、グルタルアルデヒド、マレイミド、マレイミドベンゾイルオキシコハク酸等の架橋剤、PEG、リンカーペプチド等が挙げられるが、好ましくはカルボジイミドまたはグルタルアルデヒド等である。ペプチドと、担体とを結合する具体的な手法は、「ペプチド合成の基礎と実験」泉屋 信夫他著、丸善株式会社)に記載の方法等を参照されたい。
【0026】
本発明による組成物は、上述のようにして得られる(a)または(b)に記載のペプチドまたはその誘導体と、その剤形等に応じた各種成分とを適宜混合する等公知の手法により製造することができる。
【0027】
幹細胞の増殖方法
本発明のポリペプチドまたはその誘導体を用いると、上述の通り、幹細胞を効率的に増殖させることが可能である。したがって、一つの態様によれば、幹細胞と、本発明のポリペプチドまたはその誘導体とを接触させて、幹細胞を増殖させることを含んでなる、幹細胞の増殖方法が提供される。
【0028】
上記接触工程に用いられる具体的な手法は、幹細胞を増殖しうる限り特に限定されないが、好ましくは、インビトロにて行われる。好ましい態様によれば、上記接触は、幹細胞を本発明のポリペプチドまたはその誘導体を含む培地中で培養することを含んでなる。
【0029】
また、本発明のポリペプチドまたはその誘導体の有効量、および幹細胞の培養および回収の条件などは、幹細胞の種類、性質等に応じて、当業者により適宜選択され得る。
【0030】
治療用途
また、本発明による組成物は、幹細胞の増加が所望される対象の治療において、医薬として投与することができる。したがって、別の態様によれば、本発明のポリペプチドまたはその誘導体の有効量を患者に投与することを含んでなる、対象における幹細胞の増殖方法が提供される。
【0031】
本発明のポリペプチドまたはその誘導体は、例えば、経口投与、静脈投与、筋肉注射、腹腔内注射、および皮下注射のような非経口投与により対象に投与してもよい。本発明のポリペプチドまたはその誘導体を羊水中へ補充することも可能である。好ましくは、本発明のポリペプチドまたはその誘導体は注射によって対象に投与される。
【0032】
本発明のポリペプチドまたはその誘導体を投与する対象としては、それを必要とする限り特に限定されないが、哺乳動物であり、より好ましくはヒトである。
【0033】
本発明のポリペプチドまたはその誘導体の有効量は、当業者によって適宜決定される。例えば、ヒトに投与する場合、1日あたりの用量は、通常、患者の症状、重篤度、感受性に対する個体差、体重、年齢などを考慮して、当業者によって適切に決定され得る。本発明の造血幹細胞増殖剤は、1日1回投与されてもよいし、1日数回に分けて投与されてもよい。
【0034】
また、幹細胞は、本発明のポリペプチドまたはその誘導体により増殖しうる限り特に限定されず、好ましくは、前記幹細胞が、単能性幹細胞、複能性幹細胞、多能性幹細胞、胚性幹細胞(ES細胞)、体性幹細胞、臍帯血幹細胞または人工多能性幹細胞(iPS細胞)であり、より好ましくは、造血幹細胞、表皮基底膜の幹細胞、小腸粘膜上皮の幹細胞、間充織幹細胞(MSC)、脂肪由来幹細胞(ADSC)、骨髄由来細胞、臍帯血液由来幹細胞、胎児肺由来幹細胞、羊水由来幹細胞、骨格筋由来細胞、胚性幹細胞または人工多能性幹細胞等であり、さらに好ましくは間充織幹細胞(MSC)、脂肪由来幹細胞(ADSC)である。
また、幹細胞の由来する種としては、好ましくは哺乳動物であり、より好ましくはヒトである。
【0035】
なお、遺伝子治療においては、目的の遺伝子の導入効率は、遺伝子を細胞に導入工程で、どれだけ多数の細胞が分裂を行なっているかに左右されることが知られている。したがって、本発明のポリペプチドまたは誘導体を用いて幹細胞を増殖させつつ遺伝子を導入することにより、非常に高い遺伝子導入効率を得ることが可能である。したがって、本発明の別の好ましい態様によれば、上記いずれかの方法において、幹細胞に外来遺伝子が導入する工程を含んでなる。
【0036】
導入される外来遺伝子は、幹細胞の増殖を妨げない限り特に限定されず、プラスミドなどの公知のベクター等を用いて、幹細胞に導入することができる。
導入方法は、当該技術分野において公知の手法を用いることが可能であり、エレクトロポレーション、マイクロインジェクション、リポフェクション等が挙げられる。かkる導入方法は、幹細胞の種類、ベクターのサイズ、導入効率等を勘案して当業者によって適宜選択される。
【実施例】
【0037】
以下、本発明を実施例によって説明するが、本発明はこれら実施例に限定されない。
例1:幹細胞増殖剤の製造
配列番号1で表されるアミノ酸配列からなるペプチド(以下、「SSV」というは、Fmocペプチド固相合成法(製造装置;ABI430型アプライバイオシステムズ社製)により合成した。次に、SSV5mg、KLH20mgおよびグルタルアルデヒド 30μg(片山化学工業株式会社)(SIGMA社製)をリン酸緩衝液(pH 8.0)中、室温で約6時間撹拌し、SSVおよびKLHの結合体(以下、「SSV−KLH」という。)を得た。このSSV―KLHをPBSに溶解した溶液を、以下の試験において幹細胞増殖剤として用いた。
【0038】
試験例1:SSV―KLHの幹細胞増殖能に対する影響の確認1
以下の試験例において、LEW (RT11) ラット(オス)は、行政院国家科学委員会(台湾)から取得した。また、DA (主要組織適合複合体ハプロタイプ RT1a) ラット(オス)は、日本SLC株式会社(浜松)から取得した。実験中、総ての動物は、無菌動物施設内で飼育し、水および市販ラット用食品を不断給餌した。また、総ての動物実験は、Chang Gung Memorial Hospital-Kaohsiung Medical Center(台湾)のガイドラインに従って行った。
【0039】
また、細胞は、以下に記載の時点において収集し、PBSで連続的に適宜洗浄した。さらに、生存細胞数は、トリパンブルー染色(trypan blue exclusion method)および血球計によってカウントした。
【0040】
1−1:脂肪由来幹細胞(ADSC)の調製
LEWラット(8週齢)の腹部から脂肪組織を採取し、リン酸緩衝生理食塩水(PBS、 Sigma-Aldrich、St. Louis、MO)を含むペトリ皿に維持した。次に、脂肪組織をミンチにし、コラゲナーゼタイプII (0.25 mg/ml, Sigma-Aldrich)を含むハンクス液中で懸濁させた。次に、懸濁液がスムースで均一な状態になるまで、30−60分間、アジテーション(50 rpm)とともに37 ℃にて消化を行い、さらに、遠心分離により細胞のペレットを取得した。得られた細胞ペレットは、70μmナイロンメッシュで濾過し、赤血球溶解バッファーでインキュべートし、さらに、40μmで再度濾過した後、10%ウシ胎仔血清(FBS)、ならびにペニシリン/ストレプトマイシン 100U/ml および 100μg/ml (GIBCOTM Invitrogen Corporation, Carlsbad, CA, USA)を添加したDMEDの完全培地中で再懸濁した。得られた細胞は、約80%コンフルエンスの状態になるまで、3〜6日間、加湿された5%CO2インキュベーター中で維持し、ADSCの懸濁液を得た。
【0041】
1−2:脂肪由来幹細胞の増殖アッセイ
脂肪由来幹細胞(ADSC)は、繊維芽細胞の様な外観を有し、細胞集団形成から7日後に単層を形成した。プレートに粘着した細胞は、EDTA/トリプシン処理して取得した。取得したADSCを、2000細胞/cm2で24ウェルプレートに播種した。次に、ADSCに、50〜200ng/mlのSSV−KLH溶液またはKLH溶液を加え、15日間インキュベートした。この際、コントロールとして未処理群を用意した。
【0042】
1−3:吸光度測定
インキュベート後、各群の細胞は、細胞増殖剤WST-1 (Roche Molecular Biochemicals, Mannheim, Germany) を用いて処理し、 MRX マイクロプレートリーダー (Dynex Technologies, VA, USA) を用いて、450 nm および620 nmの吸光度を測定した。なお、以下の群間比較においては、一元配置分散分析(ANOVA)およびDuncan’s post hoc testを適宜用いた。また、記述統計学、平均、標準偏差および範囲についても適宜採用した。結果は、平均値 ± 標準偏差 (SD) を基準として、p<0.05 で有意差があるものとした。
【0043】
吸光度測定の結果、SSV−KLH処理群のADSCの数は、同投与量のKLH単独処理群またはコントロール群の約120%〜140%であった。
【0044】
試験例2:SSV―KLHの幹細胞増殖能に対する影響の確認2
2−1:フローサイトメトリー
CFSEのDMSO溶液を、間充織幹細胞(MSC;1×107細胞/mL in PBS)にCFSE終濃度5mMとなるように添加した。次に、得られた溶液を37℃で10分間インキュベートした。次に、得られた溶液に、これと等量の牛胎児血清(heat inactivated fetal bovine serum(FBS))を添加し、反応を停止した。1分後、溶液中のCFSEでラベル化されたMSCを洗浄後、得られた細胞の数をカウントした。得られたMSCを、培地(10% FBS 添加DMED、100U/mL ペニシリン および100ug/mL ストレプトマイシン)に5×105細胞/mLで播種した。さらに、MSCを24ウェルプレートに2000細胞/cm2で播種し、これに10〜200mg/mlのSSV−KLH溶液またはKLH溶液を加えた。3日後、細胞を回収し、Epics ALTA flow cytometerにて解析を行った。
【0045】
図1A〜Gは、各群のフローサイトメトリーの結果を示す図である。
ここで、図1Aはコントロール(処理なし)を示す。
また、図1BはSSV−KLH処理群(SSV−KLH投与量:10ng/mL)を示す。
また、図1CはSSV−KLH処理群(SSV−KLH投与量:100ng/mL)を示す。
また、図1DはSSV−KLH処理群(SSV−KLH投与量:200ng/mL)を示す。
また、図1EはKLH単独処理群(KLH投与量:10ng/mL)を示す。
また、図1FはKLH単独処理群(KLH投与量:100ng/mL)を示す。
また、図1GはKLH単独処理群(KLH投与量:100ng/mL)を示す。
【0046】
図1B〜Dに示される通り、SSV−KLH処理群では、蛍光強度が減少しており、全体の細胞のうち、CSFEラベルされた細胞の占める割合が低下していた。一方、図E〜Gに示される通り、KLH単独処理群ではコントロールと同様の蛍光パターンを示し、蛍光強度の変化は認められず、全体の細胞のうちCSFEラベルされた細胞の占める割合は変化しなかった。この結果から、SSV−KLH処理群では、細胞増殖が誘導されて全体の細胞数が増加し、KLH単独処理群では、細胞増殖が誘導されないことが確認された。
【0047】
1−3:ADSC特異的マーカーの確認
STEM CELLS 2007; 25:818-827に記載されている手法に準じて、増殖アッセイの前後において、SSV−KLH処理群、KLH単独処理群またはコントロールにおけるADSC特異的マーカーの発現をフローサイトメトリーによって測定した。
具体的には、増殖アッセイの前後において、各群における細胞を、ラットの、CD29、CD44、 CD90、CD45 (BD Biosciences Pharmingen, San Diego, CA, USA)、MHC I、MHC II (Serotec, Oxford, UK) およびCD34 (Santa Cruz Biotechnology, Santa Cruz, CA,USA)に対するマウスモノクローナル抗体を用いて免疫染色した。免疫染色後、coulter Epics(登録商標) ALTRA(登録商標)フローサイトメーター (Beckman Coulter, CA, USA) を用いて測定を行い、その分析にはEXP O32 ソフトウェア(Beckman Coulter)を用いた。
【0048】
ADSCの表面抗原(CD29、CD44、 CD90、CD34およびCD45)の発現を測定した結果は、図2に示される通りであった。
ここで、図2Aはコントロールを示す。また、図2BはSSV−KLH処理群を示す。また、図2CはKLH単独処理群を示す。
図2に示される通り、各群の細胞は、CD29、CD44およびCD90に対して陽性を示し、CD34およびCD45に対して陰性を示した。また、図示しなかったが、各群の細胞は、MHCIに対して陽性を示し、MHCIIに対して陰性を示した。
各群の細胞は、統計学的な比較においても、上記表面抗原の発現に関し、SSV−KLH処理群と、KLH単独処理群またはコントロールとは、有意な差は認められなかった。
この結果から、SSV−KLHによって処理した場合、ADSCの特異的マーカーの発現には変化がないことが確認された。
【0049】
試験例3:脂肪生成および骨形成分化アッセイ
SSV−KLH処理群、KLH処理群およびコントロールにおいて、以下の手順に従って、幹細胞の脂肪生成および骨形成分化能を測定した。
【0050】
3−1:脂肪生成分化アッセイ
脂肪生成分化アッセイに関しては、まず、5個のADSCを12ウェルプレートに幡種し、成長培地中でコンフルエンスになるまで維持した。コンフルエンスになった後、培地は脂肪生成培地 (DMEM,イソブチルメチルキサンチン 0.5 mM、デキサメタゾン 1 mM、インスリン10 mM、インドメタシン200 mM、10%FBS)に交換し、細胞は4週間培養した。その後、ホルムアルデヒドのリン酸バッファー 養液 (4%; pH 7) で5分間処理し、Oil Red O (Sigma-Aldrich)で染色した。
【0051】
3−2:骨形成分化アッセイ
骨形成分化アッセイに関しては、脂肪形成分化アッセイと同様に、5個のADSCを培養した。コンフルエンスになった後、培地は骨形成培地(DMEM、デキサメタゾン 0.1 mM、アスコルベート−2−フォスフェート 50 mM、 β-グリセロフォスフェート 10 mM および10% FBS)に交換し、細胞は4週間培養した。その後、細胞はメタノールで固定化し、アリザリンレッドで染色した。
【0052】
脂肪生成分化アッセイおよび骨形成分化アッセイの結果、Oil red O陽性の細胞数およびアリザリンレッド陽性の細胞の数に関し、SSV−KLH処理群と、KLH単独処理群またはコントロールとは、有意な差が認められなかった。
この結果から、SSV−KLHの処理によって、ADSCの脂肪細胞および骨細胞への分化能は変化しないことが確認された。
【0053】
試験例4:間充織幹細胞(MSC)による細胞増殖抑制活性に対するSSV―KLHの影響の確認
4−1:MSCおよび脾臓細胞の取得
MSCは、上述のADSCの取得方法と同様の方法により取得した。
また、DAラットより脾臓を摘出し、ピンセットを用いて細胞塊をかき出した。得られた細胞塊をlysis buffer(150mM NH4Cl、15mM NaHCO3、0.1mM EDTA2Na [pH7.3])で懸濁し、遠心分離(1,500rpm、5min)することにより赤血球を除いた。得られた脾臓細胞は、PBSで2回洗浄後、細胞数をカウントした。
【0054】
4−2:MSCの細胞増殖抑制活性の確認
CMSE stock solution(5mM in DMSO)を脾臓細胞(1×107細胞/mL in PBS)にCFSE終濃度5mMとなるように添加し、得られた懸濁液を37℃で10分間インキュベートした。次に、得られた懸濁液に、これと等量の牛胎児血清(heat inactivated fetal bovine serum(FBS))を添加し、反応を停止した。得られた脾臓細胞を、培地(RPMI-1640 with 10% FBS, penicillin/storeptomycin 100 U/ml and 100 mg/ml, and 2mM L-glutamine)に再懸濁し、ADSCフリーあるいはコートした6ウェルプレートに1×106細胞/wellで播種した。次に、ConAを終濃度2.5ug/mlで添加し、三日後に細胞を回収し、Epics ALTA flow cytometerにて解析を行った。
一方、コントロールには、ConAおよびADSCのいずれも添加しなかった。
得られた細胞を、FSC(Forward scatter:前方散乱光)を用いたフローサイトメトリーにより測定し、図3A〜Iのグラフを得た。図3A〜Iにおいては、横軸は蛍光強度を示し、CFSEラベル化した脾臓細胞が増殖すると、CFSEの蛍光強度は減少し、ピークは左にシフトする。
【0055】
図3Aは、ConAおよびMSCのいずれも添加していない、コントロールをフローサイトメトリーで測定した結果である。図3Aにおいて、M1領域(97.5%)、M2領域(2.2%)として確認された。
図3Bは、ConAを添加した脾臓細胞をフローサイトメトリーで測定した結果である。図3Bにおいて、M2領域(34%)は増加し、M1領域(68.6%)は減少していた。
この結果から、ConAの添加により脾臓細胞の増殖が進行してCFSEの強度が減少した結果、ピークが左側にシフトしていることが確認された。
図3Cは、ConAおよびMSCを添加した脾臓細胞をフローサイトメトリーで測定した結果である。図3Cにおいて、M1領域は95.2%であり、M2領域は4.9%であり、図3Aと同水準であった。
この結果から、MSCは、ConAによる細胞増殖を抑制する作用を有することが確認された。
【0056】
4−3:SSV―KLHの添加による影響の確認
SSV―KLH(10、100または200ng/mL)で前処理したMSCと、ConAとを、4−1と同様の手法により、脾臓細胞に添加し、フローサイトメトリー測定を行った。
結果は、図3D〜Fに示される通りであった。SSV―KLHで前処理したMSCを用いても、未処理のMSCを用いた場合(図3C)と同様に、脾臓細胞の増殖は抑制されることが確認された。この結果から、SSV―KLHの添加は、脾臓細胞の増殖抑制活性に影響を与えないことが確認された。
【0057】
4−4:KLHの添加による影響の確認
KLH(10、100または200ng/mL)で前処理したMSCと、ConAとを、4−1と同様の手法により、脾臓細胞に添加し、フローサイトメトリー測定を行った。
結果は、図G〜Hに示される通りであった。KLHで前処理したMSCを用いても、未処理のMSCを用いた場合(図3C)と同様に脾臓細胞の増殖は抑制されることが確認された。この結果から、KLHの添加は、脾臓細胞の増殖抑制活性に影響を与えないことが確認された。
【特許請求の範囲】
【請求項1】
以下の(a)または(b)に記載のポリペプチドまたはその誘導体含んでなる、幹細胞増殖用組成物:
(a)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列からなるポリペプチド、
(b)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列において1個または数個のアミノ酸が、欠失、置換、欠失、挿入または付加したアミノ酸配列からなり幹細胞増活性を有する、ポリペプチド。
【請求項2】
前記(b)に記載のポリペプチドにおける1個または数個のアミノ酸が、1〜3個である、請求項1に記載の幹細胞増殖用組成物。
【請求項3】
前記誘導体が、前記ポリペプチドのアミノ末端がアシル化もしくはアミド化されたポリペプチドであるか、または前記ポリペプチドのカルボキシル末端がアミド化もしくはエステル化されたポリペプチドである、請項1に記載の組成物。
【請求項4】
前記誘導体が、前記ポリペプチドと薬学上許容可能な担体との結合体である、請求項1に記載の組成物。
【請求項5】
前記担体が、キーホールリンペットヘモシアニン、オボアルブミンまたはウシ血清アルブミンである、請項4に記載の組成物。
【請求項6】
前記担体が、キーホールリンペットヘモシアニンである、請項5に記載の組成物。
【請求項7】
前記幹細胞が、単能性幹細胞、複能性幹細胞、多能性幹細胞、胚性幹細胞、体性幹細胞、臍帯血幹細胞、人工多能性幹細胞からなる群から選択されるものである、請求項1に記載の組成物。
【請求項8】
医薬として用いられる、請求項1に記載の組成物。
【請求項9】
幹細胞と、請求項1に記載のポリペプチドまたはその誘導体とを接触させて、前記幹細胞を増殖させること含んでなる、幹細胞の増殖方法。
【請求項10】
前記接触が、前記幹細胞を請求項1に記載のポリペプチドまたはその誘導体を含む培地中で培養することを含んでなる、請求項9に記載の方法。
【請求項11】
前記接触中に、前記幹細胞に外来遺伝子を導入することをさらに含んでなる、請求項9に記載の方法。
【請求項12】
前記幹細胞が、単能性幹細胞、複能性幹細胞、多能性幹細胞、胚性幹細胞、体性幹細胞、臍帯血幹細胞、人工多能性幹細胞からなる群から選択されるものである、請求項9に記載の方法。
【請求項1】
以下の(a)または(b)に記載のポリペプチドまたはその誘導体含んでなる、幹細胞増殖用組成物:
(a)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列からなるポリペプチド、
(b)SSVLYGGPPSAA(配列番号1)で表されるアミノ酸配列において1個または数個のアミノ酸が、欠失、置換、欠失、挿入または付加したアミノ酸配列からなり幹細胞増活性を有する、ポリペプチド。
【請求項2】
前記(b)に記載のポリペプチドにおける1個または数個のアミノ酸が、1〜3個である、請求項1に記載の幹細胞増殖用組成物。
【請求項3】
前記誘導体が、前記ポリペプチドのアミノ末端がアシル化もしくはアミド化されたポリペプチドであるか、または前記ポリペプチドのカルボキシル末端がアミド化もしくはエステル化されたポリペプチドである、請項1に記載の組成物。
【請求項4】
前記誘導体が、前記ポリペプチドと薬学上許容可能な担体との結合体である、請求項1に記載の組成物。
【請求項5】
前記担体が、キーホールリンペットヘモシアニン、オボアルブミンまたはウシ血清アルブミンである、請項4に記載の組成物。
【請求項6】
前記担体が、キーホールリンペットヘモシアニンである、請項5に記載の組成物。
【請求項7】
前記幹細胞が、単能性幹細胞、複能性幹細胞、多能性幹細胞、胚性幹細胞、体性幹細胞、臍帯血幹細胞、人工多能性幹細胞からなる群から選択されるものである、請求項1に記載の組成物。
【請求項8】
医薬として用いられる、請求項1に記載の組成物。
【請求項9】
幹細胞と、請求項1に記載のポリペプチドまたはその誘導体とを接触させて、前記幹細胞を増殖させること含んでなる、幹細胞の増殖方法。
【請求項10】
前記接触が、前記幹細胞を請求項1に記載のポリペプチドまたはその誘導体を含む培地中で培養することを含んでなる、請求項9に記載の方法。
【請求項11】
前記接触中に、前記幹細胞に外来遺伝子を導入することをさらに含んでなる、請求項9に記載の方法。
【請求項12】
前記幹細胞が、単能性幹細胞、複能性幹細胞、多能性幹細胞、胚性幹細胞、体性幹細胞、臍帯血幹細胞、人工多能性幹細胞からなる群から選択されるものである、請求項9に記載の方法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2011−116715(P2011−116715A)
【公開日】平成23年6月16日(2011.6.16)
【国際特許分類】
【出願番号】特願2009−276875(P2009−276875)
【出願日】平成21年12月4日(2009.12.4)
【出願人】(507330730)学校法人 城西大学 (2)
【Fターム(参考)】
【公開日】平成23年6月16日(2011.6.16)
【国際特許分類】
【出願日】平成21年12月4日(2009.12.4)
【出願人】(507330730)学校法人 城西大学 (2)
【Fターム(参考)】
[ Back to top ]

