微小凝集粒子及びその製造方法
【課題】医薬物質を含有し、長時間に渡って持続する薬効を有し、また、含まれるポリマーの種類を選択することにより薬効の開始される時間及び/又は薬効の持続期間等を調節することのできる、数μm程度の大きさを有する微小凝集粒子及びその製造方法を提供すること。
【解決手段】極性基含有の(メタ)アクリル酸系ポリマーの分散相中に医薬物質粒子が分散して成ることを特徴とする微小凝集粒子、及び極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを含有する極性溶媒溶液と超臨界流体と接触させることを特徴とする前記微小凝集粒子の製造方法。
【解決手段】極性基含有の(メタ)アクリル酸系ポリマーの分散相中に医薬物質粒子が分散して成ることを特徴とする微小凝集粒子、及び極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを含有する極性溶媒溶液と超臨界流体と接触させることを特徴とする前記微小凝集粒子の製造方法。
【発明の詳細な説明】
【技術分野】
【0001】
この発明は微小凝集粒子及びその製造方法に関し、さらに詳しくは、医薬物質を含有し、長時間に渡って持続する薬効を有し、また、含まれるポリマーの種類を選択することにより薬効の開始される時間及び/又は薬効の持続期間等を調節することのできる、数μm程度の大きさを有する微小凝集粒子及びその製造方法に関する。
【背景技術】
【0002】
一般に、マイクロパーティクルと称される微小粒子が知られている(非特許文献1参照)。この非特許文献1によると、
『5.2 複合マイクロパーティクルの定義とその記述
マイクロパーティクルは様々の構造を有する(図11)。
・不規則な幾何学的構造を有する粒子であって、マトリックス中に埋め込まれた分子状の分散固体又は凝集体の形態を有する活性物質から成る粒子。それらは、「マイクロスフェア」と称される。;
・幾何学的に球状をなす粒子であって、固体ポリマーにより、又はタンパク質様殻により囲まれた活性物質のコアからなる粒子。それらは、「マイクロカプセル」と称される。』
との記載があり(非特許文献1の第211頁左欄第8行〜第19行参照)、
また、非特許文献1の第212頁左欄第19行〜第35行には、
『5.3.3 SAS(supercritical anti-solvent 超臨界貧溶媒)法
有機溶媒に溶解され、又は分散された活性物質及びキャリヤーが、一緒に又は別々に貧溶媒に噴霧される。貧溶媒は溶媒を吸収して、マイクロ粒子が形成される。
【0003】
例
・シュワルツ ファールマ(Schwarz Pharma)は、活性物質とキャリヤーとを含有する溶液を超臨界流体に接触させるマイクロスフェアの形成方法に、特許された[1]。結果として超臨界溶液が、粒子形成に至る圧力に減圧される。その特許は、流体が互いに接触されることのできる種々の方法を開示し、接触段階中に又は接触段階後に粒子の形成されることを記述している。』
との記載がある。
【0004】
前記非特許文献1に引用された特許[1]は、欧州特許(特許文献1)であり、その欧州特許は日本の公開公報(特許文献2)に対応する。
【0005】
特許文献2によると、その特許請求の範囲には、
『1つまたは2つ以上の有効成分を含む液体状媒質を、液体状の気体と接触させ、液体を液体状の気体から分離し、液体状の媒質から開放された有効成分/担体−組成物を得ることを特徴とする、1つまたは2つ以上の有効成分および1つまたは2つ以上の担体を含む組成物を製造するための方法。』
が開示されている。
【0006】
この特許文献2には、さらに、
『 発明に従って使用できる担体はポリマー材料である』(特許文献2の第4頁左上欄第6行)』、
『 液状気体は、特定の圧力/温度の組み合わせで、担体としてのポリマー、脂質、レシチンあるいはワックスに対しての溶解能力を示す。』(特許文献2の第5頁左上欄第11行〜第13行参照)、
『 例1(殺菌)各1gのd、l(+)−ポリラクチドに、次に示す病原菌を特定量移植する。
・・・・(省略)・・・
汚染したポリマーの試料をCO2で140バール、50℃および140バール/40℃で、12hないし0.5h静止状態で処理した。』(非特許文献2の第5頁右上欄第4行〜第17行参照)、
の記載がある。したがって、この特許文献2には、担体として使用されるポリマー材料の例としてポリペプチドという具体的な記載があるものの、それ以外の具体的開示が見あたらない。
【0007】
この特許文献2に、以下の記載がある。
『・・・噴霧は、焼結金属製のノズル(孔径約5〜10μm)を通して行う。数cmの落下距離の後に、中空の球(約100μm)でできた乾燥した粉体が得られる(図2)。この中空球は、恐らく10μmまでの大きさの一次滴剤を調整する下位単位で構成されている。』
との記載がある。
【0008】
非特許文献1によるとシュワルツ ファールマの特許は「流体が互いに接触されることのできる種々の方法を開示し、接触段階中に又は接触段階後に粒子の形成されることを記述している。」と紹介されているが、シュワルツ ファールマの特許原典に当たってみると、中空の球(約100μm)でできた乾燥した粉体が製造されることが開示されているのであって、マイクロスフェアの製造方法に関する具体的記述を見いだすことができない。
【0009】
ところで、超臨界流体を用いた微量粒子コーティングに関する記述のある特許文献3がある。この特許文献3に記載された発明は、「超臨界流体を用い、タンパク質などの有機物質または有機物質を含む無機物質との混合物ならびに化合物を、高分子などの有機物質または、その化合物でコーティングし、微小コーティング微粒子を製造し、食品、医薬品を保存したり、機能性食品、機能性薬剤、化粧品、微小画像素子、トナー、微小有機無機複合体などの機能性材料として使用する」ことに関する。この特許文献3に記載された方法によると、医薬物質から成る粒子の表面を超臨界流体によりコーティングすることができる。しかしながら、医薬物質から成る粒子の表面を例えば高分子などの有機物質でコーティングして成る微小粒子を経口投与用の薬剤として用いる場合、コーティング膜が溶解してから内部の医薬物質が露呈して医薬効果が発現されるので、コーティング膜を形成する材質の選定、及びコーティング膜の厚み等を適正に選択しなければならないと言う問題がある。
【0010】
特許文献4には、超臨界流体技術を利用して、活性物質をポリマーの層で被覆してなる種類のマクロカプセルを製造する方法が、開示されている。この特許文献4にはマイクロスフィアとマイクロカプセルとは本質的に違うものであるとの認識が示されている(特許文献4の第7頁第26行〜第27行参照)。さらに、この特許文献4には、マイクロスフィアを開示する文献として特許文献5を紹介している。
【0011】
特許文献5に開示された方法は、加水分解性ポリマーであるポリラクチド等と活性物質とを溶解する溶液を超臨界流体に噴霧することによりマイクロパーティクルを製造する方法である。この特許文献5に記載された方法により製造されるマイクロパーティクルは加水分解性ポリマーを使用しているので、活性物質として医薬物質を含有するマイクロパーティクルを医薬品として経口投与すると、胃や腸のどの部位で加水分解性ポリマーが分解するか予測がつかず、したがって、体内の所定の箇所で活性物質の薬効を働かせることができないという問題がある。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】EP0322687
【特許文献2】特開平2−4439号公報
【特許文献3】特開平11−197494号公報
【特許文献4】特表2001−504452号公報
【特許文献5】US5424076
【非特許文献】
【0013】
【非特許文献1】J.Jung.M.Perrut / J. of Suipercritical Fluids 20(2001)179-219
【発明の概要】
【発明が解決しようとする課題】
【0014】
この発明の目的は、医薬物質による医薬効果の持続性に優れたマイクロスフェアである微小凝集粒子及びその製造方法を提供することにある。
【課題を解決するための手段】
【0015】
前記課題を解決するための手段は、極性基含有の(メタ)アクリル酸系ポリマーの分散相中に医薬物質粒子が分散して成ることを特徴とする微小凝集粒子であり、
前記課題を解決するための他の手段は、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを含有する極性溶媒溶液と超臨界流体と接触させることを特徴とする微小凝集粒子の製造方法である。
【発明の効果】
【0016】
この発明に係る微小凝集粒子は、分散相である極性基含有の(メタ)アクリル酸系ポリマー中に医薬物質粒子が分散してなる、いわゆるマイクロスフェアの構造を有する微小凝集粒子である。医薬物質は通常極性基をその分子構造内に含有する。したがって、極性基含有の(メタ)アクリル酸系ポリマーにおける極性基と医薬物質における極性基とが親和性を有することにより、マイクロスフェア中の医薬物質は単に分散状態で存在するのではなく、静電引力により分散相に結合することになる。したがって、この微小凝集粒子を例えば経口投与すると、直ちに体内で医薬物質が微小凝集粒子から放出されることがなく、徐々に放出されることになる。故に、この微小凝集粒子は、医薬物質による薬効が長期間に渡って持続することになる。
【0017】
この発明に係る微小凝集粒子の製造方法においては、極性有機溶媒に、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを溶解する。有機溶媒、(メタ)アクリル酸系ポリマー及び医薬物質はいずれも極性基を含有するので、極性有機溶媒に、極性基含有の(メタ)アクリル酸系ポリマー及び医薬物質はともに良く溶解する。極性有機溶媒に極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを溶解して得られる極性溶媒溶液と、超臨界流体とを接触させると、超臨界流体中に極性有機溶媒が拡散し、一方、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とが微粉化する。この微粉化において、極性基含有の(メタ)アクリル酸系ポリマー中に医薬物質が微粒子状に分散してなる微粒子が形成される。
【図面の簡単な説明】
【0018】
【図1】図1はこの発明の方法を実施する一例である微小凝集粒子製造装置を示す概略説明図である。
【発明を実施するための形態】
【0019】
この発明について図面を参照しながら説明する。なお、この発明は図1に示される装置により製造される方法に限定されるものでないことは、言うまでもない。
【0020】
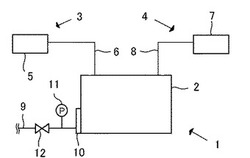
図1に示されるように、微小凝集粒子を製造する微小凝集粒子製造装置1は、耐圧容器2と、極性溶媒溶液を調製する溶液調製手段3と、超臨界流体を前記耐圧容器2に供給する超臨界流体供給手段4とを有する。
【0021】
耐圧容器2は超臨界流体を超臨界状態で保持することができる耐圧製の槽で形成される。ここで、超臨界流体としては、酸化窒素、二酸化炭素、ハロゲン化炭化水素、飽和炭化水素、不飽和炭化水素、二酸化二窒素、アンモニア及びこれらの混合物等を挙げることができる。この発明において好適な超臨界流体は、二酸化炭素である。二酸化炭素の臨界温度Tcが304.21Kであり、臨界圧力Pcが7.3825MPaであるので、取り扱いに利便性があるからである。
【0022】
前記溶液調製手段3は、調製槽5と、この調製槽5で調製された極性溶媒溶液を耐圧容器2に移送する移送路6と、移送路6の途中に介装された、図示しない溶液移送手段例えばポンプと、移送路6の途中に介装された、図示しない開閉弁とを備える。この調製槽5には、所定量の極性溶媒と、所定量の極性基含有の(メタ)アクリル酸系ポリマーと、所定量の医薬物質とが投入され、これらが混合されて極性溶媒溶液がこの調製槽6内で調製され、保存される。
【0023】
ここで、前記極性基含有の(メタ)アクリル酸系ポリマーとしては、例えば、第4級アンモニウム基を有するアクリル酸及びメタアクリル酸をモノマー単位として含有する第4級アンモニウム基含有(メタ)アクリル酸系ポリマー、アミノ基を含有するアクリル酸及びメタアクリル酸をモノマー単位として含有するアミノ基含有(メタ)アクリル酸系ポリマー、並びにカルボキシル基を含有するアクリル酸及びメタアクリル酸をモノマー単位として含有するカルボキシル基含有(メタ)アクリル酸系ポリマー等を挙げることができる。これらの中でも好ましいのは、アミノ基含有(メタ)アクリル酸系ポリマーであり、特にメタクリル酸メチル、メタクリル酸ブチル及びメタクリル酸ジメチルアミノエチルの共重合体(「オイドラギッド100」(登録商標)として入手可能)である。
【0024】
前記極性溶媒としては、メタノール、エタノール、プロパノール、ブタノール等の低級アルコール類、シクロヘキサン等のケトン類、酢酸エチル等のカルボン酸アルキルエステル類、並びに、水/低級アルコール類及びアセトン類/アルコール類等の混合溶媒等を挙げることができる。これら各種の極性溶媒の中でも低級アルコール類が好ましく、特にメタノール及びエタノールが好ましい。前記医薬物質としては、特に制限がなく、例えば鎮痛薬、解熱薬、アスピリン及びその誘導体、抗生物質、抗炎症薬、抗潰瘍薬、抗圧薬、神経弛緩薬、抗鬱薬等を挙げることができる。これら医薬物質の中でも3級アミノ基を含有する医薬品例えば塩酸ジフェニドール及び塩酸ジフェンヒドラミン等が好ましい。
【0025】
極性溶媒溶液を調製する際の、医薬物質(A)と極性基含有の(メタ)アクリル酸系ポリマー(B)との比率(重量比)[(B)/(A)]は、好適には1〜1.5である。前記重量比[(B)/(A)]が前記下限値よりも小さいと、この発明の方法によっても針状の粒子が形成されることがあり、前記重量比[(B)/(A)]が前記上限値よりも大きいと、この発明の方法によっても微小凝集粒子の粒径にバラつきが生じることがある。また、前記重量比[(B)/(A)]が前記範囲内にあると、粒径が0.1〜0.5μmの範囲内にある球状の凝集粒子が好適に形成される。
【0026】
前記極性溶媒溶液は、前記調製槽5内を適宜に加熱し、また必要に応じて攪拌することにより調製することができる。
【0027】
超臨界流体供給手段4は、超臨界流体を貯留する超臨界流体貯留槽7と、超臨界流体貯留槽7内の超臨界流体を前記耐圧容器2に移送する移送路8と、移送路8の途中に介装された、図示しない溶液移送手段例えばポンプと、移送路8の途中に介装された、図示しない開閉弁とを備える。
【0028】
前記耐圧容器2には、排出路9が接続される。この排出路9が前記耐圧容器2に接続されて開口する開口部(図示せず。)には、フィルター10が取り付けられる。フィルター10から外側に延在する排出路9には、圧力計11及び開閉弁12が装着されている。
【0029】
このフィルター10としては、この発明に係る微小凝集粒子を好適に捕集するために、例えば焼結フィルター及びガラスフィルター等で形成される。
【0030】
以上構成の微小凝集粒子製造装置1を用いて微小凝集粒子が次のようにして製造される。
【0031】
超臨界流体供給手段4により、耐圧容器2内に超臨界流体を充填する。耐圧容器2内では超臨界流体が超臨界状態で貯留される。その耐圧容器2内に、調製槽5で調製されたところの、極性溶媒に極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを溶解してなる一定量の極性溶媒溶液を、供給する。供給された極性溶媒溶液中の溶媒が超臨界流体中に直ちに拡散し、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とが固化し、微粒子化する。次いで、さらに耐圧容器2内に一定量の超臨界流体を供給する。耐圧容器2内の圧力が超臨界流体の供給により高くなると、その圧力上昇分だけ開閉弁12を開放し、耐圧容器2内の圧力一定に保持する。この動作を繰り返して耐圧容器2内を超臨界流体で置換する。(メタ)アクリル酸系ポリマーを分散相とし、この分散相中に医薬物質が粒子状に分散してなる微小凝集粒子が耐圧容器2内に生成する。
【0032】
耐圧容器2内の圧力は圧力計11により監視される。耐圧容器2内が超臨界流体で十分に置換された後に、開閉弁12が開放されて耐圧容器2内の超臨界流体が排出管9を通じて排出される。超臨界流体が排出管9により排出されるとフィルター10により耐圧容器2内に生成した微小凝集粒子が捕集される。
【0033】
また、図1に示される微小凝集粒子製造装置1を用いて次のようにして連続的に微小凝集粒子を製造することができる。
【0034】
すなわち、耐圧容器2の内部に超臨界流体貯留槽7から超臨界流体例えば二酸化炭素を充填する。耐圧容器2内の二酸化炭素を超臨界状態に維持する。このような耐圧容器2内に極性溶媒溶液と超臨界流体とを一定の比率で注入する。そうすると、耐圧容器2内で医薬物質が析出する。耐圧容器2内に超臨界流体を注入し、耐圧容器2内の圧力が一定となるように開閉弁12の開閉を調節して耐圧容器2内の圧力を一定に保持する。超臨界流体を耐圧容器2内に供給し続けることにより耐圧容器2内が超臨界流体で充分に置換される。その後に、開閉弁12を開放すると、(メタ)アクリル酸系ポリマーを分散相とし、この分散相中に医薬物質が粒子状に分散してなる微小凝集粒子がフィルターに捕集される。
【符号の説明】
【0035】
1・・・微小凝集粒子製造装置
2・・・耐圧容器
3・・・溶液調製手段
4・・・超臨界流体供給手段
5・・・調製槽
6・・・移送路
7・・・超臨界流体貯留槽
8・・・移送路
9・・・排出路
10・・・フィルター
11・・・圧力計
12・・・開閉弁
【技術分野】
【0001】
この発明は微小凝集粒子及びその製造方法に関し、さらに詳しくは、医薬物質を含有し、長時間に渡って持続する薬効を有し、また、含まれるポリマーの種類を選択することにより薬効の開始される時間及び/又は薬効の持続期間等を調節することのできる、数μm程度の大きさを有する微小凝集粒子及びその製造方法に関する。
【背景技術】
【0002】
一般に、マイクロパーティクルと称される微小粒子が知られている(非特許文献1参照)。この非特許文献1によると、
『5.2 複合マイクロパーティクルの定義とその記述
マイクロパーティクルは様々の構造を有する(図11)。
・不規則な幾何学的構造を有する粒子であって、マトリックス中に埋め込まれた分子状の分散固体又は凝集体の形態を有する活性物質から成る粒子。それらは、「マイクロスフェア」と称される。;
・幾何学的に球状をなす粒子であって、固体ポリマーにより、又はタンパク質様殻により囲まれた活性物質のコアからなる粒子。それらは、「マイクロカプセル」と称される。』
との記載があり(非特許文献1の第211頁左欄第8行〜第19行参照)、
また、非特許文献1の第212頁左欄第19行〜第35行には、
『5.3.3 SAS(supercritical anti-solvent 超臨界貧溶媒)法
有機溶媒に溶解され、又は分散された活性物質及びキャリヤーが、一緒に又は別々に貧溶媒に噴霧される。貧溶媒は溶媒を吸収して、マイクロ粒子が形成される。
【0003】
例
・シュワルツ ファールマ(Schwarz Pharma)は、活性物質とキャリヤーとを含有する溶液を超臨界流体に接触させるマイクロスフェアの形成方法に、特許された[1]。結果として超臨界溶液が、粒子形成に至る圧力に減圧される。その特許は、流体が互いに接触されることのできる種々の方法を開示し、接触段階中に又は接触段階後に粒子の形成されることを記述している。』
との記載がある。
【0004】
前記非特許文献1に引用された特許[1]は、欧州特許(特許文献1)であり、その欧州特許は日本の公開公報(特許文献2)に対応する。
【0005】
特許文献2によると、その特許請求の範囲には、
『1つまたは2つ以上の有効成分を含む液体状媒質を、液体状の気体と接触させ、液体を液体状の気体から分離し、液体状の媒質から開放された有効成分/担体−組成物を得ることを特徴とする、1つまたは2つ以上の有効成分および1つまたは2つ以上の担体を含む組成物を製造するための方法。』
が開示されている。
【0006】
この特許文献2には、さらに、
『 発明に従って使用できる担体はポリマー材料である』(特許文献2の第4頁左上欄第6行)』、
『 液状気体は、特定の圧力/温度の組み合わせで、担体としてのポリマー、脂質、レシチンあるいはワックスに対しての溶解能力を示す。』(特許文献2の第5頁左上欄第11行〜第13行参照)、
『 例1(殺菌)各1gのd、l(+)−ポリラクチドに、次に示す病原菌を特定量移植する。
・・・・(省略)・・・
汚染したポリマーの試料をCO2で140バール、50℃および140バール/40℃で、12hないし0.5h静止状態で処理した。』(非特許文献2の第5頁右上欄第4行〜第17行参照)、
の記載がある。したがって、この特許文献2には、担体として使用されるポリマー材料の例としてポリペプチドという具体的な記載があるものの、それ以外の具体的開示が見あたらない。
【0007】
この特許文献2に、以下の記載がある。
『・・・噴霧は、焼結金属製のノズル(孔径約5〜10μm)を通して行う。数cmの落下距離の後に、中空の球(約100μm)でできた乾燥した粉体が得られる(図2)。この中空球は、恐らく10μmまでの大きさの一次滴剤を調整する下位単位で構成されている。』
との記載がある。
【0008】
非特許文献1によるとシュワルツ ファールマの特許は「流体が互いに接触されることのできる種々の方法を開示し、接触段階中に又は接触段階後に粒子の形成されることを記述している。」と紹介されているが、シュワルツ ファールマの特許原典に当たってみると、中空の球(約100μm)でできた乾燥した粉体が製造されることが開示されているのであって、マイクロスフェアの製造方法に関する具体的記述を見いだすことができない。
【0009】
ところで、超臨界流体を用いた微量粒子コーティングに関する記述のある特許文献3がある。この特許文献3に記載された発明は、「超臨界流体を用い、タンパク質などの有機物質または有機物質を含む無機物質との混合物ならびに化合物を、高分子などの有機物質または、その化合物でコーティングし、微小コーティング微粒子を製造し、食品、医薬品を保存したり、機能性食品、機能性薬剤、化粧品、微小画像素子、トナー、微小有機無機複合体などの機能性材料として使用する」ことに関する。この特許文献3に記載された方法によると、医薬物質から成る粒子の表面を超臨界流体によりコーティングすることができる。しかしながら、医薬物質から成る粒子の表面を例えば高分子などの有機物質でコーティングして成る微小粒子を経口投与用の薬剤として用いる場合、コーティング膜が溶解してから内部の医薬物質が露呈して医薬効果が発現されるので、コーティング膜を形成する材質の選定、及びコーティング膜の厚み等を適正に選択しなければならないと言う問題がある。
【0010】
特許文献4には、超臨界流体技術を利用して、活性物質をポリマーの層で被覆してなる種類のマクロカプセルを製造する方法が、開示されている。この特許文献4にはマイクロスフィアとマイクロカプセルとは本質的に違うものであるとの認識が示されている(特許文献4の第7頁第26行〜第27行参照)。さらに、この特許文献4には、マイクロスフィアを開示する文献として特許文献5を紹介している。
【0011】
特許文献5に開示された方法は、加水分解性ポリマーであるポリラクチド等と活性物質とを溶解する溶液を超臨界流体に噴霧することによりマイクロパーティクルを製造する方法である。この特許文献5に記載された方法により製造されるマイクロパーティクルは加水分解性ポリマーを使用しているので、活性物質として医薬物質を含有するマイクロパーティクルを医薬品として経口投与すると、胃や腸のどの部位で加水分解性ポリマーが分解するか予測がつかず、したがって、体内の所定の箇所で活性物質の薬効を働かせることができないという問題がある。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】EP0322687
【特許文献2】特開平2−4439号公報
【特許文献3】特開平11−197494号公報
【特許文献4】特表2001−504452号公報
【特許文献5】US5424076
【非特許文献】
【0013】
【非特許文献1】J.Jung.M.Perrut / J. of Suipercritical Fluids 20(2001)179-219
【発明の概要】
【発明が解決しようとする課題】
【0014】
この発明の目的は、医薬物質による医薬効果の持続性に優れたマイクロスフェアである微小凝集粒子及びその製造方法を提供することにある。
【課題を解決するための手段】
【0015】
前記課題を解決するための手段は、極性基含有の(メタ)アクリル酸系ポリマーの分散相中に医薬物質粒子が分散して成ることを特徴とする微小凝集粒子であり、
前記課題を解決するための他の手段は、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを含有する極性溶媒溶液と超臨界流体と接触させることを特徴とする微小凝集粒子の製造方法である。
【発明の効果】
【0016】
この発明に係る微小凝集粒子は、分散相である極性基含有の(メタ)アクリル酸系ポリマー中に医薬物質粒子が分散してなる、いわゆるマイクロスフェアの構造を有する微小凝集粒子である。医薬物質は通常極性基をその分子構造内に含有する。したがって、極性基含有の(メタ)アクリル酸系ポリマーにおける極性基と医薬物質における極性基とが親和性を有することにより、マイクロスフェア中の医薬物質は単に分散状態で存在するのではなく、静電引力により分散相に結合することになる。したがって、この微小凝集粒子を例えば経口投与すると、直ちに体内で医薬物質が微小凝集粒子から放出されることがなく、徐々に放出されることになる。故に、この微小凝集粒子は、医薬物質による薬効が長期間に渡って持続することになる。
【0017】
この発明に係る微小凝集粒子の製造方法においては、極性有機溶媒に、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを溶解する。有機溶媒、(メタ)アクリル酸系ポリマー及び医薬物質はいずれも極性基を含有するので、極性有機溶媒に、極性基含有の(メタ)アクリル酸系ポリマー及び医薬物質はともに良く溶解する。極性有機溶媒に極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを溶解して得られる極性溶媒溶液と、超臨界流体とを接触させると、超臨界流体中に極性有機溶媒が拡散し、一方、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とが微粉化する。この微粉化において、極性基含有の(メタ)アクリル酸系ポリマー中に医薬物質が微粒子状に分散してなる微粒子が形成される。
【図面の簡単な説明】
【0018】
【図1】図1はこの発明の方法を実施する一例である微小凝集粒子製造装置を示す概略説明図である。
【発明を実施するための形態】
【0019】
この発明について図面を参照しながら説明する。なお、この発明は図1に示される装置により製造される方法に限定されるものでないことは、言うまでもない。
【0020】
図1に示されるように、微小凝集粒子を製造する微小凝集粒子製造装置1は、耐圧容器2と、極性溶媒溶液を調製する溶液調製手段3と、超臨界流体を前記耐圧容器2に供給する超臨界流体供給手段4とを有する。
【0021】
耐圧容器2は超臨界流体を超臨界状態で保持することができる耐圧製の槽で形成される。ここで、超臨界流体としては、酸化窒素、二酸化炭素、ハロゲン化炭化水素、飽和炭化水素、不飽和炭化水素、二酸化二窒素、アンモニア及びこれらの混合物等を挙げることができる。この発明において好適な超臨界流体は、二酸化炭素である。二酸化炭素の臨界温度Tcが304.21Kであり、臨界圧力Pcが7.3825MPaであるので、取り扱いに利便性があるからである。
【0022】
前記溶液調製手段3は、調製槽5と、この調製槽5で調製された極性溶媒溶液を耐圧容器2に移送する移送路6と、移送路6の途中に介装された、図示しない溶液移送手段例えばポンプと、移送路6の途中に介装された、図示しない開閉弁とを備える。この調製槽5には、所定量の極性溶媒と、所定量の極性基含有の(メタ)アクリル酸系ポリマーと、所定量の医薬物質とが投入され、これらが混合されて極性溶媒溶液がこの調製槽6内で調製され、保存される。
【0023】
ここで、前記極性基含有の(メタ)アクリル酸系ポリマーとしては、例えば、第4級アンモニウム基を有するアクリル酸及びメタアクリル酸をモノマー単位として含有する第4級アンモニウム基含有(メタ)アクリル酸系ポリマー、アミノ基を含有するアクリル酸及びメタアクリル酸をモノマー単位として含有するアミノ基含有(メタ)アクリル酸系ポリマー、並びにカルボキシル基を含有するアクリル酸及びメタアクリル酸をモノマー単位として含有するカルボキシル基含有(メタ)アクリル酸系ポリマー等を挙げることができる。これらの中でも好ましいのは、アミノ基含有(メタ)アクリル酸系ポリマーであり、特にメタクリル酸メチル、メタクリル酸ブチル及びメタクリル酸ジメチルアミノエチルの共重合体(「オイドラギッド100」(登録商標)として入手可能)である。
【0024】
前記極性溶媒としては、メタノール、エタノール、プロパノール、ブタノール等の低級アルコール類、シクロヘキサン等のケトン類、酢酸エチル等のカルボン酸アルキルエステル類、並びに、水/低級アルコール類及びアセトン類/アルコール類等の混合溶媒等を挙げることができる。これら各種の極性溶媒の中でも低級アルコール類が好ましく、特にメタノール及びエタノールが好ましい。前記医薬物質としては、特に制限がなく、例えば鎮痛薬、解熱薬、アスピリン及びその誘導体、抗生物質、抗炎症薬、抗潰瘍薬、抗圧薬、神経弛緩薬、抗鬱薬等を挙げることができる。これら医薬物質の中でも3級アミノ基を含有する医薬品例えば塩酸ジフェニドール及び塩酸ジフェンヒドラミン等が好ましい。
【0025】
極性溶媒溶液を調製する際の、医薬物質(A)と極性基含有の(メタ)アクリル酸系ポリマー(B)との比率(重量比)[(B)/(A)]は、好適には1〜1.5である。前記重量比[(B)/(A)]が前記下限値よりも小さいと、この発明の方法によっても針状の粒子が形成されることがあり、前記重量比[(B)/(A)]が前記上限値よりも大きいと、この発明の方法によっても微小凝集粒子の粒径にバラつきが生じることがある。また、前記重量比[(B)/(A)]が前記範囲内にあると、粒径が0.1〜0.5μmの範囲内にある球状の凝集粒子が好適に形成される。
【0026】
前記極性溶媒溶液は、前記調製槽5内を適宜に加熱し、また必要に応じて攪拌することにより調製することができる。
【0027】
超臨界流体供給手段4は、超臨界流体を貯留する超臨界流体貯留槽7と、超臨界流体貯留槽7内の超臨界流体を前記耐圧容器2に移送する移送路8と、移送路8の途中に介装された、図示しない溶液移送手段例えばポンプと、移送路8の途中に介装された、図示しない開閉弁とを備える。
【0028】
前記耐圧容器2には、排出路9が接続される。この排出路9が前記耐圧容器2に接続されて開口する開口部(図示せず。)には、フィルター10が取り付けられる。フィルター10から外側に延在する排出路9には、圧力計11及び開閉弁12が装着されている。
【0029】
このフィルター10としては、この発明に係る微小凝集粒子を好適に捕集するために、例えば焼結フィルター及びガラスフィルター等で形成される。
【0030】
以上構成の微小凝集粒子製造装置1を用いて微小凝集粒子が次のようにして製造される。
【0031】
超臨界流体供給手段4により、耐圧容器2内に超臨界流体を充填する。耐圧容器2内では超臨界流体が超臨界状態で貯留される。その耐圧容器2内に、調製槽5で調製されたところの、極性溶媒に極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを溶解してなる一定量の極性溶媒溶液を、供給する。供給された極性溶媒溶液中の溶媒が超臨界流体中に直ちに拡散し、極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とが固化し、微粒子化する。次いで、さらに耐圧容器2内に一定量の超臨界流体を供給する。耐圧容器2内の圧力が超臨界流体の供給により高くなると、その圧力上昇分だけ開閉弁12を開放し、耐圧容器2内の圧力一定に保持する。この動作を繰り返して耐圧容器2内を超臨界流体で置換する。(メタ)アクリル酸系ポリマーを分散相とし、この分散相中に医薬物質が粒子状に分散してなる微小凝集粒子が耐圧容器2内に生成する。
【0032】
耐圧容器2内の圧力は圧力計11により監視される。耐圧容器2内が超臨界流体で十分に置換された後に、開閉弁12が開放されて耐圧容器2内の超臨界流体が排出管9を通じて排出される。超臨界流体が排出管9により排出されるとフィルター10により耐圧容器2内に生成した微小凝集粒子が捕集される。
【0033】
また、図1に示される微小凝集粒子製造装置1を用いて次のようにして連続的に微小凝集粒子を製造することができる。
【0034】
すなわち、耐圧容器2の内部に超臨界流体貯留槽7から超臨界流体例えば二酸化炭素を充填する。耐圧容器2内の二酸化炭素を超臨界状態に維持する。このような耐圧容器2内に極性溶媒溶液と超臨界流体とを一定の比率で注入する。そうすると、耐圧容器2内で医薬物質が析出する。耐圧容器2内に超臨界流体を注入し、耐圧容器2内の圧力が一定となるように開閉弁12の開閉を調節して耐圧容器2内の圧力を一定に保持する。超臨界流体を耐圧容器2内に供給し続けることにより耐圧容器2内が超臨界流体で充分に置換される。その後に、開閉弁12を開放すると、(メタ)アクリル酸系ポリマーを分散相とし、この分散相中に医薬物質が粒子状に分散してなる微小凝集粒子がフィルターに捕集される。
【符号の説明】
【0035】
1・・・微小凝集粒子製造装置
2・・・耐圧容器
3・・・溶液調製手段
4・・・超臨界流体供給手段
5・・・調製槽
6・・・移送路
7・・・超臨界流体貯留槽
8・・・移送路
9・・・排出路
10・・・フィルター
11・・・圧力計
12・・・開閉弁
【特許請求の範囲】
【請求項1】
極性基含有の(メタ)アクリル酸系ポリマーの分散相中に医薬物質粒子が分散して成ることを特徴とする微小凝集粒子。
【請求項2】
極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを含有する極性溶媒溶液と超臨界流体と接触させることを特徴とする前記請求項1に記載の微小凝集粒子の製造方法。
【請求項3】
前記極性基含有の(メタ)アクリル酸系ポリマーがメタクリル酸メチル、メタクリル酸ブチル及びメタクリル酸ジメチルアミノエチルの共重合体である前記請求項2に記載の微小凝集粒子の製造方法。
【請求項1】
極性基含有の(メタ)アクリル酸系ポリマーの分散相中に医薬物質粒子が分散して成ることを特徴とする微小凝集粒子。
【請求項2】
極性基含有の(メタ)アクリル酸系ポリマーと医薬物質とを含有する極性溶媒溶液と超臨界流体と接触させることを特徴とする前記請求項1に記載の微小凝集粒子の製造方法。
【請求項3】
前記極性基含有の(メタ)アクリル酸系ポリマーがメタクリル酸メチル、メタクリル酸ブチル及びメタクリル酸ジメチルアミノエチルの共重合体である前記請求項2に記載の微小凝集粒子の製造方法。
【図1】




【公開番号】特開2010−43126(P2010−43126A)
【公開日】平成22年2月25日(2010.2.25)
【国際特許分類】
【出願番号】特願2009−264553(P2009−264553)
【出願日】平成21年11月20日(2009.11.20)
【分割の表示】特願2003−379773(P2003−379773)の分割
【原出願日】平成15年11月10日(2003.11.10)
【出願人】(000226242)日機装株式会社 (383)
【Fターム(参考)】
【公開日】平成22年2月25日(2010.2.25)
【国際特許分類】
【出願日】平成21年11月20日(2009.11.20)
【分割の表示】特願2003−379773(P2003−379773)の分割
【原出願日】平成15年11月10日(2003.11.10)
【出願人】(000226242)日機装株式会社 (383)
【Fターム(参考)】
[ Back to top ]

