微生物の集積培養方法
【課題】簡便な方法を提供する。微生物の培養に有害物質を使用する場合、その有害物質の使用量を減らす。
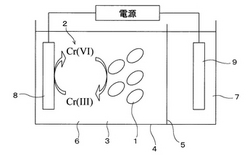
【解決手段】培養対象微生物1以外の微生物の育成環境を悪化させる物質2に対して還元活性を有する培養対象微生物1を、物質2を溶解させた培養液3中で選択的に集積培養する際、培養対象微生物によって還元された物質2を培養液3中に流した電気により酸化反応を生じさせて再生しながら培養を行う。
【解決手段】培養対象微生物1以外の微生物の育成環境を悪化させる物質2に対して還元活性を有する培養対象微生物1を、物質2を溶解させた培養液3中で選択的に集積培養する際、培養対象微生物によって還元された物質2を培養液3中に流した電気により酸化反応を生じさせて再生しながら培養を行う。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、微生物の集積培養方法に関する。さらに詳述すると、本発明は、特定の物質に対し還元活性と耐性を有する培養対象微生物を、前記物質を溶解させた培養液中で選択的に集積培養する微生物の集積培養方法であって、培養対象微生物以外の微生物に対して前記物質が毒性等の生育環境を悪化させる性質を有している場合の微生物の集積培養方法に関するものである。
【背景技術】
【0002】
クロム還元菌は、嫌気的環境で培養すると、培地中に含まれる有害な六価クロムを三価に還元する作用がある。三価クロムは、溶解度が低いため、沈殿させて溶液から分離することができる。このようにクロム還元菌の作用は、六価クロムで汚染された排水や土壌を浄化するのに有効である。
【0003】
ところで、クロム還元菌の培養には、六価クロムを培養液中に溶解させて行うが、培養初期段階においては六価クロムの毒性のために、六価クロムに耐性のあるクロム還元菌が優先的に増殖することができる。しかし、クロム還元菌の作用によって次第に培養液中の六価クロム濃度が減少してくると、それまで増殖ができないでいた雑多な菌群が増殖を開始してくるといった問題があった。これは、クロム還元菌を用いた浄化を考える際に、クロム還元菌の集積培養を困難なものとする要因となりうる。このような、雑多な菌群の増殖を防ぐには、(1)クロム還元菌を純粋分離し、雑菌の混入のないクリーンな環境で培養操作を実施する、(2)六価クロムを連続的に培地に添加しながら培養を実施する、などの手法が考えられる。
【0004】
なお、クロム還元菌を用いた六価クロムの除去方法として、特開平2−268899号公報、特開2002−281960号公報に開示されている技術がある。
【0005】
【特許文献1】特開平2−268899号
【特許文献2】特開2002−281960号
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながら、上記(1)の手法においては、特殊な培養環境を整える必要があり、簡便な培養方法とはなりえない。また、上記(2)の手法においては、結果的に有害である六価クロムを大量に使用することとなり、好ましくない。
【0007】
そして、これらの不都合は、六価クロムを使用したクロム還元菌の培養に限るものではなく、毒性のある物質を使用した培養であって、その物質に耐性のある微生物の培養についても同様である。
【0008】
本発明は、培養の対象となる微生物の選択的な培養を簡便に行うことができる微生物の集積培養方法を提供することを目的とする。また、本発明は、微生物の培養に有害物質を使用する場合、その有害物質を大量に使用しなくても培養の対象となる微生物を選択的に集積培養することができる微生物の集積培養方法を提供することを目的とする。
【課題を解決するための手段】
【0009】
かかる目的を達成するために、請求項1記載の微生物の集積培養方法は、培養対象微生物が還元活性を有し且つ耐性のある物質を溶解させた培養液中で培養対象微生物を選択的に集積培養する際、培養対象微生物によって還元された前記物質を培養液中に浸した電極に電位を与えることで酸化反応を生じさせて再生しながら培養を行うものである。
【0010】
したがって、前記物質の溶解した培養液は培養対象微生物以外の雑多な微生物にとって生息し難いものとなる。このため、前記物質に耐性のある培養対象微生物を選択的に培養することができる。培養対象微生物の培養により培養液中の前記物質がつぎつぎに還元されることになるが、培養液中の電極に電位を与えて酸化反応を生じさせることで還元された前記物質を再生させることができる。このため、前記物質を新たに補充しなくても、培養液中の前記物質の濃度を維持することができる。
【0011】
また、請求項2記載の微生物の集積培養方法は、培養液には有機物が含まれており、培養対象微生物は有機物を利用した発酵の過程で前記物質を還元するものである。即ち、培養対象微生物は呼吸するために前記物質を必要とするのではなく、発酵を行う過程で結果的に前記物質を還元する。
【0012】
また、請求項3記載の微生物の集積培養方法は、前記物質が、培養対象微生物以外の微生物に対して毒性を有しているものである。したがって、培養液が培養対象微生物以外の微生物にとって生息に適さないものとなる。
【0013】
また、請求項4記載の微生物の集積培養のように、前記物質は、六価クロム、銀、銅、水銀、ヨウ素、亜ヒ酸、マンガン、ニッケル、亜セレン酸のいずれか1つであることが好ましい。銀、銅、水銀、ヨウ素は、多くの種類の微生物に対し殺菌効果を有している。また、亜ヒ酸、マンガン、ニッケル、亜セレン酸は、多くの種類の微生物に対し生態毒性を有している。したがって、これらの物質に耐性のある微生物が、耐性の無い他の雑多な微生物に対し優先的に増殖する。
【0014】
また、請求項5記載の微生物の集積培養方法は、培養対象微生物がクロム還元菌であり、前記物質が六価クロムであり、クロム還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うものである。
【0015】
したがって、培養液はクロム還元菌以外の雑多な微生物にとって生息し難いものとなる。このため、六価クロムに耐性のあるクロム還元菌を選択的に培養することができる。クロム還元菌の培養により培養液中の六価クロムがつぎつぎに三価クロムに還元されることになるが、培養液中に浸した電極に電位を与えて酸化反応を生じさせることで三価に還元されたクロムを六価に再生させることができる。このため、培養液中の六価クロムの濃度を維持することができる。
【0016】
また、請求項6記載の微生物の集積培養方法は、培養対象微生物がウラン還元菌であり、前記物質が六価クロムであり、ウラン還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うものである。
【0017】
したがって、培養液はウラン還元菌以外の雑多な微生物にとって生息し難いものとなる。このため、六価クロムに耐性のあるウラン還元菌を選択的に培養することができる。ウラン還元菌の培養により培養液中の六価クロムがつぎつぎに三価クロムに還元されることになるが、培養液中に浸した電極に電位を与えて酸化反応を生じさせることで三価に還元されたクロムを六価に再生させることができる。このため、培養液中の六価クロムの濃度を維持することができる。
【発明の効果】
【0018】
しかして、請求項1記載の微生物の集積培養方法によれば、上述のようにして微生物を集積培養するので、培養液中に前記物質を補充しなくてもその濃度を維持することができる。このため、培養対象微生物の培養に適した環境を維持することができる。前記物質の再生には電気分解を利用するので、簡便であり、必要な装置類は簡単なもので足りる。このため、低コストで微生物を集積培養することができる。また、前記物質を再生して使用するので、その使用量が少量で足り、この点からもコストを安くすることができる。
【0019】
また、請求項2記載の微生物の集積培養方法は、培養液には有機物が含まれており、培養対象微生物は有機物を利用した発酵の過程で前記物質を還元するものである。即ち、培養対象微生物は呼吸するために前記物質を必要とするのではなく、発酵を行う過程で結果的に前記物質を還元する。
【0020】
また、請求項3記載の微生物の集積培養方法では、前記物質が培養対象微生物以外の微生物に対して毒性を有しているので、培養液が培養対象微生物以外の微生物にとって生息に適さないものとなる。このため、培養対象微生物以外の微生物の繁殖を抑え、培養対象微生物をより優先的に培養することができる。
【0021】
また、請求項4記載の微生物の集積培養のように、前記物質は、六価クロム、銀、銅、水銀、ヨウ素、亜ヒ酸、マンガン、ニッケル、亜セレン酸のいずれか1つであることが好ましい。銀、銅、水銀、ヨウ素は、多くの種類の微生物に対し殺菌効果を有している。また、亜ヒ酸、マンガン、ニッケル、亜セレン酸は、多くの種類の微生物に対し生態毒性を有している。したがって、これらの物質に耐性のある微生物を優先的に培養することができる。
【0022】
また、請求項5記載の微生物の集積培養方法では、培養対象微生物がクロム還元菌であり、前記物質が六価クロムであり、クロム還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うので、培養液中に六価クロムを補充しなくてもその濃度を維持することができる。このため、クロム還元菌の培養に適した環境を維持することができる。六価クロムの再生には電気分解を利用するので、簡便であり、必要な装置類は簡単なもので足りる。このため、低コストでクロム還元菌を集積培養することができる。また、六価クロムを再生して使用するので、その使用量が少量で足り、安全性が高く、集積培養に要するコストを更に安くすることができる。
【0023】
さらに、請求項6記載の微生物の集積培養方法は、培養対象微生物がウラン還元菌であり、前記物質が六価クロムであり、ウラン還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うので、培養液中に六価クロムを補充しなくてもその濃度を維持することができる。このため、ウラン還元菌の培養に適した環境を維持することができる。六価クロムの再生には電気分解を利用するので、簡便であり、必要な装置類は簡単なもので足りる。このため、低コストでウラン還元菌を集積培養することができる。また、六価クロムを再生して使用するので、その使用量が少量で足り、安全性が高く、集積培養に要するコストを更に安くすることができる。即ち、クロム還元菌と同様の方法で、ウラン還元菌を選択的に集積培養することができる。
【発明を実施するための最良の形態】
【0024】
以下、本発明を詳細に説明する。
【0025】
図1に、本発明の微生物の集積培養方法の実施形態の一例を概念的に示す。本発明の微生物の集積培養方法は、培養対象微生物1が還元活性を有し且つ耐性のある物質2を溶解させた培養液3中で培養対象微生物1を選択的に集積培養する際、培養対象微生物1によって還元された物質2を培養液3中に浸した電極に電位を与えることで酸化反応を生じさせて再生しながら培養を行うものである。即ち、物質2に対し耐性のある培養対象微生物1を、耐性のない微生物に優先して培養を行うものである。本実施形態では、培養対象微生物1は六価クロムに耐性のあるクロム還元菌(以下、クロム還元菌1という)であり、物質2は六価クロム(以下、六価クロム2という)であり、クロム還元菌1によって還元された三価クロムを六価クロム2に再生しながら培養を行うものである。
【0026】
電解槽4はイオン交換膜5によって培養槽6と対極槽7に仕切られており、培養槽6には六価クロム2を含む培地に懸濁させたクロム還元菌1を、対極槽7には六価クロム2を含まない培地成分を含んだ溶液を充填している。また、培養槽6には陽極8を、対極槽7には陰極9を浸している。
【0027】
培養槽6中の培地には、例えば乳酸、酵母エキス等の有機物が投入されている。クロム還元菌1はこれらの有機物を使用して発酵を行い、その過程で六価クロム2を還元する。六価クロム2は、クロム還元菌1以外の微生物に対して毒性を有しており、その他の雑多な微生物の繁殖を抑えることができる。
【0028】
つまり、六価クロム2が溶解した培養液3はクロム還元菌1にとっては増殖し易いものであるが、その他の雑多な微生物にとっては増殖し難いものであり、クロム還元菌1を選択的に培養することができる。クロム還元菌1の培養により培養液3中の六価クロム2がつぎつぎに還元されて三価クロムとなるが、陽極8に電位を与えることで三価クロムを六価クロム2に再生することができる。このため、培養液3中の六価クロム2の濃度を維持することができ、クロム還元菌1の優先的な培養に適した環境を維持することができる。
【0029】
このように、本発明では電気分解によりクロムを三価から六価に再生するので、簡便であり、必要な装置類も簡単なもので足りる。このため、低コストでクロム還元菌1を集積培養することができる。また、培養槽6中の六価クロム2を再生して使用するので、六価クロム2の使用量が少量で足り、安全性が高く、集積培養に要するコストを更に安くすることができる。
【0030】
クロム還元菌1としては、例えば表1に掲げるものがある。即ち、例えばShwanella、Pseudomonas、Sulfate reducing bacteria、Arthrobacter、Bacillus、Aerococcus、Micrococcus、Aeromonas、Thermoanaerobacter、Cellulomonas、Geobacter、Streptomyces、Escherichia、Enterobacterである。ただし、これらのクロム還元菌1に限るものではない。
【0031】
【表1】

【0032】
電気分解を行うために培養液3には、三価クロムを六価クロム2に酸化させることができる値の電位を与える。実験では、図6に示すように、1V付近の電位で三価クロムが六価クロム2に酸化された。したがって、三価クロムを六価クロム2に酸化させる電位は約1Vであると判断できるので、培養液3に1Vの電位をかけながら培養を行うことが好ましい。
【0033】
また、培養液3中の六価クロム2の濃度が高すぎると、六価クロムの毒性によりクロム還元菌1自身も増殖し難くなるので、六価クロム2の濃度の上限値は、例えば0.5m mol/Lが好ましい。
【0034】
なお、上述の形態は本発明の好適な形態の一例ではあるがこれに限定されるものではなく本発明の要旨を逸脱しない範囲において種々変形実施可能である。例えば、上述の説明では、培養対象微生物がクロム還元菌1であったが、クロム還元菌1以外の微生物でも良い。
【0035】
また、上述の説明では、物質2として六価クロムを使用していたが、六価クロムに限るものではない。例えば、銀(Ag+)、銅(Cu2+)、水銀(Hg2+)、ヨウ素(I2)、亜ヒ酸(AsO2−)、マンガン(Mn2+)、ニッケル(Ni+)、亜セレン酸(SeO32−)のいずれかでも良い。即ち、これらの物質2に還元活性のある微生物1を、これらの物質2を再生しながら培養しても良い。六価クロム2と同様に銀、銅、水銀、ヨウ素も多くの種類の微生物に対し殺菌効果を有しており、銀、銅、水銀、ヨウ素に耐性のある微生物1を選択的に集積培養することができる。また、亜ヒ酸、マンガン、ニッケル、亜セレン酸は多くの種類の微生物に対し生態毒性を有しており、亜ヒ酸、マンガン、ニッケル、亜セレン酸に耐性のある微生物1を選択的に集積培養することができる。これらの場合にも、上述のクロム還元菌1を培養する場合と同様の効果を得ることができる。
【0036】
なお、物質2が銀の場合、培養液3中のAg+を銀還元菌1がAgに還元し、これを電気分解によってAg+に再生することが考えられる。また、物質2が銅の場合、培養液3中のCu2+を銅還元菌1がCuに還元し、これを電気分解によってCu2+に再生することが考えられる。また、物質2が水銀の場合、培養液3中のHg2+を水銀還元菌1がHgに還元し、これを電気分解によってHg2+に再生することが考えられる。また、物質2がヨウ素の場合、培養液3中のI2をヨウ素還元菌1がI−に還元し、これを電気分解によってI2に再生することが考えられる。また、物質2が亜ヒ酸の場合、培養液3中の亜ヒ酸を亜ヒ酸還元菌1がヒ素に還元し、これを電気分解によって亜ヒ酸に再生することが考えられる。また、物質2がマンガンの場合、培養液3中のMn2+をマンガン還元菌1がMnに還元し、これを電気分解によってMn2+に再生することが考えられる。また、物質2がニッケルの場合、培養液3中のNi+をニッケル還元菌1がNiに還元し、これを電気分解によってNi+に再生することが考えられる。また、物質2が亜セレン酸の場合、培養液3中の亜セレン酸を亜セレン酸還元菌1がセレンに還元し、これを電気分解によって亜セレン酸に再生することが考えられる。
【0037】
また、物質2として六価クロム2を使用して、ウラン還元菌1を選択的に集積培養しても良い。即ち、ウラン還元菌1によって還元された三価クロムを培養液3中に流した電気により酸化反応を生じさせて六価クロム2に再生しながら培養を行うようにしても良い。この場合にも、クロム還元菌1を培養する場合と同様の効果を得ることができる。ウラン還元菌1として、六価クロムに対し還元活性を有し且つ耐性のあるものがある。ウランを溶解させた培養液3でウラン還元菌1を培養することが安全面、コスト面等で不利な場合がある。このような場合には、ウラン還元菌1を六価クロムを溶解させた培養液3中で培養することが安全面、コスト面等で有利となることも考えられる。
【0038】
また、上述の説明では、発酵の過程で物質2を還元する微生物1を例に説明していたが、必ずしも発酵の過程で物質3を還元する微生物1に限るものではなく、呼吸の過程で物質2を還元する微生物1を培養しても良い。
【実施例1】
【0039】
本発明により、クロム還元菌1を良好に培養できることを確認するための実験を行った。使用した培養装置を図2に示す。電解槽4は外径75mm、高さ90mmのガラス製深底シャーレの内側を、一価の陽イオン透過性の交換膜(旭化成、K−192)5で仕切った二槽式とし、片方を培養槽6、もう一方を対極槽7とした。培養槽6には白金網(40mm×70mm、80mesh)製の陽極8、および銀・塩化銀参照電極10(HS−205C、東亜DKK社)を設置した。さらに、対極槽7には炭素板(40mm×70mm、4mm厚)を陰極9として設置した。これら3本の電極8,9,10を電位制御装置11に結線する事で、培養槽6内の陽極8の電位を厳密に設定可能とした 。
【0040】
培養に際しては、電解槽4をアクリル製の嫌気ボックス12内に封入し、さらに嫌気ボックス全体を30度に設定した恒温槽(図示せず)内に設置した。嫌気ボックス12には、常時窒素ガスを注入し(0.2L/min)、嫌気雰囲気を維持した。
【0041】
培養液3の組成を表2に、その中の金属溶液の組成を表3に示す。なお、以下の実験では、全てこの組成の培養液3を用いた。
【0042】
【表2】

【表3】

【0043】
培養液3はまず、無機基本成分を調整後にオートクレーブ滅菌を施した。実験直前に、クロム塩および有機成分(Yeast Extract:0.2g/L、乳酸ナトリウム:1g/L)を混合し、フィルター(0.22μm,Millex-GS,MILLIPORE,Ireland)によりろ過除菌した。
【0044】
陽極8に+1.0Vの電位を与えながら2週間にわたり培養を行った。その結果を図3に示す。2週間の培養でクロム還元菌1の濃度が初期状態の約3倍に増加したことを確認できた。本発明によってクロム還元菌1を培養できることを確認できた。なお、クロム還元菌1の数は、光学顕微鏡観察による菌数カウントによって計測した。
【0045】
また、微生物の形状に関する、より詳細な視覚的情報の取得を目的として、原子間力顕微鏡(AFM:Digital Instruments社、Nanoscope IIIa)による観察を行った。上記実験後の試料(本発明試料)と、比較のためにバイアル瓶を用いて培養を行った試料(比較試料)について観察を行った。AFM観察試料は、アセトン中で超音波洗浄したカバーガラス(MATSUNAMI,Micro cover glass,18×18mm)を用いて作成した。カバーガラス上に微生物の懸濁液50μLを滴下し、約1時間常温で静置後、カバーガラスを蒸留水中に10秒間浸漬させ、培養液3成分を洗い流した。その後、約1時間常温大気中で乾燥させ、測定に供した。AFM測定は大気中にておこない、探針の制御法はコンタクトモードを採用した。個々のサンプルに対し、20μm×20μmの領域をスキャンし、画像を取得した。なお、比較試料を得るためのバイアル瓶を用いた培養は、以下の通り行った。即ち、微生物懸濁液にクロム塩、および有機成分を添加し、100mL容のバイアル瓶に30mL注入し、ブチルゴム栓およびアルミキャップにより密栓した。続いて、バイアル瓶内のガスを窒素に置換し、最終ガス圧を1.5気圧に調整した。バイアル瓶は30度の恒温室にて振とう培養に供した。
【0046】
その結果を図4に示す。図4(A)は比較試料についての画像写真、図4(B)は本発明試料についての画像写真である。なお、各図中右下の線の長さは5μmに相当する。比較試料では複数種の微生物の増殖が確認されたのに対し、本発明試料では菌形のそろった単一の微生物の増殖が確認できた。本発明試料で確認された微生物はクロム還元菌1であり、本発明によってクロム還元菌1を選択的に集積培養を行うことができることを確認できた。
【0047】
さらに念のため、上記実験(陽極8に+1.0Vの電位を与えながらの実験)によって集積培養した微生物を、今度は陽極8に電位を与えずに2週間培養した。その結果を図5に示す。図5からも明らかなように、培養液3中の六価クロム2の濃度の減少が確認された。これにより、上記実験によって集積培養された微生物がクロム還元菌1であることを再確認できた。
【実施例2】
【0048】
陽極8に与える電位を決定するための実験を行った。クロムをはじめとする種々の電極活性物質2の酸化還元電位の測定は、電気化学アナライザー(ALSモデル660B、BAS社)を使用し、サイクリックボルタンメトリー(CV)法により実施した。この際、電解系は3極式で行い、電極反応を見るための作用極には白金円盤電極(面積:0.785mm2、BAS社)を、参照電極には銀・塩化銀電極(RE−1B、BAS社)、さらに電流を流すための対極には白金棒電極(1mm径×5cm、自作)を使用した。それぞれの電極活性物質2、具体的には六価クロムについては1m mol/L濃度で調整し、銀,銅,水銀,ヨウ素,亜ヒ酸,マンガン,ニッケル,亜セレン酸については5m mol/L濃度で調整し、電解質溶液中に溶解させた。CV結果は、それぞれの物質2ごとに、物質2の入っていない電解質溶液をベースラインとして表示した。
【0049】
六価クロム2についての酸化電位の測定結果を図6に示す。図6において、薄い色の実線はクロムを含まない培養液3(バックグラウンド)についての測定結果、濃い色の実線は1m mol/Lのクロムイオンを含む培養液3についての測定結果である。なお、横軸(電位)は、銀塩化銀参照電極に対する値である(図7〜図14において同じ)。培養液3にクロムが存在する状態で、電気化学的に酸化還元を行わせると、0V付近(矢印A)に還元電流、+1V付近(矢印B)に酸化電流の増加が確認できた。これらはそれぞれ、Cr(VI)→Cr(III)、Cr(III)→Cr(VI)の反応に起因する電流値であると判断できる。これは、培養液3に常時+1Vの電位を加えることで、培養液3中のクロムをCr(VI)に保持できることを示している。したがって、培養中に与える電位は+1.0Vが適している。
【0050】
銀(Ag+)についての酸化電位の測定結果を図7に示す。図7において、実線は銀を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの銀イオンを含む培養液についての測定結果である。培養液に銀が存在する状態で、電気化学的に酸化還元を行わせると、+0.5V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.5Vが適している。
【0051】
銅(Cu2+)についての酸化電位の測定結果を図8に示す。図8において、実線は銅を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの銅イオンを含む培養液についての測定結果である。培養液に銅が存在する状態で、電気化学的に酸化還元を行わせると、0V付近と+0.2V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、0V又は+0.2Vが適している。
【0052】
水銀(Hg2+)についての酸化電位の測定結果を図9に示す。図9において、実線は水銀を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの水銀イオンを含む培養液についての測定結果である。培養液に水銀が存在する状態で、電気化学的に酸化還元を行わせると、+0.3V付近と+0.6V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.3V又は+0.6Vが適している。
【0053】
ヨウ素(I2)についての酸化電位の測定結果を図10に示す。図10において、実線はヨウ素を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lのヨウ素を含む培養液についての測定結果である。培養液にヨウ素が存在する状態で、電気化学的に酸化還元を行わせると、+0.5V付近と+0.8V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.5V又は+0.8Vが適している。
【0054】
亜ヒ酸(AsO2−)についての酸化電位の測定結果を図11に示す。図11において、実線は亜ヒ酸を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの亜ヒ酸を含む培養液についての測定結果である。培養液に亜ヒ酸が存在する状態で、電気化学的に酸化還元を行わせると、+0.7V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.7Vが適している。
【0055】
マンガン(Mn2+)についての酸化電位の測定結果を図12に示す。図12において、実線はマンガンを含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lのマンガンイオンを含む培養液についての測定結果である。培養液にマンガンが存在する状態で、電気化学的に酸化還元を行わせると、+0.7V付近と+1.0V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.7V又は+1.0Vが適している。
【0056】
ニッケル(Ni+)についての酸化電位の測定結果を図13に示す。図13において、実線はニッケルを含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lのニッケルイオンを含む培養液についての測定結果である。培養液にニッケルが存在する状態で、電気化学的に酸化還元を行わせると、−0.4V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、−0.4Vが適している。
【0057】
亜セレン酸(SeO32−)についての酸化電位の測定結果を図14に示す。図14において、実線は亜セレン酸を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの亜セレン酸を含む培養液についての測定結果である。培養液に亜セレン酸が存在する状態で、電気化学的に酸化還元を行わせると、+0.5V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.5Vが適している。
【実施例3】
【0058】
培養液3中の六価クロム2の濃度の適正値を求めるための実験を行った。実験ではバイアル瓶を使用し、電位を与えない状態(六価クロム2の再生を行わない状態)で実験を行った。微生物懸濁液にクロム塩、および有機成分を添加し、100mL容のバイアル瓶に30mL注入し、ブチルゴム栓およびアルミキャップにより密栓した。続いて、バイアル瓶内のガスを窒素に置換し、最終ガス圧を1.5気圧に調整した。バイアル瓶は30度の恒温室にて振とう培養に供した。微生物として2箇所の土壌(土壌A、土壌B)から採取したクロム還元菌1を使用し、培養液3中の六価クロム2の初発濃度が0.1m mol/L、0.2m mol/L、0.5m mol/L、1.0m mol/Lの4つの値について実験を行った。また、比較のために、クロム還元菌1を投入しない場合(control)についても実験を行った。
【0059】
まず最初に、クロム還元菌1による培養液3中の六価クロム濃度の時間変化についての測定結果を図15に示す。図15(A)は六価クロム2の初発濃度が0.1m mol/Lの場合、(B)は六価クロム2の初発濃度が0.2m mol/Lの場合、(C)は六価クロム2の初発濃度が0.5m mol/Lの場合、(D)は六価クロム2の初発濃度が1.0m mol/Lの場合である。なお、各図では縦軸のスケールが異なっている。六価クロム2の初発濃度が0.1と0.2m mol/Lの場合には、実験開始から1〜2週間で六価クロム2の濃度が0近くまで減少した。また、六価クロム2の初発濃度が0.5m mol/Lの場合には、六価クロム濃度の減少は僅かであった。一方、六価クロム2の初発濃度が1.0m mol/Lの場合、六価クロム濃度の有意な減少はみられなかった。
【0060】
なお、培養液3中のクロムは、六価クロム2の状態では溶液中に溶解しているが、三価クロムの状態では沈殿するので、培養液3をフィルター(0.22μm,Millex-GS,MILLIPORE,Ireland)で三価クロムをろ過することにより、六価クロム2のみを抽出し、クロム濃度を分析した。クロムの定量にはICP発光分析装置(P8000、HITACHI社)を使用した。
【0061】
次に、各初発濃度における菌濃度の時間変化についての測定結果を図16に示す。なお、図中縦軸は、クロム還元菌1を含む菌全体(クロム還元菌1以外の雑多な菌も含む)の濃度(cells/mL)である。また、図中右上四角枠内の数値(0.1/0.2/0.5/1.0)は、六価クロム2の初発濃度(m mol/L)を示している。図16(A)は土壌Aについての測定結果、図16(B)は土壌Bについての測定結果である。
【0062】
六価クロム初発濃度が0.2m mol/L以下の場合、培養後半では六価クロム2の濃度がほぼゼロになっている(図15(A)(B))ことから、図16(A)(B)の0.1、0.2m mol/Lで増えている菌は、雑多な菌も含まれていると考えられる。一方、六価クロム初発濃度0.5m mol/Lの場合、培養後半でも六価クロム2が維持されている(図15(C))ので、図16(A)(B)の0.5m mol/Lで増えている菌は、クロム還元菌1であると考えられる。すなわち、土壌A、土壌Bに含まれるクロム還元菌1は、与えられた培養液3環境において、少なくともそれぞれ、1.4×109cells/mL、6×108cells/mLまで増殖できることが確認できた。
【0063】
なお、六価クロム2が培養液3中に残っているにもかかわらず、微生物1の増殖が止まっているのは、六価クロム2が微生物1の増殖に直接関与しない物質である(即ち、微生物が呼吸するのに六価クロム2を必要とするのではなく、微生物1の発酵の過程で六価クロム2を還元する)証であり、おそらくは増殖に必要な有機物が使い尽くされたためと考えられる。
【0064】
一方、六価クロム2の初発濃度1.0m mol/Lの場合、ここで増えているのはクロム還元菌1と考えられる(図15(D)より培養液3中に六価クロム2が存在しているため)が、0.5m mol/Lの場合に比べて明らかに菌体濃度が低いことから(図16)、1.0m mol/Lの場合の六価クロム2は、クロム還元菌1自体の増殖を阻害していると考えられる。
【0065】
以上より、培養液3中の六価クロム濃度が高過ぎても培養に適さないことがわかった。そして、具体的には、クロム還元菌1の集積培養の際には、0.5m mol/L以下の六価クロム濃度にて、培養液3中の六価クロム2がなくならないような条件の下で培養することが好ましいことがわかった。
【0066】
また、培養液3中の六価クロム濃度が低すぎるとクロム還元菌1以外の雑多な菌の繁殖を許してしまうことになるので、六価クロム濃度としては、最低でも雑多な菌の繁殖を抑えることができる濃度を確保する必要がある。例えば、0.1m mol程度の濃度を確保することが好ましい。
【図面の簡単な説明】
【0067】
【図1】本発明の微生物の集積培養方法の実施形態の一例を示す概念図である。
【図2】クロム還元菌の集積培養の実験に使用した培養装置の概念図である。
【図3】クロム還元菌の集積培養の実験結果を示す図である。
【図4】培養後の微生物群の顕微鏡画像を示し、(A)は比較試料についての顕微鏡画像、(B)は本発明試料についての顕微鏡画像である。
【図5】培養後の微生物がクロム還元菌であることを再確認するための実験結果を示す図である。
【図6】クロムの酸化電位の測定結果を示す図である。
【図7】銀の酸化電位の測定結果を示す図である。
【図8】銅の酸化電位の測定結果を示す図である。
【図9】水銀の酸化電位の測定結果を示す図である。
【図10】ヨウ素の酸化電位の測定結果を示す図である。
【図11】亜ヒ酸の酸化電位の測定結果を示す図である。
【図12】マンガンの酸化電位の測定結果を示す図である。
【図13】ニッケルの酸化電位の測定結果を示す図である。
【図14】亜セレン酸の酸化電位の測定結果を示す図である。
【図15】クロム還元菌による六価クロム濃度の時間変化を示し、(A)は六価クロム初発濃度が0.1m mol/Lの場合の測定結果、(B)は六価クロム初発濃度が0.2m mol/Lの場合の測定結果、(C)は六価クロム初発濃度が0.5m mol/Lの場合の測定結果、(D)は六価クロム初発濃度が1.0m mol/Lの場合の測定結果である。
【図16】六価クロム初発濃度ごとのクロム還元菌濃度の時間変化を示し、(A)は土壌Aより採取したクロム還元菌についての測定結果、(B)は土壌Bより採取したクロム還元菌についての測定結果である。
【符号の説明】
【0068】
1 培養対象微生物
2 六価クロム(物質)
3 培養液
【技術分野】
【0001】
本発明は、微生物の集積培養方法に関する。さらに詳述すると、本発明は、特定の物質に対し還元活性と耐性を有する培養対象微生物を、前記物質を溶解させた培養液中で選択的に集積培養する微生物の集積培養方法であって、培養対象微生物以外の微生物に対して前記物質が毒性等の生育環境を悪化させる性質を有している場合の微生物の集積培養方法に関するものである。
【背景技術】
【0002】
クロム還元菌は、嫌気的環境で培養すると、培地中に含まれる有害な六価クロムを三価に還元する作用がある。三価クロムは、溶解度が低いため、沈殿させて溶液から分離することができる。このようにクロム還元菌の作用は、六価クロムで汚染された排水や土壌を浄化するのに有効である。
【0003】
ところで、クロム還元菌の培養には、六価クロムを培養液中に溶解させて行うが、培養初期段階においては六価クロムの毒性のために、六価クロムに耐性のあるクロム還元菌が優先的に増殖することができる。しかし、クロム還元菌の作用によって次第に培養液中の六価クロム濃度が減少してくると、それまで増殖ができないでいた雑多な菌群が増殖を開始してくるといった問題があった。これは、クロム還元菌を用いた浄化を考える際に、クロム還元菌の集積培養を困難なものとする要因となりうる。このような、雑多な菌群の増殖を防ぐには、(1)クロム還元菌を純粋分離し、雑菌の混入のないクリーンな環境で培養操作を実施する、(2)六価クロムを連続的に培地に添加しながら培養を実施する、などの手法が考えられる。
【0004】
なお、クロム還元菌を用いた六価クロムの除去方法として、特開平2−268899号公報、特開2002−281960号公報に開示されている技術がある。
【0005】
【特許文献1】特開平2−268899号
【特許文献2】特開2002−281960号
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながら、上記(1)の手法においては、特殊な培養環境を整える必要があり、簡便な培養方法とはなりえない。また、上記(2)の手法においては、結果的に有害である六価クロムを大量に使用することとなり、好ましくない。
【0007】
そして、これらの不都合は、六価クロムを使用したクロム還元菌の培養に限るものではなく、毒性のある物質を使用した培養であって、その物質に耐性のある微生物の培養についても同様である。
【0008】
本発明は、培養の対象となる微生物の選択的な培養を簡便に行うことができる微生物の集積培養方法を提供することを目的とする。また、本発明は、微生物の培養に有害物質を使用する場合、その有害物質を大量に使用しなくても培養の対象となる微生物を選択的に集積培養することができる微生物の集積培養方法を提供することを目的とする。
【課題を解決するための手段】
【0009】
かかる目的を達成するために、請求項1記載の微生物の集積培養方法は、培養対象微生物が還元活性を有し且つ耐性のある物質を溶解させた培養液中で培養対象微生物を選択的に集積培養する際、培養対象微生物によって還元された前記物質を培養液中に浸した電極に電位を与えることで酸化反応を生じさせて再生しながら培養を行うものである。
【0010】
したがって、前記物質の溶解した培養液は培養対象微生物以外の雑多な微生物にとって生息し難いものとなる。このため、前記物質に耐性のある培養対象微生物を選択的に培養することができる。培養対象微生物の培養により培養液中の前記物質がつぎつぎに還元されることになるが、培養液中の電極に電位を与えて酸化反応を生じさせることで還元された前記物質を再生させることができる。このため、前記物質を新たに補充しなくても、培養液中の前記物質の濃度を維持することができる。
【0011】
また、請求項2記載の微生物の集積培養方法は、培養液には有機物が含まれており、培養対象微生物は有機物を利用した発酵の過程で前記物質を還元するものである。即ち、培養対象微生物は呼吸するために前記物質を必要とするのではなく、発酵を行う過程で結果的に前記物質を還元する。
【0012】
また、請求項3記載の微生物の集積培養方法は、前記物質が、培養対象微生物以外の微生物に対して毒性を有しているものである。したがって、培養液が培養対象微生物以外の微生物にとって生息に適さないものとなる。
【0013】
また、請求項4記載の微生物の集積培養のように、前記物質は、六価クロム、銀、銅、水銀、ヨウ素、亜ヒ酸、マンガン、ニッケル、亜セレン酸のいずれか1つであることが好ましい。銀、銅、水銀、ヨウ素は、多くの種類の微生物に対し殺菌効果を有している。また、亜ヒ酸、マンガン、ニッケル、亜セレン酸は、多くの種類の微生物に対し生態毒性を有している。したがって、これらの物質に耐性のある微生物が、耐性の無い他の雑多な微生物に対し優先的に増殖する。
【0014】
また、請求項5記載の微生物の集積培養方法は、培養対象微生物がクロム還元菌であり、前記物質が六価クロムであり、クロム還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うものである。
【0015】
したがって、培養液はクロム還元菌以外の雑多な微生物にとって生息し難いものとなる。このため、六価クロムに耐性のあるクロム還元菌を選択的に培養することができる。クロム還元菌の培養により培養液中の六価クロムがつぎつぎに三価クロムに還元されることになるが、培養液中に浸した電極に電位を与えて酸化反応を生じさせることで三価に還元されたクロムを六価に再生させることができる。このため、培養液中の六価クロムの濃度を維持することができる。
【0016】
また、請求項6記載の微生物の集積培養方法は、培養対象微生物がウラン還元菌であり、前記物質が六価クロムであり、ウラン還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うものである。
【0017】
したがって、培養液はウラン還元菌以外の雑多な微生物にとって生息し難いものとなる。このため、六価クロムに耐性のあるウラン還元菌を選択的に培養することができる。ウラン還元菌の培養により培養液中の六価クロムがつぎつぎに三価クロムに還元されることになるが、培養液中に浸した電極に電位を与えて酸化反応を生じさせることで三価に還元されたクロムを六価に再生させることができる。このため、培養液中の六価クロムの濃度を維持することができる。
【発明の効果】
【0018】
しかして、請求項1記載の微生物の集積培養方法によれば、上述のようにして微生物を集積培養するので、培養液中に前記物質を補充しなくてもその濃度を維持することができる。このため、培養対象微生物の培養に適した環境を維持することができる。前記物質の再生には電気分解を利用するので、簡便であり、必要な装置類は簡単なもので足りる。このため、低コストで微生物を集積培養することができる。また、前記物質を再生して使用するので、その使用量が少量で足り、この点からもコストを安くすることができる。
【0019】
また、請求項2記載の微生物の集積培養方法は、培養液には有機物が含まれており、培養対象微生物は有機物を利用した発酵の過程で前記物質を還元するものである。即ち、培養対象微生物は呼吸するために前記物質を必要とするのではなく、発酵を行う過程で結果的に前記物質を還元する。
【0020】
また、請求項3記載の微生物の集積培養方法では、前記物質が培養対象微生物以外の微生物に対して毒性を有しているので、培養液が培養対象微生物以外の微生物にとって生息に適さないものとなる。このため、培養対象微生物以外の微生物の繁殖を抑え、培養対象微生物をより優先的に培養することができる。
【0021】
また、請求項4記載の微生物の集積培養のように、前記物質は、六価クロム、銀、銅、水銀、ヨウ素、亜ヒ酸、マンガン、ニッケル、亜セレン酸のいずれか1つであることが好ましい。銀、銅、水銀、ヨウ素は、多くの種類の微生物に対し殺菌効果を有している。また、亜ヒ酸、マンガン、ニッケル、亜セレン酸は、多くの種類の微生物に対し生態毒性を有している。したがって、これらの物質に耐性のある微生物を優先的に培養することができる。
【0022】
また、請求項5記載の微生物の集積培養方法では、培養対象微生物がクロム還元菌であり、前記物質が六価クロムであり、クロム還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うので、培養液中に六価クロムを補充しなくてもその濃度を維持することができる。このため、クロム還元菌の培養に適した環境を維持することができる。六価クロムの再生には電気分解を利用するので、簡便であり、必要な装置類は簡単なもので足りる。このため、低コストでクロム還元菌を集積培養することができる。また、六価クロムを再生して使用するので、その使用量が少量で足り、安全性が高く、集積培養に要するコストを更に安くすることができる。
【0023】
さらに、請求項6記載の微生物の集積培養方法は、培養対象微生物がウラン還元菌であり、前記物質が六価クロムであり、ウラン還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うので、培養液中に六価クロムを補充しなくてもその濃度を維持することができる。このため、ウラン還元菌の培養に適した環境を維持することができる。六価クロムの再生には電気分解を利用するので、簡便であり、必要な装置類は簡単なもので足りる。このため、低コストでウラン還元菌を集積培養することができる。また、六価クロムを再生して使用するので、その使用量が少量で足り、安全性が高く、集積培養に要するコストを更に安くすることができる。即ち、クロム還元菌と同様の方法で、ウラン還元菌を選択的に集積培養することができる。
【発明を実施するための最良の形態】
【0024】
以下、本発明を詳細に説明する。
【0025】
図1に、本発明の微生物の集積培養方法の実施形態の一例を概念的に示す。本発明の微生物の集積培養方法は、培養対象微生物1が還元活性を有し且つ耐性のある物質2を溶解させた培養液3中で培養対象微生物1を選択的に集積培養する際、培養対象微生物1によって還元された物質2を培養液3中に浸した電極に電位を与えることで酸化反応を生じさせて再生しながら培養を行うものである。即ち、物質2に対し耐性のある培養対象微生物1を、耐性のない微生物に優先して培養を行うものである。本実施形態では、培養対象微生物1は六価クロムに耐性のあるクロム還元菌(以下、クロム還元菌1という)であり、物質2は六価クロム(以下、六価クロム2という)であり、クロム還元菌1によって還元された三価クロムを六価クロム2に再生しながら培養を行うものである。
【0026】
電解槽4はイオン交換膜5によって培養槽6と対極槽7に仕切られており、培養槽6には六価クロム2を含む培地に懸濁させたクロム還元菌1を、対極槽7には六価クロム2を含まない培地成分を含んだ溶液を充填している。また、培養槽6には陽極8を、対極槽7には陰極9を浸している。
【0027】
培養槽6中の培地には、例えば乳酸、酵母エキス等の有機物が投入されている。クロム還元菌1はこれらの有機物を使用して発酵を行い、その過程で六価クロム2を還元する。六価クロム2は、クロム還元菌1以外の微生物に対して毒性を有しており、その他の雑多な微生物の繁殖を抑えることができる。
【0028】
つまり、六価クロム2が溶解した培養液3はクロム還元菌1にとっては増殖し易いものであるが、その他の雑多な微生物にとっては増殖し難いものであり、クロム還元菌1を選択的に培養することができる。クロム還元菌1の培養により培養液3中の六価クロム2がつぎつぎに還元されて三価クロムとなるが、陽極8に電位を与えることで三価クロムを六価クロム2に再生することができる。このため、培養液3中の六価クロム2の濃度を維持することができ、クロム還元菌1の優先的な培養に適した環境を維持することができる。
【0029】
このように、本発明では電気分解によりクロムを三価から六価に再生するので、簡便であり、必要な装置類も簡単なもので足りる。このため、低コストでクロム還元菌1を集積培養することができる。また、培養槽6中の六価クロム2を再生して使用するので、六価クロム2の使用量が少量で足り、安全性が高く、集積培養に要するコストを更に安くすることができる。
【0030】
クロム還元菌1としては、例えば表1に掲げるものがある。即ち、例えばShwanella、Pseudomonas、Sulfate reducing bacteria、Arthrobacter、Bacillus、Aerococcus、Micrococcus、Aeromonas、Thermoanaerobacter、Cellulomonas、Geobacter、Streptomyces、Escherichia、Enterobacterである。ただし、これらのクロム還元菌1に限るものではない。
【0031】
【表1】

【0032】
電気分解を行うために培養液3には、三価クロムを六価クロム2に酸化させることができる値の電位を与える。実験では、図6に示すように、1V付近の電位で三価クロムが六価クロム2に酸化された。したがって、三価クロムを六価クロム2に酸化させる電位は約1Vであると判断できるので、培養液3に1Vの電位をかけながら培養を行うことが好ましい。
【0033】
また、培養液3中の六価クロム2の濃度が高すぎると、六価クロムの毒性によりクロム還元菌1自身も増殖し難くなるので、六価クロム2の濃度の上限値は、例えば0.5m mol/Lが好ましい。
【0034】
なお、上述の形態は本発明の好適な形態の一例ではあるがこれに限定されるものではなく本発明の要旨を逸脱しない範囲において種々変形実施可能である。例えば、上述の説明では、培養対象微生物がクロム還元菌1であったが、クロム還元菌1以外の微生物でも良い。
【0035】
また、上述の説明では、物質2として六価クロムを使用していたが、六価クロムに限るものではない。例えば、銀(Ag+)、銅(Cu2+)、水銀(Hg2+)、ヨウ素(I2)、亜ヒ酸(AsO2−)、マンガン(Mn2+)、ニッケル(Ni+)、亜セレン酸(SeO32−)のいずれかでも良い。即ち、これらの物質2に還元活性のある微生物1を、これらの物質2を再生しながら培養しても良い。六価クロム2と同様に銀、銅、水銀、ヨウ素も多くの種類の微生物に対し殺菌効果を有しており、銀、銅、水銀、ヨウ素に耐性のある微生物1を選択的に集積培養することができる。また、亜ヒ酸、マンガン、ニッケル、亜セレン酸は多くの種類の微生物に対し生態毒性を有しており、亜ヒ酸、マンガン、ニッケル、亜セレン酸に耐性のある微生物1を選択的に集積培養することができる。これらの場合にも、上述のクロム還元菌1を培養する場合と同様の効果を得ることができる。
【0036】
なお、物質2が銀の場合、培養液3中のAg+を銀還元菌1がAgに還元し、これを電気分解によってAg+に再生することが考えられる。また、物質2が銅の場合、培養液3中のCu2+を銅還元菌1がCuに還元し、これを電気分解によってCu2+に再生することが考えられる。また、物質2が水銀の場合、培養液3中のHg2+を水銀還元菌1がHgに還元し、これを電気分解によってHg2+に再生することが考えられる。また、物質2がヨウ素の場合、培養液3中のI2をヨウ素還元菌1がI−に還元し、これを電気分解によってI2に再生することが考えられる。また、物質2が亜ヒ酸の場合、培養液3中の亜ヒ酸を亜ヒ酸還元菌1がヒ素に還元し、これを電気分解によって亜ヒ酸に再生することが考えられる。また、物質2がマンガンの場合、培養液3中のMn2+をマンガン還元菌1がMnに還元し、これを電気分解によってMn2+に再生することが考えられる。また、物質2がニッケルの場合、培養液3中のNi+をニッケル還元菌1がNiに還元し、これを電気分解によってNi+に再生することが考えられる。また、物質2が亜セレン酸の場合、培養液3中の亜セレン酸を亜セレン酸還元菌1がセレンに還元し、これを電気分解によって亜セレン酸に再生することが考えられる。
【0037】
また、物質2として六価クロム2を使用して、ウラン還元菌1を選択的に集積培養しても良い。即ち、ウラン還元菌1によって還元された三価クロムを培養液3中に流した電気により酸化反応を生じさせて六価クロム2に再生しながら培養を行うようにしても良い。この場合にも、クロム還元菌1を培養する場合と同様の効果を得ることができる。ウラン還元菌1として、六価クロムに対し還元活性を有し且つ耐性のあるものがある。ウランを溶解させた培養液3でウラン還元菌1を培養することが安全面、コスト面等で不利な場合がある。このような場合には、ウラン還元菌1を六価クロムを溶解させた培養液3中で培養することが安全面、コスト面等で有利となることも考えられる。
【0038】
また、上述の説明では、発酵の過程で物質2を還元する微生物1を例に説明していたが、必ずしも発酵の過程で物質3を還元する微生物1に限るものではなく、呼吸の過程で物質2を還元する微生物1を培養しても良い。
【実施例1】
【0039】
本発明により、クロム還元菌1を良好に培養できることを確認するための実験を行った。使用した培養装置を図2に示す。電解槽4は外径75mm、高さ90mmのガラス製深底シャーレの内側を、一価の陽イオン透過性の交換膜(旭化成、K−192)5で仕切った二槽式とし、片方を培養槽6、もう一方を対極槽7とした。培養槽6には白金網(40mm×70mm、80mesh)製の陽極8、および銀・塩化銀参照電極10(HS−205C、東亜DKK社)を設置した。さらに、対極槽7には炭素板(40mm×70mm、4mm厚)を陰極9として設置した。これら3本の電極8,9,10を電位制御装置11に結線する事で、培養槽6内の陽極8の電位を厳密に設定可能とした 。
【0040】
培養に際しては、電解槽4をアクリル製の嫌気ボックス12内に封入し、さらに嫌気ボックス全体を30度に設定した恒温槽(図示せず)内に設置した。嫌気ボックス12には、常時窒素ガスを注入し(0.2L/min)、嫌気雰囲気を維持した。
【0041】
培養液3の組成を表2に、その中の金属溶液の組成を表3に示す。なお、以下の実験では、全てこの組成の培養液3を用いた。
【0042】
【表2】

【表3】

【0043】
培養液3はまず、無機基本成分を調整後にオートクレーブ滅菌を施した。実験直前に、クロム塩および有機成分(Yeast Extract:0.2g/L、乳酸ナトリウム:1g/L)を混合し、フィルター(0.22μm,Millex-GS,MILLIPORE,Ireland)によりろ過除菌した。
【0044】
陽極8に+1.0Vの電位を与えながら2週間にわたり培養を行った。その結果を図3に示す。2週間の培養でクロム還元菌1の濃度が初期状態の約3倍に増加したことを確認できた。本発明によってクロム還元菌1を培養できることを確認できた。なお、クロム還元菌1の数は、光学顕微鏡観察による菌数カウントによって計測した。
【0045】
また、微生物の形状に関する、より詳細な視覚的情報の取得を目的として、原子間力顕微鏡(AFM:Digital Instruments社、Nanoscope IIIa)による観察を行った。上記実験後の試料(本発明試料)と、比較のためにバイアル瓶を用いて培養を行った試料(比較試料)について観察を行った。AFM観察試料は、アセトン中で超音波洗浄したカバーガラス(MATSUNAMI,Micro cover glass,18×18mm)を用いて作成した。カバーガラス上に微生物の懸濁液50μLを滴下し、約1時間常温で静置後、カバーガラスを蒸留水中に10秒間浸漬させ、培養液3成分を洗い流した。その後、約1時間常温大気中で乾燥させ、測定に供した。AFM測定は大気中にておこない、探針の制御法はコンタクトモードを採用した。個々のサンプルに対し、20μm×20μmの領域をスキャンし、画像を取得した。なお、比較試料を得るためのバイアル瓶を用いた培養は、以下の通り行った。即ち、微生物懸濁液にクロム塩、および有機成分を添加し、100mL容のバイアル瓶に30mL注入し、ブチルゴム栓およびアルミキャップにより密栓した。続いて、バイアル瓶内のガスを窒素に置換し、最終ガス圧を1.5気圧に調整した。バイアル瓶は30度の恒温室にて振とう培養に供した。
【0046】
その結果を図4に示す。図4(A)は比較試料についての画像写真、図4(B)は本発明試料についての画像写真である。なお、各図中右下の線の長さは5μmに相当する。比較試料では複数種の微生物の増殖が確認されたのに対し、本発明試料では菌形のそろった単一の微生物の増殖が確認できた。本発明試料で確認された微生物はクロム還元菌1であり、本発明によってクロム還元菌1を選択的に集積培養を行うことができることを確認できた。
【0047】
さらに念のため、上記実験(陽極8に+1.0Vの電位を与えながらの実験)によって集積培養した微生物を、今度は陽極8に電位を与えずに2週間培養した。その結果を図5に示す。図5からも明らかなように、培養液3中の六価クロム2の濃度の減少が確認された。これにより、上記実験によって集積培養された微生物がクロム還元菌1であることを再確認できた。
【実施例2】
【0048】
陽極8に与える電位を決定するための実験を行った。クロムをはじめとする種々の電極活性物質2の酸化還元電位の測定は、電気化学アナライザー(ALSモデル660B、BAS社)を使用し、サイクリックボルタンメトリー(CV)法により実施した。この際、電解系は3極式で行い、電極反応を見るための作用極には白金円盤電極(面積:0.785mm2、BAS社)を、参照電極には銀・塩化銀電極(RE−1B、BAS社)、さらに電流を流すための対極には白金棒電極(1mm径×5cm、自作)を使用した。それぞれの電極活性物質2、具体的には六価クロムについては1m mol/L濃度で調整し、銀,銅,水銀,ヨウ素,亜ヒ酸,マンガン,ニッケル,亜セレン酸については5m mol/L濃度で調整し、電解質溶液中に溶解させた。CV結果は、それぞれの物質2ごとに、物質2の入っていない電解質溶液をベースラインとして表示した。
【0049】
六価クロム2についての酸化電位の測定結果を図6に示す。図6において、薄い色の実線はクロムを含まない培養液3(バックグラウンド)についての測定結果、濃い色の実線は1m mol/Lのクロムイオンを含む培養液3についての測定結果である。なお、横軸(電位)は、銀塩化銀参照電極に対する値である(図7〜図14において同じ)。培養液3にクロムが存在する状態で、電気化学的に酸化還元を行わせると、0V付近(矢印A)に還元電流、+1V付近(矢印B)に酸化電流の増加が確認できた。これらはそれぞれ、Cr(VI)→Cr(III)、Cr(III)→Cr(VI)の反応に起因する電流値であると判断できる。これは、培養液3に常時+1Vの電位を加えることで、培養液3中のクロムをCr(VI)に保持できることを示している。したがって、培養中に与える電位は+1.0Vが適している。
【0050】
銀(Ag+)についての酸化電位の測定結果を図7に示す。図7において、実線は銀を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの銀イオンを含む培養液についての測定結果である。培養液に銀が存在する状態で、電気化学的に酸化還元を行わせると、+0.5V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.5Vが適している。
【0051】
銅(Cu2+)についての酸化電位の測定結果を図8に示す。図8において、実線は銅を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの銅イオンを含む培養液についての測定結果である。培養液に銅が存在する状態で、電気化学的に酸化還元を行わせると、0V付近と+0.2V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、0V又は+0.2Vが適している。
【0052】
水銀(Hg2+)についての酸化電位の測定結果を図9に示す。図9において、実線は水銀を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの水銀イオンを含む培養液についての測定結果である。培養液に水銀が存在する状態で、電気化学的に酸化還元を行わせると、+0.3V付近と+0.6V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.3V又は+0.6Vが適している。
【0053】
ヨウ素(I2)についての酸化電位の測定結果を図10に示す。図10において、実線はヨウ素を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lのヨウ素を含む培養液についての測定結果である。培養液にヨウ素が存在する状態で、電気化学的に酸化還元を行わせると、+0.5V付近と+0.8V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.5V又は+0.8Vが適している。
【0054】
亜ヒ酸(AsO2−)についての酸化電位の測定結果を図11に示す。図11において、実線は亜ヒ酸を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの亜ヒ酸を含む培養液についての測定結果である。培養液に亜ヒ酸が存在する状態で、電気化学的に酸化還元を行わせると、+0.7V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.7Vが適している。
【0055】
マンガン(Mn2+)についての酸化電位の測定結果を図12に示す。図12において、実線はマンガンを含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lのマンガンイオンを含む培養液についての測定結果である。培養液にマンガンが存在する状態で、電気化学的に酸化還元を行わせると、+0.7V付近と+1.0V付近(2つの矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.7V又は+1.0Vが適している。
【0056】
ニッケル(Ni+)についての酸化電位の測定結果を図13に示す。図13において、実線はニッケルを含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lのニッケルイオンを含む培養液についての測定結果である。培養液にニッケルが存在する状態で、電気化学的に酸化還元を行わせると、−0.4V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、−0.4Vが適している。
【0057】
亜セレン酸(SeO32−)についての酸化電位の測定結果を図14に示す。図14において、実線は亜セレン酸を含まない培養液(バックグラウンド)についての測定結果、破線は5m mol/Lの亜セレン酸を含む培養液についての測定結果である。培養液に亜セレン酸が存在する状態で、電気化学的に酸化還元を行わせると、+0.5V付近(矢印)に酸化電流の増加が確認できた。したがって、培養中に与える電位は、+0.5Vが適している。
【実施例3】
【0058】
培養液3中の六価クロム2の濃度の適正値を求めるための実験を行った。実験ではバイアル瓶を使用し、電位を与えない状態(六価クロム2の再生を行わない状態)で実験を行った。微生物懸濁液にクロム塩、および有機成分を添加し、100mL容のバイアル瓶に30mL注入し、ブチルゴム栓およびアルミキャップにより密栓した。続いて、バイアル瓶内のガスを窒素に置換し、最終ガス圧を1.5気圧に調整した。バイアル瓶は30度の恒温室にて振とう培養に供した。微生物として2箇所の土壌(土壌A、土壌B)から採取したクロム還元菌1を使用し、培養液3中の六価クロム2の初発濃度が0.1m mol/L、0.2m mol/L、0.5m mol/L、1.0m mol/Lの4つの値について実験を行った。また、比較のために、クロム還元菌1を投入しない場合(control)についても実験を行った。
【0059】
まず最初に、クロム還元菌1による培養液3中の六価クロム濃度の時間変化についての測定結果を図15に示す。図15(A)は六価クロム2の初発濃度が0.1m mol/Lの場合、(B)は六価クロム2の初発濃度が0.2m mol/Lの場合、(C)は六価クロム2の初発濃度が0.5m mol/Lの場合、(D)は六価クロム2の初発濃度が1.0m mol/Lの場合である。なお、各図では縦軸のスケールが異なっている。六価クロム2の初発濃度が0.1と0.2m mol/Lの場合には、実験開始から1〜2週間で六価クロム2の濃度が0近くまで減少した。また、六価クロム2の初発濃度が0.5m mol/Lの場合には、六価クロム濃度の減少は僅かであった。一方、六価クロム2の初発濃度が1.0m mol/Lの場合、六価クロム濃度の有意な減少はみられなかった。
【0060】
なお、培養液3中のクロムは、六価クロム2の状態では溶液中に溶解しているが、三価クロムの状態では沈殿するので、培養液3をフィルター(0.22μm,Millex-GS,MILLIPORE,Ireland)で三価クロムをろ過することにより、六価クロム2のみを抽出し、クロム濃度を分析した。クロムの定量にはICP発光分析装置(P8000、HITACHI社)を使用した。
【0061】
次に、各初発濃度における菌濃度の時間変化についての測定結果を図16に示す。なお、図中縦軸は、クロム還元菌1を含む菌全体(クロム還元菌1以外の雑多な菌も含む)の濃度(cells/mL)である。また、図中右上四角枠内の数値(0.1/0.2/0.5/1.0)は、六価クロム2の初発濃度(m mol/L)を示している。図16(A)は土壌Aについての測定結果、図16(B)は土壌Bについての測定結果である。
【0062】
六価クロム初発濃度が0.2m mol/L以下の場合、培養後半では六価クロム2の濃度がほぼゼロになっている(図15(A)(B))ことから、図16(A)(B)の0.1、0.2m mol/Lで増えている菌は、雑多な菌も含まれていると考えられる。一方、六価クロム初発濃度0.5m mol/Lの場合、培養後半でも六価クロム2が維持されている(図15(C))ので、図16(A)(B)の0.5m mol/Lで増えている菌は、クロム還元菌1であると考えられる。すなわち、土壌A、土壌Bに含まれるクロム還元菌1は、与えられた培養液3環境において、少なくともそれぞれ、1.4×109cells/mL、6×108cells/mLまで増殖できることが確認できた。
【0063】
なお、六価クロム2が培養液3中に残っているにもかかわらず、微生物1の増殖が止まっているのは、六価クロム2が微生物1の増殖に直接関与しない物質である(即ち、微生物が呼吸するのに六価クロム2を必要とするのではなく、微生物1の発酵の過程で六価クロム2を還元する)証であり、おそらくは増殖に必要な有機物が使い尽くされたためと考えられる。
【0064】
一方、六価クロム2の初発濃度1.0m mol/Lの場合、ここで増えているのはクロム還元菌1と考えられる(図15(D)より培養液3中に六価クロム2が存在しているため)が、0.5m mol/Lの場合に比べて明らかに菌体濃度が低いことから(図16)、1.0m mol/Lの場合の六価クロム2は、クロム還元菌1自体の増殖を阻害していると考えられる。
【0065】
以上より、培養液3中の六価クロム濃度が高過ぎても培養に適さないことがわかった。そして、具体的には、クロム還元菌1の集積培養の際には、0.5m mol/L以下の六価クロム濃度にて、培養液3中の六価クロム2がなくならないような条件の下で培養することが好ましいことがわかった。
【0066】
また、培養液3中の六価クロム濃度が低すぎるとクロム還元菌1以外の雑多な菌の繁殖を許してしまうことになるので、六価クロム濃度としては、最低でも雑多な菌の繁殖を抑えることができる濃度を確保する必要がある。例えば、0.1m mol程度の濃度を確保することが好ましい。
【図面の簡単な説明】
【0067】
【図1】本発明の微生物の集積培養方法の実施形態の一例を示す概念図である。
【図2】クロム還元菌の集積培養の実験に使用した培養装置の概念図である。
【図3】クロム還元菌の集積培養の実験結果を示す図である。
【図4】培養後の微生物群の顕微鏡画像を示し、(A)は比較試料についての顕微鏡画像、(B)は本発明試料についての顕微鏡画像である。
【図5】培養後の微生物がクロム還元菌であることを再確認するための実験結果を示す図である。
【図6】クロムの酸化電位の測定結果を示す図である。
【図7】銀の酸化電位の測定結果を示す図である。
【図8】銅の酸化電位の測定結果を示す図である。
【図9】水銀の酸化電位の測定結果を示す図である。
【図10】ヨウ素の酸化電位の測定結果を示す図である。
【図11】亜ヒ酸の酸化電位の測定結果を示す図である。
【図12】マンガンの酸化電位の測定結果を示す図である。
【図13】ニッケルの酸化電位の測定結果を示す図である。
【図14】亜セレン酸の酸化電位の測定結果を示す図である。
【図15】クロム還元菌による六価クロム濃度の時間変化を示し、(A)は六価クロム初発濃度が0.1m mol/Lの場合の測定結果、(B)は六価クロム初発濃度が0.2m mol/Lの場合の測定結果、(C)は六価クロム初発濃度が0.5m mol/Lの場合の測定結果、(D)は六価クロム初発濃度が1.0m mol/Lの場合の測定結果である。
【図16】六価クロム初発濃度ごとのクロム還元菌濃度の時間変化を示し、(A)は土壌Aより採取したクロム還元菌についての測定結果、(B)は土壌Bより採取したクロム還元菌についての測定結果である。
【符号の説明】
【0068】
1 培養対象微生物
2 六価クロム(物質)
3 培養液
【特許請求の範囲】
【請求項1】
培養対象微生物が還元活性を有し且つ耐性のある物質を溶解させた培養液中で前記培養対象微生物を選択的に集積培養する際、前記培養対象微生物によって還元された前記物質を前記培養液中に浸した電極に電位を与えることで酸化反応を生じさせて再生しながら培養を行うことを特徴とする微生物の集積培養方法。
【請求項2】
前記培養液には有機物が含まれており、前記培養対象微生物は前記有機物を利用した発酵の過程で前記物質を還元することを特徴とする請求項1記載の微生物の集積培養方法。
【請求項3】
前記物質は、前記培養対象微生物以外の微生物に対して毒性を有していることを特徴とする請求項1又は2記載の微生物の集積培養方法。
【請求項4】
前記物質は、六価クロム、銀、銅、水銀、ヨウ素、亜ヒ酸、マンガン、ニッケル、亜セレン酸のいずれか1つであることを特徴とする請求項3記載の微生物の集積培養方法。
【請求項5】
前記培養対象微生物はクロム還元菌であり、前記物質は六価クロムであり、前記クロム還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うことを特徴とする請求項1又は2記載の微生物の集積培養方法。
【請求項6】
前記培養対象微生物はウラン還元菌であり、前記物質は六価クロムであり、前記ウラン還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うことを特徴とする請求項1又は2記載の微生物の集積培養方法。
【請求項1】
培養対象微生物が還元活性を有し且つ耐性のある物質を溶解させた培養液中で前記培養対象微生物を選択的に集積培養する際、前記培養対象微生物によって還元された前記物質を前記培養液中に浸した電極に電位を与えることで酸化反応を生じさせて再生しながら培養を行うことを特徴とする微生物の集積培養方法。
【請求項2】
前記培養液には有機物が含まれており、前記培養対象微生物は前記有機物を利用した発酵の過程で前記物質を還元することを特徴とする請求項1記載の微生物の集積培養方法。
【請求項3】
前記物質は、前記培養対象微生物以外の微生物に対して毒性を有していることを特徴とする請求項1又は2記載の微生物の集積培養方法。
【請求項4】
前記物質は、六価クロム、銀、銅、水銀、ヨウ素、亜ヒ酸、マンガン、ニッケル、亜セレン酸のいずれか1つであることを特徴とする請求項3記載の微生物の集積培養方法。
【請求項5】
前記培養対象微生物はクロム還元菌であり、前記物質は六価クロムであり、前記クロム還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うことを特徴とする請求項1又は2記載の微生物の集積培養方法。
【請求項6】
前記培養対象微生物はウラン還元菌であり、前記物質は六価クロムであり、前記ウラン還元菌によって還元された三価クロムを六価クロムに再生しながら培養を行うことを特徴とする請求項1又は2記載の微生物の集積培養方法。
【図1】


【図2】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図3】


【図4】


【図5】


【図6】


【図15】


【図16】




【図2】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図3】


【図4】


【図5】


【図6】


【図15】


【図16】


【公開番号】特開2006−55134(P2006−55134A)
【公開日】平成18年3月2日(2006.3.2)
【国際特許分類】
【出願番号】特願2004−242939(P2004−242939)
【出願日】平成16年8月23日(2004.8.23)
【出願人】(000173809)財団法人電力中央研究所 (1,040)
【Fターム(参考)】
【公開日】平成18年3月2日(2006.3.2)
【国際特許分類】
【出願日】平成16年8月23日(2004.8.23)
【出願人】(000173809)財団法人電力中央研究所 (1,040)
【Fターム(参考)】
[ Back to top ]

