抗インフルエンザウイルス組成物及びインフルエンザ予防食品
【課題】 日常的に経口摂取でき、安全性に優れた抗インフルエンザウイルス組成物の製造方法を提供すること。
【解決手段】 ナガイモの可食部を擂り下ろし、これを10000rpm以下1時間以下で遠心分離することにより得られる上清液は、経口摂取可能な抗インフルエンザウイルス組成物である。これを適宜条件にて超音波処理することにより、粘度を低下させることができる。当該抗インフルエンザ組成物は、凍結乾燥などによって乾燥粉末化することができる。
【解決手段】 ナガイモの可食部を擂り下ろし、これを10000rpm以下1時間以下で遠心分離することにより得られる上清液は、経口摂取可能な抗インフルエンザウイルス組成物である。これを適宜条件にて超音波処理することにより、粘度を低下させることができる。当該抗インフルエンザ組成物は、凍結乾燥などによって乾燥粉末化することができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は抗インフルエンザウイルス組成物及びインフルエンザ予防食品に係り、特に、ナガイモに存在する抗インフルエンザウイルス活性を食品分野において利用する新規な発明に関する。
【背景技術】
【0002】
インフルエンザウイルスにはA・B・Cの3型があり、このうちA型とB型が、ヒトのインフルエンザの主要な原因になる。今まで開発されたインフルエンザ治療薬としては、ノイラミニダーゼ阻害薬であるオセルタミビル(商品名:タミフル(登録商標))があり、これはA型・B型両方に効果がある。しかしながら小児等において、異常行動を誘発する例が報告されている。同じくノイラミニダーゼ阻害薬であるザナミビル(商品名:リレンザ(登録商標))は、A型・B型両方に効果がある。また、M2蛋白阻害剤であるアマンタジン(商品名:シンメトレル(登録商標)など)は、A型のみに効果がある。
【0003】
一方、インフルエンザの予防方法としては、ワクチンの接種がある。ワクチンは、身体の免疫機構を利用して、ウイルスが入ってきても感染させないようにするものである。
【0004】
また従来から、腸内細菌を利用して自然免疫を活性化させ、抵抗性を高める技術が実験動物レベルで提案されているが、最近はさらに、ビフィドバクテリウム(Bifidobacterium)属に属する微生物を用いて、この細菌自体を有効成分とするインフルエンザ感染予防剤を製造し、これを有効成分として含有するインフルエンザ感染予防用飲食品の技術的提案もなされている(特許文献1)。
【特許文献1】特開2007−169200号公報「インフルエンザ感染予防のための医薬及び飲食品」
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかし、治療薬あるいは予防薬のいずれにせよ、医薬には本来、副作用や耐性株の出現などの危険性があり、場合によっては適用できない集団・利用者もある。もちろん、日常的に常食することができないことはいうまでもない。
【0006】
また、ワクチンによる免疫力の賦活は、年齢層(幼児、高齢者など)や、身体状態(過労、ストレス、睡眠不足など)により大きく影響するため、ワクチン接種の効果に個人差が存在する。そもそも予防効果を得るためには、ワクチンを予め接種し、血中のインフルエンザウイルスに対する抗体を高めておく必要がある。
【0007】
さらに、抗原となるインフルエンザワクチンは予め流行株を予測して製造するものであり、これには9ヶ月程度を要するために、実際に流行しているインフルエンザウイルスと、接種したインフルエンザワクチンの型が一致せず、有効性が見いだされない場合もあり、次の冬に流行するウイルス株を正確に予測することが難しいという問題点もある。
【0008】
また、微生物を用いた予防技術には相応の製造態勢、管理態勢および事業規模が必要であり、たとえば地方の中小企業等にとっても、決して導入容易な技術ではない。
【0009】
本発明の課題は上記従来技術の問題点を解決しようとするものであり、日常的に経口摂取でき、副作用もなく、安全性に優れ、その上製造容易・技術導入容易なインフルエンザ予防食品、その原料とする抗インフルエンザウイルス組成物、およびこれらの製造方法を提供することである。
【課題を解決するための手段】
【0010】
さて本願発明者らは、抗インフルエンザウイルス作用を有し、主に食品として経口的に摂取することが可能な有効成分について、地場農産物を対照として探索を行っていたところ、ナガイモの抽出成分がA型(A/H1N1、A/H3N2)及びB型のインフルエンザウイルスに対して抗ウイルス作用を示すことを見出した。ここで発見されたナガイモの抽出成分による抗ウイルス活性の作用機序は、「A型およびB型インフルエンザウイルスに接着することにより、ウイルスが細胞に感染するのを阻害する」というものであり、これは従来の治療薬や予防薬とは全く異なるものである。
【0011】
つまり上記課題は、かかるナガイモの抗インフルエンザウイルス活性を利用することによって解決し得ることを見出し、本発明に至った。すなわち、本願において特許請求もしくは少なくとも開示される発明は、以下のとおりである。
【0012】
(1) ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、経口摂取可能な抗インフルエンザウイルス組成物。
(2) 前記ヤマノイモ属植物はナガイモであることを特徴とする、(1)に記載の抗インフルエンザウイルス組成物。
(3) ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を含むことを特徴とする、抗インフルエンザウイルス組成物。
(4) ヤマノイモ属植物の地下茎または担根体を擂り下ろし、これを10000rpm以下1時間以下の遠心分離することにより上清液として得られる、経口摂取可能な抗インフルエンザウイルス組成物の製造方法。
【0013】
(5) 前記上清液の粘度を低下させるため、これを超音波処理することを特徴とする、(4)に記載の抗インフルエンザウイルス組成物の製造方法。
(6) 前記上清液の粘度を0.005Pa・s以下とすることを特徴とする、(5)に記載の抗インフルエンザウイルス組成物の製造方法。
(7) 前記上清液を乾燥処理して得られることを特徴とする、(4)ないし(6)のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
(8) 前記ヤマノイモ属植物はナガイモであることを特徴とする、(4)ないし(7)のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
【0014】
(9) ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、インフルエンザ予防食品。
(10) ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を有効成分として含有する、インフルエンザ予防食品。
(11) ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を原料として用いるインフルエンザ予防食品の製造方法であって、該抽出物が配合される以後の工程においては温度60℃以下かつpH3.0以上に維持されることを特徴とする、インフルエンザ予防食品の製造方法。
(12) 前記ヤマノイモ属植物はナガイモであることを特徴とする、(11)に記載のインフルエンザ予防食品の製造方法。
【0015】
なお、ナガイモが属するヤマノイモ科(Dioscoreaceae)は単子葉植物の科で、8属、約800種ほどがあるが、ナガイモを始めとしてそのほとんどはヤマノイモ属(Discorea)に属する。特に、地下茎または担根体(以下、これらを「いも」または「可食部」という。)が、古くから食用や薬用として利用されている。以下の説明はすべてナガイモによるものだが、今回ナガイモにおいて発見された抗ウイルス効果は、ヤマノイモ科の他の植物においても同様に存在する可能性が充分あるものと考えられる。
【発明の効果】
【0016】
本発明の抗インフルエンザウイルス組成物、それを原料に用いたインフルエンザ予防食品およびこれらの製造方法は上述のように構成されるため、これによれば、経口摂取によって、有効にインフルエンザ(A型、B型)感染を予防することができる。しかも本発明の抗インフルエンザウイルス組成物もインフルエンザ予防食品も医薬ではないため副作用もなく、安全性に優れている。
【0017】
さらに、ナガイモやその他のヤマノイモ属の作物は食経験が豊富な食材であることから、消費者の安心感も強く、日常的な経口摂取つまり常食にも何ら問題がない。その上、製造容易、技術導入も容易である。
【発明を実施するための最良の形態】
【0018】
以下、本発明についてより詳細に説明する。
本願発明の抗インフルエンザウイルス組成物の原料とするヤマノイモ属植物は、以下実施例で詳述するナガイモには限定されない。たとえば、イチョウイモ、ツクネイモ・丹波ヤマノイモ・大和イモ・伊勢イモ(以上、ツクネイモ群)、また、ヤマイモ(自然薯)であってもよい。いずれの場合も、利用する部位は可食部(いも)である。
【0019】
本発明の抗インフルエンザウイルス組成物の製造方法において、可食部の擂り下ろし処理は、要するに可食部を擂り、潰して、流動性のある状態にできる処理であればよく、具体的な方法は問わない。
【0020】
また、擂り下ろした可食部の遠心分離処理の条件も特に限定されるものでないが、たとえばナガイモの場合は、10000rpm以下1時間以下の処理によって、良好な上清液を得られる。ナガイモ以外の場合も適宜の条件により、遠心分離処理されればよい。
【0021】
遠心分離処理により得られる上清液の粘度を低下させることにより、食品素材としての取扱い性を向上させることができる。粘度低下には超音波処理が簡単で適している。処理条件は特に限定されない。ナガイモの場合でも、上清液の粘度を0.005Pa・s以下にすることは容易である。なお、他のいもの場合も、粘度低下を目的として、適宜の条件によって超音波処理することができる。
【0022】
また、上清液のままではなく、これを適宜の方法によって乾燥処理し、乾燥粉末など固体化すれば、さらに取扱い性も保存性も向上する。具体的な乾燥手段も特に限定されるものではないが、熱をかけないようにするため、凍結乾燥処理は適している。なお本発明における抽出物には、上述のように可食部を処理して上清液とし、さらにこれを高度に精製してなるものの他、そこに至るまでの途中の形態のものも該当するものとする。また、上清液の形態以外のものも該当するものとする。なお、上述の抽出操作の一部または全部をせずに、ヤマノイモ属植物の地下茎または担根体(可食部)を用いることによっても、ヤマノイモ属植物の地下茎もしくは担根体に含まれる有効成分を利用することとなるため、一定程度の抗インフルエンザ効果の得られることが期待できる。たとえば、可食部を摺り下ろした全量を遠心分離することなく全て用いる場合などである。
【0023】
ナガイモなどヤマノイモ属植物の可食部からの抽出物を原料の一部として添加することにより、インフルエンザ予防食品とすることができる。食品の形態は特に限定されない。たとえば、実施例のように固形状食品に適用する以外にも、流動状の食品や、あるいは飲料に添加してもよい。つまり本発明のインフルエンザ予防食品には、飲料品も含まれる。
【0024】
インフルエンザ予防食品の製造にあたっては、その有効成分である抽出物の熱安定性、pH安定性等の特性を考慮した製造方法が必要である。具体的には、抽出物が配合される以後の工程においては温度60℃以下で、さらにpH3.0以上に維持されることが、抽出物の抗インフルエンザウイルス活性を維持する上で重要である。
【実施例】
【0025】
以下、ナガイモについての実施例も紹介しつつ本発明をさらに詳細に説明するが、本発明はこれらの実施例等に限定されるものではない。
まず、後述する実施例に用いた抗インフルエンザ活性の試験例を示す。
[試験例1]
本試験は、本発明の抗インフルエンザウイルス組成物の有効成分であるナガイモ抽出物がインフルエンザウイルス感染細胞における細胞変性効果(CPE)を抑制するかを調べるために行った。
供試インフルエンザウイルスとしては、A/Yamagata/120/86(H1N1)、A/H3N2及びB型を用いた。培養動物細胞として、イヌ腎株化(MDCK)細胞を用いた。細胞増殖には、10%のウシ胎仔血清を添加したイーグルMEM培地を用い、細胞維持には、5μg/mlトリプシン、100μg/mlカナマイシン及び100μg/mlゲンタマイシンを添加したイーグルMEM培地を用いた。
【0026】
ナガイモ抽出液等の試料と上記インフルエンザウイルスのいずれかを含むウイルス液を等量混合後、35℃で1時間放置した。この混合液を培養したMDCK細胞に加えて1時間吸着後、試料液を除去した。試料液を除去した後のMDCK細胞に維持培地を添加し、35℃の5%CO2インキュベーターで培養を行った。顕微鏡によりCPEの有無を観察し、CPE抑制効果がある場合を陽性、ない場合を陰性とした。
【0027】
[試験例2]
本試験(プラーク形成法)は、抗インフルエンザウイルス活性の強さを定量的に調べるために行った。
30万個/3mlのMDCK細胞溶液を直径3cmのプレートに入れ、35℃のCO2インキュベーター内で2日間培養した。0.1mlのインフルエンザウイルス溶液と0.1mlのナガイモ抽出溶液を混合後、培養したMDCK細胞に添加し、35℃のCO2インキュベーター内で60分間吸着を行った。次に、A培地(イーグルMEM0.094g、ノーブルアガー0.08g、蒸留水9.367ml、7.5%NaHCO30.3ml、L−グルタミン0.1ml、100XMEM用ビタミン液(100倍濃度MEM培地用補助ビタミン液)0.01ml、30%グルコース0.033ml、トリプシン(SIGMA)0.1ml及び0.2%BSA0.1mlを含む)を重層した。
【0028】
35℃のCO2インキュベーター内で2日間培養した後、B培地(イーグルMEM0.093g、ノーブルアガー0.1g、蒸留水9.54ml、7.5%NaHCO30.3ml、L−グルタミン0.1ml、100XMEM用ビタミン液(100倍濃度MEM培地用補助ビタミン液)0.01ml、0.2%BSA0.1ml及び1%ニュートラルレッド0.05mlを含む)を重層した。35℃のCO2インキュベーター内で1日間培養した後、プラーク数を計測した。
【0029】
<実施例1 ナガイモ抽出物の調製>
ナガイモ5本(5060g)の皮を剥ぎ、可食部4170gを得た。この可食部をフードカッターで擂り下ろし、9000rpmで45分間、遠心分離を行い、2780ml(2815g)の上清液(粗抽出液)を得た。上清液を凍結乾燥後、粉砕して乾燥粉末121.8gを得た。
【0030】
ナガイモ(生)、粗抽出液及び凍結乾燥物の成分分析結果を表1に示した。粗抽出液及び凍結乾燥物の抗インフルエンザウイルス活性を試験例1により調べた結果、良好に活性を保持していた。また、粗抽出液及び乾燥物の抗インフルエンザウイルス活性は、種々の飲食品の製造において抗インフルエンザウイルス組成物として使用できる強さを有していた。
【0031】
【表1】

【0032】
粗抽出液は、そのままでも抗インフルエンザウイルス組成物として使用できるが、超音波処理によって粘度を低下させることで、さらに広範囲な飲食品への適用が可能となる。粗抽出液の粘度は、30分間以上超音波処理(周波数40kHz)することで、抗インフルエンザウイルス活性の機能を維持したまま、水に近い粘度まで低下させることが可能であった。
図1は、超音波処理時間によるナガイモ粗抽出液粘度変化を示すグラフである。
【0033】
<実施例2 ナガイモ粗抽出液の抗ウイルス活性>
ナガイモ粗抽出液に含まれる抗インフルエンザウイルス活性をもつ成分の特性を、以下のように調べた。
(1)熱安定性
実施例1における粗抽出液を、25、40、50、60若しくは70℃で60分間の加熱、又は、100℃で5分間の加熱後、試験例1により抗インフルエンザウイルス活性を調べた。その結果、25、40、50若しくは60℃で60分間の加熱では活性を維持していたが、70℃で60分間若しくは100℃で5分間の加熱では活性を失っていた。したがって活性成分は、60℃以下で安定であることが示された。
【0034】
(2)保存安定性
ナガイモ粗抽出液を、室温、冷蔵又は冷凍の温度帯で1ヶ月、3ヶ月又は6ヶ月間保存した後で抗インフルエンザウイルス活性を調べた。その結果、いずれの温度帯及び保存期間においても活性が保持されていた。したがって、活性成分は、室温で少なくとも6ヶ月間は安定であることが示された。
【0035】
(3)pH安定性
塩酸溶液を用いてナガイモ粗抽出液(pH6.8)のpHを3.0に調整した場合、白濁して凝集体が生じた。この溶液をpH6.8に戻すと透明な液となったが、活性は消失した。この結果から、活性成分はpH3.0以下では不安定であることが示された。
【0036】
(4)有効接触時間
ナガイモ粗抽出液とインフルエンザウイルス液を等量混合後、35℃で1、5、10、15、30、45又は60分間接触した。その後は、試験例1に従いCPE抑制効果を調べた。その結果、全ての接触時間でCPE抑制効果を観察できた。したがって、インフルエンザウイルスとナガイモ粗抽出液を1分間程度接触することにより、ウイルスが細胞に感染するのを抑制できることが示された。
【0037】
<実施例3 ナガイモ粗抽出液のインフルエンザ予防効果>
試験例2(プラーク形成法)を用いて、インフルエンザウイルス感染の予防に必要なナガイモ粗抽出液の量を定量的に測定した。その結果、ナガイモ粗抽出液(タンパク質量として0.03mg)で20個のインフルエンザウイルスによる細胞感染を完全に阻害することができた。
【0038】
人の1回のくしゃみによる飛沫で他人の口に吸入されるウイルス数は、約10000個であることが推定されている。したがって、10000個のインフルエンザウイルスの細胞感染を予防するナガイモ粗抽出物の量は、タンパク質として15mg(10000個/20個*0.03mg)であると推定できる。前掲表1から、1mlのナガイモ粗抽出液は、固形分として約42mg、タンパク質として約20mgを含むことから、ナガイモ粗抽出液の1mlでインフルエンザウイルスによる感染を予防できる。
【0039】
<実施例4 インフルエンザ予防食品の試作>
実施例3の結果は、1mlのナガイモ粗抽出液(乾燥物として約42mg)がインフルエンザウイルスの感染を予防できることを示した。そこで、ナガイモ粗抽出液の乾燥物を含有する食品を試作し、その食品の抗インフルエンザウイルス活性を調べた。
【0040】
<4−1 錠剤>
錠剤を、1錠の重さを約200mgに設定し、その1/4の50mgが粗抽出液乾燥物になるように配合した。配合例は2種類試みた。表2、3にそれぞれ、配合例1、2を示す。なお、配合例2では、ナガイモ粗抽出液を乾燥する際に、粗抽出液に含まれる固形分と同量のトレハロースを添加してから凍結乾燥して得た乾燥物を用いた。
【0041】
【表2】

【0042】
【表3】

【0043】
試験例1に従い試作品の抗インフルエンザウイルス活性を調べた結果、配合例1の試作品は活性を示したが、配合例2では活性が認められなかった。配合例2では、使用したクエン酸の量が配合例1と比較して多いため、活性成分の安定pH領域以下になり、活性が消失したと考えられた。したがって、本発明飲食品の製造にあたっては、工程中のみならず最終製品のpHも考慮すべきことが示された。
【0044】
<4−2 錠菓>
錠菓(ラムネ菓子)を、1個あたり40mgの粗抽出液乾燥物を含むように試作した。なお、錠菓配合例3では、ナガイモ粗抽出液を乾燥する際に、粗抽出液に含まれる固形分と同量のトレハロースを添加してから凍結乾燥して得た乾燥物を用いた。表4に、錠菓の配合例(配合例3)を示す。
【0045】
【表4】

【0046】
試験例1に従い試作品の抗インフルエンザウイルス活性を調べた結果、錠菓の配合例3では活性が認められなかった。配合例では、使用したクエン酸の量が前記錠剤の配合例1と比較して多いため、活性成分の安定pH領域以下になり、活性が消失したと考えられた。したがって、本発明飲食品の製造にあたっては、工程中のみならず最終製品のpHも考慮すべきことが示された。
【0047】
<4−3 キャラメルゼリー>
キャラメルゼリーは、生クリーム200g、水飴100g、砂糖75g及びゼラチン50gを加熱・溶解した後、品温が60℃以下になったところでナガイモ粗抽出液60mlを添加・混合し、プレートに流して放冷し、固めた。冷却後、ゼリー1個あたりナガイモ粗抽出液を1ml含むよう60等分し、粉末オブラートをまぶして試作を完成した。
【0048】
抗インフルエンザウイルス活性を測定した結果、活性が認められた。なお、製造時の温度管理を充分に行い、工程中60℃以下を厳密に維持することによって、最終製品の抗インフルエンザウイルス活性を充分なものとできることが、示唆された。
【0049】
<実施例5 ナガイモの抗インフルエンザ機能物質の同定>
1300gのナガイモ(Dioscorea batatas)をミキサーでホモゲナイズした。ホモゲナイズしたナガイモを遠心分離(105000g、45分間)し、620mlの上清液を得た。この上清液を40ml程度に小分けにし、次の実験に使用するまで−40℃で保存した。凍結した上清液(40ml)を解凍後、トリス塩酸緩衝液(10mM、pH7.6)に対して充分に透析した。10mlの透析内液(約100mgのタンパク質を含む)をDEAEセルロースカラム(8ml)に供した。その後、0mM、50mM、100mM及び1MのNaClを含むトリス塩酸緩衝液で段階的に溶出した。
【0050】
図2は、実施例5のDEAEセルロースカラムクロマトグラムである。ここに示すように、DEAEセルロースカラムクロマトグラフィーによって、F1〜F4の画分を得た。試験例1に従って各画分の抗インフルエンザウイルス活性を測定した結果、F2画分に抗インフルエンザ活性が認められた。F2画分の還元条件下でのSDS−PAGEの結果、分子量33000に主要バンドが検出された。また同じく、非還元条件下でのSDS−PAGEでは、分子量30000に主要バンドが検出された。
【0051】
F2画分を集めて、トリス塩酸緩衝液(10mM、pH7.6)に透析後、DEAEセルロースカラム(8ml)に供した。非吸着成分を溶出後、0〜100mMのNaClによるグラジエント溶出を行った。
【0052】
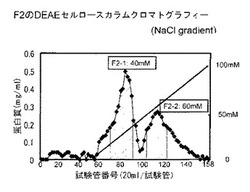
図3は、F2画分のDEAEセルロースカラムクロマトグラムである。図示するように、F2−1画分に抗インフルエンザ活性が認められた。また、MALDI/TOF−MS(マトリックス支援レーザー脱離イオン化飛行時間型質量分析法)により活性物質の分子量は、27590と算定された。
なお図4は、F2−1画分他のMALDI/TOF−MS解析結果を示すグラフである。
【0053】
F2−1画分を集めて、N末端からの15アミノ酸配列を決定した結果、
Val,Glu,Asp、Glu,Phe,Ser,Tyr,Ile,Glu,Gly,Asn,Pro,Asn,Gly,Pro(VEDEF SYIEG NPNGP)であった。この配列は、既知のDioscorea batatas由来のDB2(Mariam Gaidamashvili et al.,Characterization of the yam tuber storage proteins from dioscorea batatas exhibiting unique lectin activities.,J.Biol.Chem.,279(25),26028−26035(2004))と一致した。DB2は、Dioscorin Aに分類される貯蔵タンパク質であり、総ナガイモタンパク質の約30%を占めていた。
【産業上の利用可能性】
【0054】
本発明の抗インフルエンザウイルス組成物等によれば、経口摂取によって、有効にインフルエンザ感染を予防できる。しかも安全性も問題がない。その上、製造容易でもあり、またインフルエンザ予防食品としての応用も広範に可能であり、産業上利用性が高い発明である。
【図面の簡単な説明】
【0055】
【図1】超音波処理時間によるナガイモ粗抽出液粘度変化を示すグラフである。
【図2】実施例5のDEAEセルロースカラムクロマトグラムである。
【図3】実施例5のF2画分のDEAEセルロースカラムクロマトグラムである。
【図4】実施例5のF2−1画分他のMALDI/TOF−MS解析結果を示すグラフである。
【技術分野】
【0001】
本発明は抗インフルエンザウイルス組成物及びインフルエンザ予防食品に係り、特に、ナガイモに存在する抗インフルエンザウイルス活性を食品分野において利用する新規な発明に関する。
【背景技術】
【0002】
インフルエンザウイルスにはA・B・Cの3型があり、このうちA型とB型が、ヒトのインフルエンザの主要な原因になる。今まで開発されたインフルエンザ治療薬としては、ノイラミニダーゼ阻害薬であるオセルタミビル(商品名:タミフル(登録商標))があり、これはA型・B型両方に効果がある。しかしながら小児等において、異常行動を誘発する例が報告されている。同じくノイラミニダーゼ阻害薬であるザナミビル(商品名:リレンザ(登録商標))は、A型・B型両方に効果がある。また、M2蛋白阻害剤であるアマンタジン(商品名:シンメトレル(登録商標)など)は、A型のみに効果がある。
【0003】
一方、インフルエンザの予防方法としては、ワクチンの接種がある。ワクチンは、身体の免疫機構を利用して、ウイルスが入ってきても感染させないようにするものである。
【0004】
また従来から、腸内細菌を利用して自然免疫を活性化させ、抵抗性を高める技術が実験動物レベルで提案されているが、最近はさらに、ビフィドバクテリウム(Bifidobacterium)属に属する微生物を用いて、この細菌自体を有効成分とするインフルエンザ感染予防剤を製造し、これを有効成分として含有するインフルエンザ感染予防用飲食品の技術的提案もなされている(特許文献1)。
【特許文献1】特開2007−169200号公報「インフルエンザ感染予防のための医薬及び飲食品」
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかし、治療薬あるいは予防薬のいずれにせよ、医薬には本来、副作用や耐性株の出現などの危険性があり、場合によっては適用できない集団・利用者もある。もちろん、日常的に常食することができないことはいうまでもない。
【0006】
また、ワクチンによる免疫力の賦活は、年齢層(幼児、高齢者など)や、身体状態(過労、ストレス、睡眠不足など)により大きく影響するため、ワクチン接種の効果に個人差が存在する。そもそも予防効果を得るためには、ワクチンを予め接種し、血中のインフルエンザウイルスに対する抗体を高めておく必要がある。
【0007】
さらに、抗原となるインフルエンザワクチンは予め流行株を予測して製造するものであり、これには9ヶ月程度を要するために、実際に流行しているインフルエンザウイルスと、接種したインフルエンザワクチンの型が一致せず、有効性が見いだされない場合もあり、次の冬に流行するウイルス株を正確に予測することが難しいという問題点もある。
【0008】
また、微生物を用いた予防技術には相応の製造態勢、管理態勢および事業規模が必要であり、たとえば地方の中小企業等にとっても、決して導入容易な技術ではない。
【0009】
本発明の課題は上記従来技術の問題点を解決しようとするものであり、日常的に経口摂取でき、副作用もなく、安全性に優れ、その上製造容易・技術導入容易なインフルエンザ予防食品、その原料とする抗インフルエンザウイルス組成物、およびこれらの製造方法を提供することである。
【課題を解決するための手段】
【0010】
さて本願発明者らは、抗インフルエンザウイルス作用を有し、主に食品として経口的に摂取することが可能な有効成分について、地場農産物を対照として探索を行っていたところ、ナガイモの抽出成分がA型(A/H1N1、A/H3N2)及びB型のインフルエンザウイルスに対して抗ウイルス作用を示すことを見出した。ここで発見されたナガイモの抽出成分による抗ウイルス活性の作用機序は、「A型およびB型インフルエンザウイルスに接着することにより、ウイルスが細胞に感染するのを阻害する」というものであり、これは従来の治療薬や予防薬とは全く異なるものである。
【0011】
つまり上記課題は、かかるナガイモの抗インフルエンザウイルス活性を利用することによって解決し得ることを見出し、本発明に至った。すなわち、本願において特許請求もしくは少なくとも開示される発明は、以下のとおりである。
【0012】
(1) ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、経口摂取可能な抗インフルエンザウイルス組成物。
(2) 前記ヤマノイモ属植物はナガイモであることを特徴とする、(1)に記載の抗インフルエンザウイルス組成物。
(3) ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を含むことを特徴とする、抗インフルエンザウイルス組成物。
(4) ヤマノイモ属植物の地下茎または担根体を擂り下ろし、これを10000rpm以下1時間以下の遠心分離することにより上清液として得られる、経口摂取可能な抗インフルエンザウイルス組成物の製造方法。
【0013】
(5) 前記上清液の粘度を低下させるため、これを超音波処理することを特徴とする、(4)に記載の抗インフルエンザウイルス組成物の製造方法。
(6) 前記上清液の粘度を0.005Pa・s以下とすることを特徴とする、(5)に記載の抗インフルエンザウイルス組成物の製造方法。
(7) 前記上清液を乾燥処理して得られることを特徴とする、(4)ないし(6)のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
(8) 前記ヤマノイモ属植物はナガイモであることを特徴とする、(4)ないし(7)のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
【0014】
(9) ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、インフルエンザ予防食品。
(10) ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を有効成分として含有する、インフルエンザ予防食品。
(11) ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を原料として用いるインフルエンザ予防食品の製造方法であって、該抽出物が配合される以後の工程においては温度60℃以下かつpH3.0以上に維持されることを特徴とする、インフルエンザ予防食品の製造方法。
(12) 前記ヤマノイモ属植物はナガイモであることを特徴とする、(11)に記載のインフルエンザ予防食品の製造方法。
【0015】
なお、ナガイモが属するヤマノイモ科(Dioscoreaceae)は単子葉植物の科で、8属、約800種ほどがあるが、ナガイモを始めとしてそのほとんどはヤマノイモ属(Discorea)に属する。特に、地下茎または担根体(以下、これらを「いも」または「可食部」という。)が、古くから食用や薬用として利用されている。以下の説明はすべてナガイモによるものだが、今回ナガイモにおいて発見された抗ウイルス効果は、ヤマノイモ科の他の植物においても同様に存在する可能性が充分あるものと考えられる。
【発明の効果】
【0016】
本発明の抗インフルエンザウイルス組成物、それを原料に用いたインフルエンザ予防食品およびこれらの製造方法は上述のように構成されるため、これによれば、経口摂取によって、有効にインフルエンザ(A型、B型)感染を予防することができる。しかも本発明の抗インフルエンザウイルス組成物もインフルエンザ予防食品も医薬ではないため副作用もなく、安全性に優れている。
【0017】
さらに、ナガイモやその他のヤマノイモ属の作物は食経験が豊富な食材であることから、消費者の安心感も強く、日常的な経口摂取つまり常食にも何ら問題がない。その上、製造容易、技術導入も容易である。
【発明を実施するための最良の形態】
【0018】
以下、本発明についてより詳細に説明する。
本願発明の抗インフルエンザウイルス組成物の原料とするヤマノイモ属植物は、以下実施例で詳述するナガイモには限定されない。たとえば、イチョウイモ、ツクネイモ・丹波ヤマノイモ・大和イモ・伊勢イモ(以上、ツクネイモ群)、また、ヤマイモ(自然薯)であってもよい。いずれの場合も、利用する部位は可食部(いも)である。
【0019】
本発明の抗インフルエンザウイルス組成物の製造方法において、可食部の擂り下ろし処理は、要するに可食部を擂り、潰して、流動性のある状態にできる処理であればよく、具体的な方法は問わない。
【0020】
また、擂り下ろした可食部の遠心分離処理の条件も特に限定されるものでないが、たとえばナガイモの場合は、10000rpm以下1時間以下の処理によって、良好な上清液を得られる。ナガイモ以外の場合も適宜の条件により、遠心分離処理されればよい。
【0021】
遠心分離処理により得られる上清液の粘度を低下させることにより、食品素材としての取扱い性を向上させることができる。粘度低下には超音波処理が簡単で適している。処理条件は特に限定されない。ナガイモの場合でも、上清液の粘度を0.005Pa・s以下にすることは容易である。なお、他のいもの場合も、粘度低下を目的として、適宜の条件によって超音波処理することができる。
【0022】
また、上清液のままではなく、これを適宜の方法によって乾燥処理し、乾燥粉末など固体化すれば、さらに取扱い性も保存性も向上する。具体的な乾燥手段も特に限定されるものではないが、熱をかけないようにするため、凍結乾燥処理は適している。なお本発明における抽出物には、上述のように可食部を処理して上清液とし、さらにこれを高度に精製してなるものの他、そこに至るまでの途中の形態のものも該当するものとする。また、上清液の形態以外のものも該当するものとする。なお、上述の抽出操作の一部または全部をせずに、ヤマノイモ属植物の地下茎または担根体(可食部)を用いることによっても、ヤマノイモ属植物の地下茎もしくは担根体に含まれる有効成分を利用することとなるため、一定程度の抗インフルエンザ効果の得られることが期待できる。たとえば、可食部を摺り下ろした全量を遠心分離することなく全て用いる場合などである。
【0023】
ナガイモなどヤマノイモ属植物の可食部からの抽出物を原料の一部として添加することにより、インフルエンザ予防食品とすることができる。食品の形態は特に限定されない。たとえば、実施例のように固形状食品に適用する以外にも、流動状の食品や、あるいは飲料に添加してもよい。つまり本発明のインフルエンザ予防食品には、飲料品も含まれる。
【0024】
インフルエンザ予防食品の製造にあたっては、その有効成分である抽出物の熱安定性、pH安定性等の特性を考慮した製造方法が必要である。具体的には、抽出物が配合される以後の工程においては温度60℃以下で、さらにpH3.0以上に維持されることが、抽出物の抗インフルエンザウイルス活性を維持する上で重要である。
【実施例】
【0025】
以下、ナガイモについての実施例も紹介しつつ本発明をさらに詳細に説明するが、本発明はこれらの実施例等に限定されるものではない。
まず、後述する実施例に用いた抗インフルエンザ活性の試験例を示す。
[試験例1]
本試験は、本発明の抗インフルエンザウイルス組成物の有効成分であるナガイモ抽出物がインフルエンザウイルス感染細胞における細胞変性効果(CPE)を抑制するかを調べるために行った。
供試インフルエンザウイルスとしては、A/Yamagata/120/86(H1N1)、A/H3N2及びB型を用いた。培養動物細胞として、イヌ腎株化(MDCK)細胞を用いた。細胞増殖には、10%のウシ胎仔血清を添加したイーグルMEM培地を用い、細胞維持には、5μg/mlトリプシン、100μg/mlカナマイシン及び100μg/mlゲンタマイシンを添加したイーグルMEM培地を用いた。
【0026】
ナガイモ抽出液等の試料と上記インフルエンザウイルスのいずれかを含むウイルス液を等量混合後、35℃で1時間放置した。この混合液を培養したMDCK細胞に加えて1時間吸着後、試料液を除去した。試料液を除去した後のMDCK細胞に維持培地を添加し、35℃の5%CO2インキュベーターで培養を行った。顕微鏡によりCPEの有無を観察し、CPE抑制効果がある場合を陽性、ない場合を陰性とした。
【0027】
[試験例2]
本試験(プラーク形成法)は、抗インフルエンザウイルス活性の強さを定量的に調べるために行った。
30万個/3mlのMDCK細胞溶液を直径3cmのプレートに入れ、35℃のCO2インキュベーター内で2日間培養した。0.1mlのインフルエンザウイルス溶液と0.1mlのナガイモ抽出溶液を混合後、培養したMDCK細胞に添加し、35℃のCO2インキュベーター内で60分間吸着を行った。次に、A培地(イーグルMEM0.094g、ノーブルアガー0.08g、蒸留水9.367ml、7.5%NaHCO30.3ml、L−グルタミン0.1ml、100XMEM用ビタミン液(100倍濃度MEM培地用補助ビタミン液)0.01ml、30%グルコース0.033ml、トリプシン(SIGMA)0.1ml及び0.2%BSA0.1mlを含む)を重層した。
【0028】
35℃のCO2インキュベーター内で2日間培養した後、B培地(イーグルMEM0.093g、ノーブルアガー0.1g、蒸留水9.54ml、7.5%NaHCO30.3ml、L−グルタミン0.1ml、100XMEM用ビタミン液(100倍濃度MEM培地用補助ビタミン液)0.01ml、0.2%BSA0.1ml及び1%ニュートラルレッド0.05mlを含む)を重層した。35℃のCO2インキュベーター内で1日間培養した後、プラーク数を計測した。
【0029】
<実施例1 ナガイモ抽出物の調製>
ナガイモ5本(5060g)の皮を剥ぎ、可食部4170gを得た。この可食部をフードカッターで擂り下ろし、9000rpmで45分間、遠心分離を行い、2780ml(2815g)の上清液(粗抽出液)を得た。上清液を凍結乾燥後、粉砕して乾燥粉末121.8gを得た。
【0030】
ナガイモ(生)、粗抽出液及び凍結乾燥物の成分分析結果を表1に示した。粗抽出液及び凍結乾燥物の抗インフルエンザウイルス活性を試験例1により調べた結果、良好に活性を保持していた。また、粗抽出液及び乾燥物の抗インフルエンザウイルス活性は、種々の飲食品の製造において抗インフルエンザウイルス組成物として使用できる強さを有していた。
【0031】
【表1】

【0032】
粗抽出液は、そのままでも抗インフルエンザウイルス組成物として使用できるが、超音波処理によって粘度を低下させることで、さらに広範囲な飲食品への適用が可能となる。粗抽出液の粘度は、30分間以上超音波処理(周波数40kHz)することで、抗インフルエンザウイルス活性の機能を維持したまま、水に近い粘度まで低下させることが可能であった。
図1は、超音波処理時間によるナガイモ粗抽出液粘度変化を示すグラフである。
【0033】
<実施例2 ナガイモ粗抽出液の抗ウイルス活性>
ナガイモ粗抽出液に含まれる抗インフルエンザウイルス活性をもつ成分の特性を、以下のように調べた。
(1)熱安定性
実施例1における粗抽出液を、25、40、50、60若しくは70℃で60分間の加熱、又は、100℃で5分間の加熱後、試験例1により抗インフルエンザウイルス活性を調べた。その結果、25、40、50若しくは60℃で60分間の加熱では活性を維持していたが、70℃で60分間若しくは100℃で5分間の加熱では活性を失っていた。したがって活性成分は、60℃以下で安定であることが示された。
【0034】
(2)保存安定性
ナガイモ粗抽出液を、室温、冷蔵又は冷凍の温度帯で1ヶ月、3ヶ月又は6ヶ月間保存した後で抗インフルエンザウイルス活性を調べた。その結果、いずれの温度帯及び保存期間においても活性が保持されていた。したがって、活性成分は、室温で少なくとも6ヶ月間は安定であることが示された。
【0035】
(3)pH安定性
塩酸溶液を用いてナガイモ粗抽出液(pH6.8)のpHを3.0に調整した場合、白濁して凝集体が生じた。この溶液をpH6.8に戻すと透明な液となったが、活性は消失した。この結果から、活性成分はpH3.0以下では不安定であることが示された。
【0036】
(4)有効接触時間
ナガイモ粗抽出液とインフルエンザウイルス液を等量混合後、35℃で1、5、10、15、30、45又は60分間接触した。その後は、試験例1に従いCPE抑制効果を調べた。その結果、全ての接触時間でCPE抑制効果を観察できた。したがって、インフルエンザウイルスとナガイモ粗抽出液を1分間程度接触することにより、ウイルスが細胞に感染するのを抑制できることが示された。
【0037】
<実施例3 ナガイモ粗抽出液のインフルエンザ予防効果>
試験例2(プラーク形成法)を用いて、インフルエンザウイルス感染の予防に必要なナガイモ粗抽出液の量を定量的に測定した。その結果、ナガイモ粗抽出液(タンパク質量として0.03mg)で20個のインフルエンザウイルスによる細胞感染を完全に阻害することができた。
【0038】
人の1回のくしゃみによる飛沫で他人の口に吸入されるウイルス数は、約10000個であることが推定されている。したがって、10000個のインフルエンザウイルスの細胞感染を予防するナガイモ粗抽出物の量は、タンパク質として15mg(10000個/20個*0.03mg)であると推定できる。前掲表1から、1mlのナガイモ粗抽出液は、固形分として約42mg、タンパク質として約20mgを含むことから、ナガイモ粗抽出液の1mlでインフルエンザウイルスによる感染を予防できる。
【0039】
<実施例4 インフルエンザ予防食品の試作>
実施例3の結果は、1mlのナガイモ粗抽出液(乾燥物として約42mg)がインフルエンザウイルスの感染を予防できることを示した。そこで、ナガイモ粗抽出液の乾燥物を含有する食品を試作し、その食品の抗インフルエンザウイルス活性を調べた。
【0040】
<4−1 錠剤>
錠剤を、1錠の重さを約200mgに設定し、その1/4の50mgが粗抽出液乾燥物になるように配合した。配合例は2種類試みた。表2、3にそれぞれ、配合例1、2を示す。なお、配合例2では、ナガイモ粗抽出液を乾燥する際に、粗抽出液に含まれる固形分と同量のトレハロースを添加してから凍結乾燥して得た乾燥物を用いた。
【0041】
【表2】

【0042】
【表3】

【0043】
試験例1に従い試作品の抗インフルエンザウイルス活性を調べた結果、配合例1の試作品は活性を示したが、配合例2では活性が認められなかった。配合例2では、使用したクエン酸の量が配合例1と比較して多いため、活性成分の安定pH領域以下になり、活性が消失したと考えられた。したがって、本発明飲食品の製造にあたっては、工程中のみならず最終製品のpHも考慮すべきことが示された。
【0044】
<4−2 錠菓>
錠菓(ラムネ菓子)を、1個あたり40mgの粗抽出液乾燥物を含むように試作した。なお、錠菓配合例3では、ナガイモ粗抽出液を乾燥する際に、粗抽出液に含まれる固形分と同量のトレハロースを添加してから凍結乾燥して得た乾燥物を用いた。表4に、錠菓の配合例(配合例3)を示す。
【0045】
【表4】

【0046】
試験例1に従い試作品の抗インフルエンザウイルス活性を調べた結果、錠菓の配合例3では活性が認められなかった。配合例では、使用したクエン酸の量が前記錠剤の配合例1と比較して多いため、活性成分の安定pH領域以下になり、活性が消失したと考えられた。したがって、本発明飲食品の製造にあたっては、工程中のみならず最終製品のpHも考慮すべきことが示された。
【0047】
<4−3 キャラメルゼリー>
キャラメルゼリーは、生クリーム200g、水飴100g、砂糖75g及びゼラチン50gを加熱・溶解した後、品温が60℃以下になったところでナガイモ粗抽出液60mlを添加・混合し、プレートに流して放冷し、固めた。冷却後、ゼリー1個あたりナガイモ粗抽出液を1ml含むよう60等分し、粉末オブラートをまぶして試作を完成した。
【0048】
抗インフルエンザウイルス活性を測定した結果、活性が認められた。なお、製造時の温度管理を充分に行い、工程中60℃以下を厳密に維持することによって、最終製品の抗インフルエンザウイルス活性を充分なものとできることが、示唆された。
【0049】
<実施例5 ナガイモの抗インフルエンザ機能物質の同定>
1300gのナガイモ(Dioscorea batatas)をミキサーでホモゲナイズした。ホモゲナイズしたナガイモを遠心分離(105000g、45分間)し、620mlの上清液を得た。この上清液を40ml程度に小分けにし、次の実験に使用するまで−40℃で保存した。凍結した上清液(40ml)を解凍後、トリス塩酸緩衝液(10mM、pH7.6)に対して充分に透析した。10mlの透析内液(約100mgのタンパク質を含む)をDEAEセルロースカラム(8ml)に供した。その後、0mM、50mM、100mM及び1MのNaClを含むトリス塩酸緩衝液で段階的に溶出した。
【0050】
図2は、実施例5のDEAEセルロースカラムクロマトグラムである。ここに示すように、DEAEセルロースカラムクロマトグラフィーによって、F1〜F4の画分を得た。試験例1に従って各画分の抗インフルエンザウイルス活性を測定した結果、F2画分に抗インフルエンザ活性が認められた。F2画分の還元条件下でのSDS−PAGEの結果、分子量33000に主要バンドが検出された。また同じく、非還元条件下でのSDS−PAGEでは、分子量30000に主要バンドが検出された。
【0051】
F2画分を集めて、トリス塩酸緩衝液(10mM、pH7.6)に透析後、DEAEセルロースカラム(8ml)に供した。非吸着成分を溶出後、0〜100mMのNaClによるグラジエント溶出を行った。
【0052】
図3は、F2画分のDEAEセルロースカラムクロマトグラムである。図示するように、F2−1画分に抗インフルエンザ活性が認められた。また、MALDI/TOF−MS(マトリックス支援レーザー脱離イオン化飛行時間型質量分析法)により活性物質の分子量は、27590と算定された。
なお図4は、F2−1画分他のMALDI/TOF−MS解析結果を示すグラフである。
【0053】
F2−1画分を集めて、N末端からの15アミノ酸配列を決定した結果、
Val,Glu,Asp、Glu,Phe,Ser,Tyr,Ile,Glu,Gly,Asn,Pro,Asn,Gly,Pro(VEDEF SYIEG NPNGP)であった。この配列は、既知のDioscorea batatas由来のDB2(Mariam Gaidamashvili et al.,Characterization of the yam tuber storage proteins from dioscorea batatas exhibiting unique lectin activities.,J.Biol.Chem.,279(25),26028−26035(2004))と一致した。DB2は、Dioscorin Aに分類される貯蔵タンパク質であり、総ナガイモタンパク質の約30%を占めていた。
【産業上の利用可能性】
【0054】
本発明の抗インフルエンザウイルス組成物等によれば、経口摂取によって、有効にインフルエンザ感染を予防できる。しかも安全性も問題がない。その上、製造容易でもあり、またインフルエンザ予防食品としての応用も広範に可能であり、産業上利用性が高い発明である。
【図面の簡単な説明】
【0055】
【図1】超音波処理時間によるナガイモ粗抽出液粘度変化を示すグラフである。
【図2】実施例5のDEAEセルロースカラムクロマトグラムである。
【図3】実施例5のF2画分のDEAEセルロースカラムクロマトグラムである。
【図4】実施例5のF2−1画分他のMALDI/TOF−MS解析結果を示すグラフである。
【特許請求の範囲】
【請求項1】
ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、経口摂取可能な抗インフルエンザウイルス組成物。
【請求項2】
前記ヤマノイモ属植物はナガイモであることを特徴とする、請求項1に記載の抗インフルエンザウイルス組成物。
【請求項3】
ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を含むことを特徴とする、抗インフルエンザウイルス組成物。
【請求項4】
ヤマノイモ属植物の地下茎または担根体を擂り下ろし、これを10000rpm以下1時間以下の遠心分離することにより上清液として得られる、経口摂取可能な抗インフルエンザウイルス組成物の製造方法。
【請求項5】
前記上清液の粘度を低下させるため、これを超音波処理することを特徴とする、請求項4に記載の抗インフルエンザウイルス組成物の製造方法。
【請求項6】
前記上清液の粘度を0.005Pa・s以下とすることを特徴とする、請求項5に記載の抗インフルエンザウイルス組成物の製造方法。
【請求項7】
前記上清液を乾燥処理して得られることを特徴とする、請求項4ないし6のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
【請求項8】
前記ヤマノイモ属植物はナガイモであることを特徴とする、請求項4ないし7のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
【請求項9】
ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、インフルエンザ予防食品。
【請求項10】
ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を有効成分として含有する、インフルエンザ予防食品。
【請求項11】
ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を原料として用いるインフルエンザ予防食品の製造方法であって、該抽出物が配合される以後の工程においては温度60℃以下かつpH3.0以上に維持されることを特徴とする、インフルエンザ予防食品の製造方法。
【請求項12】
前記ヤマノイモ属植物はナガイモであることを特徴とする、請求項11に記載のインフルエンザ予防食品の製造方法。
【請求項1】
ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、経口摂取可能な抗インフルエンザウイルス組成物。
【請求項2】
前記ヤマノイモ属植物はナガイモであることを特徴とする、請求項1に記載の抗インフルエンザウイルス組成物。
【請求項3】
ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を含むことを特徴とする、抗インフルエンザウイルス組成物。
【請求項4】
ヤマノイモ属植物の地下茎または担根体を擂り下ろし、これを10000rpm以下1時間以下の遠心分離することにより上清液として得られる、経口摂取可能な抗インフルエンザウイルス組成物の製造方法。
【請求項5】
前記上清液の粘度を低下させるため、これを超音波処理することを特徴とする、請求項4に記載の抗インフルエンザウイルス組成物の製造方法。
【請求項6】
前記上清液の粘度を0.005Pa・s以下とすることを特徴とする、請求項5に記載の抗インフルエンザウイルス組成物の製造方法。
【請求項7】
前記上清液を乾燥処理して得られることを特徴とする、請求項4ないし6のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
【請求項8】
前記ヤマノイモ属植物はナガイモであることを特徴とする、請求項4ないし7のいずれかに記載の抗インフルエンザウイルス組成物の製造方法。
【請求項9】
ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を有効成分として含有する、インフルエンザ予防食品。
【請求項10】
ヤマノイモ属植物の地下茎または担根体に由来する貯蔵タンパク質DB2を有効成分として含有する、インフルエンザ予防食品。
【請求項11】
ヤマノイモ属植物の地下茎もしくは担根体に含まれる成分、またはヤマノイモ属植物の地下茎もしくは担根体からの抽出物を原料として用いるインフルエンザ予防食品の製造方法であって、該抽出物が配合される以後の工程においては温度60℃以下かつpH3.0以上に維持されることを特徴とする、インフルエンザ予防食品の製造方法。
【請求項12】
前記ヤマノイモ属植物はナガイモであることを特徴とする、請求項11に記載のインフルエンザ予防食品の製造方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2010−132630(P2010−132630A)
【公開日】平成22年6月17日(2010.6.17)
【国際特許分類】
【出願番号】特願2009−55134(P2009−55134)
【出願日】平成21年3月9日(2009.3.9)
【出願人】(591005453)青森県 (52)
【出願人】(504229284)国立大学法人弘前大学 (162)
【Fターム(参考)】
【公開日】平成22年6月17日(2010.6.17)
【国際特許分類】
【出願日】平成21年3月9日(2009.3.9)
【出願人】(591005453)青森県 (52)
【出願人】(504229284)国立大学法人弘前大学 (162)
【Fターム(参考)】
[ Back to top ]

