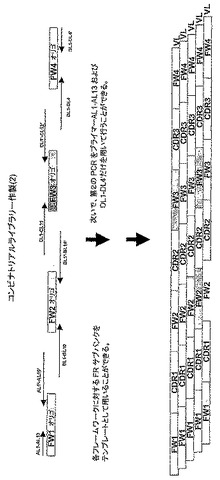
抗体のフレームワーク・シャッフル
【課題】 目的の抗原に対する抗体の免疫特異性だけでなく、目的の生物における抗体の免疫原性を容易にスクリーニングできる、迅速で手間のかからない抗体(定常領域を含むまたは含まない)のコンビナトリアルライブラリーを作製すること。
【解決手段】 本発明は、抗体を再設計または再構成して、抗原に対する抗体の免疫特異性を維持する一方、抗体の免疫原性を低下させる方法に関する。特に、本発明は、フレームワーク領域のサブバンク由来のフレームワーク領域とインフレームで融合されたドナー抗体由来の相補性決定領域(CDR)を含んでなるコンビナトリアルライブラリーを合成することにより、抗原に免疫特異的な抗体を作製する方法を提供する。
【解決手段】 本発明は、抗体を再設計または再構成して、抗原に対する抗体の免疫特異性を維持する一方、抗体の免疫原性を低下させる方法に関する。特に、本発明は、フレームワーク領域のサブバンク由来のフレームワーク領域とインフレームで融合されたドナー抗体由来の相補性決定領域(CDR)を含んでなるコンビナトリアルライブラリーを合成することにより、抗原に免疫特異的な抗体を作製する方法を提供する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
抗原と免疫特異的に結合するヒト化抗体を作製する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記第1のヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入し、かつドナー軽鎖可変領域、ヒト化軽鎖可変領域および改変された軽鎖可変領域からなる群より選択される軽鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された重鎖可変領域および軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項2】
抗原と免疫特異的に結合するヒト化抗体を作製する方法であって、
(a) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記ヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、および軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入し、かつドナー重鎖可変領域、ヒト化重鎖可変領域および改変された重鎖可変領域からなる群より選択される重鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された軽鎖可変領域および重鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、前記改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項3】
抗原と免疫特異的に結合するヒト化抗体を作製する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、および軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ
(c) ステップ(a)および(b)で作製した核酸配列を細胞中に導入するステップ;
(d) 改変された重鎖可変領域および改変された軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(e) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(f) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項4】
全ての6個のCDRがドナー抗体由来でありかつその改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項1〜3のいずれか1項に記載の方法。
【請求項5】
改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項1〜3のいずれか1項に記載の方法。
【請求項6】
改善された特性がTmであり、改善がドナー抗体と比較してTmの約5℃〜20℃の増加である、請求項1〜3のいずれか1項に記載の方法。
【請求項7】
改善された特性がpIであり、改善がドナー抗体と比較してpIの約0.5〜2.0の増加または約0.5〜2.0の減少である、請求項1〜3のいずれか1項に記載の方法。
【請求項8】
改善された特性が改善された産生レベルであり、改善がドナー抗体と比較して約25%〜500%である、請求項1〜3のいずれか1項に記載の方法。
【請求項9】
抗原と免疫特異的に結合するドナー抗体の1以上の特性を改善する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記ヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合する前記ドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入しかつドナー軽鎖可変領域、改変された軽鎖可変領域およびヒト化軽鎖可変領域からなる群より選択される軽鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された重鎖可変領域および軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項10】
抗原と免疫特異的に結合するドナー抗体の1以上の特性を改善する方法であって、
(a) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記第1のヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、および軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合する前記ドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入しかつドナー重鎖可変領域;改変された重鎖可変領域;およびヒト化重鎖可変領域からなる群より選択される重鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された軽鎖可変領域および重鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、前記改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項11】
抗原と免疫特異的に結合するドナー抗体の1以上の特性を改善する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合する前記ドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、およびa軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ
(c) ステップ(a)および(b)で作製した核酸配列を細胞中に導入するステップ;
(d) 改変された重鎖可変領域および改変された軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(e) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(f) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項12】
全ての6個のCDRがドナー抗体由来でありかつその改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項9〜11のいずれか1項に記載の方法。
【請求項13】
改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項9〜11のいずれか1項に記載の方法。
【請求項14】
改善された特性がTmであり、改善がドナー抗体と比較してTmの5℃〜20℃の増加である、請求項9〜11のいずれか1項に記載の方法。
【請求項15】
改善された特性がpIであり、改善がドナー抗体と比較してpIの約0.5〜2.0の増加または約0.5〜2.0の減少である、請求項9〜11のいずれか1項に記載の方法。
【請求項16】
改善された特性が改善された産生レベルであり、改善がドナー抗体と比較して約25%〜500%である、請求項9〜11のいずれか1項に記載の方法。
【請求項1】
抗原と免疫特異的に結合するヒト化抗体を作製する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記第1のヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入し、かつドナー軽鎖可変領域、ヒト化軽鎖可変領域および改変された軽鎖可変領域からなる群より選択される軽鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された重鎖可変領域および軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項2】
抗原と免疫特異的に結合するヒト化抗体を作製する方法であって、
(a) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記ヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、および軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入し、かつドナー重鎖可変領域、ヒト化重鎖可変領域および改変された重鎖可変領域からなる群より選択される重鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された軽鎖可変領域および重鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、前記改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項3】
抗原と免疫特異的に結合するヒト化抗体を作製する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、および軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ
(c) ステップ(a)および(b)で作製した核酸配列を細胞中に導入するステップ;
(d) 改変された重鎖可変領域および改変された軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(e) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(f) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項4】
全ての6個のCDRがドナー抗体由来でありかつその改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項1〜3のいずれか1項に記載の方法。
【請求項5】
改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項1〜3のいずれか1項に記載の方法。
【請求項6】
改善された特性がTmであり、改善がドナー抗体と比較してTmの約5℃〜20℃の増加である、請求項1〜3のいずれか1項に記載の方法。
【請求項7】
改善された特性がpIであり、改善がドナー抗体と比較してpIの約0.5〜2.0の増加または約0.5〜2.0の減少である、請求項1〜3のいずれか1項に記載の方法。
【請求項8】
改善された特性が改善された産生レベルであり、改善がドナー抗体と比較して約25%〜500%である、請求項1〜3のいずれか1項に記載の方法。
【請求項9】
抗原と免疫特異的に結合するドナー抗体の1以上の特性を改善する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記ヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合する前記ドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入しかつドナー軽鎖可変領域、改変された軽鎖可変領域およびヒト化軽鎖可変領域からなる群より選択される軽鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された重鎖可変領域および軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項10】
抗原と免疫特異的に結合するドナー抗体の1以上の特性を改善する方法であって、
(a) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む第1の核酸配列を合成するステップであって、前記第1のヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、および軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合する前記ドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 前記第1の核酸配列を細胞中に導入しかつドナー重鎖可変領域;改変された重鎖可変領域;およびヒト化重鎖可変領域からなる群より選択される重鎖可変領域をコードするヌクレオチド配列を含む第2の核酸配列を該細胞中に導入するステップ;
(c) 改変された軽鎖可変領域および重鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(d) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(e) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、前記改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項11】
抗原と免疫特異的に結合するドナー抗体の1以上の特性を改善する方法であって、
(a) 改変された重鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は重鎖フレームワーク領域1をコードする核酸配列、重鎖CDR1をコードする核酸配列、重鎖フレームワーク領域2をコードする核酸配列、重鎖CDR2をコードする核酸配列、重鎖フレームワーク領域3をコードする核酸配列、重鎖CDR3をコードする核酸配列、および重鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合する前記ドナー抗体重鎖可変領域由来でありかつ少なくとも1つの重鎖フレームワーク領域はヒト重鎖フレームワーク領域のサブバンク由来である前記ステップ;
(b) 改変された軽鎖可変領域をコードするヌクレオチド配列を含む核酸配列を合成するステップであって、前記ヌクレオチド配列は軽鎖フレームワーク領域1をコードする核酸配列、軽鎖CDR1をコードする核酸配列、軽鎖フレームワーク領域2をコードする核酸配列、軽鎖CDR2をコードする核酸配列、軽鎖フレームワーク領域3をコードする核酸配列、軽鎖CDR3をコードする核酸配列、およびa軽鎖フレームワーク領域4をコードする核酸配列を同時に融合することにより作製され、少なくとも1つのCDRは前記抗原と免疫特異的に結合するドナー抗体軽鎖可変領域由来でありかつ少なくとも1つの軽鎖フレームワーク領域はヒト軽鎖フレームワーク領域のサブバンク由来である前記ステップ
(c) ステップ(a)および(b)で作製した核酸配列を細胞中に導入するステップ;
(d) 改変された重鎖可変領域および改変された軽鎖可変領域をコードするヌクレオチド配列を発現させるステップ;
(e) 抗原と免疫特異的に結合する改変された抗体をスクリーニングするステップ;ならびに
(f) 平衡解離定数(KD)、安定性、融点(Tm)、pI、溶解度、産生レベルおよびエフェクター機能からなる群より選択される1以上の改善された特性を有する改変された抗体をスクリーニングするステップであって、改善がドナー抗体と比較して約1%〜500%であるかまたはドナー抗体と比較して2倍〜1000倍であるステップ
を含んでなる前記方法。
【請求項12】
全ての6個のCDRがドナー抗体由来でありかつその改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項9〜11のいずれか1項に記載の方法。
【請求項13】
改善された特性が抗原に対する抗体の平衡解離定数(KD)であり、改善がドナー抗体と比較して約50%〜500%である、請求項9〜11のいずれか1項に記載の方法。
【請求項14】
改善された特性がTmであり、改善がドナー抗体と比較してTmの5℃〜20℃の増加である、請求項9〜11のいずれか1項に記載の方法。
【請求項15】
改善された特性がpIであり、改善がドナー抗体と比較してpIの約0.5〜2.0の増加または約0.5〜2.0の減少である、請求項9〜11のいずれか1項に記載の方法。
【請求項16】
改善された特性が改善された産生レベルであり、改善がドナー抗体と比較して約25%〜500%である、請求項9〜11のいずれか1項に記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13A】


【図13B】


【図13C】


【図13D】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13A】


【図13B】


【図13C】


【図13D】


【公開番号】特開2013−13425(P2013−13425A)
【公開日】平成25年1月24日(2013.1.24)
【国際特許分類】
【出願番号】特願2012−236592(P2012−236592)
【出願日】平成24年10月26日(2012.10.26)
【分割の表示】特願2008−502101(P2008−502101)の分割
【原出願日】平成18年3月17日(2006.3.17)
【出願人】(504333972)メディミューン,エルエルシー (108)
【Fターム(参考)】
【公開日】平成25年1月24日(2013.1.24)
【国際特許分類】
【出願日】平成24年10月26日(2012.10.26)
【分割の表示】特願2008−502101(P2008−502101)の分割
【原出願日】平成18年3月17日(2006.3.17)
【出願人】(504333972)メディミューン,エルエルシー (108)
【Fターム(参考)】
[ Back to top ]

