抗Her2ヒトモノクローナル抗体
【課題】Her2に結合するヒト重鎖可変部抗体、及び該抗体を用いた測定法、並びに、該抗体を含有する医薬組成物もしくは試薬の提供を課題とする。
【解決手段】
Her2発現ヒト培養細胞に結合するヒト重鎖可変部抗体発現用ファージを選択するステップを複数回繰り返し行うことにより、Her2に対する結合活性を有するヒト重鎖可変部抗体を取得することに成功した。これにより、ヒト細胞、ヒト組織内のHer2と結合するヒト重鎖可変部抗体、および該抗体用いたHer2を検出するための組成物、Her2結合医薬組成物が提供された。
【解決手段】
Her2発現ヒト培養細胞に結合するヒト重鎖可変部抗体発現用ファージを選択するステップを複数回繰り返し行うことにより、Her2に対する結合活性を有するヒト重鎖可変部抗体を取得することに成功した。これにより、ヒト細胞、ヒト組織内のHer2と結合するヒト重鎖可変部抗体、および該抗体用いたHer2を検出するための組成物、Her2結合医薬組成物が提供された。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ヒトHer2に対するヒトモノクローナル抗体、及び該抗体を用いた測定法、並びに医薬組成物に関する。更に詳しくは、ヒト重鎖可変部抗体ファージライブラリーから、Her2に結合する新規な重鎖可変部抗体を選択し、それら選択した抗Her2重鎖可変部抗体を用いた免疫測定法ならびに医薬組成物に関する。
【背景技術】
【0002】
Her2は細胞膜蛋白質であり、その細胞外領域に結合する抗Her2抗体を体内に投与した際、Her2が関係するシグナル伝達などを阻害し、あるいはシグナル伝達などによる癌細胞増殖の阻害が期待できること(非特許文献1)等により乳癌など固形癌の治療効果が期待でき、また、Her2細胞外領域のポリペプチドの血中濃度が固形癌の増殖に従って増加すること(非特許文献3)等から血液を用いた診断、あるいはPETなど固形癌の診断といった病態の進行度評価法としても期待ができる。
【0003】
Her2細胞外ドメインIVに結合しHer2の生理活性を阻害するマウスモノクローナル抗体(エピトープ名:4D5)を基にして、非ヒト相補性決定領域(CDR)残基を残してヒトフレームワーク領域(FR)残基を導入することによりヒト化がなされ医薬品として開発された抗体(ハーセプチン;Trastuzumab)(非特許文献1、特許文献1)、Her2細胞外ドメインIに結合しHer2の生理活性を阻害するマウスモノクローナル抗体(エピトープ名:7C2/7F3)を基にして、そのCDR部分を残してヒト化がなされた抗体(特許文献2)などの記述がある。
【0004】
また、Her2細胞外ドメインIV(エピトープ名:4D5)に結合するエピトープ4D5を認識する低分子抗体としては、scFv(一本鎖Fv)とそのダイマー等の報告がある(非特許文献2)。ここで低分子抗体のなかで重鎖可変部抗体(VHドメイン抗体)は、免疫グロブリン(IgG)の分子量が約150 kDaであるのに対し、約25 kDaと分子量が小さいことから、1)大腸菌、酵母など微生物を宿主とする製造、2)宿主が微生物であることから原体製造コストの低減、3)細胞あるいは組織内浸透性の向上、4)製剤安定性の向上などが期待できる。
【0005】
低分子抗体である重鎖可変部抗体の取得では、ファージディスプレイ法と呼ばれる方法が、現在主に用いられている(非特許文献4、非特許文献5)。この方法では、大腸菌で重鎖可変部抗体を提示したファージを産生させ、目的の抗原に結合活性を有するファージを選択するものである。
【0006】
なお、本出願の発明に関連する先行技術文献情報を以下に示す。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特表2002-544238号公報
【特許文献2】特開2008-188013号公報
【非特許文献】
【0008】
【非特許文献1】Novel therapeutic strategies targeting the epidermal growth factor receptor (EGFR) family and its downstream effectors in breast cancer., G. Atalay, F. Cardoso, A. Awada & M. J. Piccart, Annals of Oncology, 2003; 14: 1346-1363.
【非特許文献2】PEGylation and multimerization of the anti-p185HER-2 singlechain Fv FRagment 4D5: Effects on tumor targeting., S. Kubetzko, E. Balic, R. Waibel, U. Zangemeister-Wittke, and A. Pluckthun, J Biol Chem. 2006 Nov 17;281(46):35186-201.
【非特許文献3】Potential clinical utility of serum HER-2/neu oncoprotein concentrations in patients with breast cancer., Carney WP, Neumann R, Lipton A, Leitzel K, Ali S, Price CP., Clin Chem. 2003 Oct;49(10):1579-98.
【非特許文献4】Selection of human antibody FRagments by phage display., Lee CM, Iorno N, Sierro F, Christ D., Nat Protoc. 2007;2(11):3001-8.
【非特許文献5】Sequence determinants of protein aggregation in human VH domains., Dudgeon K, Famm K, Christ D., Protein Eng Des Sel. 2009 Mar;22(3):217-20.
【発明の開示】
【発明が解決しようとする課題】
【0009】
本発明は、Her2を強制発現した動物細胞を抗原として用い、ヒト重鎖可変部抗体ファージライブラリーから、セルパニング(Cell panning)法によって、Her2に対する機能性抗体を選択し、該抗体を用いた測定法、並びに、該抗体を含有する医薬組成物もしくは試薬の提供を課題とする。
【課題を解決するための手段】
【0010】
ヒト重鎖可変部抗体ファージライブラリーから、Her2高発現細胞に対するセルパニング法を用いて、陽性クローンを取得することができた。取得した陽性クローンは免疫染色によりHer2に対する結合能が確認された。また、塩基配列解析により、取得した重鎖可変部抗体クローンの全塩基配列を決定し、その情報を基に全アミノ酸配列を決定した。
【0011】
即ち本発明は、Her2に対するヒトモノクローナル抗体、および該抗体を用いた測定法、並びに、該抗体を含有する医薬組成物もしくは試薬に関し、より具体的には、
〔1〕重鎖CDR1のアミノ酸配列としてFSLNAQDMA(配列番号:1)、重鎖CDR2のアミノ酸配列としてAINNTG(配列番号:2)、重鎖CDR3のアミノ酸配列としてANSTRRNAKLGY(配列番号:3)を有するヒトHer2に結合するヒト重鎖可変部抗体(VHドメイン抗体)、
〔2〕〔1〕に記載された重鎖CDR1〜3のそれぞれのアミノ酸配列において、1もしくは2個のアミノ酸が置換、欠失、付加されたアミノ酸配列をそれぞれ重鎖CDR1〜3とするHer2に結合するヒト重鎖可変部抗体、
〔3〕〔1〕〜〔2〕のいずれかに記載の抗体が、フレームワーク領域(FR)がヒト由来の配列であることを特徴とする、Her2に結合するヒト重鎖可変部抗体、
〔4〕配列番号:4に記載されたヒト重鎖可変部抗体のアミノ酸配列における重鎖CDR1〜3を有することを特徴とするHer2に結合するヒト重鎖可変部抗体、
〔5〕〔1〕〜〔4〕のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2検出用試薬、
〔6〕〔1〕〜〔4〕のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2結合医薬組成物を、提供する。
【発明の効果】
【0012】
発明者等はヒト重鎖可変部抗体遺伝子ライブラリーからファージディスプレイ法によるセルパニングによって、新規なヒト重鎖可変部抗体クローンを得た。
【0013】
これにより、Her2に結合する抗体を用いたHer2を検出するための組成物の作製が可能である。また、該組成物、及び方法を用いてHer2を検出する方法あるいは各種疾患を診断する方法、及び測定キットを供給できることができる。
【図面の簡単な説明】
【0014】
【図1】Her2動物細胞発現用ベクターpIRES2-EGFPの構成を示す。Her2遺伝子動物細胞用発現ベクター。SV40oriなど動物細胞用複製開始点配列、CMV由来プロモーター、SV40由来polyA付加配列、及び選択マーカーとしてKan/Neoを含む動物細胞用発現ベクター。このベクターには、更に、pUC由来複製開始点配列、選択マーカーとして前述したKan/Neo等を含み、大腸菌で増幅可能なシャトルベクターとなっている。このベクターは動物細胞で蛍光タンパク質マーカー(FP)を発現させる目的で、IRES(mRNA内部のリボソーム進入サイト)配列と連結した蛍光タンパク質マーカー(FP:AcGFP1)遺伝子が挿入されている。
【図2】ヒト重鎖可変部抗体発現ファージ(クローン番号220-14)によるHer2結合活性を示す細胞染色の顕微鏡写真を示す。pIRES2-EGFPでHEK293細胞をトランスフェクトして作製したHer2強制発現細胞を評価対象とし、クローン番号220-14のヒト重鎖可変部抗体発現用ファージによる細胞染色による抗体結合力の評価を行った。上段の顕微鏡写真は、Her2/EGFP強制発現細胞、下段は陰性コントロールとして用いた神経栄養因子受容体p75/EGFP強制発現細胞の顕微鏡写真である。左から一番目は、選択したファージ(クローン番号220-14)を用いたHer2染色結果、左から二番目は、トランスフェクションしたベクター由来EGFPの蛍光発色結果、左から三番目は、DNA結合蛍光色素Hoechst33342による細胞核の染色結果、左から四番目は、左の3つの画像を重ね合わせた顕微鏡写真を示す。これらの顕微鏡写真から、選択したファージ(クローン番号220-14)は、Her2発現細胞膜特異的に結合していることが示される。棒は顕微鏡写真に於ける80μmの長さを示す。
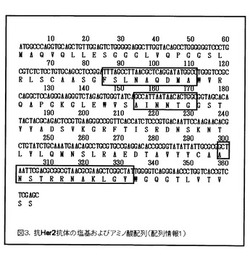
【図3】抗Her2ヒト重鎖可変部抗体(クローン番号220-14)の塩基配列とアミノ酸配列を示す。四角い枠で囲んだアミノ酸配列は、上から順番に重鎖CDR1、重鎖CDR2、重鎖CDR3の場所とそのアミノ酸配列を示す。
【発明を実施するための形態】
【0015】
本発明は、Her2に対する結合活性を有する抗Her2ヒト重鎖可変部抗体(VH ドメイン抗体)を提供する。本発明の抗体は、単離されたヒト重鎖可変部抗体もしくは精製されたヒト重鎖可変部抗体であることが好ましい。
【0016】
Her2(別名:ErbB2、UniProt ACCESSION番号:P04626)とは、全長1,225アミノ酸からなる分子量約185kDaの細胞膜貫通糖蛋白質、その細胞外領域は約630アミノ酸からなり、そのHer2細胞外領域のN-末端から順番にドメインI、II、III、IVが認められる(特許文献1、2)。Her2に対する抗体は、Her2を介するシグナル伝達を変化させることが期待される。
【0017】
本発明における「ヒト重鎖可変部抗体」とは、例えば、重鎖可変ドメイン(VH)の配列中に存在する相補性決定領域(CDR)である重鎖CDR1、重鎖CDR2および重鎖CDR3の各々のアミノ酸配列(例えば、配列番号:1〜3に示される配列)を含む抗体が挙げられる。また、本発明のヒト重鎖可変部抗体には、アミノ酸配列が改変された抗体、他の分子(例えば、ポリエチレングリコールなどの高分子等)が結合した修飾抗体、糖鎖が改変されたヒト重鎖可変部抗体などが含まれる。
【0018】
本発明の抗体にはHer2との結合性に影響を与えない範囲で、上記重鎖CDRが適宜改変された抗体が含まれる。例えば、重鎖CDR1〜3のそれぞれのアミノ酸配列において、1もしくは2個のアミノ酸が置換、欠失、付加されたアミノ酸配列をそれぞれ重鎖CDR1〜3とするHer2に結合するヒト重鎖可変部抗体が挙げられる。これらの改変された重鎖CDRを有する抗体は、上記に記載された改変される前のヒト重鎖可変部抗体と同等のHer2に対する結合活性を有する限り、本発明のヒト重鎖可変部抗体に含まれる。
【0019】
ここで「同等の活性」とは、対象となる抗体が本発明の抗体と同様の生物学的あるいは生化学的活性を有することを指す。該「活性」とは具体的には、ヒトなど動物細胞において発現しているHer2と結合する活性を指す。
【0020】
なお本発明において「同等」とは、必ずしも同程度の活性である必要はなく、活性が増強されていてもよいし、又、活性を有する限り活性が減少していてもよい。
【0021】
あるポリペプチドと同等の活性を有するポリペプチドを調製するための、当業者によく知られた方法としては、ポリペプチドに変異を導入する方法等が挙げられる。例えば、当業者であれば、部位特異的変異誘発法などを用いて、本発明の抗体(例えば、重鎖CDR領域)に適宜変異を導入することにより、該抗体と同等の活性を有する抗体を調製することができる。また、アミノ酸の変異は自然界においても生じうる。このように、本発明の抗体のアミノ酸配列において1もしくは2個のアミノ酸が変異したアミノ酸配列を有し、該抗体と同等の活性を有する抗体もまた本発明のヒト重鎖可変部抗体に含まれる。
【0022】
例えば本発明の上記重鎖CDR配列、すなわち重鎖CDR1(配列番号:1)、重鎖CDR2(配列番号:2)及びCDR3(配列番号:3)とのアミノ酸配列に対して通常は75%以上(例えば、77.8%や83.3%以上)、好ましくは90%以上(例えば、91.7%以上)の相同性(同一性)がある抗体または抗体断片は、本発明の抗体に含まれる。
【0023】
変異するアミノ酸残基においては、アミノ酸側鎖の性質が保存されている別のアミノ酸に変異されることが望ましい。例えばアミノ酸側鎖の性質としては、疎水性アミノ酸(A、I、L、M、F、P、W、V)、構造内に2つのカルボキシル基を持つアミノ酸(D、E)、構造内に2つ以上のアミノ基を持つアミノ酸塩基含有側鎖を有するアミノ離(R、K、H)、芳香族含有側鎖を有するアミノ酸(H、F、Y、W)を挙げることができる(括弧内はいずれもアミノ酸の一文字表記を表す)。
【0024】
上述の修飾に加え、本発明の抗体は、活性を保持している限り、他の物質にさらに連結されていてもよい。他の物質としては、例えばペプチド、脂質、糖および糖鎖、アセチル基、天然および合成のポリマー等が挙げられる。これらの修飾は、付加的な機能を付与するか、または抗体を安定化するために実施され得る。
【0025】
また本発明のヒト重鎖可変部抗体には、単鎖可変領域抗体断片(VH)の全長配列(重鎖可変ドメインの全長配列)に含まれる重鎖CDRによって特定されるHer2に結合するヒト重鎖可変部抗体を好適に示すことができる。
【0026】
例えば、以下に記載のHer2に結合するヒト重鎖可変部抗体が挙げられる;
配列番号:4に記載された単鎖可変領域抗体断片のアミノ酸配列における重鎖CDR1〜3を有することを特徴とするHer2に結合するヒト重鎖可変部抗体。
【0027】
また、本発明の抗体が結合するエピトープと結合するヒト重鎖可変部抗体は、当業者に公知の方法により取得することが可能である。公知の方法としては、例えば、本発明の抗体が結合するエピトープを通常の方法により決定し、該エピトープに含まれるアミノ酸配列を有するポリペプチドを免疫原としてヒト重鎖可変部抗体を作製する方法等が挙げられる。
【0028】
本発明の抗体には、上述のヒト重鎖可変部抗体、アミノ酸配列が改変された抗体、非ヒト動物キメラ抗体、他の分子(例えば、ポリエチレングリコールなどの高分子等)が結合した修飾抗体、糖鎖が改変された抗体等が含まれる。
【0029】
本発明における抗体の好ましい態様の一つとして、3つの重鎖CDR(重鎖CDR1〜重鎖CDR3)を取り囲む4つのフレームワーク領域、すなわちFR (重鎖FR1〜重鎖FR4)を他のヒト重鎖遺伝子由来のアミノ酸配列を適用した変異ヒト抗体等の改変抗体を挙げることができる。
【0030】
また、ヒト重鎖可変部のCDR(重鎖CDR1〜重鎖CDR3)がHer2に特異的に結合するヒト由来のアミノ酸配列からなり、3つのCDR(重鎖CDR1〜重鎖CDR3)を取り囲む4つの非ヒト動物由来の重鎖FRであることを特徴とするキメラ抗体等を挙げることができる。なおこれらの改変抗体は、既知の方法を用いて製造することができる。
【0031】
ヒト抗体はヒト体内における抗原性が低いと考えられ、治療目的などでヒトに投与する場合に有用である。非ヒト動物とヒトとのキメラ抗体は、抗体の安定性等について良い性質を付与できれば、体外診断などHer2の濃度測定に使用する場合に有用である。
【0032】
なお、キメラ抗体を作製した後に、アミノ酸を他のアミノ酸で置換、欠失、付加および/または挿入等してもよい。本発明のヒト重鎖可変部抗体には、そのようなアミノ酸置換等されたヒト重鎖可変部抗体も含まれる。
【0033】
なお、本発明の抗体の抗原(Her2)への結合活性は、例えばドットブロッティング法、ウエスタンブロッティング法、酵素結合免疫吸着アッセイ法(ELISA)、酵素免疫アッセイ法(EIA)、放射免疫アッセイ法(RIA)、免疫沈降法、表面プラズモン共鳴を利用した分子間の相互作用測定法、フローサイトメトリー、あるいは細胞染色法を用いて行うことができる。
【0034】
なお、これらの測定・検出方法に関する一般的な技術手段の詳細については、総説、成書などを参照することができる。例えば、各種抗体を用いた操作は、「Methods in ENZYMOLOGY」Vol. 70(Immunochemical Techniques(Part A))、同書Vol. 73(Immunochemical Techniques(PartB))、同書Vol. 74(Immunochemical Techniques(Part C))、同書Vol. 84(Immunochemical Techniques(Part D:Selected Immunoassays))、同書Vol. 92(Immunochemical Techniques(Part E:Monoclonal Antibodies and General Immunoassay Methods))、同書Vol. 121(Immunochemical Techniques(Part I:HybridomaTechnology and Monoclonal Antibodies))(以上、アカデミックプレス社発行)などを参照することができる。
【0035】
本発明におけるヒト重鎖可変部抗体は、IgGなど全長抗体(whole antibody)のうち、ヒト重鎖可変部抗体部分以外が欠損している抗体であり、ヒト等動物細胞で発現しているHer2への結合活性を有する限り特に限定されない。
【0036】
本発明におけるヒト重鎖可変部抗体単体が集合し多量体(ダイマー、トリマー、テトラマーなど)が自然にあるいは人為的に形成せしめることももあり得ることから、それら多量体もヒト重鎖可変部抗体に含まれる。
【0037】
ヒト重鎖可変部抗体に含まれる重鎖可変領域(重鎖CDR)のアミノ酸配列は、抗原結合活性(Her2との結合活性)を有する限り、1もしくは2個のアミノ酸の置換、欠失、付加及び/又は挿入されていてもよい。
【0038】
ヒト重鎖可変部抗体ファージからHer2に結合するヒト重鎖可変部抗体をコードする遺伝子を単離し、単利した該遺伝子を用いて、Her2に結合するヒト重鎖可変部抗体を大腸菌、あるいは動物細胞等を宿主とした組換え細胞で所望のヒト重鎖可変部抗体合成する行程を含む。
【0039】
さらに本発明は、本発明の抗体または抗体断片を有効成分として含むHer2検出用試薬(検査薬)を提供する。
【0040】
上記試薬を構成成分として含む検査・測定キットもまた、本発明に含まれる。
【0041】
また、本発明のヒト重鎖可変部抗体を含有するHer2を検出するための組成物を提供する。該組成物、または上記試薬を用いてHer2を検出する方法、および、各種疾患を診断する方法もまた、本発明に含まれる。
【0042】
なお本明細書において引用された全ての先行技術文献は、参照として本明細書に組み入れられる。
【実施例】
【0043】
以下に、実施例により本発明をさらに具体的に説明するが、本発明はそれに限定されるものではない。なお、実施例における各種遺伝子操作は、Molecular cloning third.ed.(Cold Spring Harbor Lab.Press,2001)に記載されている方法に従った。
【0044】
(1)Her2を発現するヒト培養細胞の構築
ヒト培養細胞(HEK293株:Human Embryo Kidney Cell)を宿主としてHer2を発現することを目的とし、Her2の全長遺伝子を図1示す培養細胞発現用ベクターpIRES2-EGFPのマルチクローニングサイトにSalI切断部位及びNruI/samI切断部位を用いて挿入し、Her2全長発現ベクターを作製した(図1)。HEK293細胞へのトランスフェクションにはLipofectamin (Invitrogen社製)とplus reagent (Invitrogen社製))を用いてInvitrogen社が示す方法に従って行った。
【0045】
(2)セルパニング法による陽性ファージの濃縮と陽性クローン単離
コントロール用細胞(非特異的ファージ吸着用細胞:HEK293株そのもの)および、Her2抗原発現細胞をそれぞれ1×107cells/mLになるようにPBSで希釈した。まずコントロール用細胞に1×1011 pfuの市販のヒト重鎖可変部抗体ファージライブラリー(ダナフォーム社;ドメイン抗体ファージミドライブラリー)を加え、4℃でインキュベートした。この操作によって予めHEK293細胞表面に結合するファージ群が取り除くことができる。30分のインキュベーの後、上清のファージ液を回収した。次に、回収したファージ液をHer2抗原発現細胞に加え、4℃で30分間インキュベートした。30分間インキュベートした後、該細胞を1 mLのPBSで3回洗浄し、1 mLの100 mM Glycine-HCl(pH2.0), 500 mM NaCl溶液を使用し室温で酸溶出処理をした。酸溶出処理5分後、上清のファージ液を回収した。回収したファージ液は、2 MのTris緩衝液 20μLを加えて直ちに中和した。回収したファージ液は、大腸菌TG1と混合し感染させ(37℃、30分)、100μg/mL アンピシリン、4%グルコースを含むLB寒天培地(10 cm2 X 15枚)に播種し、37℃で一晩培養した。なお、感染した大腸菌からのファージレスキュー操作は、市販キットの標準方法に従った。以上に記載したセルパニング法を3ラウンド行い、陽性ファージを単離出来るレベルまで濃縮操作を繰り返した。
【0046】
(3)細胞染色評価による陽性ファージの選択
3ラウンドの選択後、市販キットの標準方法に従って、48の単一クローンのファージを各々調製し、それら単一クローンのファージを用いた細胞染色による評価を実施した。その結果、220-14クローンがHer2特異的に結合することが確認された。(図2)
【0047】
(4)220-14クローンの塩基配列解析
細胞染色で陽性であった220-14クローンからファージミドを単離し、公知の方法により塩基配列解析を実施した。また、得られたヒト重鎖可変部抗体(VH ドメイン抗体)の塩基配列を配列番号:5に、また、該ヒト重鎖可変部抗体のアミノ酸配列を配列番号:4に示した。220-14クローンの塩基配列とアミノ酸配列を併記して図3に示した。図3に於いて、四角枠内の配列は重鎖CDR1、重鎖CDR2、重鎖CDR3であることを示す。重鎖CDR1、重鎖CDR2、重鎖CDR3のアミノ酸配列は、それぞれ、FSLNAQDMA(配列番号:1)、AINNTG(配列番号:2)、ANSTRRNAKLGY(配列番号:3)であった。
【技術分野】
【0001】
本発明は、ヒトHer2に対するヒトモノクローナル抗体、及び該抗体を用いた測定法、並びに医薬組成物に関する。更に詳しくは、ヒト重鎖可変部抗体ファージライブラリーから、Her2に結合する新規な重鎖可変部抗体を選択し、それら選択した抗Her2重鎖可変部抗体を用いた免疫測定法ならびに医薬組成物に関する。
【背景技術】
【0002】
Her2は細胞膜蛋白質であり、その細胞外領域に結合する抗Her2抗体を体内に投与した際、Her2が関係するシグナル伝達などを阻害し、あるいはシグナル伝達などによる癌細胞増殖の阻害が期待できること(非特許文献1)等により乳癌など固形癌の治療効果が期待でき、また、Her2細胞外領域のポリペプチドの血中濃度が固形癌の増殖に従って増加すること(非特許文献3)等から血液を用いた診断、あるいはPETなど固形癌の診断といった病態の進行度評価法としても期待ができる。
【0003】
Her2細胞外ドメインIVに結合しHer2の生理活性を阻害するマウスモノクローナル抗体(エピトープ名:4D5)を基にして、非ヒト相補性決定領域(CDR)残基を残してヒトフレームワーク領域(FR)残基を導入することによりヒト化がなされ医薬品として開発された抗体(ハーセプチン;Trastuzumab)(非特許文献1、特許文献1)、Her2細胞外ドメインIに結合しHer2の生理活性を阻害するマウスモノクローナル抗体(エピトープ名:7C2/7F3)を基にして、そのCDR部分を残してヒト化がなされた抗体(特許文献2)などの記述がある。
【0004】
また、Her2細胞外ドメインIV(エピトープ名:4D5)に結合するエピトープ4D5を認識する低分子抗体としては、scFv(一本鎖Fv)とそのダイマー等の報告がある(非特許文献2)。ここで低分子抗体のなかで重鎖可変部抗体(VHドメイン抗体)は、免疫グロブリン(IgG)の分子量が約150 kDaであるのに対し、約25 kDaと分子量が小さいことから、1)大腸菌、酵母など微生物を宿主とする製造、2)宿主が微生物であることから原体製造コストの低減、3)細胞あるいは組織内浸透性の向上、4)製剤安定性の向上などが期待できる。
【0005】
低分子抗体である重鎖可変部抗体の取得では、ファージディスプレイ法と呼ばれる方法が、現在主に用いられている(非特許文献4、非特許文献5)。この方法では、大腸菌で重鎖可変部抗体を提示したファージを産生させ、目的の抗原に結合活性を有するファージを選択するものである。
【0006】
なお、本出願の発明に関連する先行技術文献情報を以下に示す。
【先行技術文献】
【特許文献】
【0007】
【特許文献1】特表2002-544238号公報
【特許文献2】特開2008-188013号公報
【非特許文献】
【0008】
【非特許文献1】Novel therapeutic strategies targeting the epidermal growth factor receptor (EGFR) family and its downstream effectors in breast cancer., G. Atalay, F. Cardoso, A. Awada & M. J. Piccart, Annals of Oncology, 2003; 14: 1346-1363.
【非特許文献2】PEGylation and multimerization of the anti-p185HER-2 singlechain Fv FRagment 4D5: Effects on tumor targeting., S. Kubetzko, E. Balic, R. Waibel, U. Zangemeister-Wittke, and A. Pluckthun, J Biol Chem. 2006 Nov 17;281(46):35186-201.
【非特許文献3】Potential clinical utility of serum HER-2/neu oncoprotein concentrations in patients with breast cancer., Carney WP, Neumann R, Lipton A, Leitzel K, Ali S, Price CP., Clin Chem. 2003 Oct;49(10):1579-98.
【非特許文献4】Selection of human antibody FRagments by phage display., Lee CM, Iorno N, Sierro F, Christ D., Nat Protoc. 2007;2(11):3001-8.
【非特許文献5】Sequence determinants of protein aggregation in human VH domains., Dudgeon K, Famm K, Christ D., Protein Eng Des Sel. 2009 Mar;22(3):217-20.
【発明の開示】
【発明が解決しようとする課題】
【0009】
本発明は、Her2を強制発現した動物細胞を抗原として用い、ヒト重鎖可変部抗体ファージライブラリーから、セルパニング(Cell panning)法によって、Her2に対する機能性抗体を選択し、該抗体を用いた測定法、並びに、該抗体を含有する医薬組成物もしくは試薬の提供を課題とする。
【課題を解決するための手段】
【0010】
ヒト重鎖可変部抗体ファージライブラリーから、Her2高発現細胞に対するセルパニング法を用いて、陽性クローンを取得することができた。取得した陽性クローンは免疫染色によりHer2に対する結合能が確認された。また、塩基配列解析により、取得した重鎖可変部抗体クローンの全塩基配列を決定し、その情報を基に全アミノ酸配列を決定した。
【0011】
即ち本発明は、Her2に対するヒトモノクローナル抗体、および該抗体を用いた測定法、並びに、該抗体を含有する医薬組成物もしくは試薬に関し、より具体的には、
〔1〕重鎖CDR1のアミノ酸配列としてFSLNAQDMA(配列番号:1)、重鎖CDR2のアミノ酸配列としてAINNTG(配列番号:2)、重鎖CDR3のアミノ酸配列としてANSTRRNAKLGY(配列番号:3)を有するヒトHer2に結合するヒト重鎖可変部抗体(VHドメイン抗体)、
〔2〕〔1〕に記載された重鎖CDR1〜3のそれぞれのアミノ酸配列において、1もしくは2個のアミノ酸が置換、欠失、付加されたアミノ酸配列をそれぞれ重鎖CDR1〜3とするHer2に結合するヒト重鎖可変部抗体、
〔3〕〔1〕〜〔2〕のいずれかに記載の抗体が、フレームワーク領域(FR)がヒト由来の配列であることを特徴とする、Her2に結合するヒト重鎖可変部抗体、
〔4〕配列番号:4に記載されたヒト重鎖可変部抗体のアミノ酸配列における重鎖CDR1〜3を有することを特徴とするHer2に結合するヒト重鎖可変部抗体、
〔5〕〔1〕〜〔4〕のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2検出用試薬、
〔6〕〔1〕〜〔4〕のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2結合医薬組成物を、提供する。
【発明の効果】
【0012】
発明者等はヒト重鎖可変部抗体遺伝子ライブラリーからファージディスプレイ法によるセルパニングによって、新規なヒト重鎖可変部抗体クローンを得た。
【0013】
これにより、Her2に結合する抗体を用いたHer2を検出するための組成物の作製が可能である。また、該組成物、及び方法を用いてHer2を検出する方法あるいは各種疾患を診断する方法、及び測定キットを供給できることができる。
【図面の簡単な説明】
【0014】
【図1】Her2動物細胞発現用ベクターpIRES2-EGFPの構成を示す。Her2遺伝子動物細胞用発現ベクター。SV40oriなど動物細胞用複製開始点配列、CMV由来プロモーター、SV40由来polyA付加配列、及び選択マーカーとしてKan/Neoを含む動物細胞用発現ベクター。このベクターには、更に、pUC由来複製開始点配列、選択マーカーとして前述したKan/Neo等を含み、大腸菌で増幅可能なシャトルベクターとなっている。このベクターは動物細胞で蛍光タンパク質マーカー(FP)を発現させる目的で、IRES(mRNA内部のリボソーム進入サイト)配列と連結した蛍光タンパク質マーカー(FP:AcGFP1)遺伝子が挿入されている。
【図2】ヒト重鎖可変部抗体発現ファージ(クローン番号220-14)によるHer2結合活性を示す細胞染色の顕微鏡写真を示す。pIRES2-EGFPでHEK293細胞をトランスフェクトして作製したHer2強制発現細胞を評価対象とし、クローン番号220-14のヒト重鎖可変部抗体発現用ファージによる細胞染色による抗体結合力の評価を行った。上段の顕微鏡写真は、Her2/EGFP強制発現細胞、下段は陰性コントロールとして用いた神経栄養因子受容体p75/EGFP強制発現細胞の顕微鏡写真である。左から一番目は、選択したファージ(クローン番号220-14)を用いたHer2染色結果、左から二番目は、トランスフェクションしたベクター由来EGFPの蛍光発色結果、左から三番目は、DNA結合蛍光色素Hoechst33342による細胞核の染色結果、左から四番目は、左の3つの画像を重ね合わせた顕微鏡写真を示す。これらの顕微鏡写真から、選択したファージ(クローン番号220-14)は、Her2発現細胞膜特異的に結合していることが示される。棒は顕微鏡写真に於ける80μmの長さを示す。
【図3】抗Her2ヒト重鎖可変部抗体(クローン番号220-14)の塩基配列とアミノ酸配列を示す。四角い枠で囲んだアミノ酸配列は、上から順番に重鎖CDR1、重鎖CDR2、重鎖CDR3の場所とそのアミノ酸配列を示す。
【発明を実施するための形態】
【0015】
本発明は、Her2に対する結合活性を有する抗Her2ヒト重鎖可変部抗体(VH ドメイン抗体)を提供する。本発明の抗体は、単離されたヒト重鎖可変部抗体もしくは精製されたヒト重鎖可変部抗体であることが好ましい。
【0016】
Her2(別名:ErbB2、UniProt ACCESSION番号:P04626)とは、全長1,225アミノ酸からなる分子量約185kDaの細胞膜貫通糖蛋白質、その細胞外領域は約630アミノ酸からなり、そのHer2細胞外領域のN-末端から順番にドメインI、II、III、IVが認められる(特許文献1、2)。Her2に対する抗体は、Her2を介するシグナル伝達を変化させることが期待される。
【0017】
本発明における「ヒト重鎖可変部抗体」とは、例えば、重鎖可変ドメイン(VH)の配列中に存在する相補性決定領域(CDR)である重鎖CDR1、重鎖CDR2および重鎖CDR3の各々のアミノ酸配列(例えば、配列番号:1〜3に示される配列)を含む抗体が挙げられる。また、本発明のヒト重鎖可変部抗体には、アミノ酸配列が改変された抗体、他の分子(例えば、ポリエチレングリコールなどの高分子等)が結合した修飾抗体、糖鎖が改変されたヒト重鎖可変部抗体などが含まれる。
【0018】
本発明の抗体にはHer2との結合性に影響を与えない範囲で、上記重鎖CDRが適宜改変された抗体が含まれる。例えば、重鎖CDR1〜3のそれぞれのアミノ酸配列において、1もしくは2個のアミノ酸が置換、欠失、付加されたアミノ酸配列をそれぞれ重鎖CDR1〜3とするHer2に結合するヒト重鎖可変部抗体が挙げられる。これらの改変された重鎖CDRを有する抗体は、上記に記載された改変される前のヒト重鎖可変部抗体と同等のHer2に対する結合活性を有する限り、本発明のヒト重鎖可変部抗体に含まれる。
【0019】
ここで「同等の活性」とは、対象となる抗体が本発明の抗体と同様の生物学的あるいは生化学的活性を有することを指す。該「活性」とは具体的には、ヒトなど動物細胞において発現しているHer2と結合する活性を指す。
【0020】
なお本発明において「同等」とは、必ずしも同程度の活性である必要はなく、活性が増強されていてもよいし、又、活性を有する限り活性が減少していてもよい。
【0021】
あるポリペプチドと同等の活性を有するポリペプチドを調製するための、当業者によく知られた方法としては、ポリペプチドに変異を導入する方法等が挙げられる。例えば、当業者であれば、部位特異的変異誘発法などを用いて、本発明の抗体(例えば、重鎖CDR領域)に適宜変異を導入することにより、該抗体と同等の活性を有する抗体を調製することができる。また、アミノ酸の変異は自然界においても生じうる。このように、本発明の抗体のアミノ酸配列において1もしくは2個のアミノ酸が変異したアミノ酸配列を有し、該抗体と同等の活性を有する抗体もまた本発明のヒト重鎖可変部抗体に含まれる。
【0022】
例えば本発明の上記重鎖CDR配列、すなわち重鎖CDR1(配列番号:1)、重鎖CDR2(配列番号:2)及びCDR3(配列番号:3)とのアミノ酸配列に対して通常は75%以上(例えば、77.8%や83.3%以上)、好ましくは90%以上(例えば、91.7%以上)の相同性(同一性)がある抗体または抗体断片は、本発明の抗体に含まれる。
【0023】
変異するアミノ酸残基においては、アミノ酸側鎖の性質が保存されている別のアミノ酸に変異されることが望ましい。例えばアミノ酸側鎖の性質としては、疎水性アミノ酸(A、I、L、M、F、P、W、V)、構造内に2つのカルボキシル基を持つアミノ酸(D、E)、構造内に2つ以上のアミノ基を持つアミノ酸塩基含有側鎖を有するアミノ離(R、K、H)、芳香族含有側鎖を有するアミノ酸(H、F、Y、W)を挙げることができる(括弧内はいずれもアミノ酸の一文字表記を表す)。
【0024】
上述の修飾に加え、本発明の抗体は、活性を保持している限り、他の物質にさらに連結されていてもよい。他の物質としては、例えばペプチド、脂質、糖および糖鎖、アセチル基、天然および合成のポリマー等が挙げられる。これらの修飾は、付加的な機能を付与するか、または抗体を安定化するために実施され得る。
【0025】
また本発明のヒト重鎖可変部抗体には、単鎖可変領域抗体断片(VH)の全長配列(重鎖可変ドメインの全長配列)に含まれる重鎖CDRによって特定されるHer2に結合するヒト重鎖可変部抗体を好適に示すことができる。
【0026】
例えば、以下に記載のHer2に結合するヒト重鎖可変部抗体が挙げられる;
配列番号:4に記載された単鎖可変領域抗体断片のアミノ酸配列における重鎖CDR1〜3を有することを特徴とするHer2に結合するヒト重鎖可変部抗体。
【0027】
また、本発明の抗体が結合するエピトープと結合するヒト重鎖可変部抗体は、当業者に公知の方法により取得することが可能である。公知の方法としては、例えば、本発明の抗体が結合するエピトープを通常の方法により決定し、該エピトープに含まれるアミノ酸配列を有するポリペプチドを免疫原としてヒト重鎖可変部抗体を作製する方法等が挙げられる。
【0028】
本発明の抗体には、上述のヒト重鎖可変部抗体、アミノ酸配列が改変された抗体、非ヒト動物キメラ抗体、他の分子(例えば、ポリエチレングリコールなどの高分子等)が結合した修飾抗体、糖鎖が改変された抗体等が含まれる。
【0029】
本発明における抗体の好ましい態様の一つとして、3つの重鎖CDR(重鎖CDR1〜重鎖CDR3)を取り囲む4つのフレームワーク領域、すなわちFR (重鎖FR1〜重鎖FR4)を他のヒト重鎖遺伝子由来のアミノ酸配列を適用した変異ヒト抗体等の改変抗体を挙げることができる。
【0030】
また、ヒト重鎖可変部のCDR(重鎖CDR1〜重鎖CDR3)がHer2に特異的に結合するヒト由来のアミノ酸配列からなり、3つのCDR(重鎖CDR1〜重鎖CDR3)を取り囲む4つの非ヒト動物由来の重鎖FRであることを特徴とするキメラ抗体等を挙げることができる。なおこれらの改変抗体は、既知の方法を用いて製造することができる。
【0031】
ヒト抗体はヒト体内における抗原性が低いと考えられ、治療目的などでヒトに投与する場合に有用である。非ヒト動物とヒトとのキメラ抗体は、抗体の安定性等について良い性質を付与できれば、体外診断などHer2の濃度測定に使用する場合に有用である。
【0032】
なお、キメラ抗体を作製した後に、アミノ酸を他のアミノ酸で置換、欠失、付加および/または挿入等してもよい。本発明のヒト重鎖可変部抗体には、そのようなアミノ酸置換等されたヒト重鎖可変部抗体も含まれる。
【0033】
なお、本発明の抗体の抗原(Her2)への結合活性は、例えばドットブロッティング法、ウエスタンブロッティング法、酵素結合免疫吸着アッセイ法(ELISA)、酵素免疫アッセイ法(EIA)、放射免疫アッセイ法(RIA)、免疫沈降法、表面プラズモン共鳴を利用した分子間の相互作用測定法、フローサイトメトリー、あるいは細胞染色法を用いて行うことができる。
【0034】
なお、これらの測定・検出方法に関する一般的な技術手段の詳細については、総説、成書などを参照することができる。例えば、各種抗体を用いた操作は、「Methods in ENZYMOLOGY」Vol. 70(Immunochemical Techniques(Part A))、同書Vol. 73(Immunochemical Techniques(PartB))、同書Vol. 74(Immunochemical Techniques(Part C))、同書Vol. 84(Immunochemical Techniques(Part D:Selected Immunoassays))、同書Vol. 92(Immunochemical Techniques(Part E:Monoclonal Antibodies and General Immunoassay Methods))、同書Vol. 121(Immunochemical Techniques(Part I:HybridomaTechnology and Monoclonal Antibodies))(以上、アカデミックプレス社発行)などを参照することができる。
【0035】
本発明におけるヒト重鎖可変部抗体は、IgGなど全長抗体(whole antibody)のうち、ヒト重鎖可変部抗体部分以外が欠損している抗体であり、ヒト等動物細胞で発現しているHer2への結合活性を有する限り特に限定されない。
【0036】
本発明におけるヒト重鎖可変部抗体単体が集合し多量体(ダイマー、トリマー、テトラマーなど)が自然にあるいは人為的に形成せしめることももあり得ることから、それら多量体もヒト重鎖可変部抗体に含まれる。
【0037】
ヒト重鎖可変部抗体に含まれる重鎖可変領域(重鎖CDR)のアミノ酸配列は、抗原結合活性(Her2との結合活性)を有する限り、1もしくは2個のアミノ酸の置換、欠失、付加及び/又は挿入されていてもよい。
【0038】
ヒト重鎖可変部抗体ファージからHer2に結合するヒト重鎖可変部抗体をコードする遺伝子を単離し、単利した該遺伝子を用いて、Her2に結合するヒト重鎖可変部抗体を大腸菌、あるいは動物細胞等を宿主とした組換え細胞で所望のヒト重鎖可変部抗体合成する行程を含む。
【0039】
さらに本発明は、本発明の抗体または抗体断片を有効成分として含むHer2検出用試薬(検査薬)を提供する。
【0040】
上記試薬を構成成分として含む検査・測定キットもまた、本発明に含まれる。
【0041】
また、本発明のヒト重鎖可変部抗体を含有するHer2を検出するための組成物を提供する。該組成物、または上記試薬を用いてHer2を検出する方法、および、各種疾患を診断する方法もまた、本発明に含まれる。
【0042】
なお本明細書において引用された全ての先行技術文献は、参照として本明細書に組み入れられる。
【実施例】
【0043】
以下に、実施例により本発明をさらに具体的に説明するが、本発明はそれに限定されるものではない。なお、実施例における各種遺伝子操作は、Molecular cloning third.ed.(Cold Spring Harbor Lab.Press,2001)に記載されている方法に従った。
【0044】
(1)Her2を発現するヒト培養細胞の構築
ヒト培養細胞(HEK293株:Human Embryo Kidney Cell)を宿主としてHer2を発現することを目的とし、Her2の全長遺伝子を図1示す培養細胞発現用ベクターpIRES2-EGFPのマルチクローニングサイトにSalI切断部位及びNruI/samI切断部位を用いて挿入し、Her2全長発現ベクターを作製した(図1)。HEK293細胞へのトランスフェクションにはLipofectamin (Invitrogen社製)とplus reagent (Invitrogen社製))を用いてInvitrogen社が示す方法に従って行った。
【0045】
(2)セルパニング法による陽性ファージの濃縮と陽性クローン単離
コントロール用細胞(非特異的ファージ吸着用細胞:HEK293株そのもの)および、Her2抗原発現細胞をそれぞれ1×107cells/mLになるようにPBSで希釈した。まずコントロール用細胞に1×1011 pfuの市販のヒト重鎖可変部抗体ファージライブラリー(ダナフォーム社;ドメイン抗体ファージミドライブラリー)を加え、4℃でインキュベートした。この操作によって予めHEK293細胞表面に結合するファージ群が取り除くことができる。30分のインキュベーの後、上清のファージ液を回収した。次に、回収したファージ液をHer2抗原発現細胞に加え、4℃で30分間インキュベートした。30分間インキュベートした後、該細胞を1 mLのPBSで3回洗浄し、1 mLの100 mM Glycine-HCl(pH2.0), 500 mM NaCl溶液を使用し室温で酸溶出処理をした。酸溶出処理5分後、上清のファージ液を回収した。回収したファージ液は、2 MのTris緩衝液 20μLを加えて直ちに中和した。回収したファージ液は、大腸菌TG1と混合し感染させ(37℃、30分)、100μg/mL アンピシリン、4%グルコースを含むLB寒天培地(10 cm2 X 15枚)に播種し、37℃で一晩培養した。なお、感染した大腸菌からのファージレスキュー操作は、市販キットの標準方法に従った。以上に記載したセルパニング法を3ラウンド行い、陽性ファージを単離出来るレベルまで濃縮操作を繰り返した。
【0046】
(3)細胞染色評価による陽性ファージの選択
3ラウンドの選択後、市販キットの標準方法に従って、48の単一クローンのファージを各々調製し、それら単一クローンのファージを用いた細胞染色による評価を実施した。その結果、220-14クローンがHer2特異的に結合することが確認された。(図2)
【0047】
(4)220-14クローンの塩基配列解析
細胞染色で陽性であった220-14クローンからファージミドを単離し、公知の方法により塩基配列解析を実施した。また、得られたヒト重鎖可変部抗体(VH ドメイン抗体)の塩基配列を配列番号:5に、また、該ヒト重鎖可変部抗体のアミノ酸配列を配列番号:4に示した。220-14クローンの塩基配列とアミノ酸配列を併記して図3に示した。図3に於いて、四角枠内の配列は重鎖CDR1、重鎖CDR2、重鎖CDR3であることを示す。重鎖CDR1、重鎖CDR2、重鎖CDR3のアミノ酸配列は、それぞれ、FSLNAQDMA(配列番号:1)、AINNTG(配列番号:2)、ANSTRRNAKLGY(配列番号:3)であった。
【特許請求の範囲】
【請求項1】
重鎖CDR1のアミノ酸配列としてFSLNAQDMA(配列番号:1)、重鎖CDR2のアミノ酸配列としてAINNTG(配列番号:2)、重鎖CDR3のアミノ酸配列としてANSTRRNAKLGY(配列番号:3)を有するHer2に結合するヒト重鎖可変部抗体(VH ドメイン抗体)。
【請求項2】
請求項1に記載された重鎖CDR1〜3のそれぞれのアミノ酸配列において、1もしくは2個のアミノ酸が置換、欠失、付加されたアミノ酸配列をそれぞれ重鎖CDR1〜3とするHer2に結合するヒト重鎖可変部抗体。
【請求項3】
請求項1〜2のいずれかに記載の抗体が、フレームワーク領域(FR)がヒト由来の配列であることを特徴とする、Her2に結合するヒト重鎖可変部抗体。
【請求項4】
抗体がキメラ抗体またはヒト化抗体であることを特徴とする、請求項1〜3のいずれかに記載のHer2に結合するヒト重鎖可変部抗体。
【請求項5】
配列番号:4に記載されたヒト重鎖可変部抗体(VH ドメイン抗体)のアミノ酸配列における重鎖CDR1〜3を有することを特徴とするHer2に結合するヒト重鎖可変部抗体。
【請求項6】
請求項1〜5のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2検出用試薬。
【請求項7】
請求項1〜5のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2結合医薬組成物。
【請求項1】
重鎖CDR1のアミノ酸配列としてFSLNAQDMA(配列番号:1)、重鎖CDR2のアミノ酸配列としてAINNTG(配列番号:2)、重鎖CDR3のアミノ酸配列としてANSTRRNAKLGY(配列番号:3)を有するHer2に結合するヒト重鎖可変部抗体(VH ドメイン抗体)。
【請求項2】
請求項1に記載された重鎖CDR1〜3のそれぞれのアミノ酸配列において、1もしくは2個のアミノ酸が置換、欠失、付加されたアミノ酸配列をそれぞれ重鎖CDR1〜3とするHer2に結合するヒト重鎖可変部抗体。
【請求項3】
請求項1〜2のいずれかに記載の抗体が、フレームワーク領域(FR)がヒト由来の配列であることを特徴とする、Her2に結合するヒト重鎖可変部抗体。
【請求項4】
抗体がキメラ抗体またはヒト化抗体であることを特徴とする、請求項1〜3のいずれかに記載のHer2に結合するヒト重鎖可変部抗体。
【請求項5】
配列番号:4に記載されたヒト重鎖可変部抗体(VH ドメイン抗体)のアミノ酸配列における重鎖CDR1〜3を有することを特徴とするHer2に結合するヒト重鎖可変部抗体。
【請求項6】
請求項1〜5のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2検出用試薬。
【請求項7】
請求項1〜5のいずれかに記載のHer2に結合するヒト重鎖可変部抗体を有効成分として含むHer2結合医薬組成物。
【図1】


【図3】


【図2】




【図3】


【図2】


【公開番号】特開2012−158533(P2012−158533A)
【公開日】平成24年8月23日(2012.8.23)
【国際特許分類】
【出願番号】特願2011−17979(P2011−17979)
【出願日】平成23年1月31日(2011.1.31)
【出願人】(507371294)
【Fターム(参考)】
【公開日】平成24年8月23日(2012.8.23)
【国際特許分類】
【出願日】平成23年1月31日(2011.1.31)
【出願人】(507371294)

【Fターム(参考)】
[ Back to top ]

