折り畳み可能な構造体を含むデバイス
【課題】生物学的材料によって折り畳み可能な構造体デバイスと、該デバイスの製造方法を提供する。
【解決手段】構造体と、該構造体を遊離可能なように保持する基材とからなるデバイス。前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、該ヒンジ構造は、生物学的材料が前記ヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋できる寸法を有し、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される。前記デバイスの製造方法と、前記デバイス及び生物学的材料を含む、移植用デバイス及び分析用器具。
【解決手段】構造体と、該構造体を遊離可能なように保持する基材とからなるデバイス。前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、該ヒンジ構造は、生物学的材料が前記ヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋できる寸法を有し、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される。前記デバイスの製造方法と、前記デバイス及び生物学的材料を含む、移植用デバイス及び分析用器具。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、生物学的材料によって折り畳み可能な構造体デバイスと、該デバイスの製造方法とに関する。
【背景技術】
【0002】
経皮経管血管形成術その他の低侵襲治療用デバイスとして、MEMS技術その他の微細加工技術を用いた細胞足場が注目される。従来技術で報告された細胞は、MEMS技術を用いて加工したパリレン製ステンシルを用いて、同一の培養容器の基質の細胞接着特性を逐次的に変化させることにより、特定のパターンで複数の細胞タイプの細胞が配置されるように細胞を接着させて混合培養することである(非特許文献1)。また、別のアプローチでは、微細加工された櫛状の構造体を複数用意して、それぞれの櫛状の構造体の表面に異なる細胞タイプの細胞を接着させておいたうえで、両方の構造体の櫛状部分が嵌合させることにより、所定の間隔を置いて複数の細胞タイプの細胞が配置されるように混合培養することである(非特許文献2)。しかし、これらの細胞足場は立体形状ではないため、血管閉塞の治療用デバイスであるステントやコイルのように体内臓器の立体的形態を修復又は補整するために利用することができない。
【0003】
竹内らによって出願された特許文献1には、近接して配置された2個又は3個以上の平面状の細胞足場を跨ぐように細胞を播種することによって、細胞の伸展ないしは収縮によって発生する力によって前記細胞足場が引き起こされて、前記細胞を覆うように配置された、該細胞と、前記細胞足場とからなる立体的な集合体の作製が説明される。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】国際出願第PCT/JP2009/66427号出願明細書
【非特許文献】
【0005】
【非特許文献1】Wright, D.ら、Lab on a Chip,7:1272(2007)
【非特許文献2】Hui, E. E.及びBhatia, S.N.、Proc. Natl. Acad. Sci. U. S. A.,104:5722(2007)
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながらこれらの従来技術では、前記平面的な細胞足場どうしの立体的な位置関係、例えば、隣接する平面的な細胞足場の間の立体角を指定することはできない点が問題である。そこで、単に細胞の伸展ないしは収縮によって発生する力で平面的な細胞足場を立体的に配置させるだけでなく、隣接する平面的な細胞足場の間の位置関係を指定して立体的に配置させる技術を開発する必要がある。
【課題を解決するための手段】
【0007】
本発明は、構造体と、該構造体を遊離可能なように保持する基材とからなるデバイスを提供する。本発明のデバイスにおいて、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、該ヒンジ構造は、生物学的材料が前記ヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋できる寸法を有し、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される。
【0008】
本発明のデバイスにおいて、前記両岸の頂面の少なくとも一部は前記生物学的材料との接着を増強させる処理が施される場合がある。
【0009】
本発明のデバイスにおいて、前記基材は剛性の高い素材でできており、前記構造体は、前記基材との間に設けられた遊離制御剤層基板からによって、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記構造体は応力を加えることによって前記基材から遊離される場合がある。
【0010】
本発明のデバイスにおいて、前記基材は粘着力を備えた弾性の高い素材でできており、前記構造体は、前記粘着力によって、前記デバイスの外表に前記構造体の一部が露出した状態で前記弾性基材の表面に保持され、前記構造体は前記弾性基材に応力を加えることによって該弾性基材から遊離される場合がある。
【0011】
本発明のデバイスにおいて、前記デバイスの外表に露出した前記構造体は帯状で、前記ヒンジ構造は複数本が互いに平行に設けられ、前記構造体に接着した生物学的材料が収縮するとき、前記構造体が中空の立体形状となる場合がある。
【0012】
本発明のデバイスにおいて、前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体の形状となる場合がある。
【0013】
本発明のデバイスにおいて、前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状が少なくとも2個以上前記ヒンジ構造を隔てて隣接する形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体が連続する形状となる場合がある。
【0014】
本発明のデバイスにおいて、前記構造体の少なくとも一部には前記構造体の頂面から底面に達する貫通孔が設けられる場合がある。
【0015】
本発明のデバイスにおいて、前記生物学的材料は複数の種類からなり、前記構造体にはそれぞれの種類の生物学的材料が特異的に前記ヒンジ構造を跨いで接着できる処理が施される場合がある。
【0016】
本発明のデバイスにおいて、前記生物学的材料は、細胞か、収縮可能な高分子化合物かの場合がある。
【0017】
本発明のデバイスにおいて、前記生物学的材料は、動物細胞の場合がある。
【0018】
本発明のデバイスにおいて、前記構造体はポリパラキシリレンでできており、前記生体適合性ポリマー層は、2−メタクリロイルオキシエチルホスホリルコリンの層で、前記生物学的材料との接着を増強させる処理はO2プラズマ照射処理の場合がある。
【0019】
本発明のデバイスにおいて、前記構造体は自己組織的に組み上がる機能を有する場合がある。
【0020】
本発明のデバイスにおいて、前記自己組織的に組み上がる機能は、前記構造体の表面に凹陥部と凸出部とが設けられ、1個の構造体の表面の凹陥部が他の1個の構造体の表面の凸出部と相補的に嵌合することにより達成される場合がある。
【0021】
前記自己組織的に組み上がる機能は、前記構造体の表面に親水性部分及び/又は疎水性部分が設けられ、1個の構造体の表面の親水性部分が他の1個の構造体の表面の親水性部分と接し、及び/又は、1個の構造体の表面の疎水性部分が他の1個の構造体の表面の疎水性部分と接することにより達成されることを特徴とする場合がある。
【0022】
本発明は、本発明のデバイスと、生物学的材料とを含む、生体移植用器具を提供する。
【0023】
本発明の生体移植用器具は、前記デバイスから遊離させた前記構造体を患者の体内に移植し、該患者由来の生物学的材料を前記構造体に接着させて、前記生物学的材料の収縮によって前記構造体が折り畳まれるように用いられる場合がある。
【0024】
本発明は、本発明のデバイスと、生物学的材料とを含む、分析用器具を提供する。
【0025】
本発明は、構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は剛性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法を提供する。本発明のデバイスの製造方法は、前記基材の上に遊離制御剤層を形成するステップと、該遊離制御剤層の上に第1の樹脂層を形成するステップと、第1の樹脂層の上に、前記ヒンジ構造を含む前記構造体の形状に対応するように配置される第2の樹脂層を形成するステップと、第2の樹脂層の上に、第3の樹脂層を形成するステップと、第3の樹脂層の上に、前記ヒンジ構造を含まない前記構造体の形状に対応するように保護層を形成するステップと、該保護層で覆われないで第3の樹脂層が露出する部分について、前記遊離制御剤層と、第1ないし第3の樹脂層とを除去して基材を露出させるステップと、前記露出した基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含む。
【0026】
本発明は、構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は粘着力を備えた弾性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法を提供する。本発明のデバイスの製造方法は、前記ヒンジ構造を含む構造体と基板とが支持部を介して一体となるように成形するステップと、前記基板と一体に成形された構造体を、前記ヒンジ構造が設けられた面が露出するように前記基材に押し付けて、前記構造体を前記基材の表面に圧着させる押圧力により前記支持部を破壊するとともに、前記構造体を前記基材の表面に保持し、前記基板から分離させるステップと、前記基材に保持された前記構造体の上に保護層を形成するステップと、前記基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含む。
【0027】
前記本発明のデバイスの製造方法において、前記構造体を前記基材の表面に圧着させるステップと、前記基板から分離させるステップとは、複数の構造体について別々に実施され、前記複数の構造体のうちの1つが保持された基材に他の構造体が保持された基材を押し付けることにより、前記複数の構造体の1つの表面に前記他の構造体が接着された立体的な形状の構造体が形成されるステップを含む場合がある。
【0028】
前記本発明のデバイスの製造方法において、前記保持させるステップの前に、前記生物学的材料と前記構造体との接着を増強させる処理を施すステップを含む場合がある。
【0029】
本発明は、生体移植用器具の製造方法を提供する。本発明の生体移植用器具の製造方法は、本発明のデバイスと、生物学的材料とを用意するステップと、該デバイスのそれぞれの外表に露出した前記構造体の表面に前記生物学的材料を接着させるステップと、前記生物学的材料が収縮することにより前記構造体を折り畳ませるステップとを含む。
【0030】
本発明は、被験物質と生物学的材料との相互作用を分析する方法を提供する。本発明の被験物質と生物学的材料との相互作用を分析する方法は、デバイスを用意するステップと、該デバイスのそれぞれの外表に露出した前記構造体の表面に生物学的材料を接着させるステップと、前記生物学的材料が接着した構造体に被験物質を曝すステップと、前記被験物質に曝された前記生物学的材料が収縮することによって、前記構造体が折り畳まれるステップと、前記構造体が折り畳まれることによる前記構造体の立体形状の変化を解析するステップとを含む。
【0031】
本発明は、細胞と構造体とからなる集合体の作成方法を提供する。本発明の集合体の作成方法は、本発明のデバイスと、細胞とを用意するステップと、前記細胞の少なくとも1個が、前記デバイスの外表に露出した前記構造体の頂面に設けられた少なくとも1個のヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋するように播種して培養するステップと、培養下で前記細胞が収縮することにより、前記少なくとも1個のヒンジ構造を挟む少なくとも2つの前記構造体の頂面を前記細胞が引き寄せて、前記構造体を折り畳ませるステップとを含み、前記折り畳まれた構造体の表面は、前記細胞を取り囲み、凸多面体か、その一部か、これらの繰り返し構造かとなる。
【0032】
本発明は、複数の構造体と、該構造体を遊離可能なように保持する基材と、生物学的材料とからなるデバイスを提供する。本発明のデバイスにおいて、前記構造体は、前記デバイスの外表に前記複数の構造体の一部が露出した状態で前記基材の表面に保持され、前記生物学的材料は前記複数の構造体に跨って接着し、前記構造体が前記基材から遊離するとき、前記生物学的材料が前記複数の構造体を引き寄せて立体的に配置させ、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される。
【0033】
本発明の複数の構造体と、該構造体を遊離可能なように保持する基材と、生物学的材料とからなるデバイスにおいて、前記生物学的材料は動物細胞の場合がある。
【図面の簡単な説明】
【0034】
【図1】細胞が接着した構造体の製造方法の1つの実施態様を示す模式図。
【図2】細胞が接着した構造体の製造方法の別の実施態様を示す模式図。
【図3】前記別の実施態様の製造方法で製造された構造体が異なる間隔を置いて配置され、その上に3T3細胞が接着した状態を示す光学顕微鏡写真(A)及び(B)と、前記間隔を置いて配置された2個の構造体を跨いで接着する3T3細胞が存在する割合と、前記間隔(μm)との関係を示すグラフ(C)。
【図4】2個の構造体の上の多数の3T3細胞が接着する場合(A)及び(B)と、2個の構造体の上の多数の3T3細胞が接着する場合(C)及び(D)とについて、前記構造体が折り曲げられる前に前記細胞が接着した前記構造体の面が視線方向に垂直となるように撮影された顕微鏡写真(A)及び(C)と、前記構造体が折り曲げられた後に前記細胞が接着した前記構造体の面が視線方向に平行となるように撮影された顕微鏡写真(B)及び(D)と、前記構造体上に接着した3T3細胞の数と、前記構造体の折り曲げられる角度との関係を示すグラフ(E)。
【図5】本発明の1つの実施態様のデバイスの製造方法を示す模式図。
【図6】本発明の構造体の溝の幅及び深さと、該溝の底での前記デバイスの厚さと、折れ曲がる角度との関係式の説明図。
【図7】本発明の貫通孔を有する正12面体を展開した形状に配置して並べられた12個の構造体に細胞が接着して折り畳まれる前(A)と、折り畳まれる途中((B)及び(C))と、完全に折り畳まれて正12面体の形状となった状態(D)との顕微鏡写真。(D)では貫通孔を通ってガラス細管が立体化した前記構造体の内部にアクセスできた。
【図8】図8(A)及び(B)は、それぞれ、本発明の発明者の所属する東京大学(University of Tokyo)の頭文字であるU及びTの形状を示す。
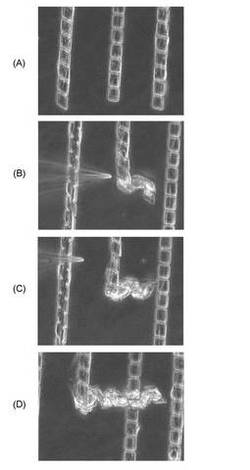
【図9】帯状に並んだ本発明の構造体に細胞が接着した顕微鏡写真で、図9(A)は前記構造体が全て基板に貼り付いている状態を示し、図9(B)、(C)及び(D)は、前記構造体の一端にガラス針を接触させて前記構造体の一端を基板から脱離させると、細胞によって前記構造体が前記一端から順番に折れ畳まれていく様子を示す。
【図10】本発明の溝状のヒンジ構造を備える構造体に細胞が接着した顕微鏡写真で、図10(a)は前記構造体が全て基板に貼り付いている状態と、本発明の構造体のうち1個の一端にガラス針を接触させている様子を示し、図10(b)及び(c)は、細胞によって前記構造体が前記一端から順番に折れ畳まれてできた筒状の立体構造を示す。
【図11】ヒンジ構造で折れ曲がった平面がなす角度をあらかじめ、それぞれ、90°((a−1)及び(a−2))と、135°((b−1)及び(b−2))と、120°((c−1)及び(c−2))とになるように加工された構造体に細胞を接着させて折り畳ませて得られた立体構造の顕微鏡写真。
【発明を実施するための形態】
【0035】
本明細書における生物学的材料とは、生物に由来するいずれかの材料を指し、生物個体、臓器、組織及び細胞と、葉緑体、染色体、分裂装置、色素胞等の細胞内小器官と、ウイルス、DNA複製酵素複合体、転写/RNAプロセッシング複合体、リボソーム、イオンチャンネル、細胞表面レセプター複合体、クラスリン被覆小胞等の分子集合体と、核酸、タンパク質等の生体高分子と、分子の高次構造の変化によって分子が収縮したり、運動したりする全ての高分子化合物とを含むが、これらに限定されない。好ましい生物学的材料は、細胞、特に、固体である基質に接着して伸展したり、運動したりする動物細胞と、アクチン−ミオシン系、ダイニン−チューブリン系を含む、天然及び人工の収縮可能な高分子とである。
【0036】
本発明における生物学的材料の接着とは、固体基質である構造体の表面と当該生物学的材料との接着をいう。前記生物学的材料が、細胞内小器官、分子集合体、生体高分子及び化合物の場合には、静電気的な荷電による吸着を含む、いずれかの共有結合及び/又は非共有結合による構造体への不動化をいう。前記生物学的材料が細胞の場合には、前記いずれかの共有結合及び/又は非共有結合による構造体への不動化のような非生理的現象と、細胞−基質間接着のような細胞の生理現象とを含む。前記細胞が2個または3個以上の場合には、細胞−細胞間接着も含む。
【0037】
本発明において、生物学的材料と構造体との接着を増強させる処理とは、構造体の表面に、コラーゲンの他、フィブロネクチン、ビトロネクチン、ラミニン、ニドジェン、テネイシン、トロンボスポンジン、von Willebrand因子、オステオポンチン、フィブリノーゲン、エラスチン、プロテオグリカン等の細胞と基質との接着に関与することが知られている物質をコーティングする処理をいう。また、構造体の表面に、プラズマ処理、フッ酸処理又は紫外線照射処理を施すことによって、前記構造体を基板から分離させる際に破壊した支持部のうち前記構造体の表面に残った部分を除去すること、及び/又は、前記構造体の表面を清浄にすることも、生物学的材料と構造体との接着を増強させる処理に含まれる。
【0038】
本発明のデバイスは、構造体と、該構造体を遊離可能なように保持する基材とからなる。前記基材は、剛性の高い素材でできている場合がある。本発明に用いることができる剛性の高い素材は、ガラス、シリコン、金属、セラミック、その他の複合材料を含むが、これらに限定されない。剛性の高い素材としては、光透過性が高く、倒立顕微鏡により本発明のデバイス上に播種された細胞を観察できるものが好ましい。
【0039】
本発明のデバイスの基材が剛性の高い素材でできている場合には、本発明の構造体は、前記基材の上に遊離制御剤の層を形成し、該遊離制御剤の層の上に、さらに複数の樹脂層を形成し、所望の形状と、ヒンジ構造とを有するように製造される。好ましい遊離制御剤は、ゼラチンのようにわずかな応力によって容易に剥離することができる物質の他、アルギン酸のようにカルシウムイオンの添加によってゲル化し、アルギン酸リアーゼによって分解される物資と、ポリ(N‐イソプロピルアクリルアミド)(PIPAAm)のように高温ではゲル化するが、低温では溶解する物質とを含むが、これらに限られない。かかる遊離制御剤を用いることによって、本発明の構造体は遊離可能なように基材に保持される。
【0040】
図1に、細胞が接着することによって引き寄せられる構造体が、剛性の高い素材でできている基材の上に設けられる場合の製造方法の例を示す。この例では前記基材はガラス製である。前記基材の上にゼラチン層を形成し、該ゼラチン層の上にポリパラキシリレン(図1(A)ではパリレン(商標)と表記される。)の層を形成する。前記ポリパラキシリレン層の上にアルミニウムを積層して、O2プラズマ処理によるエッチングを行う。該エッチングによって、前記アルミニウム層で保護されないポリパラキシリレン層及びゼラチン層は完全に除去される(図1(B))。これにより、本発明の構造体が前記基材の上に形成される。その後、2−メタクリロイルオキシエチルホスホリルコリンポリマー(MPCポリマー)をスピンコーティングする(図1(C))。それから、アルミニウム層と、その上のMPCポリマー層とを除去すること(リフトオフ)によって除去する(図1(D))。改めて露出されたポリパラキシリレン層の表面にフィブロネクチンをコーティングする(図1(E))。このようにして、前記構造体の表面は細胞との接着が増強されるが、前記基材の表面もともとはO2プラズマ処理により親水化しており、そこに両媒性のMPCポリマーをコーティングしたので、MPCポリマーでコーティングされた表面は疎水性となり、細胞−基質間接着が妨げられる。そのため、以上のとおりの手順で作製されたデバイスに細胞を播種すると、細胞は前記構造体の表面だけに選択的に接着する。そして、細胞の力によって隣接する構造体が基材から引き起こされて、折り畳まれる。
【0041】
本発明のデバイスに含まれる基材は、粘着力を備えた弾性の高い素材でできている場合がある。物理的な原理によって遊離可能なように構造体を保持することができる基材、特に、応力、圧力、振動、超音波、光、電気、熱、静電気等に応答して、粘弾性、表面の親水性、表面張力、表面の平坦性、表面の帯電状態等が変化する物質は、本発明の技術分野の専門家に周知である。本発明の構造体を保持することができ、かつ、応力、圧力、振動、超音波等に応答して前記構造体を遊離することができる基材の好ましい具体例は、シリコンゴム、ポリイミド、ポリエチレンテレフタレート(PET)又はポリジメチルシロキサン(PDMS)を含むが、これらに限られない、粘着力のある弾性基材である。
【0042】
図2に、細胞が接着することによって引き寄せられる構造体が、粘着力を備えた弾性の高い素材でできている基材の上に設けられる場合の製造方法の例を示す。この例では前記基材はポリジメチルシロキサン(PDMS)製である。出発材料は、シリコン・オン・インシュレータ(SOI)ウェーハであった。前記埋め込み酸化物層を構造体の素材とした。デバイスケイ素層は、S1805フォトレジストをマスキング層として用いる誘導結合プラズマ−反応性イオンエッチング法によりエッチングされた。前記フォトレジスト層を除去した後、前記埋め込み酸化物層は、フッ酸によりエッチングされ、構造体の形状が形成された(図2(B))。
【0043】
SiO2層上に残存したデバイスケイ素層は、ICP−RIE法により除去され、SiO2層の下の基板ケイ素層は水酸化テトラメチルアンモニウムで異方性エッチングされた。前記異方性エッチング反応は、基板ケイ素層からSiO2層が完全に分離する直前に停止された。構造体を支持するピラミッド状のケイ素構造が形成された(図2(C))。前記構造体を分離する前に、細胞と構造体との接着を増強させるために、実施例1で説明したコラーゲンの塩酸溶液にウェーハ上の構造体を3時間浸漬した。
【0044】
その後前記構造体は、押印転写法を用いてSOIウェーハから分離され、PDMSの弾性基材の上に粘着力によって保持された。1mm厚のPDMSシートがウェーハ上の構造体の上に戴置され(図2(D))、剥離された(図2(E))。このようにして、前記構造体はその一部が外表に露出した状態で前記弾性基材の表面に保持された(図2(F))。基材のPDMSは疎水性であるが、基材に保持された構造体は前記コラーゲン処理を施されているので、前記基材上に保持された前記構造体に細胞を播種すると、細胞は前記構造体の上に選択的に接着する(図2(G))。前記基材に応力を加えることによって前記構造体は前記基材から遊離する(図2(H))。
【0045】
本発明の生体適合性ポリマーは、生物学的材料を含むデバイスに用いられるときに前記生物学的材料に対して特に有害な影響を及ぼさない高分子化合物をいう。本発明の生体適合性ポリマーは、生物学的材料との非特異性吸着を抑制する場合がある。かかる生体適合性ポリマーが本発明の構造体及び基板の上にコーティングされ、該生体適合性ポリマーの層が形成されるとき、生物学的材料は前記構造体又はマイクロ流路デバイスに固着せず、容易に洗浄除去することができる。生体適合性ポリマーは、生物学的材料との非特異性吸着を抑制する両親媒性ポリマーが好ましく、2−メタクリロイルオキシエチルホスホリルコリン(MPC)ポリマーがより好ましい。また、生物学的材料が細胞外オルガネラ又は生体分子の場合には、ウシ血清アルブミンのようなタンパク質を生体適合性ポリマーとしいて用いることができる。
【0046】
本発明の構造体の表面にはヒンジ構造が少なくとも1個形成される。本発明のヒンジ構造は、前記構造体が折り目に沿って折り畳まれるとき、折り畳まれる部分を連結できるものであればいかなる構造であってもかまわない。好ましいヒンジ構造の1つは、折り目の方向に沿って前記構造体の頂面に設けられる溝である。該溝は、前記頂面の辺縁から出発して相対する辺縁まで達する場合もあるが、前記頂面の一部に設けられる場合もある。別の好ましいヒンジ構造は、折り目の方向に垂直な方向に沿って前記構造体を貫通する複数のスリットである。前記構造体が折り畳まれるとき、前記スリットで区切られた折り目の部分は、前記構造体が折り畳まれる向きと同じ向きに折れ曲がるものと、前記構造体が折り畳まれる向きと反対の向きに折れ曲がるものとが互い違いに並ぶ。
前記スリットの幅は、互い違いに異なる向きに折れ曲がることができればいかなるものであってもよい。前記スリットの幅が前記構造体の折れ目の長さに対して数分の1以上の場合には、前記構造体が折り畳まれるときの反発力が小さいという利点があるのでより好ましい。
【0047】
本発明の器具は、接着させる生物学的材料や、利用目的に応じて、無菌処理を施したり、生体毒性のない素材及び製造方法で製作される。
【0048】
本発明の構造体は、形状又は材料などが特定のものに限定されない。本明細書の実施例の構造体は、折り紙のように折り畳まれて立体形状となるため、平板の形状であることが好ましい。
【0049】
本発明の構造体は、例えば、光リソグラフィ、エッチング等の従来の微細加工技術を組合せて、犠牲層の除去により立体的な構造とすることができる(EE Text センサ・マイクロマシン工学、藤田博之編著、オーム社(2005))。代替策として、図2でも説明される押印転写法(特願2007−10867号明細書及びOnoe, H.ら、Journal of Micromechanics and Microengineering, 17: 1818−1827 (2007))を利用する場合がある。
【0050】
本発明の構造体は、従来の微細加工技術及び/又は前記押印転写法を、単独で、あるいは、組み合わせて作成された立体的な形状を有する鋳型を使って作成される成形品の場合がある。前記成形品は、プラスチック、セラミック及びハイドロゲルと、これらの複合材料とを含むが、これらに限定されない材料を用いて作成される場合がある。
【0051】
本発明の構造体について自己組織的に組み上がるとは、摩擦力、表面張力、疎水結合、磁力、静電気を含むがこれらに限定されない物理的な引力及び/又は斥力か、化学的又は生物学的な結合か、を用いて、メディウム中で構造体がランダムに衝突していくうちに、構造体の集合体が形成され、該集合体においてそれぞれの構造体は予め定められたパターンに従って配置されることをいう。本発明の構造体について自己組織的に組み上がる機能は、例えば、前記構造体の表面に凹陥部と凸出部とが設けられ、1個の構造体の表面の凹陥部が他の1個の構造体の表面の凸出部と相補的に嵌合することにより達成される場合(例えば、Yeh, H. J. J.及びSmith, J. S.、 Ieee Photonics Technology Letters: 6, 706−708 (1994)を参照せよ。)があり、あるいは、前記構造体の表面に親水性部分及び/又は疎水性部分が設けられ、1個の構造体の表面の親水性部分が他の1個の構造体の表面の親水性部分と接し、及び/又は、1個の構造体の表面の疎水性部分が他の1個の構造体の表面の疎水性部分と接することにより達成される場合(例えば、Bowden, N.ら、Langmuir :17, 1757−1765 (2001)を参照せよ。)がある。また、抗原と抗体との反応や、酵素と基質との間又は酵素と阻害剤との間の相互作用や、ポリヒスチジンとニッケルイオンとの間の相互作用等を含むが、これらに限られない、分子識別の特異性を利用した、化学的又は生物学的な結合により達成される場合がある。さらに、これらのいずれかの組合せにより達成される場合がある。
【0052】
折り畳まれる前の平板又はディスク状の形状の構造体は、メディウム中で3次元的に自由に運動できるとき、構造体どうしが自己集合することができない場合がある。かかる場合には、前記メディウム中に、該メディウムに不溶性の液体を添加して、前記メディウムと前記不溶性の液体との間の界面に構造体を浮かべることにより、構造体が2次元的な自由運動しかできないようにすると、集合体の形成を促進できる場合がある。前記メディウムに不溶性の液体は、前記メディウムより比重が大きい液体や、基材との間の表面張力が前記メディウムと基材との表面張力より小さい液体であることが好ましい。
【0053】
集合体を構成する構造体の数や配置パターンを制御して、自己組織的に組み上がるように構造体を設計すると、それぞれの集合体に接着する生物学的材料を特定の組合せだけにすることができる。これによって、折り畳まれた立体形状の構造体において、2種類又は3種類以上の細胞を、構造体の内部又は外部の特定の場所に配置することができる。
【0054】
前記構造体の表面の別の一部と前記基材の表面の一部との特異的な相互作用は、疎水性相互作用及び電磁気学的相互作用の他、生体分子と、該生体分子に対する特異的結合パートナーとの相互作用や、金属イオンと、該金属イオンに特異的なキレート剤との相互作用を含むが、これらに限定されない。前記疎水性相互作用は、前記構造体の表面の別の一部と、前記基材の表面の一部とがともに疎水性処理が施され、表面どうしが直接接触することによって発生する場合がある。代替的には、油滴のような疎水性の液体を介在することによって発生する場合がある。前記疎水性処理は、例えば、自己組織化法のような周知の表面処理技術を用いてアルカンチオールのような疎水性分子を構造体及び基材の前記表面に結合させることによって達成することができる。前記電磁気学的相互作用には、静電気又は表面荷電による引力を利用するものと、磁石による磁界を利用するものと、電界とそれにより誘導された電気双極子モーメントを利用するものとを含むが、これらに限定されない。電界とそれにより誘導された電気双極子モーメントを利用する電磁気学的相互作用には、誘導誘電泳動、静電配向等を含むが、これらに限定されない。前記生体分子と、該生体分子に対する特異的結合パートナーとの相互作用には、糖類とレクチンとの相互作用、抗原と抗原との相互作用、核酸の相補的対合による相互作用とを含むが、これらに限定されない。また、前記構造体と前記基材とが嵌合可能な形状を有することによって、特定の配向で嵌合することによる相互作用や、前記構造体が、前記基材に設けた開口を塞栓する静水圧による相互作用の組み合わせによって前記構造体が前記基材に保持される場合がある。また、以上に列挙される相互作用の2つ以上の組み合わせによって前記構造体が前記基材に保持される場合がある。
【0055】
本発明の細胞と構造体とからなる集合体に用いる構造体は、アクテュエーターを含むか、あるいは、外部の動力源に接続するかによって、1個ずつ、あるいは、2個又は3個以上を同時に、駆動することができる。あるいは、心筋細胞のような形態変化を起こす細胞を含む構造体では、細胞の動きによって前記構造体を駆動することができる。前記アクテュエーターは、周知の微細加工技術又はMEMS技術によって作成することができる。本発明の細胞と構造体とからなる集合体を用いて、1個又は2個以上の細胞の表面の物理的性質を測定することができる。ここで物理的性質とは、弾性、硬度、表面電位及び膜輸送を含むが、これらに限定されない。前記膜輸送に関する物理的性質には、浸透圧、能動輸送、その他の生体膜による物質の移動に関係する性質を含む。かかる細胞表面の物理的性質を測定するときには、前記構造体には物理的性質のセンサー、例えば、変位、速度、力、圧力などの機械量を検出するセンサーや、イオン選択性電極、イオン感応電界トランジスタ(ISFET)などのイオンセンサーを含むことが望ましい。かかる物理的性質のセンサーは周知の微細加工技術によって作成することができる(EE Text センサ・マイクロマシン工学、藤田博之編著、オーム社、2005年を参照せよ。)。さらに、前記構造体及び/又は前記基材は細胞と接触するプリント配線による電極を設けて、前記構造体が前記基材と嵌合するときに外部から電気的に接続して電気刺激を行ったり電位を測定したりする場合がある。また、前記構造体及び/又は前記基材を貫通する細孔であって、細胞膜によって電気的にシールすることができるように細胞より小さな孔径を有する貫通孔を設けて、いわゆるオートパッチ法による電気生理学的な測定を行う場合がある。この場合には、前記構造体が前記基材と嵌合するとき、前記構造体に設けた貫通孔が基材に設けた貫通孔が連通するように配置される場合がある。かかるプリント配線及び貫通孔も周知の微細加工技術又はMEMS技術によって作成することができる。
【0056】
以下に実施例を示すが、これらは実施態様の例示を意図しており本発明の範囲を限定することは意図しない。
【実施例1】
【0057】
1.構造体のヒンジ構造の寸法検討
50×50μm2の表面積と3μmの高さのフィブロネクチンでコーティングされた構造体が、3、5、10、20又は50μmの間隔を置いてMPCポリマーでコーティングされた基材上に配置されたデバイスが、図1で説明される方法に従って製造された。前記デバイスに3T3細胞が4−8×104個/cm2の播種密度で播種され、基質と接着しない細胞が培養開始4時間後に洗浄除去された。その後、24時間後に3T3細胞が隣接した構造体を跨いで増殖するかどうかを観察した。さらに、前記2枚の構造体が3T3細胞に引き起こされてなす角度と、前記構造体2個あたりに存在する細胞の数との関係も調べた。
【0058】
図3は、異なる間隔を置いて配置され、その上に3T3細胞が接着した状態を示す光学顕微鏡写真(A)及び(B)と、前記間隔を置いて配置された2個の構造体を跨いで接着する3T3細胞が存在する割合と、前記間隔(μm)との関係を示すグラフ(C)である。図3(C)から、前記構造体の間隔が10μm以下の場合には全て、2個の構造体を跨いで接着していた。
【0059】
図4は、2個の構造体の上の多数の3T3細胞が接着する場合(A)及び(B)と、2個の構造体の上の多数の3T3細胞が接着する場合(C)及び(D)とについて、前記構造体が折り曲げられる前に前記細胞が接着した前記構造体の面が視線方向に垂直となるように撮影された顕微鏡写真(A)及び(C)と、前記構造体が折り曲げられた後に前記細胞が接着した前記構造体の面が視線方向に平行となるように撮影された顕微鏡写真(B)及び(D)と、前記構造体上に接着した3T3細胞の数と、前記構造体の折り曲げられる角度との関係を示すグラフ(E)である。図4(E)から明らかなように、前記構造体上に接着した3T3細胞の数が増えると、前記構造体の折り曲げられた2つの頂面がなす角度が大きくなった。これらの知見に基づいて、以下のとおり溝状のヒンジ構造を有する構造体の寸法を決定した。
【0060】
図5は、本発明の構造体の溝の幅及び深さと、該溝の底での前記デバイスの厚さと、折れ曲がる角度との関係式の説明図である。図5から明らかなとおり、本発明の構造体の溝の幅w及び深さrと、該溝の底での前記デバイスの厚さtと、折れ曲がる角度θとの間には以下の式1の関係が成立する。
【0061】
w=(r+0.5×t)×θ (式1)
【実施例2】
【0062】
2.本発明のヒンジ構造を備えた構造体を含むデバイスの作製
図6は、本発明の1つの実施態様のデバイスの製造方法を示す模式図である。図6を参照して、本発明のデバイスは以下のとおりの手順で作成された。ガラス基板に2%ゼラチン水溶液を200rpmでスピンコーティングし、その上にポリパラキシリレン層を形成した(図6(A))。SU8樹脂を前記ポリパラキシリレン層の上にコーティングし、所望の配置パターンで、構造体と、該構造体に設けられる溝とが形成されるように遮光スクリーンを使って前記SU8樹脂の光重合を行い、未重合のSU8樹脂を洗い流した(図6(B))。前記SU8樹脂層と、前記ゼラチン層との上にポリパラキシリレン層を形成した(図6(C))。その後、前記ポリパラキシリレン層をアルミニウムでマスキングしてO2プラズマ処理を施し、マスキングされないポリパラキシリレン層及びゼラチン層を除去した(図6(D))。その後、MPCポリマーを基板上にスピンコーティングした(図6(E))。さらに、前記アルミニウム層をテトラメチルアンモニウムハイドロオキサイドを用いて除去し、前記アルミニウム層の上のMPCポリマーをリフトオフによって除去した(図6(F))。
【実施例3】
【0063】
3.さまざまな立体形状に折り畳まれた構造体
図7は、本発明の貫通孔を有する正12面体を展開した形状に配置して並べられた12個の構造体に細胞が接着して折り畳まれる前(A)と、折り畳まれる途中((B)及び(C))と、完全に折り畳まれて正12面体の形状となった状態(D)との顕微鏡写真である。図8(D)では貫通孔を通ってガラス細管が立体化した前記構造体の内部にアクセスできた。このように、本発明のデバイスを用いると、立体的に配置された1個又は2個以上の細胞に外部から電極を刺す等のやり方で細胞内電位その他の細胞生理学的な情報を得ることができる。
【0064】
図8は、帯状に並んだ本発明の構造体はさまざまな立体形状にできることを示す顕微鏡写真である。図9(A)及び(B)は、それぞれ、本発明の発明者の所属する東京大学(University of Tokyo)の頭文字であるU及びTの形状を示す。
【0065】
図9は、本発明の帯状の構造体に細胞が接着した顕微鏡写真で、図10(A)は前記構造体が全て基板に貼り付いている状態を示し、図10(B)、(C)及び(D)は、前記構造体の一端にガラス針を接触させて前記構造体の一端を基板から脱離させると、細胞によって前記構造体が前記一端から順番に折れ畳まれていく様子を示す。このようにして帯状の平面的な構造体から、螺旋又は筒のような中空の立体形状を作ることができる。
【0066】
図10は、本発明の溝状のヒンジ構造を備える構造体に細胞が接着した顕微鏡写真で、図10(a)は前記構造体が全て基板に貼り付いている状態と、本発明の構造体のうち1個の一端にガラス針を接触させている様子を示し、図10(b)及び(c)は、細胞によって前記構造体が前記一端から順番に折れ畳まれてできた筒状の立体構造を示す。
【0067】
図11(a−1)及び(a−2)と、図11(b−1)及び(b−2)と、図11(c−1)及び(c−2)とは、ヒンジ構造で折れ曲がった平面がなす角度をあらかじめ、それぞれ、90°と、135°と、120°とになるように加工された構造体に細胞を接着させて折り畳ませて得られた立体構造の顕微鏡写真である。
【0068】
以上詳しく説明したとおり、本発明のデバイスを用いると、さまざまな立体形状をした微細構造体を作製することができる。本発明のデバイスと、細胞、特に移植患者由来の細胞とを含む移植用器具は、ステント、コイルその他所望の形状をとることができ、しかも、該所望の形状は、患者自身の細胞の力で本発明のデバイスの構造体が折り畳まれるためにできあがるので、生体毒性の問題が起こりにくい。また、本発明の移植用器具は、移植されるときには帯状の構造体として移植できるので、移植するときに応力を加えて自己拡張することを防止しなくてもよい。そのため、移植手術が簡単となり、成功率を上げることができる。
【0069】
さらに、本発明の分析用器具は、細胞や、収縮性の高分子化合物のような生物学的材料が被験物質の作用で収縮すると、本発明のデバイスの構造体が折り畳まれて、その立体形状が大きく変化することを利用する。そのため、非常に微量の被験物質を鋭敏に検出したり、広い濃度範囲の被験物質を正確に測定したりすることができる。
【技術分野】
【0001】
本発明は、生物学的材料によって折り畳み可能な構造体デバイスと、該デバイスの製造方法とに関する。
【背景技術】
【0002】
経皮経管血管形成術その他の低侵襲治療用デバイスとして、MEMS技術その他の微細加工技術を用いた細胞足場が注目される。従来技術で報告された細胞は、MEMS技術を用いて加工したパリレン製ステンシルを用いて、同一の培養容器の基質の細胞接着特性を逐次的に変化させることにより、特定のパターンで複数の細胞タイプの細胞が配置されるように細胞を接着させて混合培養することである(非特許文献1)。また、別のアプローチでは、微細加工された櫛状の構造体を複数用意して、それぞれの櫛状の構造体の表面に異なる細胞タイプの細胞を接着させておいたうえで、両方の構造体の櫛状部分が嵌合させることにより、所定の間隔を置いて複数の細胞タイプの細胞が配置されるように混合培養することである(非特許文献2)。しかし、これらの細胞足場は立体形状ではないため、血管閉塞の治療用デバイスであるステントやコイルのように体内臓器の立体的形態を修復又は補整するために利用することができない。
【0003】
竹内らによって出願された特許文献1には、近接して配置された2個又は3個以上の平面状の細胞足場を跨ぐように細胞を播種することによって、細胞の伸展ないしは収縮によって発生する力によって前記細胞足場が引き起こされて、前記細胞を覆うように配置された、該細胞と、前記細胞足場とからなる立体的な集合体の作製が説明される。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】国際出願第PCT/JP2009/66427号出願明細書
【非特許文献】
【0005】
【非特許文献1】Wright, D.ら、Lab on a Chip,7:1272(2007)
【非特許文献2】Hui, E. E.及びBhatia, S.N.、Proc. Natl. Acad. Sci. U. S. A.,104:5722(2007)
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながらこれらの従来技術では、前記平面的な細胞足場どうしの立体的な位置関係、例えば、隣接する平面的な細胞足場の間の立体角を指定することはできない点が問題である。そこで、単に細胞の伸展ないしは収縮によって発生する力で平面的な細胞足場を立体的に配置させるだけでなく、隣接する平面的な細胞足場の間の位置関係を指定して立体的に配置させる技術を開発する必要がある。
【課題を解決するための手段】
【0007】
本発明は、構造体と、該構造体を遊離可能なように保持する基材とからなるデバイスを提供する。本発明のデバイスにおいて、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、該ヒンジ構造は、生物学的材料が前記ヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋できる寸法を有し、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される。
【0008】
本発明のデバイスにおいて、前記両岸の頂面の少なくとも一部は前記生物学的材料との接着を増強させる処理が施される場合がある。
【0009】
本発明のデバイスにおいて、前記基材は剛性の高い素材でできており、前記構造体は、前記基材との間に設けられた遊離制御剤層基板からによって、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記構造体は応力を加えることによって前記基材から遊離される場合がある。
【0010】
本発明のデバイスにおいて、前記基材は粘着力を備えた弾性の高い素材でできており、前記構造体は、前記粘着力によって、前記デバイスの外表に前記構造体の一部が露出した状態で前記弾性基材の表面に保持され、前記構造体は前記弾性基材に応力を加えることによって該弾性基材から遊離される場合がある。
【0011】
本発明のデバイスにおいて、前記デバイスの外表に露出した前記構造体は帯状で、前記ヒンジ構造は複数本が互いに平行に設けられ、前記構造体に接着した生物学的材料が収縮するとき、前記構造体が中空の立体形状となる場合がある。
【0012】
本発明のデバイスにおいて、前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体の形状となる場合がある。
【0013】
本発明のデバイスにおいて、前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状が少なくとも2個以上前記ヒンジ構造を隔てて隣接する形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体が連続する形状となる場合がある。
【0014】
本発明のデバイスにおいて、前記構造体の少なくとも一部には前記構造体の頂面から底面に達する貫通孔が設けられる場合がある。
【0015】
本発明のデバイスにおいて、前記生物学的材料は複数の種類からなり、前記構造体にはそれぞれの種類の生物学的材料が特異的に前記ヒンジ構造を跨いで接着できる処理が施される場合がある。
【0016】
本発明のデバイスにおいて、前記生物学的材料は、細胞か、収縮可能な高分子化合物かの場合がある。
【0017】
本発明のデバイスにおいて、前記生物学的材料は、動物細胞の場合がある。
【0018】
本発明のデバイスにおいて、前記構造体はポリパラキシリレンでできており、前記生体適合性ポリマー層は、2−メタクリロイルオキシエチルホスホリルコリンの層で、前記生物学的材料との接着を増強させる処理はO2プラズマ照射処理の場合がある。
【0019】
本発明のデバイスにおいて、前記構造体は自己組織的に組み上がる機能を有する場合がある。
【0020】
本発明のデバイスにおいて、前記自己組織的に組み上がる機能は、前記構造体の表面に凹陥部と凸出部とが設けられ、1個の構造体の表面の凹陥部が他の1個の構造体の表面の凸出部と相補的に嵌合することにより達成される場合がある。
【0021】
前記自己組織的に組み上がる機能は、前記構造体の表面に親水性部分及び/又は疎水性部分が設けられ、1個の構造体の表面の親水性部分が他の1個の構造体の表面の親水性部分と接し、及び/又は、1個の構造体の表面の疎水性部分が他の1個の構造体の表面の疎水性部分と接することにより達成されることを特徴とする場合がある。
【0022】
本発明は、本発明のデバイスと、生物学的材料とを含む、生体移植用器具を提供する。
【0023】
本発明の生体移植用器具は、前記デバイスから遊離させた前記構造体を患者の体内に移植し、該患者由来の生物学的材料を前記構造体に接着させて、前記生物学的材料の収縮によって前記構造体が折り畳まれるように用いられる場合がある。
【0024】
本発明は、本発明のデバイスと、生物学的材料とを含む、分析用器具を提供する。
【0025】
本発明は、構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は剛性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法を提供する。本発明のデバイスの製造方法は、前記基材の上に遊離制御剤層を形成するステップと、該遊離制御剤層の上に第1の樹脂層を形成するステップと、第1の樹脂層の上に、前記ヒンジ構造を含む前記構造体の形状に対応するように配置される第2の樹脂層を形成するステップと、第2の樹脂層の上に、第3の樹脂層を形成するステップと、第3の樹脂層の上に、前記ヒンジ構造を含まない前記構造体の形状に対応するように保護層を形成するステップと、該保護層で覆われないで第3の樹脂層が露出する部分について、前記遊離制御剤層と、第1ないし第3の樹脂層とを除去して基材を露出させるステップと、前記露出した基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含む。
【0026】
本発明は、構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は粘着力を備えた弾性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法を提供する。本発明のデバイスの製造方法は、前記ヒンジ構造を含む構造体と基板とが支持部を介して一体となるように成形するステップと、前記基板と一体に成形された構造体を、前記ヒンジ構造が設けられた面が露出するように前記基材に押し付けて、前記構造体を前記基材の表面に圧着させる押圧力により前記支持部を破壊するとともに、前記構造体を前記基材の表面に保持し、前記基板から分離させるステップと、前記基材に保持された前記構造体の上に保護層を形成するステップと、前記基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含む。
【0027】
前記本発明のデバイスの製造方法において、前記構造体を前記基材の表面に圧着させるステップと、前記基板から分離させるステップとは、複数の構造体について別々に実施され、前記複数の構造体のうちの1つが保持された基材に他の構造体が保持された基材を押し付けることにより、前記複数の構造体の1つの表面に前記他の構造体が接着された立体的な形状の構造体が形成されるステップを含む場合がある。
【0028】
前記本発明のデバイスの製造方法において、前記保持させるステップの前に、前記生物学的材料と前記構造体との接着を増強させる処理を施すステップを含む場合がある。
【0029】
本発明は、生体移植用器具の製造方法を提供する。本発明の生体移植用器具の製造方法は、本発明のデバイスと、生物学的材料とを用意するステップと、該デバイスのそれぞれの外表に露出した前記構造体の表面に前記生物学的材料を接着させるステップと、前記生物学的材料が収縮することにより前記構造体を折り畳ませるステップとを含む。
【0030】
本発明は、被験物質と生物学的材料との相互作用を分析する方法を提供する。本発明の被験物質と生物学的材料との相互作用を分析する方法は、デバイスを用意するステップと、該デバイスのそれぞれの外表に露出した前記構造体の表面に生物学的材料を接着させるステップと、前記生物学的材料が接着した構造体に被験物質を曝すステップと、前記被験物質に曝された前記生物学的材料が収縮することによって、前記構造体が折り畳まれるステップと、前記構造体が折り畳まれることによる前記構造体の立体形状の変化を解析するステップとを含む。
【0031】
本発明は、細胞と構造体とからなる集合体の作成方法を提供する。本発明の集合体の作成方法は、本発明のデバイスと、細胞とを用意するステップと、前記細胞の少なくとも1個が、前記デバイスの外表に露出した前記構造体の頂面に設けられた少なくとも1個のヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋するように播種して培養するステップと、培養下で前記細胞が収縮することにより、前記少なくとも1個のヒンジ構造を挟む少なくとも2つの前記構造体の頂面を前記細胞が引き寄せて、前記構造体を折り畳ませるステップとを含み、前記折り畳まれた構造体の表面は、前記細胞を取り囲み、凸多面体か、その一部か、これらの繰り返し構造かとなる。
【0032】
本発明は、複数の構造体と、該構造体を遊離可能なように保持する基材と、生物学的材料とからなるデバイスを提供する。本発明のデバイスにおいて、前記構造体は、前記デバイスの外表に前記複数の構造体の一部が露出した状態で前記基材の表面に保持され、前記生物学的材料は前記複数の構造体に跨って接着し、前記構造体が前記基材から遊離するとき、前記生物学的材料が前記複数の構造体を引き寄せて立体的に配置させ、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される。
【0033】
本発明の複数の構造体と、該構造体を遊離可能なように保持する基材と、生物学的材料とからなるデバイスにおいて、前記生物学的材料は動物細胞の場合がある。
【図面の簡単な説明】
【0034】
【図1】細胞が接着した構造体の製造方法の1つの実施態様を示す模式図。
【図2】細胞が接着した構造体の製造方法の別の実施態様を示す模式図。
【図3】前記別の実施態様の製造方法で製造された構造体が異なる間隔を置いて配置され、その上に3T3細胞が接着した状態を示す光学顕微鏡写真(A)及び(B)と、前記間隔を置いて配置された2個の構造体を跨いで接着する3T3細胞が存在する割合と、前記間隔(μm)との関係を示すグラフ(C)。
【図4】2個の構造体の上の多数の3T3細胞が接着する場合(A)及び(B)と、2個の構造体の上の多数の3T3細胞が接着する場合(C)及び(D)とについて、前記構造体が折り曲げられる前に前記細胞が接着した前記構造体の面が視線方向に垂直となるように撮影された顕微鏡写真(A)及び(C)と、前記構造体が折り曲げられた後に前記細胞が接着した前記構造体の面が視線方向に平行となるように撮影された顕微鏡写真(B)及び(D)と、前記構造体上に接着した3T3細胞の数と、前記構造体の折り曲げられる角度との関係を示すグラフ(E)。
【図5】本発明の1つの実施態様のデバイスの製造方法を示す模式図。
【図6】本発明の構造体の溝の幅及び深さと、該溝の底での前記デバイスの厚さと、折れ曲がる角度との関係式の説明図。
【図7】本発明の貫通孔を有する正12面体を展開した形状に配置して並べられた12個の構造体に細胞が接着して折り畳まれる前(A)と、折り畳まれる途中((B)及び(C))と、完全に折り畳まれて正12面体の形状となった状態(D)との顕微鏡写真。(D)では貫通孔を通ってガラス細管が立体化した前記構造体の内部にアクセスできた。
【図8】図8(A)及び(B)は、それぞれ、本発明の発明者の所属する東京大学(University of Tokyo)の頭文字であるU及びTの形状を示す。
【図9】帯状に並んだ本発明の構造体に細胞が接着した顕微鏡写真で、図9(A)は前記構造体が全て基板に貼り付いている状態を示し、図9(B)、(C)及び(D)は、前記構造体の一端にガラス針を接触させて前記構造体の一端を基板から脱離させると、細胞によって前記構造体が前記一端から順番に折れ畳まれていく様子を示す。
【図10】本発明の溝状のヒンジ構造を備える構造体に細胞が接着した顕微鏡写真で、図10(a)は前記構造体が全て基板に貼り付いている状態と、本発明の構造体のうち1個の一端にガラス針を接触させている様子を示し、図10(b)及び(c)は、細胞によって前記構造体が前記一端から順番に折れ畳まれてできた筒状の立体構造を示す。
【図11】ヒンジ構造で折れ曲がった平面がなす角度をあらかじめ、それぞれ、90°((a−1)及び(a−2))と、135°((b−1)及び(b−2))と、120°((c−1)及び(c−2))とになるように加工された構造体に細胞を接着させて折り畳ませて得られた立体構造の顕微鏡写真。
【発明を実施するための形態】
【0035】
本明細書における生物学的材料とは、生物に由来するいずれかの材料を指し、生物個体、臓器、組織及び細胞と、葉緑体、染色体、分裂装置、色素胞等の細胞内小器官と、ウイルス、DNA複製酵素複合体、転写/RNAプロセッシング複合体、リボソーム、イオンチャンネル、細胞表面レセプター複合体、クラスリン被覆小胞等の分子集合体と、核酸、タンパク質等の生体高分子と、分子の高次構造の変化によって分子が収縮したり、運動したりする全ての高分子化合物とを含むが、これらに限定されない。好ましい生物学的材料は、細胞、特に、固体である基質に接着して伸展したり、運動したりする動物細胞と、アクチン−ミオシン系、ダイニン−チューブリン系を含む、天然及び人工の収縮可能な高分子とである。
【0036】
本発明における生物学的材料の接着とは、固体基質である構造体の表面と当該生物学的材料との接着をいう。前記生物学的材料が、細胞内小器官、分子集合体、生体高分子及び化合物の場合には、静電気的な荷電による吸着を含む、いずれかの共有結合及び/又は非共有結合による構造体への不動化をいう。前記生物学的材料が細胞の場合には、前記いずれかの共有結合及び/又は非共有結合による構造体への不動化のような非生理的現象と、細胞−基質間接着のような細胞の生理現象とを含む。前記細胞が2個または3個以上の場合には、細胞−細胞間接着も含む。
【0037】
本発明において、生物学的材料と構造体との接着を増強させる処理とは、構造体の表面に、コラーゲンの他、フィブロネクチン、ビトロネクチン、ラミニン、ニドジェン、テネイシン、トロンボスポンジン、von Willebrand因子、オステオポンチン、フィブリノーゲン、エラスチン、プロテオグリカン等の細胞と基質との接着に関与することが知られている物質をコーティングする処理をいう。また、構造体の表面に、プラズマ処理、フッ酸処理又は紫外線照射処理を施すことによって、前記構造体を基板から分離させる際に破壊した支持部のうち前記構造体の表面に残った部分を除去すること、及び/又は、前記構造体の表面を清浄にすることも、生物学的材料と構造体との接着を増強させる処理に含まれる。
【0038】
本発明のデバイスは、構造体と、該構造体を遊離可能なように保持する基材とからなる。前記基材は、剛性の高い素材でできている場合がある。本発明に用いることができる剛性の高い素材は、ガラス、シリコン、金属、セラミック、その他の複合材料を含むが、これらに限定されない。剛性の高い素材としては、光透過性が高く、倒立顕微鏡により本発明のデバイス上に播種された細胞を観察できるものが好ましい。
【0039】
本発明のデバイスの基材が剛性の高い素材でできている場合には、本発明の構造体は、前記基材の上に遊離制御剤の層を形成し、該遊離制御剤の層の上に、さらに複数の樹脂層を形成し、所望の形状と、ヒンジ構造とを有するように製造される。好ましい遊離制御剤は、ゼラチンのようにわずかな応力によって容易に剥離することができる物質の他、アルギン酸のようにカルシウムイオンの添加によってゲル化し、アルギン酸リアーゼによって分解される物資と、ポリ(N‐イソプロピルアクリルアミド)(PIPAAm)のように高温ではゲル化するが、低温では溶解する物質とを含むが、これらに限られない。かかる遊離制御剤を用いることによって、本発明の構造体は遊離可能なように基材に保持される。
【0040】
図1に、細胞が接着することによって引き寄せられる構造体が、剛性の高い素材でできている基材の上に設けられる場合の製造方法の例を示す。この例では前記基材はガラス製である。前記基材の上にゼラチン層を形成し、該ゼラチン層の上にポリパラキシリレン(図1(A)ではパリレン(商標)と表記される。)の層を形成する。前記ポリパラキシリレン層の上にアルミニウムを積層して、O2プラズマ処理によるエッチングを行う。該エッチングによって、前記アルミニウム層で保護されないポリパラキシリレン層及びゼラチン層は完全に除去される(図1(B))。これにより、本発明の構造体が前記基材の上に形成される。その後、2−メタクリロイルオキシエチルホスホリルコリンポリマー(MPCポリマー)をスピンコーティングする(図1(C))。それから、アルミニウム層と、その上のMPCポリマー層とを除去すること(リフトオフ)によって除去する(図1(D))。改めて露出されたポリパラキシリレン層の表面にフィブロネクチンをコーティングする(図1(E))。このようにして、前記構造体の表面は細胞との接着が増強されるが、前記基材の表面もともとはO2プラズマ処理により親水化しており、そこに両媒性のMPCポリマーをコーティングしたので、MPCポリマーでコーティングされた表面は疎水性となり、細胞−基質間接着が妨げられる。そのため、以上のとおりの手順で作製されたデバイスに細胞を播種すると、細胞は前記構造体の表面だけに選択的に接着する。そして、細胞の力によって隣接する構造体が基材から引き起こされて、折り畳まれる。
【0041】
本発明のデバイスに含まれる基材は、粘着力を備えた弾性の高い素材でできている場合がある。物理的な原理によって遊離可能なように構造体を保持することができる基材、特に、応力、圧力、振動、超音波、光、電気、熱、静電気等に応答して、粘弾性、表面の親水性、表面張力、表面の平坦性、表面の帯電状態等が変化する物質は、本発明の技術分野の専門家に周知である。本発明の構造体を保持することができ、かつ、応力、圧力、振動、超音波等に応答して前記構造体を遊離することができる基材の好ましい具体例は、シリコンゴム、ポリイミド、ポリエチレンテレフタレート(PET)又はポリジメチルシロキサン(PDMS)を含むが、これらに限られない、粘着力のある弾性基材である。
【0042】
図2に、細胞が接着することによって引き寄せられる構造体が、粘着力を備えた弾性の高い素材でできている基材の上に設けられる場合の製造方法の例を示す。この例では前記基材はポリジメチルシロキサン(PDMS)製である。出発材料は、シリコン・オン・インシュレータ(SOI)ウェーハであった。前記埋め込み酸化物層を構造体の素材とした。デバイスケイ素層は、S1805フォトレジストをマスキング層として用いる誘導結合プラズマ−反応性イオンエッチング法によりエッチングされた。前記フォトレジスト層を除去した後、前記埋め込み酸化物層は、フッ酸によりエッチングされ、構造体の形状が形成された(図2(B))。
【0043】
SiO2層上に残存したデバイスケイ素層は、ICP−RIE法により除去され、SiO2層の下の基板ケイ素層は水酸化テトラメチルアンモニウムで異方性エッチングされた。前記異方性エッチング反応は、基板ケイ素層からSiO2層が完全に分離する直前に停止された。構造体を支持するピラミッド状のケイ素構造が形成された(図2(C))。前記構造体を分離する前に、細胞と構造体との接着を増強させるために、実施例1で説明したコラーゲンの塩酸溶液にウェーハ上の構造体を3時間浸漬した。
【0044】
その後前記構造体は、押印転写法を用いてSOIウェーハから分離され、PDMSの弾性基材の上に粘着力によって保持された。1mm厚のPDMSシートがウェーハ上の構造体の上に戴置され(図2(D))、剥離された(図2(E))。このようにして、前記構造体はその一部が外表に露出した状態で前記弾性基材の表面に保持された(図2(F))。基材のPDMSは疎水性であるが、基材に保持された構造体は前記コラーゲン処理を施されているので、前記基材上に保持された前記構造体に細胞を播種すると、細胞は前記構造体の上に選択的に接着する(図2(G))。前記基材に応力を加えることによって前記構造体は前記基材から遊離する(図2(H))。
【0045】
本発明の生体適合性ポリマーは、生物学的材料を含むデバイスに用いられるときに前記生物学的材料に対して特に有害な影響を及ぼさない高分子化合物をいう。本発明の生体適合性ポリマーは、生物学的材料との非特異性吸着を抑制する場合がある。かかる生体適合性ポリマーが本発明の構造体及び基板の上にコーティングされ、該生体適合性ポリマーの層が形成されるとき、生物学的材料は前記構造体又はマイクロ流路デバイスに固着せず、容易に洗浄除去することができる。生体適合性ポリマーは、生物学的材料との非特異性吸着を抑制する両親媒性ポリマーが好ましく、2−メタクリロイルオキシエチルホスホリルコリン(MPC)ポリマーがより好ましい。また、生物学的材料が細胞外オルガネラ又は生体分子の場合には、ウシ血清アルブミンのようなタンパク質を生体適合性ポリマーとしいて用いることができる。
【0046】
本発明の構造体の表面にはヒンジ構造が少なくとも1個形成される。本発明のヒンジ構造は、前記構造体が折り目に沿って折り畳まれるとき、折り畳まれる部分を連結できるものであればいかなる構造であってもかまわない。好ましいヒンジ構造の1つは、折り目の方向に沿って前記構造体の頂面に設けられる溝である。該溝は、前記頂面の辺縁から出発して相対する辺縁まで達する場合もあるが、前記頂面の一部に設けられる場合もある。別の好ましいヒンジ構造は、折り目の方向に垂直な方向に沿って前記構造体を貫通する複数のスリットである。前記構造体が折り畳まれるとき、前記スリットで区切られた折り目の部分は、前記構造体が折り畳まれる向きと同じ向きに折れ曲がるものと、前記構造体が折り畳まれる向きと反対の向きに折れ曲がるものとが互い違いに並ぶ。
前記スリットの幅は、互い違いに異なる向きに折れ曲がることができればいかなるものであってもよい。前記スリットの幅が前記構造体の折れ目の長さに対して数分の1以上の場合には、前記構造体が折り畳まれるときの反発力が小さいという利点があるのでより好ましい。
【0047】
本発明の器具は、接着させる生物学的材料や、利用目的に応じて、無菌処理を施したり、生体毒性のない素材及び製造方法で製作される。
【0048】
本発明の構造体は、形状又は材料などが特定のものに限定されない。本明細書の実施例の構造体は、折り紙のように折り畳まれて立体形状となるため、平板の形状であることが好ましい。
【0049】
本発明の構造体は、例えば、光リソグラフィ、エッチング等の従来の微細加工技術を組合せて、犠牲層の除去により立体的な構造とすることができる(EE Text センサ・マイクロマシン工学、藤田博之編著、オーム社(2005))。代替策として、図2でも説明される押印転写法(特願2007−10867号明細書及びOnoe, H.ら、Journal of Micromechanics and Microengineering, 17: 1818−1827 (2007))を利用する場合がある。
【0050】
本発明の構造体は、従来の微細加工技術及び/又は前記押印転写法を、単独で、あるいは、組み合わせて作成された立体的な形状を有する鋳型を使って作成される成形品の場合がある。前記成形品は、プラスチック、セラミック及びハイドロゲルと、これらの複合材料とを含むが、これらに限定されない材料を用いて作成される場合がある。
【0051】
本発明の構造体について自己組織的に組み上がるとは、摩擦力、表面張力、疎水結合、磁力、静電気を含むがこれらに限定されない物理的な引力及び/又は斥力か、化学的又は生物学的な結合か、を用いて、メディウム中で構造体がランダムに衝突していくうちに、構造体の集合体が形成され、該集合体においてそれぞれの構造体は予め定められたパターンに従って配置されることをいう。本発明の構造体について自己組織的に組み上がる機能は、例えば、前記構造体の表面に凹陥部と凸出部とが設けられ、1個の構造体の表面の凹陥部が他の1個の構造体の表面の凸出部と相補的に嵌合することにより達成される場合(例えば、Yeh, H. J. J.及びSmith, J. S.、 Ieee Photonics Technology Letters: 6, 706−708 (1994)を参照せよ。)があり、あるいは、前記構造体の表面に親水性部分及び/又は疎水性部分が設けられ、1個の構造体の表面の親水性部分が他の1個の構造体の表面の親水性部分と接し、及び/又は、1個の構造体の表面の疎水性部分が他の1個の構造体の表面の疎水性部分と接することにより達成される場合(例えば、Bowden, N.ら、Langmuir :17, 1757−1765 (2001)を参照せよ。)がある。また、抗原と抗体との反応や、酵素と基質との間又は酵素と阻害剤との間の相互作用や、ポリヒスチジンとニッケルイオンとの間の相互作用等を含むが、これらに限られない、分子識別の特異性を利用した、化学的又は生物学的な結合により達成される場合がある。さらに、これらのいずれかの組合せにより達成される場合がある。
【0052】
折り畳まれる前の平板又はディスク状の形状の構造体は、メディウム中で3次元的に自由に運動できるとき、構造体どうしが自己集合することができない場合がある。かかる場合には、前記メディウム中に、該メディウムに不溶性の液体を添加して、前記メディウムと前記不溶性の液体との間の界面に構造体を浮かべることにより、構造体が2次元的な自由運動しかできないようにすると、集合体の形成を促進できる場合がある。前記メディウムに不溶性の液体は、前記メディウムより比重が大きい液体や、基材との間の表面張力が前記メディウムと基材との表面張力より小さい液体であることが好ましい。
【0053】
集合体を構成する構造体の数や配置パターンを制御して、自己組織的に組み上がるように構造体を設計すると、それぞれの集合体に接着する生物学的材料を特定の組合せだけにすることができる。これによって、折り畳まれた立体形状の構造体において、2種類又は3種類以上の細胞を、構造体の内部又は外部の特定の場所に配置することができる。
【0054】
前記構造体の表面の別の一部と前記基材の表面の一部との特異的な相互作用は、疎水性相互作用及び電磁気学的相互作用の他、生体分子と、該生体分子に対する特異的結合パートナーとの相互作用や、金属イオンと、該金属イオンに特異的なキレート剤との相互作用を含むが、これらに限定されない。前記疎水性相互作用は、前記構造体の表面の別の一部と、前記基材の表面の一部とがともに疎水性処理が施され、表面どうしが直接接触することによって発生する場合がある。代替的には、油滴のような疎水性の液体を介在することによって発生する場合がある。前記疎水性処理は、例えば、自己組織化法のような周知の表面処理技術を用いてアルカンチオールのような疎水性分子を構造体及び基材の前記表面に結合させることによって達成することができる。前記電磁気学的相互作用には、静電気又は表面荷電による引力を利用するものと、磁石による磁界を利用するものと、電界とそれにより誘導された電気双極子モーメントを利用するものとを含むが、これらに限定されない。電界とそれにより誘導された電気双極子モーメントを利用する電磁気学的相互作用には、誘導誘電泳動、静電配向等を含むが、これらに限定されない。前記生体分子と、該生体分子に対する特異的結合パートナーとの相互作用には、糖類とレクチンとの相互作用、抗原と抗原との相互作用、核酸の相補的対合による相互作用とを含むが、これらに限定されない。また、前記構造体と前記基材とが嵌合可能な形状を有することによって、特定の配向で嵌合することによる相互作用や、前記構造体が、前記基材に設けた開口を塞栓する静水圧による相互作用の組み合わせによって前記構造体が前記基材に保持される場合がある。また、以上に列挙される相互作用の2つ以上の組み合わせによって前記構造体が前記基材に保持される場合がある。
【0055】
本発明の細胞と構造体とからなる集合体に用いる構造体は、アクテュエーターを含むか、あるいは、外部の動力源に接続するかによって、1個ずつ、あるいは、2個又は3個以上を同時に、駆動することができる。あるいは、心筋細胞のような形態変化を起こす細胞を含む構造体では、細胞の動きによって前記構造体を駆動することができる。前記アクテュエーターは、周知の微細加工技術又はMEMS技術によって作成することができる。本発明の細胞と構造体とからなる集合体を用いて、1個又は2個以上の細胞の表面の物理的性質を測定することができる。ここで物理的性質とは、弾性、硬度、表面電位及び膜輸送を含むが、これらに限定されない。前記膜輸送に関する物理的性質には、浸透圧、能動輸送、その他の生体膜による物質の移動に関係する性質を含む。かかる細胞表面の物理的性質を測定するときには、前記構造体には物理的性質のセンサー、例えば、変位、速度、力、圧力などの機械量を検出するセンサーや、イオン選択性電極、イオン感応電界トランジスタ(ISFET)などのイオンセンサーを含むことが望ましい。かかる物理的性質のセンサーは周知の微細加工技術によって作成することができる(EE Text センサ・マイクロマシン工学、藤田博之編著、オーム社、2005年を参照せよ。)。さらに、前記構造体及び/又は前記基材は細胞と接触するプリント配線による電極を設けて、前記構造体が前記基材と嵌合するときに外部から電気的に接続して電気刺激を行ったり電位を測定したりする場合がある。また、前記構造体及び/又は前記基材を貫通する細孔であって、細胞膜によって電気的にシールすることができるように細胞より小さな孔径を有する貫通孔を設けて、いわゆるオートパッチ法による電気生理学的な測定を行う場合がある。この場合には、前記構造体が前記基材と嵌合するとき、前記構造体に設けた貫通孔が基材に設けた貫通孔が連通するように配置される場合がある。かかるプリント配線及び貫通孔も周知の微細加工技術又はMEMS技術によって作成することができる。
【0056】
以下に実施例を示すが、これらは実施態様の例示を意図しており本発明の範囲を限定することは意図しない。
【実施例1】
【0057】
1.構造体のヒンジ構造の寸法検討
50×50μm2の表面積と3μmの高さのフィブロネクチンでコーティングされた構造体が、3、5、10、20又は50μmの間隔を置いてMPCポリマーでコーティングされた基材上に配置されたデバイスが、図1で説明される方法に従って製造された。前記デバイスに3T3細胞が4−8×104個/cm2の播種密度で播種され、基質と接着しない細胞が培養開始4時間後に洗浄除去された。その後、24時間後に3T3細胞が隣接した構造体を跨いで増殖するかどうかを観察した。さらに、前記2枚の構造体が3T3細胞に引き起こされてなす角度と、前記構造体2個あたりに存在する細胞の数との関係も調べた。
【0058】
図3は、異なる間隔を置いて配置され、その上に3T3細胞が接着した状態を示す光学顕微鏡写真(A)及び(B)と、前記間隔を置いて配置された2個の構造体を跨いで接着する3T3細胞が存在する割合と、前記間隔(μm)との関係を示すグラフ(C)である。図3(C)から、前記構造体の間隔が10μm以下の場合には全て、2個の構造体を跨いで接着していた。
【0059】
図4は、2個の構造体の上の多数の3T3細胞が接着する場合(A)及び(B)と、2個の構造体の上の多数の3T3細胞が接着する場合(C)及び(D)とについて、前記構造体が折り曲げられる前に前記細胞が接着した前記構造体の面が視線方向に垂直となるように撮影された顕微鏡写真(A)及び(C)と、前記構造体が折り曲げられた後に前記細胞が接着した前記構造体の面が視線方向に平行となるように撮影された顕微鏡写真(B)及び(D)と、前記構造体上に接着した3T3細胞の数と、前記構造体の折り曲げられる角度との関係を示すグラフ(E)である。図4(E)から明らかなように、前記構造体上に接着した3T3細胞の数が増えると、前記構造体の折り曲げられた2つの頂面がなす角度が大きくなった。これらの知見に基づいて、以下のとおり溝状のヒンジ構造を有する構造体の寸法を決定した。
【0060】
図5は、本発明の構造体の溝の幅及び深さと、該溝の底での前記デバイスの厚さと、折れ曲がる角度との関係式の説明図である。図5から明らかなとおり、本発明の構造体の溝の幅w及び深さrと、該溝の底での前記デバイスの厚さtと、折れ曲がる角度θとの間には以下の式1の関係が成立する。
【0061】
w=(r+0.5×t)×θ (式1)
【実施例2】
【0062】
2.本発明のヒンジ構造を備えた構造体を含むデバイスの作製
図6は、本発明の1つの実施態様のデバイスの製造方法を示す模式図である。図6を参照して、本発明のデバイスは以下のとおりの手順で作成された。ガラス基板に2%ゼラチン水溶液を200rpmでスピンコーティングし、その上にポリパラキシリレン層を形成した(図6(A))。SU8樹脂を前記ポリパラキシリレン層の上にコーティングし、所望の配置パターンで、構造体と、該構造体に設けられる溝とが形成されるように遮光スクリーンを使って前記SU8樹脂の光重合を行い、未重合のSU8樹脂を洗い流した(図6(B))。前記SU8樹脂層と、前記ゼラチン層との上にポリパラキシリレン層を形成した(図6(C))。その後、前記ポリパラキシリレン層をアルミニウムでマスキングしてO2プラズマ処理を施し、マスキングされないポリパラキシリレン層及びゼラチン層を除去した(図6(D))。その後、MPCポリマーを基板上にスピンコーティングした(図6(E))。さらに、前記アルミニウム層をテトラメチルアンモニウムハイドロオキサイドを用いて除去し、前記アルミニウム層の上のMPCポリマーをリフトオフによって除去した(図6(F))。
【実施例3】
【0063】
3.さまざまな立体形状に折り畳まれた構造体
図7は、本発明の貫通孔を有する正12面体を展開した形状に配置して並べられた12個の構造体に細胞が接着して折り畳まれる前(A)と、折り畳まれる途中((B)及び(C))と、完全に折り畳まれて正12面体の形状となった状態(D)との顕微鏡写真である。図8(D)では貫通孔を通ってガラス細管が立体化した前記構造体の内部にアクセスできた。このように、本発明のデバイスを用いると、立体的に配置された1個又は2個以上の細胞に外部から電極を刺す等のやり方で細胞内電位その他の細胞生理学的な情報を得ることができる。
【0064】
図8は、帯状に並んだ本発明の構造体はさまざまな立体形状にできることを示す顕微鏡写真である。図9(A)及び(B)は、それぞれ、本発明の発明者の所属する東京大学(University of Tokyo)の頭文字であるU及びTの形状を示す。
【0065】
図9は、本発明の帯状の構造体に細胞が接着した顕微鏡写真で、図10(A)は前記構造体が全て基板に貼り付いている状態を示し、図10(B)、(C)及び(D)は、前記構造体の一端にガラス針を接触させて前記構造体の一端を基板から脱離させると、細胞によって前記構造体が前記一端から順番に折れ畳まれていく様子を示す。このようにして帯状の平面的な構造体から、螺旋又は筒のような中空の立体形状を作ることができる。
【0066】
図10は、本発明の溝状のヒンジ構造を備える構造体に細胞が接着した顕微鏡写真で、図10(a)は前記構造体が全て基板に貼り付いている状態と、本発明の構造体のうち1個の一端にガラス針を接触させている様子を示し、図10(b)及び(c)は、細胞によって前記構造体が前記一端から順番に折れ畳まれてできた筒状の立体構造を示す。
【0067】
図11(a−1)及び(a−2)と、図11(b−1)及び(b−2)と、図11(c−1)及び(c−2)とは、ヒンジ構造で折れ曲がった平面がなす角度をあらかじめ、それぞれ、90°と、135°と、120°とになるように加工された構造体に細胞を接着させて折り畳ませて得られた立体構造の顕微鏡写真である。
【0068】
以上詳しく説明したとおり、本発明のデバイスを用いると、さまざまな立体形状をした微細構造体を作製することができる。本発明のデバイスと、細胞、特に移植患者由来の細胞とを含む移植用器具は、ステント、コイルその他所望の形状をとることができ、しかも、該所望の形状は、患者自身の細胞の力で本発明のデバイスの構造体が折り畳まれるためにできあがるので、生体毒性の問題が起こりにくい。また、本発明の移植用器具は、移植されるときには帯状の構造体として移植できるので、移植するときに応力を加えて自己拡張することを防止しなくてもよい。そのため、移植手術が簡単となり、成功率を上げることができる。
【0069】
さらに、本発明の分析用器具は、細胞や、収縮性の高分子化合物のような生物学的材料が被験物質の作用で収縮すると、本発明のデバイスの構造体が折り畳まれて、その立体形状が大きく変化することを利用する。そのため、非常に微量の被験物質を鋭敏に検出したり、広い濃度範囲の被験物質を正確に測定したりすることができる。
【特許請求の範囲】
【請求項1】
構造体と、該構造体を遊離可能なように保持する基材とからなるデバイスであって、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、該ヒンジ構造は、生物学的材料が前記ヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋できる寸法を有し、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成されることを特徴とする、デバイス。
【請求項2】
前記両岸の頂面の少なくとも一部は前記生物学的材料との接着を増強させる処理が施されることを特徴とする、請求項1に記載のデバイス。
【請求項3】
前記基材は剛性の高い素材でできており、前記構造体は、前記基材との間に設けられた遊離制御剤層によって、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記構造体は応力を加えることによって前記基材から遊離されることを特徴とする、請求項1又は2に記載のデバイス。
【請求項4】
前記基材は粘着力を備えた弾性の高い素材でできており、前記構造体は、前記粘着力によって、前記デバイスの外表に前記構造体の一部が露出した状態で前記弾性基材の表面に保持され、前記構造体は前記弾性基材に応力を加えることによって該弾性基材から遊離されることを特徴とする、請求項1又は2に記載のデバイス。
【請求項5】
前記デバイスの外表に露出した前記構造体は帯状で、前記ヒンジ構造は複数本が互いに平行に設けられ、前記構造体に接着した生物学的材料が収縮するとき、前記構造体が中空の立体形状となることを特徴とする、請求項1ないし4のいずれか1つに記載のデバイス。
【請求項6】
前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体の形状となることを特徴とする、請求項1ないし4のいずれか1つに記載のデバイス。
【請求項7】
前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状が少なくとも2個以上前記ヒンジ構造を隔てて隣接する形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体が連続する形状となることを特徴とする、請求項1ないし4のいずれか1つに記載のデバイス。
【請求項8】
前記構造体の少なくとも一部には前記構造体の頂面から底面に達する貫通孔が設けられることを特徴とする、請求項5ないし7のいずれか1つに記載のデバイス。
【請求項9】
前記生物学的材料は複数の種類からなり、前記構造体にはそれぞれの種類の生物学的材料が特異的に前記ヒンジ構造を跨いで接着できる処理が施されることを特徴とする、請求項1ないし8のいずれか1つに記載のデバイス。
【請求項10】
前記生物学的材料は、細胞か、収縮可能な高分子化合物かであることを特徴とする、請求項1ないし9のいずれか1つに記載のデバイス。
【請求項11】
前記生物学的材料は動物細胞であることを特徴とする、請求項10に記載のデバイス。
【請求項12】
前記構造体は自己組織的に組み上がる機能を有することを特徴とする、請求項1ないし11のいずれか1つに記載のデバイス。
【請求項13】
前記自己組織的に組み上がる機能は、前記構造体の表面に凹陥部と凸出部とが設けられ、1個の構造体の表面の凹陥部が他の1個の構造体の表面の凸出部と相補的に嵌合することにより達成されることを特徴とする、請求項12に記載のデバイス。
【請求項14】
前記自己組織的に組み上がる機能は、前記構造体の表面に親水性部分及び/又は疎水性部分が設けられ、1個の構造体の表面の親水性部分が他の1個の構造体の表面の親水性部分と接し、及び/又は、1個の構造体の表面の疎水性部分が他の1個の構造体の表面の疎水性部分と接することにより達成されることを特徴とする、請求項12又は13に記載のデバイス。
【請求項15】
請求項1ないし14のいずれか1つに記載のデバイスと、生物学的材料とを含むことを特徴とする、生体移植用器具。
【請求項16】
前記デバイスから遊離させた前記構造体を患者の体内に移植し、該患者由来の生物学的材料を前記構造体に接着させて、前記生物学的材料の収縮によって前記構造体が折り畳まれるように用いられることを特徴とする、請求項15に記載の生体移植用器具。
【請求項17】
請求項1ないし14のいずれか1つに記載のデバイスと、生物学的材料とを含むことを特徴とする、分析用器具。
【請求項18】
構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は剛性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法であって、
前記基材の上に遊離制御剤層を形成するステップと、
該遊離制御剤層の上に第1の樹脂層を形成するステップと、
第1の樹脂層の上に、前記ヒンジ構造を含む前記構造体の形状に対応するように配置される第2の樹脂層を形成するステップと、
第2の樹脂層の上に、第3の樹脂層を形成するステップと、
第3の樹脂層の上に、前記ヒンジ構造を含まない前記構造体の形状に対応するように保護層を形成するステップと、
該保護層で覆われないで第3の樹脂層が露出する部分について、前記遊離制御剤層と、第1ないし第3の樹脂層とを除去して基材を露出させるステップと、
前記露出した基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、
前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含むことを特徴とする、前記デバイスの製造方法。
【請求項19】
構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は粘着力を備えた弾性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法であって、
前記ヒンジ構造を含む構造体と基板とが支持部を介して一体となるように成形するステップと、
前記基板と一体に成形された構造体を、前記ヒンジ構造が設けられた面が露出するように前記基材に押し付けて、前記構造体を前記基材の表面に圧着させる押圧力により前記支持部を破壊するとともに、前記構造体を前記基材の表面に保持し、前記基板から分離させるステップと、
前記基材に保持された前記構造体の上に保護層を形成するステップと、
前記基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、
前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含むことを特徴とする、前記デバイスの製造方法。
【請求項20】
前記構造体を前記基材の表面に圧着させるステップと、前記基板から分離させるステップとは、複数の構造体について別々に実施され、
前記複数の構造体のうちの1つが保持された基材に他の構造体が保持された基材を押し付けることにより、前記複数の構造体の1つの表面に前記他の構造体が接着された立体的な形状の構造体が形成されるステップを含むことを特徴とする、請求項19に記載の製造方法。
【請求項21】
前記保持させるステップの前に、前記生物学的材料と前記構造体との接着を増強させる処理を施すステップを含むことを特徴とする、請求項18ないし20のいずれか1つに記載の製造方法。
【請求項22】
請求項1ないし14のいずれか1つに記載のデバイスと、生物学的材料とを用意するステップと、
該デバイスのそれぞれの外表に露出した前記構造体の表面に前記生物学的材料を接着させるステップと、
前記生物学的材料が収縮することにより前記構造体を折り畳ませるステップとを含むことを特徴とする、生体移植用器具の製造方法。
【請求項23】
請求項1ないし14のいずれか1つに記載のデバイスを用意するステップと、
該デバイスのそれぞれの外表に露出した前記構造体の表面に生物学的材料を接着させるステップと、
前記生物学的材料が接着した構造体に被験物質を曝すステップと、
前記被験物質に曝された前記生物学的材料が収縮することによって、前記構造体が折り畳まれるステップと、
前記構造体が折り畳まれることによる前記構造体の立体形状の変化を解析するステップとを含むことを特徴とする、被験物質と生物学的材料との相互作用を分析する方法。
【請求項24】
複数の構造体と、該構造体を遊離可能なように保持する基材と、生物学的材料とからなるデバイスであって、前記構造体は、前記デバイスの外表に前記複数の構造体の一部が露出した状態で前記基材の表面に保持され、前記生物学的材料は前記複数の構造体に跨って接着し、前記構造体が前記基材から遊離するとき、前記生物学的材料が前記複数の構造体を引き寄せて立体的に配置させ、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成されることを特徴とする、デバイス。
【請求項25】
前記生物学的材料は動物細胞であることを特徴とする、請求項24に記載のデバイス。
【請求項1】
構造体と、該構造体を遊離可能なように保持する基材とからなるデバイスであって、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、該ヒンジ構造は、生物学的材料が前記ヒンジ構造を跨いで前記ヒンジ構造の両岸を架橋できる寸法を有し、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成されることを特徴とする、デバイス。
【請求項2】
前記両岸の頂面の少なくとも一部は前記生物学的材料との接着を増強させる処理が施されることを特徴とする、請求項1に記載のデバイス。
【請求項3】
前記基材は剛性の高い素材でできており、前記構造体は、前記基材との間に設けられた遊離制御剤層によって、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記構造体は応力を加えることによって前記基材から遊離されることを特徴とする、請求項1又は2に記載のデバイス。
【請求項4】
前記基材は粘着力を備えた弾性の高い素材でできており、前記構造体は、前記粘着力によって、前記デバイスの外表に前記構造体の一部が露出した状態で前記弾性基材の表面に保持され、前記構造体は前記弾性基材に応力を加えることによって該弾性基材から遊離されることを特徴とする、請求項1又は2に記載のデバイス。
【請求項5】
前記デバイスの外表に露出した前記構造体は帯状で、前記ヒンジ構造は複数本が互いに平行に設けられ、前記構造体に接着した生物学的材料が収縮するとき、前記構造体が中空の立体形状となることを特徴とする、請求項1ないし4のいずれか1つに記載のデバイス。
【請求項6】
前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体の形状となることを特徴とする、請求項1ないし4のいずれか1つに記載のデバイス。
【請求項7】
前記デバイスの外表に露出した前記構造体は、前記ヒンジ構造を折り目として多面体を展開した形状が少なくとも2個以上前記ヒンジ構造を隔てて隣接する形状であり、前記構造体に接着した生物学的材料が収縮するとき、前記構造体は多面体が連続する形状となることを特徴とする、請求項1ないし4のいずれか1つに記載のデバイス。
【請求項8】
前記構造体の少なくとも一部には前記構造体の頂面から底面に達する貫通孔が設けられることを特徴とする、請求項5ないし7のいずれか1つに記載のデバイス。
【請求項9】
前記生物学的材料は複数の種類からなり、前記構造体にはそれぞれの種類の生物学的材料が特異的に前記ヒンジ構造を跨いで接着できる処理が施されることを特徴とする、請求項1ないし8のいずれか1つに記載のデバイス。
【請求項10】
前記生物学的材料は、細胞か、収縮可能な高分子化合物かであることを特徴とする、請求項1ないし9のいずれか1つに記載のデバイス。
【請求項11】
前記生物学的材料は動物細胞であることを特徴とする、請求項10に記載のデバイス。
【請求項12】
前記構造体は自己組織的に組み上がる機能を有することを特徴とする、請求項1ないし11のいずれか1つに記載のデバイス。
【請求項13】
前記自己組織的に組み上がる機能は、前記構造体の表面に凹陥部と凸出部とが設けられ、1個の構造体の表面の凹陥部が他の1個の構造体の表面の凸出部と相補的に嵌合することにより達成されることを特徴とする、請求項12に記載のデバイス。
【請求項14】
前記自己組織的に組み上がる機能は、前記構造体の表面に親水性部分及び/又は疎水性部分が設けられ、1個の構造体の表面の親水性部分が他の1個の構造体の表面の親水性部分と接し、及び/又は、1個の構造体の表面の疎水性部分が他の1個の構造体の表面の疎水性部分と接することにより達成されることを特徴とする、請求項12又は13に記載のデバイス。
【請求項15】
請求項1ないし14のいずれか1つに記載のデバイスと、生物学的材料とを含むことを特徴とする、生体移植用器具。
【請求項16】
前記デバイスから遊離させた前記構造体を患者の体内に移植し、該患者由来の生物学的材料を前記構造体に接着させて、前記生物学的材料の収縮によって前記構造体が折り畳まれるように用いられることを特徴とする、請求項15に記載の生体移植用器具。
【請求項17】
請求項1ないし14のいずれか1つに記載のデバイスと、生物学的材料とを含むことを特徴とする、分析用器具。
【請求項18】
構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は剛性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法であって、
前記基材の上に遊離制御剤層を形成するステップと、
該遊離制御剤層の上に第1の樹脂層を形成するステップと、
第1の樹脂層の上に、前記ヒンジ構造を含む前記構造体の形状に対応するように配置される第2の樹脂層を形成するステップと、
第2の樹脂層の上に、第3の樹脂層を形成するステップと、
第3の樹脂層の上に、前記ヒンジ構造を含まない前記構造体の形状に対応するように保護層を形成するステップと、
該保護層で覆われないで第3の樹脂層が露出する部分について、前記遊離制御剤層と、第1ないし第3の樹脂層とを除去して基材を露出させるステップと、
前記露出した基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、
前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含むことを特徴とする、前記デバイスの製造方法。
【請求項19】
構造体と、該構造体を遊離可能なように保持する基材とからなり、前記構造体は、前記デバイスの外表に前記構造体の一部が露出した状態で前記基材の表面に保持され、前記デバイスの外表に露出した前記構造体の頂面には少なくとも1個のヒンジ構造が設けられ、前記基材は粘着力を備えた弾性の高い素材でできており、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成される、デバイスの製造方法であって、
前記ヒンジ構造を含む構造体と基板とが支持部を介して一体となるように成形するステップと、
前記基板と一体に成形された構造体を、前記ヒンジ構造が設けられた面が露出するように前記基材に押し付けて、前記構造体を前記基材の表面に圧着させる押圧力により前記支持部を破壊するとともに、前記構造体を前記基材の表面に保持し、前記基板から分離させるステップと、
前記基材に保持された前記構造体の上に保護層を形成するステップと、
前記基材の上と、前記保護層の上とに、生体適合性ポリマー層を形成するステップと、
前記保護層と、該保護層の上に形成された生体適合性ポリマー層とを除去するステップとを含むことを特徴とする、前記デバイスの製造方法。
【請求項20】
前記構造体を前記基材の表面に圧着させるステップと、前記基板から分離させるステップとは、複数の構造体について別々に実施され、
前記複数の構造体のうちの1つが保持された基材に他の構造体が保持された基材を押し付けることにより、前記複数の構造体の1つの表面に前記他の構造体が接着された立体的な形状の構造体が形成されるステップを含むことを特徴とする、請求項19に記載の製造方法。
【請求項21】
前記保持させるステップの前に、前記生物学的材料と前記構造体との接着を増強させる処理を施すステップを含むことを特徴とする、請求項18ないし20のいずれか1つに記載の製造方法。
【請求項22】
請求項1ないし14のいずれか1つに記載のデバイスと、生物学的材料とを用意するステップと、
該デバイスのそれぞれの外表に露出した前記構造体の表面に前記生物学的材料を接着させるステップと、
前記生物学的材料が収縮することにより前記構造体を折り畳ませるステップとを含むことを特徴とする、生体移植用器具の製造方法。
【請求項23】
請求項1ないし14のいずれか1つに記載のデバイスを用意するステップと、
該デバイスのそれぞれの外表に露出した前記構造体の表面に生物学的材料を接着させるステップと、
前記生物学的材料が接着した構造体に被験物質を曝すステップと、
前記被験物質に曝された前記生物学的材料が収縮することによって、前記構造体が折り畳まれるステップと、
前記構造体が折り畳まれることによる前記構造体の立体形状の変化を解析するステップとを含むことを特徴とする、被験物質と生物学的材料との相互作用を分析する方法。
【請求項24】
複数の構造体と、該構造体を遊離可能なように保持する基材と、生物学的材料とからなるデバイスであって、前記構造体は、前記デバイスの外表に前記複数の構造体の一部が露出した状態で前記基材の表面に保持され、前記生物学的材料は前記複数の構造体に跨って接着し、前記構造体が前記基材から遊離するとき、前記生物学的材料が前記複数の構造体を引き寄せて立体的に配置させ、前記デバイスの外表に露出した前記基材の表面は生体適合性ポリマー層が形成されることを特徴とする、デバイス。
【請求項25】
前記生物学的材料は動物細胞であることを特徴とする、請求項24に記載のデバイス。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2013−13328(P2013−13328A)
【公開日】平成25年1月24日(2013.1.24)
【国際特許分類】
【出願番号】特願2009−251515(P2009−251515)
【出願日】平成21年10月30日(2009.10.30)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【Fターム(参考)】
【公開日】平成25年1月24日(2013.1.24)
【国際特許分類】
【出願日】平成21年10月30日(2009.10.30)
【出願人】(504137912)国立大学法人 東京大学 (1,942)
【Fターム(参考)】
[ Back to top ]

