排ガス中のハロゲン化合物及び硫黄酸化物の分析方法と、排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置と、排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット
【課題】ゴミ焼却炉などの化学反応装置から発生する排ガス中のハロゲン化合物及び硫黄酸化物を、1回のサンプリングと1回の分析で同時に精度良く測定可能な分析方法及び分析用前処理装置や分析用前処理キットを提供すること。
【解決手段】化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に吸収させ、陽イオン交換樹脂を加えてナトリウムイオンを吸着・除去した後、吸収液中に二酸化炭素のパージ用ガスを通気して二酸化炭素を除去した後、吸収液中のハロゲン化物イオン及び硫酸イオンをイオンクロマトグラフ法により測定する。IC法で分析するときの妨害原因となるアルカリ成分と炭酸イオンを除去することで、ハロゲン化合物と硫黄酸化物を同時に精度良く分析できる。また、排ガス吸収液中にオゾンを流して排ガス中のSOxをすべて硫酸イオンに変えると、正確なSOx濃度の測定・分析が可能となる。
【解決手段】化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に吸収させ、陽イオン交換樹脂を加えてナトリウムイオンを吸着・除去した後、吸収液中に二酸化炭素のパージ用ガスを通気して二酸化炭素を除去した後、吸収液中のハロゲン化物イオン及び硫酸イオンをイオンクロマトグラフ法により測定する。IC法で分析するときの妨害原因となるアルカリ成分と炭酸イオンを除去することで、ハロゲン化合物と硫黄酸化物を同時に精度良く分析できる。また、排ガス吸収液中にオゾンを流して排ガス中のSOxをすべて硫酸イオンに変えると、正確なSOx濃度の測定・分析が可能となる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、化学反応装置から発生する排ガス中のフッ素、塩化水素、臭素などのハロゲン化合物と硫黄酸化物を簡便、同時に分析可能な方法と分析用前処理装置、及び分析用前処理キットに関するものである。
【背景技術】
【0002】
例えば、都市ゴミや産業廃棄物などを燃焼した際に発生する排ガス中には、有害物質として、硫黄酸化物の他にも微量のハロゲン化合物が含まれており、これらハロゲン化合物から生成される様々な大気汚染物質の発生が問題となっている。
【0003】
一方、都市ゴミや産業廃棄物などの焼却炉等の固定発生源から発生する有毒物質の測定法として、日本工業規格(JIS)では排ガス分析方法が規定されている。この排ガス分析方法では測定対象成分が約25種類に分類され、各測定対象成分毎に測定法が定められている。そして排ガス中のハロゲン化合物のうち、フッ化水素(HF)、塩化水素(HCl)、臭化水素(HBr)及び硫黄酸化物(SOx)の分析方法についても定められているが、この方法では、これらの成分は排ガスを各成分ごとに別々に採取(サンプリング)し、別々に測定する必要がある。
【0004】
JISで規格されている排ガス中のハロゲン化合物の分析方法として、HFについてはランタン−アリザリンコンプレキソン吸光光度法(LAC法)やイオン電極法などの分析方法が採用されており、HBrについてはチオシアン酸水銀(II)吸光光度法、チオ硫酸滴定法が採用されている。
【0005】
近年、排ガスの規制強化が進み、脱硫処理や排ガス処理技術の向上もあって、これらの有害物質は低濃度化の傾向にある。したがって、上記イオン電極法や滴定法などの分析方法では、低濃度のHFやHBrを精度良く分析することは難しい。一方、このような低濃度のハロゲン化合物を測定、分析する方法としては、例えばイオンクロマトグラフ法(以下、IC法という場合がある)がある。
【0006】
そして、フッ素を測定、分析する技術として、下記特許文献1によれば、フッ素樹脂またはフッ素樹脂を含む化合物を炭酸ナトリウムなどのアルカリ塩に吸収させ、水に溶解させた後、陽イオン交換樹脂によりアルカリを除き、残った水溶液中のフッ化物イオンをIC法により測定する構成が採用されている。また、HBrを測定、分析する技術としては、発光管をアルカリ溶液中で破砕し、破砕により発生した破砕物をアルカリ溶液から除去した後、IC法により、アルカリ溶液に含まれるハロゲンを定量する構成が採用されている。しかし、これら特許文献等の構成は、対象とするハロゲン化合物を個々に測定する技術であり、また対象とする測定試料も限られ微量であるため、これらの方法を様々な物質が混在する都市ゴミや産業廃棄物などを燃焼した際に発生する排ガス中のハロゲン化合物や硫黄酸化物の分析に適用することは難しい。
【0007】
そして、現在のJISによる排ガス分析方法では、上述したように各成分ごとに別々にサンプリングし、別々に分析する必要があるが、これら排ガス中のハロゲン化合物やSOxを1回のサンプリングと1回の分析で測定できれば、測定時間の短縮と分析コストが低減でき、簡便で望ましい。
【0008】
一方、下記非特許文献1において、SOxとHClを分析する方法として採用されているIC法は、低濃度の陰イオン成分を短時間で同時分析できるという特徴がある。この方法は、0.3%又は0.03%の過酸化水素(H2O2)水で排ガスを捕集した後、IC法で塩化物イオンと硫酸イオンを測定し、排ガス中のSOxとHClを分析する方法である。
【0009】
そして、有機化合物中の4種のハロゲン(フッ素、塩素、ヨウ素、臭素)と硫黄を同時に分析する方法として、有機化合物を燃焼して過酸化水素水又は飽水ヒドラジンを含む希水酸化ナトリウム水溶液(以下、NaOH溶液という場合がある)に吸収させて試料液としてイオンクロマトグラフに取り込み、IC法により同時に分析する方法が提案されている(下記特許文献3)。
【特許文献1】特開2002−214217号公報
【特許文献2】特開2002−289100号公報
【特許文献3】特開平8−262000号公報
【非特許文献1】日本工業規格(JIS) K 0103 排ガス中の硫黄酸化物分析方法(2005)
【発明の開示】
【発明が解決しようとする課題】
【0010】
上記特許文献3による方法は、過酸化水素水又は飽水ヒドラジンを含む希水酸化ナトリウム水溶液を吸収液として使用している。そして、この測定方法は、医薬、農薬などの分野における有機化合物中のハロゲン及び硫黄を測定対象としており、試料の量も1〜数mgと少ない。したがって、試料を燃焼した際に発生する二酸化炭素やハロゲン化合物の量も少ないため、希水酸化ナトリウム水溶液を吸収液として使用可能である。
【0011】
しかし、都市ゴミや産業廃棄物などを燃焼した際に発生する排ガス中には、ハロゲン化合物の他に10数%の高濃度の二酸化炭素が含まれるため、排ガスの吸収液が希アルカリ溶液であると、排ガス中の酸性成分が十分に吸収されず、また吸収液の酸性度も高くなり、一旦吸収されたハロゲン化合物が吸収液から揮発してしまう。したがって、排ガス中のハロゲン化合物を正確に測定ができないおそれがある。
【0012】
一方、上記JISで定められた塩化水素と硫黄酸化物のIC法による分析方法においても(非特許文献1)、排ガスの吸収液として、0.3%のH2O2水溶液を用いている。H2O2水溶液を用いた場合は、塩化水素と硫黄酸化物の測定は、それぞれ塩素イオン(Cl-)、硫酸イオン(SO42-)として精度良く分析可能である。しかし、この方法で他のハロゲン成分(フッ素、臭素)と塩化水素の同時測定を試みても、0.3%のH2O2水溶液を用いたときのHFとHBrの捕集率が明らかでないこと、又、二酸化炭素を含む排ガスを吸収したときにフッ化水素と臭化水素が吸収液中から揮散するおそれがあるため、これら低濃度のハロゲン成分を正確に同時測定することは難しい。したがって、排ガスの吸収液として、何を使用すれば良いのかという問題がある。
【0013】
しかし、排ガス規制が進む中で、上記イオン電極法や滴定法などでは測定不能な排ガス中の低濃度のハロゲンを測定できると共に、排ガス中のハロゲン化合物と硫黄酸化物などの酸性成分を同時に高精度で測定、分析できる簡便な測定方法や測定装置等が求められている。
【0014】
本発明の課題は、上記問題点を解決することであり、具体的にはゴミ焼却炉などの化学反応装置から発生する排ガス中の低濃度のハロゲン化合物及び硫黄酸化物などの酸性成分を、1回のサンプリングで同時に精度良く測定可能な分析方法を提供することである。更にこのような分析方法にかかる前処理を簡便、容易、短時間で可能な分析用前処理装置や分析用前処理キットを提供することである。
【課題を解決するための手段】
【0015】
本発明は、以下のような構成を採用することにより達成できる。
請求項1記載の発明は、化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に吸収させた後、該吸収液の一定量に陽イオン交換樹脂を加えてナトリウムイオンを陽イオン交換樹脂により吸着・除去し、前記吸収液中の二酸化炭素のパージ用ガスを前記陽イオン交換樹脂を加えた吸収液中に通気して吸収液中の炭酸イオンを二酸化炭素として除去し、次いで前記吸収液中のハロゲン化物イオン及び硫酸イオンをイオンクロマトグラフ法により測定する排ガス中のハロゲン化合物及び硫黄酸化物の分析方法である。
【0016】
請求項2記載の発明は、前記二酸化炭素のパージ用ガスは、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスである請求項1記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法である。
【0017】
請求項3記載の発明は、前記二酸化炭素のパージ用ガスと共に又は別に吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記吸収液中に通気する請求項1又は2記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法である。
【0018】
請求項4記載の発明は、化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に通じて吸収させた吸収液と陽イオン交換樹脂を接触させることにより前記吸収液中のナトリウムイオンを吸着・除去し、吸収液中の二酸化炭素のパージ用ガスを前記吸収液中に通じて吸収液中の二酸化炭素を除去する中和脱ガス器と、前記二酸化炭素のパージ用ガスを前記中和脱ガス器内の吸収液中に通気する通気手段と、該通気手段により通気されるパージ用ガスにより前記吸収液から発生する二酸化炭素を排気する排気手段とを設けた排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0019】
請求項5記載の発明は、更に、前記二酸化炭素のパージ用ガスを洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去するガス洗浄装置を設けた請求項4記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0020】
請求項6記載の発明は、更に前記吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記二酸化炭素のパージ用ガスと共に又は別に前記中和脱ガス器内の吸収液に通気するためのオゾン通気手段を設けた請求項4又は5記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0021】
請求項7記載の発明は、イオンクロマトグラフ法による分析用の前処理装置である請求項4ないし6のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0022】
請求項8記載の発明は、ナトリウムイオンを吸着・除去する陽イオン交換樹脂を密封した押圧力で破壊可能な密閉容器と、該密閉容器とハロゲン化合物及び硫黄酸化物を含む排ガスを吸収した水酸化ナトリウム水溶液とを収納可能で、キャップにより密封可能な開口部を有する吸収容器とを一体化した構造である排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0023】
請求項9記載の発明は、前記排ガスを吸収した水酸化ナトリウム水溶液の吸収液中の二酸化炭素を除去するためのパージ用ガスを通気する通気口を有する請求項8記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0024】
請求項10記載の発明は、前記破壊可能な密閉容器はガラス製であり、前記吸収容器は軟質プラスチック製である請求項8又は9記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0025】
請求項11記載の発明は、イオンクロマトグラフ法による分析用の前処理キットである請求項8ないし10のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0026】
(作用)
上記非特許文献1において、SOxとHClを分析する方法として採用されているIC法は、低濃度の陰イオン成分を短時間で同時分析できるという特徴がある。本発明者らは、このような特徴のあるIC法により、SOxやHClのみならず、HFやHBrも同時に精度良く分析できる方法やこのような方法の分析用前処理装置、また、分析用前処理キットなどについて鋭意研究を重ね、以下のことを見出した。
【0027】
上記のように、非特許文献1におけるSOxとHClのIC法による分析方法では、吸収液としてH2O2水溶液を用いているが、この吸収液を用いた場合は、フッ素化合物と臭素化合物の捕集率が明らかでない。又、排ガス中の二酸化炭素を吸収することによる吸収液の液性の変化から、吸収液中の塩化物イオンとフッ化物イオンと臭化物イオンを精度良く測定することは難しい。一方、JISで定められた排ガス中のハロゲン化合物(HF、HBr、HCl)の測定は、排ガスを上記特許文献等よりも比較的高濃度の0.1M(mol/L)水酸化ナトリウム水溶液に吸収させた後、ランタン−アリザリンコンプレキソン吸光光度法(LAC法)、チオシアン酸水銀(II)吸光光度法、チオ硫酸滴定法や硝酸銀滴定法、イオン電極法などで分析する方法である(JIS K 0105(HF)、JIS K 0085(HBr)、JIS K 0107(HCl))。
【0028】
そこで、上記方法が排ガス吸収液として0.1M水酸化ナトリウム水溶液を使用することが共通していることに本発明者らは着目した。すなわち排ガス中には二酸化炭素が多く含まれるため、比較的アルカリの濃度が濃い吸収液が適している、またハロゲンガスの吸収液として酸性ガスを吸収できるという理由で採用されている0.1M水酸化ナトリウム水溶液に着目して、当該吸収液を用いて、他のハロゲン成分を捕集すれば、IC法でも測定できるのではと考え、本発明を完成させるに至った。
【0029】
しかし、IC法では、通常、数mmolの炭酸ナトリウムと炭酸水素ナトリウム溶液を溶離液として用いるために、例えば、水酸化ナトリウム水溶液を吸収液として用いた場合に、アルカリ濃度が比較的高い場合は吸収液を分析すると、水酸化ナトリウムに起因するウォーターディップが大きくなる。また、排ガス中の二酸化炭素が吸収液に捕集され、その影響を受けて、クロマトグラム上のF-及びCl-のピークと重なってF-とCl-の分離性が悪いという問題がある。
【0030】
すなわち、排ガスの吸収液に、例えば0.1Mなどの比較的高濃度の水酸化ナトリウム水溶液を使用したときの問題点として、(1)溶離液は数mMの炭酸塩溶液に対して吸収液のアルカリ濃度(100mM)が高いため、ウォーターディップが大きくなり、F-とCl-の測定を妨害する、(2)排ガス中の二酸化炭素(CO2)が同時に捕集されると、クロマトグラム上のF-及びCl-のピークと重なり分離性が悪いなどの問題がある。
【0031】
しかし、本発明によれば、排ガス中のハロゲン化合物及びSOxをNaOH溶液に吸収させた後、IC法で分析するときの妨害原因となるアルカリ成分(Na+)と炭酸イオン(CO32-)を除去して陰イオン(F-、Cl-、Br-、SO42-)を精度よく分析できるように改良したので、排ガス中のハロゲン化合物(HF、HCl、HBr)と硫黄酸化物(SOx)を同時に分析できる。
【0032】
すなわち、請求項1記載の発明によれば、排ガスを吸収した吸収液中に陽イオン交換樹脂を加えることで、ウォーターディップの原因であるナトリウムイオンを陽イオン交換樹脂により吸着・除去できる。更に、パージ用ガスを吸収液中に通気して吸収液中の二酸化炭素を除去することで、IC法におけるクロマトグラム上のF-及びCl-のピークの分離性が良くなる。なお、「ガス」とは、吸収液中の二酸化炭素を追い出すためのパージ用ガスを意味する。
【0033】
また、請求項2記載の発明によれば、請求項1記載の発明の上記作用に加えて、パージ用ガスが清浄なガスではなくても、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスをパージ用ガスとして用いることで、例えばIC法における分析阻害成分であるガス中の酸性成分や汚染成分を除去して、これら酸性成分や汚染成分による吸収液のコンタミネーションを防いで、吸収液中の二酸化炭素を除去できる。したがって、更に、クロマトグラム上のF-及びCl-のピークの分離性が良くなる。
【0034】
一方、排ガス中のSOxは、水酸化ナトリウム水溶液に吸収される際の酸化が不十分であると、不安定な亜硫酸イオンで存在する場合がある。しかし、請求項3記載の発明によれば、請求項1又は2記載の発明の上記作用に加えて、吸収液中の亜硫酸イオン(SO32-)を硫酸イオン(SO42-)に酸化させるためのオゾンを吸収液中に通気することで、排ガス中のSOxをすべて硫酸イオンに変えることができる。
【0035】
また、排ガス吸収液中にナトリウムイオンや二酸化炭素を含み、これらの成分が分析の妨害原因となる場合の種々の分析法の前処理を簡便、容易、短時間に行うことができれば、測定、分析に要する時間も節約できる。
【0036】
請求項4記載の発明によれば、装置をセッティングするだけで排ガス吸収液中のナトリウムイオンや二酸化炭素の除去操作の一連の前処理操作を行うことができる。
請求項5記載の発明によれば、請求項4記載の発明の上記作用に加えて、装置をセッティングするだけで、清浄なガスではないパージ用ガスから排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去でき、簡便、容易にパージ用ガスの洗浄を行うことができる。
【0037】
請求項6記載の発明によれば、請求項4又は5記載の発明の上記作用に加えて、排ガス吸収液中に亜硫酸イオン(SO32-)が存在する場合に、排ガス中のSOxをすべて硫酸イオンに酸化させるための操作を、装置をセッティングするだけで簡便、容易、短時間に行うことができる。
【0038】
請求項7記載の発明によれば、請求項4ないし6のいずれかに記載の発明の上記作用に加えて、IC法におけるウォーターディップの原因であるナトリウムイオンを取り除き、更にF-及びCl-のピークの分離性の阻害原因となる二酸化炭素を取り除く前処理操作を、装置をセッティングするだけで簡便、容易、短時間に行うことができる。
【0039】
請求項8記載の発明によれば、陽イオン交換樹脂を密封した密閉容器を破壊することで水酸化ナトリウム吸収液のナトリウムイオンが陽イオン交換樹脂に吸着・除去されるため、水酸化ナトリウム吸収液中のナトリウムイオンを簡便、容易に除去できる。
【0040】
請求項9記載の発明によれば、請求項8記載の発明の上記作用に加えて、通気口から二酸化炭素のパージ用ガスを通気することにより、吸収液から二酸化炭素を追い出せるので、吸収液中の二酸化炭素を除去できる。したがって、排ガス吸収液中のナトリウムイオンと二酸化炭素の除去操作が簡便、容易に行える。
【0041】
請求項10記載の発明によれば、請求項8又は9記載の発明の上記作用に加えて、軟質プラスチック製の吸収容器であるので、外部から吸収容器内の密閉容器を押してガラスを割ることで簡単に密閉容器の密封を解くことができる。またガラス製の密閉容器は軟質プラスチック製の吸収容器に収納されていることから、吸収容器を落としても密閉容器は、割れにくい。更に吸収容器は軟質プラスチック製であるので、外部からの押圧で、変形させて簡単に前処理後の試料を取り出すことができる。
また請求項11記載の発明によれば、請求項8ないし10のいずれかに記載の発明の上記作用に加えて、排ガス吸収液のIC分析用の前処理に必要な操作を簡便、容易、安価に行うことができる。
【発明の効果】
【0042】
本発明によりゴミ焼却炉などの化学反応装置から発生する排ガス中の低濃度のハロゲン化合物及び硫黄酸化物などの酸性成分を、1回のサンプリングと1回の分析で同時に精度良く測定可能である。具体的には以下の効果を有する。また、排ガス中のハロゲン化合物及び硫黄酸化物の分析が迅速、簡便、安価に行われる。
【0043】
請求項1記載の発明によれば、IC法における水酸化ナトリウム吸収液のナトリウムイオンによるウォーターディップと排ガス中の二酸化炭素の影響によるF-とCl-の分離性の問題を解消でき、F-及びCl-のピークの分離性が良好なクロマトグラムが得られる。したがって、化学反応装置から発生する排ガス中のHF、HBr、HClなどのハロゲン化合物及び硫黄酸化物を、1回のサンプリングと1回の分析で同時に精度良く測定・分析できる。
【0044】
請求項2記載の発明によれば、請求項1記載の発明の上記効果に加えて、パージ用ガスが清浄なガスではなくても、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去できるため、F-、Cl-、Br−及びSO42-を精度よく分析することができる。
【0045】
請求項3記載の発明によれば、請求項1又は2記載の発明の上記効果に加えて、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる。
請求項4記載の発明によれば、排ガス吸収液中のナトリウムイオンや二酸化炭素の除去操作の一連の前処理操作を簡便、容易に行うことができる。
【0046】
請求項5記載の発明によれば、請求項4記載の発明の上記効果に加えて、装置をセッティングするだけで、清浄なガスではないパージ用ガスから排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去する前処理が簡便、容易に行える。
請求項6記載の発明によれば、請求項4又は5記載の発明の上記効果に加えて、排ガス中のSOxをすべて硫酸イオンに酸化させるための操作を簡便、容易に短時間で行える。
【0047】
請求項7記載の発明によれば、請求項4ないし6のいずれかに記載の発明の上記効果に加えて、排ガス吸収液をIC法により分析する際の前処理を簡便、容易に行えるため、迅速な分析が可能となる。
【0048】
請求項8記載の発明によれば、水酸化ナトリウム吸収液中のナトリウムイオンを簡便、容易に除去できるので、分析の前処理としてナトリウムイオンを除去する必要がある場合に簡便、容易、迅速にその操作を行うことができる。また、吸収容器に密閉容器が収納されているという一体的でコンパクトな構造となっているため、作業性に優れ、保管や持ち運びにも便利である。更に排ガス試料を安価で迅速、簡便に処理可能である。また、pH試験紙などでも分解液がアルカリ性から中性に変わったことが簡単に確認できる。更に種々の分析法の前処理に汎用的に用いることができる。
【0049】
請求項9記載の発明によれば、請求項8記載の発明の効果に加えて、更に排ガス吸収液中の二酸化炭素を除去する必要がある場合にも簡便、容易、迅速にその操作を行うことができ、測定、分析に要する時間も節約できる。
【0050】
請求項10記載の発明によれば、上記請求項8又は9記載の発明の効果に加えて、吸収容器を落としても密閉容器は、割れにくいため、更に保存性や保管性に優れ、持ち運びに便利である。更に吸収容器を外部から押して変形させることで、簡単に前処理後の試料を取り出すことができ、更に簡便、迅速な前処理が可能となる。
請求項11記載の発明によれば、上記請求項8ないし10のいずれかに記載の発明の効果に加えて、排ガス吸収液をIC法により分析する際の前処理を簡便、容易、安価に行え、更に迅速な分析が可能となる。
【発明を実施するための最良の形態】
【0051】
以下に本発明について詳細に説明する。なお、本発明の測定、分析対象の排ガスは、燃料や廃棄物などの燃焼、鉱石のばい焼、金属の精錬、硫黄製造工程、その他の化学反応、脱硫工程などで利用される化学反応装置からの排ガスをいい、例えば都市ゴミや産業廃棄物の焼却排ガスなどが対象となる。
【0052】
測定対象の排ガスをサンプリングし、水酸化ナトリウム水溶液の吸収液に吸収させて、この吸収液の一定量を中和脱ガス器にとる。サンプリング法としては、ポンプ等で吸引するなどの既知な方法により行えばよい。例えば都市ゴミや産業廃棄物の焼却排ガス中にはCO2が多量に含まれるため、0.1M程度の水酸化ナトリウム水溶液が好ましい。水酸化ナトリウム水溶液の濃度がこの濃度よりも低いと、排ガス中の酸性成分を十分に吸収することができず、また、吸収された酸性成分が揮散する可能性がある。更に、この濃度よりも高いと、上記したウォーターディップの問題があり、また吸収液中のNa+の除去に使用する陽イオン交換樹脂の量を増やす必要が生じ、除去に要する時間や手間も掛かる。
【0053】
中和脱ガス器にとる吸収液の量は、5〜20ml程度、例えば10ml程度でよい。また、サンプリングする際のサンプリング管は特に限定しないが、排ガス中の腐食性ガスによって侵されず、または、これに吸着しないガラス管、石英管、四フッ化エチレン樹脂製などを用いると良い。
【0054】
また、中和脱ガス器としては、特に限定しないがガラス製でインピンジャーを備えたものを用いると、後述する陽イオン交換樹脂が吸収液中で良く混合されてナトリウムイオンを捕集できる。またパージ用ガスの吸引と排気を容易に行うことができるので好適である。
【0055】
次いで、この中和脱ガス器に陽イオン交換樹脂の一定量を加えて、吸収液中のナトリウムイオン(Na+)を樹脂に吸着させて、吸収液を中性溶液にする。加える陽イオン交換樹脂の量は、吸収液5〜10mlに対し1g〜2g程度で良く、吸収液の量により適宜調整すればよい。加える陽イオン交換樹脂の種類に特に限定はなく、強酸性、弱酸性のどちらを使用しても良い。またゲル形、MR(マクロレティキュラー)形など種々の形態のものを用いることができ、樹脂の母体構造としてはスチレン系やアクリル系の陽イオン交換樹脂を用いることができる。またこれら陽イオン交換樹脂は、H+型陽イオン交換樹脂であってもNa+型陽イオン交換樹脂であってもよいが、Na+型の場合は、硝酸でH+型に再生してから使用すればよい。
【0056】
次いで、CO2のパージ用ガスは空気を用い、これを中和脱ガス器に流して、中性になった吸収液中のCO2を追い出して除去する。なお、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスをCO2のパージ用ガスとして用いれば、わざわざ清浄なガスを用いなくても、これら分析阻害成分による吸収液のコンタミネーションを防いで、吸収液中の二酸化炭素を除去できる。
【0057】
分析阻害成分としては、ハロゲン化合物、硫黄酸化物などの酸性成分や二酸化炭素などがあり、パージ用ガス中にこれら酸性成分などが含まれていると、排ガス中の酸性成分等と排ガス吸収液中で混ざってしまい、正確な排ガス中のハロゲン化合物等の測定ができなくなる。パージ用ガスの洗浄は、アルカリ溶液を通すことで容易にできる。アルカリ溶液としては、水酸化ナトリウム水溶液や水酸化カリウム水溶液などを使用することができ、この中でも酸性成分や二酸化炭素を効率よく吸収することから水酸化ナトリウム水溶液が好適である。ガスの洗浄に使用する水酸化ナトリウム水溶液の濃度及び液量は、測定する排ガスの量によって異なるが、1〜5M程度であれば、10ml〜20ml程度で良い。
【0058】
また、中和脱ガス器に流すパージ用ガスは、空気又は窒素などで良い。通常の大気を用いれば、簡便でコストもかからず好適である。大気中の空気を用いる場合は、該空気を洗浄して分析阻害成分を取り除けば良い。また、パージ用ガスを吸収液中に通気する操作は、中和脱ガス器に排ガス吸収液の一定量をとり、陽イオン交換樹脂の一定量を加えて空気を吹き込んでも良い。流す時間は、10ml程度の吸収液量であれば、5〜15分程度で良い。
【0059】
一方、排ガス中のSOxが水酸化ナトリウム水溶液に捕集されると大部分はSO42-となるが、その一部はSO32-として存在する場合がある。長時間、例えば30〜60分程度、空気を通気するとSO32-はSO42-に変わるが、その時間を短縮するにはパージ用ガスと共にもしくは別に中和脱ガス器の吸収液中にオゾンを流せば良い。オゾンの発生方法は、紫外線法、無声放電法、または、電気分解法などの一般的に良く知られている方法を用いることが可能である。オゾン発生器(オゾナイザー)をパージ用ガスの通気管に取り付けると、簡便、容易に吸収液中にオゾンを流すことができる。なお、IC法などの分析法で実際に分析した結果、SO32-が存在しない場合は、オゾンを流す必要はない。
【0060】
このように、排ガス吸収液からIC法で分析するときに妨害するアルカリ成分(Na+)と炭酸イオン(CO32-)を除去することで、陰イオン(F-、Cl-、Br-、SO42-)を精度よく分析でき、排ガス中のハロゲン化合物(HF、HCl、HBr)と硫黄酸化物(SOx)を1回のサンプリングと1回の分析で同時に測定できる。また、吸収液中にオゾンを流せば、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる。そして、この方法は、IC法に限らず、排ガス吸収液からアルカリ成分(Na+)と炭酸イオン(CO32-)を除去する必要のある種々の分析法の前処理として使用可能である。
【0061】
ところで、上記特許文献3のように、有機化合物中のハロゲン化合物と硫黄を燃焼管法で分解し、そのガスを吸収液に捕集した後、イオンクロマトグラフ法で分析する方法があり、また、同様の前処理装置が市販されている(例えば、株式会社ダイヤインスツルメンツ、自動試料燃焼装置、AQF−100型)。これらの燃焼装置は有機物中のハロゲン化合物と硫黄の含有量が多いため、また、分析を自動化しているため、試料採取量は1〜数mgと少ない。燃焼管法とイオンクロマトグラフ法を組み合わせた方法で、廃棄物固形化燃料中の全塩素と硫黄を分析する方法がJISで定められている(全塩素の分析方法は、日本工業規格(JIS) Z 7302−6 廃棄物固形化燃料:全塩素分試験方法(1999)による。また、硫黄の分析方法は、日本工業規格(JIS) Z 7302−7 廃棄物固形化燃料:硫黄分試験方法(2002)による)。
【0062】
この規定によれば、試料(最大約1g)を燃焼し、過酸化水素水に吸収させ、イオンクロマトグラフ法で全塩素と硫黄を分析する。さらに、最近では、プラスチックに含まれている臭素系難燃剤であるポリ臭素化ビフェニール(PBB)やポリ臭素化ジフェニールエーテル(PBDE)中の臭素をこの燃焼管法とイオンクロマトグラフ法を組み合わせた方法で分析することが行われている。
【0063】
しかし、廃棄物固形化燃料や臭素系難燃剤中のハロゲン化合物や硫黄を分析する場合は、従来の有機物を分析する場合に比べて、試料中のハロゲン及び硫黄の含有量が少ないため、試料採取量を最大1gと多く採取しなければならない。、そのため燃焼による二酸化炭素の発生量も多くなり、過酸化水素水の吸収では、ハロゲン化合物の捕集率が十分でない。
【0064】
そこで、JISで規定されている過酸化水素水の代わりに0.1Mの水酸化ナトリウム水溶液を吸収液として用いることにより、その捕集を完全にすることができる。この吸収液の一定量について、本発明の図7に示す分析用前処理装置と図8に示す分析用前処理キットを用いることにより、廃棄物固形化燃料や臭素系難燃剤中のハロゲン化合物や硫黄の分析に応用することができる。
【実施例1】
【0065】
図1には、本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法のフローを示す。
清掃工場の煙突から排出される排ガスをJIS法により(例えばJIS K 0095など)サンプリング管で採取して測定対象とし、0.1M水酸化ナトリウム水溶液の吸収液に吸収させて、この吸収液の一定量(10ml)を中和脱ガス器に入れた。サンプリング管はステンレス製のものを用い、中和脱ガス器はガラス製のものを用いた。
【0066】
次いで、この中和脱ガス器内の吸収液にH+型陽イオン交換樹脂(オルガノ(株)製 アンバーライト(商品名) IR124HAG)の一定量(2g)を加えて、吸収液中のナトリウムイオン(Na+)を樹脂に吸着させて、吸収液を中性溶液にした。吸収液が中性溶液になったことは、pH試験紙を用いて確認しても良い。
【0067】
次いで、予め1.0Mの水酸化ナトリウム水溶液(20ml)に通して洗浄し、酸性成分等を除去したパージ用空気(大気中の空気)を5分〜15分程度、中和脱ガス器内の吸収液に一定流量(0.2〜0.5L/分)流して、中性になった吸収液中のCO2を追い出して除去した溶液を測定試料とし、その上澄み液をイオンクロマトグラフに注入してハロゲン化物イオン及び硫酸イオンの測定を行った。
【0068】
上記方法により、吸収液からナトリウムイオンと炭酸イオンを除去した液をIC法で測定した結果(クロマトグラム)を図2に示す。なお、比較例として、図3には、吸収液を直接IC法で測定したときの結果を示し、図4には、吸収液に陽イオン交換樹脂を加えてNa+を除去した段階の測定結果を示し、図5には陰イオン標準液(7種)のクロマトグラムを示す。なお、IC法の測定条件を以下に示す(図2から図5とも同じ)。
【0069】
装置:ダイオネクス社製 DX500型 カラム:ダイオネクス社製 IonPac AG12A/AS12A サプレッサ:電気透析形のASRS−II 検出器:電気伝導度 溶離液:2.7mM炭酸ナトリウムと0.3mM炭酸水素ナトリウムの混合溶液を1.3ml/分にて通液 試料注入量:25μl カラム温度:35℃
吸収液を直接IC法で測定した場合は、図3のクロマトグラムからも明らかなように、アルカリの影響によるナトリウムイオン(Na+)のピークが見られ、更に炭酸イオンの影響でF-及びCl-のピークとの分離性が悪く分析できない。吸収液に陽イオン交換樹脂を加えてNa+を除去した場合は、図4のクロマトグラムからも明らかなように、Na+のピークが消失し、クロマトグラムは改善されるが、炭酸イオンの影響でF-及びCl-が妨害され、F-及びCl-が正確に測定できない。
【0070】
しかし、図2に示すように、吸収液に陽イオン交換樹脂を加えた後、パージ用空気を吸収液中に通気して吸収液中のCO2を追い出すと、炭酸イオンの影響がなくなってベースラインも安定し、F-及びCl-のピークが改善される。このクロマトグラムは図5に示す陰イオン標準液(各成分をイオン交換水に溶かしたものであり、各濃度を以下に示す。F:1.00ppm Cl:2.00ppm NO2:3.00ppm Br:2.00ppm NO3:6.00ppm PO4:6.00ppm SO4:8.00ppm)のクロマトグラムと同様の分離性を示す。
【0071】
また、表1には実際の廃棄物焼却場において排ガスのサンプリングを4回行ったときの排ガス中のHCl、HF、HBr、SOxの分析結果を示す。
【表1】

表1の結果から、排ガス中にはHClやSOxに加えて、微量のHFとHBrが含まれていることが確認された。そして、Cl-やSO42-と共に、F-、Br-も精度良く検出できた。
【0072】
また、表2には参考例として排ガスのサンプリングを4回行って、排ガス中の塩化水素の濃度をチオシアン酸水銀(II)吸光光度法(JIS K 0107)により分析した結果と、同じ排ガスを本実施例によるIC法で分析した結果を示す。
【0073】
【表2】

【0074】
表2より、4回ともほぼ同じ濃度となる分析結果が得られたため、本実施例による方法は、排ガス中のHClをはじめとするハロゲン化合物やSOx濃度の分析方法として、信頼性が高いといえる。そして以上の結果から、排ガス中の低濃度のハロゲン化合物及び硫黄酸化物などの酸性成分を、1回のサンプリングと1回の分析で同時に精度良く測定可能であることが確認された。また、排ガス中のハロゲン化合物及び硫黄酸化物の分析を迅速、簡便、安価に行うことができる。
【実施例2】
【0075】
一方、排ガス中のSOxが0.1MのNaOH溶液に捕集されると大部分はSO42-となるが、その一部はSO32-として存在する場合がある。実施例1による図2〜図4に示すクロマトグラムには、わずかながらSO32-のピークが確認される。長時間、パージ用空気を吸収液中に通気するとSO32-はSO42-に変わるが、その時間を短縮するため、本実施例ではオゾナイザーからオゾンを発生させて、SO32-からSO42-への酸化の促進を試みた。本実施例の条件は、オゾナイザー((株)レーシー製、modelYGR−103N)を用い、パージ用空気を一定流量(0.2〜0.5L/分)で5分〜15分程度通気した。
【0076】
オゾナイザーから発生するオゾンをパージ用空気と共に吸収液中に通気した以外は実施例1と同様とした。その結果を図6に示す。
図6から、図2〜図4に示すクロマトグラムと比較して、SO32-のピークの消失が確認できた。本実施例により、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる。
【実施例3】
【0077】
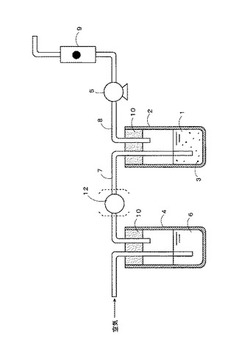
図7には、本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置の構成図を示す。
【0078】
中和脱ガス器2内の吸収液1中の二酸化炭素を除去するためのパージ用ガスを洗浄するガス洗浄容器4には、洗浄液6として1MのNaOH溶液20mlが入っており、ガスが洗浄容器4内を通過すると、ガス中のCO2と酸性成分がNaOH溶液中に吸収除去されてガス通気管7から中和脱ガス器2へ通気する。ガス洗浄容器4と中和脱ガス器2の上部は栓10などでフタをしてガス通気管7などを通している。
【0079】
インピンジャー型の中和脱ガス器2に実施例1と同様の排ガスを吸収させた0.1M水酸化ナトリウム水溶液1の一定量(10ml)と、同じく実施例1と同様の陽イオン交換樹脂3の一定量(2g)を入れると、Na+と陽イオン交換樹脂が溶液中で接触することにより、吸収液1中のNa+が陽イオン交換樹脂3に吸着・除去される。
【0080】
ポンプ5のスイッチを入れ一定の流量(0.2〜0.5L/分)で大気中の空気を一定時間(5分〜15分程度)吸引する。ポンプ5の後流側にはガス流量計9を接続している。空気はガス洗浄容器4で洗浄された後、ガス通気管7から中和脱ガス器2に流入する。この時、空気の流入により中和脱ガス器2内の陽イオン交換樹脂3が液中で混合され、液中のNa+を効率よく吸着し、吸収液1のpHがアルカリ性から中性に変わる。これと同時に液中のCO32-はCO2として中和脱ガス器2の系外へ排気管8から排出される。そして、この吸収液1の上澄み液を注射筒で1mlとり、イオンクロマトグラフに注入して実施例1と同様に吸収液1中のハロゲン化物イオン及び硫酸イオンを測定し、排ガス中のハロゲン化合物及び硫黄酸化物を分析する。
【0081】
一方、本実施例による分析用前処理装置には、ガス通気管7に実施例2で用いたオゾナイザー12を接続している(図7の点線で囲った部分)。排ガス中のSOxが0.1MのNaOH溶液に捕集されると大部分はSO42-となるが、その一部はSO32-として存在する場合がある。長時間、パージ用空気を吸収液1中に通気するとSO32-はSO42-に変わるが、その時間を短縮するため、本実施例ではオゾナイザー12からオゾンを発生させて、SO32-からSO42-への酸化を促進させている。なお、IC法などによる分析結果から、SO32-が存在しない場合は、オゾナイザーを省略してもよいのは言うまでもない。また、オゾナイザー12をガス通気管7とは別の管に接続しても良いが、ガス通気管7に接続すれば、別の管を設けることなく、オゾンを吸収液1中に通気できるため、簡便、容易、安価ででき、手間も掛からない。
【0082】
このように、本実施例による分析用前処理装置を使用すれば、例えばIC法などの分析法における水酸化ナトリウム吸収液によるウォーターディップと排ガス中の二酸化炭素によるF-とCl-の分離性の問題を解消でき、F-及びCl-のピークの分離性が良好なクロマトグラムが得られる。したがって、化学反応装置から発生する排ガス中のHF、HBr、HClなどのハロゲン化合物及び硫黄酸化物を、1回のサンプリングで同時に精度良く測定・分析するための前処理が簡便、容易、短時間にできる。また、オゾナイザー12を用いれば、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる前処理ができる。
【実施例4】
【0083】
図8には、本発明の一実施例である分析用前処理キット20の正面縦断面図を示す。
陽イオン交換樹脂(1.0〜2.0g程度)3がガラス管24内に封入されて、吸収容器21内に入っており、吸収容器21の上部はキャップ22により密封された状態として使用する。
【0084】
ガラス管24は、封入が簡易に解けるようなものであれば、ガラス管に限らず、どのような素材や形のものでも良い。また、陽イオン交換樹脂3を安定に保ち、密封できるものであればガラス管に限らない。吸収容器21の素材についても限定はないが、軽くて丈夫、安価であることからプラスチック製が好ましい。更に吸収容器21は軟質プラスチック製であればガラス管24を外部から押すことで簡単に割ることができ、また吸収容器21の側面を押すことにより吸収液1を簡単に押し出すことができるため、好適である。また、ガラス管24や吸収容器21の色について特に限定はないが、透明とすれば吸収容器21の中身がよく見えるので、操作がしやすい。
【0085】
本発明の一実施例である分析用前処理キット20は、吸収容器21の上部にねじ込み式のキャップ22を取り付けて密栓できる構造となっている。キャップ22の構造に特に限定はなく、また、吸収容器21は密封が簡易に解けるような構造であれば、キャップ22を付けることに限定されず、どのような構造であっても良い。例えばキャップ22と吸収容器21が一体的な構造であっても良い。さらにキャップ22による密封手段に限らず吸収容器21が密封でき、また密封が簡易に解ける手段(例えば栓をするなど)であれば特に限定されない。
【0086】
吸収容器21の大きさは限定されないが、直径15〜20mm程度、長さ130〜150mm程度の、持ちやすい大きさが簡便で良い。更に陽イオン交換樹脂封入ガラス管24は直径7〜9mm程度、長さ30〜45mm程度が良い。
【0087】
図9及び図10には、図8に示す分析用前処理キット20の使用例を説明する図を示す。 図9(a)に示すように、軟質プラスチック管の吸収容器21中にガラス管24に封入されたH+型陽イオン交換樹脂3の一定量(1g)を入れ、次いで図9(b)に示すように、実施例1と同様に採取した排ガス吸収液1の一定量(5ml程度)を入れる。この操作の順序に限定はなく、例えば排ガス吸収液1を入れてから、H+型陽イオン交換樹脂3を封入したガラス管24を入れても良い。次いで図9(c)に示すように、吸収容器21にキャップ22を取り付けて、図9(d)に示すように、軟質プラスチック管の吸収容器21を手で折り曲げてH+型陽イオン交換樹脂3の入ったガラス管24を割り、吸収液1とH+型陽イオン交換樹脂3を接触させ、振り混ぜる。
【0088】
そして、図10に示すように、この分析用前処理キット20のキャップ22を外し、吸収液1中の二酸化炭素を除去するためのパージ用ガスを通気する管7を入れ、ポンプ5をセットする。そしてポンプ5のスイッチを入れ一定の流量(0.2〜0.5L/分)で空気を一定時間(5分〜15分)吹き込む。キャップ22を通気穴と排気穴が2箇所空いたキャップに付け替えて、通気穴にパージ用ガスを通気する管7を差し込んでも良い。また、キャップでなくても吸収容器21自体に穴を開けておき、使用しない場合は栓やキャップをしておいても良い。
【0089】
吸収液1に空気を流すと吸収容器21中の陽イオン交換樹脂3が液中で混合され、液中のNa+を吸着すると、吸収液1のpHがアルカリ性から中性に変わる。これと同時に液中のCO32-はCO2として吸収容器21から系外へ排出される。なお、吸収液1の液性は、pH試験紙で確認できる。
【0090】
そして、この吸収液1の上澄み液を注射筒でとり、例えばイオンクロマトグラフなどの分析装置に注入して吸収液1中のハロゲン化物イオン及び硫酸イオンを測定し、排ガス中のハロゲン化合物及び硫黄酸化物を分析する。
【0091】
この分析用前処理キット20は、空気中に酸性成分が含まれていないこと(清浄な空気であること)、IC法などで分析したときにSO32-が存在しない場合に使用できる。また、吸収容器21を固定して、更に通気管7に実施例3のガス洗浄容器4やオゾナイザー12を接続すれば、実施例3の中和脱ガス器2と同様な使用方法が可能である。
【0092】
ガラス管24に封入されたH+型陽イオン交換樹脂3は、水分が保持されるため乾燥せず、また、樹脂からの陰イオン成分の溶出もなく、長期間、少なくとも約1年間程度は安定であるという特徴がある。したがって、保管性に優れ、必要なときにいつでも使用できる。そして、排ガス吸収液のナトリウムイオンや二酸化炭素を除去する前処理が簡便、容易、安価にできる。
【参考例1】
【0093】
図11には図7に示す分析用前処理装置に更に吸収液中のガスを捕集する装置を設けた場合の参考例を示す。
図11に示す分析用前処理装置は、図7の分析用前処理装置に、更に化学工業等からの排ガス中の塩素、硫化水素、シアン化水素などを吸収するための吸収容器15を接続したものである。この場合、排ガス中の二酸化炭素の濃度は1%以下である。
【0094】
図11に示すように、排ガス中に塩素、硫化水素、シアン化水素などの化合物を含む場合は、更に吸収液1中のガスを捕集する吸収容器15を設けると良い。吸収容器15に入れる吸収液16としては上記実施例等と同様に0.1M水酸化ナトリウム水溶液などの一定量(10ml)の吸収液を用いる。目的とする排ガスを中和脱ガス器2や前処理キット20の吸収容器21内の吸収液1に上記実施例と同様に吸収させて、吸収液1のpHを酸性にしてパージ用ガスを流すと、吸収液1中の塩素、硫化水素、シアン化水素などのガスが追い出されて、吸収容器15内の吸収液16に吸収、捕集される。
【0095】
そして、これら塩素、硫化水素、シアン化水素等を捕集した吸収液16を分析すれば良い。分析方法はIC法に限らず、例えば塩素であれば、4−ピリジンカルボン酸−ピラゾロン吸光光度法、硫化水素であれば、イオン電極法、シアン化水素であれば、4−ピリジンカルボン酸−ピラゾロン法及びイオン電極法で分析する。
【0096】
このように、図7の分析用前処理装置や図8の分析用前処理キット20は、化学工場などの排ガス中の塩素、硫化水素、シアン化水素を分離するための脱ガス処理にも使用することができる。
【参考例2】
【0097】
また、図7に示す分析用前処理装置と図8に示す分析用前処理キット20は、工業排水などの排水中の遊離シアンの分離にも使用することができる。
試料の排水を中和脱ガス器2や前処理キット20の吸収容器21に取り、排水中の遊離シアンをJIS K 0102に準拠した方法によりpH5に調節した後、洗浄した空気を一定流量(1.2L/分)で一定時間(60分)排水中に通気して、試料中の遊離シアン(シアン化水素)として排出させて、水酸化ナトリウム水溶液に捕集する。これをIC法もしくは他の方法により分析する。図7に示す分析用前処理装置や図8に示す分析用前処理キット20はJIS法の簡便化として使用できる。
【産業上の利用可能性】
【0098】
本発明は低濃度のハロゲン化合物や硫黄酸化物を含む排ガス試料の分析に極めて有効な分析方法、分析用前処理装置及び分析用前処理キットであり、種々の試料のハロゲン化合物や硫黄酸化物の分析法や分析用の前処理装置及び分析用前処理キットとして産業上の利用可能性が高く、環境分析などの他様々な技術分野への応用も可能である。
【図面の簡単な説明】
【0099】
【図1】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法のフローである。
【図2】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法により測定した結果である。
【図3】吸収液を直接IC法で測定した結果である。
【図4】吸収液に陽イオン交換樹脂を加えた段階の試料をIC法で測定した結果である。
【図5】陰イオン標準液(7種)のクロマトグラムである。
【図6】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法により測定した結果であり、オゾンをパージ用空気と共に吸収液中に通気した場合のクロマトグラムである。
【図7】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置の構成図である。
【図8】本発明の一実施例である分析用前処理キットの正面縦断面図である。
【図9】図8に示す分析用前処理キットの使用例を説明する図である。
【図10】図8に示す分析用前処理キットの使用例を説明する図である。
【図11】本発明の参考例である排ガス中の塩素、硫化水素、シアン化水素などの化合物の分析用前処理装置の構成図である(参考例1)。
【符号の説明】
【0100】
1 吸収液 2 中和脱ガス器
3 陽イオン交換樹脂 4 ガス洗浄容器
5 ポンプ 6 洗浄液
7 ガス通気管 8 排気管
9 ガス流量計 10 栓
12 オゾナイザー 15 吸収容器
16 吸収液 20 分析用前処理キット
21 吸収容器 22 キャップ
24 ガラス管
【技術分野】
【0001】
本発明は、化学反応装置から発生する排ガス中のフッ素、塩化水素、臭素などのハロゲン化合物と硫黄酸化物を簡便、同時に分析可能な方法と分析用前処理装置、及び分析用前処理キットに関するものである。
【背景技術】
【0002】
例えば、都市ゴミや産業廃棄物などを燃焼した際に発生する排ガス中には、有害物質として、硫黄酸化物の他にも微量のハロゲン化合物が含まれており、これらハロゲン化合物から生成される様々な大気汚染物質の発生が問題となっている。
【0003】
一方、都市ゴミや産業廃棄物などの焼却炉等の固定発生源から発生する有毒物質の測定法として、日本工業規格(JIS)では排ガス分析方法が規定されている。この排ガス分析方法では測定対象成分が約25種類に分類され、各測定対象成分毎に測定法が定められている。そして排ガス中のハロゲン化合物のうち、フッ化水素(HF)、塩化水素(HCl)、臭化水素(HBr)及び硫黄酸化物(SOx)の分析方法についても定められているが、この方法では、これらの成分は排ガスを各成分ごとに別々に採取(サンプリング)し、別々に測定する必要がある。
【0004】
JISで規格されている排ガス中のハロゲン化合物の分析方法として、HFについてはランタン−アリザリンコンプレキソン吸光光度法(LAC法)やイオン電極法などの分析方法が採用されており、HBrについてはチオシアン酸水銀(II)吸光光度法、チオ硫酸滴定法が採用されている。
【0005】
近年、排ガスの規制強化が進み、脱硫処理や排ガス処理技術の向上もあって、これらの有害物質は低濃度化の傾向にある。したがって、上記イオン電極法や滴定法などの分析方法では、低濃度のHFやHBrを精度良く分析することは難しい。一方、このような低濃度のハロゲン化合物を測定、分析する方法としては、例えばイオンクロマトグラフ法(以下、IC法という場合がある)がある。
【0006】
そして、フッ素を測定、分析する技術として、下記特許文献1によれば、フッ素樹脂またはフッ素樹脂を含む化合物を炭酸ナトリウムなどのアルカリ塩に吸収させ、水に溶解させた後、陽イオン交換樹脂によりアルカリを除き、残った水溶液中のフッ化物イオンをIC法により測定する構成が採用されている。また、HBrを測定、分析する技術としては、発光管をアルカリ溶液中で破砕し、破砕により発生した破砕物をアルカリ溶液から除去した後、IC法により、アルカリ溶液に含まれるハロゲンを定量する構成が採用されている。しかし、これら特許文献等の構成は、対象とするハロゲン化合物を個々に測定する技術であり、また対象とする測定試料も限られ微量であるため、これらの方法を様々な物質が混在する都市ゴミや産業廃棄物などを燃焼した際に発生する排ガス中のハロゲン化合物や硫黄酸化物の分析に適用することは難しい。
【0007】
そして、現在のJISによる排ガス分析方法では、上述したように各成分ごとに別々にサンプリングし、別々に分析する必要があるが、これら排ガス中のハロゲン化合物やSOxを1回のサンプリングと1回の分析で測定できれば、測定時間の短縮と分析コストが低減でき、簡便で望ましい。
【0008】
一方、下記非特許文献1において、SOxとHClを分析する方法として採用されているIC法は、低濃度の陰イオン成分を短時間で同時分析できるという特徴がある。この方法は、0.3%又は0.03%の過酸化水素(H2O2)水で排ガスを捕集した後、IC法で塩化物イオンと硫酸イオンを測定し、排ガス中のSOxとHClを分析する方法である。
【0009】
そして、有機化合物中の4種のハロゲン(フッ素、塩素、ヨウ素、臭素)と硫黄を同時に分析する方法として、有機化合物を燃焼して過酸化水素水又は飽水ヒドラジンを含む希水酸化ナトリウム水溶液(以下、NaOH溶液という場合がある)に吸収させて試料液としてイオンクロマトグラフに取り込み、IC法により同時に分析する方法が提案されている(下記特許文献3)。
【特許文献1】特開2002−214217号公報
【特許文献2】特開2002−289100号公報
【特許文献3】特開平8−262000号公報
【非特許文献1】日本工業規格(JIS) K 0103 排ガス中の硫黄酸化物分析方法(2005)
【発明の開示】
【発明が解決しようとする課題】
【0010】
上記特許文献3による方法は、過酸化水素水又は飽水ヒドラジンを含む希水酸化ナトリウム水溶液を吸収液として使用している。そして、この測定方法は、医薬、農薬などの分野における有機化合物中のハロゲン及び硫黄を測定対象としており、試料の量も1〜数mgと少ない。したがって、試料を燃焼した際に発生する二酸化炭素やハロゲン化合物の量も少ないため、希水酸化ナトリウム水溶液を吸収液として使用可能である。
【0011】
しかし、都市ゴミや産業廃棄物などを燃焼した際に発生する排ガス中には、ハロゲン化合物の他に10数%の高濃度の二酸化炭素が含まれるため、排ガスの吸収液が希アルカリ溶液であると、排ガス中の酸性成分が十分に吸収されず、また吸収液の酸性度も高くなり、一旦吸収されたハロゲン化合物が吸収液から揮発してしまう。したがって、排ガス中のハロゲン化合物を正確に測定ができないおそれがある。
【0012】
一方、上記JISで定められた塩化水素と硫黄酸化物のIC法による分析方法においても(非特許文献1)、排ガスの吸収液として、0.3%のH2O2水溶液を用いている。H2O2水溶液を用いた場合は、塩化水素と硫黄酸化物の測定は、それぞれ塩素イオン(Cl-)、硫酸イオン(SO42-)として精度良く分析可能である。しかし、この方法で他のハロゲン成分(フッ素、臭素)と塩化水素の同時測定を試みても、0.3%のH2O2水溶液を用いたときのHFとHBrの捕集率が明らかでないこと、又、二酸化炭素を含む排ガスを吸収したときにフッ化水素と臭化水素が吸収液中から揮散するおそれがあるため、これら低濃度のハロゲン成分を正確に同時測定することは難しい。したがって、排ガスの吸収液として、何を使用すれば良いのかという問題がある。
【0013】
しかし、排ガス規制が進む中で、上記イオン電極法や滴定法などでは測定不能な排ガス中の低濃度のハロゲンを測定できると共に、排ガス中のハロゲン化合物と硫黄酸化物などの酸性成分を同時に高精度で測定、分析できる簡便な測定方法や測定装置等が求められている。
【0014】
本発明の課題は、上記問題点を解決することであり、具体的にはゴミ焼却炉などの化学反応装置から発生する排ガス中の低濃度のハロゲン化合物及び硫黄酸化物などの酸性成分を、1回のサンプリングで同時に精度良く測定可能な分析方法を提供することである。更にこのような分析方法にかかる前処理を簡便、容易、短時間で可能な分析用前処理装置や分析用前処理キットを提供することである。
【課題を解決するための手段】
【0015】
本発明は、以下のような構成を採用することにより達成できる。
請求項1記載の発明は、化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に吸収させた後、該吸収液の一定量に陽イオン交換樹脂を加えてナトリウムイオンを陽イオン交換樹脂により吸着・除去し、前記吸収液中の二酸化炭素のパージ用ガスを前記陽イオン交換樹脂を加えた吸収液中に通気して吸収液中の炭酸イオンを二酸化炭素として除去し、次いで前記吸収液中のハロゲン化物イオン及び硫酸イオンをイオンクロマトグラフ法により測定する排ガス中のハロゲン化合物及び硫黄酸化物の分析方法である。
【0016】
請求項2記載の発明は、前記二酸化炭素のパージ用ガスは、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスである請求項1記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法である。
【0017】
請求項3記載の発明は、前記二酸化炭素のパージ用ガスと共に又は別に吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記吸収液中に通気する請求項1又は2記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法である。
【0018】
請求項4記載の発明は、化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に通じて吸収させた吸収液と陽イオン交換樹脂を接触させることにより前記吸収液中のナトリウムイオンを吸着・除去し、吸収液中の二酸化炭素のパージ用ガスを前記吸収液中に通じて吸収液中の二酸化炭素を除去する中和脱ガス器と、前記二酸化炭素のパージ用ガスを前記中和脱ガス器内の吸収液中に通気する通気手段と、該通気手段により通気されるパージ用ガスにより前記吸収液から発生する二酸化炭素を排気する排気手段とを設けた排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0019】
請求項5記載の発明は、更に、前記二酸化炭素のパージ用ガスを洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去するガス洗浄装置を設けた請求項4記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0020】
請求項6記載の発明は、更に前記吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記二酸化炭素のパージ用ガスと共に又は別に前記中和脱ガス器内の吸収液に通気するためのオゾン通気手段を設けた請求項4又は5記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0021】
請求項7記載の発明は、イオンクロマトグラフ法による分析用の前処理装置である請求項4ないし6のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置である。
【0022】
請求項8記載の発明は、ナトリウムイオンを吸着・除去する陽イオン交換樹脂を密封した押圧力で破壊可能な密閉容器と、該密閉容器とハロゲン化合物及び硫黄酸化物を含む排ガスを吸収した水酸化ナトリウム水溶液とを収納可能で、キャップにより密封可能な開口部を有する吸収容器とを一体化した構造である排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0023】
請求項9記載の発明は、前記排ガスを吸収した水酸化ナトリウム水溶液の吸収液中の二酸化炭素を除去するためのパージ用ガスを通気する通気口を有する請求項8記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0024】
請求項10記載の発明は、前記破壊可能な密閉容器はガラス製であり、前記吸収容器は軟質プラスチック製である請求項8又は9記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0025】
請求項11記載の発明は、イオンクロマトグラフ法による分析用の前処理キットである請求項8ないし10のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キットである。
【0026】
(作用)
上記非特許文献1において、SOxとHClを分析する方法として採用されているIC法は、低濃度の陰イオン成分を短時間で同時分析できるという特徴がある。本発明者らは、このような特徴のあるIC法により、SOxやHClのみならず、HFやHBrも同時に精度良く分析できる方法やこのような方法の分析用前処理装置、また、分析用前処理キットなどについて鋭意研究を重ね、以下のことを見出した。
【0027】
上記のように、非特許文献1におけるSOxとHClのIC法による分析方法では、吸収液としてH2O2水溶液を用いているが、この吸収液を用いた場合は、フッ素化合物と臭素化合物の捕集率が明らかでない。又、排ガス中の二酸化炭素を吸収することによる吸収液の液性の変化から、吸収液中の塩化物イオンとフッ化物イオンと臭化物イオンを精度良く測定することは難しい。一方、JISで定められた排ガス中のハロゲン化合物(HF、HBr、HCl)の測定は、排ガスを上記特許文献等よりも比較的高濃度の0.1M(mol/L)水酸化ナトリウム水溶液に吸収させた後、ランタン−アリザリンコンプレキソン吸光光度法(LAC法)、チオシアン酸水銀(II)吸光光度法、チオ硫酸滴定法や硝酸銀滴定法、イオン電極法などで分析する方法である(JIS K 0105(HF)、JIS K 0085(HBr)、JIS K 0107(HCl))。
【0028】
そこで、上記方法が排ガス吸収液として0.1M水酸化ナトリウム水溶液を使用することが共通していることに本発明者らは着目した。すなわち排ガス中には二酸化炭素が多く含まれるため、比較的アルカリの濃度が濃い吸収液が適している、またハロゲンガスの吸収液として酸性ガスを吸収できるという理由で採用されている0.1M水酸化ナトリウム水溶液に着目して、当該吸収液を用いて、他のハロゲン成分を捕集すれば、IC法でも測定できるのではと考え、本発明を完成させるに至った。
【0029】
しかし、IC法では、通常、数mmolの炭酸ナトリウムと炭酸水素ナトリウム溶液を溶離液として用いるために、例えば、水酸化ナトリウム水溶液を吸収液として用いた場合に、アルカリ濃度が比較的高い場合は吸収液を分析すると、水酸化ナトリウムに起因するウォーターディップが大きくなる。また、排ガス中の二酸化炭素が吸収液に捕集され、その影響を受けて、クロマトグラム上のF-及びCl-のピークと重なってF-とCl-の分離性が悪いという問題がある。
【0030】
すなわち、排ガスの吸収液に、例えば0.1Mなどの比較的高濃度の水酸化ナトリウム水溶液を使用したときの問題点として、(1)溶離液は数mMの炭酸塩溶液に対して吸収液のアルカリ濃度(100mM)が高いため、ウォーターディップが大きくなり、F-とCl-の測定を妨害する、(2)排ガス中の二酸化炭素(CO2)が同時に捕集されると、クロマトグラム上のF-及びCl-のピークと重なり分離性が悪いなどの問題がある。
【0031】
しかし、本発明によれば、排ガス中のハロゲン化合物及びSOxをNaOH溶液に吸収させた後、IC法で分析するときの妨害原因となるアルカリ成分(Na+)と炭酸イオン(CO32-)を除去して陰イオン(F-、Cl-、Br-、SO42-)を精度よく分析できるように改良したので、排ガス中のハロゲン化合物(HF、HCl、HBr)と硫黄酸化物(SOx)を同時に分析できる。
【0032】
すなわち、請求項1記載の発明によれば、排ガスを吸収した吸収液中に陽イオン交換樹脂を加えることで、ウォーターディップの原因であるナトリウムイオンを陽イオン交換樹脂により吸着・除去できる。更に、パージ用ガスを吸収液中に通気して吸収液中の二酸化炭素を除去することで、IC法におけるクロマトグラム上のF-及びCl-のピークの分離性が良くなる。なお、「ガス」とは、吸収液中の二酸化炭素を追い出すためのパージ用ガスを意味する。
【0033】
また、請求項2記載の発明によれば、請求項1記載の発明の上記作用に加えて、パージ用ガスが清浄なガスではなくても、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスをパージ用ガスとして用いることで、例えばIC法における分析阻害成分であるガス中の酸性成分や汚染成分を除去して、これら酸性成分や汚染成分による吸収液のコンタミネーションを防いで、吸収液中の二酸化炭素を除去できる。したがって、更に、クロマトグラム上のF-及びCl-のピークの分離性が良くなる。
【0034】
一方、排ガス中のSOxは、水酸化ナトリウム水溶液に吸収される際の酸化が不十分であると、不安定な亜硫酸イオンで存在する場合がある。しかし、請求項3記載の発明によれば、請求項1又は2記載の発明の上記作用に加えて、吸収液中の亜硫酸イオン(SO32-)を硫酸イオン(SO42-)に酸化させるためのオゾンを吸収液中に通気することで、排ガス中のSOxをすべて硫酸イオンに変えることができる。
【0035】
また、排ガス吸収液中にナトリウムイオンや二酸化炭素を含み、これらの成分が分析の妨害原因となる場合の種々の分析法の前処理を簡便、容易、短時間に行うことができれば、測定、分析に要する時間も節約できる。
【0036】
請求項4記載の発明によれば、装置をセッティングするだけで排ガス吸収液中のナトリウムイオンや二酸化炭素の除去操作の一連の前処理操作を行うことができる。
請求項5記載の発明によれば、請求項4記載の発明の上記作用に加えて、装置をセッティングするだけで、清浄なガスではないパージ用ガスから排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去でき、簡便、容易にパージ用ガスの洗浄を行うことができる。
【0037】
請求項6記載の発明によれば、請求項4又は5記載の発明の上記作用に加えて、排ガス吸収液中に亜硫酸イオン(SO32-)が存在する場合に、排ガス中のSOxをすべて硫酸イオンに酸化させるための操作を、装置をセッティングするだけで簡便、容易、短時間に行うことができる。
【0038】
請求項7記載の発明によれば、請求項4ないし6のいずれかに記載の発明の上記作用に加えて、IC法におけるウォーターディップの原因であるナトリウムイオンを取り除き、更にF-及びCl-のピークの分離性の阻害原因となる二酸化炭素を取り除く前処理操作を、装置をセッティングするだけで簡便、容易、短時間に行うことができる。
【0039】
請求項8記載の発明によれば、陽イオン交換樹脂を密封した密閉容器を破壊することで水酸化ナトリウム吸収液のナトリウムイオンが陽イオン交換樹脂に吸着・除去されるため、水酸化ナトリウム吸収液中のナトリウムイオンを簡便、容易に除去できる。
【0040】
請求項9記載の発明によれば、請求項8記載の発明の上記作用に加えて、通気口から二酸化炭素のパージ用ガスを通気することにより、吸収液から二酸化炭素を追い出せるので、吸収液中の二酸化炭素を除去できる。したがって、排ガス吸収液中のナトリウムイオンと二酸化炭素の除去操作が簡便、容易に行える。
【0041】
請求項10記載の発明によれば、請求項8又は9記載の発明の上記作用に加えて、軟質プラスチック製の吸収容器であるので、外部から吸収容器内の密閉容器を押してガラスを割ることで簡単に密閉容器の密封を解くことができる。またガラス製の密閉容器は軟質プラスチック製の吸収容器に収納されていることから、吸収容器を落としても密閉容器は、割れにくい。更に吸収容器は軟質プラスチック製であるので、外部からの押圧で、変形させて簡単に前処理後の試料を取り出すことができる。
また請求項11記載の発明によれば、請求項8ないし10のいずれかに記載の発明の上記作用に加えて、排ガス吸収液のIC分析用の前処理に必要な操作を簡便、容易、安価に行うことができる。
【発明の効果】
【0042】
本発明によりゴミ焼却炉などの化学反応装置から発生する排ガス中の低濃度のハロゲン化合物及び硫黄酸化物などの酸性成分を、1回のサンプリングと1回の分析で同時に精度良く測定可能である。具体的には以下の効果を有する。また、排ガス中のハロゲン化合物及び硫黄酸化物の分析が迅速、簡便、安価に行われる。
【0043】
請求項1記載の発明によれば、IC法における水酸化ナトリウム吸収液のナトリウムイオンによるウォーターディップと排ガス中の二酸化炭素の影響によるF-とCl-の分離性の問題を解消でき、F-及びCl-のピークの分離性が良好なクロマトグラムが得られる。したがって、化学反応装置から発生する排ガス中のHF、HBr、HClなどのハロゲン化合物及び硫黄酸化物を、1回のサンプリングと1回の分析で同時に精度良く測定・分析できる。
【0044】
請求項2記載の発明によれば、請求項1記載の発明の上記効果に加えて、パージ用ガスが清浄なガスではなくても、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去できるため、F-、Cl-、Br−及びSO42-を精度よく分析することができる。
【0045】
請求項3記載の発明によれば、請求項1又は2記載の発明の上記効果に加えて、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる。
請求項4記載の発明によれば、排ガス吸収液中のナトリウムイオンや二酸化炭素の除去操作の一連の前処理操作を簡便、容易に行うことができる。
【0046】
請求項5記載の発明によれば、請求項4記載の発明の上記効果に加えて、装置をセッティングするだけで、清浄なガスではないパージ用ガスから排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去する前処理が簡便、容易に行える。
請求項6記載の発明によれば、請求項4又は5記載の発明の上記効果に加えて、排ガス中のSOxをすべて硫酸イオンに酸化させるための操作を簡便、容易に短時間で行える。
【0047】
請求項7記載の発明によれば、請求項4ないし6のいずれかに記載の発明の上記効果に加えて、排ガス吸収液をIC法により分析する際の前処理を簡便、容易に行えるため、迅速な分析が可能となる。
【0048】
請求項8記載の発明によれば、水酸化ナトリウム吸収液中のナトリウムイオンを簡便、容易に除去できるので、分析の前処理としてナトリウムイオンを除去する必要がある場合に簡便、容易、迅速にその操作を行うことができる。また、吸収容器に密閉容器が収納されているという一体的でコンパクトな構造となっているため、作業性に優れ、保管や持ち運びにも便利である。更に排ガス試料を安価で迅速、簡便に処理可能である。また、pH試験紙などでも分解液がアルカリ性から中性に変わったことが簡単に確認できる。更に種々の分析法の前処理に汎用的に用いることができる。
【0049】
請求項9記載の発明によれば、請求項8記載の発明の効果に加えて、更に排ガス吸収液中の二酸化炭素を除去する必要がある場合にも簡便、容易、迅速にその操作を行うことができ、測定、分析に要する時間も節約できる。
【0050】
請求項10記載の発明によれば、上記請求項8又は9記載の発明の効果に加えて、吸収容器を落としても密閉容器は、割れにくいため、更に保存性や保管性に優れ、持ち運びに便利である。更に吸収容器を外部から押して変形させることで、簡単に前処理後の試料を取り出すことができ、更に簡便、迅速な前処理が可能となる。
請求項11記載の発明によれば、上記請求項8ないし10のいずれかに記載の発明の効果に加えて、排ガス吸収液をIC法により分析する際の前処理を簡便、容易、安価に行え、更に迅速な分析が可能となる。
【発明を実施するための最良の形態】
【0051】
以下に本発明について詳細に説明する。なお、本発明の測定、分析対象の排ガスは、燃料や廃棄物などの燃焼、鉱石のばい焼、金属の精錬、硫黄製造工程、その他の化学反応、脱硫工程などで利用される化学反応装置からの排ガスをいい、例えば都市ゴミや産業廃棄物の焼却排ガスなどが対象となる。
【0052】
測定対象の排ガスをサンプリングし、水酸化ナトリウム水溶液の吸収液に吸収させて、この吸収液の一定量を中和脱ガス器にとる。サンプリング法としては、ポンプ等で吸引するなどの既知な方法により行えばよい。例えば都市ゴミや産業廃棄物の焼却排ガス中にはCO2が多量に含まれるため、0.1M程度の水酸化ナトリウム水溶液が好ましい。水酸化ナトリウム水溶液の濃度がこの濃度よりも低いと、排ガス中の酸性成分を十分に吸収することができず、また、吸収された酸性成分が揮散する可能性がある。更に、この濃度よりも高いと、上記したウォーターディップの問題があり、また吸収液中のNa+の除去に使用する陽イオン交換樹脂の量を増やす必要が生じ、除去に要する時間や手間も掛かる。
【0053】
中和脱ガス器にとる吸収液の量は、5〜20ml程度、例えば10ml程度でよい。また、サンプリングする際のサンプリング管は特に限定しないが、排ガス中の腐食性ガスによって侵されず、または、これに吸着しないガラス管、石英管、四フッ化エチレン樹脂製などを用いると良い。
【0054】
また、中和脱ガス器としては、特に限定しないがガラス製でインピンジャーを備えたものを用いると、後述する陽イオン交換樹脂が吸収液中で良く混合されてナトリウムイオンを捕集できる。またパージ用ガスの吸引と排気を容易に行うことができるので好適である。
【0055】
次いで、この中和脱ガス器に陽イオン交換樹脂の一定量を加えて、吸収液中のナトリウムイオン(Na+)を樹脂に吸着させて、吸収液を中性溶液にする。加える陽イオン交換樹脂の量は、吸収液5〜10mlに対し1g〜2g程度で良く、吸収液の量により適宜調整すればよい。加える陽イオン交換樹脂の種類に特に限定はなく、強酸性、弱酸性のどちらを使用しても良い。またゲル形、MR(マクロレティキュラー)形など種々の形態のものを用いることができ、樹脂の母体構造としてはスチレン系やアクリル系の陽イオン交換樹脂を用いることができる。またこれら陽イオン交換樹脂は、H+型陽イオン交換樹脂であってもNa+型陽イオン交換樹脂であってもよいが、Na+型の場合は、硝酸でH+型に再生してから使用すればよい。
【0056】
次いで、CO2のパージ用ガスは空気を用い、これを中和脱ガス器に流して、中性になった吸収液中のCO2を追い出して除去する。なお、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスをCO2のパージ用ガスとして用いれば、わざわざ清浄なガスを用いなくても、これら分析阻害成分による吸収液のコンタミネーションを防いで、吸収液中の二酸化炭素を除去できる。
【0057】
分析阻害成分としては、ハロゲン化合物、硫黄酸化物などの酸性成分や二酸化炭素などがあり、パージ用ガス中にこれら酸性成分などが含まれていると、排ガス中の酸性成分等と排ガス吸収液中で混ざってしまい、正確な排ガス中のハロゲン化合物等の測定ができなくなる。パージ用ガスの洗浄は、アルカリ溶液を通すことで容易にできる。アルカリ溶液としては、水酸化ナトリウム水溶液や水酸化カリウム水溶液などを使用することができ、この中でも酸性成分や二酸化炭素を効率よく吸収することから水酸化ナトリウム水溶液が好適である。ガスの洗浄に使用する水酸化ナトリウム水溶液の濃度及び液量は、測定する排ガスの量によって異なるが、1〜5M程度であれば、10ml〜20ml程度で良い。
【0058】
また、中和脱ガス器に流すパージ用ガスは、空気又は窒素などで良い。通常の大気を用いれば、簡便でコストもかからず好適である。大気中の空気を用いる場合は、該空気を洗浄して分析阻害成分を取り除けば良い。また、パージ用ガスを吸収液中に通気する操作は、中和脱ガス器に排ガス吸収液の一定量をとり、陽イオン交換樹脂の一定量を加えて空気を吹き込んでも良い。流す時間は、10ml程度の吸収液量であれば、5〜15分程度で良い。
【0059】
一方、排ガス中のSOxが水酸化ナトリウム水溶液に捕集されると大部分はSO42-となるが、その一部はSO32-として存在する場合がある。長時間、例えば30〜60分程度、空気を通気するとSO32-はSO42-に変わるが、その時間を短縮するにはパージ用ガスと共にもしくは別に中和脱ガス器の吸収液中にオゾンを流せば良い。オゾンの発生方法は、紫外線法、無声放電法、または、電気分解法などの一般的に良く知られている方法を用いることが可能である。オゾン発生器(オゾナイザー)をパージ用ガスの通気管に取り付けると、簡便、容易に吸収液中にオゾンを流すことができる。なお、IC法などの分析法で実際に分析した結果、SO32-が存在しない場合は、オゾンを流す必要はない。
【0060】
このように、排ガス吸収液からIC法で分析するときに妨害するアルカリ成分(Na+)と炭酸イオン(CO32-)を除去することで、陰イオン(F-、Cl-、Br-、SO42-)を精度よく分析でき、排ガス中のハロゲン化合物(HF、HCl、HBr)と硫黄酸化物(SOx)を1回のサンプリングと1回の分析で同時に測定できる。また、吸収液中にオゾンを流せば、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる。そして、この方法は、IC法に限らず、排ガス吸収液からアルカリ成分(Na+)と炭酸イオン(CO32-)を除去する必要のある種々の分析法の前処理として使用可能である。
【0061】
ところで、上記特許文献3のように、有機化合物中のハロゲン化合物と硫黄を燃焼管法で分解し、そのガスを吸収液に捕集した後、イオンクロマトグラフ法で分析する方法があり、また、同様の前処理装置が市販されている(例えば、株式会社ダイヤインスツルメンツ、自動試料燃焼装置、AQF−100型)。これらの燃焼装置は有機物中のハロゲン化合物と硫黄の含有量が多いため、また、分析を自動化しているため、試料採取量は1〜数mgと少ない。燃焼管法とイオンクロマトグラフ法を組み合わせた方法で、廃棄物固形化燃料中の全塩素と硫黄を分析する方法がJISで定められている(全塩素の分析方法は、日本工業規格(JIS) Z 7302−6 廃棄物固形化燃料:全塩素分試験方法(1999)による。また、硫黄の分析方法は、日本工業規格(JIS) Z 7302−7 廃棄物固形化燃料:硫黄分試験方法(2002)による)。
【0062】
この規定によれば、試料(最大約1g)を燃焼し、過酸化水素水に吸収させ、イオンクロマトグラフ法で全塩素と硫黄を分析する。さらに、最近では、プラスチックに含まれている臭素系難燃剤であるポリ臭素化ビフェニール(PBB)やポリ臭素化ジフェニールエーテル(PBDE)中の臭素をこの燃焼管法とイオンクロマトグラフ法を組み合わせた方法で分析することが行われている。
【0063】
しかし、廃棄物固形化燃料や臭素系難燃剤中のハロゲン化合物や硫黄を分析する場合は、従来の有機物を分析する場合に比べて、試料中のハロゲン及び硫黄の含有量が少ないため、試料採取量を最大1gと多く採取しなければならない。、そのため燃焼による二酸化炭素の発生量も多くなり、過酸化水素水の吸収では、ハロゲン化合物の捕集率が十分でない。
【0064】
そこで、JISで規定されている過酸化水素水の代わりに0.1Mの水酸化ナトリウム水溶液を吸収液として用いることにより、その捕集を完全にすることができる。この吸収液の一定量について、本発明の図7に示す分析用前処理装置と図8に示す分析用前処理キットを用いることにより、廃棄物固形化燃料や臭素系難燃剤中のハロゲン化合物や硫黄の分析に応用することができる。
【実施例1】
【0065】
図1には、本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法のフローを示す。
清掃工場の煙突から排出される排ガスをJIS法により(例えばJIS K 0095など)サンプリング管で採取して測定対象とし、0.1M水酸化ナトリウム水溶液の吸収液に吸収させて、この吸収液の一定量(10ml)を中和脱ガス器に入れた。サンプリング管はステンレス製のものを用い、中和脱ガス器はガラス製のものを用いた。
【0066】
次いで、この中和脱ガス器内の吸収液にH+型陽イオン交換樹脂(オルガノ(株)製 アンバーライト(商品名) IR124HAG)の一定量(2g)を加えて、吸収液中のナトリウムイオン(Na+)を樹脂に吸着させて、吸収液を中性溶液にした。吸収液が中性溶液になったことは、pH試験紙を用いて確認しても良い。
【0067】
次いで、予め1.0Mの水酸化ナトリウム水溶液(20ml)に通して洗浄し、酸性成分等を除去したパージ用空気(大気中の空気)を5分〜15分程度、中和脱ガス器内の吸収液に一定流量(0.2〜0.5L/分)流して、中性になった吸収液中のCO2を追い出して除去した溶液を測定試料とし、その上澄み液をイオンクロマトグラフに注入してハロゲン化物イオン及び硫酸イオンの測定を行った。
【0068】
上記方法により、吸収液からナトリウムイオンと炭酸イオンを除去した液をIC法で測定した結果(クロマトグラム)を図2に示す。なお、比較例として、図3には、吸収液を直接IC法で測定したときの結果を示し、図4には、吸収液に陽イオン交換樹脂を加えてNa+を除去した段階の測定結果を示し、図5には陰イオン標準液(7種)のクロマトグラムを示す。なお、IC法の測定条件を以下に示す(図2から図5とも同じ)。
【0069】
装置:ダイオネクス社製 DX500型 カラム:ダイオネクス社製 IonPac AG12A/AS12A サプレッサ:電気透析形のASRS−II 検出器:電気伝導度 溶離液:2.7mM炭酸ナトリウムと0.3mM炭酸水素ナトリウムの混合溶液を1.3ml/分にて通液 試料注入量:25μl カラム温度:35℃
吸収液を直接IC法で測定した場合は、図3のクロマトグラムからも明らかなように、アルカリの影響によるナトリウムイオン(Na+)のピークが見られ、更に炭酸イオンの影響でF-及びCl-のピークとの分離性が悪く分析できない。吸収液に陽イオン交換樹脂を加えてNa+を除去した場合は、図4のクロマトグラムからも明らかなように、Na+のピークが消失し、クロマトグラムは改善されるが、炭酸イオンの影響でF-及びCl-が妨害され、F-及びCl-が正確に測定できない。
【0070】
しかし、図2に示すように、吸収液に陽イオン交換樹脂を加えた後、パージ用空気を吸収液中に通気して吸収液中のCO2を追い出すと、炭酸イオンの影響がなくなってベースラインも安定し、F-及びCl-のピークが改善される。このクロマトグラムは図5に示す陰イオン標準液(各成分をイオン交換水に溶かしたものであり、各濃度を以下に示す。F:1.00ppm Cl:2.00ppm NO2:3.00ppm Br:2.00ppm NO3:6.00ppm PO4:6.00ppm SO4:8.00ppm)のクロマトグラムと同様の分離性を示す。
【0071】
また、表1には実際の廃棄物焼却場において排ガスのサンプリングを4回行ったときの排ガス中のHCl、HF、HBr、SOxの分析結果を示す。
【表1】

表1の結果から、排ガス中にはHClやSOxに加えて、微量のHFとHBrが含まれていることが確認された。そして、Cl-やSO42-と共に、F-、Br-も精度良く検出できた。
【0072】
また、表2には参考例として排ガスのサンプリングを4回行って、排ガス中の塩化水素の濃度をチオシアン酸水銀(II)吸光光度法(JIS K 0107)により分析した結果と、同じ排ガスを本実施例によるIC法で分析した結果を示す。
【0073】
【表2】

【0074】
表2より、4回ともほぼ同じ濃度となる分析結果が得られたため、本実施例による方法は、排ガス中のHClをはじめとするハロゲン化合物やSOx濃度の分析方法として、信頼性が高いといえる。そして以上の結果から、排ガス中の低濃度のハロゲン化合物及び硫黄酸化物などの酸性成分を、1回のサンプリングと1回の分析で同時に精度良く測定可能であることが確認された。また、排ガス中のハロゲン化合物及び硫黄酸化物の分析を迅速、簡便、安価に行うことができる。
【実施例2】
【0075】
一方、排ガス中のSOxが0.1MのNaOH溶液に捕集されると大部分はSO42-となるが、その一部はSO32-として存在する場合がある。実施例1による図2〜図4に示すクロマトグラムには、わずかながらSO32-のピークが確認される。長時間、パージ用空気を吸収液中に通気するとSO32-はSO42-に変わるが、その時間を短縮するため、本実施例ではオゾナイザーからオゾンを発生させて、SO32-からSO42-への酸化の促進を試みた。本実施例の条件は、オゾナイザー((株)レーシー製、modelYGR−103N)を用い、パージ用空気を一定流量(0.2〜0.5L/分)で5分〜15分程度通気した。
【0076】
オゾナイザーから発生するオゾンをパージ用空気と共に吸収液中に通気した以外は実施例1と同様とした。その結果を図6に示す。
図6から、図2〜図4に示すクロマトグラムと比較して、SO32-のピークの消失が確認できた。本実施例により、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる。
【実施例3】
【0077】
図7には、本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置の構成図を示す。
【0078】
中和脱ガス器2内の吸収液1中の二酸化炭素を除去するためのパージ用ガスを洗浄するガス洗浄容器4には、洗浄液6として1MのNaOH溶液20mlが入っており、ガスが洗浄容器4内を通過すると、ガス中のCO2と酸性成分がNaOH溶液中に吸収除去されてガス通気管7から中和脱ガス器2へ通気する。ガス洗浄容器4と中和脱ガス器2の上部は栓10などでフタをしてガス通気管7などを通している。
【0079】
インピンジャー型の中和脱ガス器2に実施例1と同様の排ガスを吸収させた0.1M水酸化ナトリウム水溶液1の一定量(10ml)と、同じく実施例1と同様の陽イオン交換樹脂3の一定量(2g)を入れると、Na+と陽イオン交換樹脂が溶液中で接触することにより、吸収液1中のNa+が陽イオン交換樹脂3に吸着・除去される。
【0080】
ポンプ5のスイッチを入れ一定の流量(0.2〜0.5L/分)で大気中の空気を一定時間(5分〜15分程度)吸引する。ポンプ5の後流側にはガス流量計9を接続している。空気はガス洗浄容器4で洗浄された後、ガス通気管7から中和脱ガス器2に流入する。この時、空気の流入により中和脱ガス器2内の陽イオン交換樹脂3が液中で混合され、液中のNa+を効率よく吸着し、吸収液1のpHがアルカリ性から中性に変わる。これと同時に液中のCO32-はCO2として中和脱ガス器2の系外へ排気管8から排出される。そして、この吸収液1の上澄み液を注射筒で1mlとり、イオンクロマトグラフに注入して実施例1と同様に吸収液1中のハロゲン化物イオン及び硫酸イオンを測定し、排ガス中のハロゲン化合物及び硫黄酸化物を分析する。
【0081】
一方、本実施例による分析用前処理装置には、ガス通気管7に実施例2で用いたオゾナイザー12を接続している(図7の点線で囲った部分)。排ガス中のSOxが0.1MのNaOH溶液に捕集されると大部分はSO42-となるが、その一部はSO32-として存在する場合がある。長時間、パージ用空気を吸収液1中に通気するとSO32-はSO42-に変わるが、その時間を短縮するため、本実施例ではオゾナイザー12からオゾンを発生させて、SO32-からSO42-への酸化を促進させている。なお、IC法などによる分析結果から、SO32-が存在しない場合は、オゾナイザーを省略してもよいのは言うまでもない。また、オゾナイザー12をガス通気管7とは別の管に接続しても良いが、ガス通気管7に接続すれば、別の管を設けることなく、オゾンを吸収液1中に通気できるため、簡便、容易、安価ででき、手間も掛からない。
【0082】
このように、本実施例による分析用前処理装置を使用すれば、例えばIC法などの分析法における水酸化ナトリウム吸収液によるウォーターディップと排ガス中の二酸化炭素によるF-とCl-の分離性の問題を解消でき、F-及びCl-のピークの分離性が良好なクロマトグラムが得られる。したがって、化学反応装置から発生する排ガス中のHF、HBr、HClなどのハロゲン化合物及び硫黄酸化物を、1回のサンプリングで同時に精度良く測定・分析するための前処理が簡便、容易、短時間にできる。また、オゾナイザー12を用いれば、排ガス中のSOxをすべて硫酸イオンに変えることができ、正確なSOx濃度の測定・分析が可能となる前処理ができる。
【実施例4】
【0083】
図8には、本発明の一実施例である分析用前処理キット20の正面縦断面図を示す。
陽イオン交換樹脂(1.0〜2.0g程度)3がガラス管24内に封入されて、吸収容器21内に入っており、吸収容器21の上部はキャップ22により密封された状態として使用する。
【0084】
ガラス管24は、封入が簡易に解けるようなものであれば、ガラス管に限らず、どのような素材や形のものでも良い。また、陽イオン交換樹脂3を安定に保ち、密封できるものであればガラス管に限らない。吸収容器21の素材についても限定はないが、軽くて丈夫、安価であることからプラスチック製が好ましい。更に吸収容器21は軟質プラスチック製であればガラス管24を外部から押すことで簡単に割ることができ、また吸収容器21の側面を押すことにより吸収液1を簡単に押し出すことができるため、好適である。また、ガラス管24や吸収容器21の色について特に限定はないが、透明とすれば吸収容器21の中身がよく見えるので、操作がしやすい。
【0085】
本発明の一実施例である分析用前処理キット20は、吸収容器21の上部にねじ込み式のキャップ22を取り付けて密栓できる構造となっている。キャップ22の構造に特に限定はなく、また、吸収容器21は密封が簡易に解けるような構造であれば、キャップ22を付けることに限定されず、どのような構造であっても良い。例えばキャップ22と吸収容器21が一体的な構造であっても良い。さらにキャップ22による密封手段に限らず吸収容器21が密封でき、また密封が簡易に解ける手段(例えば栓をするなど)であれば特に限定されない。
【0086】
吸収容器21の大きさは限定されないが、直径15〜20mm程度、長さ130〜150mm程度の、持ちやすい大きさが簡便で良い。更に陽イオン交換樹脂封入ガラス管24は直径7〜9mm程度、長さ30〜45mm程度が良い。
【0087】
図9及び図10には、図8に示す分析用前処理キット20の使用例を説明する図を示す。 図9(a)に示すように、軟質プラスチック管の吸収容器21中にガラス管24に封入されたH+型陽イオン交換樹脂3の一定量(1g)を入れ、次いで図9(b)に示すように、実施例1と同様に採取した排ガス吸収液1の一定量(5ml程度)を入れる。この操作の順序に限定はなく、例えば排ガス吸収液1を入れてから、H+型陽イオン交換樹脂3を封入したガラス管24を入れても良い。次いで図9(c)に示すように、吸収容器21にキャップ22を取り付けて、図9(d)に示すように、軟質プラスチック管の吸収容器21を手で折り曲げてH+型陽イオン交換樹脂3の入ったガラス管24を割り、吸収液1とH+型陽イオン交換樹脂3を接触させ、振り混ぜる。
【0088】
そして、図10に示すように、この分析用前処理キット20のキャップ22を外し、吸収液1中の二酸化炭素を除去するためのパージ用ガスを通気する管7を入れ、ポンプ5をセットする。そしてポンプ5のスイッチを入れ一定の流量(0.2〜0.5L/分)で空気を一定時間(5分〜15分)吹き込む。キャップ22を通気穴と排気穴が2箇所空いたキャップに付け替えて、通気穴にパージ用ガスを通気する管7を差し込んでも良い。また、キャップでなくても吸収容器21自体に穴を開けておき、使用しない場合は栓やキャップをしておいても良い。
【0089】
吸収液1に空気を流すと吸収容器21中の陽イオン交換樹脂3が液中で混合され、液中のNa+を吸着すると、吸収液1のpHがアルカリ性から中性に変わる。これと同時に液中のCO32-はCO2として吸収容器21から系外へ排出される。なお、吸収液1の液性は、pH試験紙で確認できる。
【0090】
そして、この吸収液1の上澄み液を注射筒でとり、例えばイオンクロマトグラフなどの分析装置に注入して吸収液1中のハロゲン化物イオン及び硫酸イオンを測定し、排ガス中のハロゲン化合物及び硫黄酸化物を分析する。
【0091】
この分析用前処理キット20は、空気中に酸性成分が含まれていないこと(清浄な空気であること)、IC法などで分析したときにSO32-が存在しない場合に使用できる。また、吸収容器21を固定して、更に通気管7に実施例3のガス洗浄容器4やオゾナイザー12を接続すれば、実施例3の中和脱ガス器2と同様な使用方法が可能である。
【0092】
ガラス管24に封入されたH+型陽イオン交換樹脂3は、水分が保持されるため乾燥せず、また、樹脂からの陰イオン成分の溶出もなく、長期間、少なくとも約1年間程度は安定であるという特徴がある。したがって、保管性に優れ、必要なときにいつでも使用できる。そして、排ガス吸収液のナトリウムイオンや二酸化炭素を除去する前処理が簡便、容易、安価にできる。
【参考例1】
【0093】
図11には図7に示す分析用前処理装置に更に吸収液中のガスを捕集する装置を設けた場合の参考例を示す。
図11に示す分析用前処理装置は、図7の分析用前処理装置に、更に化学工業等からの排ガス中の塩素、硫化水素、シアン化水素などを吸収するための吸収容器15を接続したものである。この場合、排ガス中の二酸化炭素の濃度は1%以下である。
【0094】
図11に示すように、排ガス中に塩素、硫化水素、シアン化水素などの化合物を含む場合は、更に吸収液1中のガスを捕集する吸収容器15を設けると良い。吸収容器15に入れる吸収液16としては上記実施例等と同様に0.1M水酸化ナトリウム水溶液などの一定量(10ml)の吸収液を用いる。目的とする排ガスを中和脱ガス器2や前処理キット20の吸収容器21内の吸収液1に上記実施例と同様に吸収させて、吸収液1のpHを酸性にしてパージ用ガスを流すと、吸収液1中の塩素、硫化水素、シアン化水素などのガスが追い出されて、吸収容器15内の吸収液16に吸収、捕集される。
【0095】
そして、これら塩素、硫化水素、シアン化水素等を捕集した吸収液16を分析すれば良い。分析方法はIC法に限らず、例えば塩素であれば、4−ピリジンカルボン酸−ピラゾロン吸光光度法、硫化水素であれば、イオン電極法、シアン化水素であれば、4−ピリジンカルボン酸−ピラゾロン法及びイオン電極法で分析する。
【0096】
このように、図7の分析用前処理装置や図8の分析用前処理キット20は、化学工場などの排ガス中の塩素、硫化水素、シアン化水素を分離するための脱ガス処理にも使用することができる。
【参考例2】
【0097】
また、図7に示す分析用前処理装置と図8に示す分析用前処理キット20は、工業排水などの排水中の遊離シアンの分離にも使用することができる。
試料の排水を中和脱ガス器2や前処理キット20の吸収容器21に取り、排水中の遊離シアンをJIS K 0102に準拠した方法によりpH5に調節した後、洗浄した空気を一定流量(1.2L/分)で一定時間(60分)排水中に通気して、試料中の遊離シアン(シアン化水素)として排出させて、水酸化ナトリウム水溶液に捕集する。これをIC法もしくは他の方法により分析する。図7に示す分析用前処理装置や図8に示す分析用前処理キット20はJIS法の簡便化として使用できる。
【産業上の利用可能性】
【0098】
本発明は低濃度のハロゲン化合物や硫黄酸化物を含む排ガス試料の分析に極めて有効な分析方法、分析用前処理装置及び分析用前処理キットであり、種々の試料のハロゲン化合物や硫黄酸化物の分析法や分析用の前処理装置及び分析用前処理キットとして産業上の利用可能性が高く、環境分析などの他様々な技術分野への応用も可能である。
【図面の簡単な説明】
【0099】
【図1】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法のフローである。
【図2】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法により測定した結果である。
【図3】吸収液を直接IC法で測定した結果である。
【図4】吸収液に陽イオン交換樹脂を加えた段階の試料をIC法で測定した結果である。
【図5】陰イオン標準液(7種)のクロマトグラムである。
【図6】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析方法により測定した結果であり、オゾンをパージ用空気と共に吸収液中に通気した場合のクロマトグラムである。
【図7】本発明の一実施例である排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置の構成図である。
【図8】本発明の一実施例である分析用前処理キットの正面縦断面図である。
【図9】図8に示す分析用前処理キットの使用例を説明する図である。
【図10】図8に示す分析用前処理キットの使用例を説明する図である。
【図11】本発明の参考例である排ガス中の塩素、硫化水素、シアン化水素などの化合物の分析用前処理装置の構成図である(参考例1)。
【符号の説明】
【0100】
1 吸収液 2 中和脱ガス器
3 陽イオン交換樹脂 4 ガス洗浄容器
5 ポンプ 6 洗浄液
7 ガス通気管 8 排気管
9 ガス流量計 10 栓
12 オゾナイザー 15 吸収容器
16 吸収液 20 分析用前処理キット
21 吸収容器 22 キャップ
24 ガラス管
【特許請求の範囲】
【請求項1】
化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に吸収させた後、該吸収液の一定量に陽イオン交換樹脂を加えてナトリウムイオンを陽イオン交換樹脂により吸着・除去し、前記吸収液中の二酸化炭素のパージ用ガスを前記陽イオン交換樹脂を加えた吸収液中に通気して吸収液中の炭酸イオンを二酸化炭素として除去し、次いで前記吸収液中のハロゲン化物イオン及び硫酸イオンをイオンクロマトグラフ法により測定することを特徴とする排ガス中のハロゲン化合物及び硫黄酸化物の分析方法。
【請求項2】
前記二酸化炭素のパージ用ガスは、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスであることを特徴とする請求項1記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法。
【請求項3】
前記二酸化炭素のパージ用ガスと共に又は別に吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記吸収液中に通気することを特徴とする請求項1又は2記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法。
【請求項4】
化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に通じて吸収させた吸収液と陽イオン交換樹脂を接触させることにより前記吸収液中のナトリウムイオンを吸着・除去し、吸収液中の二酸化炭素のパージ用ガスを前記吸収液中に通じて吸収液中の二酸化炭素を除去する中和脱ガス器と、
前記二酸化炭素のパージ用ガスを前記中和脱ガス器内の吸収液中に通気する通気手段と、
該通気手段により通気されるパージ用ガスにより前記吸収液から発生する二酸化炭素を排気する排気手段と
を設けたことを特徴とする排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項5】
更に、前記二酸化炭素のパージ用ガスを洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去するガス洗浄装置を設けたことを特徴とする請求項4記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項6】
更に前記吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記二酸化炭素のパージ用ガスと共に又は別に前記中和脱ガス器内の吸収液に通気するためのオゾン通気手段を設けたことを特徴とする請求項4又は5記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項7】
イオンクロマトグラフ法による分析用の前処理装置であることを特徴とする請求項4ないし6のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項8】
ナトリウムイオンを吸着・除去する陽イオン交換樹脂を密封した押圧力で破壊可能な密閉容器と、該密閉容器とハロゲン化合物及び硫黄酸化物を含む排ガスを吸収した水酸化ナトリウム水溶液とを収納可能で、キャップにより密封可能な開口部を有する吸収容器とを一体化した構造であることを特徴とする排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項9】
前記排ガスを吸収した水酸化ナトリウム水溶液の吸収液中の二酸化炭素を除去するためのパージ用ガスを通気する通気口を有することを特徴とする請求項8記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項10】
前記破壊可能な密閉容器はガラス製であり、前記吸収容器は軟質プラスチック製であることを特徴とする請求項8又は9記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項11】
イオンクロマトグラフ法による分析用の前処理キットであることを特徴とする請求項8ないし10のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項1】
化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に吸収させた後、該吸収液の一定量に陽イオン交換樹脂を加えてナトリウムイオンを陽イオン交換樹脂により吸着・除去し、前記吸収液中の二酸化炭素のパージ用ガスを前記陽イオン交換樹脂を加えた吸収液中に通気して吸収液中の炭酸イオンを二酸化炭素として除去し、次いで前記吸収液中のハロゲン化物イオン及び硫酸イオンをイオンクロマトグラフ法により測定することを特徴とする排ガス中のハロゲン化合物及び硫黄酸化物の分析方法。
【請求項2】
前記二酸化炭素のパージ用ガスは、予め洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去したガスであることを特徴とする請求項1記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法。
【請求項3】
前記二酸化炭素のパージ用ガスと共に又は別に吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記吸収液中に通気することを特徴とする請求項1又は2記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析方法。
【請求項4】
化学反応装置から発生するハロゲン化合物及び硫黄酸化物を含む排ガスを水酸化ナトリウム水溶液に通じて吸収させた吸収液と陽イオン交換樹脂を接触させることにより前記吸収液中のナトリウムイオンを吸着・除去し、吸収液中の二酸化炭素のパージ用ガスを前記吸収液中に通じて吸収液中の二酸化炭素を除去する中和脱ガス器と、
前記二酸化炭素のパージ用ガスを前記中和脱ガス器内の吸収液中に通気する通気手段と、
該通気手段により通気されるパージ用ガスにより前記吸収液から発生する二酸化炭素を排気する排気手段と
を設けたことを特徴とする排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項5】
更に、前記二酸化炭素のパージ用ガスを洗浄して排ガス中のハロゲン化合物及び硫黄酸化物の分析阻害成分を除去するガス洗浄装置を設けたことを特徴とする請求項4記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項6】
更に前記吸収液中の亜硫酸イオンを硫酸イオンに酸化させるためのオゾンを前記二酸化炭素のパージ用ガスと共に又は別に前記中和脱ガス器内の吸収液に通気するためのオゾン通気手段を設けたことを特徴とする請求項4又は5記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項7】
イオンクロマトグラフ法による分析用の前処理装置であることを特徴とする請求項4ないし6のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理装置。
【請求項8】
ナトリウムイオンを吸着・除去する陽イオン交換樹脂を密封した押圧力で破壊可能な密閉容器と、該密閉容器とハロゲン化合物及び硫黄酸化物を含む排ガスを吸収した水酸化ナトリウム水溶液とを収納可能で、キャップにより密封可能な開口部を有する吸収容器とを一体化した構造であることを特徴とする排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項9】
前記排ガスを吸収した水酸化ナトリウム水溶液の吸収液中の二酸化炭素を除去するためのパージ用ガスを通気する通気口を有することを特徴とする請求項8記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項10】
前記破壊可能な密閉容器はガラス製であり、前記吸収容器は軟質プラスチック製であることを特徴とする請求項8又は9記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【請求項11】
イオンクロマトグラフ法による分析用の前処理キットであることを特徴とする請求項8ないし10のいずれかに記載の排ガス中のハロゲン化合物及び硫黄酸化物の分析用前処理キット。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2008−46026(P2008−46026A)
【公開日】平成20年2月28日(2008.2.28)
【国際特許分類】
【出願番号】特願2006−222746(P2006−222746)
【出願日】平成18年8月17日(2006.8.17)
【出願人】(506209422)地方独立行政法人 東京都立産業技術研究センター (134)
【Fターム(参考)】
【公開日】平成20年2月28日(2008.2.28)
【国際特許分類】
【出願日】平成18年8月17日(2006.8.17)
【出願人】(506209422)地方独立行政法人 東京都立産業技術研究センター (134)
【Fターム(参考)】
[ Back to top ]

