排ガス浄化触媒およびその製造方法
【課題】貴金属を含まず、300℃以上の高温雰囲気中で安定して存在し、少なくともNiより優れた触媒活性を発揮する排ガス浄化触媒およびその製造方法を提供する。
【解決手段】Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成ることを特徴とする排ガス浄化触媒。特にCO浄化用として優れている。Niと、Niよりも電気陰性度の低い周期律表3、4、5族から選択した元素とを混合し、溶解、鋳造してインゴットを作製する第1工程、上記インゴットを均質化熱処理する第2工程、および 上記均質加熱処理したインゴットを機械的に粉砕する第3工程を含む、排ガス浄化触媒の製造方法。
【解決手段】Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成ることを特徴とする排ガス浄化触媒。特にCO浄化用として優れている。Niと、Niよりも電気陰性度の低い周期律表3、4、5族から選択した元素とを混合し、溶解、鋳造してインゴットを作製する第1工程、上記インゴットを均質化熱処理する第2工程、および 上記均質加熱処理したインゴットを機械的に粉砕する第3工程を含む、排ガス浄化触媒の製造方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、排ガス浄化触媒に関し、特にCO浄化性能の高い排ガス浄化触媒およびその製造方法に関する。
【背景技術】
【0002】
自動車等の内燃機関の排ガスの成分、特に一酸化炭素(CO)ガスを、酸素(O2)ガスまたは酸化窒素(NOx)ガスとともに触媒活物質に接触させることにより、毒性のあるCOガスおよびNOxガスを無毒の二酸化炭素(CO2)ガスおよび窒素(N2)ガスに変換(浄化)することができる。
【0003】
このような排ガス浄化触媒としての活性を示す触媒活物質としては、典型的には白金(Pt)、ロジウム(Rh)等の貴金属が知られている。しかし貴金属には単価が高いという問題がある。そのため、様々な物質が貴金属の代替物質として検討され、貴金属の使用量を低減することが試みられてきた。
【0004】
例えば特許文献1には、酸化セリウム(CeO2)を含む多孔質担体にジルコニウム(Zr)と金(Au)を含有させた触媒が提示されている。
【0005】
また特許文献2には、白金(Pt)、パラジウム(Pd)、および酸化ジルコニウム(ZrO2)と酸化プラセオジウム(Pr6O11)との複合酸化物から成る触媒が提示されている。
【0006】
これらはいずれも貴金属が必須の構成成分である。これまでに、貴金属を全く含まず、少なくともニッケル(Ni)を超える触媒活性を有する触媒活物質は知られていない。
【0007】
また、一般にCOやNOxの浄化反応が進行する300℃〜1000℃程度での高温において、熱的な安定性を備えた触媒活物質も知られていない。
【0008】
特許文献3には、貴金属を含まず、しかもPtと同等のCO浄化活性を示す触媒活物質として、超微粒子状の金属間化合物Ni3Alナノ粒子が開示されている。しかしながらこれは、表面積の小さいPt粒子(0.0066m2)に対して表面積の遥かに大きいNi3Alナノ粒子(0.25〜2.2m2:Ptの約30倍〜約300倍)を比較した結果である。したがって、見かけの触媒活性が触媒粒子の表面積に比例するという周知の事実に照らせば、特許文献3においてNi3Alナノ粒子の触媒活性がPt粒子と同等であるとする結論は全く根拠が無い。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2008−73654号公報
【特許文献2】特開2010−58110号公報
【特許文献3】特開2010−137131号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、貴金属を含まず、300℃以上の高温雰囲気中で安定して存在し、少なくともNiより優れた触媒活性を発揮する排ガス浄化触媒およびその製造方法を提供することを目的とする。
【課題を解決するための手段】
【0011】
上記目的を達成するために、本発明によれば、Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成ることを特徴とする排ガス浄化触媒が提供される。
【0012】
上記目的を達成するために、本発明によれば更に、Niと、Niよりも電気陰性度の低い周期律表3、4、5族から選択した元素とを混合し、溶解、鋳造してインゴットを作製する第1工程、
上記インゴットを均質化熱処理する第2工程、および
上記均質加熱処理したインゴットを機械的に粉砕する第3工程
を含むことを特徴とする排ガス浄化触媒の製造方法が提供される。
【発明の効果】
【0013】
本発明の排ガス浄化触媒は、Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成るので、300℃以上の高温でも熱的に安定であり、かつ、Niを凌ぎ、Ptに迫る高い触媒活性を発揮する。
【図面の簡単な説明】
【0014】
【図1】図1は、Ni−Ti2元系の相図である。
【図2】図2は、Nb−Ni2元系の相図である。
【図3】図3は、Ni−Y2元系の相図である。
【図4】図4は、実施例において排ガス浄化触媒の粉末試料を調製するフローを模式的に示す。
【図5】図5は、実施例において作成した本発明の排ガス浄化触媒試料のX線回折結果を示す。
【図6】図6は、本発明の排ガス浄化触媒の結晶構造を示す。
【図7】図7は、実施例において用いたCO酸化触媒活性評価装置を模式的に示す。
【図8】図8は、(a)Ni3Al(比較例)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni3Al(比較例)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
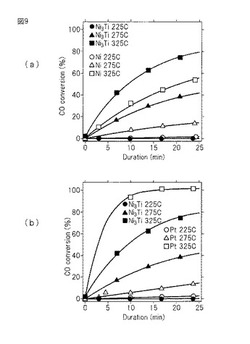
【図9】図9は、(a)Ni3Ti(本発明例の試料1)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni3Ti(本発明例の試料1)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図10】図10は、(a)Ni3Nb(本発明例の試料2)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni3Nb(本発明例の試料2)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図11】図11は、(a)Ni5Y(本発明例の試料3)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni5Y(本発明例の試料3)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図12】図12は、Ni(参照試料1)、Pt(参照試料2)、Ni3Al(比較例)、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni5Y(本発明例の試料3)の経過時間10分におけるCO酸化触媒活性を、反応温度の関数として示す。横軸が温度(Temperature)、縦軸がCO浄化率(CO conversion)である。
【図13】図13は、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の325℃におけるCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図14】図14は、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の価電子d−バンドを示す光電子分光測定結果を示す。
【図15】図15は、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)のd−バンドセンター(d-band center)と、325℃におけるCO浄化反応開始5分後のCO浄化率との関係を示す。
【発明を実施するための形態】
【0015】
本発明者は下記の着想に基づき、本発明を完成した。
【0016】
浄化反応の際には、排ガス浄化用の触媒活物質の表面と浄化対象である排ガス分子との間では、お互いの原子の最外殻電子の遣り取りが起きる。触媒活性を示さない物質にPt等の貴金属と同様な触媒活性を示す性質を付与するには、構成元素の表面の電子状態を変化させてPt等の貴金属に近い電子状態にする必要がある。
【0017】
先ず、貴金属以外で最良の触媒活性を示すNiをベースに、その電子状態を変えることを構想した。Niの電子状態を変えるには、周期律表でNiとは電子状態の異なる金属との合金化が有効である。電子状態の違いを電気陰性度χ(ポーリングの電気陰性度)でみると、Niのχ=1.91に対して、これよりも低いχ=1.2〜1.6程度の範囲(低χ範囲)と、高いχ=1.95〜2.05程度の範囲(高χ範囲)を対象として着目した。
【0018】
この電気陰性度の範囲は、周期律表でNi(χ=1.91)の属する10族に対して、低χ範囲はTi(同1.54)、Nb(同1.6)、Y(同1.22)などの属する3、4、5族に対応し、高χ範囲はB(同2.04)、Sn(同1.96)などの属する13、14、15族に対応する。
【0019】
下記反応式(1)で表されるCO浄化反応の反応速度は、触媒表面におけるCO吸着とO2解離吸着のバランスによって決定される。Ni単体および低χ元素単体のCO浄化触媒活性はCOの表面吸着力が強すぎるため著しく抑制される。これに対し、Niと低χ元素との合金はCOの非占有分子軌道のエネルギー準位差が広いため、合金表面におけるCO吸着力が弱められ、CO吸着とO2解離吸着のバランスが保たれる結果、Ni単体の表面または低χ元素単体の表面よりも浄化反応が速やかに進行する。
【0020】
CO+1/2O2→CO2……(1)
Niとの合金相手として、Niに対する触媒活性の優位性の観点から、低χ範囲の元素が望ましく、特にTi、Nb、Yが望ましい。
【0021】
Niとこれらとの合金の形態としては、固溶体よりも金属間化合物であることが望ましく、特にNi3Ti、Ni3Nb、Ni5Yであることが望ましい。固溶体合金は、例えば溶解・凝固・均質化熱処理等の製造工程および高温雰囲気中での使用時に、種々の相が生成する虞が高く、安定して単相を確保することが困難であり、望みの触媒活性を安定して得ることが困難である。Ni3Ti、Ni3Nb、Ni5Yの結晶構造は、それぞれP63/mmc、Pmmm、P6/mmmである。
【0022】
金属間化合物は、組成および相の安定性が高いため複数相が生成する虞がなく、常に安定して良好な触媒活性を得ることができる。
【0023】
本発明の望ましい形態による触媒活物質であるNi3Ti、Ni3Nb、Ni5Yは、図1〜3に示すように融点がそれぞれ1380℃(Ni3Ti)、1399℃(Ni3Nb)、1431℃(Ni5Y)である。これは、COおよびNOx浄化触媒の通常の使用温度範囲である300℃〜1000℃程度に対して遥かに高温であり、使用中の安定性は確保される。
【0024】
本発明の排ガス浄化触媒は以下のように製造することができる。
【0025】
Niと低χ元素とを混合し、溶解してインゴットを作製し、このインゴットを非酸化性雰囲気中で均質化のための熱処理を施す。
【0026】
具体的には、先ず、Niと低χ元素を望みのモル比で秤量し、典型的には酸素および水分濃度が5ppm以下のアルゴンガス雰囲気下で混合、溶解し、ボタン状のインゴットを得る。
【0027】
得られたインゴットをタンタル等の高融点金属箔に包み、酸素吸収剤とともに減圧下で石英管に封入する。この石英管を電気炉中に装入し、均質化のための熱処理を施す。その後、電気炉から石英管を取り出し、室温まで徐冷する。石英管を割り、試料を取り出した後、機械的に粉砕する。得られた粉末試料を篩い分けにより粉末粒径を揃え排ガス浄化触媒を得る。
【0028】
均質化のための熱処理温度は、合金の融点から500℃程度を減じた温度以上で、融点未満であることが望ましく、合金の融点から300℃程度を減じた温度以下であることがより望ましい。例えば、Ni3Ti、Ni3Nb、Ni5Yの融点はそれぞれ、1380℃、1399℃、1431℃であるから、それぞれ望ましい均質化熱処理温度範囲は、880〜1380℃、899〜1399℃、931〜1431℃であり、より望ましい範囲は880〜1080℃、899〜1099℃、931〜1131℃である。
【0029】
均質化熱処理の時間は、50時間以上とすることが望ましく、100時間以上とすることがより望ましい。実際の製造時間の観点から、処理時間は150時間以下とすることが望ましい。
【0030】
なお、本発明の排ガス浄化触媒の製造は、上記溶解法に限定する必要は無く、レーザーアブレーション、スパッタリング、溶液還元法等を適用することもできる。これらの方法を用いることにより、合金粉末の粒径等を制御し、例えば均一な大きさのナノ粒子から成る排ガス浄化触媒を実現することができる。
【0031】
以上はNiをベースとした合金について説明したが、Ni以外にもFe、Co、Cuをベースとして合金も可能性がある。Niは元素の周期律表でPtと同族であり最外殻電子の状態はPtと近く、周期律表でNiの近くに位置するFe、Co、Cuは貴金属のRu、Rh、Auと同族であり、上記と同様な考え方で触媒活性を高められる物質の構成元素となる可能性が考えられる。すなわち、周期律表でFe、Co、Ni、Cuの属する8、9、10、11族の元素と、低χ元素のTi、Nb、Yなどの属する3、4、5族の元素との合金または、高χ元素のB、Snなどの属する13、14、15族の元素との合金についても、更に検討する価値がある。
【0032】
また、本発明の排ガス浄化触媒は、CO、NOxのみでなく、炭化水素CxHxの浄化触媒としても可能性がある。
【実施例】
【0033】
<試料の製造>
本発明例として、金属間化合物から成る排ガス浄化触媒Ni3Ti(試料1)、Ni3Nb(試料2)、Ni5Y(試料3)を、図4に模式的に示す手順および条件にて製造した。
【0034】
先ず、金属ニッケル(純度99.9%、フルヤ金属製)、金属チタン(純度99%、フルヤ金属製)、金属ニオブ(純度99%、フルヤ金属製)、金属イットリウム(純度98%、フルヤ金属製)を、それぞれモル比でNi:Ti=3:1(試料1)、Ni:Nb=3:1(試料2)、Ni:Y=5:1(試料3)に総量3g秤量した。
【0035】
次に、各試料を、酸素濃度および水分濃度がいずれも5ppmである純粋アルゴンガス雰囲気下でアーク溶解し、ボタン状のインゴットを得た。
【0036】
比較例として、高純度化学研究所(株)製のアトマイズNi3Al粉末を、受領したままの状態で用いた。
【0037】
次に、インゴットをタンタル箔に包み、酸素吸収剤としてジルコニウム箔と共に背圧10−3Paで石英管に封入した。石英管を電気炉内に装入し、950℃×100時間の均質化熱処理を行なった。その後、電気炉から石英管を取り出し、室温まで徐冷した。石英管を割り、試料を取り出した後、メノウ乳鉢で機械粉砕した。得られた粉末試料を63μmメッシュのステンレス製篩にかけ、篩を通過した粉末を回収した。この粉末を更に53μmメッシュのステンレス製篩にかけ、篩に残った粉末を回収した。これにより、53μm〜63μmに粉末粒径を揃えた本発明の排ガス浄化触媒の試料1、2、3を得た。
【0038】
比較例のNi3Al試料についても同様に篩い分けを行なって粉末粒径を53μm〜63μmに揃えた。
【0039】
<X線回折による試料の同定>
X線回折測定装置(CuKα線:リガク製RIN2000)を用い、常温常圧大気下にて、測定インクリメント=0.02°、スキャン幅2θ=5〜95°の条件で、試料1〜3のX線回折測定を行なった。
【0040】
図5の(a)、(b)、(c)に試料1、2、3の回折結果を示す。ただし、図中の縦線は、Ni3Ti、Ni3Nb、Ni5Yの結晶データを用いて計算したシミュレーション結果である。図から分かるように、各試料の回折ピークとシミュレーションピークとはよく一致しており、試料1、2、3がそれぞれNi3Ti、Ni3Nb、Ni5Yの単相であることが確認できる。比較例の試料についても同様のX線回折測定を行いNi3Al(Cu3Au型構造、Fm3m)の単相であることが確認された。
【0041】
図6に、(a)Ni3Ti、(b)Ni3Nb、(c)Ni5Yの結晶構造を示す。それぞれ(a)試料1Ni3Ti(P63/mmc:a、b=0.5109nm、c=0.8299nm)、(b)試料2Ni3Nb(Pmmm:a、b、c=0.4565nm、0.5116nm、0.4260nm)、(c)試料3Ni5Y(P6/mmm:a、b=0.4833nm、c=0.3967nm)に対応する。
【0042】
<触媒活性の評価>
図7に示す気流循環式触媒活性評価装置(CO酸化触媒活性測定装置)を用いて、実施例の試料1〜3および比較例の試料のCO酸化触媒活性を測定した。更に、参照試料として、同じく篩い分けによって粉末粒径を53μm〜63μmに揃えたNi粉末(純度99.9%、フルヤ金属製:参照資料1)およびPt粉末(純度99%、フルヤ金属製:参照試料2)についても同様にCO酸化触媒活性を測定した。
【0043】
まず、反応管(Reaction tube)に10mgの石英綿を詰め、その上から試料粉末を50mg投入した。更に、試料粉末の上から10mgの石英綿を詰め、試料粉末を石英綿が挟み込む形にした。
【0044】
反応管を測定装置に装着した後、ヒックマンポンプ(Hickmamnn pump)を用いて、反応管を含む装置全体を背圧10−3Paまで排気した。反応管とサーキュレーションライン(Circulation line)をつなぐストップコック(Stop cock)を閉じた後、不純物濃度1ppm以下に調整した純粋COガスおよびO2ガスを高圧ボンベからレギュレータを介し、全圧がそれぞれ8×104Paに達するまで、総量3Lのガスリザーバー(Gas reservoir)に充填した。
【0045】
それぞれのガスリザーバーからサーキュレーションライン中に、1.586×104PaのO2ガスを31.60mL、8.44×103PaのCOガスw118.8mL、順次導入した。
【0046】
次に、サーキュレーションポンプ(Circulation pump)を駆動し、サーキュレーションライン内部のガスを循環させ混合した。15分後、全圧104Pa、総量150.4mLのCO:O2(モル比)混合反応ガスを得た。
【0047】
混合反応ガスの調整と並行して、反応管を包み込む形で配置した電気炉を用い、毎分5℃の昇温速度で試料温度を上げた。225、275、325℃のいずれかの温度に達した後、30分間保持して安定化させた。
【0048】
サーキュレーションラインと反応管をつなぐストップコックを開き、反応管に混合反応ガスを導いた。これにより、混合反応ガスは、試料粉末の粒子間を通って、サーキュレーションラインを循環する状態となった。サーキュレーションラインに接続されたガスさんプラスチックー(Gas sampler)により、約7分毎に3mLの混合反応ガスを取り出した。ガスクロマトグラフ(Gas chromatograph、Shimadzu GC−10A)によって混合ガスの組成分析を行なった。混合ガス中のCO2濃度とCO濃度との比を求め、これをCO浄化率(Co conversion)とした。
【0049】
図8(a)に、Ni3Al(比較例)およびNi(参照試料1)のCO酸化触媒活性を示す。縦軸がCO浄化率(CO conversion)、横軸が試料表面に反応ガスが供給された瞬間から経過した時間(Duration)である。
【0050】
225℃においては、Ni3AlもNiも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Niは経過時間25分の時点で15%のCO浄化率を示したが、Ni3Alは同じ時点で1.8%のCO浄化率を示すに留まった。325℃では、Niは経過時間25分の時点で56%のCO浄化率を示したが、Ni3Alは25%のCO浄化率を示すに留まった。すなわち、275℃以上の温度領域では、Ni3AlはNiよりも低い触媒活性を示した。
【0051】
図8(b)に、Ni3Al(比較例)およびPt(参照試料2)のCO酸化触媒活性を示す。225℃においては、Ni3AlもPtも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Ptは経過時間25分の時点で15%のCO浄化率を示し、325℃では、Ptは経過時間25分の時点で100%のCO浄化率を示した。275℃以上の温度領域では、Ni3AlはPtよりも低い触媒活性を示した。
【0052】
図9(a)に、Ni3Ti(本発明例の試料1)およびNi(参照試料1)のCO酸化触媒活性を示す。225℃においては、Ni3TiもNiも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Niは経過時間25分の時点で15%のCO浄化率を示したのに対して、Ni3Tiは同じ時点で42%のCO浄化率を示した。325℃では、Niは経過時間25分の時点で56%のCO浄化率を示したのに対して、Ni3Tiは80%のCO浄化率を示した。すなわち、275℃以上の温度領域では、Ni3TiはNiよりも高い触媒活性を示した。
【0053】
図9(b)に、Ni3Ti(本発明例の試料1)およびPt(参照試料2)のCO酸化触媒活性を示す。225℃においては、Ni3TiもPtも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Ptは経過時間25分の時点で15%のCO浄化率を示したのに対して、Ni3Tiは同じ時点で42%のCO浄化率を示した。325℃では、Ptは経過時間25分の時点で100%のCO浄化率を示したのに対して、Ni3Tiは80%のCO浄化率を示した。すなわち、275℃においては、Ni3TiはPtより高い触媒活性を示すものの、325℃においては、Ni3TiはPtの8割程度の触媒活性を示すに留まった。
【0054】
図10に、Ni3Nb(本発明例の試料2)、Ni(参照試料1)、Pt(参照試料2)のCO酸化触媒活性を示す。225℃において、Ni3Nbは、Ni(図10(a))およびPt(図10(b))と異なり、経過時間10分超において有意の活性(経過時間25分で約10%)を示した。325℃においては、経過時間25分において、Ni3NbはNi(50%)を大きく上回り、Pt(100%)に迫る、83%のCO浄化率を示した。
【0055】
図11に、Ni5Y(本発明例の試料3)、Ni(参照試料1)、Pt(参照試料2)のCO酸化触媒活性を示す。225℃および275℃においては、Ni5Yの触媒活性は、Ni(図11(a))およびPt(図11(b))のいずれの触媒活性よりも低かった。しかし、325℃においては、Ni5Yは、Niを大きく上回り、Ni3Nb(図10)に匹敵する高い触媒活性(経過時間25分で84%)を示した。
【0056】
図12に、Ni(参照試料1)、Pt(参照試料2)、Ni3Al(比較例)、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni5Y(本発明例の試料3)の経過時間10分におけるCO酸化触媒活性を、反応温度の関数として示す。Ni3Alの触媒活性は、275℃以上の温度において、他の全ての試料の触媒活性よりも低い。325℃におけるCO酸化触媒活性は、Ni3Al<Ni<Ni5Y<Ni3Ti<Ni3Nb<Ptの順である。
【0057】
〔参考例〕
本発明例の試料1〜3と同様にして、参考例1および参考例2として、Ni3SnおよびNi3Bの試料を調製し、CO酸化触媒活性を測定した。
【0058】
図13に、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の325℃におけるCO酸化触媒活性を示す。図示したように、Ni3SnはNiよりも僅かに高い触媒活性を示した。一方、Ni3Bの触媒活性はNiよりも大幅に低かった。前述のようにSn、Bは、Niに対して高χ元素であり、Niと合金することにより高い触媒活性を示す可能性のある元素群に属するが、本実験においては期待した効果が認められない。同じSn、BでもNiとの別の金属間化合物あるいは高χ範囲のうちの他の元素について検討の余地がある。
【0059】
図14に、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の価電子d−バンドを示す光電子分光測定結果を示す。Ni3Sn、Ni3B、Niのd−バンドはいずれも、フェルミ準位直下に、Ni3d軌道に由来する鋭いピークが認められる。これに対し、Ni3Ti、Ni3Nbにおいては、フェルミ準位直下のピークは認められず、d−バンド全体がNiに比べて高結合エネルギー側(低エネルギー準位側)にシフトする傾向が認められる。Ni3Ti、Ni3Nbにおいては、d−バンドのエネルギーシフトによってCO分子の表面吸着力が低下した結果、Ni3Sn、Ni3B、Niよりも高いCO酸化浄化活性が発現したものと推測される。
【0060】
図15に、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)のd−バンドセンター(d-band center)と、325℃におけるCO浄化反応開始5分後のCO浄化率との関係を示す。ここで、d−バンドセンターとは、d−バンドの状態密度にエネルギーをかけた寮の積分値を、d−バンドの状態密度の積分値で割った値として定義される。図示したように、d−バンドセンターがNiより低いNi3Sn、Ni3Ti、Ni3Nbの場合には、反応開始後5分後で20%以上のCO浄化率が得られたのに対し、d−バンドセンターがNiより高いNi3Bの場合には、CO浄化率は15%未満に留まっている。
【0061】
なお、Ni3Snは、前記の図13に示すように、325℃、30分の浄化率が70%程度であり、図9、10、11に示すように同じ測定温度および経過時間で80%あるいはそれより高い浄化率を示すNi3Ti、Ni3Nb、Ni5Yに比べて劣る。
【産業上の利用可能性】
【0062】
本発明によれば、貴金属を含まず、300℃以上の高温雰囲気中で安定して存在し、少なくともNiより優れた触媒活性を発揮する排ガス浄化触媒およびその製造方法が提供される。
【技術分野】
【0001】
本発明は、排ガス浄化触媒に関し、特にCO浄化性能の高い排ガス浄化触媒およびその製造方法に関する。
【背景技術】
【0002】
自動車等の内燃機関の排ガスの成分、特に一酸化炭素(CO)ガスを、酸素(O2)ガスまたは酸化窒素(NOx)ガスとともに触媒活物質に接触させることにより、毒性のあるCOガスおよびNOxガスを無毒の二酸化炭素(CO2)ガスおよび窒素(N2)ガスに変換(浄化)することができる。
【0003】
このような排ガス浄化触媒としての活性を示す触媒活物質としては、典型的には白金(Pt)、ロジウム(Rh)等の貴金属が知られている。しかし貴金属には単価が高いという問題がある。そのため、様々な物質が貴金属の代替物質として検討され、貴金属の使用量を低減することが試みられてきた。
【0004】
例えば特許文献1には、酸化セリウム(CeO2)を含む多孔質担体にジルコニウム(Zr)と金(Au)を含有させた触媒が提示されている。
【0005】
また特許文献2には、白金(Pt)、パラジウム(Pd)、および酸化ジルコニウム(ZrO2)と酸化プラセオジウム(Pr6O11)との複合酸化物から成る触媒が提示されている。
【0006】
これらはいずれも貴金属が必須の構成成分である。これまでに、貴金属を全く含まず、少なくともニッケル(Ni)を超える触媒活性を有する触媒活物質は知られていない。
【0007】
また、一般にCOやNOxの浄化反応が進行する300℃〜1000℃程度での高温において、熱的な安定性を備えた触媒活物質も知られていない。
【0008】
特許文献3には、貴金属を含まず、しかもPtと同等のCO浄化活性を示す触媒活物質として、超微粒子状の金属間化合物Ni3Alナノ粒子が開示されている。しかしながらこれは、表面積の小さいPt粒子(0.0066m2)に対して表面積の遥かに大きいNi3Alナノ粒子(0.25〜2.2m2:Ptの約30倍〜約300倍)を比較した結果である。したがって、見かけの触媒活性が触媒粒子の表面積に比例するという周知の事実に照らせば、特許文献3においてNi3Alナノ粒子の触媒活性がPt粒子と同等であるとする結論は全く根拠が無い。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2008−73654号公報
【特許文献2】特開2010−58110号公報
【特許文献3】特開2010−137131号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、貴金属を含まず、300℃以上の高温雰囲気中で安定して存在し、少なくともNiより優れた触媒活性を発揮する排ガス浄化触媒およびその製造方法を提供することを目的とする。
【課題を解決するための手段】
【0011】
上記目的を達成するために、本発明によれば、Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成ることを特徴とする排ガス浄化触媒が提供される。
【0012】
上記目的を達成するために、本発明によれば更に、Niと、Niよりも電気陰性度の低い周期律表3、4、5族から選択した元素とを混合し、溶解、鋳造してインゴットを作製する第1工程、
上記インゴットを均質化熱処理する第2工程、および
上記均質加熱処理したインゴットを機械的に粉砕する第3工程
を含むことを特徴とする排ガス浄化触媒の製造方法が提供される。
【発明の効果】
【0013】
本発明の排ガス浄化触媒は、Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成るので、300℃以上の高温でも熱的に安定であり、かつ、Niを凌ぎ、Ptに迫る高い触媒活性を発揮する。
【図面の簡単な説明】
【0014】
【図1】図1は、Ni−Ti2元系の相図である。
【図2】図2は、Nb−Ni2元系の相図である。
【図3】図3は、Ni−Y2元系の相図である。
【図4】図4は、実施例において排ガス浄化触媒の粉末試料を調製するフローを模式的に示す。
【図5】図5は、実施例において作成した本発明の排ガス浄化触媒試料のX線回折結果を示す。
【図6】図6は、本発明の排ガス浄化触媒の結晶構造を示す。
【図7】図7は、実施例において用いたCO酸化触媒活性評価装置を模式的に示す。
【図8】図8は、(a)Ni3Al(比較例)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni3Al(比較例)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図9】図9は、(a)Ni3Ti(本発明例の試料1)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni3Ti(本発明例の試料1)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図10】図10は、(a)Ni3Nb(本発明例の試料2)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni3Nb(本発明例の試料2)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図11】図11は、(a)Ni5Y(本発明例の試料3)およびNi(参照試料1)のCO酸化触媒活性、および(b)Ni5Y(本発明例の試料3)およびPt(参照試料2)のCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図12】図12は、Ni(参照試料1)、Pt(参照試料2)、Ni3Al(比較例)、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni5Y(本発明例の試料3)の経過時間10分におけるCO酸化触媒活性を、反応温度の関数として示す。横軸が温度(Temperature)、縦軸がCO浄化率(CO conversion)である。
【図13】図13は、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の325℃におけるCO酸化触媒活性を示す。横軸が経過時間(Duration)、縦軸がCO浄化率(CO conversion)である。
【図14】図14は、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の価電子d−バンドを示す光電子分光測定結果を示す。
【図15】図15は、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)のd−バンドセンター(d-band center)と、325℃におけるCO浄化反応開始5分後のCO浄化率との関係を示す。
【発明を実施するための形態】
【0015】
本発明者は下記の着想に基づき、本発明を完成した。
【0016】
浄化反応の際には、排ガス浄化用の触媒活物質の表面と浄化対象である排ガス分子との間では、お互いの原子の最外殻電子の遣り取りが起きる。触媒活性を示さない物質にPt等の貴金属と同様な触媒活性を示す性質を付与するには、構成元素の表面の電子状態を変化させてPt等の貴金属に近い電子状態にする必要がある。
【0017】
先ず、貴金属以外で最良の触媒活性を示すNiをベースに、その電子状態を変えることを構想した。Niの電子状態を変えるには、周期律表でNiとは電子状態の異なる金属との合金化が有効である。電子状態の違いを電気陰性度χ(ポーリングの電気陰性度)でみると、Niのχ=1.91に対して、これよりも低いχ=1.2〜1.6程度の範囲(低χ範囲)と、高いχ=1.95〜2.05程度の範囲(高χ範囲)を対象として着目した。
【0018】
この電気陰性度の範囲は、周期律表でNi(χ=1.91)の属する10族に対して、低χ範囲はTi(同1.54)、Nb(同1.6)、Y(同1.22)などの属する3、4、5族に対応し、高χ範囲はB(同2.04)、Sn(同1.96)などの属する13、14、15族に対応する。
【0019】
下記反応式(1)で表されるCO浄化反応の反応速度は、触媒表面におけるCO吸着とO2解離吸着のバランスによって決定される。Ni単体および低χ元素単体のCO浄化触媒活性はCOの表面吸着力が強すぎるため著しく抑制される。これに対し、Niと低χ元素との合金はCOの非占有分子軌道のエネルギー準位差が広いため、合金表面におけるCO吸着力が弱められ、CO吸着とO2解離吸着のバランスが保たれる結果、Ni単体の表面または低χ元素単体の表面よりも浄化反応が速やかに進行する。
【0020】
CO+1/2O2→CO2……(1)
Niとの合金相手として、Niに対する触媒活性の優位性の観点から、低χ範囲の元素が望ましく、特にTi、Nb、Yが望ましい。
【0021】
Niとこれらとの合金の形態としては、固溶体よりも金属間化合物であることが望ましく、特にNi3Ti、Ni3Nb、Ni5Yであることが望ましい。固溶体合金は、例えば溶解・凝固・均質化熱処理等の製造工程および高温雰囲気中での使用時に、種々の相が生成する虞が高く、安定して単相を確保することが困難であり、望みの触媒活性を安定して得ることが困難である。Ni3Ti、Ni3Nb、Ni5Yの結晶構造は、それぞれP63/mmc、Pmmm、P6/mmmである。
【0022】
金属間化合物は、組成および相の安定性が高いため複数相が生成する虞がなく、常に安定して良好な触媒活性を得ることができる。
【0023】
本発明の望ましい形態による触媒活物質であるNi3Ti、Ni3Nb、Ni5Yは、図1〜3に示すように融点がそれぞれ1380℃(Ni3Ti)、1399℃(Ni3Nb)、1431℃(Ni5Y)である。これは、COおよびNOx浄化触媒の通常の使用温度範囲である300℃〜1000℃程度に対して遥かに高温であり、使用中の安定性は確保される。
【0024】
本発明の排ガス浄化触媒は以下のように製造することができる。
【0025】
Niと低χ元素とを混合し、溶解してインゴットを作製し、このインゴットを非酸化性雰囲気中で均質化のための熱処理を施す。
【0026】
具体的には、先ず、Niと低χ元素を望みのモル比で秤量し、典型的には酸素および水分濃度が5ppm以下のアルゴンガス雰囲気下で混合、溶解し、ボタン状のインゴットを得る。
【0027】
得られたインゴットをタンタル等の高融点金属箔に包み、酸素吸収剤とともに減圧下で石英管に封入する。この石英管を電気炉中に装入し、均質化のための熱処理を施す。その後、電気炉から石英管を取り出し、室温まで徐冷する。石英管を割り、試料を取り出した後、機械的に粉砕する。得られた粉末試料を篩い分けにより粉末粒径を揃え排ガス浄化触媒を得る。
【0028】
均質化のための熱処理温度は、合金の融点から500℃程度を減じた温度以上で、融点未満であることが望ましく、合金の融点から300℃程度を減じた温度以下であることがより望ましい。例えば、Ni3Ti、Ni3Nb、Ni5Yの融点はそれぞれ、1380℃、1399℃、1431℃であるから、それぞれ望ましい均質化熱処理温度範囲は、880〜1380℃、899〜1399℃、931〜1431℃であり、より望ましい範囲は880〜1080℃、899〜1099℃、931〜1131℃である。
【0029】
均質化熱処理の時間は、50時間以上とすることが望ましく、100時間以上とすることがより望ましい。実際の製造時間の観点から、処理時間は150時間以下とすることが望ましい。
【0030】
なお、本発明の排ガス浄化触媒の製造は、上記溶解法に限定する必要は無く、レーザーアブレーション、スパッタリング、溶液還元法等を適用することもできる。これらの方法を用いることにより、合金粉末の粒径等を制御し、例えば均一な大きさのナノ粒子から成る排ガス浄化触媒を実現することができる。
【0031】
以上はNiをベースとした合金について説明したが、Ni以外にもFe、Co、Cuをベースとして合金も可能性がある。Niは元素の周期律表でPtと同族であり最外殻電子の状態はPtと近く、周期律表でNiの近くに位置するFe、Co、Cuは貴金属のRu、Rh、Auと同族であり、上記と同様な考え方で触媒活性を高められる物質の構成元素となる可能性が考えられる。すなわち、周期律表でFe、Co、Ni、Cuの属する8、9、10、11族の元素と、低χ元素のTi、Nb、Yなどの属する3、4、5族の元素との合金または、高χ元素のB、Snなどの属する13、14、15族の元素との合金についても、更に検討する価値がある。
【0032】
また、本発明の排ガス浄化触媒は、CO、NOxのみでなく、炭化水素CxHxの浄化触媒としても可能性がある。
【実施例】
【0033】
<試料の製造>
本発明例として、金属間化合物から成る排ガス浄化触媒Ni3Ti(試料1)、Ni3Nb(試料2)、Ni5Y(試料3)を、図4に模式的に示す手順および条件にて製造した。
【0034】
先ず、金属ニッケル(純度99.9%、フルヤ金属製)、金属チタン(純度99%、フルヤ金属製)、金属ニオブ(純度99%、フルヤ金属製)、金属イットリウム(純度98%、フルヤ金属製)を、それぞれモル比でNi:Ti=3:1(試料1)、Ni:Nb=3:1(試料2)、Ni:Y=5:1(試料3)に総量3g秤量した。
【0035】
次に、各試料を、酸素濃度および水分濃度がいずれも5ppmである純粋アルゴンガス雰囲気下でアーク溶解し、ボタン状のインゴットを得た。
【0036】
比較例として、高純度化学研究所(株)製のアトマイズNi3Al粉末を、受領したままの状態で用いた。
【0037】
次に、インゴットをタンタル箔に包み、酸素吸収剤としてジルコニウム箔と共に背圧10−3Paで石英管に封入した。石英管を電気炉内に装入し、950℃×100時間の均質化熱処理を行なった。その後、電気炉から石英管を取り出し、室温まで徐冷した。石英管を割り、試料を取り出した後、メノウ乳鉢で機械粉砕した。得られた粉末試料を63μmメッシュのステンレス製篩にかけ、篩を通過した粉末を回収した。この粉末を更に53μmメッシュのステンレス製篩にかけ、篩に残った粉末を回収した。これにより、53μm〜63μmに粉末粒径を揃えた本発明の排ガス浄化触媒の試料1、2、3を得た。
【0038】
比較例のNi3Al試料についても同様に篩い分けを行なって粉末粒径を53μm〜63μmに揃えた。
【0039】
<X線回折による試料の同定>
X線回折測定装置(CuKα線:リガク製RIN2000)を用い、常温常圧大気下にて、測定インクリメント=0.02°、スキャン幅2θ=5〜95°の条件で、試料1〜3のX線回折測定を行なった。
【0040】
図5の(a)、(b)、(c)に試料1、2、3の回折結果を示す。ただし、図中の縦線は、Ni3Ti、Ni3Nb、Ni5Yの結晶データを用いて計算したシミュレーション結果である。図から分かるように、各試料の回折ピークとシミュレーションピークとはよく一致しており、試料1、2、3がそれぞれNi3Ti、Ni3Nb、Ni5Yの単相であることが確認できる。比較例の試料についても同様のX線回折測定を行いNi3Al(Cu3Au型構造、Fm3m)の単相であることが確認された。
【0041】
図6に、(a)Ni3Ti、(b)Ni3Nb、(c)Ni5Yの結晶構造を示す。それぞれ(a)試料1Ni3Ti(P63/mmc:a、b=0.5109nm、c=0.8299nm)、(b)試料2Ni3Nb(Pmmm:a、b、c=0.4565nm、0.5116nm、0.4260nm)、(c)試料3Ni5Y(P6/mmm:a、b=0.4833nm、c=0.3967nm)に対応する。
【0042】
<触媒活性の評価>
図7に示す気流循環式触媒活性評価装置(CO酸化触媒活性測定装置)を用いて、実施例の試料1〜3および比較例の試料のCO酸化触媒活性を測定した。更に、参照試料として、同じく篩い分けによって粉末粒径を53μm〜63μmに揃えたNi粉末(純度99.9%、フルヤ金属製:参照資料1)およびPt粉末(純度99%、フルヤ金属製:参照試料2)についても同様にCO酸化触媒活性を測定した。
【0043】
まず、反応管(Reaction tube)に10mgの石英綿を詰め、その上から試料粉末を50mg投入した。更に、試料粉末の上から10mgの石英綿を詰め、試料粉末を石英綿が挟み込む形にした。
【0044】
反応管を測定装置に装着した後、ヒックマンポンプ(Hickmamnn pump)を用いて、反応管を含む装置全体を背圧10−3Paまで排気した。反応管とサーキュレーションライン(Circulation line)をつなぐストップコック(Stop cock)を閉じた後、不純物濃度1ppm以下に調整した純粋COガスおよびO2ガスを高圧ボンベからレギュレータを介し、全圧がそれぞれ8×104Paに達するまで、総量3Lのガスリザーバー(Gas reservoir)に充填した。
【0045】
それぞれのガスリザーバーからサーキュレーションライン中に、1.586×104PaのO2ガスを31.60mL、8.44×103PaのCOガスw118.8mL、順次導入した。
【0046】
次に、サーキュレーションポンプ(Circulation pump)を駆動し、サーキュレーションライン内部のガスを循環させ混合した。15分後、全圧104Pa、総量150.4mLのCO:O2(モル比)混合反応ガスを得た。
【0047】
混合反応ガスの調整と並行して、反応管を包み込む形で配置した電気炉を用い、毎分5℃の昇温速度で試料温度を上げた。225、275、325℃のいずれかの温度に達した後、30分間保持して安定化させた。
【0048】
サーキュレーションラインと反応管をつなぐストップコックを開き、反応管に混合反応ガスを導いた。これにより、混合反応ガスは、試料粉末の粒子間を通って、サーキュレーションラインを循環する状態となった。サーキュレーションラインに接続されたガスさんプラスチックー(Gas sampler)により、約7分毎に3mLの混合反応ガスを取り出した。ガスクロマトグラフ(Gas chromatograph、Shimadzu GC−10A)によって混合ガスの組成分析を行なった。混合ガス中のCO2濃度とCO濃度との比を求め、これをCO浄化率(Co conversion)とした。
【0049】
図8(a)に、Ni3Al(比較例)およびNi(参照試料1)のCO酸化触媒活性を示す。縦軸がCO浄化率(CO conversion)、横軸が試料表面に反応ガスが供給された瞬間から経過した時間(Duration)である。
【0050】
225℃においては、Ni3AlもNiも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Niは経過時間25分の時点で15%のCO浄化率を示したが、Ni3Alは同じ時点で1.8%のCO浄化率を示すに留まった。325℃では、Niは経過時間25分の時点で56%のCO浄化率を示したが、Ni3Alは25%のCO浄化率を示すに留まった。すなわち、275℃以上の温度領域では、Ni3AlはNiよりも低い触媒活性を示した。
【0051】
図8(b)に、Ni3Al(比較例)およびPt(参照試料2)のCO酸化触媒活性を示す。225℃においては、Ni3AlもPtも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Ptは経過時間25分の時点で15%のCO浄化率を示し、325℃では、Ptは経過時間25分の時点で100%のCO浄化率を示した。275℃以上の温度領域では、Ni3AlはPtよりも低い触媒活性を示した。
【0052】
図9(a)に、Ni3Ti(本発明例の試料1)およびNi(参照試料1)のCO酸化触媒活性を示す。225℃においては、Ni3TiもNiも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Niは経過時間25分の時点で15%のCO浄化率を示したのに対して、Ni3Tiは同じ時点で42%のCO浄化率を示した。325℃では、Niは経過時間25分の時点で56%のCO浄化率を示したのに対して、Ni3Tiは80%のCO浄化率を示した。すなわち、275℃以上の温度領域では、Ni3TiはNiよりも高い触媒活性を示した。
【0053】
図9(b)に、Ni3Ti(本発明例の試料1)およびPt(参照試料2)のCO酸化触媒活性を示す。225℃においては、Ni3TiもPtも、全測定範囲に亘り、有意の活性を示さなかった。275℃では、Ptは経過時間25分の時点で15%のCO浄化率を示したのに対して、Ni3Tiは同じ時点で42%のCO浄化率を示した。325℃では、Ptは経過時間25分の時点で100%のCO浄化率を示したのに対して、Ni3Tiは80%のCO浄化率を示した。すなわち、275℃においては、Ni3TiはPtより高い触媒活性を示すものの、325℃においては、Ni3TiはPtの8割程度の触媒活性を示すに留まった。
【0054】
図10に、Ni3Nb(本発明例の試料2)、Ni(参照試料1)、Pt(参照試料2)のCO酸化触媒活性を示す。225℃において、Ni3Nbは、Ni(図10(a))およびPt(図10(b))と異なり、経過時間10分超において有意の活性(経過時間25分で約10%)を示した。325℃においては、経過時間25分において、Ni3NbはNi(50%)を大きく上回り、Pt(100%)に迫る、83%のCO浄化率を示した。
【0055】
図11に、Ni5Y(本発明例の試料3)、Ni(参照試料1)、Pt(参照試料2)のCO酸化触媒活性を示す。225℃および275℃においては、Ni5Yの触媒活性は、Ni(図11(a))およびPt(図11(b))のいずれの触媒活性よりも低かった。しかし、325℃においては、Ni5Yは、Niを大きく上回り、Ni3Nb(図10)に匹敵する高い触媒活性(経過時間25分で84%)を示した。
【0056】
図12に、Ni(参照試料1)、Pt(参照試料2)、Ni3Al(比較例)、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni5Y(本発明例の試料3)の経過時間10分におけるCO酸化触媒活性を、反応温度の関数として示す。Ni3Alの触媒活性は、275℃以上の温度において、他の全ての試料の触媒活性よりも低い。325℃におけるCO酸化触媒活性は、Ni3Al<Ni<Ni5Y<Ni3Ti<Ni3Nb<Ptの順である。
【0057】
〔参考例〕
本発明例の試料1〜3と同様にして、参考例1および参考例2として、Ni3SnおよびNi3Bの試料を調製し、CO酸化触媒活性を測定した。
【0058】
図13に、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の325℃におけるCO酸化触媒活性を示す。図示したように、Ni3SnはNiよりも僅かに高い触媒活性を示した。一方、Ni3Bの触媒活性はNiよりも大幅に低かった。前述のようにSn、Bは、Niに対して高χ元素であり、Niと合金することにより高い触媒活性を示す可能性のある元素群に属するが、本実験においては期待した効果が認められない。同じSn、BでもNiとの別の金属間化合物あるいは高χ範囲のうちの他の元素について検討の余地がある。
【0059】
図14に、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)の価電子d−バンドを示す光電子分光測定結果を示す。Ni3Sn、Ni3B、Niのd−バンドはいずれも、フェルミ準位直下に、Ni3d軌道に由来する鋭いピークが認められる。これに対し、Ni3Ti、Ni3Nbにおいては、フェルミ準位直下のピークは認められず、d−バンド全体がNiに比べて高結合エネルギー側(低エネルギー準位側)にシフトする傾向が認められる。Ni3Ti、Ni3Nbにおいては、d−バンドのエネルギーシフトによってCO分子の表面吸着力が低下した結果、Ni3Sn、Ni3B、Niよりも高いCO酸化浄化活性が発現したものと推測される。
【0060】
図15に、Ni3Ti(本発明例の試料1)、Ni3Nb(本発明例の試料2)、Ni3Sn(参考例1)、Ni3B(参考例2)、Ni(参照試料1)のd−バンドセンター(d-band center)と、325℃におけるCO浄化反応開始5分後のCO浄化率との関係を示す。ここで、d−バンドセンターとは、d−バンドの状態密度にエネルギーをかけた寮の積分値を、d−バンドの状態密度の積分値で割った値として定義される。図示したように、d−バンドセンターがNiより低いNi3Sn、Ni3Ti、Ni3Nbの場合には、反応開始後5分後で20%以上のCO浄化率が得られたのに対し、d−バンドセンターがNiより高いNi3Bの場合には、CO浄化率は15%未満に留まっている。
【0061】
なお、Ni3Snは、前記の図13に示すように、325℃、30分の浄化率が70%程度であり、図9、10、11に示すように同じ測定温度および経過時間で80%あるいはそれより高い浄化率を示すNi3Ti、Ni3Nb、Ni5Yに比べて劣る。
【産業上の利用可能性】
【0062】
本発明によれば、貴金属を含まず、300℃以上の高温雰囲気中で安定して存在し、少なくともNiより優れた触媒活性を発揮する排ガス浄化触媒およびその製造方法が提供される。
【特許請求の範囲】
【請求項1】
Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成ることを特徴とする排ガス浄化触媒。
【請求項2】
請求項1において、CO浄化用であることを特徴とする排ガス浄化触媒。
【請求項3】
請求項1または2において、上記Ni3Tiは結晶構造P63/mmc(a、b=0.5109nm、c=0.8299nm)、上記Ni3Nbは結晶構造Pmmm(a、b、c=0.4565nm、0.5116nm、0.4260nm)、上記Ni5Yは結晶構造P6/mmm(a、b=0.4833nm、c=0.3967nm)であることを特徴とする排ガス浄化触媒。
【請求項4】
請求項1〜3のいずれか1項に記載の排ガス浄化触媒を製造する方法であって、
Niと、Niよりも電気陰性度の低い周期律表3、4、5族から選択した元素とを混合し、溶解、鋳造してインゴットを作製する第1工程、
上記インゴットを均質化熱処理する第2工程、および
上記均質加熱処理したインゴットを機械的に粉砕する第3工程
を含むことを特徴とする排ガス浄化触媒の製造方法。
【請求項5】
請求項4において、上記第1工程で、上記Niと混合する元素は、周期律表3族のY、周期律表4族のTi、周期律表5族のNbのうちから選択することを特徴とする排ガス浄化触媒の製造方法。
【請求項6】
請求項5において、上記第1工程で、Yを選択し、モル比でNi:Y=5:1となるように混合し、溶解、鋳造してNi5Yのインゴットを作製することを特徴とする排ガス浄化触媒の製造方法。
【請求項7】
請求項5において、上記第1工程で、Tiを選択し、モル比でNi:Ti=3:1となるように混合し、溶解、鋳造してNi3Tiのインゴットを作製することを特徴とする排ガス浄化触媒の製造方法。
【請求項8】
請求項5において、上記第1工程で、Nbを選択し、モル比でNi:Nb=3:1となるように混合し、溶解、鋳造してNi3Nbのインゴットを作製することを特徴とする排ガス浄化触媒の製造方法。
【請求項9】
請求項4〜8のいずれか1項において、上記第1工程で、酸素濃度および水分濃度がいずれも5ppmである純粋アルゴンガス雰囲気下でアーク溶解することを特徴とする排ガス浄化触媒の製造方法。
【請求項10】
請求項4〜9のいずれか1項において、上記第2工程で、均質化熱処理の温度は、インゴットの合金の融点より500℃低く、融点未満であることを特徴とする排ガス浄化触媒の製造方法。
【請求項11】
請求項10において、上記均質加熱処理の温度は、上記融点より300℃低いことを特徴とする排ガス浄化触媒の製造方法。
【請求項1】
Ni3Ti、Ni3Nb、Ni5Yのいずれか1種の金属間化合物から成ることを特徴とする排ガス浄化触媒。
【請求項2】
請求項1において、CO浄化用であることを特徴とする排ガス浄化触媒。
【請求項3】
請求項1または2において、上記Ni3Tiは結晶構造P63/mmc(a、b=0.5109nm、c=0.8299nm)、上記Ni3Nbは結晶構造Pmmm(a、b、c=0.4565nm、0.5116nm、0.4260nm)、上記Ni5Yは結晶構造P6/mmm(a、b=0.4833nm、c=0.3967nm)であることを特徴とする排ガス浄化触媒。
【請求項4】
請求項1〜3のいずれか1項に記載の排ガス浄化触媒を製造する方法であって、
Niと、Niよりも電気陰性度の低い周期律表3、4、5族から選択した元素とを混合し、溶解、鋳造してインゴットを作製する第1工程、
上記インゴットを均質化熱処理する第2工程、および
上記均質加熱処理したインゴットを機械的に粉砕する第3工程
を含むことを特徴とする排ガス浄化触媒の製造方法。
【請求項5】
請求項4において、上記第1工程で、上記Niと混合する元素は、周期律表3族のY、周期律表4族のTi、周期律表5族のNbのうちから選択することを特徴とする排ガス浄化触媒の製造方法。
【請求項6】
請求項5において、上記第1工程で、Yを選択し、モル比でNi:Y=5:1となるように混合し、溶解、鋳造してNi5Yのインゴットを作製することを特徴とする排ガス浄化触媒の製造方法。
【請求項7】
請求項5において、上記第1工程で、Tiを選択し、モル比でNi:Ti=3:1となるように混合し、溶解、鋳造してNi3Tiのインゴットを作製することを特徴とする排ガス浄化触媒の製造方法。
【請求項8】
請求項5において、上記第1工程で、Nbを選択し、モル比でNi:Nb=3:1となるように混合し、溶解、鋳造してNi3Nbのインゴットを作製することを特徴とする排ガス浄化触媒の製造方法。
【請求項9】
請求項4〜8のいずれか1項において、上記第1工程で、酸素濃度および水分濃度がいずれも5ppmである純粋アルゴンガス雰囲気下でアーク溶解することを特徴とする排ガス浄化触媒の製造方法。
【請求項10】
請求項4〜9のいずれか1項において、上記第2工程で、均質化熱処理の温度は、インゴットの合金の融点より500℃低く、融点未満であることを特徴とする排ガス浄化触媒の製造方法。
【請求項11】
請求項10において、上記均質加熱処理の温度は、上記融点より300℃低いことを特徴とする排ガス浄化触媒の製造方法。
【図5】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図1】


【図2】


【図3】


【図4】


【図6】




【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図1】


【図2】


【図3】


【図4】


【図6】


【公開番号】特開2013−71023(P2013−71023A)
【公開日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願番号】特願2011−209600(P2011−209600)
【出願日】平成23年9月26日(2011.9.26)
【出願人】(000003207)トヨタ自動車株式会社 (59,920)
【出願人】(301023238)独立行政法人物質・材料研究機構 (1,333)
【Fターム(参考)】
【公開日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願日】平成23年9月26日(2011.9.26)
【出願人】(000003207)トヨタ自動車株式会社 (59,920)
【出願人】(301023238)独立行政法人物質・材料研究機構 (1,333)
【Fターム(参考)】
[ Back to top ]

