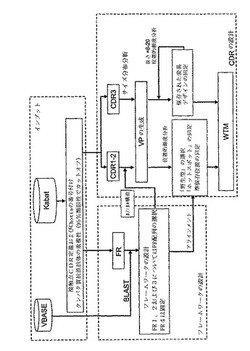
推定成熟CDRのブラスティングならびにコホートライブラリの作製およびスクリーニングによる抗体の超ヒト化
【課題】 参照抗体ライブラリ、例えばユニバーサル抗体ライブラリに含まれるヒトの多様性情報を合理的に利用する改善されたユニバーサル抗体ライブラリに関する方法および組成物を提供すること。
【解決手段】 開示されるプロセスは、クエリーCDR配列を使用して参照ライブラリに存在するヒト抗体の多様性を本発明のコホートライブラリに指揮することを含むものである。疾患を処置するのに適した治療剤を単離するためのこのようなコホートライブラリを作製およびスクリーニングする方法も開示される。
【解決手段】 開示されるプロセスは、クエリーCDR配列を使用して参照ライブラリに存在するヒト抗体の多様性を本発明のコホートライブラリに指揮することを含むものである。疾患を処置するのに適した治療剤を単離するためのこのようなコホートライブラリを作製およびスクリーニングする方法も開示される。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
少なくとも一つの相補性決定領域(CDR)をコードするポリヌクレオチドのライブラリを作製する方法であって、
a)天然に存在するCDRアミノ酸領域を含む参照抗体ライブラリに存在するCDRアミノ酸配列のバリエーションを、CDRの各アミノ酸残基の位置で決定すること;
b)標的抗原に対する抗体由来のクエリーCDRペプチド配列と参照抗体ライブラリのCDR配列のアラインメントを行うこと;および
c)合成されるライブラリのCDR配列の大部分に関して、
(i)CDR配列内の任意の一つの位置でコードされるアミノ酸残基が、候補抗原に対する抗体由来のクエリーCDRペプチド配列の対応するアラインメントを行った位置のアミノ酸残基と同一であるか;または
(ii)アラインメントを行った位置においてクエリーCDRペプチド配列と同一のアミノ酸残基が参照ライブラリに存在しない場合は、既定のアミノ酸残基である、
CDR配列をコードするポリヌクレオチドのライブラリを合成することを含み、
それによって、一つまたはそれ以上の残基の位置において天然に存在するアミノ酸残基が豊富な、標的抗原に対する抗体由来のクエリーCDRペプチド配列のCDRアナログをコードするポリヌクレオチドのライブラリが提供される、上記方法。
【請求項2】
アラインメントを行うクエリーCDRのアミノ酸長が4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、および25である、請求項1に記載の方法。
【請求項3】
既定のアミノ酸残基が、
グリシン(G)およびアラニン(A)からなる群より選択される小型の側鎖のアミノ酸残基;
セリン(S)、スレオニン(T)、システイン(C)、およびヒスチジン(H)からなる群より選択される求核性側鎖のアミノ酸残基;
バリン(V)、ロイシン(L)、イソロイシン(I)、メチオニン(M)、およびプロリン(P)からなる群より選択される疎水性側鎖のアミノ酸残基;
フェニルアラニン(F)、チロシン(Y)、およびトリプトファン(W)からなる群より選択される芳香族側鎖のアミノ酸残基;
アスパラギン酸(D)およびグルタミン酸(E)からなる群より選択される酸性側鎖のアミノ酸残基;
アスパラギン(N)およびグルタミン(Q)からなる群より選択されるアミド側鎖のアミノ酸残基;または
リジン(K)およびアルギニン(R)からなる群より選択される塩基性側鎖のアミノ酸残基、
である、請求項1に記載の方法。
【請求項4】
アラインメントが、ギャップ導入アラインメント、完全アラインメント、不連続アラインメント、またはそれらの組み合わせからなる群より選択されるプロセスによるものである、請求項1に記載の方法。
【請求項5】
CDRが、EUインデックス、Kabat、Chothiaに従い、または接触点の定義に基づき規定される、請求項1に記載の方法。
【請求項6】
請求項1に記載の方法により作製されたライブラリ。
【請求項7】
少なくとも一つの相補性決定領域(CDR)を含む抗原結合領域のライブラリであって、ライブラリのCDR配列の大部分において、
(i)CDR配列内の任意の一つの位置のアミノ酸残基が、標的抗原に対する抗体由来のクエリーCDRペプチド配列の対応するアラインメントを行った位置のアミノ酸残基と同一であるか;または
(ii)アラインメントを行った位置にクエリーCDRペプチド配列と同一のアミノ酸残基が参照ライブラリに存在しない場合は、既定のアミノ酸残基であり、
それによって、一つまたはそれ以上の残基の位置において天然に存在するアミノ酸残基が豊富な、候補抗原に対する抗体由来のクエリーCDRペプチド配列のCDRアナログのライブラリが提供される、上記ライブラリ。
【請求項8】
参照抗体ライブラリの標的抗原がタンパク質、ペプチド、低分子、脂質、多糖類、またはポリヌクレオチドである、請求項6または7に記載のライブラリ。
【請求項9】
クエリーCDRペプチド配列が合成CDR配列または脊椎動物CDR配列である、請求項6または7に記載のライブラリ。
【請求項10】
脊椎動物CDR配列がヒト、霊長類、マウス、ラット、ウサギ、またはニワトリ配列である、請求項6または7に記載のライブラリ。
【請求項11】
クエリーCDRペプチド配列が標的抗原に結合する、請求項6または7に記載のライブラリ。
【請求項12】
標的抗原がタンパク質、ペプチド、低分子、多糖類、またはポリヌクレオチドである、請求項11に記載のライブラリ。
【請求項13】
ライブラリ配列の10%より多くが既知の天然に存在するCDR配列を含む、請求項6または7に記載のライブラリ。
【請求項14】
ライブラリ配列の50%より多くが既知の天然に存在するCDR配列を含む、請求項6または7に記載のライブラリ。
【請求項15】
ライブラリ配列の80%より多くが既知の天然に存在するCDR配列を含む、請求項6または7に記載のライブラリ。
【請求項16】
ライブラリが、任意の所定のCDRについて既知の天然に存在する多様性のみを含む、請求項6または7に記載のライブラリ。
【請求項17】
ライブラリが、ヒトCDRについての全ての既知のCDRの多様性を含む、請求項6または7に記載のライブラリ。
【請求項18】
ライブラリが、ある抗原クラスについての全ての既知のCDRの多様性を含む、請求項6または7に記載のライブラリ。
【請求項19】
CDRアナログが、CDR−H1、CDR−H2、CDR−H3、CDR−L1、CDR−L2、CDR−L3、およびそれらの組み合わせからなる群より選択される、請求項6または7に記載のライブラリ。
【請求項20】
クエリーCDR配列が、CDR−H1、CDR−H2、CDR−H3、CDR−L1、CDR−L2、およびCDR−L3からなる群より選択される、請求項6または7に記載のライブラリ。
【請求項21】
二以上のCDRのアラインメントを行い、一つの合成CDRライブラリ配列の多様性が、直線的に連結されたCDRの可変性に基づき規定、拡張、または制限される、請求項6または7に記載のライブラリ。
【請求項22】
CDR−H1が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項23】
CDR−H2が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項24】
CDR−H3が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項25】
CDR−L1が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項26】
CDR−L2が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項27】
CDR−L3が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項28】
軽鎖CDR−L1(ラムダ(L))が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項29】
軽鎖CDR−L1(カッパ(K))が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項30】
軽鎖CDR−L2が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項31】
軽鎖CDR−L3が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項32】
CDRアナログが、図9〜31、34〜36、または44〜61のいずれかに示されるアミノ酸配列を含む、請求項15に記載のライブラリ。
【請求項33】
CDRアナログが含む多様性は、CDRアナログ内の一つまたはそれ以上の残基を縮重コドン、ウォークスルー型変異誘発、またはルックスルー型変異誘発を用いて示されるものである、請求項6または7に記載のライブラリ。
【請求項34】
抗体結合領域がさらに、一つまたはそれ以上のアミノ酸置換、挿入、または欠失を含む、請求項6または7に記載のライブラリ。
【請求項35】
抗原結合領域がさらに、ヒト、霊長類、マウス、ラット、ウサギ、またはニワトリ由来の天然に存在するフレームワーク領域を含む、請求項6または7に記載のライブラリ。
【請求項36】
天然に存在するフレームワーク領域がVH1、VH3、またはVH4である、請求項6または7に記載のライブラリ。
【請求項37】
ヒトフレームワーク領域が、軽鎖フレームワーク領域、重鎖フレームワーク領域、交配クローニングされたフレームワーク領域、コンセンサスフレームワーク領域、またはそれらの組み合わせである、請求項35に記載のライブラリ。
【請求項38】
ヒトフレームワーク領域が、一つまたはそれ以上のヒトCDR領域との直線的接続におけるそれらの出現頻度に従い選択される、請求項37に記載のライブラリ。
【請求項39】
CDR間のヒトフレームワーク領域をアイソタイプ一致させた、請求項37に記載のライブラリ。
【請求項40】
ライブラリが発現ライブラリである、請求項6または7に記載のライブラリ。
【請求項41】
発現ライブラリが、リボソームディスプレイライブラリ、ポリソームディスプレイライブラリ、ファージディスプレイライブラリ、ウイルスディスプレイライブラリ、細菌発現ライブラリ、酵母ディスプレイライブラリ、および哺乳動物ディスプレイライブラリからなる群より選択される、請求項40に記載のライブラリ。
【請求項42】
一つまたはそれ以上のフレームワーク領域および一つまたはそれ以上のCDR領域をコードする、既定のポリヌクレオチドを合成することによって作製され、これらの領域をコードするポリヌクレオチドがさらに十分に重複する配列を含み、それによって、ポリメラーゼ連鎖反応(PCR)条件下でこのポリヌクレオチド配列から完全な抗体結合領域をコードするポリヌクレオチドが構築され得る、請求項6または7に記載のライブラリ。
【請求項43】
請求項6または7に記載のライブラリのポリヌクレオチドによりコードされる抗体結合領域。
【請求項44】
抗体結合領域を生成させるために請求項40に記載の発現ライブラリを発現させること、および
所望の結合親和性を有する抗体結合領域を選択するために抗体結合領域をスクリーニングすることを含む、
所望の結合親和性を有するポリペプチドの同定方法。
【請求項45】
スクリーニングが抗原結合領域を標的基質と接触させることを含み、抗体結合領域が抗体結合領域をコードするポリヌクレオチドと関連付けられている、請求項44に記載の方法。
【請求項46】
選択された抗体結合領域をコードするポリヌクレオチドを同定する工程をさらに含む、請求項44に記載の方法。
【請求項47】
ポリヌクレオチドが、リボソームディスプレイライブラリ、ポリソームディスプレイライブラリ、ファージディスプレイライブラリ、ウイルスディスプレイライブラリ、細菌発現ライブラリ、酵母ディスプレイライブラリ、および哺乳動物ディスプレイライブラリからなる群より選択される発現ディスプレイを用いて抗体結合領域と関連付けられる、請求項46に記載の方法。
【請求項48】
請求項45〜47のいずれか一項に記載の方法に従い同定される抗体結合領域。
【請求項49】
一つまたはそれ以上の工程がコンピューター支援により行われる、請求項44〜48のいずれかに記載の方法。
【請求項50】
請求項49に記載の方法の一つまたはそれ以上の工程を実行するための指令を含む、電子機器において使用するのに適した媒体。
【請求項51】
請求項49に記載の方法の一つまたはそれ以上の工程を実行するための機器。
【請求項52】
a)図または表のいずれかに示される配列を有する一つまたはそれ以上のフレームワーク領域;および
b)図または表のいずれかに示される配列を有する一つまたはそれ以上のCDR領域、を含む抗体結合領域をコードし、a)のフレームワーク領域およびb)のCDR領域が一緒になって既定の抗原に対する抗体結合領域を形成する、ポリヌクレオチドのライブラリ。
【請求項1】
少なくとも一つの相補性決定領域(CDR)をコードするポリヌクレオチドのライブラリを作製する方法であって、
a)天然に存在するCDRアミノ酸領域を含む参照抗体ライブラリに存在するCDRアミノ酸配列のバリエーションを、CDRの各アミノ酸残基の位置で決定すること;
b)標的抗原に対する抗体由来のクエリーCDRペプチド配列と参照抗体ライブラリのCDR配列のアラインメントを行うこと;および
c)合成されるライブラリのCDR配列の大部分に関して、
(i)CDR配列内の任意の一つの位置でコードされるアミノ酸残基が、候補抗原に対する抗体由来のクエリーCDRペプチド配列の対応するアラインメントを行った位置のアミノ酸残基と同一であるか;または
(ii)アラインメントを行った位置においてクエリーCDRペプチド配列と同一のアミノ酸残基が参照ライブラリに存在しない場合は、既定のアミノ酸残基である、
CDR配列をコードするポリヌクレオチドのライブラリを合成することを含み、
それによって、一つまたはそれ以上の残基の位置において天然に存在するアミノ酸残基が豊富な、標的抗原に対する抗体由来のクエリーCDRペプチド配列のCDRアナログをコードするポリヌクレオチドのライブラリが提供される、上記方法。
【請求項2】
アラインメントを行うクエリーCDRのアミノ酸長が4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、および25である、請求項1に記載の方法。
【請求項3】
既定のアミノ酸残基が、
グリシン(G)およびアラニン(A)からなる群より選択される小型の側鎖のアミノ酸残基;
セリン(S)、スレオニン(T)、システイン(C)、およびヒスチジン(H)からなる群より選択される求核性側鎖のアミノ酸残基;
バリン(V)、ロイシン(L)、イソロイシン(I)、メチオニン(M)、およびプロリン(P)からなる群より選択される疎水性側鎖のアミノ酸残基;
フェニルアラニン(F)、チロシン(Y)、およびトリプトファン(W)からなる群より選択される芳香族側鎖のアミノ酸残基;
アスパラギン酸(D)およびグルタミン酸(E)からなる群より選択される酸性側鎖のアミノ酸残基;
アスパラギン(N)およびグルタミン(Q)からなる群より選択されるアミド側鎖のアミノ酸残基;または
リジン(K)およびアルギニン(R)からなる群より選択される塩基性側鎖のアミノ酸残基、
である、請求項1に記載の方法。
【請求項4】
アラインメントが、ギャップ導入アラインメント、完全アラインメント、不連続アラインメント、またはそれらの組み合わせからなる群より選択されるプロセスによるものである、請求項1に記載の方法。
【請求項5】
CDRが、EUインデックス、Kabat、Chothiaに従い、または接触点の定義に基づき規定される、請求項1に記載の方法。
【請求項6】
請求項1に記載の方法により作製されたライブラリ。
【請求項7】
少なくとも一つの相補性決定領域(CDR)を含む抗原結合領域のライブラリであって、ライブラリのCDR配列の大部分において、
(i)CDR配列内の任意の一つの位置のアミノ酸残基が、標的抗原に対する抗体由来のクエリーCDRペプチド配列の対応するアラインメントを行った位置のアミノ酸残基と同一であるか;または
(ii)アラインメントを行った位置にクエリーCDRペプチド配列と同一のアミノ酸残基が参照ライブラリに存在しない場合は、既定のアミノ酸残基であり、
それによって、一つまたはそれ以上の残基の位置において天然に存在するアミノ酸残基が豊富な、候補抗原に対する抗体由来のクエリーCDRペプチド配列のCDRアナログのライブラリが提供される、上記ライブラリ。
【請求項8】
参照抗体ライブラリの標的抗原がタンパク質、ペプチド、低分子、脂質、多糖類、またはポリヌクレオチドである、請求項6または7に記載のライブラリ。
【請求項9】
クエリーCDRペプチド配列が合成CDR配列または脊椎動物CDR配列である、請求項6または7に記載のライブラリ。
【請求項10】
脊椎動物CDR配列がヒト、霊長類、マウス、ラット、ウサギ、またはニワトリ配列である、請求項6または7に記載のライブラリ。
【請求項11】
クエリーCDRペプチド配列が標的抗原に結合する、請求項6または7に記載のライブラリ。
【請求項12】
標的抗原がタンパク質、ペプチド、低分子、多糖類、またはポリヌクレオチドである、請求項11に記載のライブラリ。
【請求項13】
ライブラリ配列の10%より多くが既知の天然に存在するCDR配列を含む、請求項6または7に記載のライブラリ。
【請求項14】
ライブラリ配列の50%より多くが既知の天然に存在するCDR配列を含む、請求項6または7に記載のライブラリ。
【請求項15】
ライブラリ配列の80%より多くが既知の天然に存在するCDR配列を含む、請求項6または7に記載のライブラリ。
【請求項16】
ライブラリが、任意の所定のCDRについて既知の天然に存在する多様性のみを含む、請求項6または7に記載のライブラリ。
【請求項17】
ライブラリが、ヒトCDRについての全ての既知のCDRの多様性を含む、請求項6または7に記載のライブラリ。
【請求項18】
ライブラリが、ある抗原クラスについての全ての既知のCDRの多様性を含む、請求項6または7に記載のライブラリ。
【請求項19】
CDRアナログが、CDR−H1、CDR−H2、CDR−H3、CDR−L1、CDR−L2、CDR−L3、およびそれらの組み合わせからなる群より選択される、請求項6または7に記載のライブラリ。
【請求項20】
クエリーCDR配列が、CDR−H1、CDR−H2、CDR−H3、CDR−L1、CDR−L2、およびCDR−L3からなる群より選択される、請求項6または7に記載のライブラリ。
【請求項21】
二以上のCDRのアラインメントを行い、一つの合成CDRライブラリ配列の多様性が、直線的に連結されたCDRの可変性に基づき規定、拡張、または制限される、請求項6または7に記載のライブラリ。
【請求項22】
CDR−H1が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項23】
CDR−H2が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項24】
CDR−H3が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項25】
CDR−L1が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項26】
CDR−L2が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項27】
CDR−L3が図13または16〜27のいずれかに示されるコホートライブラリのアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項28】
軽鎖CDR−L1(ラムダ(L))が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項29】
軽鎖CDR−L1(カッパ(K))が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項30】
軽鎖CDR−L2が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項31】
軽鎖CDR−L3が図44に示されるアミノ酸配列を含む、請求項19に記載のライブラリ。
【請求項32】
CDRアナログが、図9〜31、34〜36、または44〜61のいずれかに示されるアミノ酸配列を含む、請求項15に記載のライブラリ。
【請求項33】
CDRアナログが含む多様性は、CDRアナログ内の一つまたはそれ以上の残基を縮重コドン、ウォークスルー型変異誘発、またはルックスルー型変異誘発を用いて示されるものである、請求項6または7に記載のライブラリ。
【請求項34】
抗体結合領域がさらに、一つまたはそれ以上のアミノ酸置換、挿入、または欠失を含む、請求項6または7に記載のライブラリ。
【請求項35】
抗原結合領域がさらに、ヒト、霊長類、マウス、ラット、ウサギ、またはニワトリ由来の天然に存在するフレームワーク領域を含む、請求項6または7に記載のライブラリ。
【請求項36】
天然に存在するフレームワーク領域がVH1、VH3、またはVH4である、請求項6または7に記載のライブラリ。
【請求項37】
ヒトフレームワーク領域が、軽鎖フレームワーク領域、重鎖フレームワーク領域、交配クローニングされたフレームワーク領域、コンセンサスフレームワーク領域、またはそれらの組み合わせである、請求項35に記載のライブラリ。
【請求項38】
ヒトフレームワーク領域が、一つまたはそれ以上のヒトCDR領域との直線的接続におけるそれらの出現頻度に従い選択される、請求項37に記載のライブラリ。
【請求項39】
CDR間のヒトフレームワーク領域をアイソタイプ一致させた、請求項37に記載のライブラリ。
【請求項40】
ライブラリが発現ライブラリである、請求項6または7に記載のライブラリ。
【請求項41】
発現ライブラリが、リボソームディスプレイライブラリ、ポリソームディスプレイライブラリ、ファージディスプレイライブラリ、ウイルスディスプレイライブラリ、細菌発現ライブラリ、酵母ディスプレイライブラリ、および哺乳動物ディスプレイライブラリからなる群より選択される、請求項40に記載のライブラリ。
【請求項42】
一つまたはそれ以上のフレームワーク領域および一つまたはそれ以上のCDR領域をコードする、既定のポリヌクレオチドを合成することによって作製され、これらの領域をコードするポリヌクレオチドがさらに十分に重複する配列を含み、それによって、ポリメラーゼ連鎖反応(PCR)条件下でこのポリヌクレオチド配列から完全な抗体結合領域をコードするポリヌクレオチドが構築され得る、請求項6または7に記載のライブラリ。
【請求項43】
請求項6または7に記載のライブラリのポリヌクレオチドによりコードされる抗体結合領域。
【請求項44】
抗体結合領域を生成させるために請求項40に記載の発現ライブラリを発現させること、および
所望の結合親和性を有する抗体結合領域を選択するために抗体結合領域をスクリーニングすることを含む、
所望の結合親和性を有するポリペプチドの同定方法。
【請求項45】
スクリーニングが抗原結合領域を標的基質と接触させることを含み、抗体結合領域が抗体結合領域をコードするポリヌクレオチドと関連付けられている、請求項44に記載の方法。
【請求項46】
選択された抗体結合領域をコードするポリヌクレオチドを同定する工程をさらに含む、請求項44に記載の方法。
【請求項47】
ポリヌクレオチドが、リボソームディスプレイライブラリ、ポリソームディスプレイライブラリ、ファージディスプレイライブラリ、ウイルスディスプレイライブラリ、細菌発現ライブラリ、酵母ディスプレイライブラリ、および哺乳動物ディスプレイライブラリからなる群より選択される発現ディスプレイを用いて抗体結合領域と関連付けられる、請求項46に記載の方法。
【請求項48】
請求項45〜47のいずれか一項に記載の方法に従い同定される抗体結合領域。
【請求項49】
一つまたはそれ以上の工程がコンピューター支援により行われる、請求項44〜48のいずれかに記載の方法。
【請求項50】
請求項49に記載の方法の一つまたはそれ以上の工程を実行するための指令を含む、電子機器において使用するのに適した媒体。
【請求項51】
請求項49に記載の方法の一つまたはそれ以上の工程を実行するための機器。
【請求項52】
a)図または表のいずれかに示される配列を有する一つまたはそれ以上のフレームワーク領域;および
b)図または表のいずれかに示される配列を有する一つまたはそれ以上のCDR領域、を含む抗体結合領域をコードし、a)のフレームワーク領域およびb)のCDR領域が一緒になって既定の抗原に対する抗体結合領域を形成する、ポリヌクレオチドのライブラリ。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図7】


【図7A】


【図7B】


【図7C】


【図7D】


【図8】


【図8A】


【図8B】


【図8C】


【図8D】


【図8E】


【図9A】


【図9B】


【図10】


【図11】


【図12】


【図13A−1】


【図13A−2】


【図13A−3】


【図13A−4】


【図13B−1】


【図13B−2】


【図13B−3】


【図14A】


【図14B】


【図14C】


【図14D】


【図14E】


【図15A】


【図15B】


【図15C】


【図15D】


【図16A−1】


【図16A−2】


【図16A−3】


【図16A−4】


【図16B−1】


【図16B−2】


【図16B−3】


【図17A−1】


【図17A−2】


【図17A−3】


【図17A−4】


【図17B−1】


【図17B−2】


【図17B−3】


【図18A−1】


【図18A−2】


【図18A−3】


【図18A−4】


【図18B−1】


【図18B−2】


【図18B−3】


【図19A−1】


【図19A−2】


【図19A−3】


【図19A−4】


【図19B−1】


【図19B−2】


【図20A−1】


【図20A−2】


【図20A−3】


【図20A−4】


【図20B−1】


【図20B−2】


【図20B−3】


【図21A−1】


【図21A−2】


【図21A−3】


【図21A−4】


【図21B−1】


【図21B−2】


【図21B−3】


【図22A−1】


【図22A−2】


【図22A−3】


【図22B−1】


【図22B−2】


【図22B−3】


【図23A−1】


【図23A−2】


【図23A−3】


【図23B−1】


【図23B−2】


【図23B−3】


【図24A−1】


【図24A−2】


【図24A−3】


【図24A−4】


【図24B−1】


【図24B−2】


【図24B−3】


【図25A−1】


【図25A−2】


【図25A−3】


【図25B−1】


【図25B−2】


【図25B−3】


【図26A−1】


【図26A−2】


【図26A−3】


【図26B−1】


【図26B−2】


【図27A−1】


【図27A−2】


【図27A−3】


【図27B−1】


【図27B−2】


【図27B−3】


【図28】


【図29】


【図30A】


【図30B】


【図30C】


【図30D】


【図30E】


【図30F】


【図30G】


【図31A】


【図31B】


【図31C】


【図31D】


【図31E】


【図31F】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図44A】


【図44B】


【図44C】


【図44D】


【図44E】


【図44F】


【図45A】


【図45B】


【図45C】


【図46A】


【図46B】


【図46C】


【図47A】


【図47B】


【図48A】


【図48B】


【図49A】


【図49B】


【図50A】


【図50B】


【図51A】


【図51B】


【図52】


【図53】


【図54A】


【図54B】


【図55A】


【図55B】


【図56A】


【図56B】


【図57】


【図58】


【図59】


【図60】


【図61】


【図62A】


【図62B】


【図62C】


【図62D】


【図62E】


【図62F】


【図62G】


【図62H】


【図62I】


【図62J】


【図63】




【図2】


【図3】


【図4】


【図5】


【図6】


【図6A】


【図6B】


【図6C】


【図6D】


【図6E】


【図6F】


【図6G】


【図7】


【図7A】


【図7B】


【図7C】


【図7D】


【図8】


【図8A】


【図8B】


【図8C】


【図8D】


【図8E】


【図9A】


【図9B】


【図10】


【図11】


【図12】


【図13A−1】


【図13A−2】


【図13A−3】


【図13A−4】


【図13B−1】


【図13B−2】


【図13B−3】


【図14A】


【図14B】


【図14C】


【図14D】


【図14E】


【図15A】


【図15B】


【図15C】


【図15D】


【図16A−1】


【図16A−2】


【図16A−3】


【図16A−4】


【図16B−1】


【図16B−2】


【図16B−3】


【図17A−1】


【図17A−2】


【図17A−3】


【図17A−4】


【図17B−1】


【図17B−2】


【図17B−3】


【図18A−1】


【図18A−2】


【図18A−3】


【図18A−4】


【図18B−1】


【図18B−2】


【図18B−3】


【図19A−1】


【図19A−2】


【図19A−3】


【図19A−4】


【図19B−1】


【図19B−2】


【図20A−1】


【図20A−2】


【図20A−3】


【図20A−4】


【図20B−1】


【図20B−2】


【図20B−3】


【図21A−1】


【図21A−2】


【図21A−3】


【図21A−4】


【図21B−1】


【図21B−2】


【図21B−3】


【図22A−1】


【図22A−2】


【図22A−3】


【図22B−1】


【図22B−2】


【図22B−3】


【図23A−1】


【図23A−2】


【図23A−3】


【図23B−1】


【図23B−2】


【図23B−3】


【図24A−1】


【図24A−2】


【図24A−3】


【図24A−4】


【図24B−1】


【図24B−2】


【図24B−3】


【図25A−1】


【図25A−2】


【図25A−3】


【図25B−1】


【図25B−2】


【図25B−3】


【図26A−1】


【図26A−2】


【図26A−3】


【図26B−1】


【図26B−2】


【図27A−1】


【図27A−2】


【図27A−3】


【図27B−1】


【図27B−2】


【図27B−3】


【図28】


【図29】


【図30A】


【図30B】


【図30C】


【図30D】


【図30E】


【図30F】


【図30G】


【図31A】


【図31B】


【図31C】


【図31D】


【図31E】


【図31F】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図44A】


【図44B】


【図44C】


【図44D】


【図44E】


【図44F】


【図45A】


【図45B】


【図45C】


【図46A】


【図46B】


【図46C】


【図47A】


【図47B】


【図48A】


【図48B】


【図49A】


【図49B】


【図50A】


【図50B】


【図51A】


【図51B】


【図52】


【図53】


【図54A】


【図54B】


【図55A】


【図55B】


【図56A】


【図56B】


【図57】


【図58】


【図59】


【図60】


【図61】


【図62A】


【図62B】


【図62C】


【図62D】


【図62E】


【図62F】


【図62G】


【図62H】


【図62I】


【図62J】


【図63】


【公開番号】特開2012−97107(P2012−97107A)
【公開日】平成24年5月24日(2012.5.24)
【国際特許分類】
【出願番号】特願2011−288823(P2011−288823)
【出願日】平成23年12月28日(2011.12.28)
【分割の表示】特願2008−539535(P2008−539535)の分割
【原出願日】平成18年11月10日(2006.11.10)
【出願人】(508142745)バイオレン・インク (2)
【Fターム(参考)】
【公開日】平成24年5月24日(2012.5.24)
【国際特許分類】
【出願日】平成23年12月28日(2011.12.28)
【分割の表示】特願2008−539535(P2008−539535)の分割
【原出願日】平成18年11月10日(2006.11.10)
【出願人】(508142745)バイオレン・インク (2)
【Fターム(参考)】
[ Back to top ]

