放射線耐性シリコーン調合物およびそれで生成された医療機器
【課題】良好なポリアルキルシロキサンおよび放射線耐性成分を含む組成物およびそれで生成された医療機器を提供すること。
【解決手段】開示は、ポリアルキルシロキサンおよび放射線耐性成分を含む組成物で生成された高分子材料を対象にする。放射線耐性成分は、ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量含まれる。
【解決手段】開示は、ポリアルキルシロキサンおよび放射線耐性成分を含む組成物で生成された高分子材料を対象にする。放射線耐性成分は、ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量含まれる。
【発明の詳細な説明】
【技術分野】
【0001】
本願は、一般的に、放射線耐性シリコーン調合物およびそれで生成された医療機器に関する。
【背景技術】
【0002】
高分子材料は、ますます医療機器で使用される。特に、シリコーンゴムは、柔軟性に依存する用途で使用される。例えば、シリコーンゴムは、関節置換デバイス、外科的移植、および外科的ステントで使用される。シリコーンゴムは、またチューブ、ポンプおよびバルブを含む流体の流れるデバイス等の患者の体の外部で使用される医療装置で使用される。これらの用途のそれぞれにおいて、デバイスおよびインプラントの殺菌は、望ましい。
【0003】
従来の殺菌技術は、圧力をかけた水または蒸気の存在下で、構成要素を加熱することを含むオートクレーブを含む。他の典型的な殺菌技術は、ガンマ線での照射等の照射技術を含む。しかし、いくつかのタイプのシリコーン、そして特にポリアルキルシロキサンは、殺菌手順の間に架橋しがちである。
【0004】
最近になって、医療機器産業は、ますます医療機器を殺菌するために、照射手段に向かってきた。照射殺菌技術は、ポリアルキルシロキサン等の非極性のシリコーンポリマー中でフリーラジカルの発生を引き起こしがちである。そうしたフリーラジカルの生成は、物理的特性の変化を生じるさらなる架橋の原因となる。さらに2つのシリコーン表面が接触するデバイス中で、フリーラジカルの調合、そしてそれに続く架橋は、これらの表面の接着を生じる場合がある。
【0005】
接触した表面の接着は、カニューレ、バルブ、およびアヒルのくちばし形(duck bill shaped)の部品等の流体の流れるデバイスにおいて特に不都合である。スリットまたは重複するフラップがバルブとして働くバルブの構造において、架橋は、開口部および流体流れをコントロールする能力を減少させまたはなくす場合がある。
【発明の概要】
【発明が解決しようとする課題】
【0006】
スリットまたは開口部表面が共に接着することを防止する従来の方法は、バルブおよび開口部の外側上に滑剤および表面被膜を適用することを含む。しかし、外側への滑剤のそうした適用は、費用がかかり且つ不便なステップを製造工程に取り込む。さらに、医療機器産業は、デバイスの取り扱いを制約し、そして殺菌工程前の滑剤の導入を妨げる予め包装された製品の殺菌へと向かっている。したがって、これらの調合物で生成された、改善されたシリコーン調合物および医療機器、およびそうした医療機器を殺菌する改善された方法が望ましいであろう。
【課題を解決するための手段】
【0007】
ある特定の態様において、本開示は、ポリアルキルシロキサンと放射線耐性成分とを含む組成物で生成された高分子材料を対象にする。放射線耐性成分(radiation resistant component)は、ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量で含まれる。
【0008】
別の例示的態様において、本開示は、ポリアルキルシロキサンマトリックス、およびポリアルキルシロキサンマトリックスに提供された約70,000センチポイズ以下の粘度を有する、極性成分を含む組成物で生成された硬化した高分子材料を対象にする。
【0009】
さらなる例示的態様において、開示は、非極性のシリコーンマトリックスおよび極性のシリコーン系添加物を含む高分子材料を対象にする。
【0010】
別の例示的態様において、開示はポリアルキルシロキサンマトリックスを含み、そして約3以下の再シール性能(reseal performance)および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を有する高分子材料を対象にする。
【0011】
さらなる例示的態様において、開示は、非極性のポリアルキルシロキサンマトリックスと極性の放射線耐性成分を含む組成物で生成された高分子材料を対象にする。極性の放射線耐性成分は、約70,000センチポイズ以下の粘度を有し、そしてポリアルキルシロキサンマトリックスに、ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量で提供される。高分子材料は、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す。
【0012】
特定の態様において、開示は、シリコーンマトリックス材料と、放射線耐性成分とを含む非重合性混合物を含む殺菌した医療機器を対象にする。
【0013】
別の例示的態様において、開示は、ポリアルキルシロキサンを含む高分子材料で生成された2つの接触する表面によって規定された開口部を含み、そして開口部が約3以下の再シール性能を示し、且つ約6ポンド/平方インチ以下の、放射線照射後のバースト圧力を示す、医療機器を対象にする。
【0014】
さらなる例示的態様において、開示は、高分子材料に形成されたスリット開口部を含む医療機器を対象にする。高分子材料は、非極性のシリコーンマトリックス材料と極性の放射線耐性成分とを含む。
【0015】
さらなる例示的態様において、開示は、極性の放射線耐性成分中非極性のポリアルキルシロキサンの非重合混合物を含む高分子材料で生成された、2つの接触する表面によって規定された開口部を含む、殺菌した医療機器を対象にする。高分子材料は、約3以下の再シール性能と約6ポンド/平方インチ以下の放射線照射後のバースト圧力とを示す。
【0016】
別の例示的態様において、開示は、医療機器を生成するための方法を対象にする。方法は、ポリアルキルシロキサン前駆体と、ポリアルキルシロキサン前駆体の質量に基づいて約0.1wt%〜約20wt%の放射線耐性成分配合量の放射線耐性成分との混合物を調製することを含む。方法は、医療機器を生成させるために鋳型を混合物で満たすことおよびポリアルキルシロキサン前駆体を硬化させることをさらに含む。
【0017】
さらなる例示的態様において、開示は、医療機器の生成方法を対象にする。方法は、ポリアルキルシロキサン前駆体と約70,000センチポイズ以下の粘度を有する放射線耐性成分との混合物を調製することを含む。方法は、医療機器を生成させるために、鋳型を混合物で満たすことおよびポリアルキルシロキサン前駆体を硬化させることをさらに含む。
【0018】
ある特定の態様において、開示は、医療機器の処理方法を対象にする。方法は、医療機器を提供することを含む。医療機器は、医療機器のポリアルキルシロキサン系の部分にある2つの接触する表面によって規定された開口部を有する。方法は、医療機器を殺菌するために、外面に滑剤が適用されていない医療機器を照射することをさらに含む。
【0019】
別の例示的態様において、開示は、医療機器の生成方法を対象にする。方法は、医療機器のポリアルキルシロキサン系の部分に、2つの接触する表面を含む開口部を生成すること、および医療機器をガンマ線で照射することを含む。開口部は、外面に滑剤が適用されていない。
【0020】
さらなる例示的態様において、開示は、患者を治療する方法を対象にする。方法は、外面に滑剤が適用されていない開口部を含み、そしてポリアルキルシロキサン系のマトリックスと放射線耐性成分とを含む組成物で生成された2つの表面によって規定されたガンマ線で殺菌した医療機器を通して、薬用流体を導くことを含む。
【0021】
さらなる例示的態様において、開示は、患者を治療する方法を対象にする。方法は、2つの表面によって規定された、外面に滑剤が適用されていない開口部を含むガンマ線で殺菌した医療機器を通して、薬用流体を導くことを含む。2つの表面は、ポリアルキルシロキサンを含む組成物で生成され、そして約3以下の再シール性能を示す。滑剤のない開口部は、約6ポンド/平方インチ以下の殺菌後のバースト圧力を示す。
【図面の簡単な説明】
【0022】
本開示は、よりよく理解され、そしてその多数の特徴および利点は、当業者が添付図面を参照することにより明らかになるであろう。
【図1】図1は、医療機器の例示的態様の具体的な説明を含む。
【図2】図2は、図1中で具体的に説明された医療機器等の医療機器のシリコーン系の部分の例示的態様の具体的な説明を含む。
【図3】図3は、医療機器内の開口部の例示的態様の具体的な説明を含む。
【図4】図4は、医療機器内の開口部の例示的態様の具体的な説明を含む。
【図5】図5は、医療機器内の開口部の例示的態様の具体的な説明を含む。
【図6】図6は、医療機器を生成する例示的方法の具体的な説明を含む。
【図7】図7は、医療機器を生成する例示的方法の具体的な説明を含む。
【図8】図8は、医療機器を使用するための例示的方法の具体的な説明を含む。
【図9】図9は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図10】図10は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図11】図11は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図12】図12は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図13】図13は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【0023】
同一の参照記号の異なる図での使用は、類似のまたは同一の項目を示す。
【発明を実施するための形態】
【0024】
ある特定の態様において、開示は、照射によって殺菌された医療機器で使用できるシリコーン系の調合物を対象にする。シリコーン系の調合物は、例えばポリアルキルシロキサンマトリックス等の非極性のシリコーンマトリックスと、放射線耐性成分とから、生成できる。ある例示的態様において、放射線耐性成分は、極性の低分子量シリコーンポリマーである。放射線耐性成分は、非極性のシリコーンマトリックスの質量に基づいて、約0.1wt%〜約20wt%の量で、シリコーン系の調合物に含まれてもよい。そうしたシリコーン調合物は、ガンマ線技術等の照射技術を使用して、殺菌された医療機器の生成に有用であることができる。特に、シリコーン調合物は、カニューレ、バルブ、およびアヒルのくちばし形の部品等の流体コントロールデバイスの生成において使用してもよい。ある例示的な用途において、シリコーン調合物は、無針静脈内バルブを生成するために使用される。
【0025】
別の例示的態様において、シリコーン調合物は、シリコーンポリマーのマトリックスを含む。例えば、非極性のシリコーンポリマーを使用して、ポリマーのマトリックスを生成してもよい。シリコーンポリマーは、例えばジメチルシロキサン、ジエチルシロキサン、ジプロピルシロキサン、メチルエチルシロキサン、メチルプロピルシロキサン、またはそれらの組み合わせ等の前駆体で生成されたシリコーンポリマー等のポリアルキルシロキサンを含んでもよい。特定の態様において、ポリアルキルシロキサンは、ポリジメチルシロキサン(PDMS)等のポリジアルキルシロキサンを含む。一般的に、シリコーンポリマーは、非極性であり、そして塩素およびフッ素等のハロゲン化物官能基およびフェニル官能基がない。
【0026】
一実施態様では、シリコーンポリマーは、白金触媒による液体シリコーンゴムである。あるいは、シリコーンポリマーは、過酸化物触媒によるシリコーン調合物であってもよい。シリコーンポリマーは、液体シリコーンゴム(LSR)または高粘度のゴム状物質(HCR)であってもよい。ある特定の態様において、シリコーンポリマーは、2つの部分の反応系で生成されたLSRである。LSRの特定の態様は、Adrian,MIのWacker SiliconeによるWacker3003およびVentura、 CAのRhodia SiliconessによるRhodia 4360を含む。もう一つの例では、シリコーンポリマーは、GE Plasticsから入手可能であるGE94506HCR等のHCRである。
【0027】
シリコーン調合物は、放射線耐性成分も含んでもよい。放射線耐性成分は、少なくとも約20kGyのガンマ線等のガンマ線に曝された場合に、シリコーンマトリックスと一般的に反応しない。例えば、放射線耐性成分は、ガンマ線に曝されている間に、例えばシリコーンマトリックスと本質的に架橋結合を生成しない等の、ガンマ線に曝された場合シリコーンマトリックスと本質的に反応しなくてもよい。特に、放射線耐性成分は、少なくとも約25kGy、少なくとも約30kGy、少なくとも約40kGy、少なくとも約47kGy以上等の少なくとも約20kGy量のガンマ線に曝された場合、シリコーンマトリックスと実質的に反応しない。
【0028】
ある例示的態様において、放射線耐性成分は、極性成分である。放射線耐性成分の特定の態様は、塩素およびフッ素等のハロゲン化物の官能基を含むシリコーンオイル、およびフェニル官能基を含むシリコーンオイル等の極性のシリコーンオイルを含む。一般的に、放射線耐性成分は、ビニルおよびメトキシ末端官能基等の反応性官能基を末端に有さない。例えば、放射線耐性成分は、低分子量トリフルオロプロピルメチルシロキサンポリマーを含んでもよい。別の例示的態様において、放射線耐性成分は、低分子量ポリフェニルメチルシロキサンを含む。
【0029】
さらなる例示的態様において、放射線耐性成分は、炭化水素成分を含む。例えば、放射線耐性成分は、石油、パラフィン系ワックス、炭化水素系ゲル、炭化水素系油、ワセリン(商標)、およびAmogell(Aldrich Chemicalsから入手可能である)等の炭化水素系添加物であってもよい。
【0030】
典型的には、放射線耐性成分は、シリコーンマトリックス内の混合の前に標準状態で低粘度を示す。例えば、放射線耐性成分は、約20,000センチポイズ以下、約10,000センチポイズ以下等の約70,000センチポイズ以下の粘度を有してもよい。特定例において、放射線耐性成分は、約1000センチポイズ以下、約500センチポイズ以下、または約300センチポイズ以下等の約5,000センチポイズ以下の粘度を示す。ある特定の態様において、放射線耐性成分は、シリコーンマトリックスとの混合前に約100センチポイズ以下の粘度を示す。放射線耐性成分は、熱的に安定でもあり、実質的にそこなわれずにおり、そして少なくとも約200℃等の少なくとも約170℃の温度で実質的に分解しない。
【0031】
ある例示的態様において、シリコーン調合物は、シリコーンマトリックスと放射線耐性成分との混合物であってもよい。特に、シリコーン調合物は、放射線耐性成分とシリコーンマトリックスとのコポリマーではない(すなわち、シリコーンマトリックスは、放射線耐性成分と架橋していない)。一般的に、放射線耐性成分は、ポリアルキルシロキサンと実質的に重合していない。ある特定の態様において、シリコーンマトリックスは、約0.1wt%〜約20wt%の量の放射線耐性成分で配合される。配合は、放射線耐性成分の質量%が、シリコーンマトリックス成分の質量に基づくことを意味する。例えば、ポリマーマトリックスは、約0.5wt%〜約5wt%、または約0.5wt%〜約2wt%等の約0.5wt%〜約10wt%の量の放射線耐性成分で配合されていてもよい。
【0032】
シリコーンマトリックス中では、放射線耐性成分は、移動性能(mitigation performance)によって測定されるように移動性を示してもよい。ある特定の態様において、移動性能は、放射線耐性成分を含むシリコーンマトリックスの摩擦係数(COF)の、放射線耐性成分のないシリコーンマトリックスの摩擦係数に対する比によって決定される。例えば、移動性能は、次式によって決定できる:
移動性能=放射線耐性成分を有するマトリックスのCOF/放射線耐性成分ないマトリックスのCOF
【0033】
放射線耐性成分は、例えばほぼ約0.5以下、または約0.4以下等の約0.6以下の移動性能を示してもよい。特に、低粘度放射線耐性成分は、シリコーン調合物の表面へ移動し、そして表面間の架橋を妨げる。
【0034】
シリコーンマトリックスの物理的特性への影響が限定された放射線耐性成分も選択されてもよい。例えば、放射線耐性成分は、引っ張り強度、引き裂き強度、伸長、およびデュロメーター等の物理的特性への限定された影響を有するように、選択されてもよい。特に、配合によりポリマーマトリックスの物理的特性に限られた影響を有する、低分子量フッ素化シリコーンまたはフェニルシリコーンが選択される。約5%以下、または約1%以下等の約10%以下の配合により、放射線耐性成分は、15%以下、または10%以下等の20%未満で、物理的特性に影響することができる。例えば、ポリジメチルシロキサン等のポリアルキルシロキサンマトリックス中での5%以下の量のフッ素化シリコーンの配合は、シリコーン調合物の引っ張り強度に、15%以下の影響を与え、そしてフェニルシリコーンの配合は、シリコーン調合物に、20%以下の影響を与える。さらなる例において、5wt%以下の量でのフッ素化シリコーンまたは低分子量フェニルシリコーン配合は、引き裂き強度に、10%以下等の15%以下の影響を与える。さらなる例示的態様において、フッ素化シリコーンまたはフェニルシリコーンの5%以下の配合は、伸長特性に、15%以下の影響を与える。5%以下の量でのフッ素化またはフェニルシリコーンのそうした配合は、ショアA硬度等の硬度特性に10%以下の影響を与える。
【0035】
放射線耐性成分の特定の態様は、医療用途における使用で認可される。例えば、放射線耐性成分は、患者の体内、短期間の患者の体内、または患者の体外での使用で、認可されることができる。
【0036】
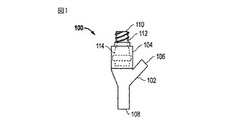
シリコーン調合物は、医療機器における使用で特に有用であることができる。特定の態様において、殺菌した医療機器は、シリコーンマトリックスと放射線耐性成分との非重合性混合物を含む。マトリックスそれ自身は、重合ポリマーとしての医療機器との関連で一般的に使用されるが、本明細書では、"非重合"は、感知できるほどにマトリックスと重合していない放射線耐性成分を意味し、そして放射線耐性成分は、低分子量ポリマーであってもよい。医療機器は、例えばシリコーンマトリックス材料で生成された2つの接触する表面によって規定された開口部を含んでもよい。図1は、流体コントロールデバイス100等の医療機器の例示的態様の具体的な説明を含む。ある特定の態様において、流体コントロールデバイスは、バルブケーシング104および流体を方向指示する部品102を含む、2部品のハウジングの内側に封入されるシリコーン系の部分114を含む。流体を方向指示する部品102は、菅類を係合するために開口部106および108を含む。開口部106および108並びにシリコーン部品114は、空洞のチャンバー(示されていない)を介して流体的に接続される。バルブケーシング104は、無針シリンジまたは他の流体の流れるデバイスと係合するように構成された係合構造112も含んでもよい。さらに、ハウジング104は、そこを通してシリコーン系のバルブ部分114が曝される開口部110を有してもよい。
【0037】
一般的に、流体が開口部106または開口部108を介してデバイス100に導かれる場合、流体は、開口部110を介して出ることを妨げられる。しかし、開口部110を介してデバイス100に方向指示された流体は、特定の圧力差がシリコーンバルブ部分114にかかる場合、開口部106および108に接続するチャンバーに流入することができる。別の態様において、バルブ部分114は、開口部110から流出させることができ、そして開口部110からデバイス100に流れることを妨げることができる。あるいは、バルブ部分114は、バルブ部分114にかかる圧力差の値に基づいて、どちらの方向へも流れることができる両方向バルブであってもよい。
【0038】
図2を見ると、バルブ表面204および開口部206を含むシリコーン系のバルブ部分202が、具体的に説明される。シリコーン系のバルブ部分は、(示されていない)ハウジングに係合するように構成された縁208も含んでもよい。ある特定の態様において、バルブ部分204は、圧力または機械的な力がバルブ表面に適用される場合、流体が流れるための開口部を提供するフラップまたはスリットを含む。
【0039】
ある特定の態様において、シリコーン調合物は、Cote、Sr.らに与えられた2000年3月21日付け米国特許6,039,302号明細書のバルブ、およびCote、Sr.らに与えられた1998年7月7日付けの米国特許第5,775,671号明細書のバルブ等の、バルブの部品を生成するために使用されてもよい。
【0040】
例えば、図3は、開口部またはスリット304を含むバルブ表面302を具体的に示す。圧力がバルブの片側に適用される場合、または圧力差がバルブに適用される場合、シリコーン系の部分の柔軟性は、スリット304を開いて流体の流れを可能にすることができる。
【0041】
図4および5は、バルブの開口部の例示的態様の断面の具体的な説明を含む。例えば、バルブの開口部400は、表面402および404等の相対する表面を生じ、バルブが閉じた位置にあるときに接触するバルブ材料にわたる切れ目またはスリットを含む。もう一つの例では、図5中で具体的に説明されるバルブの開口部500は、重なりが表面502および504等の表面の接触を生じさせ、バルブが閉じた位置にある場合に接触するフラップを含む。殺菌条件下では、存在するシリコーン調合物は、接触する表面間の架橋を制限または減少させる。
【0042】
シリコーン調合物の性能は、バルブ等の医療機器で使用される場合、再シール性能で表すことができる。再シール性能は、殺菌したバルブのバースト圧力の、殺菌前のバルブのバースト圧力に対する比である。例えば、再シール性能は、次式によって決定できる:
再シール性能=殺菌したバースト圧力/殺菌前のバースト圧力
【0043】
バースト圧力は、バルブを開放するためのバルブにかかる圧力差を表す。殺菌は、オートクレーブ内で、または例えばガンマ線での照射によって行われてもよい。上記のシリコーン材料の殺菌は、約6ポンド/平方インチ以下、約5ポンド/平方インチ以下、または約3.5ポンド/平方インチ以下等の約7ポンド/平方インチ以下の殺菌後のバースト圧力を有するバルブを生じる。特定の態様において、バルブの再シール性能は、約2.5以下、約2.0以下、または約1.5以下等の約3以下であり。上に記載したシリコーン調合物を使用する医療機器バルブの特定の態様は、約3以下および約6以下の最終の殺菌後のバースト圧力再シール性能を有する。
【0044】
医療機器は、図6中で具体的に説明された方法600により生成できる。方法600は、602で具体的に説明したように、シリコーン前駆体と放射線耐性成分との混合物の調製を含む。例えば、ジメチルシロキサン等のアルキルシロキサンモノマーは、放射線耐性成分と混合されてもよい。混合物は、触媒および他の添加物をさらに含んでもよい。医療機器のシリコーン系の部分を生成するために、604で具体的に説明したように、鋳型を混合物で満たし、そしてアルキルシロキサンモノマー類を606で具体的に説明したように硬化する。しかし、放射線耐性成分は、実質的に重合せず、そしてアルキルシロキサン前駆体と実質的に架橋または反応しない。
【0045】
一旦硬化すると、医療機器は、608で具体的に説明したように、熱的処理を通して等の追加の硬化または後硬化を経てもよく、例えば、医療機器は、少なくとも約200℃等の少なくとも約170℃温度で処理されてもよい。
【0046】
使用する医療機器をさらに調製するために、図7の方法700で具体的に説明したように、バルブの開口部が生成されてもよく、そしてデバイスが組み立てられ、包装されそして殺菌されてもよい。例えば、方法700は、702で具体的に説明したように、医療機器のシリコーン部分に開口部を生成することを含む。開口部は、例えば材料の表面の切り込みスリット切断、スライス、または打ち抜きを通して生成されてもよい。あるいは、医療機器のバルブ部分は、2つの相対するシリコーン表面を重ねることによって生成されてもよい。
【0047】
医療機器は、704で具体的に説明したように組み立てられる。例えば、医療機器のシリコーン系のバルブ部分は、ポリカーボネートハウジング等のハウジングに挿入されてもよい。ほかの態様において、バルブの開口部は、医療機器の組立後に形成されてもよい。別の態様において、シリコーン系の部分は、実質的に完全な医療機器を生成する。
【0048】
任意選択的に、医療機器は、706で具体的に説明したように包装されてもよい。例えば、医療機器は、殺菌前に個々の包装中で密封されていてもよい。あるいは、医療機器は、殺菌前に、配送に備えて箱の中に配置されてもよい。
【0049】
医療機器を、708で具体的に説明したように殺菌する。ある特定の態様において、医療機器をガンマ線で照射する。例えば、医療機器は、約25kGy、少なくとも約40kGy、または少なくとも約47kGyのガンマ線等の少なくとも約20kGyで照射してもよい。特に、医療機器は、外部への滑剤の適用なしに照射される。したがって、医療機器には、別々でそして外面に滑剤が一般的に適用されていない。
【0050】
使用に際して、図8の方法800の802で具体的に説明したように、医療機器は、流体の流路に接続されていてもよい。804で具体的に説明したように方法800は、医療機器を通して薬用流体の方向指示をすることをさらに含む。特定の態様において、医療機器は、注入管への薬用流体の方向指示を可能にする無針静脈内のバルブであってもよい。あるいは、バルブは、管を通した血液の回収を可能にすることができる。
【0051】
上記に開示された医療機器の特定の態様は、有利にも低い欠陥率を示す。欠陥は、殺菌または後硬化工程の間に、バルブまたはアヒルのくちばし形デバイスを再シーリングすることを意味する。後硬化処理は、一般的には多くの場合、硬化した製品を高温に曝すことによって追加の硬化を行うことをいう。シリコーン調合物の特定の態様は、医療機器として使用される場合には、約9%以下または約5%以下等の10%以下の殺菌後の欠陥率を示す。
【実施例】
【0052】
低分子量極性のシロキサン流体を、液体シリコーンゴム(LSR)中でガンマ線耐性添加物としてテストする。調合物は、白金系触媒およびビニル系ゴムを含む部Aと、水素化物架橋試薬、触媒阻害剤およびビニル系ゴムを含む部Bとを有する2部のLSR系を含む。約300グラムのLSR部Aと、300グラムのLSR部Bと、特定量のガンマ線耐性添加物とを、低の設定をしたKitchen−Aidミキサーを使用して、真空下(25inHg)で12分間、5クオートのボール中で混合する。特に、Gelest(FMS−121 およびFMS−123)およびNuSiI(MED400およびMED400−100)等のメーカーからのトリフルオロプロピルメチルシロキサン;またはGelest(PMM−0025)およびNuSiI(S−7400)のポリフェニルメチルシロキサン等のガンマ線耐性添加物を加えた。ミキサーを4分間隔で停止して、シリコーンを混合パンの壁からこそぎ落とす。混合を再開して、そして真空下で、全部で12分間続ける。70グラムの混合されたシリコーンゴムを、離型溶液(すなわち、水、IPA、および界面活性剤)でコートされたマイラーシート上に置く。ゴムを、鋳型の空洞をほぼ満たすまで加圧する。鋳型を閉じて、そして166℃の予め加熱したプレスで加重し、そして焼けを避けるために、直ちに圧力(25トン)を鋳型にかける。温度をかけた圧力下で、材料を5分間硬化させる。成型された部分を鋳型から除去し、そして箱型オーブン中177℃で4時間後硬化する。
【0053】
放射線耐性添加物の物理的特性への影響、殺菌条件下で移動性能および再シール性能を、テストする。60CO発生源のガンマ線照射および最小の放射線量の47kGyを使用して殺菌する。物理的特性を、引っ張り強度、引っ張り弾性率、およびヤング率のASTMテスト法D−412;引き裂き強度のASTMテスト法D−624;およびデュロメーター(硬度ショアA)のASTMテスト法D−2240を使用してテストする。
【0054】
スリット条件を評価するために、バースト圧力テストを、スリットを開けるために必要な力の量を定量化するために開発する。スリットを開けるために使用される空気圧は、ガンマ線照射に続くスリットの再シールの程度を定量化する。バースト圧力が高いと、再シール条件がさらに厳しいことを表す。再シールテストは、一様にディスクをスリットし、そして圧力チャンバー上の溝のあるハウジングにディスクを配置することを含む。ガンマ線耐性調合物のASTM厚板からディスクを切断し、そして1インチダイを使用して調製し、約0.077インチの厚さを有する6×6インチ厚板からテスト試料を切断する。スリット寸法の均一性は、一貫したデータの生成を補助する。1インチディスクに、デュロメータースタンドおよび切断スリットに取り付けられた長さ0.35インチ×幅0.012インチを有するかみそり刃を使用して、スリットを形成する。2ポンドの重りをスプリング持つデュロメーターの頭部に配置し、切断中一貫した力をかける。
【0055】
バースト圧力を決定するために、圧力計を使用して、試料のバースト圧力を記録する。バースト圧力は、スリットを開けるために必要な最小圧力として規定され、そして空気圧をチャンバーに導入するにつれて、記録する圧力が更に増加するのを防止する。空気圧を、バーストするまで連続的に調整する。
【0056】
移動性能を、摩擦係数を使用して測定する。摩擦係数測定を、Falex摩耗および摩擦試験機を使用して行った。1ポンド重りを50回転/分の回転速度で使用する。
【0057】
例1
フルオロシリコーンおよびフェニルシリコーンを含むシリコーン調合物の物理的特性を、ガンマ線耐性添加物がない標準に比較して、テストする。図9は、引っ張り強度でのガンマ線耐性添加物の影響を具体的に示す。約1wt%ガンマ線耐性添加物が、シリコーン調合物に含まれる場合、比較的小さな変化が、サンプルの引っ張り強度で記録される。(約5wt%)フェニルシリコーンの濃度が高いと、引っ張り強度への影響が大きい。しかし、影響は、約20%未満である。
【0058】
図10で具体的に説明するように、フルオロシリコーンおよびフェニルシリコーンは、シリコーン調合物の伸長特性に影響し、わずかに伸長特性が増加する。しかし、影響は、約15%以下である。
【0059】
図11で具体的に説明するように、フルオロシリコーンおよびフェニルシリコーンは、わずかにシリコーン調合物の引き裂き強度特性に影響する。1wt%のフルオロシリコーン添加物は、わずかに引き裂き強度を増加させるが、5wt%は、引き裂き強度をわずかに低下させる。一般的に、影響は約15%以下であり、そして典型的には約10%以下である。
【0060】
図12は、ショアA硬度で測定したデュロメーターでのフルオロシリコーンおよびフェニルシリコーン添加物の影響を具体的に示す。添加物の効果は、約10%以下である。
【0061】
例2
添加物の移動性能は、シリコーン調合物を混合する前の純粋な添加物成分の粘度に影響される。図13は、異なる粘度を有する添加物の摩擦係数を具体的に示す。高粘度(>10,000センチポイズ)フルオロシリコーンおよびフェニルシリコーン添加物は、低粘度(<1000センチポイズ)添加物より高い摩擦係数を有する。実際、高い粘度フルオロシリコーンの移動性能は、ほとんど1であるが、低粘度フルオロシリコーンの移動性能は約0.6以下である。低粘度フェニルシリコーンの移動性能は、約0.5以下であり、そしていくつかの態様において0.4未満である。
【0062】
例3
添加物の再シール性能は、添加物のタイプ、添加物の配合、および添加物の特性によって影響される。再シール性能は、後照射バースト圧力の前照射バースト圧力に対する比である。したがって、低い再シール値が望ましい。表1は、バースト圧力および再シール性能への添加物の影響を具体的に示す。10〜30セットのサンプルを、それぞれの調合物で調製し、そして再シール性能テストをサンプルのそれぞれで行う。表1は、調合物のそれぞれの平均性能を具体的に示す。標準は、添加物のないサンプルを表し、そして外面滑剤標準(STD−lubed)は、添加物がなく、滑剤が外面に適用されたサンプルを表す。一般的に、種々の濃度中で添加物は、標準サンプルに近いかまたは標準サンプルより良い再シール性能を有するサンプルとなる。いくつかの例において、添加物は、外面滑剤標準サンプルに近い再シール性能を有するサンプルとなる。
【0063】
表1.再シール性能への添加物の影響
【表1】

【0064】
表2は、バースト圧力および再シール性能への添加物の粘度の影響を具体的に示す。サンプルは、異なる粘度を有するフルオロシリコーン添加物を含む。低粘度の添加物を有するサンプルは、一般的に低い値を有し、従って改善された再シール性能を有する。データからモデルに基づいて予測すると、約70,000センチポイズ以下の粘度を有する添加物は、改善された再シール性能を示す。表3は、バースト圧力および再シール性能への添加物の配合量の影響を具体的に示す。再シール性能は、いくらかの例示的な添加物では、配合量と独立しているようである。一般的に、前照射と後照射バースト圧力の両者は、添加物の濃度を増加させると減少する。表4は、添加物の異なる種での、バースト圧力および再シール性能を具体的に示す。フルオロシリコーン添加物の5%の配合は、より高い率のバースト圧力を有する傾向があり、従ってフェニルシリコーンより低い再シール性能を有する。
【0065】
表2.再シール性能への粘度の影響
【表2】

表3.再シール性能への配合量の影響
【表3】

表4.添加物の種類での再シール性能
【表4】

【0066】
例4
ワセリン(商標)を、上記のように生成したシリコーンマトリックスで、低分子量の極性シロキサン流体と置き換える。表5は、バースト圧力および再シール性能でのワセリン(商標)の配合の効果を具体的に示す。ワセリン(商標)添加物は、後硬化に曝された場合でも、望ましい再シール性能を与える。一般的に、ワセリン(商標)等の炭化水素系添加物は、後硬化を含まないデバイス製造工程の再シール性能で、より大きな改善を与える。
【0067】
表5.石油添加物での再シール性能
【表5】

PC−後硬化
【0068】
上記で開示された主題は、具体的に説明するためと考えられるべきであり、そして制約すると考えられるべきではなく、そして請求項は、本発明の範囲内に入るそうした改変、増強、および他の態様の全てを範囲とすることを目的とする。従って、法律で許容される最大限まで本発明の範囲は、請求項およびそれら均等の許される限り広い解釈によって決定され、そして先の詳細な記載により制限または限定されない。
【技術分野】
【0001】
本願は、一般的に、放射線耐性シリコーン調合物およびそれで生成された医療機器に関する。
【背景技術】
【0002】
高分子材料は、ますます医療機器で使用される。特に、シリコーンゴムは、柔軟性に依存する用途で使用される。例えば、シリコーンゴムは、関節置換デバイス、外科的移植、および外科的ステントで使用される。シリコーンゴムは、またチューブ、ポンプおよびバルブを含む流体の流れるデバイス等の患者の体の外部で使用される医療装置で使用される。これらの用途のそれぞれにおいて、デバイスおよびインプラントの殺菌は、望ましい。
【0003】
従来の殺菌技術は、圧力をかけた水または蒸気の存在下で、構成要素を加熱することを含むオートクレーブを含む。他の典型的な殺菌技術は、ガンマ線での照射等の照射技術を含む。しかし、いくつかのタイプのシリコーン、そして特にポリアルキルシロキサンは、殺菌手順の間に架橋しがちである。
【0004】
最近になって、医療機器産業は、ますます医療機器を殺菌するために、照射手段に向かってきた。照射殺菌技術は、ポリアルキルシロキサン等の非極性のシリコーンポリマー中でフリーラジカルの発生を引き起こしがちである。そうしたフリーラジカルの生成は、物理的特性の変化を生じるさらなる架橋の原因となる。さらに2つのシリコーン表面が接触するデバイス中で、フリーラジカルの調合、そしてそれに続く架橋は、これらの表面の接着を生じる場合がある。
【0005】
接触した表面の接着は、カニューレ、バルブ、およびアヒルのくちばし形(duck bill shaped)の部品等の流体の流れるデバイスにおいて特に不都合である。スリットまたは重複するフラップがバルブとして働くバルブの構造において、架橋は、開口部および流体流れをコントロールする能力を減少させまたはなくす場合がある。
【発明の概要】
【発明が解決しようとする課題】
【0006】
スリットまたは開口部表面が共に接着することを防止する従来の方法は、バルブおよび開口部の外側上に滑剤および表面被膜を適用することを含む。しかし、外側への滑剤のそうした適用は、費用がかかり且つ不便なステップを製造工程に取り込む。さらに、医療機器産業は、デバイスの取り扱いを制約し、そして殺菌工程前の滑剤の導入を妨げる予め包装された製品の殺菌へと向かっている。したがって、これらの調合物で生成された、改善されたシリコーン調合物および医療機器、およびそうした医療機器を殺菌する改善された方法が望ましいであろう。
【課題を解決するための手段】
【0007】
ある特定の態様において、本開示は、ポリアルキルシロキサンと放射線耐性成分とを含む組成物で生成された高分子材料を対象にする。放射線耐性成分(radiation resistant component)は、ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量で含まれる。
【0008】
別の例示的態様において、本開示は、ポリアルキルシロキサンマトリックス、およびポリアルキルシロキサンマトリックスに提供された約70,000センチポイズ以下の粘度を有する、極性成分を含む組成物で生成された硬化した高分子材料を対象にする。
【0009】
さらなる例示的態様において、開示は、非極性のシリコーンマトリックスおよび極性のシリコーン系添加物を含む高分子材料を対象にする。
【0010】
別の例示的態様において、開示はポリアルキルシロキサンマトリックスを含み、そして約3以下の再シール性能(reseal performance)および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を有する高分子材料を対象にする。
【0011】
さらなる例示的態様において、開示は、非極性のポリアルキルシロキサンマトリックスと極性の放射線耐性成分を含む組成物で生成された高分子材料を対象にする。極性の放射線耐性成分は、約70,000センチポイズ以下の粘度を有し、そしてポリアルキルシロキサンマトリックスに、ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量で提供される。高分子材料は、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す。
【0012】
特定の態様において、開示は、シリコーンマトリックス材料と、放射線耐性成分とを含む非重合性混合物を含む殺菌した医療機器を対象にする。
【0013】
別の例示的態様において、開示は、ポリアルキルシロキサンを含む高分子材料で生成された2つの接触する表面によって規定された開口部を含み、そして開口部が約3以下の再シール性能を示し、且つ約6ポンド/平方インチ以下の、放射線照射後のバースト圧力を示す、医療機器を対象にする。
【0014】
さらなる例示的態様において、開示は、高分子材料に形成されたスリット開口部を含む医療機器を対象にする。高分子材料は、非極性のシリコーンマトリックス材料と極性の放射線耐性成分とを含む。
【0015】
さらなる例示的態様において、開示は、極性の放射線耐性成分中非極性のポリアルキルシロキサンの非重合混合物を含む高分子材料で生成された、2つの接触する表面によって規定された開口部を含む、殺菌した医療機器を対象にする。高分子材料は、約3以下の再シール性能と約6ポンド/平方インチ以下の放射線照射後のバースト圧力とを示す。
【0016】
別の例示的態様において、開示は、医療機器を生成するための方法を対象にする。方法は、ポリアルキルシロキサン前駆体と、ポリアルキルシロキサン前駆体の質量に基づいて約0.1wt%〜約20wt%の放射線耐性成分配合量の放射線耐性成分との混合物を調製することを含む。方法は、医療機器を生成させるために鋳型を混合物で満たすことおよびポリアルキルシロキサン前駆体を硬化させることをさらに含む。
【0017】
さらなる例示的態様において、開示は、医療機器の生成方法を対象にする。方法は、ポリアルキルシロキサン前駆体と約70,000センチポイズ以下の粘度を有する放射線耐性成分との混合物を調製することを含む。方法は、医療機器を生成させるために、鋳型を混合物で満たすことおよびポリアルキルシロキサン前駆体を硬化させることをさらに含む。
【0018】
ある特定の態様において、開示は、医療機器の処理方法を対象にする。方法は、医療機器を提供することを含む。医療機器は、医療機器のポリアルキルシロキサン系の部分にある2つの接触する表面によって規定された開口部を有する。方法は、医療機器を殺菌するために、外面に滑剤が適用されていない医療機器を照射することをさらに含む。
【0019】
別の例示的態様において、開示は、医療機器の生成方法を対象にする。方法は、医療機器のポリアルキルシロキサン系の部分に、2つの接触する表面を含む開口部を生成すること、および医療機器をガンマ線で照射することを含む。開口部は、外面に滑剤が適用されていない。
【0020】
さらなる例示的態様において、開示は、患者を治療する方法を対象にする。方法は、外面に滑剤が適用されていない開口部を含み、そしてポリアルキルシロキサン系のマトリックスと放射線耐性成分とを含む組成物で生成された2つの表面によって規定されたガンマ線で殺菌した医療機器を通して、薬用流体を導くことを含む。
【0021】
さらなる例示的態様において、開示は、患者を治療する方法を対象にする。方法は、2つの表面によって規定された、外面に滑剤が適用されていない開口部を含むガンマ線で殺菌した医療機器を通して、薬用流体を導くことを含む。2つの表面は、ポリアルキルシロキサンを含む組成物で生成され、そして約3以下の再シール性能を示す。滑剤のない開口部は、約6ポンド/平方インチ以下の殺菌後のバースト圧力を示す。
【図面の簡単な説明】
【0022】
本開示は、よりよく理解され、そしてその多数の特徴および利点は、当業者が添付図面を参照することにより明らかになるであろう。
【図1】図1は、医療機器の例示的態様の具体的な説明を含む。
【図2】図2は、図1中で具体的に説明された医療機器等の医療機器のシリコーン系の部分の例示的態様の具体的な説明を含む。
【図3】図3は、医療機器内の開口部の例示的態様の具体的な説明を含む。
【図4】図4は、医療機器内の開口部の例示的態様の具体的な説明を含む。
【図5】図5は、医療機器内の開口部の例示的態様の具体的な説明を含む。
【図6】図6は、医療機器を生成する例示的方法の具体的な説明を含む。
【図7】図7は、医療機器を生成する例示的方法の具体的な説明を含む。
【図8】図8は、医療機器を使用するための例示的方法の具体的な説明を含む。
【図9】図9は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図10】図10は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図11】図11は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図12】図12は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【図13】図13は、シリコーン調合物の特性上に放射線耐性添加物の影響を具体的に説明するグラフを含む。
【0023】
同一の参照記号の異なる図での使用は、類似のまたは同一の項目を示す。
【発明を実施するための形態】
【0024】
ある特定の態様において、開示は、照射によって殺菌された医療機器で使用できるシリコーン系の調合物を対象にする。シリコーン系の調合物は、例えばポリアルキルシロキサンマトリックス等の非極性のシリコーンマトリックスと、放射線耐性成分とから、生成できる。ある例示的態様において、放射線耐性成分は、極性の低分子量シリコーンポリマーである。放射線耐性成分は、非極性のシリコーンマトリックスの質量に基づいて、約0.1wt%〜約20wt%の量で、シリコーン系の調合物に含まれてもよい。そうしたシリコーン調合物は、ガンマ線技術等の照射技術を使用して、殺菌された医療機器の生成に有用であることができる。特に、シリコーン調合物は、カニューレ、バルブ、およびアヒルのくちばし形の部品等の流体コントロールデバイスの生成において使用してもよい。ある例示的な用途において、シリコーン調合物は、無針静脈内バルブを生成するために使用される。
【0025】
別の例示的態様において、シリコーン調合物は、シリコーンポリマーのマトリックスを含む。例えば、非極性のシリコーンポリマーを使用して、ポリマーのマトリックスを生成してもよい。シリコーンポリマーは、例えばジメチルシロキサン、ジエチルシロキサン、ジプロピルシロキサン、メチルエチルシロキサン、メチルプロピルシロキサン、またはそれらの組み合わせ等の前駆体で生成されたシリコーンポリマー等のポリアルキルシロキサンを含んでもよい。特定の態様において、ポリアルキルシロキサンは、ポリジメチルシロキサン(PDMS)等のポリジアルキルシロキサンを含む。一般的に、シリコーンポリマーは、非極性であり、そして塩素およびフッ素等のハロゲン化物官能基およびフェニル官能基がない。
【0026】
一実施態様では、シリコーンポリマーは、白金触媒による液体シリコーンゴムである。あるいは、シリコーンポリマーは、過酸化物触媒によるシリコーン調合物であってもよい。シリコーンポリマーは、液体シリコーンゴム(LSR)または高粘度のゴム状物質(HCR)であってもよい。ある特定の態様において、シリコーンポリマーは、2つの部分の反応系で生成されたLSRである。LSRの特定の態様は、Adrian,MIのWacker SiliconeによるWacker3003およびVentura、 CAのRhodia SiliconessによるRhodia 4360を含む。もう一つの例では、シリコーンポリマーは、GE Plasticsから入手可能であるGE94506HCR等のHCRである。
【0027】
シリコーン調合物は、放射線耐性成分も含んでもよい。放射線耐性成分は、少なくとも約20kGyのガンマ線等のガンマ線に曝された場合に、シリコーンマトリックスと一般的に反応しない。例えば、放射線耐性成分は、ガンマ線に曝されている間に、例えばシリコーンマトリックスと本質的に架橋結合を生成しない等の、ガンマ線に曝された場合シリコーンマトリックスと本質的に反応しなくてもよい。特に、放射線耐性成分は、少なくとも約25kGy、少なくとも約30kGy、少なくとも約40kGy、少なくとも約47kGy以上等の少なくとも約20kGy量のガンマ線に曝された場合、シリコーンマトリックスと実質的に反応しない。
【0028】
ある例示的態様において、放射線耐性成分は、極性成分である。放射線耐性成分の特定の態様は、塩素およびフッ素等のハロゲン化物の官能基を含むシリコーンオイル、およびフェニル官能基を含むシリコーンオイル等の極性のシリコーンオイルを含む。一般的に、放射線耐性成分は、ビニルおよびメトキシ末端官能基等の反応性官能基を末端に有さない。例えば、放射線耐性成分は、低分子量トリフルオロプロピルメチルシロキサンポリマーを含んでもよい。別の例示的態様において、放射線耐性成分は、低分子量ポリフェニルメチルシロキサンを含む。
【0029】
さらなる例示的態様において、放射線耐性成分は、炭化水素成分を含む。例えば、放射線耐性成分は、石油、パラフィン系ワックス、炭化水素系ゲル、炭化水素系油、ワセリン(商標)、およびAmogell(Aldrich Chemicalsから入手可能である)等の炭化水素系添加物であってもよい。
【0030】
典型的には、放射線耐性成分は、シリコーンマトリックス内の混合の前に標準状態で低粘度を示す。例えば、放射線耐性成分は、約20,000センチポイズ以下、約10,000センチポイズ以下等の約70,000センチポイズ以下の粘度を有してもよい。特定例において、放射線耐性成分は、約1000センチポイズ以下、約500センチポイズ以下、または約300センチポイズ以下等の約5,000センチポイズ以下の粘度を示す。ある特定の態様において、放射線耐性成分は、シリコーンマトリックスとの混合前に約100センチポイズ以下の粘度を示す。放射線耐性成分は、熱的に安定でもあり、実質的にそこなわれずにおり、そして少なくとも約200℃等の少なくとも約170℃の温度で実質的に分解しない。
【0031】
ある例示的態様において、シリコーン調合物は、シリコーンマトリックスと放射線耐性成分との混合物であってもよい。特に、シリコーン調合物は、放射線耐性成分とシリコーンマトリックスとのコポリマーではない(すなわち、シリコーンマトリックスは、放射線耐性成分と架橋していない)。一般的に、放射線耐性成分は、ポリアルキルシロキサンと実質的に重合していない。ある特定の態様において、シリコーンマトリックスは、約0.1wt%〜約20wt%の量の放射線耐性成分で配合される。配合は、放射線耐性成分の質量%が、シリコーンマトリックス成分の質量に基づくことを意味する。例えば、ポリマーマトリックスは、約0.5wt%〜約5wt%、または約0.5wt%〜約2wt%等の約0.5wt%〜約10wt%の量の放射線耐性成分で配合されていてもよい。
【0032】
シリコーンマトリックス中では、放射線耐性成分は、移動性能(mitigation performance)によって測定されるように移動性を示してもよい。ある特定の態様において、移動性能は、放射線耐性成分を含むシリコーンマトリックスの摩擦係数(COF)の、放射線耐性成分のないシリコーンマトリックスの摩擦係数に対する比によって決定される。例えば、移動性能は、次式によって決定できる:
移動性能=放射線耐性成分を有するマトリックスのCOF/放射線耐性成分ないマトリックスのCOF
【0033】
放射線耐性成分は、例えばほぼ約0.5以下、または約0.4以下等の約0.6以下の移動性能を示してもよい。特に、低粘度放射線耐性成分は、シリコーン調合物の表面へ移動し、そして表面間の架橋を妨げる。
【0034】
シリコーンマトリックスの物理的特性への影響が限定された放射線耐性成分も選択されてもよい。例えば、放射線耐性成分は、引っ張り強度、引き裂き強度、伸長、およびデュロメーター等の物理的特性への限定された影響を有するように、選択されてもよい。特に、配合によりポリマーマトリックスの物理的特性に限られた影響を有する、低分子量フッ素化シリコーンまたはフェニルシリコーンが選択される。約5%以下、または約1%以下等の約10%以下の配合により、放射線耐性成分は、15%以下、または10%以下等の20%未満で、物理的特性に影響することができる。例えば、ポリジメチルシロキサン等のポリアルキルシロキサンマトリックス中での5%以下の量のフッ素化シリコーンの配合は、シリコーン調合物の引っ張り強度に、15%以下の影響を与え、そしてフェニルシリコーンの配合は、シリコーン調合物に、20%以下の影響を与える。さらなる例において、5wt%以下の量でのフッ素化シリコーンまたは低分子量フェニルシリコーン配合は、引き裂き強度に、10%以下等の15%以下の影響を与える。さらなる例示的態様において、フッ素化シリコーンまたはフェニルシリコーンの5%以下の配合は、伸長特性に、15%以下の影響を与える。5%以下の量でのフッ素化またはフェニルシリコーンのそうした配合は、ショアA硬度等の硬度特性に10%以下の影響を与える。
【0035】
放射線耐性成分の特定の態様は、医療用途における使用で認可される。例えば、放射線耐性成分は、患者の体内、短期間の患者の体内、または患者の体外での使用で、認可されることができる。
【0036】
シリコーン調合物は、医療機器における使用で特に有用であることができる。特定の態様において、殺菌した医療機器は、シリコーンマトリックスと放射線耐性成分との非重合性混合物を含む。マトリックスそれ自身は、重合ポリマーとしての医療機器との関連で一般的に使用されるが、本明細書では、"非重合"は、感知できるほどにマトリックスと重合していない放射線耐性成分を意味し、そして放射線耐性成分は、低分子量ポリマーであってもよい。医療機器は、例えばシリコーンマトリックス材料で生成された2つの接触する表面によって規定された開口部を含んでもよい。図1は、流体コントロールデバイス100等の医療機器の例示的態様の具体的な説明を含む。ある特定の態様において、流体コントロールデバイスは、バルブケーシング104および流体を方向指示する部品102を含む、2部品のハウジングの内側に封入されるシリコーン系の部分114を含む。流体を方向指示する部品102は、菅類を係合するために開口部106および108を含む。開口部106および108並びにシリコーン部品114は、空洞のチャンバー(示されていない)を介して流体的に接続される。バルブケーシング104は、無針シリンジまたは他の流体の流れるデバイスと係合するように構成された係合構造112も含んでもよい。さらに、ハウジング104は、そこを通してシリコーン系のバルブ部分114が曝される開口部110を有してもよい。
【0037】
一般的に、流体が開口部106または開口部108を介してデバイス100に導かれる場合、流体は、開口部110を介して出ることを妨げられる。しかし、開口部110を介してデバイス100に方向指示された流体は、特定の圧力差がシリコーンバルブ部分114にかかる場合、開口部106および108に接続するチャンバーに流入することができる。別の態様において、バルブ部分114は、開口部110から流出させることができ、そして開口部110からデバイス100に流れることを妨げることができる。あるいは、バルブ部分114は、バルブ部分114にかかる圧力差の値に基づいて、どちらの方向へも流れることができる両方向バルブであってもよい。
【0038】
図2を見ると、バルブ表面204および開口部206を含むシリコーン系のバルブ部分202が、具体的に説明される。シリコーン系のバルブ部分は、(示されていない)ハウジングに係合するように構成された縁208も含んでもよい。ある特定の態様において、バルブ部分204は、圧力または機械的な力がバルブ表面に適用される場合、流体が流れるための開口部を提供するフラップまたはスリットを含む。
【0039】
ある特定の態様において、シリコーン調合物は、Cote、Sr.らに与えられた2000年3月21日付け米国特許6,039,302号明細書のバルブ、およびCote、Sr.らに与えられた1998年7月7日付けの米国特許第5,775,671号明細書のバルブ等の、バルブの部品を生成するために使用されてもよい。
【0040】
例えば、図3は、開口部またはスリット304を含むバルブ表面302を具体的に示す。圧力がバルブの片側に適用される場合、または圧力差がバルブに適用される場合、シリコーン系の部分の柔軟性は、スリット304を開いて流体の流れを可能にすることができる。
【0041】
図4および5は、バルブの開口部の例示的態様の断面の具体的な説明を含む。例えば、バルブの開口部400は、表面402および404等の相対する表面を生じ、バルブが閉じた位置にあるときに接触するバルブ材料にわたる切れ目またはスリットを含む。もう一つの例では、図5中で具体的に説明されるバルブの開口部500は、重なりが表面502および504等の表面の接触を生じさせ、バルブが閉じた位置にある場合に接触するフラップを含む。殺菌条件下では、存在するシリコーン調合物は、接触する表面間の架橋を制限または減少させる。
【0042】
シリコーン調合物の性能は、バルブ等の医療機器で使用される場合、再シール性能で表すことができる。再シール性能は、殺菌したバルブのバースト圧力の、殺菌前のバルブのバースト圧力に対する比である。例えば、再シール性能は、次式によって決定できる:
再シール性能=殺菌したバースト圧力/殺菌前のバースト圧力
【0043】
バースト圧力は、バルブを開放するためのバルブにかかる圧力差を表す。殺菌は、オートクレーブ内で、または例えばガンマ線での照射によって行われてもよい。上記のシリコーン材料の殺菌は、約6ポンド/平方インチ以下、約5ポンド/平方インチ以下、または約3.5ポンド/平方インチ以下等の約7ポンド/平方インチ以下の殺菌後のバースト圧力を有するバルブを生じる。特定の態様において、バルブの再シール性能は、約2.5以下、約2.0以下、または約1.5以下等の約3以下であり。上に記載したシリコーン調合物を使用する医療機器バルブの特定の態様は、約3以下および約6以下の最終の殺菌後のバースト圧力再シール性能を有する。
【0044】
医療機器は、図6中で具体的に説明された方法600により生成できる。方法600は、602で具体的に説明したように、シリコーン前駆体と放射線耐性成分との混合物の調製を含む。例えば、ジメチルシロキサン等のアルキルシロキサンモノマーは、放射線耐性成分と混合されてもよい。混合物は、触媒および他の添加物をさらに含んでもよい。医療機器のシリコーン系の部分を生成するために、604で具体的に説明したように、鋳型を混合物で満たし、そしてアルキルシロキサンモノマー類を606で具体的に説明したように硬化する。しかし、放射線耐性成分は、実質的に重合せず、そしてアルキルシロキサン前駆体と実質的に架橋または反応しない。
【0045】
一旦硬化すると、医療機器は、608で具体的に説明したように、熱的処理を通して等の追加の硬化または後硬化を経てもよく、例えば、医療機器は、少なくとも約200℃等の少なくとも約170℃温度で処理されてもよい。
【0046】
使用する医療機器をさらに調製するために、図7の方法700で具体的に説明したように、バルブの開口部が生成されてもよく、そしてデバイスが組み立てられ、包装されそして殺菌されてもよい。例えば、方法700は、702で具体的に説明したように、医療機器のシリコーン部分に開口部を生成することを含む。開口部は、例えば材料の表面の切り込みスリット切断、スライス、または打ち抜きを通して生成されてもよい。あるいは、医療機器のバルブ部分は、2つの相対するシリコーン表面を重ねることによって生成されてもよい。
【0047】
医療機器は、704で具体的に説明したように組み立てられる。例えば、医療機器のシリコーン系のバルブ部分は、ポリカーボネートハウジング等のハウジングに挿入されてもよい。ほかの態様において、バルブの開口部は、医療機器の組立後に形成されてもよい。別の態様において、シリコーン系の部分は、実質的に完全な医療機器を生成する。
【0048】
任意選択的に、医療機器は、706で具体的に説明したように包装されてもよい。例えば、医療機器は、殺菌前に個々の包装中で密封されていてもよい。あるいは、医療機器は、殺菌前に、配送に備えて箱の中に配置されてもよい。
【0049】
医療機器を、708で具体的に説明したように殺菌する。ある特定の態様において、医療機器をガンマ線で照射する。例えば、医療機器は、約25kGy、少なくとも約40kGy、または少なくとも約47kGyのガンマ線等の少なくとも約20kGyで照射してもよい。特に、医療機器は、外部への滑剤の適用なしに照射される。したがって、医療機器には、別々でそして外面に滑剤が一般的に適用されていない。
【0050】
使用に際して、図8の方法800の802で具体的に説明したように、医療機器は、流体の流路に接続されていてもよい。804で具体的に説明したように方法800は、医療機器を通して薬用流体の方向指示をすることをさらに含む。特定の態様において、医療機器は、注入管への薬用流体の方向指示を可能にする無針静脈内のバルブであってもよい。あるいは、バルブは、管を通した血液の回収を可能にすることができる。
【0051】
上記に開示された医療機器の特定の態様は、有利にも低い欠陥率を示す。欠陥は、殺菌または後硬化工程の間に、バルブまたはアヒルのくちばし形デバイスを再シーリングすることを意味する。後硬化処理は、一般的には多くの場合、硬化した製品を高温に曝すことによって追加の硬化を行うことをいう。シリコーン調合物の特定の態様は、医療機器として使用される場合には、約9%以下または約5%以下等の10%以下の殺菌後の欠陥率を示す。
【実施例】
【0052】
低分子量極性のシロキサン流体を、液体シリコーンゴム(LSR)中でガンマ線耐性添加物としてテストする。調合物は、白金系触媒およびビニル系ゴムを含む部Aと、水素化物架橋試薬、触媒阻害剤およびビニル系ゴムを含む部Bとを有する2部のLSR系を含む。約300グラムのLSR部Aと、300グラムのLSR部Bと、特定量のガンマ線耐性添加物とを、低の設定をしたKitchen−Aidミキサーを使用して、真空下(25inHg)で12分間、5クオートのボール中で混合する。特に、Gelest(FMS−121 およびFMS−123)およびNuSiI(MED400およびMED400−100)等のメーカーからのトリフルオロプロピルメチルシロキサン;またはGelest(PMM−0025)およびNuSiI(S−7400)のポリフェニルメチルシロキサン等のガンマ線耐性添加物を加えた。ミキサーを4分間隔で停止して、シリコーンを混合パンの壁からこそぎ落とす。混合を再開して、そして真空下で、全部で12分間続ける。70グラムの混合されたシリコーンゴムを、離型溶液(すなわち、水、IPA、および界面活性剤)でコートされたマイラーシート上に置く。ゴムを、鋳型の空洞をほぼ満たすまで加圧する。鋳型を閉じて、そして166℃の予め加熱したプレスで加重し、そして焼けを避けるために、直ちに圧力(25トン)を鋳型にかける。温度をかけた圧力下で、材料を5分間硬化させる。成型された部分を鋳型から除去し、そして箱型オーブン中177℃で4時間後硬化する。
【0053】
放射線耐性添加物の物理的特性への影響、殺菌条件下で移動性能および再シール性能を、テストする。60CO発生源のガンマ線照射および最小の放射線量の47kGyを使用して殺菌する。物理的特性を、引っ張り強度、引っ張り弾性率、およびヤング率のASTMテスト法D−412;引き裂き強度のASTMテスト法D−624;およびデュロメーター(硬度ショアA)のASTMテスト法D−2240を使用してテストする。
【0054】
スリット条件を評価するために、バースト圧力テストを、スリットを開けるために必要な力の量を定量化するために開発する。スリットを開けるために使用される空気圧は、ガンマ線照射に続くスリットの再シールの程度を定量化する。バースト圧力が高いと、再シール条件がさらに厳しいことを表す。再シールテストは、一様にディスクをスリットし、そして圧力チャンバー上の溝のあるハウジングにディスクを配置することを含む。ガンマ線耐性調合物のASTM厚板からディスクを切断し、そして1インチダイを使用して調製し、約0.077インチの厚さを有する6×6インチ厚板からテスト試料を切断する。スリット寸法の均一性は、一貫したデータの生成を補助する。1インチディスクに、デュロメータースタンドおよび切断スリットに取り付けられた長さ0.35インチ×幅0.012インチを有するかみそり刃を使用して、スリットを形成する。2ポンドの重りをスプリング持つデュロメーターの頭部に配置し、切断中一貫した力をかける。
【0055】
バースト圧力を決定するために、圧力計を使用して、試料のバースト圧力を記録する。バースト圧力は、スリットを開けるために必要な最小圧力として規定され、そして空気圧をチャンバーに導入するにつれて、記録する圧力が更に増加するのを防止する。空気圧を、バーストするまで連続的に調整する。
【0056】
移動性能を、摩擦係数を使用して測定する。摩擦係数測定を、Falex摩耗および摩擦試験機を使用して行った。1ポンド重りを50回転/分の回転速度で使用する。
【0057】
例1
フルオロシリコーンおよびフェニルシリコーンを含むシリコーン調合物の物理的特性を、ガンマ線耐性添加物がない標準に比較して、テストする。図9は、引っ張り強度でのガンマ線耐性添加物の影響を具体的に示す。約1wt%ガンマ線耐性添加物が、シリコーン調合物に含まれる場合、比較的小さな変化が、サンプルの引っ張り強度で記録される。(約5wt%)フェニルシリコーンの濃度が高いと、引っ張り強度への影響が大きい。しかし、影響は、約20%未満である。
【0058】
図10で具体的に説明するように、フルオロシリコーンおよびフェニルシリコーンは、シリコーン調合物の伸長特性に影響し、わずかに伸長特性が増加する。しかし、影響は、約15%以下である。
【0059】
図11で具体的に説明するように、フルオロシリコーンおよびフェニルシリコーンは、わずかにシリコーン調合物の引き裂き強度特性に影響する。1wt%のフルオロシリコーン添加物は、わずかに引き裂き強度を増加させるが、5wt%は、引き裂き強度をわずかに低下させる。一般的に、影響は約15%以下であり、そして典型的には約10%以下である。
【0060】
図12は、ショアA硬度で測定したデュロメーターでのフルオロシリコーンおよびフェニルシリコーン添加物の影響を具体的に示す。添加物の効果は、約10%以下である。
【0061】
例2
添加物の移動性能は、シリコーン調合物を混合する前の純粋な添加物成分の粘度に影響される。図13は、異なる粘度を有する添加物の摩擦係数を具体的に示す。高粘度(>10,000センチポイズ)フルオロシリコーンおよびフェニルシリコーン添加物は、低粘度(<1000センチポイズ)添加物より高い摩擦係数を有する。実際、高い粘度フルオロシリコーンの移動性能は、ほとんど1であるが、低粘度フルオロシリコーンの移動性能は約0.6以下である。低粘度フェニルシリコーンの移動性能は、約0.5以下であり、そしていくつかの態様において0.4未満である。
【0062】
例3
添加物の再シール性能は、添加物のタイプ、添加物の配合、および添加物の特性によって影響される。再シール性能は、後照射バースト圧力の前照射バースト圧力に対する比である。したがって、低い再シール値が望ましい。表1は、バースト圧力および再シール性能への添加物の影響を具体的に示す。10〜30セットのサンプルを、それぞれの調合物で調製し、そして再シール性能テストをサンプルのそれぞれで行う。表1は、調合物のそれぞれの平均性能を具体的に示す。標準は、添加物のないサンプルを表し、そして外面滑剤標準(STD−lubed)は、添加物がなく、滑剤が外面に適用されたサンプルを表す。一般的に、種々の濃度中で添加物は、標準サンプルに近いかまたは標準サンプルより良い再シール性能を有するサンプルとなる。いくつかの例において、添加物は、外面滑剤標準サンプルに近い再シール性能を有するサンプルとなる。
【0063】
表1.再シール性能への添加物の影響
【表1】

【0064】
表2は、バースト圧力および再シール性能への添加物の粘度の影響を具体的に示す。サンプルは、異なる粘度を有するフルオロシリコーン添加物を含む。低粘度の添加物を有するサンプルは、一般的に低い値を有し、従って改善された再シール性能を有する。データからモデルに基づいて予測すると、約70,000センチポイズ以下の粘度を有する添加物は、改善された再シール性能を示す。表3は、バースト圧力および再シール性能への添加物の配合量の影響を具体的に示す。再シール性能は、いくらかの例示的な添加物では、配合量と独立しているようである。一般的に、前照射と後照射バースト圧力の両者は、添加物の濃度を増加させると減少する。表4は、添加物の異なる種での、バースト圧力および再シール性能を具体的に示す。フルオロシリコーン添加物の5%の配合は、より高い率のバースト圧力を有する傾向があり、従ってフェニルシリコーンより低い再シール性能を有する。
【0065】
表2.再シール性能への粘度の影響
【表2】

表3.再シール性能への配合量の影響
【表3】

表4.添加物の種類での再シール性能
【表4】

【0066】
例4
ワセリン(商標)を、上記のように生成したシリコーンマトリックスで、低分子量の極性シロキサン流体と置き換える。表5は、バースト圧力および再シール性能でのワセリン(商標)の配合の効果を具体的に示す。ワセリン(商標)添加物は、後硬化に曝された場合でも、望ましい再シール性能を与える。一般的に、ワセリン(商標)等の炭化水素系添加物は、後硬化を含まないデバイス製造工程の再シール性能で、より大きな改善を与える。
【0067】
表5.石油添加物での再シール性能
【表5】

PC−後硬化
【0068】
上記で開示された主題は、具体的に説明するためと考えられるべきであり、そして制約すると考えられるべきではなく、そして請求項は、本発明の範囲内に入るそうした改変、増強、および他の態様の全てを範囲とすることを目的とする。従って、法律で許容される最大限まで本発明の範囲は、請求項およびそれら均等の許される限り広い解釈によって決定され、そして先の詳細な記載により制限または限定されない。
【特許請求の範囲】
【請求項1】
ポリアルキルシロキサンと、
ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量の放射線耐性成分と、
を含む組成物で生成された高分子材料。
【請求項2】
該放射線耐性成分が、極性である、請求項1の高分子材料。
【請求項3】
該放射線耐性成分が、シリコーン系添加物を含む、請求項2の高分子材料。
【請求項4】
該放射線耐性成分が、炭化水素系材料を含む、請求項1の高分子材料。
【請求項5】
少なくとも約20kGyのガンマ線に曝された場合、該放射線耐性成分が、該ポリアルキルシロキサンと実質的に反応しない、請求項1の高分子材料。
【請求項6】
該組成物が混合物である、請求項1の高分子材料。
【請求項7】
該放射線耐性成分が、該ポリアルキルシロキサンと実質的に重合しない、請求項6の高分子材料。
【請求項8】
該放射線耐性成分が、約70,000センチポイズ以下の粘度を有する、請求項1の高分子材料。
【請求項9】
該粘度が、約10,000センチポイズ以下である、請求項8の高分子材料。
【請求項10】
該粘度が、約1000センチポイズ以下である、請求項9の高分子材料。
【請求項11】
該粘度が、約100センチポイズ以下である、請求項10の高分子材料。
【請求項12】
該量が、約0.5wt%〜約10wt%である、請求項1の高分子材料。
【請求項13】
該量が、約0.5wt%〜約5wt%である、請求項12の高分子材料。
【請求項14】
該量が、約0.5wt%〜約2wt%である、請求項13の高分子材料。
【請求項15】
該高分子材料が、約3以下の再シール性能を示す、請求項1の高分子材料。
【請求項16】
該再シール性能が、約2.5以下である、請求項15の高分子材料。
【請求項17】
該再シール性能が、約2以下である、請求項16の高分子材料。
【請求項18】
放射線照射後のバースト圧力が、約6ポンド/平方インチ未満である、請求項15の高分子材料。
【請求項19】
該放射線耐性成分が、約0.6以下の移動性能を示す、請求項1の高分子材料。
【請求項20】
該移動性能が、約0.5以下である、請求項19の高分子材料。
【請求項21】
該移動性能が、約0.4以下である、請求項20の高分子材料。
【請求項22】
該放射線耐性成分が、フルオロシリコーンを含む、請求項1の高分子材料。
【請求項23】
該フルオロシリコーンが、ポリトリフルオロプロピルメチルシロキサンを含む、請求項22の高分子材料。
【請求項24】
該放射線耐性成分が、フェニルシリコーンを含む、請求項1の高分子材料。
【請求項25】
該フェニルシリコーンが、ポリフェニルメチルシロキサンを含む、請求項24の高分子材料。
【請求項26】
該放射線耐性成分が、医療用途で承認される、請求項1の高分子材料。
【請求項27】
該放射線耐性成分が、少なくとも約170℃温度で安定である、請求項1の高分子材料。
【請求項28】
該放射線耐性成分が、少なくとも約200℃の温度で安定である、請求項27の高分子材料。
【請求項29】
ポリアルキルシロキサンマトリックスと、
該ポリアルキルシロキサンマトリックスに提供される約70,000センチポイズ以下の粘度を有する極性成分と、
を含む組成物で生成された硬化した高分子化合物。
【請求項30】
該極性成分が、シリコーンを含む、請求項29の硬化した高分子材料。
【請求項31】
該シリコーンが、フルオロシリコーンまたはフェニルシリコーンである、請求項30の硬化した高分子材料。
【請求項32】
該粘度が、約10,000センチポイズ以下である、請求項29の硬化した高分子材料。
【請求項33】
該粘度が、約1000センチポイズ以下である、請求項32の硬化した高分子材料。
【請求項34】
該組成物が、該ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量の該極性成分の配合を含む、請求項29の硬化した高分子材料。
【請求項35】
該量が、約0.5wt%〜約10wt%である、請求項34の硬化した高分子材料。
【請求項36】
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ未満の放射線照射後のバースト圧力を示す、請求項29の硬化した高分子材料。
【請求項37】
該極性成分が、約0.6以下の移動性能を示す、請求項29の硬化した高分子材料。
【請求項38】
該極性成分が、少なくとも約170℃の温度で安定である、請求項29の硬化した高分子材料。
【請求項39】
非極性のシリコーンマトリックスと極性のシリコーン系添加物とを含む高分子材料。
【請求項40】
該非極性のシリコーンマトリックスが、ポリアルキルシロキサンを含む、請求項39の高分子材料。
【請求項41】
該極性のシリコーン系添加物が、フルオロシリコーンまたはフェニルシリコーンである、請求項39の高分子材料。
【請求項42】
該極性のシリコーン系添加物が、約70,000センチポイズ以下の粘度を有する、請求項39の高分子材料。
【請求項43】
該極性のシリコーン系添加物が、約0.6以下の移動性能を有する、請求項39の高分子材料。
【請求項44】
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、請求項39の高分子材料。
【請求項45】
ポリアルキルシロキサンマトリックスを含み、そして約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を有する高分子材料。
【請求項46】
極性のシリコーン系添加物をさらに含む、請求項45の高分子材料。
【請求項47】
該極性のシリコーン系添加物が、約0.6以下の移動性能を示す、請求項46の高分子材料。
【請求項48】
非極性のポリアルキルシロキサンマトリックスと、
該ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量で、該ポリアルキルシロキサンマトリックスに提供される約70,000センチポイズ以下の粘度を有する極性の放射線耐性成分と、
を含む組成物で生成された高分子材料であって、
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、高分子材料。
【請求項49】
シリコーンマトリックス材料と放射線耐性成分とを含む非重合性混合物を含む殺菌した医療機器。
【請求項50】
該非重合性混合物が、該シリコーンマトリックス材料の質量に基づいて、約0.1wt%〜約10wt%の放射線耐性成分の配合を含む、請求項49の殺菌された医療機器。
【請求項51】
該放射線耐性成分の配合量が、約0.5wt%〜約10wt%である、請求項50の殺菌された医療機器。
【請求項52】
該放射線耐性成分の配合量が、約0.5wt%〜約5wt%である、請求項51の殺菌された医療機器。
【請求項53】
該放射線耐性成分の配合量が、約0.5wt%〜約2wt%である、請求項52の殺菌された医療機器。
【請求項54】
分離できる互いに接触する第1の表面と第2の表面であって、該非重合性混合物で生成された該第1の表面と第2の表面をさら含む、請求項49の殺菌された医療機器。
【請求項55】
該殺菌した医療機器が、流体の通過のための内部通路を含む、請求項49の殺菌された医療機器。
【請求項56】
該殺菌した医療機器が、流体コントロールデバイスである、請求項49の殺菌された医療機器。
【請求項57】
該流体コントロールデバイスが、バルブである、請求項56の殺菌された医療機器。
【請求項58】
該バルブが、無針静脈注射バルブである、請求項57の殺菌された医療機器。
【請求項59】
該シリコーンマトリックス材料が、非極性のシリコーンで生成される、請求項49の殺菌された医療機器。
【請求項60】
該シリコーンマトリックス材料が、ポリアルキルシロキサンを含む、請求項49の殺菌された医療機器。
【請求項61】
該放射線耐性成分が、該シリコーンマトリックス材料と実質的に反応しない、請求項49の殺菌された医療機器。
【請求項62】
少なくとも約25kGyのガンマ線に曝された場合に、該放射線耐性成分が、該シリコーンマトリックス材料と実質的に反応しない、請求項61の殺菌された医療機器。
【請求項63】
少なくとも約170℃の温度に曝された場合に、該放射線耐性成分が、該シリコーンマトリックス材料と実質的に反応しない、請求項61の殺菌された医療機器。
【請求項64】
該放射線耐性成分が、極性である、請求項49の殺菌された医療機器。
【請求項65】
該放射線耐性成分が、フルオロシリコーンを含む、請求項49の殺菌された医療機器。
【請求項66】
該フルオロシリコーンが、ポリトリフルオロプロピルメチルシロキサンを含む、請求項65の殺菌された医療機器。
【請求項67】
該放射線耐性成分が、フェニルシリコーンを含む、請求項49の殺菌された医療機器。
【請求項68】
該フェニルシリコーンが、ポリフェニルメチルシロキサンを含む、請求項67の殺菌された医療機器。
【請求項69】
該殺菌した医療機器が、約3以下の再シール性能を示す、請求項49の殺菌された医療機器。
【請求項70】
該再シール性能が、約2.5以下である、請求項69の殺菌された医療機器。
【請求項71】
該再シール性能が、約2以下である、請求項70の殺菌された医療機器。
【請求項72】
放射線照射後のバースト圧力が、約6ポンド/平方インチ未満である、請求項69の殺菌された医療機器。
【請求項73】
該放射線耐性成分が、約0.6以下の移動性能を示す、請求項49の殺菌された医療機器。
【請求項74】
該移動性能が、約0.5以下である、請求項73の殺菌された医療機器。
【請求項75】
該移動性能が、約0.4以下である、請求項74の殺菌された医療機器。
【請求項76】
該放射線耐性成分が、約70,000センチポイズ以下の粘度を有する、請求項49の殺菌された医療機器。
【請求項77】
該粘度が、約10,000センチポイズ以下である、請求項76の殺菌された医療機器。
【請求項78】
該粘度が、約1000センチポイズ以下である、請求項77の殺菌された医療機器。
【請求項79】
該放射線耐性成分が、少なくとも約170℃の温度で安定である、請求項49の殺菌された医療機器。
【請求項80】
該放射線耐性成分が、少なくとも約200℃の温度で安定である、請求項79の殺菌された医療機器。
【請求項81】
該殺菌した医療機器の故障率が10%以下である、請求項49の殺菌された医療機器。
【請求項82】
ポリアルキルシロキサンを含む高分子材料で生成された2つの接触する表面によって規定されており、該開口部が約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す開口部、を含む医療機器。
【請求項83】
該医療機器が、流体コントロールデバイスである、請求項82の医療機器。
【請求項84】
該流体コントロールデバイスが、バルブである、請求項83の医療機器。
【請求項85】
該バルブが、無針静脈注射バルブである、請求項84の医療機器。
【請求項86】
該再シール性能が、約2.5以下である、請求項82の医療機器。
【請求項87】
該再シール性能が、約2以下である、請求項86の医療機器。
【請求項88】
該高分子材料が、放射線耐性成分を含む、請求項82の医療機器。
【請求項89】
該放射線耐性成分が、極性である、請求項88の医療機器。
【請求項90】
該放射線耐性成分が、ポリアルキルシロキサンと反応しない、請求項88の医療機器。
【請求項91】
該放射線耐性成分が、フルオロシリコーンまたはフェニルシリコーンである、請求項88の医療機器。
【請求項92】
該高分子材料中での該放射線耐性成分の配合量が、該ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%である、請求項88の医療機器。
【請求項93】
該配合量が、該ポリアルキルシロキサンの質量に基づいて、約0.5wt%〜約10wt%である、請求項92の医療機器。
【請求項94】
該放射線耐性成分が、約0.6以下の移動性能を示す、請求項88の医療機器。
【請求項95】
該放射線耐性成分が、約70,000センチポイズ以下のプレミックス粘度を有する、請求項88の医療機器。
【請求項96】
該医療機器の故障率が、10%以下である、請求項82の医療機器。
【請求項97】
非極性のシリコーンマトリックス材料と極性の放射線耐性成分とを含む高分子材料で生成されたスリット開口部を含む医療機器。
【請求項98】
該医療機器が、無針静脈注射バルブである、請求項97の医療機器。
【請求項99】
該極性の放射線耐性成分が、フルオロシリコーンまたはフェニルシリコーンである、請求項97の医療機器。
【請求項100】
該極性の放射線耐性成分の配合量が、該非極性のシリコーンマトリックス材料の質量に基づいて、約0.1wt%〜約20wt%である、請求項97の医療機器。
【請求項101】
該極性の放射線耐性成分が、約0.6以下の移動性能を示す、請求項97の医療機器。
【請求項102】
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、請求項97の医療機器。
【請求項103】
該医療機器が、約10%以下の故障率を示す、請求項97の医療機器。
【請求項104】
非極性のポリアルキルシロキサンと極性の放射線耐性成分との非重合性混合物を含む高分子材料で生成された2つの接触する表面によって規定される開口部を含み、該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、殺菌した医療機器。
【請求項105】
該開口部が、スリットである、請求項104の殺菌された医療機器。
【請求項106】
医療機器の生成方法であって、該方法が、
ポリアルキルシロキサン前駆体と、該ポリアルキルシロキサン前駆体の質量に基づいて約0.1wt%〜約20wt%の配合量の放射線耐性成分との混合物を用意すること、
鋳型を該混合物で満たすこと、そして
該ポリアルキルシロキサン前駆体を硬化させて、該医療機器を生成すること、
を含む、方法。
【請求項107】
該放射線耐性成分が、硬化後に該ポリアルキルシロキサン前駆体と非重合のままである、請求項106の方法。
【請求項108】
該配合量が、約0.5wt%〜約10wt%である、請求項106の方法。
【請求項109】
該放射線耐性成分が、約70,000センチポイズ以下の粘度を有する、請求項106の方法。
【請求項110】
該放射線耐性成分が、該ポリアルキルシロキサン中で約0.6以下の移動性能を有する、請求項106の方法。
【請求項111】
該放射線耐性成分が、フルオロシリコーンまたはフェニルシリコーンである、請求項106の方法。
【請求項112】
該医療機器中に、分離できる接触した2つの表面によって、規定される開口部を形成することをさら含む、請求項106の方法。
【請求項113】
該ポリアルキルシロキサン前駆体を硬化した後で、該医療機器の後硬化を行うことをさら含む、請求項106の方法。
【請求項114】
後硬化を行うことが、熱処理を含む、請求項106の方法。
【請求項115】
後硬化を行うことが、架橋することを含む、請求項106の方法。
【請求項116】
該医療機器を殺菌することをさら含む、請求項106の方法。
【請求項117】
該医療機器を殺菌することが、該医療機器をガンマ線で照射することを含む、請求項106の方法。
【請求項118】
該医療機器が、流体コントロールデバイスである、請求項106の方法。
【請求項119】
医療機器の生成方法、該方法は、
ポリアルキルシロキサン前駆体と、約70,000センチポイズ以下の粘度を有する放射線耐性成分との混合物を調製すること、
鋳型を該混合物で満たすこと、そして
該ポリアルキルシロキサン前駆体を硬化して、該医療機器を生成すること、
を含む。
【請求項120】
該混合物を調製することが、該ポリアルキルシロキサン前駆体の質量に基づいて、約0.1wt%〜約20wt%の配合量の該耐性成分を提供することを含む、請求項119の方法。
【請求項121】
該放射線耐性成分が、該ポリアルキルシロキサン中で約0.6以下の移動性能を有する、請求項119の方法。
【請求項122】
該医療機器が、流体コントロールデバイスである、請求項119の方法。
【請求項123】
医療機器の処理方法、該方法は
該医療機器を用意すること、
該医療機器が、該医療機器のポリアルキルシロキサン系の部分において、2つの接触する表面によって規定された開口部を有すること;そして、
外面に滑剤が適用されていない該医療機器を照射して、該医療機器を殺菌すること、
を含む。
【請求項124】
用意することが、包装された医療機器を用意することを含む、請求項123の方法。
【請求項125】
該医療機器を包装する、請求項123の方法。
【請求項126】
該医療機器を包装することが、該医療機器を照射する前に行われる、請求項125の方法。
【請求項127】
該開口部を形成後に、該ポリアルキルシロキサン系の部分を、支持部分に挿入する、請求項123の方法。
【請求項128】
該医療機器に該開口部を形成することをさら含む、請求項123の方法。
【請求項129】
該開口部を形成することが切断を含む、請求項128の方法。
【請求項130】
切断が打ち抜きを含む、請求項129の方法。
【請求項131】
照射が該医療機器を、ガンマ線に曝すことを含む、請求項123の方法。
【請求項132】
該医療機器を曝すことが、少なくとも約25kGyのガンマ線に曝すことを含む、請求項131の方法。
【請求項133】
該医療機器を曝すことが、少なくとも約40kGyのガンマ線に曝すことを含む、請求項132の方法。
【請求項134】
医療機器の生成方法、該方法は、
該医療機器のポリアルキルシロキサン系の部分に、2つの接触する表面を含む開口部を形成すること、そして
該開口部の外面に滑剤が適用されていない該医療機器をガンマ線で照射すること、
を含む。
【請求項135】
該開口部が、スリットである、請求項134の方法。
【請求項136】
該開口部を形成することが、該開口部を打ち抜くことを含む、請求項134の方法。
【請求項137】
該医療機器の該ポリアルキルシロキサン系の部分を、該医療機器の支持部分に挿入することをさら含む、請求項134の方法。
【請求項138】
該医療機器を照射する前に、該医療機器を包装することをさら含む、請求項134の方法。
【請求項139】
該医療機器を照射することが、該医療機器を、少なくとも約25kGyのガンマ線に曝すことを含む、請求項134の方法。
【請求項140】
ポリアルキルシロキサンと極性の放射線耐性成分とから、該医療機器の該ポリアルキルシロキサン部分を生成する、請求項134の方法。
【請求項141】
患者を治療する方法、該方法は、
外面に滑剤が適用されていない開口部を含み且つポリアルキルシロキサン系のマトリックスと放射線耐性成分とを含む組成物で生成された2つの表面によって規定されるガンマ線で殺菌した医療機器を通して薬用流体を導くこと、
を含む。
【請求項142】
該ガンマ線で殺菌した医療機器を、静脈注射ラインに連結することをさら含む、請求項141の方法。
【請求項143】
該組成物が、ポリマーの混合物である、請求項141の方法。
【請求項144】
患者を治療する方法、該方法は、
外面に滑剤が適用されていない開口部を含み且つ2つの表面によって規定されたガンマ線で殺菌した医療機器を通して、薬用液体を導くこと、
該2つの表面が、ポリアルキルシロキサンを含み、そして約3以下の再シール性能を示す組成物で生成されること、
該滑剤のない開口部が、約6ポンド/平方インチ以下の殺菌後のバースト圧力を示すこと
を含む。
【請求項145】
該ガンマ線で殺菌した医療機器を静脈注射ラインに連結することをさら含む、請求項144の方法。
【請求項146】
該再シール性能が、約2以下である、請求項144の方法。
【請求項147】
該組成物が、ポリマーの混合物である、請求項144の方法。
【請求項148】
該ポリマーの混合物が、該ポリアルキルシロキサンと放射線耐性成分とを含む、請求項147の方法。
【請求項1】
ポリアルキルシロキサンと、
ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量の放射線耐性成分と、
を含む組成物で生成された高分子材料。
【請求項2】
該放射線耐性成分が、極性である、請求項1の高分子材料。
【請求項3】
該放射線耐性成分が、シリコーン系添加物を含む、請求項2の高分子材料。
【請求項4】
該放射線耐性成分が、炭化水素系材料を含む、請求項1の高分子材料。
【請求項5】
少なくとも約20kGyのガンマ線に曝された場合、該放射線耐性成分が、該ポリアルキルシロキサンと実質的に反応しない、請求項1の高分子材料。
【請求項6】
該組成物が混合物である、請求項1の高分子材料。
【請求項7】
該放射線耐性成分が、該ポリアルキルシロキサンと実質的に重合しない、請求項6の高分子材料。
【請求項8】
該放射線耐性成分が、約70,000センチポイズ以下の粘度を有する、請求項1の高分子材料。
【請求項9】
該粘度が、約10,000センチポイズ以下である、請求項8の高分子材料。
【請求項10】
該粘度が、約1000センチポイズ以下である、請求項9の高分子材料。
【請求項11】
該粘度が、約100センチポイズ以下である、請求項10の高分子材料。
【請求項12】
該量が、約0.5wt%〜約10wt%である、請求項1の高分子材料。
【請求項13】
該量が、約0.5wt%〜約5wt%である、請求項12の高分子材料。
【請求項14】
該量が、約0.5wt%〜約2wt%である、請求項13の高分子材料。
【請求項15】
該高分子材料が、約3以下の再シール性能を示す、請求項1の高分子材料。
【請求項16】
該再シール性能が、約2.5以下である、請求項15の高分子材料。
【請求項17】
該再シール性能が、約2以下である、請求項16の高分子材料。
【請求項18】
放射線照射後のバースト圧力が、約6ポンド/平方インチ未満である、請求項15の高分子材料。
【請求項19】
該放射線耐性成分が、約0.6以下の移動性能を示す、請求項1の高分子材料。
【請求項20】
該移動性能が、約0.5以下である、請求項19の高分子材料。
【請求項21】
該移動性能が、約0.4以下である、請求項20の高分子材料。
【請求項22】
該放射線耐性成分が、フルオロシリコーンを含む、請求項1の高分子材料。
【請求項23】
該フルオロシリコーンが、ポリトリフルオロプロピルメチルシロキサンを含む、請求項22の高分子材料。
【請求項24】
該放射線耐性成分が、フェニルシリコーンを含む、請求項1の高分子材料。
【請求項25】
該フェニルシリコーンが、ポリフェニルメチルシロキサンを含む、請求項24の高分子材料。
【請求項26】
該放射線耐性成分が、医療用途で承認される、請求項1の高分子材料。
【請求項27】
該放射線耐性成分が、少なくとも約170℃温度で安定である、請求項1の高分子材料。
【請求項28】
該放射線耐性成分が、少なくとも約200℃の温度で安定である、請求項27の高分子材料。
【請求項29】
ポリアルキルシロキサンマトリックスと、
該ポリアルキルシロキサンマトリックスに提供される約70,000センチポイズ以下の粘度を有する極性成分と、
を含む組成物で生成された硬化した高分子化合物。
【請求項30】
該極性成分が、シリコーンを含む、請求項29の硬化した高分子材料。
【請求項31】
該シリコーンが、フルオロシリコーンまたはフェニルシリコーンである、請求項30の硬化した高分子材料。
【請求項32】
該粘度が、約10,000センチポイズ以下である、請求項29の硬化した高分子材料。
【請求項33】
該粘度が、約1000センチポイズ以下である、請求項32の硬化した高分子材料。
【請求項34】
該組成物が、該ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量の該極性成分の配合を含む、請求項29の硬化した高分子材料。
【請求項35】
該量が、約0.5wt%〜約10wt%である、請求項34の硬化した高分子材料。
【請求項36】
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ未満の放射線照射後のバースト圧力を示す、請求項29の硬化した高分子材料。
【請求項37】
該極性成分が、約0.6以下の移動性能を示す、請求項29の硬化した高分子材料。
【請求項38】
該極性成分が、少なくとも約170℃の温度で安定である、請求項29の硬化した高分子材料。
【請求項39】
非極性のシリコーンマトリックスと極性のシリコーン系添加物とを含む高分子材料。
【請求項40】
該非極性のシリコーンマトリックスが、ポリアルキルシロキサンを含む、請求項39の高分子材料。
【請求項41】
該極性のシリコーン系添加物が、フルオロシリコーンまたはフェニルシリコーンである、請求項39の高分子材料。
【請求項42】
該極性のシリコーン系添加物が、約70,000センチポイズ以下の粘度を有する、請求項39の高分子材料。
【請求項43】
該極性のシリコーン系添加物が、約0.6以下の移動性能を有する、請求項39の高分子材料。
【請求項44】
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、請求項39の高分子材料。
【請求項45】
ポリアルキルシロキサンマトリックスを含み、そして約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を有する高分子材料。
【請求項46】
極性のシリコーン系添加物をさらに含む、請求項45の高分子材料。
【請求項47】
該極性のシリコーン系添加物が、約0.6以下の移動性能を示す、請求項46の高分子材料。
【請求項48】
非極性のポリアルキルシロキサンマトリックスと、
該ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%の量で、該ポリアルキルシロキサンマトリックスに提供される約70,000センチポイズ以下の粘度を有する極性の放射線耐性成分と、
を含む組成物で生成された高分子材料であって、
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、高分子材料。
【請求項49】
シリコーンマトリックス材料と放射線耐性成分とを含む非重合性混合物を含む殺菌した医療機器。
【請求項50】
該非重合性混合物が、該シリコーンマトリックス材料の質量に基づいて、約0.1wt%〜約10wt%の放射線耐性成分の配合を含む、請求項49の殺菌された医療機器。
【請求項51】
該放射線耐性成分の配合量が、約0.5wt%〜約10wt%である、請求項50の殺菌された医療機器。
【請求項52】
該放射線耐性成分の配合量が、約0.5wt%〜約5wt%である、請求項51の殺菌された医療機器。
【請求項53】
該放射線耐性成分の配合量が、約0.5wt%〜約2wt%である、請求項52の殺菌された医療機器。
【請求項54】
分離できる互いに接触する第1の表面と第2の表面であって、該非重合性混合物で生成された該第1の表面と第2の表面をさら含む、請求項49の殺菌された医療機器。
【請求項55】
該殺菌した医療機器が、流体の通過のための内部通路を含む、請求項49の殺菌された医療機器。
【請求項56】
該殺菌した医療機器が、流体コントロールデバイスである、請求項49の殺菌された医療機器。
【請求項57】
該流体コントロールデバイスが、バルブである、請求項56の殺菌された医療機器。
【請求項58】
該バルブが、無針静脈注射バルブである、請求項57の殺菌された医療機器。
【請求項59】
該シリコーンマトリックス材料が、非極性のシリコーンで生成される、請求項49の殺菌された医療機器。
【請求項60】
該シリコーンマトリックス材料が、ポリアルキルシロキサンを含む、請求項49の殺菌された医療機器。
【請求項61】
該放射線耐性成分が、該シリコーンマトリックス材料と実質的に反応しない、請求項49の殺菌された医療機器。
【請求項62】
少なくとも約25kGyのガンマ線に曝された場合に、該放射線耐性成分が、該シリコーンマトリックス材料と実質的に反応しない、請求項61の殺菌された医療機器。
【請求項63】
少なくとも約170℃の温度に曝された場合に、該放射線耐性成分が、該シリコーンマトリックス材料と実質的に反応しない、請求項61の殺菌された医療機器。
【請求項64】
該放射線耐性成分が、極性である、請求項49の殺菌された医療機器。
【請求項65】
該放射線耐性成分が、フルオロシリコーンを含む、請求項49の殺菌された医療機器。
【請求項66】
該フルオロシリコーンが、ポリトリフルオロプロピルメチルシロキサンを含む、請求項65の殺菌された医療機器。
【請求項67】
該放射線耐性成分が、フェニルシリコーンを含む、請求項49の殺菌された医療機器。
【請求項68】
該フェニルシリコーンが、ポリフェニルメチルシロキサンを含む、請求項67の殺菌された医療機器。
【請求項69】
該殺菌した医療機器が、約3以下の再シール性能を示す、請求項49の殺菌された医療機器。
【請求項70】
該再シール性能が、約2.5以下である、請求項69の殺菌された医療機器。
【請求項71】
該再シール性能が、約2以下である、請求項70の殺菌された医療機器。
【請求項72】
放射線照射後のバースト圧力が、約6ポンド/平方インチ未満である、請求項69の殺菌された医療機器。
【請求項73】
該放射線耐性成分が、約0.6以下の移動性能を示す、請求項49の殺菌された医療機器。
【請求項74】
該移動性能が、約0.5以下である、請求項73の殺菌された医療機器。
【請求項75】
該移動性能が、約0.4以下である、請求項74の殺菌された医療機器。
【請求項76】
該放射線耐性成分が、約70,000センチポイズ以下の粘度を有する、請求項49の殺菌された医療機器。
【請求項77】
該粘度が、約10,000センチポイズ以下である、請求項76の殺菌された医療機器。
【請求項78】
該粘度が、約1000センチポイズ以下である、請求項77の殺菌された医療機器。
【請求項79】
該放射線耐性成分が、少なくとも約170℃の温度で安定である、請求項49の殺菌された医療機器。
【請求項80】
該放射線耐性成分が、少なくとも約200℃の温度で安定である、請求項79の殺菌された医療機器。
【請求項81】
該殺菌した医療機器の故障率が10%以下である、請求項49の殺菌された医療機器。
【請求項82】
ポリアルキルシロキサンを含む高分子材料で生成された2つの接触する表面によって規定されており、該開口部が約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す開口部、を含む医療機器。
【請求項83】
該医療機器が、流体コントロールデバイスである、請求項82の医療機器。
【請求項84】
該流体コントロールデバイスが、バルブである、請求項83の医療機器。
【請求項85】
該バルブが、無針静脈注射バルブである、請求項84の医療機器。
【請求項86】
該再シール性能が、約2.5以下である、請求項82の医療機器。
【請求項87】
該再シール性能が、約2以下である、請求項86の医療機器。
【請求項88】
該高分子材料が、放射線耐性成分を含む、請求項82の医療機器。
【請求項89】
該放射線耐性成分が、極性である、請求項88の医療機器。
【請求項90】
該放射線耐性成分が、ポリアルキルシロキサンと反応しない、請求項88の医療機器。
【請求項91】
該放射線耐性成分が、フルオロシリコーンまたはフェニルシリコーンである、請求項88の医療機器。
【請求項92】
該高分子材料中での該放射線耐性成分の配合量が、該ポリアルキルシロキサンの質量に基づいて、約0.1wt%〜約20wt%である、請求項88の医療機器。
【請求項93】
該配合量が、該ポリアルキルシロキサンの質量に基づいて、約0.5wt%〜約10wt%である、請求項92の医療機器。
【請求項94】
該放射線耐性成分が、約0.6以下の移動性能を示す、請求項88の医療機器。
【請求項95】
該放射線耐性成分が、約70,000センチポイズ以下のプレミックス粘度を有する、請求項88の医療機器。
【請求項96】
該医療機器の故障率が、10%以下である、請求項82の医療機器。
【請求項97】
非極性のシリコーンマトリックス材料と極性の放射線耐性成分とを含む高分子材料で生成されたスリット開口部を含む医療機器。
【請求項98】
該医療機器が、無針静脈注射バルブである、請求項97の医療機器。
【請求項99】
該極性の放射線耐性成分が、フルオロシリコーンまたはフェニルシリコーンである、請求項97の医療機器。
【請求項100】
該極性の放射線耐性成分の配合量が、該非極性のシリコーンマトリックス材料の質量に基づいて、約0.1wt%〜約20wt%である、請求項97の医療機器。
【請求項101】
該極性の放射線耐性成分が、約0.6以下の移動性能を示す、請求項97の医療機器。
【請求項102】
該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、請求項97の医療機器。
【請求項103】
該医療機器が、約10%以下の故障率を示す、請求項97の医療機器。
【請求項104】
非極性のポリアルキルシロキサンと極性の放射線耐性成分との非重合性混合物を含む高分子材料で生成された2つの接触する表面によって規定される開口部を含み、該高分子材料が、約3以下の再シール性能および約6ポンド/平方インチ以下の放射線照射後のバースト圧力を示す、殺菌した医療機器。
【請求項105】
該開口部が、スリットである、請求項104の殺菌された医療機器。
【請求項106】
医療機器の生成方法であって、該方法が、
ポリアルキルシロキサン前駆体と、該ポリアルキルシロキサン前駆体の質量に基づいて約0.1wt%〜約20wt%の配合量の放射線耐性成分との混合物を用意すること、
鋳型を該混合物で満たすこと、そして
該ポリアルキルシロキサン前駆体を硬化させて、該医療機器を生成すること、
を含む、方法。
【請求項107】
該放射線耐性成分が、硬化後に該ポリアルキルシロキサン前駆体と非重合のままである、請求項106の方法。
【請求項108】
該配合量が、約0.5wt%〜約10wt%である、請求項106の方法。
【請求項109】
該放射線耐性成分が、約70,000センチポイズ以下の粘度を有する、請求項106の方法。
【請求項110】
該放射線耐性成分が、該ポリアルキルシロキサン中で約0.6以下の移動性能を有する、請求項106の方法。
【請求項111】
該放射線耐性成分が、フルオロシリコーンまたはフェニルシリコーンである、請求項106の方法。
【請求項112】
該医療機器中に、分離できる接触した2つの表面によって、規定される開口部を形成することをさら含む、請求項106の方法。
【請求項113】
該ポリアルキルシロキサン前駆体を硬化した後で、該医療機器の後硬化を行うことをさら含む、請求項106の方法。
【請求項114】
後硬化を行うことが、熱処理を含む、請求項106の方法。
【請求項115】
後硬化を行うことが、架橋することを含む、請求項106の方法。
【請求項116】
該医療機器を殺菌することをさら含む、請求項106の方法。
【請求項117】
該医療機器を殺菌することが、該医療機器をガンマ線で照射することを含む、請求項106の方法。
【請求項118】
該医療機器が、流体コントロールデバイスである、請求項106の方法。
【請求項119】
医療機器の生成方法、該方法は、
ポリアルキルシロキサン前駆体と、約70,000センチポイズ以下の粘度を有する放射線耐性成分との混合物を調製すること、
鋳型を該混合物で満たすこと、そして
該ポリアルキルシロキサン前駆体を硬化して、該医療機器を生成すること、
を含む。
【請求項120】
該混合物を調製することが、該ポリアルキルシロキサン前駆体の質量に基づいて、約0.1wt%〜約20wt%の配合量の該耐性成分を提供することを含む、請求項119の方法。
【請求項121】
該放射線耐性成分が、該ポリアルキルシロキサン中で約0.6以下の移動性能を有する、請求項119の方法。
【請求項122】
該医療機器が、流体コントロールデバイスである、請求項119の方法。
【請求項123】
医療機器の処理方法、該方法は
該医療機器を用意すること、
該医療機器が、該医療機器のポリアルキルシロキサン系の部分において、2つの接触する表面によって規定された開口部を有すること;そして、
外面に滑剤が適用されていない該医療機器を照射して、該医療機器を殺菌すること、
を含む。
【請求項124】
用意することが、包装された医療機器を用意することを含む、請求項123の方法。
【請求項125】
該医療機器を包装する、請求項123の方法。
【請求項126】
該医療機器を包装することが、該医療機器を照射する前に行われる、請求項125の方法。
【請求項127】
該開口部を形成後に、該ポリアルキルシロキサン系の部分を、支持部分に挿入する、請求項123の方法。
【請求項128】
該医療機器に該開口部を形成することをさら含む、請求項123の方法。
【請求項129】
該開口部を形成することが切断を含む、請求項128の方法。
【請求項130】
切断が打ち抜きを含む、請求項129の方法。
【請求項131】
照射が該医療機器を、ガンマ線に曝すことを含む、請求項123の方法。
【請求項132】
該医療機器を曝すことが、少なくとも約25kGyのガンマ線に曝すことを含む、請求項131の方法。
【請求項133】
該医療機器を曝すことが、少なくとも約40kGyのガンマ線に曝すことを含む、請求項132の方法。
【請求項134】
医療機器の生成方法、該方法は、
該医療機器のポリアルキルシロキサン系の部分に、2つの接触する表面を含む開口部を形成すること、そして
該開口部の外面に滑剤が適用されていない該医療機器をガンマ線で照射すること、
を含む。
【請求項135】
該開口部が、スリットである、請求項134の方法。
【請求項136】
該開口部を形成することが、該開口部を打ち抜くことを含む、請求項134の方法。
【請求項137】
該医療機器の該ポリアルキルシロキサン系の部分を、該医療機器の支持部分に挿入することをさら含む、請求項134の方法。
【請求項138】
該医療機器を照射する前に、該医療機器を包装することをさら含む、請求項134の方法。
【請求項139】
該医療機器を照射することが、該医療機器を、少なくとも約25kGyのガンマ線に曝すことを含む、請求項134の方法。
【請求項140】
ポリアルキルシロキサンと極性の放射線耐性成分とから、該医療機器の該ポリアルキルシロキサン部分を生成する、請求項134の方法。
【請求項141】
患者を治療する方法、該方法は、
外面に滑剤が適用されていない開口部を含み且つポリアルキルシロキサン系のマトリックスと放射線耐性成分とを含む組成物で生成された2つの表面によって規定されるガンマ線で殺菌した医療機器を通して薬用流体を導くこと、
を含む。
【請求項142】
該ガンマ線で殺菌した医療機器を、静脈注射ラインに連結することをさら含む、請求項141の方法。
【請求項143】
該組成物が、ポリマーの混合物である、請求項141の方法。
【請求項144】
患者を治療する方法、該方法は、
外面に滑剤が適用されていない開口部を含み且つ2つの表面によって規定されたガンマ線で殺菌した医療機器を通して、薬用液体を導くこと、
該2つの表面が、ポリアルキルシロキサンを含み、そして約3以下の再シール性能を示す組成物で生成されること、
該滑剤のない開口部が、約6ポンド/平方インチ以下の殺菌後のバースト圧力を示すこと
を含む。
【請求項145】
該ガンマ線で殺菌した医療機器を静脈注射ラインに連結することをさら含む、請求項144の方法。
【請求項146】
該再シール性能が、約2以下である、請求項144の方法。
【請求項147】
該組成物が、ポリマーの混合物である、請求項144の方法。
【請求項148】
該ポリマーの混合物が、該ポリアルキルシロキサンと放射線耐性成分とを含む、請求項147の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【公開番号】特開2012−162743(P2012−162743A)
【公開日】平成24年8月30日(2012.8.30)
【国際特許分類】
【外国語出願】
【出願番号】特願2012−118650(P2012−118650)
【出願日】平成24年5月24日(2012.5.24)
【分割の表示】特願2008−521486(P2008−521486)の分割
【原出願日】平成18年7月11日(2006.7.11)
【出願人】(500149223)サン−ゴバン パフォーマンス プラスティックス コーポレイション (64)
【Fターム(参考)】
【公開日】平成24年8月30日(2012.8.30)
【国際特許分類】
【出願番号】特願2012−118650(P2012−118650)
【出願日】平成24年5月24日(2012.5.24)
【分割の表示】特願2008−521486(P2008−521486)の分割
【原出願日】平成18年7月11日(2006.7.11)
【出願人】(500149223)サン−ゴバン パフォーマンス プラスティックス コーポレイション (64)
【Fターム(参考)】
[ Back to top ]

