新規なカリウムチャネルブロッカー
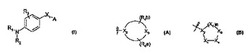
本発明は式(I)の化合物もしくはその塩、またはこれらの製薬上許容されうる誘導体を提供する;

式中、R1は置換されていてもよいアリールアルキル、置換されていてもよいアリール、置換されていてもよいヘテロアリールアルキルおよび置換されていてもよいヘテロアリールからなる群から選択され;R2は置換されていてもよいアシル、置換されていてもよいスルホニルおよび置換されていてもよいスルファモイルからなる群から選択され;R3は水素、ハロゲン、ヒドロキシル、アルコキシ、アリールオキシ、置換されていてもよいアルキル、置換されていてもよいアミノ、置換されていてもよいアミノカルボニル、置換されていてもよいアミノスルホニルまたはニトリルからなる群から選択され;X1は化学結合、CR7R8、C(=O)、C(=NH)、NR9、NHC(=O)、およびSO2からなる群から選択され;R7およびR8は、それぞれ独立して、水素、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリール;または、R7およびR8は、置換されていてもよいC4−6のシクロアルキル環を共に形成し;R9は水素、置換されていてもよいアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールからなる群から選択され;Aは置換されていてもよい飽和したまたは部分的に飽和した一般式

で表される4−7員環を表し、または

から選択され;それぞれにおいて;X2はCHまたはNであり;X3はC(R5a)2、NH、N(R5b)、OまたはSであり;X4はそれぞれ独立してC(=O)、CH2、CH(R4a)、またはN(R4a)(R4b)から選択され;R4aおよびR4bは、それぞれ独立して、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;R5aおよびR5bは、それぞれ独立して、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;R5bは、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;n=1または2である。当該化合物は有益なカリウムイオンチャネル阻害剤である。

式中、R1は置換されていてもよいアリールアルキル、置換されていてもよいアリール、置換されていてもよいヘテロアリールアルキルおよび置換されていてもよいヘテロアリールからなる群から選択され;R2は置換されていてもよいアシル、置換されていてもよいスルホニルおよび置換されていてもよいスルファモイルからなる群から選択され;R3は水素、ハロゲン、ヒドロキシル、アルコキシ、アリールオキシ、置換されていてもよいアルキル、置換されていてもよいアミノ、置換されていてもよいアミノカルボニル、置換されていてもよいアミノスルホニルまたはニトリルからなる群から選択され;X1は化学結合、CR7R8、C(=O)、C(=NH)、NR9、NHC(=O)、およびSO2からなる群から選択され;R7およびR8は、それぞれ独立して、水素、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリール;または、R7およびR8は、置換されていてもよいC4−6のシクロアルキル環を共に形成し;R9は水素、置換されていてもよいアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールからなる群から選択され;Aは置換されていてもよい飽和したまたは部分的に飽和した一般式

で表される4−7員環を表し、または

から選択され;それぞれにおいて;X2はCHまたはNであり;X3はC(R5a)2、NH、N(R5b)、OまたはSであり;X4はそれぞれ独立してC(=O)、CH2、CH(R4a)、またはN(R4a)(R4b)から選択され;R4aおよびR4bは、それぞれ独立して、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;R5aおよびR5bは、それぞれ独立して、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;R5bは、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;n=1または2である。当該化合物は有益なカリウムイオンチャネル阻害剤である。
【発明の詳細な説明】
【技術分野】
【0001】
発明の分野
本発明は、カリウムチャネル阻害剤である式(I)の化合物に関する。この種の化合物は免疫修飾および、自己免疫、慢性炎症、代謝疾患などの治療のためのKv1.3阻害剤として有用でありうる。また、この種の化合物は不整脈の治療または予防のためのKv1.5阻害剤としても有用でありうる。上記化合物を含む薬剤組成物、並びに、自己免疫および炎症性疾患の治療や不整脈の治療におけるその用途もまた、提供される。
【背景技術】
【0002】
背景
イオンチャネルは、細胞膜の脂質二重層にまたがり、Na+、K+、Ca2+およびCl−などの特定のイオンが通過できる水溶性の通路を提供するタンパク質である(Herbert,1998)。カリウムチャネルは、イオンチャネルのうちで最大かつ最も多様なサブグループであり、膜電位の調節および細胞興奮性の制御において中心的な役割を担っている(Armstrong & Hille,1998)。カリウムチャネルはそのアミノ酸配列および生物物理学的特性に基づき、遺伝子ファミリー群に分類されている(命名法についてはGutman et al.,2003を参照)。
【0003】
カリウムチャネルを調節する化合物は、自己免疫疾患、炎症性疾患、心血管疾患、神経疾患、聴覚疾患、腎疾患および代謝介在疾患などの各種の疾患領域において複数の治療用途を有している(Shieh et al.,2000; Ford et al.,2002,Xie et al,2004,Cahalan et al,1997)。カリウムチャネルKv1.3は、ニューロン、血球、破骨細胞、マクロファージ、上皮、並びにTリンパ球およびBリンパ球などの多くの組織に見られる。さらに、Kv1.3を阻害することで、乾癬、関節リウマチ、多発性硬化症、肥満、糖尿病および炎症性腸疾患などの多くの自己免疫疾患に関与しているT細胞の機能が調節されることが明らかになっている(Beeton et al.,2006)。
【0004】
自己免疫疾患のためのKv1.3チャネルブロッカー
乾癬、関節リウマチ、多発性硬化症、IBDなどの種々の自己免疫疾患の発症における自己反応性後期メモリーT細胞の役割は十分に確立されている。TEM細胞の活性化によってKv1.3チャネルの発現が相当程度アップレギュレートされ、その結果、Kv1.3が細胞からのカリウム流出の主要な経路となる。よって、Kv1.3を選択的にブロックすると細胞膜の脱分極およびCa2+流入が引き起こされ、サイトカイン産生並びに細胞増殖および細胞機能の阻害がもたらされる。このように、Kv1.3は自己免疫疾患の制御のための非常に興味深い新規な治療標的である。
【0005】
T細胞および自己免疫
T細胞は、細胞介在性免疫において中心的な役割を担っているリンパ球である。T細胞の主要な形態の一つはヘルパーT細胞(TH)であり、このTHはCD4+細胞としても知られ、自己免疫疾患の進行に重要な役割を果たしている。サイトカインであるインターロイキン2(IL−2)の産生を介して、CD4+T細胞は、細胞傷害性T細胞(CD8+)として知られるT細胞の第2の主要なタイプを生み出すことができる。ナイーブ(不活性)なCD4+T細胞およびCD8+T細胞は両方のタンパク質(CCR7+CD45RA+)を発現し、リンパ節へ進入するための鍵としてケモカイン受容体CCR7を用いる。リンパ節内部において、ナイーブT細胞は抗原と接触し、活性化プロセスを通じて、サイトカイン類を産生し増殖する「エフェクター」T細胞へと変化する。次の免疫応答が減弱すると、ほとんどのナイーブエフェクターは死滅するが、いくつかは長寿命のセントラルメモリー細胞(TCM)へと分化する。TCM細胞はナイーブ細胞と同様にリンパ節へ向かうのにCCR7を用い、そこで自身の同種抗原と遭遇する。抗原刺激によってTCM細胞は、サイトカイン類を産生し増殖する「TCMエフェクター」へと変化する。TCMエフェクターもまたナイーブエフェクターと同じ運命を辿り、その大多数は免疫応答が弱まった後に死滅し、さらなる抗原との接触のために長寿命の生存細胞をいくらか残すこととなる。抗原と繰り返し接触すると(自己免疫疾患または慢性感染で起こりうる)、TCM細胞は、短寿命の、CCR7およびCD45RAを発現していない「エフェクターメモリーT細胞」(TEM)へと分化し、抗原誘導活性化のためにリンパ節へ向かう必要がなくなる。CD8+TEM細胞の一部はCD45RAを再獲得してCCR7−CD45RA+TEMRA細胞となる。活性化によって、CD4+およびCD8+の双方のTEM細胞はTEMエフェクターへと変化し、これが炎症部位へと迅速に移動して大量の炎症性サイトカイン類、インターフェロン−γ(IFN−γ)および腫瘍壊死因子α(TNFα)を産生する。また、CD8+TEMエフェクターは大量のパーフォリンを有しており、よって非常に破壊的である(Wulff et al,2003,Beeton et al,2005)。
【0006】
T細胞および自己免疫疾患におけるKv1.3の機能的役割
ヒトT細胞は二つのK+チャネル(Kv1.3およびIKCa1)を発現しており、これによって遺伝子転写、増殖およびサイトカイン分泌に必要とされる細胞質Ca2+レベルの持続的な上昇に必要なバランスのとれたカチオンの流出がもたらされる(Panyi et al,2004,Chandy et al,2004)。このKv1.3チャネルおよびIKCa1(KCa3.1としても知られている)チャネルは膜電位を調節しており、Tリンパ球におけるCa2+シグナル伝達を促進する。Kv1.3は膜の脱分極に応答して開き、静止膜電位を維持する(初期段階)。これに対し、IKCa1は細胞質Ca2+の増加に応答して開き、膜電位を過分極させる(Beeton et al,2001)。K+チャネルを選択的に封鎖すると膜の脱分極が起こり、これによってCa2+の流入が阻害されてサイトカインの産生および細胞増殖が停止する。チャネルブロッカー毒素を用いた初期のインビトロでの研究によってKv1.3チャネルがT細胞活性化後のサイトカインIL−2の合成(遺伝子の活性化)および分泌に不可欠であることが明らかに示され(Price et al,1989)、免疫不全における当該チャネルの阻害剤の潜在的な治療上の利用に理論的根拠が与えられている。自己免疫疾患の病態における自己反応性T細胞の役割は、動物モデルで明らかに示されている。他のいくつかの自己免疫疾患において疾患特異的な自己反応性T細胞がメモリー表現型を示すことも報告されている。自己反応性TEM細胞も乾癬、関節リウマチ、多発性硬化症、IBD、白斑、ブドウ膜炎、天疱瘡、炎症性筋疾患、橋本病および強皮症に関与しているとされている(Beeton et al、2005)。「後期の」メモリーT細胞およびメモリーB細胞は、多くの自己免疫疾患、移植拒絶反応および慢性の移植片対宿主病において疾患の進行および組織の損傷に関与しているとされている。Kv1.3チャネルの調節物質は、正常な免疫応答に悪影響を及ぼすことなく疾患誘導性のエフェクターメモリーT細胞およびメモリーB細胞の選択的なターゲティングを可能とすることができ、その結果、より一般的な免疫抑制を引き起こす物質よりも好ましい副作用プロファイルを有するものと考えられる。
【0007】
Koo et al,1999によれば、Kv1.3ブロッカーであるマルガトキシン(MgTX)がインビボでの遅延型過敏症(DTH)の応答を効果的に抑制することが観察された。また、MgTXは感作されていない動物での初期の抗体応答を阻害する(二次的な抗体応答はMgTXの影響を受けない)ことも示されている。これらの最近の結果は、休止Tリンパ球ではKv1.3チャネルが支配的でその機能を調節しているのに対し、IKCa1チャネルは活性化前のTリンパ球においてより重要であるとの考え方にも合致している。コレオリド(Correolide)(Koo et al,1999)およびPAP−1(Schmitz et al,2005)はKv1.3チャネルをブロックする新規な免疫抑制剤であり、DTHモデルにおいても有効である。DTH応答に関与する細胞構成成分は自己免疫疾患および同種移植片拒絶反応においてみられるものと類似していることから、上記の結果は新規な免疫抑制剤としてのKv1.3チャネルブロッカーの開発に非常に有望である。
【0008】
「薬剤ターゲットとしての電位依存性イオンチャネル(Voltage Gated Ion Channels as Drug Targets)」においてTriggleらにより記載されているように、1980年代の初めに多くの化合物がμM〜mMの濃度でKv1.3チャネルをブロックすることが報告された。これらの化合物としては、4−アミノピリジンおよびテトラメチルアンモニウムなどの古典的なKvチャネル阻害剤、並びに、カルシウム活性化カリウムチャネルブロッカーであるキニンおよびセテイジル(ceteidil)、フェノチアジン抗精神病薬であるクロルプロマジンおよびトリフルオロペラジン、古典的なカルシウムチャネル阻害剤であるベラパミル、ジルチアゼム、ニフェジピンおよびニトレンジピン、並びにβブロッカーであるプロプラノロールなどの他の非特異的な化合物が挙げられる。
【0009】
1980年代にはまた、サソリ、ヘビおよび他の海洋生物から抽出された天然産物がKv1.3チャネルの強力な阻害剤であることが見出されたが、これらは主に、複数のスルフィド結合によって安定化された短ペプチド(<70残基)であった。これらの強力な阻害剤のうち最初のものはサソリ(Leiurus quinquestriatus hebraeus)の毒から単離され、カリブドトキシン(ChTX)と名付けられた(Sands et al, 1989)が、他のサソリ毒のスクリーニングによってより強力なKv1.3阻害毒が同定され、これらの毒としてはマルガトキシン(MgTX)(Garcia et al, 1993)、アジトキシン−2(Garcia et al, 1994)、ホンゴトキシン(Koshchak et al, 1998)、ダイオウサソリ毒2(pandinus imperator toxin 2)(Pi2)(Peter et al, 2001)およびオーソキラス スクロビキュローサス(Orthochirus scrobiculosus)(OSK1)(Mouhat et al, 2005)などが挙げられる。OSK1(最も近縁の関連チャネルに対して300倍選択的である)を除き、サソリ毒はいずれもKv1.3に対して選択的ではない。
【0010】
1980年代にはまた、サソリ、ヘビおよび他の海洋生物から抽出された天然産物がKv1.3チャネルの強力な阻害剤であることが見出されたが、これらは主に、複数のスルフィド結合によって安定化された短ペプチド(<70残基)であった。これらの強力な阻害剤のうち最初のものはサソリ(Leiurus quinquestriatus hebraeus)の毒から単離され、カリブドトキシン(ChTX)と名付けられた(Sands et al,1989)が、他のサソリ毒のスクリーニングによってより強力なKv1.3阻害毒が同定され、これらの毒としてはマルガトキシン(MgTX)(Garcia et al,1993)、アジトキシン−2(Garcia et al,1994)、ホンゴトキシン(Koshchak et al,1998)、ダイオウサソリ毒2(pandinus imperator toxin 2)(Pi2)(Peter et al,2001)およびオーソキラス スクロビキュローサス(Orthochirus scrobiculosus)(OSK1)(Mouhat et al,2005)などが挙げられる。OSK1(最も近縁の関連チャネルに対して300倍選択的である)を除き、サソリ毒はいずれもKv1.3に対して選択的ではない。
【0011】
これまでで最も強力で選択的なKv1.3ブロッカーの一つは、イソギンチャクから抽出された、スティコダクチラ ヘリアンサス(stichodactyla helianthus)毒(Shk)である(Pennington et al,1996)が、これに関してはKv1.3の封鎖を介した自己免疫疾患の治療について報告されている(US 6,077,680)。Shkおよび、選択性プロファイルが改善されたその合成誘導体であるShk−Dap22はpMで活性を示す(Pennington et al,1998)が、これらのペプチドはさらなる開発に対して好ましくない特性を有していることが判明した。
【0012】
近年ではより新規で選択的な小分子であるKv1.3チャネルブロッカーが自己免疫疾患の管理のために報告されている。これらの分子としては、イミノジヒドロキノリン類であるWIN173173およびCP339818(Nguyen et al.,1996)、ベンズヒドリルピペリジンであるUK−78,282(Hanson et al.1999)、コレオリド(Felix et al.,1999)、シクロヘキシル置換ベンズアミドであるPAC(US−06194458、WO0025774)、スルファミドベンズアミドインダン(US−06083986)、ケリノン(Baell et al.,2004)、ジクロロプレニルピラゾロピリミジン(WO−00140231)およびソラレン類(Wulff et al.,1998.,Vennekamp et al.,2004,Schmitz et al.,2005)が挙げられる。
【0013】
スルホンアミド類が、特に11−β−ヒドロキシステロイドデヒドロゲナーゼ タイプ1、CCR5、H3受容体および有糸分裂キネシン類の阻害剤として有用であることが報告されている。
【0014】
1,4−置換アリール第3級スルホンアミド類(4位がアミドで置換されたもの)が、2型糖尿病などの疾患における高血糖の治療および予防のための11−β−ヒドロキシステロイドデヒドロゲナーゼ タイプ1の阻害剤として特許請求されている(WO2004065351)。
【0015】
1,4−置換アリール第3級スルホンアミド類(4位が置換アルキル、アルコキシアミノ、スルホニル、アシル、アルコキシ、カルボニルまたはアミノカルボニルで置換されていてもよいもの)が、有効な抗癌剤としての有糸分裂キネシン類の阻害剤として特許請求されている(WO2007056078)。
【0016】
1,4−置換アリール第3級スルホンアミド類(スルホンアミドのNが低級アルキル、低級アルケニル、シクロアルキルまたはシクロアルキルおよび4位がカルボニル、アルキルまたは第2級アルコールで置換されていてもよいもの)が、クラスIII抗不整脈剤として特許請求されている(US4876262)。
【0017】
1,4−置換アリール第3級スルホンアミド類(4位がアルキル、カルボニル、またはスルフィニル基で置換されていてもよいもの)が、HIV感染症および他のCCR5介在疾患の治療のためのCCR5の阻害剤として特許請求されている(WO2000454974)。
【0018】
1,4−置換アリール第3級スルホンアミド類が、除草剤として特許請求されている(WO200690792)。
【0019】
1,4−アリール第3級メチルスルホンアミド類(4位が環状アミドで置換され、当該スルホンアミドのNがメチルナフタレンに結合しているもの)が、Xa因子の強力な阻害剤であり、強力な抗血栓作用効果を示すことが報告されている(Wenrong et al,2003)。
【0020】
1,4−置換アリール第3級フェニルスルホンアミド類(4位が第2級アルコールで置換されているもの)が、ヒトプレグナンレセプター(PXR)を阻害し、代謝調節の調節と健康を害する可能性がある化合物の分泌において重要な役割を果たすことが報告されている(Xue et al,2007)。
【発明を実施するための形態】
【0021】
この度、驚くべきことに、後述する一般式(I)の化合物がカリウムチャネルの阻害剤として機能することが見出された。これらの化合物は、カリウムチャネルKv1.3を阻害し、カリウムチャネルKv1.3の阻害に関連した疾患を治療するのに特に有用である。本発明はKv1.3介在性の疾患の治療に限られず、上記化合物はカリウムチャネルの阻害を伴う疾患治療にも有用である(Triggle et al,2006)。すなわち、第一形態において、本発明は式(I)の化合物もしくはその塩またはこれらの製薬上許容されうる誘導体を提供する:
【0022】
【化1】

【0023】
式中、
R1は置換されていてもよいアリールアルキル、置換されていてもよいアリール、置換されていてもよいヘテロアリールアルキルおよび置換されていてもよいヘテロアリールからなる群から選択され;
R2は置換されていてもよいアシル、置換されていてもよいスルホニルおよび置換されていてもよいスルファモイルからなる群から選択され;
R3は水素、ハロゲン、ヒドロキシル、アルコキシ、アリールオキシ、置換されていてもよいアルキル、置換されていてもよいアミノ、置換されていてもよいアミノカルボニル、置換されていてもよいアミノスルホニルまたはニトリルからなる群から選択され;
X1は化学結合、CR7R8、C(=O)、C(=NH)、NR9、NHC(=O)、およびSO2からなる群から選択され;
R7およびR8は、それぞれ独立して、水素、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールから選択され;または、
R7およびR8は、置換されていてもよいC4−C6のシクロアルキル環を共に形成し;
R9は水素、置換されていてもよいアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールからなる群から選択され;
Aは置換されていてもよい飽和したまたは部分的に飽和した一般式
【0024】
【化2】

【0025】
で表される4−7員環、または
【0026】
【化3】

【0027】
から選択され:
それぞれにおいて;
X2はCHまたはNであり;
X3はC(R5)2、N(R5b)、OまたはSであり;
X4は、それぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
n=1または2である。
【0028】
本明細書で用いる場合、特記しない限り、以下の定義が適用されるものとする。
【0029】
「置換されていてもよい」との語は、ある基が、同一であってもよいし異なってもよい1または2以上の置換基によって置換されていてもよいことを意味する。そうでないと特記しない限り、これらの置換基は、アルキル、シクロアルキル、−O−C(ハロゲン)3(好ましくは、−OCF3)、ビアリール、炭素環アリール、ヘテロ脂環、ヘテロアリール、アシル、アミジノ、アミド、アミノ、アルコキシアミノ、カルバモイル、カルボキシ、シアノ、エーテル、ヒドロキシル、イミノ、ハロゲン、ニトロ、スルファモイル、スルホニル、スルフィニル、スルフェニル、スルホンアミドまたはウレアから選択される。
【0030】
本明細書で用いられる場合、「アルキル基」との語は、通常、C1−4のアルキル基またはアルキル部分(例えば、メチル、エチル、n−プロピル、i−プロピル、ブチル、i−ブチルおよびt−ブチル)などの、直鎖または分枝鎖のアルキル基または1〜6個の炭素原子(好ましくは、2、3、4または5個の炭素原子)を含有する部分である。アルキル基またはアルキル部分は、非置換であってもよいし、任意の位置で置換されていてもよい。通常、アルキル基またはアルキル部分は、非置換であるか、または1、2もしくは3個の置換基を有している。適当な置換基としては、シアノ、ハロゲン、ヒドロキシル、アルキルアミノ、ジアルキルアミノ、アミド、アルキルアミド、ジアルキルアミド、アルカノイル、アルコキシ、スルホンアミド、ニトロ、アリールおよびヘテロアリールが挙げられる。アルキル部分はまた、「不飽和アルキル」部分であってもよく、これはアルキル部分が少なくとも一つのアルケンまたはアルキン部分を含有することを意味する。「アルケン」部分とは、少なくとも二つの炭素原子および少なくとも一つの炭素−炭素二重結合からなる基を意味する。「アルキン」部分とは、少なくとも二つの炭素原子および少なくとも一つの炭素−炭素三重結合からなる基を意味する。
【0031】
本明細書で用いられる場合、「シクロアルキル」との語は、3〜11個の炭素原子(すなわち、3、4、5、6、7、8、9、10または11個の炭素原子)からなる単環または二環の環または環系を意味する。当該環系は「飽和環」であってもよく、これはその環がアルケンまたはアルキン部分を含有しないことを意味する。シクロアルキル基はまた、「不飽和環」であってもよく、これは当該環系が少なくとも一つのアルケンまたはアルキン部分を含有し、かつ、当該環系が芳香族ではないことを意味する。上記シクロアルキル基は、本明細書に記載するように、置換または非置換でありうる。上述した置換基に加えて、1または2以上の環炭素原子はまた、二重結合を介してNH、SおよびOから選択される基に結合してもよい。上記シクロアルキルの置換基は、追加の置換基がアルキルである場合を除き、C1−6アルキル基などの連結基を介して結合してもよい。連結基中のアルキル基の1または2以上の水素は、ヒドロキシ、ハロゲン、シアノ、アミノ、チオール、C1−6アルコキシ、C1−6アルキルチオ、C1−6アルキルアミノおよびC1−6ジアルキルアミノからなる群から選択される部分により置換されうる。
【0032】
本明細書で用いられる場合、「アリール基」との語は通常、フェニルまたはナフチルなどのC6−10アリール基である。好ましいアリール基は、フェニルである。アリール基は、非置換であるか、または任意の位置で置換されうる。通常、アリール基は、1、2、3または4つの置換基を有する。適当な置換基としては、シアノ、ハロゲン、ヒドロキシル、ニトロ、トリフルオロメチル、アルキル、アルキルチオ、アルコキシ、アミノ、アルキルアミノ、ジアルキルアミノ、アルカノイル、アミド、N−アルキルアミド、NN−ジアルキルアミノ、スルホンアミド、アリールおよびヘテロアリールが挙げられる。
【0033】
「炭素環」との語は、1または2以上の共有結合で閉じた環構造を含有し、かつ、当該環の骨格を形成する原子がすべて炭素原子である化合物を意味する。よってこの語により、炭素環はヘテロ環と区別される。炭素環基には、非芳香族の炭素環である「シクロアルキル基」と、芳香族の炭素環である「炭素環アリール」基との双方が含まれる。当該炭素環基は、本明細書に記載するように、置換されていてもよい。
【0034】
本明細書で用いられる場合、「ヘテロ環」または「ヘテロシクロ」との語は、N、SおよびOから選択される1または2以上のヘテロ原子を含む、単環または二環の環または環系を意味する。当該環または環系は、ヘテロ原子に加えて、1〜6個の炭素原子(すなわち、1、2、3、4、5または6個の炭素原子)を含む。ヘテロ環基との語は、非芳香族のヘテロ環を意味する「ヘテロ脂環」基と、芳香族のヘテロ環を意味する「ヘテロアリール」基との双方を含む。当該ヘテロ環部分は、非置換であってもよいし、本明細書に記載するように置換されたものであってもよく、置換基は、互いに隣接するように位置するときには結合してシクロアルキルまたはヘテロ脂環式の環系(例えば、メチレンジオキシまたはジフルオロメチレンジオキシ)を形成してもよい。上記ヘテロ環の置換基は、炭素原子またはヘテロ原子を介して結合しうる。上記ヘテロ環基はまた、窒素または硫黄が環中に存在する場合には、窒素および硫黄の酸化物をも含みうる。
【0035】
本明細書で用いられる場合、「ヘテロアリール」との語は、N、SおよびOから選択される1または2以上のヘテロ原子を含む、単環または二環の環または環系を意味する。当該環または環系は、ヘテロ原子に加えて、3〜13個の炭素原子(すなわち、3、4、5、6、7、8、9、10、11、12または13個の炭素原子)を含み、かつ、ヘテロ原子を含む少なくとも一つの芳香環を含有する。当該ヘテロアリール基はまた、窒素もしくは硫黄が存在する場合には、窒素および硫黄の酸化物、またはオキソ基をそれぞれ含みうる。単環のヘテロアリール基の例としては、以下に限定されないが、フリル、チエニル、ピロリル、オキサゾリル、チアゾリル、イソキサゾリル、イソチアゾリル、ピラゾリル、イミダゾリル、トリアゾリル、テトラゾリル、オキサジアゾリル、チアジアゾリル、ピリジル、ピリミジル、ピリダジニル、ピラジニル、およびトリアジニルが挙げられる。二環のヘテロ環の例としては、以下に限定されないが、インドリル、ベンゾフラニル、ベンゾチエニル、ベンズオキサゾリル、ベンゾチアゾリル、ベンズイソキサゾリル、ベンズイソチアゾリル、インダゾリル、イソキノリニル、キノリニル、キノキサリニル、シンノリニル、フタラジニル、キナゾリニル、ベンゾトリアゾニルなどが挙げられる。三環のヘテロ環の例としては、以下に限定されないが、チアントレニル、キサンテニル、フェノキサチイニル、カルバゾリル、カルボリニル、フェナントリジニル、アクリジニル、ペリミジニル、フェナントロリニル、フェナジニル、フェノチアジニル、およびフェノキサジニルが挙げられる。当該ヘテロアリール基は、非置換であってもよいし、本明細書に記載するように置換されていてもよい。置換基は、互いに隣接するように位置するときには結合してシクロアルキルまたはヘテロ脂環式の環(例えば、メチレンジオキシおよびジフルオロメチレンジオキシ)を形成してもよい。上記ヘテロアリールの置換基は、炭素原子またはヘテロ原子を介して結合しうる。
【0036】
本明細書で用いられる場合、「アリールアルキル」との語は、アリール−C1−6アルキルまたはC1−6アルキル−アリールの式の化学部分を意味し、これらの語は本明細書で定義されている。
【0037】
本明細書で用いられる場合、「ヘテロアリールアルキル」との語は、ヘテロアリール−C1−6アルキルまたはC1−6アルキル−ヘテロアリールの式の化学部分を意味し、これらの語は本明細書で定義されている。
【0038】
本明細書で用いられる場合、「アシル」との語は、(CH2)yC(=O)Rz(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式の化学部分を意味する。
【0039】
「アミジノ」との語は、(CH2)yC(=NH)NRzR’z(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式を有する化学部分を意味する。
【0040】
「アミド」との語は、−C(=O)NRzR’zの式を有する化学部分を意味する「C−アミド」基と、−NRzC(=O)R’zの式を有する化学部分を意味する「N−アミド」基との双方を意味する。
【0041】
「アミン」または「アミノ」との語は、−NRzR’zの式を有する化学部分を意味する。アミンの定義にはまた、それらのN−酸化物を含むものと理解される。
【0042】
「シアノ」基は−CNの式の化学部分を意味する。
【0043】
本明細書で用いられる場合、「ヒドロキシ」または「ヒドロキシル」との語は、−OHの式の化学部分を意味する。
【0044】
「ハロゲン」または「ハロ」との語は、フッ素、塩素、臭素およびヨウ素からなる基から選択される原子を意味する。
【0045】
本明細書で用いられる場合、「アルカノイル」との語は、−C(=O)Rzの式の化学部分を意味する。
【0046】
「スルホン」または「スルホニル」との語は、−S(=O)2Rzの式を有する化学部分を意味する。
【0047】
「スルフィニル」との語は、−S(=O)Rzの式を有する化学部分を意味する。
【0048】
「スルフェニル」との語は、−SRzの式を有する化学部分を意味する。
【0049】
「スルファモイル」基は、−N−S(=O)2NRzR’zの式を有する化学部分を意味する。
【0050】
「スルホンアミド」との語は、−S(=O)2NRzR’zの式を有する化学部分を意味する「S−スルホアミド」基と、−N−S(=O)2R’zの式を有する化学部分を意味する「N−スルホアミド」基との双方を意味する。
【0051】
「チオカルボニル」との語は、(CH2)yC(=S)Rz(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式を有する化学部分を意味する。
【0052】
本明細書で用いられる場合、「チオ」または「チオール」との語は、−SHの式の化学部分を意味する。
【0053】
「チオアミド」との語は、(CH2)yC(=S)NRzR’zの式を有する化学部分を意味する「C−チオアミド」基と、(CH2)yNRzC(=S)R’z(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式を有する化学部分を意味する「N−チオアミド」基との双方を意味する。
【0054】
「ウレア」基は、−NRzC(=O)NRzR’zの式を有する化学部分を意味する。
【0055】
RzおよびR’zは、それぞれ独立して、水素、C1−6アルキル、シクロアルキル、C1−6アルコキシ、アリール−C1−6アルキル、アリールおよびヘテロアリールからなる群から選択される。
【0056】
好ましい一実施形態は、Aが
【0057】
【化4】

【0058】
から選択される化合物に関し;式中、
n=1または2であり;
X3はC(R5)2、N(R5b)、またはOであり;
X4は、それぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、ヒドロキシル、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。
【0059】
好ましくは、R2はC(=O)R10、SO2R10からなる群から選択され;式中、
R10は、NR11R12、置換されていてもよいアリール、および置換されていてもよいヘテロアリールから選択される。さらに好ましくは、R10は、NR11R12、式(II)、(III)、(IV)または(V)から選択される;
【0060】
【化5】

【0061】
式中、
R11およびR12は同じであるかまたは異なり、それぞれ水素、置換されていてもよいアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
G、J、L、D、およびEは同じであるかまたは異なり、それぞれCまたはNであり(G、J、L、D、またはEの少なくとも一つがNである);
R10が式(II)であるときは、LはOまたはSであってもよく、および
R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるいは置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環の環であり;
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであるか、あるいは、R15およびR16の対、またはR16およびR17の対、またはR17およびR18の対、またはR18およびR19の対が置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環の環を共に形成してもよく;
R1は置換されていてもよいアリールアルキル、および置換されていてもよいヘテロアリールアルキルから選択される。より好ましくは、R1は式(VI)から選択され;
【0062】
【化6】

【0063】
式中、
R20、R21、R22、R23およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルまたは置換されていてもよいアルコキシであり;
R25およびR26は同じであるかまたは異なり、それぞれ水素、ヒドロキシル、および置換されていてもよいC1−3アルキルである。
【0064】
R3は、水素、ハロゲン、ヒドロキシル、ニトリル、または置換されていてもよいアルキル、好ましくは水素、ハロゲンまたは置換されていてもよいアルキルからなる群から選択される。
【0065】
X1は、好ましくは化学結合、CH2、およびC(=O)からなる群から選択される。
本発明の最も好ましい化合物は式(VII)のものである:
【0066】
【化7】

【0067】
式中、
n=1または2であり;
X1は化学結合、CH2、またはC(=O)からなる群から選択され;
X3はC(R5)2、N(R5b)、またはOであり;
X4はC(=O)、またはC(R4)2であり;
R3は水素、ハロゲン、ヒドロキシルまたは置換されていてもよいC1−3アルキルからなる群から選択され;
R4は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアリールオキシ、置換されていてもよいC1−3アルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。好ましくはR4はそれぞれ独立してフルオロ、置換されていてもよいメチル、ヒドロキシ、トリフルオロメチル、置換されていてもよいフェニル、置換されていてもよいフェノキシ、置換されていてもよいベンジルオキシまたは置換されていてもよいオキサジアゾールである。
【0068】
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。好ましくは、R5は、それぞれ独立して、フルオロ、メチル、トリフルオロメチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、tert−ブチル、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、シクロヘキシルメチル、置換されていてもよいフェニル、置換されていてもよいベンジル、置換されていてもよいフェネチル、ヒドロキシル、置換されていてもよいヒドロキシエチル、ヒドロキシプロピル、ヒドロキシブチル、置換されていてもよいフェノキシ、置換されていてもよいベンジルオキシ、メトキシエチル、メトキシプロピル、フェノキシエチル、ベンジルオキシエチル、アセチル、プロピオニル、置換されていてもよいベンゾイル、フェナシル、イミダゾイル、ピラゾイル、ピリジノイル、オキサジアゾロイル、チアゾロイル、アセタミド、メチルアセタミド、ジメチルアセタミド、エチルアセタミド、ジエチルアセタミド、tert−ブチルアセタミド、ピリジルアセタミド、シクロプロピルアセタミド、シクロブチルアセタミド、シクロペンチルアセタミド、またはシクロヘキシルアセタミドである。より好ましくは、R5は、それぞれ独立して、フルオロ、置換されていてもよいメチル、ヒドロキシ、置換されていてもよいシクロヘキシル、置換されていてもよいフェニル、置換されていてもよいベンジル、置換されていてもよいフェノキシ、置換されていてもよいベンジルオキシ、またはチアゾロイルである。
【0069】
R5bは、水素、置換されていてもよいC1−3アルキル、置換されていてもよいフェニルおよび置換されていてもよいヘテロアリールである。
【0070】
R10はNR11R12または式(II)、(III)、(IV)もしくは(V)の化合物から選択され;
【0071】
【化8】

【0072】
式中、
R11およびR12は同じであるかまたは異なり、それぞれ置換されていてもよいC1−3アルキルである。好ましくは、R11およびR12は、アルキル(好ましくは、CH3)であり;G、J、L、D、およびEは同じであるかまたは異なり、それぞれC、またはNであり(G、J、L、D、またはEの少なくとも一つはNであり);
前記R10が式(II)であるときは、LはOまたはSであってもよく、および
前記R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるいは置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよい。好ましくは、R13およびR14はアルキル(好ましくは、CH3)である。
【0073】
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであるか、あるいは、R15およびR16の対、もしくはR16およびR17の対、もしくはR17およびR18の対、もしくはR18およびR19の対が、置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成しうる。
【0074】
好ましくは、R10は、置換されたイミダゾール、置換されたピラゾール、置換されたピロール、置換された置換されたオキサゾール、置換されたオキサジアゾール、置換されたチアゾール、置換されたチアジアゾール、置換されたピリジン、置換されたピリミジン、置換されたピラジン、置換されたピリダジン、置換されたトリアジン、置換されていてもよいフェニル、テトラヒドロベンゾフラン、ベンゾピラン、ジヒドロベンゾジオキシン、ベンゾキサジノン、ベンゾオキサジアゾール、ベンゾジオキソール、インドリン、インドール、インダゾール、またはベンゾモルフォリンである。最も好ましくは、R10は、置換されたイミダゾール、置換されたピラゾール、置換されたピリジン、フェニル、フルオロフェニル、シアノフェニル、テトラヒドロベンゾフラン、ベンゾピラン、ジヒドロベンゾジオキシン、ベンゾキサジノン、ベンゾオキサジアゾール、ベンゾジオキソール、インドリン、またはベンゾモルフォリンである;
R20、R21、R22、R23、およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルもしくは置換されていてもよいアルコキシである。好ましくは、R20、R21、R22、R23、およびR24は、それぞれ独立して、水素、フルオロ、クロロ、メチルから選択される。
【0075】
特に好ましい本発明の化合物は:
N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(3−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
ナフタレン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−3,4−ジメトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
2,3−ジヒドロ−ベンゾ[1,4]ジオキシン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−4−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
チオフェン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
チオフェン−3−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−4−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−2−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−4−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−2−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−2−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−メトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3,5−ジクロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−クロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(3−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(3−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(4−トリフルオロメチル−ベンジル)−ベンゼンスルホンアミド;
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(3−トリフルオロメトキシ−ベンジル)−ベンゼンスルホンアミド;
N−(2−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
2,2−ジメチル−クロマン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−4−ニトロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
フラン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−N−[3−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[3−メトキシ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(3,4−ジヒドロ−1H−イソキノリン−2−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(2,6−ジメチル−モルフォリン−4−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−4−エチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(4−ベンジル−4−ヒドロキシ−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2,3−ジメトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−クロロ−ベンジル)−N−{4−[3−(4−メトキシ−フェニル)−ピペリジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−フルオロ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−メトキシ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド;
1,3−ジメチル−1H−ピラゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2,3−ジメチル−3H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2,4−ジメチル−チアゾール−5−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド;
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−3−フルオロフェニル]−ジメチルスルファミド;
N−(4−フルオロ)ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド;
4−{4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−ベンゾイル}−2−フェニル−ピペラジン−1−カルボン酸tert−ブチルエステル;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(4−フルオロ−フェニル)−ピロリジン−1−カルボニル]−フェニル}−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−ジメチルスルファミド;
N−ベンジル−N−{4−[3−(3−イソプロピル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−ジメチルスルファミド;
N−ベンジル−N−[4−(3−ベンジロキシ−ピロリジン−1−カルボニル)−フェニル]−ジメチルスルファミド;
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド;
N−ベンジル−N−[4−(4−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[4−(2−フルオロ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−シクロヘキシルメチル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−チアゾール−2−イル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−トリフルオロメチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4,4−ジフルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
ピリジン−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−フルオロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3,4−ジクロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−4−フルオロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(2−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3,3−ジフルオロ−ピロリジン−1−カルボニル)−フェニル]−アミド;
およびそれらの製薬上許容されうる塩を含む。
【0076】
本明細書で用いられる場合、製薬上許容されうる塩は製薬上許容されうる酸または塩基の塩である。製薬上許容されうる酸は塩酸、硫酸、リン酸、二リン酸、臭化水素酸、硝酸のような無機酸およびクエン酸、フマル酸、マレイン酸、リンゴ酸、アスコルビン酸、コハク酸、乳酸、安息香酸、酢酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸またはp−トルエンスルホン酸のような有機酸を含む。製薬上許容されうる塩基はアルカリ金属(例えば、ナトリウムまたはカリウム)およびアルカリ土塁金属(例えば、カルシウムまたはマグネシウム)水酸化物およびアルキルアミン類、アリールアルキルアミン類またはヘテロ環アミン類のような有機塩基を含む。
【0077】
本発明の化合物は一またはそれ以上の不斉中心を有していてもよい。誤解のないようにするため、本明細書において記載されている化学構造はラセミおよび非ラセミ混合物ならびに純粋なエナンチオマーおよび/またはジアステレオマーを含む、示されている化合物のすべての立体異性体を包含することを意味する。
【0078】
本明細書で述べられているように、本発明の化合物は様々な症状の治療に有用である。このように、第二形態において、本発明は、薬剤に用いるための本明細書に定義されている式(I)の化合物を提供する。好ましくは、前記化合物は乾癬、関節リウマチおよび多発性硬化症を含む免疫不全のような、カリウムチャネルの阻害に必要な症状を予防または治療するために使用される。
【0079】
更なる形態において、本発明は少なくとも一つの式Iまたは本明細書に定義されている化合物および任意に一またはそれ以上の賦形剤、担体または希釈剤を含む医薬製剤を提供する。
【0080】
本発明の組成物は、投与毎にそれぞれの活性成分を所定量で含む単位投与形態において与えられうる。そのような、単位は、前記化合物を5〜100mg/日、好ましくは5〜15mg/日、10〜30mg/日、25〜50mg/日、40〜80mg/日または60〜100mg/日のいずれかが採用されうる。式Iの化合物において、100〜1000mg/日、好ましくは100〜400mg/日、300〜600mg/日または500〜1000mg/日の範囲で投与される。そのような投与は一回または数回の別個に投与することもできる。最高の投与は、治療状況、投与経路、年齢、体重、患者の状況次第であり、医者の判断に基づく。
【0081】
本発明の組成物は、適当な経路、例えば、経口(口腔または舌下を含む)、直腸、経鼻、局所(口腔、舌下または経皮を含む)、膣内または非経口(皮下、筋肉内、静脈または皮内を含む)によって投与することが採用される。そのような形態は製薬分野で知られているいかなる方法を用いて調製されてもよく、例えば、前記活性成分と担体または賦形剤とを組み合わせて用いることができる。
【0082】
経口投与において用いられる医薬製剤は、カプセルもしくはタブレット;粉末もしくは顆粒;水中もしくは非水中の溶液もしくは懸濁液、食用泡もしくはホイップ、または水中油型エマルジョンもしくは油中水型エマルジョンのような別々のものであってよい。
【0083】
経疲投与において用いられる医薬製剤は、長時間、レシピエントの表皮に接触させたまま別々にパッチするようなものであってよい。例えば、Pharmaceutical Research,3(6),318(1986)に一般的に記載されているように、有効成分をパッチからイオントフォレシスによって投与してもよい。
【0084】
局所投与において用いられる医薬製剤は、軟膏、クリーム、サスペンション、ローション、パウダー、溶液、ペースト、ゲル、スプレー、エアロゾルまたはオイルとして形成されていてもよい。
【0085】
目または他の外部の細胞組織(例えば、口や皮膚)に応用するため、前記の製剤は、好ましくは局所軟膏またはクリームとして利用される。軟膏の場合は、有効成分は、パラフィンまたは水混和性の軟膏とともに用いられてもよい。また、有効成分は、水中油型クリーム型または油中水型のクリームで形成されてもよい。
【0086】
目に局所投与するために用いられる医薬製剤は、有効成分が適当な担体、特に水系溶媒に溶解しまたは懸濁している目薬を含む。
【0087】
口に局所投与するために用いられる医薬製剤は、キャンディー、トローチおよびうがい薬を含む。
【0088】
直腸投与するために用いられる医薬製剤は、坐薬またはかん腸剤のようなものであってもよい。
【0089】
経鼻投与するために用いられる医薬製剤は、担体が固体(例えば、20〜500ミクロンの粒径である粗粉末を含む)であるような場合においては、嗅ぎタバコの形態で投与される(すなわち、鼻の近くにある粉末容器から経鼻経路からすばやく吸入される)。前記担体が液体である場合においては、例えば、鼻腔用スプレーまたは点鼻薬として投与をするため、有効成分の水溶液または油溶液を含む。
【0090】
吸入投与するために用いられる医薬製剤は、様々な種の定量噴霧用の加圧エアロゾル、噴霧器または吸入器により作り出される微粒子またはミストを含む。
【0091】
膣内投与するために用いられる医薬製剤は、ペッサリー、タンポン、クリーム、ゲル、ペースト、フォームまたはスプレーの形態であってもよい。
【0092】
非経口投与するために用いられる医薬製剤は、抗酸化剤、緩衝液、静菌薬およびレシピエントの血液と等浸透圧である溶液を含みうる水溶性および非水溶性滅菌注射剤溶液;ならびに、懸濁剤と増粘剤を含みうる水溶性および非水溶性滅菌懸濁液を含む。当該形態は、例えば、密封アンプルやバイアルのような単位用量または複数用量の容器にあってもよく、および使用の直前に、例えば、注射液における水のような滅菌液体担体を添加する必要があるフリーズドライ(凍結乾燥された)状態で保存するものであってもよい。即席注射溶液および懸濁液は滅菌粉末、顆粒およびタブレットから調製してもよい。
【0093】
好ましい単位用量の形態は、本明細書において上述されているような有効成分を一日用量もしくはサブ用量を含むものまたは適当な分量を含むものである。
【0094】
特に上記されている成分に加えて、例えば、経口投与においては香味料を含んでいるのが好ましいように、探求の結果の形態種類である当業界における慣用される他の試薬を含んでもよい。
【0095】
本発明の組成物は、例えば免疫不全の治療におけるカリウムチャネルの阻害に必要である状態を治療するために使用されうる。このように、更なる態様において、本発明は、
(i)例えば、少なくとも一つの本発明の化合物もしくは本発明の薬剤組成物を有効量、患者に投与することを含む免疫不全のようなカリウムチャネル阻害を必要とする疾患を治療または予防する方法
および
(ii)カリウムチャネル阻害に用いるための薬剤の製造における本発明の化合物の使用:
を提供する。
【0096】
特に、前記薬剤は乾癬、関節リウマチ、多発性硬化症および他の免疫不全の治療または予防においてを使用するものである。
【0097】
第一態様の好ましい実施形態は、適宜変更してすべての他の態様に利用される。
【0098】
式(I)の化合物は、例えば、以下スキーム1〜5に示される、従来のルートにより調製されうる。
【0099】
【化9】

【0100】
X1がC=Oであり、X3、X4、R1、R3、R10およびnが上述されるように定義される式(I)の化合物は、X1がC=Oであり、AはOHならびにR1、R3およびR10は上述されるように定義される式(VIII)の化合物とX3とX4が上述されるように定義される式(IX)のアミンとから、スキーム1に示されるように調製されうる。通常、本反応は、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド(EDC)または2−(7−アザ−1H−ベンズトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート(HATU)のようなカップリング試薬を用いて、テトラヒドロフラン、アセトニトリルまたはジメチルホルムアミドのような溶媒中、室温から還流温度の範囲内で当業者に周知の常法により行われる。または、X3、X4、R1、R3、R10およびnが上述されるように定義される式(I)の化合物はAがClまたはBrである式(VIII)の化合物と式(IX)のアミンとから調製することもできる。通常、この反応は、例えば、トリエチルアミンのような塩基存在下、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒中、室温から還流温度の範囲内で当業者に公知の常法により調製することもできる。
【0101】
【化10】

【0102】
AはOHでありR1、R3およびR10は上述されるように定義される式(VIII)の化合物はスキーム2に示されるように、APがOH基をtert−ブチルエステルのような適当な保護をしたものであり、R1、R2、R3は上述されるように定義されるものであり、例えば、トリフルオロ酢酸のような適当な酸存在下で、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒を利用して、0℃から還流温度の範囲内で、当業者に周知の常法で脱保護して調製することができる。
【0103】
式(X)の化合物は、R3とR10は上述されるように定義されるスルホンアミド(XII)から、R1が上述されているものであり、YがClまたはBrである式R1−Yと求電子剤との反応を、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒中、室温から還流温度の範囲内で当業者に周知の常法により調製することもできる。または、R1とR3が上述されるように定義されるアミン(XI)から、例えば、ピリジン、トリエチルアミンまたは炭酸カリウムのような塩基存在下、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒中、室温から還流温度の範囲内で、式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとの反応を当業者に周知の常法により調製することもできる。
【0104】
式(XII)の化合物は既知化合物であり、またはR3が上述されるように定義される式(XIII)の化合物から、例えば、炭酸カリウム、トリエチルアミンまたはピリジンのような塩基存在下、ジクロロメタン、テトラヒドロフランおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとの反応を当業者に周知の常法により調製することもできる。
【0105】
式(XI)の化合物は既知化合物であり、または式(XIII)の化合物から、例えば、炭酸カリウム、トリエチルアミンまたはピリジンのような塩基存在下、ジクロロメタン、テトラヒドロフランおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがClまたはBrである式R1−Yの求電子剤を用いたアルキル化のような当業者に周知の常法により調製することもできる。または、式(XI)の化合物は式(XIII)の化合物から、例えば、トリアセト水素化ホウ素ナトリウムのような還元剤存在下、ジクロロメタン、テトラヒドロフランおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがCHOである式R1−Yのアルデヒドの還元的アミノ化を周知の常法により調製することもできる。式(XIII)は既知化合物であり、または当業者に周知の常法により調製することもできる。
【0106】
【化11】

【0107】
R2がSO2R10であり、X1、X3、R1、R3、R10およびnが上述されるように定義される式(I)の化合物は式(XVI)のアミンと式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとから、例えば、トリエチルアミン、ジイソプロピルアミンまたはピリジンのような塩基存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法によりスキーム3に示すように調製することもできる。または、式(I)の化合物は式(XIV)の化合物から、例えば、炭酸セシウムのような塩基存在下、テトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがClまたはBrである式R1−Yの求電子剤との反応を当業者に周知の常法により調製することもできる。
【0108】
X1がCH2であり、R2がSO2R10であり、X3、X4、R1、R3、R10およびnが上述されるように定義される式(I)の化合物は、X1がC=Oである式(I)の化合物から、例えば、水素化アルミニウムリチウムのような還元剤の存在下、テトラヒドロフランまたはジエチルエーテルのような適当な溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。
【0109】
X1、X3、X4、R1、R3およびnが上述されるように定義される式(XVI)の化合物は既知の化合物であり、または式(XV)のアミンから、例えば、炭酸カリウム、トリエチルアミンまたはピリジンのような塩基存在下、テトラヒドロフラン、ジクロロメタンおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがClまたはBrである式R1−Yの求電子剤とのアルキル化のような当業者に周知の常法により調製することもできる。または、式(XVI)の化合物は式(XV)の化合物から、例えば、トリアセト水素化ホウ素ナトリウムのような還元剤存在下、テトラヒドロフラン、ジクロロメタンまたはアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがCHOである式R1−Yのアルデヒドの還元的アミノ化を周知の常法により調製することもできる。
【0110】
X1、X3、X4、R3、R10およびnが上述されるように定義される式(XIV)の化合物は式(XV)のアミンと式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとから、例えば、トリエチルアミン、ジイソプロピルアミンまたはピリジンのような塩基存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。
【0111】
【化12】

【0112】
X1がC=Oであり、X3、X4、R3およびnが上述されるように定義される式(XV)の化合物は、既知の化合物であり、X1がC=Oであり、AがOHであり、R3が上述されるように定義される式(XIX)の化合物から、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド(EDC)または2−(7−アザ−1H−ベンズトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート(HATU)のようなカップリング試薬と一緒に、例えば、テトラヒドロフラン、アセトニトリルまたはジメチルホルムアミドのような溶媒中、室温から還流温度の範囲内で当業者に周知の常法によりスキーム4に示されるように調製することもできる。
【0113】
X1がCH2であり、X3、X4、R3、およびnが上述されるように定義される式(XV)の化合物は、既知化合物であり、またはX1がCH2であり、AはClまたはBrのような脱離基である式(XIX)の化合物から調製でき、および式(IX)の化合物は、例えば、トリエチルアミン、ジイソプロピルアミンまたはピリジンのような塩基存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。
【0114】
X1がCH2であり、X3、X4、R1、R3、およびnが上述されるように定義される式(XV)の化合物は、X1がC=Oであり、AはHである式(XIX)の化合物から調製でき、および式(IX)の化合物は、例えば、トリアセト水素化ホウ素ナトリウムのような還元剤存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。または、X1がCH2であり、X4がCH2であり、X3、R1、R3、およびnが上述されるように定義される式(XV)の化合物は、X1がC=Oである式(XV)の化合物から、例えば、水素化アルミニウムリチウムのような還元剤存在下、例えばテトラヒドロフランまたはジエチルエーテルのような溶媒中、室温から還流温度の範囲内で、還元のような当業者に周知の常法により調製することもできる。
【0115】
X1が化学結合、CH2またはC(=O)であり、X3、X4、R3、およびnが上述されるように定義される式(XV)の化合物は、既知化合物であり、またはX1が化学結合、CH2またはC(=O)である式(XVII)の化合物から、例えば、塩化スズ(II)のような還元剤とエタノールのような溶媒中、室温から還流温度の範囲内で、還元のような当業者に周知の常法により調製することもできる。
【0116】
X1がCH2またはC(=O)である式(XVII)の化合物は、AがClまたはBrのような脱離基であるニトロ化合物(XVIII)と式(IX)の化合物とからピリジン、トリエチルアミンまたは炭酸カリウムのような塩基を使用して、テトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の温度範囲内で、当業者に周知の常法により合成することができる。
【0117】
【化13】

【0118】
X1が化学結合であり、X3、X4、R3、およびnが上述されるように定義される式(XVII)の化合物は、既知化合物であり、または式(XX)の化合物と式(IX)の化合物とから、例えば、ジクロロメタン、アセトニトリル、テトラヒドロフラン、またはNN−ジメチルホルムアミドのような溶媒中、室温から還流温度の範囲内の温度で、当業者に周知の常法により、N−メチルモルフォリンのような塩基を使用して調製することもできる。または、X1が化学結合である式(XVII)の化合物は、例えば、ピリジンまたはトリエチルアミンのような塩基存在下、ジクロロメタン、アセトニトリル、テトラヒドロフランのような適当な溶媒中、YがClまたはBrである式(XXI)の求電子剤との反応のように当業者に周知の常法により調製することもできる。式(XX)、(XXII)および(XXI)の化合物は当業者に既知の方法により調製することができる。
【0119】
本発明の化合物はカリウムチャネル阻害剤(Kv)であることがわかっており、したがって、治療効果に有益である。そのような化合物は新規であり、本発明はまたこれらの化合物を提供する。以下に例示される実施例および、当業者に理解されるように、特別な試薬または条件はそれぞれの化合物に必要なように修正されうる。上述される反応において使用される多くの出発材料は市販のものから利用されまたは参考文献に引用される方法で製造されうる。
【実施例】
【0120】
HPLC分析を以下の方法によって行った:
溶媒:[MeCN−0.05% HCO2H:H2O−0.1%HCO2H],10−95%勾配 3min,95% 2.5min;カラム: Phenomenex Gemini 50x4.6mm i.d., C18逆相;流速 0.75mL/min(別途記載のない場合)
溶媒:[MeCN−0.05% HCO2H:H2O−0.01%HCO2H],5−95%勾配 5min,95% 3min;カラム:Phenomenex Gemini 50x4.6mm i.d.,C18逆相;流速 1.5mL/min(別途記載のない場合)。
【0121】
溶媒:[MeCN:H2O−0.1%HCO2H],5−95%勾配 3.5min,95% 2min;カラム:Phenomenex Gemini 50x3mm i.d.,C18逆相;流速 1mL/min(別途記載のない場合)。
【0122】
溶媒:[MeCN−0.05% HCO2H:H2O−0.1%HCO2H],5−95%勾配 6 min,95% 3min;カラム:Phenomenex Gemini 50x4.6mm i.d.,C18逆相;流速 1mL/min(別途記載のない場合)。
【0123】
分取用HPLCによる精製は以下のように行われた:
溶媒:[MeCN−0.05% HCO2H:H2O−0.1%HCO2H],5−95%勾配 12min,95% 3min;カラム:Waters X−Bridge 100x19 mm i.d.,C18逆相;流速 16mL/min(別途記載のない場合)。
【0124】
実施例1)N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(方法A)
i)(4−ニトロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
0℃で攪拌している4−ニトロ塩化ベンゾイル(6.23g,33.9mmol)とN−フェニルピペラジン(4.71ml,30.8mmol)の無水ジオキサン(250ml)溶液に、トリエチルアミン(4.73ml,33.9mmol)を加え、当該混合物を還流温度(110℃)で5時間攪拌した。冷却後、水(100ml)でクエンチし、得られた水溶性混合物を酢酸エチル(2x75ml)で抽出した。その有機抽出液を混合し、硫酸マグネシウムで乾燥し、濃縮して黄色の油状の粗生成物を得た。純粋な生成物を40%の石油酢酸エチルの混合物から結晶化し、白色結晶(6.5g,62%)として標記化合物を得た。HPLCの保持時間 6.9min。マススペクトル(ES+) m/z 312(M+H)。
【0125】
以下の化合物を、適当な出発原料を使用して、前記記載の方法により合成した。
【0126】
1−(4−ニトロ−ベンゼンスルホニル)−4−フェニル−ピペラジン
ii)(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
塩化スズ二水和物(5.44g,24.1mmol)の濃塩酸(32ml)溶液を、冷却しながら攪拌している(4−ニトロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン(1.0g,3.2mmol)の無水ジエチルエーテル(32ml)溶液にゆっくり加えた。当該混合物を室温で1時間攪拌し、冷却しながら、10Mの水酸化ナトリウム(水溶液)でわずかに塩基性(〜pH9)になるまで注意してクエンチした。当該水溶液を酢酸エチル(100ml)で抽出し、有機抽出物を硫酸マグネシウムで乾燥した。その後、真空内で濃縮し、標記化合物をクリーム色の固体(667mg,収率73%)として得た。HPLCの保持時間 6.2min。マススペクトル(ES+) m/z 282(M+H)。
【0127】
iii)[4−(4−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
攪拌している(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン(200mg,0.71mmol)の1,2−ジクロロエタン(4ml)溶液に、3−クロロベンズアルデヒド(99.7mg,0.71mmol)を0℃で加えた。トリアセト水素化ホウ素ナトリウム(210mg,0.99mmol)と酢酸(40.6μl、0.71mmol)を加え、窒素雰囲気下、室温でオーバーナイト、攪拌した。水酸化ナトリウム(水溶液)(pH8)を加えて反応をクエンチし、ジエチルエーテル(3x20ml)で抽出した。有機抽出液を混合し、硫酸マグネシウムで乾燥し、真空内に濃縮した。残留物をフラッシュクロマトグラフィにより精製し、標記化合物を黄色固体(72mg,収率25%)として得た。HPLCの保持時間 7.5min。マススペクトル(ES+) m/z 406(M+H)。
【0128】
以下の化合物を適当な出発物質を使用して前記記載の方法により合成した。
(4−ベンジルアミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−フルオロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3,4−ジメトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
ベンジル−[4−(4−フェニル−ピペラジン−1−スルホニル)−フェニル]−アミン
(4−フルオロ−ベンジル)−[4−(4−フェニル−ピペラジン−1−スルホニル)−フェニル]−アミン
iv)N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(1)
攪拌している、[4−(4−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン(30mg,0.07mmol)とフェニルスルホニルクロライド(14.2μl、0.11mmol)の無水ジクロロメタン(1ml)溶液に、ピリジン(7.2μl、0.09mmol)を加え、室温で18時間攪拌した。PS−トリス(32mg,0.13mmol)を加え、当該混合物を3時間激しく攪拌し濾過した。濾液を真空内で濃縮し、標記化合物を黄色固体(48mg,収率98%)として得た。HPLCの保持時間 7.7min。マススペクトル(ES+) m/z 547(M+H)。
【0129】
他の化合物を、表2に列挙されている適当な出発原料を使用して実施例1に記載されている方法Aにより調製した。
【0130】
実施例2)N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(方法B)
i)(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
攪拌している、4−アミノ安息香酸(5g,36.5mmol)の懸濁したアセトニトリル溶液に、1−エチル−3−(3−ジメチルアミノプロピル)−塩酸カルボジイミド(7.67g,40.2mmol)、ヒドロキシベンゾトリアゾール水和物(0.49g,3.65mmol)、1−フェニルピペラジン(11.2ml、3.65mmol)を加え、次いで、トリエチルアミン(12.8ml、91.3mmol)を加えた。当該反応混合物を室温で16時間攪拌した。水を加えて希釈し、ジクロロメタン(3x100ml)を使用して抽出した。有機層を混合し、硫酸マグネシウムで乾燥し、真空内で濃縮した。得られた残渣をフラッシュカラムクロマトグラフィ(SiO2)により酢酸エチル/ジクロロメタン(1:1)で溶出して精製し、標記化合物をオフホワイトの固体として得た。HPLCの保持時間 7.1min。マススペクトル(ES+) m/z 282(M+H)。
【0131】
以下の化合物を適当な出発原料を使用して前記記載の方法により合成した。
【0132】
(4−アミノ−3−フルオロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−アミノ−3−メチル−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
ii)4−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−ベンゾニトリル
攪拌している(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン(0.5g,1.78mmol)のテトラヒドロフラン(10mL)溶液に4−シアノベンズアルデヒドを加え、次いで水素化ホウ素ナトリウムを加え、当該反応を50℃に2時間加熱した。冷却して、当該反応を水(10mL)を加えてクエンチし、塩化アンモニウムを加えて水溶液を塩基性(〜pH8)にした。当該水溶液をジクロロメタン(3x10ml)を使用して抽出し、有機抽出液を混合して、硫酸マグネシウムの上で乾燥し、真空内で濃縮し、標記化合物をオフホワイトの固体(604mg,収率98%)として得た。HPLCの保持時間 7.17min。マススペクトル(ES+) m/z 397(M+H)。
【0133】
以下の化合物を適当な出発物質を使用して前記記載の方法により合成した。
【0134】
[4−(4−ジメチルアミノ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−tert−ブトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−フルオロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(ビフェニル−4−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−フェニル−ピペラジン−1−イル)−{4−[(ピリジン−3−イルメチル)−アミノ]−フェニル}−メタノン
[4−(2−メチル−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−メチル−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(ナフタレン−2−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(ナフタレン−1−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(シクロペンチルメチル−アミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
4−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−安息香酸メチルエステル
(4−フェニル−ピペラジン−1−イル)−[4−(4−トリフルオロメチル−ベンジルアミノ)−フェニル]−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(2−トリフルオロメトキシ−ベンジルアミノ)−フェニル]−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(3−トリフルオロメトキシ−ベンジルアミノ)−フェニル]−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(4−トリフルオロメトキシ−ベンジルアミノ)−フェニル]−メタノン
2−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−ベンゾニトリル
(4−フェニル−ピペラジン−1−イル)−{4−[(チオフェン−3−イルメチル)−アミノ]−フェニル}−メタノン
{4−[(フラン−3−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(フラン−2−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−フェネチルアミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(シクロプロピルメチル−アミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−ベンジロキシ−エチルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(シクロヘキシルメチル−アミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(3−フェニル−プロピルアミノ)−フェニル]−メタノン
{4−[(1−メチル−1H−ピラゾール−4−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−3−フルオロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−3−メチル−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−エトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2,3−ジメトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
iii)N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(2)
4−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−ベンゾニトリル(50mg,0.13mmol)、フェニルスルホニルクロライド(80mg,0.42mmol)およびピリジン(0.04mL,0.44mmol)のジクロロメタン(5ml)混合液を16時間還流した。当該混合物を室温まで冷却して、水(4ml)を加えてクエンチした。有機層を回収して、硫酸マグネシウムで乾燥し、真空内で濃縮した。その残渣を分取用薄層クロマトグラフィ(ジクロロメタン/酢酸エチル 1:1)で精製し、標記化合物を白色固体(16.4mg,収率27%)として得た。HPLCの保持時間 6.71min。マススペクトル(ES+) m/z 475(M+H)。
【0135】
以下の化合物を表1に列記されている適当な出発物質を使用して、実施例2に記載の方法Bにより調製した。
【0136】
実施例3)N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド:(方法C)
i)4−ベンジルアミノ−安息香酸
ベンズアルデヒド(9.63ml,95mmol)、酢酸(4.9ml,91.3mmol)を、攪拌している4−アミノ安息香酸(10g,73mmol)のテトラヒドロフラン(200ml)溶液に加え、次いでトリアセト水素化ホウ素ナトリウム(31g,146mmol)を加え、16時間室温で攪拌した。当該反応混合物を水(200ml)で希釈し、ジクロロメタン(2x200ml)で抽出した。当該有機層を混合し、ブラインで洗浄し、硫酸マグネシウムで乾燥し、その後真空内で濃縮した。残渣をフラッシュクロマトグラフィ(SiO2)を用いてジエチルエーテル/ジクロロメタン(1:4)で溶出し、精製した。標記化合物をオフホワイトの固体(4.74g,収率28%)として得た。HPLCの保持時間 5.32min。マススペクトル(ES+) m/z 228(M+H)。
【0137】
ii)(4−ベンジルアミノ−フェニル)−ピペリジンピペリジン−1−イル−メタノン
ピペリジン(0.174ml,1.8mmol)、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド塩酸塩(184mg,0.97mmol)、ヒドロキシベンゾトリアゾール水和物(10mg,結晶)を、攪拌している4−(ベンジルアミノ)安息香酸(200mg,0.88mmol)のアセトニトリル(2ml)懸濁溶液に加え、次いでトリエチルアミン(0.31ml,2.2mmol)を加え、16時間室温で攪拌した。当該混合物を水(2ml)で希釈し、ジクロロメタン(2x2ml)で抽出した。当該有機層を混合し、ブラインで洗浄し、硫酸マグネシウムで乾燥し、その後真空内で濃縮した。残渣をフラッシュクロマトグラフィ(SiO2)を用いて酢酸エチル/ジクロロメタン(1:4)で溶出し、精製した。標記化合物をオフホワイトの固体(122mg,収率47%)として得た。
【0138】
以下の化合物を適当な出発原料を使用して記載されている方法によって合成した:
(4−ベンジルアミノ−2−メチル−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−3−フルオロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−2−メトキシ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
N−ベンジル−N−{4−[4−(2−メトキシ−エチル)−ピペラジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド
N−ベンジル−N−{4−[4−(2−オキソ−2−ピロリジン−1−イル−エチル)−ピペラジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド
(4−ベンジルアミノ−フェニル)−(3,4−ジヒドロ−1H−イソキノリン−2−イル)−メタノン
(4−ベンジルアミノ−フェニル)−(2,6−ジメチル−モルホリン−4−イル)−メタノン
iii)N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(3)
ベンゼンスルホニルクロライド(57μl,0.46mmol)を、攪拌している(4−ベンジルアミノ−フェニル)−ピペリジン−1−イル−メタノン(39mg,0.14mmol)のジクロロメタン(1ml)溶液に加え、次いでピリジン(42μl,0.5mmol)を加え、20時間40℃で加熱した。当該反応を室温まで冷却し、混合物を水(5ml)とジクロロメタン(5ml)間に分離した。有機層を回収し、真空内で濃縮し、分取用TLCにより精製し、標記化合物を白色固体(38mg,収率62%)として得た。HPLCの保持時間 5.8min。マススペクトル(ES+) m/z 435(M+H)。
【0139】
他の化合物を表1に列挙されている適当な出発原料を使用して実施例3に記載されている方法Cにより調製した。
【0140】
実施例4)N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド :(方法D)
i)4−(4−クロロ−ベンジルアミノ)−安息香酸tert−ブチルエステル
tert−ブチル−4−アミノベンゾエート(5.0g,26mmol)、酢酸(2.23ml,39mmol)を、攪拌している4−クロロベンズアルデヒド(5.46g,39mmol)のジクロロメタン(50ml)の溶液に加え、次いでトリアセト水素化ホウ素ナトリウム(13.7g,65mmol)を加え、16時間室温で攪拌した。当該反応混合物に氷(100ml)を加えてクエンチし、得られた水溶液を炭酸ナトリウム(固体)を使用して中和した。ジクロロメタン(3x100ml)を使用して当該水溶液から抽出し、有機層を混合し、硫酸マグネシウムで乾燥し、その後真空内で濃縮し、標記化合物を白色固体(10g,収率81%)として得た。HPLCの保持時間 8.09min。マススペクトル(ES+) m/z 318(M+H)。
【0141】
以下の化合物は適当な出発原料を使用して記載されている方法により合成した:
4−(ベンジルアミノ)−安息香酸tert−ブチルエステル
4−(4−フルオロ−ベンジルアミノ)−安息香酸tert ブチルエステル
4−(ベンジルアミノ)−3−フルオロ−安息香酸tert ブチルエステル
ii)4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸tert−ブチルエステル
4−(4−クロロ−ベンジルアミノ)−安息香酸tert−ブチルエステル(6g,6.3mmol)、フェニルスルホニルクロライド(2.9ml,21mmol)およびピリジン(1.86mL,23mmol)をジクロロメタン(25ml)中16時間加熱還流した。当該反応混合物を室温まで冷却し、ジクロロメタン(25ml)で希釈し、水(2x25ml)で洗浄した。有機層を回収し、硫酸マグネシウムで乾燥し、真空内で濃縮し、フラッシュクロマトグラフィ(ヘキサン/酢酸9:1)によって黄色のオイルを精製し、標記化合物を白色固体(2.2g,収率76%)として得た。HPLCの保持時間 8.54min。
【0142】
以下の化合物を適当な出発原料を使用して記載されている方法により合成した:
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸tert−ブチルエステル
4−[(4−クロロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸tert−ブチルエステル
4−[(4−フルオロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸tert ブチルエステル
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−3−フルオロ−安息香酸tert ブチルエステル
4−(ベンゼンスルホニル−ベンジル−アミノ)−安息香酸tert−ブチルエステル
iii)4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸
4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸tert−ブチルエステル(2.1g,4.4mmol)の10%トリフルオロ酢酸/ジクロロメタン(50mL)溶液を16時間室温で攪拌した。当該反応混合物を真空内で濃縮し、残渣を炭酸水素ナトリウム(飽和溶液、25mL)とジクロロメタン(20mL)間に分離した。水層を分離し、10%HCl(aq)を用いて酸性(pH1)にし、得られた溶液をジクロロメタン(3x75mL)を用いて抽出した。その有機層を混合し、硫酸マグネシウムで乾燥し、真空内で濃縮し、標記化合物を白色固体(1.1g,収率62%)として得た。
【0143】
以下の化合物を適当な出発原料を使用して記載されている方法により合成した:
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸
4−[(4−クロロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸
4−[(4−フルオロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−3−フルオロ−安息香酸
4−(ベンゼンスルホニル−ベンジル−アミノ)−安息香酸
iv)N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(4)
3−(4−メチルフェニル)ピペリジン(40mg,0.19mmol)、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド塩酸塩(EDC)(24mg,0.13mmol)を、攪拌している4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸(50mg,0.13mmol)のアセトニトリル(1mL)溶液に加え、次いでヒドロキシベンゾトリアゾール(HOBt)(1.7mg,0.013mmol)を加え、16時間室温で攪拌した。当該反応混合物を水(3ml)で希釈し、ジクロロメタン(3x2ml)を用いて抽出した。有機抽出液を混合し、硫酸マグネシウムで乾燥し、真空内で濃縮し、得られた残渣をフラッシュクロマトグラフィ(ジクロロメタン/酢酸エチル 9:1)により精製し、標記化合物を白色発泡体(31mg,収率44%)として得た。HPLCの保持時間 8.25min。マススペクトル(ES+) m/z 559(M+H)。
【0144】
適当な出発原料を使用して実施例4に記載されている方法Dにより調製された他の化合物を表1に列挙する
実施例5)N−ベンジル−N’N’−ジメチル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−スルファミド :(方法E)
i)N−ベンジル−N’N’−ジメチル−N−(4−安息香酸tert−ブチルエステル)−スルファミド
4−ベンジルアミノ−安息香酸tert−ブチルエステル(2g,7mmol)とN,N−ジメチルスルファモイルクロライド(3.8ml,35mmol)のピリジン(20ml)溶液を2時間100℃で加熱した。当該反応混合物を室温に冷却し、,N−ジメチルスルファモイルクロライド(1ml,9mmol)を加え、当該反応を16時間100℃で加熱した。当該反応混合物を室温に冷却し、トルエン(3x100ml)を用いて共沸混合物として真空内で濃縮した。残渣を酢酸エチル(3x100ml)を用いて洗浄し、当該洗浄物を真空内で濃縮して橙のオイルを得た。当該オイルを15%酢酸エチル/ヘキサンを用いてシリカゲルを用いたフラッシュクロマトグラフィにより精製し、標記化合物を白色固体として得た。HPLCの保持時間 6.75min。1HNMR(CDCl3) aH 1.56,s(9H),2.77,s(6H),4.85,s(2H),7.18−7.27,m(5H),7.33,d(2H、J= 8.84),7.9、d(2H、J=8.84).
ii)N−ベンジル−N’N’−ジメチル−N−(4−安息香酸)スルファミド
N−ベンジル−N−(4−安息香酸tert−ブチルエステル)−N’N’−ジメチルスルファミド(1g,2.5mmol)のジクロロメタン(80ml)溶液を0℃に冷却した。トリフルオロ酢酸(20ml)を5分かけて滴下して加え、当該反応を室温まで熱し、その後2時間攪拌した。当該反応混合物を真空内に濃縮し、残渣をヘキサン(100ml)を使用して粉末にした。得られた懸濁液を濾過により標記化合物をベージュ色の固体(0.7g,84%)として得た。HPLCの保持時間 4.28min。マススペクトル(ES+) m/z 333(M+H)。
【0145】
iii)N−ベンジル−N’N’−ジメチル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−スルファミド(5)
攪拌している1−(2−シアノフェニル)−ピペラジン(32mg,0.17mmol)の乾燥ジメチルホルムアミド(1ml)溶液に、N−ベンジル−N’N’−ジメチル−N−(4−安息香酸)スルファミド(50mg,0.15mmol)、トリエチルアミン(0.065ml,0.45mmol)および2−(7−アザ−1H−ベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウムヘキサフルオロホスフェート(63mg,0.17mmol)を加え、当該反応を16時間室温で攪拌した。溶媒を減圧下除去し、残渣を分取用HPLCにより精製した。HPLCの保持時間 6.0min。マススペクトル(ES+) m/z 504(M+H)。
【0146】
適当な出発原料を使用して実施例5に記載されている方法Eにより調製された他の化合物を表1に列挙する。
【0147】
実施例6)N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−N’,N’−ジメチルスルファミド(方法F)
i)(4−アミノ−フェニル)−(2−フェニル−モルフォリンモルフォリン−4−イル)−メタノン
攪拌している、安息香酸(160mg,1mmol)と2−フェニルモルフォリン塩酸塩(300mg,1.5mmol)のアセトニトリル(10ml)懸濁液にトリエチルアミン(0.4ml,3mmol)を加え、次いでHATUを加え、当該反応混合物を16時間室温で攪拌した。当該反応をジクロロメタン(25ml)を用いて希釈し、炭酸水素ナトリウム(25ml,飽和溶液)を用いて洗浄した。有機層を回収し、硫酸マグネシウムで乾燥し、真空内に濃縮した。残渣をシリカゲルフラッシュクロマトグラフィにより酢酸エチルを用いて溶出して精製し、標記化合物を透明なオイル(240mg,収率84%)として得た。HPLCの保持時間 5.05min。マススペクトル(ES+) m/z 283(M+H)。
【0148】
ii)(4−ベンジルアミノ−フェニル)−(2−フェニル−モルフォリン−4−イル)−メタノン
攪拌している(4−アミノ−フェニル)−(2−フェニル−モルフォリン−4−イル)−メタノン(240mg,0.84mmol)のジクロロメタン(20ml)溶液にベンズアルデヒド(0.1ml,1mmol)を加え、当該反応混合物を2時間45℃で加熱した。当該反応混合物を室温に冷却し、トリアセト水素化ホウ素ナトリウム(250mg,1.2mmol)を加え、当該反応を48時間室温で攪拌した。当該反応をジクロロメタン(10ml)を用いて希釈し、水(10ml)を加えてクエンチした。当該水溶液をジクロロメタン(2x10ml)を用いて洗浄し、有機層を混合し、真空内で濃縮し、その残渣をフラッシュクロマトグラフィにより精製し、標記化合物を無色のオイル(0.22g,収率70%)として得た。HPLCの保持時間 6.18min。マススペクトル(ES+) m/z 373(M+H)。
【0149】
iii)N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−N’,N’−ジメチルスルファミド(6)
(4−ベンジルアミノ−フェニル)−(2−フェニル−モルフォリン−4−イル)−メタノン(80mg,0.21mmol)とN,N−ジメチルスルファモイルクロライド(0.3ml,2mmol)のピリジン(5ml)溶液を16時間70℃で加熱した。得られた溶液を塩酸2N(20ml)で洗浄し、有機層を回収し、硫酸マグネシウムで乾燥した。溶媒を減圧除去し、残渣を50%酢酸エチル/ヘキサンを用いて溶出する分取用薄層クロマトグラフィにより精製し、標記化合物を無色のオイル(35mg,収率35%)として得た。HPLCの保持時間 6.1min。マススペクトル(ES+) m/z 480(M+H)。
【0150】
適当な出発原料を使用して実施例6に記載されている方法Fにより調製された他の化合物を表1に列挙する。
【0151】
実施例7)1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−ピペラジン−1−カルボニル)−フェニル]−アミド(方法G)。
【0152】
攪拌しているN−メチルピペラジン(20mg,0.2mmol)、トリエチルアミン(28μl 、0.2mmol)、および2−(7−アザ−1H−ベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート(42mg,0.11mmol)を4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸(37mg,0.1mmol)の乾燥ジメチルホルム(1ml)溶液に加え、当該溶液を16時間室温で攪拌した。当該反応混合物を真空内で濃縮し、その残渣を分取用HPLCを用いて精製し、標記化合物を透明なオイル(30mg,収率66%)として得た。HPLCの保持時間 4.5min。マススペクトル(ES+) m/z 454(M+H)。
【0153】
適当な出発原料を使用して実施例7に記載されている方法Gにより調製された他の化合物を表1に列挙する。
【0154】
実施例8)1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド(方法H)
i)4−(4−フェニル−ピペラジン−1−イルメチル)−フェニルアミン
水素化ホウ素ナトリウム(63 mg,1.68 mmol)のエタノール(1ml)溶液を、4−(4−フェニルピペラジン−1−イルメチル)−ニトロ−アニリン(1g,3.36 mmol)とスズ(II)ジクロリドニ水和物(2.27 g,10.10 mmol)のエタノール(20ml)溶液に60℃で滴下した。当該反応を0℃に冷却した後、得られた溶液を2時間攪拌し、水酸化ナトリウム(2M)を加えて塩基性(pH>10)にした。その水層をジクロロメタン(3x20ml)を用いて抽出し、混合した有機層をブラインで洗浄した。その後、硫酸マグネシウムで乾燥し、真空内で濃縮した。残渣をカラムクロマトグラフィ(ヘキサン/酢酸エチル 1:1)によって精製し、標記化合物を淡黄色の固体(441mg,49%)として得た。HPLCの保持時間 5.82min。マススペクトル(ES+) m/z 268(M+H)。
【0155】
ii)ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル)−アミン
トリアセト水素化ホウ素ナトリウム(282 mg,1.34 mmol)を、攪拌している4−(4−フェニル−ピペラジン−1−イルメチル)−フェニルアミン、ベンズアルデヒド(75 μl,0.73 mmol)および酢酸(43 μl,0.73 mmol)の乾燥ジクロロメタン(6 ml)溶液に1度に加え、16時間室温で攪拌した。水を加え、有機層を分離し、ブラインで洗浄し、硫酸マグネシウムで乾燥した。当該溶液を真空内に濃縮し、粗残渣をカラムクロマトグラフィ(ヘキサン/酢酸エチル 1:1)によって精製し、標記化合物を無色の固体(175 mg,72%)として得た。HPLCの保持時間 7.53min。マススペクトル(ES+) m/z 358(M+H)。
【0156】
iii)1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド(8)
ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル)−アミン(30mg,0.08mmol)、1−メチルイミダゾール−4−スルホニルクロライド(51 mg,0.27 mmol)およびピリジン(24 μl,0.30 mmol)の乾燥ジクロロメタン(2ml)溶液を加熱して15時間還流した。当該反応混合物を室温に冷却し、真空内で濃縮した。その残渣をカラムクロマトグラフィ(ジクロロメタン中、5%メタノール)により精製し、標記化合物をオフホワイトの固体(22mg,55%)として得た。HPLCの保持時間 7.04min。マススペクトル(ES+) m/z 502(M+H)。1H−NMR(CDCl3) aH 2.54(4H,m,2xCH2),3.16(4H,m,2xCH2),3.45(2H,br s,CH2),3.71(3H,s,CH3),4.99(2H,s,CH2),6.84(1H,t,J = 7.3 Hz,ArH),6.89(2H,m,2xArH),7.10(2H,m,2xArH),7.17−7.30(10H,m,10xArH),7.55(1H,m,ArH).
【0157】
【表1−1】

【0158】
【表1−2】

【0159】
【表1−3】

【0160】
【表1−4】

【0161】
【表1−5】

【0162】
【表1−6】

【0163】
【表1−7】

【0164】
【表1−8】

【0165】
実施例101:Kv1.3オートパッチ電気生理学手法
10μL/mL[100x]グルタミン、500μg/mL G418(ゲンタマイシン)、および1%HT添加物(50x、ヒポキサンチンおよびチミジン)を添加した、CHO細胞用のEx−cell302無血清培地中で、ヒトKv1.3のcDNA(pcDNA3.1中のもの)により安定的にトランスフェクトされた細胞を培養した。全細胞モードのオートパッチ技術を用い、これらの細胞により化合物を試験した。
【0166】
外部浴の溶液の含有物(mM):150 NaCl, 10 KCl, 1 MgCl2, 3 CaCl2, 10 HEPES, pH 7.4(NaOHによる)。パッチピペットを下記組成の電極溶液で満たした(mM):100 K−Gluconate, 20 KCl, 1 MgCl2, 1 CaCl2, 10 HEPES, 11 EGTA, 5 ATP−Na2, 2 グルタチオン, pH 7.2(KOHによる)。
【0167】
化合物をDMSO(100%)に溶解させ、使用直前に外部浴中で1μMの濃度に調製した。実験はすべて室温にて行なった。
【0168】
6×106細胞の密度を有する細胞懸濁物(10mL)を15mL遠心チューブに分取し、使用前は4℃にて保存した。使用前にチューブを取り出し、1000rpmで4分間、室温にて遠心分離した。次いで上清を捨て、チューブの底に細胞ペレットを得た。次いで、1mLの冷たい(4℃)濾過された(0.22μm)0.05%BSA/外部浴溶液(0.05g BSA/100mL外部浴溶液)を用いて当該ペレットを再懸濁させた。チューブの底を手動で撹拌し、次いで静かに粉砕した。次いで細胞懸濁液を、14℃に温度制御されたオートパッチ(商標)培養器に入れ、定期的に粉砕した。
【0169】
一定長さのテフロンキャピラリーチューブを細胞懸濁液に漬け、陰圧により液柱を吸い上げた。Ag/AgCl参照電極を用いてこの液柱を電気的に接続した。ホウケイ酸ガラスパッチピペット(from 1.5mm OD, thin−walled filamented, GC150−TF capillary glass, Harvard)を、DMZピペットガラス電極製作器(Zeitz Instruments)を用いて引き出し、ピペットの先端または本体に泡が残らないように気をつけながら内部ピペット溶液を用いて再充填した。パッチピペットは通常、2.5〜3.5MΩの抵抗を有していた。充填後、ピペットの先端および軸の一部(〜15mm)をシグマコート(Sigma)に漬けた。記録用ピペットをマルチウェルアレイ中に配置し、オートパッチ(AutoPatch)TM機器上に載せた。自動化パッチクランプおよび薬剤の投与についてはオペレータにより開始したが、その後は予めセットした条件および基準を満たす限りは実験をAutoPatch.exeにより継続した。
【0170】
細胞のパッチクランプの記録全体について、Pulseソフトウェア(v8.54またはv8.76, HEKA, Gemany)で制御されるEPC9またはEPC10増幅器(HEKA,Germany)、細胞アプリケータ、自動化薬剤投与システム(DAS)、バルブコントローラ(VF1)および吸引装置(すべて室温)を備えたAutoPatchTM装置を用いて行った。この装置は完全にAutoPatch.exeの制御下にあり、オペレータによる介入は水浴タンクを再充填したり技術的なミスによる細胞の損失を防止したりする必要がある場合のみ行った。
【0171】
灌流および薬剤投与の前に検証工程を行い、観測される電流が実験条件を満たすことを確認した。細胞には、外部溶液を〜2mL/minの流速で連続的に灌流させた。灌流チャンバは80〜85μLの可動体積を有しており、これにより薬液の迅速な交換が可能であった。
【0172】
電気生理学の電位ステップのプロトコールおよびデータの分析は以下のように行った。データについては5kHzでサンプリングし、2.5kHzのバンド幅で−3dBでフィルタリングした。細胞については−80mVの電位に維持した。500ミリ秒間の+30mVへの電位ステップを15秒毎に印加することで電流を発生させた。化合物を投与している間のhKv1.3電流のオンライン分析を、Pulse(v8.54またはv8.76, HEKA, Germany)、Excel(Microsoft, USA)およびAutoPatchTMのソフトウェアにより行い、電位ステップの間ずっと全電荷を測定した。薬剤の存在による電荷移動の阻害を、コントロールと比較して算出した。
【0173】
参考文献
Herbert, “General principles of the structure of ion channels”, Am. J. Med, 104, 87−98, 1998.
Armstrong & Hille, “Voltage−gated ion channels and electrical excitability”, Neuron, 20, 371,380, 1998.
Gutman GA et al., “International Union of Pharmacology. XLI. Compendium of voltage−gated ion channels: potassium channels”. Pharmacol Rev. Dec; 55(4):583−6, 2003.
Shieh et al., “Potassium Channels: Molecular Defects, Diseases, and Therapeutic Opportunities”, Pharmacol Rev, 52(4), 557−594, 2000.
Ford et al., “Potassium Channels: Gene Family, Therapeutic Relevance, High−Throughput Screening Technologies and Drug Discovery”, Prog Drug Res, 58, 133−168, 2002.
Xie M et al., “Ion Channel Drug Discovery Expands into New Disease Areas”, Current Drug Discovery, 31−33, 2004.
Beeton et al., “Kv1.3 channels are a therapeutic target for T cell−mediated autoimmune diseases”, Proceeds of the National Academy of Sciences, 46, 103, 17414−17419, 2006
Cahalan MD & Chandy KG, “Ion Channels in the Immune System as Targets for Immunosuppression”, Current Opinion in Biotechnology, 8, 749−756, 1997.
Wulff H, Beeton C, Chandy KG: Potassium channels as therapeutic targets for autoimmune disorders.(2003) Curr. Opin. Drug Dis. 6(5):640−647
Beeton C, Pennington MW, Wulff H, Singh S, Nugent D, Crossley G, Khaytin I, Calabresi PA, Chen CY, Gutman GA, Chandy KG. Targeting effector memory T−cells with a selective peptide inhibitor of Kv1.3 channels for therapy of autoimmune diseases.(2005) Mol Pharmacol. 67(4):1369−81.
Panyi G, Varga Z, Gaspar R. Abstract Ion channels and lymphocyte activation.(2004) Immunology Lett. 92:55−66.
Chandy KG, Wulff H, Beeton C, Pennington M, Gutman G, Cahalan M: K+ channels as targets for specific immunomodulation. TIPS.(2004) 25(5):280−289
Beeton C, Barbaria J, Giraud P, Devaux J, Benoliel A, Gola M, Sabatier JM, Bernard D, Crest M, Beraud E: Selective blocking of voltage−gated K+ channel improves experimental autoimmune encephalomyelitis and inhibits T cell activation.(2001) J. Immunol. 166:936−944
Price MJ, Lee SC, Deutsch C: Charybdotoxin inhibits proliferation and interleukin−2 production of human peripheral blood lymphocytes.(1989) Proc. Natl. Acad. Sci. 86:10171−10175
Koo GC, Blake JT, Shah K, Staruch MJ, Dumont F, Wunderler DL, Sanchez M, McManus OB, Sirontina−Meisher A, Fischer P, Boltz RC, Goetz MA, Baker R, Bao J, Kayser F, Rupprecht KM, Parsons WH, Tong X, Ita IE, Pivnichny J, Vincent S, Cunningham P, Hora D, Feeney W, Kaczorowski G, Springer MS: Correolide and derivatives are novel immunosuppressants blocking the lymphocyte Kv1.3 potassium channels.(1999) Cell. Immunol., 197:99−107
Schmitz A, Sankaranarayanan A, Azam P, Schmidt−Lassen K, Homerick D, Hansel W, Wulff H: Design of PAP−1, a selective small molecule Kv1.3 blocker, for the suppression of effector memory cells in autoimmune diseases.(2005) Mol. Pharmacol., 68:1254−1270
Triggle D.J, Gopalakkrishnan M, Rampe D, Zheng W: Voltage gated Ion channels as Drug Targets, Wiley, 2005)
Sands et al,: Charabydotoxin blocks voltage−gated K+ channels in human and murine T lymphocytes. J. Gen− Physiol. 1989, 93, 10061−1074.
Garcia et al, Purification, characterisation and biosynthesis of margatoxin, a component of Centruroides maragritatus venom that selectively inhibits voltage−gated potassium channels, J. Biol. Chem. 1993, 268, 18866−1887
Garcia et al,: Purification and characterisation of three inhibitors of voltage dependent K+ channels from Leiurus quinquesttriatus var. hebraeus. Biochemistry, 1994, 33, 6834−6839
Koshchak et al., Subunit composition of brain voltage−gated potassium channels determined by hongotoxin−1, a novel peptide derived from Centruroides limbatus venom. J. Biol. Chem. 1998, 273, 2639−2644.
Peter et al, Effect of toxins Pi2 and Pi3 on human T Lymphocyte kv1.3 channels: the role of Glu7 and Lys24. J. Membr. Biol. 2001, 179, 13−25
Mouhat et al, K+ channel types targeted by synthetic OSK1, a toxin from Orthochirus scrobiculosus scorpion venom Biochem. J. 2005, 385, 95−104
Pennington et al, Identification of there separate binding sites on Shk toxin, a potent inhibitor of voltage dependent potassium channels in human T−lymphocytes and rat brain. Biochem. Biophys. Res. Commun. 1996, 219, 696−701
Pennington et al, ShK−Dap22, a potent Kv1.3−specific immunosuppressive polypeptide. J. Biol. Chem. 1998, 273, 32697−35707
Nguyen A et al., “Novel Nonpeptide Agents Potently Block the C−Type Inactivated Conformation of Kv1.3 and Suppress T Cell Activation”, Mol. Pharmacol., 50, 1672−1679, 1996.
Hanson DC et al., “UK−78,282, a Novel Piperidine Compound That Potently Blocks the Kv1.3 Voltage−Gated Potassium Channel and Inhibits Human T Cell Activation”, Br. J. Pharmacol., 126, 1707−1716, 1999.
Felix JP et al., “Identification and Biochemical Characterization of a Novel Norterpene Inhibitor of the Human Lymphocyte Voltage−Gated Potassium Channel, Kv1.3”, Biochemistry, 38(16), 4922−4930, 1999.
Baell JB et al., “Khellinone Derivatives as Blockers of he Voltage−Gated Potassium Channel Kv1.3: Synthesis and Immunosuppressive Activity” J. Med. Chem., 47, 2326−2336, 2004.
Wulff H et al., “Alkoxypsoralens, Novel Nonpeptide Blockers of Shaker−Type K+ Channels: Synthesis and Photoreactivity”, J. Med. Chem., 41, 4542−4549, 1998.
Vennekamp J, Wulff H, Beeton C, Calabresi PA, Grissmer S, Hansel W, and Chandy KG. Kv1.3−blocking 5−phenylalkoxypsoralens: a new class of immunomodulators.(2004) Mol. Pharmacol.65, 1364−74.
Wenrong et al., Design, synthesis and structure-Activity relationships of benzoxazinone−Based factor Xa inhibitors,Bioorg. Med. Chem. Lett.; EN; 13 3; 2003; 561−566
Xue et al., Crystal structure of the PXR-T1317 complex provides a scaffold to examine the potential for receptor antagonism, Bioorg. Med. Chem. Lett.; EN; 15; 5; 2007; 2156−2166
Triggle et al., Voltage−Gated Ion channels as drug targets, Methods and Principles in Medicinal Chemistry.; Vol. 29; 2006; 214−274
【技術分野】
【0001】
発明の分野
本発明は、カリウムチャネル阻害剤である式(I)の化合物に関する。この種の化合物は免疫修飾および、自己免疫、慢性炎症、代謝疾患などの治療のためのKv1.3阻害剤として有用でありうる。また、この種の化合物は不整脈の治療または予防のためのKv1.5阻害剤としても有用でありうる。上記化合物を含む薬剤組成物、並びに、自己免疫および炎症性疾患の治療や不整脈の治療におけるその用途もまた、提供される。
【背景技術】
【0002】
背景
イオンチャネルは、細胞膜の脂質二重層にまたがり、Na+、K+、Ca2+およびCl−などの特定のイオンが通過できる水溶性の通路を提供するタンパク質である(Herbert,1998)。カリウムチャネルは、イオンチャネルのうちで最大かつ最も多様なサブグループであり、膜電位の調節および細胞興奮性の制御において中心的な役割を担っている(Armstrong & Hille,1998)。カリウムチャネルはそのアミノ酸配列および生物物理学的特性に基づき、遺伝子ファミリー群に分類されている(命名法についてはGutman et al.,2003を参照)。
【0003】
カリウムチャネルを調節する化合物は、自己免疫疾患、炎症性疾患、心血管疾患、神経疾患、聴覚疾患、腎疾患および代謝介在疾患などの各種の疾患領域において複数の治療用途を有している(Shieh et al.,2000; Ford et al.,2002,Xie et al,2004,Cahalan et al,1997)。カリウムチャネルKv1.3は、ニューロン、血球、破骨細胞、マクロファージ、上皮、並びにTリンパ球およびBリンパ球などの多くの組織に見られる。さらに、Kv1.3を阻害することで、乾癬、関節リウマチ、多発性硬化症、肥満、糖尿病および炎症性腸疾患などの多くの自己免疫疾患に関与しているT細胞の機能が調節されることが明らかになっている(Beeton et al.,2006)。
【0004】
自己免疫疾患のためのKv1.3チャネルブロッカー
乾癬、関節リウマチ、多発性硬化症、IBDなどの種々の自己免疫疾患の発症における自己反応性後期メモリーT細胞の役割は十分に確立されている。TEM細胞の活性化によってKv1.3チャネルの発現が相当程度アップレギュレートされ、その結果、Kv1.3が細胞からのカリウム流出の主要な経路となる。よって、Kv1.3を選択的にブロックすると細胞膜の脱分極およびCa2+流入が引き起こされ、サイトカイン産生並びに細胞増殖および細胞機能の阻害がもたらされる。このように、Kv1.3は自己免疫疾患の制御のための非常に興味深い新規な治療標的である。
【0005】
T細胞および自己免疫
T細胞は、細胞介在性免疫において中心的な役割を担っているリンパ球である。T細胞の主要な形態の一つはヘルパーT細胞(TH)であり、このTHはCD4+細胞としても知られ、自己免疫疾患の進行に重要な役割を果たしている。サイトカインであるインターロイキン2(IL−2)の産生を介して、CD4+T細胞は、細胞傷害性T細胞(CD8+)として知られるT細胞の第2の主要なタイプを生み出すことができる。ナイーブ(不活性)なCD4+T細胞およびCD8+T細胞は両方のタンパク質(CCR7+CD45RA+)を発現し、リンパ節へ進入するための鍵としてケモカイン受容体CCR7を用いる。リンパ節内部において、ナイーブT細胞は抗原と接触し、活性化プロセスを通じて、サイトカイン類を産生し増殖する「エフェクター」T細胞へと変化する。次の免疫応答が減弱すると、ほとんどのナイーブエフェクターは死滅するが、いくつかは長寿命のセントラルメモリー細胞(TCM)へと分化する。TCM細胞はナイーブ細胞と同様にリンパ節へ向かうのにCCR7を用い、そこで自身の同種抗原と遭遇する。抗原刺激によってTCM細胞は、サイトカイン類を産生し増殖する「TCMエフェクター」へと変化する。TCMエフェクターもまたナイーブエフェクターと同じ運命を辿り、その大多数は免疫応答が弱まった後に死滅し、さらなる抗原との接触のために長寿命の生存細胞をいくらか残すこととなる。抗原と繰り返し接触すると(自己免疫疾患または慢性感染で起こりうる)、TCM細胞は、短寿命の、CCR7およびCD45RAを発現していない「エフェクターメモリーT細胞」(TEM)へと分化し、抗原誘導活性化のためにリンパ節へ向かう必要がなくなる。CD8+TEM細胞の一部はCD45RAを再獲得してCCR7−CD45RA+TEMRA細胞となる。活性化によって、CD4+およびCD8+の双方のTEM細胞はTEMエフェクターへと変化し、これが炎症部位へと迅速に移動して大量の炎症性サイトカイン類、インターフェロン−γ(IFN−γ)および腫瘍壊死因子α(TNFα)を産生する。また、CD8+TEMエフェクターは大量のパーフォリンを有しており、よって非常に破壊的である(Wulff et al,2003,Beeton et al,2005)。
【0006】
T細胞および自己免疫疾患におけるKv1.3の機能的役割
ヒトT細胞は二つのK+チャネル(Kv1.3およびIKCa1)を発現しており、これによって遺伝子転写、増殖およびサイトカイン分泌に必要とされる細胞質Ca2+レベルの持続的な上昇に必要なバランスのとれたカチオンの流出がもたらされる(Panyi et al,2004,Chandy et al,2004)。このKv1.3チャネルおよびIKCa1(KCa3.1としても知られている)チャネルは膜電位を調節しており、Tリンパ球におけるCa2+シグナル伝達を促進する。Kv1.3は膜の脱分極に応答して開き、静止膜電位を維持する(初期段階)。これに対し、IKCa1は細胞質Ca2+の増加に応答して開き、膜電位を過分極させる(Beeton et al,2001)。K+チャネルを選択的に封鎖すると膜の脱分極が起こり、これによってCa2+の流入が阻害されてサイトカインの産生および細胞増殖が停止する。チャネルブロッカー毒素を用いた初期のインビトロでの研究によってKv1.3チャネルがT細胞活性化後のサイトカインIL−2の合成(遺伝子の活性化)および分泌に不可欠であることが明らかに示され(Price et al,1989)、免疫不全における当該チャネルの阻害剤の潜在的な治療上の利用に理論的根拠が与えられている。自己免疫疾患の病態における自己反応性T細胞の役割は、動物モデルで明らかに示されている。他のいくつかの自己免疫疾患において疾患特異的な自己反応性T細胞がメモリー表現型を示すことも報告されている。自己反応性TEM細胞も乾癬、関節リウマチ、多発性硬化症、IBD、白斑、ブドウ膜炎、天疱瘡、炎症性筋疾患、橋本病および強皮症に関与しているとされている(Beeton et al、2005)。「後期の」メモリーT細胞およびメモリーB細胞は、多くの自己免疫疾患、移植拒絶反応および慢性の移植片対宿主病において疾患の進行および組織の損傷に関与しているとされている。Kv1.3チャネルの調節物質は、正常な免疫応答に悪影響を及ぼすことなく疾患誘導性のエフェクターメモリーT細胞およびメモリーB細胞の選択的なターゲティングを可能とすることができ、その結果、より一般的な免疫抑制を引き起こす物質よりも好ましい副作用プロファイルを有するものと考えられる。
【0007】
Koo et al,1999によれば、Kv1.3ブロッカーであるマルガトキシン(MgTX)がインビボでの遅延型過敏症(DTH)の応答を効果的に抑制することが観察された。また、MgTXは感作されていない動物での初期の抗体応答を阻害する(二次的な抗体応答はMgTXの影響を受けない)ことも示されている。これらの最近の結果は、休止Tリンパ球ではKv1.3チャネルが支配的でその機能を調節しているのに対し、IKCa1チャネルは活性化前のTリンパ球においてより重要であるとの考え方にも合致している。コレオリド(Correolide)(Koo et al,1999)およびPAP−1(Schmitz et al,2005)はKv1.3チャネルをブロックする新規な免疫抑制剤であり、DTHモデルにおいても有効である。DTH応答に関与する細胞構成成分は自己免疫疾患および同種移植片拒絶反応においてみられるものと類似していることから、上記の結果は新規な免疫抑制剤としてのKv1.3チャネルブロッカーの開発に非常に有望である。
【0008】
「薬剤ターゲットとしての電位依存性イオンチャネル(Voltage Gated Ion Channels as Drug Targets)」においてTriggleらにより記載されているように、1980年代の初めに多くの化合物がμM〜mMの濃度でKv1.3チャネルをブロックすることが報告された。これらの化合物としては、4−アミノピリジンおよびテトラメチルアンモニウムなどの古典的なKvチャネル阻害剤、並びに、カルシウム活性化カリウムチャネルブロッカーであるキニンおよびセテイジル(ceteidil)、フェノチアジン抗精神病薬であるクロルプロマジンおよびトリフルオロペラジン、古典的なカルシウムチャネル阻害剤であるベラパミル、ジルチアゼム、ニフェジピンおよびニトレンジピン、並びにβブロッカーであるプロプラノロールなどの他の非特異的な化合物が挙げられる。
【0009】
1980年代にはまた、サソリ、ヘビおよび他の海洋生物から抽出された天然産物がKv1.3チャネルの強力な阻害剤であることが見出されたが、これらは主に、複数のスルフィド結合によって安定化された短ペプチド(<70残基)であった。これらの強力な阻害剤のうち最初のものはサソリ(Leiurus quinquestriatus hebraeus)の毒から単離され、カリブドトキシン(ChTX)と名付けられた(Sands et al, 1989)が、他のサソリ毒のスクリーニングによってより強力なKv1.3阻害毒が同定され、これらの毒としてはマルガトキシン(MgTX)(Garcia et al, 1993)、アジトキシン−2(Garcia et al, 1994)、ホンゴトキシン(Koshchak et al, 1998)、ダイオウサソリ毒2(pandinus imperator toxin 2)(Pi2)(Peter et al, 2001)およびオーソキラス スクロビキュローサス(Orthochirus scrobiculosus)(OSK1)(Mouhat et al, 2005)などが挙げられる。OSK1(最も近縁の関連チャネルに対して300倍選択的である)を除き、サソリ毒はいずれもKv1.3に対して選択的ではない。
【0010】
1980年代にはまた、サソリ、ヘビおよび他の海洋生物から抽出された天然産物がKv1.3チャネルの強力な阻害剤であることが見出されたが、これらは主に、複数のスルフィド結合によって安定化された短ペプチド(<70残基)であった。これらの強力な阻害剤のうち最初のものはサソリ(Leiurus quinquestriatus hebraeus)の毒から単離され、カリブドトキシン(ChTX)と名付けられた(Sands et al,1989)が、他のサソリ毒のスクリーニングによってより強力なKv1.3阻害毒が同定され、これらの毒としてはマルガトキシン(MgTX)(Garcia et al,1993)、アジトキシン−2(Garcia et al,1994)、ホンゴトキシン(Koshchak et al,1998)、ダイオウサソリ毒2(pandinus imperator toxin 2)(Pi2)(Peter et al,2001)およびオーソキラス スクロビキュローサス(Orthochirus scrobiculosus)(OSK1)(Mouhat et al,2005)などが挙げられる。OSK1(最も近縁の関連チャネルに対して300倍選択的である)を除き、サソリ毒はいずれもKv1.3に対して選択的ではない。
【0011】
これまでで最も強力で選択的なKv1.3ブロッカーの一つは、イソギンチャクから抽出された、スティコダクチラ ヘリアンサス(stichodactyla helianthus)毒(Shk)である(Pennington et al,1996)が、これに関してはKv1.3の封鎖を介した自己免疫疾患の治療について報告されている(US 6,077,680)。Shkおよび、選択性プロファイルが改善されたその合成誘導体であるShk−Dap22はpMで活性を示す(Pennington et al,1998)が、これらのペプチドはさらなる開発に対して好ましくない特性を有していることが判明した。
【0012】
近年ではより新規で選択的な小分子であるKv1.3チャネルブロッカーが自己免疫疾患の管理のために報告されている。これらの分子としては、イミノジヒドロキノリン類であるWIN173173およびCP339818(Nguyen et al.,1996)、ベンズヒドリルピペリジンであるUK−78,282(Hanson et al.1999)、コレオリド(Felix et al.,1999)、シクロヘキシル置換ベンズアミドであるPAC(US−06194458、WO0025774)、スルファミドベンズアミドインダン(US−06083986)、ケリノン(Baell et al.,2004)、ジクロロプレニルピラゾロピリミジン(WO−00140231)およびソラレン類(Wulff et al.,1998.,Vennekamp et al.,2004,Schmitz et al.,2005)が挙げられる。
【0013】
スルホンアミド類が、特に11−β−ヒドロキシステロイドデヒドロゲナーゼ タイプ1、CCR5、H3受容体および有糸分裂キネシン類の阻害剤として有用であることが報告されている。
【0014】
1,4−置換アリール第3級スルホンアミド類(4位がアミドで置換されたもの)が、2型糖尿病などの疾患における高血糖の治療および予防のための11−β−ヒドロキシステロイドデヒドロゲナーゼ タイプ1の阻害剤として特許請求されている(WO2004065351)。
【0015】
1,4−置換アリール第3級スルホンアミド類(4位が置換アルキル、アルコキシアミノ、スルホニル、アシル、アルコキシ、カルボニルまたはアミノカルボニルで置換されていてもよいもの)が、有効な抗癌剤としての有糸分裂キネシン類の阻害剤として特許請求されている(WO2007056078)。
【0016】
1,4−置換アリール第3級スルホンアミド類(スルホンアミドのNが低級アルキル、低級アルケニル、シクロアルキルまたはシクロアルキルおよび4位がカルボニル、アルキルまたは第2級アルコールで置換されていてもよいもの)が、クラスIII抗不整脈剤として特許請求されている(US4876262)。
【0017】
1,4−置換アリール第3級スルホンアミド類(4位がアルキル、カルボニル、またはスルフィニル基で置換されていてもよいもの)が、HIV感染症および他のCCR5介在疾患の治療のためのCCR5の阻害剤として特許請求されている(WO2000454974)。
【0018】
1,4−置換アリール第3級スルホンアミド類が、除草剤として特許請求されている(WO200690792)。
【0019】
1,4−アリール第3級メチルスルホンアミド類(4位が環状アミドで置換され、当該スルホンアミドのNがメチルナフタレンに結合しているもの)が、Xa因子の強力な阻害剤であり、強力な抗血栓作用効果を示すことが報告されている(Wenrong et al,2003)。
【0020】
1,4−置換アリール第3級フェニルスルホンアミド類(4位が第2級アルコールで置換されているもの)が、ヒトプレグナンレセプター(PXR)を阻害し、代謝調節の調節と健康を害する可能性がある化合物の分泌において重要な役割を果たすことが報告されている(Xue et al,2007)。
【発明を実施するための形態】
【0021】
この度、驚くべきことに、後述する一般式(I)の化合物がカリウムチャネルの阻害剤として機能することが見出された。これらの化合物は、カリウムチャネルKv1.3を阻害し、カリウムチャネルKv1.3の阻害に関連した疾患を治療するのに特に有用である。本発明はKv1.3介在性の疾患の治療に限られず、上記化合物はカリウムチャネルの阻害を伴う疾患治療にも有用である(Triggle et al,2006)。すなわち、第一形態において、本発明は式(I)の化合物もしくはその塩またはこれらの製薬上許容されうる誘導体を提供する:
【0022】
【化1】

【0023】
式中、
R1は置換されていてもよいアリールアルキル、置換されていてもよいアリール、置換されていてもよいヘテロアリールアルキルおよび置換されていてもよいヘテロアリールからなる群から選択され;
R2は置換されていてもよいアシル、置換されていてもよいスルホニルおよび置換されていてもよいスルファモイルからなる群から選択され;
R3は水素、ハロゲン、ヒドロキシル、アルコキシ、アリールオキシ、置換されていてもよいアルキル、置換されていてもよいアミノ、置換されていてもよいアミノカルボニル、置換されていてもよいアミノスルホニルまたはニトリルからなる群から選択され;
X1は化学結合、CR7R8、C(=O)、C(=NH)、NR9、NHC(=O)、およびSO2からなる群から選択され;
R7およびR8は、それぞれ独立して、水素、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールから選択され;または、
R7およびR8は、置換されていてもよいC4−C6のシクロアルキル環を共に形成し;
R9は水素、置換されていてもよいアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールからなる群から選択され;
Aは置換されていてもよい飽和したまたは部分的に飽和した一般式
【0024】
【化2】

【0025】
で表される4−7員環、または
【0026】
【化3】

【0027】
から選択され:
それぞれにおいて;
X2はCHまたはNであり;
X3はC(R5)2、N(R5b)、OまたはSであり;
X4は、それぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
n=1または2である。
【0028】
本明細書で用いる場合、特記しない限り、以下の定義が適用されるものとする。
【0029】
「置換されていてもよい」との語は、ある基が、同一であってもよいし異なってもよい1または2以上の置換基によって置換されていてもよいことを意味する。そうでないと特記しない限り、これらの置換基は、アルキル、シクロアルキル、−O−C(ハロゲン)3(好ましくは、−OCF3)、ビアリール、炭素環アリール、ヘテロ脂環、ヘテロアリール、アシル、アミジノ、アミド、アミノ、アルコキシアミノ、カルバモイル、カルボキシ、シアノ、エーテル、ヒドロキシル、イミノ、ハロゲン、ニトロ、スルファモイル、スルホニル、スルフィニル、スルフェニル、スルホンアミドまたはウレアから選択される。
【0030】
本明細書で用いられる場合、「アルキル基」との語は、通常、C1−4のアルキル基またはアルキル部分(例えば、メチル、エチル、n−プロピル、i−プロピル、ブチル、i−ブチルおよびt−ブチル)などの、直鎖または分枝鎖のアルキル基または1〜6個の炭素原子(好ましくは、2、3、4または5個の炭素原子)を含有する部分である。アルキル基またはアルキル部分は、非置換であってもよいし、任意の位置で置換されていてもよい。通常、アルキル基またはアルキル部分は、非置換であるか、または1、2もしくは3個の置換基を有している。適当な置換基としては、シアノ、ハロゲン、ヒドロキシル、アルキルアミノ、ジアルキルアミノ、アミド、アルキルアミド、ジアルキルアミド、アルカノイル、アルコキシ、スルホンアミド、ニトロ、アリールおよびヘテロアリールが挙げられる。アルキル部分はまた、「不飽和アルキル」部分であってもよく、これはアルキル部分が少なくとも一つのアルケンまたはアルキン部分を含有することを意味する。「アルケン」部分とは、少なくとも二つの炭素原子および少なくとも一つの炭素−炭素二重結合からなる基を意味する。「アルキン」部分とは、少なくとも二つの炭素原子および少なくとも一つの炭素−炭素三重結合からなる基を意味する。
【0031】
本明細書で用いられる場合、「シクロアルキル」との語は、3〜11個の炭素原子(すなわち、3、4、5、6、7、8、9、10または11個の炭素原子)からなる単環または二環の環または環系を意味する。当該環系は「飽和環」であってもよく、これはその環がアルケンまたはアルキン部分を含有しないことを意味する。シクロアルキル基はまた、「不飽和環」であってもよく、これは当該環系が少なくとも一つのアルケンまたはアルキン部分を含有し、かつ、当該環系が芳香族ではないことを意味する。上記シクロアルキル基は、本明細書に記載するように、置換または非置換でありうる。上述した置換基に加えて、1または2以上の環炭素原子はまた、二重結合を介してNH、SおよびOから選択される基に結合してもよい。上記シクロアルキルの置換基は、追加の置換基がアルキルである場合を除き、C1−6アルキル基などの連結基を介して結合してもよい。連結基中のアルキル基の1または2以上の水素は、ヒドロキシ、ハロゲン、シアノ、アミノ、チオール、C1−6アルコキシ、C1−6アルキルチオ、C1−6アルキルアミノおよびC1−6ジアルキルアミノからなる群から選択される部分により置換されうる。
【0032】
本明細書で用いられる場合、「アリール基」との語は通常、フェニルまたはナフチルなどのC6−10アリール基である。好ましいアリール基は、フェニルである。アリール基は、非置換であるか、または任意の位置で置換されうる。通常、アリール基は、1、2、3または4つの置換基を有する。適当な置換基としては、シアノ、ハロゲン、ヒドロキシル、ニトロ、トリフルオロメチル、アルキル、アルキルチオ、アルコキシ、アミノ、アルキルアミノ、ジアルキルアミノ、アルカノイル、アミド、N−アルキルアミド、NN−ジアルキルアミノ、スルホンアミド、アリールおよびヘテロアリールが挙げられる。
【0033】
「炭素環」との語は、1または2以上の共有結合で閉じた環構造を含有し、かつ、当該環の骨格を形成する原子がすべて炭素原子である化合物を意味する。よってこの語により、炭素環はヘテロ環と区別される。炭素環基には、非芳香族の炭素環である「シクロアルキル基」と、芳香族の炭素環である「炭素環アリール」基との双方が含まれる。当該炭素環基は、本明細書に記載するように、置換されていてもよい。
【0034】
本明細書で用いられる場合、「ヘテロ環」または「ヘテロシクロ」との語は、N、SおよびOから選択される1または2以上のヘテロ原子を含む、単環または二環の環または環系を意味する。当該環または環系は、ヘテロ原子に加えて、1〜6個の炭素原子(すなわち、1、2、3、4、5または6個の炭素原子)を含む。ヘテロ環基との語は、非芳香族のヘテロ環を意味する「ヘテロ脂環」基と、芳香族のヘテロ環を意味する「ヘテロアリール」基との双方を含む。当該ヘテロ環部分は、非置換であってもよいし、本明細書に記載するように置換されたものであってもよく、置換基は、互いに隣接するように位置するときには結合してシクロアルキルまたはヘテロ脂環式の環系(例えば、メチレンジオキシまたはジフルオロメチレンジオキシ)を形成してもよい。上記ヘテロ環の置換基は、炭素原子またはヘテロ原子を介して結合しうる。上記ヘテロ環基はまた、窒素または硫黄が環中に存在する場合には、窒素および硫黄の酸化物をも含みうる。
【0035】
本明細書で用いられる場合、「ヘテロアリール」との語は、N、SおよびOから選択される1または2以上のヘテロ原子を含む、単環または二環の環または環系を意味する。当該環または環系は、ヘテロ原子に加えて、3〜13個の炭素原子(すなわち、3、4、5、6、7、8、9、10、11、12または13個の炭素原子)を含み、かつ、ヘテロ原子を含む少なくとも一つの芳香環を含有する。当該ヘテロアリール基はまた、窒素もしくは硫黄が存在する場合には、窒素および硫黄の酸化物、またはオキソ基をそれぞれ含みうる。単環のヘテロアリール基の例としては、以下に限定されないが、フリル、チエニル、ピロリル、オキサゾリル、チアゾリル、イソキサゾリル、イソチアゾリル、ピラゾリル、イミダゾリル、トリアゾリル、テトラゾリル、オキサジアゾリル、チアジアゾリル、ピリジル、ピリミジル、ピリダジニル、ピラジニル、およびトリアジニルが挙げられる。二環のヘテロ環の例としては、以下に限定されないが、インドリル、ベンゾフラニル、ベンゾチエニル、ベンズオキサゾリル、ベンゾチアゾリル、ベンズイソキサゾリル、ベンズイソチアゾリル、インダゾリル、イソキノリニル、キノリニル、キノキサリニル、シンノリニル、フタラジニル、キナゾリニル、ベンゾトリアゾニルなどが挙げられる。三環のヘテロ環の例としては、以下に限定されないが、チアントレニル、キサンテニル、フェノキサチイニル、カルバゾリル、カルボリニル、フェナントリジニル、アクリジニル、ペリミジニル、フェナントロリニル、フェナジニル、フェノチアジニル、およびフェノキサジニルが挙げられる。当該ヘテロアリール基は、非置換であってもよいし、本明細書に記載するように置換されていてもよい。置換基は、互いに隣接するように位置するときには結合してシクロアルキルまたはヘテロ脂環式の環(例えば、メチレンジオキシおよびジフルオロメチレンジオキシ)を形成してもよい。上記ヘテロアリールの置換基は、炭素原子またはヘテロ原子を介して結合しうる。
【0036】
本明細書で用いられる場合、「アリールアルキル」との語は、アリール−C1−6アルキルまたはC1−6アルキル−アリールの式の化学部分を意味し、これらの語は本明細書で定義されている。
【0037】
本明細書で用いられる場合、「ヘテロアリールアルキル」との語は、ヘテロアリール−C1−6アルキルまたはC1−6アルキル−ヘテロアリールの式の化学部分を意味し、これらの語は本明細書で定義されている。
【0038】
本明細書で用いられる場合、「アシル」との語は、(CH2)yC(=O)Rz(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式の化学部分を意味する。
【0039】
「アミジノ」との語は、(CH2)yC(=NH)NRzR’z(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式を有する化学部分を意味する。
【0040】
「アミド」との語は、−C(=O)NRzR’zの式を有する化学部分を意味する「C−アミド」基と、−NRzC(=O)R’zの式を有する化学部分を意味する「N−アミド」基との双方を意味する。
【0041】
「アミン」または「アミノ」との語は、−NRzR’zの式を有する化学部分を意味する。アミンの定義にはまた、それらのN−酸化物を含むものと理解される。
【0042】
「シアノ」基は−CNの式の化学部分を意味する。
【0043】
本明細書で用いられる場合、「ヒドロキシ」または「ヒドロキシル」との語は、−OHの式の化学部分を意味する。
【0044】
「ハロゲン」または「ハロ」との語は、フッ素、塩素、臭素およびヨウ素からなる基から選択される原子を意味する。
【0045】
本明細書で用いられる場合、「アルカノイル」との語は、−C(=O)Rzの式の化学部分を意味する。
【0046】
「スルホン」または「スルホニル」との語は、−S(=O)2Rzの式を有する化学部分を意味する。
【0047】
「スルフィニル」との語は、−S(=O)Rzの式を有する化学部分を意味する。
【0048】
「スルフェニル」との語は、−SRzの式を有する化学部分を意味する。
【0049】
「スルファモイル」基は、−N−S(=O)2NRzR’zの式を有する化学部分を意味する。
【0050】
「スルホンアミド」との語は、−S(=O)2NRzR’zの式を有する化学部分を意味する「S−スルホアミド」基と、−N−S(=O)2R’zの式を有する化学部分を意味する「N−スルホアミド」基との双方を意味する。
【0051】
「チオカルボニル」との語は、(CH2)yC(=S)Rz(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式を有する化学部分を意味する。
【0052】
本明細書で用いられる場合、「チオ」または「チオール」との語は、−SHの式の化学部分を意味する。
【0053】
「チオアミド」との語は、(CH2)yC(=S)NRzR’zの式を有する化学部分を意味する「C−チオアミド」基と、(CH2)yNRzC(=S)R’z(ここで、yは1〜6(すなわち、1、2、3、4、5または6)である)の式を有する化学部分を意味する「N−チオアミド」基との双方を意味する。
【0054】
「ウレア」基は、−NRzC(=O)NRzR’zの式を有する化学部分を意味する。
【0055】
RzおよびR’zは、それぞれ独立して、水素、C1−6アルキル、シクロアルキル、C1−6アルコキシ、アリール−C1−6アルキル、アリールおよびヘテロアリールからなる群から選択される。
【0056】
好ましい一実施形態は、Aが
【0057】
【化4】

【0058】
から選択される化合物に関し;式中、
n=1または2であり;
X3はC(R5)2、N(R5b)、またはOであり;
X4は、それぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、ヒドロキシル、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。
【0059】
好ましくは、R2はC(=O)R10、SO2R10からなる群から選択され;式中、
R10は、NR11R12、置換されていてもよいアリール、および置換されていてもよいヘテロアリールから選択される。さらに好ましくは、R10は、NR11R12、式(II)、(III)、(IV)または(V)から選択される;
【0060】
【化5】

【0061】
式中、
R11およびR12は同じであるかまたは異なり、それぞれ水素、置換されていてもよいアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
G、J、L、D、およびEは同じであるかまたは異なり、それぞれCまたはNであり(G、J、L、D、またはEの少なくとも一つがNである);
R10が式(II)であるときは、LはOまたはSであってもよく、および
R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるいは置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環の環であり;
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであるか、あるいは、R15およびR16の対、またはR16およびR17の対、またはR17およびR18の対、またはR18およびR19の対が置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環の環を共に形成してもよく;
R1は置換されていてもよいアリールアルキル、および置換されていてもよいヘテロアリールアルキルから選択される。より好ましくは、R1は式(VI)から選択され;
【0062】
【化6】

【0063】
式中、
R20、R21、R22、R23およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルまたは置換されていてもよいアルコキシであり;
R25およびR26は同じであるかまたは異なり、それぞれ水素、ヒドロキシル、および置換されていてもよいC1−3アルキルである。
【0064】
R3は、水素、ハロゲン、ヒドロキシル、ニトリル、または置換されていてもよいアルキル、好ましくは水素、ハロゲンまたは置換されていてもよいアルキルからなる群から選択される。
【0065】
X1は、好ましくは化学結合、CH2、およびC(=O)からなる群から選択される。
本発明の最も好ましい化合物は式(VII)のものである:
【0066】
【化7】

【0067】
式中、
n=1または2であり;
X1は化学結合、CH2、またはC(=O)からなる群から選択され;
X3はC(R5)2、N(R5b)、またはOであり;
X4はC(=O)、またはC(R4)2であり;
R3は水素、ハロゲン、ヒドロキシルまたは置換されていてもよいC1−3アルキルからなる群から選択され;
R4は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアリールオキシ、置換されていてもよいC1−3アルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。好ましくはR4はそれぞれ独立してフルオロ、置換されていてもよいメチル、ヒドロキシ、トリフルオロメチル、置換されていてもよいフェニル、置換されていてもよいフェノキシ、置換されていてもよいベンジルオキシまたは置換されていてもよいオキサジアゾールである。
【0068】
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。好ましくは、R5は、それぞれ独立して、フルオロ、メチル、トリフルオロメチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、tert−ブチル、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、シクロヘキシルメチル、置換されていてもよいフェニル、置換されていてもよいベンジル、置換されていてもよいフェネチル、ヒドロキシル、置換されていてもよいヒドロキシエチル、ヒドロキシプロピル、ヒドロキシブチル、置換されていてもよいフェノキシ、置換されていてもよいベンジルオキシ、メトキシエチル、メトキシプロピル、フェノキシエチル、ベンジルオキシエチル、アセチル、プロピオニル、置換されていてもよいベンゾイル、フェナシル、イミダゾイル、ピラゾイル、ピリジノイル、オキサジアゾロイル、チアゾロイル、アセタミド、メチルアセタミド、ジメチルアセタミド、エチルアセタミド、ジエチルアセタミド、tert−ブチルアセタミド、ピリジルアセタミド、シクロプロピルアセタミド、シクロブチルアセタミド、シクロペンチルアセタミド、またはシクロヘキシルアセタミドである。より好ましくは、R5は、それぞれ独立して、フルオロ、置換されていてもよいメチル、ヒドロキシ、置換されていてもよいシクロヘキシル、置換されていてもよいフェニル、置換されていてもよいベンジル、置換されていてもよいフェノキシ、置換されていてもよいベンジルオキシ、またはチアゾロイルである。
【0069】
R5bは、水素、置換されていてもよいC1−3アルキル、置換されていてもよいフェニルおよび置換されていてもよいヘテロアリールである。
【0070】
R10はNR11R12または式(II)、(III)、(IV)もしくは(V)の化合物から選択され;
【0071】
【化8】

【0072】
式中、
R11およびR12は同じであるかまたは異なり、それぞれ置換されていてもよいC1−3アルキルである。好ましくは、R11およびR12は、アルキル(好ましくは、CH3)であり;G、J、L、D、およびEは同じであるかまたは異なり、それぞれC、またはNであり(G、J、L、D、またはEの少なくとも一つはNであり);
前記R10が式(II)であるときは、LはOまたはSであってもよく、および
前記R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるいは置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよい。好ましくは、R13およびR14はアルキル(好ましくは、CH3)である。
【0073】
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであるか、あるいは、R15およびR16の対、もしくはR16およびR17の対、もしくはR17およびR18の対、もしくはR18およびR19の対が、置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成しうる。
【0074】
好ましくは、R10は、置換されたイミダゾール、置換されたピラゾール、置換されたピロール、置換された置換されたオキサゾール、置換されたオキサジアゾール、置換されたチアゾール、置換されたチアジアゾール、置換されたピリジン、置換されたピリミジン、置換されたピラジン、置換されたピリダジン、置換されたトリアジン、置換されていてもよいフェニル、テトラヒドロベンゾフラン、ベンゾピラン、ジヒドロベンゾジオキシン、ベンゾキサジノン、ベンゾオキサジアゾール、ベンゾジオキソール、インドリン、インドール、インダゾール、またはベンゾモルフォリンである。最も好ましくは、R10は、置換されたイミダゾール、置換されたピラゾール、置換されたピリジン、フェニル、フルオロフェニル、シアノフェニル、テトラヒドロベンゾフラン、ベンゾピラン、ジヒドロベンゾジオキシン、ベンゾキサジノン、ベンゾオキサジアゾール、ベンゾジオキソール、インドリン、またはベンゾモルフォリンである;
R20、R21、R22、R23、およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルもしくは置換されていてもよいアルコキシである。好ましくは、R20、R21、R22、R23、およびR24は、それぞれ独立して、水素、フルオロ、クロロ、メチルから選択される。
【0075】
特に好ましい本発明の化合物は:
N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(3−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
ナフタレン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−3,4−ジメトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
2,3−ジヒドロ−ベンゾ[1,4]ジオキシン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−4−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
チオフェン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
チオフェン−3−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−4−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−2−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−4−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−2−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−2−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−メトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3,5−ジクロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−3−クロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(3−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(3−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(4−トリフルオロメチル−ベンジル)−ベンゼンスルホンアミド;
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(3−トリフルオロメトキシ−ベンジル)−ベンゼンスルホンアミド;
N−(2−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
2,2−ジメチル−クロマン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−4−ニトロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
フラン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−N−[3−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[3−メトキシ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(3,4−ジヒドロ−1H−イソキノリン−2−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(2,6−ジメチル−モルフォリン−4−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−4−エチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−ベンジル−N−[4−(4−ベンジル−4−ヒドロキシ−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(2,3−ジメトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド;
N−(4−クロロ−ベンジル)−N−{4−[3−(4−メトキシ−フェニル)−ピペリジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−フルオロ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−メトキシ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド;
1,3−ジメチル−1H−ピラゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2,3−ジメチル−3H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2,4−ジメチル−チアゾール−5−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド;
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−3−フルオロフェニル]−ジメチルスルファミド;
N−(4−フルオロ)ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド;
4−{4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−ベンゾイル}−2−フェニル−ピペラジン−1−カルボン酸tert−ブチルエステル;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(4−フルオロ−フェニル)−ピロリジン−1−カルボニル]−フェニル}−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
N−ベンジル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−ジメチルスルファミド;
N−ベンジル−N−{4−[3−(3−イソプロピル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−ジメチルスルファミド;
N−ベンジル−N−[4−(3−ベンジロキシ−ピロリジン−1−カルボニル)−フェニル]−ジメチルスルファミド;
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド;
N−ベンジル−N−[4−(4−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[4−(2−フルオロ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−シクロヘキシルメチル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−チアゾール−2−イル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−トリフルオロメチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4,4−ジフルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
ピリジン−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−フルオロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3,4−ジクロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−4−フルオロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(2−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド;
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3,3−ジフルオロ−ピロリジン−1−カルボニル)−フェニル]−アミド;
およびそれらの製薬上許容されうる塩を含む。
【0076】
本明細書で用いられる場合、製薬上許容されうる塩は製薬上許容されうる酸または塩基の塩である。製薬上許容されうる酸は塩酸、硫酸、リン酸、二リン酸、臭化水素酸、硝酸のような無機酸およびクエン酸、フマル酸、マレイン酸、リンゴ酸、アスコルビン酸、コハク酸、乳酸、安息香酸、酢酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸またはp−トルエンスルホン酸のような有機酸を含む。製薬上許容されうる塩基はアルカリ金属(例えば、ナトリウムまたはカリウム)およびアルカリ土塁金属(例えば、カルシウムまたはマグネシウム)水酸化物およびアルキルアミン類、アリールアルキルアミン類またはヘテロ環アミン類のような有機塩基を含む。
【0077】
本発明の化合物は一またはそれ以上の不斉中心を有していてもよい。誤解のないようにするため、本明細書において記載されている化学構造はラセミおよび非ラセミ混合物ならびに純粋なエナンチオマーおよび/またはジアステレオマーを含む、示されている化合物のすべての立体異性体を包含することを意味する。
【0078】
本明細書で述べられているように、本発明の化合物は様々な症状の治療に有用である。このように、第二形態において、本発明は、薬剤に用いるための本明細書に定義されている式(I)の化合物を提供する。好ましくは、前記化合物は乾癬、関節リウマチおよび多発性硬化症を含む免疫不全のような、カリウムチャネルの阻害に必要な症状を予防または治療するために使用される。
【0079】
更なる形態において、本発明は少なくとも一つの式Iまたは本明細書に定義されている化合物および任意に一またはそれ以上の賦形剤、担体または希釈剤を含む医薬製剤を提供する。
【0080】
本発明の組成物は、投与毎にそれぞれの活性成分を所定量で含む単位投与形態において与えられうる。そのような、単位は、前記化合物を5〜100mg/日、好ましくは5〜15mg/日、10〜30mg/日、25〜50mg/日、40〜80mg/日または60〜100mg/日のいずれかが採用されうる。式Iの化合物において、100〜1000mg/日、好ましくは100〜400mg/日、300〜600mg/日または500〜1000mg/日の範囲で投与される。そのような投与は一回または数回の別個に投与することもできる。最高の投与は、治療状況、投与経路、年齢、体重、患者の状況次第であり、医者の判断に基づく。
【0081】
本発明の組成物は、適当な経路、例えば、経口(口腔または舌下を含む)、直腸、経鼻、局所(口腔、舌下または経皮を含む)、膣内または非経口(皮下、筋肉内、静脈または皮内を含む)によって投与することが採用される。そのような形態は製薬分野で知られているいかなる方法を用いて調製されてもよく、例えば、前記活性成分と担体または賦形剤とを組み合わせて用いることができる。
【0082】
経口投与において用いられる医薬製剤は、カプセルもしくはタブレット;粉末もしくは顆粒;水中もしくは非水中の溶液もしくは懸濁液、食用泡もしくはホイップ、または水中油型エマルジョンもしくは油中水型エマルジョンのような別々のものであってよい。
【0083】
経疲投与において用いられる医薬製剤は、長時間、レシピエントの表皮に接触させたまま別々にパッチするようなものであってよい。例えば、Pharmaceutical Research,3(6),318(1986)に一般的に記載されているように、有効成分をパッチからイオントフォレシスによって投与してもよい。
【0084】
局所投与において用いられる医薬製剤は、軟膏、クリーム、サスペンション、ローション、パウダー、溶液、ペースト、ゲル、スプレー、エアロゾルまたはオイルとして形成されていてもよい。
【0085】
目または他の外部の細胞組織(例えば、口や皮膚)に応用するため、前記の製剤は、好ましくは局所軟膏またはクリームとして利用される。軟膏の場合は、有効成分は、パラフィンまたは水混和性の軟膏とともに用いられてもよい。また、有効成分は、水中油型クリーム型または油中水型のクリームで形成されてもよい。
【0086】
目に局所投与するために用いられる医薬製剤は、有効成分が適当な担体、特に水系溶媒に溶解しまたは懸濁している目薬を含む。
【0087】
口に局所投与するために用いられる医薬製剤は、キャンディー、トローチおよびうがい薬を含む。
【0088】
直腸投与するために用いられる医薬製剤は、坐薬またはかん腸剤のようなものであってもよい。
【0089】
経鼻投与するために用いられる医薬製剤は、担体が固体(例えば、20〜500ミクロンの粒径である粗粉末を含む)であるような場合においては、嗅ぎタバコの形態で投与される(すなわち、鼻の近くにある粉末容器から経鼻経路からすばやく吸入される)。前記担体が液体である場合においては、例えば、鼻腔用スプレーまたは点鼻薬として投与をするため、有効成分の水溶液または油溶液を含む。
【0090】
吸入投与するために用いられる医薬製剤は、様々な種の定量噴霧用の加圧エアロゾル、噴霧器または吸入器により作り出される微粒子またはミストを含む。
【0091】
膣内投与するために用いられる医薬製剤は、ペッサリー、タンポン、クリーム、ゲル、ペースト、フォームまたはスプレーの形態であってもよい。
【0092】
非経口投与するために用いられる医薬製剤は、抗酸化剤、緩衝液、静菌薬およびレシピエントの血液と等浸透圧である溶液を含みうる水溶性および非水溶性滅菌注射剤溶液;ならびに、懸濁剤と増粘剤を含みうる水溶性および非水溶性滅菌懸濁液を含む。当該形態は、例えば、密封アンプルやバイアルのような単位用量または複数用量の容器にあってもよく、および使用の直前に、例えば、注射液における水のような滅菌液体担体を添加する必要があるフリーズドライ(凍結乾燥された)状態で保存するものであってもよい。即席注射溶液および懸濁液は滅菌粉末、顆粒およびタブレットから調製してもよい。
【0093】
好ましい単位用量の形態は、本明細書において上述されているような有効成分を一日用量もしくはサブ用量を含むものまたは適当な分量を含むものである。
【0094】
特に上記されている成分に加えて、例えば、経口投与においては香味料を含んでいるのが好ましいように、探求の結果の形態種類である当業界における慣用される他の試薬を含んでもよい。
【0095】
本発明の組成物は、例えば免疫不全の治療におけるカリウムチャネルの阻害に必要である状態を治療するために使用されうる。このように、更なる態様において、本発明は、
(i)例えば、少なくとも一つの本発明の化合物もしくは本発明の薬剤組成物を有効量、患者に投与することを含む免疫不全のようなカリウムチャネル阻害を必要とする疾患を治療または予防する方法
および
(ii)カリウムチャネル阻害に用いるための薬剤の製造における本発明の化合物の使用:
を提供する。
【0096】
特に、前記薬剤は乾癬、関節リウマチ、多発性硬化症および他の免疫不全の治療または予防においてを使用するものである。
【0097】
第一態様の好ましい実施形態は、適宜変更してすべての他の態様に利用される。
【0098】
式(I)の化合物は、例えば、以下スキーム1〜5に示される、従来のルートにより調製されうる。
【0099】
【化9】

【0100】
X1がC=Oであり、X3、X4、R1、R3、R10およびnが上述されるように定義される式(I)の化合物は、X1がC=Oであり、AはOHならびにR1、R3およびR10は上述されるように定義される式(VIII)の化合物とX3とX4が上述されるように定義される式(IX)のアミンとから、スキーム1に示されるように調製されうる。通常、本反応は、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド(EDC)または2−(7−アザ−1H−ベンズトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート(HATU)のようなカップリング試薬を用いて、テトラヒドロフラン、アセトニトリルまたはジメチルホルムアミドのような溶媒中、室温から還流温度の範囲内で当業者に周知の常法により行われる。または、X3、X4、R1、R3、R10およびnが上述されるように定義される式(I)の化合物はAがClまたはBrである式(VIII)の化合物と式(IX)のアミンとから調製することもできる。通常、この反応は、例えば、トリエチルアミンのような塩基存在下、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒中、室温から還流温度の範囲内で当業者に公知の常法により調製することもできる。
【0101】
【化10】

【0102】
AはOHでありR1、R3およびR10は上述されるように定義される式(VIII)の化合物はスキーム2に示されるように、APがOH基をtert−ブチルエステルのような適当な保護をしたものであり、R1、R2、R3は上述されるように定義されるものであり、例えば、トリフルオロ酢酸のような適当な酸存在下で、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒を利用して、0℃から還流温度の範囲内で、当業者に周知の常法で脱保護して調製することができる。
【0103】
式(X)の化合物は、R3とR10は上述されるように定義されるスルホンアミド(XII)から、R1が上述されているものであり、YがClまたはBrである式R1−Yと求電子剤との反応を、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒中、室温から還流温度の範囲内で当業者に周知の常法により調製することもできる。または、R1とR3が上述されるように定義されるアミン(XI)から、例えば、ピリジン、トリエチルアミンまたは炭酸カリウムのような塩基存在下、テトラヒドロフラン、アセトニトリルまたはジクロロメタンのような溶媒中、室温から還流温度の範囲内で、式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとの反応を当業者に周知の常法により調製することもできる。
【0104】
式(XII)の化合物は既知化合物であり、またはR3が上述されるように定義される式(XIII)の化合物から、例えば、炭酸カリウム、トリエチルアミンまたはピリジンのような塩基存在下、ジクロロメタン、テトラヒドロフランおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとの反応を当業者に周知の常法により調製することもできる。
【0105】
式(XI)の化合物は既知化合物であり、または式(XIII)の化合物から、例えば、炭酸カリウム、トリエチルアミンまたはピリジンのような塩基存在下、ジクロロメタン、テトラヒドロフランおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがClまたはBrである式R1−Yの求電子剤を用いたアルキル化のような当業者に周知の常法により調製することもできる。または、式(XI)の化合物は式(XIII)の化合物から、例えば、トリアセト水素化ホウ素ナトリウムのような還元剤存在下、ジクロロメタン、テトラヒドロフランおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがCHOである式R1−Yのアルデヒドの還元的アミノ化を周知の常法により調製することもできる。式(XIII)は既知化合物であり、または当業者に周知の常法により調製することもできる。
【0106】
【化11】

【0107】
R2がSO2R10であり、X1、X3、R1、R3、R10およびnが上述されるように定義される式(I)の化合物は式(XVI)のアミンと式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとから、例えば、トリエチルアミン、ジイソプロピルアミンまたはピリジンのような塩基存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法によりスキーム3に示すように調製することもできる。または、式(I)の化合物は式(XIV)の化合物から、例えば、炭酸セシウムのような塩基存在下、テトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがClまたはBrである式R1−Yの求電子剤との反応を当業者に周知の常法により調製することもできる。
【0108】
X1がCH2であり、R2がSO2R10であり、X3、X4、R1、R3、R10およびnが上述されるように定義される式(I)の化合物は、X1がC=Oである式(I)の化合物から、例えば、水素化アルミニウムリチウムのような還元剤の存在下、テトラヒドロフランまたはジエチルエーテルのような適当な溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。
【0109】
X1、X3、X4、R1、R3およびnが上述されるように定義される式(XVI)の化合物は既知の化合物であり、または式(XV)のアミンから、例えば、炭酸カリウム、トリエチルアミンまたはピリジンのような塩基存在下、テトラヒドロフラン、ジクロロメタンおよびアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがClまたはBrである式R1−Yの求電子剤とのアルキル化のような当業者に周知の常法により調製することもできる。または、式(XVI)の化合物は式(XV)の化合物から、例えば、トリアセト水素化ホウ素ナトリウムのような還元剤存在下、テトラヒドロフラン、ジクロロメタンまたはアセトニトリルのような溶媒中、室温から還流温度の範囲内で、R1が上述されるものであり、YがCHOである式R1−Yのアルデヒドの還元的アミノ化を周知の常法により調製することもできる。
【0110】
X1、X3、X4、R3、R10およびnが上述されるように定義される式(XIV)の化合物は式(XV)のアミンと式R10−SO2Clであるスルホニルまたはスルファモイルクロライドとから、例えば、トリエチルアミン、ジイソプロピルアミンまたはピリジンのような塩基存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。
【0111】
【化12】

【0112】
X1がC=Oであり、X3、X4、R3およびnが上述されるように定義される式(XV)の化合物は、既知の化合物であり、X1がC=Oであり、AがOHであり、R3が上述されるように定義される式(XIX)の化合物から、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド(EDC)または2−(7−アザ−1H−ベンズトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート(HATU)のようなカップリング試薬と一緒に、例えば、テトラヒドロフラン、アセトニトリルまたはジメチルホルムアミドのような溶媒中、室温から還流温度の範囲内で当業者に周知の常法によりスキーム4に示されるように調製することもできる。
【0113】
X1がCH2であり、X3、X4、R3、およびnが上述されるように定義される式(XV)の化合物は、既知化合物であり、またはX1がCH2であり、AはClまたはBrのような脱離基である式(XIX)の化合物から調製でき、および式(IX)の化合物は、例えば、トリエチルアミン、ジイソプロピルアミンまたはピリジンのような塩基存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。
【0114】
X1がCH2であり、X3、X4、R1、R3、およびnが上述されるように定義される式(XV)の化合物は、X1がC=Oであり、AはHである式(XIX)の化合物から調製でき、および式(IX)の化合物は、例えば、トリアセト水素化ホウ素ナトリウムのような還元剤存在下、例えばテトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の範囲内で、当業者に周知の常法により調製することもできる。または、X1がCH2であり、X4がCH2であり、X3、R1、R3、およびnが上述されるように定義される式(XV)の化合物は、X1がC=Oである式(XV)の化合物から、例えば、水素化アルミニウムリチウムのような還元剤存在下、例えばテトラヒドロフランまたはジエチルエーテルのような溶媒中、室温から還流温度の範囲内で、還元のような当業者に周知の常法により調製することもできる。
【0115】
X1が化学結合、CH2またはC(=O)であり、X3、X4、R3、およびnが上述されるように定義される式(XV)の化合物は、既知化合物であり、またはX1が化学結合、CH2またはC(=O)である式(XVII)の化合物から、例えば、塩化スズ(II)のような還元剤とエタノールのような溶媒中、室温から還流温度の範囲内で、還元のような当業者に周知の常法により調製することもできる。
【0116】
X1がCH2またはC(=O)である式(XVII)の化合物は、AがClまたはBrのような脱離基であるニトロ化合物(XVIII)と式(IX)の化合物とからピリジン、トリエチルアミンまたは炭酸カリウムのような塩基を使用して、テトラヒドロフラン、アセトニトリル、ジクロロメタンまたはトルエンのような溶媒中、室温から還流温度の温度範囲内で、当業者に周知の常法により合成することができる。
【0117】
【化13】

【0118】
X1が化学結合であり、X3、X4、R3、およびnが上述されるように定義される式(XVII)の化合物は、既知化合物であり、または式(XX)の化合物と式(IX)の化合物とから、例えば、ジクロロメタン、アセトニトリル、テトラヒドロフラン、またはNN−ジメチルホルムアミドのような溶媒中、室温から還流温度の範囲内の温度で、当業者に周知の常法により、N−メチルモルフォリンのような塩基を使用して調製することもできる。または、X1が化学結合である式(XVII)の化合物は、例えば、ピリジンまたはトリエチルアミンのような塩基存在下、ジクロロメタン、アセトニトリル、テトラヒドロフランのような適当な溶媒中、YがClまたはBrである式(XXI)の求電子剤との反応のように当業者に周知の常法により調製することもできる。式(XX)、(XXII)および(XXI)の化合物は当業者に既知の方法により調製することができる。
【0119】
本発明の化合物はカリウムチャネル阻害剤(Kv)であることがわかっており、したがって、治療効果に有益である。そのような化合物は新規であり、本発明はまたこれらの化合物を提供する。以下に例示される実施例および、当業者に理解されるように、特別な試薬または条件はそれぞれの化合物に必要なように修正されうる。上述される反応において使用される多くの出発材料は市販のものから利用されまたは参考文献に引用される方法で製造されうる。
【実施例】
【0120】
HPLC分析を以下の方法によって行った:
溶媒:[MeCN−0.05% HCO2H:H2O−0.1%HCO2H],10−95%勾配 3min,95% 2.5min;カラム: Phenomenex Gemini 50x4.6mm i.d., C18逆相;流速 0.75mL/min(別途記載のない場合)
溶媒:[MeCN−0.05% HCO2H:H2O−0.01%HCO2H],5−95%勾配 5min,95% 3min;カラム:Phenomenex Gemini 50x4.6mm i.d.,C18逆相;流速 1.5mL/min(別途記載のない場合)。
【0121】
溶媒:[MeCN:H2O−0.1%HCO2H],5−95%勾配 3.5min,95% 2min;カラム:Phenomenex Gemini 50x3mm i.d.,C18逆相;流速 1mL/min(別途記載のない場合)。
【0122】
溶媒:[MeCN−0.05% HCO2H:H2O−0.1%HCO2H],5−95%勾配 6 min,95% 3min;カラム:Phenomenex Gemini 50x4.6mm i.d.,C18逆相;流速 1mL/min(別途記載のない場合)。
【0123】
分取用HPLCによる精製は以下のように行われた:
溶媒:[MeCN−0.05% HCO2H:H2O−0.1%HCO2H],5−95%勾配 12min,95% 3min;カラム:Waters X−Bridge 100x19 mm i.d.,C18逆相;流速 16mL/min(別途記載のない場合)。
【0124】
実施例1)N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(方法A)
i)(4−ニトロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
0℃で攪拌している4−ニトロ塩化ベンゾイル(6.23g,33.9mmol)とN−フェニルピペラジン(4.71ml,30.8mmol)の無水ジオキサン(250ml)溶液に、トリエチルアミン(4.73ml,33.9mmol)を加え、当該混合物を還流温度(110℃)で5時間攪拌した。冷却後、水(100ml)でクエンチし、得られた水溶性混合物を酢酸エチル(2x75ml)で抽出した。その有機抽出液を混合し、硫酸マグネシウムで乾燥し、濃縮して黄色の油状の粗生成物を得た。純粋な生成物を40%の石油酢酸エチルの混合物から結晶化し、白色結晶(6.5g,62%)として標記化合物を得た。HPLCの保持時間 6.9min。マススペクトル(ES+) m/z 312(M+H)。
【0125】
以下の化合物を、適当な出発原料を使用して、前記記載の方法により合成した。
【0126】
1−(4−ニトロ−ベンゼンスルホニル)−4−フェニル−ピペラジン
ii)(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
塩化スズ二水和物(5.44g,24.1mmol)の濃塩酸(32ml)溶液を、冷却しながら攪拌している(4−ニトロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン(1.0g,3.2mmol)の無水ジエチルエーテル(32ml)溶液にゆっくり加えた。当該混合物を室温で1時間攪拌し、冷却しながら、10Mの水酸化ナトリウム(水溶液)でわずかに塩基性(〜pH9)になるまで注意してクエンチした。当該水溶液を酢酸エチル(100ml)で抽出し、有機抽出物を硫酸マグネシウムで乾燥した。その後、真空内で濃縮し、標記化合物をクリーム色の固体(667mg,収率73%)として得た。HPLCの保持時間 6.2min。マススペクトル(ES+) m/z 282(M+H)。
【0127】
iii)[4−(4−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
攪拌している(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン(200mg,0.71mmol)の1,2−ジクロロエタン(4ml)溶液に、3−クロロベンズアルデヒド(99.7mg,0.71mmol)を0℃で加えた。トリアセト水素化ホウ素ナトリウム(210mg,0.99mmol)と酢酸(40.6μl、0.71mmol)を加え、窒素雰囲気下、室温でオーバーナイト、攪拌した。水酸化ナトリウム(水溶液)(pH8)を加えて反応をクエンチし、ジエチルエーテル(3x20ml)で抽出した。有機抽出液を混合し、硫酸マグネシウムで乾燥し、真空内に濃縮した。残留物をフラッシュクロマトグラフィにより精製し、標記化合物を黄色固体(72mg,収率25%)として得た。HPLCの保持時間 7.5min。マススペクトル(ES+) m/z 406(M+H)。
【0128】
以下の化合物を適当な出発物質を使用して前記記載の方法により合成した。
(4−ベンジルアミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−フルオロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3,4−ジメトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
ベンジル−[4−(4−フェニル−ピペラジン−1−スルホニル)−フェニル]−アミン
(4−フルオロ−ベンジル)−[4−(4−フェニル−ピペラジン−1−スルホニル)−フェニル]−アミン
iv)N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(1)
攪拌している、[4−(4−クロロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン(30mg,0.07mmol)とフェニルスルホニルクロライド(14.2μl、0.11mmol)の無水ジクロロメタン(1ml)溶液に、ピリジン(7.2μl、0.09mmol)を加え、室温で18時間攪拌した。PS−トリス(32mg,0.13mmol)を加え、当該混合物を3時間激しく攪拌し濾過した。濾液を真空内で濃縮し、標記化合物を黄色固体(48mg,収率98%)として得た。HPLCの保持時間 7.7min。マススペクトル(ES+) m/z 547(M+H)。
【0129】
他の化合物を、表2に列挙されている適当な出発原料を使用して実施例1に記載されている方法Aにより調製した。
【0130】
実施例2)N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(方法B)
i)(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
攪拌している、4−アミノ安息香酸(5g,36.5mmol)の懸濁したアセトニトリル溶液に、1−エチル−3−(3−ジメチルアミノプロピル)−塩酸カルボジイミド(7.67g,40.2mmol)、ヒドロキシベンゾトリアゾール水和物(0.49g,3.65mmol)、1−フェニルピペラジン(11.2ml、3.65mmol)を加え、次いで、トリエチルアミン(12.8ml、91.3mmol)を加えた。当該反応混合物を室温で16時間攪拌した。水を加えて希釈し、ジクロロメタン(3x100ml)を使用して抽出した。有機層を混合し、硫酸マグネシウムで乾燥し、真空内で濃縮した。得られた残渣をフラッシュカラムクロマトグラフィ(SiO2)により酢酸エチル/ジクロロメタン(1:1)で溶出して精製し、標記化合物をオフホワイトの固体として得た。HPLCの保持時間 7.1min。マススペクトル(ES+) m/z 282(M+H)。
【0131】
以下の化合物を適当な出発原料を使用して前記記載の方法により合成した。
【0132】
(4−アミノ−3−フルオロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−アミノ−3−メチル−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
ii)4−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−ベンゾニトリル
攪拌している(4−アミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン(0.5g,1.78mmol)のテトラヒドロフラン(10mL)溶液に4−シアノベンズアルデヒドを加え、次いで水素化ホウ素ナトリウムを加え、当該反応を50℃に2時間加熱した。冷却して、当該反応を水(10mL)を加えてクエンチし、塩化アンモニウムを加えて水溶液を塩基性(〜pH8)にした。当該水溶液をジクロロメタン(3x10ml)を使用して抽出し、有機抽出液を混合して、硫酸マグネシウムの上で乾燥し、真空内で濃縮し、標記化合物をオフホワイトの固体(604mg,収率98%)として得た。HPLCの保持時間 7.17min。マススペクトル(ES+) m/z 397(M+H)。
【0133】
以下の化合物を適当な出発物質を使用して前記記載の方法により合成した。
【0134】
[4−(4−ジメチルアミノ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−tert−ブトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−フルオロ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(ビフェニル−4−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−フェニル−ピペラジン−1−イル)−{4−[(ピリジン−3−イルメチル)−アミノ]−フェニル}−メタノン
[4−(2−メチル−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(4−メチル−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(ナフタレン−2−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(ナフタレン−1−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(シクロペンチルメチル−アミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
4−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−安息香酸メチルエステル
(4−フェニル−ピペラジン−1−イル)−[4−(4−トリフルオロメチル−ベンジルアミノ)−フェニル]−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(2−トリフルオロメトキシ−ベンジルアミノ)−フェニル]−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(3−トリフルオロメトキシ−ベンジルアミノ)−フェニル]−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(4−トリフルオロメトキシ−ベンジルアミノ)−フェニル]−メタノン
2−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−ベンゾニトリル
(4−フェニル−ピペラジン−1−イル)−{4−[(チオフェン−3−イルメチル)−アミノ]−フェニル}−メタノン
{4−[(フラン−3−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
{4−[(フラン−2−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−フェネチルアミノ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(シクロプロピルメチル−アミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−ベンジロキシ−エチルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(シクロヘキシルメチル−アミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−フェニル−ピペラジン−1−イル)−[4−(3−フェニル−プロピルアミノ)−フェニル]−メタノン
{4−[(1−メチル−1H−ピラゾール−4−イルメチル)−アミノ]−フェニル}−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−3−フルオロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−3−メチル−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2−エトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(2,3−ジメトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
[4−(3−メトキシ−ベンジルアミノ)−フェニル]−(4−フェニル−ピペラジン−1−イル)−メタノン
iii)N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(2)
4−{[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニルアミノ]−メチル}−ベンゾニトリル(50mg,0.13mmol)、フェニルスルホニルクロライド(80mg,0.42mmol)およびピリジン(0.04mL,0.44mmol)のジクロロメタン(5ml)混合液を16時間還流した。当該混合物を室温まで冷却して、水(4ml)を加えてクエンチした。有機層を回収して、硫酸マグネシウムで乾燥し、真空内で濃縮した。その残渣を分取用薄層クロマトグラフィ(ジクロロメタン/酢酸エチル 1:1)で精製し、標記化合物を白色固体(16.4mg,収率27%)として得た。HPLCの保持時間 6.71min。マススペクトル(ES+) m/z 475(M+H)。
【0135】
以下の化合物を表1に列記されている適当な出発物質を使用して、実施例2に記載の方法Bにより調製した。
【0136】
実施例3)N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド:(方法C)
i)4−ベンジルアミノ−安息香酸
ベンズアルデヒド(9.63ml,95mmol)、酢酸(4.9ml,91.3mmol)を、攪拌している4−アミノ安息香酸(10g,73mmol)のテトラヒドロフラン(200ml)溶液に加え、次いでトリアセト水素化ホウ素ナトリウム(31g,146mmol)を加え、16時間室温で攪拌した。当該反応混合物を水(200ml)で希釈し、ジクロロメタン(2x200ml)で抽出した。当該有機層を混合し、ブラインで洗浄し、硫酸マグネシウムで乾燥し、その後真空内で濃縮した。残渣をフラッシュクロマトグラフィ(SiO2)を用いてジエチルエーテル/ジクロロメタン(1:4)で溶出し、精製した。標記化合物をオフホワイトの固体(4.74g,収率28%)として得た。HPLCの保持時間 5.32min。マススペクトル(ES+) m/z 228(M+H)。
【0137】
ii)(4−ベンジルアミノ−フェニル)−ピペリジンピペリジン−1−イル−メタノン
ピペリジン(0.174ml,1.8mmol)、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド塩酸塩(184mg,0.97mmol)、ヒドロキシベンゾトリアゾール水和物(10mg,結晶)を、攪拌している4−(ベンジルアミノ)安息香酸(200mg,0.88mmol)のアセトニトリル(2ml)懸濁溶液に加え、次いでトリエチルアミン(0.31ml,2.2mmol)を加え、16時間室温で攪拌した。当該混合物を水(2ml)で希釈し、ジクロロメタン(2x2ml)で抽出した。当該有機層を混合し、ブラインで洗浄し、硫酸マグネシウムで乾燥し、その後真空内で濃縮した。残渣をフラッシュクロマトグラフィ(SiO2)を用いて酢酸エチル/ジクロロメタン(1:4)で溶出し、精製した。標記化合物をオフホワイトの固体(122mg,収率47%)として得た。
【0138】
以下の化合物を適当な出発原料を使用して記載されている方法によって合成した:
(4−ベンジルアミノ−2−メチル−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−3−フルオロ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
(4−ベンジルアミノ−2−メトキシ−フェニル)−(4−フェニル−ピペラジン−1−イル)−メタノン
N−ベンジル−N−{4−[4−(2−メトキシ−エチル)−ピペラジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド
N−ベンジル−N−{4−[4−(2−オキソ−2−ピロリジン−1−イル−エチル)−ピペラジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド
(4−ベンジルアミノ−フェニル)−(3,4−ジヒドロ−1H−イソキノリン−2−イル)−メタノン
(4−ベンジルアミノ−フェニル)−(2,6−ジメチル−モルホリン−4−イル)−メタノン
iii)N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(3)
ベンゼンスルホニルクロライド(57μl,0.46mmol)を、攪拌している(4−ベンジルアミノ−フェニル)−ピペリジン−1−イル−メタノン(39mg,0.14mmol)のジクロロメタン(1ml)溶液に加え、次いでピリジン(42μl,0.5mmol)を加え、20時間40℃で加熱した。当該反応を室温まで冷却し、混合物を水(5ml)とジクロロメタン(5ml)間に分離した。有機層を回収し、真空内で濃縮し、分取用TLCにより精製し、標記化合物を白色固体(38mg,収率62%)として得た。HPLCの保持時間 5.8min。マススペクトル(ES+) m/z 435(M+H)。
【0139】
他の化合物を表1に列挙されている適当な出発原料を使用して実施例3に記載されている方法Cにより調製した。
【0140】
実施例4)N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド :(方法D)
i)4−(4−クロロ−ベンジルアミノ)−安息香酸tert−ブチルエステル
tert−ブチル−4−アミノベンゾエート(5.0g,26mmol)、酢酸(2.23ml,39mmol)を、攪拌している4−クロロベンズアルデヒド(5.46g,39mmol)のジクロロメタン(50ml)の溶液に加え、次いでトリアセト水素化ホウ素ナトリウム(13.7g,65mmol)を加え、16時間室温で攪拌した。当該反応混合物に氷(100ml)を加えてクエンチし、得られた水溶液を炭酸ナトリウム(固体)を使用して中和した。ジクロロメタン(3x100ml)を使用して当該水溶液から抽出し、有機層を混合し、硫酸マグネシウムで乾燥し、その後真空内で濃縮し、標記化合物を白色固体(10g,収率81%)として得た。HPLCの保持時間 8.09min。マススペクトル(ES+) m/z 318(M+H)。
【0141】
以下の化合物は適当な出発原料を使用して記載されている方法により合成した:
4−(ベンジルアミノ)−安息香酸tert−ブチルエステル
4−(4−フルオロ−ベンジルアミノ)−安息香酸tert ブチルエステル
4−(ベンジルアミノ)−3−フルオロ−安息香酸tert ブチルエステル
ii)4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸tert−ブチルエステル
4−(4−クロロ−ベンジルアミノ)−安息香酸tert−ブチルエステル(6g,6.3mmol)、フェニルスルホニルクロライド(2.9ml,21mmol)およびピリジン(1.86mL,23mmol)をジクロロメタン(25ml)中16時間加熱還流した。当該反応混合物を室温まで冷却し、ジクロロメタン(25ml)で希釈し、水(2x25ml)で洗浄した。有機層を回収し、硫酸マグネシウムで乾燥し、真空内で濃縮し、フラッシュクロマトグラフィ(ヘキサン/酢酸9:1)によって黄色のオイルを精製し、標記化合物を白色固体(2.2g,収率76%)として得た。HPLCの保持時間 8.54min。
【0142】
以下の化合物を適当な出発原料を使用して記載されている方法により合成した:
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸tert−ブチルエステル
4−[(4−クロロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸tert−ブチルエステル
4−[(4−フルオロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸tert ブチルエステル
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−3−フルオロ−安息香酸tert ブチルエステル
4−(ベンゼンスルホニル−ベンジル−アミノ)−安息香酸tert−ブチルエステル
iii)4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸
4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸tert−ブチルエステル(2.1g,4.4mmol)の10%トリフルオロ酢酸/ジクロロメタン(50mL)溶液を16時間室温で攪拌した。当該反応混合物を真空内で濃縮し、残渣を炭酸水素ナトリウム(飽和溶液、25mL)とジクロロメタン(20mL)間に分離した。水層を分離し、10%HCl(aq)を用いて酸性(pH1)にし、得られた溶液をジクロロメタン(3x75mL)を用いて抽出した。その有機層を混合し、硫酸マグネシウムで乾燥し、真空内で濃縮し、標記化合物を白色固体(1.1g,収率62%)として得た。
【0143】
以下の化合物を適当な出発原料を使用して記載されている方法により合成した:
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸
4−[(4−クロロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸
4−[(4−フルオロ−ベンジル)−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸
4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−3−フルオロ−安息香酸
4−(ベンゼンスルホニル−ベンジル−アミノ)−安息香酸
iv)N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド(4)
3−(4−メチルフェニル)ピペリジン(40mg,0.19mmol)、1−エチル−3−(3−ジメチルアミノプロピル)−カルボジイミド塩酸塩(EDC)(24mg,0.13mmol)を、攪拌している4−[ベンゼンスルホニル−(4−クロロ−ベンジル)−アミノ]−安息香酸(50mg,0.13mmol)のアセトニトリル(1mL)溶液に加え、次いでヒドロキシベンゾトリアゾール(HOBt)(1.7mg,0.013mmol)を加え、16時間室温で攪拌した。当該反応混合物を水(3ml)で希釈し、ジクロロメタン(3x2ml)を用いて抽出した。有機抽出液を混合し、硫酸マグネシウムで乾燥し、真空内で濃縮し、得られた残渣をフラッシュクロマトグラフィ(ジクロロメタン/酢酸エチル 9:1)により精製し、標記化合物を白色発泡体(31mg,収率44%)として得た。HPLCの保持時間 8.25min。マススペクトル(ES+) m/z 559(M+H)。
【0144】
適当な出発原料を使用して実施例4に記載されている方法Dにより調製された他の化合物を表1に列挙する
実施例5)N−ベンジル−N’N’−ジメチル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−スルファミド :(方法E)
i)N−ベンジル−N’N’−ジメチル−N−(4−安息香酸tert−ブチルエステル)−スルファミド
4−ベンジルアミノ−安息香酸tert−ブチルエステル(2g,7mmol)とN,N−ジメチルスルファモイルクロライド(3.8ml,35mmol)のピリジン(20ml)溶液を2時間100℃で加熱した。当該反応混合物を室温に冷却し、,N−ジメチルスルファモイルクロライド(1ml,9mmol)を加え、当該反応を16時間100℃で加熱した。当該反応混合物を室温に冷却し、トルエン(3x100ml)を用いて共沸混合物として真空内で濃縮した。残渣を酢酸エチル(3x100ml)を用いて洗浄し、当該洗浄物を真空内で濃縮して橙のオイルを得た。当該オイルを15%酢酸エチル/ヘキサンを用いてシリカゲルを用いたフラッシュクロマトグラフィにより精製し、標記化合物を白色固体として得た。HPLCの保持時間 6.75min。1HNMR(CDCl3) aH 1.56,s(9H),2.77,s(6H),4.85,s(2H),7.18−7.27,m(5H),7.33,d(2H、J= 8.84),7.9、d(2H、J=8.84).
ii)N−ベンジル−N’N’−ジメチル−N−(4−安息香酸)スルファミド
N−ベンジル−N−(4−安息香酸tert−ブチルエステル)−N’N’−ジメチルスルファミド(1g,2.5mmol)のジクロロメタン(80ml)溶液を0℃に冷却した。トリフルオロ酢酸(20ml)を5分かけて滴下して加え、当該反応を室温まで熱し、その後2時間攪拌した。当該反応混合物を真空内に濃縮し、残渣をヘキサン(100ml)を使用して粉末にした。得られた懸濁液を濾過により標記化合物をベージュ色の固体(0.7g,84%)として得た。HPLCの保持時間 4.28min。マススペクトル(ES+) m/z 333(M+H)。
【0145】
iii)N−ベンジル−N’N’−ジメチル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−スルファミド(5)
攪拌している1−(2−シアノフェニル)−ピペラジン(32mg,0.17mmol)の乾燥ジメチルホルムアミド(1ml)溶液に、N−ベンジル−N’N’−ジメチル−N−(4−安息香酸)スルファミド(50mg,0.15mmol)、トリエチルアミン(0.065ml,0.45mmol)および2−(7−アザ−1H−ベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウムヘキサフルオロホスフェート(63mg,0.17mmol)を加え、当該反応を16時間室温で攪拌した。溶媒を減圧下除去し、残渣を分取用HPLCにより精製した。HPLCの保持時間 6.0min。マススペクトル(ES+) m/z 504(M+H)。
【0146】
適当な出発原料を使用して実施例5に記載されている方法Eにより調製された他の化合物を表1に列挙する。
【0147】
実施例6)N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−N’,N’−ジメチルスルファミド(方法F)
i)(4−アミノ−フェニル)−(2−フェニル−モルフォリンモルフォリン−4−イル)−メタノン
攪拌している、安息香酸(160mg,1mmol)と2−フェニルモルフォリン塩酸塩(300mg,1.5mmol)のアセトニトリル(10ml)懸濁液にトリエチルアミン(0.4ml,3mmol)を加え、次いでHATUを加え、当該反応混合物を16時間室温で攪拌した。当該反応をジクロロメタン(25ml)を用いて希釈し、炭酸水素ナトリウム(25ml,飽和溶液)を用いて洗浄した。有機層を回収し、硫酸マグネシウムで乾燥し、真空内に濃縮した。残渣をシリカゲルフラッシュクロマトグラフィにより酢酸エチルを用いて溶出して精製し、標記化合物を透明なオイル(240mg,収率84%)として得た。HPLCの保持時間 5.05min。マススペクトル(ES+) m/z 283(M+H)。
【0148】
ii)(4−ベンジルアミノ−フェニル)−(2−フェニル−モルフォリン−4−イル)−メタノン
攪拌している(4−アミノ−フェニル)−(2−フェニル−モルフォリン−4−イル)−メタノン(240mg,0.84mmol)のジクロロメタン(20ml)溶液にベンズアルデヒド(0.1ml,1mmol)を加え、当該反応混合物を2時間45℃で加熱した。当該反応混合物を室温に冷却し、トリアセト水素化ホウ素ナトリウム(250mg,1.2mmol)を加え、当該反応を48時間室温で攪拌した。当該反応をジクロロメタン(10ml)を用いて希釈し、水(10ml)を加えてクエンチした。当該水溶液をジクロロメタン(2x10ml)を用いて洗浄し、有機層を混合し、真空内で濃縮し、その残渣をフラッシュクロマトグラフィにより精製し、標記化合物を無色のオイル(0.22g,収率70%)として得た。HPLCの保持時間 6.18min。マススペクトル(ES+) m/z 373(M+H)。
【0149】
iii)N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−N’,N’−ジメチルスルファミド(6)
(4−ベンジルアミノ−フェニル)−(2−フェニル−モルフォリン−4−イル)−メタノン(80mg,0.21mmol)とN,N−ジメチルスルファモイルクロライド(0.3ml,2mmol)のピリジン(5ml)溶液を16時間70℃で加熱した。得られた溶液を塩酸2N(20ml)で洗浄し、有機層を回収し、硫酸マグネシウムで乾燥した。溶媒を減圧除去し、残渣を50%酢酸エチル/ヘキサンを用いて溶出する分取用薄層クロマトグラフィにより精製し、標記化合物を無色のオイル(35mg,収率35%)として得た。HPLCの保持時間 6.1min。マススペクトル(ES+) m/z 480(M+H)。
【0150】
適当な出発原料を使用して実施例6に記載されている方法Fにより調製された他の化合物を表1に列挙する。
【0151】
実施例7)1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−ピペラジン−1−カルボニル)−フェニル]−アミド(方法G)。
【0152】
攪拌しているN−メチルピペラジン(20mg,0.2mmol)、トリエチルアミン(28μl 、0.2mmol)、および2−(7−アザ−1H−ベンゾトリアゾール−1−イル)−1,1,3,3−テトラメチルウロニウム ヘキサフルオロホスフェート(42mg,0.11mmol)を4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−安息香酸(37mg,0.1mmol)の乾燥ジメチルホルム(1ml)溶液に加え、当該溶液を16時間室温で攪拌した。当該反応混合物を真空内で濃縮し、その残渣を分取用HPLCを用いて精製し、標記化合物を透明なオイル(30mg,収率66%)として得た。HPLCの保持時間 4.5min。マススペクトル(ES+) m/z 454(M+H)。
【0153】
適当な出発原料を使用して実施例7に記載されている方法Gにより調製された他の化合物を表1に列挙する。
【0154】
実施例8)1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド(方法H)
i)4−(4−フェニル−ピペラジン−1−イルメチル)−フェニルアミン
水素化ホウ素ナトリウム(63 mg,1.68 mmol)のエタノール(1ml)溶液を、4−(4−フェニルピペラジン−1−イルメチル)−ニトロ−アニリン(1g,3.36 mmol)とスズ(II)ジクロリドニ水和物(2.27 g,10.10 mmol)のエタノール(20ml)溶液に60℃で滴下した。当該反応を0℃に冷却した後、得られた溶液を2時間攪拌し、水酸化ナトリウム(2M)を加えて塩基性(pH>10)にした。その水層をジクロロメタン(3x20ml)を用いて抽出し、混合した有機層をブラインで洗浄した。その後、硫酸マグネシウムで乾燥し、真空内で濃縮した。残渣をカラムクロマトグラフィ(ヘキサン/酢酸エチル 1:1)によって精製し、標記化合物を淡黄色の固体(441mg,49%)として得た。HPLCの保持時間 5.82min。マススペクトル(ES+) m/z 268(M+H)。
【0155】
ii)ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル)−アミン
トリアセト水素化ホウ素ナトリウム(282 mg,1.34 mmol)を、攪拌している4−(4−フェニル−ピペラジン−1−イルメチル)−フェニルアミン、ベンズアルデヒド(75 μl,0.73 mmol)および酢酸(43 μl,0.73 mmol)の乾燥ジクロロメタン(6 ml)溶液に1度に加え、16時間室温で攪拌した。水を加え、有機層を分離し、ブラインで洗浄し、硫酸マグネシウムで乾燥した。当該溶液を真空内に濃縮し、粗残渣をカラムクロマトグラフィ(ヘキサン/酢酸エチル 1:1)によって精製し、標記化合物を無色の固体(175 mg,72%)として得た。HPLCの保持時間 7.53min。マススペクトル(ES+) m/z 358(M+H)。
【0156】
iii)1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド(8)
ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル)−アミン(30mg,0.08mmol)、1−メチルイミダゾール−4−スルホニルクロライド(51 mg,0.27 mmol)およびピリジン(24 μl,0.30 mmol)の乾燥ジクロロメタン(2ml)溶液を加熱して15時間還流した。当該反応混合物を室温に冷却し、真空内で濃縮した。その残渣をカラムクロマトグラフィ(ジクロロメタン中、5%メタノール)により精製し、標記化合物をオフホワイトの固体(22mg,55%)として得た。HPLCの保持時間 7.04min。マススペクトル(ES+) m/z 502(M+H)。1H−NMR(CDCl3) aH 2.54(4H,m,2xCH2),3.16(4H,m,2xCH2),3.45(2H,br s,CH2),3.71(3H,s,CH3),4.99(2H,s,CH2),6.84(1H,t,J = 7.3 Hz,ArH),6.89(2H,m,2xArH),7.10(2H,m,2xArH),7.17−7.30(10H,m,10xArH),7.55(1H,m,ArH).
【0157】
【表1−1】

【0158】
【表1−2】

【0159】
【表1−3】

【0160】
【表1−4】

【0161】
【表1−5】

【0162】
【表1−6】

【0163】
【表1−7】

【0164】
【表1−8】

【0165】
実施例101:Kv1.3オートパッチ電気生理学手法
10μL/mL[100x]グルタミン、500μg/mL G418(ゲンタマイシン)、および1%HT添加物(50x、ヒポキサンチンおよびチミジン)を添加した、CHO細胞用のEx−cell302無血清培地中で、ヒトKv1.3のcDNA(pcDNA3.1中のもの)により安定的にトランスフェクトされた細胞を培養した。全細胞モードのオートパッチ技術を用い、これらの細胞により化合物を試験した。
【0166】
外部浴の溶液の含有物(mM):150 NaCl, 10 KCl, 1 MgCl2, 3 CaCl2, 10 HEPES, pH 7.4(NaOHによる)。パッチピペットを下記組成の電極溶液で満たした(mM):100 K−Gluconate, 20 KCl, 1 MgCl2, 1 CaCl2, 10 HEPES, 11 EGTA, 5 ATP−Na2, 2 グルタチオン, pH 7.2(KOHによる)。
【0167】
化合物をDMSO(100%)に溶解させ、使用直前に外部浴中で1μMの濃度に調製した。実験はすべて室温にて行なった。
【0168】
6×106細胞の密度を有する細胞懸濁物(10mL)を15mL遠心チューブに分取し、使用前は4℃にて保存した。使用前にチューブを取り出し、1000rpmで4分間、室温にて遠心分離した。次いで上清を捨て、チューブの底に細胞ペレットを得た。次いで、1mLの冷たい(4℃)濾過された(0.22μm)0.05%BSA/外部浴溶液(0.05g BSA/100mL外部浴溶液)を用いて当該ペレットを再懸濁させた。チューブの底を手動で撹拌し、次いで静かに粉砕した。次いで細胞懸濁液を、14℃に温度制御されたオートパッチ(商標)培養器に入れ、定期的に粉砕した。
【0169】
一定長さのテフロンキャピラリーチューブを細胞懸濁液に漬け、陰圧により液柱を吸い上げた。Ag/AgCl参照電極を用いてこの液柱を電気的に接続した。ホウケイ酸ガラスパッチピペット(from 1.5mm OD, thin−walled filamented, GC150−TF capillary glass, Harvard)を、DMZピペットガラス電極製作器(Zeitz Instruments)を用いて引き出し、ピペットの先端または本体に泡が残らないように気をつけながら内部ピペット溶液を用いて再充填した。パッチピペットは通常、2.5〜3.5MΩの抵抗を有していた。充填後、ピペットの先端および軸の一部(〜15mm)をシグマコート(Sigma)に漬けた。記録用ピペットをマルチウェルアレイ中に配置し、オートパッチ(AutoPatch)TM機器上に載せた。自動化パッチクランプおよび薬剤の投与についてはオペレータにより開始したが、その後は予めセットした条件および基準を満たす限りは実験をAutoPatch.exeにより継続した。
【0170】
細胞のパッチクランプの記録全体について、Pulseソフトウェア(v8.54またはv8.76, HEKA, Gemany)で制御されるEPC9またはEPC10増幅器(HEKA,Germany)、細胞アプリケータ、自動化薬剤投与システム(DAS)、バルブコントローラ(VF1)および吸引装置(すべて室温)を備えたAutoPatchTM装置を用いて行った。この装置は完全にAutoPatch.exeの制御下にあり、オペレータによる介入は水浴タンクを再充填したり技術的なミスによる細胞の損失を防止したりする必要がある場合のみ行った。
【0171】
灌流および薬剤投与の前に検証工程を行い、観測される電流が実験条件を満たすことを確認した。細胞には、外部溶液を〜2mL/minの流速で連続的に灌流させた。灌流チャンバは80〜85μLの可動体積を有しており、これにより薬液の迅速な交換が可能であった。
【0172】
電気生理学の電位ステップのプロトコールおよびデータの分析は以下のように行った。データについては5kHzでサンプリングし、2.5kHzのバンド幅で−3dBでフィルタリングした。細胞については−80mVの電位に維持した。500ミリ秒間の+30mVへの電位ステップを15秒毎に印加することで電流を発生させた。化合物を投与している間のhKv1.3電流のオンライン分析を、Pulse(v8.54またはv8.76, HEKA, Germany)、Excel(Microsoft, USA)およびAutoPatchTMのソフトウェアにより行い、電位ステップの間ずっと全電荷を測定した。薬剤の存在による電荷移動の阻害を、コントロールと比較して算出した。
【0173】
参考文献
Herbert, “General principles of the structure of ion channels”, Am. J. Med, 104, 87−98, 1998.
Armstrong & Hille, “Voltage−gated ion channels and electrical excitability”, Neuron, 20, 371,380, 1998.
Gutman GA et al., “International Union of Pharmacology. XLI. Compendium of voltage−gated ion channels: potassium channels”. Pharmacol Rev. Dec; 55(4):583−6, 2003.
Shieh et al., “Potassium Channels: Molecular Defects, Diseases, and Therapeutic Opportunities”, Pharmacol Rev, 52(4), 557−594, 2000.
Ford et al., “Potassium Channels: Gene Family, Therapeutic Relevance, High−Throughput Screening Technologies and Drug Discovery”, Prog Drug Res, 58, 133−168, 2002.
Xie M et al., “Ion Channel Drug Discovery Expands into New Disease Areas”, Current Drug Discovery, 31−33, 2004.
Beeton et al., “Kv1.3 channels are a therapeutic target for T cell−mediated autoimmune diseases”, Proceeds of the National Academy of Sciences, 46, 103, 17414−17419, 2006
Cahalan MD & Chandy KG, “Ion Channels in the Immune System as Targets for Immunosuppression”, Current Opinion in Biotechnology, 8, 749−756, 1997.
Wulff H, Beeton C, Chandy KG: Potassium channels as therapeutic targets for autoimmune disorders.(2003) Curr. Opin. Drug Dis. 6(5):640−647
Beeton C, Pennington MW, Wulff H, Singh S, Nugent D, Crossley G, Khaytin I, Calabresi PA, Chen CY, Gutman GA, Chandy KG. Targeting effector memory T−cells with a selective peptide inhibitor of Kv1.3 channels for therapy of autoimmune diseases.(2005) Mol Pharmacol. 67(4):1369−81.
Panyi G, Varga Z, Gaspar R. Abstract Ion channels and lymphocyte activation.(2004) Immunology Lett. 92:55−66.
Chandy KG, Wulff H, Beeton C, Pennington M, Gutman G, Cahalan M: K+ channels as targets for specific immunomodulation. TIPS.(2004) 25(5):280−289
Beeton C, Barbaria J, Giraud P, Devaux J, Benoliel A, Gola M, Sabatier JM, Bernard D, Crest M, Beraud E: Selective blocking of voltage−gated K+ channel improves experimental autoimmune encephalomyelitis and inhibits T cell activation.(2001) J. Immunol. 166:936−944
Price MJ, Lee SC, Deutsch C: Charybdotoxin inhibits proliferation and interleukin−2 production of human peripheral blood lymphocytes.(1989) Proc. Natl. Acad. Sci. 86:10171−10175
Koo GC, Blake JT, Shah K, Staruch MJ, Dumont F, Wunderler DL, Sanchez M, McManus OB, Sirontina−Meisher A, Fischer P, Boltz RC, Goetz MA, Baker R, Bao J, Kayser F, Rupprecht KM, Parsons WH, Tong X, Ita IE, Pivnichny J, Vincent S, Cunningham P, Hora D, Feeney W, Kaczorowski G, Springer MS: Correolide and derivatives are novel immunosuppressants blocking the lymphocyte Kv1.3 potassium channels.(1999) Cell. Immunol., 197:99−107
Schmitz A, Sankaranarayanan A, Azam P, Schmidt−Lassen K, Homerick D, Hansel W, Wulff H: Design of PAP−1, a selective small molecule Kv1.3 blocker, for the suppression of effector memory cells in autoimmune diseases.(2005) Mol. Pharmacol., 68:1254−1270
Triggle D.J, Gopalakkrishnan M, Rampe D, Zheng W: Voltage gated Ion channels as Drug Targets, Wiley, 2005)
Sands et al,: Charabydotoxin blocks voltage−gated K+ channels in human and murine T lymphocytes. J. Gen− Physiol. 1989, 93, 10061−1074.
Garcia et al, Purification, characterisation and biosynthesis of margatoxin, a component of Centruroides maragritatus venom that selectively inhibits voltage−gated potassium channels, J. Biol. Chem. 1993, 268, 18866−1887
Garcia et al,: Purification and characterisation of three inhibitors of voltage dependent K+ channels from Leiurus quinquesttriatus var. hebraeus. Biochemistry, 1994, 33, 6834−6839
Koshchak et al., Subunit composition of brain voltage−gated potassium channels determined by hongotoxin−1, a novel peptide derived from Centruroides limbatus venom. J. Biol. Chem. 1998, 273, 2639−2644.
Peter et al, Effect of toxins Pi2 and Pi3 on human T Lymphocyte kv1.3 channels: the role of Glu7 and Lys24. J. Membr. Biol. 2001, 179, 13−25
Mouhat et al, K+ channel types targeted by synthetic OSK1, a toxin from Orthochirus scrobiculosus scorpion venom Biochem. J. 2005, 385, 95−104
Pennington et al, Identification of there separate binding sites on Shk toxin, a potent inhibitor of voltage dependent potassium channels in human T−lymphocytes and rat brain. Biochem. Biophys. Res. Commun. 1996, 219, 696−701
Pennington et al, ShK−Dap22, a potent Kv1.3−specific immunosuppressive polypeptide. J. Biol. Chem. 1998, 273, 32697−35707
Nguyen A et al., “Novel Nonpeptide Agents Potently Block the C−Type Inactivated Conformation of Kv1.3 and Suppress T Cell Activation”, Mol. Pharmacol., 50, 1672−1679, 1996.
Hanson DC et al., “UK−78,282, a Novel Piperidine Compound That Potently Blocks the Kv1.3 Voltage−Gated Potassium Channel and Inhibits Human T Cell Activation”, Br. J. Pharmacol., 126, 1707−1716, 1999.
Felix JP et al., “Identification and Biochemical Characterization of a Novel Norterpene Inhibitor of the Human Lymphocyte Voltage−Gated Potassium Channel, Kv1.3”, Biochemistry, 38(16), 4922−4930, 1999.
Baell JB et al., “Khellinone Derivatives as Blockers of he Voltage−Gated Potassium Channel Kv1.3: Synthesis and Immunosuppressive Activity” J. Med. Chem., 47, 2326−2336, 2004.
Wulff H et al., “Alkoxypsoralens, Novel Nonpeptide Blockers of Shaker−Type K+ Channels: Synthesis and Photoreactivity”, J. Med. Chem., 41, 4542−4549, 1998.
Vennekamp J, Wulff H, Beeton C, Calabresi PA, Grissmer S, Hansel W, and Chandy KG. Kv1.3−blocking 5−phenylalkoxypsoralens: a new class of immunomodulators.(2004) Mol. Pharmacol.65, 1364−74.
Wenrong et al., Design, synthesis and structure-Activity relationships of benzoxazinone−Based factor Xa inhibitors,Bioorg. Med. Chem. Lett.; EN; 13 3; 2003; 561−566
Xue et al., Crystal structure of the PXR-T1317 complex provides a scaffold to examine the potential for receptor antagonism, Bioorg. Med. Chem. Lett.; EN; 15; 5; 2007; 2156−2166
Triggle et al., Voltage−Gated Ion channels as drug targets, Methods and Principles in Medicinal Chemistry.; Vol. 29; 2006; 214−274
【特許請求の範囲】
【請求項1】
式(I)の化合物もしくはその塩、またはこれらの製薬上許容されうる誘導体;
【化1】

式中、
R1は置換されていてもよいアリールアルキル、置換されていてもよいアリール、置換されていてもよいヘテロアリールアルキルおよび置換されていてもよいヘテロアリールからなる群から選択され;
R2は置換されていてもよいアシル、置換されていてもよいスルホニルおよび置換されていてもよいスルファモイルからなる群から選択され;
R3は水素、ハロゲン、ヒドロキシル、アルコキシ、アリールオキシ、置換されていてもよいアルキル、置換されていてもよいアミノ、置換されていてもよいアミノカルボニル、置換されていてもよいアミノまたはニトリルからなる群から選択され;
X1は化学結合、CR7R8、C(=O)、C(=NH)、NR9、NHC(=O)、およびSO2からなる群から選択され;
R7およびR8は、それぞれ独立して、水素、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールから選択され;または、
R7およびR8は、置換されていてもよいC4−C6のシクロアルキル環を共に形成し;
R9は水素、置換されていてもよいアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールからなる群から選択され;
Aは、置換されていてもよい飽和したまたは部分的に飽和した一般式
【化2】

で表される4−7員環、または
【化3】

から選択され:
それぞれにおいて;
X2はCHまたはNであり;
X3はC(R5)2、N(R5b)、OまたはSであり;
X4は、それぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
n=1または2である。
【請求項2】
Aが
【化4】

から選択される、請求項1に記載の化合物;
式中、
n=1または2であり;
X3はC(R5)2、N(R5b)、またはOであり;
X4はそれぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、ヒドロキシル、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。
【請求項3】
R2はC(=O)R10、SO2R10からなる群から選択され;
R10はNR11R12、置換されていてもよいアリール、および置換されていてもよいヘテロアリールであり;
R11およびR12は同じであるかまたは異なり、それぞれ水素、置換されていてもよいアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである、請求項1または2に記載の化合物。
【請求項4】
R10がNR11R12から選択される、請求項3に記載の化合物。
【請求項5】
R10が式(II)、(III)、(IV)または(V)の化合物から選択される、請求項3に記載の化合物;
【化5】

式中、
G、J、L、D、およびEは同じであるかまたは異なりそれぞれCまたはNであり(G、J、L、D、またはEの少なくとも一つがNであり);
R10が式(II)であるときは、LはOまたはSであってもよく、および
R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるい置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよく;
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであるか、あるいは、R15およびR16の対、もしくはR16およびR17の対、もしくはR17およびR18の対、もしくはR18およびR19の対が置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよい。
【請求項6】
R1が置換されていてもよいアリールアルキル、および置換されていてもよいヘテロアリールアルキルから選択される、請求項1〜5のいずれか1項に記載の化合物。
【請求項7】
R1が式(VI)から選択される、請求項1〜6のいずれか1項に記載の化合物;
【化6】

式中、
R20、R21、R22、R23およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルまたは置換されていてもよいアルコキシであり;
R25およびR26は同じであるかまたは異なり、それぞれ水素、ヒドロキシル、および置換されていてもよいC1−3アルキルである。
【請求項8】
R3が水素、ハロゲン、ヒドロキシル、ニトリル、または置換されていてもよいアルキルから選択される、請求項1〜7のいずれか1項に記載の化合物。
【請求項9】
X1が化学結合、CH2、およびC(=O)からなる群から選択される、請求項1〜8のいずれか1項に記載の化合物。
【請求項10】
式(VII)である請求項1〜9のいずれか1項に記載の化合物;
【化7】

式中、
n=1または2であり;
X1は化学結合、CH2、またはC(=O)からなる群から選択され;
X3はC(R5)2、N(R5b)、またはOであり;
X4はそれぞれ独立してC(=O)、またはC(R4)2から選択され;
R3は水素、ハロゲンまたは置換されていてもよいC1−3アルキルからなる群から選択され;
R4はそれぞれ独立して、水素、ハロゲン、ヒドロキシル、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5はそれぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R10はNR11R12または式(II)、(III)、(IV)もしくは(V)の化合物から選択され;
【化8】

式中、
R11およびR12は同じであるかまたは異なり、それぞれ置換されていてもよいC1−3アルキルであり;
G、J、L、D、およびEは同じであるかまたは異なり、それぞれC、またはNであり(G、J、L、D、またはEの少なくとも一つはNであり);
R10が式(II)であるときは、LはOまたはSであってもよく、および
R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるいは置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよく;
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであり、またはR15およびR16の対、もしくはR16およびR17の対、もしくはR17およびR18の対、もしくはR18およびR19の対が置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよく;
R20、R21、R22、R23、およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルもしくは置換されていてもよいアルコキシである。
【請求項11】
N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(3−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
ナフタレン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−3,4−ジメトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
2,3−ジヒドロ−ベンゾ[1,4]ジオキシン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−4−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
チオフェン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
チオフェン−3−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−4−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−2−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−4−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−2−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−2−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−メトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3,5−ジクロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−クロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(3−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(3−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(4−トリフルオロメチル−ベンジル)−ベンゼンスルホンアミド
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(3−トリフルオロメトキシ−ベンジル)−ベンゼンスルホンアミド
N−(2−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
2,2−ジメチル−クロマン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−4−ニトロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
フラン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−N−[3−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[3−メトキシ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(3,4−ジヒドロ−1H−イソキノリン−2−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(2,6−ジメチル−モルフォリン−4−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−4−エチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(4−ベンジル−4−ヒドロキシ−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2,3−ジメトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−クロロ−ベンジル)−N−{4−[3−(4−メトキシ−フェニル)−ピペリジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−フルオロ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−メトキシ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド
1,3−ジメチル−1H−ピラゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2,3−ジメチル−3H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2,4−ジメチル−チアゾール−5−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−3−フルオロフェニル]−ジメチルスルファミド
N−(4−フルオロ)ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド
4−{4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−ベンゾイル}−2−フェニル−ピペラジン−1−カルボン酸tert−ブチルエステル
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(4−フルオロ−フェニル)−ピロリジン−1−カルボニル]−フェニル}−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−ジメチルスルファミド
N−ベンジル−N−{4−[3−(3−イソプロピル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−ジメチルスルファミド
N−ベンジル−N−[4−(3−ベンジルオキシ−ピロリジン−1−カルボニル)−フェニル]−ジメチルスルファミド
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド
N−ベンジル−N−[4−(4−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[4−(2−フルオロ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−シクロヘキシルメチル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−チアゾール−2−イル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−トリフルオロメチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4,4−ジフルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
ピリジン−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−フルオロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3,4−ジクロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−4−フルオロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(2−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3,3−ジフルオロ−ピロリジン−1−カルボニル)−フェニル]−アミド
およびそれらの製薬上許容されうる塩から選択される、請求項1〜10のいずれか1項に記載の化合物。
【請求項12】
請求項1〜11のいずれか1項に記載の化合物の少なくとも一つを含み、一以上の製薬上許容されうる賦形剤、希釈剤および/または担体を含んでもよい、薬剤組成物。
【請求項13】
薬剤に使用する請求項1〜11のいずれか1項に記載の化合物。
【請求項14】
カリウムチャネル阻害を必要とする疾患の予防または治療に使用する請求項13に記載の化合物。
【請求項15】
前記疾患が乾癬、関節リウマチ、多発性硬化症、または他の免疫不全である、請求項14に記載の化合物。
【請求項16】
請求項1〜11のいずれか1項に記載の少なくとも一つの化合物または請求項12に記載の薬剤組成物の有効量を患者に投与することを含む、カリウムチャネル阻害を必要とする疾患を予防または治療する方法。
【請求項17】
前記疾患が乾癬、関節リウマチ、多発性硬化症、または他の免疫不全である、請求項16に記載の方法。
【請求項18】
カリウムチャネル阻害に用いるための薬剤の製造における、請求項1〜11のいずれか1項に記載の化合物の使用。
【請求項19】
前記薬剤は乾癬、関節リウマチ、多発性硬化症、または他の免疫不全の治療に使用される、請求項18に記載の使用。
【請求項1】
式(I)の化合物もしくはその塩、またはこれらの製薬上許容されうる誘導体;
【化1】

式中、
R1は置換されていてもよいアリールアルキル、置換されていてもよいアリール、置換されていてもよいヘテロアリールアルキルおよび置換されていてもよいヘテロアリールからなる群から選択され;
R2は置換されていてもよいアシル、置換されていてもよいスルホニルおよび置換されていてもよいスルファモイルからなる群から選択され;
R3は水素、ハロゲン、ヒドロキシル、アルコキシ、アリールオキシ、置換されていてもよいアルキル、置換されていてもよいアミノ、置換されていてもよいアミノカルボニル、置換されていてもよいアミノまたはニトリルからなる群から選択され;
X1は化学結合、CR7R8、C(=O)、C(=NH)、NR9、NHC(=O)、およびSO2からなる群から選択され;
R7およびR8は、それぞれ独立して、水素、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールから選択され;または、
R7およびR8は、置換されていてもよいC4−C6のシクロアルキル環を共に形成し;
R9は水素、置換されていてもよいアルキル、置換されていてもよいアリールおよび置換されていてもよいヘテロアリールからなる群から選択され;
Aは、置換されていてもよい飽和したまたは部分的に飽和した一般式
【化2】

で表される4−7員環、または
【化3】

から選択され:
それぞれにおいて;
X2はCHまたはNであり;
X3はC(R5)2、N(R5b)、OまたはSであり;
X4は、それぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
n=1または2である。
【請求項2】
Aが
【化4】

から選択される、請求項1に記載の化合物;
式中、
n=1または2であり;
X3はC(R5)2、N(R5b)、またはOであり;
X4はそれぞれ独立して、C(=O)、またはC(R4)2から選択され;
R4は、それぞれ独立して、水素、ハロゲン、ヒドロキシル、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5は、それぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである。
【請求項3】
R2はC(=O)R10、SO2R10からなる群から選択され;
R10はNR11R12、置換されていてもよいアリール、および置換されていてもよいヘテロアリールであり;
R11およびR12は同じであるかまたは異なり、それぞれ水素、置換されていてもよいアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールである、請求項1または2に記載の化合物。
【請求項4】
R10がNR11R12から選択される、請求項3に記載の化合物。
【請求項5】
R10が式(II)、(III)、(IV)または(V)の化合物から選択される、請求項3に記載の化合物;
【化5】

式中、
G、J、L、D、およびEは同じであるかまたは異なりそれぞれCまたはNであり(G、J、L、D、またはEの少なくとも一つがNであり);
R10が式(II)であるときは、LはOまたはSであってもよく、および
R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるい置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよく;
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであるか、あるいは、R15およびR16の対、もしくはR16およびR17の対、もしくはR17およびR18の対、もしくはR18およびR19の対が置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよい。
【請求項6】
R1が置換されていてもよいアリールアルキル、および置換されていてもよいヘテロアリールアルキルから選択される、請求項1〜5のいずれか1項に記載の化合物。
【請求項7】
R1が式(VI)から選択される、請求項1〜6のいずれか1項に記載の化合物;
【化6】

式中、
R20、R21、R22、R23およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルまたは置換されていてもよいアルコキシであり;
R25およびR26は同じであるかまたは異なり、それぞれ水素、ヒドロキシル、および置換されていてもよいC1−3アルキルである。
【請求項8】
R3が水素、ハロゲン、ヒドロキシル、ニトリル、または置換されていてもよいアルキルから選択される、請求項1〜7のいずれか1項に記載の化合物。
【請求項9】
X1が化学結合、CH2、およびC(=O)からなる群から選択される、請求項1〜8のいずれか1項に記載の化合物。
【請求項10】
式(VII)である請求項1〜9のいずれか1項に記載の化合物;
【化7】

式中、
n=1または2であり;
X1は化学結合、CH2、またはC(=O)からなる群から選択され;
X3はC(R5)2、N(R5b)、またはOであり;
X4はそれぞれ独立してC(=O)、またはC(R4)2から選択され;
R3は水素、ハロゲンまたは置換されていてもよいC1−3アルキルからなる群から選択され;
R4はそれぞれ独立して、水素、ハロゲン、ヒドロキシル、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R5はそれぞれ独立して、水素、ハロゲン、置換されていてもよいアミノ、ヒドロキシル、置換されていてもよいアルコキシ、置換されていてもよいアリールオキシ、置換されていてもよいアルキル、置換されていてもよいアルカノイル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;および
R5bは、水素、置換されていてもよいアシル、置換されていてもよいアルキル、置換されていてもよいシクロアルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールまたは置換されていてもよいヘテロアリールであり;
R10はNR11R12または式(II)、(III)、(IV)もしくは(V)の化合物から選択され;
【化8】

式中、
R11およびR12は同じであるかまたは異なり、それぞれ置換されていてもよいC1−3アルキルであり;
G、J、L、D、およびEは同じであるかまたは異なり、それぞれC、またはNであり(G、J、L、D、またはEの少なくとも一つはNであり);
R10が式(II)であるときは、LはOまたはSであってもよく、および
R10が式(III)であるときは、GはOまたはSであってもよく;
R13およびR14は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいC1−3アルキル、置換されていてもよいアリールアルキル、置換されていてもよいアリールもしくは置換されていてもよいヘテロアリールであるか、あるいは置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよく;
R15、R16、R17、R18、およびR19は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルであり、またはR15およびR16の対、もしくはR16およびR17の対、もしくはR17およびR18の対、もしくはR18およびR19の対が置換されていてもよい飽和したまたは部分的に飽和した5−7員のヘテロ環もしくは炭素環を共に形成してもよく;
R20、R21、R22、R23、およびR24は同じであるかまたは異なり、それぞれ水素、ハロゲン、ヒドロキシル、置換されていてもよいアミノ、ニトリル、置換されていてもよいC1−3アルキルもしくは置換されていてもよいアルコキシである。
【請求項11】
N−(4−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(3−クロロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
ナフタレン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−3,4−ジメトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
2,3−ジヒドロ−ベンゾ[1,4]ジオキシン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−4−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
チオフェン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
チオフェン−3−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−4−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−2−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−フルオロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−4−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−2−シアノ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−2−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−メチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−メトキシ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3,5−ジクロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−3−クロロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(3−フルオロ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(3−メトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−メチル−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(4−トリフルオロメチル−ベンジル)−ベンゼンスルホンアミド
N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−N−(3−トリフルオロメトキシ−ベンジル)−ベンゼンスルホンアミド
N−(2−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−シアノ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
2,2−ジメチル−クロマン−6−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−4−ニトロ−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
フラン−2−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−N−[3−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[3−メトキシ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(3,4−ジヒドロ−1H−イソキノリン−2−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(2,6−ジメチル−モルフォリン−4−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−4−エチル−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−ベンジル−N−[4−(4−ベンジル−4−ヒドロキシ−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(2,3−ジメトキシ−ベンジル)−N−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−クロロ−ベンジル)−N−[4−(3−p−トリル−ピペリジン−1−カルボニル)−フェニル]−ベンゼンスルホンアミド
N−(4−クロロ−ベンジル)−N−{4−[3−(4−メトキシ−フェニル)−ピペリジン−1−カルボニル]−フェニル}−ベンゼンスルホンアミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−メチル−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−フルオロ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−メトキシ−ベンジル)−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フェニル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(3−メチル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−アミド
1,3−ジメチル−1H−ピラゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2,3−ジメチル−3H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2,4−ジメチル−チアゾール−5−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−フェニル−ピペラジン−1−イルメチル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[2−フルオロ−4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド
N−ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−3−フルオロフェニル]−ジメチルスルファミド
N−(4−フルオロ)ベンジル−N−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−ジメチルスルファミド
4−{4−[ベンジル−(1−メチル−1H−イミダゾール−4−スルホニル)−アミノ]−ベンゾイル}−2−フェニル−ピペラジン−1−カルボン酸tert−ブチルエステル
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[3−(4−フルオロ−フェニル)−ピロリジン−1−カルボニル]−フェニル}−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
N−ベンジル−N−{4−[4−(2−シアノ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−ジメチルスルファミド
N−ベンジル−N−{4−[3−(3−イソプロピル−[1,2,4]オキサジアゾール−5−イル)−ピペリジン−1−カルボニル]−フェニル}−ジメチルスルファミド
N−ベンジル−N−[4−(3−ベンジルオキシ−ピロリジン−1−カルボニル)−フェニル]−ジメチルスルファミド
N−ベンジル−N−[4−(4−ヒドロキシ−4−フェニル−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド
N−ベンジル−N−[4−(4−フェノキシ−ピペリジン−1−カルボニル)−フェニル]−ジメチルスルファミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−{4−[4−(2−フルオロ−フェニル)−ピペラジン−1−カルボニル]−フェニル}−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−シクロヘキシルメチル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4−チアゾール−2−イル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−トリフルオロメチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(4,4−ジフルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸ベンジル−[4−(3−フルオロ−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(2−フェニル−モルフォリン−4−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
ピリジン−3−スルホン酸(4−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
2−メチル−2H−ピラゾール−3−スルホン酸ベンジル−[4−(4−メチル−3−フェニル−ピペラジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−フルオロ−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−メチル−ベンジル)−[4−(3−メチル−ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3,4−ジクロロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(3−クロロ−4−フルオロ−ベンジル)−[4−(ピペリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(2−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3−メチル−ピロリジン−1−カルボニル)−フェニル]−アミド
1−メチル−1H−イミダゾール−4−スルホン酸(4−クロロ−ベンジル)−[4−(3,3−ジフルオロ−ピロリジン−1−カルボニル)−フェニル]−アミド
およびそれらの製薬上許容されうる塩から選択される、請求項1〜10のいずれか1項に記載の化合物。
【請求項12】
請求項1〜11のいずれか1項に記載の化合物の少なくとも一つを含み、一以上の製薬上許容されうる賦形剤、希釈剤および/または担体を含んでもよい、薬剤組成物。
【請求項13】
薬剤に使用する請求項1〜11のいずれか1項に記載の化合物。
【請求項14】
カリウムチャネル阻害を必要とする疾患の予防または治療に使用する請求項13に記載の化合物。
【請求項15】
前記疾患が乾癬、関節リウマチ、多発性硬化症、または他の免疫不全である、請求項14に記載の化合物。
【請求項16】
請求項1〜11のいずれか1項に記載の少なくとも一つの化合物または請求項12に記載の薬剤組成物の有効量を患者に投与することを含む、カリウムチャネル阻害を必要とする疾患を予防または治療する方法。
【請求項17】
前記疾患が乾癬、関節リウマチ、多発性硬化症、または他の免疫不全である、請求項16に記載の方法。
【請求項18】
カリウムチャネル阻害に用いるための薬剤の製造における、請求項1〜11のいずれか1項に記載の化合物の使用。
【請求項19】
前記薬剤は乾癬、関節リウマチ、多発性硬化症、または他の免疫不全の治療に使用される、請求項18に記載の使用。
【公表番号】特表2012−500834(P2012−500834A)
【公表日】平成24年1月12日(2012.1.12)
【国際特許分類】
【出願番号】特願2011−524445(P2011−524445)
【出願日】平成21年8月27日(2009.8.27)
【国際出願番号】PCT/GB2009/002075
【国際公開番号】WO2010/023445
【国際公開日】平成22年3月4日(2010.3.4)
【公序良俗違反の表示】
(特許庁注:以下のものは登録商標)
1.テフロン
【出願人】(510190613)ゼンション・リミテッド (3)
【氏名又は名称原語表記】XENTION LIMITED
【Fターム(参考)】
【公表日】平成24年1月12日(2012.1.12)
【国際特許分類】
【出願日】平成21年8月27日(2009.8.27)
【国際出願番号】PCT/GB2009/002075
【国際公開番号】WO2010/023445
【国際公開日】平成22年3月4日(2010.3.4)
【公序良俗違反の表示】
(特許庁注:以下のものは登録商標)
1.テフロン
【出願人】(510190613)ゼンション・リミテッド (3)
【氏名又は名称原語表記】XENTION LIMITED
【Fターム(参考)】
[ Back to top ]

