新規なN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネート
【課題】 工業的にゼオライトを製造する際の鋳型化合物として、簡便な製法を用いて容易に得られるN,N,N−トリメチルアダマンタンアンモニウム塩を提供する。
【解決手段】 本発明のN,N,N−トリメチル−1−アダマンタンアンモニウム塩は、
下記式(1)
【化1】

で表されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートである。
【解決手段】 本発明のN,N,N−トリメチル−1−アダマンタンアンモニウム塩は、
下記式(1)
【化1】

で表されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートである。
【発明の詳細な説明】
【技術分野】
【0001】
本発明はN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートに関する。N,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートは、ゼオライトを製造する際の鋳型化合物として有用な新規な化合物である。
【背景技術】
【0002】
ゼオライトは、主としてアルミニウム源とケイ素源を含有する原料を水性合成ゲル中で反応させて結晶を形成させ、該結晶を成長させた後、乾燥させ、次いで焼成処理に付して細孔から水を除去することによって一般に得られる。その際、合成ゲル中において鋳型化合物を使用することにより、各種のゼオライトが設計されている。
【0003】
ゼオライトを製造するための鋳型化合物として、アダマンタン化合物を使用することは公知である。
【0004】
例えば、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物を用いてゼオライトSSZ−13が調製されている(例えば、特許文献1参照)。また、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物等を用いて種々のゼオライトが調製されている(例えば、特許文献2参照)。さらに、N,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物等を用いてゼオライトSSZ−23が調製されている(例えば、特許文献3参照)
これらのアダマンタン化合物の合成法としては、例えば、1−アミノアダマンタンにトリブチルアミン存在下で3倍モルのメチルヨウ化物を反応させてN,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物を得る方法が記載されている(例えば、特許文献1、特許文献2参照)。
【0005】
また、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物を酸化銀と水中で反応させてN,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物を得るる方法が記載されている(例えば、特許文献2参照)。
【0006】
さらに、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物をイオン交換樹脂を用いてイオン交換する方法によってN,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物を得る方法が記載されている(例えば、特許文献3参照)。
【0007】
しかしながら、これら従来の製法では、原料の1−アミノアダマンタン及び反応試薬として用いられるメチルヨウ化物が高価なため、得られるN,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物や、N,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物をゼオライト製造用の工業的な原料として用いることは、経済的に不利である。
【0008】
したがって、工業的にゼオライトを製造する際の鋳型化合物として、簡便な製法を用いて高収率で容易に得られるN,N,N−トリメチルアダマンタンアンモニウム塩が望まれていた。
【発明の開示】
【発明が解決しようとする課題】
【0009】
本発明は、前記の背景技術に鑑みてなされたものであり、その目的は、工業的にゼオライトを製造する際の鋳型化合物として、簡便な製法を用いて容易に得られるN,N,N−トリメチルアダマンタンアンモニウム塩を提供することである。
【0010】
【特許文献1】米国特許第4665110号明細書
【特許文献2】米国特許第4544538号明細書
【特許文献3】特公平06−11648号明細書
【課題を解決するための手段】
【0011】
本発明者らは前記の課題を解決するために鋭意検討した結果、N,N,−ジメチル−1−アミノアダマンタンと炭酸ジメチルから、新規なN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートを合成することが出来ることを見出し、本発明を完成するに至った。
【0012】
すなわち、本発明は、下記式(1)
【0013】
【化1】

で表されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートである。
【発明の効果】
【0014】
本発明の上記式(1)で表されるN,N,N−トリメチル−1−アダマンタンアンモニウム塩は、簡便な製法を用いて容易に得ることができるため、本発明は工業的に極めて有用である。
【0015】
以下、本発明を詳細に説明する。
【0016】
本発明の上記式(1)で示されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートは、例えば、N,N−ジメチル−1−アミノアダマンタンと炭酸ジメチルとの反応で合成することができる。
【0017】
上記の反応で使用されるN,N−ジメチル−1−アミノアダマンタンは、例えば、1−ハロゲン化アダマンタンとジメチルアミンを、触媒としてヨウ素の存在下で反応させることにより、簡便にかつ安価に得ることができる。
【0018】
上記の反応で使用される炭酸ジメチルの使用量は、特に限定するものではないが、N,N,−ジメチル−1−アミノアダマンタン1モル当たり、1〜20モルの範囲であることが好ましく、更に好ましくは1モル〜10モルの範囲である。1モル未満であると反応が化学量論的に進行せずに未反応のN,N,−ジメチル−1−アミノアダマンタンが残存し、20モル以上ではコスト的に不利である。
【0019】
上記したN,N−ジメチル−1−アミノアダマンタンと炭酸ジメチルとの反応は、無溶媒条件又は不活性溶媒存在下で実施される。反応に用いられる不活性溶媒としては、例えば、ペンタン、ヘキサン、ヘプタン、オクタン、ノナン、デカン、ウンデカン、ドデカン、トリデカン等の直鎖状脂肪族炭化水素類、ジメチルブタン、メチルペンタン、ジメチルペンタン、メチルヘキサン、トリメチルペンタン、ジメチルヘキサン、メチルヘプタン等の分岐状脂肪族炭化水素類、シクロペンタン、シクロヘキサン、シクロオクタン、メチルシクロペンタン、メチルシクロへキサン、メチルシクロヘプタン、メチルシクロオクタン、ジメチルシクロペンタン、ジメチルシクロヘキサン、ジメチルシクロヘプタン、ジメチルシクロオクタン、エチルシクロペンタン、エチルシクロヘキサン、エチルシクロヘプタン、エチルシクロオクタン等の環状脂肪族炭化水素類、ジメチルエーテル、ジエチルエーテル、n−プロピルエーテル、n−ブチルエーテル、n−ペンチルエーテル、n−ヘキシルエーテル、n−オクチルエーテル等の直鎖状脂肪族エーテル類、イソプロピルエーテル、イソブチルエーテル、ブチルメチルエーテル、ブチルエチルエーテル、sec−ブチルメチルエーテル、tert−ブチルメチルエーテル、tert−ブチルエチルエーテル等の分岐状脂肪族エーテル類、混合物として石油エーテル、石油ベンジン、リグロイン等、ジメチルスルホキサイド、ジエチルエーテル、DMF、HMPA等の極性溶媒、更には、メタノール、エタノール、n−プロパノール、n−ブタノール、n−ペンタノール、n−ヘプタノール、n−オクタノール、n−ノナノール、n−デカノール、n−ウンデカノール、n−ドデカノール、n−トリデカノール、n−テトラデカノール、n−ヘキサデカノール、n−オクタデカノール等の直鎖状一級アルコール類、2−メチル−1−プロパノール、2−メチル−1−ブタノール、3−メチル−1−ブタノール、2−エチル−1−ブタノール、4−メチル−1−ペンタノール、3−メチル−1−ペンタノール、3−メチル−1−ペンタノール、2−メチル−1−ペンタノール、2−メチル−3−ペンタノール、2,2−ジメチル−1−プロパノール、3,3−ジメチル−1−ブタノール、2−エチル−1−ブタノール、2−エチル−1−ヘキサノール、5−メチル−1−ヘキサノール、2,2,4−トリメチル−1−ペンタノール、2,4,4−トリメチル−1−ペンタノール、3,5−ジメチル−1−ヘキサノール、2−プロピル−1−ペンタノール、2−エチル−1−ヘキサノール、3,5,5−トリメチル−1−ヘキサノール、3,7−ジメチル−1−オクタノール、6−メチル−1−オクタノール等の分岐鎖状一級アルコール類、イソプロパノール、2−ブタノール、2−ペンタノール、2−ヘキサノール、2−ヘプタノール、2−オクタノール、2−ノナノール、2−デカノールブタノール、2−ウンデカノール、2−ドデカノール、2−トリデカノール、2−テトラデカノール、2−ヘキサデカノール、2−オクタデカノール、3−メチル−2−ブタノール、4−メチル−2−ペンタノール、3−メチル−2−ペンタノール、3,3−ジメチル−2−ブタノール、2,2−ジメチル−3−ペンタノール、2−メチル−3−ヘキサノール、2,4−ジメチル−3−ペンタノール、5−メチル−2−ヘキサノール、4,4−ジメチル−2−ペンタノール、6−メチル−2−ヘプタノール、4−メチル−3−ヘプタノール、2,6−ジメチル−4−ヘプタノール、2,6,8−トリメチル−4−ノナノール等の分岐状二級アルコール類、シクロヘキサノール、シクロヘプタノール、シクロブタノール、シクロペンタノール等の脂環式一級アルコール類、tert−ブタノール、2−メチル−2−ブタノール、3−メチル−3−ペンタノール、2,3−ジメチル−2−ブタノール、3−エチル−3−ペンタノール、2−メチル−2−ヘキサノール、2,3−ジメチル−3−ペンタノール、3−メチル−3−オクタノール、3,7−ジメチル−3−オクタノール等の三級アルコール類等が挙げられる。これらのうち、ジメチルスルホキサイド、ジエチルエーテル、THF、DMF、HMPA、メタノール、エタノール、n−プロパノール、2−プロパノールは、工業的に入手し易い極性溶媒であり反応溶媒として好ましい。これらの溶媒を単独で又は任意の割合で混合して使用しても良い。本発明においては、取り扱いの容易さと経済性から、それらの中でも特にメタノールが好ましい。
【0020】
上記の反応において、使用される溶媒量は、特に限定するものではないが、N,N,−ジメチルアミノアダマンタン1g当たり、通常0.1g〜100gの範囲、好ましくは0.5g〜2.0gの範囲である。溶媒量がN,N,−ジメチルアミノアダマンタン1g当たり0.1gよりも少ない量では、反応系が粘調になり、反応速度が低下するおそれがある。また、100g以上の量では、反応液が希薄となり、反応速度が低下するおそれがある。
【0021】
上記の反応において、加熱反応を行う際に、炭酸ジメチル及び低沸点のアルコールは揮発しやすいため、この場合には反応を密閉容器で行うことが望ましい。反応時の圧力は、特に限定するものではないが、常圧〜10MPaの範囲で十分である。
【0022】
上記の反応において、反応温度としては、特に限定するものではないが、50〜300℃の範囲が好ましく、更に好ましくは100〜200℃の範囲である。50℃よりも低い温度では、十分な反応速度が得られない場合があり、また、300℃を超える温度では、目的生成物の分解等も起こりやすくなるため好ましくない。
【0023】
上記の反応において、目的物の単離は、通常は生成した四級塩をろ過することで可能である。但し、反応が充分進行して原料のN,N,−ジメチル−1−アミノアダマンタンが残存していない場合は、反応後に得られた反応液から未反応の炭酸ジメチルと溶媒を留去することのみで直接目的物を得ることが出来る。
【実施例】
【0024】
以下に、本発明の詳細について実施例を用いて具体的に説明するが、本発明はそれらに限定して解釈されるものではない。なお、本実施例における生成物の収率は、1H−NMRにて確認した。
【0025】
なお、以下の実施例において、1H−NMR及び13C−NMRの測定は、Varian社製Gemini−200を使用した。
【0026】
また、液体クロマトグラフィーによる質量分析は、ブルカー・ダルトニクス社製、TOF−MS、microTOFを使用した(イオン源 ESI、測定モード 陽イオン)。
【0027】
調製例.
撹拌子を入れたステンレス製の30ml簡易耐圧容器に、1−ブロモアダマンタン1.0g(4.7mmol)、ヨウ素0.24g(0.93mmol)を入れ、反応器を窒素雰囲気下でドライアイスバスにつけて冷却した状態でボンベからジメチルアミンガスを通じてジメチルアミン9.6g(212mmol)を冷却捕集した。反応器を密閉後、オイルバスに漬け加温撹拌し180℃まで昇温し、続けて同条件で4時間反応を行った。尚、反応時の圧力は10Mpaを越えることはなかった。反応終了後に反応器を室温まで冷却し、得られたスラリー状物に48%苛性水溶液とジクロロメタンを加えて中和、抽出を行い、分液して得られた反応液についてガスクロマトグラフィー分析(内部標準法)を行った。その結果、1−ブロモアダマンタンの転化率は97.1%であり、N,N−ジメチル−1−アミノアダマンタンが収率91.6%で得られ、アダマンタン−1−オールが1.7%とアダマンタンが2.3%得られたことを確認した。
【0028】
実施例1.
攪拌子を入れたステンレス製の30ml簡易耐圧容器に、N,N,−ジメチル−1−アミノアダマンタン3.59g(20mmol)、炭酸ジメチル5.40g(60mmol)、メタノール2.92gを入れ、反応器内を窒素で置換した。反応器を密閉後、オイルバスに漬けて加熱攪拌し145℃まで昇温し、続けて同条件で10時間反応を行った。反応終了後に反応器を室温まで冷却し、得られた液をエバポレーターで減圧し、未反応の炭酸ジメチル、溶媒のメタノールを留去した。この時に得られた結晶は、白色の粉体結晶であり、収量は5.30gであった。生成物について、核磁気共鳴スペクトル(NMR)分析、質量スペクトル、元素分析、及び赤外吸収スペクトル(IR)分析を行った。その結果を以下に示す。
【0029】
NMR分析:1H−NMR(CDCl3) δ(ppm):3.52(s,3H)、3.27(s,9H)、3.36(s,3H)、2.05−2.07(d,6H)、1.71(m,6H)。
13C−NMR(CDCl3) δ(ppm):158.2,71.6,52.3,47.4,47.3,35.1,34.8,30.0。
【0030】
液体クロマトグラフィーによる質量分析 ESI法 (m/e):N,N,N−トリメチル−1−アダマンタンアンモニウム骨格の分子量 194.191(M+)。
【0031】
元素分析(測定値):C67.6,H10.3,N5.2
(理論値 :C66.9,H10.1,N5.2)。
【0032】
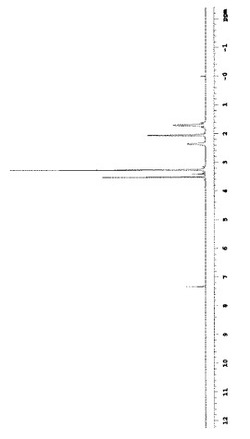
生成物のNMR分析を行った結果、N,N,−ジメチル−1−アミノアダマンタンを含有しておらず、転化率は100%であった。生成物の1H−NMRの測定結果を図1に示し、13C−NMRの測定結果を図2にを示す。また、生成物の液体クロマトグラフィーによる質量スペクトルを測定したところ、N,N,N−トリメチル−1−アダマンタンアンモニウム骨格の分子量(M+=194.191)が確認された。これらと元素分析の結果も本化合物の構造を支持しており、N,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートが98.4%の収率で得られたことを確認した。
【0033】
実施例2.
200mlオートクレーブに、N,N,−ジメチル−1−アミノアダマンタン17.93g(0.1mol)、炭酸ジメチル90.08g(1.0mol)を入れ、反応器内を窒素で置換した。反応器を密閉後、加熱攪拌し145℃まで昇温し、続けて同条件で5時間反応を行った。その際、反応時の圧力は10MPaを超えることはなかった。反応終了後に反応器を室温まで冷却し、得られたスラリー状物を窒素雰囲気下でろ過して白色の湿結晶を得た。
【0034】
この結晶はNMR分析の結果、N,N,−ジメチル−1−アミノアダマンタンを含有しておらず、N,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートが59.7%の収率で得られたことを確認した。
【図面の簡単な説明】
【0035】
【図1】実施例1で得られたN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートの1H−NMRスペクトル図である。
【図2】実施例1で得られたN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートの13C−NMRスペクトル図である。
【技術分野】
【0001】
本発明はN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートに関する。N,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートは、ゼオライトを製造する際の鋳型化合物として有用な新規な化合物である。
【背景技術】
【0002】
ゼオライトは、主としてアルミニウム源とケイ素源を含有する原料を水性合成ゲル中で反応させて結晶を形成させ、該結晶を成長させた後、乾燥させ、次いで焼成処理に付して細孔から水を除去することによって一般に得られる。その際、合成ゲル中において鋳型化合物を使用することにより、各種のゼオライトが設計されている。
【0003】
ゼオライトを製造するための鋳型化合物として、アダマンタン化合物を使用することは公知である。
【0004】
例えば、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物を用いてゼオライトSSZ−13が調製されている(例えば、特許文献1参照)。また、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物等を用いて種々のゼオライトが調製されている(例えば、特許文献2参照)。さらに、N,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物等を用いてゼオライトSSZ−23が調製されている(例えば、特許文献3参照)
これらのアダマンタン化合物の合成法としては、例えば、1−アミノアダマンタンにトリブチルアミン存在下で3倍モルのメチルヨウ化物を反応させてN,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物を得る方法が記載されている(例えば、特許文献1、特許文献2参照)。
【0005】
また、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物を酸化銀と水中で反応させてN,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物を得るる方法が記載されている(例えば、特許文献2参照)。
【0006】
さらに、N,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物をイオン交換樹脂を用いてイオン交換する方法によってN,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物を得る方法が記載されている(例えば、特許文献3参照)。
【0007】
しかしながら、これら従来の製法では、原料の1−アミノアダマンタン及び反応試薬として用いられるメチルヨウ化物が高価なため、得られるN,N,N−トリメチル−1−アダマンタンアンモニウムヨウ化物や、N,N,N−トリメチル−1−アダマンタンアンモニウム水酸化物をゼオライト製造用の工業的な原料として用いることは、経済的に不利である。
【0008】
したがって、工業的にゼオライトを製造する際の鋳型化合物として、簡便な製法を用いて高収率で容易に得られるN,N,N−トリメチルアダマンタンアンモニウム塩が望まれていた。
【発明の開示】
【発明が解決しようとする課題】
【0009】
本発明は、前記の背景技術に鑑みてなされたものであり、その目的は、工業的にゼオライトを製造する際の鋳型化合物として、簡便な製法を用いて容易に得られるN,N,N−トリメチルアダマンタンアンモニウム塩を提供することである。
【0010】
【特許文献1】米国特許第4665110号明細書
【特許文献2】米国特許第4544538号明細書
【特許文献3】特公平06−11648号明細書
【課題を解決するための手段】
【0011】
本発明者らは前記の課題を解決するために鋭意検討した結果、N,N,−ジメチル−1−アミノアダマンタンと炭酸ジメチルから、新規なN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートを合成することが出来ることを見出し、本発明を完成するに至った。
【0012】
すなわち、本発明は、下記式(1)
【0013】
【化1】

で表されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートである。
【発明の効果】
【0014】
本発明の上記式(1)で表されるN,N,N−トリメチル−1−アダマンタンアンモニウム塩は、簡便な製法を用いて容易に得ることができるため、本発明は工業的に極めて有用である。
【0015】
以下、本発明を詳細に説明する。
【0016】
本発明の上記式(1)で示されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートは、例えば、N,N−ジメチル−1−アミノアダマンタンと炭酸ジメチルとの反応で合成することができる。
【0017】
上記の反応で使用されるN,N−ジメチル−1−アミノアダマンタンは、例えば、1−ハロゲン化アダマンタンとジメチルアミンを、触媒としてヨウ素の存在下で反応させることにより、簡便にかつ安価に得ることができる。
【0018】
上記の反応で使用される炭酸ジメチルの使用量は、特に限定するものではないが、N,N,−ジメチル−1−アミノアダマンタン1モル当たり、1〜20モルの範囲であることが好ましく、更に好ましくは1モル〜10モルの範囲である。1モル未満であると反応が化学量論的に進行せずに未反応のN,N,−ジメチル−1−アミノアダマンタンが残存し、20モル以上ではコスト的に不利である。
【0019】
上記したN,N−ジメチル−1−アミノアダマンタンと炭酸ジメチルとの反応は、無溶媒条件又は不活性溶媒存在下で実施される。反応に用いられる不活性溶媒としては、例えば、ペンタン、ヘキサン、ヘプタン、オクタン、ノナン、デカン、ウンデカン、ドデカン、トリデカン等の直鎖状脂肪族炭化水素類、ジメチルブタン、メチルペンタン、ジメチルペンタン、メチルヘキサン、トリメチルペンタン、ジメチルヘキサン、メチルヘプタン等の分岐状脂肪族炭化水素類、シクロペンタン、シクロヘキサン、シクロオクタン、メチルシクロペンタン、メチルシクロへキサン、メチルシクロヘプタン、メチルシクロオクタン、ジメチルシクロペンタン、ジメチルシクロヘキサン、ジメチルシクロヘプタン、ジメチルシクロオクタン、エチルシクロペンタン、エチルシクロヘキサン、エチルシクロヘプタン、エチルシクロオクタン等の環状脂肪族炭化水素類、ジメチルエーテル、ジエチルエーテル、n−プロピルエーテル、n−ブチルエーテル、n−ペンチルエーテル、n−ヘキシルエーテル、n−オクチルエーテル等の直鎖状脂肪族エーテル類、イソプロピルエーテル、イソブチルエーテル、ブチルメチルエーテル、ブチルエチルエーテル、sec−ブチルメチルエーテル、tert−ブチルメチルエーテル、tert−ブチルエチルエーテル等の分岐状脂肪族エーテル類、混合物として石油エーテル、石油ベンジン、リグロイン等、ジメチルスルホキサイド、ジエチルエーテル、DMF、HMPA等の極性溶媒、更には、メタノール、エタノール、n−プロパノール、n−ブタノール、n−ペンタノール、n−ヘプタノール、n−オクタノール、n−ノナノール、n−デカノール、n−ウンデカノール、n−ドデカノール、n−トリデカノール、n−テトラデカノール、n−ヘキサデカノール、n−オクタデカノール等の直鎖状一級アルコール類、2−メチル−1−プロパノール、2−メチル−1−ブタノール、3−メチル−1−ブタノール、2−エチル−1−ブタノール、4−メチル−1−ペンタノール、3−メチル−1−ペンタノール、3−メチル−1−ペンタノール、2−メチル−1−ペンタノール、2−メチル−3−ペンタノール、2,2−ジメチル−1−プロパノール、3,3−ジメチル−1−ブタノール、2−エチル−1−ブタノール、2−エチル−1−ヘキサノール、5−メチル−1−ヘキサノール、2,2,4−トリメチル−1−ペンタノール、2,4,4−トリメチル−1−ペンタノール、3,5−ジメチル−1−ヘキサノール、2−プロピル−1−ペンタノール、2−エチル−1−ヘキサノール、3,5,5−トリメチル−1−ヘキサノール、3,7−ジメチル−1−オクタノール、6−メチル−1−オクタノール等の分岐鎖状一級アルコール類、イソプロパノール、2−ブタノール、2−ペンタノール、2−ヘキサノール、2−ヘプタノール、2−オクタノール、2−ノナノール、2−デカノールブタノール、2−ウンデカノール、2−ドデカノール、2−トリデカノール、2−テトラデカノール、2−ヘキサデカノール、2−オクタデカノール、3−メチル−2−ブタノール、4−メチル−2−ペンタノール、3−メチル−2−ペンタノール、3,3−ジメチル−2−ブタノール、2,2−ジメチル−3−ペンタノール、2−メチル−3−ヘキサノール、2,4−ジメチル−3−ペンタノール、5−メチル−2−ヘキサノール、4,4−ジメチル−2−ペンタノール、6−メチル−2−ヘプタノール、4−メチル−3−ヘプタノール、2,6−ジメチル−4−ヘプタノール、2,6,8−トリメチル−4−ノナノール等の分岐状二級アルコール類、シクロヘキサノール、シクロヘプタノール、シクロブタノール、シクロペンタノール等の脂環式一級アルコール類、tert−ブタノール、2−メチル−2−ブタノール、3−メチル−3−ペンタノール、2,3−ジメチル−2−ブタノール、3−エチル−3−ペンタノール、2−メチル−2−ヘキサノール、2,3−ジメチル−3−ペンタノール、3−メチル−3−オクタノール、3,7−ジメチル−3−オクタノール等の三級アルコール類等が挙げられる。これらのうち、ジメチルスルホキサイド、ジエチルエーテル、THF、DMF、HMPA、メタノール、エタノール、n−プロパノール、2−プロパノールは、工業的に入手し易い極性溶媒であり反応溶媒として好ましい。これらの溶媒を単独で又は任意の割合で混合して使用しても良い。本発明においては、取り扱いの容易さと経済性から、それらの中でも特にメタノールが好ましい。
【0020】
上記の反応において、使用される溶媒量は、特に限定するものではないが、N,N,−ジメチルアミノアダマンタン1g当たり、通常0.1g〜100gの範囲、好ましくは0.5g〜2.0gの範囲である。溶媒量がN,N,−ジメチルアミノアダマンタン1g当たり0.1gよりも少ない量では、反応系が粘調になり、反応速度が低下するおそれがある。また、100g以上の量では、反応液が希薄となり、反応速度が低下するおそれがある。
【0021】
上記の反応において、加熱反応を行う際に、炭酸ジメチル及び低沸点のアルコールは揮発しやすいため、この場合には反応を密閉容器で行うことが望ましい。反応時の圧力は、特に限定するものではないが、常圧〜10MPaの範囲で十分である。
【0022】
上記の反応において、反応温度としては、特に限定するものではないが、50〜300℃の範囲が好ましく、更に好ましくは100〜200℃の範囲である。50℃よりも低い温度では、十分な反応速度が得られない場合があり、また、300℃を超える温度では、目的生成物の分解等も起こりやすくなるため好ましくない。
【0023】
上記の反応において、目的物の単離は、通常は生成した四級塩をろ過することで可能である。但し、反応が充分進行して原料のN,N,−ジメチル−1−アミノアダマンタンが残存していない場合は、反応後に得られた反応液から未反応の炭酸ジメチルと溶媒を留去することのみで直接目的物を得ることが出来る。
【実施例】
【0024】
以下に、本発明の詳細について実施例を用いて具体的に説明するが、本発明はそれらに限定して解釈されるものではない。なお、本実施例における生成物の収率は、1H−NMRにて確認した。
【0025】
なお、以下の実施例において、1H−NMR及び13C−NMRの測定は、Varian社製Gemini−200を使用した。
【0026】
また、液体クロマトグラフィーによる質量分析は、ブルカー・ダルトニクス社製、TOF−MS、microTOFを使用した(イオン源 ESI、測定モード 陽イオン)。
【0027】
調製例.
撹拌子を入れたステンレス製の30ml簡易耐圧容器に、1−ブロモアダマンタン1.0g(4.7mmol)、ヨウ素0.24g(0.93mmol)を入れ、反応器を窒素雰囲気下でドライアイスバスにつけて冷却した状態でボンベからジメチルアミンガスを通じてジメチルアミン9.6g(212mmol)を冷却捕集した。反応器を密閉後、オイルバスに漬け加温撹拌し180℃まで昇温し、続けて同条件で4時間反応を行った。尚、反応時の圧力は10Mpaを越えることはなかった。反応終了後に反応器を室温まで冷却し、得られたスラリー状物に48%苛性水溶液とジクロロメタンを加えて中和、抽出を行い、分液して得られた反応液についてガスクロマトグラフィー分析(内部標準法)を行った。その結果、1−ブロモアダマンタンの転化率は97.1%であり、N,N−ジメチル−1−アミノアダマンタンが収率91.6%で得られ、アダマンタン−1−オールが1.7%とアダマンタンが2.3%得られたことを確認した。
【0028】
実施例1.
攪拌子を入れたステンレス製の30ml簡易耐圧容器に、N,N,−ジメチル−1−アミノアダマンタン3.59g(20mmol)、炭酸ジメチル5.40g(60mmol)、メタノール2.92gを入れ、反応器内を窒素で置換した。反応器を密閉後、オイルバスに漬けて加熱攪拌し145℃まで昇温し、続けて同条件で10時間反応を行った。反応終了後に反応器を室温まで冷却し、得られた液をエバポレーターで減圧し、未反応の炭酸ジメチル、溶媒のメタノールを留去した。この時に得られた結晶は、白色の粉体結晶であり、収量は5.30gであった。生成物について、核磁気共鳴スペクトル(NMR)分析、質量スペクトル、元素分析、及び赤外吸収スペクトル(IR)分析を行った。その結果を以下に示す。
【0029】
NMR分析:1H−NMR(CDCl3) δ(ppm):3.52(s,3H)、3.27(s,9H)、3.36(s,3H)、2.05−2.07(d,6H)、1.71(m,6H)。
13C−NMR(CDCl3) δ(ppm):158.2,71.6,52.3,47.4,47.3,35.1,34.8,30.0。
【0030】
液体クロマトグラフィーによる質量分析 ESI法 (m/e):N,N,N−トリメチル−1−アダマンタンアンモニウム骨格の分子量 194.191(M+)。
【0031】
元素分析(測定値):C67.6,H10.3,N5.2
(理論値 :C66.9,H10.1,N5.2)。
【0032】
生成物のNMR分析を行った結果、N,N,−ジメチル−1−アミノアダマンタンを含有しておらず、転化率は100%であった。生成物の1H−NMRの測定結果を図1に示し、13C−NMRの測定結果を図2にを示す。また、生成物の液体クロマトグラフィーによる質量スペクトルを測定したところ、N,N,N−トリメチル−1−アダマンタンアンモニウム骨格の分子量(M+=194.191)が確認された。これらと元素分析の結果も本化合物の構造を支持しており、N,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートが98.4%の収率で得られたことを確認した。
【0033】
実施例2.
200mlオートクレーブに、N,N,−ジメチル−1−アミノアダマンタン17.93g(0.1mol)、炭酸ジメチル90.08g(1.0mol)を入れ、反応器内を窒素で置換した。反応器を密閉後、加熱攪拌し145℃まで昇温し、続けて同条件で5時間反応を行った。その際、反応時の圧力は10MPaを超えることはなかった。反応終了後に反応器を室温まで冷却し、得られたスラリー状物を窒素雰囲気下でろ過して白色の湿結晶を得た。
【0034】
この結晶はNMR分析の結果、N,N,−ジメチル−1−アミノアダマンタンを含有しておらず、N,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートが59.7%の収率で得られたことを確認した。
【図面の簡単な説明】
【0035】
【図1】実施例1で得られたN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートの1H−NMRスペクトル図である。
【図2】実施例1で得られたN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネートの13C−NMRスペクトル図である。
【特許請求の範囲】
【請求項1】
下記式(1)
【化1】

で表されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネート。
【請求項1】
下記式(1)
【化1】

で表されるN,N,N−トリメチル−1−アダマンタンアンモニウムメチルカーボネート。
【図1】


【図2】




【図2】


【公開番号】特開2010−116349(P2010−116349A)
【公開日】平成22年5月27日(2010.5.27)
【国際特許分類】
【出願番号】特願2008−290888(P2008−290888)
【出願日】平成20年11月13日(2008.11.13)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
【公開日】平成22年5月27日(2010.5.27)
【国際特許分類】
【出願日】平成20年11月13日(2008.11.13)
【出願人】(000003300)東ソー株式会社 (1,901)
【Fターム(参考)】
[ Back to top ]

