新規カチオン性脂質を含む方法及び組成物
本発明は、新規カチオン性脂質、カチオン性脂質を含む組成物、及びカチオン性脂質を使用する方法を提供する。幾つかの請求項において、カチオン性脂質は細胞毒性活性を有し、細胞を殺すために、単独に又は細胞毒性生物活性化合物と組み合わせて使用することができる。これらの請求項の幾つかにおいて、カチオン性脂質は、細胞毒性生物活性化合物の細胞毒性活性を亢進する。疾患又は迷惑な病態に悩む患者を治療する方法を提供するが、この方法は患者への新規カチオン性脂質を含む輸送システムの投与を含むことを特徴とする。本発明は更に、本発明の新規カチオン性脂質を含む輸送システムを作成する方法を提供する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
下記化学式(I)で表されるカチオン性脂質、又はその医薬的に許容された塩。
【化1】

式中、m及びnは、それぞれ独立して、1〜8の整数を表し、R1及びR2は、それぞれ独立して、−(CH2)p−CH3(式中、pは8〜24の整数を表す。)を表し、R3及びR4は、それぞれ独立して、水素原子、アルキル基及び置換アルキル基から成る群から選択され、Q1及びQ2は、
【化2】

から成る群から選択され、但し、少なくともQ1及びQ2のいずれかは
【化3】

である。
【請求項2】
mが2であり、nが4であり、pが13であり、R3及びR4が各々メチル基であり、かつ前記化学式(I)で表されるカチオン性脂質が
【化4】

【化5】

及び
【化6】

から成る群から選択される請求項1に記載のカチオン性脂質。
【請求項3】
mが2であり、nが3であり、pが17であり、R3が水素原子であり、R4がメチル基であり、Q1及びQ2が
【化7】

であり、かつ前記化学式(I)で表されるカチオン性脂質が下記化学構造
【化8】

を有する請求項1に記載のカチオン性脂質。
【請求項4】
mが2であり、nが4であり、pが17であり、R3及びR4がそれぞれメチル基であり、Q1及びQ2が
【化7】

であり、かつ前記化学式(I)で表されるカチオン性脂質が下記化学構造
【化9】

を有する請求項1に記載のカチオン性脂質。
【請求項5】
前記カチオン性脂質が細胞毒性活性を有する請求項1〜4のいずれか一項に記載のカチオン性脂質。
【請求項6】
請求項5に記載のカチオン性脂質及び医薬的に許容された担体から成る医薬組成物。
【請求項7】
脂質媒体及び生物活性化合物から成る輸送システムであって、該脂質媒体が該生物活性化合物を包み込み、該脂質媒体が請求項1〜5のいずれか一項に記載のカチオン性脂質から成る輸送システム。
【請求項8】
前記脂質媒体が共脂質(co-lipid)を含む請求項7に記載の輸送システム。
【請求項9】
前記共脂質がコレステロール又はジオレオイル−ホスファチジルエタノールアミン(DOPE)から成る請求項8に記載の輸送システム。
【請求項10】
前記脂質媒体がリポソームから成る請求項7に記載の輸送システム。
【請求項11】
前記リポソームがカチオン性リポソームから成る請求項10に記載の輸送システム。
【請求項12】
更に、更にポリカチオンを含む請求項7〜11のいずれか一項に記載の輸送システムであって、前記脂質媒体が該ポリカチオンを包み込む輸送システム。
【請求項13】
前記ポリカチオンがポリカチオン性ポリペプチドから成る請求項12に記載の輸送システム。
【請求項14】
前記ポリカチオン性ポリペプチドがプロタミンから成る請求項13に記載の輸送システム。
【請求項15】
前記生物活性化合物が細胞毒性生物活性化合物から成る請求項7〜14のいずれか一項に記載の輸送システム。
【請求項16】
前記生物活性化合物がポリヌクレオチドから成る請求項7〜14のいずれか一項に記載の輸送システム。
【請求項17】
前記ポリヌクレオチドがサイレンサー配列を含み、このサイレンサー配列の細胞内での発現又は細胞内への導入が、標的ポリヌクレオチド又はそれにコード化されたポリペプチドの発現を減少させる請求項16に記載の輸送システム。
【請求項18】
前記サイレンサー配列が干渉RNAから成る請求項17に記載の輸送システム。
【請求項19】
前記干渉RNAがsiRNAから成る請求項18に記載の輸送システム。
【請求項20】
前記標的ポリヌクレオチドが腫瘍遺伝子を含む請求項17に記載の輸送システム。
【請求項21】
前記腫瘍遺伝子が表皮成長因子受容体を含む請求項20に記載の輸送システム。
【請求項22】
前記ポリヌクレオチドが興味の対象となるポリペプチドのコード配列を含む請求項16に記載の輸送システム。
【請求項23】
前記興味の対象となるポリペプチドが腫瘍抑制因子を含む請求項22に記載の輸送システム。
【請求項24】
更にポリアニオン性担体巨大分子を含む請求項7〜23のいずれか一項に記載の輸送システムであって、該ポリアニオン性担体巨大分子が前記脂質媒体に包み込まれる輸送システム。
【請求項25】
前記ポリアニオン性担体巨大分子が担体ポリヌクレオチドから成る請求項24に記載の輸送システム。
【請求項26】
前記ポリアニオン性担体巨大分子がポリアニオン性担体ポリサッカライド、ポリアニオン性担体ポリペプチド又はこの組合せから成る請求項24に記載の輸送システム。
【請求項27】
前記ポリアニオン性担体ポリサッカライドがグリコサミノグリカンから成る請求項26に記載の輸送システム。
【請求項28】
前記グリコサミノグリカンが、ヘパリン硫酸、ヒアルロン酸、コンドロイチン硫酸、デルマチン硫酸、ケラタン硫酸、及びデキストラン硫酸から成る群から選択される請求項27に記載の輸送システム。
【請求項29】
前記グリコサミノグリカンがヒアルロン酸から成る請求項28に記載の輸送システム。
【請求項30】
前記ポリアニオン性担体ポリペプチドが、ポリグルタミン酸又はポリアスパラギン酸から成る請求項26に記載の輸送システム。
【請求項31】
前記脂質媒体が外部表面を有し、該外部表面がポリエチレングリコール(PEG)分子を含む請求項7〜30のいずれか一項に記載の輸送システム。
【請求項32】
前記脂質媒体が担持2重層を含む請求項7〜31のいずれか一項に記載の輸送システム。
【請求項33】
前記輸送システムがステルス輸送システムから成る請求項31又は32に記載の輸送システム。
【請求項34】
前記輸送システムの前記脂質媒体が外部表面を有し、該外部表面が向標的リガンドを含み、それによって、前記向標的リガンドが、前記標的輸送システムをして標的細胞を標的として狙わせる標的輸送システムを形成する請求項7〜33のいずれか一項に記載の輸送システム。
【請求項35】
前記向標的リガンドがベンズアミド誘導体から成る請求項35に記載の輸送システム。
【請求項36】
前記ベンズアミド誘導体がアニサミドから成る請求項35に記載の輸送システム。
【請求項37】
前記アニサミド(AA)が、1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン-N-カルボキシ-ポリエチレングリコール(DSPE-PEG)と接合して、DSPE-PEG-AAを生成する請求項36に記載の輸送システム。
【請求項38】
前記標的細胞が癌細胞から成る請求項34〜37のいずれか一項に記載の輸送システム。
【請求項39】
前記癌細胞が膀胱癌、脳腫瘍、乳癌、子宮頸癌、結腸直腸癌、食道癌、子宮内膜癌、肝臓癌、咽頭癌、肺癌、骨肉腫、卵巣癌、膵臓癌、前立腺癌、腎臓癌、及び甲状腺癌から成る群から選択される請求項38に記載の輸送システム。
【請求項40】
前記癌細胞が肺癌から成る請求項39に記載の輸送システム。
【請求項41】
請求項7〜40のいずれか一項に記載の輸送システム及び医薬的に許容される担体から成る医薬組成物。
【請求項42】
細胞に生物活性化合物を輸送する方法であって、請求項7〜40のいずれか一項に記載の輸送システムに細胞を接触させることから成る方法。
【請求項43】
細胞を殺す方法であって、請求項5に記載のカチオン性脂質に細胞を接触させることから成る方法。
【請求項44】
細胞を殺す方法であって、請求項7〜40のいずれか一項に記載の輸送システムに細胞を接触させることから成り、前記カチオン性脂質が細胞毒性活性を有する方法。
【請求項45】
選択的に細胞を殺す方法であって、細胞を脂質−向標的リガンド接合体に接触させることから成り、該脂質−向標的リガンド接合体が請求項5に記載のカチオン性脂質から成り、該カチオン性脂質が向標的リガンドと物理的に会合する方法。
【請求項46】
選択的に細胞を殺す方法であって、細胞を標的輸送システムに接触させることから成り、該標的輸送システムが生物活性化合物を包み込む脂質媒体から成り、該脂質媒体が請求項5に記載のカチオン性脂質を含み、該脂質媒体が外部表面を有し、該外部表面が向標的リガンドを含む方法。
【請求項47】
前記生物活性化合物が細胞毒性生物活性化合物を含む請求項46に記載の方法。
【請求項48】
前記向標的リガンドがベンズアミド誘導体を含む請求項45〜47のいずれか一項に記載の方法。
【請求項49】
前記ベンズアミド誘導体がアニサミドから成る請求項48に記載の方法。
【請求項50】
患者の癌を治療する方法であって、該患者に請求項6に記載の医薬組成物を投与することから成る方法。
【請求項51】
患者の疾患又は迷惑な病態を治療する方法であって、該患者に請求項41に記載の医薬組成物を投与することから成り、前記生物活性化合物が該疾患又は迷惑な病態に対して治療活性を持つ方法。
【請求項52】
前記疾患が癌を含む請求項51に記載の方法。
【請求項53】
前記癌が肺癌から成る請求項50又は52に記載の方法。
【請求項54】
患者における細胞毒性生物活性化合物の細胞毒性活性を亢進する方法であって、患者に請求項6に記載の医薬組成物及び該細胞毒性生物活性化合物を投与することから成る方法。
【請求項55】
患者における細胞毒性生物活性化合物の細胞毒性活性を亢進する方法であって、患者に請求項41に記載の医薬組成物を投与することから成り、患者への請求項41に記載の医薬組成物の投与することから成り、該輸送システムの前記カチオン性脂質及び前記生物活性化合物が細胞毒性活性を有する方法。
【請求項56】
脂質媒体及び生物活性化合物から成り、該脂質媒体が該生物活性化合物を包み込む細胞毒性輸送システムを作成する方法であって、請求項5に記載のカチオン性脂質を含む脂質媒体と生物活性化合物とを混合することから成り、それにより細胞毒性輸送システムが形成される方法。
【請求項57】
前記生物活性化合物が細胞毒性生物活性化合物を含む請求項56に記載の方法。
【請求項58】
ポリカチオン及びポリヌクレオチドを包み込む脂質媒体から成る細胞毒性ポリヌクレオチド輸送システムを作成する方法であって、
a)ポリヌクレオチド及びポリカチオンを混合し、それによりポリヌクレオチド/ポリカチオン溶液を作成する工程、及び
b)請求項5の記載のカチオン性脂質から成る脂質媒体とこのポリヌクレオチド/ポリカチオン溶液とを混合し、それにより細胞毒性輸送システムを作成する工程、
から成る方法。
【請求項59】
ポリカチオン及びポリヌクレオチドを包み込む脂質媒体から成る細胞毒性ポリヌクレオチド輸送システムを作成する方法であって、
a)請求項5の記載のカチオン性脂質から成る脂質媒体とポリカチオンとを混合し、それにより脂質媒体/ポリカチオン溶液を作成する工程、及び
b)この脂質媒体/ポリカチオン溶液とポリヌクレオチドとを混合し、それにより細胞毒性輸送システムを作成する工程、
から成る方法。
【請求項60】
前記ポリヌクレオチドが細胞毒性ポリヌクレオチドから成る請求項58又は59に記載の方法。
【請求項61】
前記工程b)がコア担持2重層から成る含む脂質媒体を作成する工程を含む請求項58又は59に記載の方法。
【請求項62】
前記脂質媒体がリポソームから成る請求項56〜61のいずれか一項に記載の方法。
【請求項63】
前記リポソームがカチオン性リポソームから成る請求項62に記載の方法。
【請求項64】
更に、後挿入工程を含む請求項56〜63のいずれか一項に記載の方法であって、この後挿入工程において、脂質−向標的リガンド接合体及び脂質−PEG接合体の少なくとも1つが、前記脂質媒体に後挿入され、この後挿入工程が、前記輸送システム又は前記ポリヌクレオチド輸送システムを形成した後に行われる方法。
【請求項65】
前記細胞毒性輸送システム又は前記細胞毒性ポリヌクレオチド輸送システムが、ステルス細胞毒性輸送システム、又はステルス細胞毒性ポリヌクレオチド輸送システムから成る請求項64に記載の方法。
【請求項66】
前記後挿入工程が、前記輸送システム又は前記ポリヌクレオチド輸送システムを約5〜約20モル%の濃度の脂質−PEG接合体と共にインキュベートする工程から成る請求項64又は65に記載の方法。
【請求項67】
前記脂質−PEG接合体の濃度が約10モル%である請求項66に記載の方法。
【請求項68】
前記脂質−PEG接合体が、分子量が約2000g/molのPEG分子を含む請求項64〜67のいずれか一項に記載の方法。
【請求項69】
前記脂質−PEG接合体が1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン-N-カルボキシ−ポリエチレングリコール2000 (DSPE-PEG2000)を含む請求項68に記載の方法。
【請求項1】
下記化学式(I)で表されるカチオン性脂質、又はその医薬的に許容された塩。
【化1】

式中、m及びnは、それぞれ独立して、1〜8の整数を表し、R1及びR2は、それぞれ独立して、−(CH2)p−CH3(式中、pは8〜24の整数を表す。)を表し、R3及びR4は、それぞれ独立して、水素原子、アルキル基及び置換アルキル基から成る群から選択され、Q1及びQ2は、
【化2】

から成る群から選択され、但し、少なくともQ1及びQ2のいずれかは
【化3】

である。
【請求項2】
mが2であり、nが4であり、pが13であり、R3及びR4が各々メチル基であり、かつ前記化学式(I)で表されるカチオン性脂質が
【化4】

【化5】

及び
【化6】

から成る群から選択される請求項1に記載のカチオン性脂質。
【請求項3】
mが2であり、nが3であり、pが17であり、R3が水素原子であり、R4がメチル基であり、Q1及びQ2が
【化7】

であり、かつ前記化学式(I)で表されるカチオン性脂質が下記化学構造
【化8】

を有する請求項1に記載のカチオン性脂質。
【請求項4】
mが2であり、nが4であり、pが17であり、R3及びR4がそれぞれメチル基であり、Q1及びQ2が
【化7】

であり、かつ前記化学式(I)で表されるカチオン性脂質が下記化学構造
【化9】

を有する請求項1に記載のカチオン性脂質。
【請求項5】
前記カチオン性脂質が細胞毒性活性を有する請求項1〜4のいずれか一項に記載のカチオン性脂質。
【請求項6】
請求項5に記載のカチオン性脂質及び医薬的に許容された担体から成る医薬組成物。
【請求項7】
脂質媒体及び生物活性化合物から成る輸送システムであって、該脂質媒体が該生物活性化合物を包み込み、該脂質媒体が請求項1〜5のいずれか一項に記載のカチオン性脂質から成る輸送システム。
【請求項8】
前記脂質媒体が共脂質(co-lipid)を含む請求項7に記載の輸送システム。
【請求項9】
前記共脂質がコレステロール又はジオレオイル−ホスファチジルエタノールアミン(DOPE)から成る請求項8に記載の輸送システム。
【請求項10】
前記脂質媒体がリポソームから成る請求項7に記載の輸送システム。
【請求項11】
前記リポソームがカチオン性リポソームから成る請求項10に記載の輸送システム。
【請求項12】
更に、更にポリカチオンを含む請求項7〜11のいずれか一項に記載の輸送システムであって、前記脂質媒体が該ポリカチオンを包み込む輸送システム。
【請求項13】
前記ポリカチオンがポリカチオン性ポリペプチドから成る請求項12に記載の輸送システム。
【請求項14】
前記ポリカチオン性ポリペプチドがプロタミンから成る請求項13に記載の輸送システム。
【請求項15】
前記生物活性化合物が細胞毒性生物活性化合物から成る請求項7〜14のいずれか一項に記載の輸送システム。
【請求項16】
前記生物活性化合物がポリヌクレオチドから成る請求項7〜14のいずれか一項に記載の輸送システム。
【請求項17】
前記ポリヌクレオチドがサイレンサー配列を含み、このサイレンサー配列の細胞内での発現又は細胞内への導入が、標的ポリヌクレオチド又はそれにコード化されたポリペプチドの発現を減少させる請求項16に記載の輸送システム。
【請求項18】
前記サイレンサー配列が干渉RNAから成る請求項17に記載の輸送システム。
【請求項19】
前記干渉RNAがsiRNAから成る請求項18に記載の輸送システム。
【請求項20】
前記標的ポリヌクレオチドが腫瘍遺伝子を含む請求項17に記載の輸送システム。
【請求項21】
前記腫瘍遺伝子が表皮成長因子受容体を含む請求項20に記載の輸送システム。
【請求項22】
前記ポリヌクレオチドが興味の対象となるポリペプチドのコード配列を含む請求項16に記載の輸送システム。
【請求項23】
前記興味の対象となるポリペプチドが腫瘍抑制因子を含む請求項22に記載の輸送システム。
【請求項24】
更にポリアニオン性担体巨大分子を含む請求項7〜23のいずれか一項に記載の輸送システムであって、該ポリアニオン性担体巨大分子が前記脂質媒体に包み込まれる輸送システム。
【請求項25】
前記ポリアニオン性担体巨大分子が担体ポリヌクレオチドから成る請求項24に記載の輸送システム。
【請求項26】
前記ポリアニオン性担体巨大分子がポリアニオン性担体ポリサッカライド、ポリアニオン性担体ポリペプチド又はこの組合せから成る請求項24に記載の輸送システム。
【請求項27】
前記ポリアニオン性担体ポリサッカライドがグリコサミノグリカンから成る請求項26に記載の輸送システム。
【請求項28】
前記グリコサミノグリカンが、ヘパリン硫酸、ヒアルロン酸、コンドロイチン硫酸、デルマチン硫酸、ケラタン硫酸、及びデキストラン硫酸から成る群から選択される請求項27に記載の輸送システム。
【請求項29】
前記グリコサミノグリカンがヒアルロン酸から成る請求項28に記載の輸送システム。
【請求項30】
前記ポリアニオン性担体ポリペプチドが、ポリグルタミン酸又はポリアスパラギン酸から成る請求項26に記載の輸送システム。
【請求項31】
前記脂質媒体が外部表面を有し、該外部表面がポリエチレングリコール(PEG)分子を含む請求項7〜30のいずれか一項に記載の輸送システム。
【請求項32】
前記脂質媒体が担持2重層を含む請求項7〜31のいずれか一項に記載の輸送システム。
【請求項33】
前記輸送システムがステルス輸送システムから成る請求項31又は32に記載の輸送システム。
【請求項34】
前記輸送システムの前記脂質媒体が外部表面を有し、該外部表面が向標的リガンドを含み、それによって、前記向標的リガンドが、前記標的輸送システムをして標的細胞を標的として狙わせる標的輸送システムを形成する請求項7〜33のいずれか一項に記載の輸送システム。
【請求項35】
前記向標的リガンドがベンズアミド誘導体から成る請求項35に記載の輸送システム。
【請求項36】
前記ベンズアミド誘導体がアニサミドから成る請求項35に記載の輸送システム。
【請求項37】
前記アニサミド(AA)が、1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン-N-カルボキシ-ポリエチレングリコール(DSPE-PEG)と接合して、DSPE-PEG-AAを生成する請求項36に記載の輸送システム。
【請求項38】
前記標的細胞が癌細胞から成る請求項34〜37のいずれか一項に記載の輸送システム。
【請求項39】
前記癌細胞が膀胱癌、脳腫瘍、乳癌、子宮頸癌、結腸直腸癌、食道癌、子宮内膜癌、肝臓癌、咽頭癌、肺癌、骨肉腫、卵巣癌、膵臓癌、前立腺癌、腎臓癌、及び甲状腺癌から成る群から選択される請求項38に記載の輸送システム。
【請求項40】
前記癌細胞が肺癌から成る請求項39に記載の輸送システム。
【請求項41】
請求項7〜40のいずれか一項に記載の輸送システム及び医薬的に許容される担体から成る医薬組成物。
【請求項42】
細胞に生物活性化合物を輸送する方法であって、請求項7〜40のいずれか一項に記載の輸送システムに細胞を接触させることから成る方法。
【請求項43】
細胞を殺す方法であって、請求項5に記載のカチオン性脂質に細胞を接触させることから成る方法。
【請求項44】
細胞を殺す方法であって、請求項7〜40のいずれか一項に記載の輸送システムに細胞を接触させることから成り、前記カチオン性脂質が細胞毒性活性を有する方法。
【請求項45】
選択的に細胞を殺す方法であって、細胞を脂質−向標的リガンド接合体に接触させることから成り、該脂質−向標的リガンド接合体が請求項5に記載のカチオン性脂質から成り、該カチオン性脂質が向標的リガンドと物理的に会合する方法。
【請求項46】
選択的に細胞を殺す方法であって、細胞を標的輸送システムに接触させることから成り、該標的輸送システムが生物活性化合物を包み込む脂質媒体から成り、該脂質媒体が請求項5に記載のカチオン性脂質を含み、該脂質媒体が外部表面を有し、該外部表面が向標的リガンドを含む方法。
【請求項47】
前記生物活性化合物が細胞毒性生物活性化合物を含む請求項46に記載の方法。
【請求項48】
前記向標的リガンドがベンズアミド誘導体を含む請求項45〜47のいずれか一項に記載の方法。
【請求項49】
前記ベンズアミド誘導体がアニサミドから成る請求項48に記載の方法。
【請求項50】
患者の癌を治療する方法であって、該患者に請求項6に記載の医薬組成物を投与することから成る方法。
【請求項51】
患者の疾患又は迷惑な病態を治療する方法であって、該患者に請求項41に記載の医薬組成物を投与することから成り、前記生物活性化合物が該疾患又は迷惑な病態に対して治療活性を持つ方法。
【請求項52】
前記疾患が癌を含む請求項51に記載の方法。
【請求項53】
前記癌が肺癌から成る請求項50又は52に記載の方法。
【請求項54】
患者における細胞毒性生物活性化合物の細胞毒性活性を亢進する方法であって、患者に請求項6に記載の医薬組成物及び該細胞毒性生物活性化合物を投与することから成る方法。
【請求項55】
患者における細胞毒性生物活性化合物の細胞毒性活性を亢進する方法であって、患者に請求項41に記載の医薬組成物を投与することから成り、患者への請求項41に記載の医薬組成物の投与することから成り、該輸送システムの前記カチオン性脂質及び前記生物活性化合物が細胞毒性活性を有する方法。
【請求項56】
脂質媒体及び生物活性化合物から成り、該脂質媒体が該生物活性化合物を包み込む細胞毒性輸送システムを作成する方法であって、請求項5に記載のカチオン性脂質を含む脂質媒体と生物活性化合物とを混合することから成り、それにより細胞毒性輸送システムが形成される方法。
【請求項57】
前記生物活性化合物が細胞毒性生物活性化合物を含む請求項56に記載の方法。
【請求項58】
ポリカチオン及びポリヌクレオチドを包み込む脂質媒体から成る細胞毒性ポリヌクレオチド輸送システムを作成する方法であって、
a)ポリヌクレオチド及びポリカチオンを混合し、それによりポリヌクレオチド/ポリカチオン溶液を作成する工程、及び
b)請求項5の記載のカチオン性脂質から成る脂質媒体とこのポリヌクレオチド/ポリカチオン溶液とを混合し、それにより細胞毒性輸送システムを作成する工程、
から成る方法。
【請求項59】
ポリカチオン及びポリヌクレオチドを包み込む脂質媒体から成る細胞毒性ポリヌクレオチド輸送システムを作成する方法であって、
a)請求項5の記載のカチオン性脂質から成る脂質媒体とポリカチオンとを混合し、それにより脂質媒体/ポリカチオン溶液を作成する工程、及び
b)この脂質媒体/ポリカチオン溶液とポリヌクレオチドとを混合し、それにより細胞毒性輸送システムを作成する工程、
から成る方法。
【請求項60】
前記ポリヌクレオチドが細胞毒性ポリヌクレオチドから成る請求項58又は59に記載の方法。
【請求項61】
前記工程b)がコア担持2重層から成る含む脂質媒体を作成する工程を含む請求項58又は59に記載の方法。
【請求項62】
前記脂質媒体がリポソームから成る請求項56〜61のいずれか一項に記載の方法。
【請求項63】
前記リポソームがカチオン性リポソームから成る請求項62に記載の方法。
【請求項64】
更に、後挿入工程を含む請求項56〜63のいずれか一項に記載の方法であって、この後挿入工程において、脂質−向標的リガンド接合体及び脂質−PEG接合体の少なくとも1つが、前記脂質媒体に後挿入され、この後挿入工程が、前記輸送システム又は前記ポリヌクレオチド輸送システムを形成した後に行われる方法。
【請求項65】
前記細胞毒性輸送システム又は前記細胞毒性ポリヌクレオチド輸送システムが、ステルス細胞毒性輸送システム、又はステルス細胞毒性ポリヌクレオチド輸送システムから成る請求項64に記載の方法。
【請求項66】
前記後挿入工程が、前記輸送システム又は前記ポリヌクレオチド輸送システムを約5〜約20モル%の濃度の脂質−PEG接合体と共にインキュベートする工程から成る請求項64又は65に記載の方法。
【請求項67】
前記脂質−PEG接合体の濃度が約10モル%である請求項66に記載の方法。
【請求項68】
前記脂質−PEG接合体が、分子量が約2000g/molのPEG分子を含む請求項64〜67のいずれか一項に記載の方法。
【請求項69】
前記脂質−PEG接合体が1,2-ジステアロイル-sn-グリセロ-3-ホスホエタノールアミン-N-カルボキシ−ポリエチレングリコール2000 (DSPE-PEG2000)を含む請求項68に記載の方法。
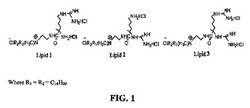
【図1】


【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図6A】


【図6B】


【図6C】


【図6D】


【図7】


【図8A】


【図8B】


【図9】


【図10】




【図2】


【図3】


【図4】


【図5A】


【図5B】


【図5C】


【図6A】


【図6B】


【図6C】


【図6D】


【図7】


【図8A】


【図8B】


【図9】


【図10】


【公表番号】特表2011−520962(P2011−520962A)
【公表日】平成23年7月21日(2011.7.21)
【国際特許分類】
【出願番号】特願2011−510547(P2011−510547)
【出願日】平成21年5月1日(2009.5.1)
【国際出願番号】PCT/US2009/042476
【国際公開番号】WO2009/142892
【国際公開日】平成21年11月26日(2009.11.26)
【出願人】(501345323)ザ ユニバーシティ オブ ノース カロライナ アット チャペル ヒル (52)
【氏名又は名称原語表記】THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL
【住所又は居所原語表記】308 Bynum Hall,Campus Box 4105,Chapel Hill,North Carolina 27599−4105, United States of America
【Fターム(参考)】
【公表日】平成23年7月21日(2011.7.21)
【国際特許分類】
【出願日】平成21年5月1日(2009.5.1)
【国際出願番号】PCT/US2009/042476
【国際公開番号】WO2009/142892
【国際公開日】平成21年11月26日(2009.11.26)
【出願人】(501345323)ザ ユニバーシティ オブ ノース カロライナ アット チャペル ヒル (52)
【氏名又は名称原語表記】THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL
【住所又は居所原語表記】308 Bynum Hall,Campus Box 4105,Chapel Hill,North Carolina 27599−4105, United States of America
【Fターム(参考)】
[ Back to top ]

