新規乳酸菌
【課題】 抗菌性物質を産生する新規な乳酸菌を提供する。
【解決手段】本発明は、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株(受託番号NITE P−1027)である。また、乳酸菌MSC007株の培養物である。さらに、該培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物である。そして、乳酸菌MSC007株を用いて発酵する工程を用いて製造された食品組成物である。該培養物及び/又は該抽出組成物を有効成分として含有することを特徴とする抗菌剤である。
【解決手段】本発明は、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株(受託番号NITE P−1027)である。また、乳酸菌MSC007株の培養物である。さらに、該培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物である。そして、乳酸菌MSC007株を用いて発酵する工程を用いて製造された食品組成物である。該培養物及び/又は該抽出組成物を有効成分として含有することを特徴とする抗菌剤である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、新規乳酸菌に関し、より詳細には、抗菌性物質を産生する新規乳酸菌に関する。
【背景技術】
【0002】
乳酸菌は、ヨーグルトの製造に用いられる等、これまで多くのものが知られている(例えば、特許文献1参照。)。
特許文献1に記載のように、「乳酸菌は様々な機能を有していることが知られており、その中でも抗菌作用は近年注目されてきている。乳酸菌が生産する抗菌性物質として、乳酸や酢酸などの有機酸、過酸化水素、ジアセチル、ロイテリン、バクテリオシンなどがある。その中でバクテリオシンは、一般に近縁のグラム陽性菌に対して抗菌作用を示すタンパク質性もしくはペプチド性の物質である。乳酸菌のバクテリオシンは、人間の消化酵素で分解消化されること、乳酸菌が古くから広く食品に利用されていて安全性が高いことなどから、精力的にその探索が実施されてきている。」(特許文献1、発明の詳細な説明中の段落番号0002〜0003)。
また、乳酸菌が生産するバクテリオシンとしては、ロイコノストック(Leuconostoc)属によって生産されたバクテリオシンを利用した食品用保存料が挙げられる(特許文献2参照)。しかしながら、この食品用保存料はバクテリオシンと有機酸およびその塩類等からなる化合物群との組み合わせによる相乗効果によって広い抗菌スペクトルを持たせようとしたものである。また、どのような菌種の細菌に対して抗菌効果を示したのかも明らかにされていない。
【0003】
また、本発明者は、以前から乳酸菌の研究に携わり、既に乳酸菌に関連する特許出願も行ってきた(例えば、特許文献3、特許文献4等)。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特許第4302476号公報
【特許文献2】特許第3040294号公報
【特許文献3】特開2007−236227号公報
【特許文献4】特開2006−76961号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
上述のように、乳酸菌が生産する抗菌性物質は有用であることから、抗菌性物質を産生する新規な乳酸菌を提供することを目的とする。
【課題を解決するための手段】
【0006】
本発明の本発明者らは、抗菌性物質を産生する新規な乳酸菌の探索を行なった結果、自然界や発酵食品に広く分布しているロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株が、ボツリヌス菌(Clostridium botulinum)A型、リステリア・モノサイトゲネス菌(Listeria monocytogenes)、ペディオコッカス・アシディラクチシ菌(Pediococcus acidilactici)、エンテロコッカス・フェカーリス菌(Enterococcus faecalis)及びラクトバチルス・デルブリュッキ菌(Lactobacillus delbrueckii subsp.lactis)等の菌に対して抗菌性を示す物質を産生することを見出し、本発明を完成させるに至った。
【0007】
即ち、本発明の乳酸菌株(以下、「本菌株」という。)は、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株(受託番号NITE P−1027)である。
本菌株(乳酸菌MSC007株、受託番号NITE P−1027)は、後述の如く、主としてグラム陽性菌に対して有効な抗菌性物質を産生する。
【0008】
本発明は、本菌株の培養物(以下、「本培養物」という。)も提供する。
本発明は、本培養物(本菌株の培養物)を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物(以下、「本抽出組成物」という。)も提供する。
本発明は、本菌株を用いて発酵する工程を用いて製造された食品組成物(以下、「本食品組成物」という。)も提供する。
本発明は、本培養物及び/又は本抽出組成物を有効成分として含有することを特徴とする抗菌剤(以下、「本抗菌剤」という。)も提供する。本抗菌剤は、食品、動物飼料及び洗浄剤よりなる群より選ばれる少なくとも1つの製品の保存剤として好適に使用できる。また、本抗菌剤は、pH10以下に調整されてもよい。
【図面の簡単な説明】
【0009】
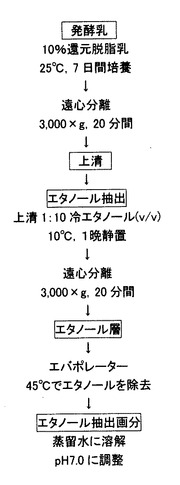
【図1】抗菌活性測定用の試験液の調製方法を示すフローチャートである。
【発明を実施するための形態】
【0010】
本発明の新規な乳酸菌株(本菌株)は、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株(受託番号NITE P−1027)である。
本菌株であるロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株(受託番号NITE P−1027)は、自然界や発酵食品に広く分布しているロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌から分離されたものである。
本菌株は、以下に示す菌学的性質を有する。これらの菌学的性質は、乳酸菌の科学と技術(学会出版センター、1996年)及びBergey’s Manual of Systematic Bacteriology, Second Edition(2009年)に記載の方法に準拠し検査した。
【表1】

【0011】
以上の特徴をBergey’s Manual of Systematic Bacteriology, Second Edition(2009年)を参照して近縁菌種を検索した結果、本菌株はロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)の特徴と一致した。
遺伝学的性質は以下の如くである。本菌株について16SrDNAの塩基配列500ベースペア(bp)を解読し、アポロンDB-BA5.0データベースで近縁菌種の相同性検索を行った結果、登録されているロイコノストック・メセンテロイデス・サブスピーシーズ・デキストラニカム(Leuconostoc mesenteroides subsp.dextranicum)NRIC1539株及びロイコノストック・メセンテロイデス・サブスピーシーズ・メセンテロイデス(Leuconostoc mesenteroides subsp.mesenteroides)NCDO523株の16SrDNAの塩基配列と100.0%の相同率を示した。また、国際塩基配列データベースではロイコノストック・メセンテロイデス・サブスピーシーズ・デキストラニカム(Leuconostoc mesenteroides subsp.dextranicum)QL2株及びロイコノストック・メセンテロイデス・サブスピーシーズ・メセンテロイデス(Leuconostoc mesenteroides subsp.mesenteroides)ATCC8293株の16SrDNAの塩基配列と100.0%の相同率を示した。
従って、本菌株をロイコノストック・メセンテロイデス( Leuconostoc mesenteroides)と同定した。
【0012】
このロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)MSC007株は、千葉県木更津市かずさ鎌足2−5−8に住所を有する独立行政法人製品評価技術基盤機構特許微生物寄託センター(NPMD)に平成23年1月6日(寄託日)付で上記名称(識別の表示:Leuconostoc mesenteroides MSC007)で寄託されており、受託番号はNITE P−1027である。
【0013】
本菌株乳酸菌MSC007株は、上述したように、天然に存する乳酸菌から分離されたものであり、本菌株乳酸菌MSC007株それ自身及びその培養物についてもヒトを含む動物に対する毒性はなく、ヒトを含む動物に対して経口摂取や皮膚への塗布を安全に行うことができる。
【0014】
本菌株乳酸菌MSC007株は、多くの菌に対する抗菌性物質を産生する。該抗菌性物質は、後に詳述する表2(MSC007の抗菌スペクトル)に示す通り、ボツリヌス菌(Clostridium botulinum)A型、リステリア・モノサイトゲネス菌(Listeria monocytogenes)、ペディオコッカス・アシディラクチシ菌(Pediococcus acidilactici)、エンテロコッカス・フェカーリス菌(Enterococcus faecalis)及びラクトバチルス・デルブリュッキ菌(Lactobacillus delbrueckii subsp.lactis)等のようなグラム陽性菌に対して特に有効な抗菌性を示す。
加えて、本菌株乳酸菌MSC007株は、pH7、80℃で15分間の処理条件下で熱安定性を示す。
そして、本菌株乳酸菌MSC007株が産生する抗菌性物質は、上述したグラム陽性菌に対して有効であると共に次のような特徴を有する。
(イ)プロテアーゼで消化される。
(ロ)pH10以下(例えば、pH2〜10)で安定性を示す。
【0015】
本菌株乳酸菌MSC007株の分離菌株の保存は、MRSブイヨンで培養した培養菌液を10%還元脱脂乳培地に0.5%量程度添加し、そのまま−20℃から−80℃で冷凍することで保存できる。
そして、使用にあたっては、菌株を含む保存物をMRSブイヨンに1%量程度添加し、25℃で24時間保つことで培養することができる。
本菌株乳酸菌MSC007株の培養に使用することのできる培地としては、本菌株が増殖し得るものであれば任意のものでよい。例えば、使用可能な培地としては、炭素源、窒素源、無機塩類、ビタミン、アミノ酸等を含む通常用いられる培地(液体培地、固体培地など)であるが、乳酸菌の培養に適する培地を用いてもよい。乳酸菌の培養に適する培地としては、例えば、MRSブイヨン、MRS寒天培地、BCP加プレートカウント培地、10%還元脱脂乳培地等が挙げられる。
本菌株乳酸菌MSC007株の培養は、とくに嫌気的条件下で行う必要はなく、通常の好気的条件下で培養することができる。培養条件は特に限定はないが、温度は20〜30℃、pHは6〜7、培養時間は1〜7日間の範囲とされてもよい。
【0016】
本培養物は、本菌株ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株(受託番号NITE P−1027)の培養物である。
本菌株乳酸菌MSC007株の培養は、上述したような条件下にて行うことができ、その培養物(本培養物)は本菌株乳酸菌MSC007株が産生する前記の抗菌性物質を含有する。従って、本培養物自身も、それが含有する該抗菌性物質に基づく抗菌性を有する。
また、本培養物としては、本菌株を液状または固形培地で培養した培養物全体を用いることもできるが、必要に応じて培養物の一部を分取した分取物としてもよい。分取物としては、培養液(菌体含有)、コロニー、培養上清(菌体不含)等を例示できる。そして、本培養物として培養上清を用いる場合には、培養液から菌体を遠心分離等によって分離し、培養上清液のpHを炭酸ナトリウム、水酸化ナトリウム、水酸化カリウム等によりpHを10以下に調整(例えば、pH2〜10程度)して、本抗菌剤として利用することもできる。更に、培養上清液の粗精製物を本抗菌剤として用いることもでき、この粗精製物は、例えば、培養上清液をイオン交換、限外濾過、逆浸透、ゲル濾過等の方法で抗菌活性を有する画分を取得することで調製することもできる。
【0017】
本抽出組成物は、本培養物(本菌株の培養物)を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物である。
本培養物に含まれる前記抗菌性物質は、本培養物と炭素数1〜3のアルコールとを接触させると、アルコール層に抽出されるので、本培養物からアルコール層に抽出される抽出画分を含む本抽出組成物は前記抗菌性物質を含有する。
従って、本抽出組成物も、それが含有する前記抗菌性物質に基づく抗菌性を有する。
ここに用いる炭素数1〜3のアルコールとしては、メチルアルコール、エチルアルコール、n−プロピルアルコール、イソプロピルアルコールを例示できるが、本抽出組成物に残留する場合の低毒性を考慮すれば、エチルアルコールが好ましい。
また、炭素数1〜3のアルコールを接触させ抽出する本培養物としては、本乳酸菌株を培養した培養物そのものでもよいが、本培養物に含まれる前記抗菌性物質は本培養物を遠心分離や静置分離した際に得られる上清に含まれるので、本培養物を遠心分離や静置分離して生じる上清を該アルコール層と接触させるようにしてもよい。
【0018】
本抽出組成物は、本培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られるものであり、本培養物から抽出された前記抗菌性物質を含有するアルコール層は、本抽出組成物中にアルコールが含まれてもよい場合には、アルコールを留去せず、そのままアルコールを含んだ状態の本抽出組成物としてもよい。そして、本培養物から抽出された前記抗菌性物質を含有するアルコール層は、それが含有するアルコールの一部又は全部を留去したり、及び/又は、それが含有する水分の一部又は全部を留去して本抽出組成物としてもよい。さらに、本培養物から抽出された前記抗菌性物質を含有するアルコール層は、乾燥固化して本抽出組成物としてもよい。
また、本抽出組成物は、水に安定して溶解するので、水溶液としておくこともできる。本抽出組成物に含まれる前記抗菌性物質はpH10以下で安定した抗菌性を発揮するのでpH10以下(例えば、pH=2〜10)の水溶液としてもよい。
【0019】
本抽出組成物は、上述の通り、本培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られるものであればよく何ら限定されるものではないが、例えば、本培養物にエチルアルコールを接触させる接触ステップと、接触ステップにより培養物と接触したエチルアルコール層を回収する回収ステップと、回収ステップにより回収されたエチルアルコール層のエチルアルコールを留去し抽出組成物とする留去ステップと、を含んでなる製造方法により製造されうる。
【0020】
接触ステップでは、本培養物にエチルアルコールを接触させる。
接触ステップにおける本培養物(体積)に対するエチルアルコール(体積)の比率(エチルアルコール(体積)/本培養物(体積))は、あまり小さいと前記抗菌性物質がエチルアルコール層に十分抽出されず、逆にあまり多いとエチルアルコール層が多すぎて回収ステップや留去ステップを実施することが大変になるため、これらを両立する範囲とされてもよく、特に限定されるものではないが、通常、1〜10とされてもよい。また、接触ステップにおける本培養物及びエチルアルコールの温度は、あまり低いと凍結により前記抗菌性物質がエチルアルコール層に十分抽出されない恐れがあり、逆にあまり高いと前記抗菌性物質が変性を起こす恐れが生じるので、これらを両立する範囲とされてもよく、特に限定されるものではないが、通常、1℃〜15℃とされてもよい。そして、接触ステップにおける本培養物及びエチルアルコールの接触時間は、あまり短いと前記抗菌性物質がエチルアルコール層に十分抽出されず、逆にあまり長いと時間がかかりすぎるので、これらを両立する範囲とされてもよく、特に限定されるものではないが、通常、4時間〜24時間とされてもよい。
また、接触ステップにおいてエチルアルコール層と接触させる本培養物としては、本乳酸菌株を培養した培養物そのものでもよいが、本培養物に含まれる前記抗菌性物質は本培養物を遠心分離や静置分離した際に得られる上清に含まれるので、本培養物を遠心分離や静置分離して生じる上清を接触ステップにおいてエチルアルコール層と接触させるようにしてもよい。
【0021】
回収ステップでは、接触ステップにより培養物と接触したエチルアルコール層を回収する。
接触ステップにおいて培養物と接触したエチルアルコール層は、培養物層とは液−液分離するので比重差を利用して遠心分離や静置分離の後に、分液することでエチルアルコール層を回収できる(上層に透明なエチルアルコール層、下層に白色の培養物層が形成される)。かかるエチルアルコール層には、本菌株が産生する前記の抗菌性物質が含まれている。
【0022】
留去ステップでは、回収ステップにより回収されたエチルアルコール層のエチルアルコールを留去し本抽出組成物とする。
回収ステップで回収されたエチルアルコール層からエチルアルコールを留去するには、エチルアルコールを蒸発させ除去すればよく、常圧下又は減圧下でエチルアルコールを蒸発除去してもよい(前記抗菌性物質を含む本抽出組成物が高温により劣化することを防止又は減少させることからは減圧下で行うようにしてもよい。)。
また、本抽出組成物中にエチルアルコールが含まれてもよい場合には、エチルアルコールを完全に留去せず、エチルアルコールを含んだ状態の本抽出組成物としてもよい。
本抽出組成物は、水に安定して溶解するので、水溶液としておくこともできる。本抽出組成物に含まれる前記抗菌性物質はpH10以下で安定した抗菌性を発揮するのでpH10以下(例えば、pH=2〜10)の水溶液としてもよい。
【0023】
本食品組成物は、本菌株を用いて発酵する工程を用いて製造された食品組成物である。
本菌株乳酸菌MSC007株は、本菌株が属する乳酸菌株及び前記抗菌性物質の特徴に基づき、特に食品分野へ好適に用いることが可能である。即ち、本菌株は、本菌株を用いて発酵原料を発酵する工程を用いて発酵食品を製造するために使用することができる。なお、本菌株は、他の食品用微生物と組み合わせて発酵させることができる。
発酵原料としては、例えば、野菜、果物、乳等の発酵原料があげられ、これらを本菌株を用いて発酵させることで、本食品組成物である漬物、味噌、醤油、乳製品、ヨーグルト等を得ることができる。例えば、野菜、果物、乳等の発酵原料に本菌株を添加する場合には、原料1グラムあたり104個〜107個(1万個〜1千万個)の割合で本菌株を添加し、20〜30℃で発酵させるようにしてもよい。
【0024】
本抗菌剤は、本培養物及び/又は本抽出組成物を有効成分として含有することを特徴とする抗菌剤である。
本培養物及び本抽出組成物に含まれる前記抗菌性物質に基づく抗菌性が本抗菌剤において発揮され、本抗菌剤が含む前記抗菌性物質の動物(ヒトを含む)に対する安全性から本抗菌剤は食品、動物飼料及び洗浄剤よりなる群より選ばれる少なくとも1つの製品の保存剤として好適に用いられる。なお、ここにいう洗浄剤としては、手洗い用洗浄剤、食品用洗浄剤、住居用洗浄剤及び医療機器用洗浄剤等が含まれる。
本抗菌剤の該製品への配合量は該製品の種類などにより適宜設定すればよいが、例えば、本培養物及び/又は本抽出組成物の量に換算して、1〜100重量%の割合とされてもよい。
そして、本抗菌剤に含まれる前記抗菌性物質はpH10以下で安定した抗菌性を発揮するので本抗菌剤はpH10以下(例えば、pH=2〜10)に調整されてもよい。
【実施例】
【0025】
以下、実施例により本発明を更に詳細に説明する。なお、実施例において使用する「MSC007株」は、上述の如く、自然界や発酵食品に広く分布しているロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)から分離されたものであり、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株として2011年1月6日(寄託日)付けで独立行政法人製品評価技術基盤機構特許微生物寄託センター(NPMD)(千葉県木更津市かずさ鎌足2−5−8)に受託番号NITE P−1027として寄託されている。
【0026】
実験例1:MSC007株の抗菌スペクトル
(試験対象菌の培養)
試験の対象菌を準備し、各々の対象菌を液体培地で培養する。対象菌としては、表2に示す通り、ボツリヌス菌(Clostridium botulinum)A型、リステリア・モノサイトゲネス菌(Listeria monocytogenes)、ペディオコッカス・アシディラクチシ菌(Pediococcus acidilactici)、エンテロコッカス・フェカーリス菌(Enterococcus faecalis)及びラクトバチルス・デルブリュッキ菌(Lactobacillus delbrueckii subsp.lactis)を用いた。
これらの対象菌のうちボツリヌス菌A型の培養にはTPGY(Trypticase-Peptone-Glucose-Yeast extract)ブイヨンを用い、リステリア・モノサイトゲネス菌の培養には普通ブイヨンを用い、そして乳酸菌であるペディオコッカス・アシディラクチシ菌、エンテロコッカス・フェカーリス菌及びラクトバチルス・デルブリュッキ菌の培養にはMRSブイヨン(乳酸菌用の液体培地)を用い、35℃で24時間培養した。
【0027】
(試験液の調製)
阻止円を評価するための試験液の調製方法を図1を参照して説明する。
予め、MSC007株をMRSブイヨン(乳酸菌用の液体培地)を用いて25℃で24時間の3回培養し(前培養)、前培養液を得た。
そして、市販の還元脱脂粉乳を蒸留水に溶解し、10%還元脱脂乳培地を調製した。
調製した10%還元脱脂乳培地100mlにMSC007株の前培養液1mlを接種した。MSC007株の前培養液を接種した10%還元脱脂乳培地を25℃で7日間培養した。
培養した培養液を20分間遠心分離(3000G)した。
遠心分離した上清を分取した。
分取した上清50ml(約10℃)に500mlのエチルアルコール(約10℃)を徐々に加えながら混合し、その後、その混合物を10℃のまま1晩静置した。
1晩静置した該混合物を20分間遠心分離(3000G)した。
遠心分離した該混合物からエチルアルコール層を分液し回収した。
分液したエチルアルコール層をロータリエバポレーターにかけ、減圧下(約45℃)にてエチルアルコールを留去した。
エチルアルコールを留去し残留した画分約1mlに蒸留水を加え溶解させ10mlとした。これに10N−水酸化ナトリウム水溶液を添加してpH7.0に調整し、試験液とした。
【0028】
(抗菌活性測定用寒天培地の調製)
対象菌それぞれの培養液を、約50℃に保たれた活性測定用寒天培地(予め加熱殺菌し溶解させ調製した)に1%接種し混合して抗菌活性測定用寒天培地を調製した。なお、活性測定用寒天培地として、対象菌のうちボツリヌス菌A型には、TPGY(Trypticase-Peptone-Glucose-Yeast extract)培地を用い、その他のリステリア・モノサイトゲネス菌、ペディオコッカス・アシディラクチシ菌、エンテロコッカス・フェカーリス菌及びラクトバチルス・デルブリュッキ菌には標準寒天(nutrient agar)培地を用いた。
対象菌の培養液を接種した抗菌活性測定用寒天培地それぞれ20mlを、直径9cmのシャーレに注入し、抗菌活性測定用寒天培地を固化させた。
各シャーレ内で固化した抗菌活性測定用寒天培地に直径約6mmの穴(ほぼ直円柱状)をあけた(ピペット等を用いて該穴を形成した)。
【0029】
(抗菌活性の評価)
抗菌活性測定用寒天培地の穴(ウエル)に50μlの試験液を注入した。
その後、穴(ウエル)に50μlの試験液を注入したシャーレそれぞれを4℃で2時間静置した後、35℃で24時間から48時間培養した。なお、対象菌のうちボツリヌス菌A型はアネロパック(登録商標)を用い嫌気ジャーにて培養し、他の対象菌は、恒温器内にて通常通り培養した。
培養後、穴(ウエル)の周囲に形成された透明な阻止円の直径(mm)を測定した。阻止円の直径は、抗菌活性測定用寒天培地の穴(ウエル)が直径6mmであるので、6mmを超えれば抗菌性を示している。
【0030】
測定した阻止円の直径(mm)を表2に表す。
表2に示すように、ボツリヌス菌A型、リステリア・モノサイトゲネス菌、ペディオコッカス・アシディラクチシ菌、エンテロコッカス・フェカーリス菌及びラクトバチルス・デルブリュッキ菌のいずれに対しても、MSC007株の培養物からエチルアルコールにて抽出した成分は十分な抗菌性を示した。
【表2】

【0031】
(抗菌性のpH及び温度による変化測定)
上述の試験液の調整において、エチルアルコールを留去し残留した画分約1mlに蒸留水を加え溶解させ10mlとした。これに2N−塩酸水溶液又は10N−水酸化ナトリウム水溶液を添加してpHを2〜11の間で段階的に変化(pH1刻みで変化)させたものを試験液とし、各pHの試験液について熱処理を行い抗菌性への影響を測定した。試験液の熱処理は、60℃で15分間、80℃で15分間、105℃で15分間、そして121℃で15分間の4種類行い、それぞれの熱処理がなされた試験液と共に熱処理しない試験液(コントロール(対照))とを用い、対象菌をリステリア・モノサイトゲネス菌として上と同様に試験した。
表3中の数値は、熱処理しない試験液(コントロール(対照))におけるpHの影響を評価するため、(pH7のときの熱処理しない試験液(コントロール(対照))の直径(mm)−6mm)に対する(各pHのときの熱処理しない試験液(コントロール(対照))の直径(mm)−6mm)の割合(%)を示した。そして、各pHにおける熱処理の影響を評価するため、(各pHのときの熱処理しない試験液(コントロール(対照))の直径(mm)−6mm)に対する(各pHのときの熱処理した試験液の直径(mm)−6mm)の割合(%)を示した。これらにおける「6mm」は抗菌活性測定用寒天培地の穴(ウエル)の直径6mmを意味しているので、阻止円の直径(mm)から6mmを減じた数値は抗菌性の強さを示す。即ち、上記のような抗菌活性(%)によって、熱処理しない試験液(コントロール(対照))におけるpHの影響(pH7を基準100とする)と共に、各pHにおける熱処理の影響(各pHにおける熱処理しないものを基準100とする)を評価できる。
【表3】

【0032】
表3から明らかなように、MSC007株の培養物からエチルアルコールにて抽出した成分は、熱処理されなければ(コントロール)pH2〜11の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜10の範囲であれば該菌により強い抗菌性を示し、pH2〜9の範囲であれば該菌に一層強い抗菌性を示し、そしてpH2〜8の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、60℃で15分間の熱処理を受けると、pH2〜10の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜9の範囲であれば該菌により強い抗菌性を示し、そしてpH2〜8の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、80℃で15分間の熱処理を受けると、pH2〜9の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜8の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、105℃で15分間の熱処理を受けると、pH2〜8の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜7の範囲であれば該菌により強い抗菌性を示し、そしてpH2〜6の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、121℃で15分間の熱処理を受けると、pH2〜6の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜5の範囲であれば全域にわたって安定して強い抗菌性を示す。
以上のように、MSC007株の培養物からエチルアルコールにて抽出した成分は、低pH領域における加熱耐性を有しており、このような低pH下での加熱を受ける食品、動物飼料及び洗浄剤等の保存剤として好適に用いることができる。
【0033】
(抗菌性の酵素処理による影響測定)
上述の試験液の調整において、エチルアルコールを留去し残留した画分約1mlに蒸留水を加え溶解させ10mlとした。これに2N−塩酸水溶液又は10N−水酸化ナトリウム水溶液を添加して、表4に示す各種プロテアーゼの至適pHに調整した。各種プロテアーゼを5mg/mlの濃度で加え、表4に示す温度で1時間反応させた後、85℃で30分間加熱して酵素を失活させた。2N−塩酸水溶液又は10N−水酸化ナトリウム水溶液を用いて、再度、pH7.0に調整したものを試験液とした。リステリア・モノサイトゲネス菌を対象菌として上と同様に試験した。
なお、プロテアーゼとしては、表4に示すとおり、ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシンを用いた。また、プロテアーゼの代わりに蒸留水を添加したものをコントロール(対照)とし、抗菌性を示す物質が過酸化水素に基づくか否かを確認するためにカタラーゼを5mg/ml添加して実験を行った。
表4中の抗菌活性(%)は、(コントロールの阻止円の直径(mm)−6mm)に対する(各実験例(ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシン、カタラーゼ)の阻止円の直径(mm)−6mm)の割合(%)として示した。(コントロールの阻止円の直径(mm)−6mm)及び(各実験例(ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシン、カタラーゼ)の阻止円の直径(mm)−6mm)における2つの「6mm」は抗菌活性測定用寒天培地の穴(ウエル)の直径6mmを意味しているので、阻止円の直径(mm)から6mmを減じた数値は抗菌性の強さを示す。即ち、上記のような抗菌活性(%)によって、各実験例(ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシン、カタラーゼ)における処理によって、これらの処理がされていないコントロール(対照)に対して抗菌作用がどの程度影響を受けているかを見ることができる。
表4に示す実験結果から明らかなように、MSC007株の培養物に含まれる抗菌性物質は、ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシンのプロテアーゼにより消化され(抗菌活性0%。即ち、阻止円が観察されない。)、過酸化水素に基づくものではないことが明らかになった(抗菌活性100%。カタラーゼを添加しても、コントロールの阻止円の直径(mm)と変化なし。)。
【表4】

【0034】
(本抗菌剤の保存剤としての使用例)
以下、本抗菌剤を食品、動物飼料及び洗浄剤の製品の保存剤として用いる場合の処方例を示す。
なお、これら処方例における本抗菌剤は、上述したpH7に調整された試験液と同様に調製したものを用いた。
【0035】
(処方例1)本抗菌剤を白菜の漬物(食品)の保存剤として用いる処方例
白菜 10kg
食塩 0.3kg
赤唐辛子 10本
昆布 50cm
柚子 2個
本抗菌剤 0.5kg
【0036】
(処方例2)本抗菌剤を豚用飼料(動物飼料)の保存剤として用いる処方例
とうもろこし 60kg
ライ麦 10kg
大豆粕 22kg
米ぬか粕 1.5kg
炭酸カルシウム 0.5kg
リン酸カルシウム 0.5kg
食塩 0.5kg
本抗菌剤 5kg
【0037】
(処方例3)本抗菌剤を除菌剤(洗浄剤)の保存剤として用いる処方例
エチルアルコール 20kg
本抗菌剤 20kg
クエン酸 0.5kg
香料 0.5kg
精製水 59kg
【受託番号】
【0038】
NITE P−1027
【技術分野】
【0001】
本発明は、新規乳酸菌に関し、より詳細には、抗菌性物質を産生する新規乳酸菌に関する。
【背景技術】
【0002】
乳酸菌は、ヨーグルトの製造に用いられる等、これまで多くのものが知られている(例えば、特許文献1参照。)。
特許文献1に記載のように、「乳酸菌は様々な機能を有していることが知られており、その中でも抗菌作用は近年注目されてきている。乳酸菌が生産する抗菌性物質として、乳酸や酢酸などの有機酸、過酸化水素、ジアセチル、ロイテリン、バクテリオシンなどがある。その中でバクテリオシンは、一般に近縁のグラム陽性菌に対して抗菌作用を示すタンパク質性もしくはペプチド性の物質である。乳酸菌のバクテリオシンは、人間の消化酵素で分解消化されること、乳酸菌が古くから広く食品に利用されていて安全性が高いことなどから、精力的にその探索が実施されてきている。」(特許文献1、発明の詳細な説明中の段落番号0002〜0003)。
また、乳酸菌が生産するバクテリオシンとしては、ロイコノストック(Leuconostoc)属によって生産されたバクテリオシンを利用した食品用保存料が挙げられる(特許文献2参照)。しかしながら、この食品用保存料はバクテリオシンと有機酸およびその塩類等からなる化合物群との組み合わせによる相乗効果によって広い抗菌スペクトルを持たせようとしたものである。また、どのような菌種の細菌に対して抗菌効果を示したのかも明らかにされていない。
【0003】
また、本発明者は、以前から乳酸菌の研究に携わり、既に乳酸菌に関連する特許出願も行ってきた(例えば、特許文献3、特許文献4等)。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特許第4302476号公報
【特許文献2】特許第3040294号公報
【特許文献3】特開2007−236227号公報
【特許文献4】特開2006−76961号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
上述のように、乳酸菌が生産する抗菌性物質は有用であることから、抗菌性物質を産生する新規な乳酸菌を提供することを目的とする。
【課題を解決するための手段】
【0006】
本発明の本発明者らは、抗菌性物質を産生する新規な乳酸菌の探索を行なった結果、自然界や発酵食品に広く分布しているロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株が、ボツリヌス菌(Clostridium botulinum)A型、リステリア・モノサイトゲネス菌(Listeria monocytogenes)、ペディオコッカス・アシディラクチシ菌(Pediococcus acidilactici)、エンテロコッカス・フェカーリス菌(Enterococcus faecalis)及びラクトバチルス・デルブリュッキ菌(Lactobacillus delbrueckii subsp.lactis)等の菌に対して抗菌性を示す物質を産生することを見出し、本発明を完成させるに至った。
【0007】
即ち、本発明の乳酸菌株(以下、「本菌株」という。)は、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株(受託番号NITE P−1027)である。
本菌株(乳酸菌MSC007株、受託番号NITE P−1027)は、後述の如く、主としてグラム陽性菌に対して有効な抗菌性物質を産生する。
【0008】
本発明は、本菌株の培養物(以下、「本培養物」という。)も提供する。
本発明は、本培養物(本菌株の培養物)を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物(以下、「本抽出組成物」という。)も提供する。
本発明は、本菌株を用いて発酵する工程を用いて製造された食品組成物(以下、「本食品組成物」という。)も提供する。
本発明は、本培養物及び/又は本抽出組成物を有効成分として含有することを特徴とする抗菌剤(以下、「本抗菌剤」という。)も提供する。本抗菌剤は、食品、動物飼料及び洗浄剤よりなる群より選ばれる少なくとも1つの製品の保存剤として好適に使用できる。また、本抗菌剤は、pH10以下に調整されてもよい。
【図面の簡単な説明】
【0009】
【図1】抗菌活性測定用の試験液の調製方法を示すフローチャートである。
【発明を実施するための形態】
【0010】
本発明の新規な乳酸菌株(本菌株)は、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株(受託番号NITE P−1027)である。
本菌株であるロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する新規な乳酸菌MSC007株(受託番号NITE P−1027)は、自然界や発酵食品に広く分布しているロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌から分離されたものである。
本菌株は、以下に示す菌学的性質を有する。これらの菌学的性質は、乳酸菌の科学と技術(学会出版センター、1996年)及びBergey’s Manual of Systematic Bacteriology, Second Edition(2009年)に記載の方法に準拠し検査した。
【表1】

【0011】
以上の特徴をBergey’s Manual of Systematic Bacteriology, Second Edition(2009年)を参照して近縁菌種を検索した結果、本菌株はロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)の特徴と一致した。
遺伝学的性質は以下の如くである。本菌株について16SrDNAの塩基配列500ベースペア(bp)を解読し、アポロンDB-BA5.0データベースで近縁菌種の相同性検索を行った結果、登録されているロイコノストック・メセンテロイデス・サブスピーシーズ・デキストラニカム(Leuconostoc mesenteroides subsp.dextranicum)NRIC1539株及びロイコノストック・メセンテロイデス・サブスピーシーズ・メセンテロイデス(Leuconostoc mesenteroides subsp.mesenteroides)NCDO523株の16SrDNAの塩基配列と100.0%の相同率を示した。また、国際塩基配列データベースではロイコノストック・メセンテロイデス・サブスピーシーズ・デキストラニカム(Leuconostoc mesenteroides subsp.dextranicum)QL2株及びロイコノストック・メセンテロイデス・サブスピーシーズ・メセンテロイデス(Leuconostoc mesenteroides subsp.mesenteroides)ATCC8293株の16SrDNAの塩基配列と100.0%の相同率を示した。
従って、本菌株をロイコノストック・メセンテロイデス( Leuconostoc mesenteroides)と同定した。
【0012】
このロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)MSC007株は、千葉県木更津市かずさ鎌足2−5−8に住所を有する独立行政法人製品評価技術基盤機構特許微生物寄託センター(NPMD)に平成23年1月6日(寄託日)付で上記名称(識別の表示:Leuconostoc mesenteroides MSC007)で寄託されており、受託番号はNITE P−1027である。
【0013】
本菌株乳酸菌MSC007株は、上述したように、天然に存する乳酸菌から分離されたものであり、本菌株乳酸菌MSC007株それ自身及びその培養物についてもヒトを含む動物に対する毒性はなく、ヒトを含む動物に対して経口摂取や皮膚への塗布を安全に行うことができる。
【0014】
本菌株乳酸菌MSC007株は、多くの菌に対する抗菌性物質を産生する。該抗菌性物質は、後に詳述する表2(MSC007の抗菌スペクトル)に示す通り、ボツリヌス菌(Clostridium botulinum)A型、リステリア・モノサイトゲネス菌(Listeria monocytogenes)、ペディオコッカス・アシディラクチシ菌(Pediococcus acidilactici)、エンテロコッカス・フェカーリス菌(Enterococcus faecalis)及びラクトバチルス・デルブリュッキ菌(Lactobacillus delbrueckii subsp.lactis)等のようなグラム陽性菌に対して特に有効な抗菌性を示す。
加えて、本菌株乳酸菌MSC007株は、pH7、80℃で15分間の処理条件下で熱安定性を示す。
そして、本菌株乳酸菌MSC007株が産生する抗菌性物質は、上述したグラム陽性菌に対して有効であると共に次のような特徴を有する。
(イ)プロテアーゼで消化される。
(ロ)pH10以下(例えば、pH2〜10)で安定性を示す。
【0015】
本菌株乳酸菌MSC007株の分離菌株の保存は、MRSブイヨンで培養した培養菌液を10%還元脱脂乳培地に0.5%量程度添加し、そのまま−20℃から−80℃で冷凍することで保存できる。
そして、使用にあたっては、菌株を含む保存物をMRSブイヨンに1%量程度添加し、25℃で24時間保つことで培養することができる。
本菌株乳酸菌MSC007株の培養に使用することのできる培地としては、本菌株が増殖し得るものであれば任意のものでよい。例えば、使用可能な培地としては、炭素源、窒素源、無機塩類、ビタミン、アミノ酸等を含む通常用いられる培地(液体培地、固体培地など)であるが、乳酸菌の培養に適する培地を用いてもよい。乳酸菌の培養に適する培地としては、例えば、MRSブイヨン、MRS寒天培地、BCP加プレートカウント培地、10%還元脱脂乳培地等が挙げられる。
本菌株乳酸菌MSC007株の培養は、とくに嫌気的条件下で行う必要はなく、通常の好気的条件下で培養することができる。培養条件は特に限定はないが、温度は20〜30℃、pHは6〜7、培養時間は1〜7日間の範囲とされてもよい。
【0016】
本培養物は、本菌株ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株(受託番号NITE P−1027)の培養物である。
本菌株乳酸菌MSC007株の培養は、上述したような条件下にて行うことができ、その培養物(本培養物)は本菌株乳酸菌MSC007株が産生する前記の抗菌性物質を含有する。従って、本培養物自身も、それが含有する該抗菌性物質に基づく抗菌性を有する。
また、本培養物としては、本菌株を液状または固形培地で培養した培養物全体を用いることもできるが、必要に応じて培養物の一部を分取した分取物としてもよい。分取物としては、培養液(菌体含有)、コロニー、培養上清(菌体不含)等を例示できる。そして、本培養物として培養上清を用いる場合には、培養液から菌体を遠心分離等によって分離し、培養上清液のpHを炭酸ナトリウム、水酸化ナトリウム、水酸化カリウム等によりpHを10以下に調整(例えば、pH2〜10程度)して、本抗菌剤として利用することもできる。更に、培養上清液の粗精製物を本抗菌剤として用いることもでき、この粗精製物は、例えば、培養上清液をイオン交換、限外濾過、逆浸透、ゲル濾過等の方法で抗菌活性を有する画分を取得することで調製することもできる。
【0017】
本抽出組成物は、本培養物(本菌株の培養物)を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物である。
本培養物に含まれる前記抗菌性物質は、本培養物と炭素数1〜3のアルコールとを接触させると、アルコール層に抽出されるので、本培養物からアルコール層に抽出される抽出画分を含む本抽出組成物は前記抗菌性物質を含有する。
従って、本抽出組成物も、それが含有する前記抗菌性物質に基づく抗菌性を有する。
ここに用いる炭素数1〜3のアルコールとしては、メチルアルコール、エチルアルコール、n−プロピルアルコール、イソプロピルアルコールを例示できるが、本抽出組成物に残留する場合の低毒性を考慮すれば、エチルアルコールが好ましい。
また、炭素数1〜3のアルコールを接触させ抽出する本培養物としては、本乳酸菌株を培養した培養物そのものでもよいが、本培養物に含まれる前記抗菌性物質は本培養物を遠心分離や静置分離した際に得られる上清に含まれるので、本培養物を遠心分離や静置分離して生じる上清を該アルコール層と接触させるようにしてもよい。
【0018】
本抽出組成物は、本培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られるものであり、本培養物から抽出された前記抗菌性物質を含有するアルコール層は、本抽出組成物中にアルコールが含まれてもよい場合には、アルコールを留去せず、そのままアルコールを含んだ状態の本抽出組成物としてもよい。そして、本培養物から抽出された前記抗菌性物質を含有するアルコール層は、それが含有するアルコールの一部又は全部を留去したり、及び/又は、それが含有する水分の一部又は全部を留去して本抽出組成物としてもよい。さらに、本培養物から抽出された前記抗菌性物質を含有するアルコール層は、乾燥固化して本抽出組成物としてもよい。
また、本抽出組成物は、水に安定して溶解するので、水溶液としておくこともできる。本抽出組成物に含まれる前記抗菌性物質はpH10以下で安定した抗菌性を発揮するのでpH10以下(例えば、pH=2〜10)の水溶液としてもよい。
【0019】
本抽出組成物は、上述の通り、本培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られるものであればよく何ら限定されるものではないが、例えば、本培養物にエチルアルコールを接触させる接触ステップと、接触ステップにより培養物と接触したエチルアルコール層を回収する回収ステップと、回収ステップにより回収されたエチルアルコール層のエチルアルコールを留去し抽出組成物とする留去ステップと、を含んでなる製造方法により製造されうる。
【0020】
接触ステップでは、本培養物にエチルアルコールを接触させる。
接触ステップにおける本培養物(体積)に対するエチルアルコール(体積)の比率(エチルアルコール(体積)/本培養物(体積))は、あまり小さいと前記抗菌性物質がエチルアルコール層に十分抽出されず、逆にあまり多いとエチルアルコール層が多すぎて回収ステップや留去ステップを実施することが大変になるため、これらを両立する範囲とされてもよく、特に限定されるものではないが、通常、1〜10とされてもよい。また、接触ステップにおける本培養物及びエチルアルコールの温度は、あまり低いと凍結により前記抗菌性物質がエチルアルコール層に十分抽出されない恐れがあり、逆にあまり高いと前記抗菌性物質が変性を起こす恐れが生じるので、これらを両立する範囲とされてもよく、特に限定されるものではないが、通常、1℃〜15℃とされてもよい。そして、接触ステップにおける本培養物及びエチルアルコールの接触時間は、あまり短いと前記抗菌性物質がエチルアルコール層に十分抽出されず、逆にあまり長いと時間がかかりすぎるので、これらを両立する範囲とされてもよく、特に限定されるものではないが、通常、4時間〜24時間とされてもよい。
また、接触ステップにおいてエチルアルコール層と接触させる本培養物としては、本乳酸菌株を培養した培養物そのものでもよいが、本培養物に含まれる前記抗菌性物質は本培養物を遠心分離や静置分離した際に得られる上清に含まれるので、本培養物を遠心分離や静置分離して生じる上清を接触ステップにおいてエチルアルコール層と接触させるようにしてもよい。
【0021】
回収ステップでは、接触ステップにより培養物と接触したエチルアルコール層を回収する。
接触ステップにおいて培養物と接触したエチルアルコール層は、培養物層とは液−液分離するので比重差を利用して遠心分離や静置分離の後に、分液することでエチルアルコール層を回収できる(上層に透明なエチルアルコール層、下層に白色の培養物層が形成される)。かかるエチルアルコール層には、本菌株が産生する前記の抗菌性物質が含まれている。
【0022】
留去ステップでは、回収ステップにより回収されたエチルアルコール層のエチルアルコールを留去し本抽出組成物とする。
回収ステップで回収されたエチルアルコール層からエチルアルコールを留去するには、エチルアルコールを蒸発させ除去すればよく、常圧下又は減圧下でエチルアルコールを蒸発除去してもよい(前記抗菌性物質を含む本抽出組成物が高温により劣化することを防止又は減少させることからは減圧下で行うようにしてもよい。)。
また、本抽出組成物中にエチルアルコールが含まれてもよい場合には、エチルアルコールを完全に留去せず、エチルアルコールを含んだ状態の本抽出組成物としてもよい。
本抽出組成物は、水に安定して溶解するので、水溶液としておくこともできる。本抽出組成物に含まれる前記抗菌性物質はpH10以下で安定した抗菌性を発揮するのでpH10以下(例えば、pH=2〜10)の水溶液としてもよい。
【0023】
本食品組成物は、本菌株を用いて発酵する工程を用いて製造された食品組成物である。
本菌株乳酸菌MSC007株は、本菌株が属する乳酸菌株及び前記抗菌性物質の特徴に基づき、特に食品分野へ好適に用いることが可能である。即ち、本菌株は、本菌株を用いて発酵原料を発酵する工程を用いて発酵食品を製造するために使用することができる。なお、本菌株は、他の食品用微生物と組み合わせて発酵させることができる。
発酵原料としては、例えば、野菜、果物、乳等の発酵原料があげられ、これらを本菌株を用いて発酵させることで、本食品組成物である漬物、味噌、醤油、乳製品、ヨーグルト等を得ることができる。例えば、野菜、果物、乳等の発酵原料に本菌株を添加する場合には、原料1グラムあたり104個〜107個(1万個〜1千万個)の割合で本菌株を添加し、20〜30℃で発酵させるようにしてもよい。
【0024】
本抗菌剤は、本培養物及び/又は本抽出組成物を有効成分として含有することを特徴とする抗菌剤である。
本培養物及び本抽出組成物に含まれる前記抗菌性物質に基づく抗菌性が本抗菌剤において発揮され、本抗菌剤が含む前記抗菌性物質の動物(ヒトを含む)に対する安全性から本抗菌剤は食品、動物飼料及び洗浄剤よりなる群より選ばれる少なくとも1つの製品の保存剤として好適に用いられる。なお、ここにいう洗浄剤としては、手洗い用洗浄剤、食品用洗浄剤、住居用洗浄剤及び医療機器用洗浄剤等が含まれる。
本抗菌剤の該製品への配合量は該製品の種類などにより適宜設定すればよいが、例えば、本培養物及び/又は本抽出組成物の量に換算して、1〜100重量%の割合とされてもよい。
そして、本抗菌剤に含まれる前記抗菌性物質はpH10以下で安定した抗菌性を発揮するので本抗菌剤はpH10以下(例えば、pH=2〜10)に調整されてもよい。
【実施例】
【0025】
以下、実施例により本発明を更に詳細に説明する。なお、実施例において使用する「MSC007株」は、上述の如く、自然界や発酵食品に広く分布しているロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)から分離されたものであり、ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株として2011年1月6日(寄託日)付けで独立行政法人製品評価技術基盤機構特許微生物寄託センター(NPMD)(千葉県木更津市かずさ鎌足2−5−8)に受託番号NITE P−1027として寄託されている。
【0026】
実験例1:MSC007株の抗菌スペクトル
(試験対象菌の培養)
試験の対象菌を準備し、各々の対象菌を液体培地で培養する。対象菌としては、表2に示す通り、ボツリヌス菌(Clostridium botulinum)A型、リステリア・モノサイトゲネス菌(Listeria monocytogenes)、ペディオコッカス・アシディラクチシ菌(Pediococcus acidilactici)、エンテロコッカス・フェカーリス菌(Enterococcus faecalis)及びラクトバチルス・デルブリュッキ菌(Lactobacillus delbrueckii subsp.lactis)を用いた。
これらの対象菌のうちボツリヌス菌A型の培養にはTPGY(Trypticase-Peptone-Glucose-Yeast extract)ブイヨンを用い、リステリア・モノサイトゲネス菌の培養には普通ブイヨンを用い、そして乳酸菌であるペディオコッカス・アシディラクチシ菌、エンテロコッカス・フェカーリス菌及びラクトバチルス・デルブリュッキ菌の培養にはMRSブイヨン(乳酸菌用の液体培地)を用い、35℃で24時間培養した。
【0027】
(試験液の調製)
阻止円を評価するための試験液の調製方法を図1を参照して説明する。
予め、MSC007株をMRSブイヨン(乳酸菌用の液体培地)を用いて25℃で24時間の3回培養し(前培養)、前培養液を得た。
そして、市販の還元脱脂粉乳を蒸留水に溶解し、10%還元脱脂乳培地を調製した。
調製した10%還元脱脂乳培地100mlにMSC007株の前培養液1mlを接種した。MSC007株の前培養液を接種した10%還元脱脂乳培地を25℃で7日間培養した。
培養した培養液を20分間遠心分離(3000G)した。
遠心分離した上清を分取した。
分取した上清50ml(約10℃)に500mlのエチルアルコール(約10℃)を徐々に加えながら混合し、その後、その混合物を10℃のまま1晩静置した。
1晩静置した該混合物を20分間遠心分離(3000G)した。
遠心分離した該混合物からエチルアルコール層を分液し回収した。
分液したエチルアルコール層をロータリエバポレーターにかけ、減圧下(約45℃)にてエチルアルコールを留去した。
エチルアルコールを留去し残留した画分約1mlに蒸留水を加え溶解させ10mlとした。これに10N−水酸化ナトリウム水溶液を添加してpH7.0に調整し、試験液とした。
【0028】
(抗菌活性測定用寒天培地の調製)
対象菌それぞれの培養液を、約50℃に保たれた活性測定用寒天培地(予め加熱殺菌し溶解させ調製した)に1%接種し混合して抗菌活性測定用寒天培地を調製した。なお、活性測定用寒天培地として、対象菌のうちボツリヌス菌A型には、TPGY(Trypticase-Peptone-Glucose-Yeast extract)培地を用い、その他のリステリア・モノサイトゲネス菌、ペディオコッカス・アシディラクチシ菌、エンテロコッカス・フェカーリス菌及びラクトバチルス・デルブリュッキ菌には標準寒天(nutrient agar)培地を用いた。
対象菌の培養液を接種した抗菌活性測定用寒天培地それぞれ20mlを、直径9cmのシャーレに注入し、抗菌活性測定用寒天培地を固化させた。
各シャーレ内で固化した抗菌活性測定用寒天培地に直径約6mmの穴(ほぼ直円柱状)をあけた(ピペット等を用いて該穴を形成した)。
【0029】
(抗菌活性の評価)
抗菌活性測定用寒天培地の穴(ウエル)に50μlの試験液を注入した。
その後、穴(ウエル)に50μlの試験液を注入したシャーレそれぞれを4℃で2時間静置した後、35℃で24時間から48時間培養した。なお、対象菌のうちボツリヌス菌A型はアネロパック(登録商標)を用い嫌気ジャーにて培養し、他の対象菌は、恒温器内にて通常通り培養した。
培養後、穴(ウエル)の周囲に形成された透明な阻止円の直径(mm)を測定した。阻止円の直径は、抗菌活性測定用寒天培地の穴(ウエル)が直径6mmであるので、6mmを超えれば抗菌性を示している。
【0030】
測定した阻止円の直径(mm)を表2に表す。
表2に示すように、ボツリヌス菌A型、リステリア・モノサイトゲネス菌、ペディオコッカス・アシディラクチシ菌、エンテロコッカス・フェカーリス菌及びラクトバチルス・デルブリュッキ菌のいずれに対しても、MSC007株の培養物からエチルアルコールにて抽出した成分は十分な抗菌性を示した。
【表2】

【0031】
(抗菌性のpH及び温度による変化測定)
上述の試験液の調整において、エチルアルコールを留去し残留した画分約1mlに蒸留水を加え溶解させ10mlとした。これに2N−塩酸水溶液又は10N−水酸化ナトリウム水溶液を添加してpHを2〜11の間で段階的に変化(pH1刻みで変化)させたものを試験液とし、各pHの試験液について熱処理を行い抗菌性への影響を測定した。試験液の熱処理は、60℃で15分間、80℃で15分間、105℃で15分間、そして121℃で15分間の4種類行い、それぞれの熱処理がなされた試験液と共に熱処理しない試験液(コントロール(対照))とを用い、対象菌をリステリア・モノサイトゲネス菌として上と同様に試験した。
表3中の数値は、熱処理しない試験液(コントロール(対照))におけるpHの影響を評価するため、(pH7のときの熱処理しない試験液(コントロール(対照))の直径(mm)−6mm)に対する(各pHのときの熱処理しない試験液(コントロール(対照))の直径(mm)−6mm)の割合(%)を示した。そして、各pHにおける熱処理の影響を評価するため、(各pHのときの熱処理しない試験液(コントロール(対照))の直径(mm)−6mm)に対する(各pHのときの熱処理した試験液の直径(mm)−6mm)の割合(%)を示した。これらにおける「6mm」は抗菌活性測定用寒天培地の穴(ウエル)の直径6mmを意味しているので、阻止円の直径(mm)から6mmを減じた数値は抗菌性の強さを示す。即ち、上記のような抗菌活性(%)によって、熱処理しない試験液(コントロール(対照))におけるpHの影響(pH7を基準100とする)と共に、各pHにおける熱処理の影響(各pHにおける熱処理しないものを基準100とする)を評価できる。
【表3】

【0032】
表3から明らかなように、MSC007株の培養物からエチルアルコールにて抽出した成分は、熱処理されなければ(コントロール)pH2〜11の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜10の範囲であれば該菌により強い抗菌性を示し、pH2〜9の範囲であれば該菌に一層強い抗菌性を示し、そしてpH2〜8の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、60℃で15分間の熱処理を受けると、pH2〜10の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜9の範囲であれば該菌により強い抗菌性を示し、そしてpH2〜8の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、80℃で15分間の熱処理を受けると、pH2〜9の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜8の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、105℃で15分間の熱処理を受けると、pH2〜8の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜7の範囲であれば該菌により強い抗菌性を示し、そしてpH2〜6の範囲であれば全域にわたって安定して強い抗菌性を示す。
MSC007株の培養物からエチルアルコールにて抽出した成分は、121℃で15分間の熱処理を受けると、pH2〜6の範囲にてリステリア・モノサイトゲネス菌に抗菌性を示すが、pH2〜5の範囲であれば全域にわたって安定して強い抗菌性を示す。
以上のように、MSC007株の培養物からエチルアルコールにて抽出した成分は、低pH領域における加熱耐性を有しており、このような低pH下での加熱を受ける食品、動物飼料及び洗浄剤等の保存剤として好適に用いることができる。
【0033】
(抗菌性の酵素処理による影響測定)
上述の試験液の調整において、エチルアルコールを留去し残留した画分約1mlに蒸留水を加え溶解させ10mlとした。これに2N−塩酸水溶液又は10N−水酸化ナトリウム水溶液を添加して、表4に示す各種プロテアーゼの至適pHに調整した。各種プロテアーゼを5mg/mlの濃度で加え、表4に示す温度で1時間反応させた後、85℃で30分間加熱して酵素を失活させた。2N−塩酸水溶液又は10N−水酸化ナトリウム水溶液を用いて、再度、pH7.0に調整したものを試験液とした。リステリア・モノサイトゲネス菌を対象菌として上と同様に試験した。
なお、プロテアーゼとしては、表4に示すとおり、ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシンを用いた。また、プロテアーゼの代わりに蒸留水を添加したものをコントロール(対照)とし、抗菌性を示す物質が過酸化水素に基づくか否かを確認するためにカタラーゼを5mg/ml添加して実験を行った。
表4中の抗菌活性(%)は、(コントロールの阻止円の直径(mm)−6mm)に対する(各実験例(ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシン、カタラーゼ)の阻止円の直径(mm)−6mm)の割合(%)として示した。(コントロールの阻止円の直径(mm)−6mm)及び(各実験例(ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシン、カタラーゼ)の阻止円の直径(mm)−6mm)における2つの「6mm」は抗菌活性測定用寒天培地の穴(ウエル)の直径6mmを意味しているので、阻止円の直径(mm)から6mmを減じた数値は抗菌性の強さを示す。即ち、上記のような抗菌活性(%)によって、各実験例(ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシン、カタラーゼ)における処理によって、これらの処理がされていないコントロール(対照)に対して抗菌作用がどの程度影響を受けているかを見ることができる。
表4に示す実験結果から明らかなように、MSC007株の培養物に含まれる抗菌性物質は、ペプシン、プロナーゼE、トリプシン、プロティナーゼK、プロテアーゼ、α−キモトリプシンのプロテアーゼにより消化され(抗菌活性0%。即ち、阻止円が観察されない。)、過酸化水素に基づくものではないことが明らかになった(抗菌活性100%。カタラーゼを添加しても、コントロールの阻止円の直径(mm)と変化なし。)。
【表4】

【0034】
(本抗菌剤の保存剤としての使用例)
以下、本抗菌剤を食品、動物飼料及び洗浄剤の製品の保存剤として用いる場合の処方例を示す。
なお、これら処方例における本抗菌剤は、上述したpH7に調整された試験液と同様に調製したものを用いた。
【0035】
(処方例1)本抗菌剤を白菜の漬物(食品)の保存剤として用いる処方例
白菜 10kg
食塩 0.3kg
赤唐辛子 10本
昆布 50cm
柚子 2個
本抗菌剤 0.5kg
【0036】
(処方例2)本抗菌剤を豚用飼料(動物飼料)の保存剤として用いる処方例
とうもろこし 60kg
ライ麦 10kg
大豆粕 22kg
米ぬか粕 1.5kg
炭酸カルシウム 0.5kg
リン酸カルシウム 0.5kg
食塩 0.5kg
本抗菌剤 5kg
【0037】
(処方例3)本抗菌剤を除菌剤(洗浄剤)の保存剤として用いる処方例
エチルアルコール 20kg
本抗菌剤 20kg
クエン酸 0.5kg
香料 0.5kg
精製水 59kg
【受託番号】
【0038】
NITE P−1027
【特許請求の範囲】
【請求項1】
ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株(受託番号NITE P−1027)。
【請求項2】
請求項1に記載の乳酸菌株の培養物。
【請求項3】
請求項2に記載の培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物。
【請求項4】
請求項1に記載の乳酸菌株を用いて発酵する工程を用いて製造された食品組成物。
【請求項5】
請求項2に記載の培養物及び/又は請求項3に記載の抽出組成物を有効成分として含有することを特徴とする、抗菌剤。
【請求項6】
食品、動物飼料及び洗浄剤よりなる群より選ばれる少なくとも1つの製品の保存剤として用いられる、請求項5に記載の抗菌剤。
【請求項7】
pH10以下に調整されてなる、請求項5又は6に記載の抗菌剤。
【請求項1】
ロイコノストック・メセンテロイデス(Leuconostoc mesenteroides)に属する乳酸菌MSC007株(受託番号NITE P−1027)。
【請求項2】
請求項1に記載の乳酸菌株の培養物。
【請求項3】
請求項2に記載の培養物を炭素数1〜3のアルコールを用いて抽出する工程を経て得られる抽出組成物。
【請求項4】
請求項1に記載の乳酸菌株を用いて発酵する工程を用いて製造された食品組成物。
【請求項5】
請求項2に記載の培養物及び/又は請求項3に記載の抽出組成物を有効成分として含有することを特徴とする、抗菌剤。
【請求項6】
食品、動物飼料及び洗浄剤よりなる群より選ばれる少なくとも1つの製品の保存剤として用いられる、請求項5に記載の抗菌剤。
【請求項7】
pH10以下に調整されてなる、請求項5又は6に記載の抗菌剤。
【図1】




【公開番号】特開2012−170378(P2012−170378A)
【公開日】平成24年9月10日(2012.9.10)
【国際特許分類】
【出願番号】特願2011−34112(P2011−34112)
【出願日】平成23年2月21日(2011.2.21)
【出願人】(511045475)株式会社農 (2)
【出願人】(504147243)国立大学法人 岡山大学 (444)
【Fターム(参考)】
【公開日】平成24年9月10日(2012.9.10)
【国際特許分類】
【出願日】平成23年2月21日(2011.2.21)
【出願人】(511045475)株式会社農 (2)
【出願人】(504147243)国立大学法人 岡山大学 (444)
【Fターム(参考)】
[ Back to top ]

