有価金属回収方法
【課題】例えばリチウムイオン電池の廃電池等、有価金属であるニッケルやコバルトを含む金属複合体から有価金属を回収するための有価金属回収方法において、ニッケル、コバルト等の有価金属の高い回収率を保持しつつ、それらの有価金属を含む合金から効率よくリンのみを分離すること。
【解決手段】ニッケルとコバルトを含有する金属複合体からの有価金属回収方法であって、金属複合体を熔融して熔融物を得る熔融工程と、熔融工程時の熔融物に対して、又は、熔融工程前の金属複合体に対して行われ、金属複合体を酸化処理する酸化工程と、熔融物から、スラグを分離して、有価金属を含む合金を回収するスラグ分離工程と、合金に含有されるリンを分離する脱リン工程とを備え、この脱リン工程が、合金に石灰含有物を添加し、次いで、前記合金を酸化する工程である。
【解決手段】ニッケルとコバルトを含有する金属複合体からの有価金属回収方法であって、金属複合体を熔融して熔融物を得る熔融工程と、熔融工程時の熔融物に対して、又は、熔融工程前の金属複合体に対して行われ、金属複合体を酸化処理する酸化工程と、熔融物から、スラグを分離して、有価金属を含む合金を回収するスラグ分離工程と、合金に含有されるリンを分離する脱リン工程とを備え、この脱リン工程が、合金に石灰含有物を添加し、次いで、前記合金を酸化する工程である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、例えばリチウムイオン電池の廃電池に含有する有価金属を回収する方法に関し、更に詳しくは、そのような有価金属の回収プロセスにおいて、有価金属の回収率に悪影響を与えることなく、有価金属を含有する合金から不要なリンのみを除去することのできる有価金属回収方法に関する。
【背景技術】
【0002】
リチウムイオン電池等の、使用済み或いは工程内の不良品である電池(以下廃電池という)をリサイクルし、含有する有価金属を回収しようとする処理方法には、大きく分けて乾式法と湿式法がある。
【0003】
乾式法は、破砕した廃電池を熔融処理し、コバルト、ニッケル、銅に代表される回収対象である有価金属と、鉄やアルミニウムに代表される付加価値の低いその他の金属等とを、それらの間の酸素親和力の差を利用して分離回収するものである。すなわち、鉄等の付加価値の低い元素を極力酸化してスラグとし、かつコバルト等の有価物は酸化を極力抑制して合金として回収するものである。
【0004】
例えば、特許文献1には、高温の加熱炉を使用し、廃電池にフラックスを添加し、スラグを分離する処理を繰り返すことで有価金属であるニッケルやコバルトを80%前後回収できる方法が開示されている。
【0005】
又、特許文献2には、スラグ分離のための熔融処理に先行して、廃電池を非酸化性雰囲気で加熱して炭素を除去する脱炭素工程を行うことによって、有価金属であるニッケルやコバルトの回収率を向上できる方法が開示されている。
【0006】
ここで、リチウムイオン電池の電解質はエチレンカーボネート(EC)/ジエチルカーボネート(DEC)/ジメチルカーボネート(DMC)等の混合有機溶剤にLiPF6を混合したものが通常用いられている。このLiPF6中のP(リン)は、比較的酸化され易い性質を有するものの、鉄、コバルト、ニッケル等鉄族元素との親和力も比較的高い性質がある。
【0007】
リチウムイオン電池の乾式法による処理によって生じる合金中には、ニッケル、コバルト、鉄というFe系元素が含まれていることから、鉄鋼製錬時と同様に一部のリンが合金中に含まれることになる。合金中に存在するリンは、乾式法による工程で得た合金から各元素を金属として回収する後工程の湿式法による工程での除去が難しく、不純物として処理系内に蓄積する。そのため、操業の継続が困難となる。
【0008】
そのために、有価金属であるニッケルやコバルトを回収するための有価金属回収方法においては、乾式工程でのリンの除去が必要となる。例えば、鉄鋼製錬においては、特許文献3に記載されているように、転炉操業時に鋳鉄溶湯中に酸化剤及び石灰系フラックスを添加してリンを除去する脱リン処理が行われている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】米国特許第7169206号公報
【特許文献2】特開2002−327215号公報
【特許文献3】特開2002−285220号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
しかしながら、特許文献3に開示されている脱リン方法においては、リンを酸化させる一方で、ニッケルやコバルト等の有価金属については酸化を適度に抑制することについては何らの考慮もなされていない。このため、特許文献3に開示されている方法をリチウムイオン電池から有価金属を回収するプロセスに適用すると、脱リンのプロセスが有価金属の回収率を下げる要因となってしまう。一方、特許文献1及び特許文献2においては、リチウムイオン電池を乾式処理して得られた合金からの脱リンの処理方法については何ら開示されていない。有価金属であるニッケルやコバルトを回収するための有価金属回収方法においては、ニッケル、コバルト等の有価金属の高い回収率を保持しつつ、効率よく脱リンを行うことのできる有価金属の回収方法が新たに求められているのが現状であった。
【0011】
本発明は、リチウムイオン電池の廃電池からニッケル、コバルトを含む有価金属を回収する有価金属回収プロセスにおいて、有価金属の回収率を落とさずに、有価金属を含む合金の脱リン処理を行うことのできる有価金属回収方法を提供することを目的とする。
【課題を解決するための手段】
【0012】
本発明者らは、有価金属回収プロセスにおける脱リン工程を、有価金属を含む合金に所定の石灰含有物を添加し、次いで、当該合金を酸化する工程とすることによって、有価金属の回収率を低下させることなく、有価金属を含む合金の脱リン処理を行うことができることを見出し、本発明を完成するに至った。より具体的には、本発明は以下のものを提供する。
【0013】
(1) ニッケルとコバルトを含有する金属複合体から、該ニッケルと該コバルトを含む有価金属を回収する有価金属回収方法であって、前記金属複合体を熔融して熔融物を得る熔融工程と、前記熔融工程時の前記熔融物に対して、又は、前記熔融工程前の前記金属複合体に対して行われ、前記金属複合体を酸化処理する酸化工程と、前記熔融物から、スラグを分離して、有価金属を含む合金を回収するスラグ分離工程と、前記合金に含有されるリンを分離する脱リン工程と、を備え、前記脱リン工程は、前記合金に石灰含有物を添加し、次いで、前記合金を酸化する工程である有価金属回収方法。
【0014】
(2) 前記石灰含有物が消石灰、炭酸カルシウム、酸化カルシウムのうちの少なくとも1種類を含むものである(1)に記載の有価金属回収方法。
【0015】
(3) 前記石灰含有物の添加量が、酸化カルシウム質量に換算した場合に、前記合金質量に対して0.1質量%以上8質量%以下の範囲である(1)又は(2)のいずれかに記載の有価金属回収方法。
【0016】
(4) 前記脱リン工程において、前記石灰含有物を添加する際に、フッ化カルシウムを併せて添加する(1)から(3)のいずれかに記載の有価金属回収方法。
【0017】
(5) 酸化カルシウムに換算した前記石灰含有物の添加量と前記フッ化カルシウムの添加量との比率が40:60から5:95の範囲である(4)に記載の有価金属回収方法。
【0018】
(6) 前記金属複合体がリチウムイオン電池である(1)から(5)のいずれかに記載の有価金属回収方法。
【発明の効果】
【0019】
本発明によれば、リチウムイオン電池の廃電池等からニッケル、コバルトを含む有価金属を回収する有価金属回収プロセスにおいて、有価金属の回収率に悪影響を与えることなく脱リン処理を行うことにより、高い回収率で有価金属を回収することができる。
【図面の簡単な説明】
【0020】
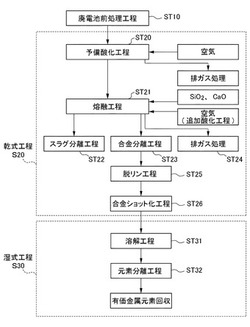
【図1】本発明の一例である、廃電池からの有価金属回収方法を示すフローチャートである。
【発明を実施するための形態】
【0021】
以下、本発明の一実施形態について図面を参照しながら説明する。図1は、金属複合体からの有価金属回収方法の一例を示すフローチャートである。本実施形態においては、金属複合体がリチウムイオン電池の廃電池である場合について説明するが、本発明はこれに限定されるものではない。
【0022】
<全体プロセス>
図1に示すように、この有価金属回収方法は、廃電池前処理工程ST10と、予備酸化工程ST20と、乾式工程S20と、湿式工程S30とからなる。このように、本実施例における有価金属回収方法は乾式工程S20において合金を得て、その後に湿式工程S30によって有価金属元素を分離回収するトータルプロセスである。なお、本発明における廃電池とは、使用済み電池のみならず、工程内の不良品等も含む意味である。また、処理対象に廃電池を含んでいればよく、廃電池以外のその他の金属や樹脂等を適宜加えることを排除するものではない。その場合にはその他の金属や樹脂を含めて本発明の廃電池である。
【0023】
<廃電池前処理工程ST10>
廃電池前処理工程ST10は、廃電池の爆発防止を目的として行われる。すなわち、廃電池は密閉系であり内部に電解液等を有しているため、このまま乾式の熔融処理を行うと爆発の恐れがあり危険である。このため、何らかの方法でガス抜きのための開孔処理を施す必要がある。これが廃電池前処理工程ST10を行う目的である。
【0024】
廃電池前処理工程ST10の具体的な方法は特に限定されないが、例えば針状の刃先で廃電池に物理的に開孔すればよい。なお、本発明においては後の乾式処理において熔融工程を経るために、個々の部材の分離等は不要である。
【0025】
<予備酸化工程ST20>
【0026】
この予備酸化工程ST20は、本発明における酸化工程の好ましい工程であり、本発明における、「前記熔融工程前の前記廃電池に対して行われ、前記廃電池を酸化処理する酸化工程」に該当する。
【0027】
予備酸化工程ST20においては、廃電池前処理工程ST10で得られた前処理済廃電池を600℃〜1250℃の温度で焙焼しながら酸素を供給することにより予備酸化処理を行う。従来の有価金属回収方法においては、乾式工程における熔融工程内で酸化処理を行っていたが、本発明の有価金属回収方法においては、熔融工程ST21の前に予備酸化工程ST20を設けて、当該工程内において予備酸化処理を行うことにより、より好ましい態様での実施が可能である。
【0028】
この予備酸化処理は、熔融工程ST21を行う前の段階に行うものであり、熔融工程ST21を行う溶融炉とは別途に予備酸化炉を設けて当該予備酸化炉内において行う。この予備酸化炉としては、予備酸化工程ST20において廃電池を焙焼しながら酸素を供給することにより、その内部で酸化処理を行うことが可能であるあらゆる形式のキルンを用いることができる。一例として、従来よりセメント製造等に用いられているロータリーキルン、又はトンネルキルン(ハースファーネス)を好適に用いることができる。
【0029】
キルンを用いた予備酸化工程ST20においては、まず、キルン本体の内部温度を600〜1250℃となるように加熱する。廃電池は攪拌、焙焼されながらキルン本体内を排出口の方向に向かって移動してゆく。このとき、キルン本体内の温度が600℃未満であるとアルミニウムや炭素の酸化が充分に進まず好ましくない。上記温度が600℃以上から1250℃の範囲であれば、アルミニウムや炭素の酸化は充分に進む一方で、鉄の酸化は相対的に低い酸化度に止まるため、後のスラグ分離工程において酸化アルミニウムを好適にスラグ分離できる。また、上記温度が、1250℃を超えると、主に廃電池の外部シェルに用いられている鉄等の一部がキルン本体の内壁等に付着してしまい、円滑な操業の妨げになったり、或いはキルン自体の劣化につながる場合があり好ましくない。
【0030】
上述した通り、600〜1250℃の温度で焙焼されながらキルン本体内を移動してゆく廃電池の酸化度を調整するために、キルン本体内に適量の酸化剤(例えば空気等)を導入する。例えばリチウムイオン電池の正極材料には、アルミ箔が使用されている。また、負極材料としては、カーボンが用いられている。更に電池の外部シェルは鉄製或いはアルミニウム製であり、集合電池の外部パッケージにはプラスチックが用いられている。これらの材質は基本的に還元剤として作用する。このためこれらの材料をガスやスラグ化するトータルの反応は酸化反応になる。そのため、キルン本体内に酸素導入が必要となる。予備酸化工程ST20において空気を導入しているのはこのためである。
【0031】
酸化剤は特に限定されないが、取り扱いが容易な点から、空気、純酸素、酸素富化気体等の酸素を含む気体等が好ましく用いられる。これらは予備酸化工程ST20においてキルン本体10内に直接送り込まれる。なお、ここでの酸化剤の導入量については、酸化処理の対象となる各物質の酸化に必要な化学当量の1.2倍程度が目安となる。
【0032】
本発明における予備酸化工程ST20は、熔融工程ST21内で酸化処理を行う場合と比べて、より低温での酸化処理であるため、反応速度が比較的緩やかであり、また、キルン本体の空間内に所定量の酸素を直接導入することにより、キルン本体内を移動していく廃電池を酸化させる方法であるため、酸素量、酸化時間及び温度の調整等により、酸化の制御が容易である。よって、酸化のばらつきを抑えて、より厳密な酸化度の調整を行うことが可能である。
【0033】
予備酸化工程ST20における酸化度の調整は以下のように行う。廃電池の材料を構成する主要元素は、酸素との親和力の差により一般的に、アルミニウム>リチウム>炭素>マンガン>リン>鉄>コバルト>ニッケル>銅、の順に酸化されていく。すなわちアルミニウムが最も酸化され易く、銅が最も酸化されにくい。予備酸化工程ST20においては、まずアルミニウムの全量が酸化するまで酸化を促進させる。このとき、更に、鉄の一部が酸化されるまで酸化を促進させてもよいが、コバルトが酸化されてスラグ側へ回収されてしまわない程度の酸化度に止めることが必要である。前述した通り、予備酸化工程ST20においては、酸素量、酸化時間及び温度の調整等により、そのような厳密な酸化度の調整が可能となっている。このように酸化度を調整することによって、スラグ分離工程ST22において酸化アルミニウムのほぼ全量をスラグとして分離することができる。
【0034】
なお、本発明における酸化工程は上記の焙焼による予備酸化工程ST20には限定されず、熔融工程ST21において、熔融物内にまた酸素を吹き込むための金属製チューブであるランスを挿入して空気等の酸化剤を吹き込むバブリングによって行ってもよい。これが、本発明における、「前記熔融工程時の前記熔融物に対して、行われ、前記廃電池を酸化処理する酸化工程」に該当する。
【0035】
<熔融工程ST21>
乾式工程S20においては、予備酸化工程ST20で予備酸化処理の行われた廃電池を1450℃以上、好ましくは1650℃以下の温度で熔融して廃電池の熔融物を得る熔融工程ST21をまず行う。熔融工程ST21は従来公知の電気炉等で行うことができる。熔融工程ST21によって、生成される熔融物には、アルミニウム等の酸化物を含有するスラグと、有価金属たるニッケル、コバルト、銅と、有価金属ではない鉄を含む合金とが含まれる。予備酸化工程ST20を行った場合、従来のように熔融工程ST21において熔融した廃電池に酸化処理を行う必要はない。
【0036】
ただし、予備酸化工程ST20における酸化が不足している場合や、その他、酸化度の調整が必要な場合には、熔融工程ST21において、微小時間の追加酸化処理を行う追加酸化工程を設けることができる。この追加酸化工程により、より微細に適切な酸化度の制御が可能となる。また、追加酸化工程は、従来の熔融時の酸化処理と比較して微少な時間で行うことができるため作業効率への悪影響は少なく、ランスの消耗も少なくて済むのでコストアップの問題も生じにくい。
【0037】
熔融工程ST21では、廃電池の熔融物にSiO2(二酸化珪素)及びCaO(石灰)等をフラックスとして添加する。ここでのSiO2/CaOの比は好ましくは0.5から1.5、より好ましく0.8から1.1の間である。これにより、後述するスラグ分離工程ST22で分離されるスラグの熔融温度を低下させることができる。このフラックスの添加は、必ずしも熔融工程ST21において行う必要はなく、熔融工程ST21に先行する予備酸化工程ST20において行っても同様の効果を得ることが可能である。なお、熔融工程ST21における粉塵や排ガス等は、従来公知の排ガス処理において無害化処理が施される。
【0038】
熔融工程ST21によって、鉄やアルミニウム等の酸化物であるスラグと、有価金属たるニッケル、コバルト、銅の合金とが生成する。両者は比重が異なるために、それぞれスラグ分離工程ST22、合金分離工程ST23でそれぞれ回収される。このとき、スラグ中の酸化アルミニウムの含有量が相対的に多いと高融点で高粘度のスラグとなるが、上記のように熔融工程ST21においてスラグの融点低下のためにSiO2及びCaOを添加しているために、スラグの融点低下による低粘性化を図ることができる。このためスラグ分離工程ST22を効率的に行なうことができる。なお、熔融工程ST21における粉塵や排ガス等は、従来公知の排ガス処理ST24において無害化処理される。
【0039】
<脱リン工程ST25>
合金分離工程ST23を経た後、更に得られた合金対して、本発明の特徴的な工程である脱リン工程ST25を行う。リチウムイオン電池においては、有機溶剤に炭酸エチレンや炭酸ジエチル等、リチウム塩としてLiPF6(ヘキサフルオロリン酸リチウム)等が電解質として使用される。このLiPF6中のリンは比較的酸化され易い性質を有するものの、鉄、コバルト、ニッケル等鉄族元素との親和力も比較的高い性質がある。合金中のリンは、乾式処理で得た合金から各元素を金属として回収する後工程の湿式工程での除去が難しく、不純物として処理系内に蓄積するために操業の継続ができなくなる。このため、この脱リン工程ST25で除去する。
【0040】
以下、脱リン工程ST25の具体的な実施方法について説明する。先ず、合金分離工程ST23を経た合金を、炉の傾転或いはタップによりスラグと分離し、レードル等の保温容器に受ける。
【0041】
分離した合金上に石灰含有物を添加し、ランス等で酸素含有ガスを吹くことにより、合金中のリンを酸化してCaO中に吸収させる。ここで、本発明における石灰含有物の定義とは広義の石灰を意味し、具体的には、反応により生石灰CaOを生じるものであればよく、生石灰CaOや消石灰Ca(OH)2のみならず、CaCo3等のカルシウム塩も含まれる。
【0042】
石灰含有物の添加量は、処理を行う容器の形状により適宜調整すればよいが、容器内の熔融合金の表面を覆う量は必要である。一般に、合金質量に対し、CaO質量で0.1質量%〜8質量%程度であることが好ましい。
【0043】
脱リン工程ST25においては、上記の石灰含有物に加えてCaF2を更に添加することが更に好ましい。CaF2を添加する場合には、CaO:CaF2=40:60〜5:95質量%の比で添加することが好ましい。この範囲の比でCaF2を添加することにより、フラックスの融点が低下して石灰含有物やCaF2が熔融状態となって上記の合金に吸収され易くなるので好ましい。
【0044】
酸素含有ガスについては、空気、酸素付加空気、純酸素のいずれでもあってもよい。反応によりCaOを生じる石灰等を添加し、酸素含有ガスを吹き込むことで合金中のリンを酸化してCaO中に吸収させることができる。
【0045】
必要酸素量は、合金中に含有されるリンの量によって適宜調整すればよい。又、マンガン系バッテリーを処理して合金中にMnが含まれる場合には、リンに優先して酸化されるため、その分の酸素量が必要となる。この場合、Mnは、ほぼ全量がフラックスに吸収され、MnO−CaO−CaF2系スラグとなる。この処理は、傾転によりスラグを炉内で合金と分離できる場合、合金製造炉内で行ってもよい。
【0046】
このようにして得られる合金は、廃電池がリチウムイオン電池の場合、正極材物質由来のコバルト、ニッケル、電解質由来のリチウム、負極材導電物質由来の銅等が成分となる。
【0047】
<合金ショット化工程ST26>
乾式工程S20の最後に、合金ショット化工程ST26を行う。この工程において、脱リン工程ST25を経た合金を冷却する際に、粒状物(ショット化合金又は単にショットともいう)とする。
【0048】
後述するように、乾式工程S20を広義の前処理とすることで不純物の少ない合金を得るとともに湿式工程S30に投入する処理量も大幅に減らすことで、乾式工程S20と湿式工程S30とを組み合わせることが可能である。しかしながら、湿式工程S30は基本的に大量処理に向かない複雑なプロセスであるので、乾式工程S20と組み合わせるためには湿式工程S30の処理時間、なかでも溶解工程ST31を短時間で行う必要がある。合金ショット化工程ST26により、合金を粒状物化することにより、溶解時間を短縮することができる。
【0049】
ここで、粒状物とは、表面積で言えば平均表面積が1mm2から300mm2であることが好ましく、平均質量で言えば0.4mgから2.2gの範囲であることが好ましい。この範囲の下限未満であると、粒子が細かすぎて取り扱いが困難になること、更に反応が早すぎて過度の発熱により一度に溶解することができ難くなるという問題が生じるので好ましくなく、この範囲の上限を超えると、後の湿式工程での溶解速度が低下するので好ましくない。合金をショット化して粒状化する方法は、従来公知の流水中への熔融金属の流入による急冷という方法を用いることができる。
【0050】
<湿式工程S30>
【0051】
廃電池からの有価金属回収プロセスは、特許文献1及び2のように合金として回収したままでは意味がなく、有価金属元素として回収する必要がある。廃電池を乾式工程で予め処理することによって、上記のような有価金属のみの合金とすることで、後の湿式工程を単純化することができる。このとき、この湿式での処理量は投入廃電池の量にくらべて質量比で1/4から1/3程度まで少なくなっていることも湿式工程との組み合わせを有利にする。
【0052】
このように、乾式工程S20を広義の前処理とすることで不純物の少ない合金を得るとともに処理量も大幅に減らすことで、乾式工程S20と湿式工程S30を組み合わせることが工業的に可能である。
【0053】
湿式工程S30は従来公知の方法を用いることができ、特に限定されない。一例を挙げれば、廃電池がリチウムイオン電池の場合の、コバルト、ニッケル、銅、鉄からなる合金の場合、酸溶解(溶解工程ST31)の後、脱鉄、銅分離回収、ニッケル/コバルト分離、ニッケル回収及び、コバルト回収という手順で元素分離工程ST32を経ることにより有価金属元素を回収することができる。
【0054】
<処理量>
本発明の方法は大量処理に向く乾式工程と少量処理に向く湿式工程を組み合わせた従来にない廃電池のリサイクル方法である。そして、乾式工程を最初に行なうために大量処理が可能である。少なくとも1日あたり1t以上、好ましくは1日あたり10t以上である場合に本発明を好適に使用できる。
【0055】
廃電池の種類は特に限定されないが、コバルトやリチウムという稀少金属が回収でき、その使用用途も自動車用電池等に拡大されており、大規模な回収工程が必要となるリチウムイオン電池が本発明の処理対象として好ましく例示できる。
【実施例】
【0056】
以下、実施例及び比較例により本発明を更に具体的に説明するが、本発明は、以下の実施例に限定されるものではない。
【0057】
試料として、リチウムイオン電池を熔融して鉄を適正に酸化して除去した時に、生成される合金と同様の組成に調合した金属を全体量で100g用意し、金属試料とした。金属試料の組成は、Co=53%、Ni=3%、Fe=24%、Cu=19%、P=1%である。Ni,Co,Cuは金属を、Pはリン化鉄を用い、リン化鉄で不足したFe分には金属鉄を使用した。
【0058】
金属試料をアルミナ製るつぼに投入し、るつぼ内を窒素雰囲気下で1500℃に保持し、金属試料が均一に溶融したことを確認した後に、石英チューブと注射器を用いて、金属試料の一部を脱リン処理前のサンプルとして採取した。アルミナ製るつぼは、外径42mm×高さ50mm、容積40mlの円筒状のるつぼ(ニッカトー製:C2るつぼ)を用いた。
【0059】
続いて、試薬として、CaO:3g、CaF2:4gを混合し、薬包紙に包んで、熔融金属上に投入した。その後、アルミナ製チューブを通じて、酸素を2l/minの流量で熔融金属浴中に3分間吹き込んだ後に、石英チューブと注射器を用いて、金属試料の一部を脱リン処理後のサンプルとして採取した。
【0060】
採取した処理前後のサンプルを酸で溶解し、ICPを用いて元素の分析を行った。その結果を表1に示す。
【0061】
【表1】

【0062】
表1に示す通り、本発明に係る脱リン工程による処理を施した後には、合金に含有される各元素のうち、リンの含有量のみが低減している。又、同処理後、その他の含有成分であるコバルト等の有価金属については全く低減がみられなかった。この結果より、使用済みリチウムイオン電池の廃電池からニッケル、コバルト及び銅を含む有価金属を回収するプロセスにおいて、熔融炉に装入して熔融・還元し、合金を得る処理において、合金上に石灰含有物を添加し、ランス等で含酸素含有ガスを吹きこむことにより、合金中のリンを効果的に除去できることが分かる。
【符号の説明】
【0063】
ST10 廃電池前処理工程
ST20 予備酸化工程
S20 乾式工程
ST21 熔融工程
ST22 スラグ分離工程
ST23 合金分離工程
ST24 排ガス処理
ST25 脱リン工程
ST26 合金ショット化工程
S30 湿式工程
ST31 溶解工程
ST32 元素分離工程
【技術分野】
【0001】
本発明は、例えばリチウムイオン電池の廃電池に含有する有価金属を回収する方法に関し、更に詳しくは、そのような有価金属の回収プロセスにおいて、有価金属の回収率に悪影響を与えることなく、有価金属を含有する合金から不要なリンのみを除去することのできる有価金属回収方法に関する。
【背景技術】
【0002】
リチウムイオン電池等の、使用済み或いは工程内の不良品である電池(以下廃電池という)をリサイクルし、含有する有価金属を回収しようとする処理方法には、大きく分けて乾式法と湿式法がある。
【0003】
乾式法は、破砕した廃電池を熔融処理し、コバルト、ニッケル、銅に代表される回収対象である有価金属と、鉄やアルミニウムに代表される付加価値の低いその他の金属等とを、それらの間の酸素親和力の差を利用して分離回収するものである。すなわち、鉄等の付加価値の低い元素を極力酸化してスラグとし、かつコバルト等の有価物は酸化を極力抑制して合金として回収するものである。
【0004】
例えば、特許文献1には、高温の加熱炉を使用し、廃電池にフラックスを添加し、スラグを分離する処理を繰り返すことで有価金属であるニッケルやコバルトを80%前後回収できる方法が開示されている。
【0005】
又、特許文献2には、スラグ分離のための熔融処理に先行して、廃電池を非酸化性雰囲気で加熱して炭素を除去する脱炭素工程を行うことによって、有価金属であるニッケルやコバルトの回収率を向上できる方法が開示されている。
【0006】
ここで、リチウムイオン電池の電解質はエチレンカーボネート(EC)/ジエチルカーボネート(DEC)/ジメチルカーボネート(DMC)等の混合有機溶剤にLiPF6を混合したものが通常用いられている。このLiPF6中のP(リン)は、比較的酸化され易い性質を有するものの、鉄、コバルト、ニッケル等鉄族元素との親和力も比較的高い性質がある。
【0007】
リチウムイオン電池の乾式法による処理によって生じる合金中には、ニッケル、コバルト、鉄というFe系元素が含まれていることから、鉄鋼製錬時と同様に一部のリンが合金中に含まれることになる。合金中に存在するリンは、乾式法による工程で得た合金から各元素を金属として回収する後工程の湿式法による工程での除去が難しく、不純物として処理系内に蓄積する。そのため、操業の継続が困難となる。
【0008】
そのために、有価金属であるニッケルやコバルトを回収するための有価金属回収方法においては、乾式工程でのリンの除去が必要となる。例えば、鉄鋼製錬においては、特許文献3に記載されているように、転炉操業時に鋳鉄溶湯中に酸化剤及び石灰系フラックスを添加してリンを除去する脱リン処理が行われている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】米国特許第7169206号公報
【特許文献2】特開2002−327215号公報
【特許文献3】特開2002−285220号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
しかしながら、特許文献3に開示されている脱リン方法においては、リンを酸化させる一方で、ニッケルやコバルト等の有価金属については酸化を適度に抑制することについては何らの考慮もなされていない。このため、特許文献3に開示されている方法をリチウムイオン電池から有価金属を回収するプロセスに適用すると、脱リンのプロセスが有価金属の回収率を下げる要因となってしまう。一方、特許文献1及び特許文献2においては、リチウムイオン電池を乾式処理して得られた合金からの脱リンの処理方法については何ら開示されていない。有価金属であるニッケルやコバルトを回収するための有価金属回収方法においては、ニッケル、コバルト等の有価金属の高い回収率を保持しつつ、効率よく脱リンを行うことのできる有価金属の回収方法が新たに求められているのが現状であった。
【0011】
本発明は、リチウムイオン電池の廃電池からニッケル、コバルトを含む有価金属を回収する有価金属回収プロセスにおいて、有価金属の回収率を落とさずに、有価金属を含む合金の脱リン処理を行うことのできる有価金属回収方法を提供することを目的とする。
【課題を解決するための手段】
【0012】
本発明者らは、有価金属回収プロセスにおける脱リン工程を、有価金属を含む合金に所定の石灰含有物を添加し、次いで、当該合金を酸化する工程とすることによって、有価金属の回収率を低下させることなく、有価金属を含む合金の脱リン処理を行うことができることを見出し、本発明を完成するに至った。より具体的には、本発明は以下のものを提供する。
【0013】
(1) ニッケルとコバルトを含有する金属複合体から、該ニッケルと該コバルトを含む有価金属を回収する有価金属回収方法であって、前記金属複合体を熔融して熔融物を得る熔融工程と、前記熔融工程時の前記熔融物に対して、又は、前記熔融工程前の前記金属複合体に対して行われ、前記金属複合体を酸化処理する酸化工程と、前記熔融物から、スラグを分離して、有価金属を含む合金を回収するスラグ分離工程と、前記合金に含有されるリンを分離する脱リン工程と、を備え、前記脱リン工程は、前記合金に石灰含有物を添加し、次いで、前記合金を酸化する工程である有価金属回収方法。
【0014】
(2) 前記石灰含有物が消石灰、炭酸カルシウム、酸化カルシウムのうちの少なくとも1種類を含むものである(1)に記載の有価金属回収方法。
【0015】
(3) 前記石灰含有物の添加量が、酸化カルシウム質量に換算した場合に、前記合金質量に対して0.1質量%以上8質量%以下の範囲である(1)又は(2)のいずれかに記載の有価金属回収方法。
【0016】
(4) 前記脱リン工程において、前記石灰含有物を添加する際に、フッ化カルシウムを併せて添加する(1)から(3)のいずれかに記載の有価金属回収方法。
【0017】
(5) 酸化カルシウムに換算した前記石灰含有物の添加量と前記フッ化カルシウムの添加量との比率が40:60から5:95の範囲である(4)に記載の有価金属回収方法。
【0018】
(6) 前記金属複合体がリチウムイオン電池である(1)から(5)のいずれかに記載の有価金属回収方法。
【発明の効果】
【0019】
本発明によれば、リチウムイオン電池の廃電池等からニッケル、コバルトを含む有価金属を回収する有価金属回収プロセスにおいて、有価金属の回収率に悪影響を与えることなく脱リン処理を行うことにより、高い回収率で有価金属を回収することができる。
【図面の簡単な説明】
【0020】
【図1】本発明の一例である、廃電池からの有価金属回収方法を示すフローチャートである。
【発明を実施するための形態】
【0021】
以下、本発明の一実施形態について図面を参照しながら説明する。図1は、金属複合体からの有価金属回収方法の一例を示すフローチャートである。本実施形態においては、金属複合体がリチウムイオン電池の廃電池である場合について説明するが、本発明はこれに限定されるものではない。
【0022】
<全体プロセス>
図1に示すように、この有価金属回収方法は、廃電池前処理工程ST10と、予備酸化工程ST20と、乾式工程S20と、湿式工程S30とからなる。このように、本実施例における有価金属回収方法は乾式工程S20において合金を得て、その後に湿式工程S30によって有価金属元素を分離回収するトータルプロセスである。なお、本発明における廃電池とは、使用済み電池のみならず、工程内の不良品等も含む意味である。また、処理対象に廃電池を含んでいればよく、廃電池以外のその他の金属や樹脂等を適宜加えることを排除するものではない。その場合にはその他の金属や樹脂を含めて本発明の廃電池である。
【0023】
<廃電池前処理工程ST10>
廃電池前処理工程ST10は、廃電池の爆発防止を目的として行われる。すなわち、廃電池は密閉系であり内部に電解液等を有しているため、このまま乾式の熔融処理を行うと爆発の恐れがあり危険である。このため、何らかの方法でガス抜きのための開孔処理を施す必要がある。これが廃電池前処理工程ST10を行う目的である。
【0024】
廃電池前処理工程ST10の具体的な方法は特に限定されないが、例えば針状の刃先で廃電池に物理的に開孔すればよい。なお、本発明においては後の乾式処理において熔融工程を経るために、個々の部材の分離等は不要である。
【0025】
<予備酸化工程ST20>
【0026】
この予備酸化工程ST20は、本発明における酸化工程の好ましい工程であり、本発明における、「前記熔融工程前の前記廃電池に対して行われ、前記廃電池を酸化処理する酸化工程」に該当する。
【0027】
予備酸化工程ST20においては、廃電池前処理工程ST10で得られた前処理済廃電池を600℃〜1250℃の温度で焙焼しながら酸素を供給することにより予備酸化処理を行う。従来の有価金属回収方法においては、乾式工程における熔融工程内で酸化処理を行っていたが、本発明の有価金属回収方法においては、熔融工程ST21の前に予備酸化工程ST20を設けて、当該工程内において予備酸化処理を行うことにより、より好ましい態様での実施が可能である。
【0028】
この予備酸化処理は、熔融工程ST21を行う前の段階に行うものであり、熔融工程ST21を行う溶融炉とは別途に予備酸化炉を設けて当該予備酸化炉内において行う。この予備酸化炉としては、予備酸化工程ST20において廃電池を焙焼しながら酸素を供給することにより、その内部で酸化処理を行うことが可能であるあらゆる形式のキルンを用いることができる。一例として、従来よりセメント製造等に用いられているロータリーキルン、又はトンネルキルン(ハースファーネス)を好適に用いることができる。
【0029】
キルンを用いた予備酸化工程ST20においては、まず、キルン本体の内部温度を600〜1250℃となるように加熱する。廃電池は攪拌、焙焼されながらキルン本体内を排出口の方向に向かって移動してゆく。このとき、キルン本体内の温度が600℃未満であるとアルミニウムや炭素の酸化が充分に進まず好ましくない。上記温度が600℃以上から1250℃の範囲であれば、アルミニウムや炭素の酸化は充分に進む一方で、鉄の酸化は相対的に低い酸化度に止まるため、後のスラグ分離工程において酸化アルミニウムを好適にスラグ分離できる。また、上記温度が、1250℃を超えると、主に廃電池の外部シェルに用いられている鉄等の一部がキルン本体の内壁等に付着してしまい、円滑な操業の妨げになったり、或いはキルン自体の劣化につながる場合があり好ましくない。
【0030】
上述した通り、600〜1250℃の温度で焙焼されながらキルン本体内を移動してゆく廃電池の酸化度を調整するために、キルン本体内に適量の酸化剤(例えば空気等)を導入する。例えばリチウムイオン電池の正極材料には、アルミ箔が使用されている。また、負極材料としては、カーボンが用いられている。更に電池の外部シェルは鉄製或いはアルミニウム製であり、集合電池の外部パッケージにはプラスチックが用いられている。これらの材質は基本的に還元剤として作用する。このためこれらの材料をガスやスラグ化するトータルの反応は酸化反応になる。そのため、キルン本体内に酸素導入が必要となる。予備酸化工程ST20において空気を導入しているのはこのためである。
【0031】
酸化剤は特に限定されないが、取り扱いが容易な点から、空気、純酸素、酸素富化気体等の酸素を含む気体等が好ましく用いられる。これらは予備酸化工程ST20においてキルン本体10内に直接送り込まれる。なお、ここでの酸化剤の導入量については、酸化処理の対象となる各物質の酸化に必要な化学当量の1.2倍程度が目安となる。
【0032】
本発明における予備酸化工程ST20は、熔融工程ST21内で酸化処理を行う場合と比べて、より低温での酸化処理であるため、反応速度が比較的緩やかであり、また、キルン本体の空間内に所定量の酸素を直接導入することにより、キルン本体内を移動していく廃電池を酸化させる方法であるため、酸素量、酸化時間及び温度の調整等により、酸化の制御が容易である。よって、酸化のばらつきを抑えて、より厳密な酸化度の調整を行うことが可能である。
【0033】
予備酸化工程ST20における酸化度の調整は以下のように行う。廃電池の材料を構成する主要元素は、酸素との親和力の差により一般的に、アルミニウム>リチウム>炭素>マンガン>リン>鉄>コバルト>ニッケル>銅、の順に酸化されていく。すなわちアルミニウムが最も酸化され易く、銅が最も酸化されにくい。予備酸化工程ST20においては、まずアルミニウムの全量が酸化するまで酸化を促進させる。このとき、更に、鉄の一部が酸化されるまで酸化を促進させてもよいが、コバルトが酸化されてスラグ側へ回収されてしまわない程度の酸化度に止めることが必要である。前述した通り、予備酸化工程ST20においては、酸素量、酸化時間及び温度の調整等により、そのような厳密な酸化度の調整が可能となっている。このように酸化度を調整することによって、スラグ分離工程ST22において酸化アルミニウムのほぼ全量をスラグとして分離することができる。
【0034】
なお、本発明における酸化工程は上記の焙焼による予備酸化工程ST20には限定されず、熔融工程ST21において、熔融物内にまた酸素を吹き込むための金属製チューブであるランスを挿入して空気等の酸化剤を吹き込むバブリングによって行ってもよい。これが、本発明における、「前記熔融工程時の前記熔融物に対して、行われ、前記廃電池を酸化処理する酸化工程」に該当する。
【0035】
<熔融工程ST21>
乾式工程S20においては、予備酸化工程ST20で予備酸化処理の行われた廃電池を1450℃以上、好ましくは1650℃以下の温度で熔融して廃電池の熔融物を得る熔融工程ST21をまず行う。熔融工程ST21は従来公知の電気炉等で行うことができる。熔融工程ST21によって、生成される熔融物には、アルミニウム等の酸化物を含有するスラグと、有価金属たるニッケル、コバルト、銅と、有価金属ではない鉄を含む合金とが含まれる。予備酸化工程ST20を行った場合、従来のように熔融工程ST21において熔融した廃電池に酸化処理を行う必要はない。
【0036】
ただし、予備酸化工程ST20における酸化が不足している場合や、その他、酸化度の調整が必要な場合には、熔融工程ST21において、微小時間の追加酸化処理を行う追加酸化工程を設けることができる。この追加酸化工程により、より微細に適切な酸化度の制御が可能となる。また、追加酸化工程は、従来の熔融時の酸化処理と比較して微少な時間で行うことができるため作業効率への悪影響は少なく、ランスの消耗も少なくて済むのでコストアップの問題も生じにくい。
【0037】
熔融工程ST21では、廃電池の熔融物にSiO2(二酸化珪素)及びCaO(石灰)等をフラックスとして添加する。ここでのSiO2/CaOの比は好ましくは0.5から1.5、より好ましく0.8から1.1の間である。これにより、後述するスラグ分離工程ST22で分離されるスラグの熔融温度を低下させることができる。このフラックスの添加は、必ずしも熔融工程ST21において行う必要はなく、熔融工程ST21に先行する予備酸化工程ST20において行っても同様の効果を得ることが可能である。なお、熔融工程ST21における粉塵や排ガス等は、従来公知の排ガス処理において無害化処理が施される。
【0038】
熔融工程ST21によって、鉄やアルミニウム等の酸化物であるスラグと、有価金属たるニッケル、コバルト、銅の合金とが生成する。両者は比重が異なるために、それぞれスラグ分離工程ST22、合金分離工程ST23でそれぞれ回収される。このとき、スラグ中の酸化アルミニウムの含有量が相対的に多いと高融点で高粘度のスラグとなるが、上記のように熔融工程ST21においてスラグの融点低下のためにSiO2及びCaOを添加しているために、スラグの融点低下による低粘性化を図ることができる。このためスラグ分離工程ST22を効率的に行なうことができる。なお、熔融工程ST21における粉塵や排ガス等は、従来公知の排ガス処理ST24において無害化処理される。
【0039】
<脱リン工程ST25>
合金分離工程ST23を経た後、更に得られた合金対して、本発明の特徴的な工程である脱リン工程ST25を行う。リチウムイオン電池においては、有機溶剤に炭酸エチレンや炭酸ジエチル等、リチウム塩としてLiPF6(ヘキサフルオロリン酸リチウム)等が電解質として使用される。このLiPF6中のリンは比較的酸化され易い性質を有するものの、鉄、コバルト、ニッケル等鉄族元素との親和力も比較的高い性質がある。合金中のリンは、乾式処理で得た合金から各元素を金属として回収する後工程の湿式工程での除去が難しく、不純物として処理系内に蓄積するために操業の継続ができなくなる。このため、この脱リン工程ST25で除去する。
【0040】
以下、脱リン工程ST25の具体的な実施方法について説明する。先ず、合金分離工程ST23を経た合金を、炉の傾転或いはタップによりスラグと分離し、レードル等の保温容器に受ける。
【0041】
分離した合金上に石灰含有物を添加し、ランス等で酸素含有ガスを吹くことにより、合金中のリンを酸化してCaO中に吸収させる。ここで、本発明における石灰含有物の定義とは広義の石灰を意味し、具体的には、反応により生石灰CaOを生じるものであればよく、生石灰CaOや消石灰Ca(OH)2のみならず、CaCo3等のカルシウム塩も含まれる。
【0042】
石灰含有物の添加量は、処理を行う容器の形状により適宜調整すればよいが、容器内の熔融合金の表面を覆う量は必要である。一般に、合金質量に対し、CaO質量で0.1質量%〜8質量%程度であることが好ましい。
【0043】
脱リン工程ST25においては、上記の石灰含有物に加えてCaF2を更に添加することが更に好ましい。CaF2を添加する場合には、CaO:CaF2=40:60〜5:95質量%の比で添加することが好ましい。この範囲の比でCaF2を添加することにより、フラックスの融点が低下して石灰含有物やCaF2が熔融状態となって上記の合金に吸収され易くなるので好ましい。
【0044】
酸素含有ガスについては、空気、酸素付加空気、純酸素のいずれでもあってもよい。反応によりCaOを生じる石灰等を添加し、酸素含有ガスを吹き込むことで合金中のリンを酸化してCaO中に吸収させることができる。
【0045】
必要酸素量は、合金中に含有されるリンの量によって適宜調整すればよい。又、マンガン系バッテリーを処理して合金中にMnが含まれる場合には、リンに優先して酸化されるため、その分の酸素量が必要となる。この場合、Mnは、ほぼ全量がフラックスに吸収され、MnO−CaO−CaF2系スラグとなる。この処理は、傾転によりスラグを炉内で合金と分離できる場合、合金製造炉内で行ってもよい。
【0046】
このようにして得られる合金は、廃電池がリチウムイオン電池の場合、正極材物質由来のコバルト、ニッケル、電解質由来のリチウム、負極材導電物質由来の銅等が成分となる。
【0047】
<合金ショット化工程ST26>
乾式工程S20の最後に、合金ショット化工程ST26を行う。この工程において、脱リン工程ST25を経た合金を冷却する際に、粒状物(ショット化合金又は単にショットともいう)とする。
【0048】
後述するように、乾式工程S20を広義の前処理とすることで不純物の少ない合金を得るとともに湿式工程S30に投入する処理量も大幅に減らすことで、乾式工程S20と湿式工程S30とを組み合わせることが可能である。しかしながら、湿式工程S30は基本的に大量処理に向かない複雑なプロセスであるので、乾式工程S20と組み合わせるためには湿式工程S30の処理時間、なかでも溶解工程ST31を短時間で行う必要がある。合金ショット化工程ST26により、合金を粒状物化することにより、溶解時間を短縮することができる。
【0049】
ここで、粒状物とは、表面積で言えば平均表面積が1mm2から300mm2であることが好ましく、平均質量で言えば0.4mgから2.2gの範囲であることが好ましい。この範囲の下限未満であると、粒子が細かすぎて取り扱いが困難になること、更に反応が早すぎて過度の発熱により一度に溶解することができ難くなるという問題が生じるので好ましくなく、この範囲の上限を超えると、後の湿式工程での溶解速度が低下するので好ましくない。合金をショット化して粒状化する方法は、従来公知の流水中への熔融金属の流入による急冷という方法を用いることができる。
【0050】
<湿式工程S30>
【0051】
廃電池からの有価金属回収プロセスは、特許文献1及び2のように合金として回収したままでは意味がなく、有価金属元素として回収する必要がある。廃電池を乾式工程で予め処理することによって、上記のような有価金属のみの合金とすることで、後の湿式工程を単純化することができる。このとき、この湿式での処理量は投入廃電池の量にくらべて質量比で1/4から1/3程度まで少なくなっていることも湿式工程との組み合わせを有利にする。
【0052】
このように、乾式工程S20を広義の前処理とすることで不純物の少ない合金を得るとともに処理量も大幅に減らすことで、乾式工程S20と湿式工程S30を組み合わせることが工業的に可能である。
【0053】
湿式工程S30は従来公知の方法を用いることができ、特に限定されない。一例を挙げれば、廃電池がリチウムイオン電池の場合の、コバルト、ニッケル、銅、鉄からなる合金の場合、酸溶解(溶解工程ST31)の後、脱鉄、銅分離回収、ニッケル/コバルト分離、ニッケル回収及び、コバルト回収という手順で元素分離工程ST32を経ることにより有価金属元素を回収することができる。
【0054】
<処理量>
本発明の方法は大量処理に向く乾式工程と少量処理に向く湿式工程を組み合わせた従来にない廃電池のリサイクル方法である。そして、乾式工程を最初に行なうために大量処理が可能である。少なくとも1日あたり1t以上、好ましくは1日あたり10t以上である場合に本発明を好適に使用できる。
【0055】
廃電池の種類は特に限定されないが、コバルトやリチウムという稀少金属が回収でき、その使用用途も自動車用電池等に拡大されており、大規模な回収工程が必要となるリチウムイオン電池が本発明の処理対象として好ましく例示できる。
【実施例】
【0056】
以下、実施例及び比較例により本発明を更に具体的に説明するが、本発明は、以下の実施例に限定されるものではない。
【0057】
試料として、リチウムイオン電池を熔融して鉄を適正に酸化して除去した時に、生成される合金と同様の組成に調合した金属を全体量で100g用意し、金属試料とした。金属試料の組成は、Co=53%、Ni=3%、Fe=24%、Cu=19%、P=1%である。Ni,Co,Cuは金属を、Pはリン化鉄を用い、リン化鉄で不足したFe分には金属鉄を使用した。
【0058】
金属試料をアルミナ製るつぼに投入し、るつぼ内を窒素雰囲気下で1500℃に保持し、金属試料が均一に溶融したことを確認した後に、石英チューブと注射器を用いて、金属試料の一部を脱リン処理前のサンプルとして採取した。アルミナ製るつぼは、外径42mm×高さ50mm、容積40mlの円筒状のるつぼ(ニッカトー製:C2るつぼ)を用いた。
【0059】
続いて、試薬として、CaO:3g、CaF2:4gを混合し、薬包紙に包んで、熔融金属上に投入した。その後、アルミナ製チューブを通じて、酸素を2l/minの流量で熔融金属浴中に3分間吹き込んだ後に、石英チューブと注射器を用いて、金属試料の一部を脱リン処理後のサンプルとして採取した。
【0060】
採取した処理前後のサンプルを酸で溶解し、ICPを用いて元素の分析を行った。その結果を表1に示す。
【0061】
【表1】

【0062】
表1に示す通り、本発明に係る脱リン工程による処理を施した後には、合金に含有される各元素のうち、リンの含有量のみが低減している。又、同処理後、その他の含有成分であるコバルト等の有価金属については全く低減がみられなかった。この結果より、使用済みリチウムイオン電池の廃電池からニッケル、コバルト及び銅を含む有価金属を回収するプロセスにおいて、熔融炉に装入して熔融・還元し、合金を得る処理において、合金上に石灰含有物を添加し、ランス等で含酸素含有ガスを吹きこむことにより、合金中のリンを効果的に除去できることが分かる。
【符号の説明】
【0063】
ST10 廃電池前処理工程
ST20 予備酸化工程
S20 乾式工程
ST21 熔融工程
ST22 スラグ分離工程
ST23 合金分離工程
ST24 排ガス処理
ST25 脱リン工程
ST26 合金ショット化工程
S30 湿式工程
ST31 溶解工程
ST32 元素分離工程
【特許請求の範囲】
【請求項1】
ニッケルとコバルトを含有する金属複合体から、該ニッケルと該コバルトを含む有価金属を回収する有価金属回収方法であって、
前記金属複合体を熔融して熔融物を得る熔融工程と、
前記熔融工程時の前記熔融物に対して、又は、前記熔融工程前の前記金属複合体に対して行われ、前記金属複合体を酸化処理する酸化工程と、
前記熔融物から、スラグを分離して、有価金属を含む合金を回収するスラグ分離工程と、
前記合金に含有されるリンを分離する脱リン工程と、を備え、
前記脱リン工程は、前記合金に石灰含有物を添加し、次いで、前記合金を酸化する工程である有価金属回収方法。
【請求項2】
前記石灰含有物が、消石灰、炭酸カルシウム、酸化カルシウムのうちの少なくとも1種類を含むものである請求項1に記載の有価金属回収方法。
【請求項3】
前記石灰含有物の添加量が、酸化カルシウム質量に換算した場合に、前記合金質量に対して0.1質量%以上8質量%以下の範囲である請求項1又は2のいずれかに記載の有価金属回収方法。
【請求項4】
前記脱リン工程において、前記石灰含有物を添加する際に、更にフッ化カルシウムを添加する請求項1から3のいずれかに記載の有価金属回収方法。
【請求項5】
酸化カルシウムに換算した前記石灰含有物の添加量と前記フッ化カルシウムの添加量との比率が40:60から5:95の範囲である請求項4に記載の有価金属回収方法。
【請求項6】
前記金属複合体がリチウムイオン電池の廃電池である請求項1から5のいずれかに記載の有価金属回収方法。
【請求項1】
ニッケルとコバルトを含有する金属複合体から、該ニッケルと該コバルトを含む有価金属を回収する有価金属回収方法であって、
前記金属複合体を熔融して熔融物を得る熔融工程と、
前記熔融工程時の前記熔融物に対して、又は、前記熔融工程前の前記金属複合体に対して行われ、前記金属複合体を酸化処理する酸化工程と、
前記熔融物から、スラグを分離して、有価金属を含む合金を回収するスラグ分離工程と、
前記合金に含有されるリンを分離する脱リン工程と、を備え、
前記脱リン工程は、前記合金に石灰含有物を添加し、次いで、前記合金を酸化する工程である有価金属回収方法。
【請求項2】
前記石灰含有物が、消石灰、炭酸カルシウム、酸化カルシウムのうちの少なくとも1種類を含むものである請求項1に記載の有価金属回収方法。
【請求項3】
前記石灰含有物の添加量が、酸化カルシウム質量に換算した場合に、前記合金質量に対して0.1質量%以上8質量%以下の範囲である請求項1又は2のいずれかに記載の有価金属回収方法。
【請求項4】
前記脱リン工程において、前記石灰含有物を添加する際に、更にフッ化カルシウムを添加する請求項1から3のいずれかに記載の有価金属回収方法。
【請求項5】
酸化カルシウムに換算した前記石灰含有物の添加量と前記フッ化カルシウムの添加量との比率が40:60から5:95の範囲である請求項4に記載の有価金属回収方法。
【請求項6】
前記金属複合体がリチウムイオン電池の廃電池である請求項1から5のいずれかに記載の有価金属回収方法。
【図1】




【公開番号】特開2013−91826(P2013−91826A)
【公開日】平成25年5月16日(2013.5.16)
【国際特許分類】
【出願番号】特願2011−234143(P2011−234143)
【出願日】平成23年10月25日(2011.10.25)
【出願人】(000183303)住友金属鉱山株式会社 (2,015)
【Fターム(参考)】
【公開日】平成25年5月16日(2013.5.16)
【国際特許分類】
【出願日】平成23年10月25日(2011.10.25)
【出願人】(000183303)住友金属鉱山株式会社 (2,015)
【Fターム(参考)】
[ Back to top ]

