有機発光素子及びその製造方法、並びに表示装置
【課題】高効率かつ長寿命の有機発光素子を提供する。
【解決手段】陽極2と陰極6と、陽極2と陰極6との間に挟持され少なくとも第一の有機化合物層(正孔注入層3)と、第二の有機化合物層(正孔輸送層4)と、第三の有機化合物層(発光層5)とがこの順に含まれる積層体と、から構成され、
第1の有機化合物層(正孔注入層3)にアリールアミンポリマーが含まれ、第2の有機化合物層(正孔輸送層4)にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする、有機発光素子10。
【解決手段】陽極2と陰極6と、陽極2と陰極6との間に挟持され少なくとも第一の有機化合物層(正孔注入層3)と、第二の有機化合物層(正孔輸送層4)と、第三の有機化合物層(発光層5)とがこの順に含まれる積層体と、から構成され、
第1の有機化合物層(正孔注入層3)にアリールアミンポリマーが含まれ、第2の有機化合物層(正孔輸送層4)にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする、有機発光素子10。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、有機発光素子及びその製造方法、並びに表示装置に関する。
【背景技術】
【0002】
有機発光素子を製造する場合、その製造プロセスは乾式法と湿式法とに分類される。乾式法とは、主に低分子系材料を使用し、真空蒸着法等の気相プロセスを用いて薄膜形成を行う方法である。これに対し湿式法とは、成膜工程において主に高分子系材料を使用し、スピン塗布法、インクジェット塗布法、ディスペンサー塗布法、スプレー塗布法、浸漬塗布法等の方法を用いて薄膜形成を行う方法である。
【0003】
ここで真空蒸着法等の乾式法は、生産装置がバッチ式であり、素子作製において素子の発光のために必要のない部分にも素子の構成材料からなる薄膜が形成される。このため必要量よりはるかに多くの材料が無駄に消費されてしまうことから、生産性の観点からすると課題のある方法であると言える。
【0004】
一方、湿式法を用いて有機発光素子を製造すると、連続式処理による生産が可能である。例えば、インクジェット塗布法、ディスペンサー塗布法のように液滴吐出法によって塗布する塗布液の種類、位置等を選択することができる。これらの方法では、素子の必要とする部分にのみに選択して材料を塗り分けるという、いわゆるパターンニングが可能となり、生産性を大幅に改善することができる。
【0005】
このため昨今においては、有機発光素子を構成する電荷注入層、電荷輸送層、発光層等の有機化合物層を、生産性のよい塗布法を用いて成膜することに関心が高まっている。
【0006】
例えば、正孔注入層を塗布法で形成する場合、使用される正孔注入層の構成材料(正孔注入材料)として、ポリ(3,4−エチレンジオキシチオフェン)とポリスチレンスルホン酸の混合物(PEDOT/PSS)が知られている(非特許文献1参照)。このPEDOT/PSSは水溶性であるので、PEDOT/PSS膜から上の層となる薄膜を形成する際は、その層の構成材料を有機溶媒に溶解して調製した塗布液を使用し、塗布法を用いることで薄膜を形成し、その薄膜を積層することができる。しかし、このPEDOT/PSSを使用した有機発光素子は、初期特性に優れるが長時間使用した場合に輝度劣化が著しいことが問題である。この輝度劣化を改善するために、PEDOT/PSS膜と発光層との間に不溶性の重合体である中間層を組み込んだ有機発光素子が報告されている(特許文献1及び2参照)。
【0007】
一方で、有機発光素子の高効率化及び耐久性向上のためには、複数の有機化合物層が積層した素子構造とすることが有効である。ここで、塗布法で有機化合物層を積層する場合は、下地となる有機化合物層上に次の層の構成材料を含む溶液を塗布する際に、下地となる有機化合物層が溶解するという問題を回避する必要がある。ここで下地となる有機化合物層の溶解を防ぐ方法として、溶媒に対する溶解度の差を利用する方法が報告されている(特許文献3参照)。また架橋剤を使用して下地の有機化合物層である薄膜の架橋反応を誘起させて薄膜自体を不溶化する方法も報告されている(特許文献4及び5参照)。
【0008】
しかし溶媒に対する溶解度の差を利用する方法では、各層の構成材料の溶解性の観点から、積層のために利用できる溶媒が限定されるため、使用できる材料も自ずと制約されるという問題があった。また架橋剤を使用して不溶化する方法では、架橋剤が層を構成する材料の電荷輸送性に悪影響を及ぼすため、発光効率等の初期特性や長時間の発光による輝度劣化等の耐久特性が十分でないという問題があった。
【0009】
【特許文献1】特開2005−183404号公報
【特許文献2】特開2005−243300号公報
【特許文献3】特開平11−251065号公報
【特許文献4】特開平11−87605号公報
【特許文献5】特開2005−340042号公報
【非特許文献1】Appl.Phys.Lett.,75,1679(1999)
【発明の開示】
【発明が解決しようとする課題】
【0010】
本発明の目的は、高効率かつ長寿命の有機発光素子を提供することにある。また、本発明の他の目的は、塗布法により高効率かつ長寿命の有機発光素子を製造することを可能にするための有機発光素子の製造方法を提供することにある。
【課題を解決するための手段】
【0011】
本発明の有機発光素子は、陽極と陰極と、該陽極と該陰極との間に挟持され少なくとも第一の有機化合物層と、第二の有機化合物層と、第三の有機化合物層とがこの順に含まれる積層体と、から構成され、該陽極又は該陰極と該第一の有機化合物層と、該第一の有機化合物層と該第二の有機化合物層と、並びに該第二の有機化合物層と該第三の有機化合物層と、が互いに接しており、該第一の有機化合物層にアリールアミンポリマーが含まれ、該第二の有機化合物層にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする。
【発明の効果】
【0012】
本発明によれば、高効率かつ長寿命の有機発光素子を提供することができる。また、本発明によれば、塗布法により高効率かつ長寿命の有機発光素子を製造することを可能にするための有機発光素子の製造方法を提供することができる。
【発明を実施するための最良の形態】
【0013】
まず本発明の有機発光素子について説明する。本発明の有機発光素子は、陽極と陰極と、該陽極と該陰極との間に挟持され少なくとも第一の有機化合物層と、第二の有機化合物層と、第三の有機化合物層とがこの順に含まれる積層体と、から構成される。
【0014】
以下、図面を参照しながら本発明の有機発光素子を詳細に説明する。
【0015】
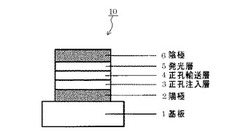
図1は、本発明の有機発光素子における第一の実施形態を示す断面図である。図1の有機発光素子10は、基板1上に陽極2、正孔注入層3、正孔輸送層4、発光層5及び陰極6が順次設けられている。
【0016】
図2は、本発明の有機発光素子における第二の実施形態を示す断面図である。図2の有機発光素子20は、図1の有機発光素子10において、発光層5と陰極6との間に電子注入層7が設けられている。
【0017】
図3は、本発明の有機発光素子における第三の実施形態を示す断面図である。図3の有機発光素子30は、図2の有機発光素子20において、発光層5と電子注入層7との間に電子輸送層8が設けられている。
【0018】
ただし、図1乃至図3はあくまでごく基本的な素子構成であり、本発明の有機発光素子の構成はこれらに限定されるものではない。例えば、電極と有機化合物層との界面に絶縁性層、接着層又は干渉層を設ける、正孔注入層又は正孔輸送層が異なる二層から構成される等多様な層構成をとることができる。尚、本発明の有機発光素子は、陽極又は陰極と第一の有機化合物層とが互いに接している。また、第一の有機化合物層と第二の有機化合物層とが互いに接している。さらに、第二の有機化合物層と第三の有機化合物層とが互いに接している。
【0019】
上記のように、本発明の有機発光素子は、有機化合物層を少なくとも3つ含むものである。有機化合物層として、例えば、正孔注入層、正孔輸送層、発光層、正孔/エキシトンブロッキング層、電子輸送層、電子注入層等が挙げられる。
【0020】
本発明の有機発光素子においては、第一の有機化合物層にアリールアミンポリマーが含まれ、第二の有機化合物層にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする。
【0021】
まず第一の有機化合物層に含まれるアリールアミンポリマーについて説明する。ここでいうアリールアミンポリマーは、好ましくは、下記一般式(1)で示されるポリマーである。
【0022】
【化1】

【0023】
式(1)において、R11及びR12は、それぞれ水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、アルコキシ基又はハロゲン原子を表す。
【0024】
R11及びR12で表されるアルキル基として、メチル基、エチル基、プロピル基、n−ブチル基等が挙げられる。
【0025】
R11及びR12で表されるアラルキル基として、ベンジル基、フェネチル基、ナフチルメチル基等が挙げられる。
【0026】
R11及びR12で表されるアリール基として、フェニル基、ビフェニルイル基、ターフェニルイル基等が挙げられる。
【0027】
R11及びR12で表されるアルコキシ基として、メトキシ基、エトキシ基、プロポキシ基等が挙げられる。
【0028】
R11及びR12で表されるハロゲン原子として、フッ素、塩素、臭素等が挙げられる。
【0029】
上記アルキル基、アラルキル基及びアリール基がさらに有してもよい置環基として、メチル基、エチル基、プロピル基、ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0030】
式(1)において、Ar11及びAr12は、それぞれ置換あるいは無置換のアリール基又は縮合多環芳香族基を表す。
【0031】
Ar11及びAr12で表されるアリール基として、フェニル基、ビフェニルイル基、ターフェニルイル基等が挙げられる。
【0032】
Ar11及びAr12で表される縮合多環芳香族基として、フルオレニル基、フルオランテニル基、ナフチル基、フェナントリル基、ジヒドロフェナントレニル基、ピレニル基、ペリレニル基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基等が挙げられる。
【0033】
上記アリール基及び縮合多環芳香族基がさらに有してもよい置環基として、メチル基、エチル基、n−プロピル基、n−ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0034】
式(1)において、Ar13は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。
【0035】
Ar13で表される2価のアリール基として、フェニレン基、ビフェニレン基、ターフェニレン基等が挙げられる。
【0036】
Ar13で表される2価の縮合多環芳香族基として、フルオレン、フルオランテン、ナフタレン、フェナントレン、ジヒドロフェナントレン、ピレン、ペリレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン等を基本骨格とする2価の置換基が挙げられる。
【0037】
上記アリール基及び縮合多環芳香族基がさらに有してもよい置環基として、メチル基、エチル基、n−プロピル基、n−ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0038】
式(1)において、Ar14は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。
【0039】
Ar14で表される2価のアリール基として、フェニレン基、ビフェニレン基等が挙げられる。
【0040】
Ar14で表される2価の縮合多環芳香族基として、フルオレン、フルオランテン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン、ピレン、ペリレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン等を基本骨格とする2価の置換基が挙げられる。
【0041】
上記アリール基及び縮合多環芳香族基がさらに有してもよい置環基として、メチル基、エチル基、n−プロピル基、n−ブチル基、tert−ブチル基、3−メチルブチル基、2−エチルヘキシル基、オクチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0042】
式(1)において、mは、10以上300以下の整数を表す。
【0043】
式(1)において、nは、0以上300以下の整数を表す。
【0044】
式(1)のアリールアミンポリマーは、mやnの数値によって、溶媒に対するポリマー自体の溶解度を適宜調整することが可能である。特に規定するものではないが、溶媒に対する十分な溶解性を高くできる点で、mは、好ましくは、10以上100以下である。同様に、nは、好ましくは、0以上100以下である。またポリマーの分子量は、当該ポリマーを合成する際の反応温度、反応溶媒、反応溶媒量、触媒等の様々な因子により決まる。
【0045】
式(1)のアリールアミンポリマーの具体例を、以下に示す。ただし、本発明はこれら具体例に限定されるものではない。
【0046】
【化2】

【0047】
【化3】

【0048】
【化4】

【0049】
【化5】

【0050】
【化6】

【0051】
【化7】

【0052】
【化8】

【0053】
【化9】

【0054】
【化10】

【0055】
【化11】

【0056】
【化12】

【0057】
次に、第二の有機化合物層に含まれる(メタ)アクリル酸エステルポリマーについて説明する。
【0058】
第二の有機化合物層に含まれる(メタ)アクリル酸エステルポリマーとは、アリールアミン骨格を有する(メタ)アクリル酸エステルポリマーであるが、好ましくは、下記一般式(2)で示されるポリマーである。
【0059】
【化13】

【0060】
式(2)において、A21及びA22は、それぞれ炭素数1以上8以下の2価の炭化水素基を表す。
【0061】
A21及びA22で表される炭素数1以上8以下の2価の炭化水素基として、メチレン基、エチレン基、プロピレン基、ブチレン基、ペンチレン基、オクチレン基等が挙げられる。これら2価の炭化水素基は、メチル基、エチル基、プロピル基、ブチル基等の分枝をさらに有していてもよい。また、炭素数が2以上の場合、これら2価の炭化水素基に含まれるメチレンのうち1つがエーテル結合に置換されていてもよい。
【0062】
式(2)において、Ar21及びAr22は、それぞれ置換あるいは無置換のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。
【0063】
Ar21及びAr22で表されるアリール基とは、ベンゼン環を2つ以上含む1価のアリール基をいう。例えば、ビフェニルイル基等が挙げられる。
【0064】
Ar21及びAr22で表される縮合多環芳香族基とは、ベンゼン環を2つ以上含む縮合多環芳香族基をいう。例えば、フルオレニル基、フルオランテニル基、ナフチル基、フェナントリル基、ジヒドロフェナントリル基、ピレニル基、ペリレニル基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基等が挙げられる。好ましくは、フルオレニル基である。
【0065】
上記のアリール基及び縮合多環芳香族基がさらに有してもよい置換基として、メチル基、エチル基、プロピル基、ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0066】
式(2)において、Ar23は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。
【0067】
Ar23で表される2価のアリール基とは、ベンゼン環を2つ以上含む2価のアリール基をいう。例えば、ビフェニレン基等が挙げられる。
【0068】
Ar23で表される2価の縮合多環芳香族基とは、ベンゼン環を2つ以上含む2価の縮合多環芳香族基をいう。例えば、フルオレン、フルオランテン、フェニルナフタレン、フェナントレン、ジヒドロフェナントレン、ピレン、ペリレン、ベンゾアントラセン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン等を基本骨格とした2価の置換基が挙げられる。
【0069】
上記の2価のアリール基及び2価の縮合多環芳香族基がさらに有してもよい置換基として、メチル基、エチル基、プロピル基、ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0070】
式(2)において、R21及びR22は、それぞれ水素原子又はメチル基を表す。
【0071】
式(2)の(メタ)アクリルポリマーは、特定の(メタ)アクリル酸エステル化合物を加熱重合することで得られるものである。尚、その(メタ)アクリル酸エステル化合物の具体的な構造については後述する。
【0072】
本発明の有機発光素子において、第一の有機化合物層に含まれるアリールアミンポリマー及び第二の有機化合物層に含まれる(メタ)アクリル酸エステル化合物は、いずれも電荷輸送機能に優れる特定のアリールアミン構造を含む化合物である。このように共通した部分構造を有する有機化合物を、互いに隣接する層にそれぞれ含ませることにより、電極からの電荷注入性や層内の電荷輸送性が向上する。
【0073】
また、アリールアミン骨格を有する化合物は、古くから正孔輸送性材料として知られており、電子供与性のアミンに由来してHOMOエネルギーを高く調節することが可能な物質である。有機発光素子において、HOMOエネルギーは、素子の発光効率や耐久性に強い影響を与えるパラメータであることが一般的に知られている。このため、式(1)のアリールアミンポリマーを含む第一の有機化合物層と、式(2)の(メタ)アクリル酸エステルポリマーを含む第二の有機化合物層と、の各々のHOMOエネルギーを特定の範囲内の値で微細に調整することが可能となる。このように、本発明の有機発光素子は、第一の有機化合物層と第二の有機化合物層とが隣接するように積層されている。このため同等のHOMOエネルギーを有する有機化合物層が隣接して積層している形式となり、層間における電荷注入性が向上される。
【0074】
次に、本発明の有機発光素子を構成する他の構成部材について説明する。
【0075】
陽極を構成する材料は、仕事関数がなるべく大きなものがよい。例えば、金、銀、白金、ニッケル、パラジウム、コバルト、セレン、バナジウム等の金属単体あるいはこれらを複数組み合わせた合金、酸化錫、酸化亜鉛、酸化錫インジウム(ITO),酸化亜鉛インジウム等の金属酸化物が使用できる。また、ポリアニリン、ポリピロール、ポリチオフェン、ポリフェニレンスルフィド等の導電性ポリマーも使用できる。これらの電極物質は、一種類を単独で使用してもよく、二種類以上を併用して使用してもよい。
【0076】
一方、陰極の構成材料は、仕事関数のなるべく小さなものがよい。例えば、リチウム、ナトリウム、カリウム、セシウム、カルシウム、マグネシウム、アルミニウム、インジウム、銀、鉛、錫、クロム等の金属単体、これら金属単体を複数組み合わせた合金又はこれら金属単体の塩等を使用することができる。また酸化錫インジウム(ITO)等の金属酸化物の利用も可能である。ここで、陰極は一層で構成されていてもよく、複数の層で構成されていてもよい。
【0077】
本発明の有機発光素子で使用する基板としては、特に限定するものではないが、金属製基板、セラミックス製基板等の不透明性基板、ガラス、石英、プラスチックシート等の透明性基板が用いられる。また、基板にカラーフィルター膜、蛍光色変換フィルター膜、誘電体反射膜等を用いて発色光をコントロールすることも可能である。
【0078】
尚、作製した有機発光素子に対して、酸素や水分等との接触を防止する目的で、保護層又は封止層を設けることもできる。保護層としては、ダイヤモンド薄膜、金属酸化物、金属窒化物等の無機材料膜、フッ素樹脂、ポリパラキシレン、ポリエチレン、シリコーン樹脂、ポリスチレン樹脂、エポキシ樹脂、フェノール樹脂、尿素樹脂等の高分子膜又は光硬化性樹脂等が挙げられる。また、ガラス、気体不透過性フィルム、金属等をカバーし、適当な封止樹脂により素子自体をパッケージングすることもできる。
【0079】
次に、本発明の有機発光素子の製造方法について説明する。
【0080】
本発明の有機発光素子の製造方法は、以下に示す工程を含むことを特徴とする。
(i)下部電極上に塗布法によりアリールアミンポリマーからなる第一の有機化合物層を形成する工程(以下、第一の工程という。)
(ii)第一の有機化合物層上に塗布法によりアリールアミン骨格を有する(メタ)アクリル酸エステル化合物からなる薄膜を形成する工程(以下、第二の工程という。)
(iii)第二の工程で形成した薄膜を加熱硬化して第二の有機化合物層を形成する工程(以下、第三の工程という。)
(iv)第二の有機化合物層上に塗布法により第三の有機化合物層を形成する工程(以下、第四の工程という。)
【0081】
まず第一の工程について説明する。第一の工程によって形成される第一の有機化合物層を構成するアリールアミンポリマーとは、式(1)で示されるアリールアミンポリマーである。
【0082】
塗布法により、式(1)のアリールアミンポリマーからなる第一の有機化合物層を形成する際には、以下に説明する第一の塗料組成物を調製して、この第一の塗料組成物を塗布して薄膜を形成した方がよい。この第一の塗料組成物を使用すれば、有機発光素子を構成する有機化合物層、特に、電荷注入層又は電荷輸送層を塗布法により作製することが可能となり、比較的安価で大面積の有機発光素子を容易に作製することができる。
【0083】
ここで第一の塗料組成物には、式(1)のアリールアミンポリマーが少なくとも一種類含まれるものである。式(1)のアリールアミンポリマーは、一種類を単独で使用してもよいし、二種類以上を混合して使用してもよい。
【0084】
また式(1)のアリールアミンポリマーと他の有機化合物とを組み合わせて膜を形成してもよい。式(1)のアリールアミンポリマーと組み合わせて使用することができる有機化合物として、例えば、トリアリールアミン誘導体、フェニレンジアミン誘導体、トリアゾール誘導体、オキサジアゾール誘導体、イミダゾール誘導体、ピラゾリン誘導体、ピラゾロン誘導体、オキサゾール誘導体、フルオレノン誘導体、ヒドラゾン誘導体、スチルベン誘導体、フタロシアニン誘導体、ポルフィリン誘導体、ポリ(ビニルカルバゾール)、ポリ(シリレン)、ポリ(チオフェン)等が挙げられるが、これらに限定されるものではない。
【0085】
この第一の塗料組成物を調製するために使用する溶媒として、例えば、トルエン、キシレン、メシチレン、テトラリン、n−ドデシルベンゼン、メチルナフタレン等の炭化水素系溶剤、テトラヒドロフラン、ジオキサン、ジグライム等のエーテル系溶剤、クロロホルム、モノクロロベンゼン、1,2−ジクロロベンゼン等のハロゲン系溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン系溶剤、酢酸メチル、酢酸エチル、酢酸n−ブチル等のエステル系溶剤、メタノール、エタノール、n−プロパノール等のアルコール系溶剤、等が挙げられる。これらの溶媒は一種類を単独で使用してもよいし、二種類以上を混合して使用してもよい。また、これらの溶媒の粘度や、溶液中のアリールアミンポリマーの濃度を調整することにより、アリールアミンポリマー薄膜の膜厚を調整することができる。
【0086】
第一の塗料組成物に含まれる式(1)のアリールアミンポリマーの含有量は、組成物全体を基準として、好ましくは、0.05重量%以上20重量%以下であり、より好ましくは、0.1重量%以上5重量%以下である。
【0087】
第一の塗料組成物を電極上に塗布する方法として、具体的には、キャスト法、スピンコート法、スリットコーター法、印刷法、インクジェット法、デイスペンス法、スプレー法、ディップ法、LB膜法等が挙げられる。
【0088】
第一の工程によって形成される第一の有機化合物層の膜厚は、5μmより薄く、好ましくは500nm以下であり、より好ましくは5nm乃至500nmである。
【0089】
次に、第二の工程について説明する。第二の工程によって形成される薄膜を構成するアリールアミン骨格を有する(メタ)アクリル酸エステル化合物とは、好ましくは、下記一般式(3)で示される(メタ)アクリル酸エステル化合物である。
【0090】
【化14】

【0091】
式(3)において、A21及びA22は、それぞれ炭素数1以上8以下の2価の炭化水素基を表す。Ar21及びAr22は、それぞれ置換あるいは無置換のアリール基又は置換あるいは無置換の1価の縮合多環芳香族基を表す。Ar23は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。R21及びR22は、それぞれ水素原子又はメチル基を表す。
【0092】
A21、A22、Ar21、Ar22及びAr23の具体例は、式(2)の(メタ)アクリル酸エステルポリマーの具体例と同様である。またAr21及びAr22で表されるアリール基及び縮合多環芳香族基がさらに有してもよい置換基の具体例も、式(2)の(メタ)アクリル酸エステルポリマーの具体例と同様である。さらにAr23で表される2価のアリール基及び2価の縮合多環芳香族基がさらに有してもよい置換基の具体例も、式(2)の(メタ)アクリル酸エステルポリマーの具体例と同様である。
【0093】
次に、本発明の重合性官能基を有するアリールアミン化合物の具体例を、例示化合物として以下に示す。ただし、本発明はこれら具体例に限定されるものではない。
【0094】
【化15】

【0095】
【化16】

【0096】
【化17】

【0097】
【化18】

【0098】
【化19】

【0099】
【化20】

【0100】
第二の工程を行うにあたり、塗布法等の湿式法により薄膜を形成する際には、式(3)の(メタ)アクリル酸エステル化合物を含む第二の塗料組成物を調製し、この第二の塗料組成物を塗布して成膜する方法がよい。
【0101】
ここで第二の塗料組成物とは、式(3)の(メタ)アクリル酸エステル化合物を少なくとも一種類含有する。式(3)の(メタ)アクリル酸エステル化合物は一種類を単独で使用してもよいし、また二種類以上を混合して使用してもよい。
【0102】
さらに式(3)の(メタ)アクリル酸エステル化合物と、他の有機化合物とを組み合わせて薄膜を形成することもできる。式(3)の(メタ)アクリル酸エステル化合物と組み合わせて使用することができる有機化合物として、例えば、トリアリールアミン誘導体、フェニレンジアミン誘導体、トリアゾール誘導体、オキサジアゾール誘導体、イミダゾール誘導体、ピラゾリン誘導体、ピラゾロン誘導体、オキサゾール誘導体、フルオレノン誘導体、ヒドラゾン誘導体、スチルベン誘導体、フタロシアニン誘導体、ポルフィリン誘導体、及びポリ(ビニルカルバゾール)、ポリ(シリレン)、ポリ(チオフェン)等が挙げられるが、これらに限定されるものではない。
【0103】
第二の塗料組成物に使用する溶媒としては、例えば、トルエン、キシレン、メシチレン、テトラリン、n−ドデシルベンゼン、メチルナフタレン等の炭化水素系溶剤、テトラヒドロフラン、ジオキサン、ジグライム等のエーテル系溶剤、クロロホルム、モノクロロベンゼン、1,2−ジクロロベンゼン等のハロゲン系溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン系溶剤、酢酸メチル、酢酸エチル、酢酸n−ブチル等のエステル系溶剤、メタノール、エタノール、n−プロパノール等のアルコール系溶剤等が挙げられる。これらの溶媒は一種類を単独で使用してもよいし、二種類以上を混合して使用してもよい。また、これらの溶媒の粘度や、溶液中の(メタ)アクリル酸エステル化合物の濃度を調整することにより、(メタ)アクリル酸エステル化合物からなる薄膜の膜厚を調整することができる。
【0104】
第二の塗料組成物に含まれる式(3)の(メタ)アクリル酸エステル化合物の含有量は、組成物全体を基準として、好ましくは、0.05重量%以上20重量%以下であり、より好ましくは、0.1重量%以上5重量%以下である。
【0105】
塗布法の具体的な手段として、キャスト法、スピンコート法、スリットコーター法、印刷法、インクジェット法、デイスペンス法、スプレー法、ディップ法、LB膜法等が挙げられる。
【0106】
ところで、(メタ)アクリル酸エステル化合物からなる薄膜を塗布法で成膜する場合は、適当な結着樹脂と組み合わせて膜を形成することもできる。
【0107】
上記結着樹脂としては様々な結着性樹脂から選択することができる。例えば、ポリビニルカルバゾール樹脂、ポリカーボネート樹脂、ポリエステル樹脂、ポリアリーレート樹脂、ポリスチレン樹脂、ポリアクリル樹脂、ポリメタクリル樹脂、ポリビニルブチラール樹脂、ポリビニルアセタール樹脂、ジアリルフタレート樹脂、フェノール樹脂、エポキシ樹脂、シリコーン樹脂、ポリスルホン樹脂、尿素樹脂等が挙げられるが、これらに限定されるものではない。また、結着樹脂の形態はホモポリマーであってもよいし共重合体ポリマーであってもよい。また、結着樹脂は一種類を単独で使用してもよいし、また二種類以上を混合して使用してもよい。
【0108】
また、(メタ)アクリル酸エステル化合物からなる薄膜を塗布法で成膜する場合は、重合開始剤を第二の塗料組成物に添加した上で薄膜を形成することもできる。重合開始剤としては、例えば、ラジカル重合開始剤、カチオン重合開始剤、光重合開始剤等が挙げられる。
【0109】
上記の第二の塗料組成物は、式(1)のアリールアミンポリマーを溶解させない溶剤を使用して調製するのが好ましい。こうすることで第一の有機化合物層の上部へ、第二の有機化合物層となる薄膜を成膜・積層することができる。
【0110】
次に、第三の工程について説明する。第二の工程において形成された(メタ)アクリル酸エステル化合物からなる薄膜を加熱硬化する際は、その加熱温度は特に限定されないが、一般的には130℃乃至200℃の範囲で行う。
【0111】
第三の工程を行うことによって形成される第二の有機化合物層の膜厚は、5μmより薄く、好ましくは500nm以下であり、より好ましくは5nm乃至500nmである。
【0112】
本発明の有機発光素子において、式(1)のアリールアミンポリマーを含む第一の有機化合物層の上部に、他の有機化合物層を塗布法により形成する場合、第一の有機化合物層から層を構成する物質が溶け出さないことが求められる。
【0113】
一方で、第一の有機化合物層を構成する式(1)のアリールアミンポリマーは、直鎖状にモノマーユニットが連なった構造のポリマーである。ここで直鎖状のアリールアミンポリマーは、一般的に、有機溶剤への溶解性が高い。このため、塗布法により他の有機層を積層するときに当該アリールアミンポリマーが溶け出さないようにためには、第一の有機化合物層上に塗布可能な溶剤の種類は限定される。塗布可能な溶剤の種類が限定されると、塗布により成膜できる有機材料の種類もまた限定される。従って、利用可能な有機材料の種類を増やすために、好ましくは、第一の有機化合物層を不溶化する。
【0114】
本発明の有機発光素子の製造方法では、第一の有機化合物層を不溶化するために、第一の有機化合物の上に、アリールアミン骨格を有する(メタ)アクリル酸エステル化合物が含まれる薄膜を塗布により成膜し、加熱処理を行う方法を採用する。この方法によって形成される第二の有機化合物層は、加熱処理を行うことにより、薄膜を構成する(メタ)アクリル酸エステル化合物が重合反応を起こすので、層自体が不溶化する。
【0115】
ところで、式(3)の(メタ)アクリル酸エステル化合物は、加熱、重合開始剤等によるラジカル重合反応により、分子間架橋反応が起こる。この分子間架橋反応により、アリールアミン骨格を有する(メタ)アクリル酸エステルポリマー薄膜が形成される。この薄膜は架橋構造を有する化合物で構成されているポリマー薄膜であるので、溶媒に対して不溶の薄膜となっている。このため、次の第四の工程として、この薄膜の上から塗布法により他の有機化合物層を積層したとしても、既に形成したポリマー薄膜が溶媒によって溶かされることはない。またこのポリマー薄膜を形成することによって、ポリマー薄膜自体のみならず、当該ポリマー薄膜より下の層を構成する材料が塗料に含まれる溶媒によって溶解されるのを防ぐことができる。よって本発明の有機発光素子の製造方法では、層を構成する材料同士の混入がない安定した積層体を有する素子を作製することができる。
【0116】
以上より、第二の工程により第二の有機化合物層となる薄膜の成膜を行った後、第三の工程により加熱処理を行うことで、当該薄膜の構成材料である(メタ)アクリル酸エステル化合物は重合反応を起こし、当該薄膜は溶媒に対して不溶な薄膜となる。このような薄膜を形成することにより、第一の有機化合物層は第二の有機化合物層と同様に有機溶剤に不溶となるので、第四の工程において、第二の有機化合物層である薄膜の上部へ、塗布法により第三の有機化合物層となる薄膜を形成・積層することが可能となる。
【0117】
以上の(i)乃至(iv)で示した4工程により、本発明の有機発光素子の主要構成となる3つの層(第一の有機化合物層、第二の有機化合物層、第三の有機化合物層)を塗布法によって形成することができる。一方で、式(1)で示されるアリールアミンポリマー及び式(3)で示される(メタ)アクリル酸エステル化合物は、蒸着法による成膜には適さない。このため、本発明の有機発光素子の主要構成となる3つの層を形成する際には、蒸着法を採用することができない。
【0118】
上記に示した本発明の製造方法により製造される有機発光素子は、少なくとも3つの有機化合物層からなる積層構造を有している。ここで有機化合物層として、具体的には、正孔注入層、正孔輸送層、発光層、正孔/エキシトンブロッキング層、電子輸送層、電子注入層等が挙げられる。これらの層のうち、上述した第一の有機化合物層、第二の有機化合物層及び第三の有機化合物層に該当する層は、塗布法によって形成されるものである。一方、これら3つの層以外の有機化合物層は、真空蒸着法や溶液塗布法等の如何なる方法によっても形成することができる。ここで製造される有機発光素子の膜厚は5μmより薄く、好ましくは、1μm以下であり、より好ましくは、5nm以上500nm以下である。
【0119】
本発明の有機発光素子を適宜組み合わせることにより、ディスプレイ等の表示装置を構成することができる。即ち、本発明の表示装置は、本発明の有機発光素子と、該有機発光素子の駆動回路と、を複数具備するものであり、パッシブマトリックス方式又はアクティブマトリックス方式で駆動される。以下、図面を参照しながら、本発明の有機発光素子を、アクティブマトリクス方式に組み合わせた表示装置について説明する。
【0120】
図4は、本発明の表示装置の一部分を示す断面模式図である。図4で示される表示装置40は、基板41上に設けられている有機発光素子部42と、有機発光素子部42の外部に配置されている回路部43と、回路部43に隣接して設けられているデータ配線44と、から構成される。ここで回路部43には、ドライブトランジスタ(TFT1)451と、スイッチングトランジスタ(TFT2)452と、保持容量(Ch)46と、が設けられている。
【0121】
図4において、有機発光素子は1個のみ図示されているが、実際に表示装置を構築する場合は、有機発光素子は二次元状に複数配置されている。有機発光素子が二次元状に配置されている表示装置の具体例は後述する。また本実施形態において、有機発光素子部42は、下部電極47と、有機化合物層48と、上部電極49とがこの順に積層されているものである。この有機発光素子部42において、有機化合物層48は、少なくとも上記の第一の有機化合物層、第二の有機化合物層及び第三の有機化合物層が含まれる。
【0122】
図5は、図4の表示装置の回路部における回路の構成の詳細を示す図である。図5で示される回路は、電流プログラミング方式とよばれる代表的な回路構成である。尚、本発明のディスプレイで採用できる回路はこれに限るものではない。図5で示される回路50は、ドライブトランジスタ(TFT1)451、スイッチングトランジスタ(TFT2)452、保持容量(Ch)46、有機発光素子51から構成されている。尚、周知な回路構成であるため動作の詳細については説明を省略する。
【0123】
ところで本発明の有機発光素子は、1つの発光点として利用して、ディスプレイ等の表示装置や照明装置や電子写真方式の画像形成装置の露光光源に使用することができる。
【0124】
本発明の有機発光素子をディスプレイに利用した場合について以下に説明する。
【0125】
図6は、図4及び図5で示される有機発光素子部及び回路部を1画素としてマトリックス状に配置した表示装置を示す模式図である。
【0126】
図6の表示装置60において、画素61は、配線を介してゲートドライバ62と、ソースドライバ63とに接続され、各ドライバから供給される駆動パルスにより、発光状態あるいは非発光状態となる。
【0127】
このように本発明の有機発光素子が、画素として同一面内に面内方向に複数配置されている領域が本発明の表示装置の表示領域である。即ち、本発明の有機発光素子は本発明の表示装置の表示領域として使用することができる。
【0128】
本発明の表示装置は、例えば、テレビやPC用の表示装置、あるいは画像を表示する部分を有する機器であれば如何なる実施形態も問わない。例えば、本発明の表示装置が搭載される携帯型表示装置であってもよい。あるいはデジタルカメラ等の電子撮像装置や携帯電話の表示部に本発明の表示装置を使用することができる。
【0129】
図7は、図6の表示装置をパネルモジュール化した構成例を示す模式図である。図7のパネルモジュール70は、図6に示される表示装置60に加え、インターフェースドライバ71と、ゲートドライバ62と、ソースドライバ63と、を筐体72で一体化したものである。尚、図7のパネルモジュール70において、図示はしていないが、接続端子等の外部機器との接続に必要な部品(インターフェース)が筐体72に内蔵されている。
【実施例】
【0130】
[HOMOレベルの評価]
各実施例及び各比較例において使用した材料のうち主要な材料については、材料自体のHOMOエネルギーを評価した。ここでHOMOエネルギーとは、材料自体の最高被占分子軌道(HOMO)と真空準位との間のエネルギー差に相当するものであり、イオン化ポテンシャルと同義である。HOMOエネルギーの評価方法としては、光電子分光法により測定した値から評価する方法を採用した。また光電子分光の測定装置として、光電子分光装置AC−2(理研機器製)を用いた。
【0131】
<合成例1>[例示化合物No.1−1の合成]
【0132】
【化21】

【0133】
(i)500mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
2−ヨードフルオレン誘導体(化合物[1]):30g(93.7mmol)
アセトアミド(化合物[2]):5.5g(93.7mmol)
銅粉:11.9g(187.4mmol)
炭酸カリウム:25.9g(187.4mmol)
1,2−ジクロロベンゼン:250ml
【0134】
次に、反応溶液を180℃に加熱し16時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出した。次に、有機層を無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより、化合物[3]を白色結晶として20.0g(収率85%)得た。
【0135】
(ii)300mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
4,4’−ジヨードビフェニル(化合物[4]):10.1g(24.9mmol)
化合物[3]:15.0g(59.7mmol)
銅粉:6.3g(99.6mmol)
炭酸カリウム:13.8g(99.6mmol)
1,2−ジクロロベンゼン:150ml
【0136】
次に、反応溶液を180℃に加熱し24時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出した。次に、有機層を無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより、中間体化合物[5]を白色結晶として11.7g(収率72%)得た。
【0137】
(iii)300mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[5]:10.0g(15.3mmol)
2−メトキシエタノール:50ml
トルエン:50ml
【0138】
次に、窒素雰囲気下、室温で、ナトリウムメトキサイド2.1g(38.3mmol)をさらに添加した後、反応溶液を60℃に加熱し3時間攪拌した。反応終了後、水を加えてから、有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。次に、有機層を減圧濃縮した後、濃縮物についてシリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサンとトルエンとの混合溶媒)で精製することにより、アリールアミン化合物である中間体化合物[6]を白色結晶として8.3g(収率95%)得た。
【0139】
(iv)100ml三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[6]:1.5g(2.64mmol)
4,4’−ジブロモビフェニル(化合物[7]):0.82g(2.64mmol)
キシレン:50ml
次に、窒素雰囲気下、室温で、ナトリウムtert−ブトキサイド0.25g(2.64mmol)を添加した。次に、酢酸パラジウム0.03g(0.13mmol)とトリ−tert−ブチルホスフィン0.025g(0.13mmol)とを添加した後、反応溶液を130℃に加熱し12時間撹拌した。反応終了後、水を加えてから有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。次に、有機層を減圧濃縮した後、濃縮物についてシリカゲルカラムクロマトグラフィー(展開溶媒:トルエン)で精製した。次に、メタノールで再沈殿を行い、沈殿物をろ取することにより、例示化合物No.1−1を黄色アモルファスとして0.91g(収率48%)得た。
【0140】
<合成例2>[例示化合物No.1−2の合成]
【0141】
【化22】

【0142】
(i)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[6]:3.0g(5.27mmol)
4−ブロモヨードベンゼン(化合物[8]):3.6g(12.7mmol)
銅粉:1.0g(15.8mmol)
炭酸カリウム:2.2g(15.8mmol)
1,2−ジクロロベンゼン:100ml
【0143】
次に、反応溶液を180℃に加熱し24時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出し、無水硫酸ナトリウムで乾燥した後、溶媒を減圧留去した。これによって得られた粗生成物についてシリカゲルカラムカラムクロマトグラフィー(展開溶媒:ヘキサンとトルエンとの混合溶媒)で精製することにより、アリールアミン化合物である中間体化合物[9]を黄色結晶として2.41g(収率52%)得た。
【0144】
(ii)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[9]:1.5g(1.71mmol)
ジピナコールボラン体(化合物[10]):0.76g(1.71mmol)
トルエン:50ml
エタノ−ル:20ml
【0145】
次に、反応溶液を窒素雰囲気下、室温で攪拌しながら、炭酸ナトリウム3.2gと水15mlとを混合して調製した水溶液を滴下し、次いでテトラキス(トリフェニルホスフィン)パラジウム(0)0.10g(0.09mmol)を添加した。次に、反応溶液を還流させながら10時間攪拌した。反応終了後、有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。有機層を減圧濃縮した後、得られた濃縮物について、シリカゲルカラムクロマトグラフィー(展開溶媒:トルエン)で精製した。次に、メタノールで再沈殿して、沈殿物をろ取することにより、例示化合物No.1−2を黄色アモルファスとして0.90g(収率58%)得た。
【0146】
<合成例3>[例示化合物No.1−4の合成]
【0147】
【化23】

【0148】
(i)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[6]:3.0g(5.27mmol)
3−ブロモヨードベンゼン(化合物[11]):3.6g(12.7mmol)
銅粉:1.0g(15.8mmol)
炭酸カリウム:2.2g(15.8mmol)
1,2−ジクロロベンゼン:100ml
【0149】
次に、反応溶液を180℃に加熱し24時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出し無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。これによって得られた粗生成物について、シリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサンとトルエンとの混合溶媒)で精製することにより、アリールアミン化合物である中間体化合物[12]を白色結晶として2.87g(収率62%)得た。
【0150】
(ii)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[12]:1.5g(1.71mmol)
ジピナコールボラン体(化合物[10]):0.76g(1.71mmol)
トルエン:50ml
エタノ−ル:20ml
【0151】
次に、反応溶液を窒素雰囲気下室温で攪拌しながら、炭酸ナトリウム3.2gと水15mlとを混合して調製した水溶液を滴下し、次いでテトラキス(トリフェニルホスフィン)パラジウム(0)0.10g(0.09mmol)を添加した。次に、反応溶液を還流させながら10時間攪拌した。反応終了後、有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。次に、溶媒を減圧留去した。これにより得られた粗生成物について、シリカゲルカラムクロマトグラフィー(展開溶媒:トルエン)で精製した後、メタノールで再沈殿を行い、沈殿物をろ取することにより、例示化合物No.1−4を白色アモルファスとして0.65g(収率42%)得た。
【0152】
<合成例4>[例示化合物No.2−1の合成]
フラスコ内で、以下の試薬、溶媒を仕込み、フラスコを氷水バスで冷却した。
下記式で示されるジヒドロキシ体:1.0g(1.37mmol)
【0153】
【化24】

トリエチルアミン:0.49g(4.80mmol)
テトラヒドロフラン:10ml
【0154】
次に、反応溶液の温度を10℃以下に保ちながら、この反応溶液中にアクリル酸クロライド0.37g(4.11mmol)を滴下した。滴下終了後、反応溶液を徐々に昇温させ、反応用液の温度を50℃に保ちながらさらに30分間反応を続けた。
【0155】
反応終了後、反応溶液を冷却した。次に、この反応溶液に、酢酸エチル100mlと、10%水酸化ナトリウム水溶液50mlとをそれぞれ加えて攪拌した後、分液操作を行い、有機層を回収した。回収した有機層を、さらにイオン交換水30mlで2回洗浄し、硫酸マグネシウムで乾燥させた。
【0156】
次に、この有機層中の溶媒を、ロータリーエバポレーターを用いて除去し、粗生成物を得た。この粗生成物について、シリカゲルカラムクロマトグラフィーを用いて精製を行った。具体的には、シリカゲル約10gを使用し、展開溶媒は、始めはトルエンを使用し、途中からトルエン/テトラヒドロフラン混合溶媒(混合比:10/1)を使用した。
【0157】
最後に目的化合物に該当するフラクションを回収し溶媒を減圧除去することにより、目的とする例示化合物No.2−1を0.77g得た。
【0158】
<合成例5>[例示化合物No.2−8の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.12mmol)
【0159】
【化25】

トリエチルアミン:0.42g(3.92mmol)
テトラヒドロフラン:10ml
アクリル酸クロライド:0.30g(3.36mmol)
【0160】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−8を0.75g得た。
【0161】
<合成例6>[例示化合物No.2−9の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.24mmol)
【0162】
【化26】

トリエチルアミン:0.44g(4.34mmol)
テトラヒドロフラン:10ml
アクリル酸クロライド:0.33g(3.72mmol)
【0163】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−9を0.72g得た。
【0164】
<合成例7>[例示化合物No.2−10の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.19mmol)
【0165】
【化27】

トリエチルアミン:0.43g(4.18mmol)
テトラヒドロフラン:10ml
アクリル酸クロライド:0.32g(3.57mmol)
【0166】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−10を0.77g得た。
【0167】
<合成例8>[例示化合物No.2−15の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.19mmol)
【0168】
【化28】

トリエチルアミン:0.43g(4.18mmol)
テトラヒドロフラン:10ml
メタクリル酸クロライド:0.37g(3.57mmol)
【0169】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−15を0.78g得た。
【0170】
[実施例1]
図2に示される有機発光素子を作製した。
【0171】
ガラス基板(基板1)上に、酸化錫インジウム(ITO)をスパッタ法にて成膜することにより陽極2を形成した。このとき陽極2の膜厚を120nmとした。次に、このITOが成膜されている基板をアセトン、イソプロピルアルコール(IPA)で順次超音波洗浄し、次いでIPAで煮沸洗浄した後乾燥した。次に、このITOが成膜されている基板をUV/オゾン洗浄した。以上のように処理した基板を透明導電性支持基板として使用した。
【0172】
次に、例示化合物No.1−1をクロロホルムに溶解し、濃度0.5重量%のクロロホルム溶液(以下、本実施例において正孔注入層形成用塗料という。)を調製した。次に、この正孔注入層形成用塗料を陽極2上に滴下しスピンコートすることにより正孔注入層3を形成した。このとき正孔注入層3の膜厚は15nmであった。
【0173】
次に、例示化合物No.2−10をメチルイソブチルケトンに溶解し、濃度0.5重量%のメチルイソブチルケトン溶液(以下、本実施例において正孔輸送層形成用塗料という。)を調製した。次に、この正孔輸送層形成用塗料を正孔注入層3上に滴下しスピンコートして薄膜を形成した。次に、この薄膜を200℃で30分間加熱し硬化することにより正孔輸送層4を形成した。このとき正孔輸送層4の膜厚は15nmであった。尚、加熱処理を行うことにより、当該薄膜を構成する例示化合物No.2−10が架橋反応を起こし、当該薄膜は硬化した。このため正孔輸送層4は、溶剤に対して不溶の膜となった。
【0174】
次に、以下に示す試薬、溶媒を混合し、発光層形成用塗料を調製した。
【0175】
Ir(ppy)3(トリス(2−フェニルピリジン)イリジウム):0.01質量部
PBD(2−(4−ビフェニル)−5−(4−ブチルフェニル)−1,3,4−オキサジアゾール):0.3質量部
PVK(ポリビニルカルバゾール、Mn=35000):0.7質量部
【0176】
【化29】

クロロベンゼン:99質量部
【0177】
次に、この発光層形成用塗料を正孔輸送層4上に滴下し、回転数1000rpmで1分間スピンコートを行うことで薄膜を形成した。次に、120℃で30分間加熱して当該薄膜中の溶剤を蒸発させることにより発光層5を形成した。このとき発光層5の膜厚は100nmであった。
【0178】
次に、真空蒸着法によりフッ化リチウムを発光層5上に蒸着することで電子注入層7を形成した。このとき電子注入層7の膜厚を0.5nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度を0.01nm/secの条件とした。
【0179】
次に、真空蒸着法によりアルミニウムを電子注入層7上に蒸着することで陰極6を形成した。このとき陰極6の膜厚を100nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度は1.0nm/sec乃至1.2nm/secの条件とした。
【0180】
次に、窒素雰囲気下において、保護用ガラス板を被せてアクリル樹脂系接着剤で封止した。以上のようにして有機発光素子を得た。
【0181】
得られた素子について、ITO電極を陽極に、アルミニウム電極を陰極にして7Vの直流電圧を印加すると、素子に電流が流れた。このときの電流密度は29mA/cm2であり、輝度3010cd/m2の緑色発光が観測された。また、電流密度を10mA/cm2に保ち50時間連続駆動したところ、960cd/m2(初期輝度)から700cd/m2(50時間後の輝度)に変化した。
【0182】
[実施例2]
実施例1において、例示化合物No.1−1に代えて例示化合物No.1−2を使用して正孔注入層3を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0183】
[実施例3]
実施例1において、例示化合物No.1−1に代えて例示化合物No.1−4を使用して正孔注入層3を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0184】
[実施例4]
実施例1において、例示化合物No.2−10に代えて例示化合物No.2−15を使用して正孔輸送層4を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0185】
[実施例5]
実施例1において、例示化合物No.2−10に代えて例示化合物No.2−12を使用して正孔輸送層4を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0186】
[実施例6]
実施例1において、例示化合物No.2−10に代えて例示化合物No.2−1を使用して正孔輸送層4を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0187】
[比較例1]
実施例1において、例示化合物No.1−1に代えて下記式に示される比較化合物No.1(4−ポリエチレンジオキシチオフェン/ポリスチレンスルホン酸(PEDOT/PSS)、商品名:バイトロンP Al−4083、バイエル社製)を使用した。また、陽極2上に比較化合物No.1を滴下しスピンコートした後、120℃で30分加熱することで、膜厚30nmの正孔注入層3を形成した。これらを除いては実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0188】
【化30】

【0189】
【表1】

【0190】
[実施例7]
図2に示される有機発光素子を作製した。
【0191】
ガラス基板(基板1)上に、酸化錫インジウム(ITO)をスパッタ法にて成膜することにより陽極2を形成した。このとき陽極2の膜厚を120nmとした。次に、このITOが成膜されている基板をアセトン、イソプロピルアルコール(IPA)で順次超音波洗浄し、IPAで煮沸洗浄後乾燥をした。次に、このITOが成膜されている基板をUV/オゾン洗浄した。以上のようにして処理した基板を透明導電性支持基板として使用した。
【0192】
次に、例示化合物No.1−1をp−キシレンに溶解し、濃度0.5重量%のp−キシレン溶液(以下、本実施例において正孔注入層形成用塗料という。)を調製した。この正孔注入層形成用塗料を陽極2上に滴下しスピンコートすることにより正孔注入層3を形成した。このとき正孔注入層3の膜厚は15nmであった。
【0193】
次に、例示化合物No.2−10をメチルイソブチルケトンに溶解し、濃度0.5重量%のメチルイソブチルケトン溶液(以下、本実施例において正孔輸送層形成用塗料という。)を調製した。次に、この正孔輸送層形成用塗料を正孔注入層3上に滴下しスピンコートして薄膜を形成した。次に、この薄膜を200℃で30分間加熱し硬化することにより正孔輸送層4を形成した。このとき正孔輸送層4の膜厚は15nmであった。尚、加熱処理を行うことにより、当該薄膜を構成する例示化合物No.2−10が架橋反応を起こし、当該薄膜は硬化した。このため正孔輸送層4は、溶剤に対して不溶の膜となった。
【0194】
次に、以下に示す試薬、溶媒を混合し発光層形成用塗料を調製した。
例示化合物No.2−10:1質量部
下記式に示される緑色燐光材料:0.01質量部
【0195】
【化31】

クロロホルム:99質量部
【0196】
次に、この発光層形成用塗料を正孔輸送層4上に滴下し、回転数1000rpmで1分間スピンコートを行うことで薄膜を形成した。次に、80℃で30分間加熱し当該薄膜中に含まれる溶剤を蒸発させることにより発光層5を形成した。このとき発光層3の膜厚は80nmであった。
【0197】
次に、真空蒸着法によりフッ化リチウムを発光層5上に蒸着することで電子注入層7を形成した。このとき電子注入層7の膜厚を0.5nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度を0.01nm/secの条件とした。
【0198】
次に、真空蒸着法によりアルミニウムを電子注入層7上に蒸着することで陰極6を形成した。このとき陰極6の膜厚を100nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度を1.0nm/sec乃至1.2nm/secの条件とした。
【0199】
次に、窒素雰囲気下において、保護用ガラス板を被せてアクリル樹脂系接着剤で封止した。以上のようにして有機発光素子を得た。
【0200】
得られた素子について、ITO電極を陽極に、アルミニウム電極を陰極にして7Vの直流電圧を印加すると、素子に電流が流れた。このときの電流密度は20mA/cm2であり、輝度1200cd/m2の赤色発光が観測された。また、電流密度を30mA/cm2に保ち50時間連続駆動したところ、1800cd/m2(初期輝度)から1100cd/m2(50時間後の輝度)に変化した。
【0201】
[実施例8]
実施例7において、例示化合物No.1−1に代えて例示化合物No.1−2を使用して正孔注入層3を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0202】
[実施例9]
実施例7において、例示化合物No.1−1に代えて例示化合物No.1−4を使用して正孔注入層3を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0203】
[実施例10]
実施例7において、例示化合物No.2−10に代えて例示化合物No.2−8を使用して正孔輸送層4を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0204】
[実施例11]
実施例7において、例示化合物No.2−10に代えて例示化合物No.2−9を使用して正孔輸送層4を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0205】
[実施例12]
実施例7において、例示化合物No.2−10に代えて例示化合物No.2−1を使用して正孔輸送層4を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0206】
[比較例2]
実施例7において、例示化合物No.1−1に代えて下記式に示される比較化合物No.2(ポリ[(9,9−ジヘキシルフルオレン−2,7−ジイル]−コ−[ピリジン−3,5−ジイル)]、H.W.SANDS社製)を使用した。また、陽極2上に比較化合物No.2を溶解した濃度0.5重量%のトルエン溶液を滴下しスピンコートした後、120℃で30分加熱することで、膜厚15nmの正孔注入層3を形成した。これらを除いては実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0207】
【化32】

【0208】
【表2】

【図面の簡単な説明】
【0209】
【図1】本発明の有機発光素子における第一の実施形態を示す断面図である。
【図2】本発明の有機発光素子における第二の実施形態を示す断面図である。
【図3】本発明の有機発光素子における第三の実施形態を示す断面図である。
【図4】本発明の表示装置の一部分を示す断面模式図である。
【図5】図4の表示装置の回路部における回路の構成の詳細を示す図である。
【図6】図4及び図5で示される有機発光素子部及び回路部を1画素としてマトリックス状に配置した表示装置を示す模式図である。
【図7】図6の表示装置をパネルモジュール化した構成例を示す模式図である。
【符号の説明】
【0210】
1,41 基板
2 陽極
3 発光層
4 陰極
5 正孔輸送層
6 電子輸送層
7 正孔注入層
8 電子注入層
10,20,30,51 有機発光素子
40,60 表示装置
42 有機発光素子部
43 回路部
44 データ配線
451 ドライブトランジスタ(TFT1)
452 スイッチィングトランジスタ(TFT2)
46 保持容量(Ch)
47 下部電極
48 有機化合物層
49 上部電極
50 回路
61 画素
62 ケースドライバ
63 ソースドライバ
70 パネルモジュール
71 インターフェースドライバ
72 筐体
【技術分野】
【0001】
本発明は、有機発光素子及びその製造方法、並びに表示装置に関する。
【背景技術】
【0002】
有機発光素子を製造する場合、その製造プロセスは乾式法と湿式法とに分類される。乾式法とは、主に低分子系材料を使用し、真空蒸着法等の気相プロセスを用いて薄膜形成を行う方法である。これに対し湿式法とは、成膜工程において主に高分子系材料を使用し、スピン塗布法、インクジェット塗布法、ディスペンサー塗布法、スプレー塗布法、浸漬塗布法等の方法を用いて薄膜形成を行う方法である。
【0003】
ここで真空蒸着法等の乾式法は、生産装置がバッチ式であり、素子作製において素子の発光のために必要のない部分にも素子の構成材料からなる薄膜が形成される。このため必要量よりはるかに多くの材料が無駄に消費されてしまうことから、生産性の観点からすると課題のある方法であると言える。
【0004】
一方、湿式法を用いて有機発光素子を製造すると、連続式処理による生産が可能である。例えば、インクジェット塗布法、ディスペンサー塗布法のように液滴吐出法によって塗布する塗布液の種類、位置等を選択することができる。これらの方法では、素子の必要とする部分にのみに選択して材料を塗り分けるという、いわゆるパターンニングが可能となり、生産性を大幅に改善することができる。
【0005】
このため昨今においては、有機発光素子を構成する電荷注入層、電荷輸送層、発光層等の有機化合物層を、生産性のよい塗布法を用いて成膜することに関心が高まっている。
【0006】
例えば、正孔注入層を塗布法で形成する場合、使用される正孔注入層の構成材料(正孔注入材料)として、ポリ(3,4−エチレンジオキシチオフェン)とポリスチレンスルホン酸の混合物(PEDOT/PSS)が知られている(非特許文献1参照)。このPEDOT/PSSは水溶性であるので、PEDOT/PSS膜から上の層となる薄膜を形成する際は、その層の構成材料を有機溶媒に溶解して調製した塗布液を使用し、塗布法を用いることで薄膜を形成し、その薄膜を積層することができる。しかし、このPEDOT/PSSを使用した有機発光素子は、初期特性に優れるが長時間使用した場合に輝度劣化が著しいことが問題である。この輝度劣化を改善するために、PEDOT/PSS膜と発光層との間に不溶性の重合体である中間層を組み込んだ有機発光素子が報告されている(特許文献1及び2参照)。
【0007】
一方で、有機発光素子の高効率化及び耐久性向上のためには、複数の有機化合物層が積層した素子構造とすることが有効である。ここで、塗布法で有機化合物層を積層する場合は、下地となる有機化合物層上に次の層の構成材料を含む溶液を塗布する際に、下地となる有機化合物層が溶解するという問題を回避する必要がある。ここで下地となる有機化合物層の溶解を防ぐ方法として、溶媒に対する溶解度の差を利用する方法が報告されている(特許文献3参照)。また架橋剤を使用して下地の有機化合物層である薄膜の架橋反応を誘起させて薄膜自体を不溶化する方法も報告されている(特許文献4及び5参照)。
【0008】
しかし溶媒に対する溶解度の差を利用する方法では、各層の構成材料の溶解性の観点から、積層のために利用できる溶媒が限定されるため、使用できる材料も自ずと制約されるという問題があった。また架橋剤を使用して不溶化する方法では、架橋剤が層を構成する材料の電荷輸送性に悪影響を及ぼすため、発光効率等の初期特性や長時間の発光による輝度劣化等の耐久特性が十分でないという問題があった。
【0009】
【特許文献1】特開2005−183404号公報
【特許文献2】特開2005−243300号公報
【特許文献3】特開平11−251065号公報
【特許文献4】特開平11−87605号公報
【特許文献5】特開2005−340042号公報
【非特許文献1】Appl.Phys.Lett.,75,1679(1999)
【発明の開示】
【発明が解決しようとする課題】
【0010】
本発明の目的は、高効率かつ長寿命の有機発光素子を提供することにある。また、本発明の他の目的は、塗布法により高効率かつ長寿命の有機発光素子を製造することを可能にするための有機発光素子の製造方法を提供することにある。
【課題を解決するための手段】
【0011】
本発明の有機発光素子は、陽極と陰極と、該陽極と該陰極との間に挟持され少なくとも第一の有機化合物層と、第二の有機化合物層と、第三の有機化合物層とがこの順に含まれる積層体と、から構成され、該陽極又は該陰極と該第一の有機化合物層と、該第一の有機化合物層と該第二の有機化合物層と、並びに該第二の有機化合物層と該第三の有機化合物層と、が互いに接しており、該第一の有機化合物層にアリールアミンポリマーが含まれ、該第二の有機化合物層にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする。
【発明の効果】
【0012】
本発明によれば、高効率かつ長寿命の有機発光素子を提供することができる。また、本発明によれば、塗布法により高効率かつ長寿命の有機発光素子を製造することを可能にするための有機発光素子の製造方法を提供することができる。
【発明を実施するための最良の形態】
【0013】
まず本発明の有機発光素子について説明する。本発明の有機発光素子は、陽極と陰極と、該陽極と該陰極との間に挟持され少なくとも第一の有機化合物層と、第二の有機化合物層と、第三の有機化合物層とがこの順に含まれる積層体と、から構成される。
【0014】
以下、図面を参照しながら本発明の有機発光素子を詳細に説明する。
【0015】
図1は、本発明の有機発光素子における第一の実施形態を示す断面図である。図1の有機発光素子10は、基板1上に陽極2、正孔注入層3、正孔輸送層4、発光層5及び陰極6が順次設けられている。
【0016】
図2は、本発明の有機発光素子における第二の実施形態を示す断面図である。図2の有機発光素子20は、図1の有機発光素子10において、発光層5と陰極6との間に電子注入層7が設けられている。
【0017】
図3は、本発明の有機発光素子における第三の実施形態を示す断面図である。図3の有機発光素子30は、図2の有機発光素子20において、発光層5と電子注入層7との間に電子輸送層8が設けられている。
【0018】
ただし、図1乃至図3はあくまでごく基本的な素子構成であり、本発明の有機発光素子の構成はこれらに限定されるものではない。例えば、電極と有機化合物層との界面に絶縁性層、接着層又は干渉層を設ける、正孔注入層又は正孔輸送層が異なる二層から構成される等多様な層構成をとることができる。尚、本発明の有機発光素子は、陽極又は陰極と第一の有機化合物層とが互いに接している。また、第一の有機化合物層と第二の有機化合物層とが互いに接している。さらに、第二の有機化合物層と第三の有機化合物層とが互いに接している。
【0019】
上記のように、本発明の有機発光素子は、有機化合物層を少なくとも3つ含むものである。有機化合物層として、例えば、正孔注入層、正孔輸送層、発光層、正孔/エキシトンブロッキング層、電子輸送層、電子注入層等が挙げられる。
【0020】
本発明の有機発光素子においては、第一の有機化合物層にアリールアミンポリマーが含まれ、第二の有機化合物層にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする。
【0021】
まず第一の有機化合物層に含まれるアリールアミンポリマーについて説明する。ここでいうアリールアミンポリマーは、好ましくは、下記一般式(1)で示されるポリマーである。
【0022】
【化1】

【0023】
式(1)において、R11及びR12は、それぞれ水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、アルコキシ基又はハロゲン原子を表す。
【0024】
R11及びR12で表されるアルキル基として、メチル基、エチル基、プロピル基、n−ブチル基等が挙げられる。
【0025】
R11及びR12で表されるアラルキル基として、ベンジル基、フェネチル基、ナフチルメチル基等が挙げられる。
【0026】
R11及びR12で表されるアリール基として、フェニル基、ビフェニルイル基、ターフェニルイル基等が挙げられる。
【0027】
R11及びR12で表されるアルコキシ基として、メトキシ基、エトキシ基、プロポキシ基等が挙げられる。
【0028】
R11及びR12で表されるハロゲン原子として、フッ素、塩素、臭素等が挙げられる。
【0029】
上記アルキル基、アラルキル基及びアリール基がさらに有してもよい置環基として、メチル基、エチル基、プロピル基、ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0030】
式(1)において、Ar11及びAr12は、それぞれ置換あるいは無置換のアリール基又は縮合多環芳香族基を表す。
【0031】
Ar11及びAr12で表されるアリール基として、フェニル基、ビフェニルイル基、ターフェニルイル基等が挙げられる。
【0032】
Ar11及びAr12で表される縮合多環芳香族基として、フルオレニル基、フルオランテニル基、ナフチル基、フェナントリル基、ジヒドロフェナントレニル基、ピレニル基、ペリレニル基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基等が挙げられる。
【0033】
上記アリール基及び縮合多環芳香族基がさらに有してもよい置環基として、メチル基、エチル基、n−プロピル基、n−ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0034】
式(1)において、Ar13は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。
【0035】
Ar13で表される2価のアリール基として、フェニレン基、ビフェニレン基、ターフェニレン基等が挙げられる。
【0036】
Ar13で表される2価の縮合多環芳香族基として、フルオレン、フルオランテン、ナフタレン、フェナントレン、ジヒドロフェナントレン、ピレン、ペリレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン等を基本骨格とする2価の置換基が挙げられる。
【0037】
上記アリール基及び縮合多環芳香族基がさらに有してもよい置環基として、メチル基、エチル基、n−プロピル基、n−ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0038】
式(1)において、Ar14は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。
【0039】
Ar14で表される2価のアリール基として、フェニレン基、ビフェニレン基等が挙げられる。
【0040】
Ar14で表される2価の縮合多環芳香族基として、フルオレン、フルオランテン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン、ピレン、ペリレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン等を基本骨格とする2価の置換基が挙げられる。
【0041】
上記アリール基及び縮合多環芳香族基がさらに有してもよい置環基として、メチル基、エチル基、n−プロピル基、n−ブチル基、tert−ブチル基、3−メチルブチル基、2−エチルヘキシル基、オクチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0042】
式(1)において、mは、10以上300以下の整数を表す。
【0043】
式(1)において、nは、0以上300以下の整数を表す。
【0044】
式(1)のアリールアミンポリマーは、mやnの数値によって、溶媒に対するポリマー自体の溶解度を適宜調整することが可能である。特に規定するものではないが、溶媒に対する十分な溶解性を高くできる点で、mは、好ましくは、10以上100以下である。同様に、nは、好ましくは、0以上100以下である。またポリマーの分子量は、当該ポリマーを合成する際の反応温度、反応溶媒、反応溶媒量、触媒等の様々な因子により決まる。
【0045】
式(1)のアリールアミンポリマーの具体例を、以下に示す。ただし、本発明はこれら具体例に限定されるものではない。
【0046】
【化2】

【0047】
【化3】

【0048】
【化4】

【0049】
【化5】

【0050】
【化6】

【0051】
【化7】

【0052】
【化8】

【0053】
【化9】

【0054】
【化10】

【0055】
【化11】

【0056】
【化12】

【0057】
次に、第二の有機化合物層に含まれる(メタ)アクリル酸エステルポリマーについて説明する。
【0058】
第二の有機化合物層に含まれる(メタ)アクリル酸エステルポリマーとは、アリールアミン骨格を有する(メタ)アクリル酸エステルポリマーであるが、好ましくは、下記一般式(2)で示されるポリマーである。
【0059】
【化13】

【0060】
式(2)において、A21及びA22は、それぞれ炭素数1以上8以下の2価の炭化水素基を表す。
【0061】
A21及びA22で表される炭素数1以上8以下の2価の炭化水素基として、メチレン基、エチレン基、プロピレン基、ブチレン基、ペンチレン基、オクチレン基等が挙げられる。これら2価の炭化水素基は、メチル基、エチル基、プロピル基、ブチル基等の分枝をさらに有していてもよい。また、炭素数が2以上の場合、これら2価の炭化水素基に含まれるメチレンのうち1つがエーテル結合に置換されていてもよい。
【0062】
式(2)において、Ar21及びAr22は、それぞれ置換あるいは無置換のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。
【0063】
Ar21及びAr22で表されるアリール基とは、ベンゼン環を2つ以上含む1価のアリール基をいう。例えば、ビフェニルイル基等が挙げられる。
【0064】
Ar21及びAr22で表される縮合多環芳香族基とは、ベンゼン環を2つ以上含む縮合多環芳香族基をいう。例えば、フルオレニル基、フルオランテニル基、ナフチル基、フェナントリル基、ジヒドロフェナントリル基、ピレニル基、ペリレニル基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基等が挙げられる。好ましくは、フルオレニル基である。
【0065】
上記のアリール基及び縮合多環芳香族基がさらに有してもよい置換基として、メチル基、エチル基、プロピル基、ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0066】
式(2)において、Ar23は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。
【0067】
Ar23で表される2価のアリール基とは、ベンゼン環を2つ以上含む2価のアリール基をいう。例えば、ビフェニレン基等が挙げられる。
【0068】
Ar23で表される2価の縮合多環芳香族基とは、ベンゼン環を2つ以上含む2価の縮合多環芳香族基をいう。例えば、フルオレン、フルオランテン、フェニルナフタレン、フェナントレン、ジヒドロフェナントレン、ピレン、ペリレン、ベンゾアントラセン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン等を基本骨格とした2価の置換基が挙げられる。
【0069】
上記の2価のアリール基及び2価の縮合多環芳香族基がさらに有してもよい置換基として、メチル基、エチル基、プロピル基、ブチル基、tert−ブチル基、トリフルオロメチル基等のアルキル基、ベンジル基、フェネチル基、ナフチルメチル基等のアラルキル基、フェニル基、ナフチル基、アンスリル基、ピレニル基、フルオレニル基等の芳香族炭化水素環基、カルバゾリル基、ジベンゾフリル基、ジベンゾチエニル基、チエニル基等の芳香族複素環基、メトキシ基、エトキシ基、プロポキシ基等のアルコキシ基、フェノキシ基、ナフトキシ基等のアリールオキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子、ニトロ基、シアノ基等が挙げられる。
【0070】
式(2)において、R21及びR22は、それぞれ水素原子又はメチル基を表す。
【0071】
式(2)の(メタ)アクリルポリマーは、特定の(メタ)アクリル酸エステル化合物を加熱重合することで得られるものである。尚、その(メタ)アクリル酸エステル化合物の具体的な構造については後述する。
【0072】
本発明の有機発光素子において、第一の有機化合物層に含まれるアリールアミンポリマー及び第二の有機化合物層に含まれる(メタ)アクリル酸エステル化合物は、いずれも電荷輸送機能に優れる特定のアリールアミン構造を含む化合物である。このように共通した部分構造を有する有機化合物を、互いに隣接する層にそれぞれ含ませることにより、電極からの電荷注入性や層内の電荷輸送性が向上する。
【0073】
また、アリールアミン骨格を有する化合物は、古くから正孔輸送性材料として知られており、電子供与性のアミンに由来してHOMOエネルギーを高く調節することが可能な物質である。有機発光素子において、HOMOエネルギーは、素子の発光効率や耐久性に強い影響を与えるパラメータであることが一般的に知られている。このため、式(1)のアリールアミンポリマーを含む第一の有機化合物層と、式(2)の(メタ)アクリル酸エステルポリマーを含む第二の有機化合物層と、の各々のHOMOエネルギーを特定の範囲内の値で微細に調整することが可能となる。このように、本発明の有機発光素子は、第一の有機化合物層と第二の有機化合物層とが隣接するように積層されている。このため同等のHOMOエネルギーを有する有機化合物層が隣接して積層している形式となり、層間における電荷注入性が向上される。
【0074】
次に、本発明の有機発光素子を構成する他の構成部材について説明する。
【0075】
陽極を構成する材料は、仕事関数がなるべく大きなものがよい。例えば、金、銀、白金、ニッケル、パラジウム、コバルト、セレン、バナジウム等の金属単体あるいはこれらを複数組み合わせた合金、酸化錫、酸化亜鉛、酸化錫インジウム(ITO),酸化亜鉛インジウム等の金属酸化物が使用できる。また、ポリアニリン、ポリピロール、ポリチオフェン、ポリフェニレンスルフィド等の導電性ポリマーも使用できる。これらの電極物質は、一種類を単独で使用してもよく、二種類以上を併用して使用してもよい。
【0076】
一方、陰極の構成材料は、仕事関数のなるべく小さなものがよい。例えば、リチウム、ナトリウム、カリウム、セシウム、カルシウム、マグネシウム、アルミニウム、インジウム、銀、鉛、錫、クロム等の金属単体、これら金属単体を複数組み合わせた合金又はこれら金属単体の塩等を使用することができる。また酸化錫インジウム(ITO)等の金属酸化物の利用も可能である。ここで、陰極は一層で構成されていてもよく、複数の層で構成されていてもよい。
【0077】
本発明の有機発光素子で使用する基板としては、特に限定するものではないが、金属製基板、セラミックス製基板等の不透明性基板、ガラス、石英、プラスチックシート等の透明性基板が用いられる。また、基板にカラーフィルター膜、蛍光色変換フィルター膜、誘電体反射膜等を用いて発色光をコントロールすることも可能である。
【0078】
尚、作製した有機発光素子に対して、酸素や水分等との接触を防止する目的で、保護層又は封止層を設けることもできる。保護層としては、ダイヤモンド薄膜、金属酸化物、金属窒化物等の無機材料膜、フッ素樹脂、ポリパラキシレン、ポリエチレン、シリコーン樹脂、ポリスチレン樹脂、エポキシ樹脂、フェノール樹脂、尿素樹脂等の高分子膜又は光硬化性樹脂等が挙げられる。また、ガラス、気体不透過性フィルム、金属等をカバーし、適当な封止樹脂により素子自体をパッケージングすることもできる。
【0079】
次に、本発明の有機発光素子の製造方法について説明する。
【0080】
本発明の有機発光素子の製造方法は、以下に示す工程を含むことを特徴とする。
(i)下部電極上に塗布法によりアリールアミンポリマーからなる第一の有機化合物層を形成する工程(以下、第一の工程という。)
(ii)第一の有機化合物層上に塗布法によりアリールアミン骨格を有する(メタ)アクリル酸エステル化合物からなる薄膜を形成する工程(以下、第二の工程という。)
(iii)第二の工程で形成した薄膜を加熱硬化して第二の有機化合物層を形成する工程(以下、第三の工程という。)
(iv)第二の有機化合物層上に塗布法により第三の有機化合物層を形成する工程(以下、第四の工程という。)
【0081】
まず第一の工程について説明する。第一の工程によって形成される第一の有機化合物層を構成するアリールアミンポリマーとは、式(1)で示されるアリールアミンポリマーである。
【0082】
塗布法により、式(1)のアリールアミンポリマーからなる第一の有機化合物層を形成する際には、以下に説明する第一の塗料組成物を調製して、この第一の塗料組成物を塗布して薄膜を形成した方がよい。この第一の塗料組成物を使用すれば、有機発光素子を構成する有機化合物層、特に、電荷注入層又は電荷輸送層を塗布法により作製することが可能となり、比較的安価で大面積の有機発光素子を容易に作製することができる。
【0083】
ここで第一の塗料組成物には、式(1)のアリールアミンポリマーが少なくとも一種類含まれるものである。式(1)のアリールアミンポリマーは、一種類を単独で使用してもよいし、二種類以上を混合して使用してもよい。
【0084】
また式(1)のアリールアミンポリマーと他の有機化合物とを組み合わせて膜を形成してもよい。式(1)のアリールアミンポリマーと組み合わせて使用することができる有機化合物として、例えば、トリアリールアミン誘導体、フェニレンジアミン誘導体、トリアゾール誘導体、オキサジアゾール誘導体、イミダゾール誘導体、ピラゾリン誘導体、ピラゾロン誘導体、オキサゾール誘導体、フルオレノン誘導体、ヒドラゾン誘導体、スチルベン誘導体、フタロシアニン誘導体、ポルフィリン誘導体、ポリ(ビニルカルバゾール)、ポリ(シリレン)、ポリ(チオフェン)等が挙げられるが、これらに限定されるものではない。
【0085】
この第一の塗料組成物を調製するために使用する溶媒として、例えば、トルエン、キシレン、メシチレン、テトラリン、n−ドデシルベンゼン、メチルナフタレン等の炭化水素系溶剤、テトラヒドロフラン、ジオキサン、ジグライム等のエーテル系溶剤、クロロホルム、モノクロロベンゼン、1,2−ジクロロベンゼン等のハロゲン系溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン系溶剤、酢酸メチル、酢酸エチル、酢酸n−ブチル等のエステル系溶剤、メタノール、エタノール、n−プロパノール等のアルコール系溶剤、等が挙げられる。これらの溶媒は一種類を単独で使用してもよいし、二種類以上を混合して使用してもよい。また、これらの溶媒の粘度や、溶液中のアリールアミンポリマーの濃度を調整することにより、アリールアミンポリマー薄膜の膜厚を調整することができる。
【0086】
第一の塗料組成物に含まれる式(1)のアリールアミンポリマーの含有量は、組成物全体を基準として、好ましくは、0.05重量%以上20重量%以下であり、より好ましくは、0.1重量%以上5重量%以下である。
【0087】
第一の塗料組成物を電極上に塗布する方法として、具体的には、キャスト法、スピンコート法、スリットコーター法、印刷法、インクジェット法、デイスペンス法、スプレー法、ディップ法、LB膜法等が挙げられる。
【0088】
第一の工程によって形成される第一の有機化合物層の膜厚は、5μmより薄く、好ましくは500nm以下であり、より好ましくは5nm乃至500nmである。
【0089】
次に、第二の工程について説明する。第二の工程によって形成される薄膜を構成するアリールアミン骨格を有する(メタ)アクリル酸エステル化合物とは、好ましくは、下記一般式(3)で示される(メタ)アクリル酸エステル化合物である。
【0090】
【化14】

【0091】
式(3)において、A21及びA22は、それぞれ炭素数1以上8以下の2価の炭化水素基を表す。Ar21及びAr22は、それぞれ置換あるいは無置換のアリール基又は置換あるいは無置換の1価の縮合多環芳香族基を表す。Ar23は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。R21及びR22は、それぞれ水素原子又はメチル基を表す。
【0092】
A21、A22、Ar21、Ar22及びAr23の具体例は、式(2)の(メタ)アクリル酸エステルポリマーの具体例と同様である。またAr21及びAr22で表されるアリール基及び縮合多環芳香族基がさらに有してもよい置換基の具体例も、式(2)の(メタ)アクリル酸エステルポリマーの具体例と同様である。さらにAr23で表される2価のアリール基及び2価の縮合多環芳香族基がさらに有してもよい置換基の具体例も、式(2)の(メタ)アクリル酸エステルポリマーの具体例と同様である。
【0093】
次に、本発明の重合性官能基を有するアリールアミン化合物の具体例を、例示化合物として以下に示す。ただし、本発明はこれら具体例に限定されるものではない。
【0094】
【化15】

【0095】
【化16】

【0096】
【化17】

【0097】
【化18】

【0098】
【化19】

【0099】
【化20】

【0100】
第二の工程を行うにあたり、塗布法等の湿式法により薄膜を形成する際には、式(3)の(メタ)アクリル酸エステル化合物を含む第二の塗料組成物を調製し、この第二の塗料組成物を塗布して成膜する方法がよい。
【0101】
ここで第二の塗料組成物とは、式(3)の(メタ)アクリル酸エステル化合物を少なくとも一種類含有する。式(3)の(メタ)アクリル酸エステル化合物は一種類を単独で使用してもよいし、また二種類以上を混合して使用してもよい。
【0102】
さらに式(3)の(メタ)アクリル酸エステル化合物と、他の有機化合物とを組み合わせて薄膜を形成することもできる。式(3)の(メタ)アクリル酸エステル化合物と組み合わせて使用することができる有機化合物として、例えば、トリアリールアミン誘導体、フェニレンジアミン誘導体、トリアゾール誘導体、オキサジアゾール誘導体、イミダゾール誘導体、ピラゾリン誘導体、ピラゾロン誘導体、オキサゾール誘導体、フルオレノン誘導体、ヒドラゾン誘導体、スチルベン誘導体、フタロシアニン誘導体、ポルフィリン誘導体、及びポリ(ビニルカルバゾール)、ポリ(シリレン)、ポリ(チオフェン)等が挙げられるが、これらに限定されるものではない。
【0103】
第二の塗料組成物に使用する溶媒としては、例えば、トルエン、キシレン、メシチレン、テトラリン、n−ドデシルベンゼン、メチルナフタレン等の炭化水素系溶剤、テトラヒドロフラン、ジオキサン、ジグライム等のエーテル系溶剤、クロロホルム、モノクロロベンゼン、1,2−ジクロロベンゼン等のハロゲン系溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン系溶剤、酢酸メチル、酢酸エチル、酢酸n−ブチル等のエステル系溶剤、メタノール、エタノール、n−プロパノール等のアルコール系溶剤等が挙げられる。これらの溶媒は一種類を単独で使用してもよいし、二種類以上を混合して使用してもよい。また、これらの溶媒の粘度や、溶液中の(メタ)アクリル酸エステル化合物の濃度を調整することにより、(メタ)アクリル酸エステル化合物からなる薄膜の膜厚を調整することができる。
【0104】
第二の塗料組成物に含まれる式(3)の(メタ)アクリル酸エステル化合物の含有量は、組成物全体を基準として、好ましくは、0.05重量%以上20重量%以下であり、より好ましくは、0.1重量%以上5重量%以下である。
【0105】
塗布法の具体的な手段として、キャスト法、スピンコート法、スリットコーター法、印刷法、インクジェット法、デイスペンス法、スプレー法、ディップ法、LB膜法等が挙げられる。
【0106】
ところで、(メタ)アクリル酸エステル化合物からなる薄膜を塗布法で成膜する場合は、適当な結着樹脂と組み合わせて膜を形成することもできる。
【0107】
上記結着樹脂としては様々な結着性樹脂から選択することができる。例えば、ポリビニルカルバゾール樹脂、ポリカーボネート樹脂、ポリエステル樹脂、ポリアリーレート樹脂、ポリスチレン樹脂、ポリアクリル樹脂、ポリメタクリル樹脂、ポリビニルブチラール樹脂、ポリビニルアセタール樹脂、ジアリルフタレート樹脂、フェノール樹脂、エポキシ樹脂、シリコーン樹脂、ポリスルホン樹脂、尿素樹脂等が挙げられるが、これらに限定されるものではない。また、結着樹脂の形態はホモポリマーであってもよいし共重合体ポリマーであってもよい。また、結着樹脂は一種類を単独で使用してもよいし、また二種類以上を混合して使用してもよい。
【0108】
また、(メタ)アクリル酸エステル化合物からなる薄膜を塗布法で成膜する場合は、重合開始剤を第二の塗料組成物に添加した上で薄膜を形成することもできる。重合開始剤としては、例えば、ラジカル重合開始剤、カチオン重合開始剤、光重合開始剤等が挙げられる。
【0109】
上記の第二の塗料組成物は、式(1)のアリールアミンポリマーを溶解させない溶剤を使用して調製するのが好ましい。こうすることで第一の有機化合物層の上部へ、第二の有機化合物層となる薄膜を成膜・積層することができる。
【0110】
次に、第三の工程について説明する。第二の工程において形成された(メタ)アクリル酸エステル化合物からなる薄膜を加熱硬化する際は、その加熱温度は特に限定されないが、一般的には130℃乃至200℃の範囲で行う。
【0111】
第三の工程を行うことによって形成される第二の有機化合物層の膜厚は、5μmより薄く、好ましくは500nm以下であり、より好ましくは5nm乃至500nmである。
【0112】
本発明の有機発光素子において、式(1)のアリールアミンポリマーを含む第一の有機化合物層の上部に、他の有機化合物層を塗布法により形成する場合、第一の有機化合物層から層を構成する物質が溶け出さないことが求められる。
【0113】
一方で、第一の有機化合物層を構成する式(1)のアリールアミンポリマーは、直鎖状にモノマーユニットが連なった構造のポリマーである。ここで直鎖状のアリールアミンポリマーは、一般的に、有機溶剤への溶解性が高い。このため、塗布法により他の有機層を積層するときに当該アリールアミンポリマーが溶け出さないようにためには、第一の有機化合物層上に塗布可能な溶剤の種類は限定される。塗布可能な溶剤の種類が限定されると、塗布により成膜できる有機材料の種類もまた限定される。従って、利用可能な有機材料の種類を増やすために、好ましくは、第一の有機化合物層を不溶化する。
【0114】
本発明の有機発光素子の製造方法では、第一の有機化合物層を不溶化するために、第一の有機化合物の上に、アリールアミン骨格を有する(メタ)アクリル酸エステル化合物が含まれる薄膜を塗布により成膜し、加熱処理を行う方法を採用する。この方法によって形成される第二の有機化合物層は、加熱処理を行うことにより、薄膜を構成する(メタ)アクリル酸エステル化合物が重合反応を起こすので、層自体が不溶化する。
【0115】
ところで、式(3)の(メタ)アクリル酸エステル化合物は、加熱、重合開始剤等によるラジカル重合反応により、分子間架橋反応が起こる。この分子間架橋反応により、アリールアミン骨格を有する(メタ)アクリル酸エステルポリマー薄膜が形成される。この薄膜は架橋構造を有する化合物で構成されているポリマー薄膜であるので、溶媒に対して不溶の薄膜となっている。このため、次の第四の工程として、この薄膜の上から塗布法により他の有機化合物層を積層したとしても、既に形成したポリマー薄膜が溶媒によって溶かされることはない。またこのポリマー薄膜を形成することによって、ポリマー薄膜自体のみならず、当該ポリマー薄膜より下の層を構成する材料が塗料に含まれる溶媒によって溶解されるのを防ぐことができる。よって本発明の有機発光素子の製造方法では、層を構成する材料同士の混入がない安定した積層体を有する素子を作製することができる。
【0116】
以上より、第二の工程により第二の有機化合物層となる薄膜の成膜を行った後、第三の工程により加熱処理を行うことで、当該薄膜の構成材料である(メタ)アクリル酸エステル化合物は重合反応を起こし、当該薄膜は溶媒に対して不溶な薄膜となる。このような薄膜を形成することにより、第一の有機化合物層は第二の有機化合物層と同様に有機溶剤に不溶となるので、第四の工程において、第二の有機化合物層である薄膜の上部へ、塗布法により第三の有機化合物層となる薄膜を形成・積層することが可能となる。
【0117】
以上の(i)乃至(iv)で示した4工程により、本発明の有機発光素子の主要構成となる3つの層(第一の有機化合物層、第二の有機化合物層、第三の有機化合物層)を塗布法によって形成することができる。一方で、式(1)で示されるアリールアミンポリマー及び式(3)で示される(メタ)アクリル酸エステル化合物は、蒸着法による成膜には適さない。このため、本発明の有機発光素子の主要構成となる3つの層を形成する際には、蒸着法を採用することができない。
【0118】
上記に示した本発明の製造方法により製造される有機発光素子は、少なくとも3つの有機化合物層からなる積層構造を有している。ここで有機化合物層として、具体的には、正孔注入層、正孔輸送層、発光層、正孔/エキシトンブロッキング層、電子輸送層、電子注入層等が挙げられる。これらの層のうち、上述した第一の有機化合物層、第二の有機化合物層及び第三の有機化合物層に該当する層は、塗布法によって形成されるものである。一方、これら3つの層以外の有機化合物層は、真空蒸着法や溶液塗布法等の如何なる方法によっても形成することができる。ここで製造される有機発光素子の膜厚は5μmより薄く、好ましくは、1μm以下であり、より好ましくは、5nm以上500nm以下である。
【0119】
本発明の有機発光素子を適宜組み合わせることにより、ディスプレイ等の表示装置を構成することができる。即ち、本発明の表示装置は、本発明の有機発光素子と、該有機発光素子の駆動回路と、を複数具備するものであり、パッシブマトリックス方式又はアクティブマトリックス方式で駆動される。以下、図面を参照しながら、本発明の有機発光素子を、アクティブマトリクス方式に組み合わせた表示装置について説明する。
【0120】
図4は、本発明の表示装置の一部分を示す断面模式図である。図4で示される表示装置40は、基板41上に設けられている有機発光素子部42と、有機発光素子部42の外部に配置されている回路部43と、回路部43に隣接して設けられているデータ配線44と、から構成される。ここで回路部43には、ドライブトランジスタ(TFT1)451と、スイッチングトランジスタ(TFT2)452と、保持容量(Ch)46と、が設けられている。
【0121】
図4において、有機発光素子は1個のみ図示されているが、実際に表示装置を構築する場合は、有機発光素子は二次元状に複数配置されている。有機発光素子が二次元状に配置されている表示装置の具体例は後述する。また本実施形態において、有機発光素子部42は、下部電極47と、有機化合物層48と、上部電極49とがこの順に積層されているものである。この有機発光素子部42において、有機化合物層48は、少なくとも上記の第一の有機化合物層、第二の有機化合物層及び第三の有機化合物層が含まれる。
【0122】
図5は、図4の表示装置の回路部における回路の構成の詳細を示す図である。図5で示される回路は、電流プログラミング方式とよばれる代表的な回路構成である。尚、本発明のディスプレイで採用できる回路はこれに限るものではない。図5で示される回路50は、ドライブトランジスタ(TFT1)451、スイッチングトランジスタ(TFT2)452、保持容量(Ch)46、有機発光素子51から構成されている。尚、周知な回路構成であるため動作の詳細については説明を省略する。
【0123】
ところで本発明の有機発光素子は、1つの発光点として利用して、ディスプレイ等の表示装置や照明装置や電子写真方式の画像形成装置の露光光源に使用することができる。
【0124】
本発明の有機発光素子をディスプレイに利用した場合について以下に説明する。
【0125】
図6は、図4及び図5で示される有機発光素子部及び回路部を1画素としてマトリックス状に配置した表示装置を示す模式図である。
【0126】
図6の表示装置60において、画素61は、配線を介してゲートドライバ62と、ソースドライバ63とに接続され、各ドライバから供給される駆動パルスにより、発光状態あるいは非発光状態となる。
【0127】
このように本発明の有機発光素子が、画素として同一面内に面内方向に複数配置されている領域が本発明の表示装置の表示領域である。即ち、本発明の有機発光素子は本発明の表示装置の表示領域として使用することができる。
【0128】
本発明の表示装置は、例えば、テレビやPC用の表示装置、あるいは画像を表示する部分を有する機器であれば如何なる実施形態も問わない。例えば、本発明の表示装置が搭載される携帯型表示装置であってもよい。あるいはデジタルカメラ等の電子撮像装置や携帯電話の表示部に本発明の表示装置を使用することができる。
【0129】
図7は、図6の表示装置をパネルモジュール化した構成例を示す模式図である。図7のパネルモジュール70は、図6に示される表示装置60に加え、インターフェースドライバ71と、ゲートドライバ62と、ソースドライバ63と、を筐体72で一体化したものである。尚、図7のパネルモジュール70において、図示はしていないが、接続端子等の外部機器との接続に必要な部品(インターフェース)が筐体72に内蔵されている。
【実施例】
【0130】
[HOMOレベルの評価]
各実施例及び各比較例において使用した材料のうち主要な材料については、材料自体のHOMOエネルギーを評価した。ここでHOMOエネルギーとは、材料自体の最高被占分子軌道(HOMO)と真空準位との間のエネルギー差に相当するものであり、イオン化ポテンシャルと同義である。HOMOエネルギーの評価方法としては、光電子分光法により測定した値から評価する方法を採用した。また光電子分光の測定装置として、光電子分光装置AC−2(理研機器製)を用いた。
【0131】
<合成例1>[例示化合物No.1−1の合成]
【0132】
【化21】

【0133】
(i)500mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
2−ヨードフルオレン誘導体(化合物[1]):30g(93.7mmol)
アセトアミド(化合物[2]):5.5g(93.7mmol)
銅粉:11.9g(187.4mmol)
炭酸カリウム:25.9g(187.4mmol)
1,2−ジクロロベンゼン:250ml
【0134】
次に、反応溶液を180℃に加熱し16時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出した。次に、有機層を無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより、化合物[3]を白色結晶として20.0g(収率85%)得た。
【0135】
(ii)300mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
4,4’−ジヨードビフェニル(化合物[4]):10.1g(24.9mmol)
化合物[3]:15.0g(59.7mmol)
銅粉:6.3g(99.6mmol)
炭酸カリウム:13.8g(99.6mmol)
1,2−ジクロロベンゼン:150ml
【0136】
次に、反応溶液を180℃に加熱し24時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出した。次に、有機層を無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより、中間体化合物[5]を白色結晶として11.7g(収率72%)得た。
【0137】
(iii)300mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[5]:10.0g(15.3mmol)
2−メトキシエタノール:50ml
トルエン:50ml
【0138】
次に、窒素雰囲気下、室温で、ナトリウムメトキサイド2.1g(38.3mmol)をさらに添加した後、反応溶液を60℃に加熱し3時間攪拌した。反応終了後、水を加えてから、有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。次に、有機層を減圧濃縮した後、濃縮物についてシリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサンとトルエンとの混合溶媒)で精製することにより、アリールアミン化合物である中間体化合物[6]を白色結晶として8.3g(収率95%)得た。
【0139】
(iv)100ml三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[6]:1.5g(2.64mmol)
4,4’−ジブロモビフェニル(化合物[7]):0.82g(2.64mmol)
キシレン:50ml
次に、窒素雰囲気下、室温で、ナトリウムtert−ブトキサイド0.25g(2.64mmol)を添加した。次に、酢酸パラジウム0.03g(0.13mmol)とトリ−tert−ブチルホスフィン0.025g(0.13mmol)とを添加した後、反応溶液を130℃に加熱し12時間撹拌した。反応終了後、水を加えてから有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。次に、有機層を減圧濃縮した後、濃縮物についてシリカゲルカラムクロマトグラフィー(展開溶媒:トルエン)で精製した。次に、メタノールで再沈殿を行い、沈殿物をろ取することにより、例示化合物No.1−1を黄色アモルファスとして0.91g(収率48%)得た。
【0140】
<合成例2>[例示化合物No.1−2の合成]
【0141】
【化22】

【0142】
(i)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[6]:3.0g(5.27mmol)
4−ブロモヨードベンゼン(化合物[8]):3.6g(12.7mmol)
銅粉:1.0g(15.8mmol)
炭酸カリウム:2.2g(15.8mmol)
1,2−ジクロロベンゼン:100ml
【0143】
次に、反応溶液を180℃に加熱し24時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出し、無水硫酸ナトリウムで乾燥した後、溶媒を減圧留去した。これによって得られた粗生成物についてシリカゲルカラムカラムクロマトグラフィー(展開溶媒:ヘキサンとトルエンとの混合溶媒)で精製することにより、アリールアミン化合物である中間体化合物[9]を黄色結晶として2.41g(収率52%)得た。
【0144】
(ii)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[9]:1.5g(1.71mmol)
ジピナコールボラン体(化合物[10]):0.76g(1.71mmol)
トルエン:50ml
エタノ−ル:20ml
【0145】
次に、反応溶液を窒素雰囲気下、室温で攪拌しながら、炭酸ナトリウム3.2gと水15mlとを混合して調製した水溶液を滴下し、次いでテトラキス(トリフェニルホスフィン)パラジウム(0)0.10g(0.09mmol)を添加した。次に、反応溶液を還流させながら10時間攪拌した。反応終了後、有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。有機層を減圧濃縮した後、得られた濃縮物について、シリカゲルカラムクロマトグラフィー(展開溶媒:トルエン)で精製した。次に、メタノールで再沈殿して、沈殿物をろ取することにより、例示化合物No.1−2を黄色アモルファスとして0.90g(収率58%)得た。
【0146】
<合成例3>[例示化合物No.1−4の合成]
【0147】
【化23】

【0148】
(i)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[6]:3.0g(5.27mmol)
3−ブロモヨードベンゼン(化合物[11]):3.6g(12.7mmol)
銅粉:1.0g(15.8mmol)
炭酸カリウム:2.2g(15.8mmol)
1,2−ジクロロベンゼン:100ml
【0149】
次に、反応溶液を180℃に加熱し24時間攪拌した。反応終了後、反応溶液をろ過し、有機層をクロロホルムで抽出し無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。これによって得られた粗生成物について、シリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサンとトルエンとの混合溶媒)で精製することにより、アリールアミン化合物である中間体化合物[12]を白色結晶として2.87g(収率62%)得た。
【0150】
(ii)200mlの三ツ口フラスコに、以下に示す試薬、溶媒を仕込んだ。
中間体化合物[12]:1.5g(1.71mmol)
ジピナコールボラン体(化合物[10]):0.76g(1.71mmol)
トルエン:50ml
エタノ−ル:20ml
【0151】
次に、反応溶液を窒素雰囲気下室温で攪拌しながら、炭酸ナトリウム3.2gと水15mlとを混合して調製した水溶液を滴下し、次いでテトラキス(トリフェニルホスフィン)パラジウム(0)0.10g(0.09mmol)を添加した。次に、反応溶液を還流させながら10時間攪拌した。反応終了後、有機層をトルエンで抽出し無水硫酸ナトリウムで乾燥した。次に、溶媒を減圧留去した。これにより得られた粗生成物について、シリカゲルカラムクロマトグラフィー(展開溶媒:トルエン)で精製した後、メタノールで再沈殿を行い、沈殿物をろ取することにより、例示化合物No.1−4を白色アモルファスとして0.65g(収率42%)得た。
【0152】
<合成例4>[例示化合物No.2−1の合成]
フラスコ内で、以下の試薬、溶媒を仕込み、フラスコを氷水バスで冷却した。
下記式で示されるジヒドロキシ体:1.0g(1.37mmol)
【0153】
【化24】

トリエチルアミン:0.49g(4.80mmol)
テトラヒドロフラン:10ml
【0154】
次に、反応溶液の温度を10℃以下に保ちながら、この反応溶液中にアクリル酸クロライド0.37g(4.11mmol)を滴下した。滴下終了後、反応溶液を徐々に昇温させ、反応用液の温度を50℃に保ちながらさらに30分間反応を続けた。
【0155】
反応終了後、反応溶液を冷却した。次に、この反応溶液に、酢酸エチル100mlと、10%水酸化ナトリウム水溶液50mlとをそれぞれ加えて攪拌した後、分液操作を行い、有機層を回収した。回収した有機層を、さらにイオン交換水30mlで2回洗浄し、硫酸マグネシウムで乾燥させた。
【0156】
次に、この有機層中の溶媒を、ロータリーエバポレーターを用いて除去し、粗生成物を得た。この粗生成物について、シリカゲルカラムクロマトグラフィーを用いて精製を行った。具体的には、シリカゲル約10gを使用し、展開溶媒は、始めはトルエンを使用し、途中からトルエン/テトラヒドロフラン混合溶媒(混合比:10/1)を使用した。
【0157】
最後に目的化合物に該当するフラクションを回収し溶媒を減圧除去することにより、目的とする例示化合物No.2−1を0.77g得た。
【0158】
<合成例5>[例示化合物No.2−8の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.12mmol)
【0159】
【化25】

トリエチルアミン:0.42g(3.92mmol)
テトラヒドロフラン:10ml
アクリル酸クロライド:0.30g(3.36mmol)
【0160】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−8を0.75g得た。
【0161】
<合成例6>[例示化合物No.2−9の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.24mmol)
【0162】
【化26】

トリエチルアミン:0.44g(4.34mmol)
テトラヒドロフラン:10ml
アクリル酸クロライド:0.33g(3.72mmol)
【0163】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−9を0.72g得た。
【0164】
<合成例7>[例示化合物No.2−10の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.19mmol)
【0165】
【化27】

トリエチルアミン:0.43g(4.18mmol)
テトラヒドロフラン:10ml
アクリル酸クロライド:0.32g(3.57mmol)
【0166】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−10を0.77g得た。
【0167】
<合成例8>[例示化合物No.2−15の合成]
各合成試薬を下記の量使用し、合成例4と同様な操作により合成を行った。
下記構造式で示されるジヒドロキシ体:1.0g(1.19mmol)
【0168】
【化28】

トリエチルアミン:0.43g(4.18mmol)
テトラヒドロフラン:10ml
メタクリル酸クロライド:0.37g(3.57mmol)
【0169】
反応終了後、合成例4と同様に精製を行うことにより、目的とする例示化合物No.2−15を0.78g得た。
【0170】
[実施例1]
図2に示される有機発光素子を作製した。
【0171】
ガラス基板(基板1)上に、酸化錫インジウム(ITO)をスパッタ法にて成膜することにより陽極2を形成した。このとき陽極2の膜厚を120nmとした。次に、このITOが成膜されている基板をアセトン、イソプロピルアルコール(IPA)で順次超音波洗浄し、次いでIPAで煮沸洗浄した後乾燥した。次に、このITOが成膜されている基板をUV/オゾン洗浄した。以上のように処理した基板を透明導電性支持基板として使用した。
【0172】
次に、例示化合物No.1−1をクロロホルムに溶解し、濃度0.5重量%のクロロホルム溶液(以下、本実施例において正孔注入層形成用塗料という。)を調製した。次に、この正孔注入層形成用塗料を陽極2上に滴下しスピンコートすることにより正孔注入層3を形成した。このとき正孔注入層3の膜厚は15nmであった。
【0173】
次に、例示化合物No.2−10をメチルイソブチルケトンに溶解し、濃度0.5重量%のメチルイソブチルケトン溶液(以下、本実施例において正孔輸送層形成用塗料という。)を調製した。次に、この正孔輸送層形成用塗料を正孔注入層3上に滴下しスピンコートして薄膜を形成した。次に、この薄膜を200℃で30分間加熱し硬化することにより正孔輸送層4を形成した。このとき正孔輸送層4の膜厚は15nmであった。尚、加熱処理を行うことにより、当該薄膜を構成する例示化合物No.2−10が架橋反応を起こし、当該薄膜は硬化した。このため正孔輸送層4は、溶剤に対して不溶の膜となった。
【0174】
次に、以下に示す試薬、溶媒を混合し、発光層形成用塗料を調製した。
【0175】
Ir(ppy)3(トリス(2−フェニルピリジン)イリジウム):0.01質量部
PBD(2−(4−ビフェニル)−5−(4−ブチルフェニル)−1,3,4−オキサジアゾール):0.3質量部
PVK(ポリビニルカルバゾール、Mn=35000):0.7質量部
【0176】
【化29】

クロロベンゼン:99質量部
【0177】
次に、この発光層形成用塗料を正孔輸送層4上に滴下し、回転数1000rpmで1分間スピンコートを行うことで薄膜を形成した。次に、120℃で30分間加熱して当該薄膜中の溶剤を蒸発させることにより発光層5を形成した。このとき発光層5の膜厚は100nmであった。
【0178】
次に、真空蒸着法によりフッ化リチウムを発光層5上に蒸着することで電子注入層7を形成した。このとき電子注入層7の膜厚を0.5nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度を0.01nm/secの条件とした。
【0179】
次に、真空蒸着法によりアルミニウムを電子注入層7上に蒸着することで陰極6を形成した。このとき陰極6の膜厚を100nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度は1.0nm/sec乃至1.2nm/secの条件とした。
【0180】
次に、窒素雰囲気下において、保護用ガラス板を被せてアクリル樹脂系接着剤で封止した。以上のようにして有機発光素子を得た。
【0181】
得られた素子について、ITO電極を陽極に、アルミニウム電極を陰極にして7Vの直流電圧を印加すると、素子に電流が流れた。このときの電流密度は29mA/cm2であり、輝度3010cd/m2の緑色発光が観測された。また、電流密度を10mA/cm2に保ち50時間連続駆動したところ、960cd/m2(初期輝度)から700cd/m2(50時間後の輝度)に変化した。
【0182】
[実施例2]
実施例1において、例示化合物No.1−1に代えて例示化合物No.1−2を使用して正孔注入層3を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0183】
[実施例3]
実施例1において、例示化合物No.1−1に代えて例示化合物No.1−4を使用して正孔注入層3を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0184】
[実施例4]
実施例1において、例示化合物No.2−10に代えて例示化合物No.2−15を使用して正孔輸送層4を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0185】
[実施例5]
実施例1において、例示化合物No.2−10に代えて例示化合物No.2−12を使用して正孔輸送層4を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0186】
[実施例6]
実施例1において、例示化合物No.2−10に代えて例示化合物No.2−1を使用して正孔輸送層4を形成した。これ以外は実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0187】
[比較例1]
実施例1において、例示化合物No.1−1に代えて下記式に示される比較化合物No.1(4−ポリエチレンジオキシチオフェン/ポリスチレンスルホン酸(PEDOT/PSS)、商品名:バイトロンP Al−4083、バイエル社製)を使用した。また、陽極2上に比較化合物No.1を滴下しスピンコートした後、120℃で30分加熱することで、膜厚30nmの正孔注入層3を形成した。これらを除いては実施例1と同様の方法により有機発光素子を作製した。また得られた素子について実施例1と同様に評価を行った。結果を表1に示す。
【0188】
【化30】

【0189】
【表1】

【0190】
[実施例7]
図2に示される有機発光素子を作製した。
【0191】
ガラス基板(基板1)上に、酸化錫インジウム(ITO)をスパッタ法にて成膜することにより陽極2を形成した。このとき陽極2の膜厚を120nmとした。次に、このITOが成膜されている基板をアセトン、イソプロピルアルコール(IPA)で順次超音波洗浄し、IPAで煮沸洗浄後乾燥をした。次に、このITOが成膜されている基板をUV/オゾン洗浄した。以上のようにして処理した基板を透明導電性支持基板として使用した。
【0192】
次に、例示化合物No.1−1をp−キシレンに溶解し、濃度0.5重量%のp−キシレン溶液(以下、本実施例において正孔注入層形成用塗料という。)を調製した。この正孔注入層形成用塗料を陽極2上に滴下しスピンコートすることにより正孔注入層3を形成した。このとき正孔注入層3の膜厚は15nmであった。
【0193】
次に、例示化合物No.2−10をメチルイソブチルケトンに溶解し、濃度0.5重量%のメチルイソブチルケトン溶液(以下、本実施例において正孔輸送層形成用塗料という。)を調製した。次に、この正孔輸送層形成用塗料を正孔注入層3上に滴下しスピンコートして薄膜を形成した。次に、この薄膜を200℃で30分間加熱し硬化することにより正孔輸送層4を形成した。このとき正孔輸送層4の膜厚は15nmであった。尚、加熱処理を行うことにより、当該薄膜を構成する例示化合物No.2−10が架橋反応を起こし、当該薄膜は硬化した。このため正孔輸送層4は、溶剤に対して不溶の膜となった。
【0194】
次に、以下に示す試薬、溶媒を混合し発光層形成用塗料を調製した。
例示化合物No.2−10:1質量部
下記式に示される緑色燐光材料:0.01質量部
【0195】
【化31】

クロロホルム:99質量部
【0196】
次に、この発光層形成用塗料を正孔輸送層4上に滴下し、回転数1000rpmで1分間スピンコートを行うことで薄膜を形成した。次に、80℃で30分間加熱し当該薄膜中に含まれる溶剤を蒸発させることにより発光層5を形成した。このとき発光層3の膜厚は80nmであった。
【0197】
次に、真空蒸着法によりフッ化リチウムを発光層5上に蒸着することで電子注入層7を形成した。このとき電子注入層7の膜厚を0.5nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度を0.01nm/secの条件とした。
【0198】
次に、真空蒸着法によりアルミニウムを電子注入層7上に蒸着することで陰極6を形成した。このとき陰極6の膜厚を100nmとし、蒸着時の真空度を1.0×10-4Paとし、成膜速度を1.0nm/sec乃至1.2nm/secの条件とした。
【0199】
次に、窒素雰囲気下において、保護用ガラス板を被せてアクリル樹脂系接着剤で封止した。以上のようにして有機発光素子を得た。
【0200】
得られた素子について、ITO電極を陽極に、アルミニウム電極を陰極にして7Vの直流電圧を印加すると、素子に電流が流れた。このときの電流密度は20mA/cm2であり、輝度1200cd/m2の赤色発光が観測された。また、電流密度を30mA/cm2に保ち50時間連続駆動したところ、1800cd/m2(初期輝度)から1100cd/m2(50時間後の輝度)に変化した。
【0201】
[実施例8]
実施例7において、例示化合物No.1−1に代えて例示化合物No.1−2を使用して正孔注入層3を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0202】
[実施例9]
実施例7において、例示化合物No.1−1に代えて例示化合物No.1−4を使用して正孔注入層3を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0203】
[実施例10]
実施例7において、例示化合物No.2−10に代えて例示化合物No.2−8を使用して正孔輸送層4を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0204】
[実施例11]
実施例7において、例示化合物No.2−10に代えて例示化合物No.2−9を使用して正孔輸送層4を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0205】
[実施例12]
実施例7において、例示化合物No.2−10に代えて例示化合物No.2−1を使用して正孔輸送層4を形成した。これ以外は実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0206】
[比較例2]
実施例7において、例示化合物No.1−1に代えて下記式に示される比較化合物No.2(ポリ[(9,9−ジヘキシルフルオレン−2,7−ジイル]−コ−[ピリジン−3,5−ジイル)]、H.W.SANDS社製)を使用した。また、陽極2上に比較化合物No.2を溶解した濃度0.5重量%のトルエン溶液を滴下しスピンコートした後、120℃で30分加熱することで、膜厚15nmの正孔注入層3を形成した。これらを除いては実施例7と同様の方法により有機発光素子を作製した。また得られた素子について実施例7と同様に評価を行った。結果を表2に示す。
【0207】
【化32】

【0208】
【表2】

【図面の簡単な説明】
【0209】
【図1】本発明の有機発光素子における第一の実施形態を示す断面図である。
【図2】本発明の有機発光素子における第二の実施形態を示す断面図である。
【図3】本発明の有機発光素子における第三の実施形態を示す断面図である。
【図4】本発明の表示装置の一部分を示す断面模式図である。
【図5】図4の表示装置の回路部における回路の構成の詳細を示す図である。
【図6】図4及び図5で示される有機発光素子部及び回路部を1画素としてマトリックス状に配置した表示装置を示す模式図である。
【図7】図6の表示装置をパネルモジュール化した構成例を示す模式図である。
【符号の説明】
【0210】
1,41 基板
2 陽極
3 発光層
4 陰極
5 正孔輸送層
6 電子輸送層
7 正孔注入層
8 電子注入層
10,20,30,51 有機発光素子
40,60 表示装置
42 有機発光素子部
43 回路部
44 データ配線
451 ドライブトランジスタ(TFT1)
452 スイッチィングトランジスタ(TFT2)
46 保持容量(Ch)
47 下部電極
48 有機化合物層
49 上部電極
50 回路
61 画素
62 ケースドライバ
63 ソースドライバ
70 パネルモジュール
71 インターフェースドライバ
72 筐体
【特許請求の範囲】
【請求項1】
陽極と陰極と、
該陽極と該陰極との間に挟持され少なくとも第一の有機化合物層と、第二の有機化合物層と、第三の有機化合物層とがこの順に含まれる積層体と、から構成され、
該陽極又は該陰極と該第一の有機化合物層と、該第一の有機化合物層と該第二の有機化合物層と、並びに該第二の有機化合物層と該第三の有機化合物層と、が互いに接しており、
該第一の有機化合物層にアリールアミンポリマーが含まれ、該第二の有機化合物層にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする、有機発光素子。
【請求項2】
前記アリールアミンポリマーが下記一般式(1)で示される化合物であることを特徴とする、請求項1に記載の有機発光素子。
【化1】

(式(1)において、R11及びR12は、それぞれ水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、アルコキシ基又はハロゲン原子を表す。Ar11及びAr12は、それぞれ置換あるいは無置換のアリール基又は縮合多環芳香族基を表す。Ar13は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。Ar14は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。mは、10以上300以下の整数を表す。nは、0以上300以下の整数を表す。)
【請求項3】
前記(メタ)アクリル酸エステルポリマーが下記一般式(2)で示される化合物であることを特徴とする、請求項1に記載の有機発光素子。
【化2】

(式(2)において、A21及びA22は、それぞれ炭素数1以上8以下の2価の炭化水素基を表す。Ar21及びAr22は、それぞれ置換あるいは無置換のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。Ar23は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。R21及びR22は、それぞれ水素原子又はメチル基を表す。)
【請求項4】
前記Ar21及びAr22が、置換あるいは無置換のフルオレニル基であることを特徴とする請求項3に記載の有機発光素子。
【請求項5】
下部電極上に塗布法によりアリールアミンポリマーからなる第一の有機化合物層を形成する工程と、
該第一の有機化合物層上に塗布法によりアリールアミン骨格を有する(メタ)アクリル酸エステル化合物からなる薄膜を形成する工程と、
該薄膜を加熱硬化して第二の有機化合物層を形成する工程と、
第二の有機化合物層上に塗布法により第三の有機化合物層を形成する工程と、を含むことを特徴とする、有機発光素子の製造方法。
【請求項6】
前記アリールアミンポリマーが下記一般式(1)で示される化合物であることを特徴とする、請求項5に記載の有機発光素子の製造方法。
【化3】

【請求項7】
前記(メタ)アクリル酸エステル化合物が一般式(3)で示される化合物であることを特徴とする、請求項5に記載の有機発光素子の製造方法。
【化4】

【請求項8】
請求項1乃至4のいずれか一項に記載の有機発光素子を具備することを特徴とする、表示装置。
【請求項1】
陽極と陰極と、
該陽極と該陰極との間に挟持され少なくとも第一の有機化合物層と、第二の有機化合物層と、第三の有機化合物層とがこの順に含まれる積層体と、から構成され、
該陽極又は該陰極と該第一の有機化合物層と、該第一の有機化合物層と該第二の有機化合物層と、並びに該第二の有機化合物層と該第三の有機化合物層と、が互いに接しており、
該第一の有機化合物層にアリールアミンポリマーが含まれ、該第二の有機化合物層にアリールアミン骨格を有する(メタ)アクリル酸エステルポリマーが含まれることを特徴とする、有機発光素子。
【請求項2】
前記アリールアミンポリマーが下記一般式(1)で示される化合物であることを特徴とする、請求項1に記載の有機発光素子。
【化1】

(式(1)において、R11及びR12は、それぞれ水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、アルコキシ基又はハロゲン原子を表す。Ar11及びAr12は、それぞれ置換あるいは無置換のアリール基又は縮合多環芳香族基を表す。Ar13は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。Ar14は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。mは、10以上300以下の整数を表す。nは、0以上300以下の整数を表す。)
【請求項3】
前記(メタ)アクリル酸エステルポリマーが下記一般式(2)で示される化合物であることを特徴とする、請求項1に記載の有機発光素子。
【化2】

(式(2)において、A21及びA22は、それぞれ炭素数1以上8以下の2価の炭化水素基を表す。Ar21及びAr22は、それぞれ置換あるいは無置換のアリール基又は置換あるいは無置換の縮合多環芳香族基を表す。Ar23は、置換あるいは無置換の2価のアリール基又は置換あるいは無置換の2価の縮合多環芳香族基を表す。R21及びR22は、それぞれ水素原子又はメチル基を表す。)
【請求項4】
前記Ar21及びAr22が、置換あるいは無置換のフルオレニル基であることを特徴とする請求項3に記載の有機発光素子。
【請求項5】
下部電極上に塗布法によりアリールアミンポリマーからなる第一の有機化合物層を形成する工程と、
該第一の有機化合物層上に塗布法によりアリールアミン骨格を有する(メタ)アクリル酸エステル化合物からなる薄膜を形成する工程と、
該薄膜を加熱硬化して第二の有機化合物層を形成する工程と、
第二の有機化合物層上に塗布法により第三の有機化合物層を形成する工程と、を含むことを特徴とする、有機発光素子の製造方法。
【請求項6】
前記アリールアミンポリマーが下記一般式(1)で示される化合物であることを特徴とする、請求項5に記載の有機発光素子の製造方法。
【化3】

【請求項7】
前記(メタ)アクリル酸エステル化合物が一般式(3)で示される化合物であることを特徴とする、請求項5に記載の有機発光素子の製造方法。
【化4】

【請求項8】
請求項1乃至4のいずれか一項に記載の有機発光素子を具備することを特徴とする、表示装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2009−158535(P2009−158535A)
【公開日】平成21年7月16日(2009.7.16)
【国際特許分類】
【出願番号】特願2007−331901(P2007−331901)
【出願日】平成19年12月25日(2007.12.25)
【出願人】(000001007)キヤノン株式会社 (59,756)
【Fターム(参考)】
【公開日】平成21年7月16日(2009.7.16)
【国際特許分類】
【出願日】平成19年12月25日(2007.12.25)
【出願人】(000001007)キヤノン株式会社 (59,756)
【Fターム(参考)】
[ Back to top ]

