検体分析装置
【課題】
できるだけ血球分析装置が元々有している機能を生かして、コストパフォーマンスや効率や処理能力の優れた、体液測定機能を有する血球分析装置を提供する。
【解決手段】
血液測定のための測定モードと体液測定のための測定モードとを選択的に設定する測定モード設定部と、上記測定モード設定部による設定に基づき血球分析装置における各種処理のうち特定の処理について各測定モードに対応した個別処理を実行し各測定結果を出力するよう血球分析装置を動作させる制御部と、を備え、吸引した血液検体および体液試料に対しそれぞれ上記測定モードに対応した処理を行わせる。
できるだけ血球分析装置が元々有している機能を生かして、コストパフォーマンスや効率や処理能力の優れた、体液測定機能を有する血球分析装置を提供する。
【解決手段】
血液測定のための測定モードと体液測定のための測定モードとを選択的に設定する測定モード設定部と、上記測定モード設定部による設定に基づき血球分析装置における各種処理のうち特定の処理について各測定モードに対応した個別処理を実行し各測定結果を出力するよう血球分析装置を動作させる制御部と、を備え、吸引した血液検体および体液試料に対しそれぞれ上記測定モードに対応した処理を行わせる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、検体として、血液だけでなく、脳脊髄液(髄液)や胸水(胸膜液)や腹水等の、血液以外の体液も測定することができる検体分析装置に関する。
【背景技術】
【0002】
体から採取した血液を被検試料として検査装置で測定し、診断や治療モニターの一助とすることは臨床検査の分野で日常的によく行われている。また、血液以外の体液を被検試料として検査装置で測定することも行われている。通常、体液は透明であり、その中に細胞はほとんど含まれないが、疾患や関係器官に腫瘍や損傷等がある場合には、出血(血球)や異常細胞、細菌等の細胞が認められることになる。
【0003】
例えば、体液の1つである脳脊髄液を測定した場合、測定結果からつぎのような推定が可能となる。
・赤血球の増加:くも膜下出血
・好中球の増加:髄膜炎
・好酸球の増加:感染性疾患(寄生虫や真菌)
・単核球の増加:結核性髄膜炎、ウィルス性髄膜炎
・他の細胞:腫瘍の髄膜進展
体液中の細胞を測定することが可能な血球分析装置として、特許文献1に開示されたものがある。この特許文献1には、体液を長期に安定保存するために、オペレータが、体液検体を試薬(アルデヒド、界面活性剤およびシクロデキストリン)と混和して、事前に測定試料を調製し、この測定試料を分析装置に与えて体液の分析を行うことが記載されている。
【0004】
【特許文献1】特開2003−344393号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、上述の特許文献1には、体液測定の際に、分析装置によって測定試料を調製するのではなく、分析装置を操作するオペレータが測定試料を調製する必要があった。また、特許文献1に開示された分析装置においては、体液測定の際に、体液に適した測定動作を行うことは開示されていない。
【0006】
本発明は、かかる事情に鑑みてなされたものであり、オペレータが測定試料調製のような煩雑な作業を行う必要が無く、体液を高精度に分析することが可能な検体分析装置を提供することを目的とする。
【課題を解決するための手段】
【0007】
本発明に係る検体分析装置は、検体を吸引する吸引部と、前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、前記モード設定手段により血液測定モードが設定された場合に、血液検体測定用の動作を実行するように前記測定部を動作制御する第1動作制御手段と、前記モード設定手段により体液測定モードが設定された場合に、前記血液検体測定用の動作とは異なる体液検体測定用の動作を実行するように前記測定部を動作制御する第2動作制御手段とを備えることを特徴とする。
【0008】
このようにすることにより、オペレータは検体分析装置に検体を吸引させるだけで、検体分析装置が自動的に測定試料を調製し、血液検体及び体液検体のそれぞれに適した測定動作を自動的に実行することとなる。したがって、オペレータの煩雑な手間が必要なく、血液検体及び体液検体をそれぞれ高精度に分析することが可能となる。
【0009】
上記発明においては、前記血液検体測定用の動作は、前記測定部が測定試料を所定の第1時間測定する動作であり、前記体液検体測定用の動作は、前記測定部が測定試料を前記第1時間とは異なる第2時間測定する動作であることが好ましい。これにより、血液検体と体液検体を、それぞれに適した時間で測定することができる。
【0010】
上記発明においては、前記第2時間は、前記第1時間より長い時間であることが好ましい。これにより、通常は血液に比べて細胞濃度が低い体液を、血液を測定する場合よりも長時間測定することとなり、より高精度に体液を測定することができる。
【0011】
上記発明においては、前記血液検体測定用の動作は、前記測定部が血液検体と所定の第1の量の試薬とを混和して測定試料を調製する動作であり、前記体液検体測定用の動作は、前記測定部が体液検体と前記第1の量とは異なる第2の量の試薬とを混和して測定試料を調製する動作であることが好ましい。これにより、血液検体と体液検体のそれぞれの場合において、それぞれに適した試薬の量で測定試料を調製することができる。
【0012】
上記発明においては、前記体液検体を測定する前に、検体を含有しないブランク試料を測定するように前記測定部を動作制御するブランク測定動作制御手段をさらに備えることが好ましい。これにより、通常は血液に比べて細胞濃度が低い体液を測定する際に、前回測定された検体が測定部に残留すること(キャリーオーバー)による影響の程度を確認することができる。
【0013】
上記発明においては、前記測定部が体液検体を測定した測定結果を所定の基準値と比較する比較手段と、前記比較手段による比較の結果、前記測定結果が前記基準値よりも大きい場合に、洗浄動作を実行するように前記測定部を動作制御する洗浄制御手段とをさらに備えることが好ましい。これにより、測定した体液検体の濃度が高い場合に、測定部を洗浄し、キャリーオーバーを抑制することが可能となる。
【0014】
本発明の第2の局面に係る検体分析装置は、検体を吸引する吸引部と、前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、前記モード設定手段により血液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、所定の第1分析処理を実行する第1分析手段と、前記モード選択手段により体液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、前記第1分析処理とは異なる第2分析処理を実行する第2分析手段とを備えることを特徴とする。
【0015】
このようにすることにより、オペレータは検体分析装置に検体を吸引させるだけで、検体分析装置が自動的に測定試料を調製及び測定し、血液検体及び体液検体のそれぞれに適した分析処理を自動的に実行することとなる。したがって、オペレータの煩雑な手間が必要なく、血液検体及び体液検体をそれぞれ高精度に分析することが可能となる。
【0016】
上記発明においては、前記第1分析処理は、白血球を少なくとも4種類に分類する処理を含み、前記第2分析処理は、白血球を前記第1分類処理よりも少ない種類に分類する処理を含むことが好ましい。
【発明の効果】
【0017】
本発明に係る検体分析装置によれば、オペレータの煩雑な手間が必要なく、血液検体及び体液検体をそれぞれ高精度に分析することが可能となる等、本発明は優れた効果を奏する。
【発明を実施するための最良の形態】
【0018】
本発明の実施の形態に係る検体分析装置について、図面を参照しながら説明する。
【0019】
図1は、検体分析装置1を示している。この分析装置1は、血液検査を行うための多項目自動血球分析装置として構成されており、検体容器(採血管)に収容された血液検体の測定を行い、検体に含まれる血球の特徴を表す特徴情報を取得し、その特徴情報に対して分析処理を行う。また、この検体分析装置1は、体液の分析を行うことも可能である。本実施形態の血球分析装置において、分析対象の体液とは、血液以外の、体腔内に存在する体腔液をいう。具体的には、脳脊髄液(髄液、CSF:脳室とくも膜下腔に満たされている液)、胸水(胸膜液、PE:胸膜腔に溜まった液)、腹水(腹膜腔に溜まった液)、心嚢液(心膜腔に溜まった液)、関節液(滑液:関節、滑液嚢、腱鞘に存在する液)、などをいう。また、腹膜透析(CAPD)の透析液や腹腔内洗浄液なども体液の一種として分析可能である。通常、これらの体液中には、細胞はほとんど認められないが、疾患や関係器官に腫瘍や損傷等がある場合には、血球、異常細胞、細菌等の細胞が含有されることがある。例えば、脳脊髄液の場合、分析結果から次のような臨床的な推定が可能となる。例えば、赤血球が増加している場合には、くも膜下出血、好中球が増加している場合には髄膜炎、好酸球が増加している場合には、感染性疾患(寄生虫や真菌)、単核球が増加している場合には、結核性髄膜炎やウィルス性髄膜炎、他の細胞が増加している場合には腫瘍の髄膜進展を疑うことができる。また、腹水、胸水などにおいては、血球以外に中皮細胞、マクロファージ、腫瘍細胞等の有核細胞が含まれている場合、このような血球以外の有核細胞を分析することにより、癌などの疾患を疑う指標となりえる。
【0020】
分析装置1は、試料である血液及び体液の測定を行う機能を有する測定部2と、測定部2から出力された測定結果を処理して分析結果を得るデータ処理部3とを有して構成されている。データ処理部3は、制御部301と、表示部302と、入力部303とを備えている。なお、図1では、測定部2とデータ処理部3とが別体の装置として構成されているが、両者が一体の装置として構成されていてもよい。
【0021】
図2は、分析装置1の測定部2のブロック図を示している。図2に示すように、測定部2は、血球の検出部4、検出部4の出力(アナログ信号)に対して処理を行うアナログ処理部5、マイクロコンピュータ部6、表示・操作部7、血液及び体液の測定のための装置機構部8を備えている。また、装置機構部8には、次のような流体機構部81が含まれている。
【0022】
図3は、流体機構部81の構成を示すブロック図である。図3に示すように、流体機構部81は、検体吸引ノズル18と、複数の試薬容器と、サンプリングバルブ12と、反応チャンバ13〜17とを備えている。検体吸引ノズル18は、検体容器から検体を吸引し、その検体をサンプリングバルブ12へと送出する。サンプリングバルブ12は、導入された検体を所定量の複数のアリコートに分割する。この分割数は、測定モード(ディスクリートモード)によって異なっており、赤血球数、白血球数、血小板数、及びヘモグロビン濃度を測定するCBCモードでは、検体が3つのアリコートに分割される。また、上記のCBCの測定項目に加え、白血球を5分類するCBC+DIFFモードでは、検体が4つのアリコートに分割される。また、CBC+DIFFモードの測定項目に加え、網状赤血球を測定するCBC+DIFF+RETモードでは、5つのアリコートに分割される。同様に、CBC+DIFFモードの測定項目に加え、有核赤血球を測定するCBC+DIFF+NRBCモードでも、検体が5つのアリコートに分割される。また、CBC+DIFFモード+RETの測定項目に加え、有核赤血球を測定するCBC+DIFF+RET+NRBCモードでは、6つのアリコートに分割される。以上の測定モードは、全て血液を測定する血液測定モードである。最後に、体液を測定する体液測定モードでは、検体が2つのアリコートに分割される。
【0023】
また、このサンプリングバルブ12には、試薬容器から試薬(希釈液)が導入され、分割された検体のアリコートが、試薬と共に反応チャンバ13〜17及び後述するHGB検出部43へと送出されるようになっている。反応チャンバ13には、サンプリングバルブ12で採取された所定量の検体(アリコート)と、所定量の希釈液と、所定量の染色液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、白血球4分類(DIFF)用の測定試料が作製される。
【0024】
この希釈液としてはシスメックス株式会社から提供されている試薬「ストマトライザ−4DL」が好適使用できる。この試薬は界面活性剤を含有し赤血球を溶血させる。染色液としては同じくシスメックス株式会社から提供されている試薬「ストマトライザ−4DS」が好適使用できる。この染色液はエチレングリコール、低級アルコール、ポリメチン系色素を含有し、上記希釈液で溶血後、血球成分が染色され、最終的に50倍希釈試料が作製される。
【0025】
また、体液測定モードが選択された場合には、体液検体によりこの白血球4分類用の測定試料と検体の量が同一、試薬が同一、及び試薬の量が同一の条件で白血球分類用の測定試料が作成される。ただし、後述するように、体液測定モードの白血球分類では、白血球が4種類ではなく2種類に分類される。
【0026】
反応チャンバ14にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈溶血剤と、所定量の染色液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、有核赤血球(NRBC)測定用の測定試料が作製される。
【0027】
反応チャンバ15にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈液と、所定量の染色液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、網状赤血球(RET)測定用の測定試料が作製される。
【0028】
反応チャンバ16にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈溶血剤とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、白血球/好塩基球(WBC/BASO)用の測定試料が作製される。
【0029】
反応チャンバ17にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、赤血球/血小板(RBC/PLT)用の測定試料が作製される。
【0030】
また、サンプリングバルブ12で採取された所定量の検体と、所定量の希釈溶血剤とが後述するHGB検出部43へ供給されるようになっている。
【0031】
次に、検出部4は、白血球を検出するための白血球検出部41を備えている。また、この白血球検出部41は、有核赤血球及び網状赤血球の検出にも用いられる。なお、検出部4は、白血球検出部の他、赤血球数及び血小板数を測定するRBC/PLT検出部42、血液中の血色素量を測定するHGB検出部43も備えている。
【0032】
前記白血球検出部41は、光学式検出部として構成されており、具体的には、フローサイトメトリー法による検出部として構成されている。ここで、サイトメトリーとは、細胞やその他の生物学的な粒子の物理的な性質や化学的な性質を測定することであり、フローサイトメトリーとは細い流れの中に、これらの粒子を通過させて測定を行う方法をいう。図4は、白血球検出部41の光学系を示している。同図において、レーザダイオード401から出射されたビームは、コリメートレンズ402を介してシースフローセル403内を通過する血球に照射される。この白血球検出部41では、光が照射されたシースフローセル内の血球から発せされる前方散乱光の強度、側方散乱光の強度、側方蛍光の強度が血球の特徴パラメータとして検出される。
【0033】
ここで、光散乱は、血球のような粒子が光の進行方向に障害物として存在し、光がその進行方向を変えることによって生じる現象である。この散乱光を検出することによって、粒子の大きさや成分に関する粒子の特徴情報を得ることができる。なお、前方散乱光とは、照射された光の進行方向と略同じ方向に粒子から発せられる散乱光のことである。前方散乱光からは、粒子(血球)の大きさに関する特徴情報を得ることができる。また、側方散乱光とは、照射された光の進行方向と略垂直方向に粒子から発せられる散乱光のことである。側方散乱光からは、粒子内部に関する特徴情報を得ることができる。血球粒子にレーザ光が照射された場合、側方散乱光強度は細胞内部の複雑さ(核の形状、大きさ、密度や顆粒の量)に依存する。したがって、側方散乱光強度のこの特性を利用することで、血球を分類(弁別)した上で、血球の数を測定することができる。なお、本実施形態においては、散乱光として前方散乱光と側方散乱光とを用いる構成について述べたが、これに限定されるものではなく、分析に必要な粒子の特徴が表れる散乱光信号を得られるのであれば、光源からシースフローセルを透過する光の光軸に対してどのような角度の散乱光を用いてもよい。
【0034】
また、染色された血球のような蛍光物質に光を照射すると、照射した光の波長より長い波長の光を発する。蛍光の強度はよく染色されていれば強くなり、この蛍光強度を測定することによって血球の染色度合いに関する特徴情報を得ることができる。したがって、(側方)蛍光強度の差によって、白血球の分類その他の測定を行うことができる。
【0035】
図4に示すように、シースフローセル403を通過する血球(白血球や有核赤血球)から発せられる前方散乱光は、集光レンズ404とピンホール部405を介してフォトダイオード(前方散乱光受光部)406によって受光される。側方散乱光は、集光レンズ407、ダイクロイックミラー408、光学フィルタ409、及びピンホール部410を介してフォトマルチプライヤ(側方散乱光受光部)411によって受光される。また、側方蛍光は、集光レンズ407及びダイクロイックミラー408を介してフォトマルチプライヤ(側方蛍光受光部)412によって受光される。各受光部406,411,412から出力された受光信号は、それぞれ、アンプ51,52,53等からなるアナログ処理部5によって増幅・波形処理等のアナログ処理が施され、マイクロコンピュータ部6に与えられる。
【0036】
次に、RBC/PLT検出部42の構成について説明する。図5はRBC/PLT検出部42の概略構成を示す模式図である。RBC/PLT検出部42は、赤血球数及び血小板数を、シースフローDC検出法により測定することが可能である。RBC/PLT検出部42は、図5に示すようなシースフローセル42aを有している。このシースフローセル42aには、上方へ向けて開口した試料ノズル42bが設けられており、反応チャンバ17からこの試料ノズル42bに試料が供給されるようになっている。また、シースフローセル42aは、上方へ向かうにしたがって細くなっているテーパ状のチャンバ42cを有しており、このチャンバ42cの内部中央に前述した試料ノズル42bが配されている。また、チャンバ42cの上端には、アパーチャ42dが設けられており、このアパーチャ42dは、試料ノズル42bと中心位置が合わせられている。試料供給部から供給された測定試料は、試料ノズル42bの先端から上方へ向けて送出され、それと同時にチャンバ42cにはフロントシース液が供給され、フロントシース液がアパーチャ42dへ向けて上方へと流れる。ここで、フロントシース液に取り囲まれるように測定試料が流れ、テーパ状のチャンバ42cによって測定試料の流れが細く絞り込まれて、測定試料中の血球が一つずつアパーチャ42dを通過することとなる。アパーチャ42dには電極が設けられており、この電極間に直流電流が供給されるようになっている。そして、測定試料がアパーチャ42dを通流するときのアパーチャ42dにおける直流抵抗の変化を検出し、この電気信号を制御部25へ出力するようになっている。前記直流抵抗は、アパーチャ42dを血球が通過するときに増大するため、この電気信号はアパーチャ42dの血球の通過情報を反映しており、この電気信号を信号処理することによって、赤血球及び血小板を計数するようになっている。
【0037】
また、アパーチャ42dの上方には、上下に延びた回収管42eが設けられている。また、この回収管42eは、アパーチャ42dを介してチャンバ42cと連なるチャンバ42fの内部に配されている。回収管42eの下端部は、チャンバ42fの内壁から離隔している。チャンバ42fは、バックシース液が供給されるようになっており、このバックシース液は、チャンバ42fの回収管42eの外側領域を下方へ向けて通流する。回収管42eの外側を流れるバックシース液は、チャンバ42fの下端部に到達した後、回収管42eの下端部とチャンバ42fの内壁との間を通り、回収管42eの内部へと流入する。このため、アパーチャ42dを通過した血球の舞い戻りが防止され、これにより血球の誤検出が防止される。
【0038】
次に、HGB検出部43の構成について説明する。HGB検出部43は、血色素量(HGB)を、SLSヘモグロビン法によって測定することが可能である。図6は、HGB検出部43の構成を示す斜視図である。HGB検出部43は、希釈試料を収容するセル43aと、セル43aへ向けて発光する発光ダイオード43bと、セル43aを透過した透過光を受光する受光素子43cとを有している。サンプリングバルブ12により定量された血液が希釈液及び所定の溶血剤によって所定希釈率で希釈され、希釈試料が作成される。この溶血剤は、血液中のヘモグロビンをSLS−ヘモグロビンへと転化する性質を有している。かかる希釈試料は、セル43aへと供給され、セル43aに収容される。この状態で、発光ダイオード43bを発光させ、セル43aを挟んで発光ダイオード43bに対向配置された受光素子43cにて透過光が受光される。発光ダイオード43bは、SLS−ヘモグロビンによる吸光率が高い波長の光を発するようになっており、また、セル43aは透光性の高いプラスチック材料で構成されているので、受光素子43cでは、発光ダイオード43bの発光が略希釈試料によってのみ吸光された透過光が受光されることとなる。受光素子43cは、受光量(吸光度)に応じた電気信号をマイクロコンピュータ部6へと出力するようになっており、マイクロコンピュータ部6では、この吸光度と予め測定された希釈液のみの吸光度とを比較し、ヘモグロビン値を算出するようになっている。
【0039】
マイクロコンピュータ部6は、アナログ処理部5から与えられたアナログ信号をデジタル信号に変換するA/D変換部61を備えている。A/D変換部61の出力は、マイクロコンピュータ部6の演算部62に与えられ、演算部62において受光信号に対する所定の処理を行う演算が行われる。演算部62は、検出部4の出力に基づいて、分布データ(2次元のスキャッタグラム(未分類のもの)及び1次元のヒストグラム)を作成する。
【0040】
また、マイクロコンピュータ部6は、制御用プロセッサ及び制御用プロセッサの動作のためのメモリからなる制御部63と、分析用プロセッサ及び分析用プロセッサの動作のためのメモリからなるデータ分析部64とを備えている。制御部63は、採血管を自動供給するサンプラ(図示省略)、試料の調製・測定のための流体系などからなる装置機構部8の制御及びその他の制御を行うものである。データ分析部64は、各分布データに対してクラスタリングなどの分析処理を実行する。分析結果はインターフェース65を介して外部のデータ処理部3に送られ、データの画面表示や記憶等の処理がなされる。
【0041】
さらに、マイクロコンピュータ部6は、表示・操作部7との間に介在するインタフェース部66、装置機構部8との間に介在するインタフェース部67を備えている。また、演算部62、制御部63、及びインタフェース部66,67は、バス68を介して接続され、制御部63とデータ分析部64とはバス69を介して接続されている。表示・操作部7には、オペレータが測定開始を指示するためのスタートスイッチと、装置の状態、各種設定値、及び分析結果を表示したり、オペレータからの入力を受け付けるたりするためのタッチパネル式の液晶表示部とが含まれている。
【0042】
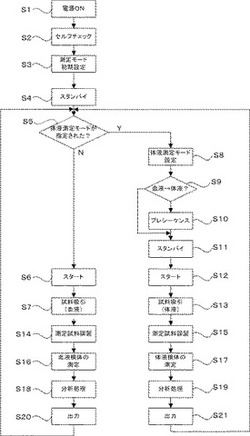
次に、本実施の形態に係る検体分析装置1の動作について説明する。図7は、本実施の形態に係る検体分析装置の動作の流れを示すフローチャートである。ユーザ(オペレータ)が検体分析装置1の電源を入れることにより(ステップS1)、検体分析装置1が起動する。この検体分析装置1は、起動時において、まずセルフチェックを実行する(ステップS2)。このセルフチェックでは、マイクロコンピュータ部6のテスト、検体分析装置1の各動作機構部の動作チェックに加え、検体を含有しないブランク試料を測定するブランクチェック動作が行われる。つぎに、マイクロコンピュータ部6は、測定モードを初期設定する(ステップS3)。この初期設定値は、CBC+DIFFモードとされる。具体的には、ステップS3の処理では、血液測定を行うためのパラメータ(動作条件)、例えば、使用する反応チャンバ、測定の時間設定等が設定される。このように、本実施の形態に係る検体分析装置では、血液測定モードが初期動作モードとして設定される。これにより、検体分析装置1は、測定開始を受付可能なスタンバイ状態となる。マイクロコンピュータ部6は、液晶表示部にスタンバイ状態を通知する画面を表示する(ステップS4)。
【0043】
このスタンバイ状態において、オペレータは表示・操作部7を操作することにより、測定モードの変更が可能である。図8は測定モードを設定するための入力画面を示す模式図である。この画面には、検体番号120、検体の取り込みモードの種類121、ディスクリートテスト(測定モード)の種類122、検体の種類123の核表示領域を備える。検体の取り込みモードとしては、オペレータが手動で検体容器を検体吸引ノズル18に挿入し、検体吸引を行うマニュアルモード、事前にオペレータが検体を試薬と混和して測定試料を調製し、この測定試料を検体吸引ノズル18によって吸引するキャピラリモード、検体容器を自動搬送する搬送装置により検体を供給するクローズドモードの3つのモードが設けられている。また、検体の種類としては、通常の血液検体であるNormal、HPC(造血前駆細胞)であるHPC、及び体液であるBody Fluidが設けられている。オペレータは、検体の取り込みモード、測定モード、及び検体の種類をそれぞれ指定することが可能である。そして、オペレータは、血液測定モードを指定する場合には、検体の種類をNormalに指定し、任意の検体の取り込みモード及び測定モードを指定する。また、体液測定モードを指定する場合には、オペレータは、取り込みモードに「マニュアルモード」を、ディスクリートテストに「CBC+DIFF」、「CBC+DIFF+RET」、「CBC+DIFF+NRBC」及び「CBC+DIFF+NRBC+RET」のうちのいずれかを、検体の種類に「Body Fluid」をそれぞれ指定する。ステップS4において、このようにしてオペレータは所望の測定モードを指定する。オペレータは、初期設定の測定モードを変更することなく血液測定を行う場合には(ステップS5でN)、スタートスイッチを押して測定開始を指示する。マイクロコンピュータ部6は、測定開始の指示を受け付け(ステップS6)、検体吸引ノズルから血液検体を吸引する(ステップS7)。
【0044】
血液検体が吸引された後は、上述のようにサンプリングバルブ18に検体が導入され、測定モードのディスクリートテストの種類に応じて測定に必要な試料調整が行われる(ステップS14)。そして、測定試料の測定動作が実行される(ステップS16)。例えば、ディスクリートテストの種類が「7」に設定されている場合には、HGB、WBC/BASO、DIFF、RET、NRBC、RBC/PLT用の各測定用試料が作製される。その後、WBC/BASO、DIFF、RET、NRBC用測定試料が白血球検出部41にて測定され、RBC/PLT用測定試料がRBC/PLT検出部42にて測定され、HGB用測定試料がHGB検出部43にて測定される。このとき、白血球検出部41は1つしか設けられていないため、NRBC、WBC/BASO、DIFF、RETの各測定用試料はNRBC、WBC/BASO、DIFF、RETの順で白血球検出部41に導入され、順番に測定される。この測定動作において、演算部62は、粒子分布図(スキャッタグラム、ヒストグラム)を作成する。ここでは、DIFF測定によって得られた光学情報からスキャッタグラムを作成する場合とについて説明する。演算部62は、DIFF測定において白血球検出部41から出力された受光信号のうち側方散乱光と側方蛍光の信号を特徴パラメータとして、2次元のスキャッタグラム(粒子分布図)を生成する。このスキャッタグラム(以下、DIFFスキャッタグラムという)は、X軸に側方散乱光強度、Y軸に側方蛍光強度をとって描いたものであり、通常、「赤血球ゴーストの粒子集団」、「リンパ球の粒子集団」、「単球の粒子集団」、「好中球+好塩基球の粒子集団」及び「好酸球の粒子集団」が出現する。これらの粒子集団は、データ分析部64によってDIFFスキャッタグラムを処理することにより認識される。
【0045】
その後、測定によって得られた粒子分布図に基づいて分析処理が行われる(ステップS18)。この分析処理においては、マイクロコンピュータ部6のデータ分析部64は、DIFF測定用試料を白血球検出部41によって測定したときに演算部62によって作成されたDIFFスキャッタグラムに対して、図12に示すような4つの白血球のクラスター(リンパ球のクラスター、単球のクラスター、好中球+好塩基球のクラスター、及び好酸球のクラスター)と、赤血球ゴーストのクラスターとを分類する。本実施形態の分析処理においては、スキャッタグラム上にプロットされた各粒子と各クラスターの重心位置との距離から、各粒子の各クラスターへの帰属度が得られる。そして、これらの帰属度に応じて、各粒子が各クラスターに割り当てられる。この粒子分類方法は、特開平5−149863号公報に詳細に記載されている。また、WBC/BASO測定によって得られたスキャッタグラム上で、好塩基球のクラスターと、好塩基球以外の白血球のクラスターと、赤血球ゴーストのクラスターとが分類される。また、DIFFスキャッタグラムの分析処理によって白血球を4つに分類・計数した結果(図12参照)と、WBC/BASOスキャッタグラムの分析処理によって白血球を2つに分類・計数した結果とに基づいて、血液試料に含まれる白血球を5分類する。具体的には、データ分析部64は、DIFFスキャッタグラムの分析処理によって得られた「好中球+好塩基球の血球数」から、WBC/BASOスキャッタグラムの分析処理によって得られた「好塩基球の血球数」を減算し、好中球の血球数と好塩基球の血球数をそれぞれ取得する。これにより、白血球が5分類(リンパ球、単球、好中球、好塩基球、好酸球)され、各分類項目の血球数が取得される。また、この他にも、RBC/PLTの測定では、検出部42の特徴情報に基づいて作成された1次元のヒストグラムの曲線の谷を検出し、赤血球と血小板とが分類される。このようにして得られた分析結果は、データ処理部3の表示部302に出力される(ステップS21)。
【0046】
一方、マイクロコンピュータ部6は、ステップS5において、上述のようにして測定モードを体液測定モードに指定する入力を受け付けた場合には、体液測定を行うためのパラメータ(動作条件)、例えば、使用する反応チャンバ、測定の時間設定等を設定する(ステップS8)。本実施の形態においては、測定の時間は、後述するように血液測定の場合の3倍の時間とされる。
【0047】
測定モードが他の測定モード(ここでは血液測定モード)から体液測定モードに切り替えられた場合には(ステップS9)、測定部2はプレシーケンスを開始する(ステップS10)。このプレシーケンスは、体液測定の準備のための処理である。体液測定モードでは血球成分が低濃度の検体を測定することになるため、血液測定モード(図8では「1:Normal」として表示されている)から体液測定モードに設定を切り替えたときにプレシーケンスを行い、体液測定結果にバックグラウンドの影響が及ばないことを確認する。
【0048】
プレシーケンスには、ブランクチェック動作が含まれている。このプレシーケンスでのブランクチェックの判定基準は、血球測定モードにおいて行われるブランクチェック(例えば電源立ち上げ後や自動洗浄後に行われる)の判定基準よりも厳しく、数分の1以下の値に設定されている。なお、体液測定モードから血液測定モードに設定を変更した場合には、通常血液測定結果にバックグラウンドの影響(キャリーオーバーの影響)は及ばないため、このプレシーケンスは実施されない。また、体液測定モードにおいて繰り返し体液検体を測定する場合も、通常バックグラウンドの影響は及ばないため、プレシーケンスは実施されない。ただし、体液検体にも極めて粒子数の多いものがあるため、体液検体の分析結果が所定値以上である場合には、次検体の分析結果に影響する虞があることをオペレータに通知するために、「測定結果が高いため、次検体の測定に影響を与える恐れがあります。ブランクチェック測定を行います。「確認」を押してください」のようなメッセージを画面上に出力し、オペレータが「確認」ボタンを押すことで、ブランクチェックを行うように構成することが好ましい。また、この場合には、画面に「中止」ボタンを設け、オペレータが「中止」ボタンを押すとブランクチェックを実施せず、スタンバイ画面に遷移する構成とすることもできる。さらには、ブランクチェックを行わなかった場合に、測定結果に対して信頼性が低いことを示すフラグを付与することが好ましい。このように必要な場合に限定して追加的にブランクチェックを実施することにより、時間や試薬類の消費を抑制することができる。
【0049】
図9は、血液測定モードから体液測定モードに測定モードが変更された場合に実施されるプレシーケンスの処理手順を示すフローチャートである。検体分析装置1は、測定部2でブランク試料の測定を行うことによりブランクチェックを実施し(ステップS31)、マイクロコンピュータ部6が測定結果を所定の許容値と比較して、測定結果が許容値以下か否かを判定する(ステップS32)。測定結果が許容値以下であった場合には、マイクロコンピュータ部6はプレシーケンスを終了し、処理をリターンする。測定値が許容値以下でない場合には、マイクロコンピュータ部6は、定められた回数(例えば3回)ブランクチェックを実行したか否かを判定し(ステップS33)、ブランクチェックの実施回数が所定回数に到達していない場合には、処理をステップS31へ戻し、前記所定回数内で再度ブランクチェックを実施する。所定回数内でブランクチェックの測定結果が許容値以下にならなかった場合には、表示・操作部7にブランクチェックの測定結果ならびに「確認」ボタン、「ブランクチェック」ボタン、「自動洗浄」ボタンを含む画面を表示する(ステップS34)。オペレータにより「確認」ボタンが押された場合には(ステップS35)、マイクロコンピュータ部6はプレシーケンスを終了し、処理をリターンする。「ブランクチェック」ボタンが押された場合には(ステップS36)、処理をステップS31へ戻して再びブランクチェックを実施し、「自動洗浄」ボタンが押された場合には(ステップS37)、専用の洗浄液による自動洗浄を実施した後(ステップS38)、処理をステップS31へ戻して再びプランクチェックを実施する。
【0050】
上述のようなプレシーケンスが終了すると、検体分析装置1は、スタンバイ状態となる(ステップS11)。オペレータは、体液測定を開始する場合には、血液検体のマニュアル測定のときと同様に測定部2の検体吸引ノズル18を検体容器中の体液検体に浸し、スタートスイッチを押す。マイクロコンピュータ部6は、このように測定開始の指示を受け付けると(ステップS12)、体液検体の吸引を開始する(ステップS13)。
【0051】
体液検体が吸引された後は、血液検体の場合と同様に体液検体がサンプリングバルブ91に導入される。そして、反応チャンバ13によってRBC/PLT測定用試料が作製される(ステップS15)。その後、DIFF用測定試料が白血球検出部41にて測定され、RBC/PLT用測定試料がRBC/PLT検出部42にて測定される(ステップS17)。体液測定モードの場合は、白血球検出部41で測定されるのはDIFF用測定試料のみであるので、血液測定モードでの測定時間より長く測定を行っても、血液測定のときより短時間に測定を完了することが可能である。このように、血液測定の測定時間よりも体液測定の測定時間を長くすることにより、粒子濃度の低い体液検体の分析精度を向上させることが可能である。測定時間を長くすれば計数される粒子数が増えるため、測定精度が向上するが、過度に長時間測定すると検体処理能力が低下し、また測定試料を白血球検出部41へ送出するシリンジポンプの能力に限界があることから、2〜6倍が適当である。本実施の形態においては、体液測定モード時の測定時間を血液測定モード時の3倍としている。
【0052】
一方、RBC/PLT用測定試料はいずれの測定モードにおいても同様に電気抵抗式検出部41に導入され、一定流速条件下にて測定が行われる。その後、測定によって得られた特徴情報に基づいて分析処理が行われ(ステップS19)、分析結果がデータ処理部3の表示部302に出力される(ステップS21)。血液測定モードでの分析処理においては、DIFFスキャッタグラムなどを分析して、5種類の白血球サブクラス(好中球:NEUT、リンパ球:LYMPH、単球:MONO、好酸球:EO、好塩基球:BASO)の情報(数や比率)を算出するが、体液測定モードでの分析処理においては、血球数が少ないことやダメージを受けている場合もあるので、一部統合した形で、2種類のサブクラス(単核球:MN、多核球:PMN)に分類している。なお、リンパ球、単球は単核球に属し、好中球、好酸球、好塩基球は多核球に属する。この分類アルゴリズムは、血液測定モードでの分析処理で説明したアルゴリズムと同様であるので、説明を省略する。
【0053】
ところで、体液試料中には、血球以外の異粒子(マクロファージや中皮細胞、腫瘍細胞等)が存在することがある。脳脊髄液にはこれら異粒子が存在することはまれであるが、その他の体液である、胸水や腹水には比較的よく現れる。よって、体液の種類にかかわらず体液中の血球を精度よく分類計数するためには、これら異粒子の影響を排除する必要がある。そこで、この発明では異粒子が本血球分析装置のDIFFスキャッタグラムの上部に出現するという新規な知見に基づき、目的とする体液試料中の白血球をより精度よく測定できるようにしている。なお、前記の従来技術にはこの点は考慮されていない。
【0054】
図10は、本実施形態の血球分析装置1の体液測定モードで、体液と白血球測定用試薬から調製されたDIFF用測定試料を測定、分析することにより得られるスキャッタグラムの模式図である。スキャッタグラムの縦軸は側方蛍光強度(上方ほど蛍光強度が大きい)を表し、横軸は側方散乱光強度(右方ほど散乱光強度が大きい)を表す。スキャッタグラムの蛍光強度が小さい領域LFには溶血により生じた赤血球ゴーストGcが分布し、蛍光強度が大きい領域HFには中皮細胞等の異粒子が分布し、中間領域MFには単核白血球Mc、多核白血球Pcが分布する。そこで、スキャッタグラムの解析において、領域LFおよびHFを除いた領域MFに分布している粒子成分を白血球として解析を行い、上記2つのグループに分類、計数する。なお、単核白血球Mcにはリンパ球および単球が含まれ、多核白血球Pcには好中球、好酸球および好塩基球が含まれる。
【0055】
このように体液中の白血球を分析する場合には、体液に含有される血球数が少ないことやダメージを受けている場合もあるので、臨床的に有意な情報として、白血球を単核白血球と多核白血球に分類し計数している。
【0056】
また、体液中には、血球以外の異粒子(マクロファージ、中皮細胞、腫瘍細胞等の有核細胞)が存在することがある。脳脊髄液にはこれら異粒子が存在することはまれであるが、その他の体液である、胸水や腹水には比較的よく現れる。図10のスキャッタグラムにおいては、このような白血球以外の有核細胞は、領域HFに分布する。このように本実施形態においては、白血球以外の有核細胞を白血球と分けることができるので、このような白血球以外の有核細胞を含む体液であっても、正確な白血球数を求めることが可能になる。また、領域HFに出現する細胞を計数することにより、異常な細胞の出現の度合いを提供することが可能になる。なお、本実施形態においては、各領域を分画する閾値により、各細胞を領域LF、MFおよびHFに分画しているが、この閾値をマニュアルで変更できるようにしてもよい。
【0057】
図11は上記のスキャッタグラムの解析法の妥当性を示すために本実施形態の血球分析装置1による分析結果と参照法による計数結果を比較した図である。被検試料は胸水であり、図中の「本法」は本実施形態の血球分析装置1により算出された白血球の数(WBC)とその他の異粒子の数(Others)を表し、「Ref」は参照法(フックス・ローゼンタール計算盤法およびサイトスピン法)による算出結果を表す。例1、2,3とも異粒子が多く出現している胸水を分析した結果であるが、本実施形態の血球分析装置1による分析結果と参照法との間に相関関係があることがわかる。
【0058】
図13は、血液から調製された上記DIFF用測定試料の分析結果として、データ処理部3の表示部302に表示される画面100を示す。画面100の上部には検体番号101を表示する検体番号表示領域が設けられ、その近傍には患者属性を表示する属性表示領域が設けられている。属性表示領域には、具体的には検体番号、患者ID、患者名、性年月日、性別、病棟、担当医、測定年月日、測定時刻、コメントなどが表示される。属性表示領域の下部には測定結果を表示する測定結果表示領域が設けられている。測定結果表示領域は複数のページからなり、これらページは複数のタブ102により選択されることにより画面表示される。タブはメイン画面、グラフ画面、その他、測定項目にあわせたものが複数用意されている。図12はグラフ画面のタブが選択された場合の表示画面である。測定値表示領域の左半分には、測定結果である測定値を表示する測定値表示領域103とフラグを表示するフラグ表示領域104とが設けられ、右半分には測定結果である分布図105を表示する分布図表示領域が設けられている。測定値表示領域にはWBC、RBC、・・・、NEUT#、・・・、BASO#、NEUT%、・・・、BASO%などの項目とデータと単位が表示され、フラグ表示領域104にはWBC、PLT、RBCあるいはRETに関する、臨床検査上有益な情報となりうる検体異常や疾患の疑いを示すフラッギング結果が表示される。
【0059】
分布図表示領域105には6つの分布図が表示されている。上段左側のスキャッタグラムは、DIFF用のスキャッタグラムである。上段右側はWBC/BASO用、中段左側は幼若球(IMI)用、中段右側はRET用の、各スキャッタグラムである。下段左側はRBC用ヒストグラム、下段右側はPLT用ヒストグラムである。
【0060】
図14は体液から調製された上記DIFF用測定試料の測定結果として、データ処理部3の表示部302に表示される画面110を示す。画面110の上部には検体番号を表示する検体番号表示領域111が設けられ、その近傍には患者属性表示領域が設けられている。検体番号表示領域111の左端には、体液測定モードで測定を行ったことを示す「F」が表示されている。このことにより、この分析結果が体液測定の結果であることを明確に認識することができる。測定結果表示領域はタブ112で選択可能な複数のページからなっている。この例では「体液測定(Body Fluid)」のタブが選択されている。
【0061】
測定値表示領域113には、血液測定モードでの測定結果とは異なる、体液用の測定項目名である、WBC−BF(WBC数)、RBC―BF(RBC数)、MN#(単核球数(リンパ球+単球))、PMN#(多核球数(好中球+好塩基球+好酸球))、MN%(白血球中の単核球比率)、PMN%(白血球中の多核球比率)と測定値と単位が各対応付けられて表示されている。体液測定においても、血液測定と同様にフラグ表示領域114が設けられている。分布図表示領域には2つの分布図115が表示されており、上段のスキャッタグラムはDIFF用のスキャッタグラムである。下段はRBC用ヒストグラムである。
【0062】
図15は図14の画面110において、タブ112で「リサーチBF(Research(BF))」のタブが選択された例である。この画面はリサーチパラメータ表示領域116が表示されること以外は画面110と同様の項目が表示される。リサーチパラメータ表示領域116には、図10において、領域HFに存在する粒子数である「HF−BF#」、領域HFと領域MFを含む領域に存在する粒子数に対する領域HFに存在する粒子数の比率である「HF−BF%」、領域HFと領域MFを含む領域に存在する粒子の数である「TC−BF#」が表示される。なお、「HF−BF%」はHF−BFのTC−BFに対する割合である。
【0063】
図16はデータ処理部3の表示部302に表示される、記憶検体の一覧表示画面120である。130は患者属性表示領域である。その上方にはタブ選択による測定結果を表示する測定結果表示領域が設けられている。測定結果表示領域の左端の列131は測定結果のバリデート作業の未あるいは済を示すためのものである。Vで表記されているのがバリデート済みを表す。その右の列132は測定モードを示すためのものである。「F」で示されているのが体液測定モードでの測定結果である。体液測定モードでブランクチェックが必要な高値検体であったが、ブランクチェックを行わなかった場合には、そのことを示すために反転表記でFと表記することができる。
【0064】
以上、本件発明の血球分析装置の構成、機能について、血球分析装置に予め備えられたものとして説明したが、同機能をコンピュータプログラムにて実現し、従来の血球分析装置にそのコンピュータプログラムをインストールすることにより従来の血球分析装置に本発明に係る機能を発揮されるように構成することもできる。
【0065】
なお、本実施の形態においては、血液測定モードにおける白血球分類測定と、体液測定モードにおける白血球分類測定とでそれぞれ測定試料を作成するときの検体量、試薬の種類、及び試薬の量を同一とする構成について述べたが、これに限定されるものではなく、体液測定モードにおける白血球分類測定用の測定試料を作成するための検体量及び試薬の量を、血液測定モードにおける白血球分類測定用の測定試料を作成するための検体量及び試薬の量よりそれぞれ多くすることも可能である。体液測定モードにおける白血球分類測定では、血液測定モードの場合よりも測定時間が長く、測定に必要な測定試料の量が多いため、このようにすることにより、血液測定モードの白血球分類測定及び体液測定モードの白血球分類測定のそれぞれにおいて、適切な量の測定試料を作成することが可能となる。
【0066】
また、本実施の形態においては、散乱光と蛍光とを用いて体液測定モードにおける白血球分類を行う構成について述べたが、これに限定されるものではなく、例えば散乱光と吸収光とを用いて体液測定モードにおける白血球分類を行う構成としてもよい。吸収光の測定は、白血球を染色する染色試薬を他の試薬と共に検体に混合して測定試料を調製し、その測定試料をフローセルに供給してフローセル中に試料流を形成させ、その試料流に光を照射し、試料流から出射される光をフォトダイオード等の受光素子によって受光することで可能となる。フローセル中を白血球が通過したときに白血球により光が吸収され、その吸収の程度が受光素子の受光量として捉えられる。このような吸収光の測定については、米国特許第5122453号及び米国特許第5138181に開示されている。また、散乱光の代わりに電気抵抗を測定し、その電気抵抗値と吸収光とによって白血球の分類測定を行うこともできる。
【図面の簡単な説明】
【0067】
【図1】本発明の血球分析装置の外観図である。
【図2】分析装置の測定部のブロック図である。
【図3】流体機構部のブロック図である。
【図4】白血球検出部の光学系を示す図である。
【図5】RBC/PLT検出部を示す図である。
【図6】HGB検出部を示す図である。
【図7】検体の測定処理を示すフローチャートである。
【図8】測定モードを設定するための表示画面を示す図である。
【図9】プレシーケンスの処理を表すフロー図である。
【図10】体液から調製したDIFF用測定試料を測定したスキャッタグラムの模式図である。
【図11】実施形態の血球分析装置による測定結果と参照法による測定結果を対比した図である。
【図12】血液から調製したDIFF用測定試料を測定したスキャッタグラムの模式図である。
【図13】血液測定モードでの測定結果を表す表示画面である。
【図14】体液測定モードでの測定結果を表す表示画面である。
【図15】体液測定モードでの測定結果を表す表示画面である。
【図16】体液測定モードでの測定結果を表す表示画面である。
【符号の説明】
【0068】
1 血球分析装置
2 測定部
3 データ処理部
4 検出部
5 アナログ信号処理部
6 マイクロコンピュータ部
7 表示操作部
8 流体処理部
【技術分野】
【0001】
本発明は、検体として、血液だけでなく、脳脊髄液(髄液)や胸水(胸膜液)や腹水等の、血液以外の体液も測定することができる検体分析装置に関する。
【背景技術】
【0002】
体から採取した血液を被検試料として検査装置で測定し、診断や治療モニターの一助とすることは臨床検査の分野で日常的によく行われている。また、血液以外の体液を被検試料として検査装置で測定することも行われている。通常、体液は透明であり、その中に細胞はほとんど含まれないが、疾患や関係器官に腫瘍や損傷等がある場合には、出血(血球)や異常細胞、細菌等の細胞が認められることになる。
【0003】
例えば、体液の1つである脳脊髄液を測定した場合、測定結果からつぎのような推定が可能となる。
・赤血球の増加:くも膜下出血
・好中球の増加:髄膜炎
・好酸球の増加:感染性疾患(寄生虫や真菌)
・単核球の増加:結核性髄膜炎、ウィルス性髄膜炎
・他の細胞:腫瘍の髄膜進展
体液中の細胞を測定することが可能な血球分析装置として、特許文献1に開示されたものがある。この特許文献1には、体液を長期に安定保存するために、オペレータが、体液検体を試薬(アルデヒド、界面活性剤およびシクロデキストリン)と混和して、事前に測定試料を調製し、この測定試料を分析装置に与えて体液の分析を行うことが記載されている。
【0004】
【特許文献1】特開2003−344393号公報
【発明の開示】
【発明が解決しようとする課題】
【0005】
しかしながら、上述の特許文献1には、体液測定の際に、分析装置によって測定試料を調製するのではなく、分析装置を操作するオペレータが測定試料を調製する必要があった。また、特許文献1に開示された分析装置においては、体液測定の際に、体液に適した測定動作を行うことは開示されていない。
【0006】
本発明は、かかる事情に鑑みてなされたものであり、オペレータが測定試料調製のような煩雑な作業を行う必要が無く、体液を高精度に分析することが可能な検体分析装置を提供することを目的とする。
【課題を解決するための手段】
【0007】
本発明に係る検体分析装置は、検体を吸引する吸引部と、前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、前記モード設定手段により血液測定モードが設定された場合に、血液検体測定用の動作を実行するように前記測定部を動作制御する第1動作制御手段と、前記モード設定手段により体液測定モードが設定された場合に、前記血液検体測定用の動作とは異なる体液検体測定用の動作を実行するように前記測定部を動作制御する第2動作制御手段とを備えることを特徴とする。
【0008】
このようにすることにより、オペレータは検体分析装置に検体を吸引させるだけで、検体分析装置が自動的に測定試料を調製し、血液検体及び体液検体のそれぞれに適した測定動作を自動的に実行することとなる。したがって、オペレータの煩雑な手間が必要なく、血液検体及び体液検体をそれぞれ高精度に分析することが可能となる。
【0009】
上記発明においては、前記血液検体測定用の動作は、前記測定部が測定試料を所定の第1時間測定する動作であり、前記体液検体測定用の動作は、前記測定部が測定試料を前記第1時間とは異なる第2時間測定する動作であることが好ましい。これにより、血液検体と体液検体を、それぞれに適した時間で測定することができる。
【0010】
上記発明においては、前記第2時間は、前記第1時間より長い時間であることが好ましい。これにより、通常は血液に比べて細胞濃度が低い体液を、血液を測定する場合よりも長時間測定することとなり、より高精度に体液を測定することができる。
【0011】
上記発明においては、前記血液検体測定用の動作は、前記測定部が血液検体と所定の第1の量の試薬とを混和して測定試料を調製する動作であり、前記体液検体測定用の動作は、前記測定部が体液検体と前記第1の量とは異なる第2の量の試薬とを混和して測定試料を調製する動作であることが好ましい。これにより、血液検体と体液検体のそれぞれの場合において、それぞれに適した試薬の量で測定試料を調製することができる。
【0012】
上記発明においては、前記体液検体を測定する前に、検体を含有しないブランク試料を測定するように前記測定部を動作制御するブランク測定動作制御手段をさらに備えることが好ましい。これにより、通常は血液に比べて細胞濃度が低い体液を測定する際に、前回測定された検体が測定部に残留すること(キャリーオーバー)による影響の程度を確認することができる。
【0013】
上記発明においては、前記測定部が体液検体を測定した測定結果を所定の基準値と比較する比較手段と、前記比較手段による比較の結果、前記測定結果が前記基準値よりも大きい場合に、洗浄動作を実行するように前記測定部を動作制御する洗浄制御手段とをさらに備えることが好ましい。これにより、測定した体液検体の濃度が高い場合に、測定部を洗浄し、キャリーオーバーを抑制することが可能となる。
【0014】
本発明の第2の局面に係る検体分析装置は、検体を吸引する吸引部と、前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、前記モード設定手段により血液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、所定の第1分析処理を実行する第1分析手段と、前記モード選択手段により体液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、前記第1分析処理とは異なる第2分析処理を実行する第2分析手段とを備えることを特徴とする。
【0015】
このようにすることにより、オペレータは検体分析装置に検体を吸引させるだけで、検体分析装置が自動的に測定試料を調製及び測定し、血液検体及び体液検体のそれぞれに適した分析処理を自動的に実行することとなる。したがって、オペレータの煩雑な手間が必要なく、血液検体及び体液検体をそれぞれ高精度に分析することが可能となる。
【0016】
上記発明においては、前記第1分析処理は、白血球を少なくとも4種類に分類する処理を含み、前記第2分析処理は、白血球を前記第1分類処理よりも少ない種類に分類する処理を含むことが好ましい。
【発明の効果】
【0017】
本発明に係る検体分析装置によれば、オペレータの煩雑な手間が必要なく、血液検体及び体液検体をそれぞれ高精度に分析することが可能となる等、本発明は優れた効果を奏する。
【発明を実施するための最良の形態】
【0018】
本発明の実施の形態に係る検体分析装置について、図面を参照しながら説明する。
【0019】
図1は、検体分析装置1を示している。この分析装置1は、血液検査を行うための多項目自動血球分析装置として構成されており、検体容器(採血管)に収容された血液検体の測定を行い、検体に含まれる血球の特徴を表す特徴情報を取得し、その特徴情報に対して分析処理を行う。また、この検体分析装置1は、体液の分析を行うことも可能である。本実施形態の血球分析装置において、分析対象の体液とは、血液以外の、体腔内に存在する体腔液をいう。具体的には、脳脊髄液(髄液、CSF:脳室とくも膜下腔に満たされている液)、胸水(胸膜液、PE:胸膜腔に溜まった液)、腹水(腹膜腔に溜まった液)、心嚢液(心膜腔に溜まった液)、関節液(滑液:関節、滑液嚢、腱鞘に存在する液)、などをいう。また、腹膜透析(CAPD)の透析液や腹腔内洗浄液なども体液の一種として分析可能である。通常、これらの体液中には、細胞はほとんど認められないが、疾患や関係器官に腫瘍や損傷等がある場合には、血球、異常細胞、細菌等の細胞が含有されることがある。例えば、脳脊髄液の場合、分析結果から次のような臨床的な推定が可能となる。例えば、赤血球が増加している場合には、くも膜下出血、好中球が増加している場合には髄膜炎、好酸球が増加している場合には、感染性疾患(寄生虫や真菌)、単核球が増加している場合には、結核性髄膜炎やウィルス性髄膜炎、他の細胞が増加している場合には腫瘍の髄膜進展を疑うことができる。また、腹水、胸水などにおいては、血球以外に中皮細胞、マクロファージ、腫瘍細胞等の有核細胞が含まれている場合、このような血球以外の有核細胞を分析することにより、癌などの疾患を疑う指標となりえる。
【0020】
分析装置1は、試料である血液及び体液の測定を行う機能を有する測定部2と、測定部2から出力された測定結果を処理して分析結果を得るデータ処理部3とを有して構成されている。データ処理部3は、制御部301と、表示部302と、入力部303とを備えている。なお、図1では、測定部2とデータ処理部3とが別体の装置として構成されているが、両者が一体の装置として構成されていてもよい。
【0021】
図2は、分析装置1の測定部2のブロック図を示している。図2に示すように、測定部2は、血球の検出部4、検出部4の出力(アナログ信号)に対して処理を行うアナログ処理部5、マイクロコンピュータ部6、表示・操作部7、血液及び体液の測定のための装置機構部8を備えている。また、装置機構部8には、次のような流体機構部81が含まれている。
【0022】
図3は、流体機構部81の構成を示すブロック図である。図3に示すように、流体機構部81は、検体吸引ノズル18と、複数の試薬容器と、サンプリングバルブ12と、反応チャンバ13〜17とを備えている。検体吸引ノズル18は、検体容器から検体を吸引し、その検体をサンプリングバルブ12へと送出する。サンプリングバルブ12は、導入された検体を所定量の複数のアリコートに分割する。この分割数は、測定モード(ディスクリートモード)によって異なっており、赤血球数、白血球数、血小板数、及びヘモグロビン濃度を測定するCBCモードでは、検体が3つのアリコートに分割される。また、上記のCBCの測定項目に加え、白血球を5分類するCBC+DIFFモードでは、検体が4つのアリコートに分割される。また、CBC+DIFFモードの測定項目に加え、網状赤血球を測定するCBC+DIFF+RETモードでは、5つのアリコートに分割される。同様に、CBC+DIFFモードの測定項目に加え、有核赤血球を測定するCBC+DIFF+NRBCモードでも、検体が5つのアリコートに分割される。また、CBC+DIFFモード+RETの測定項目に加え、有核赤血球を測定するCBC+DIFF+RET+NRBCモードでは、6つのアリコートに分割される。以上の測定モードは、全て血液を測定する血液測定モードである。最後に、体液を測定する体液測定モードでは、検体が2つのアリコートに分割される。
【0023】
また、このサンプリングバルブ12には、試薬容器から試薬(希釈液)が導入され、分割された検体のアリコートが、試薬と共に反応チャンバ13〜17及び後述するHGB検出部43へと送出されるようになっている。反応チャンバ13には、サンプリングバルブ12で採取された所定量の検体(アリコート)と、所定量の希釈液と、所定量の染色液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、白血球4分類(DIFF)用の測定試料が作製される。
【0024】
この希釈液としてはシスメックス株式会社から提供されている試薬「ストマトライザ−4DL」が好適使用できる。この試薬は界面活性剤を含有し赤血球を溶血させる。染色液としては同じくシスメックス株式会社から提供されている試薬「ストマトライザ−4DS」が好適使用できる。この染色液はエチレングリコール、低級アルコール、ポリメチン系色素を含有し、上記希釈液で溶血後、血球成分が染色され、最終的に50倍希釈試料が作製される。
【0025】
また、体液測定モードが選択された場合には、体液検体によりこの白血球4分類用の測定試料と検体の量が同一、試薬が同一、及び試薬の量が同一の条件で白血球分類用の測定試料が作成される。ただし、後述するように、体液測定モードの白血球分類では、白血球が4種類ではなく2種類に分類される。
【0026】
反応チャンバ14にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈溶血剤と、所定量の染色液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、有核赤血球(NRBC)測定用の測定試料が作製される。
【0027】
反応チャンバ15にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈液と、所定量の染色液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、網状赤血球(RET)測定用の測定試料が作製される。
【0028】
反応チャンバ16にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈溶血剤とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、白血球/好塩基球(WBC/BASO)用の測定試料が作製される。
【0029】
反応チャンバ17にはサンプリングバルブ12で採取された所定量の検体と、所定量の希釈液とが図示しない定量ポンプにより供給され、これらの検体と試薬とが混合され、赤血球/血小板(RBC/PLT)用の測定試料が作製される。
【0030】
また、サンプリングバルブ12で採取された所定量の検体と、所定量の希釈溶血剤とが後述するHGB検出部43へ供給されるようになっている。
【0031】
次に、検出部4は、白血球を検出するための白血球検出部41を備えている。また、この白血球検出部41は、有核赤血球及び網状赤血球の検出にも用いられる。なお、検出部4は、白血球検出部の他、赤血球数及び血小板数を測定するRBC/PLT検出部42、血液中の血色素量を測定するHGB検出部43も備えている。
【0032】
前記白血球検出部41は、光学式検出部として構成されており、具体的には、フローサイトメトリー法による検出部として構成されている。ここで、サイトメトリーとは、細胞やその他の生物学的な粒子の物理的な性質や化学的な性質を測定することであり、フローサイトメトリーとは細い流れの中に、これらの粒子を通過させて測定を行う方法をいう。図4は、白血球検出部41の光学系を示している。同図において、レーザダイオード401から出射されたビームは、コリメートレンズ402を介してシースフローセル403内を通過する血球に照射される。この白血球検出部41では、光が照射されたシースフローセル内の血球から発せされる前方散乱光の強度、側方散乱光の強度、側方蛍光の強度が血球の特徴パラメータとして検出される。
【0033】
ここで、光散乱は、血球のような粒子が光の進行方向に障害物として存在し、光がその進行方向を変えることによって生じる現象である。この散乱光を検出することによって、粒子の大きさや成分に関する粒子の特徴情報を得ることができる。なお、前方散乱光とは、照射された光の進行方向と略同じ方向に粒子から発せられる散乱光のことである。前方散乱光からは、粒子(血球)の大きさに関する特徴情報を得ることができる。また、側方散乱光とは、照射された光の進行方向と略垂直方向に粒子から発せられる散乱光のことである。側方散乱光からは、粒子内部に関する特徴情報を得ることができる。血球粒子にレーザ光が照射された場合、側方散乱光強度は細胞内部の複雑さ(核の形状、大きさ、密度や顆粒の量)に依存する。したがって、側方散乱光強度のこの特性を利用することで、血球を分類(弁別)した上で、血球の数を測定することができる。なお、本実施形態においては、散乱光として前方散乱光と側方散乱光とを用いる構成について述べたが、これに限定されるものではなく、分析に必要な粒子の特徴が表れる散乱光信号を得られるのであれば、光源からシースフローセルを透過する光の光軸に対してどのような角度の散乱光を用いてもよい。
【0034】
また、染色された血球のような蛍光物質に光を照射すると、照射した光の波長より長い波長の光を発する。蛍光の強度はよく染色されていれば強くなり、この蛍光強度を測定することによって血球の染色度合いに関する特徴情報を得ることができる。したがって、(側方)蛍光強度の差によって、白血球の分類その他の測定を行うことができる。
【0035】
図4に示すように、シースフローセル403を通過する血球(白血球や有核赤血球)から発せられる前方散乱光は、集光レンズ404とピンホール部405を介してフォトダイオード(前方散乱光受光部)406によって受光される。側方散乱光は、集光レンズ407、ダイクロイックミラー408、光学フィルタ409、及びピンホール部410を介してフォトマルチプライヤ(側方散乱光受光部)411によって受光される。また、側方蛍光は、集光レンズ407及びダイクロイックミラー408を介してフォトマルチプライヤ(側方蛍光受光部)412によって受光される。各受光部406,411,412から出力された受光信号は、それぞれ、アンプ51,52,53等からなるアナログ処理部5によって増幅・波形処理等のアナログ処理が施され、マイクロコンピュータ部6に与えられる。
【0036】
次に、RBC/PLT検出部42の構成について説明する。図5はRBC/PLT検出部42の概略構成を示す模式図である。RBC/PLT検出部42は、赤血球数及び血小板数を、シースフローDC検出法により測定することが可能である。RBC/PLT検出部42は、図5に示すようなシースフローセル42aを有している。このシースフローセル42aには、上方へ向けて開口した試料ノズル42bが設けられており、反応チャンバ17からこの試料ノズル42bに試料が供給されるようになっている。また、シースフローセル42aは、上方へ向かうにしたがって細くなっているテーパ状のチャンバ42cを有しており、このチャンバ42cの内部中央に前述した試料ノズル42bが配されている。また、チャンバ42cの上端には、アパーチャ42dが設けられており、このアパーチャ42dは、試料ノズル42bと中心位置が合わせられている。試料供給部から供給された測定試料は、試料ノズル42bの先端から上方へ向けて送出され、それと同時にチャンバ42cにはフロントシース液が供給され、フロントシース液がアパーチャ42dへ向けて上方へと流れる。ここで、フロントシース液に取り囲まれるように測定試料が流れ、テーパ状のチャンバ42cによって測定試料の流れが細く絞り込まれて、測定試料中の血球が一つずつアパーチャ42dを通過することとなる。アパーチャ42dには電極が設けられており、この電極間に直流電流が供給されるようになっている。そして、測定試料がアパーチャ42dを通流するときのアパーチャ42dにおける直流抵抗の変化を検出し、この電気信号を制御部25へ出力するようになっている。前記直流抵抗は、アパーチャ42dを血球が通過するときに増大するため、この電気信号はアパーチャ42dの血球の通過情報を反映しており、この電気信号を信号処理することによって、赤血球及び血小板を計数するようになっている。
【0037】
また、アパーチャ42dの上方には、上下に延びた回収管42eが設けられている。また、この回収管42eは、アパーチャ42dを介してチャンバ42cと連なるチャンバ42fの内部に配されている。回収管42eの下端部は、チャンバ42fの内壁から離隔している。チャンバ42fは、バックシース液が供給されるようになっており、このバックシース液は、チャンバ42fの回収管42eの外側領域を下方へ向けて通流する。回収管42eの外側を流れるバックシース液は、チャンバ42fの下端部に到達した後、回収管42eの下端部とチャンバ42fの内壁との間を通り、回収管42eの内部へと流入する。このため、アパーチャ42dを通過した血球の舞い戻りが防止され、これにより血球の誤検出が防止される。
【0038】
次に、HGB検出部43の構成について説明する。HGB検出部43は、血色素量(HGB)を、SLSヘモグロビン法によって測定することが可能である。図6は、HGB検出部43の構成を示す斜視図である。HGB検出部43は、希釈試料を収容するセル43aと、セル43aへ向けて発光する発光ダイオード43bと、セル43aを透過した透過光を受光する受光素子43cとを有している。サンプリングバルブ12により定量された血液が希釈液及び所定の溶血剤によって所定希釈率で希釈され、希釈試料が作成される。この溶血剤は、血液中のヘモグロビンをSLS−ヘモグロビンへと転化する性質を有している。かかる希釈試料は、セル43aへと供給され、セル43aに収容される。この状態で、発光ダイオード43bを発光させ、セル43aを挟んで発光ダイオード43bに対向配置された受光素子43cにて透過光が受光される。発光ダイオード43bは、SLS−ヘモグロビンによる吸光率が高い波長の光を発するようになっており、また、セル43aは透光性の高いプラスチック材料で構成されているので、受光素子43cでは、発光ダイオード43bの発光が略希釈試料によってのみ吸光された透過光が受光されることとなる。受光素子43cは、受光量(吸光度)に応じた電気信号をマイクロコンピュータ部6へと出力するようになっており、マイクロコンピュータ部6では、この吸光度と予め測定された希釈液のみの吸光度とを比較し、ヘモグロビン値を算出するようになっている。
【0039】
マイクロコンピュータ部6は、アナログ処理部5から与えられたアナログ信号をデジタル信号に変換するA/D変換部61を備えている。A/D変換部61の出力は、マイクロコンピュータ部6の演算部62に与えられ、演算部62において受光信号に対する所定の処理を行う演算が行われる。演算部62は、検出部4の出力に基づいて、分布データ(2次元のスキャッタグラム(未分類のもの)及び1次元のヒストグラム)を作成する。
【0040】
また、マイクロコンピュータ部6は、制御用プロセッサ及び制御用プロセッサの動作のためのメモリからなる制御部63と、分析用プロセッサ及び分析用プロセッサの動作のためのメモリからなるデータ分析部64とを備えている。制御部63は、採血管を自動供給するサンプラ(図示省略)、試料の調製・測定のための流体系などからなる装置機構部8の制御及びその他の制御を行うものである。データ分析部64は、各分布データに対してクラスタリングなどの分析処理を実行する。分析結果はインターフェース65を介して外部のデータ処理部3に送られ、データの画面表示や記憶等の処理がなされる。
【0041】
さらに、マイクロコンピュータ部6は、表示・操作部7との間に介在するインタフェース部66、装置機構部8との間に介在するインタフェース部67を備えている。また、演算部62、制御部63、及びインタフェース部66,67は、バス68を介して接続され、制御部63とデータ分析部64とはバス69を介して接続されている。表示・操作部7には、オペレータが測定開始を指示するためのスタートスイッチと、装置の状態、各種設定値、及び分析結果を表示したり、オペレータからの入力を受け付けるたりするためのタッチパネル式の液晶表示部とが含まれている。
【0042】
次に、本実施の形態に係る検体分析装置1の動作について説明する。図7は、本実施の形態に係る検体分析装置の動作の流れを示すフローチャートである。ユーザ(オペレータ)が検体分析装置1の電源を入れることにより(ステップS1)、検体分析装置1が起動する。この検体分析装置1は、起動時において、まずセルフチェックを実行する(ステップS2)。このセルフチェックでは、マイクロコンピュータ部6のテスト、検体分析装置1の各動作機構部の動作チェックに加え、検体を含有しないブランク試料を測定するブランクチェック動作が行われる。つぎに、マイクロコンピュータ部6は、測定モードを初期設定する(ステップS3)。この初期設定値は、CBC+DIFFモードとされる。具体的には、ステップS3の処理では、血液測定を行うためのパラメータ(動作条件)、例えば、使用する反応チャンバ、測定の時間設定等が設定される。このように、本実施の形態に係る検体分析装置では、血液測定モードが初期動作モードとして設定される。これにより、検体分析装置1は、測定開始を受付可能なスタンバイ状態となる。マイクロコンピュータ部6は、液晶表示部にスタンバイ状態を通知する画面を表示する(ステップS4)。
【0043】
このスタンバイ状態において、オペレータは表示・操作部7を操作することにより、測定モードの変更が可能である。図8は測定モードを設定するための入力画面を示す模式図である。この画面には、検体番号120、検体の取り込みモードの種類121、ディスクリートテスト(測定モード)の種類122、検体の種類123の核表示領域を備える。検体の取り込みモードとしては、オペレータが手動で検体容器を検体吸引ノズル18に挿入し、検体吸引を行うマニュアルモード、事前にオペレータが検体を試薬と混和して測定試料を調製し、この測定試料を検体吸引ノズル18によって吸引するキャピラリモード、検体容器を自動搬送する搬送装置により検体を供給するクローズドモードの3つのモードが設けられている。また、検体の種類としては、通常の血液検体であるNormal、HPC(造血前駆細胞)であるHPC、及び体液であるBody Fluidが設けられている。オペレータは、検体の取り込みモード、測定モード、及び検体の種類をそれぞれ指定することが可能である。そして、オペレータは、血液測定モードを指定する場合には、検体の種類をNormalに指定し、任意の検体の取り込みモード及び測定モードを指定する。また、体液測定モードを指定する場合には、オペレータは、取り込みモードに「マニュアルモード」を、ディスクリートテストに「CBC+DIFF」、「CBC+DIFF+RET」、「CBC+DIFF+NRBC」及び「CBC+DIFF+NRBC+RET」のうちのいずれかを、検体の種類に「Body Fluid」をそれぞれ指定する。ステップS4において、このようにしてオペレータは所望の測定モードを指定する。オペレータは、初期設定の測定モードを変更することなく血液測定を行う場合には(ステップS5でN)、スタートスイッチを押して測定開始を指示する。マイクロコンピュータ部6は、測定開始の指示を受け付け(ステップS6)、検体吸引ノズルから血液検体を吸引する(ステップS7)。
【0044】
血液検体が吸引された後は、上述のようにサンプリングバルブ18に検体が導入され、測定モードのディスクリートテストの種類に応じて測定に必要な試料調整が行われる(ステップS14)。そして、測定試料の測定動作が実行される(ステップS16)。例えば、ディスクリートテストの種類が「7」に設定されている場合には、HGB、WBC/BASO、DIFF、RET、NRBC、RBC/PLT用の各測定用試料が作製される。その後、WBC/BASO、DIFF、RET、NRBC用測定試料が白血球検出部41にて測定され、RBC/PLT用測定試料がRBC/PLT検出部42にて測定され、HGB用測定試料がHGB検出部43にて測定される。このとき、白血球検出部41は1つしか設けられていないため、NRBC、WBC/BASO、DIFF、RETの各測定用試料はNRBC、WBC/BASO、DIFF、RETの順で白血球検出部41に導入され、順番に測定される。この測定動作において、演算部62は、粒子分布図(スキャッタグラム、ヒストグラム)を作成する。ここでは、DIFF測定によって得られた光学情報からスキャッタグラムを作成する場合とについて説明する。演算部62は、DIFF測定において白血球検出部41から出力された受光信号のうち側方散乱光と側方蛍光の信号を特徴パラメータとして、2次元のスキャッタグラム(粒子分布図)を生成する。このスキャッタグラム(以下、DIFFスキャッタグラムという)は、X軸に側方散乱光強度、Y軸に側方蛍光強度をとって描いたものであり、通常、「赤血球ゴーストの粒子集団」、「リンパ球の粒子集団」、「単球の粒子集団」、「好中球+好塩基球の粒子集団」及び「好酸球の粒子集団」が出現する。これらの粒子集団は、データ分析部64によってDIFFスキャッタグラムを処理することにより認識される。
【0045】
その後、測定によって得られた粒子分布図に基づいて分析処理が行われる(ステップS18)。この分析処理においては、マイクロコンピュータ部6のデータ分析部64は、DIFF測定用試料を白血球検出部41によって測定したときに演算部62によって作成されたDIFFスキャッタグラムに対して、図12に示すような4つの白血球のクラスター(リンパ球のクラスター、単球のクラスター、好中球+好塩基球のクラスター、及び好酸球のクラスター)と、赤血球ゴーストのクラスターとを分類する。本実施形態の分析処理においては、スキャッタグラム上にプロットされた各粒子と各クラスターの重心位置との距離から、各粒子の各クラスターへの帰属度が得られる。そして、これらの帰属度に応じて、各粒子が各クラスターに割り当てられる。この粒子分類方法は、特開平5−149863号公報に詳細に記載されている。また、WBC/BASO測定によって得られたスキャッタグラム上で、好塩基球のクラスターと、好塩基球以外の白血球のクラスターと、赤血球ゴーストのクラスターとが分類される。また、DIFFスキャッタグラムの分析処理によって白血球を4つに分類・計数した結果(図12参照)と、WBC/BASOスキャッタグラムの分析処理によって白血球を2つに分類・計数した結果とに基づいて、血液試料に含まれる白血球を5分類する。具体的には、データ分析部64は、DIFFスキャッタグラムの分析処理によって得られた「好中球+好塩基球の血球数」から、WBC/BASOスキャッタグラムの分析処理によって得られた「好塩基球の血球数」を減算し、好中球の血球数と好塩基球の血球数をそれぞれ取得する。これにより、白血球が5分類(リンパ球、単球、好中球、好塩基球、好酸球)され、各分類項目の血球数が取得される。また、この他にも、RBC/PLTの測定では、検出部42の特徴情報に基づいて作成された1次元のヒストグラムの曲線の谷を検出し、赤血球と血小板とが分類される。このようにして得られた分析結果は、データ処理部3の表示部302に出力される(ステップS21)。
【0046】
一方、マイクロコンピュータ部6は、ステップS5において、上述のようにして測定モードを体液測定モードに指定する入力を受け付けた場合には、体液測定を行うためのパラメータ(動作条件)、例えば、使用する反応チャンバ、測定の時間設定等を設定する(ステップS8)。本実施の形態においては、測定の時間は、後述するように血液測定の場合の3倍の時間とされる。
【0047】
測定モードが他の測定モード(ここでは血液測定モード)から体液測定モードに切り替えられた場合には(ステップS9)、測定部2はプレシーケンスを開始する(ステップS10)。このプレシーケンスは、体液測定の準備のための処理である。体液測定モードでは血球成分が低濃度の検体を測定することになるため、血液測定モード(図8では「1:Normal」として表示されている)から体液測定モードに設定を切り替えたときにプレシーケンスを行い、体液測定結果にバックグラウンドの影響が及ばないことを確認する。
【0048】
プレシーケンスには、ブランクチェック動作が含まれている。このプレシーケンスでのブランクチェックの判定基準は、血球測定モードにおいて行われるブランクチェック(例えば電源立ち上げ後や自動洗浄後に行われる)の判定基準よりも厳しく、数分の1以下の値に設定されている。なお、体液測定モードから血液測定モードに設定を変更した場合には、通常血液測定結果にバックグラウンドの影響(キャリーオーバーの影響)は及ばないため、このプレシーケンスは実施されない。また、体液測定モードにおいて繰り返し体液検体を測定する場合も、通常バックグラウンドの影響は及ばないため、プレシーケンスは実施されない。ただし、体液検体にも極めて粒子数の多いものがあるため、体液検体の分析結果が所定値以上である場合には、次検体の分析結果に影響する虞があることをオペレータに通知するために、「測定結果が高いため、次検体の測定に影響を与える恐れがあります。ブランクチェック測定を行います。「確認」を押してください」のようなメッセージを画面上に出力し、オペレータが「確認」ボタンを押すことで、ブランクチェックを行うように構成することが好ましい。また、この場合には、画面に「中止」ボタンを設け、オペレータが「中止」ボタンを押すとブランクチェックを実施せず、スタンバイ画面に遷移する構成とすることもできる。さらには、ブランクチェックを行わなかった場合に、測定結果に対して信頼性が低いことを示すフラグを付与することが好ましい。このように必要な場合に限定して追加的にブランクチェックを実施することにより、時間や試薬類の消費を抑制することができる。
【0049】
図9は、血液測定モードから体液測定モードに測定モードが変更された場合に実施されるプレシーケンスの処理手順を示すフローチャートである。検体分析装置1は、測定部2でブランク試料の測定を行うことによりブランクチェックを実施し(ステップS31)、マイクロコンピュータ部6が測定結果を所定の許容値と比較して、測定結果が許容値以下か否かを判定する(ステップS32)。測定結果が許容値以下であった場合には、マイクロコンピュータ部6はプレシーケンスを終了し、処理をリターンする。測定値が許容値以下でない場合には、マイクロコンピュータ部6は、定められた回数(例えば3回)ブランクチェックを実行したか否かを判定し(ステップS33)、ブランクチェックの実施回数が所定回数に到達していない場合には、処理をステップS31へ戻し、前記所定回数内で再度ブランクチェックを実施する。所定回数内でブランクチェックの測定結果が許容値以下にならなかった場合には、表示・操作部7にブランクチェックの測定結果ならびに「確認」ボタン、「ブランクチェック」ボタン、「自動洗浄」ボタンを含む画面を表示する(ステップS34)。オペレータにより「確認」ボタンが押された場合には(ステップS35)、マイクロコンピュータ部6はプレシーケンスを終了し、処理をリターンする。「ブランクチェック」ボタンが押された場合には(ステップS36)、処理をステップS31へ戻して再びブランクチェックを実施し、「自動洗浄」ボタンが押された場合には(ステップS37)、専用の洗浄液による自動洗浄を実施した後(ステップS38)、処理をステップS31へ戻して再びプランクチェックを実施する。
【0050】
上述のようなプレシーケンスが終了すると、検体分析装置1は、スタンバイ状態となる(ステップS11)。オペレータは、体液測定を開始する場合には、血液検体のマニュアル測定のときと同様に測定部2の検体吸引ノズル18を検体容器中の体液検体に浸し、スタートスイッチを押す。マイクロコンピュータ部6は、このように測定開始の指示を受け付けると(ステップS12)、体液検体の吸引を開始する(ステップS13)。
【0051】
体液検体が吸引された後は、血液検体の場合と同様に体液検体がサンプリングバルブ91に導入される。そして、反応チャンバ13によってRBC/PLT測定用試料が作製される(ステップS15)。その後、DIFF用測定試料が白血球検出部41にて測定され、RBC/PLT用測定試料がRBC/PLT検出部42にて測定される(ステップS17)。体液測定モードの場合は、白血球検出部41で測定されるのはDIFF用測定試料のみであるので、血液測定モードでの測定時間より長く測定を行っても、血液測定のときより短時間に測定を完了することが可能である。このように、血液測定の測定時間よりも体液測定の測定時間を長くすることにより、粒子濃度の低い体液検体の分析精度を向上させることが可能である。測定時間を長くすれば計数される粒子数が増えるため、測定精度が向上するが、過度に長時間測定すると検体処理能力が低下し、また測定試料を白血球検出部41へ送出するシリンジポンプの能力に限界があることから、2〜6倍が適当である。本実施の形態においては、体液測定モード時の測定時間を血液測定モード時の3倍としている。
【0052】
一方、RBC/PLT用測定試料はいずれの測定モードにおいても同様に電気抵抗式検出部41に導入され、一定流速条件下にて測定が行われる。その後、測定によって得られた特徴情報に基づいて分析処理が行われ(ステップS19)、分析結果がデータ処理部3の表示部302に出力される(ステップS21)。血液測定モードでの分析処理においては、DIFFスキャッタグラムなどを分析して、5種類の白血球サブクラス(好中球:NEUT、リンパ球:LYMPH、単球:MONO、好酸球:EO、好塩基球:BASO)の情報(数や比率)を算出するが、体液測定モードでの分析処理においては、血球数が少ないことやダメージを受けている場合もあるので、一部統合した形で、2種類のサブクラス(単核球:MN、多核球:PMN)に分類している。なお、リンパ球、単球は単核球に属し、好中球、好酸球、好塩基球は多核球に属する。この分類アルゴリズムは、血液測定モードでの分析処理で説明したアルゴリズムと同様であるので、説明を省略する。
【0053】
ところで、体液試料中には、血球以外の異粒子(マクロファージや中皮細胞、腫瘍細胞等)が存在することがある。脳脊髄液にはこれら異粒子が存在することはまれであるが、その他の体液である、胸水や腹水には比較的よく現れる。よって、体液の種類にかかわらず体液中の血球を精度よく分類計数するためには、これら異粒子の影響を排除する必要がある。そこで、この発明では異粒子が本血球分析装置のDIFFスキャッタグラムの上部に出現するという新規な知見に基づき、目的とする体液試料中の白血球をより精度よく測定できるようにしている。なお、前記の従来技術にはこの点は考慮されていない。
【0054】
図10は、本実施形態の血球分析装置1の体液測定モードで、体液と白血球測定用試薬から調製されたDIFF用測定試料を測定、分析することにより得られるスキャッタグラムの模式図である。スキャッタグラムの縦軸は側方蛍光強度(上方ほど蛍光強度が大きい)を表し、横軸は側方散乱光強度(右方ほど散乱光強度が大きい)を表す。スキャッタグラムの蛍光強度が小さい領域LFには溶血により生じた赤血球ゴーストGcが分布し、蛍光強度が大きい領域HFには中皮細胞等の異粒子が分布し、中間領域MFには単核白血球Mc、多核白血球Pcが分布する。そこで、スキャッタグラムの解析において、領域LFおよびHFを除いた領域MFに分布している粒子成分を白血球として解析を行い、上記2つのグループに分類、計数する。なお、単核白血球Mcにはリンパ球および単球が含まれ、多核白血球Pcには好中球、好酸球および好塩基球が含まれる。
【0055】
このように体液中の白血球を分析する場合には、体液に含有される血球数が少ないことやダメージを受けている場合もあるので、臨床的に有意な情報として、白血球を単核白血球と多核白血球に分類し計数している。
【0056】
また、体液中には、血球以外の異粒子(マクロファージ、中皮細胞、腫瘍細胞等の有核細胞)が存在することがある。脳脊髄液にはこれら異粒子が存在することはまれであるが、その他の体液である、胸水や腹水には比較的よく現れる。図10のスキャッタグラムにおいては、このような白血球以外の有核細胞は、領域HFに分布する。このように本実施形態においては、白血球以外の有核細胞を白血球と分けることができるので、このような白血球以外の有核細胞を含む体液であっても、正確な白血球数を求めることが可能になる。また、領域HFに出現する細胞を計数することにより、異常な細胞の出現の度合いを提供することが可能になる。なお、本実施形態においては、各領域を分画する閾値により、各細胞を領域LF、MFおよびHFに分画しているが、この閾値をマニュアルで変更できるようにしてもよい。
【0057】
図11は上記のスキャッタグラムの解析法の妥当性を示すために本実施形態の血球分析装置1による分析結果と参照法による計数結果を比較した図である。被検試料は胸水であり、図中の「本法」は本実施形態の血球分析装置1により算出された白血球の数(WBC)とその他の異粒子の数(Others)を表し、「Ref」は参照法(フックス・ローゼンタール計算盤法およびサイトスピン法)による算出結果を表す。例1、2,3とも異粒子が多く出現している胸水を分析した結果であるが、本実施形態の血球分析装置1による分析結果と参照法との間に相関関係があることがわかる。
【0058】
図13は、血液から調製された上記DIFF用測定試料の分析結果として、データ処理部3の表示部302に表示される画面100を示す。画面100の上部には検体番号101を表示する検体番号表示領域が設けられ、その近傍には患者属性を表示する属性表示領域が設けられている。属性表示領域には、具体的には検体番号、患者ID、患者名、性年月日、性別、病棟、担当医、測定年月日、測定時刻、コメントなどが表示される。属性表示領域の下部には測定結果を表示する測定結果表示領域が設けられている。測定結果表示領域は複数のページからなり、これらページは複数のタブ102により選択されることにより画面表示される。タブはメイン画面、グラフ画面、その他、測定項目にあわせたものが複数用意されている。図12はグラフ画面のタブが選択された場合の表示画面である。測定値表示領域の左半分には、測定結果である測定値を表示する測定値表示領域103とフラグを表示するフラグ表示領域104とが設けられ、右半分には測定結果である分布図105を表示する分布図表示領域が設けられている。測定値表示領域にはWBC、RBC、・・・、NEUT#、・・・、BASO#、NEUT%、・・・、BASO%などの項目とデータと単位が表示され、フラグ表示領域104にはWBC、PLT、RBCあるいはRETに関する、臨床検査上有益な情報となりうる検体異常や疾患の疑いを示すフラッギング結果が表示される。
【0059】
分布図表示領域105には6つの分布図が表示されている。上段左側のスキャッタグラムは、DIFF用のスキャッタグラムである。上段右側はWBC/BASO用、中段左側は幼若球(IMI)用、中段右側はRET用の、各スキャッタグラムである。下段左側はRBC用ヒストグラム、下段右側はPLT用ヒストグラムである。
【0060】
図14は体液から調製された上記DIFF用測定試料の測定結果として、データ処理部3の表示部302に表示される画面110を示す。画面110の上部には検体番号を表示する検体番号表示領域111が設けられ、その近傍には患者属性表示領域が設けられている。検体番号表示領域111の左端には、体液測定モードで測定を行ったことを示す「F」が表示されている。このことにより、この分析結果が体液測定の結果であることを明確に認識することができる。測定結果表示領域はタブ112で選択可能な複数のページからなっている。この例では「体液測定(Body Fluid)」のタブが選択されている。
【0061】
測定値表示領域113には、血液測定モードでの測定結果とは異なる、体液用の測定項目名である、WBC−BF(WBC数)、RBC―BF(RBC数)、MN#(単核球数(リンパ球+単球))、PMN#(多核球数(好中球+好塩基球+好酸球))、MN%(白血球中の単核球比率)、PMN%(白血球中の多核球比率)と測定値と単位が各対応付けられて表示されている。体液測定においても、血液測定と同様にフラグ表示領域114が設けられている。分布図表示領域には2つの分布図115が表示されており、上段のスキャッタグラムはDIFF用のスキャッタグラムである。下段はRBC用ヒストグラムである。
【0062】
図15は図14の画面110において、タブ112で「リサーチBF(Research(BF))」のタブが選択された例である。この画面はリサーチパラメータ表示領域116が表示されること以外は画面110と同様の項目が表示される。リサーチパラメータ表示領域116には、図10において、領域HFに存在する粒子数である「HF−BF#」、領域HFと領域MFを含む領域に存在する粒子数に対する領域HFに存在する粒子数の比率である「HF−BF%」、領域HFと領域MFを含む領域に存在する粒子の数である「TC−BF#」が表示される。なお、「HF−BF%」はHF−BFのTC−BFに対する割合である。
【0063】
図16はデータ処理部3の表示部302に表示される、記憶検体の一覧表示画面120である。130は患者属性表示領域である。その上方にはタブ選択による測定結果を表示する測定結果表示領域が設けられている。測定結果表示領域の左端の列131は測定結果のバリデート作業の未あるいは済を示すためのものである。Vで表記されているのがバリデート済みを表す。その右の列132は測定モードを示すためのものである。「F」で示されているのが体液測定モードでの測定結果である。体液測定モードでブランクチェックが必要な高値検体であったが、ブランクチェックを行わなかった場合には、そのことを示すために反転表記でFと表記することができる。
【0064】
以上、本件発明の血球分析装置の構成、機能について、血球分析装置に予め備えられたものとして説明したが、同機能をコンピュータプログラムにて実現し、従来の血球分析装置にそのコンピュータプログラムをインストールすることにより従来の血球分析装置に本発明に係る機能を発揮されるように構成することもできる。
【0065】
なお、本実施の形態においては、血液測定モードにおける白血球分類測定と、体液測定モードにおける白血球分類測定とでそれぞれ測定試料を作成するときの検体量、試薬の種類、及び試薬の量を同一とする構成について述べたが、これに限定されるものではなく、体液測定モードにおける白血球分類測定用の測定試料を作成するための検体量及び試薬の量を、血液測定モードにおける白血球分類測定用の測定試料を作成するための検体量及び試薬の量よりそれぞれ多くすることも可能である。体液測定モードにおける白血球分類測定では、血液測定モードの場合よりも測定時間が長く、測定に必要な測定試料の量が多いため、このようにすることにより、血液測定モードの白血球分類測定及び体液測定モードの白血球分類測定のそれぞれにおいて、適切な量の測定試料を作成することが可能となる。
【0066】
また、本実施の形態においては、散乱光と蛍光とを用いて体液測定モードにおける白血球分類を行う構成について述べたが、これに限定されるものではなく、例えば散乱光と吸収光とを用いて体液測定モードにおける白血球分類を行う構成としてもよい。吸収光の測定は、白血球を染色する染色試薬を他の試薬と共に検体に混合して測定試料を調製し、その測定試料をフローセルに供給してフローセル中に試料流を形成させ、その試料流に光を照射し、試料流から出射される光をフォトダイオード等の受光素子によって受光することで可能となる。フローセル中を白血球が通過したときに白血球により光が吸収され、その吸収の程度が受光素子の受光量として捉えられる。このような吸収光の測定については、米国特許第5122453号及び米国特許第5138181に開示されている。また、散乱光の代わりに電気抵抗を測定し、その電気抵抗値と吸収光とによって白血球の分類測定を行うこともできる。
【図面の簡単な説明】
【0067】
【図1】本発明の血球分析装置の外観図である。
【図2】分析装置の測定部のブロック図である。
【図3】流体機構部のブロック図である。
【図4】白血球検出部の光学系を示す図である。
【図5】RBC/PLT検出部を示す図である。
【図6】HGB検出部を示す図である。
【図7】検体の測定処理を示すフローチャートである。
【図8】測定モードを設定するための表示画面を示す図である。
【図9】プレシーケンスの処理を表すフロー図である。
【図10】体液から調製したDIFF用測定試料を測定したスキャッタグラムの模式図である。
【図11】実施形態の血球分析装置による測定結果と参照法による測定結果を対比した図である。
【図12】血液から調製したDIFF用測定試料を測定したスキャッタグラムの模式図である。
【図13】血液測定モードでの測定結果を表す表示画面である。
【図14】体液測定モードでの測定結果を表す表示画面である。
【図15】体液測定モードでの測定結果を表す表示画面である。
【図16】体液測定モードでの測定結果を表す表示画面である。
【符号の説明】
【0068】
1 血球分析装置
2 測定部
3 データ処理部
4 検出部
5 アナログ信号処理部
6 マイクロコンピュータ部
7 表示操作部
8 流体処理部
【特許請求の範囲】
【請求項1】
検体を吸引する吸引部と、
前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、
血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、
前記モード設定手段により血液測定モードが設定された場合に、血液検体測定用の動作を実行するように前記測定部を動作制御する第1動作制御手段と、
前記モード設定手段により体液測定モードが設定された場合に、前記血液検体測定用の動作とは異なる体液検体測定用の動作を実行するように前記測定部を動作制御する第2動作制御手段と、
を備える検体分析装置。
【請求項2】
前記血液検体測定用の動作は、前記測定部が測定試料を所定の第1時間測定する動作であり、前記体液検体測定用の動作は、前記測定部が測定試料を前記第1時間とは異なる第2時間測定する動作である請求項1に記載の検体分析装置。
【請求項3】
前記第2時間は、前記第1時間より長い時間である請求項2に記載の検体分析装置。
【請求項4】
前記血液検体測定用の動作は、前記測定部が血液検体と所定の第1の量の試薬とを混和して測定試料を調製する動作であり、前記体液検体測定用の動作は、前記測定部が体液検体と前記第1の量とは異なる第2の量の試薬とを混和して測定試料を調製する動作である請求項1乃至3のいずれかに記載の検体分析装置。
【請求項5】
前記体液検体を測定する前に、検体を含有しないブランク試料を測定するように前記測定部を動作制御するブランク測定動作制御手段をさらに備える請求項1乃至4のいずれかに記載の検体分析装置。
【請求項6】
前記測定部が体液検体を測定した測定結果を所定の基準値と比較する比較手段と、
前記比較手段による比較の結果、前記測定結果が前記基準値よりも大きい場合に、洗浄動作を実行するように前記測定部を動作制御する洗浄制御手段と
をさらに備える請求項1乃至5のいずれかに記載の検体分析装置。
【請求項7】
検体を吸引する吸引部と、
前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、
血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、
前記モード設定手段により血液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、所定の第1分析処理を実行する第1分析手段と、
前記モード選択手段により体液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、前記第1分析処理とは異なる第2分析処理を実行する第2分析手段と、
を備える検体分析装置。
【請求項8】
前記第1分析処理は、白血球を少なくとも4種類に分類する処理を含み、
前記第2分析処理は、白血球を前記第1分類処理よりも少ない種類に分類する処理を含む、
請求項7に記載の検体分析装置。
【請求項1】
検体を吸引する吸引部と、
前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、
血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、
前記モード設定手段により血液測定モードが設定された場合に、血液検体測定用の動作を実行するように前記測定部を動作制御する第1動作制御手段と、
前記モード設定手段により体液測定モードが設定された場合に、前記血液検体測定用の動作とは異なる体液検体測定用の動作を実行するように前記測定部を動作制御する第2動作制御手段と、
を備える検体分析装置。
【請求項2】
前記血液検体測定用の動作は、前記測定部が測定試料を所定の第1時間測定する動作であり、前記体液検体測定用の動作は、前記測定部が測定試料を前記第1時間とは異なる第2時間測定する動作である請求項1に記載の検体分析装置。
【請求項3】
前記第2時間は、前記第1時間より長い時間である請求項2に記載の検体分析装置。
【請求項4】
前記血液検体測定用の動作は、前記測定部が血液検体と所定の第1の量の試薬とを混和して測定試料を調製する動作であり、前記体液検体測定用の動作は、前記測定部が体液検体と前記第1の量とは異なる第2の量の試薬とを混和して測定試料を調製する動作である請求項1乃至3のいずれかに記載の検体分析装置。
【請求項5】
前記体液検体を測定する前に、検体を含有しないブランク試料を測定するように前記測定部を動作制御するブランク測定動作制御手段をさらに備える請求項1乃至4のいずれかに記載の検体分析装置。
【請求項6】
前記測定部が体液検体を測定した測定結果を所定の基準値と比較する比較手段と、
前記比較手段による比較の結果、前記測定結果が前記基準値よりも大きい場合に、洗浄動作を実行するように前記測定部を動作制御する洗浄制御手段と
をさらに備える請求項1乃至5のいずれかに記載の検体分析装置。
【請求項7】
検体を吸引する吸引部と、
前記吸引部により吸引された検体と試薬とを混和して測定試料を調製し、調製された測定試料を測定し、前記測定試料中の成分の特徴を表す特徴情報を取得する測定部と、
血液検体を測定するための血液測定モード及び血液検体とは異なる体液検体を測定するための体液測定モードの一方を動作モードに設定するためのモード設定手段と、
前記モード設定手段により血液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、所定の第1分析処理を実行する第1分析手段と、
前記モード選択手段により体液測定モードが設定された場合に、前記測定部によって取得された特徴情報に対して、前記第1分析処理とは異なる第2分析処理を実行する第2分析手段と、
を備える検体分析装置。
【請求項8】
前記第1分析処理は、白血球を少なくとも4種類に分類する処理を含み、
前記第2分析処理は、白血球を前記第1分類処理よりも少ない種類に分類する処理を含む、
請求項7に記載の検体分析装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【公開番号】特開2008−209383(P2008−209383A)
【公開日】平成20年9月11日(2008.9.11)
【国際特許分類】
【出願番号】特願2007−95226(P2007−95226)
【出願日】平成19年3月30日(2007.3.30)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
【公開日】平成20年9月11日(2008.9.11)
【国際特許分類】
【出願日】平成19年3月30日(2007.3.30)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
[ Back to top ]

