検体濃度の光学測定システムおよび方法
放射励起可能な指示薬分子周囲における検体の濃度を測定する方法およびセンサ。刺激波形を用いて、放射線源を駆動する。指示薬分子を放射線源に露出する。指示薬分子によって放出されるフォトルミネセンス放射を表す応答波形を発生する。刺激波形と応答波形との間における位相差が、検体の濃度の関数となり、検体濃度の判定を可能にする。
【発明の詳細な説明】
【技術分野】
【0001】
関連出願に対する相互引用
[0001] 本願は、2008年7月28日に出願された米国仮特許出願第61/084,100号の優先権を主張する。この特許出願をここで引用したことにより、その内容全体が本願にも含まれるものとする。
【0002】
[0002] 発明の分野
[0003] 本発明は、検体濃度の測定システムおよび方法に関する。更に特定すれば、本発明は位相に基づくプロトコル(phase-based protocol)を用いて検体濃度の測定を可能にする微小センサおよびセンサ・インターフェース・モジュールに関する。
【従来技術】
【0003】
[0004] 関連技術の解説
[0005] 放射線源による光センサの励起に基づいて、この光センサの発光特性を測定するために、フォトルミネセンス検知が用いられている。フォトルミネセンス検知は、例えば、蛍光物質のフォトルミネセンス寿命、検体の濃度、フォトルミネセンス強度、またはその他の化学的パラメータを測定するために用いることができる。フォトルミネセンス検知を用いてこれらのパラメータを検出するデバイスは、通例、振幅に基づくプロトコル、時間に基づくプロトコル、または位相に基づくプロトコルを用いて、所望のパラメータを求める。
【0004】
[0006] このようなデバイスは、通例、かさばり、高価であり、しかも輸送が容易でない。これらのデバイスは、約10,000米ドルの価格になることもあり、ほぼ大型画面の陰極線管テレビジョンのサイズであることもあり、多数の機器を含むこともある。これらのデバイスの中には携帯用として市販されているものもあるが、通例、これらのデバイスを種々の場所に輸送するためには、棚が2つある研究室用カート(two-shelf lab cart)のような移動機器が必要となる。これは、少なくとも部分的に、高価な回路および複雑なデータ処理のためであり、所望の結果を得るために、これらを有為なノウハウと組み合わせる必要がある。加えて、これらのデバイスは、通例、動作するために大量の電力を必要とする。
【0005】
[0007] 現在のシステムには、これらおよびその他の欠点がある。
【発明の概要】
【発明が解決しようとする課題】
【0006】
[0008] 本発明は、検体の濃度を測定するデバイスおよび方法に関する。更に特定すれば、本発明は、センサ、およびこのセンサと通信して媒体における検体の濃度を測定するセンサ・インターフェース・モジュール(SIM)に関する。これらのセンサおよびSIMは、例えば、生物化学酸素要求量、不活性化(inerting)、燃焼、環境、化学、ダイビング/生命支援(diving/life support)、ならびに麻酔学、呼吸、および酸素濃度計のような医療用途というような、種々の気体環境において用いることができる。また、これらのセンサおよびSIMは、例えば、生物化学酸素要求量、埋め込み可能センサ、魚類養殖(fish farming)、水族館、汚染監視、化学的処理、および醸造/醗酵というような、種々の液内環境においても用いることができる。これらの用途の各々は、例えば、酸素、グルコース、二酸化炭素、毒物、温度というような種々の検体の濃度を、例えば、空気、血液、水、あるいはその他の気体または液体媒体というような媒体内において判定するために用いることができる。
【課題を解決するための手段】
【0007】
[0009] 一実施形態によれば、本発明は、光センサおよびセンサ・インターフェース・モジュール(SIM)を含む。このセンサは、放射源、光電変換器、および指示薬分子(indicator molecule)を含む。センサ・インターフェース・モジュールは、センサと通信して放射源を駆動し、センサによって得られたデータを受け取るマイクロコントローラを含む。このマイクロコントローラは、放射源に指示薬分子を照射させる。指示薬分子は、放射源によって放出される光のためにルミネセンスを発し、媒体内に存在する検体に基づいてある種の特性を呈する。センサは、このルミネセンスに関するデータを、処理のために、マイクロコントローラに送信する。受信したデータ、既知のデータ、およびシュテルン−フォルマーの関係に基づいて、マイクロコントローラは検体の濃度を判定する。本発明の一実施形態によれば、センサ・インターフェース・モジュールは、データをシステム・ユーザに提示することができるように、このモジュールがデータを外部データ・システムに送信することを可能にするインターフェースを含む。
【0008】
[0010] 一態様において、本発明は、マイクロコントローラを有する、検体濃度測定デバイスを提供する。マイクロコントローラは、所定の周波数の周期的ディジタル信号を当該マイクロコントローラのディジタル出力バス上に出力し、マイクロコントローラのアナログ入力上にある刺激波形と応答波形との間における位相差を計算するように構成されている。
【0009】
[0011] また、このデバイスは、周期的ディジタル信号を周期的電圧波形に変換するディジタル/アナログ変換器と、周期的電圧波形を平滑化し、刺激波形を出力するロー・パス・フィルタと、刺激波形を周期的電流波形に変換し、放射源を駆動するように動作可能な電圧/電流変換器であって、放射源が指示薬分子上に放射する、電圧/電流変換器とを含む。
【0010】
[0012] 更に、このデバイスは、光電変換器からの電流を応答電圧波形に変換するように動作可能なバンドパス・トランスインピーダンス増幅器も含む。指示薬分子からの放射が光電変換器に入射し、位相差が、指示薬分子に局限的な検体濃度の関数である。
【0011】
[0013] 本発明の一実施形態によれば、媒体内にある検体の濃度を測定する方法を提供する。この方法は、複数の指示薬分子が供給されるセンサを用いる。指示薬分子は、特定の検体がある場合に、所定の特性を呈する。センサは、励起源を駆動するために用いられる刺激波形を発生する。
【0012】
[0014] 指示薬分子は、用いられるセンサの種類に基づいて、励起源によって励起され、濃度判定が望まれる検体と関連のある特性を呈する。呈された特性に対する応答波形が、その特性の表現として発生される。刺激波形および応答波形をオーバーサンプリングし、検体の濃度に依存する位相遅延を判定する。次いで、判定した位相遅延およびシュテルン−フォルマー(Stern-Volmer)関係を用いて、検体濃度を判定することができる。
【0013】
[0015] 本発明の別の実施形態によれば、検体濃度判定方法は、マイクロコントローラの出力上に周期的ディジタル出力信号を発生するステップを含む。この周期的ディジタル出力信号を平滑化駆動電流波形に変換する。この平滑化駆動電流波形は、周期的ディジタル出力信号と同じ周波数である。
【0014】
[0016] また、この方法は、平滑化駆動電流によって放射源を駆動するステップであって、放射源からの放射が指示薬分子に入射する、ステップと、光電変換器によって、指示薬分子の放射励起エネルギを検出するステップであって、この光電変換器が、平滑化駆動電流波形と同じ周波数の波形を出力する、ステップと、平滑化駆動電流波形と出力された光電変換器波形との間における位相差を測定するステップとを含む。位相差は、指示薬分子に局限的な検体濃度と相関がある。
【0015】
[0017] 本発明の上述のおよびその他の特徴ならびに利点、更には本発明の好ましい実施形態の構造および動作について、添付図面を参照しながら以下に詳細に説明する。
【図面の簡単な説明】
【0016】
[0018] 添付図面は、本明細書に組み込まれその一部をなすが、本発明の種々の実施形態を図示し、更に説明と共に、本発明の原理を説明し、当業者が本発明を行い使用することを可能にする役割を果たす。
【図1】図1は、本発明の一実施形態による検体濃度測定システムの模式図である。
【図2】図2は、本発明の一実施形態によるセンサ・インターフェース・モジュールの模式図である。
【図3】図3は、本発明の一実施形態によるフォトルミネセンス型センサの上面図である。
【図4】図4は、本発明の一実施形態によるフォトルミネセンス型センサの断面図である。
【図5】図5は、本発明の一実施形態による検体濃度測定方法を示すフローチャートである。
【図6】図6は、本発明の一実施形態による検体濃度測定方法を示すフローチャートである。
【図7】図7A〜図7Eは、本発明の一実施形態にしたがって検体濃度を測定するために用いられるデバイスの回路における所定の地点に現れる波形例を示す。
【図8】図8は、本発明の一実施形態によるフォトルミネセンスに基づくセンサの図である。
【発明を実施するための形態】
【0017】
[0026] 一実施形態によれば、本発明は検体濃度測定システムおよび方法に関する。このシステムおよび方法は、光センサおよびセンサ・インターフェース・モジュール(SIM)を用いて、フォトルミネセンスを用いて検体の濃度を測定する。これらのセンサおよびSIMは、当該センサおよびSIMが非常に小型で携帯用となることを可能にするように、フォトルミネセンス情報を伝達し処理する。実施形態によっては、これらのセンサおよびSIMが人の掌に納まる程度の大きさとなり、更に小型化することも可能である。
【0018】
[0027] 図1は、本発明の一実施形態による検体濃度測定デバイス100の模式図である。デバイス100は、検体源110、センサ120、センサ・インターフェース・モジュール(SIM)130、およびデータ・システム140を含む。検体源110は、例えば、濃度測定が望まれる検体を含む媒体とすることができる。この媒体は、例えば、空気、血液、水、あるいはその他の気体媒体または液体媒体とすることができる。センサ120は、好ましくは、光センサであり、蛍光指示薬分子(以下で更に詳しく説明する)を用いて、媒体内における、例えば、酸素、グルコース、および毒物というような検体の濃度測定を可能にする。本発明の一実施形態によれば、センサ120は、いずれかの既知の有線またはワイヤレス接続を用いて、SIM130と通信することができる。センサ120は、SIM130と通信して、例えば、気体媒体、またはセンサ120が埋め込まれている被験者の血液における酸素濃度を測定することができる。データ・システム140は、例えば、データ収集システム、マイクロプロセッサ、またはマイクロコンピュータとすることができる。
【0019】
[0028] センサ120は、好ましくは、放射線源(radiation source)150と変換器160とを含む。一実施形態によれば、放射線源150は、検体を含有する媒体を照射する発光ダイオード(LED)を含む。センサ120は、マイクロコントローラ170から放射線源150を制御する命令を得て、得られたデータを処理のためにマイクロコントローラ170に送信する。センサ120は、インターフェース180を用いて、SIM130と通信する。変換器160は、センサ120が受信したアナログ情報を、マイクロコントローラ170によって処理されるデータに変換する。
【0020】
[0029] 本発明の一実施形態によれば、センサ120およびSIM130は、回路ボード190上に設けることができる。回路ボード190は、検査、較正、およびその他の機能をデバイス100が実行することを可能にする。回路ボード190は、SIM130とデータ・システム140との間において通信を可能にするインターフェース200を含む。SIM130は、データ・システム140と通信して、センサ120およびSIM130によって得られたまたは発生した読み取り値、測定値、またはその他のデータを、データ・システム140によって処理、表示、または格納することを可能にすることができる。
【0021】
[0030] 先に論じたように、センサ120およびSIM130は、好ましくは、人の掌に納まるサイズであり、更に小型化することもできる。非限定的な一実施形態によれば、SIM130は、約0.34立方インチ以下の空間を占有し、センサ120は、0.009立方インチ以下の空間を占有し、約1から200ミリアンペアの範囲で直流(DC)二乗平均(RMS)電力を消費し、約100ミリ秒(ms)以下の検体濃度変化に応答し、真空レベルから平方インチ当たり数千ポンド(psi)の範囲の周囲圧力において動作する。
【0022】
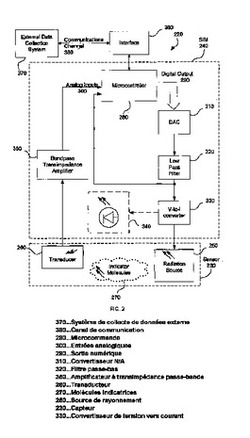
[0031] 図2は、本発明の一実施形態による検体濃度測定デバイス220の模式図である。デバイス220は、センサ230およびセンサ・インターフェース・モジュール(SIM)240を含む。センサ230は、濃度測定が望まれる検体を含有する媒体内に設けられる。センサ230およびSIM240は、検体濃度を判定するために用いられるデータに関して、互いに通信する。センサ230は、放射線源250、変換器260、および指示薬分子270を含み、以下で更に詳しく説明する。
【0023】
[0032] センサ・インターフェース・モジュール(SIM)240はマイクロコントローラ280を含む。マイクロコントローラ280は、指示薬分子270にルミネセンスを発生させる放射線源250を駆動するために用いられる励起信号を発生する。本発明の一実施形態によれば、指示薬分子270は、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩(complex tris(4,7-diphenyl-1, 10-phenanthroline) ruthenium(II) perchlorate)、ユーロピウムまたはテルビウム・コンプレックスのようなランタニド系指示薬、芳香族炭化水素、あるいは位相変調によって測定するときに検出可能な差が得られる程に十分長いルミネセンス寿命を有する検体に相応しい指示薬または分子伝達系であればいずれでもよい。検体の例には、酸素、二酸化炭素、グルコース、および温度が含まれるが、これらに限定されるものではない。
【0024】
[0033] 放射線源250は、用いられる指示薬の種類に応じて異なってもよい。例えば、指示薬がコンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩である場合、その崩壊時間は約4ミリ秒であり、青色発光ダイオード(LED)を用いることができる。これは、青色LEDからの発光が、約460ナノメートルにピーク波長を有し、これがコンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩の光学励起スペクトルと良く一致するからである。緑色および赤色LEDのようなその他のLED、またはその他の放射線源も用いることができる。一般に、好ましい放射線源またはLEDは、指示薬の光学励起スペクトルと一致するピーク発光を有する。ランタニド指示薬を用いる場合、約360〜380ナノメートルにピーク発光波長を有する紫色LEDを用いるとよい。ランタニド系指示薬の例については、米国特許第6,344,360号に記載されている。この特許をここで引用したことにより、その内容全体が本願にも含まれるものとする。指示薬分子の更に別の例が、米国特許第5,517,313号に記載されており、この特許もここで引用したことにより、その内容全体が本願にも含まれるものとする。
【0025】
[0034] 励起信号は、マイクロコントローラ280によって処理されるパラメータに基づいて発生する。励起信号は、測定対象検体が呈する既知の特性に基づく。これによって、基準信号が供給され、この基準信号と測定信号を比較することができる(以下で更に詳しく説明する)。一実施形態によれば、マイクロコントローラ280は、ディジタル出力チャネル290と1つ以上のアナログ入力チャネル300とを有するように構成されている。ディジタル出力チャネル290は、センサ230の放射線源250に励起信号を送信するために用いることができる。アナログ入力チャネル300は、センサ230の変換器260によって送信された信号を受信するために用いることができる。Microchip Technology Inc.(マイクロチップ・テクノロジ社)からのPIC24ファミリーの中にあるマイクロコントローラ、または他の互換性のあるマイクロコントローラというようなマイクロコントローラを、マイクロコントローラ280として用いることができる。本発明の一実施形態によれば、マイクロコントローラ280はディジタル信号プロセッサを含む。
【0026】
[0035] センサ・インターフェース・モジュール(SIM)240は、更に、マイクロコントローラ280のディジタル出力チャネル290を用いて送信された信号をアナログ電圧に変換するためのディジタル/アナログ変換器(DAC)310も含む。一実施形態では、マイクロコントローラ280のディジタル出力チャネル290は、ビット0...ビット3を有する4ビット・バスであり、ディジタル/アナログ変換器310は単純な抵抗器ラダー(ladder)である。非限定的な実施形態の一例では、ディジタル/アナログ変換器310は、ビット3に接続されている111kΩ抵抗器、ビット2に接続されている270kΩ抵抗器、ビット1に接続されている400kΩ抵抗器、およびビット0に接続されている800kΩ抵抗器を含む。ディジタル/アナログ変換器310の出力は、各抵抗器のリード(マイクロコントローラとは反対側のノード)が接続されているノードである。当業者に知られている他の抵抗器ラダーおよびネットワークも、ディジタル/アナログ変換器310として用いることができる。更に、ディジタル/アナログ変換器310を集積回路上に実装することもできる。
【0027】
[0036] 更に、センサ・インターフェース・モジュール(SIM)240はロー・パス・フィルタ320も備えている。ロー・パス・フィルタ320は、ディジタル/アナログ変換器310からの電圧波形出力を、電圧波形出力の正弦波近似に変換する。ロー・パス・フィルタ320は、当業者には周知の抵抗器−キャパシタ(RC)設計とするとよい。例示的な一実施形態では、抵抗(R)および容量(C)は、周波数f、例えば、10kHzの信号を通過させ、それよりも高い周波数のノイズ源を全て抑制するように選択される。ロー・パス・フィルタ320の電圧波形出力は、マイクロコントローラ280のアナログ入力300に送信される。ロー・パス・フィルタ320は、可変容量キャパシタを含むこともできる。本発明の非限定的な一実施形態によれば、このロー・パス・フィルタを形成するキャパシタおよび抵抗器は、それぞれ、約470pFおよび15kΩの値を有するとよい。
【0028】
[0037] 更に、センサ・インターフェース・モジュール(SIM)240は、電圧−電流変換器330を含む。一実施形態では、電圧−電流変換器330は、その入力、即ち、ロー・パス・フィルタ320の電圧波形出力の正弦波近似を、入力電圧に比例する電流に変換する。電圧−電流変換器330の出力は、放射線源250を駆動する励起信号を含む。放射線源250は、その放射出力が指示薬分子270に到達するように位置付けられている。放射線源250によって放出された光が、指示薬分子270に、測定対象検体の存在に基づく特定の態様でルミネセンスを発生させる。このルミネセンスが、変換器260によって信号として検出される。変換器260は、指示薬分子270から照射するルミネセンスの関数となる信号を出力する。変換器260は、例えば、フォトダイオード、フォトトランジスタ、光電子増倍管、またはその他の光検出器とすることができる。
【0029】
[0038] 電圧−電流変換器330は、オプションとして、発光ダイオード(LED)340を駆動するために、放射線源250を駆動する電流を忠実に再現する(mirror)、カレント・ミラーと通信状態にあってもよい。一実施形態では、LED340は、センサ・インターフェース・モジュール(SIM)240を検査するために用いることができる赤色LEDである。
【0030】
[0039] 変換器260の出力は、バンドパス・トランスインピーダンス増幅器350に接続されている。バンドパス・トランスインピーダンス増幅器350は、バンドパス利得応答を含み、その電流入力の関数となる電圧波形を発生する。バンドパス・トランスインピーダンス増幅器350の出力は、マイクロコントローラ280のアナログ入力300に送信される。
【0031】
[0040] また、デバイス220は通信インターフェース360も含むことができる。通信インターフェース360は、マイクロコントローラ280が検体濃度に関するデータを外部データ・システム370に対して送信および受信することを可能にする。マイクロコントローラ280およびデータ・システム370は、例えば、マイクロコントローラ・シリアル・チャネルのような、通信チャネル380を通じて通信することができる。データ・システム370は、例えば、データ収集システム、マイクロプロセッサ、マイクロコンピュータ、またはその他のデバイスとすることができる。
【0032】
[0041] マイクロコントローラ280は、例えば、格納されているプログラムを用いて、その通信チャネル380を通じて送信されたコマンド・コードを受信しそれに対して動作し、周期的に変化するディジタル出力、サンプル電圧をアナログ入力上に発生し、検体濃度に関するデータを計算し通信チャネル380を通じて送信するように構成されている。センサ・インターフェース・モジュール(SIM)240は、1つの測定値を取り込むように、または指定された遅延の後、連続的な反復測定値を流す(run)ように設定することができる。
【0033】
[0042] 図3および図4は、それぞれ、本発明の一実施形態によるセンサ400の平面図および断面図である。センサ400は、例えば、光センサとすることができる。センサ400は、放射源430に合わせたウェル420、および光電変換器450に合わせたウェル440とが形成された基板410を含む。放射源430は、例えば、発光ダイオード(LED)とすることができ、変換器450は、例えば、光電変換器、フォトダイオード、またはその他の変換器とすることができる。利点の中でもとりわけ、この構成は、放射源430による変換器450の直接照明を減少させる。
【0034】
[0043] 更に、センサ400は、センサ400の透過および反射特性を最適化する導波路460を含むことができる。一実施形態では、指示薬分子470は、導波路460の上面の少なくとも一部に配置されている。センサ・インターフェース・モジュール(SIM)480が、放射源430および変換器450に近接して位置付けられている。通信チャネル490が、センサ400を外部データ・システム(図2に示す)と接続することができる。他の実施形態では、センサ400は外部データ・システムとワイヤレスで通信する。
【0035】
[0044] 図5は、本発明の一実施形態による検体濃度測定方法を示す。この方法は、検体の特定の特性を判定するために用いられるセンサの種類を選択するステップ510を含む。例えば、被験者の血液における酸素濃度を検知するために、光センサを用いることができる。
【0036】
[0045] ステップ520において、指示薬分子をセンサ上に供給する。指示薬分子は、好ましくは、センサによる検出が可能な検体特性に反応する。例えば、放射線源は、指示薬分子のルミネセンスが光センサによって検出されるように、指示薬分子を励起するために用いることができる。例えば、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩指示薬分子を励起するためには、青色発光ダイオード(LED)を用いることができる。
【0037】
[0046] ステップ530において、濃度測定が望まれる検体の種類に基づいて、刺激波形を発生する。光センサを用いる場合、例えば、これは、刺激波形を用いてLEDに所定の形態を有する放射を放出することを指令することを含むとよい。ステップ540において、このセンサによって特定の特性を検出することができるデバイスを用いて指示薬分子を励起する。例えば、光センサが用いられている場合、このデバイスは放射線源とするとよい。
【0038】
[0047] 次いで、センサは、ステップ550において、指示薬分子によって励起された特性を検出する。光センサおよび放射線源を用いる場合、光センサは、指示薬分子によって放出されるフォトルミネセンス放射を検出する。このフォトルミネセンス放射は、センサのフィルタによって受け取られ、センサのフォトダイオードによって変換される。ステップ560において、受け取られた指示薬分子の特性、例えば、指示薬分子から受け取られたフォトルミネセンス放射の特性に基づいて、応答波形を発生する。光センサの例では、フォトダイオードからの電流は、刺激波形のそれと同じ形態となり、位相が遅延するだけである。
【0039】
[0048] 次に、ステップ570において、刺激波形と応答波形との間における位相遅延をステップ580において判定できるように、発生した刺激波形および応答波形をオーバーサンプリングする。ステップ590において、この位相遅延を用いて、検体濃度を判定することができる。これは、位相遅延が検体濃度に比例するからである。即ち、蛍光を発する分子は、放射線刺激の除去後、既知の時間期間、つまり、崩壊時間または励起状態寿命の間蛍光を発する。蛍光の強度および崩壊時間の双方は、所与の蛍光消光剤の濃度との線形関係にしたがって変化する。非限定的な一例では、対象の検体の濃度は、シュテルン−フォルマーの式に記述される関係に基づいて、位相遅延から判定することができる。
【0040】
【数1】

【0041】
ここで、τは崩壊時間、Iは消光剤Qの存在下における蛍光の強度、τ0は崩壊時間、そしてI0は消光剤Qがない場合の蛍光の強度、Ksvはシュテルン−フォルマー消光定数、[Q]は消光剤Qの濃度である。つまり、τを測定することができれば、Qの濃度は、例えば、シュテルン−フォルマーの式によって判定することができる。
【0042】
[0049] 図6は、本発明の一実施形態による検体濃度測定方法を示す。ステップ610において、マイクロコントローラのディジタル出力バス上に周期的なディジタル出力信号を発生する。例えば、マイクロコントローラは、周波数fを有する量子化した正弦波を表す一連のディジタル出力信号を発生することができる。この一連の出力は、DC基準線値までの上昇勾配を含み、それに続いて、基準線上に重畳された一連の量子化正弦波を含み、そしてスタンバイ状態に戻る。
【0043】
[0050] ステップ620において、マイクロコントローラのディジタル出力信号を、平滑化した電流波形に変換する。これは、例えば、図7Aに示すような電圧波形W201を実現するためのディジタル/アナログ変換器にディジタル出力信号を通過させることによって行うことができる。図7A〜図7Eは、それぞれ、図2におけるコンポーネント340、350、360、270、および400の出力に関して測定された場合の、電流または電圧波形例W201、W202、W203、W240、およびW206をそれぞれ示す。原点および時間軸の目盛りは、図7A〜図7Eの各々について実質的に同一である。これらの波形は、信号が通過する経路を示す。即ち、信号は、ディジタル出力から出てアナログ電圧正弦波になり、アナログ電流正弦波になり、発光ダイオード(LED)および位相検出器を経て移相電流正弦波になり、更に移相電圧正弦波になり、そしてオーバーサンプリングのためにアナログ/ディジタル変換器に達する。
【0044】
[0051] 電圧波形W201をロー・パス・フィルタに通過させると、区分的線形波形が平滑化されて、図7Bに示すような電圧可変正弦波W202を得ることができる。次いで、電圧可変正弦波W202を電圧−電流変換器に通過させると、図7Cに示すような電流可変正弦波W203を生成することができる。
【0045】
[0052] ステップ630において、平滑化した電流波形を用いて、放射源を駆動する。即ち、電流可変正弦波W203が放射源を駆動し、放射源は指示薬分子を励起し、これらの指示薬分子からフォトルミネセンスが光電変換器に入射し、これによって変換される。
【0046】
[0053] ステップ640において、例えば、指示薬分子のルミネセンス放射を検出する。即ち、光電変換器が、図7Dに示すような、励起信号電流波形W120を生成する。電流波形W120は、波形W203と同じ正弦波形を有し、位相が遅延しているだけである。この位相遅延φは、ルミネセンス変換の崩壊時間の関数であり、崩壊時間は、指示薬分子が露出される検体の濃度に依存する。
【0047】
[0054] 光電変換器からの電流をバンドパス・トランスインピーダンス増幅器に通過させることができる。このバンドパス・トランスインピーダンス増幅器は、図7Eに示すような、電圧波形W206を発生する。バンドパス利得は、ノイズを濾波するために用いられ、周波数fの信号が通過するときにピークとなる。
【0048】
[0055] ステップ650において、平滑化電流信号と光電変換器出力波形との間における位相差を判定する。電圧波形W202およびW206は、マイクロコントローラのアナログ入力を駆動するために用いることができる。内部では、マイクロコントローラの各アナログ入力がアナログ/ディジタル変換器を駆動する。マイクロコントローラの制御の下で、電圧波形W202およびW206をディジタル的にオーバーサンプリングして、励起信号に関する位相遅延φを導出する。
【0049】
[0056] 内部では、マイクロコントローラ・プログラムの制御の下で、マイクロコントローラは波形W206およびW202の多数の完全な正弦波サイクル上において測定を行う。一実施形態では、マイクロコントローラによってこれらの測定値の平均を取り、放射線源駆動の測定値および指示薬分子からの応答を生成する。これらの測定値を振幅およびDCオフセットについて正規化し、駆動正弦波および応答正弦波を生成する。これら2つの正弦波間における位相差φから、回路の励起に対する応答において、遅延の測定値が求められる。この遅延は、電子遅延および崩壊時間の複合であり、指示薬分子に拘束(bound)された検体濃度の関数となる。例えば、室温および21%O2におけるフォトルミネセンスの崩壊時間は、4.8μsと測定される。
【0050】
[0057] 反復アルゴリズムを用いて、波形W202およびW206からのローカル・オーバーサンプル・データを測定して位相を求める。この反復アルゴリズムは、マイクロコントローラ・プログラムの一部であり、可能性のある連続位相度数(successive degrees of possible phase)にわたって反復する。例えば、信号の位相を形成する(bracket)1対の連続値を特定する。次いで、これら2つの位相を形成する値の間における内挿補間によって、信号の位相を推定する。線形内挿補間以外の方法も用いることができる。例えば、正弦波関数は最終位相値の高精度な推定値を生成することができる。これは、反復アルゴリズムが誤差値または一致基準(match metric)のゼロ交差を決定するからである。このアルゴリズムは、正/負符号変化によって測定されるデータを挟む値間において内挿補間を行う。
【0051】
[0058] 一実施形態では、反復アルゴリムに対する一致基準が、1)入力信号、2)任意の位相遅延刻みを有する一連の値について発生した推定量、および3)1間隔において積分された重み付け関数の積である。一実施形態では、積分間隔が−πからπまでであり、重み付け関数は、推定位相値(estimator phase value)の余弦である。推定位相値は、推定量および重み付け関数の位相角を記述するダミー関数である。重み付け関数は、推定量関数のゼロ交差付近における信号を強調する。これによって、位相測定値の判別を改善しつつ、利得またはフォトルミネセンス振幅におけるノイズおよび変動の影響を低減させる。
【0052】
[0059] 奇数関数であればいずれの基準でも、反復アルゴリズムに対する一致基準として役に立つ。原則的に、nのあらゆる値についての推定位相値のcosn関数であればいずれも、重み付け関数として使うことができる。余弦累乗(cosine power)が高い程、位相判別の信号対ノイズ比が向上する。他の重み付け関数を用いることもできる。
【0053】
[0060] 位相差φは、検知化学薬物(sensor chemistry)(例えば、指示薬分子)にローカルな検体濃度に対する関係を支持する。拡散に帰することができる化学薬品の深さ以内におけるあらゆる空間的分散を無視すると、位相差φは、測定時点におけるある地点での瞬時的検体濃度を表す。測定された位相差φは、先に論じたように、シュテルン−フォルマー関係にしたがって変化する。これは、検知化学薬品の振幅および崩壊時間定数(τ)の双方がこの関係にしたがって変化する基礎的な関係に起因する。
【0054】
[0061] 図7Cに示すような正弦波励起では、崩壊時間定数は直接位相遅延に言い換えられる(translate)。崩壊時間の変動、つまり、位相差φはシュテルン−フォルマー関係によって支配されるのであり、検知化学薬品の検体との反応によって生ずる振幅の損失には依存しない。検知化学薬品(例えば、指示薬分子)から受けた信号振幅が、位相検出アルゴリズムの集束を可能にする程に十分ノイズよりも大きいのであれば、センサ・インターフェース・モジュールは位相測定値を発生する。これは、振幅に基づくセンサに対する格別な利点であり、例えば、振幅に基づく光酸素センサの場合、測定された振幅に対する光酸化および酸素濃度の寄与を分離する必要がある。しかしながら、本発明を具体化するセンサの寿命終了時には、測定毎の変動が増々目立つ(noisy)ようになり、次いでランダムになる。センサ交換警告を示すために、この測定された変動に対して閾値を設定するとよい。
【0055】
[0062] 動作において、外部デバイスからマイクロコントローラに、通信チャネルを通じてコマンドを送って、マイクロコントローラにデータを収集するように命令することができる。次いで、外部デバイスによってデータを引き出すことができる。また、温度測定値を送信することもできる。外部デバイスは、タイミングを測定し、センサ・インターフェース・モジュールと通信し、測定されたデータを表示または使用することができる。
【0056】
[0063] スタンバイの間、放射線源および光電変換器を駆動しない。センサを駆動するための短いプログラム・シーケンスを用いて、センサのデューティ・サイクルを大幅に減少させ、その結果、検知化学薬品の検体との反応性を低下させ、センサの寿命を長持ちさせることができる。
【0057】
[0064] 図8は、本発明の一実施形態による光センサ800を示す。光センサ800は、センサ本体810および基板820を有する。一実施形態では、センサ本体810に指示薬分子830を被覆することができ、またはセンサ本体810を多数の層で構成し、これらの層の1つが指示薬分子830を含有するマトリクス層(図示せず)を備えるようにすることもできる。指示薬分子830は、検体を検知するために所望の環境に露出される(例えば、所望の環境に局限的)。光センサ800は、例えば、豆形または薬品カプセル形で同様のサイズとするとよく、生体内またはその他の現場における配備が可能になる。
【0058】
[0065] 基板820上に実装されているのは、放射線源840、例えば、発光ダイオード(LED)であり、指示薬分子830と相互作用する波長範囲で放射を放出する。例えば、フォトルミネセンスに基づくセンサの場合、指示薬分子830にルミネセンスを発生させる波長を用いるとよい。また、基板820上には、光電変換器850も実装されている。光電変換器850は、例えば、光検出器またはフォトダイオードとするとよい。フォトルミネセンスに基づくセンサという例示的な場合では、光電変換器850は、指示薬分子830によって放出されるフォトルミネセンス光に感応し、これに応答して、指示薬分子830のフォトルミネセンスのレベルを示す信号を発生する。
【0059】
[0066] 放射線源840、光電変換器850、および指示薬分子830は、放射線源840から放出された放射が指示薬分子830に入射し、指示薬分子830からの放射、例えば、フォトルミネセンスが光電変換器850に入射するように、互いに対して位置付けられている。放射の入射は、反射および/または媒体の透過後に生じてもよい。一実施形態では、光学フィルタ860を用いて、光電変換器850に到達する放射を、放射線源840によって放出された放射に対する指示薬分子の応答と関連のある波長に限定することができる。
【0060】
[0067] また、光センサ800は、当該光センサ800に限られた温度を測定するための温度プローブ870、放射線源840に送信する信号を発生し、光電変換器850から信号を受信するセンサ・インターフェース・モジュール(SIM)880、外部システム(図示せず)とワイヤレスで通信する送信機890、および電源900も含むことができる。電源900は、指示薬(indicator)を含むことができ、電源900をしかるべき電磁場に露出させることによって、指示薬から電流を誘発することができる。本発明にしたがって用いることができる酸素センサの例が、米国特許第5,517,313号および第6,940,590号に記載されている。これらの特許をここで引用したことにより、その内容全体が本願にも含まれるものとする。
【0061】
[0068] 一実施形態によれば、構成パラメータに基づいて、測定された位相差を補正することによって、検体濃度測定の精度を高めることができる。1つの較正ステップは、電子遅延、またはオフセット・ヌル構成パラメータ(offset null configuration parameter)を判定することである。オフセット・ヌルによって、主に電子コンポーネントの許容度による、ユニット毎のばらつきを解消する。オフセット・ヌルの判定は、光センサの製造時またはセンサの構成設定中に、固定温度および検体濃度で行うことができる。
【0062】
[0069] 別の較正ステップでは、既知の検体濃度および種々の温度において位相差を測定し、相対湿度および圧力のような他のセンサ環境素因を既知の値に固定する。この較正ステップでは、位相差を先に論じたように判定し、実際の検体濃度の値を最も普遍的な法則から導出するか、または経験的に測定することができる。実際には、特に高い精度を要求する用途においては、これらの手法をどのように組み合わせてもよい。較正は、個々のデバイスについて、または特定のSIM/センサ・アーキテクチャについて行うことができ、あるいは他の基準で行ってもよい。
【0063】
[0070] 位相差対検体濃度/温度の関係は、用途によっては厳密には線形にはならないこともあるので、これら2つの較正設定ステップに基づく伝達関数を求める。この伝達関数の一部を含む、オフセット・ヌルおよび温度双方の補正表を、マイクロコントローラ外部の表に入れること、またはセンサ・インターフェース・モジュール上にあるメモリに記憶されている表にロードすることができる。高い精度を要求する用途については、追加の較正ステップにおいて、圧力および湿度というような他の湿度入力変数を考慮することもでき、伝達関数はこれらの変数も含む。
【0064】
[0071] 本明細書において記載したセンサは、酸素センサに限定されるのではない。例えば、バッテリ給電式、代謝(metabolic)および大気(atmospheric)センサを用いることもできる。また、本発明によるセンサを人に埋め込み、人体における種々の生物的検体(例えば、酸素、二酸化炭素、グルコース、毒物)を測定するために用いることもできる。加えて、本明細書において記載した発明は、種々の用途および動作環境において用いることができる。例えば、本発明は、ガス混合、不活性化、溶融酸素、環境変化率(environmental rate-of-change)、生物化学的酸素要求量(BOD)、反応モニタ、加熱/換気/空調(HVAC)システム、燃焼監視、ならびに発酵供給およびオフ・ガス監視(fermentation feed and off gas monitors)と共に用いることもできる。
【0065】
[0072] 本発明の一実施形態によるセンサおよびセンサ・インターフェース・モジュール(SIM)を生物化学的酸素要求(BOD)用途においてどのように用いることができるかについて、その一例は排水監視に関する。自然水路または工業的排水の中にある酸化可能素材は、生物化学的(バクテリア)プロセスまたは化学的プロセスの双方によって酸化される。その結果、水の酸素含有量が減少する。基本的に、生物化学的酸化に対する反応は次のように記述することができる。
【0066】
酸化可能素材+バクテリア+栄養分+O2 → CO2+H2O+NO3またはSO4のような酸化された無機物
[0073] この式では、バクテリアおよび酸素が左側にあり、この式から酸素濃度の変化を監視することにより、存在するバクテリアに直接比例するこの反応全体の速度が効果的に監視される。
【0067】
[0074] 全ての自然水路はバクテリアおよび栄養分を含むので、殆どあらゆる廃物混合物がこのような水路に流入すると、(先に示した反応のような)バクテリア反応を開始する。これらのバクテリア反応により、生物化学的酸素要求量(BOD)として測定されるものが生ずる。
【0068】
[0075] 排水において最も共通して測定される構成成分の1つが、生物化学的酸素要求量である。排水は、種々の無機および有機物質で構成される。有機物質とは、炭素に基づき、例えば、糞便や、洗剤、石鹸、脂肪、グリス等を含む分子のことを指す。これらの大きな有機分子は、バクテリアによって容易に分解される。しかしながら、大きな分子をそれよりも小さな分子に分解し、最終的に二酸化炭素および水に分解するプロセスには酸素が必要となる。このプロセスに必要とされる酸素量は、生物化学的酸素要求量(BOD)として知られている。一例では、5日BOD即ちBOD5が、5日間の間に微小有機物によって消費された酸素量によって測定され、これは、汚水における生物分解性有機物の量、または汚水の強度の最も共通な尺度となる。
【0069】
[0076] BODは、従来の汚水処理プラントから地表水または水流に放出される廃水の強度を測定するために従前から用いられている。これは、BODが高い汚水は、受け取る水における酸素を枯渇させ、魚類の殺生および生態系の変化を発生させる虞れがあるからである。非限定的な一例では、地表水放出に対する規準に基づいて、BODに対する二次処理規格が、30mg BOD/L(即ち、廃水を分解するために5日間で30mgのO2が水1リットル毎に消費される。)に設定されている。
【0070】
[0077] 生物化学的酸素要求量(BOD)用途の一例では、本明細書において記載したセンサおよびセンサ・インターフェース・モジュール(SIM)を、排水または他の媒体に対して適した位置に置き、例えば、酸素濃度変化を監視するためというような、所望の測定を行うことができる。
【0071】
[0078] 本発明によるセンサおよびセンサ・インターフェース・モジュール(SIM)は、温度を測定するために用いることもできる。例えば、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩を指示薬分子として用い、プラスチックまたはガラスのような材料の中に埋め込むこと、あるいは全体的に酸素不浸透性の金属筐体内に入れられた総合センサ(sensor overall)の中に埋め込むことができる。指示薬分子が照射され、ルミネセンスを発生させる。一定の酸素濃度では、ルミネセンスは時間の関数として変化し(即ち、温度、温度が低い程ルミナンスは大きくなり、温度が高い程小さくなる)、センサによって検出される。温度は、SIMからのルミネセンスまたは位相変化に基づいて判定することができる。
【0072】
[0079] 以上本発明の種々の実施形態および変形について説明したが、これらは、限定ではなく一例として紹介したに過ぎないことは言うまでもない。つまり、本発明の広さおよび範囲は、これまでに記載した実施形態例のいずれによっても限定されることはなく、以下の特許請求の範囲およびその同等物のみにしたがって定められてしかるべきである。
【技術分野】
【0001】
関連出願に対する相互引用
[0001] 本願は、2008年7月28日に出願された米国仮特許出願第61/084,100号の優先権を主張する。この特許出願をここで引用したことにより、その内容全体が本願にも含まれるものとする。
【0002】
[0002] 発明の分野
[0003] 本発明は、検体濃度の測定システムおよび方法に関する。更に特定すれば、本発明は位相に基づくプロトコル(phase-based protocol)を用いて検体濃度の測定を可能にする微小センサおよびセンサ・インターフェース・モジュールに関する。
【従来技術】
【0003】
[0004] 関連技術の解説
[0005] 放射線源による光センサの励起に基づいて、この光センサの発光特性を測定するために、フォトルミネセンス検知が用いられている。フォトルミネセンス検知は、例えば、蛍光物質のフォトルミネセンス寿命、検体の濃度、フォトルミネセンス強度、またはその他の化学的パラメータを測定するために用いることができる。フォトルミネセンス検知を用いてこれらのパラメータを検出するデバイスは、通例、振幅に基づくプロトコル、時間に基づくプロトコル、または位相に基づくプロトコルを用いて、所望のパラメータを求める。
【0004】
[0006] このようなデバイスは、通例、かさばり、高価であり、しかも輸送が容易でない。これらのデバイスは、約10,000米ドルの価格になることもあり、ほぼ大型画面の陰極線管テレビジョンのサイズであることもあり、多数の機器を含むこともある。これらのデバイスの中には携帯用として市販されているものもあるが、通例、これらのデバイスを種々の場所に輸送するためには、棚が2つある研究室用カート(two-shelf lab cart)のような移動機器が必要となる。これは、少なくとも部分的に、高価な回路および複雑なデータ処理のためであり、所望の結果を得るために、これらを有為なノウハウと組み合わせる必要がある。加えて、これらのデバイスは、通例、動作するために大量の電力を必要とする。
【0005】
[0007] 現在のシステムには、これらおよびその他の欠点がある。
【発明の概要】
【発明が解決しようとする課題】
【0006】
[0008] 本発明は、検体の濃度を測定するデバイスおよび方法に関する。更に特定すれば、本発明は、センサ、およびこのセンサと通信して媒体における検体の濃度を測定するセンサ・インターフェース・モジュール(SIM)に関する。これらのセンサおよびSIMは、例えば、生物化学酸素要求量、不活性化(inerting)、燃焼、環境、化学、ダイビング/生命支援(diving/life support)、ならびに麻酔学、呼吸、および酸素濃度計のような医療用途というような、種々の気体環境において用いることができる。また、これらのセンサおよびSIMは、例えば、生物化学酸素要求量、埋め込み可能センサ、魚類養殖(fish farming)、水族館、汚染監視、化学的処理、および醸造/醗酵というような、種々の液内環境においても用いることができる。これらの用途の各々は、例えば、酸素、グルコース、二酸化炭素、毒物、温度というような種々の検体の濃度を、例えば、空気、血液、水、あるいはその他の気体または液体媒体というような媒体内において判定するために用いることができる。
【課題を解決するための手段】
【0007】
[0009] 一実施形態によれば、本発明は、光センサおよびセンサ・インターフェース・モジュール(SIM)を含む。このセンサは、放射源、光電変換器、および指示薬分子(indicator molecule)を含む。センサ・インターフェース・モジュールは、センサと通信して放射源を駆動し、センサによって得られたデータを受け取るマイクロコントローラを含む。このマイクロコントローラは、放射源に指示薬分子を照射させる。指示薬分子は、放射源によって放出される光のためにルミネセンスを発し、媒体内に存在する検体に基づいてある種の特性を呈する。センサは、このルミネセンスに関するデータを、処理のために、マイクロコントローラに送信する。受信したデータ、既知のデータ、およびシュテルン−フォルマーの関係に基づいて、マイクロコントローラは検体の濃度を判定する。本発明の一実施形態によれば、センサ・インターフェース・モジュールは、データをシステム・ユーザに提示することができるように、このモジュールがデータを外部データ・システムに送信することを可能にするインターフェースを含む。
【0008】
[0010] 一態様において、本発明は、マイクロコントローラを有する、検体濃度測定デバイスを提供する。マイクロコントローラは、所定の周波数の周期的ディジタル信号を当該マイクロコントローラのディジタル出力バス上に出力し、マイクロコントローラのアナログ入力上にある刺激波形と応答波形との間における位相差を計算するように構成されている。
【0009】
[0011] また、このデバイスは、周期的ディジタル信号を周期的電圧波形に変換するディジタル/アナログ変換器と、周期的電圧波形を平滑化し、刺激波形を出力するロー・パス・フィルタと、刺激波形を周期的電流波形に変換し、放射源を駆動するように動作可能な電圧/電流変換器であって、放射源が指示薬分子上に放射する、電圧/電流変換器とを含む。
【0010】
[0012] 更に、このデバイスは、光電変換器からの電流を応答電圧波形に変換するように動作可能なバンドパス・トランスインピーダンス増幅器も含む。指示薬分子からの放射が光電変換器に入射し、位相差が、指示薬分子に局限的な検体濃度の関数である。
【0011】
[0013] 本発明の一実施形態によれば、媒体内にある検体の濃度を測定する方法を提供する。この方法は、複数の指示薬分子が供給されるセンサを用いる。指示薬分子は、特定の検体がある場合に、所定の特性を呈する。センサは、励起源を駆動するために用いられる刺激波形を発生する。
【0012】
[0014] 指示薬分子は、用いられるセンサの種類に基づいて、励起源によって励起され、濃度判定が望まれる検体と関連のある特性を呈する。呈された特性に対する応答波形が、その特性の表現として発生される。刺激波形および応答波形をオーバーサンプリングし、検体の濃度に依存する位相遅延を判定する。次いで、判定した位相遅延およびシュテルン−フォルマー(Stern-Volmer)関係を用いて、検体濃度を判定することができる。
【0013】
[0015] 本発明の別の実施形態によれば、検体濃度判定方法は、マイクロコントローラの出力上に周期的ディジタル出力信号を発生するステップを含む。この周期的ディジタル出力信号を平滑化駆動電流波形に変換する。この平滑化駆動電流波形は、周期的ディジタル出力信号と同じ周波数である。
【0014】
[0016] また、この方法は、平滑化駆動電流によって放射源を駆動するステップであって、放射源からの放射が指示薬分子に入射する、ステップと、光電変換器によって、指示薬分子の放射励起エネルギを検出するステップであって、この光電変換器が、平滑化駆動電流波形と同じ周波数の波形を出力する、ステップと、平滑化駆動電流波形と出力された光電変換器波形との間における位相差を測定するステップとを含む。位相差は、指示薬分子に局限的な検体濃度と相関がある。
【0015】
[0017] 本発明の上述のおよびその他の特徴ならびに利点、更には本発明の好ましい実施形態の構造および動作について、添付図面を参照しながら以下に詳細に説明する。
【図面の簡単な説明】
【0016】
[0018] 添付図面は、本明細書に組み込まれその一部をなすが、本発明の種々の実施形態を図示し、更に説明と共に、本発明の原理を説明し、当業者が本発明を行い使用することを可能にする役割を果たす。
【図1】図1は、本発明の一実施形態による検体濃度測定システムの模式図である。
【図2】図2は、本発明の一実施形態によるセンサ・インターフェース・モジュールの模式図である。
【図3】図3は、本発明の一実施形態によるフォトルミネセンス型センサの上面図である。
【図4】図4は、本発明の一実施形態によるフォトルミネセンス型センサの断面図である。
【図5】図5は、本発明の一実施形態による検体濃度測定方法を示すフローチャートである。
【図6】図6は、本発明の一実施形態による検体濃度測定方法を示すフローチャートである。
【図7】図7A〜図7Eは、本発明の一実施形態にしたがって検体濃度を測定するために用いられるデバイスの回路における所定の地点に現れる波形例を示す。
【図8】図8は、本発明の一実施形態によるフォトルミネセンスに基づくセンサの図である。
【発明を実施するための形態】
【0017】
[0026] 一実施形態によれば、本発明は検体濃度測定システムおよび方法に関する。このシステムおよび方法は、光センサおよびセンサ・インターフェース・モジュール(SIM)を用いて、フォトルミネセンスを用いて検体の濃度を測定する。これらのセンサおよびSIMは、当該センサおよびSIMが非常に小型で携帯用となることを可能にするように、フォトルミネセンス情報を伝達し処理する。実施形態によっては、これらのセンサおよびSIMが人の掌に納まる程度の大きさとなり、更に小型化することも可能である。
【0018】
[0027] 図1は、本発明の一実施形態による検体濃度測定デバイス100の模式図である。デバイス100は、検体源110、センサ120、センサ・インターフェース・モジュール(SIM)130、およびデータ・システム140を含む。検体源110は、例えば、濃度測定が望まれる検体を含む媒体とすることができる。この媒体は、例えば、空気、血液、水、あるいはその他の気体媒体または液体媒体とすることができる。センサ120は、好ましくは、光センサであり、蛍光指示薬分子(以下で更に詳しく説明する)を用いて、媒体内における、例えば、酸素、グルコース、および毒物というような検体の濃度測定を可能にする。本発明の一実施形態によれば、センサ120は、いずれかの既知の有線またはワイヤレス接続を用いて、SIM130と通信することができる。センサ120は、SIM130と通信して、例えば、気体媒体、またはセンサ120が埋め込まれている被験者の血液における酸素濃度を測定することができる。データ・システム140は、例えば、データ収集システム、マイクロプロセッサ、またはマイクロコンピュータとすることができる。
【0019】
[0028] センサ120は、好ましくは、放射線源(radiation source)150と変換器160とを含む。一実施形態によれば、放射線源150は、検体を含有する媒体を照射する発光ダイオード(LED)を含む。センサ120は、マイクロコントローラ170から放射線源150を制御する命令を得て、得られたデータを処理のためにマイクロコントローラ170に送信する。センサ120は、インターフェース180を用いて、SIM130と通信する。変換器160は、センサ120が受信したアナログ情報を、マイクロコントローラ170によって処理されるデータに変換する。
【0020】
[0029] 本発明の一実施形態によれば、センサ120およびSIM130は、回路ボード190上に設けることができる。回路ボード190は、検査、較正、およびその他の機能をデバイス100が実行することを可能にする。回路ボード190は、SIM130とデータ・システム140との間において通信を可能にするインターフェース200を含む。SIM130は、データ・システム140と通信して、センサ120およびSIM130によって得られたまたは発生した読み取り値、測定値、またはその他のデータを、データ・システム140によって処理、表示、または格納することを可能にすることができる。
【0021】
[0030] 先に論じたように、センサ120およびSIM130は、好ましくは、人の掌に納まるサイズであり、更に小型化することもできる。非限定的な一実施形態によれば、SIM130は、約0.34立方インチ以下の空間を占有し、センサ120は、0.009立方インチ以下の空間を占有し、約1から200ミリアンペアの範囲で直流(DC)二乗平均(RMS)電力を消費し、約100ミリ秒(ms)以下の検体濃度変化に応答し、真空レベルから平方インチ当たり数千ポンド(psi)の範囲の周囲圧力において動作する。
【0022】
[0031] 図2は、本発明の一実施形態による検体濃度測定デバイス220の模式図である。デバイス220は、センサ230およびセンサ・インターフェース・モジュール(SIM)240を含む。センサ230は、濃度測定が望まれる検体を含有する媒体内に設けられる。センサ230およびSIM240は、検体濃度を判定するために用いられるデータに関して、互いに通信する。センサ230は、放射線源250、変換器260、および指示薬分子270を含み、以下で更に詳しく説明する。
【0023】
[0032] センサ・インターフェース・モジュール(SIM)240はマイクロコントローラ280を含む。マイクロコントローラ280は、指示薬分子270にルミネセンスを発生させる放射線源250を駆動するために用いられる励起信号を発生する。本発明の一実施形態によれば、指示薬分子270は、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩(complex tris(4,7-diphenyl-1, 10-phenanthroline) ruthenium(II) perchlorate)、ユーロピウムまたはテルビウム・コンプレックスのようなランタニド系指示薬、芳香族炭化水素、あるいは位相変調によって測定するときに検出可能な差が得られる程に十分長いルミネセンス寿命を有する検体に相応しい指示薬または分子伝達系であればいずれでもよい。検体の例には、酸素、二酸化炭素、グルコース、および温度が含まれるが、これらに限定されるものではない。
【0024】
[0033] 放射線源250は、用いられる指示薬の種類に応じて異なってもよい。例えば、指示薬がコンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩である場合、その崩壊時間は約4ミリ秒であり、青色発光ダイオード(LED)を用いることができる。これは、青色LEDからの発光が、約460ナノメートルにピーク波長を有し、これがコンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩の光学励起スペクトルと良く一致するからである。緑色および赤色LEDのようなその他のLED、またはその他の放射線源も用いることができる。一般に、好ましい放射線源またはLEDは、指示薬の光学励起スペクトルと一致するピーク発光を有する。ランタニド指示薬を用いる場合、約360〜380ナノメートルにピーク発光波長を有する紫色LEDを用いるとよい。ランタニド系指示薬の例については、米国特許第6,344,360号に記載されている。この特許をここで引用したことにより、その内容全体が本願にも含まれるものとする。指示薬分子の更に別の例が、米国特許第5,517,313号に記載されており、この特許もここで引用したことにより、その内容全体が本願にも含まれるものとする。
【0025】
[0034] 励起信号は、マイクロコントローラ280によって処理されるパラメータに基づいて発生する。励起信号は、測定対象検体が呈する既知の特性に基づく。これによって、基準信号が供給され、この基準信号と測定信号を比較することができる(以下で更に詳しく説明する)。一実施形態によれば、マイクロコントローラ280は、ディジタル出力チャネル290と1つ以上のアナログ入力チャネル300とを有するように構成されている。ディジタル出力チャネル290は、センサ230の放射線源250に励起信号を送信するために用いることができる。アナログ入力チャネル300は、センサ230の変換器260によって送信された信号を受信するために用いることができる。Microchip Technology Inc.(マイクロチップ・テクノロジ社)からのPIC24ファミリーの中にあるマイクロコントローラ、または他の互換性のあるマイクロコントローラというようなマイクロコントローラを、マイクロコントローラ280として用いることができる。本発明の一実施形態によれば、マイクロコントローラ280はディジタル信号プロセッサを含む。
【0026】
[0035] センサ・インターフェース・モジュール(SIM)240は、更に、マイクロコントローラ280のディジタル出力チャネル290を用いて送信された信号をアナログ電圧に変換するためのディジタル/アナログ変換器(DAC)310も含む。一実施形態では、マイクロコントローラ280のディジタル出力チャネル290は、ビット0...ビット3を有する4ビット・バスであり、ディジタル/アナログ変換器310は単純な抵抗器ラダー(ladder)である。非限定的な実施形態の一例では、ディジタル/アナログ変換器310は、ビット3に接続されている111kΩ抵抗器、ビット2に接続されている270kΩ抵抗器、ビット1に接続されている400kΩ抵抗器、およびビット0に接続されている800kΩ抵抗器を含む。ディジタル/アナログ変換器310の出力は、各抵抗器のリード(マイクロコントローラとは反対側のノード)が接続されているノードである。当業者に知られている他の抵抗器ラダーおよびネットワークも、ディジタル/アナログ変換器310として用いることができる。更に、ディジタル/アナログ変換器310を集積回路上に実装することもできる。
【0027】
[0036] 更に、センサ・インターフェース・モジュール(SIM)240はロー・パス・フィルタ320も備えている。ロー・パス・フィルタ320は、ディジタル/アナログ変換器310からの電圧波形出力を、電圧波形出力の正弦波近似に変換する。ロー・パス・フィルタ320は、当業者には周知の抵抗器−キャパシタ(RC)設計とするとよい。例示的な一実施形態では、抵抗(R)および容量(C)は、周波数f、例えば、10kHzの信号を通過させ、それよりも高い周波数のノイズ源を全て抑制するように選択される。ロー・パス・フィルタ320の電圧波形出力は、マイクロコントローラ280のアナログ入力300に送信される。ロー・パス・フィルタ320は、可変容量キャパシタを含むこともできる。本発明の非限定的な一実施形態によれば、このロー・パス・フィルタを形成するキャパシタおよび抵抗器は、それぞれ、約470pFおよび15kΩの値を有するとよい。
【0028】
[0037] 更に、センサ・インターフェース・モジュール(SIM)240は、電圧−電流変換器330を含む。一実施形態では、電圧−電流変換器330は、その入力、即ち、ロー・パス・フィルタ320の電圧波形出力の正弦波近似を、入力電圧に比例する電流に変換する。電圧−電流変換器330の出力は、放射線源250を駆動する励起信号を含む。放射線源250は、その放射出力が指示薬分子270に到達するように位置付けられている。放射線源250によって放出された光が、指示薬分子270に、測定対象検体の存在に基づく特定の態様でルミネセンスを発生させる。このルミネセンスが、変換器260によって信号として検出される。変換器260は、指示薬分子270から照射するルミネセンスの関数となる信号を出力する。変換器260は、例えば、フォトダイオード、フォトトランジスタ、光電子増倍管、またはその他の光検出器とすることができる。
【0029】
[0038] 電圧−電流変換器330は、オプションとして、発光ダイオード(LED)340を駆動するために、放射線源250を駆動する電流を忠実に再現する(mirror)、カレント・ミラーと通信状態にあってもよい。一実施形態では、LED340は、センサ・インターフェース・モジュール(SIM)240を検査するために用いることができる赤色LEDである。
【0030】
[0039] 変換器260の出力は、バンドパス・トランスインピーダンス増幅器350に接続されている。バンドパス・トランスインピーダンス増幅器350は、バンドパス利得応答を含み、その電流入力の関数となる電圧波形を発生する。バンドパス・トランスインピーダンス増幅器350の出力は、マイクロコントローラ280のアナログ入力300に送信される。
【0031】
[0040] また、デバイス220は通信インターフェース360も含むことができる。通信インターフェース360は、マイクロコントローラ280が検体濃度に関するデータを外部データ・システム370に対して送信および受信することを可能にする。マイクロコントローラ280およびデータ・システム370は、例えば、マイクロコントローラ・シリアル・チャネルのような、通信チャネル380を通じて通信することができる。データ・システム370は、例えば、データ収集システム、マイクロプロセッサ、マイクロコンピュータ、またはその他のデバイスとすることができる。
【0032】
[0041] マイクロコントローラ280は、例えば、格納されているプログラムを用いて、その通信チャネル380を通じて送信されたコマンド・コードを受信しそれに対して動作し、周期的に変化するディジタル出力、サンプル電圧をアナログ入力上に発生し、検体濃度に関するデータを計算し通信チャネル380を通じて送信するように構成されている。センサ・インターフェース・モジュール(SIM)240は、1つの測定値を取り込むように、または指定された遅延の後、連続的な反復測定値を流す(run)ように設定することができる。
【0033】
[0042] 図3および図4は、それぞれ、本発明の一実施形態によるセンサ400の平面図および断面図である。センサ400は、例えば、光センサとすることができる。センサ400は、放射源430に合わせたウェル420、および光電変換器450に合わせたウェル440とが形成された基板410を含む。放射源430は、例えば、発光ダイオード(LED)とすることができ、変換器450は、例えば、光電変換器、フォトダイオード、またはその他の変換器とすることができる。利点の中でもとりわけ、この構成は、放射源430による変換器450の直接照明を減少させる。
【0034】
[0043] 更に、センサ400は、センサ400の透過および反射特性を最適化する導波路460を含むことができる。一実施形態では、指示薬分子470は、導波路460の上面の少なくとも一部に配置されている。センサ・インターフェース・モジュール(SIM)480が、放射源430および変換器450に近接して位置付けられている。通信チャネル490が、センサ400を外部データ・システム(図2に示す)と接続することができる。他の実施形態では、センサ400は外部データ・システムとワイヤレスで通信する。
【0035】
[0044] 図5は、本発明の一実施形態による検体濃度測定方法を示す。この方法は、検体の特定の特性を判定するために用いられるセンサの種類を選択するステップ510を含む。例えば、被験者の血液における酸素濃度を検知するために、光センサを用いることができる。
【0036】
[0045] ステップ520において、指示薬分子をセンサ上に供給する。指示薬分子は、好ましくは、センサによる検出が可能な検体特性に反応する。例えば、放射線源は、指示薬分子のルミネセンスが光センサによって検出されるように、指示薬分子を励起するために用いることができる。例えば、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩指示薬分子を励起するためには、青色発光ダイオード(LED)を用いることができる。
【0037】
[0046] ステップ530において、濃度測定が望まれる検体の種類に基づいて、刺激波形を発生する。光センサを用いる場合、例えば、これは、刺激波形を用いてLEDに所定の形態を有する放射を放出することを指令することを含むとよい。ステップ540において、このセンサによって特定の特性を検出することができるデバイスを用いて指示薬分子を励起する。例えば、光センサが用いられている場合、このデバイスは放射線源とするとよい。
【0038】
[0047] 次いで、センサは、ステップ550において、指示薬分子によって励起された特性を検出する。光センサおよび放射線源を用いる場合、光センサは、指示薬分子によって放出されるフォトルミネセンス放射を検出する。このフォトルミネセンス放射は、センサのフィルタによって受け取られ、センサのフォトダイオードによって変換される。ステップ560において、受け取られた指示薬分子の特性、例えば、指示薬分子から受け取られたフォトルミネセンス放射の特性に基づいて、応答波形を発生する。光センサの例では、フォトダイオードからの電流は、刺激波形のそれと同じ形態となり、位相が遅延するだけである。
【0039】
[0048] 次に、ステップ570において、刺激波形と応答波形との間における位相遅延をステップ580において判定できるように、発生した刺激波形および応答波形をオーバーサンプリングする。ステップ590において、この位相遅延を用いて、検体濃度を判定することができる。これは、位相遅延が検体濃度に比例するからである。即ち、蛍光を発する分子は、放射線刺激の除去後、既知の時間期間、つまり、崩壊時間または励起状態寿命の間蛍光を発する。蛍光の強度および崩壊時間の双方は、所与の蛍光消光剤の濃度との線形関係にしたがって変化する。非限定的な一例では、対象の検体の濃度は、シュテルン−フォルマーの式に記述される関係に基づいて、位相遅延から判定することができる。
【0040】
【数1】

【0041】
ここで、τは崩壊時間、Iは消光剤Qの存在下における蛍光の強度、τ0は崩壊時間、そしてI0は消光剤Qがない場合の蛍光の強度、Ksvはシュテルン−フォルマー消光定数、[Q]は消光剤Qの濃度である。つまり、τを測定することができれば、Qの濃度は、例えば、シュテルン−フォルマーの式によって判定することができる。
【0042】
[0049] 図6は、本発明の一実施形態による検体濃度測定方法を示す。ステップ610において、マイクロコントローラのディジタル出力バス上に周期的なディジタル出力信号を発生する。例えば、マイクロコントローラは、周波数fを有する量子化した正弦波を表す一連のディジタル出力信号を発生することができる。この一連の出力は、DC基準線値までの上昇勾配を含み、それに続いて、基準線上に重畳された一連の量子化正弦波を含み、そしてスタンバイ状態に戻る。
【0043】
[0050] ステップ620において、マイクロコントローラのディジタル出力信号を、平滑化した電流波形に変換する。これは、例えば、図7Aに示すような電圧波形W201を実現するためのディジタル/アナログ変換器にディジタル出力信号を通過させることによって行うことができる。図7A〜図7Eは、それぞれ、図2におけるコンポーネント340、350、360、270、および400の出力に関して測定された場合の、電流または電圧波形例W201、W202、W203、W240、およびW206をそれぞれ示す。原点および時間軸の目盛りは、図7A〜図7Eの各々について実質的に同一である。これらの波形は、信号が通過する経路を示す。即ち、信号は、ディジタル出力から出てアナログ電圧正弦波になり、アナログ電流正弦波になり、発光ダイオード(LED)および位相検出器を経て移相電流正弦波になり、更に移相電圧正弦波になり、そしてオーバーサンプリングのためにアナログ/ディジタル変換器に達する。
【0044】
[0051] 電圧波形W201をロー・パス・フィルタに通過させると、区分的線形波形が平滑化されて、図7Bに示すような電圧可変正弦波W202を得ることができる。次いで、電圧可変正弦波W202を電圧−電流変換器に通過させると、図7Cに示すような電流可変正弦波W203を生成することができる。
【0045】
[0052] ステップ630において、平滑化した電流波形を用いて、放射源を駆動する。即ち、電流可変正弦波W203が放射源を駆動し、放射源は指示薬分子を励起し、これらの指示薬分子からフォトルミネセンスが光電変換器に入射し、これによって変換される。
【0046】
[0053] ステップ640において、例えば、指示薬分子のルミネセンス放射を検出する。即ち、光電変換器が、図7Dに示すような、励起信号電流波形W120を生成する。電流波形W120は、波形W203と同じ正弦波形を有し、位相が遅延しているだけである。この位相遅延φは、ルミネセンス変換の崩壊時間の関数であり、崩壊時間は、指示薬分子が露出される検体の濃度に依存する。
【0047】
[0054] 光電変換器からの電流をバンドパス・トランスインピーダンス増幅器に通過させることができる。このバンドパス・トランスインピーダンス増幅器は、図7Eに示すような、電圧波形W206を発生する。バンドパス利得は、ノイズを濾波するために用いられ、周波数fの信号が通過するときにピークとなる。
【0048】
[0055] ステップ650において、平滑化電流信号と光電変換器出力波形との間における位相差を判定する。電圧波形W202およびW206は、マイクロコントローラのアナログ入力を駆動するために用いることができる。内部では、マイクロコントローラの各アナログ入力がアナログ/ディジタル変換器を駆動する。マイクロコントローラの制御の下で、電圧波形W202およびW206をディジタル的にオーバーサンプリングして、励起信号に関する位相遅延φを導出する。
【0049】
[0056] 内部では、マイクロコントローラ・プログラムの制御の下で、マイクロコントローラは波形W206およびW202の多数の完全な正弦波サイクル上において測定を行う。一実施形態では、マイクロコントローラによってこれらの測定値の平均を取り、放射線源駆動の測定値および指示薬分子からの応答を生成する。これらの測定値を振幅およびDCオフセットについて正規化し、駆動正弦波および応答正弦波を生成する。これら2つの正弦波間における位相差φから、回路の励起に対する応答において、遅延の測定値が求められる。この遅延は、電子遅延および崩壊時間の複合であり、指示薬分子に拘束(bound)された検体濃度の関数となる。例えば、室温および21%O2におけるフォトルミネセンスの崩壊時間は、4.8μsと測定される。
【0050】
[0057] 反復アルゴリズムを用いて、波形W202およびW206からのローカル・オーバーサンプル・データを測定して位相を求める。この反復アルゴリズムは、マイクロコントローラ・プログラムの一部であり、可能性のある連続位相度数(successive degrees of possible phase)にわたって反復する。例えば、信号の位相を形成する(bracket)1対の連続値を特定する。次いで、これら2つの位相を形成する値の間における内挿補間によって、信号の位相を推定する。線形内挿補間以外の方法も用いることができる。例えば、正弦波関数は最終位相値の高精度な推定値を生成することができる。これは、反復アルゴリズムが誤差値または一致基準(match metric)のゼロ交差を決定するからである。このアルゴリズムは、正/負符号変化によって測定されるデータを挟む値間において内挿補間を行う。
【0051】
[0058] 一実施形態では、反復アルゴリムに対する一致基準が、1)入力信号、2)任意の位相遅延刻みを有する一連の値について発生した推定量、および3)1間隔において積分された重み付け関数の積である。一実施形態では、積分間隔が−πからπまでであり、重み付け関数は、推定位相値(estimator phase value)の余弦である。推定位相値は、推定量および重み付け関数の位相角を記述するダミー関数である。重み付け関数は、推定量関数のゼロ交差付近における信号を強調する。これによって、位相測定値の判別を改善しつつ、利得またはフォトルミネセンス振幅におけるノイズおよび変動の影響を低減させる。
【0052】
[0059] 奇数関数であればいずれの基準でも、反復アルゴリズムに対する一致基準として役に立つ。原則的に、nのあらゆる値についての推定位相値のcosn関数であればいずれも、重み付け関数として使うことができる。余弦累乗(cosine power)が高い程、位相判別の信号対ノイズ比が向上する。他の重み付け関数を用いることもできる。
【0053】
[0060] 位相差φは、検知化学薬物(sensor chemistry)(例えば、指示薬分子)にローカルな検体濃度に対する関係を支持する。拡散に帰することができる化学薬品の深さ以内におけるあらゆる空間的分散を無視すると、位相差φは、測定時点におけるある地点での瞬時的検体濃度を表す。測定された位相差φは、先に論じたように、シュテルン−フォルマー関係にしたがって変化する。これは、検知化学薬品の振幅および崩壊時間定数(τ)の双方がこの関係にしたがって変化する基礎的な関係に起因する。
【0054】
[0061] 図7Cに示すような正弦波励起では、崩壊時間定数は直接位相遅延に言い換えられる(translate)。崩壊時間の変動、つまり、位相差φはシュテルン−フォルマー関係によって支配されるのであり、検知化学薬品の検体との反応によって生ずる振幅の損失には依存しない。検知化学薬品(例えば、指示薬分子)から受けた信号振幅が、位相検出アルゴリズムの集束を可能にする程に十分ノイズよりも大きいのであれば、センサ・インターフェース・モジュールは位相測定値を発生する。これは、振幅に基づくセンサに対する格別な利点であり、例えば、振幅に基づく光酸素センサの場合、測定された振幅に対する光酸化および酸素濃度の寄与を分離する必要がある。しかしながら、本発明を具体化するセンサの寿命終了時には、測定毎の変動が増々目立つ(noisy)ようになり、次いでランダムになる。センサ交換警告を示すために、この測定された変動に対して閾値を設定するとよい。
【0055】
[0062] 動作において、外部デバイスからマイクロコントローラに、通信チャネルを通じてコマンドを送って、マイクロコントローラにデータを収集するように命令することができる。次いで、外部デバイスによってデータを引き出すことができる。また、温度測定値を送信することもできる。外部デバイスは、タイミングを測定し、センサ・インターフェース・モジュールと通信し、測定されたデータを表示または使用することができる。
【0056】
[0063] スタンバイの間、放射線源および光電変換器を駆動しない。センサを駆動するための短いプログラム・シーケンスを用いて、センサのデューティ・サイクルを大幅に減少させ、その結果、検知化学薬品の検体との反応性を低下させ、センサの寿命を長持ちさせることができる。
【0057】
[0064] 図8は、本発明の一実施形態による光センサ800を示す。光センサ800は、センサ本体810および基板820を有する。一実施形態では、センサ本体810に指示薬分子830を被覆することができ、またはセンサ本体810を多数の層で構成し、これらの層の1つが指示薬分子830を含有するマトリクス層(図示せず)を備えるようにすることもできる。指示薬分子830は、検体を検知するために所望の環境に露出される(例えば、所望の環境に局限的)。光センサ800は、例えば、豆形または薬品カプセル形で同様のサイズとするとよく、生体内またはその他の現場における配備が可能になる。
【0058】
[0065] 基板820上に実装されているのは、放射線源840、例えば、発光ダイオード(LED)であり、指示薬分子830と相互作用する波長範囲で放射を放出する。例えば、フォトルミネセンスに基づくセンサの場合、指示薬分子830にルミネセンスを発生させる波長を用いるとよい。また、基板820上には、光電変換器850も実装されている。光電変換器850は、例えば、光検出器またはフォトダイオードとするとよい。フォトルミネセンスに基づくセンサという例示的な場合では、光電変換器850は、指示薬分子830によって放出されるフォトルミネセンス光に感応し、これに応答して、指示薬分子830のフォトルミネセンスのレベルを示す信号を発生する。
【0059】
[0066] 放射線源840、光電変換器850、および指示薬分子830は、放射線源840から放出された放射が指示薬分子830に入射し、指示薬分子830からの放射、例えば、フォトルミネセンスが光電変換器850に入射するように、互いに対して位置付けられている。放射の入射は、反射および/または媒体の透過後に生じてもよい。一実施形態では、光学フィルタ860を用いて、光電変換器850に到達する放射を、放射線源840によって放出された放射に対する指示薬分子の応答と関連のある波長に限定することができる。
【0060】
[0067] また、光センサ800は、当該光センサ800に限られた温度を測定するための温度プローブ870、放射線源840に送信する信号を発生し、光電変換器850から信号を受信するセンサ・インターフェース・モジュール(SIM)880、外部システム(図示せず)とワイヤレスで通信する送信機890、および電源900も含むことができる。電源900は、指示薬(indicator)を含むことができ、電源900をしかるべき電磁場に露出させることによって、指示薬から電流を誘発することができる。本発明にしたがって用いることができる酸素センサの例が、米国特許第5,517,313号および第6,940,590号に記載されている。これらの特許をここで引用したことにより、その内容全体が本願にも含まれるものとする。
【0061】
[0068] 一実施形態によれば、構成パラメータに基づいて、測定された位相差を補正することによって、検体濃度測定の精度を高めることができる。1つの較正ステップは、電子遅延、またはオフセット・ヌル構成パラメータ(offset null configuration parameter)を判定することである。オフセット・ヌルによって、主に電子コンポーネントの許容度による、ユニット毎のばらつきを解消する。オフセット・ヌルの判定は、光センサの製造時またはセンサの構成設定中に、固定温度および検体濃度で行うことができる。
【0062】
[0069] 別の較正ステップでは、既知の検体濃度および種々の温度において位相差を測定し、相対湿度および圧力のような他のセンサ環境素因を既知の値に固定する。この較正ステップでは、位相差を先に論じたように判定し、実際の検体濃度の値を最も普遍的な法則から導出するか、または経験的に測定することができる。実際には、特に高い精度を要求する用途においては、これらの手法をどのように組み合わせてもよい。較正は、個々のデバイスについて、または特定のSIM/センサ・アーキテクチャについて行うことができ、あるいは他の基準で行ってもよい。
【0063】
[0070] 位相差対検体濃度/温度の関係は、用途によっては厳密には線形にはならないこともあるので、これら2つの較正設定ステップに基づく伝達関数を求める。この伝達関数の一部を含む、オフセット・ヌルおよび温度双方の補正表を、マイクロコントローラ外部の表に入れること、またはセンサ・インターフェース・モジュール上にあるメモリに記憶されている表にロードすることができる。高い精度を要求する用途については、追加の較正ステップにおいて、圧力および湿度というような他の湿度入力変数を考慮することもでき、伝達関数はこれらの変数も含む。
【0064】
[0071] 本明細書において記載したセンサは、酸素センサに限定されるのではない。例えば、バッテリ給電式、代謝(metabolic)および大気(atmospheric)センサを用いることもできる。また、本発明によるセンサを人に埋め込み、人体における種々の生物的検体(例えば、酸素、二酸化炭素、グルコース、毒物)を測定するために用いることもできる。加えて、本明細書において記載した発明は、種々の用途および動作環境において用いることができる。例えば、本発明は、ガス混合、不活性化、溶融酸素、環境変化率(environmental rate-of-change)、生物化学的酸素要求量(BOD)、反応モニタ、加熱/換気/空調(HVAC)システム、燃焼監視、ならびに発酵供給およびオフ・ガス監視(fermentation feed and off gas monitors)と共に用いることもできる。
【0065】
[0072] 本発明の一実施形態によるセンサおよびセンサ・インターフェース・モジュール(SIM)を生物化学的酸素要求(BOD)用途においてどのように用いることができるかについて、その一例は排水監視に関する。自然水路または工業的排水の中にある酸化可能素材は、生物化学的(バクテリア)プロセスまたは化学的プロセスの双方によって酸化される。その結果、水の酸素含有量が減少する。基本的に、生物化学的酸化に対する反応は次のように記述することができる。
【0066】
酸化可能素材+バクテリア+栄養分+O2 → CO2+H2O+NO3またはSO4のような酸化された無機物
[0073] この式では、バクテリアおよび酸素が左側にあり、この式から酸素濃度の変化を監視することにより、存在するバクテリアに直接比例するこの反応全体の速度が効果的に監視される。
【0067】
[0074] 全ての自然水路はバクテリアおよび栄養分を含むので、殆どあらゆる廃物混合物がこのような水路に流入すると、(先に示した反応のような)バクテリア反応を開始する。これらのバクテリア反応により、生物化学的酸素要求量(BOD)として測定されるものが生ずる。
【0068】
[0075] 排水において最も共通して測定される構成成分の1つが、生物化学的酸素要求量である。排水は、種々の無機および有機物質で構成される。有機物質とは、炭素に基づき、例えば、糞便や、洗剤、石鹸、脂肪、グリス等を含む分子のことを指す。これらの大きな有機分子は、バクテリアによって容易に分解される。しかしながら、大きな分子をそれよりも小さな分子に分解し、最終的に二酸化炭素および水に分解するプロセスには酸素が必要となる。このプロセスに必要とされる酸素量は、生物化学的酸素要求量(BOD)として知られている。一例では、5日BOD即ちBOD5が、5日間の間に微小有機物によって消費された酸素量によって測定され、これは、汚水における生物分解性有機物の量、または汚水の強度の最も共通な尺度となる。
【0069】
[0076] BODは、従来の汚水処理プラントから地表水または水流に放出される廃水の強度を測定するために従前から用いられている。これは、BODが高い汚水は、受け取る水における酸素を枯渇させ、魚類の殺生および生態系の変化を発生させる虞れがあるからである。非限定的な一例では、地表水放出に対する規準に基づいて、BODに対する二次処理規格が、30mg BOD/L(即ち、廃水を分解するために5日間で30mgのO2が水1リットル毎に消費される。)に設定されている。
【0070】
[0077] 生物化学的酸素要求量(BOD)用途の一例では、本明細書において記載したセンサおよびセンサ・インターフェース・モジュール(SIM)を、排水または他の媒体に対して適した位置に置き、例えば、酸素濃度変化を監視するためというような、所望の測定を行うことができる。
【0071】
[0078] 本発明によるセンサおよびセンサ・インターフェース・モジュール(SIM)は、温度を測定するために用いることもできる。例えば、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩を指示薬分子として用い、プラスチックまたはガラスのような材料の中に埋め込むこと、あるいは全体的に酸素不浸透性の金属筐体内に入れられた総合センサ(sensor overall)の中に埋め込むことができる。指示薬分子が照射され、ルミネセンスを発生させる。一定の酸素濃度では、ルミネセンスは時間の関数として変化し(即ち、温度、温度が低い程ルミナンスは大きくなり、温度が高い程小さくなる)、センサによって検出される。温度は、SIMからのルミネセンスまたは位相変化に基づいて判定することができる。
【0072】
[0079] 以上本発明の種々の実施形態および変形について説明したが、これらは、限定ではなく一例として紹介したに過ぎないことは言うまでもない。つまり、本発明の広さおよび範囲は、これまでに記載した実施形態例のいずれによっても限定されることはなく、以下の特許請求の範囲およびその同等物のみにしたがって定められてしかるべきである。
【特許請求の範囲】
【請求項1】
検体濃度測定デバイスであって、
センサであって、変換器と通信する少なくとも1つの指示薬分子を備えている、センサと、
前記センサと通信するセンサ・インターフェース・モジュールであって、マイクロコントローラを備えている、センサ・インターフェース・モジュールと、
を備えており、前記センサ・インターフェース・モジュールが、前記少なくとも1つの指示薬分子の励起放出の時間ドメイン測定を容易にする、検体濃度測定デバイス。
【請求項2】
請求項1記載のデバイスにおいて、前記センサが光センサである、デバイス。
【請求項3】
請求項2記載のデバイスにおいて、前記光センサが放射線源を備えている、デバイス。
【請求項4】
請求項3記載のデバイスにおいて、前記放射線源が発光ダイオード(LED)を備えている、デバイス。
【請求項5】
請求項4記載のデバイスにおいて、前記LEDが、青色LED、紫色LED、および赤色LEDの内いずれか1つを備えている、デバイス。
【請求項6】
請求項1記載のデバイスにおいて、前記センサ・インターフェース・モジュールが、前記センサと前記センサ・インターフェース・モジュールとの間における通信を可能にするインターフェースを備えている、デバイス。
【請求項7】
請求項6記載のデバイスにおいて、前記インターフェースがアナログ・インターフェースを備えている、デバイス。
【請求項8】
請求項1記載のデバイスであって、更に、外部データ・システムを備えている、デバイス。
【請求項9】
請求項8記載のデバイスであって、更に、前記センサ・インターフェース・モジュールと前記外部データ・システムとの間における通信を可能にするインターフェースを備えている、デバイス。
【請求項10】
請求項1記載のデバイスにおいて、前記少なくとも1つの指示薬分子が、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩、ランタニド系指示薬、および芳香族炭化水素の内いずれか1つを含む、デバイス。
【請求項11】
請求項10記載のデバイスにおいて、前記ランタニド系指示薬が、ユーロピニウムおよびテルビウム・コンプレックスの内いずれか1つを含む、デバイス。
【請求項12】
請求項1記載のデバイスにおいて、前記少なくとも1つの指示薬分子が前記センサに隣接する、デバイス。
【請求項13】
請求項1記載のデバイスにおいて、前記センサおよび前記センサ・インターフェース・モジュールが、回路ボード上に設けることができ、この回路ボードを用いて通信する、デバイス。
【請求項14】
検体濃度測定方法であって、
センサを選択するステップと、
前記センサに隣接して指示薬分子を設けるステップと、
前記検体に基づいて刺激波形を発生するステップと、
前記指示薬分子を励起するステップと、
前記励起された指示薬分子に対する前記検体の応答特性に基づいて、この検体の特性を検出するステップと、
前記検体濃度を判定するステップと、
を備えている、方法。
【請求項15】
請求項14記載の方法において、刺激波形を発生する前記ステップが、電圧波形を正弦波のように近似するステップを含む、方法。
【請求項16】
請求項14記載の方法であって、更に、前記刺激波形および前記応答波形をオーバーサンプリングするステップを備えている、方法。
【請求項17】
請求項14記載の方法であって、更に、前記刺激波形と前記応答波形との間における位相遅延を判定するステップを備えている、方法。
【請求項18】
請求項14記載の方法において、前記指示薬分子を励起する前記ステップが、前記指示薬分子を照射するステップを含む、方法。
【請求項19】
請求項17記載の方法であって、更に、前記指示薬分子のフォトルミネセンス放射を検出するステップを備えている、方法。
【請求項20】
請求項14記載の方法において、センサを選択する前記ステップが、光センサを選択するステップを含む、方法。
【請求項21】
請求項14記載の方法であって、更に、前記刺激波形を用いて放射線源を駆動するステップを備えている、方法。
【請求項22】
検体濃度測定デバイスであって、
所定の周波数の周期的ディジタル信号を出力し、刺激波形と応答波形との間における位相差を計算するように構成されているマイクロコントローラと、
前記周期的ディジタル信号を周期的電圧波形に変換するように動作可能なディジタル/アナログ変換器と、
前記周期的電圧波形を平滑化し、前記刺激波形を出力するように動作可能なロー・パス・フィルタと、
前記刺激波形を周期的電流波形に変換し、放射線源を駆動するように動作可能な電圧/電流変換器であって、前記放射線源が指示薬分子上に放射する、電圧/電流変換器と、
光電変換器からの電流を前記応答波形に変換するように動作可能なバンドパス・トランスインピーダンス増幅器であって、前記指示薬分子からの放射が光電変換器に入射する、バンドパス・トランスインピーダンス増幅器と、
を備えており、前記位相差が、前記指示薬分子に局限的な検体濃度の関数である、デバイス。
【請求項23】
請求項21記載のデバイスにおいて、前記周期的ディジタル信号が、9kHzから11kHzの範囲の周波数を有する、デバイス。
【請求項24】
請求項21記載のデバイスにおいて、前記マイクロコントローラが、更に、検体濃度の計算に関するパラメータを、前記デバイスの外部にある装置とシリアルに伝達するように構成されている、デバイス。
【請求項25】
請求項21記載のデバイスにおいて、当該デバイスが外部デバイスと通信する、デバイス。
【請求項26】
請求項24記載のデバイスにおいて、前記外部デバイスがデータ収集システムを備えている、デバイス。
【請求項27】
請求項21記載のデバイスにおいて、前記放射線源が発光ダイオードを備えている、デバイス。
【請求項28】
請求項21記載のデバイスにおいて、前記マイクロコントローラが、更に、以下のようにして、前記ディジタル出力バス上に前記周期的ディジタル信号を出力するように構成されている、デバイス。
(a)前記マイクロコントローラが、濃度データを取り込む命令を受信するのを待ち、前記命令が前記マイクロコントローラのシリアル入力ポートに送信される。
(b)前記マイクロコントローラが、前記ディジタル出力バス上にランプ信号を出力する。
(c)前記マイクロコントローラが、前記ディジタル出力バスに、所定の周波数の量子化正弦波を表す信号を出力する。
(d)前記マイクロコントローラが、前記ディジタル出力バスをスタンバイ値に設定する。
【請求項29】
請求項21記載のデバイスにおいて、前記マイクロコントローラが、更に、伝達関数を用いて、前記位相差を検体濃度値に変換するように構成されている、デバイス。
【請求項30】
請求項28記載のデバイスにおいて、前記伝達関数が、温度、圧力、および湿度の内いずれか1つの従属変数を含む、デバイス。
【請求項31】
検体濃度センサであって、
請求項21記載のデバイスを備えており、このデバイスが検体に隣接する、検体濃度センサ。
【請求項32】
請求項30記載の検体濃度センサにおいて、前記検体がO2であり、前記放射線源がLEDを備えており、前記光電変換器がフォトダイオードを備えており、前記指示薬分子が、O2が存在する場合に、フォトルミネセンス消光を呈する、検体濃度センサ。
【請求項33】
検体濃度判定方法であって、
マイクロコントローラの出力上に、周期的ディジタル出力信号を発生するステップと、
前記周期的ディジタル出力信号を平滑化駆動電流波形に変換するステップであって、前記平滑化駆動電流波形が、前記周期的ディジタル出力信号と同じ周波数である、ステップと、
前記平滑化駆動電流によって放射線源を駆動するステップであって、前記放射線源からの放射が指示薬分子に入射する、ステップと、
光電変換器によって、前記指示薬分子の放射線励起を検出するステップであって、前記光電変換器が、前記平滑化駆動電流波形と同じ周波数の波形を出力する、ステップと、
前記平滑化駆動電流波形と前記出力された光電変換器波形との間における位相差を測定するステップと、
を備えており、前記位相差が、前記指示薬分子に局限的な検体濃度と相関がある、方法。
【請求項34】
請求項32記載の方法において、前記検体がO2であり、前記放射線源がLEDを備えており、前記光電変換器がフォトダイオードを備えており、前記指示薬分子が、O2が存在する場合に、フォトルミネセンス消光を呈する、方法。
【請求項35】
検体濃度測定方法であって、
センサを選択するステップと、
前記センサに隣接して指示薬分子を設けるステップと、
前記検体に基づいて刺激波形を発生するステップと、
前記指示薬分子を励起するステップと、
前記励起した指示薬分子に対するその応答特性に基づいて、前記検体の特性を検出するステップと、
前記検体濃度を判定するステップと、
を備えている、方法。
【請求項36】
請求項34記載の方法であって、更に、前記刺激波形および前記応答波形をオーバーサンプリングするステップを備えている、方法。
【請求項37】
請求項34記載の方法であって、更に、前記刺激波形と前記応答波形との間における位相遅延を判定するステップを備えている、方法。
【請求項38】
請求項34記載の方法において、前記指示薬分子を励起するステップが、前記指示薬分子を照射するステップを含む、方法。
【請求項39】
請求項37記載の方法であって、更に、前記指示薬分子のフォトルミネセンス放射を検出するステップを備えている、方法。
【請求項40】
請求項34記載の方法において、センサを選択する前記ステップが、光センサを選択するステップを含む、方法。
【請求項41】
請求項34記載の方法であって、更に、前記刺激波形によって放射線源を駆動するステップを備えている、方法。
【請求項42】
媒体内における酸素の存在を判定する方法であって、
酸素センサを選択するステップと、
前記センサに指示薬分子を供給するステップと、
前記センサを媒体内に配置するステップと、
センサ・インターフェース・モジュールから位相変調信号を前記センサに送信するステップと、
前記位相変調信号の変化率を判定するステップと、
前記媒体内における酸素濃度を判定するステップと、
を備えている、方法。
【請求項43】
請求項41記載の方法において、前記媒体が、水、血液、および空気の内いずれか1つを含む、方法。
【請求項1】
検体濃度測定デバイスであって、
センサであって、変換器と通信する少なくとも1つの指示薬分子を備えている、センサと、
前記センサと通信するセンサ・インターフェース・モジュールであって、マイクロコントローラを備えている、センサ・インターフェース・モジュールと、
を備えており、前記センサ・インターフェース・モジュールが、前記少なくとも1つの指示薬分子の励起放出の時間ドメイン測定を容易にする、検体濃度測定デバイス。
【請求項2】
請求項1記載のデバイスにおいて、前記センサが光センサである、デバイス。
【請求項3】
請求項2記載のデバイスにおいて、前記光センサが放射線源を備えている、デバイス。
【請求項4】
請求項3記載のデバイスにおいて、前記放射線源が発光ダイオード(LED)を備えている、デバイス。
【請求項5】
請求項4記載のデバイスにおいて、前記LEDが、青色LED、紫色LED、および赤色LEDの内いずれか1つを備えている、デバイス。
【請求項6】
請求項1記載のデバイスにおいて、前記センサ・インターフェース・モジュールが、前記センサと前記センサ・インターフェース・モジュールとの間における通信を可能にするインターフェースを備えている、デバイス。
【請求項7】
請求項6記載のデバイスにおいて、前記インターフェースがアナログ・インターフェースを備えている、デバイス。
【請求項8】
請求項1記載のデバイスであって、更に、外部データ・システムを備えている、デバイス。
【請求項9】
請求項8記載のデバイスであって、更に、前記センサ・インターフェース・モジュールと前記外部データ・システムとの間における通信を可能にするインターフェースを備えている、デバイス。
【請求項10】
請求項1記載のデバイスにおいて、前記少なくとも1つの指示薬分子が、コンプレックス・トリス(4,7−ジフェニル−1,10−フェナントロリン)ルテニウム(II)過塩素酸塩、ランタニド系指示薬、および芳香族炭化水素の内いずれか1つを含む、デバイス。
【請求項11】
請求項10記載のデバイスにおいて、前記ランタニド系指示薬が、ユーロピニウムおよびテルビウム・コンプレックスの内いずれか1つを含む、デバイス。
【請求項12】
請求項1記載のデバイスにおいて、前記少なくとも1つの指示薬分子が前記センサに隣接する、デバイス。
【請求項13】
請求項1記載のデバイスにおいて、前記センサおよび前記センサ・インターフェース・モジュールが、回路ボード上に設けることができ、この回路ボードを用いて通信する、デバイス。
【請求項14】
検体濃度測定方法であって、
センサを選択するステップと、
前記センサに隣接して指示薬分子を設けるステップと、
前記検体に基づいて刺激波形を発生するステップと、
前記指示薬分子を励起するステップと、
前記励起された指示薬分子に対する前記検体の応答特性に基づいて、この検体の特性を検出するステップと、
前記検体濃度を判定するステップと、
を備えている、方法。
【請求項15】
請求項14記載の方法において、刺激波形を発生する前記ステップが、電圧波形を正弦波のように近似するステップを含む、方法。
【請求項16】
請求項14記載の方法であって、更に、前記刺激波形および前記応答波形をオーバーサンプリングするステップを備えている、方法。
【請求項17】
請求項14記載の方法であって、更に、前記刺激波形と前記応答波形との間における位相遅延を判定するステップを備えている、方法。
【請求項18】
請求項14記載の方法において、前記指示薬分子を励起する前記ステップが、前記指示薬分子を照射するステップを含む、方法。
【請求項19】
請求項17記載の方法であって、更に、前記指示薬分子のフォトルミネセンス放射を検出するステップを備えている、方法。
【請求項20】
請求項14記載の方法において、センサを選択する前記ステップが、光センサを選択するステップを含む、方法。
【請求項21】
請求項14記載の方法であって、更に、前記刺激波形を用いて放射線源を駆動するステップを備えている、方法。
【請求項22】
検体濃度測定デバイスであって、
所定の周波数の周期的ディジタル信号を出力し、刺激波形と応答波形との間における位相差を計算するように構成されているマイクロコントローラと、
前記周期的ディジタル信号を周期的電圧波形に変換するように動作可能なディジタル/アナログ変換器と、
前記周期的電圧波形を平滑化し、前記刺激波形を出力するように動作可能なロー・パス・フィルタと、
前記刺激波形を周期的電流波形に変換し、放射線源を駆動するように動作可能な電圧/電流変換器であって、前記放射線源が指示薬分子上に放射する、電圧/電流変換器と、
光電変換器からの電流を前記応答波形に変換するように動作可能なバンドパス・トランスインピーダンス増幅器であって、前記指示薬分子からの放射が光電変換器に入射する、バンドパス・トランスインピーダンス増幅器と、
を備えており、前記位相差が、前記指示薬分子に局限的な検体濃度の関数である、デバイス。
【請求項23】
請求項21記載のデバイスにおいて、前記周期的ディジタル信号が、9kHzから11kHzの範囲の周波数を有する、デバイス。
【請求項24】
請求項21記載のデバイスにおいて、前記マイクロコントローラが、更に、検体濃度の計算に関するパラメータを、前記デバイスの外部にある装置とシリアルに伝達するように構成されている、デバイス。
【請求項25】
請求項21記載のデバイスにおいて、当該デバイスが外部デバイスと通信する、デバイス。
【請求項26】
請求項24記載のデバイスにおいて、前記外部デバイスがデータ収集システムを備えている、デバイス。
【請求項27】
請求項21記載のデバイスにおいて、前記放射線源が発光ダイオードを備えている、デバイス。
【請求項28】
請求項21記載のデバイスにおいて、前記マイクロコントローラが、更に、以下のようにして、前記ディジタル出力バス上に前記周期的ディジタル信号を出力するように構成されている、デバイス。
(a)前記マイクロコントローラが、濃度データを取り込む命令を受信するのを待ち、前記命令が前記マイクロコントローラのシリアル入力ポートに送信される。
(b)前記マイクロコントローラが、前記ディジタル出力バス上にランプ信号を出力する。
(c)前記マイクロコントローラが、前記ディジタル出力バスに、所定の周波数の量子化正弦波を表す信号を出力する。
(d)前記マイクロコントローラが、前記ディジタル出力バスをスタンバイ値に設定する。
【請求項29】
請求項21記載のデバイスにおいて、前記マイクロコントローラが、更に、伝達関数を用いて、前記位相差を検体濃度値に変換するように構成されている、デバイス。
【請求項30】
請求項28記載のデバイスにおいて、前記伝達関数が、温度、圧力、および湿度の内いずれか1つの従属変数を含む、デバイス。
【請求項31】
検体濃度センサであって、
請求項21記載のデバイスを備えており、このデバイスが検体に隣接する、検体濃度センサ。
【請求項32】
請求項30記載の検体濃度センサにおいて、前記検体がO2であり、前記放射線源がLEDを備えており、前記光電変換器がフォトダイオードを備えており、前記指示薬分子が、O2が存在する場合に、フォトルミネセンス消光を呈する、検体濃度センサ。
【請求項33】
検体濃度判定方法であって、
マイクロコントローラの出力上に、周期的ディジタル出力信号を発生するステップと、
前記周期的ディジタル出力信号を平滑化駆動電流波形に変換するステップであって、前記平滑化駆動電流波形が、前記周期的ディジタル出力信号と同じ周波数である、ステップと、
前記平滑化駆動電流によって放射線源を駆動するステップであって、前記放射線源からの放射が指示薬分子に入射する、ステップと、
光電変換器によって、前記指示薬分子の放射線励起を検出するステップであって、前記光電変換器が、前記平滑化駆動電流波形と同じ周波数の波形を出力する、ステップと、
前記平滑化駆動電流波形と前記出力された光電変換器波形との間における位相差を測定するステップと、
を備えており、前記位相差が、前記指示薬分子に局限的な検体濃度と相関がある、方法。
【請求項34】
請求項32記載の方法において、前記検体がO2であり、前記放射線源がLEDを備えており、前記光電変換器がフォトダイオードを備えており、前記指示薬分子が、O2が存在する場合に、フォトルミネセンス消光を呈する、方法。
【請求項35】
検体濃度測定方法であって、
センサを選択するステップと、
前記センサに隣接して指示薬分子を設けるステップと、
前記検体に基づいて刺激波形を発生するステップと、
前記指示薬分子を励起するステップと、
前記励起した指示薬分子に対するその応答特性に基づいて、前記検体の特性を検出するステップと、
前記検体濃度を判定するステップと、
を備えている、方法。
【請求項36】
請求項34記載の方法であって、更に、前記刺激波形および前記応答波形をオーバーサンプリングするステップを備えている、方法。
【請求項37】
請求項34記載の方法であって、更に、前記刺激波形と前記応答波形との間における位相遅延を判定するステップを備えている、方法。
【請求項38】
請求項34記載の方法において、前記指示薬分子を励起するステップが、前記指示薬分子を照射するステップを含む、方法。
【請求項39】
請求項37記載の方法であって、更に、前記指示薬分子のフォトルミネセンス放射を検出するステップを備えている、方法。
【請求項40】
請求項34記載の方法において、センサを選択する前記ステップが、光センサを選択するステップを含む、方法。
【請求項41】
請求項34記載の方法であって、更に、前記刺激波形によって放射線源を駆動するステップを備えている、方法。
【請求項42】
媒体内における酸素の存在を判定する方法であって、
酸素センサを選択するステップと、
前記センサに指示薬分子を供給するステップと、
前記センサを媒体内に配置するステップと、
センサ・インターフェース・モジュールから位相変調信号を前記センサに送信するステップと、
前記位相変調信号の変化率を判定するステップと、
前記媒体内における酸素濃度を判定するステップと、
を備えている、方法。
【請求項43】
請求項41記載の方法において、前記媒体が、水、血液、および空気の内いずれか1つを含む、方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7A】


【図7B】


【図7C】


【図7D】


【図7E】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7A】


【図7B】


【図7C】


【図7D】


【図7E】


【図8】


【公表番号】特表2011−529577(P2011−529577A)
【公表日】平成23年12月8日(2011.12.8)
【国際特許分類】
【出願番号】特願2011−521208(P2011−521208)
【出願日】平成21年7月24日(2009.7.24)
【国際出願番号】PCT/US2009/051633
【国際公開番号】WO2010/014505
【国際公開日】平成22年2月4日(2010.2.4)
【出願人】(501078166)センサーズ・フォー・メデセン・アンド・サイエンス・インコーポレーテッド (17)
【Fターム(参考)】
【公表日】平成23年12月8日(2011.12.8)
【国際特許分類】
【出願日】平成21年7月24日(2009.7.24)
【国際出願番号】PCT/US2009/051633
【国際公開番号】WO2010/014505
【国際公開日】平成22年2月4日(2010.2.4)
【出願人】(501078166)センサーズ・フォー・メデセン・アンド・サイエンス・インコーポレーテッド (17)
【Fターム(参考)】
[ Back to top ]

