検体補正機構およびマーカー定量装置
【課題】生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる検体補正機構およびマーカー定量装置を提供すること。
【解決手段】生体試料を含有する検体における単位体積あたりの疾患関連マーカー含有量を前記検体に含有される単位細胞数あたりの前記疾患関連マーカー含有量に補正する検体補正機構1であって、前記検体の性状を測定する検体性状測定部10と、検体性状測定部10による測定結果に基づく補正値を算出する補正値算出部20と、前記単位体積あたりの前記疾患関連マーカー含有量と前記補正値とに基づいて前記単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部30と、を備える。
【解決手段】生体試料を含有する検体における単位体積あたりの疾患関連マーカー含有量を前記検体に含有される単位細胞数あたりの前記疾患関連マーカー含有量に補正する検体補正機構1であって、前記検体の性状を測定する検体性状測定部10と、検体性状測定部10による測定結果に基づく補正値を算出する補正値算出部20と、前記単位体積あたりの前記疾患関連マーカー含有量と前記補正値とに基づいて前記単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部30と、を備える。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、検体補正機構およびマーカー定量装置に関する。
【背景技術】
【0002】
従来、生体から採取される生体試料を分析して疾患の検査や診断を行うことが知られている。例えば、特許文献1には、生体試料の一形態である糞便を用いて便潜血の診断を行う際に用いられる器具である糞便採取容器が開示されている。
特許文献1に記載の糞便採取容器は、先端に切欠部、凹部、または貫通孔の少なくともひとつを有して先端において糞便を採取する採取棒と、採取棒が挿通される穴を有するとともに糞便を懸濁させるための液体を収容しうる容器本体とを備え、採取棒を容器本体の穴に挿通することで所定体積の糞便を容易に採取できる。
【0003】
また、特許文献2には、便潜血検査方法が開示されている。この特許文献2に記載の便潜血検査方法は、糞便の乾燥重量に相関し糞便の含水率に逆相関する指標として糞便中に存在する常在物質の濃度を測定することを特徴としている。また、特許文献2には、常在物質の濃度を測定する方法として、糞便懸濁液に対して照射された波長既知の光線の吸光度を測定する方法が開示されている。特許文献2に記載の便潜血検査方法によれば、便の含水率に逆相関的する便潜血量のデータに対して常在物質の濃度によって補正をかけることができるので、便の性状の個人差や日々の変動によらず精度よく便潜血検査ができる。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】実公平05−017652号公報
【特許文献2】国際公開第01/061343号パンフレット
【発明の概要】
【発明が解決しようとする課題】
【0005】
近年の遺伝子解析技術の発達に伴い、疾患に関連するDNAや、疾患に関連するDNAからの転写産物である疾患関連マーカー(mRNA)に基づいて疾患の有無を診断する方法が注目されている。ここで、生体試料中の疾患関連マーカーの量に基づいて疾患を診断するためには、生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量が標準化されていることを要する。
糞便中における被験者由来細胞は、主に新陳代謝で便中に剥離したものである。体調等により便の滞留時間が長くなることで水分量が減少する。また、繊維量が多いと便通が良くなり便の滞留時間が短くなる。このため、糞便中の被験者由来細胞数は便の通過時間に相関する。
【0006】
しかしながら、特許文献1に記載の糞便採取容器および特許文献2に記載の便潜血検査方法では、便の通過時間に相関する指標がないため、糞便中に存在する被験者由来細胞の数に相関する情報を得ることができなかった。このため、単位細胞数当たりの疾患関連遺伝子の発現量の情報を得ることは困難であった。
【0007】
本発明は、上述した事情に鑑みてなされたものであって、その目的は生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる検体補正機構およびマーカー定量装置の提供を図ることにある。
【課題を解決するための手段】
【0008】
上記課題を解決するために、この発明は以下の手段を提案している。
本発明の検体補正機構は、生体試料を含有する検体における単位体積あたりの疾患関連マーカー含有量を前記検体に含有される単位細胞数あたりの前記疾患関連マーカー含有量に補正する検体補正機構であって、前記検体の性状を測定する検体性状測定部と、前記検体性状測定部による測定結果に基づく補正値を算出する補正値算出部と、前記単位体積あたりの前記疾患関連マーカー含有量と前記補正値とに基づいて前記単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部と、を備えることを特徴としている。
なお、本発明において、検体の性状とは、検体の物理的特性を指し、例えば検体の重量、固形成分の割合、および比重などである。
【0009】
また、前記検体性状測定部は、前記検体の重量を測定する検体重量測定機構を有することが好ましい。
【0010】
また、前記検体重量測定機構は、前記検体が収容され重量既知の検体容器と前記検体とをあわせて重量測定して前記検体容器と前記検体との合計重量を測定する測定部と、前記合計重量から前記検体容器の重量を差し引いて前記検体の正味重量を算出する重量算出部と、を有することが好ましい。
【0011】
また、前記検体性状測定部は、前記検体が収容され少なくとも一部において光線が透過可能な検体容器に対して照射される光線の減衰量に基づいて前記検体容器中の固形成分の含有率を測定する光学的測定機構を有することが好ましい。
【0012】
また、前記光学的測定機構は、前記検体容器の外部から内部方向へ測定光を照射する発光部と、前記検体容器を挟んで前記発光部と反対側に設けられて前記検体容器及び前記検体を透過した前記測定光を受光する受光部と、を有することが好ましい。
【0013】
また、前記光学的測定機構は、前記検体容器の外部から内部方向へ測定光を照射する発光部と、前記検体容器に対して前記発光部と同じ側に設けられて前記検体容器及び前記検体によって反射された前記測定光を受光する受光部と、を有していてもよい。
【0014】
また、前記光学的測定機構は、前記検体容器における開口から底までの間で所定間隔置きに配置された複数の前記発光部と、前記発光部のそれぞれに対応して配置された前記受光部と、をさらに有していることが好ましい。
【0015】
また、本発明の検体補正機構は、前記検体容器に対して開口から底へ向かう1G以上の重力を生じさせて前記検体の固形成分を前記検体容器の底に沈殿させる分離部をさらに有していることが好ましい。
【0016】
本発明のマーカー定量装置は、本発明の検体補正機構と、前記検体から前記疾患関連マーカーを抽出するマーカー抽出部と、を備えることを特徴としている。
【0017】
また、本発明のマーカー定量装置は、前記検体の単位体積あたりの前記疾患関連マーカーの含有量を検出するマーカー検出部をさらに備えることが好ましい。
【発明の効果】
【0018】
本発明の検体補正機構およびマーカー定量装置によれば、生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【図面の簡単な説明】
【0019】
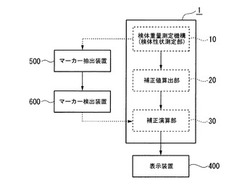
【図1】本発明の第1実施形態の検体補正機構の構成を示すブロック図である。
【図2】同検体補正機構の一部の構成を示すブロック図である。
【図3】同検体補正機構の使用時の動作を示すフローチャートである。
【図4】本発明の第2実施形態のマーカー定量装置の構成を示すブロック図である。
【図5】同マーカー定量装置の使用時の動作を示すフローチャートである。
【図6】本発明の第3実施形態のマーカー定量装置の構成を示すブロック図である。
【図7】同マーカー定量装置の一部の構成を一部断面視で示す側面図である。
【図8】同マーカー定量装置の使用時の動作を示すフローチャートである。
【図9】同マーカー定量装置の変形例における一部の構成を示す平面図である。
【図10】本発明の第4実施形態のマーカー定量装置の構成を示すブロック図である。
【図11】同マーカー定量装置の一部の構成を詳細に示すブロック図である。
【図12】(A)は同マーカー定量装置の一部の構成を一部断面視で示す側面図、(B)は同マーカー定量装置の使用時の動作を一部断面視で示す側面図である。
【図13】(A)は本発明のマーカー定量装置の実施例1を示すブロック図、(B)は実施例1のマーカー定量装置の一部の構成を示す斜視図である。
【図14】実施例1のマーカー定量装置の一部の構成を一部断面視で示す側面図である。
【図15】本発明のマーカー定量装置の実施例2を一部断面視で示す側面図である。
【発明を実施するための形態】
【0020】
(第1実施形態)
以下、本発明の第1実施形態の検体補正機構について図1ないし図3を参照して説明する。図1は本発明の第1実施形態の検体補正機構1の構成を示すブロック図である。また、図2は検体補正機構1の一部の構成を示すブロック図である。
検体補正機構1は、生態から採取される一定体積の試料、具体的には一定体積の糞便試料を検体とする解析に好適に採用できる機構である。
【0021】
図1に示すように、本実施形態の検体補正機構1は、検体の性状を測定する検体重量測定機構(検体性状測定部)10と、検体性状測定部による測定結果に基づく補正値を算出する補正値算出部20と、補正値算出部20によって算出された補正値に基づいて単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部30と、を備えている。
【0022】
また、本実施形態の検体補正機構1は、補正演算部30と電気的に接続されて算出結果を表示するための表示装置400と、検体から疾患関連マーカーを含むmRNAを抽出するためのマーカー抽出装置500と、マーカー抽出装置500によって抽出されたmRNAから疾患関連マーカーを検出するためのマーカー検出装置600と共に使用される。
マーカー検出装置600では、検体の全量に対する疾患関連マーカーの含有量が定量的に検出される。
なお、本実施形態では、マーカー抽出装置500と、マーカー検出装置600とは、それぞれ適用可能な周知のマーカー抽出装置あるいはマーカー検出装置を適宜採用することができる。
【0023】
検体重量測定機構10は、検体性状測定部の一例であり、検体の重量を測定して重量情報を補正値算出部20に送信する機構である。検体重量測定機構10は、検体の重量を測定する測定部11と、測定部11において測定された値に基づいて検体の正味重量を算出する重量算出部12と、を有している。
【0024】
検体は図示しない重量既知の検体容器に収容されており、測定部11は検体容器と検体とをあわせて測定することで検体容器と検体との合計重量を測定する。例えば、測定部11には電子天秤等の秤量機器を採用することができる。
重量算出部12は、上述の合計重量から検体容器の重量を差し引く演算を行って、その結果を検体の正味重量として補正値算出部20に送信する。
【0025】
補正値算出部20は、検体重量測定機構10から送信された上述の正味重量に基づいて補正値を算出する。具体的には、補正値は正味重量の逆数である。
【0026】
補正演算部30は、上記マーカー検出装置600によって検出された疾患関連マーカーの含有量に上述の補正値を乗じて演算する回路である。
【0027】
以下では、検体補正機構1の作用について詳述する。図3は検体補正機構1の使用時の動作を示すフローチャートである。以下では、検体として糞便試料を使用する例を示すが、検体としては他の生体試料を用いることもできる。
【0028】
本実施形態では、糞便試料は一定体積の糞便を採便できる周知の採便棒によって採取され、所定容量の保存液が収容された上述の検体容器にともに収容されている。
【0029】
本実施形態で検査対象となる疾患関連マーカーは、患部における細胞に特異的に発現する遺伝子からの転写産物(疾患関連mRNA)などである。例えば大腸癌に関連性の高いmRNAを発現する大腸上皮細胞は、主に新陳代謝によって剥離して便に所定数だけ含まれている。このとき腸内の便の滞留時間が長くなると、便中に剥離してくる大腸上皮細胞数が便の滞留時間に比例して増加する。また、腸内における便の滞留時間が長くなると、腸の作用による水分再吸収により便が固く、かつ重くなる傾向になる。
【0030】
本実施形態では、腸内における便の滞留時間と便の重量との間の正の相関性に着目し、便の重量に基づく補正値を用いて一定体積の便検体に含まれる剥離細胞数を標準化している。
【0031】
具体的には、まず、便重量W1+保存液重量W2+保存ケース重量W3の合計質量Wを検体重量測定機構10の測定部11において測定する(検体重量測定工程S10)。
【0032】
続いて、マーカー抽出装置500において、検体容器に収容された検体の全量を用いて所定のプロセスによってTotal RNAを抽出し、mRNAを精製する。
続いて、マーカー検出装置600では、上述のTotal RNAに対してoligo dTプライマーによってmRNA特異的に逆転写反応が行われる。これにより、検体T中に存在するmRNA(疾患関連マーカーを含む)に対して安定的なcDNAが合成される。
【0033】
さらに、マーカー検出装置600では、所定容量のcDNA/緩衝液溶液を出発物質として増幅反応が行なわれる。この増幅反応には、例えば検査対象となる疾患関連mRNAに対して特異性を有する合成オリゴ(プライマー)を用いてRT−PCR、あるいはRealTime−RT−PCRを行う。このとき、cDNA/緩衝液溶液を段階希釈して希釈系列を構成して増幅反応を行ってもよい。
増幅反応によって、所定体積の検体から抽出されたmRNAに含有された疾患関連mRNAが特異的に増幅され疾患関連mRNAの発現量E1が定量される。
【0034】
続いて、補正演算部30において、上記合計質量Wと、発現量E1とがともに入力される。保存液重量W2、保存ケース重量W3は予め定められて用意されているのでそれぞれ一定値である。このため、測定部11で計測された合計質量Wから保存液重量W2、保存ケース重量W3を減算することで便質量(正味重量)W1が算出される。
【0035】
発現量E1は、検査対象mRNAを発現する便中に剥離した大腸上皮細胞数に相関性があり、また便中に剥離した大腸上皮細胞数は大腸内の滞留時間にほぼ比例する。また、被験者の体調等により便の滞留時間が長くなることで水分量が減少する。さらに、便中の繊維量が多いと便通が良くなり便の滞留時間が短くなる。このため、所定体積の糞便試料に対する発現量E1の値は、便の水分量や繊維量に応じてばらつく。このため、所定体積の糞便試料に対する発現量E1という結果に基づいて大腸上皮細胞数に応じた発現量を知るためには、後述する補正が必要になる。
【0036】
補正値算出部20では、検体重量測定機構10から送信された上述の便重量(正味重量)の逆数が算出され、補正値として採用される。補正値は、補正演算部30によって参照される(補正値算出工程S20)。
【0037】
補正演算部30では、疾患関連mRNAの発現量E1に対して、上述の補正値である便重量(正味重量)W1の逆数を乗算する(補正演算工程S30)。腸内における便の滞留時間との間に正の相関性を有する便重量の逆数が補正値として採用されたことで、一定体積の便検体に含まれる剥離細胞数を標準化している。補正演算部30において演算された結果は表示装置400に表示される。
【0038】
以上説明したように、本発明の検体補正機構によれば、所定体積の糞便試料の便重量W1に基づいて、便重量W1の逆数を疾患関連マーカーの発現量E1に乗じている。このため、生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0039】
このため、検体採取量や検体の状態による検査マーカー検出値のバラツキを抑えることができる。例えば下痢便、便秘便による便mRNA検査の検出結果のバラツキを抑えることができるので、一定の細胞量あたりの対象mRNAの発現量を高精度に検出することが可能となる。
【0040】
(第2実施形態)
次に、本発明の第2実施形態のマーカー定量装置について図4および図5を参照して説明する。なお、以下に説明する各実施形態において、上述した第1実施形態の検体補正機構1と構成を共通とする箇所には同一符号を付けて、説明を省略することにする。
【0041】
図4は、本実施形態のマーカー定量装置2の構成を示すブロック図である。マーカー定量装置2は、第1実施形態の検体補正機構1に加えて、マーカー抽出装置500に代えて検体補正機構1と一体的に設けられ、検体から疾患関連マーカーを抽出するマーカー抽出部50を備えている点で上述の第1実施形態と構成が異なっている。
【0042】
図5は、マーカー定量装置2の使用時の動作を示すフローチャートである。図5に示すように、マーカー定量装置2では、補正値算出工程S20と補正演算工程S30との間にマーカー抽出工程S50が介在されている。
【0043】
以下では、本実施形態のマーカー抽出工程S50に適用可能な一例を示す。なお、マーカー抽出工程S50は、疾患関連マーカーを検出可能な状態で抽出する適宜の手法を採用することができ、以下に説明する一例に限定されるものではない。
【0044】
補正値算出工程S20が完了した後で、補正演算工程S30に好適に適用できる補正値が算出されたことが確定した後、検体重量測定工程S10が完了した検体Tの全量が用いられて検体T中のTotal RNAが抽出される。
マーカー抽出工程S50では、Total RNAは緩衝液に溶解された状態で提供される。その後、使用者によって直ちにマーカー検出装置600におけるマーカーの検出に供される。
【0045】
マーカー検出装置600では、第1実施形態と同様に、Total RNAに対してmRNA特異的に逆転写反応が行われる。次に、所定容量のcDNA/緩衝液溶液を出発物質として増幅反応が行なわれる。この増幅反応には、例えば検査対象となる疾患関連mRNAに対して特異性を有する合成オリゴ(プライマー)を用いてRT−PCR、あるいはRealTime−RT−PCRを行う。このとき、cDNA/緩衝液溶液を段階希釈して希釈系列を構成して増幅反応を行ってもよい。
増幅反応によって、所定体積の検体から抽出されたmRNAに含有された疾患関連mRNAが特異的に増幅され疾患関連mRNAの発現量E1が定量される。
【0046】
マーカー検出装置600において検出された検出結果は、第1実施形態と同様に補正演算工程S30において補正値によって補正されて表示装置400において検体Tにおける単位細胞数当たりの疾患関連マーカー発現強度として表示される。
【0047】
本実施形態でも、第1実施形態の検体補正機構1と同様に生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0048】
また、マーカー定量装置2によれば、検体重量測定機構10において検体Tの重量が測定されたのち、直ちにマーカー抽出部50において疾患関連マーカーを含むmRNAが抽出される。マーカー抽出部50において抽出されたmRNAのサンプルは緩衝液内に保存されているため、例えば検体T中に存在するRNase等によるmRNAの分解が抑制されている。このため、マーカー抽出工程S50の後にmRNAのサンプルを凍結保存などの適宜の保存方法によって長期に保存し、一連の工程を中断することができる。その結果、疾患関連マーカーの検出精度を高く維持しつつ一連の工程の時間的な自由度を高めることができる。
【0049】
(第3実施形態)
次に、本発明の第3実施形態のマーカー定量装置について図6ないし図9を参照して説明する。なお、以下に説明する各実施形態において、上述した第1実施形態の検体補正機構1および第2実施形態のマーカー定量装置2と構成を共通とする箇所には同一符号を付けて、説明を省略することにする。
【0050】
図6は、本実施形態のマーカー定量装置3の構成を示すブロック図である。また、図7はマーカー定量装置3の一部の構成を一部断面で示す側面図である。図6および図7に示すように、マーカー定量装置3は、第2実施形態の検体補正機構1に代えて設けられた検体補正機構101と、表示装置400に代えて検体補正機構101と一体的に設けられた表示部40と、マーカー検出装置600に代えて検体補正機構101と一体的に設けられたマーカー検出部60と、を備えている点で上述の第2実施形態と構成が異なっている。
【0051】
検体補正機構101は、第1実施形態の検体重量測定機構10に加えて光学的測定機構80を有する検体性状測定部110と、補正値算出部20に代えて設けられた補正値算出部120とを備えている。
【0052】
光学的測定機構80は、図7に示すように、検体容器100の外部から内部方向へ測定光Lを照射する発光部81と、検体容器100を挟んで発光部81と反対側に設けられて検体容器100及び検体Tを透過した測定光Lを受光する受光部82と、を有している。受光部82では、検体容器100の側壁100c、100dを透過して受光された測定光Lを光電変換することで電気信号にしている。
【0053】
補正値算出部120は、検体重量測定機構10によって測定された結果と光学的測定機構80によって測定された結果との両方に基づく補正値を算出する。
【0054】
以下では、本実施形態のマーカー定量装置3の使用時の動作について図8を参照して説明する。
まず、検体性状測定工程S110において、第2実施形態のマーカー定量装置2と同様に検体重量測定機構10によって検体の重量が測定され、便重量W1が算出される(検体重量測定工程S10)。
【0055】
検体重量測定工程S10に続いて、光学的測定機構80によって検体に含有される水分量が測定される(光学的測定工程S80)。具体的には、図7に示すように発光部81における照明光量I1と受光部82における測定光量I2から、検体容器100および検体Tの透過率(I2/I1)が測定される。
【0056】
これは、便の水分量の状態、例えば下痢便か便秘便かの程度を表す。便の水分量と便の腸内滞留時間との間には負の相関性がある。また上述のように便の腸内滞留時間と便中の大腸上皮細胞数との間には正の相関がある。したがって、透過率(I2/I1)と便中の大腸上皮細胞数との間には不の相関性がある。
補正値算出部120では、第1実施形態と同様の便重量W1の逆数と、上述の透過率(I2/I1)とが補正値として採用され、I2/(I1×W1)が補正値となる(補正値算出工程S120)。
【0057】
マーカー抽出部50では、第2実施形態と同様に検体中のmRNAが抽出される(マーカー抽出工程S50)。マーカー抽出部50において抽出されたmRNAは、直ちにマーカー検出部60へと搬送される。
【0058】
以下では、本実施形態のマーカー検出工程S60に適用可能な一例を示す。なお、マーカー検出工程S50は、疾患関連マーカーを検出する適宜の手法を採用することができ、以下に説明する一例に限定されるものではない。
【0059】
マーカー抽出工程S50において抽出されたmRNAは、所定体積の緩衝液にmRNAが溶解された状態でマーカー検出部60に搬送される。マーカー検出部60では、所定容量のmRNA/緩衝液溶液を出発物質として増幅反応が行なわれる。この増幅反応には、例えば検査対象となる疾患関連mRNAに対して特異性を有する合成オリゴ(プライマー)を用いてRT−PCR、あるいはRealTime−RT−PCRを行う。このとき、mRNA/緩衝液溶液を段階希釈して希釈系列を構成して増幅反応を行ってもよい。
増幅反応によって、所定体積の検体から抽出されたmRNAに含有された疾患関連mRNAが特異的に増幅され疾患関連mRNAの発現量E1が定量される。
【0060】
マーカー検出工程S60で検出された発現量E1は、補正値算出部120において算出された上述の補正値であるI2/(I1×W1)が乗じられてその結果が表示部40に表示される。
【0061】
本実施形態のマーカー定量装置3においても、第1実施形態の検体補正機構1と同様に検体補正機構101によって生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0062】
さらに、検体補正機構101には光学的測定機構80が設けられているので、検体に含有される水分量に対する補正がさらになされている。このため、疾患関連マーカーを定量する精度が高まる。
【0063】
また、マーカー抽出部50およびマーカー検出部60がマーカー定量装置3に一体に構成されているので、採取された検体の重量および透過率が測定されてから補正後の結果が表示されるまでの工程を人手が介在することなく自動化することができる。
【0064】
(変形例)
以下では、本実施形態のマーカー定量装置3の変形例の構成について図9を参照して説明する。図9は、本変形例のマーカー定量装置の一部の構成を一部断面で示す平面図で、光学的測定機構80に代えて設けられた光学的測定機構80aの概略構成を示している。
図9に示すように、光学的測定機構80aは、検体容器100の側壁100c側に発光部81aと受光部82aとがともに配置されている点で光学的測定機構80と構成が異なっている。
【0065】
すなわち、本変形例の光学的測定機構80aは、発光部81aから検体Tに向けて照射される測定光Laが検体Tあるいは側壁100cにおいて反射された反射光を受光部82aにおいて検出するものである。
【0066】
このような構成であっても、検体Tにおける光の反射率を検出することで検体容器100の内部に収容された検体Tの濃度(すなわち含水率)を測定することができる。
【0067】
(第4実施形態)
次に、本発明の第4実施形態のマーカー定量装置について図10ないし図12(B)を参照して説明する。図10は、本実施形態のマーカー定量装置の構成を示すブロック図である。また、図11はマーカー定量装置4の一部の構成を詳細に示すブロック図である。
本実施形態のマーカー定量装置4は、第3実施形態のマーカー定量装置3に対して、光学的測定機構80に代えて光学的測定機構180を備えている点で構成が異なっている。
【0068】
図12(A)は、マーカー定量装置4の一部の構成を一部断面で示す側面図で、光学的測定機構180の構成を示している。図11及ぶ図12(A)に示すように、光学的測定機構180は、検体容器100における開口部100aから底部100bまでの間で所定間隔置きに配置された複数の発光部181と、発光部181のそれぞれに対応して配置された受光部182と、検体Tの固形成分を検体容器100の底部100bに沈殿させる分離部183と、を有している。
【0069】
さらに、発光部181と受光部182と分離部183とはそれぞれ光学測定制御部184に電気的に接続されて制御されている。
【0070】
発光部181と受光部182とにおけるそれぞれの構成は発光部81と受光部82との構成と同様である。
【0071】
分離部183は、検体容器100に対して開口部100aから底部100bへ向かう1G以上の重力を生じさせるもので、例えば所定の回転中心を旋回の中心として旋回動作するローターを有する遠心分離装置を好適に適用することができる。
【0072】
図12(B)は、マーカー定量装置4の使用時の動作を示す図で、光学的測定機構180の使用時の一過程を示している。図12(B)に示すように、検体容器100の内部に収容された検体Tは、分離部183によって底部100bに固形成分Taが、開口部100a側には上清である液体成分Tbが位置するように層をなして分離されている。
【0073】
ここで、固形成分Taの量は検体容器100における底部100bからの高さに比例している。光学的測定機構180では、固形成分Taによって測定光が遮光される領域と、液体成分Tbによって測定光が透過する領域とに分かれる。
【0074】
また、光学的測定機構180に設けられた発光部181、受光部182の一対における測定光の通過領域に固形成分Taと液体成分Tbとの界面が位置しているときには、測定光の通過領域を遮光する量に比例して受光部182における測定光の受光量が減衰する。
このため、光学的測定機構180によれば、検体容器100の内部に収容された検体Tの固形成分Taが検体容器100の底部100bからどれだけの高さにあるかを測定することができる。
【0075】
この測定結果は、検体容器100に収容された検体Tの固形成分が検体容器中で均一に分散されている場合の吸光度に対して正の相関性を有する。補正値算出部120では、この高さに基づいて、検体重量測定機構10による測定結果を合わせて後続の補正演算部30で用いられる補正値を算出する。
【0076】
本実施形態のマーカー定量装置4においても第1実施形態の検体補正機構1と同様に検体補正機構101によって生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0077】
また、光学的測定機構80に代えて設けられた光学的測定機構180は検体Tの固形成分Taと液体成分Tbとを分離して固形成分Taを検体容器100の底部100bに沈殿させることができる。さらに、検体容器100の深さ方向に所定間隔置きに発光部181と受光部182との対が設けられている。このため、検体容器100の内部に収容された検体Tが検体容器100中で均一に分散し得ない性状であってもその濃度(すなわち含水率)を精度よく測定することができる。
【0078】
次に、以下に示す実施例に基づいて、本発明の検体補正機構およびマーカー定量装置についてより詳細に説明する。
【実施例1】
【0079】
図13(A)は、本実施例のマーカー定量装置の一部の概略構成を示す構成図である。また、図13(B)は本実施例のマーカー定量装置の一部の構成を示す斜視図である。本実施例では、本発明の第3実施形態のマーカー定量装置3のより具体的な構成の一例を示す。
【0080】
図13(A)及び図13(B)に示すように、マーカー抽出部50は、検体容器100(図4参照)内の検体Tに対する所定の抽出反応を行うための試薬を供給する図示しない試薬供給部51と、検体容器100を所定の回転中心O1回りに旋回動作させる遠心/攪拌ユニット52と、遠心/攪拌ユニット52によって遠心分離された後に検体容器100内に生じる上清を所定のプロトコールに従って回収あるいは廃棄するための図示しないロボットハンド部53および液体処理部54とを有している。なお、遠心/攪拌ユニット52は、検体容器100を上記旋回軸回りに時計回りおよび反時計回りに交互に回動することによって検体容器100を振動可能であり、検体容器100の内容物(例えば検体Tの溶液)を攪拌することができる。
【0081】
図13(B)は、遠心/攪拌ユニット52の概略構成を示す斜視図である。図13(B)に示すように、遠心/攪拌ユニット52は、回転中心O1回りに回転動作自在な回転軸52aと、回転軸52aを回転動作させるモーターMと、回転軸52aに固定されており回転軸52aの径方向外側に向かって延びて形成された略円板状のターンテーブル52bと、を有している。さらに、遠心/攪拌ユニット52は、ターンテーブル52bに対して着脱自在であって検体容器100を搭載するためのバケット55を有している。
【0082】
図14は、遠心/攪拌ユニット52におけるバケット55付近の構成を一部断面視で示す側面図である。図14に示すように、バケット55は、ターンテーブル52bに着脱自在に連結され容器形状に形成された外枠55aと、外枠55aの内部に配置され光透過性を有する素材によって容器形状に形成された内枠55bとを有している。内枠55bの内部には、検体容器100が配置可能である。
【0083】
検体重量測機構10はバケット55の底部に配置されており、測定部11として内枠55bの距離変位を測定するための静電容量センサが設けられ、重量算出部12として測定部11(静電容量センサ)から出力される出力値を重量に換算する演算回路(不図示)を有している。また、内枠55bにおいて測定部11に対向する面には導体からなる基準部10aが設けられており、測定部11に対するグランド電位が流れている。
【0084】
また、外枠55aと内枠55bとの間には、弾性部材10bが介在されている。弾性部材10bは、検体容器100および内枠55bの重量に応じて所定のバネ定数を有する例えばコイルスプリングなどのバネ材を採用することができる。弾性部材10bのバネ定数は測定対象に応じて適宜選択することができる。
【0085】
測定部11は、所定の基準位置から測定対象物が変位する際の変位量に基づいた出力値を出力するセンサであり、本実施例では、弾性部材10bの自然長が基準位置として設定されている。
【0086】
内枠55bと検体重量測機構10とは外枠55a内において相対的に近接・離間動作可能である。具体的には、検体重量測定機構10とバケット55とは、重力の方向に沿って相対的に直線動作し、内枠55bの重量が弾性部材10bに作用する。このため、内枠55bおよび内枠55bに収容された検体容器100(および検体容器100内の検体T)の重量に応じて弾性部材10bが収縮する。測定部11(静電容量センサ)では、上述の基準位置からの内枠55bの変位量が測定され、弾性部材10bの反発力と上記重量とが平衡状態となった位置における変位量が出力値として重量算出部12(演算回路)へと出力される。
【0087】
光学的測定機構80は、バケット55の内部に配置され、発光部81および受光部82は内枠55bに固定されている。すなわち発光部81および受光部82の重量は内枠55bの重量に含まれている。光学的測定機構80を構成する部材のうち内枠55bに配置された部材は検体重量測機構10において重量既知の部分として差し引き可能である。
光学的測定機構80の発光部81から照射される測定光Lは、内枠55bを透過して検体容器100に入射し、受光部82で受光される。
【0088】
また検体重量測定機構10および光学的測定機構80における信号・電源線Cは、バケット55とターンテーブル52bとの間で揺動の軸に設けられたロータリーコネクタ52cを介して接続されている。
【0089】
本実施例では、検体重量測定機構10における測定部11に静電容量センサが採用されているため、検体重量測定機構10を小型化することができる。このため、バケット55の内部に検体重量測定機構10を配置することができ、検体の性状を測定する際に検体容器を移動させる必要がない。したがって、検体重量測定工程にかかる時間を好適に短縮することができるとともに、検体の性状の測定を高精度に行うことができる。
また、検体重量測定機構10と光学的測定機構80とがマーカー抽出部50におけるバケット55の内部に構成されている。このため、検体Tの重量測定と光学的測定とが行われた後に検体容器100を移動させることなくマーカー抽出工程S50を行うことができる。
【0090】
また、本実施例で示した遠心/攪拌ユニット52は、上述のように検体容器100の内容物を攪拌可能であるので、均一に攪拌された検体Tを速やかに光学的測定機構80で測定することができる。このため、光学的測定を高精度で行うことができる。
【0091】
なお、本実施例で示した構成は、第3実施形態のマーカー定量装置3に対してだけでなく、上述の各実施形態に示した検体重量測定機構10として適宜適用することができる。
【0092】
例えば、第1実施形態の検体補正機構1に本実施例の構成である静電容量センサ(測定部11)を用いた検体重量測定機構を適用した場合には、一般的な電子天秤に比して検体重量測定機構を小型に構成することができる。その結果、上述と同様に検体重量測定工程において検体を移動せず検体性状を測定することが出来るので、一連の工程に要する時間の短縮ができ、また検出精度を向上させることができる。
【0093】
また、本実施例の構成を第2実施形態のマーカー定量装置2に適用した場合には、検体容器100がマーカー抽出部50におけるバケット55に予め搭載された状態で検体の重量を測定することができる。このため、検体重量測定工程S10からマーカー抽出工程S50の間における検体容器100の移動が不要であり、工程に要する時間を短縮することができる。
【0094】
また、本実施例の構成を第4実施形態のマーカー定量装置4に適用した場合には、マーカー抽出部50の遠心/攪拌ユニット52と分離部183とは一台で兼用することができる。さらに、遠心分離によって検体Tの固形成分Taと液体成分Tbとが分離された後に検体容器100の移動が不要であるので、検体Tの固形成分Taが十分に沈殿した状態で光学的測定機構180を作用させることができる。このため、高精度な光学的測定を行うことができる。
【実施例2】
【0095】
以下では、本発明のマーカー定量装置の実施例2について図15を参照して説明する。
図15は、本実施例のマーカー定量装置の一部の構成を示す斜視図である。図14に示すように、本実施例では、上述の実施例1とは異なる構成を有する検体重量測定機構10を有している。
【0096】
検体重量測定機構10は、実施例1と同様に弾性部材10bと、測定部11(静電容量センサ)と、重量算出部12とを有している。また、本実施例では、一端14aと他端14bとを有するとともに中間部に支点14cを有するてこ14をさらに有している。本実施例のてこ14は、支点14cから一端14aまでの長さは支点14cから他端14bまでの長さよりも短く構成されている。
【0097】
本実施例では、てこ14の一端14aは弾性部材10b側に延びており、弾性部材10bの伸縮によって一端14aが例えば図15に示す移動量Xだけ移動すると、一端14aの移動量に比例した移動量Yだけ他端14bが移動する。
【0098】
また、てこ14の他端14bは導体を有しており、測定部11(静電容量センサ)のグランド電位が流れている。このため、てこ14の他端14bと測定部11との距離が変化することで他端14bと測定部11との間の静電容量が変化する。
【0099】
本実施例では、バケット55が弾性部材10bに接触して弾性部材10bが収縮する長さに比例する長さだけてこ14の他端14bを移動させることができる。本実施例では支点14cから一端14aまでの長さが支点14cから他端14bまでの長さよりも短いので、一端14aの移動量よりも他端14bの移動量のほうが大きい。このため、検体Tの重量をより精度よく測定することができる。
【0100】
以上、本発明の実施形態について図面を参照して詳述したが、具体的な構成はこの実施形態に限られるものではなく、本発明の要旨を逸脱しない範囲の設計変更等も含まれる。
例えば、上記各実施形態に示したように、検体補正機構およびマーカー定量装置における構成は一体化していてもよく、また機能ブロックとして別体に構成されていても良い。さらに、上述した構成例以外にも構成要素を適宜一体化、または分離して設けることができる。
【0101】
また、上述の各実施形態では疾患関連マーカーとしてmRNAの発現量を測定する例を示したが、これに限らず、適宜のマーカー検出装置が採用されることで疾患関連のmRNA及びDNAの変異、欠失、あるいはメチレーションをマーカーとして検出することもできる。また、疾患関連遺伝子の翻訳産物であるタンパク質に対しても適宜の抽出/検出装置が採用されることで同様の効果が得られる。
【0102】
また、上述の実施形態及び変形例において示した構成要素は適宜に組み合わせて構成することが可能である。
たとえば、第4実施形態で説明したマーカー定量装置4における複数の発光部181と複数の受光部182との組み合わせは、第3実施形態のマーカー定量装置3における発光部81と受光部82との組み合わせと置き換えてマーカー定量装置3に設けることができる。
【0103】
また、上述の実施例で説明した遠心/攪拌ユニット52は、遠心分離の機能と攪拌の機能とのそれぞれを別々あるいは一体として、第1実施形態に記載の検体補正機構1や、第2実施形態に記載のマーカー定量装置2に設けられても良い。これにより、検体容器100に収容された検体を好適に分離あるいは攪拌できる。
【産業上の利用可能性】
【0104】
本発明の検体補正機構は、生体から採取される検体を分析する分析装置に対して好適に適用可能である。特に、個人間、日内変動、あるいはその他要因で性状が変動する生体試料において疾患関連マーカーを検出する臨床検査装置に対してより好適に適用することができる。
【符号の説明】
【0105】
1、101 検体補正機構
2、3、4 マーカー定量装置
10 検体重量測定機構(検体性状測定部)
11 測定部
12 重量算出部
20、120 補正値算出部
30 補正演算部
40 表示部
50 マーカー抽出部
60 マーカー検出部
80、80a、180 光学的測定機構
81、81a、181 発光部
82、82a、182 受光部
100 検体容器
100a 開口部
100b 底部
110 検体性状測定部
【技術分野】
【0001】
本発明は、検体補正機構およびマーカー定量装置に関する。
【背景技術】
【0002】
従来、生体から採取される生体試料を分析して疾患の検査や診断を行うことが知られている。例えば、特許文献1には、生体試料の一形態である糞便を用いて便潜血の診断を行う際に用いられる器具である糞便採取容器が開示されている。
特許文献1に記載の糞便採取容器は、先端に切欠部、凹部、または貫通孔の少なくともひとつを有して先端において糞便を採取する採取棒と、採取棒が挿通される穴を有するとともに糞便を懸濁させるための液体を収容しうる容器本体とを備え、採取棒を容器本体の穴に挿通することで所定体積の糞便を容易に採取できる。
【0003】
また、特許文献2には、便潜血検査方法が開示されている。この特許文献2に記載の便潜血検査方法は、糞便の乾燥重量に相関し糞便の含水率に逆相関する指標として糞便中に存在する常在物質の濃度を測定することを特徴としている。また、特許文献2には、常在物質の濃度を測定する方法として、糞便懸濁液に対して照射された波長既知の光線の吸光度を測定する方法が開示されている。特許文献2に記載の便潜血検査方法によれば、便の含水率に逆相関的する便潜血量のデータに対して常在物質の濃度によって補正をかけることができるので、便の性状の個人差や日々の変動によらず精度よく便潜血検査ができる。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】実公平05−017652号公報
【特許文献2】国際公開第01/061343号パンフレット
【発明の概要】
【発明が解決しようとする課題】
【0005】
近年の遺伝子解析技術の発達に伴い、疾患に関連するDNAや、疾患に関連するDNAからの転写産物である疾患関連マーカー(mRNA)に基づいて疾患の有無を診断する方法が注目されている。ここで、生体試料中の疾患関連マーカーの量に基づいて疾患を診断するためには、生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量が標準化されていることを要する。
糞便中における被験者由来細胞は、主に新陳代謝で便中に剥離したものである。体調等により便の滞留時間が長くなることで水分量が減少する。また、繊維量が多いと便通が良くなり便の滞留時間が短くなる。このため、糞便中の被験者由来細胞数は便の通過時間に相関する。
【0006】
しかしながら、特許文献1に記載の糞便採取容器および特許文献2に記載の便潜血検査方法では、便の通過時間に相関する指標がないため、糞便中に存在する被験者由来細胞の数に相関する情報を得ることができなかった。このため、単位細胞数当たりの疾患関連遺伝子の発現量の情報を得ることは困難であった。
【0007】
本発明は、上述した事情に鑑みてなされたものであって、その目的は生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる検体補正機構およびマーカー定量装置の提供を図ることにある。
【課題を解決するための手段】
【0008】
上記課題を解決するために、この発明は以下の手段を提案している。
本発明の検体補正機構は、生体試料を含有する検体における単位体積あたりの疾患関連マーカー含有量を前記検体に含有される単位細胞数あたりの前記疾患関連マーカー含有量に補正する検体補正機構であって、前記検体の性状を測定する検体性状測定部と、前記検体性状測定部による測定結果に基づく補正値を算出する補正値算出部と、前記単位体積あたりの前記疾患関連マーカー含有量と前記補正値とに基づいて前記単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部と、を備えることを特徴としている。
なお、本発明において、検体の性状とは、検体の物理的特性を指し、例えば検体の重量、固形成分の割合、および比重などである。
【0009】
また、前記検体性状測定部は、前記検体の重量を測定する検体重量測定機構を有することが好ましい。
【0010】
また、前記検体重量測定機構は、前記検体が収容され重量既知の検体容器と前記検体とをあわせて重量測定して前記検体容器と前記検体との合計重量を測定する測定部と、前記合計重量から前記検体容器の重量を差し引いて前記検体の正味重量を算出する重量算出部と、を有することが好ましい。
【0011】
また、前記検体性状測定部は、前記検体が収容され少なくとも一部において光線が透過可能な検体容器に対して照射される光線の減衰量に基づいて前記検体容器中の固形成分の含有率を測定する光学的測定機構を有することが好ましい。
【0012】
また、前記光学的測定機構は、前記検体容器の外部から内部方向へ測定光を照射する発光部と、前記検体容器を挟んで前記発光部と反対側に設けられて前記検体容器及び前記検体を透過した前記測定光を受光する受光部と、を有することが好ましい。
【0013】
また、前記光学的測定機構は、前記検体容器の外部から内部方向へ測定光を照射する発光部と、前記検体容器に対して前記発光部と同じ側に設けられて前記検体容器及び前記検体によって反射された前記測定光を受光する受光部と、を有していてもよい。
【0014】
また、前記光学的測定機構は、前記検体容器における開口から底までの間で所定間隔置きに配置された複数の前記発光部と、前記発光部のそれぞれに対応して配置された前記受光部と、をさらに有していることが好ましい。
【0015】
また、本発明の検体補正機構は、前記検体容器に対して開口から底へ向かう1G以上の重力を生じさせて前記検体の固形成分を前記検体容器の底に沈殿させる分離部をさらに有していることが好ましい。
【0016】
本発明のマーカー定量装置は、本発明の検体補正機構と、前記検体から前記疾患関連マーカーを抽出するマーカー抽出部と、を備えることを特徴としている。
【0017】
また、本発明のマーカー定量装置は、前記検体の単位体積あたりの前記疾患関連マーカーの含有量を検出するマーカー検出部をさらに備えることが好ましい。
【発明の効果】
【0018】
本発明の検体補正機構およびマーカー定量装置によれば、生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【図面の簡単な説明】
【0019】
【図1】本発明の第1実施形態の検体補正機構の構成を示すブロック図である。
【図2】同検体補正機構の一部の構成を示すブロック図である。
【図3】同検体補正機構の使用時の動作を示すフローチャートである。
【図4】本発明の第2実施形態のマーカー定量装置の構成を示すブロック図である。
【図5】同マーカー定量装置の使用時の動作を示すフローチャートである。
【図6】本発明の第3実施形態のマーカー定量装置の構成を示すブロック図である。
【図7】同マーカー定量装置の一部の構成を一部断面視で示す側面図である。
【図8】同マーカー定量装置の使用時の動作を示すフローチャートである。
【図9】同マーカー定量装置の変形例における一部の構成を示す平面図である。
【図10】本発明の第4実施形態のマーカー定量装置の構成を示すブロック図である。
【図11】同マーカー定量装置の一部の構成を詳細に示すブロック図である。
【図12】(A)は同マーカー定量装置の一部の構成を一部断面視で示す側面図、(B)は同マーカー定量装置の使用時の動作を一部断面視で示す側面図である。
【図13】(A)は本発明のマーカー定量装置の実施例1を示すブロック図、(B)は実施例1のマーカー定量装置の一部の構成を示す斜視図である。
【図14】実施例1のマーカー定量装置の一部の構成を一部断面視で示す側面図である。
【図15】本発明のマーカー定量装置の実施例2を一部断面視で示す側面図である。
【発明を実施するための形態】
【0020】
(第1実施形態)
以下、本発明の第1実施形態の検体補正機構について図1ないし図3を参照して説明する。図1は本発明の第1実施形態の検体補正機構1の構成を示すブロック図である。また、図2は検体補正機構1の一部の構成を示すブロック図である。
検体補正機構1は、生態から採取される一定体積の試料、具体的には一定体積の糞便試料を検体とする解析に好適に採用できる機構である。
【0021】
図1に示すように、本実施形態の検体補正機構1は、検体の性状を測定する検体重量測定機構(検体性状測定部)10と、検体性状測定部による測定結果に基づく補正値を算出する補正値算出部20と、補正値算出部20によって算出された補正値に基づいて単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部30と、を備えている。
【0022】
また、本実施形態の検体補正機構1は、補正演算部30と電気的に接続されて算出結果を表示するための表示装置400と、検体から疾患関連マーカーを含むmRNAを抽出するためのマーカー抽出装置500と、マーカー抽出装置500によって抽出されたmRNAから疾患関連マーカーを検出するためのマーカー検出装置600と共に使用される。
マーカー検出装置600では、検体の全量に対する疾患関連マーカーの含有量が定量的に検出される。
なお、本実施形態では、マーカー抽出装置500と、マーカー検出装置600とは、それぞれ適用可能な周知のマーカー抽出装置あるいはマーカー検出装置を適宜採用することができる。
【0023】
検体重量測定機構10は、検体性状測定部の一例であり、検体の重量を測定して重量情報を補正値算出部20に送信する機構である。検体重量測定機構10は、検体の重量を測定する測定部11と、測定部11において測定された値に基づいて検体の正味重量を算出する重量算出部12と、を有している。
【0024】
検体は図示しない重量既知の検体容器に収容されており、測定部11は検体容器と検体とをあわせて測定することで検体容器と検体との合計重量を測定する。例えば、測定部11には電子天秤等の秤量機器を採用することができる。
重量算出部12は、上述の合計重量から検体容器の重量を差し引く演算を行って、その結果を検体の正味重量として補正値算出部20に送信する。
【0025】
補正値算出部20は、検体重量測定機構10から送信された上述の正味重量に基づいて補正値を算出する。具体的には、補正値は正味重量の逆数である。
【0026】
補正演算部30は、上記マーカー検出装置600によって検出された疾患関連マーカーの含有量に上述の補正値を乗じて演算する回路である。
【0027】
以下では、検体補正機構1の作用について詳述する。図3は検体補正機構1の使用時の動作を示すフローチャートである。以下では、検体として糞便試料を使用する例を示すが、検体としては他の生体試料を用いることもできる。
【0028】
本実施形態では、糞便試料は一定体積の糞便を採便できる周知の採便棒によって採取され、所定容量の保存液が収容された上述の検体容器にともに収容されている。
【0029】
本実施形態で検査対象となる疾患関連マーカーは、患部における細胞に特異的に発現する遺伝子からの転写産物(疾患関連mRNA)などである。例えば大腸癌に関連性の高いmRNAを発現する大腸上皮細胞は、主に新陳代謝によって剥離して便に所定数だけ含まれている。このとき腸内の便の滞留時間が長くなると、便中に剥離してくる大腸上皮細胞数が便の滞留時間に比例して増加する。また、腸内における便の滞留時間が長くなると、腸の作用による水分再吸収により便が固く、かつ重くなる傾向になる。
【0030】
本実施形態では、腸内における便の滞留時間と便の重量との間の正の相関性に着目し、便の重量に基づく補正値を用いて一定体積の便検体に含まれる剥離細胞数を標準化している。
【0031】
具体的には、まず、便重量W1+保存液重量W2+保存ケース重量W3の合計質量Wを検体重量測定機構10の測定部11において測定する(検体重量測定工程S10)。
【0032】
続いて、マーカー抽出装置500において、検体容器に収容された検体の全量を用いて所定のプロセスによってTotal RNAを抽出し、mRNAを精製する。
続いて、マーカー検出装置600では、上述のTotal RNAに対してoligo dTプライマーによってmRNA特異的に逆転写反応が行われる。これにより、検体T中に存在するmRNA(疾患関連マーカーを含む)に対して安定的なcDNAが合成される。
【0033】
さらに、マーカー検出装置600では、所定容量のcDNA/緩衝液溶液を出発物質として増幅反応が行なわれる。この増幅反応には、例えば検査対象となる疾患関連mRNAに対して特異性を有する合成オリゴ(プライマー)を用いてRT−PCR、あるいはRealTime−RT−PCRを行う。このとき、cDNA/緩衝液溶液を段階希釈して希釈系列を構成して増幅反応を行ってもよい。
増幅反応によって、所定体積の検体から抽出されたmRNAに含有された疾患関連mRNAが特異的に増幅され疾患関連mRNAの発現量E1が定量される。
【0034】
続いて、補正演算部30において、上記合計質量Wと、発現量E1とがともに入力される。保存液重量W2、保存ケース重量W3は予め定められて用意されているのでそれぞれ一定値である。このため、測定部11で計測された合計質量Wから保存液重量W2、保存ケース重量W3を減算することで便質量(正味重量)W1が算出される。
【0035】
発現量E1は、検査対象mRNAを発現する便中に剥離した大腸上皮細胞数に相関性があり、また便中に剥離した大腸上皮細胞数は大腸内の滞留時間にほぼ比例する。また、被験者の体調等により便の滞留時間が長くなることで水分量が減少する。さらに、便中の繊維量が多いと便通が良くなり便の滞留時間が短くなる。このため、所定体積の糞便試料に対する発現量E1の値は、便の水分量や繊維量に応じてばらつく。このため、所定体積の糞便試料に対する発現量E1という結果に基づいて大腸上皮細胞数に応じた発現量を知るためには、後述する補正が必要になる。
【0036】
補正値算出部20では、検体重量測定機構10から送信された上述の便重量(正味重量)の逆数が算出され、補正値として採用される。補正値は、補正演算部30によって参照される(補正値算出工程S20)。
【0037】
補正演算部30では、疾患関連mRNAの発現量E1に対して、上述の補正値である便重量(正味重量)W1の逆数を乗算する(補正演算工程S30)。腸内における便の滞留時間との間に正の相関性を有する便重量の逆数が補正値として採用されたことで、一定体積の便検体に含まれる剥離細胞数を標準化している。補正演算部30において演算された結果は表示装置400に表示される。
【0038】
以上説明したように、本発明の検体補正機構によれば、所定体積の糞便試料の便重量W1に基づいて、便重量W1の逆数を疾患関連マーカーの発現量E1に乗じている。このため、生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0039】
このため、検体採取量や検体の状態による検査マーカー検出値のバラツキを抑えることができる。例えば下痢便、便秘便による便mRNA検査の検出結果のバラツキを抑えることができるので、一定の細胞量あたりの対象mRNAの発現量を高精度に検出することが可能となる。
【0040】
(第2実施形態)
次に、本発明の第2実施形態のマーカー定量装置について図4および図5を参照して説明する。なお、以下に説明する各実施形態において、上述した第1実施形態の検体補正機構1と構成を共通とする箇所には同一符号を付けて、説明を省略することにする。
【0041】
図4は、本実施形態のマーカー定量装置2の構成を示すブロック図である。マーカー定量装置2は、第1実施形態の検体補正機構1に加えて、マーカー抽出装置500に代えて検体補正機構1と一体的に設けられ、検体から疾患関連マーカーを抽出するマーカー抽出部50を備えている点で上述の第1実施形態と構成が異なっている。
【0042】
図5は、マーカー定量装置2の使用時の動作を示すフローチャートである。図5に示すように、マーカー定量装置2では、補正値算出工程S20と補正演算工程S30との間にマーカー抽出工程S50が介在されている。
【0043】
以下では、本実施形態のマーカー抽出工程S50に適用可能な一例を示す。なお、マーカー抽出工程S50は、疾患関連マーカーを検出可能な状態で抽出する適宜の手法を採用することができ、以下に説明する一例に限定されるものではない。
【0044】
補正値算出工程S20が完了した後で、補正演算工程S30に好適に適用できる補正値が算出されたことが確定した後、検体重量測定工程S10が完了した検体Tの全量が用いられて検体T中のTotal RNAが抽出される。
マーカー抽出工程S50では、Total RNAは緩衝液に溶解された状態で提供される。その後、使用者によって直ちにマーカー検出装置600におけるマーカーの検出に供される。
【0045】
マーカー検出装置600では、第1実施形態と同様に、Total RNAに対してmRNA特異的に逆転写反応が行われる。次に、所定容量のcDNA/緩衝液溶液を出発物質として増幅反応が行なわれる。この増幅反応には、例えば検査対象となる疾患関連mRNAに対して特異性を有する合成オリゴ(プライマー)を用いてRT−PCR、あるいはRealTime−RT−PCRを行う。このとき、cDNA/緩衝液溶液を段階希釈して希釈系列を構成して増幅反応を行ってもよい。
増幅反応によって、所定体積の検体から抽出されたmRNAに含有された疾患関連mRNAが特異的に増幅され疾患関連mRNAの発現量E1が定量される。
【0046】
マーカー検出装置600において検出された検出結果は、第1実施形態と同様に補正演算工程S30において補正値によって補正されて表示装置400において検体Tにおける単位細胞数当たりの疾患関連マーカー発現強度として表示される。
【0047】
本実施形態でも、第1実施形態の検体補正機構1と同様に生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0048】
また、マーカー定量装置2によれば、検体重量測定機構10において検体Tの重量が測定されたのち、直ちにマーカー抽出部50において疾患関連マーカーを含むmRNAが抽出される。マーカー抽出部50において抽出されたmRNAのサンプルは緩衝液内に保存されているため、例えば検体T中に存在するRNase等によるmRNAの分解が抑制されている。このため、マーカー抽出工程S50の後にmRNAのサンプルを凍結保存などの適宜の保存方法によって長期に保存し、一連の工程を中断することができる。その結果、疾患関連マーカーの検出精度を高く維持しつつ一連の工程の時間的な自由度を高めることができる。
【0049】
(第3実施形態)
次に、本発明の第3実施形態のマーカー定量装置について図6ないし図9を参照して説明する。なお、以下に説明する各実施形態において、上述した第1実施形態の検体補正機構1および第2実施形態のマーカー定量装置2と構成を共通とする箇所には同一符号を付けて、説明を省略することにする。
【0050】
図6は、本実施形態のマーカー定量装置3の構成を示すブロック図である。また、図7はマーカー定量装置3の一部の構成を一部断面で示す側面図である。図6および図7に示すように、マーカー定量装置3は、第2実施形態の検体補正機構1に代えて設けられた検体補正機構101と、表示装置400に代えて検体補正機構101と一体的に設けられた表示部40と、マーカー検出装置600に代えて検体補正機構101と一体的に設けられたマーカー検出部60と、を備えている点で上述の第2実施形態と構成が異なっている。
【0051】
検体補正機構101は、第1実施形態の検体重量測定機構10に加えて光学的測定機構80を有する検体性状測定部110と、補正値算出部20に代えて設けられた補正値算出部120とを備えている。
【0052】
光学的測定機構80は、図7に示すように、検体容器100の外部から内部方向へ測定光Lを照射する発光部81と、検体容器100を挟んで発光部81と反対側に設けられて検体容器100及び検体Tを透過した測定光Lを受光する受光部82と、を有している。受光部82では、検体容器100の側壁100c、100dを透過して受光された測定光Lを光電変換することで電気信号にしている。
【0053】
補正値算出部120は、検体重量測定機構10によって測定された結果と光学的測定機構80によって測定された結果との両方に基づく補正値を算出する。
【0054】
以下では、本実施形態のマーカー定量装置3の使用時の動作について図8を参照して説明する。
まず、検体性状測定工程S110において、第2実施形態のマーカー定量装置2と同様に検体重量測定機構10によって検体の重量が測定され、便重量W1が算出される(検体重量測定工程S10)。
【0055】
検体重量測定工程S10に続いて、光学的測定機構80によって検体に含有される水分量が測定される(光学的測定工程S80)。具体的には、図7に示すように発光部81における照明光量I1と受光部82における測定光量I2から、検体容器100および検体Tの透過率(I2/I1)が測定される。
【0056】
これは、便の水分量の状態、例えば下痢便か便秘便かの程度を表す。便の水分量と便の腸内滞留時間との間には負の相関性がある。また上述のように便の腸内滞留時間と便中の大腸上皮細胞数との間には正の相関がある。したがって、透過率(I2/I1)と便中の大腸上皮細胞数との間には不の相関性がある。
補正値算出部120では、第1実施形態と同様の便重量W1の逆数と、上述の透過率(I2/I1)とが補正値として採用され、I2/(I1×W1)が補正値となる(補正値算出工程S120)。
【0057】
マーカー抽出部50では、第2実施形態と同様に検体中のmRNAが抽出される(マーカー抽出工程S50)。マーカー抽出部50において抽出されたmRNAは、直ちにマーカー検出部60へと搬送される。
【0058】
以下では、本実施形態のマーカー検出工程S60に適用可能な一例を示す。なお、マーカー検出工程S50は、疾患関連マーカーを検出する適宜の手法を採用することができ、以下に説明する一例に限定されるものではない。
【0059】
マーカー抽出工程S50において抽出されたmRNAは、所定体積の緩衝液にmRNAが溶解された状態でマーカー検出部60に搬送される。マーカー検出部60では、所定容量のmRNA/緩衝液溶液を出発物質として増幅反応が行なわれる。この増幅反応には、例えば検査対象となる疾患関連mRNAに対して特異性を有する合成オリゴ(プライマー)を用いてRT−PCR、あるいはRealTime−RT−PCRを行う。このとき、mRNA/緩衝液溶液を段階希釈して希釈系列を構成して増幅反応を行ってもよい。
増幅反応によって、所定体積の検体から抽出されたmRNAに含有された疾患関連mRNAが特異的に増幅され疾患関連mRNAの発現量E1が定量される。
【0060】
マーカー検出工程S60で検出された発現量E1は、補正値算出部120において算出された上述の補正値であるI2/(I1×W1)が乗じられてその結果が表示部40に表示される。
【0061】
本実施形態のマーカー定量装置3においても、第1実施形態の検体補正機構1と同様に検体補正機構101によって生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0062】
さらに、検体補正機構101には光学的測定機構80が設けられているので、検体に含有される水分量に対する補正がさらになされている。このため、疾患関連マーカーを定量する精度が高まる。
【0063】
また、マーカー抽出部50およびマーカー検出部60がマーカー定量装置3に一体に構成されているので、採取された検体の重量および透過率が測定されてから補正後の結果が表示されるまでの工程を人手が介在することなく自動化することができる。
【0064】
(変形例)
以下では、本実施形態のマーカー定量装置3の変形例の構成について図9を参照して説明する。図9は、本変形例のマーカー定量装置の一部の構成を一部断面で示す平面図で、光学的測定機構80に代えて設けられた光学的測定機構80aの概略構成を示している。
図9に示すように、光学的測定機構80aは、検体容器100の側壁100c側に発光部81aと受光部82aとがともに配置されている点で光学的測定機構80と構成が異なっている。
【0065】
すなわち、本変形例の光学的測定機構80aは、発光部81aから検体Tに向けて照射される測定光Laが検体Tあるいは側壁100cにおいて反射された反射光を受光部82aにおいて検出するものである。
【0066】
このような構成であっても、検体Tにおける光の反射率を検出することで検体容器100の内部に収容された検体Tの濃度(すなわち含水率)を測定することができる。
【0067】
(第4実施形態)
次に、本発明の第4実施形態のマーカー定量装置について図10ないし図12(B)を参照して説明する。図10は、本実施形態のマーカー定量装置の構成を示すブロック図である。また、図11はマーカー定量装置4の一部の構成を詳細に示すブロック図である。
本実施形態のマーカー定量装置4は、第3実施形態のマーカー定量装置3に対して、光学的測定機構80に代えて光学的測定機構180を備えている点で構成が異なっている。
【0068】
図12(A)は、マーカー定量装置4の一部の構成を一部断面で示す側面図で、光学的測定機構180の構成を示している。図11及ぶ図12(A)に示すように、光学的測定機構180は、検体容器100における開口部100aから底部100bまでの間で所定間隔置きに配置された複数の発光部181と、発光部181のそれぞれに対応して配置された受光部182と、検体Tの固形成分を検体容器100の底部100bに沈殿させる分離部183と、を有している。
【0069】
さらに、発光部181と受光部182と分離部183とはそれぞれ光学測定制御部184に電気的に接続されて制御されている。
【0070】
発光部181と受光部182とにおけるそれぞれの構成は発光部81と受光部82との構成と同様である。
【0071】
分離部183は、検体容器100に対して開口部100aから底部100bへ向かう1G以上の重力を生じさせるもので、例えば所定の回転中心を旋回の中心として旋回動作するローターを有する遠心分離装置を好適に適用することができる。
【0072】
図12(B)は、マーカー定量装置4の使用時の動作を示す図で、光学的測定機構180の使用時の一過程を示している。図12(B)に示すように、検体容器100の内部に収容された検体Tは、分離部183によって底部100bに固形成分Taが、開口部100a側には上清である液体成分Tbが位置するように層をなして分離されている。
【0073】
ここで、固形成分Taの量は検体容器100における底部100bからの高さに比例している。光学的測定機構180では、固形成分Taによって測定光が遮光される領域と、液体成分Tbによって測定光が透過する領域とに分かれる。
【0074】
また、光学的測定機構180に設けられた発光部181、受光部182の一対における測定光の通過領域に固形成分Taと液体成分Tbとの界面が位置しているときには、測定光の通過領域を遮光する量に比例して受光部182における測定光の受光量が減衰する。
このため、光学的測定機構180によれば、検体容器100の内部に収容された検体Tの固形成分Taが検体容器100の底部100bからどれだけの高さにあるかを測定することができる。
【0075】
この測定結果は、検体容器100に収容された検体Tの固形成分が検体容器中で均一に分散されている場合の吸光度に対して正の相関性を有する。補正値算出部120では、この高さに基づいて、検体重量測定機構10による測定結果を合わせて後続の補正演算部30で用いられる補正値を算出する。
【0076】
本実施形態のマーカー定量装置4においても第1実施形態の検体補正機構1と同様に検体補正機構101によって生体試料中に存在する被験者由来細胞の数によって疾患関連マーカーの量を標準化できる。
【0077】
また、光学的測定機構80に代えて設けられた光学的測定機構180は検体Tの固形成分Taと液体成分Tbとを分離して固形成分Taを検体容器100の底部100bに沈殿させることができる。さらに、検体容器100の深さ方向に所定間隔置きに発光部181と受光部182との対が設けられている。このため、検体容器100の内部に収容された検体Tが検体容器100中で均一に分散し得ない性状であってもその濃度(すなわち含水率)を精度よく測定することができる。
【0078】
次に、以下に示す実施例に基づいて、本発明の検体補正機構およびマーカー定量装置についてより詳細に説明する。
【実施例1】
【0079】
図13(A)は、本実施例のマーカー定量装置の一部の概略構成を示す構成図である。また、図13(B)は本実施例のマーカー定量装置の一部の構成を示す斜視図である。本実施例では、本発明の第3実施形態のマーカー定量装置3のより具体的な構成の一例を示す。
【0080】
図13(A)及び図13(B)に示すように、マーカー抽出部50は、検体容器100(図4参照)内の検体Tに対する所定の抽出反応を行うための試薬を供給する図示しない試薬供給部51と、検体容器100を所定の回転中心O1回りに旋回動作させる遠心/攪拌ユニット52と、遠心/攪拌ユニット52によって遠心分離された後に検体容器100内に生じる上清を所定のプロトコールに従って回収あるいは廃棄するための図示しないロボットハンド部53および液体処理部54とを有している。なお、遠心/攪拌ユニット52は、検体容器100を上記旋回軸回りに時計回りおよび反時計回りに交互に回動することによって検体容器100を振動可能であり、検体容器100の内容物(例えば検体Tの溶液)を攪拌することができる。
【0081】
図13(B)は、遠心/攪拌ユニット52の概略構成を示す斜視図である。図13(B)に示すように、遠心/攪拌ユニット52は、回転中心O1回りに回転動作自在な回転軸52aと、回転軸52aを回転動作させるモーターMと、回転軸52aに固定されており回転軸52aの径方向外側に向かって延びて形成された略円板状のターンテーブル52bと、を有している。さらに、遠心/攪拌ユニット52は、ターンテーブル52bに対して着脱自在であって検体容器100を搭載するためのバケット55を有している。
【0082】
図14は、遠心/攪拌ユニット52におけるバケット55付近の構成を一部断面視で示す側面図である。図14に示すように、バケット55は、ターンテーブル52bに着脱自在に連結され容器形状に形成された外枠55aと、外枠55aの内部に配置され光透過性を有する素材によって容器形状に形成された内枠55bとを有している。内枠55bの内部には、検体容器100が配置可能である。
【0083】
検体重量測機構10はバケット55の底部に配置されており、測定部11として内枠55bの距離変位を測定するための静電容量センサが設けられ、重量算出部12として測定部11(静電容量センサ)から出力される出力値を重量に換算する演算回路(不図示)を有している。また、内枠55bにおいて測定部11に対向する面には導体からなる基準部10aが設けられており、測定部11に対するグランド電位が流れている。
【0084】
また、外枠55aと内枠55bとの間には、弾性部材10bが介在されている。弾性部材10bは、検体容器100および内枠55bの重量に応じて所定のバネ定数を有する例えばコイルスプリングなどのバネ材を採用することができる。弾性部材10bのバネ定数は測定対象に応じて適宜選択することができる。
【0085】
測定部11は、所定の基準位置から測定対象物が変位する際の変位量に基づいた出力値を出力するセンサであり、本実施例では、弾性部材10bの自然長が基準位置として設定されている。
【0086】
内枠55bと検体重量測機構10とは外枠55a内において相対的に近接・離間動作可能である。具体的には、検体重量測定機構10とバケット55とは、重力の方向に沿って相対的に直線動作し、内枠55bの重量が弾性部材10bに作用する。このため、内枠55bおよび内枠55bに収容された検体容器100(および検体容器100内の検体T)の重量に応じて弾性部材10bが収縮する。測定部11(静電容量センサ)では、上述の基準位置からの内枠55bの変位量が測定され、弾性部材10bの反発力と上記重量とが平衡状態となった位置における変位量が出力値として重量算出部12(演算回路)へと出力される。
【0087】
光学的測定機構80は、バケット55の内部に配置され、発光部81および受光部82は内枠55bに固定されている。すなわち発光部81および受光部82の重量は内枠55bの重量に含まれている。光学的測定機構80を構成する部材のうち内枠55bに配置された部材は検体重量測機構10において重量既知の部分として差し引き可能である。
光学的測定機構80の発光部81から照射される測定光Lは、内枠55bを透過して検体容器100に入射し、受光部82で受光される。
【0088】
また検体重量測定機構10および光学的測定機構80における信号・電源線Cは、バケット55とターンテーブル52bとの間で揺動の軸に設けられたロータリーコネクタ52cを介して接続されている。
【0089】
本実施例では、検体重量測定機構10における測定部11に静電容量センサが採用されているため、検体重量測定機構10を小型化することができる。このため、バケット55の内部に検体重量測定機構10を配置することができ、検体の性状を測定する際に検体容器を移動させる必要がない。したがって、検体重量測定工程にかかる時間を好適に短縮することができるとともに、検体の性状の測定を高精度に行うことができる。
また、検体重量測定機構10と光学的測定機構80とがマーカー抽出部50におけるバケット55の内部に構成されている。このため、検体Tの重量測定と光学的測定とが行われた後に検体容器100を移動させることなくマーカー抽出工程S50を行うことができる。
【0090】
また、本実施例で示した遠心/攪拌ユニット52は、上述のように検体容器100の内容物を攪拌可能であるので、均一に攪拌された検体Tを速やかに光学的測定機構80で測定することができる。このため、光学的測定を高精度で行うことができる。
【0091】
なお、本実施例で示した構成は、第3実施形態のマーカー定量装置3に対してだけでなく、上述の各実施形態に示した検体重量測定機構10として適宜適用することができる。
【0092】
例えば、第1実施形態の検体補正機構1に本実施例の構成である静電容量センサ(測定部11)を用いた検体重量測定機構を適用した場合には、一般的な電子天秤に比して検体重量測定機構を小型に構成することができる。その結果、上述と同様に検体重量測定工程において検体を移動せず検体性状を測定することが出来るので、一連の工程に要する時間の短縮ができ、また検出精度を向上させることができる。
【0093】
また、本実施例の構成を第2実施形態のマーカー定量装置2に適用した場合には、検体容器100がマーカー抽出部50におけるバケット55に予め搭載された状態で検体の重量を測定することができる。このため、検体重量測定工程S10からマーカー抽出工程S50の間における検体容器100の移動が不要であり、工程に要する時間を短縮することができる。
【0094】
また、本実施例の構成を第4実施形態のマーカー定量装置4に適用した場合には、マーカー抽出部50の遠心/攪拌ユニット52と分離部183とは一台で兼用することができる。さらに、遠心分離によって検体Tの固形成分Taと液体成分Tbとが分離された後に検体容器100の移動が不要であるので、検体Tの固形成分Taが十分に沈殿した状態で光学的測定機構180を作用させることができる。このため、高精度な光学的測定を行うことができる。
【実施例2】
【0095】
以下では、本発明のマーカー定量装置の実施例2について図15を参照して説明する。
図15は、本実施例のマーカー定量装置の一部の構成を示す斜視図である。図14に示すように、本実施例では、上述の実施例1とは異なる構成を有する検体重量測定機構10を有している。
【0096】
検体重量測定機構10は、実施例1と同様に弾性部材10bと、測定部11(静電容量センサ)と、重量算出部12とを有している。また、本実施例では、一端14aと他端14bとを有するとともに中間部に支点14cを有するてこ14をさらに有している。本実施例のてこ14は、支点14cから一端14aまでの長さは支点14cから他端14bまでの長さよりも短く構成されている。
【0097】
本実施例では、てこ14の一端14aは弾性部材10b側に延びており、弾性部材10bの伸縮によって一端14aが例えば図15に示す移動量Xだけ移動すると、一端14aの移動量に比例した移動量Yだけ他端14bが移動する。
【0098】
また、てこ14の他端14bは導体を有しており、測定部11(静電容量センサ)のグランド電位が流れている。このため、てこ14の他端14bと測定部11との距離が変化することで他端14bと測定部11との間の静電容量が変化する。
【0099】
本実施例では、バケット55が弾性部材10bに接触して弾性部材10bが収縮する長さに比例する長さだけてこ14の他端14bを移動させることができる。本実施例では支点14cから一端14aまでの長さが支点14cから他端14bまでの長さよりも短いので、一端14aの移動量よりも他端14bの移動量のほうが大きい。このため、検体Tの重量をより精度よく測定することができる。
【0100】
以上、本発明の実施形態について図面を参照して詳述したが、具体的な構成はこの実施形態に限られるものではなく、本発明の要旨を逸脱しない範囲の設計変更等も含まれる。
例えば、上記各実施形態に示したように、検体補正機構およびマーカー定量装置における構成は一体化していてもよく、また機能ブロックとして別体に構成されていても良い。さらに、上述した構成例以外にも構成要素を適宜一体化、または分離して設けることができる。
【0101】
また、上述の各実施形態では疾患関連マーカーとしてmRNAの発現量を測定する例を示したが、これに限らず、適宜のマーカー検出装置が採用されることで疾患関連のmRNA及びDNAの変異、欠失、あるいはメチレーションをマーカーとして検出することもできる。また、疾患関連遺伝子の翻訳産物であるタンパク質に対しても適宜の抽出/検出装置が採用されることで同様の効果が得られる。
【0102】
また、上述の実施形態及び変形例において示した構成要素は適宜に組み合わせて構成することが可能である。
たとえば、第4実施形態で説明したマーカー定量装置4における複数の発光部181と複数の受光部182との組み合わせは、第3実施形態のマーカー定量装置3における発光部81と受光部82との組み合わせと置き換えてマーカー定量装置3に設けることができる。
【0103】
また、上述の実施例で説明した遠心/攪拌ユニット52は、遠心分離の機能と攪拌の機能とのそれぞれを別々あるいは一体として、第1実施形態に記載の検体補正機構1や、第2実施形態に記載のマーカー定量装置2に設けられても良い。これにより、検体容器100に収容された検体を好適に分離あるいは攪拌できる。
【産業上の利用可能性】
【0104】
本発明の検体補正機構は、生体から採取される検体を分析する分析装置に対して好適に適用可能である。特に、個人間、日内変動、あるいはその他要因で性状が変動する生体試料において疾患関連マーカーを検出する臨床検査装置に対してより好適に適用することができる。
【符号の説明】
【0105】
1、101 検体補正機構
2、3、4 マーカー定量装置
10 検体重量測定機構(検体性状測定部)
11 測定部
12 重量算出部
20、120 補正値算出部
30 補正演算部
40 表示部
50 マーカー抽出部
60 マーカー検出部
80、80a、180 光学的測定機構
81、81a、181 発光部
82、82a、182 受光部
100 検体容器
100a 開口部
100b 底部
110 検体性状測定部
【特許請求の範囲】
【請求項1】
生体試料を含有する検体における単位体積あたりの疾患関連マーカー含有量を前記検体に含有される単位細胞数あたりの前記疾患関連マーカー含有量に補正する検体補正機構であって、
前記検体の性状を測定する検体性状測定部と、
前記検体性状測定部による測定結果に基づく補正値を算出する補正値算出部と、
前記単位体積あたりの前記疾患関連マーカー含有量と前記補正値とに基づいて前記単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部と、
を備える検体補正機構。
【請求項2】
前記検体性状測定部は、前記検体の重量を測定する検体重量測定機構を有する請求項1に記載の検体補正機構。
【請求項3】
前記検体重量測定機構は、
前記検体が収容され重量既知の検体容器と前記検体とをあわせて重量測定して前記検体容器と前記検体との合計重量を測定する測定部と、
前記合計重量から前記検体容器の重量を差し引いて前記検体の正味重量を算出する重量算出部と、
を有する請求項2に記載の検体補正機構。
【請求項4】
前記検体性状測定部は、
前記検体が収容され少なくとも一部において光線が透過可能な検体容器に対して照射される光線の減衰量に基づいて前記検体容器中の固形成分の含有率を測定する光学的測定機構を有する請求項1に記載の検体補正機構。
【請求項5】
前記光学的測定機構は、
前記検体容器の外部から内部方向へ測定光を照射する発光部と、
前記検体容器を挟んで前記発光部と反対側に設けられて前記検体容器及び前記検体を透過した前記測定光を受光する受光部と、
を有する請求項4に記載の検体補正機構。
【請求項6】
前記光学的測定機構は、
前記検体容器の外部から内部方向へ測定光を照射する発光部と、
前記検体容器に対して前記発光部と同じ側に設けられて前記検体容器及び前記検体によって反射された前記測定光を受光する受光部と、
を有する請求項4に記載の検体補正機構。
【請求項7】
前記光学的測定機構は、
前記検体容器における開口から底までの間で所定間隔置きに配置された複数の前記発光部と、
前記発光部のそれぞれに対応して配置された前記受光部と、
をさらに有する請求項5または6に記載の検体補正機構。
【請求項8】
前記検体容器に対して開口から底へ向かう1G以上の重力を生じさせて前記検体の固形成分を前記検体容器の底に沈殿させる分離部をさらに有する請求項3〜7のいずれか一項に記載の検体補正機構。
【請求項9】
請求項1〜8のいずれか一項に記載の検体補正機構と、
前記検体から前記疾患関連マーカーを抽出するマーカー抽出部と、
を備えるマーカー定量装置。
【請求項10】
前記検体の単位体積あたりの前記疾患関連マーカーの含有量を検出するマーカー検出部をさらに備える請求項9に記載のマーカー定量装置。
【請求項1】
生体試料を含有する検体における単位体積あたりの疾患関連マーカー含有量を前記検体に含有される単位細胞数あたりの前記疾患関連マーカー含有量に補正する検体補正機構であって、
前記検体の性状を測定する検体性状測定部と、
前記検体性状測定部による測定結果に基づく補正値を算出する補正値算出部と、
前記単位体積あたりの前記疾患関連マーカー含有量と前記補正値とに基づいて前記単位細胞数あたりの疾患関連マーカー含有量を算出する補正演算部と、
を備える検体補正機構。
【請求項2】
前記検体性状測定部は、前記検体の重量を測定する検体重量測定機構を有する請求項1に記載の検体補正機構。
【請求項3】
前記検体重量測定機構は、
前記検体が収容され重量既知の検体容器と前記検体とをあわせて重量測定して前記検体容器と前記検体との合計重量を測定する測定部と、
前記合計重量から前記検体容器の重量を差し引いて前記検体の正味重量を算出する重量算出部と、
を有する請求項2に記載の検体補正機構。
【請求項4】
前記検体性状測定部は、
前記検体が収容され少なくとも一部において光線が透過可能な検体容器に対して照射される光線の減衰量に基づいて前記検体容器中の固形成分の含有率を測定する光学的測定機構を有する請求項1に記載の検体補正機構。
【請求項5】
前記光学的測定機構は、
前記検体容器の外部から内部方向へ測定光を照射する発光部と、
前記検体容器を挟んで前記発光部と反対側に設けられて前記検体容器及び前記検体を透過した前記測定光を受光する受光部と、
を有する請求項4に記載の検体補正機構。
【請求項6】
前記光学的測定機構は、
前記検体容器の外部から内部方向へ測定光を照射する発光部と、
前記検体容器に対して前記発光部と同じ側に設けられて前記検体容器及び前記検体によって反射された前記測定光を受光する受光部と、
を有する請求項4に記載の検体補正機構。
【請求項7】
前記光学的測定機構は、
前記検体容器における開口から底までの間で所定間隔置きに配置された複数の前記発光部と、
前記発光部のそれぞれに対応して配置された前記受光部と、
をさらに有する請求項5または6に記載の検体補正機構。
【請求項8】
前記検体容器に対して開口から底へ向かう1G以上の重力を生じさせて前記検体の固形成分を前記検体容器の底に沈殿させる分離部をさらに有する請求項3〜7のいずれか一項に記載の検体補正機構。
【請求項9】
請求項1〜8のいずれか一項に記載の検体補正機構と、
前記検体から前記疾患関連マーカーを抽出するマーカー抽出部と、
を備えるマーカー定量装置。
【請求項10】
前記検体の単位体積あたりの前記疾患関連マーカーの含有量を検出するマーカー検出部をさらに備える請求項9に記載のマーカー定量装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【公開番号】特開2011−17597(P2011−17597A)
【公開日】平成23年1月27日(2011.1.27)
【国際特許分類】
【出願番号】特願2009−162015(P2009−162015)
【出願日】平成21年7月8日(2009.7.8)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
【公開日】平成23年1月27日(2011.1.27)
【国際特許分類】
【出願日】平成21年7月8日(2009.7.8)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
[ Back to top ]

