検査チップ及び該検査チップを用いた検査方法
【課題】簡単な操作で検体の検査することができ、使い勝手の良い一体型の検査チップを提供する。
【解決手段】本発明に係る検査チップ10は、チップ本体11と、チップ本体11に設けられ、被検査液Lを貯留する前処理部12と、チップ本体11に設けられ、試薬15を収容保持する反応部13と、チップ本体11に対してスライド自在に取り付けられた検体輸送部21とを備え、検体輸送部21には液吸収部23が設けられており、検体輸送部21をスライドさせた第1の位置で、液吸収部23が前処理部12に貯留された被検査液Lと接触することで吸液し、検体輸送部21をスライドさせた第2の位置で、被検査液Lを吸液した液吸収部23が反応部13に保持された試薬15に接触する構成である。
【解決手段】本発明に係る検査チップ10は、チップ本体11と、チップ本体11に設けられ、被検査液Lを貯留する前処理部12と、チップ本体11に設けられ、試薬15を収容保持する反応部13と、チップ本体11に対してスライド自在に取り付けられた検体輸送部21とを備え、検体輸送部21には液吸収部23が設けられており、検体輸送部21をスライドさせた第1の位置で、液吸収部23が前処理部12に貯留された被検査液Lと接触することで吸液し、検体輸送部21をスライドさせた第2の位置で、被検査液Lを吸液した液吸収部23が反応部13に保持された試薬15に接触する構成である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、血液、尿、体液、組織、細胞、食物、廃液、池水、河川水、海水、又は雨水などの検体中に含まれる一つ以上の成分を分析するための、一体化された分析チップ及び測定方法に関する。
【背景技術】
【0002】
血液、尿等を検体として人の病気を診断する方法は、人体を損ねることなく簡便に診断できる方法として、従来から長く行われてきている。この方法の一つとして、ウェットケミストリー分析法がある。ウェットケミストリー分析法は、いわゆる溶液試薬を用いる方法であって、歴史も古く、多数の検査項目について検出試薬が開発されており、測定機も簡易小型機から大型全自動機まで各種のものがある。ウェットケミストリーに使用される検体は、血漿、血清、尿等であって、通常全血をそのまま検体として使用することはない。
【0003】
ウェットケミストリー分析法では、保存期間中は試薬の安定性を考慮していくつかの群に分けておき、溶解、調製時に混合することもできるし、試薬添加の手順をいくつかのステップに分けることも可能である。更に、測定検体の数に応じて、適量の試薬を溶解、調製しておくことができるので、1回の測定当りの試薬コストも少なくて済む。ウェットケミストリー分析法では、多数の溶液の取扱を組み合わせて自動化することは複雑で厄介ではあるが、臨床検査機器の開発は歴史もあり、社会的な要請も高かったため、既に大・中・小いずれの処理能力を必要とする分野についても、効率良い自動機器が開発、実用化されている。しかし、その多くは工程が複雑で、装置も大きいという問題点あり、開業医や即時に診断結果を得ることが求められる救急病院などのニーズを満たせないことが多かった。
【0004】
例えば、下記特許文献1及び2には、多くの遠心分離の工程を必要とする、区画されたプラスチック容器を使用した液体試料の生物学的分析法が記述されている。これらの生物学的分析法では、容器は多数の貯蔵室、反応室、検量小室から構成され、それらの室同士の間が毛細管で連結されている。このような構成では、構造が複雑であり、遠心装置には煩雑な操作工程が必要であった。
【0005】
また、下記特許文献3には遠心操作と複雑な流路構造などを必要せずに、液体の分析混合物内で逐次的な分析を行い、最小数の作業工程だけを必要とし、操作と作業が容易である分析装置を提供した。開業医や小規模な臨床試験室で容易に利用できる。
【0006】
【特許文献1】米国特許4673653号
【特許文献2】米国特許4743558号
【特許文献3】特開平3−46566号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
しかし、近年、高齢化社会への急速な移行、高度治療の発達などを背景とした医療費の高騰への対応として、在宅ケアが提唱され、今後の医療制度の1つの核となるものとして実施の具体的方法が検討されている。
【0008】
在宅ケアは、基本的に、患者は各家庭に居ながらにして常に医師による適切な監視、指導、管理下にあり、必要に応じて適切な治療ができる点にある。例えば慢性患者や高齢者の場合には、急激な病態変化がなければ安定した生理的状態にあり、一定の治療を続けて、その治療効果を継続的に監視し続けていることが最も大切なこととなる。
【0009】
在宅ケアシステムには、(1)小型で(2)簡便に(3)微量の血液を用いて(4)多項目を(5)迅速に(6)精度よく測定できる血液分析方法が望ましいのはいうまでもない。特に、高齢者(場合によっては小児)を対象とする場合、微量の血液の採取ですむ分析方法の開発が望まれている。
これに対して、ウェットケミストリー分析法を用いた一体型の家庭用分析装置が提案されている(特開2001−258868号公報)が、簡便さ、大きさ、安い点でも満足できるものではなかった。
【0010】
また、上記特許文献1から3の従来技術では、一つの項目を検査するための各種操作を一つの装置の中に集約して、行うのに多量の検査液を使用することになり、装置も大がかりで検査に至るまでに装置を回転させる等、大がかりな動作が必要となる。
【0011】
本発明の目的は、検体以外の全ての試薬等を分析用チップ内に封入した、メンテナンスの必要のないオール・イン・ワン・タイプの構造を有し、分析に必要な検体及び試薬の量を微量とすることができ、さらに、簡便に短時間で且つ低コストで分析を行うことが可能であって、一つの機構で1検査を実施でき、煩雑な操作をする必要がない、少量の検査液にて一つ動作で、多項目の検査を容易にした小型の検査チップ及びその検査チップを使用した検査方法を提供することにある。
【課題を解決するための手段】
【0012】
本発明の上記目的は、下記構成によって達成される。
(1) 被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、チップ本体と、前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、前記チップ本体に設けられ、前記試薬を収容保持する反応部と、前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、前記検体輸送部には液吸収体が設けられており、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで吸液し、前記検体輸送部をスライドさせた第2の位置で、前記被検査液を吸液した前記液吸収体が前記反応部に保持された前記試薬に接触することを特徴とする検査チップ。
(2) 前記検体輸送部には、前記チップ本体に対してスライドさせた状態で、前記前処理部に残留した前記被検査液と接触して吸液可能な残液吸収材が設けられていることを特徴とする上記(1)に記載の検査チップ。
(3) 前記液吸収体が前記反応部に接触する位置にある状態で、前記残液吸収材が前処理部に残留した前記被検査液に接触する構成であることを特徴とする上記(2)に記載の検査チップ。
(4) 前記チップ本体には、前記前処理部に前記被検査液を導入するための導入部が設けられていることを特徴とする上記(1)から(3)のいずれか1つに記載の検査チップ。
(5) 前記反応部に乾燥試薬が保持されていることを特徴とする上記(1)から(4)のいずれか1つに記載の検査チップ。
(6) 前記反応部が複数設けられていることを特徴とする上記(1)から(5)のいずれか1つに記載の検査チップ。
(7) 前記液吸収部が複数設けられていることを特徴とする上記(1)から(6)のいずれか1つに記載の検査チップ。
(8) 前記試薬がHbA1cを検出する材料であることを特徴とする上記(1)から(7)のいずれか1つに記載の検査チップ。
(9) 前記試薬がCRPを検出する材料であることを特徴とする上記(1)から(7)のいずれか1つに記載の検査チップ。
(10) 被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、チップ本体と、前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、前記検体輸送部には液吸収体が設けられ、前記液吸収体には前記試薬を保持可能な反応部が設けられ、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで該被検査液を吸液するとともに、前記被検査液が前記反応部の前記試薬に接触することを特徴とする検査チップ。
(11) 上記(1)から(10)のいずれか1つに記載の検査チップを用いて、前記被検査液を前記試薬に反応させる検査を行うことを特徴とする検査方法。
【0013】
上記の本発明に係る検査チップにおいて、チップ基板材は無機材質でも良いし、有機材質でもいい。基板に使用される無機材質の例を挙げれば金属、シリコン、テフロン(登録商標)、ガラス、セラミックスなどである。有機材質はプラスチック、ゴムなどである。
【0014】
プラスチックの例としては、PCO、PS、PC、PMMA、PE、PET、PP等を挙げることができる。ゴムの例としては、天然ゴム、合成ゴム、シリコンゴム、PDMS等を挙げることができる。シリコン含有物質としては、ガラス、石英、シリコンウエファー等のアモルファスシリコン、ポリメチルシロキサンなどのシリコーンが挙げられる。
【0015】
コストと加工のし易さの面では、プラスチックは好ましい。特に好ましい例としては、PMMA、PCO、PS、PC、PET、PEN等を挙げることができる。
【0016】
検体を採取し、前処理部に供給する手段としては、一定秤量できるキャピラリーを用いることが好ましい。キャピラリーの材質はプラスチックとガラスが好ましい。
【0017】
キャピラリーの内表面の親水性を持つことが必要である。キャピラリーの材質が親水性ではない時親水化処理が必要である。親水化処理法として、従来の表面処理方法が適用できる。大きく分けて、化学的表面処理法と物理的表面処理法がある。化学的表面処理法としては、薬品処理、カップリング剤による処理、蒸気処理、グラフト化、電気化学的方法、添加剤による表面改質などがある。物理的表面処理法としては、UV照射、電子線処理、イオンビーム照射、低音プラズマ処理、CASING処理、グロー、コロナ放電処理、酸素プラズマなどの方法がある。
【0018】
なお、上記のように液体の検体と処理試薬とを混合して検体の前処理をするための容器には、一定体積の処理試薬溶液が予め封入されている。処理試薬溶液の体積は20〜20000μLが好ましい、より好ましくは50〜2000μL、さらに好ましくは100〜1000μLである。
【0019】
また、検体の前処理容器中の処理試薬溶液を漏出しないようにシール部材で密封されることが好ましい。前記試薬部位は非流動性の反応試薬が好ましい。さらに好ましいのは多層乾式分析要素(乾燥試薬)である。
【0020】
本発明でいう多層乾式分析要素とは、検体中の被測定成分の定性・定量分析に必要な全てのまたはその一部分の試薬を1層以上の層に組み込んだ乾式分析要素のことをいう。いわゆるドライケミストリーを使用した分析要素である。具体的には、このような多層乾式分析要素の例は、富士フイルム研究報告、第40号(富士写真フイルム株式会 社、1995年発行)p.83や、臨床病理、臨時増刊、特集第106号、ドライケミストリー・簡易検査の新たなる展開(臨床病理刊行会、1997年発行) 等に記載されているものをあげることができる。
【0021】
上記した多層乾式分析要素は、通常少なくとも一つの機能層を含む。機能層の数は一つ以上であれば特に限定されず、1層でもよいし、2層以上の複数の層とすることもできる。
【0022】
機能層の具体例としては、展開層、展開層と展開層以外の機能層とを接着する接着層、液状試薬を吸水する吸水層、化学反応により生成した色素の拡散を防止する媒染層、ガスを選択的に透過させるガス透過層、層間での物質移動を抑制・促進させる中間層、反射測光を安定に行うための光遮蔽層、内因性色素の影響を抑制する色遮蔽層、分析対象物と反応する試薬を含む試薬層、発色剤を含む発色層などが挙げられ、これらは必要に応じて適宜選択することができる。
【0023】
多層乾式分析要素の一例としては、例えば、支持体の上には、場合によっては下塗層等の他の層を介して、機能層として親水性ポリマー層を設けることができる。親水性ポリマー層としては、例えば、無孔性、吸水性かつ水浸透性の層であり、基本的に親水性ポリマーのみなる吸水層、親水性ポリマーをバインダーとし発色反応に直接関与する発色試薬の一部又は全部を含む試薬層、及び親水性ポリマー中に発色色素を固定し不動にする成分(例:媒染剤)を含有する検出層などを設けることができる。
【0024】
(試薬層)
試薬層は水性液体中の被検成分と反応して光学的に検出可能な変化を生じる試薬組成物の少なくとも一部が親水性ポリマーバインダー中に実質的に一様に分散されている吸水性で水浸透性の層である。この試薬層には指示薬層、発色層なども含まれる。
【0025】
試薬層のバインダーとして用いることができる親水性ポリマーは、一般には水吸収時の膨潤率が30℃で約150%から約2000%、好ましくは約250%から約1500%の範囲の天然または合成親水性ポリマーである。そのような親水性ポリマーの例としては、特開昭60−108753号公報等に開示されているゼラチン(例、酸処理ゼラチン、脱イオンゼラチン等)、ゼラチン誘導体(例、フタル化ゼラチン、ヒドロキシアクリレートグラフトゼラチン等)、アガロース、プルラン、プルラン誘導体、ポリアクリルアミド、ポリビニルアルコール、ポリビニルピロリドン等をあげることができる。
【0026】
試薬層は架橋剤を用いて適宜に架橋硬化された層とすることができる。架橋剤の例として、例えば、ゼラチンに対する1,2−ビス(ビニルスルホニルアセトアミド)エタン、ビス(ビニルスルホニルメチル)エーテル等の公知のビニルスルホン系架橋剤、アルデヒド等、メタリルアルコールコポリマーに対するアルデヒド、2個のグリシジル基含有エポキシ化合物等がある。
【0027】
試薬層の乾燥時の厚さは約1μmから約100μmの範囲であることが好ましく、より好ましくは約3μmから約30μmの範囲である。また試薬層は実質的に透明であることが好ましい。
【0028】
多層乾式分析要素の試薬層やその他の層に含める試薬としては、被験物質に応じてその検出に適した試薬を選択することができる。
【0029】
(光遮蔽層)
前記試薬層の上に必要に応じて光遮蔽層を設けることができる。光遮蔽層は、光吸収性または光反射性(これらを合わせて光遮蔽性という。)を有する微粒子が少量の被膜形成能を有する親水性ポリマーバインダーに分散保持されている水透過性または水浸透性の層である。光遮蔽層は試薬層にて発生した検出可能な変化(色変化、発色等)を光透過性を有する支持体側から反射測光する際に、後述する展開層に点着供給された水性液体の色、特に試料が全血である場合のヘモグロビンの赤色等、を遮蔽するとともに光反射層または背景層としても機能する。
光反射性を有する微粒子の例としては、二酸化チタン微粒子(ルチル型、アナターゼ型またはブルカイト型の粒子径が約0.1μmから約1.2μmの微結晶粒子等)、硫酸バリウム微粒子、アルミニウム微粒子または微小フレーク等を挙げることができ、光吸収性微粒子の例としては、カーボンブラック、ガスブラック、カーボンミクロビーズ等を挙げることができ、これらのうちでは二酸化チタン微粒子、硫酸バリウム微粒子が好ましい。特に好ましいのは、アナターゼ型二酸化チタン微粒子である。
【0030】
被膜形成能を有する親水性ポリマーバインダーの例としては、前述の試薬層の製造に用いられる親水性ポリマーと同様の親水性ポリマーのほかに、弱親水性の再生セルロース、セルロースアセテート等を挙げることができ、これらのうちではゼラチン、ゼラチン誘導体、ポリアクリルアミド等が好ましい。なお、ゼラチン、ゼラチン誘導体は公知の硬化剤(架橋剤)を混合して用いることができる。
【0031】
光遮蔽層は、光遮蔽性微粒子と親水性ポリマーとの水性分散液を公知の方法により試薬層の上に塗布し乾燥することにより設けることができる。また光遮蔽層を設ける代りに、前述の展開層中に光遮蔽性微粒子を含有させてもよい。
【0032】
(接着層)
試薬層の上に、場合によっては光遮蔽層等の層を介して、展開層を接着し積層するために接着層を設けてもよい。
【0033】
接着層は、水で湿潤しているとき、または水を含んで膨潤しているときに展開層を接着することができ、これにより各層を一体化できるような親水性ポリマーからなることが好ましい。接着層の製造に用いることができる親水性ポリマーの例としては、試薬層の製造に用いられる親水性ポリマーと同様な親水性ポリマーがあげられる。これらのうちではゼラチン、ゼラチン誘導体、ポリアクリルアミド等が好ましい。接着層の乾燥膜厚は一般に約0.5μmから約20μm、好ましくは約1μmから約10μmの範囲である。
【0034】
なお、接着層は試薬層上以外にも、他の層間の接着力を向上させるため所望の層上に設けてもよい。接着層は親水性ポリマーと、必要によって加えられる界面活性剤等を含む水溶液を公知の方法で、支持体や試薬層等の上に塗布する方法などにより設けることができる。
【0035】
(吸水層)
多層乾式分析要素には、支持体と試薬層の間に吸水層を設けることができる。吸水層は水を吸収して膨潤する親水性ポリマーを主成分とする層で、吸水層の界面に到達または浸透した水性液体試料の水を吸収できる層であり、特に検体として全血試料を用いる場合には水性液体成分である血漿の試薬層への浸透を促進する作用を有する。吸水層に用いられる親水性ポリマーは前述の試薬層に使用されるもののなかから選択することができる。吸水層には一般的にはゼラチンまたはゼラチン誘導体、ポリアクリルアミド、ポリビニルアルコール、特に前述のゼラチン又は脱イオンゼラチンが好ましく、試薬層と同じ前述のゼラチンが最も好ましい。吸水層の乾燥時の厚さは約3μmから約100μm、好ましくは約5μmから約30μmの範囲、被覆量では約3g/m2から約100g/m2、好ましくは約5g/m2から約30g/m2の範囲である。吸水層には後述するpH緩衝剤、公知の塩基性ポリマー等を含有させて使用時(分析操作実施時)のpHを調節することができる。さらに吸水層には公知の媒染剤、ポリマー媒染剤等を含有させることができる。
【0036】
(検出層)
検出層は、一般に、被検成分の存在下で生成した色素等が拡散し、光透過性支持体を通して光学的に検出され得る層で、親水性ポリマーにより構成することができる。媒染剤、例えばアニオン性色素に対してカチオン性ポリマーを、含んでもよい。前述の吸水層は、一般に、被検成分の存在下で生成する色素が実質的に拡散しないような層を言い、この点で検出層とは区別される。
【0037】
多層乾式分析要素は、公知の方法により調製、作製することができ、一辺約1mmから約30mmの正方形またはほぼ同サイズの円形等の小片に裁断して用いることができるが、必要に応じてさらに小さくすることも可能である。このような多層乾式分析要素はすでに多数開発・商品化されており、富士ドライケム(富士写真フイルム(株)製)などはその1例である。本発明においては、このような多層乾式分析要素そのものを使用する。またはその一部分を使用することもできる。
【0038】
上記多層乾式分析要素は、複数的に試薬部に配置する。前記多層乾式分析要素の配置方向は液体吸収部(展開層)と平行させるのが好ましい。この検体の移動する手段としては、液体吸収体を用い、この液体吸収体をスライダーに固定し、スライダーを検体前処理容器の上部に通過することによって、液体吸収体と検体処理液と接触させる。さらに、前記吸収体を反応部に移動させ、反応部にある多層乾式分析要素と合体して、検体の移送が完成する。
【0039】
上記の液体吸収体は検体液と接触した場合に一定量の検体液を包容する性質を有する限り、繊維質材料でもよいし、非繊維質材料でもよい。繊維質材料としては、例えば濾紙、不織布、織物布地(例えば、特開昭55−164356号公報、特開昭57−66359号公報等に記載の織物布地)、編物布地(例えば、特開昭60−222769号公報等に記載の編物布地)、ガラス繊維濾紙等を用いることができる。
【0040】
非繊維質材料としては、特公昭53−21677号公報、米国特許3,992,158等に記載のメンブランフイルタ(ブラッシュポリマー層)、ポリマーミクロビーズ、ガラスミクロビーズ、珪藻土が親水性ポリマーバインダーに保持されてなる連続微空隙含有多孔性層等の非繊維等方的多孔性物質層、特開昭55−90859号公報に記載のポリマーミクロビーズが水で膨潤しないポリマー接着剤で点接触状に接着されてなる連続微空隙含有多孔性物質層(三次元格子状粒状構造物層)からなる非繊維等方的多孔性物質層等を用いることができる。
【0041】
多孔性物質膜としては、有機高分子からなる多孔膜を使用することもできる。具体的には、6,6−ナイロン、6−ナイロン、アクリレート共重合体、ポリアクリレート、ポリアクリロニトリル、ポリアクリロニトリル共重合体、ポリアミド、ポリイミド、ポリアミドイミド、ポリウレタン、ポリエーテルスルホン、ポリスルホン、ポリエーテルスルホンとポリスルホンの混合物、ポリエステル、ポリエステルカーボネート、ポリエチレン、ポリエチレンクロロトリフルオロエチレン共重合体、ポリエチレンテトラフルオロエチレン共重合体、ポリ塩化ビニル、ポリオレフィン、ポリカーボネート、ポリテトラフルオロエチレン、ポリビニリデンジフルオライド、ポリフェニレンスルフェレンスルフィド、ポリフルオロカーボネート、ポリポロピレン、ポリベンズイミダゾール、ポリメアクリル酸メイル、スチレンーアクリロニトリル共重合体、スチレンーブタジエン共重合体、エチレンー酢酸ビニル共重合体の鹸化物、ポリビニルアルコール、セルロースアセテートブチレートの鹸化物、セルロースアセテートブチレートブチレート、セルロースアセテートブチレートの鹸化物またはこれらの混合物などを使用することができる。
【0042】
特開昭61-4959(対応米国特許 5,019,347; 対応欧州公開 EP 0166365A)、特開昭62-116258 、特開昭62-138756(対応欧州公開 EP 0226465A)、特開昭62-138757(対応欧州公開 EP 0226465A)、特開昭62-138758(対応欧州公開 EP 0226465A)等に記載の部分接着された複数の多孔性層の積層物も好適である。
【0043】
また、高分子ゲル(天然高分子ゲル:ゼラチン、寒天、アガロペクチン、デンプン、アミロース、アミロペクチン、カラギーナン、ジエランガム、キタンサンガム、カードラン、コラーゲン、アルギニン酸、ペクチン、コンニャクマンナン、メチルセルロース、ヒドロキシプロピルセルロ−ス、デキストラン;合成高分子ゲル:ポリエチレン,ポリスチレン、ポリアクリレート、ポリアクリル酸、ポリメタクリル酸、ポリグルタミン酸、ポリビニルピリジン、ポリビニルイミダゾール、アクリルアミド、 ビニルピロリドン、メタクリル酸ヒドロキシエチル、0−ベンジルーL−グルタメート、ポリエチレングリコール、ヒアルロン酸)、ラテックス粒子、無機材料(多孔質炭素多孔質炭化珪素、多孔質ガラスビーズ、シリカゲル、酸化アルミナ、ゼオライト、メソポーラス)も好適である。
【0044】
検出手段としては、多層乾式分析要素内の発色又は変色を光透過性支持体側から反射測光し、予め作成した検量線を用いて比色測定法の原理により検体中の被験物質の量を求めることができる。また必要に応じて透過測光することも可能である。さらに、本発明の分析チップはエリアセンサによっても測定できる。
【0045】
エリアセンサは、CCD等の固体撮像素子であり、多項目測定乾式分析要素中の試薬担持部の試薬と血液等の検体とが反応した際に光源から照射される光によって反射する光を受光し、受光した光を電気信号に変換してコンピュータに出力するものである。エリアセンサは、試薬担持部から反射する光を面単位で受光可能である。このため、各試薬のエリアを同時に、すなわち複数項目について測定が可能である。また、検体からの反射光をCCD等のエリアセンサを用いて受光しているが、エリアセンサに限らず、ラインセンサを用いても構わない。
【発明の効果】
【0046】
本発明によれば、検体以外の全ての試薬等を分析用チップ内に封入した、メンテナンスの必要のないオール・イン・ワン・タイプの構造を有し、分析に必要な検体及び試薬の量を微量とすることができ、さらに、簡便に短時間で且つ低コストで分析を行うことが可能であって、一つの機構で1検査を実施でき、煩雑な操作をする必要がなく、少量の検査液にてワン動作で、多項目の検査を容易にした小型の検査チップ及びその検査チップを使用した検査方法を提供できる。
【発明を実施するための最良の形態】
【0047】
以下、本発明の実施形態を図面に基づいて詳しく説明する。
最初に、本発明に係る検査チップの構成を説明する。
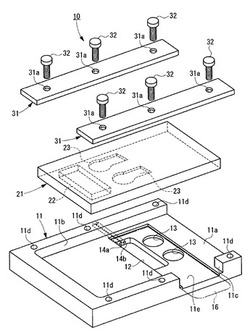
図1は、検査チップの分解斜視図である。図2は、検査チップの上面図である。図3は、検査チップの断面図である。図4及び図5は、検査チップの動作の状態を示す図である。
【0048】
検査チップ10は、チップ本体11と、検体輸送部21と、検体輸送部21をチップ本体11に対してスライド自在に取り付ける取付部材31とから概略構成されている。
【0049】
チップ本体11は、略長方体形状を有し、透視可能な透明又は半透明な材料から構成されている。チップ本体11は、上方視した状態(図1の上方からみた状態)で矩形形状を有し、スライドする検体輸送部21を支持する支持板部11aと、支持板部11aの周縁辺のうち3辺から上方に垂直に立設された側板部11bとを有している。
【0050】
チップ本体11の支持板部11aには、検体輸送部21の下面側とスライド時に摺接する面である上面に凹設された凹部面11eが形成されている。また、凹部面11eの上面側には、凹部である前処理部12と、前処理部12の近傍に、支持板部11aの上面に凹設されてなる反応部13とが設けられている。
【0051】
本実施形態においては、前処理部12には、予め、検体となる希釈液が貯留されており、検査時に前処理部12に微量の血液が導入され、前処理部12において希釈液と血液とが混合されることで被検査液Lが生成される。また、反応部13には、被検査液Lの反応を調べるための試薬が収容保持される。
【0052】
本実施形態の検査チップ10において、前処理部12及び反応部13を密閉するため、凹部面11eにテープ状のシール部材16が接着されている構成とすることが好ましい。こうすることで、前処理部12に貯留された希釈液や反応部13に収容保持された試薬が漏れ出てしまうことを防止することができる。
【0053】
また、チップ本体11は、凹部面11e近傍の側板部11cの一部に切欠部11cが設けられている。凹部面11eの接着されたシール部材16の一部が切欠部11cに配置され、チップ本体11の外部に突出している。検査時には、使用者がチップ本体11の切欠部11cから突出したシール部材16を把持し、引き抜くことで、シール部材16が凹部面11eから引き剥がされ、前処理部12及び反応部13が開放される。
【0054】
チップ本体11には、前処理部12に一方の端部が連通し、且つ、チップ本体11の外側面に他方の端部が連通する一対の導入部14a,14bが設けられている。これら一対の導入部14a,14bの一方を介して、血液が前処理部12の内部に導入される。このとき、予め、導入部14a,14bの一方(本実施形態では導入部14b)には、図示しない栓部材が装填され、検査時に開栓ピン18を導入部14bに挿入することで、栓部材を前処理部12内に押し出し、導入部14bを開通させた後に、血液を導入部14bを介して前処理部12内に導入する。このとき、他方の導入部14aは、導入部14bから導入する血液が前処理部12内の空気によって逆流することを防止するための空気抜けとして機能する。また、他方の導入部14aが、検査時以外において開栓ピン18を収容保持するためのピン保持部として機能することが好ましい。
【0055】
検体輸送部21は、略長方体形状を有する板状部材である。検体輸送部21の下側面には、残液吸収材24を収容保持できるように凹設された、吸収材保持部22と、液吸収体25を収容保持できるように凹設された、液吸収部23とが形成されている。
【0056】
検体輸送部21は、チップ本体11に取り付けた状態で、チップ本体11の側板部11cによってその3辺の位置が支持されることで、チップ本体11に対する位置が規制される。
【0057】
取付部材31は、チップ本体11の側板部11bの長手寸法と略同一寸法を有する長方形板状の部材であって、それぞれに複数(本実施形態ではそれぞれ3つ)のネジ挿通穴31aが形成されている。また、チップ本体の側板部11bの上端面には、複数のネジ止め孔11dが形成されている。取付部材31をチップ本体11に取り付ける場合には、ネジ挿通穴31aにネジ32をそれぞれ挿通するとともに、ネジ32の先端をチップ本体の側板部11bのネジ止め孔11dに螺合することで、取付部材31をチップ本体11に固定することができる。
【0058】
図2に示すように、取付部材31をチップ本体11に固定した状態で、チップ本体11上に支持された検体輸送部21の上面の一部が、チップ本体11と取付部材31との間で挟まれて支持される。このため、検体輸送部21がチップ本体内11の上面から水平に離間することが回避される。
【0059】
本実施形態の検査チップ10は、使用者が、検体輸送部21をチップ本体11の支持板部11a上の、側板部11bが設けられていない端縁辺側へ手指で押し動かすことにより、スライドさせて移動できる。
【0060】
なお、本実施形態の検査チップ10においては、チップ本体11の反応部13と、検体輸送部21の液吸収部23との数をそれぞれ2つとしたが、検査する量や検査項目等に応じて、数を変更してもよい。
【0061】
次に、本発明に係る検査チップの動作の一例を説明する。
先ず、検査チップ10の前処理部12に、希釈液を予め貯留させ、また、反応部13に試薬15を収容保持させておく。そして、導入部14a,14bの一方から微量の血液を前処理部12内に導入する。前処理部12内において希釈液と血液とを混合させて被検査液Lを生成する。その後、シール部材16を剥して前処理部12の凹部を開放させる。
【0062】
次に、検体搬送部21の一部を手指で把持し、図2及び図3に示すように、該検体搬送部21をスライドさせることで、チップ本体11に対する位置を変える。
【0063】
図4に示すように、検体搬送部21の液吸収部23をチップ本体11の前処理部12の上方にくる位置(第1の位置)にスライド移動させると、液吸収部23に収容保持され液吸収体25の一部が前処理部12に貯留された被検査液Lと接触することで、該被検査液Lを吸液する。
【0064】
ここで、検体輸送部21が第1の位置にある状態で、液吸収体25は、その一部が前処理部12側へ弾性変形する形状、構成、又はそのような素材であることが好ましい。こうすれば、液吸収体25を前処理部12に貯留された被検査液Lにより確実に接触させることができる。
【0065】
続いて、図5に示すように、検体搬送部21を更にスライドさせ、検体搬送部21の液吸収部23がチップ本体11の反応部13の上方にくる位置(第2の位置)まで移動すると、液吸収部23の液吸収体25に吸液されている被検査液Lが反応部13の試薬15と接触する。このとき、被検査液Lと試薬15とが所定の反応を起し、使用者が検査チップ10の外部から、透明なチップ本体11及び検体搬送部21を介して視認することができ、被検査液Lと試薬15との反応に基づいて、検査の状態を観察することができる。
【0066】
このとき、検体輸送部21の残液吸収材24が、前処理部12に残留した被検査液Lと接触することで、残留した被検査液Lが残液吸収材24に吸液される構成とすることが好ましい。こうすれば、前処理部12から残留した被検査液Lが漏れ出ることを防止することができるため、使い勝手が良い。
【0067】
検査チップ10は、検査時に導入する検体(本実施形態では血液)のを除く、他の全ての試薬等を検査前に予めチップ本体11内に封入して保存することができるためメンテナンスが不要である。また、検査に必要十分の量の検体を前処理室に導入し、
また、最低限の試薬を反応部に収容保持すればよいため、検査に必要な検体及び試薬の量を微量とすることができる。
さらに、検体搬送部21をチップ本体11に対して手指でスライドさせるといいた簡単な構成であるため、検査にかかる作業を簡便にすることができるとともに、検査にかかる時間を短時間とすることができ、且つ、検査を低コストで行うことが可能である。
【0068】
チップ本体11に対してスライド自在な検体輸送部21を備えた機構であるため、1つの機構で1つの検査を実施でき、従来の検査方法のように、煩雑な操作を行う必要がなく、反応部13及び液吸収部23の数を増やすことで、一回の操作で多項目の検査を容易に行うことができる。
【0069】
以下、本発明に係る実施例とその比較例を挙げて本発明を詳しく説明する。なお、本発明は以下の実施例に限定されるものではない。本実施例においては、図1から5に示す上記実施形態の検査チップを使用した。
(実施例1)
実施例1の作動を説明する。
最初に、検査チップ10の導入部14bに、採血キャピラリーを挿入し、血液を前処理部12内に導入する。ここで、採血キャピラリーは別穿刺器具(図示せず)により皮膚上に摘出された血液を毛細管作用により吸引し、吸引と同時に秤量を行う部材である。
秤量された血液1μLを含んだ採血キャピラリー1はキャピラリー押し(図示せず)により押し込まれて前処理部12内(希釈液200μL封入されている)に挿入される。その後、検査チップ10全体を揺することで秤量された採血キャピラリー内の血液が前処理部12内に貯留された希釈液に溶け、該希釈液と混合されることになる。このとき、前処理部12内の採血キャピラリーは撹拌子の役目をはたす事になり混合を補助する。
【0070】
その後、検査試薬部シール16を矢印の方向に引くことでシールが剥がれて、液吸液部23で被検査液を搬送する準備が完了する。
【0071】
次に、検体輸送部21の上面を手指の腹面で保持し、図2及び図3で示す矢印の方向に押し進めることで、液吸液部23と吸収材保持部22との位置が代わり、液吸液部23が前処理部12上を通過することで液吸収体25被検査液Lを吸収する。そして、該液吸収体25が反応部13に収容保持された試薬15に接触することで、液吸収体25に吸液されている被検査液Lと試薬15との間で反応が行われ、使用者が反応後の比色検査を視認可能となる。検体輸送部21の吸収材保持部22に保持された残液吸収材24が、前処理部12上に到達し、該算液吸収材24が前処理部12内に残留した被検査液Lを吸収して検査チップ内からの液漏れを防止する。
【0072】
(実施例2)
次に、CRPの検出の動作を説明する。
本実施例において、特開2003-75445号公報に記載の実施例と同様の方法で、CRP用多層乾式スライドを作製した。
CRP濃度が既知のCRP標準血清1μLをキャピラリー1で秤量し、前処理部12(希釈液200μLを事前入れたもの)内に挿入される。その後、検査チップ10全体を振動させて、希釈液と血液とを混合する。その後、シール部材16を剥して前処理部12の凹部を開放させた。検体輸送部21をスライドさせることで、液吸収体25と残液吸収材24とがともに移動を開始し、液吸収体25が前処理室12上を通過することで被検査液Lを吸収し、反応部13の試薬15に到達し接触する。
【0073】
ここで、検査チップ10近傍の環境雰囲気を37℃に保って、分光光度計(MCPD-2000(大塚電子))でPET支持体側から中心波長650nmの可視光で反射光学濃度を測定した。点着から3分後および5分後の反射光学濃度の差(ΔOD5-3)を求めて、検量線からCRPの量を求める(測定回数、N=5)。CRPの測定値 (g/dL) は3.3±0.15であり、CVは4.5%であった。
【0074】
(実施例3)
次に、下記実施例のように、ヘモグロビン(Hb)とグリコヘモグロビン(HbA1c)の検出を行った。
本実施例では、特開平8−122335号公報に記載の実施例2と同様の方法で、ヘモグロビンA1c用多層乾式スライドを作製した。そして、全血1μLをキャピラリーで秤量し、前処理部12(溶血液200μLを事前入れ)内に挿入される。その後、検査チップ10全体を振動させて、血液と希釈液とを混合する。その後、シール部材16を剥して前処理部12の凹部を開放させた。検体輸送部21をスライドさせることで、液吸収体25と残液吸収材22とが移動し、液吸収体25が前処理部12上を通過する際に被検査液Lを吸収し、試薬15に接触する。
【0075】
検査チップ10近傍の環境雰囲気を37℃に保って、分光光度計(MCPD-2000(大塚電子))でPET支持体側から中心波長650nmの可視光で反射光学濃度を測定した。点着から3分後および5分後の反射光学濃度の差(ΔOD5-3)を求めて、検量線からヘモグロビンA1Cの量を求めた(測定回数N=3とした。)。ヘモグロビンA1Cの測定値 (g/dL)は、1.07±0.04となり、CVは3.7%となった。同時にもう一枚のヘモグロビン(Hb)スライドの支持体側から、中心波長420nmの可視光で反射光学濃度を測定した。点着から0.5分後の反射光学濃度ODから、検量線からヘモグロビン(Hb)の量を求める(測定回数、N=3)。ヘモグロビン(Hb)の測定値 (g/dL)は13.2±0.4となり、CVは3.0%となった。
【0076】
図6及び図7に、本発明に係る検査チップの変形例を示す。なお、以下に説明する実施形態において、すでに説明した部材などと同等な構成・作用を有する部材等については、図中に同一符号又は相当符号を付すことにより、説明を簡略化或いは省略する。図6は、本発明に係る検査チップの変形例を示す上面図である。また、図7は、図6に示す検査チップの液吸収体の構成を示す図である。なお、図6で示す検査チップ20は、上記実施形態の検査チップ10の構成及び動作と基本的に同じである。以下、異なる点についてのみ説明する。
【0077】
検査チップ20は、検体輸送部21の液吸収部23に収容保持された液吸収体55が被検査液を吸液する機能、試薬との反応を行う機能とを兼ね備えた構成である。このため、検査チップ20は、チップ本体11に前処理部12が形成されているものの、上記実施形態の検査チップ10における反応部13が形成されていない。
【0078】
液吸収体55は、検体輸送部21の液吸収部23に固定される基端部55aと、基端部55aに対して変形し、検体輸送部21をスライドさせた際に、チップ本体11の前処理部12に貯留された被検査液と接触する部位である接触部55bとから構成されている。そして、接触部55bには、被検査液と接触することで所定の変化を起す試薬を含有した試薬を保持する反応部45が形成されている。反応部45に含有される試薬の材料としては、上記実施形態の反応部13に収容保持される試薬15と同じものを用いることができる。
【0079】
チップ本体11の前処理部12の近傍には、スライドさせた検体輸送部21の液吸収体55の第2の位置に対向する位置に、開口43が設けられている。使用者は、第1の位置で液吸収体55を前処理部12の被検査液Lに接触させた後、検体輸送部21を第2の位置に移動することで、開口43を介して液吸収体55の反応部45の色変化を観察することができる。
【0080】
以上説明したように、本発明の検査チップは、秤量採血し希釈液と混合させ、混合精度の良い被検査液を製作し、その被検査液に液吸収体を接触させることで正確な検査ができる。このため、従来技術では、1項目の検査を行うのに多量の検査液を使用することになり、装置も大がかりで検査に至るまでに装置を回転させる等、大がかりな動作が必要となるが、本発明の検査チップ及びその検査チップを用いた検査方法によれば、上記従来の問題点を回避して検査の効率を高めることができる。
【産業上の利用可能性】
【0081】
本発明は、アレルギー反応検査試薬として利用可能で数項目アレルギー反応の検査を一度で検査できる検査チップとして適用できる。
【図面の簡単な説明】
【0082】
【図1】検査チップの分解斜視図である。
【図2】検査チップの上面図である。
【図3】検査チップの断面図である。
【図4】検体輸送部が第1の位置にある状態を示す図である。
【図5】検体輸送部が第2の位置にある状態を示す図である。
【図6】本発明に係る検査チップの変形例を示す上面図である。
【図7】図6に示す検査チップの液吸収体の構成を示す図である。
【符号の説明】
【0083】
10,20 検査チップ
11 チップ本体
12 前処理部
13 反応部
15 試薬
21 検体輸送部
22 吸収材保持部
23 液吸収部
24 残液吸収材
25 液吸収体
L 被検査液
【技術分野】
【0001】
本発明は、血液、尿、体液、組織、細胞、食物、廃液、池水、河川水、海水、又は雨水などの検体中に含まれる一つ以上の成分を分析するための、一体化された分析チップ及び測定方法に関する。
【背景技術】
【0002】
血液、尿等を検体として人の病気を診断する方法は、人体を損ねることなく簡便に診断できる方法として、従来から長く行われてきている。この方法の一つとして、ウェットケミストリー分析法がある。ウェットケミストリー分析法は、いわゆる溶液試薬を用いる方法であって、歴史も古く、多数の検査項目について検出試薬が開発されており、測定機も簡易小型機から大型全自動機まで各種のものがある。ウェットケミストリーに使用される検体は、血漿、血清、尿等であって、通常全血をそのまま検体として使用することはない。
【0003】
ウェットケミストリー分析法では、保存期間中は試薬の安定性を考慮していくつかの群に分けておき、溶解、調製時に混合することもできるし、試薬添加の手順をいくつかのステップに分けることも可能である。更に、測定検体の数に応じて、適量の試薬を溶解、調製しておくことができるので、1回の測定当りの試薬コストも少なくて済む。ウェットケミストリー分析法では、多数の溶液の取扱を組み合わせて自動化することは複雑で厄介ではあるが、臨床検査機器の開発は歴史もあり、社会的な要請も高かったため、既に大・中・小いずれの処理能力を必要とする分野についても、効率良い自動機器が開発、実用化されている。しかし、その多くは工程が複雑で、装置も大きいという問題点あり、開業医や即時に診断結果を得ることが求められる救急病院などのニーズを満たせないことが多かった。
【0004】
例えば、下記特許文献1及び2には、多くの遠心分離の工程を必要とする、区画されたプラスチック容器を使用した液体試料の生物学的分析法が記述されている。これらの生物学的分析法では、容器は多数の貯蔵室、反応室、検量小室から構成され、それらの室同士の間が毛細管で連結されている。このような構成では、構造が複雑であり、遠心装置には煩雑な操作工程が必要であった。
【0005】
また、下記特許文献3には遠心操作と複雑な流路構造などを必要せずに、液体の分析混合物内で逐次的な分析を行い、最小数の作業工程だけを必要とし、操作と作業が容易である分析装置を提供した。開業医や小規模な臨床試験室で容易に利用できる。
【0006】
【特許文献1】米国特許4673653号
【特許文献2】米国特許4743558号
【特許文献3】特開平3−46566号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
しかし、近年、高齢化社会への急速な移行、高度治療の発達などを背景とした医療費の高騰への対応として、在宅ケアが提唱され、今後の医療制度の1つの核となるものとして実施の具体的方法が検討されている。
【0008】
在宅ケアは、基本的に、患者は各家庭に居ながらにして常に医師による適切な監視、指導、管理下にあり、必要に応じて適切な治療ができる点にある。例えば慢性患者や高齢者の場合には、急激な病態変化がなければ安定した生理的状態にあり、一定の治療を続けて、その治療効果を継続的に監視し続けていることが最も大切なこととなる。
【0009】
在宅ケアシステムには、(1)小型で(2)簡便に(3)微量の血液を用いて(4)多項目を(5)迅速に(6)精度よく測定できる血液分析方法が望ましいのはいうまでもない。特に、高齢者(場合によっては小児)を対象とする場合、微量の血液の採取ですむ分析方法の開発が望まれている。
これに対して、ウェットケミストリー分析法を用いた一体型の家庭用分析装置が提案されている(特開2001−258868号公報)が、簡便さ、大きさ、安い点でも満足できるものではなかった。
【0010】
また、上記特許文献1から3の従来技術では、一つの項目を検査するための各種操作を一つの装置の中に集約して、行うのに多量の検査液を使用することになり、装置も大がかりで検査に至るまでに装置を回転させる等、大がかりな動作が必要となる。
【0011】
本発明の目的は、検体以外の全ての試薬等を分析用チップ内に封入した、メンテナンスの必要のないオール・イン・ワン・タイプの構造を有し、分析に必要な検体及び試薬の量を微量とすることができ、さらに、簡便に短時間で且つ低コストで分析を行うことが可能であって、一つの機構で1検査を実施でき、煩雑な操作をする必要がない、少量の検査液にて一つ動作で、多項目の検査を容易にした小型の検査チップ及びその検査チップを使用した検査方法を提供することにある。
【課題を解決するための手段】
【0012】
本発明の上記目的は、下記構成によって達成される。
(1) 被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、チップ本体と、前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、前記チップ本体に設けられ、前記試薬を収容保持する反応部と、前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、前記検体輸送部には液吸収体が設けられており、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで吸液し、前記検体輸送部をスライドさせた第2の位置で、前記被検査液を吸液した前記液吸収体が前記反応部に保持された前記試薬に接触することを特徴とする検査チップ。
(2) 前記検体輸送部には、前記チップ本体に対してスライドさせた状態で、前記前処理部に残留した前記被検査液と接触して吸液可能な残液吸収材が設けられていることを特徴とする上記(1)に記載の検査チップ。
(3) 前記液吸収体が前記反応部に接触する位置にある状態で、前記残液吸収材が前処理部に残留した前記被検査液に接触する構成であることを特徴とする上記(2)に記載の検査チップ。
(4) 前記チップ本体には、前記前処理部に前記被検査液を導入するための導入部が設けられていることを特徴とする上記(1)から(3)のいずれか1つに記載の検査チップ。
(5) 前記反応部に乾燥試薬が保持されていることを特徴とする上記(1)から(4)のいずれか1つに記載の検査チップ。
(6) 前記反応部が複数設けられていることを特徴とする上記(1)から(5)のいずれか1つに記載の検査チップ。
(7) 前記液吸収部が複数設けられていることを特徴とする上記(1)から(6)のいずれか1つに記載の検査チップ。
(8) 前記試薬がHbA1cを検出する材料であることを特徴とする上記(1)から(7)のいずれか1つに記載の検査チップ。
(9) 前記試薬がCRPを検出する材料であることを特徴とする上記(1)から(7)のいずれか1つに記載の検査チップ。
(10) 被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、チップ本体と、前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、前記検体輸送部には液吸収体が設けられ、前記液吸収体には前記試薬を保持可能な反応部が設けられ、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで該被検査液を吸液するとともに、前記被検査液が前記反応部の前記試薬に接触することを特徴とする検査チップ。
(11) 上記(1)から(10)のいずれか1つに記載の検査チップを用いて、前記被検査液を前記試薬に反応させる検査を行うことを特徴とする検査方法。
【0013】
上記の本発明に係る検査チップにおいて、チップ基板材は無機材質でも良いし、有機材質でもいい。基板に使用される無機材質の例を挙げれば金属、シリコン、テフロン(登録商標)、ガラス、セラミックスなどである。有機材質はプラスチック、ゴムなどである。
【0014】
プラスチックの例としては、PCO、PS、PC、PMMA、PE、PET、PP等を挙げることができる。ゴムの例としては、天然ゴム、合成ゴム、シリコンゴム、PDMS等を挙げることができる。シリコン含有物質としては、ガラス、石英、シリコンウエファー等のアモルファスシリコン、ポリメチルシロキサンなどのシリコーンが挙げられる。
【0015】
コストと加工のし易さの面では、プラスチックは好ましい。特に好ましい例としては、PMMA、PCO、PS、PC、PET、PEN等を挙げることができる。
【0016】
検体を採取し、前処理部に供給する手段としては、一定秤量できるキャピラリーを用いることが好ましい。キャピラリーの材質はプラスチックとガラスが好ましい。
【0017】
キャピラリーの内表面の親水性を持つことが必要である。キャピラリーの材質が親水性ではない時親水化処理が必要である。親水化処理法として、従来の表面処理方法が適用できる。大きく分けて、化学的表面処理法と物理的表面処理法がある。化学的表面処理法としては、薬品処理、カップリング剤による処理、蒸気処理、グラフト化、電気化学的方法、添加剤による表面改質などがある。物理的表面処理法としては、UV照射、電子線処理、イオンビーム照射、低音プラズマ処理、CASING処理、グロー、コロナ放電処理、酸素プラズマなどの方法がある。
【0018】
なお、上記のように液体の検体と処理試薬とを混合して検体の前処理をするための容器には、一定体積の処理試薬溶液が予め封入されている。処理試薬溶液の体積は20〜20000μLが好ましい、より好ましくは50〜2000μL、さらに好ましくは100〜1000μLである。
【0019】
また、検体の前処理容器中の処理試薬溶液を漏出しないようにシール部材で密封されることが好ましい。前記試薬部位は非流動性の反応試薬が好ましい。さらに好ましいのは多層乾式分析要素(乾燥試薬)である。
【0020】
本発明でいう多層乾式分析要素とは、検体中の被測定成分の定性・定量分析に必要な全てのまたはその一部分の試薬を1層以上の層に組み込んだ乾式分析要素のことをいう。いわゆるドライケミストリーを使用した分析要素である。具体的には、このような多層乾式分析要素の例は、富士フイルム研究報告、第40号(富士写真フイルム株式会 社、1995年発行)p.83や、臨床病理、臨時増刊、特集第106号、ドライケミストリー・簡易検査の新たなる展開(臨床病理刊行会、1997年発行) 等に記載されているものをあげることができる。
【0021】
上記した多層乾式分析要素は、通常少なくとも一つの機能層を含む。機能層の数は一つ以上であれば特に限定されず、1層でもよいし、2層以上の複数の層とすることもできる。
【0022】
機能層の具体例としては、展開層、展開層と展開層以外の機能層とを接着する接着層、液状試薬を吸水する吸水層、化学反応により生成した色素の拡散を防止する媒染層、ガスを選択的に透過させるガス透過層、層間での物質移動を抑制・促進させる中間層、反射測光を安定に行うための光遮蔽層、内因性色素の影響を抑制する色遮蔽層、分析対象物と反応する試薬を含む試薬層、発色剤を含む発色層などが挙げられ、これらは必要に応じて適宜選択することができる。
【0023】
多層乾式分析要素の一例としては、例えば、支持体の上には、場合によっては下塗層等の他の層を介して、機能層として親水性ポリマー層を設けることができる。親水性ポリマー層としては、例えば、無孔性、吸水性かつ水浸透性の層であり、基本的に親水性ポリマーのみなる吸水層、親水性ポリマーをバインダーとし発色反応に直接関与する発色試薬の一部又は全部を含む試薬層、及び親水性ポリマー中に発色色素を固定し不動にする成分(例:媒染剤)を含有する検出層などを設けることができる。
【0024】
(試薬層)
試薬層は水性液体中の被検成分と反応して光学的に検出可能な変化を生じる試薬組成物の少なくとも一部が親水性ポリマーバインダー中に実質的に一様に分散されている吸水性で水浸透性の層である。この試薬層には指示薬層、発色層なども含まれる。
【0025】
試薬層のバインダーとして用いることができる親水性ポリマーは、一般には水吸収時の膨潤率が30℃で約150%から約2000%、好ましくは約250%から約1500%の範囲の天然または合成親水性ポリマーである。そのような親水性ポリマーの例としては、特開昭60−108753号公報等に開示されているゼラチン(例、酸処理ゼラチン、脱イオンゼラチン等)、ゼラチン誘導体(例、フタル化ゼラチン、ヒドロキシアクリレートグラフトゼラチン等)、アガロース、プルラン、プルラン誘導体、ポリアクリルアミド、ポリビニルアルコール、ポリビニルピロリドン等をあげることができる。
【0026】
試薬層は架橋剤を用いて適宜に架橋硬化された層とすることができる。架橋剤の例として、例えば、ゼラチンに対する1,2−ビス(ビニルスルホニルアセトアミド)エタン、ビス(ビニルスルホニルメチル)エーテル等の公知のビニルスルホン系架橋剤、アルデヒド等、メタリルアルコールコポリマーに対するアルデヒド、2個のグリシジル基含有エポキシ化合物等がある。
【0027】
試薬層の乾燥時の厚さは約1μmから約100μmの範囲であることが好ましく、より好ましくは約3μmから約30μmの範囲である。また試薬層は実質的に透明であることが好ましい。
【0028】
多層乾式分析要素の試薬層やその他の層に含める試薬としては、被験物質に応じてその検出に適した試薬を選択することができる。
【0029】
(光遮蔽層)
前記試薬層の上に必要に応じて光遮蔽層を設けることができる。光遮蔽層は、光吸収性または光反射性(これらを合わせて光遮蔽性という。)を有する微粒子が少量の被膜形成能を有する親水性ポリマーバインダーに分散保持されている水透過性または水浸透性の層である。光遮蔽層は試薬層にて発生した検出可能な変化(色変化、発色等)を光透過性を有する支持体側から反射測光する際に、後述する展開層に点着供給された水性液体の色、特に試料が全血である場合のヘモグロビンの赤色等、を遮蔽するとともに光反射層または背景層としても機能する。
光反射性を有する微粒子の例としては、二酸化チタン微粒子(ルチル型、アナターゼ型またはブルカイト型の粒子径が約0.1μmから約1.2μmの微結晶粒子等)、硫酸バリウム微粒子、アルミニウム微粒子または微小フレーク等を挙げることができ、光吸収性微粒子の例としては、カーボンブラック、ガスブラック、カーボンミクロビーズ等を挙げることができ、これらのうちでは二酸化チタン微粒子、硫酸バリウム微粒子が好ましい。特に好ましいのは、アナターゼ型二酸化チタン微粒子である。
【0030】
被膜形成能を有する親水性ポリマーバインダーの例としては、前述の試薬層の製造に用いられる親水性ポリマーと同様の親水性ポリマーのほかに、弱親水性の再生セルロース、セルロースアセテート等を挙げることができ、これらのうちではゼラチン、ゼラチン誘導体、ポリアクリルアミド等が好ましい。なお、ゼラチン、ゼラチン誘導体は公知の硬化剤(架橋剤)を混合して用いることができる。
【0031】
光遮蔽層は、光遮蔽性微粒子と親水性ポリマーとの水性分散液を公知の方法により試薬層の上に塗布し乾燥することにより設けることができる。また光遮蔽層を設ける代りに、前述の展開層中に光遮蔽性微粒子を含有させてもよい。
【0032】
(接着層)
試薬層の上に、場合によっては光遮蔽層等の層を介して、展開層を接着し積層するために接着層を設けてもよい。
【0033】
接着層は、水で湿潤しているとき、または水を含んで膨潤しているときに展開層を接着することができ、これにより各層を一体化できるような親水性ポリマーからなることが好ましい。接着層の製造に用いることができる親水性ポリマーの例としては、試薬層の製造に用いられる親水性ポリマーと同様な親水性ポリマーがあげられる。これらのうちではゼラチン、ゼラチン誘導体、ポリアクリルアミド等が好ましい。接着層の乾燥膜厚は一般に約0.5μmから約20μm、好ましくは約1μmから約10μmの範囲である。
【0034】
なお、接着層は試薬層上以外にも、他の層間の接着力を向上させるため所望の層上に設けてもよい。接着層は親水性ポリマーと、必要によって加えられる界面活性剤等を含む水溶液を公知の方法で、支持体や試薬層等の上に塗布する方法などにより設けることができる。
【0035】
(吸水層)
多層乾式分析要素には、支持体と試薬層の間に吸水層を設けることができる。吸水層は水を吸収して膨潤する親水性ポリマーを主成分とする層で、吸水層の界面に到達または浸透した水性液体試料の水を吸収できる層であり、特に検体として全血試料を用いる場合には水性液体成分である血漿の試薬層への浸透を促進する作用を有する。吸水層に用いられる親水性ポリマーは前述の試薬層に使用されるもののなかから選択することができる。吸水層には一般的にはゼラチンまたはゼラチン誘導体、ポリアクリルアミド、ポリビニルアルコール、特に前述のゼラチン又は脱イオンゼラチンが好ましく、試薬層と同じ前述のゼラチンが最も好ましい。吸水層の乾燥時の厚さは約3μmから約100μm、好ましくは約5μmから約30μmの範囲、被覆量では約3g/m2から約100g/m2、好ましくは約5g/m2から約30g/m2の範囲である。吸水層には後述するpH緩衝剤、公知の塩基性ポリマー等を含有させて使用時(分析操作実施時)のpHを調節することができる。さらに吸水層には公知の媒染剤、ポリマー媒染剤等を含有させることができる。
【0036】
(検出層)
検出層は、一般に、被検成分の存在下で生成した色素等が拡散し、光透過性支持体を通して光学的に検出され得る層で、親水性ポリマーにより構成することができる。媒染剤、例えばアニオン性色素に対してカチオン性ポリマーを、含んでもよい。前述の吸水層は、一般に、被検成分の存在下で生成する色素が実質的に拡散しないような層を言い、この点で検出層とは区別される。
【0037】
多層乾式分析要素は、公知の方法により調製、作製することができ、一辺約1mmから約30mmの正方形またはほぼ同サイズの円形等の小片に裁断して用いることができるが、必要に応じてさらに小さくすることも可能である。このような多層乾式分析要素はすでに多数開発・商品化されており、富士ドライケム(富士写真フイルム(株)製)などはその1例である。本発明においては、このような多層乾式分析要素そのものを使用する。またはその一部分を使用することもできる。
【0038】
上記多層乾式分析要素は、複数的に試薬部に配置する。前記多層乾式分析要素の配置方向は液体吸収部(展開層)と平行させるのが好ましい。この検体の移動する手段としては、液体吸収体を用い、この液体吸収体をスライダーに固定し、スライダーを検体前処理容器の上部に通過することによって、液体吸収体と検体処理液と接触させる。さらに、前記吸収体を反応部に移動させ、反応部にある多層乾式分析要素と合体して、検体の移送が完成する。
【0039】
上記の液体吸収体は検体液と接触した場合に一定量の検体液を包容する性質を有する限り、繊維質材料でもよいし、非繊維質材料でもよい。繊維質材料としては、例えば濾紙、不織布、織物布地(例えば、特開昭55−164356号公報、特開昭57−66359号公報等に記載の織物布地)、編物布地(例えば、特開昭60−222769号公報等に記載の編物布地)、ガラス繊維濾紙等を用いることができる。
【0040】
非繊維質材料としては、特公昭53−21677号公報、米国特許3,992,158等に記載のメンブランフイルタ(ブラッシュポリマー層)、ポリマーミクロビーズ、ガラスミクロビーズ、珪藻土が親水性ポリマーバインダーに保持されてなる連続微空隙含有多孔性層等の非繊維等方的多孔性物質層、特開昭55−90859号公報に記載のポリマーミクロビーズが水で膨潤しないポリマー接着剤で点接触状に接着されてなる連続微空隙含有多孔性物質層(三次元格子状粒状構造物層)からなる非繊維等方的多孔性物質層等を用いることができる。
【0041】
多孔性物質膜としては、有機高分子からなる多孔膜を使用することもできる。具体的には、6,6−ナイロン、6−ナイロン、アクリレート共重合体、ポリアクリレート、ポリアクリロニトリル、ポリアクリロニトリル共重合体、ポリアミド、ポリイミド、ポリアミドイミド、ポリウレタン、ポリエーテルスルホン、ポリスルホン、ポリエーテルスルホンとポリスルホンの混合物、ポリエステル、ポリエステルカーボネート、ポリエチレン、ポリエチレンクロロトリフルオロエチレン共重合体、ポリエチレンテトラフルオロエチレン共重合体、ポリ塩化ビニル、ポリオレフィン、ポリカーボネート、ポリテトラフルオロエチレン、ポリビニリデンジフルオライド、ポリフェニレンスルフェレンスルフィド、ポリフルオロカーボネート、ポリポロピレン、ポリベンズイミダゾール、ポリメアクリル酸メイル、スチレンーアクリロニトリル共重合体、スチレンーブタジエン共重合体、エチレンー酢酸ビニル共重合体の鹸化物、ポリビニルアルコール、セルロースアセテートブチレートの鹸化物、セルロースアセテートブチレートブチレート、セルロースアセテートブチレートの鹸化物またはこれらの混合物などを使用することができる。
【0042】
特開昭61-4959(対応米国特許 5,019,347; 対応欧州公開 EP 0166365A)、特開昭62-116258 、特開昭62-138756(対応欧州公開 EP 0226465A)、特開昭62-138757(対応欧州公開 EP 0226465A)、特開昭62-138758(対応欧州公開 EP 0226465A)等に記載の部分接着された複数の多孔性層の積層物も好適である。
【0043】
また、高分子ゲル(天然高分子ゲル:ゼラチン、寒天、アガロペクチン、デンプン、アミロース、アミロペクチン、カラギーナン、ジエランガム、キタンサンガム、カードラン、コラーゲン、アルギニン酸、ペクチン、コンニャクマンナン、メチルセルロース、ヒドロキシプロピルセルロ−ス、デキストラン;合成高分子ゲル:ポリエチレン,ポリスチレン、ポリアクリレート、ポリアクリル酸、ポリメタクリル酸、ポリグルタミン酸、ポリビニルピリジン、ポリビニルイミダゾール、アクリルアミド、 ビニルピロリドン、メタクリル酸ヒドロキシエチル、0−ベンジルーL−グルタメート、ポリエチレングリコール、ヒアルロン酸)、ラテックス粒子、無機材料(多孔質炭素多孔質炭化珪素、多孔質ガラスビーズ、シリカゲル、酸化アルミナ、ゼオライト、メソポーラス)も好適である。
【0044】
検出手段としては、多層乾式分析要素内の発色又は変色を光透過性支持体側から反射測光し、予め作成した検量線を用いて比色測定法の原理により検体中の被験物質の量を求めることができる。また必要に応じて透過測光することも可能である。さらに、本発明の分析チップはエリアセンサによっても測定できる。
【0045】
エリアセンサは、CCD等の固体撮像素子であり、多項目測定乾式分析要素中の試薬担持部の試薬と血液等の検体とが反応した際に光源から照射される光によって反射する光を受光し、受光した光を電気信号に変換してコンピュータに出力するものである。エリアセンサは、試薬担持部から反射する光を面単位で受光可能である。このため、各試薬のエリアを同時に、すなわち複数項目について測定が可能である。また、検体からの反射光をCCD等のエリアセンサを用いて受光しているが、エリアセンサに限らず、ラインセンサを用いても構わない。
【発明の効果】
【0046】
本発明によれば、検体以外の全ての試薬等を分析用チップ内に封入した、メンテナンスの必要のないオール・イン・ワン・タイプの構造を有し、分析に必要な検体及び試薬の量を微量とすることができ、さらに、簡便に短時間で且つ低コストで分析を行うことが可能であって、一つの機構で1検査を実施でき、煩雑な操作をする必要がなく、少量の検査液にてワン動作で、多項目の検査を容易にした小型の検査チップ及びその検査チップを使用した検査方法を提供できる。
【発明を実施するための最良の形態】
【0047】
以下、本発明の実施形態を図面に基づいて詳しく説明する。
最初に、本発明に係る検査チップの構成を説明する。
図1は、検査チップの分解斜視図である。図2は、検査チップの上面図である。図3は、検査チップの断面図である。図4及び図5は、検査チップの動作の状態を示す図である。
【0048】
検査チップ10は、チップ本体11と、検体輸送部21と、検体輸送部21をチップ本体11に対してスライド自在に取り付ける取付部材31とから概略構成されている。
【0049】
チップ本体11は、略長方体形状を有し、透視可能な透明又は半透明な材料から構成されている。チップ本体11は、上方視した状態(図1の上方からみた状態)で矩形形状を有し、スライドする検体輸送部21を支持する支持板部11aと、支持板部11aの周縁辺のうち3辺から上方に垂直に立設された側板部11bとを有している。
【0050】
チップ本体11の支持板部11aには、検体輸送部21の下面側とスライド時に摺接する面である上面に凹設された凹部面11eが形成されている。また、凹部面11eの上面側には、凹部である前処理部12と、前処理部12の近傍に、支持板部11aの上面に凹設されてなる反応部13とが設けられている。
【0051】
本実施形態においては、前処理部12には、予め、検体となる希釈液が貯留されており、検査時に前処理部12に微量の血液が導入され、前処理部12において希釈液と血液とが混合されることで被検査液Lが生成される。また、反応部13には、被検査液Lの反応を調べるための試薬が収容保持される。
【0052】
本実施形態の検査チップ10において、前処理部12及び反応部13を密閉するため、凹部面11eにテープ状のシール部材16が接着されている構成とすることが好ましい。こうすることで、前処理部12に貯留された希釈液や反応部13に収容保持された試薬が漏れ出てしまうことを防止することができる。
【0053】
また、チップ本体11は、凹部面11e近傍の側板部11cの一部に切欠部11cが設けられている。凹部面11eの接着されたシール部材16の一部が切欠部11cに配置され、チップ本体11の外部に突出している。検査時には、使用者がチップ本体11の切欠部11cから突出したシール部材16を把持し、引き抜くことで、シール部材16が凹部面11eから引き剥がされ、前処理部12及び反応部13が開放される。
【0054】
チップ本体11には、前処理部12に一方の端部が連通し、且つ、チップ本体11の外側面に他方の端部が連通する一対の導入部14a,14bが設けられている。これら一対の導入部14a,14bの一方を介して、血液が前処理部12の内部に導入される。このとき、予め、導入部14a,14bの一方(本実施形態では導入部14b)には、図示しない栓部材が装填され、検査時に開栓ピン18を導入部14bに挿入することで、栓部材を前処理部12内に押し出し、導入部14bを開通させた後に、血液を導入部14bを介して前処理部12内に導入する。このとき、他方の導入部14aは、導入部14bから導入する血液が前処理部12内の空気によって逆流することを防止するための空気抜けとして機能する。また、他方の導入部14aが、検査時以外において開栓ピン18を収容保持するためのピン保持部として機能することが好ましい。
【0055】
検体輸送部21は、略長方体形状を有する板状部材である。検体輸送部21の下側面には、残液吸収材24を収容保持できるように凹設された、吸収材保持部22と、液吸収体25を収容保持できるように凹設された、液吸収部23とが形成されている。
【0056】
検体輸送部21は、チップ本体11に取り付けた状態で、チップ本体11の側板部11cによってその3辺の位置が支持されることで、チップ本体11に対する位置が規制される。
【0057】
取付部材31は、チップ本体11の側板部11bの長手寸法と略同一寸法を有する長方形板状の部材であって、それぞれに複数(本実施形態ではそれぞれ3つ)のネジ挿通穴31aが形成されている。また、チップ本体の側板部11bの上端面には、複数のネジ止め孔11dが形成されている。取付部材31をチップ本体11に取り付ける場合には、ネジ挿通穴31aにネジ32をそれぞれ挿通するとともに、ネジ32の先端をチップ本体の側板部11bのネジ止め孔11dに螺合することで、取付部材31をチップ本体11に固定することができる。
【0058】
図2に示すように、取付部材31をチップ本体11に固定した状態で、チップ本体11上に支持された検体輸送部21の上面の一部が、チップ本体11と取付部材31との間で挟まれて支持される。このため、検体輸送部21がチップ本体内11の上面から水平に離間することが回避される。
【0059】
本実施形態の検査チップ10は、使用者が、検体輸送部21をチップ本体11の支持板部11a上の、側板部11bが設けられていない端縁辺側へ手指で押し動かすことにより、スライドさせて移動できる。
【0060】
なお、本実施形態の検査チップ10においては、チップ本体11の反応部13と、検体輸送部21の液吸収部23との数をそれぞれ2つとしたが、検査する量や検査項目等に応じて、数を変更してもよい。
【0061】
次に、本発明に係る検査チップの動作の一例を説明する。
先ず、検査チップ10の前処理部12に、希釈液を予め貯留させ、また、反応部13に試薬15を収容保持させておく。そして、導入部14a,14bの一方から微量の血液を前処理部12内に導入する。前処理部12内において希釈液と血液とを混合させて被検査液Lを生成する。その後、シール部材16を剥して前処理部12の凹部を開放させる。
【0062】
次に、検体搬送部21の一部を手指で把持し、図2及び図3に示すように、該検体搬送部21をスライドさせることで、チップ本体11に対する位置を変える。
【0063】
図4に示すように、検体搬送部21の液吸収部23をチップ本体11の前処理部12の上方にくる位置(第1の位置)にスライド移動させると、液吸収部23に収容保持され液吸収体25の一部が前処理部12に貯留された被検査液Lと接触することで、該被検査液Lを吸液する。
【0064】
ここで、検体輸送部21が第1の位置にある状態で、液吸収体25は、その一部が前処理部12側へ弾性変形する形状、構成、又はそのような素材であることが好ましい。こうすれば、液吸収体25を前処理部12に貯留された被検査液Lにより確実に接触させることができる。
【0065】
続いて、図5に示すように、検体搬送部21を更にスライドさせ、検体搬送部21の液吸収部23がチップ本体11の反応部13の上方にくる位置(第2の位置)まで移動すると、液吸収部23の液吸収体25に吸液されている被検査液Lが反応部13の試薬15と接触する。このとき、被検査液Lと試薬15とが所定の反応を起し、使用者が検査チップ10の外部から、透明なチップ本体11及び検体搬送部21を介して視認することができ、被検査液Lと試薬15との反応に基づいて、検査の状態を観察することができる。
【0066】
このとき、検体輸送部21の残液吸収材24が、前処理部12に残留した被検査液Lと接触することで、残留した被検査液Lが残液吸収材24に吸液される構成とすることが好ましい。こうすれば、前処理部12から残留した被検査液Lが漏れ出ることを防止することができるため、使い勝手が良い。
【0067】
検査チップ10は、検査時に導入する検体(本実施形態では血液)のを除く、他の全ての試薬等を検査前に予めチップ本体11内に封入して保存することができるためメンテナンスが不要である。また、検査に必要十分の量の検体を前処理室に導入し、
また、最低限の試薬を反応部に収容保持すればよいため、検査に必要な検体及び試薬の量を微量とすることができる。
さらに、検体搬送部21をチップ本体11に対して手指でスライドさせるといいた簡単な構成であるため、検査にかかる作業を簡便にすることができるとともに、検査にかかる時間を短時間とすることができ、且つ、検査を低コストで行うことが可能である。
【0068】
チップ本体11に対してスライド自在な検体輸送部21を備えた機構であるため、1つの機構で1つの検査を実施でき、従来の検査方法のように、煩雑な操作を行う必要がなく、反応部13及び液吸収部23の数を増やすことで、一回の操作で多項目の検査を容易に行うことができる。
【0069】
以下、本発明に係る実施例とその比較例を挙げて本発明を詳しく説明する。なお、本発明は以下の実施例に限定されるものではない。本実施例においては、図1から5に示す上記実施形態の検査チップを使用した。
(実施例1)
実施例1の作動を説明する。
最初に、検査チップ10の導入部14bに、採血キャピラリーを挿入し、血液を前処理部12内に導入する。ここで、採血キャピラリーは別穿刺器具(図示せず)により皮膚上に摘出された血液を毛細管作用により吸引し、吸引と同時に秤量を行う部材である。
秤量された血液1μLを含んだ採血キャピラリー1はキャピラリー押し(図示せず)により押し込まれて前処理部12内(希釈液200μL封入されている)に挿入される。その後、検査チップ10全体を揺することで秤量された採血キャピラリー内の血液が前処理部12内に貯留された希釈液に溶け、該希釈液と混合されることになる。このとき、前処理部12内の採血キャピラリーは撹拌子の役目をはたす事になり混合を補助する。
【0070】
その後、検査試薬部シール16を矢印の方向に引くことでシールが剥がれて、液吸液部23で被検査液を搬送する準備が完了する。
【0071】
次に、検体輸送部21の上面を手指の腹面で保持し、図2及び図3で示す矢印の方向に押し進めることで、液吸液部23と吸収材保持部22との位置が代わり、液吸液部23が前処理部12上を通過することで液吸収体25被検査液Lを吸収する。そして、該液吸収体25が反応部13に収容保持された試薬15に接触することで、液吸収体25に吸液されている被検査液Lと試薬15との間で反応が行われ、使用者が反応後の比色検査を視認可能となる。検体輸送部21の吸収材保持部22に保持された残液吸収材24が、前処理部12上に到達し、該算液吸収材24が前処理部12内に残留した被検査液Lを吸収して検査チップ内からの液漏れを防止する。
【0072】
(実施例2)
次に、CRPの検出の動作を説明する。
本実施例において、特開2003-75445号公報に記載の実施例と同様の方法で、CRP用多層乾式スライドを作製した。
CRP濃度が既知のCRP標準血清1μLをキャピラリー1で秤量し、前処理部12(希釈液200μLを事前入れたもの)内に挿入される。その後、検査チップ10全体を振動させて、希釈液と血液とを混合する。その後、シール部材16を剥して前処理部12の凹部を開放させた。検体輸送部21をスライドさせることで、液吸収体25と残液吸収材24とがともに移動を開始し、液吸収体25が前処理室12上を通過することで被検査液Lを吸収し、反応部13の試薬15に到達し接触する。
【0073】
ここで、検査チップ10近傍の環境雰囲気を37℃に保って、分光光度計(MCPD-2000(大塚電子))でPET支持体側から中心波長650nmの可視光で反射光学濃度を測定した。点着から3分後および5分後の反射光学濃度の差(ΔOD5-3)を求めて、検量線からCRPの量を求める(測定回数、N=5)。CRPの測定値 (g/dL) は3.3±0.15であり、CVは4.5%であった。
【0074】
(実施例3)
次に、下記実施例のように、ヘモグロビン(Hb)とグリコヘモグロビン(HbA1c)の検出を行った。
本実施例では、特開平8−122335号公報に記載の実施例2と同様の方法で、ヘモグロビンA1c用多層乾式スライドを作製した。そして、全血1μLをキャピラリーで秤量し、前処理部12(溶血液200μLを事前入れ)内に挿入される。その後、検査チップ10全体を振動させて、血液と希釈液とを混合する。その後、シール部材16を剥して前処理部12の凹部を開放させた。検体輸送部21をスライドさせることで、液吸収体25と残液吸収材22とが移動し、液吸収体25が前処理部12上を通過する際に被検査液Lを吸収し、試薬15に接触する。
【0075】
検査チップ10近傍の環境雰囲気を37℃に保って、分光光度計(MCPD-2000(大塚電子))でPET支持体側から中心波長650nmの可視光で反射光学濃度を測定した。点着から3分後および5分後の反射光学濃度の差(ΔOD5-3)を求めて、検量線からヘモグロビンA1Cの量を求めた(測定回数N=3とした。)。ヘモグロビンA1Cの測定値 (g/dL)は、1.07±0.04となり、CVは3.7%となった。同時にもう一枚のヘモグロビン(Hb)スライドの支持体側から、中心波長420nmの可視光で反射光学濃度を測定した。点着から0.5分後の反射光学濃度ODから、検量線からヘモグロビン(Hb)の量を求める(測定回数、N=3)。ヘモグロビン(Hb)の測定値 (g/dL)は13.2±0.4となり、CVは3.0%となった。
【0076】
図6及び図7に、本発明に係る検査チップの変形例を示す。なお、以下に説明する実施形態において、すでに説明した部材などと同等な構成・作用を有する部材等については、図中に同一符号又は相当符号を付すことにより、説明を簡略化或いは省略する。図6は、本発明に係る検査チップの変形例を示す上面図である。また、図7は、図6に示す検査チップの液吸収体の構成を示す図である。なお、図6で示す検査チップ20は、上記実施形態の検査チップ10の構成及び動作と基本的に同じである。以下、異なる点についてのみ説明する。
【0077】
検査チップ20は、検体輸送部21の液吸収部23に収容保持された液吸収体55が被検査液を吸液する機能、試薬との反応を行う機能とを兼ね備えた構成である。このため、検査チップ20は、チップ本体11に前処理部12が形成されているものの、上記実施形態の検査チップ10における反応部13が形成されていない。
【0078】
液吸収体55は、検体輸送部21の液吸収部23に固定される基端部55aと、基端部55aに対して変形し、検体輸送部21をスライドさせた際に、チップ本体11の前処理部12に貯留された被検査液と接触する部位である接触部55bとから構成されている。そして、接触部55bには、被検査液と接触することで所定の変化を起す試薬を含有した試薬を保持する反応部45が形成されている。反応部45に含有される試薬の材料としては、上記実施形態の反応部13に収容保持される試薬15と同じものを用いることができる。
【0079】
チップ本体11の前処理部12の近傍には、スライドさせた検体輸送部21の液吸収体55の第2の位置に対向する位置に、開口43が設けられている。使用者は、第1の位置で液吸収体55を前処理部12の被検査液Lに接触させた後、検体輸送部21を第2の位置に移動することで、開口43を介して液吸収体55の反応部45の色変化を観察することができる。
【0080】
以上説明したように、本発明の検査チップは、秤量採血し希釈液と混合させ、混合精度の良い被検査液を製作し、その被検査液に液吸収体を接触させることで正確な検査ができる。このため、従来技術では、1項目の検査を行うのに多量の検査液を使用することになり、装置も大がかりで検査に至るまでに装置を回転させる等、大がかりな動作が必要となるが、本発明の検査チップ及びその検査チップを用いた検査方法によれば、上記従来の問題点を回避して検査の効率を高めることができる。
【産業上の利用可能性】
【0081】
本発明は、アレルギー反応検査試薬として利用可能で数項目アレルギー反応の検査を一度で検査できる検査チップとして適用できる。
【図面の簡単な説明】
【0082】
【図1】検査チップの分解斜視図である。
【図2】検査チップの上面図である。
【図3】検査チップの断面図である。
【図4】検体輸送部が第1の位置にある状態を示す図である。
【図5】検体輸送部が第2の位置にある状態を示す図である。
【図6】本発明に係る検査チップの変形例を示す上面図である。
【図7】図6に示す検査チップの液吸収体の構成を示す図である。
【符号の説明】
【0083】
10,20 検査チップ
11 チップ本体
12 前処理部
13 反応部
15 試薬
21 検体輸送部
22 吸収材保持部
23 液吸収部
24 残液吸収材
25 液吸収体
L 被検査液
【特許請求の範囲】
【請求項1】
被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、
チップ本体と、
前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、
前記チップ本体に設けられ、前記試薬を収容保持する反応部と、
前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、
前記検体輸送部には液吸収体が設けられており、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで吸液し、前記検体輸送部をスライドさせた第2の位置で、前記被検査液を吸液した前記液吸収体が前記反応部に保持された前記試薬に接触することを特徴とする検査チップ。
【請求項2】
前記検体輸送部には、前記チップ本体に対してスライドさせた状態で、前記前処理部に残留した前記被検査液と接触して吸液可能な残液吸収材が設けられていることを特徴とする請求項1に記載の検査チップ。
【請求項3】
前記液吸収体が前記反応部に接触する位置にある状態で、前記残液吸収材が前処理部に残留した前記被検査液に接触する構成であることを特徴とする請求項2に記載の検査チップ。
【請求項4】
前記チップ本体には、前記前処理部に前記被検査液を導入するための導入部が設けられていることを特徴とする請求項1から3のいずれか1つに記載の検査チップ。
【請求項5】
前記反応部に乾燥試薬が保持されていることを特徴とする請求項1から4のいずれか1つに記載の検査チップ。
【請求項6】
前記反応部が複数設けられていることを特徴とする請求項1から5のいずれか1つに記載の検査チップ。
【請求項7】
前記液吸収部が複数設けられていることを特徴とする請求項1から6のいずれか1つに記載の検査チップ。
【請求項8】
前記試薬がHbA1cを検出する材料であることを特徴とする請求項1から7のいずれか1つに記載の検査チップ。
【請求項9】
前記試薬がCRPを検出する材料であることを特徴とする請求項1から7のいずれか1つに記載の検査チップ。
【請求項10】
被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、
チップ本体と、
前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、
前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、
前記検体輸送部には液吸収体が設けられ、前記液吸収体には前記試薬を保持可能な反応部が設けられ、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで該被検査液を吸液するとともに、前記被検査液が前記反応部の前記試薬に接触することを特徴とする検査チップ。
【請求項11】
上記請求項1から10のいずれか1つに記載の検査チップを用いて、前記被検査液を前記試薬に反応させる検査を行うことを特徴とする検査方法。
【請求項1】
被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、
チップ本体と、
前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、
前記チップ本体に設けられ、前記試薬を収容保持する反応部と、
前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、
前記検体輸送部には液吸収体が設けられており、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで吸液し、前記検体輸送部をスライドさせた第2の位置で、前記被検査液を吸液した前記液吸収体が前記反応部に保持された前記試薬に接触することを特徴とする検査チップ。
【請求項2】
前記検体輸送部には、前記チップ本体に対してスライドさせた状態で、前記前処理部に残留した前記被検査液と接触して吸液可能な残液吸収材が設けられていることを特徴とする請求項1に記載の検査チップ。
【請求項3】
前記液吸収体が前記反応部に接触する位置にある状態で、前記残液吸収材が前処理部に残留した前記被検査液に接触する構成であることを特徴とする請求項2に記載の検査チップ。
【請求項4】
前記チップ本体には、前記前処理部に前記被検査液を導入するための導入部が設けられていることを特徴とする請求項1から3のいずれか1つに記載の検査チップ。
【請求項5】
前記反応部に乾燥試薬が保持されていることを特徴とする請求項1から4のいずれか1つに記載の検査チップ。
【請求項6】
前記反応部が複数設けられていることを特徴とする請求項1から5のいずれか1つに記載の検査チップ。
【請求項7】
前記液吸収部が複数設けられていることを特徴とする請求項1から6のいずれか1つに記載の検査チップ。
【請求項8】
前記試薬がHbA1cを検出する材料であることを特徴とする請求項1から7のいずれか1つに記載の検査チップ。
【請求項9】
前記試薬がCRPを検出する材料であることを特徴とする請求項1から7のいずれか1つに記載の検査チップ。
【請求項10】
被検査液を試薬と反応させ、該被検査液を検査する検査チップであって、
チップ本体と、
前記チップ本体に設けられ、前記被検査液を貯留する前処理部と、
前記チップ本体に対してスライド自在に取り付けられた検体輸送部とを備え、
前記検体輸送部には液吸収体が設けられ、前記液吸収体には前記試薬を保持可能な反応部が設けられ、前記検体輸送部をスライドさせた第1の位置で、前記液吸収体が前記前処理部に貯留された前記被検査液と接触することで該被検査液を吸液するとともに、前記被検査液が前記反応部の前記試薬に接触することを特徴とする検査チップ。
【請求項11】
上記請求項1から10のいずれか1つに記載の検査チップを用いて、前記被検査液を前記試薬に反応させる検査を行うことを特徴とする検査方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2007−93275(P2007−93275A)
【公開日】平成19年4月12日(2007.4.12)
【国際特許分類】
【出願番号】特願2005−279932(P2005−279932)
【出願日】平成17年9月27日(2005.9.27)
【出願人】(306037311)富士フイルム株式会社 (25,513)
【Fターム(参考)】
【公開日】平成19年4月12日(2007.4.12)
【国際特許分類】
【出願日】平成17年9月27日(2005.9.27)
【出願人】(306037311)富士フイルム株式会社 (25,513)
【Fターム(参考)】
[ Back to top ]

