概日遺伝子活性化剤を含む皮膚修復組成物およびsirt1遺伝子活性化剤の相乗的組合せ
皮膚細胞の損傷DNAの修復を高めるための組成物および方法。皮膚細胞における概日遺伝子発現をアップレギュレートする少なくとも1種の作用物質および皮膚細胞における有糸分裂を遅らせる少なくとも1種の非概日作用物質を含む局所組成物。好ましくは、前記組成物は、1種以上のケラチノサイトclockおよびper1遺伝子活性化剤を、SIRT1または1種以上のsirt1活性化剤と共に含有する。さらに好ましくは、sirt1活性化剤は特定のペプチド性sirt1活性化剤とレスベラトロールとの相乗的組合せである。好ましくは、前記組成物は使いやすく、効果があり、化粧品的に許容され、化学的に、熱力学的におよび光に安定であり、局所使用に安全であり、副作用がほとんどまたは全くなく、また、パーソナルケア市場で商業的に実現可能なものである。
【発明の詳細な説明】
【技術分野】
【0001】
本出願は、2007年8月13日付けの係属中の米国特許出願US 11/837,658号の一部継続出願、および2009年2月9日付けの係属中の米国特許出願US 12/367,705号の一部継続出願であり、両出願の全内容を参照により本明細書に組み入れる。
【0002】
技術分野
本発明はスキントリートメントの分野に関するものである。より具体的には、本発明は、皮膚細胞における損傷DNAの修復を高めるための組成物および方法に関する。
【背景技術】
【0003】
皮膚がさまざまな環境要因と生活要因から毎日攻撃を受けていることは、今やよく理解されている。こうした要因のショートリストには、UVA放射線、UVB放射線、汚染、タバコの煙、貧しい食生活、不十分な休息、および心理的ストレスが含まれる。この攻撃は皮膚細胞のDNAとタンパク質への損傷として現れる。皮膚のラインやシワは皮膚細胞の損傷のより軽度の結果の一つであるが、メラノーマはより重篤な結果の一つである。
【0004】
DNA損傷
一部の環境および生活要因は皮膚細胞のDNAおよび/またはタンパク質と直接的に相互作用して損傷を引き起こし、一部の要因は間接的に損傷を引き起こし、また、一部の要因は両方をすることができる。直接的DNA損傷の例は、皮膚細胞のDNAがスペクトルのUVB部からの光子を吸収するときであると考えられる。光子の吸収はDNA配列に突然変異を起こすことがある。例えば、全メラノーマ発生の約8%は直接のDNA突然変異によるものである。
【0005】
皮膚細胞DNAおよびタンパク質の間接的損傷の例は、紫外線光子が皮膚に入って、発色団によって吸収されるときに見られる。励起状態では、発色団は活性酸素種の形成につながる反応に加わる。例えば、ヒトの皮膚では、UVB曝露は過酸化水素の産生と関連しており、一方UVAは一重項酸素の産生に関連している。皮膚がこれらの反応種を中和することによって恒常性を維持できない場合、その反応種は酸化を通して皮膚細胞のDNAとタンパク質を傷つけることになる。こうしたDNAおよびタンパク質への損傷は、酸化的ストレスと呼ばれており、皮膚老化の主な原因となる。さらに、全メラノーマ発生の約92%は間接的な酸化的DNA損傷によるものである。
【0006】
DNA損傷:予防および封じ込め-対-修復
DNAを含む皮膚細胞にはケラチノサイト幹細胞およびメラノサイトが含まれる。1回のサンバーンは、影響を受けた細胞において、T-T(チアミン-チアミン)ダイマー;8-オキソ-7,8-ジヒドロ-2'-デオキシグアノシン(8-オキソ-DG);06MeG (06-メチルグアニン);シクロブタンピリミジンダイマー(CPD);および6-4光分解生成物(6-4PP)など、何十万ものDNA変異原性塩基修飾をもたらすと推定される。これらの変異は皮膚細胞内のさまざまな反応を引き出し、そうした応答はさらなるDNA損傷または細胞のアポトーシスの予防につながる可能性がある。例えば、メラノサイトでのメラニン産生は、防護手段として、UV放射線によりアップレギュレートされることが知られている。UVからの脅威に対処するため、メラニンが表皮下層のメラノサイトによって産生され、外側に移動するケラチノサイトの助けを借りて、表皮上層および下層の全体に分布する。まず第一に、メラニンは、メラノサイトおよびケラチノサイト幹細胞が位置する表皮下層に入り込むUVの量を制限するUVフィルターとして作用することによって、さらなるUV誘発DNA損傷を予防するようである。しかし、第二次の防護として、メラニンは、ケラチノサイトのアポトーシスを誘導することによって、UV放射線によるDNA損傷を封じ込める。アポトーシスを促進することによって、娘細胞に伝えられる機会が少なくなり、損傷したDNAは封じ込められる(例えば、Yamaguchi et al., Melanin mediated apoptosis of epidermal cells damaged by ultraviolet radiation: factors influencing the incidence of skin cancer (紫外線による損傷を受けた表皮細胞のメラニン介在アポトーシス:皮膚がんの発生に影響を及ぼす因子); Arch Dermatol Res. 2008 Apr; 300 Suppl 1: S43-S50を参照されたい)。
【0007】
DNA損傷の予防および封じ込めとは別に、健全なケラチノサイトとメラノサイトは、DNA損傷を修復するための天然の内部機構をもっている。こうした機構は予防および封じ込めの機構とは異なっており、別の(しかし、時には重複する)反応カスケードを含んでいる。本発明の組成物および方法は、DNA損傷の修復に最も関係している。
【0008】
細胞修復機構は、我々が論じてきたUV誘発損傷だけでなく、さまざまな原因で生じるDNA損傷を修復するために存在する。しかしながら、DNA損傷の修復には時間がかかる。例えば、UVB曝露によって形成されたTTダイマーおよび6-4PP損傷の修復には、外的影響によって加速されないとすると、それぞれ48時間および8時間ほどかかる可能性がある。UVAもしくはUVB曝露、オゾン、またはタバコの煙および汚染による8-オキソ-dGおよび06MeG損傷の修復には、2時間ほどかかることがある。DNA損傷は細胞分裂が起こる前に修復されることが理想的である。もしそうでないなら、好ましい結果はアポトーシスである。しかし、DNA損傷がたまたまアポトーシスのアップレギュレーションに悪影響を及ぼす場合、または突然変異が検出されない場合には、損傷したDNAが次世代に伝わる可能性がある。本発明の組成物および方法は、細胞分裂が起こる前にDNA損傷の修復を最大限に高めることに最も関係している。
【0009】
細胞の予防および修復機構は概日時計によって制御される
通常の状態では、DNAの発現および修復を含めた細胞機能は、不定期に等確率で起こるものではない。それどころか、それぞれの細胞には約24時間の内因性周期(または時計)(すなわち、概日リズム)があり、細胞の活動はこの内因性周期によって調節されている。外部刺激がなければ、各細胞はその内因性時計に従ってフリーラン(free-run)するだろう。しかし、全身の細胞の内因性時計は同期化されている。細胞の活動を互いに同期化し、かつ環境と同期化するために、身体は環境からのシグナルを受け取ることができる。最も顕著な環境シグナルは日光の存在または不在である。こうして、概日周期は太陽日の位相にほぼ一致する明期と暗期で構成される。
【0010】
今では、概日リズムによって、細胞が細胞に影響を及ぼす可能性のある環境の変化を予知して、そうした変化にタイムリーに適応できることは理解されている。細胞の概日リズムの遺伝機構が適切に機能している限り、細胞は、その多くの機能のそれぞれを、細胞の生存および/または恒常性にとって最適な時期に、同期化された方法で実行する。例えば、昼が近づくにつれて(皮膚がUVから攻撃を受ける前であっても)、特定の遺伝子が、予測されるUV線によるダメージから細胞を保護するタンパク質を産生するように活性化される。その後、昼が終わりに近づくにつれて、これらの遺伝子はオフの状態になる。他方、概日遺伝子自体は環境要因によって攻撃を受ける可能性がある。細胞の概日リズムを調節している1つ以上の遺伝子が損傷すると、細胞は環境および他の細胞と同期化しない(out of sync)ことがある。
【0011】
コア概日機構
転写因子は、特定のDNA配列と結合して、DNAからの遺伝情報のRNAへの転写を制御しているタンパク質である。コア概日機構(core circadian mechanism)、または「細胞時計」は、位相を異にする(out-of-phase)、負および正のフィードバックループに参加する転写因子(振動遺伝子の転写をもたらす)で構成されている。
【0012】
哺乳類の主要な負のフィードバックループでは、CLOCKおよびBMAL1転写因子のヘテロダイマーがperiod (per)およびcryptochrome (cry)遺伝子の転写を活性化する。ヒトでは、period遺伝子は実際には3つの遺伝子per1、per2、およびper3からなるファミリーであり、また、cry遺伝子ファミリーにはcry1およびcry2の遺伝子が含まれる。それらの翻訳に続いて、PERおよびCRYタンパク質は細胞質に移動して、PER/CRY複合体を形成する。翻訳後制御は意図的な遅延を生じさせ、その後PER/CRY複合体は細胞核内に移動する。核内のPERとCRYの濃度は24時間周期の昼間の終わりにピークに達し、その時点でCRYタンパク質はCLOCK/BMAL1ヘテロダイマーの転写活性を抑制するように作用する。したがって、CRYは自らの転写をオフにするようである。
【0013】
他方、1つの正のフィードバックループでは、核に移行した後のPER2がBMAL1の転写をアップレギュレートして、最終的にはperiodおよびcry遺伝子の転写をもたらすようである。さらに、CLOCK/BMAL1ダイマーはrev-erbαおよびrora遺伝子をアップレギュレートするようである。roraはBMAL1転写を活性化する一方で、rev-erbαはCLOCKとBMAL1を抑制する。いわゆる「カノニカル時計遺伝子」(canonical clock genes)(clock、bmal1、per1、per2、per3、cry1およびcry2)のピーク活性は位相を異にして、結果的に、約24時間の周期をもつ自立的なループが生じる。
【0014】
細胞周期
細胞周期は、細胞の分裂と複製をもたらす、細胞内で起こる一連の事象をさす。その周期は通常、完了するまでに約24時間を必要とする4または5つの連続相として説明される。細胞周期の各相には、所定の相のすべての必要なプロセスが次の相の開始までに完了していることを保証するチェックポイントがある。ヒト細胞において、「第1」相は、細胞のDNAが複製および合成される合成(S)期である。S期は一般に6〜8時間続く。3〜4時間続くG2期では、タンパク質が合成され、かつ細胞の大きさが倍になる。有糸分裂(M)においては、核膜が破れて、遺伝物質の各コピーが細胞の反対極に分離できるようになる。染色体の各セットの周りに新しい核膜が形成されるのに続いて、細胞が2つに絞り込まれる(細胞質分裂)。M期は約1時間の長さである。最も長い第4相(6〜12時間)は、RNAとタンパク質の合成により特徴づけられるG1である。G1期から、細胞は再びS期に入ることもあれば、G0期に入ることもある。G0では、細胞は休止状態にある。G0は数日間または数年間続く場合もある。幹細胞はG0期から戻って、G1に入ることができる。分化した細胞は一般的にG0から戻ることはない。また、DNAが損傷を受けた細胞は、アポトーシスよりはむしろ、G0に入る。
【0015】
細胞周期チェックポイントは損傷DNAが受け継がれるのを阻止する
細胞分裂時には、細胞周期を経る細胞の進行状況を制御するためにチェックポイントが用いられる。チェックポイントは、すべての必要なプロセス(損傷DNAの修復を含む)が完了するまで、細胞が次の相に進行するのを防いでいる。このように、チェックポイントは、損傷を受けたまたは不完全なDNAが娘細胞に伝わらないようにしている。いくつかのチェックポイントが存在する。G1/Sチェックポイント(制限チェックポイント)は細胞周期を中断して、休止期に入るかまたは入らないの「決定」を行うことができる。G2/Mチェックポイントでは、損傷を受けたDNAが検出されると(これは珍しいことではない)、細胞周期が停止される。複製後チェックポイントは、合成期に複製された損傷DNAに関係する。損傷DNAの複製は、複製後修復過程が完了するまで細胞周期の進行を止める細胞応答を引き出す。ヒト細胞では、複製後チェックポイントは、有糸分裂期の開始を遅らせることによって修復のための時間をつくる。chk1遺伝子は複製後チェックポイントでの制御をもたらす一方、p53遺伝子はG1/SおよびG2/Mチェックポイントの両方でその制御機構を始動させるのに重要な役割を果たしている。
【0016】
概日時計は細胞増殖をも制御する
近年、細胞増殖を制御する上での概日時計の重要性が高く評価されている。例えば:
「概日タイミングの破壊は・・・細胞分裂の正常な調節に広範囲にわたって影響を及ぼす。」(Reddy et al., 2005 Circadian clocks: neural and peripheral pacemakers that impact upon the cell division cycle (概日時計:細胞分裂周期に影響を及ぼす神経および末梢ペースメーカー). Mutation Research 574 76-91)。
【0017】
「時計成分が細胞周期調節機構と相互作用するメカニズムへの詳細な洞察は、最近のマウス研究から端を発している。例えば、・・・肝組織の除去(部分的肝切除)とその後の有糸分裂の第1波の間の遅延は、手術が行われた日の時間に左右される。」(Vallone et al., 2007 Start the clock! Circadian rhythms and development (時計を起動させよ! 概日リズムと発生). Developmental Dynamics 236 142-155)。
【0018】
「シアノバクテリアから高等脊椎動物まで、夜間に起こるように細胞周期のS期と有糸分裂を「ゲーティング」する概日時計の多くの例が存在する。」(Vallone et al.) [おそらく、DNA合成と有糸分裂は太陽からの有害なUVまたは他の電離放射線からDNAを保護するために夜間に起こる]。
【0019】
こうして、概日時計は、DNAおよびタンパク質の合成、有糸分裂および細胞質分裂、RNAの合成および修復の細胞周期に包括的な影響を及ぼしている。したがって、環境要因が細胞の概日機構を妨げるとき、細胞機能が損なわれる。本発明者らは、治療が細胞の概日時計を同調させるかもしくは再同期化できるとき、または治療が概日遺伝子発現の「正常」レベルを回復できるとき、細胞機能が改善されるか、細胞損傷が加速的に修復されるか、またはアポトーシスがよりタイムリーに起こる可能性がある、と予想している。
【0020】
環境は概日リズムを同期しない状態に置くことができる
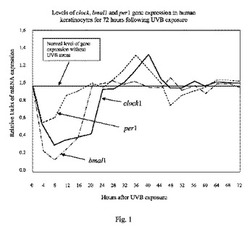
細胞の概日リズムを制御している1つ以上の遺伝子を妨げる作用物質は、細胞を、環境および他の細胞と同期しない状態に置くことができる。例えば、UV曝露後数時間、おそらく20時間もの間、ヒトケラチノサイトにおけるclock、bmal1およびper1遺伝子発現のレベルは大幅に低下する(図1参照)。「大幅に低下する」とは、これらの遺伝子が先に説明した通常の概日周期で経験する最小発現より少ないことを意味する。さらに、UV曝露後、遺伝子発現の通常のパターン(ほぼ正弦波として記載される)が失われる。
【0021】
図1において、水平線はclock遺伝子発現の通常の平均レベルを示しており、UV曝露後約44時間で開始して、その線についての典型的な概日変化を示している。対照的に、UVB曝露の直後に、遺伝子発現のレベルは通常をはるかに下回るレベルに落ちて、約20時間で通常のレベルに戻らなかった。その20時間にわたり、遺伝子発現の通常のパターンが3種すべての遺伝子で失われた。そして、遺伝子発現のレベルがほぼ通常のレベルに戻った場合でも、いつもの正弦波発現パターンが回復するのに約20時間から約44時間の時間が必要であった。こうして、UV曝露は2つの影響を及ぼした。一方の影響は概日遺伝子の発現レベルの劇的な低下であり、他方はそのパターン、すなわち、それらの発現のタイミングである。UV曝露後0時間から約44時間まで、DNAとタンパク質の合成、有糸分裂と細胞質分裂、RNAの合成と修復、ならびにプログラムされた細胞死(アポトーシス)のタイミングがすべて損なわれる。
【0022】
当然、UV曝露は昼間、特に午前10時から午後2時の決定的時間帯に起こる。すでに述べたように、核内のPERおよびCRYタンパク質の濃度は、24時間周期の昼間の終わりにピークに達し、その時点でCRYタンパク質はCLOCK/BMAL1ヘテロダイマーの転写を抑制するように作用する。clockおよびbmal1発現をオフにする臨界濃度への到達の遅れは概日周期を長くするだろう。こうして、UV曝露は概日周期を長くする傾向がある。これは細胞周期を環境と同期しない状態にする。DNA複製および有糸分裂が、細胞複製にとって最適な夜間に起こらない可能性がある。また、概日遺伝子が細胞周期に及ぼすゲーティングの影響が損なわれて、結果的にDNA損傷が検出されないか、修復されないことがあり、また、娘細胞に伝わる可能性がある。
【0023】
サーチュインは有糸分裂の開始を遅らせることが報告されている
サーチュイン1 (SIRT1またはSilent information regulator two ortholog 1の別名でも知られる)は、ストレスに応答して代謝と細胞生存を制御している酵素である。それは細胞の寿命に関連づけられる。SIRT1酵素をコードするsirt1遺伝子は概日遺伝子ではない。Chuaらは、SIRT1が細胞周期を停止させることによって複製老化を促進すると提案している(Chua et al. (2005) Mammalian SIRT1 limits replicative life span in response to chronic genotoxic stress (哺乳動物SIRT1は慢性の遺伝毒性ストレスに応答して複製寿命を制限する). Cell Metabolism 2, 67-76)。
【0024】
US 2009-0082278 (その全内容を参照により本明細書に組み入れる)はさらに、この遺伝子と、それをアップレギュレートすることができる局所皮膚組成物を記載している。段落8〜13には次のように書かれている:
「出願人は最近、老化過程と細胞保護に大きな役割を有する皮膚細胞の機構への新たなタンパク質の関与を発見した。」
「出願人は、SIRTタンパク質、より正確にはSIRT1タンパク質が皮膚細胞で発現されること、また、その発現は皮膚細胞が遭遇するさまざまなストレスに関連していることを実証した。彼らは特に、異なる作用物質を使用するこのタンパク質の発現誘導が細胞の保護を可能にし、また、細胞がストレスおよび内因性老化と戦うのにいっそう役立つことを実証した。」
「SIRTタンパク質はサーチュインファミリーの一部であり、ヒストン脱アセチル化において重要な役割を果たすNAD+依存性核タンパク質である。SIRタンパク質をコードするSIR遺伝子(Silent Information Regulators)は、1979年にS.セレビシエ(S. cerevisiae)で初めて記述された(Rine J and A l., Genetics 1979)。後に、C.エレガンス(C. elegans)でのSIR2Pタンパク質の過剰発現はこの生物の寿命を延ばすことが実証された(Tissenbaum and A l., Nature 2001)。この研究によって、これらのタンパク質は長寿に関係していると仮定することができた。」
「SIRT1タンパク質は最も特性解析されたヒトサーチュインであり、多数の転写調節因子と相互作用する。ヒトSIRT1タンパク質はp53の調節に関与するものとして(Cheng H L and A l. Proc Natl Acad Sci USA. 2003)、最近では、細胞老化のモジュレーターとして(Langley E and A l., EMBO J. 2002)記載されている。その他のヒトSIRTタンパク質も発見されている(SIRT2、SIRT3、SIRT4-7)。ヒトSIRT2タンパク質はほとんど研究されていない;しかし、いくつかの研究によって、有糸分裂活性の制御におけるその役割(Dryden S C and A l. Mol Cell Bio. 2003)ならびにp53タンパク質の調節へのその関与(Vaziri H and A l., Cell. 2001)が実証されている。これまでのところ、デアセチラーゼサーチュインは、細胞死の調節およびその生活環において重要な役割を果たす酵素の一ファミリーと見なされている(Porcu M. and Chiarugi A, Trends Pharmacol Sci., 2005)。」
「本発明[すなわち、US 2009-0082278]は、化粧品的にまたは薬学的に許容される媒体中に、皮膚細胞でのSIRTタンパク質の合成を活性化する可能性がある少なくとも1種の化合物を含む、化粧料または医薬組成物に関する。優先的に、本発明によると、これらの化合物はSIRTタンパク質の特定のクラス、SIRT1タンパク質を活性化するだろう。」
「これまで、皮膚細胞における、SIRTファミリーのタンパク質の合成の誘導物質として機能する化合物の使用は記載されていない。」
【0025】
本明細書は、これまで、概日遺伝子活性化剤と共同してsirt1活性化剤を含む組成物の使用が、US2009-0082278にさえも、記載されたことがない点を強調する。本出願人の知る限りでは、ヒト表皮ケラチノサイトにおけるCLOCKおよびPER1タンパク質のレベル低下に対処する局所組成物であって、1種以上の非概日(non-circadian)有糸分裂遅延物質を含む組成物は知られていない。
【0026】
DNA修復用の局所組成物
細胞修復過程を促進するために皮膚に適用する局所製品は知られている。例えば、そうした製品は、自然の細胞DNA修復の有効性を向上させるためのDNA修復酵素、ケラチノサイト水和を維持するための保水剤成分、皮膚のバリア機能を改善するための保湿成分などを含むことができる。これらの成分はケラチノサイトの自己修復能を改善するかもしれないが、改善の余地は常にあるものである。従来技術とは対照的に、本発明は、損傷DNAが娘細胞に伝わるのを阻止する手段と組み合わせた、皮膚細胞における無傷の概日タンパク質のレベルを復元する手段および概日遺伝子発現の通常のパターンを回復させる手段を提供する。
【発明の概要】
【0027】
発明の目的
本発明の目的は、下記の組成物を適用したとき、加速されたやり方で、皮膚細胞における概日タンパク質の通常のレベルを復元しかつ概日遺伝子発現の通常のパターンを回復させる、局所組成物を提供することである。
【0028】
本発明の目的は、clockおよびper1遺伝子発現をアップレギュレートすることによって、また、皮膚細胞の有糸分裂を遅らせることによって、光損傷および/または酸化的損傷を受けた皮膚を修復する、局所組成物を提供することである。
【0029】
本発明の目的は、損傷を受けた皮膚細胞DNAが増殖する機会を減らす、局所組成物を提供することである。
【0030】
本発明の目的は、環境攻撃、特にUV曝露によって損傷された皮膚細胞DNAが増殖する機会を減らす、局所組成物を提供することである。
【0031】
本発明のさらなる目的は、少なくとも1種のケラチノサイトclockまたはper1遺伝子活性化剤と、少なくとも1種の非概日の有糸分裂遅延物質と、場合により少なくとも1種のDNA修復酵素と、を含む皮膚処置用の組成物を提供することである。
【0032】
概要
上記のすべては、皮膚細胞の概日遺伝子発現をアップレギュレートする少なくとも1種の作用物質と、皮膚細胞の有糸分裂を遅らせる少なくとも1種の非概日作用物質とを含む局所組成物によって達成される。clock遺伝子およびper1遺伝子をアップレギュレートする(または活性化する)一方で、SIRT1のレベルをも増加させる作用物質を含む組成物は、相乗的に、細胞の生存、細胞の寿命を促進し、環境攻撃による細胞損傷を抑制し、DNA損傷の修復を改善し、かつ損傷を受けた皮膚細胞DNAが増殖する機会を相乗的に減らすことが見いだされた。場合により、前記組成物は1種以上のDNA修復酵素を含有する。
【0033】
本発明の好ましい実施形態は、上記の効果を示す局所皮膚組成物である。好ましくは、前記組成物は、1種以上のケラチノサイトclockおよびper1遺伝子活性化剤を、SIRT1または1種以上のsirt1活性化剤と共に、含んでなる。好ましくは、前記組成物は使いやすく、効果があり、化粧品的に許容され、化学的に、熱力学的におよび光に安定であり、局所使用に安全であり、副作用がほとんどまたは全くなく、また、パーソナルケア市場で商業的に実現可能なものである。
【図面の簡単な説明】
【0034】
【図1】UV曝露後72時間にわたる、ヒトケラチノサイトにおけるclock、bmal1およびper1遺伝子発現のレベルを示す。
【図2】ヒトケラチノサイトの生存に及ぼす、sirt1活性化剤であるOrsirtine(商標)とレスベラトロールの効果を示す。
【図3】sirt1活性化剤であるOrsirtine(商標)およびレスベラトロールと組み合わせた、概日遺伝子活性化剤の効果を示す。
【発明を実施するための形態】
【0035】
詳細な説明
本出願人の知る限りでは、通常の概日周期を回復させるための概日遺伝子活性化剤の局所適用と共同した、細胞周期の停止を促進するためのsirt1活性化剤を含む局所組成物の使用は、これまで記載されたことがない。
【0036】
定義
本明細書に記載されるすべてのパーセンテージは、特に断らない限り、重量パーセントである。遺伝子に関連して、「活性化する」および「アップレギュレートする」または語源的に関連のある用語は、遺伝子によってコードされる1種以上のタンパク質の発現を引き出す成分を意味する。
【0037】
用語「時計遺伝子」は、clock、bmal1、period、およびcryptochrome遺伝子を含む、いわゆる「カノニカル」概日遺伝子のいずれかをさすために、文献中で用いられることがある。本明細書中で、「clock」(イタリック体で)は常にCLOCKタンパク質をコードする遺伝子をさす。まとめて、本明細書中では遺伝子clock、bmal1、period、およびcryptochromeを「概日遺伝子」(circadian genes)と呼ぶ。
【0038】
用語「DNA修復酵素」は、DNAの塩基変異原性損傷を修復することができる酵素を意味する。そうした酵素はしばしばそれらが修復するDNA損傷のタイプごとに分類される。例えば、BER (塩基除去修復)酵素、ヌクレオチド除去修復(NER)酵素;ミスマッチ修復(MMR)酵素;DNAヘリカーゼ;DNAポリメラーゼなど。例えば、8-オキソ-7,8-ジヒドロ-2'-デオキシグアノシンなどの変異はOGG1 (8-オキソグアニングリコシラーゼ)によって修復される。T-Tダイマーはヌクレオチド除去修復酵素フォトリアーゼ(Photolyase)によって修復される。6-4光産物はNERによって修復される。06-メチルグアニンは06-アルキルグアニントランスフェラーゼ(AGT)によって修復される。
【0039】
皮膚または皮膚細胞に関して、「修復」とは、ケラチノサイトの生存能力、強度、および寿命が一般的に改善されることを意味する。修復の例としては、損傷したケラチノサイトDNAを修復すること、およびUV光、タバコの煙または他の環境攻撃による細胞水和の損失を回復させることが含まれる。
【0040】
「局所使用に安全」とは、化粧品の安全性を管理するあらゆる地域および地方の規制に従うことを意味する。「化粧品的に許容される」とは、当業者には理解されるように、組成物の外観、感触および香りが消費者の受容性の範囲内であることを意味する。「化学的に安定」、「熱力学的に安定」および「光に安定」とは、製造から少なくとも6ヶ月間(より好ましくは3年間)、組成物が化粧品的に許容される状態にあることを意味する。「パーソナルケア市場で商業的に実現可能」とは、組成物の製造および流通コストがパーソナルケア業界ですでに経験しているコストより高くならないことを意味する。
【0041】
clockおよびperiod1のアップレギュレーション
本発明の組成物は、clockおよび/またはper1ケラチノサイト遺伝子をアップレギュレートする少なくとも1種の作用物質を含有する。これらの作用物質の推奨濃度は、合計で、最終組成物の全重量に対して、約0.000001〜約40%、好ましくは約0.000005〜35%、より好ましくは約0.00001〜25%の範囲である。一般的に、これらの範囲は有効量であると理解される。「有効量」とは、環境攻撃のもとでヒト皮膚に適用される局所組成物中のこれらの作用物質の濃度がケラチノサイトの生存率を5%以上改善するのに十分であることを意味する。適当なclockまたはper1活性化剤は、植物エキス、ポリペプチド、ペプチド、アミノ酸などの形態で存在し得る。
【0042】
特に好ましいclockおよび/またはper1遺伝子活性化剤は、式(I)のペプチドを含む:
R1-(AA)n-X1-S-T-P-X2-(AA)p-R2
式中、(AA)n-X1-S-T-P-X2-(AA)pは(配列番号1)であり、そして
X1は、トレオニンまたはセリンを表すか、ゼロに等しく、
X2は、イソロイシンまたはロイシンまたはプロリンまたはバリンまたはアラニンまたはグリシンを表すか、ゼロに等しく、
AAは、任意のアミノ酸またはその誘導体を表し、nおよびpは0〜4の整数であり(0と4を含める)、
R1は、N末端アミノ酸の1級アミン官能基を表し、そのアミン官能基は遊離であるか、アセチル基、ベンゾイル基、トシル基、またはベンジルオキシカルボニル基から選択できる保護基で置換されており、
R2は、C末端アミノ酸のカルボキシル官能基のヒドロキシル基を表し、そのヒドロキシル基はC1-C20アルキル鎖またはNH2、NHY、もしくはNYY基(ここで、YはC1-C4アルキル鎖を表す)から選択できる保護基で置換されており、
そして、一般式(I)の配列は約3〜13個のアミノ酸残基から構成される。
【0043】
一般式(I)の配列は、アミノ酸X1およびX2の、他の化学的に等価なアミノ酸による置換を含むことができ、ここで、そのアミノ酸は以下のものである:アラニン(A)、アルギニン(R)、アスパラギン(N)、アスパラギン酸(D)、システイン(C)、グルタミン酸(E)、グルタミン(Q)、グリシン(G)、ヒスチジン(H)、イソロイシン(I)、ロイシン(L)、リシン(K)、メチオニン(M)、フェニルアラニン(F)、プロリン(P)、セリン(S)、トレオニン(T)、トリプトファン(W)、チロシン(Y)およびバリン(V)。
【0044】
式(I)のより好ましい配列は、以下のようなペプチドである:
(配列番号2) Y-V-S-T-P-Y-N-NH2
Tyr-Val-Ser-Thr-Pro-Tyr-Asn-NH2
(配列番号3) NH2-V-S-T-P-E-NH2
NH2-Val-Ser-Thr-Pro-Glu-NH2
S-T-P-NH2
Ser-Thr-Pro-NH2
(配列番号4) NH2-L-H-S-T-P-P-NH2
NH2-Leu-His-Ser-Thr-Pro-Pro-NH2
(配列番号5) CH3NH-R-H-S-T-P-E-NH2
CH3-NH-Arg-His-Ser-Thr-Pro-Glu-NH2
(配列番号6) CH3NH-H-S-T-P-E-CH3NH
CH3-NH-His-Ser-Thr-Pro-Glu-CH3-NH
【0045】
より好ましいものは、S-T-P-NH2ペプチド、配列番号4、またはそれらの混合物である。最も好ましいものは、ISP-Vinscience社により製造されたChronolux(登録商標)という商標名のペプチド(Tripeptide-32のINCI名をもつ)である。
【0046】
関連出願US12/367,705の図1、2および3、ならびにこれらの図面を説明する本文には、少なくとも1種のDNA修復酵素と組み合わせた場合に特に、UV誘発ストレスに対するケラチノサイトの生存率を改善するChronolux(登録商標)の能力が示されている。
【0047】
clockおよびper1遺伝子活性化剤を同時に適用することが有益な結果を生み出すであろうということは、直ちには明白でない。結局のところ、通常の概日リズムでは、CLOCKおよびPeriod1タンパク質の細胞内濃度は位相を異にする。それにもかかわらず、有益な結果が達成される。環境攻撃を受けている皮膚細胞はCLOCKおよびPERIOD1タンパク質のレベルが激減するので、両タンパク質を可能な限り速やかにアップレギュレートすることによって効果が得られると考えられる。
【0048】
サーチュイン1のアップレギュレーション
本発明者らは、予期せざることに、clockおよびper1遺伝子活性化剤の適用により得られる有益な結果が、ケラチノサイトsirt1活性化剤と組み合わせたときに改善され、時には大幅に改善される、ことを見いだした。SIRT1は細胞周期の停止を誘導する傾向がある。概日機構の複雑さおよび細胞周期とのその調節相互作用を考えると、概日タンパク質の通常のレベルを復元すると同時に、細胞周期の停止を誘導することが有益であろうとは、従来技術から予想されなかったことである。
【0049】
いずれの理論にも拘束されることを望まないが、PER1は、24時間周期の監視を介すること以外に、細胞周期に直接的な効果を及ぼすことが理解されるだろう。例えば、PER1は、概日周期のコア成分としてのその役割のほかに、細胞周期の停止につながるATMキナーゼ経路を活性化できると報告されている。ATM(血管拡張性失調症変異型)キナーゼは、DNA二本鎖切断に応答して動員される核タンパク質キナーゼである。ATMキナーゼは、細胞周期の停止および有糸分裂への進入遅延に関与する、細胞周期チェックポイント調節因子CHK1およびCHK2をリン酸化する。PER1が何らかの環境ストレスの結果として過小発現されると、細胞周期の停止が起こらなかったり、遅れたりすることがある。したがって、有糸分裂または細胞質分裂の前に、損傷DNAの修復を行うのに十分な時間がない可能性がある。それと同時に、PER1の発現低下はアポトーシスの減少とも関連している。こうして、死滅するはずの損傷細胞が生き残って、分裂することがある。したがって、環境ストレスがPER1のレベルの異常な減少(細胞周期を停止させることができず、かつ損傷DNAの伝播につながるアポトーシスの減少をもたらす)をまねくと考えると、per1活性化がこの問題を解決しうると期待するかもしれない。それにもかかわらず、本発明者らは、sirt1遺伝子活性化剤をclockおよびper1遺伝子活性化剤と組み合わせて用いるとき、ケラチノサイトの生存率が大幅に改善されることを観察した。いずれの理論にも拘束されることを望まないが、この観察は、損傷DNAが娘細胞に伝えられる前に修復を行うのに十分な速度で、per1単独での活性化がPER1のレベルを復元できない、ことを暗に示している。
【0050】
「SIRT1活性化剤」とは、SIRT1タンパク質の内因性生産をサポートする可能性がある任意の化合物、特にDNAまたはRNAなどの前駆体の正の制御に関与する分子、を意味する。皮膚細胞におけるSIRT1タンパク質の合成を活性化する可能性があるこうした化合物の中で、ポリフェノールなど、さまざまな分子が記載されている。より具体的には、trans-スチルベンの誘導体(例えば、レスベラトロール、ピセアタンノール)、カルコン類の誘導体(例えば、イソリキリチゲニン、ブテイン)、およびフラボン類の誘導体(例えば、フィステイン(fistein)、ルテオリン、クェルセチン)が挙げられる。少なくとも1種のDNA修復酵素と組み合わせた、レスベラトロールまたはレスベラトロール誘導体の有効性は、関連出願US 11/837,658に示されている。しかし、特定のペプチドは、皮膚のペプチドへのそれらの固有の構造類似性のため、好ましいsirt1活性化剤である。よりいっそう好ましいものは、1種以上のペプチド性活性化剤とレスベラトロールの相乗的組合せである(これについては、以下参照)。
【0051】
ペプチド性sirt1活性化剤
ペプチドは、皮膚のペプチドへのそれらの固有の構造類似性のため、好ましいsirt1活性化剤である。ペプチド性の化合物の中で、タンパク質断片、ペプチドおよびポリペプチドの断片、ペプチド、ならびにペプチド結合で一緒に連結された2個以上のアミノ酸の全ての配列を挙げることができる。本発明の好ましい実施形態において、ペプチド断片は大きさが3〜50アミノ酸、より好ましくは3〜10アミノ酸の範囲である。これらのペプチド断片の全ては生物学的活性をもつものである。好ましいペプチドは以下のものである:
(配列番号7) (AA)n-G-L-Y-D-N-L-E-(AA)n
(AA)n-Gly-Leu-Tyr-Asp-Asn-Leu-Glu-(AA)n
式中、(AA)は任意の特定のアミノ酸またはその誘導体であり、nは0〜3の整数である(0と3を含める)。特に好ましいペプチドは以下のものである:
(配列番号8) G-L-Y-D-N-L-E
Gly-Leu-Tyr-Asp-Asn-Leu-Glu
このペプチドは、ISP Vincience社からOrsirtine(商標)GL (INCI名:Water (and) Glycerin (and) Oryza Sativa (Rice) Extract)として入手可能である。本発明の組成物において、ペプチド性SIRT1活性化剤は、最終組成物の全重量に対して、約0.000001%〜20%、好ましくは約0.0001〜5%の量で存在する。
【0052】
レスベラトロールおよびその誘導体
レスベラトロールは、別名を3,5,4'-トリヒドロキシスチルベンともいい、赤ブドウ、ラズベリー、ブルーベリー、および他の特定の植物ベリー類または抽出物中に存在するポリヒドロキシ置換スチルベン化合物であって、以下の一般式を有する:
【化1】

【0053】
レスベラトロールは効果的な抗酸化物質であることがわかっており、また、強力な抗増殖および抗炎症作用を示す。最近、レスベラトロールは、酵母、回虫、ミバエ、短命の魚、およびマウスなど、さまざまな生物においてカロリー制限(CR)を模倣し、こうした生物の老化プロセスを遅らせ、かつそれらの寿命を大幅に引き延ばすことが報告された。どのような特定の理論にも拘束されることを望まないが、本発明者らは、レスベラトロールが細胞増殖を低下させ、かつアポトーシス過程を減速させ、それによって細胞でのDNA損傷の修復のためのより多くの時間を可能にする、と考えている。レスベラトロールは、DNA修復酵素と組み合わせたとき、細胞の自然なDNA修復能をブーストするかまたは他の方法で高める上で相乗効果をもたらすと予想される。
【0054】
しかし、レスベラトロールは特定の化粧品製剤中で潜在的に不安定なことがある。具体的には、レスベラトロールは水性ベースの製剤中で加水分解を受けやすく、また、そうした製剤を変色させる可能性がある。水性ベースの製剤中でのレスベラトロールの不安定性に対処する1つの方法は、化粧品製剤中でより安定なレスベラトロール誘導体を形成するために、3、5および4'位のヒドロキシ基を他の官能基で置換することによってレスベラトロールを修飾することである。そのような誘導体はレスベラトロールより好適である。無機酸、有機カルボン酸、モノ-、ジ-もしくはポリサッカライド、または他の官能基のレスベラトロール誘導体は水性ベースの製剤中でより安定であることが見いだされた。置換基はレスベラトロールのフェノール基を保護しかつ安定化するように機能し、水性ベースの化粧品製剤中で使用するのにレスベラトロール誘導体をより適したものにする。置換基はまた、皮膚への適用時にその化合物から、好ましくは皮膚表面上の酵素および他の成分によって、容易に加水分解されて、皮膚にレスベラトロールの活性形態を放出し得る。本発明のレスベラトロール誘導体は以下の一般式を有する:
【化2】

【0055】
式中、X、YおよびZは水素または保護基のいずれかであるが、X、YおよびZの少なくとも1つは保護基であることを条件とする。本発明の化粧料または局所組成物中で使用するのに適した代表的なレスベラトロール誘導体については、以下でより詳細に説明する。
【0056】
A. 無機または有機酸のレスベラトロールエステル
無機酸のレスベラトロールエステル[上記式中、X、YおよびZの1つ以上がホスフェート、ニトレート、スルホネートおよびカーボネートなどの無機酸の官能基である]は本発明で使用することができる。以下は、本発明の実施に特に適している代表的な無機酸エステルのリストである:
3-ホスフェート-5,4'-ジヒドロキシスチルベン
5-ホスフェート-3,4'-ジヒドロキシスチルベン
4'-ホスフェート-3,5-ジヒドロキシスチルベン
3,5-ジホスフェート-4'-ヒドロキシスチルベン
3,4'-ジホスフェート-5-ヒドロキシスチルベン
4',5-ジホスフェート-3-ヒドロキシスチルベン
3,5,4'-トリホスフェートスチルベン
3-ニトレート-5,4'-ジヒドロキシスチルベン
5-ニトレート-3,4'-ジヒドロキシスチルベン
4'-ニトレート-3,5-ジヒドロキシスチルベン
3,5-ジニトレート-4'-ヒドロキシスチルベン
3,4'-ジニトレート-5-ヒドロキシスチルベン
4',5-ジニトレート-3-ヒドロキシスチルベン
3,5,4'-トリニトレートスチルベン
3-スルホネート-5,4'-ジヒドロキシスチルベン
5-スルホネート-3,4'-ジヒドロキシスチルベン
4'-スルホネート-3,5-ジヒドロキシスチルベン
3,5-ジスルホネート-4'-ヒドロキシスチルベン
3,4'-ジスルホネート-5-ヒドロキシスチルベン
4',5-ジスルホネート-3-ヒドロキシスチルベン
3,5,4'-トリスルホネートスチルベン
3-カーボネート-5,4'-ジヒドロキシスチルベン
5-カーボネート-3,4'-ジヒドロキシスチルベン
4'-カーボネート-3,5-ジヒドロキシスチルベン
3,5-ジカーボネート-4'-ヒドロキシスチルベン
3,4'-ジカーボネート-5-ヒドロキシスチルベン
4',5-ジカーボネート-3-ヒドロキシスチルベン
3,5,4'-トリカーボネートスチルベン。
【0057】
上に挙げたレスベラトロールエステルの薬学的に許容される塩も本発明の化粧料組成物中で使用することができる。そうした塩はNa、K、Mg、Ca、Fe、およびNH4からなる群より選択される1つ以上の1価または2価陽イオンを含む。塩は、水酸化ナトリウム、水酸化カリウムなどの対応する塩基を、レスベラトロールエステルを含有する溶液に添加することによって形成される。
【0058】
レスベラトロールの無機酸エステルは、フェノールまたはポリフェノールのヒドロキシル基をホスフェート、スルホネートまたはカーボネート官能基で置換する周知の化学的方法によって容易に形成することができる。例えば、米国特許第4003966号は、フェノール類を選択的にリン酸化してそのリン酸エステルを形成するワンステップ法を記載しており、あらゆる目的のためにその全内容を参照により本明細書に組み入れる。
【0059】
本発明の実施に特に好ましいレスベラトロール誘導体は、以下の式を有する3,4',5-トリホスフェートスチルベン(別名をレスベラトロール3リン酸エステルともいう)である:
【化3】

【0060】
レスベラトロール3リン酸を含めて、レスベラトロールのリン酸エステルは、国際特許出願公開公報WO 2006/029484A1に開示されており、その全内容を参照により本明細書に組み入れる。レスベラトロール3リン酸はWO 2006/029484A1の実施例2に記載の方法により合成することができる。より具体的には、100mlのアセトニトリルに溶解したレスベラトロール(3,4,5-トリヒドロキシスチルベン)(25mmols, 5.7g)とジメチルアミノピリジン(7.5mmols, 0.93g)の溶液を窒素下に−10℃まで冷却する。10分後、四塩化炭素(375mmol, 36.2ml)とDIEA (159mmol, 27.7ml)を加え、この混合物を撹拌しながら30分間維持する。ジベンジルホスフェート(113mmols, 25.0ml)を加え、この混合物を室温でさらに12時間撹拌する。反応の経過をTLC(シリカF254、溶離剤:酢酸エチル/n-ヘキサン80/20 v/v)でモニタリングする。1リットルの0.5M KH2PO4を加え、その後この混合物を酢酸エチルで抽出する。得られた生成物のトリ(ジベンジルホスフェート)レスベラトロールをシリカゲルでろ過し、最初に酢酸エチル/n-ヘキサン(80/20 v/v)の混合溶媒で洗浄して、残存する未反応のレスベラトロールを除き、次にメタノールで洗浄して精製すると、黄色のオイルが得られる。
【0061】
0℃の無水DCM 200mL中のトリ(ジベンジルホスフェート)レスベラトロール(12.5mmol)に、ブロモメチルシラン(79mmols, 10.4mL)を添加する。2時間後、300mLのH2Oを加え、その反応混合物を1時間撹拌する。水相を酢酸エチルで再度洗浄し、その後凍結乾燥すると、オレンジ色のオイルが得られる。
【0062】
400mLのエタノール中に可溶化した、上で得られた生成物に、CH3ONa (37mmol; 2.03g)を加えて、その反応を室温で12時間撹拌する。エタノールをrotavaporエバポレータで蒸発させ、残留物をH2O中に可溶化する。水相を酢酸エチルで洗浄して凍結乾燥させる。得られた白色固体の質量スペクトルは、レスベラトロール3リン酸(PM=468.1)の存在を示し、レスベラトロールに対する総収率>90%を有する。
【0063】
必要ならば、レスベラトロール3リン酸を水酸化ナトリウム、水酸化カリウムなどの無機または有機塩基で中和してもよい。特に好ましいのは、レスベラトロール3リン酸を水酸化ナトリウムで中和してレスベラトロール3リン酸3ナトリウムを形成する場合である。レスベラトロール3リン酸はまた、レスベラトロール3リン酸3ナトリウム(trisodium resveratrol triphosphate)のCTFA名を有し、中和された形で味の素社から購入することができる。
【0064】
B. レスベラトロールのカルボン酸エステル
本発明で使用できるレスベラトロール誘導体の別のグループは、レスベラトロールと脂肪族または芳香族カルボン酸とのエステル[上記式中、X、YおよびZの1つ以上が-C(O)-R1基であり、ここでR1は、直鎖、分岐鎖、飽和もしくは不飽和、または環状のC1-C40アルキル、置換C1-C40アルキル、C1-C40アルケニル、置換C1-C40アルケニル、C1-C40アルキニル、置換C1-C40アルキニル、アリール、C1-C40アリール、およびC1-C40置換アリールからなる群より選択される]である。好ましい一実施形態では、R1基が直鎖または分岐鎖の脂肪族の(fatty)、つまりC6-30の、飽和または不飽和アルキル基である。置換基はC1-40直鎖または分岐鎖、飽和または不飽和アルキル、ハロゲン(例えばフルオロ)、水素、アルコキシ、ヒドロキシルなどから選択される。
【0065】
レスベラトロールのエステルを形成するために使用できるカルボン酸の例としては、限定するものではないが、以下のものが挙げられる:飽和モノカルボン酸、例えば、酢酸、プロピオン酸、酪酸(C4)、バレリアン酸、ヘキサン酸、カプリル酸(C8)、ラウリン酸、ステアリン酸(C18)、イソステアリン酸(分岐C18)、リノール酸、リノレン酸、ミリスチン酸(C14)、アラキジン酸(C20)、アラキドン酸、エルカ酸、ベヘン酸(C22)、ラウリン酸(C12)、カプリン酸(C10)、カプロン酸(C6)、およびパルミチン酸(C16); 不飽和モノカルボン酸、例えば、アクリル酸、メタクリル酸、ソルビン酸、オレイン酸、リノール酸、リノレン酸、ドコサヘキサエン酸、およびエイコサペンタエン酸; アミノ酸、例えば、アルギニン、グルタミン、およびチロシン; ケト酸、例えば、ピルビン酸、およびアセト酢酸; 芳香族カルボン酸、例えば、アスコルビン酸、安息香酸、サリチル酸、およびフェルラ酸; ジ-およびトリ-カルボン酸、例えば、シュウ酸、マロン酸、リンゴ酸、コハク酸、およびグルタル酸。記号「C」の後の数字は、アルキル鎖中の炭素原子の数を示す。
【0066】
本発明の実施に特に適している代表的なレスベラトロールのカルボン酸エステルのリストは以下のとおりである:
3-アセテート-5,4'-ジヒドロキシスチルベン
5-アセテート-3,4'-ジヒドロキシスチルベン
4'-アセテート-3,5-ジヒドロキシスチルベン
3,5-ジアセテート-4'-ヒドロキシスチルベン
3,4'-ジアセテート-5-ヒドロキシスチルベン
4',5-ジアセテート-3-ヒドロキシスチルベン
3,5,4'-トリアセテートスチルベン
3-プロピオネート-5,4'-ジヒドロキシスチルベン
5-プロピオネート-3,4'-ジヒドロキシスチルベン
4'-プロピオネート-3,5-ジヒドロキシスチルベン
3,5-ジプロピオネート-4'-ヒドロキシスチルベン
3,4'-ジプロピオネート-5-ヒドロキシスチルベン
4',5-ジプロピオネート-3-ヒドロキシスチルベン
3,5,4'-トリプロピオネートスチルベン
3-ブチレート-5,4'-ジヒドロキシスチルベン
5-ブチレート-3,4'-ジヒドロキシスチルベン
4'-ブチレート-3,5-ジヒドロキシスチルベン
3,5-ジブチレート-4'-ヒドロキシスチルベン
3,4'-ジブチレート-5-ヒドロキシスチルベン
4',5-ジブチレート-3-ヒドロキシスチルベン
3,5,4'-トリブチレートスチルベン
3-バレレート-5,4'-ジヒドロキシスチルベン
5-バレレート-3,4'-ジヒドロキシスチルベン
4'-バレレート-3,5-ジヒドロキシスチルベン
3,5-ジバレレート-4'-ヒドロキシスチルベン
3,4'-ジバレレート-5-ヒドロキシスチルベン
4',5-ジバレレート-3-ヒドロキシスチルベン
3,5,4'-トリバレレートスチルベン
3-ヘキサノエート-5,4'-ジヒドロキシスチルベン
5-ヘキサノエート-3,4'-ジヒドロキシスチルベン
4'-ヘキサノエート-3,5-ジヒドロキシスチルベン
3,5-ジヘキサノエート-4'-ヒドロキシスチルベン
3,4'-ジヘキサノエート-5-ヒドロキシスチルベン
4',5-ジヘキサノエート-3-ヒドロキシスチルベン
3,5,4'-トリヘキサノエートスチルベン
3-カプリレート-5,4'-ジヒドロキシスチルベン
5-カプリレート-3,4'-ジヒドロキシスチルベン
4'-カプリレート-3,5-ジヒドロキシスチルベン
3,5-ジカプリレート-4'-ヒドロキシスチルベン
3,4'-ジカプリレート-5-ヒドロキシスチルベン
4',5-ジカプリレート-3-ヒドロキシスチルベン
3,5,4'-トリカプリレートスチルベン
3-ラウレート-5,4'-ジヒドロキシスチルベン
5-ラウレート-3,4'-ジヒドロキシスチルベン
4'-ラウレート-3,5-ジヒドロキシスチルベン
3,5-ジラウレート-4'-ヒドロキシスチルベン
3,4'-ジラウレート-5-ヒドロキシスチルベン
4',5-ジラウレート-3-ヒドロキシスチルベン
3,5,4'-トリラウレートスチルベン
3-ステアレート-5,4'-ジヒドロキシスチルベン
5-ステアレート-3,4'-ジヒドロキシスチルベン
4'-ステアレート-3,5-ジヒドロキシスチルベン
3,5-ジステアレート-4'-ヒドロキシスチルベン
3,4'-ジステアレート-5-ヒドロキシスチルベン
4',5-ジステアレート-3-ヒドロキシスチルベン
3,5,4'-トリステアレートスチルベン
3-パルミテート-5,4'-ジヒドロキシスチルベン
5-パルミテート-3,4'-ジヒドロキシスチルベン
4'-パルミテート-3,5-ジヒドロキシスチルベン
3,5-ジパルミテート-4'-ヒドロキシスチルベン
3,4'-ジパルミテート-5-ヒドロキシスチルベン
4',5-ジパルミテート-3-ヒドロキシスチルベン
3,5,4'-トリパルミテートスチルベン
3-アクリレート-5,4'-ジヒドロキシスチルベン
5-アクリレート-3,4'-ジヒドロキシスチルベン
4'-アクリレート-3,5-ジヒドロキシスチルベン
3,5-ジアクリレート-4'-ヒドロキシスチルベン
3,4'-ジアクリレート-5-ヒドロキシスチルベン
4',5-ジアクリレート-3-ヒドロキシスチルベン
3,5,4'-トリアクリレートスチルベン
3-メタクリレート-5,4'-ジヒドロキシスチルベン
5-メタクリレート-3,4'-ジヒドロキシスチルベン
4'-メタクリレート-3,5-ジヒドロキシスチルベン
3,5-ジメタクリレート-4'-ヒドロキシスチルベン
3,4'-ジメタクリレート-5-ヒドロキシスチルベン
4',5-ジメタクリレート-3-ヒドロキシスチルベン
3,5,4'-トリメタクリレートスチルベン
3-ソルベート-5,4'-ジヒドロキシスチルベン
5-ソルベート-3,4'-ジヒドロキシスチルベン
4'-ソルベート-3,5-ジヒドロキシスチルベン
3,5-ジソルベート-4'-ヒドロキシスチルベン
3,4'-ジソルベート-5-ヒドロキシスチルベン
4',5-ジソルベート-3-ヒドロキシスチルベン
3,5,4'-トリソルベートスチルベン
3-オレエート-5,4'-ジヒドロキシスチルベン
5-オレエート-3,4'-ジヒドロキシスチルベン
4'-オレエート-3,5-ジヒドロキシスチルベン
3,5-ジオレエート-4'-ヒドロキシスチルベン
3,4'-ジオレエート-5-ヒドロキシスチルベン
4',5-ジオレエート-3-ヒドロキシスチルベン
3,5,4'-トリオレエートスチルベン
3-リノレート-5,4'-ジヒドロキシスチルベン
5-リノレート-3,4'-ジヒドロキシスチルベン
4'-リノレート-3,5-ジヒドロキシスチルベン
3,5-ジリノレート-4'-ヒドロキシスチルベン
3,4'-ジリノレート-5-ヒドロキシスチルベン
4',5-ジリノレート-3-ヒドロキシスチルベン
3,5,4'-トリリノレートスチルベン
3-リノレネート-5,4'-ジヒドロキシスチルベン
5-リノレネート-3,4'-ジヒドロキシスチルベン
4'-リノレネート-3,5-ジヒドロキシスチルベン
3,5-ジリノレネート-4'-ヒドロキシスチルベン
3,4'-ジリノレネート-5-ヒドロキシスチルベン
4',5-ジリノレネート-3-ヒドロキシスチルベン
3,5,4'-トリリノレネートスチルベン
3-ドコサヘキサノエート-5,4'-ジヒドロキシスチルベン
5-ドコサヘキサノエート-3,4'-ジヒドロキシスチルベン
4'-ドコサヘキサノエート-3,5-ジヒドロキシスチルベン
3,5-ジドコサヘキサノエート-4'-ヒドロキシスチルベン
3,4'-ジドコサヘキサノエート-5-ヒドロキシスチルベン
4',5-ジドコサヘキサノエート-3-ヒドロキシスチルベン
3,5,4'-トリドコサヘキサノエートスチルベン
3-エイコサペンタエノイック-5,4'-ジヒドロキシスチルベン
5-エイコサペンタエノイック-3,4'-ジヒドロキシスチルベン
4'-エイコサペンタエノイック-3,5-ジヒドロキシスチルベン
3,5-ジエイコサペンタエノイック-4'-ヒドロキシスチルベン
3,4'-ジエイコサペンタエノイック-5-ヒドロキシスチルベン
4',5-ジエイコサペンタエノイック-3-ヒドロキシスチルベン
3,5,4'-トリエイコサペンタエノイックスチルベン
3-アルギネート-5,4'-ジヒドロキシスチルベン
5-アルギネート-3,4'-ジヒドロキシスチルベン
4'-アルギネート-3,5-ジヒドロキシスチルベン
3,5-ジアルギネート-4'-ヒドロキシスチルベン
3,4'-ジアルギネート-5-ヒドロキシスチルベン
4',5-ジアルギネート-3-ヒドロキシスチルベン
3,5,4'-トリアルギネートスチルベン
3-グルタメート-5,4'-ジヒドロキシスチルベン
5-グルタメート-3,4'-ジヒドロキシスチルベン
4'-グルタメート-3,5-ジヒドロキシスチルベン
3,5-ジグルタメート-4'-ヒドロキシスチルベン
3,4'-ジグルタメート-5-ヒドロキシスチルベン
4',5-ジグルタメート-3-ヒドロキシスチルベン
3,5,4'-トリグルタメートスチルベン
3-チロセート-5,4'-ジヒドロキシスチルベン
5-チロセート-3,4'-ジヒドロキシスチルベン
4'-チロセート-3,5-ジヒドロキシスチルベン
3,5-ジチロセート-4'-ヒドロキシスチルベン
3,4'-ジチロセート-5-ヒドロキシスチルベン
4',5-ジチロセート-3-ヒドロキシスチルベン
3,5,4'-トリチロセートスチルベン
3-ピルベート-5,4'-ジヒドロキシスチルベン
5-ピルベート-3,4'-ジヒドロキシスチルベン
4'-ピルベート-3,5-ジヒドロキシスチルベン
3,5-ジピルベート-4'-ヒドロキシスチルベン
3,4'-ジピルベート-5-ヒドロキシスチルベン
4',5-ジピルベート-3-ヒドロキシスチルベン
3,5,4'-トリピルベートスチルベン
3-アセトアセテート-5,4'-ジヒドロキシスチルベン
5-アセトアセテート-3,4'-ジヒドロキシスチルベン
4'-アセトアセテート-3,5-ジヒドロキシスチルベン
3,5-ジアセトアセテート-4'-ヒドロキシスチルベン
3,4'-ジアセトアセテート-5-ヒドロキシスチルベン
4',5-ジアセトアセテート-3-ヒドロキシスチルベン
3,5,4'-トリアセトアセテートスチルベン
3-アスコルベート-5,4'-ジヒドロキシスチルベン
5-アスコルベート-3,4'-ジヒドロキシスチルベン
4'-アスコルベート-3,5-ジヒドロキシスチルベン
3,5-ジアスコルベート-4'-ヒドロキシスチルベン
3,4'-ジアスコルベート-5-ヒドロキシスチルベン
4',5-ジアスコルベート-3-ヒドロキシスチルベン
3,5,4'-トリアスコルベートスチルベン
3-ベンゾエート-5,4'-ジヒドロキシスチルベン
5-ベンゾエート-3,4'-ジヒドロキシスチルベン
4'-ベンゾエート-3,5-ジヒドロキシスチルベン
3,5-ジベンゾエート-4'-ヒドロキシスチルベン
3,4'-ジベンゾエート-5-ヒドロキシスチルベン
4',5-ジベンゾエート-3-ヒドロキシスチルベン
3,5,4'-トリベンゾエートスチルベン
3-サリチレート-5,4'-ジヒドロキシスチルベン
5-サリチレート-3,4'-ジヒドロキシスチルベン
4'-サリチレート-3,5-ジヒドロキシスチルベン
3,5-ジサリチレート-4'-ヒドロキシスチルベン
3,4'-ジサリチレート-5-ヒドロキシスチルベン
4',5-ジサリチレート-3-ヒドロキシスチルベン
3,5,4'-トリサリチレートスチルベン
3-フェルレート-5,4'-ジヒドロキシスチルベン
5-フェルレート-3,4'-ジヒドロキシスチルベン
4'-フェルレート-3,5-ジヒドロキシスチルベン
3,5-ジフェルレート-4'-ヒドロキシスチルベン
3,4'-ジフェルレート-5-ヒドロキシスチルベン
4',5-ジフェルレート-3-ヒドロキシスチルベン
3,5,4'-トリフェルレートスチルベン
3-オキサレート-5,4'-ジヒドロキシスチルベン
5-オキサレート-3,4'-ジヒドロキシスチルベン
4'-オキサレート-3,5-ジヒドロキシスチルベン
3,5-ジオキサレート-4'-ヒドロキシスチルベン
3,4'-ジオキサレート-5-ヒドロキシスチルベン
4',5-ジオキサレート-3-ヒドロキシスチルベン
3,5,4'-トリオキサレートスチルベン
3-マロネート-5,4'-ジヒドロキシスチルベン
5-マロネート-3,4'-ジヒドロキシスチルベン
4'-マロネート-3,5-ジヒドロキシスチルベン
3,5-ジマロネート-4'-ヒドロキシスチルベン
3,4'-ジマロネート-5-ヒドロキシスチルベン
4',5-ジマロネート-3-ヒドロキシスチルベン
3,5,4'-トリマロネートスチルベン
3-マレート-5,4'-ジヒドロキシスチルベン
5-マレート-3,4'-ジヒドロキシスチルベン
4'-マレート-3,5-ジヒドロキシスチルベン
3,5-ジマレート-4'-ヒドロキシスチルベン
3,4'-ジマレート-5-ヒドロキシスチルベン
4',5-ジマレート-3-ヒドロキシスチルベン
3,5,4'-トリマレートスチルベン
3-スクシネート-5,4'-ジヒドロキシスチルベン
5-スクシネート-3,4'-ジヒドロキシスチルベン
4'-スクシネート-3,5-ジヒドロキシスチルベン
3,5-ジスクシネート-4'-ヒドロキシスチルベン
3,4'-ジスクシネート-5-ヒドロキシスチルベン
4',5-ジスクシネート-3-ヒドロキシスチルベン
3,5,4'-トリスクシネートスチルベン
3-グルタレート-5,4'-ジヒドロキシスチルベン
5-グルタレート-3,4'-ジヒドロキシスチルベン
4'-グルタレート-3,5-ジヒドロキシスチルベン
3,5-ジグルタレート-4'-ヒドロキシスチルベン
3,4'-ジグルタレート-5-ヒドロキシスチルベン
4',5-ジグルタレート-3-ヒドロキシスチルベン
3,5,4'-トリグルタレートスチルベン
3-グルタレート-5,4'-ジヒドロキシスチルベン
5-グルタレート-3,4'-ジヒドロキシスチルベン
4'-グルタレート-3,5-ジヒドロキシスチルベン
3,5-ジグルタレート-4'-ヒドロキシスチルベン
3,4'-ジグルタレート-5-ヒドロキシスチルベン
4',5-ジグルタレート-3-ヒドロキシスチルベン
3,5,4'-トリグルタレートスチルベン。
【0067】
特に好ましいレスベラトロールのカルボン酸エステルのグループは、レスベラトロールの飽和または不飽和脂肪酸エステル、例えば、レスベラトロール酪酸エステル、レスベラトロールバレリアン酸エステル、レスベラトロールヘキサン酸エステル、レスベラトロールソルビン酸エステル、レスベラトロールラウリン酸エステル、レスベラトロールステアリン酸エステル、レスベラトロールパルミチン酸エステル、レスベラトロールオレイン酸エステル、レスベラトロールリノール酸エステル、レスベラトロールリノレン酸エステル、レスベラトロールエイコサペンタエン酸エステル、およびレスベラトロールドコサヘキサエン酸エステルである。このようなレスベラトロールの脂肪酸エステルは、米国特許第6,572,882号(あらゆる目的のために、その全内容を参照により本明細書に組み入れる)に記載されるように、アルカリ性水性媒体中でSchotten-Baumann反応に従ってレスベラトロールを酸誘導体でエステル化することにより、容易に形成することができる。
【0068】
特に好ましいレスベラトロールのカルボン酸エステルのもう一つのグループは、レスベラトロールの芳香族カルボン酸エステル、例えばレスベラトロールフェルラ酸エステルであり、このエステルは水性媒体中でレスベラトロールをフェルラ酸と反応させることによって形成される。
【0069】
C. レスベラトロールのエーテル誘導体
本発明で使用できるレスベラトロール誘導体のさらに別のグループは、レスベラトロールのエーテル[上記式中、X、YおよびZの1つ以上が-R2であり、ここでR2は、直鎖、分岐鎖または環状のC1-C40アルキル、置換C1-C40アルキル、C1-C40アルケニル、置換C1-C40アルケニル、C1-C40アルキニル、置換C1-C40アルキニル、C1-C40アリール、置換C1-C40アリール、ならびにモノ-、ジ-、オリゴ-およびポリサッカライドからなる群より選択される]である。本発明の実施に特に適している代表的なレスベラトロールエーテルのリストは以下のとおりである:
3-メトキシ-5,4'-ジヒドロキシスチルベン
5-メトキシ-3,4'-ジヒドロキシスチルベン
4'-メトキシ-3,5-ジヒドロキシスチルベン
3,5-ジメトキシ-4'-ヒドロキシスチルベン
3,4'-ジメトキシ-5-ヒドロキシスチルベン
4',5-ジメトキシ-3-ヒドロキシスチルベン
3,5,4'-トリメトキシスチルベン
3-エトキシ-5,4'-ジヒドロキシスチルベン
5-エトキシ-3,4'-ジヒドロキシスチルベン
4'-エトキシ-3,5-ジヒドロキシスチルベン
3,5-ジエトキシ-4'-ヒドロキシスチルベン
3,4'-ジエトキシ-5-ヒドロキシスチルベン
4',5-ジエトキシ-3-ヒドロキシスチルベン
3,5,4'-トリエトキシスチルベン
3-プロピルオキシ-5,4'-ジヒドロキシスチルベン
5-プロピルオキシ-3,4'-ジヒドロキシスチルベン
4'-プロピルオキシ-3,5-ジヒドロキシスチルベン
3,5-ジプロピルオキシ-4'-ヒドロキシスチルベン
3,4'-ジプロピルオキシ-5-ヒドロキシスチルベン
4',5-ジプロピルオキシ-3-ヒドロキシスチルベン
3,5,4'-トリプロピルオキシスチルベン
3-フェニルオキシ-5,4'-ジヒドロキシスチルベン
5-フェニルオキシ-3,4'-ジヒドロキシスチルベン
4'-フェニルオキシ-3,5-ジヒドロキシスチルベン
3,5-ジフェニルオキシ-4'-ヒドロキシスチルベン
3,4'-ジフェニルオキシ-5-ヒドロキシスチルベン
4',5-ジフェニルオキシ-3-ヒドロキシスチルベン
3,5,4'-トリフェニルオキシスチルベン
3-グルコシド-5,4'-ジヒドロキシスチルベン
5-グルコシド-3,4'-ジヒドロキシスチルベン
4'-グルコシド-3,5-ジヒドロキシスチルベン
3,5-ジグルコシド-4'-ヒドロキシスチルベン
3,4'-ジグルコシド-5-ヒドロキシスチルベン
4',5-ジグルコシド-3-ヒドロキシスチルベン
3,5,4'-トリグルコシドスチルベン。
【0070】
本発明の一つの具体的実施形態では、メトキシ置換されたレスベラトロール誘導体が用いられる。例えば、本発明の組成物は3,5-ジメトキシ-4'-ヒドロキシスチルベンを含むことができ、これはインドのキノ樹脂木(Indian Kino Tree)(プテロカルプス・マルスピウム(Pterocarpus marsupium))から抽出することができ、また、Sigma-Aldrich社(St. Louis, MO)からPTEROSTILBENEという商標名で販売されている。
【0071】
本発明の別の具体的実施形態では、レスベラトロール誘導体が1つ以上のサッカライド含有保護基、例えば、グルコース、ガラクトース、マンノース、フルクトース、スクロース、ラクトース、マルトース、トレハロースなどを含む。例えば、レスベラトロールグルコシドは、イタドリ(polygonum cuspidatum)組織などの植物もしくは植物材料またはブドウ(vitis vinifera)細胞のin vitro培養物からの抽出によって得られ、本発明の化粧料組成物中で用いられる。
【0072】
D. レスベラトロールの窒素含有誘導体
本発明の組成物で用いるレスベラトロール誘導体は1つ以上の窒素含有官能基を含むことができ、すなわち、上記式中のA、BおよびCの1つ以上がアミド、アミン、イミン、アミジン、およびカルボキシアミジンからなる群より選択される。本発明の実施に特に適している代表的なレスベラトロールエーテルのリストは以下のとおりである:
3-アミド-5,4'-ジヒドロキシスチルベン 5-アミド-3,4'-ジヒドロキシスチルベン
4'-アミド-3,5-ジヒドロキシスチルベン 3,5-ジアミド-4'-ヒドロキシスチルベン
3,4'-ジアミド-5-ヒドロキシスチルベン 4',5-ジアミド-3-ヒドロキシスチルベン
3,5,4'-トリアミドスチルベン 3-アミノ-5,4'-ジヒドロキシスチルベン
5-アミノ-3,4'-ジヒドロキシスチルベン 4'-アミノ-3,5-ジヒドロキシスチルベン
3,5-ジアミノ-4'-ヒドロキシスチルベン 3,4'-ジアミノ-5-ヒドロキシスチルベン
4',5-ジアミノ-3-ヒドロキシスチルベン 3,5,4'-トリアミノスチルベン
3-イミノ-5,4'-ジヒドロキシスチルベン 5-イミノ-3,4'-ジヒドロキシスチルベン
4'-イミノ-3,5-ジヒドロキシスチルベン 3,5-ジイミノ-4'-ヒドロキシスチルベン
3,4'-ジイミノ-5-ヒドロキシスチルベン 4',5-ジイミノ-3-ヒドロキシスチルベン
3,5,4'-トリイミノスチルベン 3-アミジノ-5,4'-ジヒドロキシスチルベン
5-アミジノ-3,4'-ジヒドロキシスチルベン 4'-アミジノ-3,5-ジヒドロキシスチルベン
3,5-ジアミジノ-4'-ヒドロキシスチルベン 3,4'-ジアミジノ-5-ヒドロキシスチルベン
4',5-ジアミジノ-3-ヒドロキシスチルベン 3,5,4'-トリアミジノスチルベン。
【0073】
好ましくは、しかし必ずしも必要ではないが、本発明のレスベラトロール誘導体は、皮膚の真皮へのより効果的な送達のために、単独で、あるいはDNA修復酵素および/または1種以上の追加のスキンケア活性剤と組み合わせて、リポソームにカプセル化される。レスベラトロール誘導体は、本発明の化粧料組成物中に、全組成物の全重量に対して、約0.001%〜約95%、好ましくは約0.005%〜約90%、より好ましくは約0.1%〜約20%の範囲の量で存在する。
【0074】
DNA修復酵素
本発明の組成物は、場合により少なくとも1種のDNA修復酵素を含んでもよい。これは、少なくとも1種のDNA修復酵素を必要としておりかつsirt1活性化剤の使用を意図していない、US 11/837,658とは違っている。任意成分であるDNA修復酵素の推奨濃度は、最終組成物の全重量に対して、約0.00001〜約35%、好ましくは約0.00005〜約30%、より好ましくは約0.0001〜約25%である。
【0075】
米国特許第5,077,211号; 第5,190,762号; 第5,272,079号; および第5,296,231号(これら全ての内容を参照により本明細書に組み入れる)に開示されるDNA修復酵素は、本発明の組成物および方法で用いるのに適している。そのようなDNA修復酵素の一例は、AGI/Dermatics社からRoxisomes(登録商標)という商標名で購入することができ、Arabidopsis Thaliana extract(シロイヌナズナエキス)のINCI名を有する。これは単独で、またはレシチンおよび水との混合物として存在しうる。このDNA修復酵素は、8-オキソ-ジグアニンの塩基変異損傷を修復するのに有効であることが知られている。
【0076】
使用できる別のタイプのDNA修復酵素は、06-メチルグアニン塩基変異損傷の修復に有効であることが知られているものである。これはAGI/Dermatics社からAdasomes(登録商標)という商標名で販売されており、Lactobacillus ferment(乳酸桿菌発酵液)のINCI名を有する。この酵素は単独で、またはレシチンおよび水と混合して、本発明の組成物に加えることができる。
【0077】
使用できる別のタイプのDNA修復酵素は、T-Tダイマーを修復するのに有効であることが知られているものである。こうした酵素は生物学的または植物学的物質の混合物中に存在する。そのような成分の例は、AGI/Dermatics社からUltrasomes(登録商標)またはPhotosomes(登録商標)という商標名で販売されている。Ultrasomes(登録商標)は、ミクロコッカス溶解液(さまざまなミクロコッカス菌種の制御された溶解の最終産物)、レシチンおよび水の混合物を含む。Photosomes(登録商標)は、プランクトンエキス(次の生物:海洋藻類、微小緑藻類、珪藻類、緑青藻類および窒素固定藻類のうち1種以上を含む海洋バイオマスのエキスである)、水およびレシチンの混合物を含む。
【0078】
別のタイプのDNA修復酵素は、さまざまな不活化細菌の溶解液、例えばビフィズス菌溶解液またはビフィズス菌発酵溶解液の成分であり、後者は、ビフィズス菌を培養し、不活化し、その後破壊したときの代謝産物と細胞質画分を含むビフィズス菌由来の溶解液である。この物質はBifida Ferment Lysate(ビフィズス菌発酵エキス)というINCI名を有する。
【0079】
他の適当なDNA修復酵素にはエンドヌクレアーゼVが含まれ、これはバクテリオファージT4のdenV遺伝子により産生される。さらに、以下の酵素も適している:T4エンドヌクレアーゼ; O6-メチルグアニン-DNAメチルトランスフェラーゼ; フォトリアーゼ、例えばウラシル-およびヒポキサンチン-DNAグリコシラーゼ; 脱ピリミジン/脱プリン部位エンドヌクレアーゼ; DNAエキソヌクレアーゼ、損傷塩基グリコシラーゼ(例:3-メチルアデニン-DNAグリコシラーゼ); 単独または複合体での修復エンドヌクレアーゼ(correndonucleases)(例:大腸菌uvrA/uvrB/uvrCエンドヌクレアーゼ複合体); APEXヌクレアーゼ、これはしばしば「APE」と呼ばれる多機能性DNA修復酵素である; ジヒドロ葉酸レダクターゼ; ターミナルトランスフェラーゼ; トポイソメラーゼ; O6ベンジルグアニン; DNAグリコシラーゼ。
【0080】
適当なDNA修復酵素の他のタイプは、酵素が手助けする修復のタイプによって分類することができ、以下のものが挙げられる:BER(塩基除去修復)またはBER因子酵素、例えばウラシル-DNAグリコシラーゼ(UNG); 一本鎖選択的単機能性ウラシルDNAグリコシラーゼ(SMUG1); 3,N(4)-エテノシトシングリコシラーゼ(MBD4); チミンDNA-グリコシラーゼ(TDG); A/G-特異的アデニンDNAグリコシラーゼ(MUTYH); 8-オキソグアニンDNAグリコシラーゼ(OGG1); エンドヌクレアーゼIII様(NTHL1); 3-メチルアデニンDNAグリコシダーゼ(MPG); DNAグリコシラーゼ/APリアーゼ(NEIL1または2); APエンドヌクレアーゼ(APEX 1および2)、DNAリガーゼ(LIG3)、リガーゼアクセサリー因子(XRCC1); DNA 5'-キナーゼ/3'-ホスファターゼ(PNKP); ADP-リボシルトランスフェラーゼ(PARP1または2)。
【0081】
DNA修復酵素の別のカテゴリーには、損傷を直接修復すると考えられるもの、例えば、O6-MeGアルキルトランスフェラーゼ(MGMT); 1-meAジオキシゲナーゼ(ALKBH2またはALKBH3)が含まれる。
【0082】
DNA/タンパク質架橋を修復するように機能しうる酵素のさらに別のカテゴリーにはTyr-DNAホスホジエステラーゼ(TDP1)が含まれる。
【0083】
さらに、MMR(ミスマッチ除去修復)DNA修復酵素、例えば、MutSタンパク質ホモログ(MSH2); ミスマッチ修復タンパク質(MSH3); mutSホモログ4(MSH4); MutSホモログ5(MSH5); またはG/Tミスマッチ結合タンパク質(MSH6); DNAミスマッチ修復タンパク質(PMS1、PMS2、MLH1、MLH3); Postmeiotic segregation increased 2-likeタンパク質(PMS2L3); またはpostmeiotic segregation increased 2-like 4偽遺伝子(PMS2L4)も適している。
【0084】
さらに、適しているDNA修復酵素はヌクレオチド除去修復(NER)酵素として知られるものであり、例えば、色素性乾皮症C群相補性タンパク質(Xeroderma pigmentosum group C-complementing protein)(XPC); RAD23 (S. cerevisiae)ホモログ(RAD23B); カルトラクチンアイソフォーム(caltractin isoform)(CETN2); RFAタンパク質1、2または3 (RPA1、2または3); 3'-5' DNAヘリカーゼ(ERCC3); 5'-3' DNAヘリカーゼ(ERCC2); 塩基性転写因子(GTF2H1、GTF2H2、GTF2H3、GTF2H4、GTF2H5); CDK活性化キナーゼ(CDK7、CCNH); サイクリンG1相互作用タンパク質(cyclin G1-interacting protein)(MNAT1); DNA除去修復タンパク質ERCC-51; 除去修復交差相補群1(excision repair cross-complementing 1)(ERCC1); DNAリガーゼ1 (LIG1); ATP依存性ヘリカーゼ(ERCC6)などが挙げられる。
【0085】
さらに、相同組換えを促進するカテゴリー中のDNA修復酵素も適しており、限定するものではないが、DNA修復タンパク質RAD51ホモログ(RAD51、RAD51L1、RAD51Bなど); DNA修復タンパク質XRCC2; DNA修復タンパク質XRCC3; DNA修復タンパク質RAD52; ATPase (RAD50); 3'エキソヌクレアーゼ(MRE11A)などが含まれる。
【0086】
DNAポリメラーゼであるDNA修復酵素も適しており、DNAポリメラーゼβサブユニット(POLB); DNAポリメラーゼγ(POLG); DNAポリメラーゼサブユニットδ(POLD1); DNAポリメラーゼIIサブユニットA (POLE); DNAポリメラーゼδ補助タンパク質(PCNA); DNAポリメラーゼζ(POLZ); MAD2ホモログ((REV7); DNAポリメラーゼη(POLH): DNAポリメラーゼκ(POLK)などが挙げられる。
【0087】
「編集・プロセッシングヌクレアーゼ」(editing and processing nucleases)と呼ばれることが多い、さまざまなタイプのDNA修復酵素には、3'-ヌクレアーゼ; 3'-エキソヌクレアーゼ; 5'-エキソヌクレアーゼ; エンドヌクレアーゼなとが含まれる。DNA修復酵素の他の例には、DNAヘリカーゼ、例えばATP DNAヘリカーゼなどが含まれる。DNA修復酵素は植物エキス、細菌溶解液、生物学的物質などの成分として存在し得る。例えば、植物エキスがDNA修復酵素を含むことがある。
【実施例】
【0088】
実施例1: sirt1活性化剤(Orsirtine(商標)およびレスベラトロール)はケラチノサイトの生存を相乗的に改善する
有糸分裂遅延剤であるOrsirtine(商標)((配列番号8) G-L-Y-D-N-L-E)およびレスベラトロールを、UVB照射したヒトケラチノサイトの生存を改善するそれらの能力について試験した。
【0089】
方法:
正常なヒトケラチノサイトを、ヒトケラチノサイト増殖サプリメント(Human Keratinocyte Growth Supplement)を添加したEpilife培地で培養した。その細胞を96ウェルプレート(Costar)に継代培養した。ケラチノサイトをレスベラトロール(25μM)およびOrsirtine(1%、3%)単独で、さらにレスベラトロール(25μM)とOrsirtine(3%)の複合体で前処理した。ケラチノサイトを未希釈の複合体で、また、1:2、1:4および1:8 (複合体:Epilife培地)の希釈物で処理した。
【0090】
ケラチノサイトをこれらの処理剤と共に37℃、5%CO2で一晩インキュベートした。24時間後、その処理剤を吸引し、ケラチノサイトをD-PBSで1回洗浄した。照射のために100μlのD-PBSを添加した。細胞に0、45、90および135mJ/cm2のUVBを照射した。照射後、D-PBSを除去した。ケラチノサイトを適切に後処理して、37℃、5%CO2で一晩インキュベートした。翌日、MTS試薬(CellTiter96、Promega社)を利用して、細胞の生存率についてアッセイした。37℃、5%CO2で約2時間のインキュベーション後に、吸光度をSpectraMax190分光光度計(Molecular Devices社)で490nmにて読み取った。
【0091】
結果および結論:
図2を参照すると、低UV照射(45mJ/cm2)では、細胞は強烈なダメージを示さないことが報告されているで、生存率の改善はごくわずかであると予想された。しかし、我々が観察したものは、レスベラトロールだけで処理した細胞が20%の生存率の低下を示し、また、Orsitine(3%)だけで処理した細胞が8%の生存率の低下を示す、ということである。それにもかかわらず、1:2希釈複合体(レスベラトロール25μMとOrsirtine 3%)で、または未希釈複合体で処理した細胞は、対照と同じ試験結果であった。さらに、複合体を1:4に、次いで1:8に希釈すると、生存率が低下する。こうして、レスベラトロール単独、およびOrsirtine 3%単独では、細胞の生存が低下する。しかしながら、レスベラトロールとOrsirtine 3%の組合せは細胞の生存を低下させない。しかし、この組合せは、対照と比べて、細胞の生存率を改善することができるのか?
90mJ/cm2のUV照射では、未処理の細胞の生存率は47%であった。それに引き換え、未希釈および希釈した複合体(レスベラトロール25μMとOrsirtine 3%)で処理した細胞の生存率は、次のように用量依存的関係にあった:
【表1】

【0092】
一方、Orsirtine単独またはレスベラトロール単独で処理した細胞の生存率は次のとおりであった:
【表2】

【0093】
135mJ/cm2のUV照射では、未処理の細胞の生存率は19%であった。それに引き換え、未希釈および希釈した複合体で処理した細胞の生存率は、次のように準用量依存的関係にあった:
【表3】

【0094】
一方、Orsirtine単独またはレスベラトロール単独で処理した細胞の生存率は次のとおりであった:
【表4】

【0095】
複合体(レスベラトロール25μMとOrsirtine 3%)は、レスベラトロールおよびOrsirtine単独と比べて、UVB誘導細胞毒性に対して顕著な保護を与えるとともに、細胞の生存を高める、と結論づけることができる。
【0096】
これらの数字はまた、ケラチノサイト生存率に対するOrsirtineとレスベラトロールの組合せの効果が相乗的であることを示唆するようである。例えば、3%のOrsirtineは単独で生存率を11%(90mJ/cm2のUVBの場合)および26%(135mJ/cm2のUVBの場合)増加させる。25μMのレスベラトロールは単独で生存率を15%(90mJ/cm2のUVBの場合)低下させ、かつ生存率を22%(135mJ/cm2のUVBの場合)増加させた。ところが、未希釈の組合せ(3%Orsirtineと25μMレスベラトロール)は、ケラチノサイトの生存率を、大幅にかつ予想外に、64%(90mJ/cm2のUVBの場合)および131%(135mJ/cm2のUVBの場合)増加させた。1:8まで希釈したときでさえ、この組合せはまだケラチノサイトの生存率を28%(90mJ/cm2のUVBの場合)および11%(135mJ/cm2のUVBの場合)増加させる。このことは完全に予想外である。Orsirtineは既知のサーチュイン活性化剤であり、また、レスベラトロールは疑わしいサーチュイン活性化剤であるので、ケラチノサイトの生存率の大幅な改善は当業者には予想されないことである。せいぜい、相加効果が予想されたかもしれないが、相乗効果は予想されなかった。
【0097】
(配列番号8) G-L-Y-D-N-L-Eとレスベラトロールのどのような相対濃度がケラチノサイトの生存率に大きな相乗効果をもたらすのだろうか?この質問には、今やその効果が確認されているのだから、日常的な実験によって答を出すことができる。「sirt1活性化剤とレスベラトロールの相乗的組合せ」とは、ケラチノサイトの生存率(そうした生存率は当技術分野で公知の方法により測定される)を、個別の各物質の効果の合計量を超える分量だけ、増加させる(配列番号7)(AA)n-G-L-Y-D-N-L-E-(AA)nとレスベラトロールまたはその誘導体との組合せを意味する。
【0098】
実施例2: sirt1活性化剤は、正しい濃度で、UVB曝露に対する概日遺伝子活性化剤とDNA修復酵素の性能を改善する
実施例1に記載の方法に従って、2種の複合体をいくつかの希釈率で、UV曝露後に、ケラチノサイトの生存に対するそれらの効果について試験した。複合体Iは、ヒトケラチノサイト増殖サプリメントを添加したEpilife培地と、Chronolux (0.1%)、ビフィズス菌エキス(12.4%)、Adasome (0.05%)およびRoxisome (0.05%)から成っていた。複合体IIは、複合体IにOrsirtine (0.08%)とレスベラトロール(25μM)を加えたものから成っていた。複合体Iは未希釈ならびに1:2および1:4 (複合体:Epilife培地)の希釈で試験した。複合体IIは未希釈ならびに1:2、1:4および1:8の希釈で試験した。培地を対照として用いた。ケラチノサイトを100、150および200mL/cm2のレベルのUVBに曝露した。
【0099】
結果および結論:
図3を参照すると、また、同じUVB曝露内で複合体IIを複合体Iと比較すると、
【表5】

【0100】
2つを除く全ての場合に、Orsirtine(商標)およびレスベラトロールは、概日遺伝子活性化剤だけと比較して、UVB曝露後のケラチノサイトの生存を改善する。しかし、第1列(100mJ/cm2)の2つの段を下に移動すると、これらのデータは、概日遺伝子活性化剤と組み合わせたsirt1活性化剤が少ないほど良好である、ことを示唆するようである。ところが、このパターンは第2列および第3列(150mJ/cm2および200mJ/cm2)で破られ、sirt1および概日遺伝子活性化剤の最適な組合せはケラチノサイトが曝露されるUVBの量に依存する、ことを示唆している。実際、3段目(未希釈)を左から右に移動すると、これらのデータは、Orsirtineとレスベラトロールの添加がより多量のUVB曝露に対して正当化される、ことを示唆している。このパターンは1:2希釈のサンプルでも見られるが、1:4希釈のサンプルでは逆転し、より低いUVB曝露には、より少ないsirt1活性化が必要であることを示唆している。こうして、全体として見れば、これらの実験の結果は、概日遺伝子活性化剤とsirt1活性化剤の最適な相対濃度がUVBの曝露量に依存することを示唆している。しかしながら、全ての複合体II試験サンプル(概日活性化剤+sirt1活性化剤)は、対照と比べて、ケラチノサイト生存率の改善を示した。今や当業者は概日遺伝子活性化剤とsirt1活性化剤の相対濃度が結果有効変数(results-effective variable)である(これまで不明であった)ことを知っているので、最適な相対濃度を決定するには日常的な実験が必要であるにすぎない。
【0101】
組成物
本発明の組成物の形態は一般的に限定されない。例えば、本発明の組成物はエマルション、水性の溶液もしくは分散液、ゲル、または無水系の形態であってよい。エマルションの形態である場合、組成物は油中水型または水中油型のエマルションであり得る。エマルションの形態である場合、その組成物は約1〜99%、好ましくは約5〜90%、より好ましくは約10〜85%の水と、約1〜99%、好ましくは約5〜90%、より好ましくは約5〜75%の油を含むことができる。水性懸濁液または分散液の場合には、組成物は一般的に約1〜99.9%、好ましくは約5〜95%、より好ましくは約10〜90%の水を含み、残りの成分が活性成分または他の処方成分である。
【0102】
好ましくは、組成物は化粧品的または薬学的に許容される製品を提供する他の成分を含有する。そうした成分のクラスには、保湿剤、UVAおよびUVBサンスクリーン剤、界面活性剤、植物エキス、生物学的物質、水相構造化剤(すなわち、多糖類、アクリレートポリマー、高分子量PEGまたはポリグリセリン)、揮発性および不揮発性オイル(シリコーンを含む)、ビタミン、および酸化防止剤が含まれるだろう。
【0103】
また、概日遺伝子活性化剤とsirt1活性化剤は別々の組成物中に存在することが可能であり、その別々の組成物は、皮膚の同じ領域に連続して適用してもよいし、または各組成物の有効量を分配して混ぜ合わせてから、その混合物を皮膚に塗布することによって適用してもよい。
【0104】
好ましい組成物
好ましい組成物は水性溶液またはエマルションの形態であり、少なくとも1種の非イオン性有機界面活性剤、少なくとも1種の化学的サンスクリーン剤、少なくとも1種のclockまたはper1遺伝子活性化剤、少なくとも1種のペプチド性sirt1活性化剤、および少なくとも1種のDNA修復酵素を含有する。少なくとも1種の植物エキスおよび少なくとも1種のオイルも好ましいものである。
【0105】
より好ましいものは、非イオン性有機界面活性剤がアルコキシル化アルコールであり、化学的サンスクリーン剤がUVBサンスクリーン剤であり、clockまたはper1ケラチノサイト遺伝子活性化剤がTripeptide-32であり、sirt1活性化剤がOrsirtine(商標)様分子とレスベラトロールの組合せであり、DNA修復酵素がシロイヌナズナエキス(Arabidopsis Thaliana extract)とミクロコッカス溶解液(Micrococcus lysate)とビフィズス菌発酵エキス(Bifida Ferment lysate)と乳酸桿菌発酵液(Lactobacillus ferment)とプランクトンエキス(Plankton extract)の混合物であり、そして少なくとも1種のオイルが有機エステルまたは炭化水素である場合の組成物である。
【0106】
本発明の方法
本発明の方法は主に、ヒトケラチノサイト、好ましくは顔のケラチノサイトへの損傷(損傷は環境攻撃に応答して発生する)を修復することに向けられる。一方法は、損傷を受けたヒト皮膚に、少なくとも1種のケラチノサイトclockまたはper1遺伝子活性化剤と少なくとも1種のsirt1活性化剤を含む1つ以上の組成物を適用することからなる。場合により、本方法の組成物は少なくとも1種のDNA修復酵素を含んでもよい。損傷が発生した後に本組成物を適用することによって、通常の概日周期がより速やかに回復される。しかし、有糸分裂前の細胞周期の停止は、DNA修復のためにより多くの時間を割り当てられる。この方法によって、かなりの細胞損傷が回復に向かい、かつ/または娘細胞に伝わるのをチェックされる。本方法はまた、ケラチノサイトの生存率と寿命を改善することができる。
【0107】
本発明はさらに、ヒトケラチノサイト、好ましくは顔のケラチノサイトへの損傷(損傷は環境攻撃に応答して発生するだろう)を予防または抑制する方法に向けられる。この方法は、環境損傷を受けるリスクがあるヒト皮膚に、少なくとも1種のケラチノサイトclockまたはper1遺伝子活性化剤と少なくとも1種のsirt1活性化剤を含む1つ以上の組成物を適用することからなる。場合により、本方法の組成物は少なくとも1種のDNA修復酵素を含んでもよい。損傷が発生する前に本組成物を適用することによって、通常の概日周期がより厳密に維持され、また、通常の細胞周期の修復過程がより厳密に維持される。この方法によって、かなりの細胞損傷が予防され、かつ/または娘細胞に伝わるのをチェックされる。本方法はまた、ケラチノサイトの生存率と寿命を改善することができる。
【0108】
本発明の方法では、組成物を1日1回以上皮膚に適用することができる。例えば、日常活動を始める前の午前中におよび/または就寝する直前の夜に、組成物を皮膚に適用する。これらの時間帯は、皮膚が一般的に最少量の環境攻撃のもとにある(皮膚細胞の修復が最大になりうることを意味する)ため、好適である。これらの時間帯で、「就寝する直前」または「毎晩休む直前」とは、床に入る1時間以内、より好ましくは床に入る30分以内を意味する。午前中はどちらかといえば予防的アプローチであるが、就寝する直前または夜はむしろ修復アプローチである。本組成物はレジメンの一部として適用することができる;すなわち、皮膚を洗浄して化粧水(toner)で処置し、その後本発明の組成物を適用する。本組成物は、洗浄剤と化粧水と本発明の組成物を含むキットの一部であり得る。
【0109】
好ましくは、本組成物は、DNA損傷を受けたケラチノサイトを修復しかつ皮膚の一般的な改善を得るために、就寝直前に顔および/または首と胸元の皮膚に適用される。顔の皮膚を夜に就寝する直前に処置するための組成物中でclockおよびper1遺伝子活性化剤とsirt1活性化剤(と好ましくはDNA修復酵素)を併用すると、ケラチノサイトのDNA損傷の修復が最大となり、さらに細胞の生存率、寿命および健康が促進される。
【0110】
上述したように、概日遺伝子活性化剤とsirt1活性化剤は別々の組成物中に存在することが可能である。その場合に、本発明の方法は、各組成物を皮膚の同じ領域に連続して適用するステップを含むか、または各組成物の有効量を分配するステップと、その組成物を混合するステップと、その後混合物を皮膚に適用するステップを含む。
【0111】
実施例
本発明を、例示のみの目的のために記載される以下の実施例に関連して、さらに説明することにする。スキントリートメント組成物は次のように調製することができる。
【0112】
実施例1
【表6】


【0113】
実施例2〜4
clock遺伝子活性化剤(Chronolux(登録商標)、tripeptide-32)を含むが、sirt1活性化剤を含まない第1のスキントリートメント組成物は、処方A(実施例2)に従って調製することができる。clock遺伝子活性化剤(Chronolux(登録商標))とsirt1活性化剤(Orsirtine(商標)およびレスベラトロール)を含む第2のスキントリートメント組成物は、処方B(実施例3)に従って調製することができる。sirt1活性化剤(Orsirtine(商標))を含むが、概日遺伝子活性化剤を含まない第3のスキントリートメント組成物は、処方C(実施例4)に従って調製することができる。これらの組成物は、各成分を一緒にし、十分に混合して液体とすることによって調製される。組成物は褐色のガラスビンに保存することができる
組成物Aは、概日遺伝子活性化剤とsirt1活性化剤(Orsirtine(商標)およびレスベラトロール)を含む。したがって、組成物Aは単独での使用を目的としている。組成物BはChronolux(登録商標)(概日遺伝子活性化剤)を含むが、sirt1遺伝子活性化剤を含まない。したがって、組成物Bは、sirt1遺伝子活性化能を有する別の組成物(例えば、組成物C)と一緒の使用を目的としている。
【表7】


【表8】


【0114】
本発明を好ましい実施形態に関連して説明してきたが、本発明の範囲を、記載された特定の形態に限定することを意図したものではない。それどころか、この説明は、添付の特許請求の範囲により規定される本発明の精神および範囲内に含まれるような変更、修飾および均等物をカバーすることを意図したものである。
【技術分野】
【0001】
本出願は、2007年8月13日付けの係属中の米国特許出願US 11/837,658号の一部継続出願、および2009年2月9日付けの係属中の米国特許出願US 12/367,705号の一部継続出願であり、両出願の全内容を参照により本明細書に組み入れる。
【0002】
技術分野
本発明はスキントリートメントの分野に関するものである。より具体的には、本発明は、皮膚細胞における損傷DNAの修復を高めるための組成物および方法に関する。
【背景技術】
【0003】
皮膚がさまざまな環境要因と生活要因から毎日攻撃を受けていることは、今やよく理解されている。こうした要因のショートリストには、UVA放射線、UVB放射線、汚染、タバコの煙、貧しい食生活、不十分な休息、および心理的ストレスが含まれる。この攻撃は皮膚細胞のDNAとタンパク質への損傷として現れる。皮膚のラインやシワは皮膚細胞の損傷のより軽度の結果の一つであるが、メラノーマはより重篤な結果の一つである。
【0004】
DNA損傷
一部の環境および生活要因は皮膚細胞のDNAおよび/またはタンパク質と直接的に相互作用して損傷を引き起こし、一部の要因は間接的に損傷を引き起こし、また、一部の要因は両方をすることができる。直接的DNA損傷の例は、皮膚細胞のDNAがスペクトルのUVB部からの光子を吸収するときであると考えられる。光子の吸収はDNA配列に突然変異を起こすことがある。例えば、全メラノーマ発生の約8%は直接のDNA突然変異によるものである。
【0005】
皮膚細胞DNAおよびタンパク質の間接的損傷の例は、紫外線光子が皮膚に入って、発色団によって吸収されるときに見られる。励起状態では、発色団は活性酸素種の形成につながる反応に加わる。例えば、ヒトの皮膚では、UVB曝露は過酸化水素の産生と関連しており、一方UVAは一重項酸素の産生に関連している。皮膚がこれらの反応種を中和することによって恒常性を維持できない場合、その反応種は酸化を通して皮膚細胞のDNAとタンパク質を傷つけることになる。こうしたDNAおよびタンパク質への損傷は、酸化的ストレスと呼ばれており、皮膚老化の主な原因となる。さらに、全メラノーマ発生の約92%は間接的な酸化的DNA損傷によるものである。
【0006】
DNA損傷:予防および封じ込め-対-修復
DNAを含む皮膚細胞にはケラチノサイト幹細胞およびメラノサイトが含まれる。1回のサンバーンは、影響を受けた細胞において、T-T(チアミン-チアミン)ダイマー;8-オキソ-7,8-ジヒドロ-2'-デオキシグアノシン(8-オキソ-DG);06MeG (06-メチルグアニン);シクロブタンピリミジンダイマー(CPD);および6-4光分解生成物(6-4PP)など、何十万ものDNA変異原性塩基修飾をもたらすと推定される。これらの変異は皮膚細胞内のさまざまな反応を引き出し、そうした応答はさらなるDNA損傷または細胞のアポトーシスの予防につながる可能性がある。例えば、メラノサイトでのメラニン産生は、防護手段として、UV放射線によりアップレギュレートされることが知られている。UVからの脅威に対処するため、メラニンが表皮下層のメラノサイトによって産生され、外側に移動するケラチノサイトの助けを借りて、表皮上層および下層の全体に分布する。まず第一に、メラニンは、メラノサイトおよびケラチノサイト幹細胞が位置する表皮下層に入り込むUVの量を制限するUVフィルターとして作用することによって、さらなるUV誘発DNA損傷を予防するようである。しかし、第二次の防護として、メラニンは、ケラチノサイトのアポトーシスを誘導することによって、UV放射線によるDNA損傷を封じ込める。アポトーシスを促進することによって、娘細胞に伝えられる機会が少なくなり、損傷したDNAは封じ込められる(例えば、Yamaguchi et al., Melanin mediated apoptosis of epidermal cells damaged by ultraviolet radiation: factors influencing the incidence of skin cancer (紫外線による損傷を受けた表皮細胞のメラニン介在アポトーシス:皮膚がんの発生に影響を及ぼす因子); Arch Dermatol Res. 2008 Apr; 300 Suppl 1: S43-S50を参照されたい)。
【0007】
DNA損傷の予防および封じ込めとは別に、健全なケラチノサイトとメラノサイトは、DNA損傷を修復するための天然の内部機構をもっている。こうした機構は予防および封じ込めの機構とは異なっており、別の(しかし、時には重複する)反応カスケードを含んでいる。本発明の組成物および方法は、DNA損傷の修復に最も関係している。
【0008】
細胞修復機構は、我々が論じてきたUV誘発損傷だけでなく、さまざまな原因で生じるDNA損傷を修復するために存在する。しかしながら、DNA損傷の修復には時間がかかる。例えば、UVB曝露によって形成されたTTダイマーおよび6-4PP損傷の修復には、外的影響によって加速されないとすると、それぞれ48時間および8時間ほどかかる可能性がある。UVAもしくはUVB曝露、オゾン、またはタバコの煙および汚染による8-オキソ-dGおよび06MeG損傷の修復には、2時間ほどかかることがある。DNA損傷は細胞分裂が起こる前に修復されることが理想的である。もしそうでないなら、好ましい結果はアポトーシスである。しかし、DNA損傷がたまたまアポトーシスのアップレギュレーションに悪影響を及ぼす場合、または突然変異が検出されない場合には、損傷したDNAが次世代に伝わる可能性がある。本発明の組成物および方法は、細胞分裂が起こる前にDNA損傷の修復を最大限に高めることに最も関係している。
【0009】
細胞の予防および修復機構は概日時計によって制御される
通常の状態では、DNAの発現および修復を含めた細胞機能は、不定期に等確率で起こるものではない。それどころか、それぞれの細胞には約24時間の内因性周期(または時計)(すなわち、概日リズム)があり、細胞の活動はこの内因性周期によって調節されている。外部刺激がなければ、各細胞はその内因性時計に従ってフリーラン(free-run)するだろう。しかし、全身の細胞の内因性時計は同期化されている。細胞の活動を互いに同期化し、かつ環境と同期化するために、身体は環境からのシグナルを受け取ることができる。最も顕著な環境シグナルは日光の存在または不在である。こうして、概日周期は太陽日の位相にほぼ一致する明期と暗期で構成される。
【0010】
今では、概日リズムによって、細胞が細胞に影響を及ぼす可能性のある環境の変化を予知して、そうした変化にタイムリーに適応できることは理解されている。細胞の概日リズムの遺伝機構が適切に機能している限り、細胞は、その多くの機能のそれぞれを、細胞の生存および/または恒常性にとって最適な時期に、同期化された方法で実行する。例えば、昼が近づくにつれて(皮膚がUVから攻撃を受ける前であっても)、特定の遺伝子が、予測されるUV線によるダメージから細胞を保護するタンパク質を産生するように活性化される。その後、昼が終わりに近づくにつれて、これらの遺伝子はオフの状態になる。他方、概日遺伝子自体は環境要因によって攻撃を受ける可能性がある。細胞の概日リズムを調節している1つ以上の遺伝子が損傷すると、細胞は環境および他の細胞と同期化しない(out of sync)ことがある。
【0011】
コア概日機構
転写因子は、特定のDNA配列と結合して、DNAからの遺伝情報のRNAへの転写を制御しているタンパク質である。コア概日機構(core circadian mechanism)、または「細胞時計」は、位相を異にする(out-of-phase)、負および正のフィードバックループに参加する転写因子(振動遺伝子の転写をもたらす)で構成されている。
【0012】
哺乳類の主要な負のフィードバックループでは、CLOCKおよびBMAL1転写因子のヘテロダイマーがperiod (per)およびcryptochrome (cry)遺伝子の転写を活性化する。ヒトでは、period遺伝子は実際には3つの遺伝子per1、per2、およびper3からなるファミリーであり、また、cry遺伝子ファミリーにはcry1およびcry2の遺伝子が含まれる。それらの翻訳に続いて、PERおよびCRYタンパク質は細胞質に移動して、PER/CRY複合体を形成する。翻訳後制御は意図的な遅延を生じさせ、その後PER/CRY複合体は細胞核内に移動する。核内のPERとCRYの濃度は24時間周期の昼間の終わりにピークに達し、その時点でCRYタンパク質はCLOCK/BMAL1ヘテロダイマーの転写活性を抑制するように作用する。したがって、CRYは自らの転写をオフにするようである。
【0013】
他方、1つの正のフィードバックループでは、核に移行した後のPER2がBMAL1の転写をアップレギュレートして、最終的にはperiodおよびcry遺伝子の転写をもたらすようである。さらに、CLOCK/BMAL1ダイマーはrev-erbαおよびrora遺伝子をアップレギュレートするようである。roraはBMAL1転写を活性化する一方で、rev-erbαはCLOCKとBMAL1を抑制する。いわゆる「カノニカル時計遺伝子」(canonical clock genes)(clock、bmal1、per1、per2、per3、cry1およびcry2)のピーク活性は位相を異にして、結果的に、約24時間の周期をもつ自立的なループが生じる。
【0014】
細胞周期
細胞周期は、細胞の分裂と複製をもたらす、細胞内で起こる一連の事象をさす。その周期は通常、完了するまでに約24時間を必要とする4または5つの連続相として説明される。細胞周期の各相には、所定の相のすべての必要なプロセスが次の相の開始までに完了していることを保証するチェックポイントがある。ヒト細胞において、「第1」相は、細胞のDNAが複製および合成される合成(S)期である。S期は一般に6〜8時間続く。3〜4時間続くG2期では、タンパク質が合成され、かつ細胞の大きさが倍になる。有糸分裂(M)においては、核膜が破れて、遺伝物質の各コピーが細胞の反対極に分離できるようになる。染色体の各セットの周りに新しい核膜が形成されるのに続いて、細胞が2つに絞り込まれる(細胞質分裂)。M期は約1時間の長さである。最も長い第4相(6〜12時間)は、RNAとタンパク質の合成により特徴づけられるG1である。G1期から、細胞は再びS期に入ることもあれば、G0期に入ることもある。G0では、細胞は休止状態にある。G0は数日間または数年間続く場合もある。幹細胞はG0期から戻って、G1に入ることができる。分化した細胞は一般的にG0から戻ることはない。また、DNAが損傷を受けた細胞は、アポトーシスよりはむしろ、G0に入る。
【0015】
細胞周期チェックポイントは損傷DNAが受け継がれるのを阻止する
細胞分裂時には、細胞周期を経る細胞の進行状況を制御するためにチェックポイントが用いられる。チェックポイントは、すべての必要なプロセス(損傷DNAの修復を含む)が完了するまで、細胞が次の相に進行するのを防いでいる。このように、チェックポイントは、損傷を受けたまたは不完全なDNAが娘細胞に伝わらないようにしている。いくつかのチェックポイントが存在する。G1/Sチェックポイント(制限チェックポイント)は細胞周期を中断して、休止期に入るかまたは入らないの「決定」を行うことができる。G2/Mチェックポイントでは、損傷を受けたDNAが検出されると(これは珍しいことではない)、細胞周期が停止される。複製後チェックポイントは、合成期に複製された損傷DNAに関係する。損傷DNAの複製は、複製後修復過程が完了するまで細胞周期の進行を止める細胞応答を引き出す。ヒト細胞では、複製後チェックポイントは、有糸分裂期の開始を遅らせることによって修復のための時間をつくる。chk1遺伝子は複製後チェックポイントでの制御をもたらす一方、p53遺伝子はG1/SおよびG2/Mチェックポイントの両方でその制御機構を始動させるのに重要な役割を果たしている。
【0016】
概日時計は細胞増殖をも制御する
近年、細胞増殖を制御する上での概日時計の重要性が高く評価されている。例えば:
「概日タイミングの破壊は・・・細胞分裂の正常な調節に広範囲にわたって影響を及ぼす。」(Reddy et al., 2005 Circadian clocks: neural and peripheral pacemakers that impact upon the cell division cycle (概日時計:細胞分裂周期に影響を及ぼす神経および末梢ペースメーカー). Mutation Research 574 76-91)。
【0017】
「時計成分が細胞周期調節機構と相互作用するメカニズムへの詳細な洞察は、最近のマウス研究から端を発している。例えば、・・・肝組織の除去(部分的肝切除)とその後の有糸分裂の第1波の間の遅延は、手術が行われた日の時間に左右される。」(Vallone et al., 2007 Start the clock! Circadian rhythms and development (時計を起動させよ! 概日リズムと発生). Developmental Dynamics 236 142-155)。
【0018】
「シアノバクテリアから高等脊椎動物まで、夜間に起こるように細胞周期のS期と有糸分裂を「ゲーティング」する概日時計の多くの例が存在する。」(Vallone et al.) [おそらく、DNA合成と有糸分裂は太陽からの有害なUVまたは他の電離放射線からDNAを保護するために夜間に起こる]。
【0019】
こうして、概日時計は、DNAおよびタンパク質の合成、有糸分裂および細胞質分裂、RNAの合成および修復の細胞周期に包括的な影響を及ぼしている。したがって、環境要因が細胞の概日機構を妨げるとき、細胞機能が損なわれる。本発明者らは、治療が細胞の概日時計を同調させるかもしくは再同期化できるとき、または治療が概日遺伝子発現の「正常」レベルを回復できるとき、細胞機能が改善されるか、細胞損傷が加速的に修復されるか、またはアポトーシスがよりタイムリーに起こる可能性がある、と予想している。
【0020】
環境は概日リズムを同期しない状態に置くことができる
細胞の概日リズムを制御している1つ以上の遺伝子を妨げる作用物質は、細胞を、環境および他の細胞と同期しない状態に置くことができる。例えば、UV曝露後数時間、おそらく20時間もの間、ヒトケラチノサイトにおけるclock、bmal1およびper1遺伝子発現のレベルは大幅に低下する(図1参照)。「大幅に低下する」とは、これらの遺伝子が先に説明した通常の概日周期で経験する最小発現より少ないことを意味する。さらに、UV曝露後、遺伝子発現の通常のパターン(ほぼ正弦波として記載される)が失われる。
【0021】
図1において、水平線はclock遺伝子発現の通常の平均レベルを示しており、UV曝露後約44時間で開始して、その線についての典型的な概日変化を示している。対照的に、UVB曝露の直後に、遺伝子発現のレベルは通常をはるかに下回るレベルに落ちて、約20時間で通常のレベルに戻らなかった。その20時間にわたり、遺伝子発現の通常のパターンが3種すべての遺伝子で失われた。そして、遺伝子発現のレベルがほぼ通常のレベルに戻った場合でも、いつもの正弦波発現パターンが回復するのに約20時間から約44時間の時間が必要であった。こうして、UV曝露は2つの影響を及ぼした。一方の影響は概日遺伝子の発現レベルの劇的な低下であり、他方はそのパターン、すなわち、それらの発現のタイミングである。UV曝露後0時間から約44時間まで、DNAとタンパク質の合成、有糸分裂と細胞質分裂、RNAの合成と修復、ならびにプログラムされた細胞死(アポトーシス)のタイミングがすべて損なわれる。
【0022】
当然、UV曝露は昼間、特に午前10時から午後2時の決定的時間帯に起こる。すでに述べたように、核内のPERおよびCRYタンパク質の濃度は、24時間周期の昼間の終わりにピークに達し、その時点でCRYタンパク質はCLOCK/BMAL1ヘテロダイマーの転写を抑制するように作用する。clockおよびbmal1発現をオフにする臨界濃度への到達の遅れは概日周期を長くするだろう。こうして、UV曝露は概日周期を長くする傾向がある。これは細胞周期を環境と同期しない状態にする。DNA複製および有糸分裂が、細胞複製にとって最適な夜間に起こらない可能性がある。また、概日遺伝子が細胞周期に及ぼすゲーティングの影響が損なわれて、結果的にDNA損傷が検出されないか、修復されないことがあり、また、娘細胞に伝わる可能性がある。
【0023】
サーチュインは有糸分裂の開始を遅らせることが報告されている
サーチュイン1 (SIRT1またはSilent information regulator two ortholog 1の別名でも知られる)は、ストレスに応答して代謝と細胞生存を制御している酵素である。それは細胞の寿命に関連づけられる。SIRT1酵素をコードするsirt1遺伝子は概日遺伝子ではない。Chuaらは、SIRT1が細胞周期を停止させることによって複製老化を促進すると提案している(Chua et al. (2005) Mammalian SIRT1 limits replicative life span in response to chronic genotoxic stress (哺乳動物SIRT1は慢性の遺伝毒性ストレスに応答して複製寿命を制限する). Cell Metabolism 2, 67-76)。
【0024】
US 2009-0082278 (その全内容を参照により本明細書に組み入れる)はさらに、この遺伝子と、それをアップレギュレートすることができる局所皮膚組成物を記載している。段落8〜13には次のように書かれている:
「出願人は最近、老化過程と細胞保護に大きな役割を有する皮膚細胞の機構への新たなタンパク質の関与を発見した。」
「出願人は、SIRTタンパク質、より正確にはSIRT1タンパク質が皮膚細胞で発現されること、また、その発現は皮膚細胞が遭遇するさまざまなストレスに関連していることを実証した。彼らは特に、異なる作用物質を使用するこのタンパク質の発現誘導が細胞の保護を可能にし、また、細胞がストレスおよび内因性老化と戦うのにいっそう役立つことを実証した。」
「SIRTタンパク質はサーチュインファミリーの一部であり、ヒストン脱アセチル化において重要な役割を果たすNAD+依存性核タンパク質である。SIRタンパク質をコードするSIR遺伝子(Silent Information Regulators)は、1979年にS.セレビシエ(S. cerevisiae)で初めて記述された(Rine J and A l., Genetics 1979)。後に、C.エレガンス(C. elegans)でのSIR2Pタンパク質の過剰発現はこの生物の寿命を延ばすことが実証された(Tissenbaum and A l., Nature 2001)。この研究によって、これらのタンパク質は長寿に関係していると仮定することができた。」
「SIRT1タンパク質は最も特性解析されたヒトサーチュインであり、多数の転写調節因子と相互作用する。ヒトSIRT1タンパク質はp53の調節に関与するものとして(Cheng H L and A l. Proc Natl Acad Sci USA. 2003)、最近では、細胞老化のモジュレーターとして(Langley E and A l., EMBO J. 2002)記載されている。その他のヒトSIRTタンパク質も発見されている(SIRT2、SIRT3、SIRT4-7)。ヒトSIRT2タンパク質はほとんど研究されていない;しかし、いくつかの研究によって、有糸分裂活性の制御におけるその役割(Dryden S C and A l. Mol Cell Bio. 2003)ならびにp53タンパク質の調節へのその関与(Vaziri H and A l., Cell. 2001)が実証されている。これまでのところ、デアセチラーゼサーチュインは、細胞死の調節およびその生活環において重要な役割を果たす酵素の一ファミリーと見なされている(Porcu M. and Chiarugi A, Trends Pharmacol Sci., 2005)。」
「本発明[すなわち、US 2009-0082278]は、化粧品的にまたは薬学的に許容される媒体中に、皮膚細胞でのSIRTタンパク質の合成を活性化する可能性がある少なくとも1種の化合物を含む、化粧料または医薬組成物に関する。優先的に、本発明によると、これらの化合物はSIRTタンパク質の特定のクラス、SIRT1タンパク質を活性化するだろう。」
「これまで、皮膚細胞における、SIRTファミリーのタンパク質の合成の誘導物質として機能する化合物の使用は記載されていない。」
【0025】
本明細書は、これまで、概日遺伝子活性化剤と共同してsirt1活性化剤を含む組成物の使用が、US2009-0082278にさえも、記載されたことがない点を強調する。本出願人の知る限りでは、ヒト表皮ケラチノサイトにおけるCLOCKおよびPER1タンパク質のレベル低下に対処する局所組成物であって、1種以上の非概日(non-circadian)有糸分裂遅延物質を含む組成物は知られていない。
【0026】
DNA修復用の局所組成物
細胞修復過程を促進するために皮膚に適用する局所製品は知られている。例えば、そうした製品は、自然の細胞DNA修復の有効性を向上させるためのDNA修復酵素、ケラチノサイト水和を維持するための保水剤成分、皮膚のバリア機能を改善するための保湿成分などを含むことができる。これらの成分はケラチノサイトの自己修復能を改善するかもしれないが、改善の余地は常にあるものである。従来技術とは対照的に、本発明は、損傷DNAが娘細胞に伝わるのを阻止する手段と組み合わせた、皮膚細胞における無傷の概日タンパク質のレベルを復元する手段および概日遺伝子発現の通常のパターンを回復させる手段を提供する。
【発明の概要】
【0027】
発明の目的
本発明の目的は、下記の組成物を適用したとき、加速されたやり方で、皮膚細胞における概日タンパク質の通常のレベルを復元しかつ概日遺伝子発現の通常のパターンを回復させる、局所組成物を提供することである。
【0028】
本発明の目的は、clockおよびper1遺伝子発現をアップレギュレートすることによって、また、皮膚細胞の有糸分裂を遅らせることによって、光損傷および/または酸化的損傷を受けた皮膚を修復する、局所組成物を提供することである。
【0029】
本発明の目的は、損傷を受けた皮膚細胞DNAが増殖する機会を減らす、局所組成物を提供することである。
【0030】
本発明の目的は、環境攻撃、特にUV曝露によって損傷された皮膚細胞DNAが増殖する機会を減らす、局所組成物を提供することである。
【0031】
本発明のさらなる目的は、少なくとも1種のケラチノサイトclockまたはper1遺伝子活性化剤と、少なくとも1種の非概日の有糸分裂遅延物質と、場合により少なくとも1種のDNA修復酵素と、を含む皮膚処置用の組成物を提供することである。
【0032】
概要
上記のすべては、皮膚細胞の概日遺伝子発現をアップレギュレートする少なくとも1種の作用物質と、皮膚細胞の有糸分裂を遅らせる少なくとも1種の非概日作用物質とを含む局所組成物によって達成される。clock遺伝子およびper1遺伝子をアップレギュレートする(または活性化する)一方で、SIRT1のレベルをも増加させる作用物質を含む組成物は、相乗的に、細胞の生存、細胞の寿命を促進し、環境攻撃による細胞損傷を抑制し、DNA損傷の修復を改善し、かつ損傷を受けた皮膚細胞DNAが増殖する機会を相乗的に減らすことが見いだされた。場合により、前記組成物は1種以上のDNA修復酵素を含有する。
【0033】
本発明の好ましい実施形態は、上記の効果を示す局所皮膚組成物である。好ましくは、前記組成物は、1種以上のケラチノサイトclockおよびper1遺伝子活性化剤を、SIRT1または1種以上のsirt1活性化剤と共に、含んでなる。好ましくは、前記組成物は使いやすく、効果があり、化粧品的に許容され、化学的に、熱力学的におよび光に安定であり、局所使用に安全であり、副作用がほとんどまたは全くなく、また、パーソナルケア市場で商業的に実現可能なものである。
【図面の簡単な説明】
【0034】
【図1】UV曝露後72時間にわたる、ヒトケラチノサイトにおけるclock、bmal1およびper1遺伝子発現のレベルを示す。
【図2】ヒトケラチノサイトの生存に及ぼす、sirt1活性化剤であるOrsirtine(商標)とレスベラトロールの効果を示す。
【図3】sirt1活性化剤であるOrsirtine(商標)およびレスベラトロールと組み合わせた、概日遺伝子活性化剤の効果を示す。
【発明を実施するための形態】
【0035】
詳細な説明
本出願人の知る限りでは、通常の概日周期を回復させるための概日遺伝子活性化剤の局所適用と共同した、細胞周期の停止を促進するためのsirt1活性化剤を含む局所組成物の使用は、これまで記載されたことがない。
【0036】
定義
本明細書に記載されるすべてのパーセンテージは、特に断らない限り、重量パーセントである。遺伝子に関連して、「活性化する」および「アップレギュレートする」または語源的に関連のある用語は、遺伝子によってコードされる1種以上のタンパク質の発現を引き出す成分を意味する。
【0037】
用語「時計遺伝子」は、clock、bmal1、period、およびcryptochrome遺伝子を含む、いわゆる「カノニカル」概日遺伝子のいずれかをさすために、文献中で用いられることがある。本明細書中で、「clock」(イタリック体で)は常にCLOCKタンパク質をコードする遺伝子をさす。まとめて、本明細書中では遺伝子clock、bmal1、period、およびcryptochromeを「概日遺伝子」(circadian genes)と呼ぶ。
【0038】
用語「DNA修復酵素」は、DNAの塩基変異原性損傷を修復することができる酵素を意味する。そうした酵素はしばしばそれらが修復するDNA損傷のタイプごとに分類される。例えば、BER (塩基除去修復)酵素、ヌクレオチド除去修復(NER)酵素;ミスマッチ修復(MMR)酵素;DNAヘリカーゼ;DNAポリメラーゼなど。例えば、8-オキソ-7,8-ジヒドロ-2'-デオキシグアノシンなどの変異はOGG1 (8-オキソグアニングリコシラーゼ)によって修復される。T-Tダイマーはヌクレオチド除去修復酵素フォトリアーゼ(Photolyase)によって修復される。6-4光産物はNERによって修復される。06-メチルグアニンは06-アルキルグアニントランスフェラーゼ(AGT)によって修復される。
【0039】
皮膚または皮膚細胞に関して、「修復」とは、ケラチノサイトの生存能力、強度、および寿命が一般的に改善されることを意味する。修復の例としては、損傷したケラチノサイトDNAを修復すること、およびUV光、タバコの煙または他の環境攻撃による細胞水和の損失を回復させることが含まれる。
【0040】
「局所使用に安全」とは、化粧品の安全性を管理するあらゆる地域および地方の規制に従うことを意味する。「化粧品的に許容される」とは、当業者には理解されるように、組成物の外観、感触および香りが消費者の受容性の範囲内であることを意味する。「化学的に安定」、「熱力学的に安定」および「光に安定」とは、製造から少なくとも6ヶ月間(より好ましくは3年間)、組成物が化粧品的に許容される状態にあることを意味する。「パーソナルケア市場で商業的に実現可能」とは、組成物の製造および流通コストがパーソナルケア業界ですでに経験しているコストより高くならないことを意味する。
【0041】
clockおよびperiod1のアップレギュレーション
本発明の組成物は、clockおよび/またはper1ケラチノサイト遺伝子をアップレギュレートする少なくとも1種の作用物質を含有する。これらの作用物質の推奨濃度は、合計で、最終組成物の全重量に対して、約0.000001〜約40%、好ましくは約0.000005〜35%、より好ましくは約0.00001〜25%の範囲である。一般的に、これらの範囲は有効量であると理解される。「有効量」とは、環境攻撃のもとでヒト皮膚に適用される局所組成物中のこれらの作用物質の濃度がケラチノサイトの生存率を5%以上改善するのに十分であることを意味する。適当なclockまたはper1活性化剤は、植物エキス、ポリペプチド、ペプチド、アミノ酸などの形態で存在し得る。
【0042】
特に好ましいclockおよび/またはper1遺伝子活性化剤は、式(I)のペプチドを含む:
R1-(AA)n-X1-S-T-P-X2-(AA)p-R2
式中、(AA)n-X1-S-T-P-X2-(AA)pは(配列番号1)であり、そして
X1は、トレオニンまたはセリンを表すか、ゼロに等しく、
X2は、イソロイシンまたはロイシンまたはプロリンまたはバリンまたはアラニンまたはグリシンを表すか、ゼロに等しく、
AAは、任意のアミノ酸またはその誘導体を表し、nおよびpは0〜4の整数であり(0と4を含める)、
R1は、N末端アミノ酸の1級アミン官能基を表し、そのアミン官能基は遊離であるか、アセチル基、ベンゾイル基、トシル基、またはベンジルオキシカルボニル基から選択できる保護基で置換されており、
R2は、C末端アミノ酸のカルボキシル官能基のヒドロキシル基を表し、そのヒドロキシル基はC1-C20アルキル鎖またはNH2、NHY、もしくはNYY基(ここで、YはC1-C4アルキル鎖を表す)から選択できる保護基で置換されており、
そして、一般式(I)の配列は約3〜13個のアミノ酸残基から構成される。
【0043】
一般式(I)の配列は、アミノ酸X1およびX2の、他の化学的に等価なアミノ酸による置換を含むことができ、ここで、そのアミノ酸は以下のものである:アラニン(A)、アルギニン(R)、アスパラギン(N)、アスパラギン酸(D)、システイン(C)、グルタミン酸(E)、グルタミン(Q)、グリシン(G)、ヒスチジン(H)、イソロイシン(I)、ロイシン(L)、リシン(K)、メチオニン(M)、フェニルアラニン(F)、プロリン(P)、セリン(S)、トレオニン(T)、トリプトファン(W)、チロシン(Y)およびバリン(V)。
【0044】
式(I)のより好ましい配列は、以下のようなペプチドである:
(配列番号2) Y-V-S-T-P-Y-N-NH2
Tyr-Val-Ser-Thr-Pro-Tyr-Asn-NH2
(配列番号3) NH2-V-S-T-P-E-NH2
NH2-Val-Ser-Thr-Pro-Glu-NH2
S-T-P-NH2
Ser-Thr-Pro-NH2
(配列番号4) NH2-L-H-S-T-P-P-NH2
NH2-Leu-His-Ser-Thr-Pro-Pro-NH2
(配列番号5) CH3NH-R-H-S-T-P-E-NH2
CH3-NH-Arg-His-Ser-Thr-Pro-Glu-NH2
(配列番号6) CH3NH-H-S-T-P-E-CH3NH
CH3-NH-His-Ser-Thr-Pro-Glu-CH3-NH
【0045】
より好ましいものは、S-T-P-NH2ペプチド、配列番号4、またはそれらの混合物である。最も好ましいものは、ISP-Vinscience社により製造されたChronolux(登録商標)という商標名のペプチド(Tripeptide-32のINCI名をもつ)である。
【0046】
関連出願US12/367,705の図1、2および3、ならびにこれらの図面を説明する本文には、少なくとも1種のDNA修復酵素と組み合わせた場合に特に、UV誘発ストレスに対するケラチノサイトの生存率を改善するChronolux(登録商標)の能力が示されている。
【0047】
clockおよびper1遺伝子活性化剤を同時に適用することが有益な結果を生み出すであろうということは、直ちには明白でない。結局のところ、通常の概日リズムでは、CLOCKおよびPeriod1タンパク質の細胞内濃度は位相を異にする。それにもかかわらず、有益な結果が達成される。環境攻撃を受けている皮膚細胞はCLOCKおよびPERIOD1タンパク質のレベルが激減するので、両タンパク質を可能な限り速やかにアップレギュレートすることによって効果が得られると考えられる。
【0048】
サーチュイン1のアップレギュレーション
本発明者らは、予期せざることに、clockおよびper1遺伝子活性化剤の適用により得られる有益な結果が、ケラチノサイトsirt1活性化剤と組み合わせたときに改善され、時には大幅に改善される、ことを見いだした。SIRT1は細胞周期の停止を誘導する傾向がある。概日機構の複雑さおよび細胞周期とのその調節相互作用を考えると、概日タンパク質の通常のレベルを復元すると同時に、細胞周期の停止を誘導することが有益であろうとは、従来技術から予想されなかったことである。
【0049】
いずれの理論にも拘束されることを望まないが、PER1は、24時間周期の監視を介すること以外に、細胞周期に直接的な効果を及ぼすことが理解されるだろう。例えば、PER1は、概日周期のコア成分としてのその役割のほかに、細胞周期の停止につながるATMキナーゼ経路を活性化できると報告されている。ATM(血管拡張性失調症変異型)キナーゼは、DNA二本鎖切断に応答して動員される核タンパク質キナーゼである。ATMキナーゼは、細胞周期の停止および有糸分裂への進入遅延に関与する、細胞周期チェックポイント調節因子CHK1およびCHK2をリン酸化する。PER1が何らかの環境ストレスの結果として過小発現されると、細胞周期の停止が起こらなかったり、遅れたりすることがある。したがって、有糸分裂または細胞質分裂の前に、損傷DNAの修復を行うのに十分な時間がない可能性がある。それと同時に、PER1の発現低下はアポトーシスの減少とも関連している。こうして、死滅するはずの損傷細胞が生き残って、分裂することがある。したがって、環境ストレスがPER1のレベルの異常な減少(細胞周期を停止させることができず、かつ損傷DNAの伝播につながるアポトーシスの減少をもたらす)をまねくと考えると、per1活性化がこの問題を解決しうると期待するかもしれない。それにもかかわらず、本発明者らは、sirt1遺伝子活性化剤をclockおよびper1遺伝子活性化剤と組み合わせて用いるとき、ケラチノサイトの生存率が大幅に改善されることを観察した。いずれの理論にも拘束されることを望まないが、この観察は、損傷DNAが娘細胞に伝えられる前に修復を行うのに十分な速度で、per1単独での活性化がPER1のレベルを復元できない、ことを暗に示している。
【0050】
「SIRT1活性化剤」とは、SIRT1タンパク質の内因性生産をサポートする可能性がある任意の化合物、特にDNAまたはRNAなどの前駆体の正の制御に関与する分子、を意味する。皮膚細胞におけるSIRT1タンパク質の合成を活性化する可能性があるこうした化合物の中で、ポリフェノールなど、さまざまな分子が記載されている。より具体的には、trans-スチルベンの誘導体(例えば、レスベラトロール、ピセアタンノール)、カルコン類の誘導体(例えば、イソリキリチゲニン、ブテイン)、およびフラボン類の誘導体(例えば、フィステイン(fistein)、ルテオリン、クェルセチン)が挙げられる。少なくとも1種のDNA修復酵素と組み合わせた、レスベラトロールまたはレスベラトロール誘導体の有効性は、関連出願US 11/837,658に示されている。しかし、特定のペプチドは、皮膚のペプチドへのそれらの固有の構造類似性のため、好ましいsirt1活性化剤である。よりいっそう好ましいものは、1種以上のペプチド性活性化剤とレスベラトロールの相乗的組合せである(これについては、以下参照)。
【0051】
ペプチド性sirt1活性化剤
ペプチドは、皮膚のペプチドへのそれらの固有の構造類似性のため、好ましいsirt1活性化剤である。ペプチド性の化合物の中で、タンパク質断片、ペプチドおよびポリペプチドの断片、ペプチド、ならびにペプチド結合で一緒に連結された2個以上のアミノ酸の全ての配列を挙げることができる。本発明の好ましい実施形態において、ペプチド断片は大きさが3〜50アミノ酸、より好ましくは3〜10アミノ酸の範囲である。これらのペプチド断片の全ては生物学的活性をもつものである。好ましいペプチドは以下のものである:
(配列番号7) (AA)n-G-L-Y-D-N-L-E-(AA)n
(AA)n-Gly-Leu-Tyr-Asp-Asn-Leu-Glu-(AA)n
式中、(AA)は任意の特定のアミノ酸またはその誘導体であり、nは0〜3の整数である(0と3を含める)。特に好ましいペプチドは以下のものである:
(配列番号8) G-L-Y-D-N-L-E
Gly-Leu-Tyr-Asp-Asn-Leu-Glu
このペプチドは、ISP Vincience社からOrsirtine(商標)GL (INCI名:Water (and) Glycerin (and) Oryza Sativa (Rice) Extract)として入手可能である。本発明の組成物において、ペプチド性SIRT1活性化剤は、最終組成物の全重量に対して、約0.000001%〜20%、好ましくは約0.0001〜5%の量で存在する。
【0052】
レスベラトロールおよびその誘導体
レスベラトロールは、別名を3,5,4'-トリヒドロキシスチルベンともいい、赤ブドウ、ラズベリー、ブルーベリー、および他の特定の植物ベリー類または抽出物中に存在するポリヒドロキシ置換スチルベン化合物であって、以下の一般式を有する:
【化1】

【0053】
レスベラトロールは効果的な抗酸化物質であることがわかっており、また、強力な抗増殖および抗炎症作用を示す。最近、レスベラトロールは、酵母、回虫、ミバエ、短命の魚、およびマウスなど、さまざまな生物においてカロリー制限(CR)を模倣し、こうした生物の老化プロセスを遅らせ、かつそれらの寿命を大幅に引き延ばすことが報告された。どのような特定の理論にも拘束されることを望まないが、本発明者らは、レスベラトロールが細胞増殖を低下させ、かつアポトーシス過程を減速させ、それによって細胞でのDNA損傷の修復のためのより多くの時間を可能にする、と考えている。レスベラトロールは、DNA修復酵素と組み合わせたとき、細胞の自然なDNA修復能をブーストするかまたは他の方法で高める上で相乗効果をもたらすと予想される。
【0054】
しかし、レスベラトロールは特定の化粧品製剤中で潜在的に不安定なことがある。具体的には、レスベラトロールは水性ベースの製剤中で加水分解を受けやすく、また、そうした製剤を変色させる可能性がある。水性ベースの製剤中でのレスベラトロールの不安定性に対処する1つの方法は、化粧品製剤中でより安定なレスベラトロール誘導体を形成するために、3、5および4'位のヒドロキシ基を他の官能基で置換することによってレスベラトロールを修飾することである。そのような誘導体はレスベラトロールより好適である。無機酸、有機カルボン酸、モノ-、ジ-もしくはポリサッカライド、または他の官能基のレスベラトロール誘導体は水性ベースの製剤中でより安定であることが見いだされた。置換基はレスベラトロールのフェノール基を保護しかつ安定化するように機能し、水性ベースの化粧品製剤中で使用するのにレスベラトロール誘導体をより適したものにする。置換基はまた、皮膚への適用時にその化合物から、好ましくは皮膚表面上の酵素および他の成分によって、容易に加水分解されて、皮膚にレスベラトロールの活性形態を放出し得る。本発明のレスベラトロール誘導体は以下の一般式を有する:
【化2】

【0055】
式中、X、YおよびZは水素または保護基のいずれかであるが、X、YおよびZの少なくとも1つは保護基であることを条件とする。本発明の化粧料または局所組成物中で使用するのに適した代表的なレスベラトロール誘導体については、以下でより詳細に説明する。
【0056】
A. 無機または有機酸のレスベラトロールエステル
無機酸のレスベラトロールエステル[上記式中、X、YおよびZの1つ以上がホスフェート、ニトレート、スルホネートおよびカーボネートなどの無機酸の官能基である]は本発明で使用することができる。以下は、本発明の実施に特に適している代表的な無機酸エステルのリストである:
3-ホスフェート-5,4'-ジヒドロキシスチルベン
5-ホスフェート-3,4'-ジヒドロキシスチルベン
4'-ホスフェート-3,5-ジヒドロキシスチルベン
3,5-ジホスフェート-4'-ヒドロキシスチルベン
3,4'-ジホスフェート-5-ヒドロキシスチルベン
4',5-ジホスフェート-3-ヒドロキシスチルベン
3,5,4'-トリホスフェートスチルベン
3-ニトレート-5,4'-ジヒドロキシスチルベン
5-ニトレート-3,4'-ジヒドロキシスチルベン
4'-ニトレート-3,5-ジヒドロキシスチルベン
3,5-ジニトレート-4'-ヒドロキシスチルベン
3,4'-ジニトレート-5-ヒドロキシスチルベン
4',5-ジニトレート-3-ヒドロキシスチルベン
3,5,4'-トリニトレートスチルベン
3-スルホネート-5,4'-ジヒドロキシスチルベン
5-スルホネート-3,4'-ジヒドロキシスチルベン
4'-スルホネート-3,5-ジヒドロキシスチルベン
3,5-ジスルホネート-4'-ヒドロキシスチルベン
3,4'-ジスルホネート-5-ヒドロキシスチルベン
4',5-ジスルホネート-3-ヒドロキシスチルベン
3,5,4'-トリスルホネートスチルベン
3-カーボネート-5,4'-ジヒドロキシスチルベン
5-カーボネート-3,4'-ジヒドロキシスチルベン
4'-カーボネート-3,5-ジヒドロキシスチルベン
3,5-ジカーボネート-4'-ヒドロキシスチルベン
3,4'-ジカーボネート-5-ヒドロキシスチルベン
4',5-ジカーボネート-3-ヒドロキシスチルベン
3,5,4'-トリカーボネートスチルベン。
【0057】
上に挙げたレスベラトロールエステルの薬学的に許容される塩も本発明の化粧料組成物中で使用することができる。そうした塩はNa、K、Mg、Ca、Fe、およびNH4からなる群より選択される1つ以上の1価または2価陽イオンを含む。塩は、水酸化ナトリウム、水酸化カリウムなどの対応する塩基を、レスベラトロールエステルを含有する溶液に添加することによって形成される。
【0058】
レスベラトロールの無機酸エステルは、フェノールまたはポリフェノールのヒドロキシル基をホスフェート、スルホネートまたはカーボネート官能基で置換する周知の化学的方法によって容易に形成することができる。例えば、米国特許第4003966号は、フェノール類を選択的にリン酸化してそのリン酸エステルを形成するワンステップ法を記載しており、あらゆる目的のためにその全内容を参照により本明細書に組み入れる。
【0059】
本発明の実施に特に好ましいレスベラトロール誘導体は、以下の式を有する3,4',5-トリホスフェートスチルベン(別名をレスベラトロール3リン酸エステルともいう)である:
【化3】

【0060】
レスベラトロール3リン酸を含めて、レスベラトロールのリン酸エステルは、国際特許出願公開公報WO 2006/029484A1に開示されており、その全内容を参照により本明細書に組み入れる。レスベラトロール3リン酸はWO 2006/029484A1の実施例2に記載の方法により合成することができる。より具体的には、100mlのアセトニトリルに溶解したレスベラトロール(3,4,5-トリヒドロキシスチルベン)(25mmols, 5.7g)とジメチルアミノピリジン(7.5mmols, 0.93g)の溶液を窒素下に−10℃まで冷却する。10分後、四塩化炭素(375mmol, 36.2ml)とDIEA (159mmol, 27.7ml)を加え、この混合物を撹拌しながら30分間維持する。ジベンジルホスフェート(113mmols, 25.0ml)を加え、この混合物を室温でさらに12時間撹拌する。反応の経過をTLC(シリカF254、溶離剤:酢酸エチル/n-ヘキサン80/20 v/v)でモニタリングする。1リットルの0.5M KH2PO4を加え、その後この混合物を酢酸エチルで抽出する。得られた生成物のトリ(ジベンジルホスフェート)レスベラトロールをシリカゲルでろ過し、最初に酢酸エチル/n-ヘキサン(80/20 v/v)の混合溶媒で洗浄して、残存する未反応のレスベラトロールを除き、次にメタノールで洗浄して精製すると、黄色のオイルが得られる。
【0061】
0℃の無水DCM 200mL中のトリ(ジベンジルホスフェート)レスベラトロール(12.5mmol)に、ブロモメチルシラン(79mmols, 10.4mL)を添加する。2時間後、300mLのH2Oを加え、その反応混合物を1時間撹拌する。水相を酢酸エチルで再度洗浄し、その後凍結乾燥すると、オレンジ色のオイルが得られる。
【0062】
400mLのエタノール中に可溶化した、上で得られた生成物に、CH3ONa (37mmol; 2.03g)を加えて、その反応を室温で12時間撹拌する。エタノールをrotavaporエバポレータで蒸発させ、残留物をH2O中に可溶化する。水相を酢酸エチルで洗浄して凍結乾燥させる。得られた白色固体の質量スペクトルは、レスベラトロール3リン酸(PM=468.1)の存在を示し、レスベラトロールに対する総収率>90%を有する。
【0063】
必要ならば、レスベラトロール3リン酸を水酸化ナトリウム、水酸化カリウムなどの無機または有機塩基で中和してもよい。特に好ましいのは、レスベラトロール3リン酸を水酸化ナトリウムで中和してレスベラトロール3リン酸3ナトリウムを形成する場合である。レスベラトロール3リン酸はまた、レスベラトロール3リン酸3ナトリウム(trisodium resveratrol triphosphate)のCTFA名を有し、中和された形で味の素社から購入することができる。
【0064】
B. レスベラトロールのカルボン酸エステル
本発明で使用できるレスベラトロール誘導体の別のグループは、レスベラトロールと脂肪族または芳香族カルボン酸とのエステル[上記式中、X、YおよびZの1つ以上が-C(O)-R1基であり、ここでR1は、直鎖、分岐鎖、飽和もしくは不飽和、または環状のC1-C40アルキル、置換C1-C40アルキル、C1-C40アルケニル、置換C1-C40アルケニル、C1-C40アルキニル、置換C1-C40アルキニル、アリール、C1-C40アリール、およびC1-C40置換アリールからなる群より選択される]である。好ましい一実施形態では、R1基が直鎖または分岐鎖の脂肪族の(fatty)、つまりC6-30の、飽和または不飽和アルキル基である。置換基はC1-40直鎖または分岐鎖、飽和または不飽和アルキル、ハロゲン(例えばフルオロ)、水素、アルコキシ、ヒドロキシルなどから選択される。
【0065】
レスベラトロールのエステルを形成するために使用できるカルボン酸の例としては、限定するものではないが、以下のものが挙げられる:飽和モノカルボン酸、例えば、酢酸、プロピオン酸、酪酸(C4)、バレリアン酸、ヘキサン酸、カプリル酸(C8)、ラウリン酸、ステアリン酸(C18)、イソステアリン酸(分岐C18)、リノール酸、リノレン酸、ミリスチン酸(C14)、アラキジン酸(C20)、アラキドン酸、エルカ酸、ベヘン酸(C22)、ラウリン酸(C12)、カプリン酸(C10)、カプロン酸(C6)、およびパルミチン酸(C16); 不飽和モノカルボン酸、例えば、アクリル酸、メタクリル酸、ソルビン酸、オレイン酸、リノール酸、リノレン酸、ドコサヘキサエン酸、およびエイコサペンタエン酸; アミノ酸、例えば、アルギニン、グルタミン、およびチロシン; ケト酸、例えば、ピルビン酸、およびアセト酢酸; 芳香族カルボン酸、例えば、アスコルビン酸、安息香酸、サリチル酸、およびフェルラ酸; ジ-およびトリ-カルボン酸、例えば、シュウ酸、マロン酸、リンゴ酸、コハク酸、およびグルタル酸。記号「C」の後の数字は、アルキル鎖中の炭素原子の数を示す。
【0066】
本発明の実施に特に適している代表的なレスベラトロールのカルボン酸エステルのリストは以下のとおりである:
3-アセテート-5,4'-ジヒドロキシスチルベン
5-アセテート-3,4'-ジヒドロキシスチルベン
4'-アセテート-3,5-ジヒドロキシスチルベン
3,5-ジアセテート-4'-ヒドロキシスチルベン
3,4'-ジアセテート-5-ヒドロキシスチルベン
4',5-ジアセテート-3-ヒドロキシスチルベン
3,5,4'-トリアセテートスチルベン
3-プロピオネート-5,4'-ジヒドロキシスチルベン
5-プロピオネート-3,4'-ジヒドロキシスチルベン
4'-プロピオネート-3,5-ジヒドロキシスチルベン
3,5-ジプロピオネート-4'-ヒドロキシスチルベン
3,4'-ジプロピオネート-5-ヒドロキシスチルベン
4',5-ジプロピオネート-3-ヒドロキシスチルベン
3,5,4'-トリプロピオネートスチルベン
3-ブチレート-5,4'-ジヒドロキシスチルベン
5-ブチレート-3,4'-ジヒドロキシスチルベン
4'-ブチレート-3,5-ジヒドロキシスチルベン
3,5-ジブチレート-4'-ヒドロキシスチルベン
3,4'-ジブチレート-5-ヒドロキシスチルベン
4',5-ジブチレート-3-ヒドロキシスチルベン
3,5,4'-トリブチレートスチルベン
3-バレレート-5,4'-ジヒドロキシスチルベン
5-バレレート-3,4'-ジヒドロキシスチルベン
4'-バレレート-3,5-ジヒドロキシスチルベン
3,5-ジバレレート-4'-ヒドロキシスチルベン
3,4'-ジバレレート-5-ヒドロキシスチルベン
4',5-ジバレレート-3-ヒドロキシスチルベン
3,5,4'-トリバレレートスチルベン
3-ヘキサノエート-5,4'-ジヒドロキシスチルベン
5-ヘキサノエート-3,4'-ジヒドロキシスチルベン
4'-ヘキサノエート-3,5-ジヒドロキシスチルベン
3,5-ジヘキサノエート-4'-ヒドロキシスチルベン
3,4'-ジヘキサノエート-5-ヒドロキシスチルベン
4',5-ジヘキサノエート-3-ヒドロキシスチルベン
3,5,4'-トリヘキサノエートスチルベン
3-カプリレート-5,4'-ジヒドロキシスチルベン
5-カプリレート-3,4'-ジヒドロキシスチルベン
4'-カプリレート-3,5-ジヒドロキシスチルベン
3,5-ジカプリレート-4'-ヒドロキシスチルベン
3,4'-ジカプリレート-5-ヒドロキシスチルベン
4',5-ジカプリレート-3-ヒドロキシスチルベン
3,5,4'-トリカプリレートスチルベン
3-ラウレート-5,4'-ジヒドロキシスチルベン
5-ラウレート-3,4'-ジヒドロキシスチルベン
4'-ラウレート-3,5-ジヒドロキシスチルベン
3,5-ジラウレート-4'-ヒドロキシスチルベン
3,4'-ジラウレート-5-ヒドロキシスチルベン
4',5-ジラウレート-3-ヒドロキシスチルベン
3,5,4'-トリラウレートスチルベン
3-ステアレート-5,4'-ジヒドロキシスチルベン
5-ステアレート-3,4'-ジヒドロキシスチルベン
4'-ステアレート-3,5-ジヒドロキシスチルベン
3,5-ジステアレート-4'-ヒドロキシスチルベン
3,4'-ジステアレート-5-ヒドロキシスチルベン
4',5-ジステアレート-3-ヒドロキシスチルベン
3,5,4'-トリステアレートスチルベン
3-パルミテート-5,4'-ジヒドロキシスチルベン
5-パルミテート-3,4'-ジヒドロキシスチルベン
4'-パルミテート-3,5-ジヒドロキシスチルベン
3,5-ジパルミテート-4'-ヒドロキシスチルベン
3,4'-ジパルミテート-5-ヒドロキシスチルベン
4',5-ジパルミテート-3-ヒドロキシスチルベン
3,5,4'-トリパルミテートスチルベン
3-アクリレート-5,4'-ジヒドロキシスチルベン
5-アクリレート-3,4'-ジヒドロキシスチルベン
4'-アクリレート-3,5-ジヒドロキシスチルベン
3,5-ジアクリレート-4'-ヒドロキシスチルベン
3,4'-ジアクリレート-5-ヒドロキシスチルベン
4',5-ジアクリレート-3-ヒドロキシスチルベン
3,5,4'-トリアクリレートスチルベン
3-メタクリレート-5,4'-ジヒドロキシスチルベン
5-メタクリレート-3,4'-ジヒドロキシスチルベン
4'-メタクリレート-3,5-ジヒドロキシスチルベン
3,5-ジメタクリレート-4'-ヒドロキシスチルベン
3,4'-ジメタクリレート-5-ヒドロキシスチルベン
4',5-ジメタクリレート-3-ヒドロキシスチルベン
3,5,4'-トリメタクリレートスチルベン
3-ソルベート-5,4'-ジヒドロキシスチルベン
5-ソルベート-3,4'-ジヒドロキシスチルベン
4'-ソルベート-3,5-ジヒドロキシスチルベン
3,5-ジソルベート-4'-ヒドロキシスチルベン
3,4'-ジソルベート-5-ヒドロキシスチルベン
4',5-ジソルベート-3-ヒドロキシスチルベン
3,5,4'-トリソルベートスチルベン
3-オレエート-5,4'-ジヒドロキシスチルベン
5-オレエート-3,4'-ジヒドロキシスチルベン
4'-オレエート-3,5-ジヒドロキシスチルベン
3,5-ジオレエート-4'-ヒドロキシスチルベン
3,4'-ジオレエート-5-ヒドロキシスチルベン
4',5-ジオレエート-3-ヒドロキシスチルベン
3,5,4'-トリオレエートスチルベン
3-リノレート-5,4'-ジヒドロキシスチルベン
5-リノレート-3,4'-ジヒドロキシスチルベン
4'-リノレート-3,5-ジヒドロキシスチルベン
3,5-ジリノレート-4'-ヒドロキシスチルベン
3,4'-ジリノレート-5-ヒドロキシスチルベン
4',5-ジリノレート-3-ヒドロキシスチルベン
3,5,4'-トリリノレートスチルベン
3-リノレネート-5,4'-ジヒドロキシスチルベン
5-リノレネート-3,4'-ジヒドロキシスチルベン
4'-リノレネート-3,5-ジヒドロキシスチルベン
3,5-ジリノレネート-4'-ヒドロキシスチルベン
3,4'-ジリノレネート-5-ヒドロキシスチルベン
4',5-ジリノレネート-3-ヒドロキシスチルベン
3,5,4'-トリリノレネートスチルベン
3-ドコサヘキサノエート-5,4'-ジヒドロキシスチルベン
5-ドコサヘキサノエート-3,4'-ジヒドロキシスチルベン
4'-ドコサヘキサノエート-3,5-ジヒドロキシスチルベン
3,5-ジドコサヘキサノエート-4'-ヒドロキシスチルベン
3,4'-ジドコサヘキサノエート-5-ヒドロキシスチルベン
4',5-ジドコサヘキサノエート-3-ヒドロキシスチルベン
3,5,4'-トリドコサヘキサノエートスチルベン
3-エイコサペンタエノイック-5,4'-ジヒドロキシスチルベン
5-エイコサペンタエノイック-3,4'-ジヒドロキシスチルベン
4'-エイコサペンタエノイック-3,5-ジヒドロキシスチルベン
3,5-ジエイコサペンタエノイック-4'-ヒドロキシスチルベン
3,4'-ジエイコサペンタエノイック-5-ヒドロキシスチルベン
4',5-ジエイコサペンタエノイック-3-ヒドロキシスチルベン
3,5,4'-トリエイコサペンタエノイックスチルベン
3-アルギネート-5,4'-ジヒドロキシスチルベン
5-アルギネート-3,4'-ジヒドロキシスチルベン
4'-アルギネート-3,5-ジヒドロキシスチルベン
3,5-ジアルギネート-4'-ヒドロキシスチルベン
3,4'-ジアルギネート-5-ヒドロキシスチルベン
4',5-ジアルギネート-3-ヒドロキシスチルベン
3,5,4'-トリアルギネートスチルベン
3-グルタメート-5,4'-ジヒドロキシスチルベン
5-グルタメート-3,4'-ジヒドロキシスチルベン
4'-グルタメート-3,5-ジヒドロキシスチルベン
3,5-ジグルタメート-4'-ヒドロキシスチルベン
3,4'-ジグルタメート-5-ヒドロキシスチルベン
4',5-ジグルタメート-3-ヒドロキシスチルベン
3,5,4'-トリグルタメートスチルベン
3-チロセート-5,4'-ジヒドロキシスチルベン
5-チロセート-3,4'-ジヒドロキシスチルベン
4'-チロセート-3,5-ジヒドロキシスチルベン
3,5-ジチロセート-4'-ヒドロキシスチルベン
3,4'-ジチロセート-5-ヒドロキシスチルベン
4',5-ジチロセート-3-ヒドロキシスチルベン
3,5,4'-トリチロセートスチルベン
3-ピルベート-5,4'-ジヒドロキシスチルベン
5-ピルベート-3,4'-ジヒドロキシスチルベン
4'-ピルベート-3,5-ジヒドロキシスチルベン
3,5-ジピルベート-4'-ヒドロキシスチルベン
3,4'-ジピルベート-5-ヒドロキシスチルベン
4',5-ジピルベート-3-ヒドロキシスチルベン
3,5,4'-トリピルベートスチルベン
3-アセトアセテート-5,4'-ジヒドロキシスチルベン
5-アセトアセテート-3,4'-ジヒドロキシスチルベン
4'-アセトアセテート-3,5-ジヒドロキシスチルベン
3,5-ジアセトアセテート-4'-ヒドロキシスチルベン
3,4'-ジアセトアセテート-5-ヒドロキシスチルベン
4',5-ジアセトアセテート-3-ヒドロキシスチルベン
3,5,4'-トリアセトアセテートスチルベン
3-アスコルベート-5,4'-ジヒドロキシスチルベン
5-アスコルベート-3,4'-ジヒドロキシスチルベン
4'-アスコルベート-3,5-ジヒドロキシスチルベン
3,5-ジアスコルベート-4'-ヒドロキシスチルベン
3,4'-ジアスコルベート-5-ヒドロキシスチルベン
4',5-ジアスコルベート-3-ヒドロキシスチルベン
3,5,4'-トリアスコルベートスチルベン
3-ベンゾエート-5,4'-ジヒドロキシスチルベン
5-ベンゾエート-3,4'-ジヒドロキシスチルベン
4'-ベンゾエート-3,5-ジヒドロキシスチルベン
3,5-ジベンゾエート-4'-ヒドロキシスチルベン
3,4'-ジベンゾエート-5-ヒドロキシスチルベン
4',5-ジベンゾエート-3-ヒドロキシスチルベン
3,5,4'-トリベンゾエートスチルベン
3-サリチレート-5,4'-ジヒドロキシスチルベン
5-サリチレート-3,4'-ジヒドロキシスチルベン
4'-サリチレート-3,5-ジヒドロキシスチルベン
3,5-ジサリチレート-4'-ヒドロキシスチルベン
3,4'-ジサリチレート-5-ヒドロキシスチルベン
4',5-ジサリチレート-3-ヒドロキシスチルベン
3,5,4'-トリサリチレートスチルベン
3-フェルレート-5,4'-ジヒドロキシスチルベン
5-フェルレート-3,4'-ジヒドロキシスチルベン
4'-フェルレート-3,5-ジヒドロキシスチルベン
3,5-ジフェルレート-4'-ヒドロキシスチルベン
3,4'-ジフェルレート-5-ヒドロキシスチルベン
4',5-ジフェルレート-3-ヒドロキシスチルベン
3,5,4'-トリフェルレートスチルベン
3-オキサレート-5,4'-ジヒドロキシスチルベン
5-オキサレート-3,4'-ジヒドロキシスチルベン
4'-オキサレート-3,5-ジヒドロキシスチルベン
3,5-ジオキサレート-4'-ヒドロキシスチルベン
3,4'-ジオキサレート-5-ヒドロキシスチルベン
4',5-ジオキサレート-3-ヒドロキシスチルベン
3,5,4'-トリオキサレートスチルベン
3-マロネート-5,4'-ジヒドロキシスチルベン
5-マロネート-3,4'-ジヒドロキシスチルベン
4'-マロネート-3,5-ジヒドロキシスチルベン
3,5-ジマロネート-4'-ヒドロキシスチルベン
3,4'-ジマロネート-5-ヒドロキシスチルベン
4',5-ジマロネート-3-ヒドロキシスチルベン
3,5,4'-トリマロネートスチルベン
3-マレート-5,4'-ジヒドロキシスチルベン
5-マレート-3,4'-ジヒドロキシスチルベン
4'-マレート-3,5-ジヒドロキシスチルベン
3,5-ジマレート-4'-ヒドロキシスチルベン
3,4'-ジマレート-5-ヒドロキシスチルベン
4',5-ジマレート-3-ヒドロキシスチルベン
3,5,4'-トリマレートスチルベン
3-スクシネート-5,4'-ジヒドロキシスチルベン
5-スクシネート-3,4'-ジヒドロキシスチルベン
4'-スクシネート-3,5-ジヒドロキシスチルベン
3,5-ジスクシネート-4'-ヒドロキシスチルベン
3,4'-ジスクシネート-5-ヒドロキシスチルベン
4',5-ジスクシネート-3-ヒドロキシスチルベン
3,5,4'-トリスクシネートスチルベン
3-グルタレート-5,4'-ジヒドロキシスチルベン
5-グルタレート-3,4'-ジヒドロキシスチルベン
4'-グルタレート-3,5-ジヒドロキシスチルベン
3,5-ジグルタレート-4'-ヒドロキシスチルベン
3,4'-ジグルタレート-5-ヒドロキシスチルベン
4',5-ジグルタレート-3-ヒドロキシスチルベン
3,5,4'-トリグルタレートスチルベン
3-グルタレート-5,4'-ジヒドロキシスチルベン
5-グルタレート-3,4'-ジヒドロキシスチルベン
4'-グルタレート-3,5-ジヒドロキシスチルベン
3,5-ジグルタレート-4'-ヒドロキシスチルベン
3,4'-ジグルタレート-5-ヒドロキシスチルベン
4',5-ジグルタレート-3-ヒドロキシスチルベン
3,5,4'-トリグルタレートスチルベン。
【0067】
特に好ましいレスベラトロールのカルボン酸エステルのグループは、レスベラトロールの飽和または不飽和脂肪酸エステル、例えば、レスベラトロール酪酸エステル、レスベラトロールバレリアン酸エステル、レスベラトロールヘキサン酸エステル、レスベラトロールソルビン酸エステル、レスベラトロールラウリン酸エステル、レスベラトロールステアリン酸エステル、レスベラトロールパルミチン酸エステル、レスベラトロールオレイン酸エステル、レスベラトロールリノール酸エステル、レスベラトロールリノレン酸エステル、レスベラトロールエイコサペンタエン酸エステル、およびレスベラトロールドコサヘキサエン酸エステルである。このようなレスベラトロールの脂肪酸エステルは、米国特許第6,572,882号(あらゆる目的のために、その全内容を参照により本明細書に組み入れる)に記載されるように、アルカリ性水性媒体中でSchotten-Baumann反応に従ってレスベラトロールを酸誘導体でエステル化することにより、容易に形成することができる。
【0068】
特に好ましいレスベラトロールのカルボン酸エステルのもう一つのグループは、レスベラトロールの芳香族カルボン酸エステル、例えばレスベラトロールフェルラ酸エステルであり、このエステルは水性媒体中でレスベラトロールをフェルラ酸と反応させることによって形成される。
【0069】
C. レスベラトロールのエーテル誘導体
本発明で使用できるレスベラトロール誘導体のさらに別のグループは、レスベラトロールのエーテル[上記式中、X、YおよびZの1つ以上が-R2であり、ここでR2は、直鎖、分岐鎖または環状のC1-C40アルキル、置換C1-C40アルキル、C1-C40アルケニル、置換C1-C40アルケニル、C1-C40アルキニル、置換C1-C40アルキニル、C1-C40アリール、置換C1-C40アリール、ならびにモノ-、ジ-、オリゴ-およびポリサッカライドからなる群より選択される]である。本発明の実施に特に適している代表的なレスベラトロールエーテルのリストは以下のとおりである:
3-メトキシ-5,4'-ジヒドロキシスチルベン
5-メトキシ-3,4'-ジヒドロキシスチルベン
4'-メトキシ-3,5-ジヒドロキシスチルベン
3,5-ジメトキシ-4'-ヒドロキシスチルベン
3,4'-ジメトキシ-5-ヒドロキシスチルベン
4',5-ジメトキシ-3-ヒドロキシスチルベン
3,5,4'-トリメトキシスチルベン
3-エトキシ-5,4'-ジヒドロキシスチルベン
5-エトキシ-3,4'-ジヒドロキシスチルベン
4'-エトキシ-3,5-ジヒドロキシスチルベン
3,5-ジエトキシ-4'-ヒドロキシスチルベン
3,4'-ジエトキシ-5-ヒドロキシスチルベン
4',5-ジエトキシ-3-ヒドロキシスチルベン
3,5,4'-トリエトキシスチルベン
3-プロピルオキシ-5,4'-ジヒドロキシスチルベン
5-プロピルオキシ-3,4'-ジヒドロキシスチルベン
4'-プロピルオキシ-3,5-ジヒドロキシスチルベン
3,5-ジプロピルオキシ-4'-ヒドロキシスチルベン
3,4'-ジプロピルオキシ-5-ヒドロキシスチルベン
4',5-ジプロピルオキシ-3-ヒドロキシスチルベン
3,5,4'-トリプロピルオキシスチルベン
3-フェニルオキシ-5,4'-ジヒドロキシスチルベン
5-フェニルオキシ-3,4'-ジヒドロキシスチルベン
4'-フェニルオキシ-3,5-ジヒドロキシスチルベン
3,5-ジフェニルオキシ-4'-ヒドロキシスチルベン
3,4'-ジフェニルオキシ-5-ヒドロキシスチルベン
4',5-ジフェニルオキシ-3-ヒドロキシスチルベン
3,5,4'-トリフェニルオキシスチルベン
3-グルコシド-5,4'-ジヒドロキシスチルベン
5-グルコシド-3,4'-ジヒドロキシスチルベン
4'-グルコシド-3,5-ジヒドロキシスチルベン
3,5-ジグルコシド-4'-ヒドロキシスチルベン
3,4'-ジグルコシド-5-ヒドロキシスチルベン
4',5-ジグルコシド-3-ヒドロキシスチルベン
3,5,4'-トリグルコシドスチルベン。
【0070】
本発明の一つの具体的実施形態では、メトキシ置換されたレスベラトロール誘導体が用いられる。例えば、本発明の組成物は3,5-ジメトキシ-4'-ヒドロキシスチルベンを含むことができ、これはインドのキノ樹脂木(Indian Kino Tree)(プテロカルプス・マルスピウム(Pterocarpus marsupium))から抽出することができ、また、Sigma-Aldrich社(St. Louis, MO)からPTEROSTILBENEという商標名で販売されている。
【0071】
本発明の別の具体的実施形態では、レスベラトロール誘導体が1つ以上のサッカライド含有保護基、例えば、グルコース、ガラクトース、マンノース、フルクトース、スクロース、ラクトース、マルトース、トレハロースなどを含む。例えば、レスベラトロールグルコシドは、イタドリ(polygonum cuspidatum)組織などの植物もしくは植物材料またはブドウ(vitis vinifera)細胞のin vitro培養物からの抽出によって得られ、本発明の化粧料組成物中で用いられる。
【0072】
D. レスベラトロールの窒素含有誘導体
本発明の組成物で用いるレスベラトロール誘導体は1つ以上の窒素含有官能基を含むことができ、すなわち、上記式中のA、BおよびCの1つ以上がアミド、アミン、イミン、アミジン、およびカルボキシアミジンからなる群より選択される。本発明の実施に特に適している代表的なレスベラトロールエーテルのリストは以下のとおりである:
3-アミド-5,4'-ジヒドロキシスチルベン 5-アミド-3,4'-ジヒドロキシスチルベン
4'-アミド-3,5-ジヒドロキシスチルベン 3,5-ジアミド-4'-ヒドロキシスチルベン
3,4'-ジアミド-5-ヒドロキシスチルベン 4',5-ジアミド-3-ヒドロキシスチルベン
3,5,4'-トリアミドスチルベン 3-アミノ-5,4'-ジヒドロキシスチルベン
5-アミノ-3,4'-ジヒドロキシスチルベン 4'-アミノ-3,5-ジヒドロキシスチルベン
3,5-ジアミノ-4'-ヒドロキシスチルベン 3,4'-ジアミノ-5-ヒドロキシスチルベン
4',5-ジアミノ-3-ヒドロキシスチルベン 3,5,4'-トリアミノスチルベン
3-イミノ-5,4'-ジヒドロキシスチルベン 5-イミノ-3,4'-ジヒドロキシスチルベン
4'-イミノ-3,5-ジヒドロキシスチルベン 3,5-ジイミノ-4'-ヒドロキシスチルベン
3,4'-ジイミノ-5-ヒドロキシスチルベン 4',5-ジイミノ-3-ヒドロキシスチルベン
3,5,4'-トリイミノスチルベン 3-アミジノ-5,4'-ジヒドロキシスチルベン
5-アミジノ-3,4'-ジヒドロキシスチルベン 4'-アミジノ-3,5-ジヒドロキシスチルベン
3,5-ジアミジノ-4'-ヒドロキシスチルベン 3,4'-ジアミジノ-5-ヒドロキシスチルベン
4',5-ジアミジノ-3-ヒドロキシスチルベン 3,5,4'-トリアミジノスチルベン。
【0073】
好ましくは、しかし必ずしも必要ではないが、本発明のレスベラトロール誘導体は、皮膚の真皮へのより効果的な送達のために、単独で、あるいはDNA修復酵素および/または1種以上の追加のスキンケア活性剤と組み合わせて、リポソームにカプセル化される。レスベラトロール誘導体は、本発明の化粧料組成物中に、全組成物の全重量に対して、約0.001%〜約95%、好ましくは約0.005%〜約90%、より好ましくは約0.1%〜約20%の範囲の量で存在する。
【0074】
DNA修復酵素
本発明の組成物は、場合により少なくとも1種のDNA修復酵素を含んでもよい。これは、少なくとも1種のDNA修復酵素を必要としておりかつsirt1活性化剤の使用を意図していない、US 11/837,658とは違っている。任意成分であるDNA修復酵素の推奨濃度は、最終組成物の全重量に対して、約0.00001〜約35%、好ましくは約0.00005〜約30%、より好ましくは約0.0001〜約25%である。
【0075】
米国特許第5,077,211号; 第5,190,762号; 第5,272,079号; および第5,296,231号(これら全ての内容を参照により本明細書に組み入れる)に開示されるDNA修復酵素は、本発明の組成物および方法で用いるのに適している。そのようなDNA修復酵素の一例は、AGI/Dermatics社からRoxisomes(登録商標)という商標名で購入することができ、Arabidopsis Thaliana extract(シロイヌナズナエキス)のINCI名を有する。これは単独で、またはレシチンおよび水との混合物として存在しうる。このDNA修復酵素は、8-オキソ-ジグアニンの塩基変異損傷を修復するのに有効であることが知られている。
【0076】
使用できる別のタイプのDNA修復酵素は、06-メチルグアニン塩基変異損傷の修復に有効であることが知られているものである。これはAGI/Dermatics社からAdasomes(登録商標)という商標名で販売されており、Lactobacillus ferment(乳酸桿菌発酵液)のINCI名を有する。この酵素は単独で、またはレシチンおよび水と混合して、本発明の組成物に加えることができる。
【0077】
使用できる別のタイプのDNA修復酵素は、T-Tダイマーを修復するのに有効であることが知られているものである。こうした酵素は生物学的または植物学的物質の混合物中に存在する。そのような成分の例は、AGI/Dermatics社からUltrasomes(登録商標)またはPhotosomes(登録商標)という商標名で販売されている。Ultrasomes(登録商標)は、ミクロコッカス溶解液(さまざまなミクロコッカス菌種の制御された溶解の最終産物)、レシチンおよび水の混合物を含む。Photosomes(登録商標)は、プランクトンエキス(次の生物:海洋藻類、微小緑藻類、珪藻類、緑青藻類および窒素固定藻類のうち1種以上を含む海洋バイオマスのエキスである)、水およびレシチンの混合物を含む。
【0078】
別のタイプのDNA修復酵素は、さまざまな不活化細菌の溶解液、例えばビフィズス菌溶解液またはビフィズス菌発酵溶解液の成分であり、後者は、ビフィズス菌を培養し、不活化し、その後破壊したときの代謝産物と細胞質画分を含むビフィズス菌由来の溶解液である。この物質はBifida Ferment Lysate(ビフィズス菌発酵エキス)というINCI名を有する。
【0079】
他の適当なDNA修復酵素にはエンドヌクレアーゼVが含まれ、これはバクテリオファージT4のdenV遺伝子により産生される。さらに、以下の酵素も適している:T4エンドヌクレアーゼ; O6-メチルグアニン-DNAメチルトランスフェラーゼ; フォトリアーゼ、例えばウラシル-およびヒポキサンチン-DNAグリコシラーゼ; 脱ピリミジン/脱プリン部位エンドヌクレアーゼ; DNAエキソヌクレアーゼ、損傷塩基グリコシラーゼ(例:3-メチルアデニン-DNAグリコシラーゼ); 単独または複合体での修復エンドヌクレアーゼ(correndonucleases)(例:大腸菌uvrA/uvrB/uvrCエンドヌクレアーゼ複合体); APEXヌクレアーゼ、これはしばしば「APE」と呼ばれる多機能性DNA修復酵素である; ジヒドロ葉酸レダクターゼ; ターミナルトランスフェラーゼ; トポイソメラーゼ; O6ベンジルグアニン; DNAグリコシラーゼ。
【0080】
適当なDNA修復酵素の他のタイプは、酵素が手助けする修復のタイプによって分類することができ、以下のものが挙げられる:BER(塩基除去修復)またはBER因子酵素、例えばウラシル-DNAグリコシラーゼ(UNG); 一本鎖選択的単機能性ウラシルDNAグリコシラーゼ(SMUG1); 3,N(4)-エテノシトシングリコシラーゼ(MBD4); チミンDNA-グリコシラーゼ(TDG); A/G-特異的アデニンDNAグリコシラーゼ(MUTYH); 8-オキソグアニンDNAグリコシラーゼ(OGG1); エンドヌクレアーゼIII様(NTHL1); 3-メチルアデニンDNAグリコシダーゼ(MPG); DNAグリコシラーゼ/APリアーゼ(NEIL1または2); APエンドヌクレアーゼ(APEX 1および2)、DNAリガーゼ(LIG3)、リガーゼアクセサリー因子(XRCC1); DNA 5'-キナーゼ/3'-ホスファターゼ(PNKP); ADP-リボシルトランスフェラーゼ(PARP1または2)。
【0081】
DNA修復酵素の別のカテゴリーには、損傷を直接修復すると考えられるもの、例えば、O6-MeGアルキルトランスフェラーゼ(MGMT); 1-meAジオキシゲナーゼ(ALKBH2またはALKBH3)が含まれる。
【0082】
DNA/タンパク質架橋を修復するように機能しうる酵素のさらに別のカテゴリーにはTyr-DNAホスホジエステラーゼ(TDP1)が含まれる。
【0083】
さらに、MMR(ミスマッチ除去修復)DNA修復酵素、例えば、MutSタンパク質ホモログ(MSH2); ミスマッチ修復タンパク質(MSH3); mutSホモログ4(MSH4); MutSホモログ5(MSH5); またはG/Tミスマッチ結合タンパク質(MSH6); DNAミスマッチ修復タンパク質(PMS1、PMS2、MLH1、MLH3); Postmeiotic segregation increased 2-likeタンパク質(PMS2L3); またはpostmeiotic segregation increased 2-like 4偽遺伝子(PMS2L4)も適している。
【0084】
さらに、適しているDNA修復酵素はヌクレオチド除去修復(NER)酵素として知られるものであり、例えば、色素性乾皮症C群相補性タンパク質(Xeroderma pigmentosum group C-complementing protein)(XPC); RAD23 (S. cerevisiae)ホモログ(RAD23B); カルトラクチンアイソフォーム(caltractin isoform)(CETN2); RFAタンパク質1、2または3 (RPA1、2または3); 3'-5' DNAヘリカーゼ(ERCC3); 5'-3' DNAヘリカーゼ(ERCC2); 塩基性転写因子(GTF2H1、GTF2H2、GTF2H3、GTF2H4、GTF2H5); CDK活性化キナーゼ(CDK7、CCNH); サイクリンG1相互作用タンパク質(cyclin G1-interacting protein)(MNAT1); DNA除去修復タンパク質ERCC-51; 除去修復交差相補群1(excision repair cross-complementing 1)(ERCC1); DNAリガーゼ1 (LIG1); ATP依存性ヘリカーゼ(ERCC6)などが挙げられる。
【0085】
さらに、相同組換えを促進するカテゴリー中のDNA修復酵素も適しており、限定するものではないが、DNA修復タンパク質RAD51ホモログ(RAD51、RAD51L1、RAD51Bなど); DNA修復タンパク質XRCC2; DNA修復タンパク質XRCC3; DNA修復タンパク質RAD52; ATPase (RAD50); 3'エキソヌクレアーゼ(MRE11A)などが含まれる。
【0086】
DNAポリメラーゼであるDNA修復酵素も適しており、DNAポリメラーゼβサブユニット(POLB); DNAポリメラーゼγ(POLG); DNAポリメラーゼサブユニットδ(POLD1); DNAポリメラーゼIIサブユニットA (POLE); DNAポリメラーゼδ補助タンパク質(PCNA); DNAポリメラーゼζ(POLZ); MAD2ホモログ((REV7); DNAポリメラーゼη(POLH): DNAポリメラーゼκ(POLK)などが挙げられる。
【0087】
「編集・プロセッシングヌクレアーゼ」(editing and processing nucleases)と呼ばれることが多い、さまざまなタイプのDNA修復酵素には、3'-ヌクレアーゼ; 3'-エキソヌクレアーゼ; 5'-エキソヌクレアーゼ; エンドヌクレアーゼなとが含まれる。DNA修復酵素の他の例には、DNAヘリカーゼ、例えばATP DNAヘリカーゼなどが含まれる。DNA修復酵素は植物エキス、細菌溶解液、生物学的物質などの成分として存在し得る。例えば、植物エキスがDNA修復酵素を含むことがある。
【実施例】
【0088】
実施例1: sirt1活性化剤(Orsirtine(商標)およびレスベラトロール)はケラチノサイトの生存を相乗的に改善する
有糸分裂遅延剤であるOrsirtine(商標)((配列番号8) G-L-Y-D-N-L-E)およびレスベラトロールを、UVB照射したヒトケラチノサイトの生存を改善するそれらの能力について試験した。
【0089】
方法:
正常なヒトケラチノサイトを、ヒトケラチノサイト増殖サプリメント(Human Keratinocyte Growth Supplement)を添加したEpilife培地で培養した。その細胞を96ウェルプレート(Costar)に継代培養した。ケラチノサイトをレスベラトロール(25μM)およびOrsirtine(1%、3%)単独で、さらにレスベラトロール(25μM)とOrsirtine(3%)の複合体で前処理した。ケラチノサイトを未希釈の複合体で、また、1:2、1:4および1:8 (複合体:Epilife培地)の希釈物で処理した。
【0090】
ケラチノサイトをこれらの処理剤と共に37℃、5%CO2で一晩インキュベートした。24時間後、その処理剤を吸引し、ケラチノサイトをD-PBSで1回洗浄した。照射のために100μlのD-PBSを添加した。細胞に0、45、90および135mJ/cm2のUVBを照射した。照射後、D-PBSを除去した。ケラチノサイトを適切に後処理して、37℃、5%CO2で一晩インキュベートした。翌日、MTS試薬(CellTiter96、Promega社)を利用して、細胞の生存率についてアッセイした。37℃、5%CO2で約2時間のインキュベーション後に、吸光度をSpectraMax190分光光度計(Molecular Devices社)で490nmにて読み取った。
【0091】
結果および結論:
図2を参照すると、低UV照射(45mJ/cm2)では、細胞は強烈なダメージを示さないことが報告されているで、生存率の改善はごくわずかであると予想された。しかし、我々が観察したものは、レスベラトロールだけで処理した細胞が20%の生存率の低下を示し、また、Orsitine(3%)だけで処理した細胞が8%の生存率の低下を示す、ということである。それにもかかわらず、1:2希釈複合体(レスベラトロール25μMとOrsirtine 3%)で、または未希釈複合体で処理した細胞は、対照と同じ試験結果であった。さらに、複合体を1:4に、次いで1:8に希釈すると、生存率が低下する。こうして、レスベラトロール単独、およびOrsirtine 3%単独では、細胞の生存が低下する。しかしながら、レスベラトロールとOrsirtine 3%の組合せは細胞の生存を低下させない。しかし、この組合せは、対照と比べて、細胞の生存率を改善することができるのか?
90mJ/cm2のUV照射では、未処理の細胞の生存率は47%であった。それに引き換え、未希釈および希釈した複合体(レスベラトロール25μMとOrsirtine 3%)で処理した細胞の生存率は、次のように用量依存的関係にあった:
【表1】

【0092】
一方、Orsirtine単独またはレスベラトロール単独で処理した細胞の生存率は次のとおりであった:
【表2】

【0093】
135mJ/cm2のUV照射では、未処理の細胞の生存率は19%であった。それに引き換え、未希釈および希釈した複合体で処理した細胞の生存率は、次のように準用量依存的関係にあった:
【表3】

【0094】
一方、Orsirtine単独またはレスベラトロール単独で処理した細胞の生存率は次のとおりであった:
【表4】

【0095】
複合体(レスベラトロール25μMとOrsirtine 3%)は、レスベラトロールおよびOrsirtine単独と比べて、UVB誘導細胞毒性に対して顕著な保護を与えるとともに、細胞の生存を高める、と結論づけることができる。
【0096】
これらの数字はまた、ケラチノサイト生存率に対するOrsirtineとレスベラトロールの組合せの効果が相乗的であることを示唆するようである。例えば、3%のOrsirtineは単独で生存率を11%(90mJ/cm2のUVBの場合)および26%(135mJ/cm2のUVBの場合)増加させる。25μMのレスベラトロールは単独で生存率を15%(90mJ/cm2のUVBの場合)低下させ、かつ生存率を22%(135mJ/cm2のUVBの場合)増加させた。ところが、未希釈の組合せ(3%Orsirtineと25μMレスベラトロール)は、ケラチノサイトの生存率を、大幅にかつ予想外に、64%(90mJ/cm2のUVBの場合)および131%(135mJ/cm2のUVBの場合)増加させた。1:8まで希釈したときでさえ、この組合せはまだケラチノサイトの生存率を28%(90mJ/cm2のUVBの場合)および11%(135mJ/cm2のUVBの場合)増加させる。このことは完全に予想外である。Orsirtineは既知のサーチュイン活性化剤であり、また、レスベラトロールは疑わしいサーチュイン活性化剤であるので、ケラチノサイトの生存率の大幅な改善は当業者には予想されないことである。せいぜい、相加効果が予想されたかもしれないが、相乗効果は予想されなかった。
【0097】
(配列番号8) G-L-Y-D-N-L-Eとレスベラトロールのどのような相対濃度がケラチノサイトの生存率に大きな相乗効果をもたらすのだろうか?この質問には、今やその効果が確認されているのだから、日常的な実験によって答を出すことができる。「sirt1活性化剤とレスベラトロールの相乗的組合せ」とは、ケラチノサイトの生存率(そうした生存率は当技術分野で公知の方法により測定される)を、個別の各物質の効果の合計量を超える分量だけ、増加させる(配列番号7)(AA)n-G-L-Y-D-N-L-E-(AA)nとレスベラトロールまたはその誘導体との組合せを意味する。
【0098】
実施例2: sirt1活性化剤は、正しい濃度で、UVB曝露に対する概日遺伝子活性化剤とDNA修復酵素の性能を改善する
実施例1に記載の方法に従って、2種の複合体をいくつかの希釈率で、UV曝露後に、ケラチノサイトの生存に対するそれらの効果について試験した。複合体Iは、ヒトケラチノサイト増殖サプリメントを添加したEpilife培地と、Chronolux (0.1%)、ビフィズス菌エキス(12.4%)、Adasome (0.05%)およびRoxisome (0.05%)から成っていた。複合体IIは、複合体IにOrsirtine (0.08%)とレスベラトロール(25μM)を加えたものから成っていた。複合体Iは未希釈ならびに1:2および1:4 (複合体:Epilife培地)の希釈で試験した。複合体IIは未希釈ならびに1:2、1:4および1:8の希釈で試験した。培地を対照として用いた。ケラチノサイトを100、150および200mL/cm2のレベルのUVBに曝露した。
【0099】
結果および結論:
図3を参照すると、また、同じUVB曝露内で複合体IIを複合体Iと比較すると、
【表5】

【0100】
2つを除く全ての場合に、Orsirtine(商標)およびレスベラトロールは、概日遺伝子活性化剤だけと比較して、UVB曝露後のケラチノサイトの生存を改善する。しかし、第1列(100mJ/cm2)の2つの段を下に移動すると、これらのデータは、概日遺伝子活性化剤と組み合わせたsirt1活性化剤が少ないほど良好である、ことを示唆するようである。ところが、このパターンは第2列および第3列(150mJ/cm2および200mJ/cm2)で破られ、sirt1および概日遺伝子活性化剤の最適な組合せはケラチノサイトが曝露されるUVBの量に依存する、ことを示唆している。実際、3段目(未希釈)を左から右に移動すると、これらのデータは、Orsirtineとレスベラトロールの添加がより多量のUVB曝露に対して正当化される、ことを示唆している。このパターンは1:2希釈のサンプルでも見られるが、1:4希釈のサンプルでは逆転し、より低いUVB曝露には、より少ないsirt1活性化が必要であることを示唆している。こうして、全体として見れば、これらの実験の結果は、概日遺伝子活性化剤とsirt1活性化剤の最適な相対濃度がUVBの曝露量に依存することを示唆している。しかしながら、全ての複合体II試験サンプル(概日活性化剤+sirt1活性化剤)は、対照と比べて、ケラチノサイト生存率の改善を示した。今や当業者は概日遺伝子活性化剤とsirt1活性化剤の相対濃度が結果有効変数(results-effective variable)である(これまで不明であった)ことを知っているので、最適な相対濃度を決定するには日常的な実験が必要であるにすぎない。
【0101】
組成物
本発明の組成物の形態は一般的に限定されない。例えば、本発明の組成物はエマルション、水性の溶液もしくは分散液、ゲル、または無水系の形態であってよい。エマルションの形態である場合、組成物は油中水型または水中油型のエマルションであり得る。エマルションの形態である場合、その組成物は約1〜99%、好ましくは約5〜90%、より好ましくは約10〜85%の水と、約1〜99%、好ましくは約5〜90%、より好ましくは約5〜75%の油を含むことができる。水性懸濁液または分散液の場合には、組成物は一般的に約1〜99.9%、好ましくは約5〜95%、より好ましくは約10〜90%の水を含み、残りの成分が活性成分または他の処方成分である。
【0102】
好ましくは、組成物は化粧品的または薬学的に許容される製品を提供する他の成分を含有する。そうした成分のクラスには、保湿剤、UVAおよびUVBサンスクリーン剤、界面活性剤、植物エキス、生物学的物質、水相構造化剤(すなわち、多糖類、アクリレートポリマー、高分子量PEGまたはポリグリセリン)、揮発性および不揮発性オイル(シリコーンを含む)、ビタミン、および酸化防止剤が含まれるだろう。
【0103】
また、概日遺伝子活性化剤とsirt1活性化剤は別々の組成物中に存在することが可能であり、その別々の組成物は、皮膚の同じ領域に連続して適用してもよいし、または各組成物の有効量を分配して混ぜ合わせてから、その混合物を皮膚に塗布することによって適用してもよい。
【0104】
好ましい組成物
好ましい組成物は水性溶液またはエマルションの形態であり、少なくとも1種の非イオン性有機界面活性剤、少なくとも1種の化学的サンスクリーン剤、少なくとも1種のclockまたはper1遺伝子活性化剤、少なくとも1種のペプチド性sirt1活性化剤、および少なくとも1種のDNA修復酵素を含有する。少なくとも1種の植物エキスおよび少なくとも1種のオイルも好ましいものである。
【0105】
より好ましいものは、非イオン性有機界面活性剤がアルコキシル化アルコールであり、化学的サンスクリーン剤がUVBサンスクリーン剤であり、clockまたはper1ケラチノサイト遺伝子活性化剤がTripeptide-32であり、sirt1活性化剤がOrsirtine(商標)様分子とレスベラトロールの組合せであり、DNA修復酵素がシロイヌナズナエキス(Arabidopsis Thaliana extract)とミクロコッカス溶解液(Micrococcus lysate)とビフィズス菌発酵エキス(Bifida Ferment lysate)と乳酸桿菌発酵液(Lactobacillus ferment)とプランクトンエキス(Plankton extract)の混合物であり、そして少なくとも1種のオイルが有機エステルまたは炭化水素である場合の組成物である。
【0106】
本発明の方法
本発明の方法は主に、ヒトケラチノサイト、好ましくは顔のケラチノサイトへの損傷(損傷は環境攻撃に応答して発生する)を修復することに向けられる。一方法は、損傷を受けたヒト皮膚に、少なくとも1種のケラチノサイトclockまたはper1遺伝子活性化剤と少なくとも1種のsirt1活性化剤を含む1つ以上の組成物を適用することからなる。場合により、本方法の組成物は少なくとも1種のDNA修復酵素を含んでもよい。損傷が発生した後に本組成物を適用することによって、通常の概日周期がより速やかに回復される。しかし、有糸分裂前の細胞周期の停止は、DNA修復のためにより多くの時間を割り当てられる。この方法によって、かなりの細胞損傷が回復に向かい、かつ/または娘細胞に伝わるのをチェックされる。本方法はまた、ケラチノサイトの生存率と寿命を改善することができる。
【0107】
本発明はさらに、ヒトケラチノサイト、好ましくは顔のケラチノサイトへの損傷(損傷は環境攻撃に応答して発生するだろう)を予防または抑制する方法に向けられる。この方法は、環境損傷を受けるリスクがあるヒト皮膚に、少なくとも1種のケラチノサイトclockまたはper1遺伝子活性化剤と少なくとも1種のsirt1活性化剤を含む1つ以上の組成物を適用することからなる。場合により、本方法の組成物は少なくとも1種のDNA修復酵素を含んでもよい。損傷が発生する前に本組成物を適用することによって、通常の概日周期がより厳密に維持され、また、通常の細胞周期の修復過程がより厳密に維持される。この方法によって、かなりの細胞損傷が予防され、かつ/または娘細胞に伝わるのをチェックされる。本方法はまた、ケラチノサイトの生存率と寿命を改善することができる。
【0108】
本発明の方法では、組成物を1日1回以上皮膚に適用することができる。例えば、日常活動を始める前の午前中におよび/または就寝する直前の夜に、組成物を皮膚に適用する。これらの時間帯は、皮膚が一般的に最少量の環境攻撃のもとにある(皮膚細胞の修復が最大になりうることを意味する)ため、好適である。これらの時間帯で、「就寝する直前」または「毎晩休む直前」とは、床に入る1時間以内、より好ましくは床に入る30分以内を意味する。午前中はどちらかといえば予防的アプローチであるが、就寝する直前または夜はむしろ修復アプローチである。本組成物はレジメンの一部として適用することができる;すなわち、皮膚を洗浄して化粧水(toner)で処置し、その後本発明の組成物を適用する。本組成物は、洗浄剤と化粧水と本発明の組成物を含むキットの一部であり得る。
【0109】
好ましくは、本組成物は、DNA損傷を受けたケラチノサイトを修復しかつ皮膚の一般的な改善を得るために、就寝直前に顔および/または首と胸元の皮膚に適用される。顔の皮膚を夜に就寝する直前に処置するための組成物中でclockおよびper1遺伝子活性化剤とsirt1活性化剤(と好ましくはDNA修復酵素)を併用すると、ケラチノサイトのDNA損傷の修復が最大となり、さらに細胞の生存率、寿命および健康が促進される。
【0110】
上述したように、概日遺伝子活性化剤とsirt1活性化剤は別々の組成物中に存在することが可能である。その場合に、本発明の方法は、各組成物を皮膚の同じ領域に連続して適用するステップを含むか、または各組成物の有効量を分配するステップと、その組成物を混合するステップと、その後混合物を皮膚に適用するステップを含む。
【0111】
実施例
本発明を、例示のみの目的のために記載される以下の実施例に関連して、さらに説明することにする。スキントリートメント組成物は次のように調製することができる。
【0112】
実施例1
【表6】


【0113】
実施例2〜4
clock遺伝子活性化剤(Chronolux(登録商標)、tripeptide-32)を含むが、sirt1活性化剤を含まない第1のスキントリートメント組成物は、処方A(実施例2)に従って調製することができる。clock遺伝子活性化剤(Chronolux(登録商標))とsirt1活性化剤(Orsirtine(商標)およびレスベラトロール)を含む第2のスキントリートメント組成物は、処方B(実施例3)に従って調製することができる。sirt1活性化剤(Orsirtine(商標))を含むが、概日遺伝子活性化剤を含まない第3のスキントリートメント組成物は、処方C(実施例4)に従って調製することができる。これらの組成物は、各成分を一緒にし、十分に混合して液体とすることによって調製される。組成物は褐色のガラスビンに保存することができる
組成物Aは、概日遺伝子活性化剤とsirt1活性化剤(Orsirtine(商標)およびレスベラトロール)を含む。したがって、組成物Aは単独での使用を目的としている。組成物BはChronolux(登録商標)(概日遺伝子活性化剤)を含むが、sirt1遺伝子活性化剤を含まない。したがって、組成物Bは、sirt1遺伝子活性化能を有する別の組成物(例えば、組成物C)と一緒の使用を目的としている。
【表7】


【表8】


【0114】
本発明を好ましい実施形態に関連して説明してきたが、本発明の範囲を、記載された特定の形態に限定することを意図したものではない。それどころか、この説明は、添付の特許請求の範囲により規定される本発明の精神および範囲内に含まれるような変更、修飾および均等物をカバーすることを意図したものである。
【特許請求の範囲】
【請求項1】
少なくとも1種のケラチノサイト概日遺伝子活性化剤および少なくとも1種のケラチノサイトsirt1遺伝子活性化剤を含むスキンケア組成物。
【請求項2】
ケラチノサイト概日遺伝子活性化剤が3〜13個のアミノ酸残基を有するペプチドを含み、かつ式(I):
(配列番号1) R1-(AA)n-X1-S-T-P-X2-(AA)p-R2
[式中、
X1は、トレオニン、セリンを表すか、ゼロに等しく;
X2は、イソロイシン、ロイシン、プロリン、バリン、アラニン、グリシンを表すか、ゼロに等しく;
AAは、任意のアミノ酸またはその誘導体を表し;
nおよびpは、0〜4の整数であり;
R1は、N末端アミノ酸の1級アミン官能基を表し、そのアミン官能基は遊離であるか、アセチル基、ベンゾイル基、トシル基、またはベンジルオキシカルボニル基から選択できる保護基で置換されており;
R2は、C末端アミノ酸のカルボキシル官能基のヒドロキシル基を表し、そのヒドロキシル基はC1-C20アルキル鎖またはNH2、NHY、もしくはNYY基(ここで、YはC1-C4アルキル鎖を表す)から選択できる保護基で置換されていてもよい]
で表され、そして式(I)の配列は、アミノ酸X1およびX2の、他の化学的に等価なアミノ酸による置換を含むことができる、請求項1記載の組成物。
【請求項3】
概日遺伝子活性化剤が、
(配列番号2) Y-V-S-T-P-Y-N-NH2
Tyr-Val-Ser-Thr-Pro-Tyr-Asn-NH2
(配列番号3) NH2-V-S-T-P-E-NH2
NH2-Val-Ser-Thr-Pro-Glu-NH2
S-T-P-NH2
Ser-Thr-Pro-NH2
(配列番号4) NH2-L-H-S-T-P-P-NH2
NH2-Leu-His-Ser-Thr-Pro-Pro-NH2
(配列番号5) CH3NH-R-H-S-T-P-E-NH2
CH3-NH-Arg-His-Ser-Thr-Pro-Glu-NH2
(配列番号6) CH3NH-H-S-T-P-E-CH3NH
CH3-NH-His-Ser-Thr-Pro-Glu-CH3-NH
およびこれらの混合物からなる群より選択される、請求項2記載の組成物。
【請求項4】
概日遺伝子活性化剤がTripeptide-32を含む、請求項3記載の組成物。
【請求項5】
ケラチノサイトsirt1遺伝子活性化剤が1種以上のtrans-スチルベンもしくはその誘導体、ケラチノサイトsirt1遺伝子を活性化できる1種以上のペプチド、またはこれらの組合せである、請求項1記載の組成物。
【請求項6】
レスベラトロールと、式(II)のペプチド:
(配列番号7) (AA)n-G-L-Y-D-N-L-E-(AA)n
[式中、(AA)は任意の特定のアミノ酸またはその誘導体であり;nは0〜3の整数である]
との相乗的組合せを含む、請求項5記載の組成物。
【請求項7】
前記ペプチドが、
(配列番号8) G-L-Y-D-N-L-E
Gly-Leu-Tyr-Asp-Asn-Leu-Glu
である、請求項6記載の組成物。
【請求項8】
tripeptide-32を、最終組成物の全重量に対して0.00001〜25%;
(配列番号8) G-L-Y-D-N-L-Eを、最終組成物の全重量に対して0.0001%〜5%;および
レスベラトロールを、最終組成物の全重量に対して0.001%〜約95%;
含有するスキンケア組成物。
【請求項9】
少なくとも1種のDNA修復酵素を、最終組成物の全重量に対して0.0001%〜25%、さらに含有する、請求項8記載の組成物。
【請求項10】
DNA修復酵素が、塩基除去修復(BER)酵素、ヌクレオチド除去修復(NER)酵素、DNAポリメラーゼ、DNAヘリカーゼ、ミスマッチ修復(MMR)酵素、およびこれらの混合物からなる群より選択される、請求項9記載の組成物。
【請求項11】
DNA修復酵素が、シロイヌナズナエキス(Arabidopsis Thaliana extract)、乳酸桿菌発酵液(Lactobacillus ferment)、ミクロコッカス溶解液(Micrococcus lysate)、プランクトンエキス(Plankton extract)、ビフィズス菌発酵エキス(Bifida ferment lysate)、およびこれらの混合物からなる群より選択される、請求項9記載の組成物。
【請求項12】
以下のステップを含んでなる、環境攻撃によるヒトケラチノサイトへの損傷を抑制する方法:
ケラチノサイト損傷のリスクがある皮膚に、0.00001〜25%の少なくとも1種のケラチノサイト概日遺伝子活性化剤を含む組成物を適用するステップ;および
ケラチノサイト損傷のリスクがある皮膚に、0.0001%〜5%の少なくとも1種のケラチノサイトsirt1遺伝子活性化剤を含む組成物を適用するステップ。
【請求項13】
少なくとも1種のケラチノサイト概日遺伝子活性化剤および少なくとも1種のケラチノサイトsirt1遺伝子活性化剤が別々の組成物中に存在し、各組成物が連続して適用される、請求項12記載の方法。
【請求項14】
少なくとも1種のケラチノサイト概日遺伝子活性化剤および少なくとも1種のケラチノサイトsirt1遺伝子活性化剤が単一の組成物の一部であり、該組成物が、化学的に、熱力学的におよび光に安定であり、局所使用に安全であり、副作用がほとんどまたは全くなく、かつパーソナルケア市場で商業的に実現可能なものである、請求項12記載の方法。
【請求項15】
以下のステップを含んでなる、環境攻撃によるヒトケラチノサイトへの損傷を修復する方法:
顔に、0.00001〜25%の少なくとも1種のケラチノサイト概日遺伝子活性化剤を含む組成物を適用するステップ;および
顔に、0.0001%〜5%の少なくとも1種のケラチノサイトsirt1遺伝子活性化剤を含む組成物を適用するステップ。
【請求項16】
概日遺伝子およびsirt1遺伝子活性化剤が床に入る30分以内に適用される、請求項15記載の方法。
【請求項17】
ヒト皮膚の一部分を洗浄するステップ;
その後、皮膚の該部分に化粧水(toner)を適用するステップ;および
その後、概日遺伝子およびsirt1遺伝子活性化剤を適用するステップ;
を含んで成る、請求項15記載の方法。
【請求項18】
式IIとレスベラトロールまたはその誘導体との相乗的組合せを含む、化学的に、熱力学的におよび光に安定であり、かつ局所使用に安全である局所組成物。
【請求項19】
ヒトケラチノサイトへのUVB損傷を修復するための請求項1記載の組成物の使用。
【請求項20】
ヒトケラチノサイトへのUVB損傷を修復するための請求項18記載の組成物の使用。
【請求項21】
多糖類、アクリルポリマーまたはこれらの混合物を含む、少なくとも1種の水相構造化剤;
アルコキシル化アルコールである、少なくとも1種の非イオン性有機界面活性剤;および
C2-4アルキレングリコールまたはグリセリンである、少なくとも1種の保湿剤;
をさらに含む、請求項1記載の組成物。
【請求項1】
少なくとも1種のケラチノサイト概日遺伝子活性化剤および少なくとも1種のケラチノサイトsirt1遺伝子活性化剤を含むスキンケア組成物。
【請求項2】
ケラチノサイト概日遺伝子活性化剤が3〜13個のアミノ酸残基を有するペプチドを含み、かつ式(I):
(配列番号1) R1-(AA)n-X1-S-T-P-X2-(AA)p-R2
[式中、
X1は、トレオニン、セリンを表すか、ゼロに等しく;
X2は、イソロイシン、ロイシン、プロリン、バリン、アラニン、グリシンを表すか、ゼロに等しく;
AAは、任意のアミノ酸またはその誘導体を表し;
nおよびpは、0〜4の整数であり;
R1は、N末端アミノ酸の1級アミン官能基を表し、そのアミン官能基は遊離であるか、アセチル基、ベンゾイル基、トシル基、またはベンジルオキシカルボニル基から選択できる保護基で置換されており;
R2は、C末端アミノ酸のカルボキシル官能基のヒドロキシル基を表し、そのヒドロキシル基はC1-C20アルキル鎖またはNH2、NHY、もしくはNYY基(ここで、YはC1-C4アルキル鎖を表す)から選択できる保護基で置換されていてもよい]
で表され、そして式(I)の配列は、アミノ酸X1およびX2の、他の化学的に等価なアミノ酸による置換を含むことができる、請求項1記載の組成物。
【請求項3】
概日遺伝子活性化剤が、
(配列番号2) Y-V-S-T-P-Y-N-NH2
Tyr-Val-Ser-Thr-Pro-Tyr-Asn-NH2
(配列番号3) NH2-V-S-T-P-E-NH2
NH2-Val-Ser-Thr-Pro-Glu-NH2
S-T-P-NH2
Ser-Thr-Pro-NH2
(配列番号4) NH2-L-H-S-T-P-P-NH2
NH2-Leu-His-Ser-Thr-Pro-Pro-NH2
(配列番号5) CH3NH-R-H-S-T-P-E-NH2
CH3-NH-Arg-His-Ser-Thr-Pro-Glu-NH2
(配列番号6) CH3NH-H-S-T-P-E-CH3NH
CH3-NH-His-Ser-Thr-Pro-Glu-CH3-NH
およびこれらの混合物からなる群より選択される、請求項2記載の組成物。
【請求項4】
概日遺伝子活性化剤がTripeptide-32を含む、請求項3記載の組成物。
【請求項5】
ケラチノサイトsirt1遺伝子活性化剤が1種以上のtrans-スチルベンもしくはその誘導体、ケラチノサイトsirt1遺伝子を活性化できる1種以上のペプチド、またはこれらの組合せである、請求項1記載の組成物。
【請求項6】
レスベラトロールと、式(II)のペプチド:
(配列番号7) (AA)n-G-L-Y-D-N-L-E-(AA)n
[式中、(AA)は任意の特定のアミノ酸またはその誘導体であり;nは0〜3の整数である]
との相乗的組合せを含む、請求項5記載の組成物。
【請求項7】
前記ペプチドが、
(配列番号8) G-L-Y-D-N-L-E
Gly-Leu-Tyr-Asp-Asn-Leu-Glu
である、請求項6記載の組成物。
【請求項8】
tripeptide-32を、最終組成物の全重量に対して0.00001〜25%;
(配列番号8) G-L-Y-D-N-L-Eを、最終組成物の全重量に対して0.0001%〜5%;および
レスベラトロールを、最終組成物の全重量に対して0.001%〜約95%;
含有するスキンケア組成物。
【請求項9】
少なくとも1種のDNA修復酵素を、最終組成物の全重量に対して0.0001%〜25%、さらに含有する、請求項8記載の組成物。
【請求項10】
DNA修復酵素が、塩基除去修復(BER)酵素、ヌクレオチド除去修復(NER)酵素、DNAポリメラーゼ、DNAヘリカーゼ、ミスマッチ修復(MMR)酵素、およびこれらの混合物からなる群より選択される、請求項9記載の組成物。
【請求項11】
DNA修復酵素が、シロイヌナズナエキス(Arabidopsis Thaliana extract)、乳酸桿菌発酵液(Lactobacillus ferment)、ミクロコッカス溶解液(Micrococcus lysate)、プランクトンエキス(Plankton extract)、ビフィズス菌発酵エキス(Bifida ferment lysate)、およびこれらの混合物からなる群より選択される、請求項9記載の組成物。
【請求項12】
以下のステップを含んでなる、環境攻撃によるヒトケラチノサイトへの損傷を抑制する方法:
ケラチノサイト損傷のリスクがある皮膚に、0.00001〜25%の少なくとも1種のケラチノサイト概日遺伝子活性化剤を含む組成物を適用するステップ;および
ケラチノサイト損傷のリスクがある皮膚に、0.0001%〜5%の少なくとも1種のケラチノサイトsirt1遺伝子活性化剤を含む組成物を適用するステップ。
【請求項13】
少なくとも1種のケラチノサイト概日遺伝子活性化剤および少なくとも1種のケラチノサイトsirt1遺伝子活性化剤が別々の組成物中に存在し、各組成物が連続して適用される、請求項12記載の方法。
【請求項14】
少なくとも1種のケラチノサイト概日遺伝子活性化剤および少なくとも1種のケラチノサイトsirt1遺伝子活性化剤が単一の組成物の一部であり、該組成物が、化学的に、熱力学的におよび光に安定であり、局所使用に安全であり、副作用がほとんどまたは全くなく、かつパーソナルケア市場で商業的に実現可能なものである、請求項12記載の方法。
【請求項15】
以下のステップを含んでなる、環境攻撃によるヒトケラチノサイトへの損傷を修復する方法:
顔に、0.00001〜25%の少なくとも1種のケラチノサイト概日遺伝子活性化剤を含む組成物を適用するステップ;および
顔に、0.0001%〜5%の少なくとも1種のケラチノサイトsirt1遺伝子活性化剤を含む組成物を適用するステップ。
【請求項16】
概日遺伝子およびsirt1遺伝子活性化剤が床に入る30分以内に適用される、請求項15記載の方法。
【請求項17】
ヒト皮膚の一部分を洗浄するステップ;
その後、皮膚の該部分に化粧水(toner)を適用するステップ;および
その後、概日遺伝子およびsirt1遺伝子活性化剤を適用するステップ;
を含んで成る、請求項15記載の方法。
【請求項18】
式IIとレスベラトロールまたはその誘導体との相乗的組合せを含む、化学的に、熱力学的におよび光に安定であり、かつ局所使用に安全である局所組成物。
【請求項19】
ヒトケラチノサイトへのUVB損傷を修復するための請求項1記載の組成物の使用。
【請求項20】
ヒトケラチノサイトへのUVB損傷を修復するための請求項18記載の組成物の使用。
【請求項21】
多糖類、アクリルポリマーまたはこれらの混合物を含む、少なくとも1種の水相構造化剤;
アルコキシル化アルコールである、少なくとも1種の非イオン性有機界面活性剤;および
C2-4アルキレングリコールまたはグリセリンである、少なくとも1種の保湿剤;
をさらに含む、請求項1記載の組成物。
【図1】


【図2】


【図3】




【図2】


【図3】


【公表番号】特表2012−531414(P2012−531414A)
【公表日】平成24年12月10日(2012.12.10)
【国際特許分類】
【出願番号】特願2012−517561(P2012−517561)
【出願日】平成22年6月9日(2010.6.9)
【国際出願番号】PCT/US2010/037871
【国際公開番号】WO2011/005406
【国際公開日】平成23年1月13日(2011.1.13)
【出願人】(598100128)イーエルシー マネージメント エルエルシー (112)
【Fターム(参考)】
【公表日】平成24年12月10日(2012.12.10)
【国際特許分類】
【出願日】平成22年6月9日(2010.6.9)
【国際出願番号】PCT/US2010/037871
【国際公開番号】WO2011/005406
【国際公開日】平成23年1月13日(2011.1.13)
【出願人】(598100128)イーエルシー マネージメント エルエルシー (112)
【Fターム(参考)】
[ Back to top ]

