様々な架橋度を有するヒドロゲル移植物
【課題】ヒドロゲルを含む移植物を提供すること。
【解決手段】本発明は、ヒドロゲルを含む移植物を提供する。この移植物は、ヒドロゲルを含み、このヒドロゲルは、求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;求核基を含む、第二反応性前駆体と;少なくとも一つのビニル基を含む、少なくとも一つの開始性前駆体とを含む。この第一反応性前駆体は、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含む。
【解決手段】本発明は、ヒドロゲルを含む移植物を提供する。この移植物は、ヒドロゲルを含み、このヒドロゲルは、求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;求核基を含む、第二反応性前駆体と;少なくとも一つのビニル基を含む、少なくとも一つの開始性前駆体とを含む。この第一反応性前駆体は、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含む。
【発明の詳細な説明】
【技術分野】
【0001】
(関連する出願との相互参照)
本願は、米国仮特許出願第61/348,896号(2010年5月27日出願)の利益と、優先権を主張し、この仮特許出願の開示は参照によりその全体が本明細書中に援用される。
【0002】
ヒドロゲルは、多様な目的で体内において使用されうる。例えば、ヒドロゲルが、接着剤またはシーラントとして使用されうる。コーティングまたは移植物の形成においても、ヒドロゲルが使用されうる。このような移植物またはコーティングは、局所投与用の薬物も含みうる。
【背景技術】
【0003】
ヒドロゲルは、前駆体成分から形成されうる。これらの成分は、反応性でありえ、すなわち成分が接触時に互い反応し、または紫外(UV)光、イオン、熱、可視光、ガンマ線、電子ビーム、それらの組み合わせなどの外部の開始剤への曝露により反応させられうる。もたらされるヒドロゲルの特徴は、特定のタイプの前駆体の特徴に限定されうる。
【0004】
反応性ヒドロゲル前駆体および開始性ヒドロゲル前駆体の両者の性質を示すヒドロゲルを形成することが、有利であると考えられる。
【発明の概要】
【課題を解決するための手段】
【0005】
本開示は、ヒドロゲルならびにそれを作製および使用する方法を提供する。これらのヒドロゲルを含むデバイスも、提供される。例えば、ある実施形態では、本開示のヒドロゲルが、医療デバイスを組織に付着させるために利用されうる。
【0006】
ある実施形態では、本開示は、求電子基を有するマルチアーム(multi−arm)ポリエーテルを含む第一反応性前駆体と、第二反応性前駆体求核基と、少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体とを含むヒドロゲルを含む、移植物を提供する。
【0007】
ある実施形態では、本開示のヒドロゲルは、求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体と、求核基を含む第二反応性前駆体とを組み合わせて含む、第一ヒドロゲルと;少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体を含む、第二ヒドロゲルとを含む、複合ヒドロゲル組成物を含み得、第二ヒドロゲルが、第一ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成する。
【0008】
本開示の方法は、ある実施形態では、第一反応性前駆体を、第二反応性前駆体および少なくとも一つのビニル基を含む開始性前駆体と接触させるステップと;第一反応性前駆体および第二反応性前駆体を架橋して、ヒドロゲルを形成するステップと;ヒドロゲルの表面を開始剤に曝露して開始性前駆体の架橋を開始し、ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成するステップとを含む、移植物を形成する方法を含みうる。
【0009】
他の実施形態では、本開示の移植物は、求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;求核基を含む第二反応性前駆体と;少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体とを含む、ヒドロゲルを含み得、第一反応性前駆体が第二反応性前駆体と反応して第一ヒドロゲルを形成し、開始性前駆体が開始剤との接触時に第二ヒドロゲルを形成し、第二ヒドロゲルが第一ヒドロゲルを包含するバリヤ層を形成する。
【0010】
したがって、本発明は以下の項目を提供する:
(項目1)
ヒドロゲルを含む移植物であって、該ヒドロゲルは
求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;
求核基を含む、第二反応性前駆体と;
少なくとも一つのビニル基を含む、少なくとも一つの開始性前駆体と
を含む、移植物。
(項目2)
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、上記項目のうちのいずれかに記載の移植物。
(項目3)
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、上記項目のうちのいずれかに記載の移植物。
(項目4)
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目5)
生物活性剤をさらに含む、上記項目のうちのいずれかに記載の移植物。
(項目6)
前記第一反応性前駆体が前記第二反応性前駆体と反応して第一ヒドロゲルを形成し、前記開始性前駆体が、開始剤との接触時に第二ヒドロゲルを形成する、上記項目のうちのいずれかに記載の移植物。
(項目7)
前記開始剤が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目8)
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目9)
前記第二ヒドロゲルが、前記第一ヒドロゲルの少なくとも一部の上にバリヤ層を形成する、上記項目のうちのいずれかに記載の移植物。
(項目10)
前記第一ヒドロゲルが、組織欠損内に配置され、前記第二ヒドロゲルが、該欠損の上にバリヤ層を提供する、上記項目のうちのいずれかに記載の移植物。
(項目11)
前記第一ヒドロゲルが、約5kPa〜約500kPaのモジュラスを有し、前記第二ヒドロゲルが、約50kPa〜約5,000kPaのモジュラスを有する、上記項目のうちのいずれかに記載の移植物。
(項目12)
前記第一ヒドロゲルが、約4週〜約10週の期間にわたり分解し、前記第二ヒドロゲルが、約6週〜約6ヵ月の期間にわたり分解する、上記項目のうちのいずれかに記載の移植物。
(項目13)
前記移植物が、マトリックス、人工血管、心臓弁、人工臓器、人工骨、移植可能微小凸レンズ、血管グラフト、ステント、縫合糸、ステープル、クリップ、メッシュ、スリング、ネジ、ピン、ケーブル、軟骨移植物、脊椎移植物、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目14)
前記移植物が、軟骨移植物を含み、前記第一ヒドロゲルが、軟骨の欠損内にあり、前記第二ヒドロゲルが、該欠損の上にバリヤ層を形成する、上記項目のうちのいずれかに記載の移植物。
(項目15)
前記移植物が、前記第二ヒドロゲルにより囲まれた前記第一ヒドロゲルを含む、椎間板移植物を含む、上記項目のうちのいずれかに記載の移植物。
(項目16)
前記移植物が、人工皮膚を含む、上記項目のうちのいずれかに記載の移植物。
(項目17)
求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体を、求核基を含む第二反応性前駆体と組み合わせて含む、第一ヒドロゲルと;
少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体を含む、第二ヒドロゲルと
を含む、複合ヒドロゲル組成物であり、
該第二ヒドロゲルが、該第一ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成する、複合ヒドロゲル組成物。
(項目18)
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目19)
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目20)
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目21)
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第二ヒドロゲルをさらに架橋する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目22)
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目23)
生物活性剤をさらに含む、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目24)
前記生物活性剤が、前記第一ヒドロゲル中にある、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目25)
前記生物活性剤が、約3日〜約6週の期間にわたり前記第一ヒドロゲルから放出される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目26)
前記第二ヒドロゲルが、前記複合ヒドロゲル組成物の約5重量%〜約30重量%を構成する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目27)
前記第一ヒドロゲル中に少なくとも一つの分散領域を形成する少なくとも一つの開始性前駆体を含む第三ヒドロゲルをさらに含む、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目28)
前記第二ヒドロゲルおよび前記第三ヒドロゲルが、同じである、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目29)
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第三ヒドロゲルをさらに架橋する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目30)
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目31)
上記項目のうちのいずれかに記載の前記複合ヒドロゲル組成物を含む、薬物送達デバイス。
【0011】
本開示の様々な実施形態が、本明細書の以下で図に関して記載される。
【図面の簡単な説明】
【0012】
【図1A】図1Aは、本開示によるヒドロゲル移植物の側面図である。
【図1B】図1Bは、開始剤への曝露を描写した、図1Aのヒドロゲルの断面図である。
【図1C】図1Cは、開始剤への曝露後の図1Aのヒドロゲルの断面図である。
【図2A】図2Aは、本開示によるヒドロゲル移植物の斜視図である。
【図2B】図2Bは、開始剤への曝露を描写した、図2Aのヒドロゲルの側面図である。
【図2C】図2Cは、開始剤への曝露後の図2Aのヒドロゲルの断面図である。
【図3A】図3Aは、本開示のヒドロゲルの形成の間に使用されるテンプレートの側面図である。
【図3B】図3Bは、本開示によるテンプレート用のブロッキングデバイスまたはスクリーンの上面図である。
【図3C】図3Cは、本開示により使用されるテンプレートおよびブロッキングデバイスの側面図である。
【図3D】図3Dは、本開示のヒドロゲル移植物の側面図である。
【図4】図4は、開始性前駆体の架橋前および後の、本開示のヒドロゲル移植物のモジュラスを描写したグラフである。
【図5A】図5Aは、本開示のヒドロゲルを含むコーティングを有するメッシュ移植物の上面図である。
【図5B】図5Bは、本開示のヒドロゲルの一部の分解後の、図5Aの移植物の上面図である。
【図6A】図6Aは、本開示のヒドロゲルを用いて形成される縫合糸アンカの断面図である。
【図6B】図6Bは、開始性前駆体の架橋を描写した、図6Aの縫合糸アンカの断面図である。
【図6C】図6Cは、開始性前駆体の架橋後の、図6Aの縫合糸アンカの断面図である。
【図7A】図7Aは、本開示のヒドロゲルを用いた組織への接着のための移植物の上面図である。
【図7B】図7Bは、開始性前駆体の架橋前の、図7Aの移植物の上面図である。
【図7C】図7Cは、開始性前駆体の架橋後の、図7Aの移植物の上面図である。
【図8】図8は、表2に提示されるデータのグラフである。
【図9】図9は、開始性ヒドロゲルおよび非開始性ヒドロゲルにつき、加えた力と圧縮量を比較したグラフである。
【図10】図10は、種々の組織ならびにコラーゲンおよびゼラチンを含む他の材料の弾性モジュラスを描写したグラフである。
【図11】図11は、組織の欠損を修復するための、本開示の組成物の使用の描写である。
【図12A】図12Aは、一つのヒドロゲルで形成された分散領域を第二ヒドロゲル中に有する、本開示の組成物を含む移植物の図である。
【図12B】図12Bは、一つのヒドロゲルで形成された分散領域を第二ヒドロゲル中に有する、本開示の組成物を含む移植物の代替図である。
【発明を実施するための形態】
【0013】
外部の開始を必要とする前駆体、すなわち開始性前駆体と組み合わせた、開始剤の使用を必要としない反応性前駆体の架橋から形成されうるヒドロゲルが、本明細書に記載される。前駆体は、例えば、モノマーまたはマクロマーでありうる。本明細書において用いられるところの、「ヒドロゲル前駆体(単数または複数)」、「第一ヒドロゲル前駆体」、および「第二ヒドロゲル前駆体」という用語は、開始剤の使用を伴ってまたは伴わずに組み合わせられてヒドロゲルを形成しうる成分をさすために用いられうる。したがってこれらの前駆体は、ある実施形態では、反応性前駆体および開始性前駆体の組み合わせを含みうる。本明細書において用いられるところの、「反応性前駆体(単数または複数)」、「第一反応性ヒドロゲル前駆体(単数または複数)」、および「第二反応性ヒドロゲル前駆体(単数または複数)」という用語は、互いに対して曝露された時に架橋してヒドロゲルを形成しうる前駆体を含む。本明細書において用いられるところの、「開始性(initiated)前駆体(単数または複数)」、「第一開始性ヒドロゲル前駆体(単数または複数)」および「第二開始性ヒドロゲル前駆体(単数または複数)」という用語は、本明細書において「開始剤」と称されることもある外部ソースに曝露された時に架橋する、ヒドロゲル前駆体を表すために用いられうる。開始剤は、例えば、イオン、UV光、酸化還元反応成分、それらの組み合わせ、ならびに当業者の認識範囲内である他の開始剤を含む。
【0014】
ヒドロゲル前駆体は、反応性前駆体であるか開始性前駆体であるかを問わず、生物学的に不活性および水溶性のコアを有しうる。コアが水溶性のポリマー領域である場合、用いられうる適切なポリマーには、ポリエーテル類、例えば、ポリエチレングリコール(「PEG」)、ポリエチレンオキシド(「PEO」)、ポリエチレンオキシド−コ−ポリプロピレンオキシド(「PPO」)、コ−ポリエチレンオキシドブロックまたはランダムコポリマー類、およびポリビニルアルコール(「PVA」)等のポリアルキレンオキシド類;ポリ(ビニルピロリジノン)(「PVP」);ポリ(アミノ酸類);デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロースおよび/またはヒドロキシメチルセルロース等のポリ(サッカライド類);ヒアルロン酸;ならびにアルブミン、コラーゲン、カゼイン、およびゼラチン等のタンパク質類が含まれる。ある実施形態では、前述のポリマー材料の組み合わせを利用してコアが形成されうる。いくつかの実施形態においては、ポリエーテル類、特にポリ(オキシアルキレン類)またはポリ(エチレングリコール)またはポリエチレングリコール(「PEG」)が利用されうる。
【0015】
コアの分子的性状が小さい場合、様々な親水官能基のいずれかが、ヒドロゲル前駆体を水溶性にするために用いられうる。ある実施形態では、水溶性のヒドロキシル、アミン、スルホン酸およびカルボン酸のような官能基が、前駆体を水溶性にするために用いられうる。例えば、スべリン酸(subaric acid)のN−ヒドロキシスクシンイミド(「NHS」)エステルは水に不溶であるが、スルホン酸基をスクシンイミド環に付加することにより、アミン基に対する反応性により反応基として使用されうるその能力に影響することなくスべリン酸(subaric acid)のNHSエステルを水溶性にできる。
【0016】
ある実施形態では、共有結合、イオン結合、または疎水結合により、反応性前駆体からヒドロゲルが形成されうる。物理的(非共有結合)架橋は、錯形成、水素結合、脱溶媒和、Van der Waals相互作用、イオン結合、それらの組み合わせなどから生じ得、in situで組み合わせられるまで物理的に分離されている成分を混合することにより、または温度、pH、イオン強度、それらの組み合わせなどを含む生理学的環境中の一般的条件の結果として開始されうる。化学的(共有結合)架橋は、フリーラジカル重合、縮合重合、アニオンまたはカチオン重合、段階成長重合、求電子−求核反応、それらの組み合わせなどを含むがこれに限られない、多くの機構のいずれかによって達成されうる。
【0017】
ある実施形態では、ヒドロゲルの反応性前駆体部分は、単一のタイプの反応性前駆体または複数のタイプの反応性前駆体から形成されうる。他の実施形態においては、ヒドロゲルが複数のタイプの反応性前駆体、例えば二つの反応性前駆体から形成される場合、反応性前駆体は、第一および第二反応性前駆体と称されうる。一つより多くの反応性前駆体が利用される場合には、ある実施形態では、反応性ヒドロゲル前駆体の少なくとも一つは架橋剤であり得、少なくとも一つの他の反応性ヒドロゲル前駆体は高分子であり得、本明細書において「官能性ポリマー」と称されうる。
【0018】
いくつかの実施形態においては、反応性前駆体は、前駆体が混合されると自然に架橋するが、堆積プロセスの間は一つより多くの前駆体が個々に安定している、生体適合性の複数前駆体系を含みうる。反応性前駆体が反応を許容する(例えばpHまたは溶媒に関して)環境において混合されると、官能基が互いに反応して共有結合を形成する。反応性前駆体の少なくともいくつかが他の二つ以上の前駆体と反応できるときに、反応性前駆体が架橋する。例えば、二つの第一タイプの官能基をもつ前駆体を、第一タイプの官能基と反応できる少なくとも三つの第二タイプの官能基をもつ架橋前駆体と反応させうる。
【0019】
このような反応成分は、例えば、求電子基を有する第一反応性前駆体と、求核基を有する第二反応性前駆体とを含む。求電子剤は、求核剤と反応して共有結合を形成する。共有結合架橋または共有結合は、異なるポリマーを互いに共有結合する働きをする異なるポリマー上の官能基の反応により形成される化学基をさす。ある実施形態では、第一反応性前駆体上の第一求電子官能基組が、第二反応性前駆体上の第二求核官能基組と反応しうる。ある実施形態では、このような系は、二官能性アルキレンオキシドまたは多官能性アルキレンオキシド含有部分を含む第一反応性前駆体と、二官能性アミンまたは多官能性アミンであるマクロマーを含む第二反応性前駆体とを含む。
【0020】
ある実施形態では、反応性ヒドロゲル前駆体は多官能性でありうる、すなわち、例えば第一反応性ヒドロゲル前駆体上の求電子官能基が第二反応性ヒドロゲル前駆体上の求核官能基と反応して共有結合を形成しうるように、二つ以上の求電子または求核官能基を含みうる。求電子−求核反応の結果として前駆体が結合して架橋ポリマー産物を形成するように、第一または第二反応性ヒドロゲル前駆体の少なくとも一つが、二つ以上の官能基を含む。
【0021】
ある実施形態では、求核および求電子反応性前駆体の両者が架橋反応において用いられる限りにおいて、第一および第二反応性ヒドロゲル前駆体の各々が、一つのカテゴリの官能基だけ、求核基だけまたは求電子官能基だけを含む。したがって、例えば、第一反応性ヒドロゲル前駆体がN−ヒドロキシスクシンイミド等の求電子官能基を有する場合には、第二反応性ヒドロゲル前駆体がアミン等の求核官能基を有しうる。一方で、第一反応性ヒドロゲル前駆体がスルホスクシンイミド等の求電子官能基を有する場合には、第二反応性ヒドロゲル前駆体がアミンまたはチオール等の求核官能基を有しうる。
【0022】
ある実施形態では、複数のNHS基により官能基化されたマルチアームPEG等の多官能性求電子性ポリマーが、第一反応性ヒドロゲル前駆体として用いられ、トリリジン等の多官能性求核性ポリマーが、第二反応性ヒドロゲル前駆体として用いられうる。複数のNHS基により官能基化されたマルチアームPEGは、例えば、4、6または8のアームと、約5,000〜約25,000の分子量を有しうる。適切な第一および第二反応性ヒドロゲル前駆体の他の例は、米国特許第6,152,943号;第6,165,201号;第6,179,862号;第6,514,534号;第6,566,406号;第6,605,294号;第6,673,093号;第6,703,047号;第6,818,018号;第7,009,034号;および第7,347,850号に記載されており、その各々の開示の全体が参照により本明細書に組み込まれる。
【0023】
例えば様々な組織に対する粘着、外科医が正確かつ都合よくin situ形成ヒドロゲル前駆体を配置することを可能にする望ましい硬化時間、生体適合性のための高い含水量、シーラントに用いるための機械的強度、および/または配置後の破壊に抵抗するための靭性を含む、ヒドロゲル前駆体の特定の性質が有用でありうる。したがって、直ちに殺菌され、天然材料の使用に伴いうる疾患感染の危険性を回避する合成材料が、使用されうる。実際に、例えばFOCALSEAL(登録商標)(Genzyme,Inc.)、COSEAL(登録商標)(Angiotech Pharmaceuticals)、およびDURASEAL(登録商標)(Confluent Surgical,Inc)等の市販の製品において用いられるような合成前駆体を用いて作られる特定の重合可能なヒドロゲルが、当業者の認識範囲内である。他の周知のヒドロゲルには、例えば米国特許第6,656,200号;第5,874,500号;第5,543,441号;第5,514,379号;第5,410,016号;第5,162,430号;第5,324,775号;第5,752,974号;および第5,550,187号に開示されるものが含まれる。
【0024】
反応性前駆体から架橋ポリマーヒドロゲルを形成するための反応条件は、使用される反応性前駆体の性質に依存しうる。ある実施形態では、緩衝水溶液において約5〜約12のpHで反応が行われる。バッファーには、例えば、ホウ酸ナトリウムバッファー(pH10)およびトリエタノールアミンバッファー(pH7)が含まれる。いくつかの実施形態においては、エタノールまたはイソプロパノール等の有機溶剤が、反応速度を改善し、または所与の製剤の粘性を調整するために加えられうる。
【0025】
ヒドロゲル前駆体が合成である場合(例えば、ポリアルキレンオキシドベースである場合)、モル等量の反応物を用いることが所望されうる。場合によっては、官能基の加水分解による反応等の副反応を補うために、モル過剰の架橋剤が加えられうる。
【0026】
反応性前駆体、ある実施形態では架橋剤および架橋可能ポリマーを選択するときには、ポリマーの少なくとも一つが、一分子あたり二つより多くの官能基と、もたらされるヒドロゲルが生分解可能であることが望ましい場合には少なくとも一つの分解可能領域とを有しうる。ある実施形態では、各反応性ポリマー前駆体は、二つより多くの官能基を有し得、ある実施形態では、四つより多くの能基を有しうる。
【0027】
反応性前駆体から形成される、もたらされる生体適合性の架橋ポリマーの架橋密度は、前駆体、ある実施形態では架橋剤および官能性ポリマーの全体の分子量、および一分子あたりにつき利用可能な官能基の数により制御されうる。600Da等の架橋間のより低い分子量からは、10,000Da等のより高い分子量と比較して、はるかに高い架橋密度が得られる。3000Da以上の分子量のより高分子量の官能性ポリマーにより、弾性ゲルが得られる。
【0028】
架橋密度は、溶液中の前駆体、ある実施形態では架橋剤および官能性ポリマーの全体の固形分によっても制御されうる。固形分を増加させることにより、単位体積あたりの架橋可能基の数および潜在的架橋密度が増加する。架橋密度を制御するさらにもう一つの方法は、求核基の求電子基に対する化学量を調節することによる。1対1の比は最大の架橋密度をもたらしうるが、反応性官能基の他の比(例えば、求電子剤:求核剤)は所望の製剤に適合すると想定される。
【0029】
ある実施形態では、第一反応性前駆体は、マルチアームPEGであり得、ビニル基を含む開環無水物により官能基化されNHSでエンドキャップされうる。第二反応性前駆体は、多官能性アミン成分でありうる。開示のヒドロゲルは、このように少なくとも二つの前駆体から形成されうる。
【0030】
いくつかの実施形態では、上記のように、ヒドロゲル前駆体が開始性前駆体を含みうる。本開示による使用のための開始性前駆体は、エチレン性不飽和の官能基を有しうる。このようなエチレン性不飽和の官能基を有するこのような前駆体は、上述のように生物学的に不活性および水溶性のコアを有しうる。このようなコアは、当業者の認識範囲内の任意の手段により官能基化されうる。
【0031】
エチレン性不飽和の官能基、ある実施形態ではビニル基は、重合反応を開始するために開始剤を用いて重合されうる。少なくとも二つのエチレン性不飽和の官能基を伴う前駆体が、架橋ポリマーを形成しうる。いくつかの組成物は、そのような官能基を一つだけ有するある前駆体と、前駆体を架橋するための複数の官能基を有する追加的な架橋前駆体とを有する。エチレン性不飽和の官能基は、様々な技術、例えばフリーラジカル重合、縮合重合、または付加重合により、重合されうる。本開示により使用されうる例示的な開始性前駆体には、アクリレート類;無水イタコン酸、無水マレイン酸、無水シトラコン酸、それらの組み合わせなど等の、ビニル基含有無水物類が含まれる。他の例示的な開始性前駆体には、例えば、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率をもつビニルモノマー、シロキサン官能性ビニル化合物、ビニル基をもつポリエチレングリコール−シリコーンコモノマー、トリアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、それらの組み合わせなどが含まれる。
【0032】
開始性前駆体の重合に利用される好適な開始剤には、熱開始剤、光活性化開始剤、酸化還元(レドックス)系、フリーラジカル開始剤、放射、熱開始系、それらの組み合わせなどが含まれるがこれに限られない。ある実施形態では、適切な放射源には、熱、可視光、紫外(UV)光、ガンマ線、電子ビーム、それらの組み合わせなどが含まれる。ある実施形態では、光開始剤も使用されうる。このような光開始剤には、フリーラジカル開始剤、臭素酸鉄等のレドックス開始剤、過硫酸アンモニウム/酢酸、過硫酸アンモニウム−テトラメチルジアミン、過硫酸カリウム/VA044(Wako Chemicals Inc.,Richmond VA)などが含まれるがこれに限られない。UV光も、色素媒介光酸化、グルタルアルデヒド架橋、デキサメチレン(dexamethylene)ジイソシアネート架橋、カルボジイミド架橋、それらの組み合わせなどとともに使用されうる。
【0033】
ある実施形態では、ヒドロゲルを生分解可能または吸収可能にするために、官能基の間に存在する生分解可能な結合を有する一つ以上のヒドロゲル前駆体が含まれうる。いくつかの実施形態では、これらの結合は、例えば、生理溶液において加水分解されうるエステルでありうる。このような結合の使用は、タンパク分解作用により分解されうるタンパク質結合と対照的である。生分解可能な結合は、ヒドロゲル前駆体の一つ以上の水溶性コアの一部も形成しうる。代替的または追加的に、ヒドロゲル前駆体の官能基が、それら間の反応の生成物から生分解可能な結合がもたらされるように、選択されうる。各アプローチにおいて、もたらされる生分解可能な生体適合性の架橋ポリマーが所望の時間内で分解または吸収されるように、生分解可能な結合が選択されうる。一般に、生理学的条件下でヒドロゲルを非毒性または低毒性産物に分解させる生分解可能な結合が選択されうる。
【0034】
上述の生分解可能な架橋剤または小分子が、アルブミン、他の血清タンパク質類、および/または血清濃縮物等のタンパク質類と反応させられて、架橋ポリマーネットワークが生成されうる。一般に、架橋剤の水溶液がタンパク質類の濃縮溶液と混合されて、架橋ヒドロゲルが生成されうる。架橋ステップの間に緩衝剤、例えばホウ酸塩バッファーまたはトリエタノールアミンを加えることにより、反応が加速されうる。
【0035】
ゲル化につながる架橋反応は、ある実施形態では、約1秒〜約5分以内、ある実施形態では約3秒〜約1分で生じうる。通常の技術を有する当業者は、これらの明示される範囲内のすべての範囲および値が企図されることを即座に理解する。場合によっては、10秒未満でゲル化が生じうる。
【0036】
架橋ヒドロゲルの分解は、架橋剤の生分解可能なセグメント、ならびにヒドロゲルが曝露される任意の酵素に依存しうる。一切の分解酵素の非存在下では、架橋ポリマーは、生分解可能なセグメントの加水分解だけにより分解しうる。分解速度は、水溶性コアを形成するポリマーに、特に形成される任意のエステル結合の構造および位置に依存しうる。例えば、開環重合においてエステル結合が形成されうる。開環重合は、例えば、PEGと、環状エステルまたは例えばフラン−2,5−ジオン、1,4−ジオキサン−2,5−ジオン、グルタル酸無水物、コハク酸無水物、マレイン酸無水物、イタコン酸無水物、メチルコハク酸無水物、2,2−ジメチルコハク酸無水物、2ドデセン−1−イルコハク酸無水物、シス−1,2,3,6−テトラヒドロフタル酸無水物、シトラコン酸無水物、2,3−ジメチルマレイン酸無水物、1−シクロペンテン−1,2−ジカルボン酸無水物、3,4,5,6−テトラヒドロフタル酸無水物、3エチル−3−メチルグルタル酸無水物、3,3−ジメチルグルタル酸無水物、3−メチルグルタル酸無水物、それらの組み合わせなどを含む無水物との間に起こりうる。そして、もたらされるポリマーが、ある実施形態ではスクシンイミド基で官能基化された後、本開示のヒドロゲルを形成するために反応性前駆体として利用されうる(例えばアミン等の架橋剤と組み合わせることによる)。開環重合のためPEGと組み合わせられるモノマー、およびこうしてもたらされる分解可能なエステル基が、in vivoのヒドロゲルの持久性に影響する。この反応性前駆体を形成するために使用されるモノマーの固形分およびアーム長も、その分解速度に影響しうる。
【0037】
例えば、ある実施形態では、生成物は、PEGとグルタル酸無水物、イタコン酸無水物、メチルコハク酸無水物、2,2−ジメチルコハク酸無水物、2ドデセン−1−イルコハク酸無水物、シス−1,2,3,6−テトラヒドロフタル酸無水物、シトラコン酸無水物、2,3−ジメチル無水マレイン酸、1−シクロペンテン−1,2−ジカルボン酸無水物、3,4,5,6−テトラヒドロフタル酸無水物、3エチル−3−メチルグルタル酸無水物、3,3−ジメチルグルタル酸無水物、3−メチルグルタル酸無水物、それらの組み合わせなど等の無水物を含む第二成分との間の開環重合でありうる。もたらされる生成物は、約6週〜約8週の期間にわたり分解するヒドロゲルを形成しうる。
【0038】
他の実施形態においては、PEGとコハク酸無水物の間の開環重合の生成物は、約2日〜約7日の期間にわたり分解しうる。PEGおよびマレイン酸無水物が使用される実施形態においては、生成物は約6ヵ月の期間にわたり分解しうる。開環マレイン酸無水物のビニル基は、二次的ビニル重合に関係しうる。したがって、ある実施形態では、開環マレイン酸無水物のビニル基が、開始性前駆体として働きうる。
【0039】
オリゴヒドロキシ酸ブロック等の生分解可能ブロックにより生成される疎水性またはPLURONICまたはTETRONICポリマーにおけるPPOブロックの疎水性は、小さな有機薬物分子の溶解において有用でありうる。生分解可能または疎水性のブロックの取り込みにより影響される他の性質には、吸水性、機械的性質、および温度感受性が含まれる。
【0040】
合成架橋ゲルは、生分解可能領域の加水分解により分解する。合成ペプチド配列を含むゲルの分解は、配列の分解に必要な特定の酵素およびその濃度に依存しうる。場合によっては、分解プロセスを加速するために、架橋反応の間に特定の酵素が加えられうる。
【0041】
ヒドロゲル前駆体は、使用前に溶液中に配置され、溶液が組織に送達されうる。二つの溶液が使用される場合には、各溶液に、接触時に互い反応しうる一つ以上の前駆体が含まれうる。溶液は別々に貯蔵され、組織に送達されるときに混合されうる。
【0042】
in situ形成材料系の一部として利用されるいずれの溶液も、有害または有毒の溶媒を含んではならない。ある実施形態では、前駆体(単数または複数)は、緩衝等張食塩水等の生理学的適合性の溶液における適用を可能にするために、水等の溶媒において実質的に可溶性でありうる。水溶性コーティングは薄膜を形成しうるが、ある実施形態では、厚みの制御された三次元ゲルを形成してもよい。ゲルも、身体から回収される必要がないように生分解可能でありうる。本明細書で用いられるところの「生分解可能」という用語は、生体吸収性材料および生体再吸収性材料の両者を含むものと定義される。生分解可能とは、分解生成物が排出可能または身体に吸収可能であるように、材料が分離し、または身体環境下で構造的完全性を失うこと(例えば酵素的分解または加水分解)、または体内の生理学的条件下で崩壊させられる(物理的または化学的に)ことを意味する。
【0043】
様々な用途で、ヒドロゲルの異なる特徴が必要とされうる。一般に、ヒドロゲル前駆体は、示される生体適合性および毒性の欠如をもとに選択されなければならない。
【0044】
ある実施形態では、ヒドロゲルは、(例えばフリーラジカル重合により架橋できる)少なくとも一つの反応性前駆体と、少なくとも一つの開始性前駆体とから形成され、または、前駆体の一つ以上が架橋に参加してin situ形成材料を形成する、三つ以上の前駆体により作られうる。
【0045】
ヒドロゲル形成の前に、開始性前駆体、ある実施形態では直鎖状PEGアクリレートが、約7〜約11、ある実施形態では約8〜約10のpHを有する高pHのバッファー、例えばホウ酸ナトリウム中で再構成されうる。開始性前駆体、ある実施形態では求電子性官能基を有するマルチアームPEGが、約3〜約6、ある実施形態では約4〜約5のpHを有するリン酸ナトリウム等の低pHのバッファーにより再構成されうる。
【0046】
ある実施形態では、直鎖状PEGアクリレートが開始性前駆体として使用されうる。したがってある実施形態では、第一反応性ヒドロゲル前駆体、第二反応性ヒドロゲル前駆体および開始性前駆体を接触させることにより、ヒドロゲルが形成されうる。第一反応性前駆体および第二反応性前駆体の反応時に、ヒドロゲルが形成しうる。開始性前駆体を架橋し、これによってより高密度のヒドロゲルを作製するために、成分が開始剤に曝露されてもよい。
【0047】
ある実施形態では、もたらされるヒドロゲルが、相互貫通ネットワークを形成しうる。ある実施形態では、相互貫通ネットワークは、二つのヒドロゲルネットワーク、すなわち開始性前駆体と組み合わされた少なくとも二つの反応性前駆体により形成されるヒドロゲルより形成されうる。他の実施形態においては、相互貫通ネットワークは、反応基も有する開始性前駆体から形成されうる。このような前駆体は、他の反応性前駆体と反応できるとともに、開始剤への曝露時に反応開始されうる。
【0048】
例えば、ある実施形態では、マルチアームPEGとトリリジンの間に第一ヒドロゲルが形成しうる。エチレン性不飽和のモノマーを開始剤に曝露することにより、第二ヒドロゲルが形成されうる。これらの二つのヒドロゲルが、開始剤への曝露の前に組み合わされうる。これらのヒドロゲルの開始剤への曝露から、ヒドロゲルの相互貫通ネットワークがもたらされ、その各々が様々な分解速度等、別々の性質を有しうる。さらに、反応性前駆体および開始性前駆体の量を変化させることにより、もたらされる組成物の性質が異なりうる。
【0049】
他の実施形態においては、マルチアームPEGがビニル基により官能基化され、トリリジンと反応させられて第一ヒドロゲルが形成されうる。ビニル基により官能基化されたPEGを開始剤により反応開始させることにより、ビニル基の架橋によりヒドロゲルの架橋が増加し得、これにより相互貫通ネットワークが形成されうる。他の実施形態においては、ビニル基により官能化されたマルチアームPEGが、限定的にアミンと反応し、その後開始剤が加えられてビニル基の架橋が増加されうる。
【0050】
反応性前駆体が第一ヒドロゲルを形成し、開始性前駆体が第二ヒドロゲルを形成し、二つのヒドロゲルが合わさって相互貫通ネットワークを形成する場合、ある実施形態では、反応性前駆体から形成される第一ヒドロゲルが、開始性前駆体から形成される第二ヒドロゲルよりも急速に分解し、これにより、例えば組織内部成長、血管新生、それらの組み合わせなどによる治癒を可能にする空間を形成しうる。
【0051】
ある実施形態では、様々な分解度の相互貫通(interpretation)ネットワークを有する本開示のヒドロゲルは、組織足場として働き、これにより組織集積/内部成長の手段を提供しうる。組織足場は、成長および発達成分を伴う細胞も提供できる。したがって、本開示のヒドロゲルが組織足場として利用される場合には、それは、必要な栄養分および生物活性剤を周囲組織に提供することにより本来の組織の再成長を助けうる。いくつかの実施形態においては、本明細書に記載のように、ヒドロゲル自体がコラーゲン、ゼラチン、ヒアルロン酸、それらの組み合わせなど等の天然成分を含み得、したがって、組織足場が分解するに伴い天然成分が放出され、あるいは移植部位で分解しうる。
【0052】
他の実施形態においては、本開示のヒドロゲル組成物は、一方が他方の中に分散された、二つのヒドロゲルを有しうる。例えば、ある実施形態では、本開示の組成物は、反応性前駆体から形成される第一ヒドロゲルを含み得、当該第一ヒドロゲルの中には少なくとも一つの分散領域を伴い、当該分散領域が、開始性前駆体から形成される第二ヒドロゲルにより形成される。他の実施形態においては、反応性前駆体で形成される第一ヒドロゲルが、開始性前駆体から形成される第二ヒドロゲルの中に、少なくとも一つの分散領域を形成しうる。一つのヒドロゲルにより形成される分散領域が、第二ヒドロゲル中に一つの領域、例えば中心領域またはコアを形成し得、または一つのヒドロゲルにより形成される分散領域が、第二ヒドロゲル中にたくさんの小領域を形成しうる。
【0053】
反応性前駆体および開始性前駆体の濃度を変化させることにより、もたらされるヒドロゲルの性質が異なりうる。例えば、ある実施形態では、溶液が、約200g/モル〜約50,000g/モル、ある実施形態では約500g/モル〜約35,000g/モルの分子量を有するアクリレートを、約5g/ml〜約40g/ml、ある実施形態では約10g/ml〜約20g/mlの濃度で含みうる。溶液は、約5mg/ml〜約100mg/ml、ある実施形態では約10mg/ml〜約20mg/mlの濃度で、光開始剤も含みうる。光開始剤は、例えば、4,4’−ビス(ジエチルアミノ)ベンゾフェノン、2,2−ジメトキシ−2−フェニルアセトフェノン、カンファーキノン/4−ジメチルアミノ安息香酸、エオシン、アゾビスイソブチロニトリル(AIBN)、ジメトキシベンゾフェノン、それらの組み合わせなどでありうる。アクリレート/光開始剤溶液は約4.25%〜約17%、ある実施形態では約6%〜約14%、ある実施形態では約8.5%の濃度を有しうる。ある実施形態では、アクリレート/光開始剤溶液は、約0.05g/ml〜約2g/ml、ある実施形態では約0.1g/ml〜約1g/ml、ある実施形態では約0.26g/mlの濃度でリン酸ナトリウムバッファー中にありうるマルチアームPEGと組み合わせられうる。これらの溶液が反応して、本開示のヒドロゲルを形成しうる。
【0054】
先述のように、反応性前駆体への開始性前駆体の付加およびその後の開始剤への曝露により、もたらされるヒドロゲルの性質が変更されうる。さらに、反応性前駆体に対する開始性前駆体の比が、機械的性質に影響しうる。図4にグラフで描写され、下表1にリストされるように、反応性前駆体および開始性前駆体の混合物中に存在する開始性前駆体の割合が、反応性ヒドロゲルの架橋後のヒドロゲルの強度に大きく影響する。
【0055】
【表1】

したがって、本開示によれば、反応性前駆体の反応と開始性前駆体の開始という、二つの異なる機構によりヒドロゲルが形成されうる。したがって、もたらされるヒドロゲルは、同様に二つの異なるヒドロゲルで作られうる。例えば、第一ヒドロゲルが反応性前駆体から形成されうる一方で、第二ヒドロゲルが開始性前駆体から形成されうる。
【0056】
第一ヒドロゲルは、約10%〜約30%、ある実施形態では約15%〜約25%の量の第一反応性前駆体と、約70%〜約90%、ある実施形態では約75%〜約85%の量の第二反応性前駆体とを含みうる。他の実施形態においては、第一ヒドロゲルは、約70%〜約90%、ある実施形態では約75%〜約85%の量の第一反応性前駆体と、約10%〜約30%、ある実施形態では約15%〜約25%の量の第二反応性前駆体とを含みうる。
【0057】
本開示の組成物を形成するために利用される材料のモジュラスは、組成物の最終用途に依存しうる。例えば、組織足場として使用するために組織に適用される組成物は、医療デバイスを組織に付着させるための使用を目的とする組成物よりもずっと低いモジュラスを有しうる。
【0058】
ある実施形態では、反応性前駆体から形成される第一ヒドロゲルは、約5キロパスカル(kPa)〜約90kPa、ある実施形態では約10kPa〜約50kPaのモジュラスを有し、開始性前駆体から形成される第二ヒドロゲルは、約50kPa〜約5,000kPa、ある実施形態では約100kPa〜約4,000kPaのモジュラスを有しうる。
【0059】
もたらされるヒドロゲルの分解速度に応じて、反応性前駆体により形成されるヒドロゲルの部分が、開始性前駆体により形成されるヒドロゲルの部分よりも急速に分解し得、これにより、組織内部成長、視覚化などを可能にしうる空間がヒドロゲル中に形成されうる。ある実施形態では、反応性前駆体から形成される第一ヒドロゲルは、約1週〜約12週、ある実施形態では約4週〜約10週の期間にわたり分解しうる一方、開始性前駆体から形成される第二ヒドロゲルは、少なくとも約2週の期間にわたり分解し、ある実施形態では分解しない、すなわち永久に体内に残りうる。いくつかの実施形態において、第二ヒドロゲルは、少なくとも約6ヵ月の期間にわたり分解しうる。いくつかの実施形態において、第二ヒドロゲルは、約6週〜約6ヵ月の期間にわたり分解しうる。
【0060】
第二ヒドロゲルが第一ヒドロゲルの上にバリヤ層を形成する場合には、第一ヒドロゲルは約5kPa〜約60kPa、ある実施形態では約10kPa〜約50kPaのモジュラスを有し得、バリヤ層を形成する第二ヒドロゲルは、約100kPa〜約1,000kPa、ある実施形態では約200kPa〜約900kPaのモジュラスを有しうる。したがって、第一ヒドロゲルは約1日〜約7日、ある実施形態では約2日〜約6日の期間にわたり分解し得、バリヤ層は少なくとも約6ヵ月、ある実施形態では約6ヵ月〜約12ヵ月の期間にわたり分解しうる。
【0061】
ヒドロゲルが相互貫通ネットワークを形成する場合には、第一ヒドロゲルが約5kPa〜約20kPa、ある実施形態では約8kPa〜約17kPaのモジュラスを有し、第二ヒドロゲルは約50kPa〜約500kPa、ある実施形態では約75kPa〜約400kPaのモジュラスを有しうる。
【0062】
ヒドロゲルが医療デバイスを組織に付着させるための付着デバイスを形成するために用いられる場合には、第一前駆体が約10kPa〜約50kPa、ある実施形態では約15kPa〜約45kPaのモジュラスを有し得、第二ヒドロゲルが約60kPa〜約200kPa、ある実施形態では約75kPa〜約175kPaのモジュラスを有しうる。第二ヒドロゲルを形成する開始性前駆体は、付着デバイスの約40重量%〜約90重量%、ある実施形態では付着デバイスの約50重量%〜約75重量%の量で存在しうる。第一ヒドロゲルは約1日〜約7日、ある実施形態では約2日〜約6日の期間にわたり分解し得、第二ヒドロゲルは少なくとも約6ヵ月、ある実施形態では約6ヵ月〜約12ヵ月の期間にわたり分解しうる。
【0063】
本開示の組成物が生物活性剤を送達するために用いられる場合には、第一ヒドロゲルが約5kPa〜約50kPa、ある実施形態では約10kPa〜約40kPaのモジュラスを有し得、第二ヒドロゲルが約10kPa〜約100kPa、ある実施形態では約20kPa〜約80kPaのモジュラスを有しうる。
【0064】
ある実施形態では、一つの反応性前駆体と一つの開始性前駆体が第一溶液中に配置されればよく、第二反応性前駆体および任意の開始性前駆体が第二溶液中に配置されうる。これらの溶液の混合時には、反応性前駆体が架橋してベースヒドロゲルを形成しうるが、開始性前駆体は開始剤に曝露されるまで架橋しえない。他の実施形態においては、一つの反応性前駆体および一つ以上の開始性前駆体(単数または複数)が第一溶液中に配置されればよく、第二反応性前駆体が第二溶液中に配置されうる。
【0065】
反応性前駆体および開始性前駆体の組み合わせからもたらされるヒドロゲルの密度は、ヒドロゲルを形成するために使用される開始剤に基づいて、さらに制御されうる。例えば、NHSでキャップされたマルチアームPEG第一反応性ヒドロゲル前駆体、多官能性アミン第二反応性ヒドロゲル前駆体、および直鎖状PEGアクリレート開始性前駆体からは、未反応アクリレート基を含むヒドロゲルがもたらされうる。開始剤、ある実施形態ではUV光に対する曝露時には、アクリレート基がそれ自体とだけでなくPEGアームの末端と反応しうる。開始剤に対する曝露を制御することにより、このようにある量のアクリレート架橋を用いてヒドロゲルの密度をさらに調整しうる。
【0066】
ヒドロゲル密度の調整は、もたらされるヒドロゲルの浸透性に影響し得、例えば、より高密度のヒドロゲルは浸透性がより低くなりうる。ある実施形態では、開始性前駆体(単数または複数)が高密度に架橋され、その結果、反応性前駆体から形成されるヒドロゲル内または外面上に、浸透性がより低いバリヤ層を形成し、このようにして複合ヒドロゲル組成物が形成されうる。
【0067】
本開示によれば、開始性前駆体から形成されるポリマーは、もたらされる複合ヒドロゲルの約5重量パーセント〜約30重量パーセント、ある実施形態ではもたらされるヒドロゲルの約10重量パーセント〜約20重量パーセントを占めればよく、反応性前駆体から形成されるポリマーが、もたらされるヒドロゲルの約5重量パーセント〜約60重量パーセント、ある実施形態ではもたらされるヒドロゲルの約15重量パーセント〜約40重量パーセントを占めうる。もたらされるヒドロゲルの残部は、液体/水からなる。
【0068】
本開示のヒドロゲルの形成は、in situで起こりうる。他の実施形態においては、ヒドロゲル形成はex vivoで、すなわちin situ配置の前に起こりうる。反応性前駆体の開始性前駆体との組み合わせにより、両方のタイプの架橋前駆体の性質を示すヒドロゲルの形成が可能になる。いくつかの実施形態においては、ヒドロゲルの表面を開始剤に曝露する前に、ヒドロゲルが組織欠損内で望ましい形に成形されうる。
【0069】
In situ形成は、一般に、組織への適用時に活性化されて架橋ヒドロゲルを形成しうるヒドロゲル前駆体を有することにより達成されうる。活性化は、組織への前駆体適用前、適用中、または適用後に行われうる。活性化には、例えば、重合プロセスを誘導するステップ、フリーラジカル重合を開始するステップ、または互いに反応する官能基を有する前駆体を混合するステップを含む。したがって、in situ重合には、化学部分の活性化による共有結合の形成と、材料が患者上、患者内、または患者上および患者内の両方に配置される予定の位置での、不溶性物質、例えばヒドロゲルの作製が含まれる。In situ重合可能ポリマーは、患者内でポリマーを形成するように反応させられうるヒドロゲル前駆体から調製されうる。上記のように、ある実施形態では、反応性前駆体および開始性前駆体の両者からヒドロゲルが形成されうる。
【0070】
前述のように、ヒドロゲル前駆体が使用前に溶液中に配置され、溶液が患者に送達されうる。ある実施形態では、前駆体は、緩衝等張食塩水等の生理学的適合性の溶液における適用を可能にするために、実質的に水溶性でありうる。米国特許第4,874,368号、第4,631,055号;第4,735,616号;第4,359,049号;第4,978,336号;第5,116,315号;第4,902,281号;第4,932,942号;第6,179,862号;第6,673,093号;第6,152,943号;および第7,347,850号に記載されているもの等の二重シリンジまたは類似のデバイスを使用して、前駆体溶液を適用しうる。
【0071】
一般に、二つ以上のヒドロゲル前駆体が、噴霧器を介して組織に適用されて、in situでコーティングが形成されうる。例えば、少なくともうち一つが開始性前駆体を含む二つの反応性前駆体溶液が、噴霧器の別々のチャンバ内に配置されうる。噴霧器が作動されると、出てきたスプレーが組織に接触し、二つの反応性前駆体の混合および架橋が生じて、組織表面にコーティング(例えばヒドロゲル)が形成される。
【0072】
ある実施形態では、噴霧器は、二つ以上の反応性前駆体溶液の各々のための別々のスプレーノズルを含み、各ノズルが別々または共通のガス流出口に囲まれている。反応性前駆体溶液は、別々の区画、例えばマルチシリンダシリンジ中に貯蔵され、圧力下でスプレーノズルに移される。ガス流出口を通るガス流の存在下で、架橋可能溶液が霧化され、ガス流中で混合されてスプレーを形成し、これを用いて組織がコーティングされうる。ある実施形態では、CO2ガスカートリッジが、前駆体の送達を促進するために、可逆的または永久にデバイス上に装備されうる。
【0073】
ある実施形態は、吸引−洗浄装置をヒドロゲル前駆体送達デバイスと組み合わせるステップを含む。このような組み合わせの利点は、凝固血および接着イオジェニック(adhesioniogenic)材料を組織から洗浄でき、組み合わせることにより単一のデバイスを用いたヒドロゲルの配置が可能になりうることである。
【0074】
本開示のヒドロゲルは、例えば接着剤、止血剤、シーラント、移植物、保護バリヤ、薬物送達デバイス、それらの組み合わせなど等の要素を形成するためにも使用されうる。形成されうる移植物には、例えば、マトリックス、人工血管、心臓弁、人工臓器、人工骨、移植可能微小凸レンズ、血管グラフト、ステント、縫合糸、ステープル、クリップ、メッシュ、スリング、ネジ、ピン、ケーブル、軟骨移植物、脊椎移植物およびそれらの組み合わせが含まれる。移植物は、哺乳類の体内の軟組織または硬組織を増強するためにも使用されうる。軟組織増強の用途の例には、括約筋(例えば泌尿器、肛門、食道)増強;人工皮膚としての使用;皮膚のしわの治療;および/または瘢痕の治療が含まれる。硬組織増強の例には、骨および/または軟骨組織の修復および/または置換が含まれる。本開示のヒドロゲルおよび/または移植物で治療できる他の組織欠損には、例えば、胃食道逆流疾患(GERD)を治療するための下部食道括約筋を含む括約筋バルキング;尿失禁を治療するための尿道周囲バルキング;例えばポリープ切除術における、組織解剖および/または切除を助ける組織層間のクッション作製;癒着防止;形成手術において真皮充填材として;唇、乳房、および他の身体組織の欠損の治療;それらの組み合わせなどが含まれる。
【0075】
ある実施形態では、ヒドロゲルを用いて、開始性前駆体により生成されるヒドロゲルにより形成される剛性または高密度の外部と、反応性前駆体により生成されるヒドロゲルにより形成される、より低密度のより可撓性のある内部とを有する、半可撓性の椎間板を形成しうる。ある実施形態では、置換が必要な椎間板に類似する形に作られたテンプレートが用いられうる。テンプレートがヒドロゲル前駆体で満たされて、ヒドロゲルが形成されうる。それから、表面上の開始性前駆体の架橋を誘導するためにヒドロゲルが開始剤に曝露され、これによりヒドロゲル内部を包含する高密度の外層またはバリヤ層が形成されうる。
【0076】
椎間板移植物の形成では、手術中または手術前に移植物が形成されうる。例えば、まずキャリパまたは類似のデバイスを用いて修復される欠損の長さおよび寸法を測定することにより、手術中に適切な移植物サイズが決定されうる。それから外科スタッフは、反応性前駆体および開始性前駆体をテンプレートに導入し、反応性前駆体に第一ヒドロゲルを形成させることにより、上述のテンプレートを利用して、所望のサイズの移植物を形成しうる。それから組成物が開始剤に曝露され、これにより第一ヒドロゲル内部を包含する高密度の外層またはバリヤ層が形成され、これにより椎間板移植物が生成されうる。
【0077】
あるいは、X線、MRIなどを含む放射線撮影技術を用いて、適当な移植物のサイズが術前に決定され、手術前に椎間板移植物が上述のように形成されうる。
【0078】
他の実施形態においては、反応性前駆体が組織欠損に適用され、これにより、その中に第一ヒドロゲルを形成し、開始性前駆体がバリヤ層として機能する第二ヒドロゲルを、組織欠損をカバーする第一ヒドロゲルの表面の少なくとも一部の上に形成しうる。
【0079】
ヒドロゲルを形成するための材料の選択は、本開示のヒドロゲル組成物の最終用途に応じて調整されうる。例えば、タンパク質癒着を防止せねばならない場合にはポリエチレングリコール系ポリマーが所望され得;摺動、滑動および/または潤滑性の強化が望ましい場合にはヒアルロン酸系ポリマーが所望され得;細胞付着のための接着部位を提供するためにはコラーゲン系ポリマーが所望され得;長期および/または永久移植物などには合成ポリマーが所望されうる、などである。
【0080】
ある実施形態では、反応性ヒドロゲル前駆体は、生物活性剤を含むヒドロゲルを形成しうる。開始性前駆体が、反応前または反応後に前駆体に加えられうる。それから、開始性前駆体が反応開始されてバリヤ層を形成しうる。バリヤ層は、反応性前駆体により形成されるヒドロゲルからの生物活性剤のバリヤの方向への拡散を妨げ、これにより、生物活性剤を一方向に、すなわちバリヤ層と反対の方向に投与させる。
【0081】
ある実施形態では、反応性および開始性ヒドロゲル前駆体が、モールドの底の上の層に組み合わせられてもよい。それからベース層が開始剤に曝露されて、底層がさらに架橋されうる。それから前駆体を含む第二層が底層の上に配置され、スクリーンを用いて開始剤に対する第二層の曝露が制限されうる。こうして、遮蔽された部分は架橋しないが、遮蔽されない部分はさらに架橋し、これにより層中に様々な程度の架橋を提供しうる。追加の層は、同じまたは異なるスクリーンを用いて加えられうる。各層が、同じでも異なってもよい生物活性剤を含みうる。様々な量の架橋により、交互の分解速度が提供され、これにより生物活性剤の様々な放出速度が提供されうる。開始剤は、医療デバイスとの接触前または後に、ヒドロゲルと接触させられうる。ヒドロゲルにより組織に付着させられうる医療デバイスには、縫合糸、ステープル、タック、クリップ、リベット、それらの組み合わせなどが含まれる。
【0082】
他の実施形態においては、反応性および開始性ヒドロゲル前駆体の混合物が、メッシュ等の移植物に吹き付けられまたは適用されうる。メッシュは、開始性ヒドロゲルのための開始剤を含むフィラメント状基材でありうる。反応性ヒドロゲルが、メッシュの上にコーティングを形成しうる。コーティングは数日にわたり分解し、これにより接着が防止されうる。コーティングの分解は、メッシュに組織内部成長のための孔をつくるのにも役立ちうる。開始性ヒドロゲルは同様の分解をせず、これにより組織に対するメッシュの接着が維持される。
【0083】
他の実施形態においては、メッシュが反応性前駆体および開始性前駆体(単数または複数)と接触されればよく、反応性前駆体が第一ヒドロゲルを形成し、開始性前駆体が第二ヒドロゲルを形成して、メッシュを組織に固定しうる。ある実施形態では、第一ヒドロゲルが、第二ヒドロゲルの前に形成しうる。他の実施形態においては、第二ヒドロゲルが、第一ヒドロゲルの前に形成されうる。第一ヒドロゲルが第二ヒドロゲルの前に形成するいくつかの実施形態においては、第一ヒドロゲルは、メッシュの組織に対する一時的な接着および配置を許容して、メッシュの組織に対する再配置および再接着を可能にでき、その後に第二ヒドロゲルがメッシュの永久配置のために形成される。このような場合には、第一ヒドロゲルは、メッシュの組織に対する接着および再接着のために少なくとも10分間、ある実施形態では約10分間〜約40分間、ある実施形態では約12分間〜約25分間、粘着性を保たなければならない。この時間以後に、第二ヒドロゲルが形成されうる。
【0084】
ある実施形態では、本開示のメッシュ移植物は、フィラメント状基材の少なくとも一部の上にフィルムコーティングを有する、フィラメント状基材を含みうる。ある実施形態では、フィルムコーティングは、少なくとも一つのビニル基を有する開始性前駆体を含む凍結乾燥組成物を、求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体と求核基を含む第二反応性前駆体とを含む第一ヒドロゲルと組み合わせて含みうる。使用においては、第一ヒドロゲルが再水和されてメッシュが取り外し可能に組織に付着させられ、開始性前駆体が開始剤に曝露されて第二ヒドロゲルが形成され、メッシュが組織にしっかりと固定されうる。第一ヒドロゲルは、体液との接触、食塩水の追加、それらの組み合わせなどの時に再水和されうる。
【0085】
さらに他の実施形態においては、反応性および開始性ヒドロゲル前駆体の混合物が、組み合わせられて組織の表面下に注入されればよく、組織表面上にもプールされうる。こうして形成された組織表面下および組織表面上のヒドロゲルが、縫合糸または他の医療デバイスと接触させられうる。それから医療デバイスがヒドロゲルアンカと接触させられ、これがデバイスを組織に固定するのを助けうる。例えば、縫合糸アンカでは、ヒドロゲルが形成され、縫合糸がそれに通されうる。開始性前駆体からの第二ヒドロゲルの形成の前に、反応性前駆体が第一ヒドロゲルを形成しうる。他の実施形態においては、反応性前駆体から形成されるヒドロゲルの前に、開始性前駆体から形成されるヒドロゲルが形成されうる。
【0086】
他の実施形態においては、反応性および開始性ヒドロゲル前駆体の混合物を用いて、アンカまたはリベット等の移植物付着デバイスが形成されうる。メッシュまたは他の移植物が、前駆体により組織に固定されうる。移植物は、上述の縫合糸アンカと同様に、混合物が押し出される穴を有しうる、すなわちヒドロゲルが組織の表面下に注入され、組織をカバーする移植物の表面上にプールされうる。それから、適所に移植物を保つために反応性ヒドロゲルが形成され、移植の後に、ヒドロゲル混合物が開始剤に曝露され、移植物が組織に固定されうる。
【0087】
例えば、ある実施形態では、求電子基を有するマルチアームポリエーテルを有する第一反応性前駆体と、求核基を有する第二反応性前駆体と、少なくとも一つのビニル基を有する少なくとも一つの開始性前駆体とを含む混合物が形成されうる。メッシュが組織と接触させられ、混合物がメッシュを通して組織に注入されうる。混合物が、メッシュと接触して組織表面下および組織表面上に第一ヒドロゲルを形成しうる。開始性前駆体が開始剤と接触させられて第二ヒドロゲルが形成され、これによりメッシュを組織に付着させるための付着デバイスが形成されうる。
【0088】
ヒドロゲル前駆体(単数または複数)および/またはもたらされるヒドロゲルは、外科的手技の間のその可視性を改善するために、可視化剤を含みうる。可視化剤は、移植可能医療デバイスにおける使用に適する、色素等の様々な非毒性の着色物質から選択されうる。適切な色素は当業者の認識範囲内であり、例えば米国特許第7,009,034号に記載のような、例えばin situで形成されるヒドロゲルの厚さを視覚化するための染料を含みうる。いくつかの実施形態においては、適切な色素には、例えば、FD&Cブルー#1、FD&Cブルー#2、FD&Cブルー#3、FD&Cブルー#6、D&Cグリーン#6、メチレンブルー、インドシアニングリーン、他の着色色素、およびそれらの組み合わせが含まれうる。蛍光化合物(例えばフルオレセイン(flurescein)またはエオシン)、X線造影剤(例えばヨード化合物)、超音波造影剤、およびMRI造影剤(例えばガドリニウム含有化合物)のような追加的な可視化剤が、使用されうると想定される。
【0089】
可視化剤は、ヒドロゲル前駆体溶液中に存在しうる。着色物質は、もたらされるヒドロゲル中に取り込まれても取り込まれなくてもよい。
【0090】
可視化剤は、少量で、ある実施形態では1%重量/体積未満、ある実施形態では0.01%重量/体積未満、ある実施形態では0.001%重量/体積未満の濃度で用いられうる。
【0091】
ヒドロゲル前駆体、ならびにその反応生成物は、薬物療法または生物活性剤の送達にも用いられうる。ある実施形態では、ヒドロゲルが追加の生物活性剤でコーティングされ、またはこれを含みうる。本明細書で用いられるところの「生物活性剤」という用語は、最広義の意味で用いられ、臨床用途を有する任意の物質または物質の混合物を含む。したがって、生物活性剤は、例えば色素のように、それ自体薬理活性を有しても有しなくてもよい。あるいは、生物活性剤は、治療または予防効果を提供する任意の薬剤、組織成長、細胞成長、細胞分化に影響または関与する化合物、癒着防止化合物、免疫応答等の生物学的作用を誘発することが可能でありうる化合物であり得、または一つ以上の生物学的プロセスにおいて他の任意の役割を果たすものでもありうる。生物活性剤は、物質の任意の適切な形、例えばフィルム、粉末、液体、ゲルなどの形でヒドロゲルに適用されうると想定される。
【0092】
上記のように、マルチアームPEGまたはPEGスターを含む実施形態においては、生物活性剤が、PEGのコア、PEGのアーム、またはそれらの組み合わせに取り込まれうる。ある実施形態では、生物活性剤が、PEG鎖の反応基に付着させられうる。生物活性剤は、共有結合的に、非共有結合的に、すなわち静電的に、チオール媒介またはペプチド媒介結合を通して、またはビオチン−アジビン(adivin)化学などを使用して、結合されうる。
【0093】
本開示にしたがって利用されうる生物活性剤のクラスの例には、例えば癒着防止剤;抗菌物質;鎮痛剤;解熱剤;麻酔剤;抗てんかん剤;抗ヒスタミン剤;抗炎症剤;心臓血管薬;診断用剤;交感神経作用剤;コリン性作用剤;抗ムスカリン剤;抗痙攣剤;ホルモン類;成長因子;筋弛緩剤;アドレナリン作動ニューロン遮断剤;抗腫瘍剤;免疫原性剤;免疫抑制剤;胃腸薬;利尿剤;ステロイド類;脂質類;リポ多糖類;多糖類;血小板活性化剤;凝血因子;および酵素が含まれる。生物活性剤の組み合わせが使用されうることも企図される。
【0094】
ヒドロゲル、ある実施形態ではヒドロゲル移植物と、周囲組織との間に癒着が形成するのを防ぐために、癒着防止剤が使用されうる。これらの薬剤のいくつかの例には、ポリ(ビニルピロリドン)、カルボキシメチルセルロース、ヒアルロン酸、ポリエチレンオキシド、ポリビニルアルコール類、およびそれらの組み合わせ等の親水性ポリマーが含まれるがこれに限られない。
【0095】
生物活性剤として含まれうる適切な抗菌剤には、トリクロサン、別名2,4,4’−トリクロロ−2’−ヒドロキシジフェニルエーテル;クロルヘキシジンならびに酢酸クロルヘキシジン、グルコン酸クロルヘキシジン、塩酸クロルヘキシジン、および硫酸クロルヘキシジンを含むその塩類;銀ならびに酢酸銀、安息香酸銀、炭酸銀、クエン酸銀、ヨウ素酸銀、ヨウ化銀、乳酸銀、ラウリン酸銀、硝酸銀、酸化銀、パルミチン酸銀、プロテイン銀およびスルファジアジン銀を含むその塩類;ポリミキシン;テトラサイクリン;トブラマイシンおよびゲンタマイシン、リファンピシン、バシトラシン、ネオマイシン、クロラムフェニコール、およびミコナゾール等のアミノグリコシド類;オキソリン酸、ノルフロキサシン、ナリジキシン酸、ペフロキサシン、エノキサシンおよびシプロフロキサシン等のキノロン類;オキサシリンおよびピプラシル等のペニシリン類;ノノキシノール9;フシジン酸;セファロスポリン類;およびそれらの組み合わせが含まれる。加えて、ウシラクトフェリンおよびラクトフェリシンB等の、抗菌タンパク質類およびペプチド類が、生物活性剤として含まれうる。
【0096】
生物活性剤として含まれうる他の生物活性剤には、局所麻酔剤;非ステロイド性抗受精剤;副交感神経作動剤;精神治療剤;精神安定剤;鬱血除去剤;催眠鎮静剤;ステロイド類;スルホンアミド類;交感神経様作動剤;ワクチン類;ビタミン類;抗マラリア剤;抗片頭痛剤;L−ドーパ等のパーキンソン病治療剤;抗痙攣剤;抗コリン作用剤(例えばオキシブチニン);鎮咳剤;気管支拡張剤;冠状血管拡張剤およびニトログリセリン等の心臓血管剤;アルカロイド類;鎮痛剤;コデイン、ジヒドロコデイノン、メペリジン、モルヒネなど等の麻酔剤;サリチル酸類、アスピリン、アセトアミノフェン、d−プロポキシフェンなど等の非麻酔剤;ナルトレキソンおよびナロキソン等のオピオイド受容体アンタゴニスト類;抗癌剤;抗痙攣剤;制吐剤;抗ヒスタミン剤;ホルモン剤、ヒドロコルチゾン、プレドニソロン、プレドニゾン、非ホルモン剤、アロプリノール、インドメタシン、フェニルブタゾンなど等の抗炎症剤;プロスタグランジン類;細胞毒;化学療法剤、エストロゲン類;抗菌剤;抗生物質;抗真菌薬;抗ウイルス剤;抗凝固剤;抗痙攣剤;抗うつ薬;抗ヒスタミン剤;および免疫学的薬剤が含まれる。
【0097】
ヒドロゲルに含まれうる適切な生物活性剤の他の例には、例えば、ウイルスおよび細胞;ペプチド類、ポリペプチド類、およびタンパク質類、ならびにそのアナログ類、突然変異タンパク質類および活性断片;イムノグロブリン類;抗体類;サイトカイン類(例えばリンホカイン類、モノカイン類、ケモカイン類);血液凝血因子;造血因子;インターロイキン類(IL−2、IL−3、IL−4、IL−6);インターフェロン類(β−IFN、α−IFNおよびγ−IFN);エリスロポエチン;ヌクレアーゼ類;腫瘍壊死因子;コロニー形成刺激因子(例えばGCSF、GM−CSF、MCSF);インシュリン;抗腫瘍剤および腫瘍抑制剤;フィブリン、トロンビン、フィブリノーゲン、合成トロンビン、合成フィブリン、合成フィブリノーゲン等の血液タンパク質類;生殖腺刺激ホルモン類(例えばFSH、LH、CG等);ホルモン類およびホルモンアナログ類(例えば成長ホルモン);ワクチン類(例えば腫瘍、細菌および、ウイルス抗原);ソマトスタチン;抗原;血液凝固因子;成長因子(例えば神経成長因子、インスリン様成長因子);骨形態形成タンパク質類;TGF−B;タンパク質阻害剤;タンパク質アンタゴニスト類;タンパク質アゴニスト類;アンチセンス分子、DNA、RNA、RNAi等の核酸類;オリゴヌクレオチド類;ポリヌクレオチド類;およびリボザイム類が含まれる。
【0098】
生物活性剤は、ボーラスとして、ある期間にわたり、またはその組み合わせにおいてヒドロゲルから放出されうる。反応性前駆体はより浸透性のあるヒドロゲルを形成し、ヒドロゲルからの生物活性剤の拡散を許容しうる。ある実施形態では、開始性前駆体が架橋されて、反応性前駆体から形成されたヒドロゲルの上にバリヤ層を形成し、これにより、そこからの生物活性剤の拡散を減少させうる。
【0099】
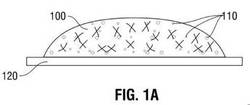
次に、本開示の実施形態を、図を参照して記載する。図1Aを参照すると、反応性前駆体が架橋して、in situで組織120上に生物活性剤110を任意に含むヒドロゲル100を形成する。図1Bに示すように、その後ヒドロゲル100がUV光等の開始剤130に曝露されて、中に含まれる開始性前駆体(単数または複数)の反応が開始されうる。図1Cは、ヒドロゲル100上のバリヤ層140の形成を示すが、これは開始性前駆体(単数または複数)により形成され、ヒドロゲルからの生物活性剤110の拡散を妨げる。したがって生物活性剤110は、バリヤ層140の存在により、生物活性剤110を必要とする組織120内に一方向に拡散しうるが、組織120に隣接するいかなる管腔または領域にも拡散しない。生物活性剤の一方向性分布は、例えば、硬膜、肺、または腸への化学療法剤;心臓血管組織への抗凝固薬;心臓への抗不整脈薬;損傷組織への抗炎症剤または鎮痛剤;損傷組織を治療するための止血剤;および同類のもの、ならびにそれらの組み合わせの直接送達に使用されうる。
【0100】
図2Aに示すように、反応性前駆体から椎間板(spinal disc)の形でヒドロゲル200が形成されうる。図2Bはヒドロゲル200の側面図であり、これが開始剤220に曝露されて、ヒドロゲル200中の任意の開始性前駆体がゲル化されうる。図2Cは、反応性前駆体から形成されたヒドロゲル200と開始性前駆体から形成されたより高密度のバリヤ層230とを有する、もたらされるディスクの断面図である。開始性前駆体の反応により表面領域の密度が高められ、これにより、ヒドロゲル200の表面上により高密度のヒドロゲル230の「皮膜」またはバリヤが作製されうる。このような様式で、非分解性椎間板代用物等の移植物が形成されうる。
【0101】
ある実施形態では、二相ヒドロゲル移植物が形成されうる。例えば、テンプレートおよび/またはスクリーンを使用して、二相ヒドロゲル移植物が形成されうる。テンプレートおよびスクリーン(単数または複数)は、任意の形またはサイズでありうる。ある実施形態では、テンプレートは、(実験室ビーカーと同様の)ベースを有するシリンダであり得、スクリーンは、様々なサイズの一連の円形ディスクを含みうる。テンプレートおよびスクリーンを利用して、高密度底層、中間層、および高密度最上層が、テンプレートおよびスクリーン(単数または複数)により形成されうる。例えば、反応性および開始性ヒドロゲル前駆体をテンプレートのベースに適用し、反応性前駆体にヒドロゲルを形成させ、それからヒドロゲルを開始剤に曝露して開始性前駆体(単数または複数)を架橋し、これにより高密度底層を形成することにより、高密度底層が形成されうる。そして、これに反応性前駆体を、開始性前駆体を任意に用いて適用し、それらを反応させることにより、中間層が底層の上に形成されうる。それから、例えば中間層にスクリーンを適用してから反応性および開始性ヒドロゲル前駆体の両方を中間層に適用し、反応性前駆体にヒドロゲル層を形成させることにより、高密度最上層が形成されうる。それから、最上部のヒドロゲルが開始剤に曝露されて、最上部のヒドロゲル中の開始性前駆体(単数または複数)が架橋されて、高密度最上層が形成されうる。スクリーンは、中間層の任意の開始性前駆体の架橋を防ぐ。スクリーンは残存してもよいし、ある実施形態ではスクリーンが除去されうる。したがってもたらされるゲルは、より高密度の最上層およびより高密度の底層、ならびにより低密度の中間層を有する。
【0102】
形成される層の各々が、同じまたは異なるヒドロゲル前駆体を含みうる。加えて、層の各々が、生物活性剤を含みうる。各層中の生物活性剤のタイプおよび量は、同じでも異なってもよい。
【0103】
二相薬物送達ヒドロゲル移植物を形成する方法を、図3を参照してさらに記載する。図3に示すように、ヒドロゲル前駆体の層がテンプレート310内に配置される。反応性前駆体は、互いに曝露された時にヒドロゲル300を形成する。開始性ヒドロゲル前駆体は、架橋を増加させるために開始剤320に曝露され、これにより高密度底層が形成される。図3Bは、様々なサイズのいくつかのスクリーン330を示す。スクリーン330が、ヒドロゲル300上に配置されうる。それから、追加的前駆体がヒドロゲル300の上に加えられ、反応させられ、開始剤320に任意に曝露されて次の層(図示せず)が形成されうる。このプロセスが繰り返されて、前駆体の開始剤への曝露をブロックするスクリーンの存在によってより低密度のコアを有する高密度架橋ゲルが作製されうる。図3Cに示すように、遮蔽された中心350は、ヒドロゲル340のスクリーンによりカバーされない部分よりも低密度のままでありうる。ある実施形態では、異なるサイズおよび/または形のスクリーン330を用いて、異なる中心が形成されうる。もたらされる二相薬物送達ヒドロゲル移植物340は、このようにして、より高密度のヒドロゲル340と、中心部を形成するより低密度のヒドロゲル350を含みうる。
【0104】
in situ配置時には、二相薬物送達ヒドロゲルの中心ヒドロゲル部分350が、より高密度のヒドロゲル340よりも速い速度で分解しうる。したがって、より高密度のヒドロゲル340のより遅い分解速度により、生物活性剤の時間をかけた段階的放出が提供され、ヒドロゲル340が分解した時に、より低密度の中心350からの追加的放出がボーラスとして提供されうる。他の実施形態においては、中心ヒドロゲルが周囲のヒドロゲルよりもゆっくり分解し、ボーラス送達と、その後のより遅い放出維持量が可能になりうる。これは、持続放出の用途で有益であると分かるかもしれない。即時/持続放出薬物送達システムは、例えば麻酔剤、抗凝血剤、抗炎症剤、化学療法剤、ペプチド類、成長因子、それらの組み合わせなどの送達の用途で有用でありうる。
【0105】
移植物を形成するための本開示によるヒドロゲルの別の使用が、図5Aおよび5Bに描写される。移植物400は、メッシュ410を含む。メッシュ410は、過マンガン酸/酢酸、過硫酸アンモニウム/酢酸、過硫酸カリウム/2,2’−アゾビス[2−(2−イミダゾリン(dimidazolin)−2−イル)プロパン]ジヒドロクロリド(2,2’−アゾビス[2−(2−イミダゾリン(dimidazolin)−2−イル)プロパン]ジヒドロクロリドは、VA044(Wako)として市販されている、過硫酸アンモニウム/テトラメチレンジアミン、それらの組み合わせなど等の開始剤でコーティングされうる。PEG−NHSおよびPEG−アクリレート420等の求電子性反応性前駆体および開始性前駆体の混合物が、メッシュ410に噴霧されうる。それからメッシュ410全体が、トリリジン等の求核性反応性前駆体および未反応アクリレート等の追加的な開始性前駆体でコーティングされうる。メッシュ410に接触するPEG−アクリレートが、メッシュおよび架橋430中の過マンガン酸/酢酸により反応開始されうる。PEG−NHSおよびトリリジンも反応して、メッシュ410の孔を含むメッシュ全体の表面全体に、より低密度に架橋したヒドロゲル420を形成しうる。図5Bに描写するように、PEG−NHS−トリリジンヒドロゲル420は、約4日〜約6日の期間にわたり分解して、メッシュ410の孔440を露出させ、これにより組織内部成長のための空間を可能にしうる。このようなメッシュは、例えばヘルニア修復において使用されうる。
【0106】
他の実施形態においては、図6Aに示すように、縫合糸アンカ600を形成するために本開示のヒドロゲルが利用されうる。シリンジ610により、求電子性および求核性(反応性)ヒドロゲル前駆体および開始性ヒドロゲル前駆体の混合物620が組織630の下に注入されて、組織630の表面640の下および上の両方に軟質ヒドロゲル620が形成されうる。図6Bに示すように、軟質ヒドロゲル620がUV光670により反応開始されて、高密度に架橋した縫合糸アンカ650が作製されうる。それから、図6Cに示すように、縫合糸660が縫合糸アンカ650に通されうる。このような縫合糸アンカは、例えば、in situ損傷閉鎖、骨アンカ、腱修復、それらの組み合わせなどのために用いられうる。
【0107】
図にはないが、他の実施形態においては、まず潜在的ヒドロゲル前駆体を反応開始させてから、開始性ヒドロゲルの形成後に反応性前駆体を反応させうる。
【0108】
さらに他の実施形態においては、図7A〜Cに示すように、移植物を組織に接着するために、本開示のヒドロゲルからリベットが形成されうる。ヘルニア修復のために、移植物700が腹膜710に適用されうる。シリンジ720を用いて、腹膜710の下から(または図にはないが上から)、移植物700の穴701、702、703、704、705、706、707、および708を通してヒドロゲル混合物730を注入しうる。ヒドロゲル混合物730は、腹膜の下に軟質ヒドロゲル740を形成し、穴701、702、703、704、705、706、707、および708を満たし、移植物700の非組織側にわずかにプールしうる。それから軟質ヒドロゲル740が開始剤750に曝露されて、高密度に架橋したヒドロゲルリベット760が形成され、これにより、移植物700が腹膜710に接着されうる。
【0109】
上記のように、ある実施形態では、本開示のヒドロゲル組成物は様々なモジュラスを有しうる。当業者は、ある実施形態では、組成物が適用される予定の組織にもとづいて、本開示の組成物を形成するために利用される成分を調整しうる。図10は、様々な組織についての弾性モジュラスを提供し、これを、所望のモジュラスを有する本開示の組成物の調製する際にガイドとして利用しうる。
【0110】
ある実施形態では、図11に描写するように、ヒドロゲル組成物が、組織の欠損を直すために利用されうる。図11は、軟骨下骨の欠損を修復するための、本開示の組成物の使用を描写する。反応性前駆体および開始性前駆体が、軟骨下骨865の欠損820に適用され、これによりその中に第一ヒドロゲル800が形成されうる。放射線源830が、欠損を囲む関節軟骨855に隣接するヒドロゲル800の表面に適用され、これにより、バリヤ層840として機能する第二ヒドロゲルが表面上に形成されうる。
【0111】
上記のように、ある実施形態では、本開示のヒドロゲル組成物は、第二ヒドロゲルに分散された一つのヒドロゲルを含みうる。図12Aに描写するように、分散領域920は、反応性前駆体で形成された第一ヒドロゲル910の中に、開始性前駆体で形成された第二ヒドロゲルで形成されたコアを含みうる。あるいは、図12Bに描写するように、第一ヒドロゲル910の中に多くの分散領域920が形成されうる。図12Aおよび12Bには示されないが、いくつかの実施形態では、開始性前駆体から形成されるバリヤ層が、本開示のヒドロゲル組成物の上に形成されうる。
【0112】
生物活性剤が、第一ヒドロゲル、第二ヒドロゲル、または両方に含まれうる。生物活性剤は、ある実施形態では、リポソーム、ミクロスフェア、微小気泡、それらの組み合わせなどの中にありうる。生物活性剤が第一および第二ヒドロゲル中に存在する場合には、同じまたは異なる生物活性剤がヒドロゲルに含まれうる。第一ヒドロゲルからは約1日〜約6週、ある実施形態では約1週〜約4週の期間にわたり生物活性剤が放出され、第二ヒドロゲルからは約5日〜約12週、ある実施形態では約2週〜約8週の期間にわたり生物活性剤が放出されうる。
【0113】
複数の放出プロフィールを有するヒドロゲルを含む組成物の例には、米国特許出願公開第2009/0047349号に開示されるものが含まれ、その開示の全体が参照により本明細書に組み込まれる。
【0114】
以下の実施例は、本開示の実施形態を例示するために提出される。これらの実施例は、例示だけを目的とし、本開示の範囲を制限することを目的としない。また、別段の定めがない限り、部およびパーセントは重量を基準とする。本明細書で使用されるところの「室温」とは、約20℃〜約30℃の温度をさす。
【実施例】
【0115】
(実施例1)
溶液調製
第一反応性前駆体:リン酸バッファーpH4.04中PEG−ジアクリレートの80%溶液を調製した。この溶液にPEG−NHSを、0.13g/mlの濃度で加えた(3mlのリン酸バッファー中80%ジアクリレート中0.39グラムのPEG−NHS)。
【0116】
第二反応性前駆体:ホウ酸塩バッファー中リジンの0.01g/ml溶液を調製し、pHを8.6に調節した。
【0117】
開始性前駆体:エタノール中4,4’−ビス(ジエチル−アミノ)ベンゾフェノン(励起波長365nm)の10mg/ml溶液を調製した。
【0118】
表2(下)に詳しく記載されるように、様々な量の開始性前駆体溶液を第一反応性前駆体に加えた。
【0119】
第一および第二反応性前駆体の反応
等しい体積の第一および第二反応性前駆体を、別々のシリンジにロードした。シリンジを接続し、溶液を15秒間混合した。次に、ヒドロゲルの完全な架橋を確保するために、溶液を15分間おいた。
【0120】
開始性前駆体の架橋
それから各架橋ヒドロゲルを、それぞれのシリンジから除去し、いくつかのシリンダに切った。それから、架橋ヒドロゲルを様々な量のUV光(表2参照)に曝露して開始性前駆体の架橋を開始させ、開始性ヒドロゲルを形成した。ゲルのシリンダに長い針を貫通させ、UV源の下に配置し、回転させて均一に硬化させた。
【0121】
ヒドロゲル組成物試験
シリンダが硬化したら、各々を12mmのフラットプローブの下に配置し、最初の高さの最大80%まで、または壊れるまで、0.08mm/秒の速度で20グラムのトリガー力および5グラムの破壊感度で圧縮した。各硬化ヒドロゲルについての結果が、表2に記録されている。図8は、表2のデータを示す棒グラフである(サンプルと100マイクロリットルの光開始剤)。図9は、開始性ヒドロゲル(上の線)と非開始性ヒドロゲル(下の線)の比較である。
【0122】
【表2】

(実施例2)
第二ヒドロゲル前駆体中のリジンの代わりにトリリジンを使用して、実施例1の調製を繰り返した。試験の結果が、下表3に提供される。
【0123】
【表3】

上記の実施例で示すように、開始性前駆体の量および開始剤のUV曝露の量を変化させることにより、様々な程度の架橋が達成された。加えて、使用される第一および第二ヒドロゲル前駆体に応じて、UV曝露の前に様々なレベルの架橋が達成された。
【0124】
以上の記載は、多くの詳細を含むが、これらの詳細は、本明細書の開示の範囲に対する制限としてではなく、その特に有用な実施形態の単なる例示として解釈されねばならない。当業者は、添付の請求項に記載の本開示の範囲および精神の範囲内の、他の多くの可能性を思い付くだろう。
【0125】
摘要
本開示は、ヒドロゲル組成物およびそれを使用する方法に関する。ヒドロゲル組成物は、接触時に互いに反応する前駆体ならびに開始剤との接触時に反応する前駆体を含みうる。ある実施形態では、もたらされるヒドロゲルは、様々なレベルの架橋と、より高密度の領域およびより低密度の領域を有しうる。
【技術分野】
【0001】
(関連する出願との相互参照)
本願は、米国仮特許出願第61/348,896号(2010年5月27日出願)の利益と、優先権を主張し、この仮特許出願の開示は参照によりその全体が本明細書中に援用される。
【0002】
ヒドロゲルは、多様な目的で体内において使用されうる。例えば、ヒドロゲルが、接着剤またはシーラントとして使用されうる。コーティングまたは移植物の形成においても、ヒドロゲルが使用されうる。このような移植物またはコーティングは、局所投与用の薬物も含みうる。
【背景技術】
【0003】
ヒドロゲルは、前駆体成分から形成されうる。これらの成分は、反応性でありえ、すなわち成分が接触時に互い反応し、または紫外(UV)光、イオン、熱、可視光、ガンマ線、電子ビーム、それらの組み合わせなどの外部の開始剤への曝露により反応させられうる。もたらされるヒドロゲルの特徴は、特定のタイプの前駆体の特徴に限定されうる。
【0004】
反応性ヒドロゲル前駆体および開始性ヒドロゲル前駆体の両者の性質を示すヒドロゲルを形成することが、有利であると考えられる。
【発明の概要】
【課題を解決するための手段】
【0005】
本開示は、ヒドロゲルならびにそれを作製および使用する方法を提供する。これらのヒドロゲルを含むデバイスも、提供される。例えば、ある実施形態では、本開示のヒドロゲルが、医療デバイスを組織に付着させるために利用されうる。
【0006】
ある実施形態では、本開示は、求電子基を有するマルチアーム(multi−arm)ポリエーテルを含む第一反応性前駆体と、第二反応性前駆体求核基と、少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体とを含むヒドロゲルを含む、移植物を提供する。
【0007】
ある実施形態では、本開示のヒドロゲルは、求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体と、求核基を含む第二反応性前駆体とを組み合わせて含む、第一ヒドロゲルと;少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体を含む、第二ヒドロゲルとを含む、複合ヒドロゲル組成物を含み得、第二ヒドロゲルが、第一ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成する。
【0008】
本開示の方法は、ある実施形態では、第一反応性前駆体を、第二反応性前駆体および少なくとも一つのビニル基を含む開始性前駆体と接触させるステップと;第一反応性前駆体および第二反応性前駆体を架橋して、ヒドロゲルを形成するステップと;ヒドロゲルの表面を開始剤に曝露して開始性前駆体の架橋を開始し、ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成するステップとを含む、移植物を形成する方法を含みうる。
【0009】
他の実施形態では、本開示の移植物は、求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;求核基を含む第二反応性前駆体と;少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体とを含む、ヒドロゲルを含み得、第一反応性前駆体が第二反応性前駆体と反応して第一ヒドロゲルを形成し、開始性前駆体が開始剤との接触時に第二ヒドロゲルを形成し、第二ヒドロゲルが第一ヒドロゲルを包含するバリヤ層を形成する。
【0010】
したがって、本発明は以下の項目を提供する:
(項目1)
ヒドロゲルを含む移植物であって、該ヒドロゲルは
求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;
求核基を含む、第二反応性前駆体と;
少なくとも一つのビニル基を含む、少なくとも一つの開始性前駆体と
を含む、移植物。
(項目2)
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、上記項目のうちのいずれかに記載の移植物。
(項目3)
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、上記項目のうちのいずれかに記載の移植物。
(項目4)
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目5)
生物活性剤をさらに含む、上記項目のうちのいずれかに記載の移植物。
(項目6)
前記第一反応性前駆体が前記第二反応性前駆体と反応して第一ヒドロゲルを形成し、前記開始性前駆体が、開始剤との接触時に第二ヒドロゲルを形成する、上記項目のうちのいずれかに記載の移植物。
(項目7)
前記開始剤が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目8)
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目9)
前記第二ヒドロゲルが、前記第一ヒドロゲルの少なくとも一部の上にバリヤ層を形成する、上記項目のうちのいずれかに記載の移植物。
(項目10)
前記第一ヒドロゲルが、組織欠損内に配置され、前記第二ヒドロゲルが、該欠損の上にバリヤ層を提供する、上記項目のうちのいずれかに記載の移植物。
(項目11)
前記第一ヒドロゲルが、約5kPa〜約500kPaのモジュラスを有し、前記第二ヒドロゲルが、約50kPa〜約5,000kPaのモジュラスを有する、上記項目のうちのいずれかに記載の移植物。
(項目12)
前記第一ヒドロゲルが、約4週〜約10週の期間にわたり分解し、前記第二ヒドロゲルが、約6週〜約6ヵ月の期間にわたり分解する、上記項目のうちのいずれかに記載の移植物。
(項目13)
前記移植物が、マトリックス、人工血管、心臓弁、人工臓器、人工骨、移植可能微小凸レンズ、血管グラフト、ステント、縫合糸、ステープル、クリップ、メッシュ、スリング、ネジ、ピン、ケーブル、軟骨移植物、脊椎移植物、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の移植物。
(項目14)
前記移植物が、軟骨移植物を含み、前記第一ヒドロゲルが、軟骨の欠損内にあり、前記第二ヒドロゲルが、該欠損の上にバリヤ層を形成する、上記項目のうちのいずれかに記載の移植物。
(項目15)
前記移植物が、前記第二ヒドロゲルにより囲まれた前記第一ヒドロゲルを含む、椎間板移植物を含む、上記項目のうちのいずれかに記載の移植物。
(項目16)
前記移植物が、人工皮膚を含む、上記項目のうちのいずれかに記載の移植物。
(項目17)
求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体を、求核基を含む第二反応性前駆体と組み合わせて含む、第一ヒドロゲルと;
少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体を含む、第二ヒドロゲルと
を含む、複合ヒドロゲル組成物であり、
該第二ヒドロゲルが、該第一ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成する、複合ヒドロゲル組成物。
(項目18)
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目19)
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目20)
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目21)
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第二ヒドロゲルをさらに架橋する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目22)
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目23)
生物活性剤をさらに含む、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目24)
前記生物活性剤が、前記第一ヒドロゲル中にある、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目25)
前記生物活性剤が、約3日〜約6週の期間にわたり前記第一ヒドロゲルから放出される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目26)
前記第二ヒドロゲルが、前記複合ヒドロゲル組成物の約5重量%〜約30重量%を構成する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目27)
前記第一ヒドロゲル中に少なくとも一つの分散領域を形成する少なくとも一つの開始性前駆体を含む第三ヒドロゲルをさらに含む、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目28)
前記第二ヒドロゲルおよび前記第三ヒドロゲルが、同じである、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目29)
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第三ヒドロゲルをさらに架橋する、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目30)
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、上記項目のうちのいずれかに記載の複合ヒドロゲル組成物。
(項目31)
上記項目のうちのいずれかに記載の前記複合ヒドロゲル組成物を含む、薬物送達デバイス。
【0011】
本開示の様々な実施形態が、本明細書の以下で図に関して記載される。
【図面の簡単な説明】
【0012】
【図1A】図1Aは、本開示によるヒドロゲル移植物の側面図である。
【図1B】図1Bは、開始剤への曝露を描写した、図1Aのヒドロゲルの断面図である。
【図1C】図1Cは、開始剤への曝露後の図1Aのヒドロゲルの断面図である。
【図2A】図2Aは、本開示によるヒドロゲル移植物の斜視図である。
【図2B】図2Bは、開始剤への曝露を描写した、図2Aのヒドロゲルの側面図である。
【図2C】図2Cは、開始剤への曝露後の図2Aのヒドロゲルの断面図である。
【図3A】図3Aは、本開示のヒドロゲルの形成の間に使用されるテンプレートの側面図である。
【図3B】図3Bは、本開示によるテンプレート用のブロッキングデバイスまたはスクリーンの上面図である。
【図3C】図3Cは、本開示により使用されるテンプレートおよびブロッキングデバイスの側面図である。
【図3D】図3Dは、本開示のヒドロゲル移植物の側面図である。
【図4】図4は、開始性前駆体の架橋前および後の、本開示のヒドロゲル移植物のモジュラスを描写したグラフである。
【図5A】図5Aは、本開示のヒドロゲルを含むコーティングを有するメッシュ移植物の上面図である。
【図5B】図5Bは、本開示のヒドロゲルの一部の分解後の、図5Aの移植物の上面図である。
【図6A】図6Aは、本開示のヒドロゲルを用いて形成される縫合糸アンカの断面図である。
【図6B】図6Bは、開始性前駆体の架橋を描写した、図6Aの縫合糸アンカの断面図である。
【図6C】図6Cは、開始性前駆体の架橋後の、図6Aの縫合糸アンカの断面図である。
【図7A】図7Aは、本開示のヒドロゲルを用いた組織への接着のための移植物の上面図である。
【図7B】図7Bは、開始性前駆体の架橋前の、図7Aの移植物の上面図である。
【図7C】図7Cは、開始性前駆体の架橋後の、図7Aの移植物の上面図である。
【図8】図8は、表2に提示されるデータのグラフである。
【図9】図9は、開始性ヒドロゲルおよび非開始性ヒドロゲルにつき、加えた力と圧縮量を比較したグラフである。
【図10】図10は、種々の組織ならびにコラーゲンおよびゼラチンを含む他の材料の弾性モジュラスを描写したグラフである。
【図11】図11は、組織の欠損を修復するための、本開示の組成物の使用の描写である。
【図12A】図12Aは、一つのヒドロゲルで形成された分散領域を第二ヒドロゲル中に有する、本開示の組成物を含む移植物の図である。
【図12B】図12Bは、一つのヒドロゲルで形成された分散領域を第二ヒドロゲル中に有する、本開示の組成物を含む移植物の代替図である。
【発明を実施するための形態】
【0013】
外部の開始を必要とする前駆体、すなわち開始性前駆体と組み合わせた、開始剤の使用を必要としない反応性前駆体の架橋から形成されうるヒドロゲルが、本明細書に記載される。前駆体は、例えば、モノマーまたはマクロマーでありうる。本明細書において用いられるところの、「ヒドロゲル前駆体(単数または複数)」、「第一ヒドロゲル前駆体」、および「第二ヒドロゲル前駆体」という用語は、開始剤の使用を伴ってまたは伴わずに組み合わせられてヒドロゲルを形成しうる成分をさすために用いられうる。したがってこれらの前駆体は、ある実施形態では、反応性前駆体および開始性前駆体の組み合わせを含みうる。本明細書において用いられるところの、「反応性前駆体(単数または複数)」、「第一反応性ヒドロゲル前駆体(単数または複数)」、および「第二反応性ヒドロゲル前駆体(単数または複数)」という用語は、互いに対して曝露された時に架橋してヒドロゲルを形成しうる前駆体を含む。本明細書において用いられるところの、「開始性(initiated)前駆体(単数または複数)」、「第一開始性ヒドロゲル前駆体(単数または複数)」および「第二開始性ヒドロゲル前駆体(単数または複数)」という用語は、本明細書において「開始剤」と称されることもある外部ソースに曝露された時に架橋する、ヒドロゲル前駆体を表すために用いられうる。開始剤は、例えば、イオン、UV光、酸化還元反応成分、それらの組み合わせ、ならびに当業者の認識範囲内である他の開始剤を含む。
【0014】
ヒドロゲル前駆体は、反応性前駆体であるか開始性前駆体であるかを問わず、生物学的に不活性および水溶性のコアを有しうる。コアが水溶性のポリマー領域である場合、用いられうる適切なポリマーには、ポリエーテル類、例えば、ポリエチレングリコール(「PEG」)、ポリエチレンオキシド(「PEO」)、ポリエチレンオキシド−コ−ポリプロピレンオキシド(「PPO」)、コ−ポリエチレンオキシドブロックまたはランダムコポリマー類、およびポリビニルアルコール(「PVA」)等のポリアルキレンオキシド類;ポリ(ビニルピロリジノン)(「PVP」);ポリ(アミノ酸類);デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロースおよび/またはヒドロキシメチルセルロース等のポリ(サッカライド類);ヒアルロン酸;ならびにアルブミン、コラーゲン、カゼイン、およびゼラチン等のタンパク質類が含まれる。ある実施形態では、前述のポリマー材料の組み合わせを利用してコアが形成されうる。いくつかの実施形態においては、ポリエーテル類、特にポリ(オキシアルキレン類)またはポリ(エチレングリコール)またはポリエチレングリコール(「PEG」)が利用されうる。
【0015】
コアの分子的性状が小さい場合、様々な親水官能基のいずれかが、ヒドロゲル前駆体を水溶性にするために用いられうる。ある実施形態では、水溶性のヒドロキシル、アミン、スルホン酸およびカルボン酸のような官能基が、前駆体を水溶性にするために用いられうる。例えば、スべリン酸(subaric acid)のN−ヒドロキシスクシンイミド(「NHS」)エステルは水に不溶であるが、スルホン酸基をスクシンイミド環に付加することにより、アミン基に対する反応性により反応基として使用されうるその能力に影響することなくスべリン酸(subaric acid)のNHSエステルを水溶性にできる。
【0016】
ある実施形態では、共有結合、イオン結合、または疎水結合により、反応性前駆体からヒドロゲルが形成されうる。物理的(非共有結合)架橋は、錯形成、水素結合、脱溶媒和、Van der Waals相互作用、イオン結合、それらの組み合わせなどから生じ得、in situで組み合わせられるまで物理的に分離されている成分を混合することにより、または温度、pH、イオン強度、それらの組み合わせなどを含む生理学的環境中の一般的条件の結果として開始されうる。化学的(共有結合)架橋は、フリーラジカル重合、縮合重合、アニオンまたはカチオン重合、段階成長重合、求電子−求核反応、それらの組み合わせなどを含むがこれに限られない、多くの機構のいずれかによって達成されうる。
【0017】
ある実施形態では、ヒドロゲルの反応性前駆体部分は、単一のタイプの反応性前駆体または複数のタイプの反応性前駆体から形成されうる。他の実施形態においては、ヒドロゲルが複数のタイプの反応性前駆体、例えば二つの反応性前駆体から形成される場合、反応性前駆体は、第一および第二反応性前駆体と称されうる。一つより多くの反応性前駆体が利用される場合には、ある実施形態では、反応性ヒドロゲル前駆体の少なくとも一つは架橋剤であり得、少なくとも一つの他の反応性ヒドロゲル前駆体は高分子であり得、本明細書において「官能性ポリマー」と称されうる。
【0018】
いくつかの実施形態においては、反応性前駆体は、前駆体が混合されると自然に架橋するが、堆積プロセスの間は一つより多くの前駆体が個々に安定している、生体適合性の複数前駆体系を含みうる。反応性前駆体が反応を許容する(例えばpHまたは溶媒に関して)環境において混合されると、官能基が互いに反応して共有結合を形成する。反応性前駆体の少なくともいくつかが他の二つ以上の前駆体と反応できるときに、反応性前駆体が架橋する。例えば、二つの第一タイプの官能基をもつ前駆体を、第一タイプの官能基と反応できる少なくとも三つの第二タイプの官能基をもつ架橋前駆体と反応させうる。
【0019】
このような反応成分は、例えば、求電子基を有する第一反応性前駆体と、求核基を有する第二反応性前駆体とを含む。求電子剤は、求核剤と反応して共有結合を形成する。共有結合架橋または共有結合は、異なるポリマーを互いに共有結合する働きをする異なるポリマー上の官能基の反応により形成される化学基をさす。ある実施形態では、第一反応性前駆体上の第一求電子官能基組が、第二反応性前駆体上の第二求核官能基組と反応しうる。ある実施形態では、このような系は、二官能性アルキレンオキシドまたは多官能性アルキレンオキシド含有部分を含む第一反応性前駆体と、二官能性アミンまたは多官能性アミンであるマクロマーを含む第二反応性前駆体とを含む。
【0020】
ある実施形態では、反応性ヒドロゲル前駆体は多官能性でありうる、すなわち、例えば第一反応性ヒドロゲル前駆体上の求電子官能基が第二反応性ヒドロゲル前駆体上の求核官能基と反応して共有結合を形成しうるように、二つ以上の求電子または求核官能基を含みうる。求電子−求核反応の結果として前駆体が結合して架橋ポリマー産物を形成するように、第一または第二反応性ヒドロゲル前駆体の少なくとも一つが、二つ以上の官能基を含む。
【0021】
ある実施形態では、求核および求電子反応性前駆体の両者が架橋反応において用いられる限りにおいて、第一および第二反応性ヒドロゲル前駆体の各々が、一つのカテゴリの官能基だけ、求核基だけまたは求電子官能基だけを含む。したがって、例えば、第一反応性ヒドロゲル前駆体がN−ヒドロキシスクシンイミド等の求電子官能基を有する場合には、第二反応性ヒドロゲル前駆体がアミン等の求核官能基を有しうる。一方で、第一反応性ヒドロゲル前駆体がスルホスクシンイミド等の求電子官能基を有する場合には、第二反応性ヒドロゲル前駆体がアミンまたはチオール等の求核官能基を有しうる。
【0022】
ある実施形態では、複数のNHS基により官能基化されたマルチアームPEG等の多官能性求電子性ポリマーが、第一反応性ヒドロゲル前駆体として用いられ、トリリジン等の多官能性求核性ポリマーが、第二反応性ヒドロゲル前駆体として用いられうる。複数のNHS基により官能基化されたマルチアームPEGは、例えば、4、6または8のアームと、約5,000〜約25,000の分子量を有しうる。適切な第一および第二反応性ヒドロゲル前駆体の他の例は、米国特許第6,152,943号;第6,165,201号;第6,179,862号;第6,514,534号;第6,566,406号;第6,605,294号;第6,673,093号;第6,703,047号;第6,818,018号;第7,009,034号;および第7,347,850号に記載されており、その各々の開示の全体が参照により本明細書に組み込まれる。
【0023】
例えば様々な組織に対する粘着、外科医が正確かつ都合よくin situ形成ヒドロゲル前駆体を配置することを可能にする望ましい硬化時間、生体適合性のための高い含水量、シーラントに用いるための機械的強度、および/または配置後の破壊に抵抗するための靭性を含む、ヒドロゲル前駆体の特定の性質が有用でありうる。したがって、直ちに殺菌され、天然材料の使用に伴いうる疾患感染の危険性を回避する合成材料が、使用されうる。実際に、例えばFOCALSEAL(登録商標)(Genzyme,Inc.)、COSEAL(登録商標)(Angiotech Pharmaceuticals)、およびDURASEAL(登録商標)(Confluent Surgical,Inc)等の市販の製品において用いられるような合成前駆体を用いて作られる特定の重合可能なヒドロゲルが、当業者の認識範囲内である。他の周知のヒドロゲルには、例えば米国特許第6,656,200号;第5,874,500号;第5,543,441号;第5,514,379号;第5,410,016号;第5,162,430号;第5,324,775号;第5,752,974号;および第5,550,187号に開示されるものが含まれる。
【0024】
反応性前駆体から架橋ポリマーヒドロゲルを形成するための反応条件は、使用される反応性前駆体の性質に依存しうる。ある実施形態では、緩衝水溶液において約5〜約12のpHで反応が行われる。バッファーには、例えば、ホウ酸ナトリウムバッファー(pH10)およびトリエタノールアミンバッファー(pH7)が含まれる。いくつかの実施形態においては、エタノールまたはイソプロパノール等の有機溶剤が、反応速度を改善し、または所与の製剤の粘性を調整するために加えられうる。
【0025】
ヒドロゲル前駆体が合成である場合(例えば、ポリアルキレンオキシドベースである場合)、モル等量の反応物を用いることが所望されうる。場合によっては、官能基の加水分解による反応等の副反応を補うために、モル過剰の架橋剤が加えられうる。
【0026】
反応性前駆体、ある実施形態では架橋剤および架橋可能ポリマーを選択するときには、ポリマーの少なくとも一つが、一分子あたり二つより多くの官能基と、もたらされるヒドロゲルが生分解可能であることが望ましい場合には少なくとも一つの分解可能領域とを有しうる。ある実施形態では、各反応性ポリマー前駆体は、二つより多くの官能基を有し得、ある実施形態では、四つより多くの能基を有しうる。
【0027】
反応性前駆体から形成される、もたらされる生体適合性の架橋ポリマーの架橋密度は、前駆体、ある実施形態では架橋剤および官能性ポリマーの全体の分子量、および一分子あたりにつき利用可能な官能基の数により制御されうる。600Da等の架橋間のより低い分子量からは、10,000Da等のより高い分子量と比較して、はるかに高い架橋密度が得られる。3000Da以上の分子量のより高分子量の官能性ポリマーにより、弾性ゲルが得られる。
【0028】
架橋密度は、溶液中の前駆体、ある実施形態では架橋剤および官能性ポリマーの全体の固形分によっても制御されうる。固形分を増加させることにより、単位体積あたりの架橋可能基の数および潜在的架橋密度が増加する。架橋密度を制御するさらにもう一つの方法は、求核基の求電子基に対する化学量を調節することによる。1対1の比は最大の架橋密度をもたらしうるが、反応性官能基の他の比(例えば、求電子剤:求核剤)は所望の製剤に適合すると想定される。
【0029】
ある実施形態では、第一反応性前駆体は、マルチアームPEGであり得、ビニル基を含む開環無水物により官能基化されNHSでエンドキャップされうる。第二反応性前駆体は、多官能性アミン成分でありうる。開示のヒドロゲルは、このように少なくとも二つの前駆体から形成されうる。
【0030】
いくつかの実施形態では、上記のように、ヒドロゲル前駆体が開始性前駆体を含みうる。本開示による使用のための開始性前駆体は、エチレン性不飽和の官能基を有しうる。このようなエチレン性不飽和の官能基を有するこのような前駆体は、上述のように生物学的に不活性および水溶性のコアを有しうる。このようなコアは、当業者の認識範囲内の任意の手段により官能基化されうる。
【0031】
エチレン性不飽和の官能基、ある実施形態ではビニル基は、重合反応を開始するために開始剤を用いて重合されうる。少なくとも二つのエチレン性不飽和の官能基を伴う前駆体が、架橋ポリマーを形成しうる。いくつかの組成物は、そのような官能基を一つだけ有するある前駆体と、前駆体を架橋するための複数の官能基を有する追加的な架橋前駆体とを有する。エチレン性不飽和の官能基は、様々な技術、例えばフリーラジカル重合、縮合重合、または付加重合により、重合されうる。本開示により使用されうる例示的な開始性前駆体には、アクリレート類;無水イタコン酸、無水マレイン酸、無水シトラコン酸、それらの組み合わせなど等の、ビニル基含有無水物類が含まれる。他の例示的な開始性前駆体には、例えば、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率をもつビニルモノマー、シロキサン官能性ビニル化合物、ビニル基をもつポリエチレングリコール−シリコーンコモノマー、トリアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、それらの組み合わせなどが含まれる。
【0032】
開始性前駆体の重合に利用される好適な開始剤には、熱開始剤、光活性化開始剤、酸化還元(レドックス)系、フリーラジカル開始剤、放射、熱開始系、それらの組み合わせなどが含まれるがこれに限られない。ある実施形態では、適切な放射源には、熱、可視光、紫外(UV)光、ガンマ線、電子ビーム、それらの組み合わせなどが含まれる。ある実施形態では、光開始剤も使用されうる。このような光開始剤には、フリーラジカル開始剤、臭素酸鉄等のレドックス開始剤、過硫酸アンモニウム/酢酸、過硫酸アンモニウム−テトラメチルジアミン、過硫酸カリウム/VA044(Wako Chemicals Inc.,Richmond VA)などが含まれるがこれに限られない。UV光も、色素媒介光酸化、グルタルアルデヒド架橋、デキサメチレン(dexamethylene)ジイソシアネート架橋、カルボジイミド架橋、それらの組み合わせなどとともに使用されうる。
【0033】
ある実施形態では、ヒドロゲルを生分解可能または吸収可能にするために、官能基の間に存在する生分解可能な結合を有する一つ以上のヒドロゲル前駆体が含まれうる。いくつかの実施形態では、これらの結合は、例えば、生理溶液において加水分解されうるエステルでありうる。このような結合の使用は、タンパク分解作用により分解されうるタンパク質結合と対照的である。生分解可能な結合は、ヒドロゲル前駆体の一つ以上の水溶性コアの一部も形成しうる。代替的または追加的に、ヒドロゲル前駆体の官能基が、それら間の反応の生成物から生分解可能な結合がもたらされるように、選択されうる。各アプローチにおいて、もたらされる生分解可能な生体適合性の架橋ポリマーが所望の時間内で分解または吸収されるように、生分解可能な結合が選択されうる。一般に、生理学的条件下でヒドロゲルを非毒性または低毒性産物に分解させる生分解可能な結合が選択されうる。
【0034】
上述の生分解可能な架橋剤または小分子が、アルブミン、他の血清タンパク質類、および/または血清濃縮物等のタンパク質類と反応させられて、架橋ポリマーネットワークが生成されうる。一般に、架橋剤の水溶液がタンパク質類の濃縮溶液と混合されて、架橋ヒドロゲルが生成されうる。架橋ステップの間に緩衝剤、例えばホウ酸塩バッファーまたはトリエタノールアミンを加えることにより、反応が加速されうる。
【0035】
ゲル化につながる架橋反応は、ある実施形態では、約1秒〜約5分以内、ある実施形態では約3秒〜約1分で生じうる。通常の技術を有する当業者は、これらの明示される範囲内のすべての範囲および値が企図されることを即座に理解する。場合によっては、10秒未満でゲル化が生じうる。
【0036】
架橋ヒドロゲルの分解は、架橋剤の生分解可能なセグメント、ならびにヒドロゲルが曝露される任意の酵素に依存しうる。一切の分解酵素の非存在下では、架橋ポリマーは、生分解可能なセグメントの加水分解だけにより分解しうる。分解速度は、水溶性コアを形成するポリマーに、特に形成される任意のエステル結合の構造および位置に依存しうる。例えば、開環重合においてエステル結合が形成されうる。開環重合は、例えば、PEGと、環状エステルまたは例えばフラン−2,5−ジオン、1,4−ジオキサン−2,5−ジオン、グルタル酸無水物、コハク酸無水物、マレイン酸無水物、イタコン酸無水物、メチルコハク酸無水物、2,2−ジメチルコハク酸無水物、2ドデセン−1−イルコハク酸無水物、シス−1,2,3,6−テトラヒドロフタル酸無水物、シトラコン酸無水物、2,3−ジメチルマレイン酸無水物、1−シクロペンテン−1,2−ジカルボン酸無水物、3,4,5,6−テトラヒドロフタル酸無水物、3エチル−3−メチルグルタル酸無水物、3,3−ジメチルグルタル酸無水物、3−メチルグルタル酸無水物、それらの組み合わせなどを含む無水物との間に起こりうる。そして、もたらされるポリマーが、ある実施形態ではスクシンイミド基で官能基化された後、本開示のヒドロゲルを形成するために反応性前駆体として利用されうる(例えばアミン等の架橋剤と組み合わせることによる)。開環重合のためPEGと組み合わせられるモノマー、およびこうしてもたらされる分解可能なエステル基が、in vivoのヒドロゲルの持久性に影響する。この反応性前駆体を形成するために使用されるモノマーの固形分およびアーム長も、その分解速度に影響しうる。
【0037】
例えば、ある実施形態では、生成物は、PEGとグルタル酸無水物、イタコン酸無水物、メチルコハク酸無水物、2,2−ジメチルコハク酸無水物、2ドデセン−1−イルコハク酸無水物、シス−1,2,3,6−テトラヒドロフタル酸無水物、シトラコン酸無水物、2,3−ジメチル無水マレイン酸、1−シクロペンテン−1,2−ジカルボン酸無水物、3,4,5,6−テトラヒドロフタル酸無水物、3エチル−3−メチルグルタル酸無水物、3,3−ジメチルグルタル酸無水物、3−メチルグルタル酸無水物、それらの組み合わせなど等の無水物を含む第二成分との間の開環重合でありうる。もたらされる生成物は、約6週〜約8週の期間にわたり分解するヒドロゲルを形成しうる。
【0038】
他の実施形態においては、PEGとコハク酸無水物の間の開環重合の生成物は、約2日〜約7日の期間にわたり分解しうる。PEGおよびマレイン酸無水物が使用される実施形態においては、生成物は約6ヵ月の期間にわたり分解しうる。開環マレイン酸無水物のビニル基は、二次的ビニル重合に関係しうる。したがって、ある実施形態では、開環マレイン酸無水物のビニル基が、開始性前駆体として働きうる。
【0039】
オリゴヒドロキシ酸ブロック等の生分解可能ブロックにより生成される疎水性またはPLURONICまたはTETRONICポリマーにおけるPPOブロックの疎水性は、小さな有機薬物分子の溶解において有用でありうる。生分解可能または疎水性のブロックの取り込みにより影響される他の性質には、吸水性、機械的性質、および温度感受性が含まれる。
【0040】
合成架橋ゲルは、生分解可能領域の加水分解により分解する。合成ペプチド配列を含むゲルの分解は、配列の分解に必要な特定の酵素およびその濃度に依存しうる。場合によっては、分解プロセスを加速するために、架橋反応の間に特定の酵素が加えられうる。
【0041】
ヒドロゲル前駆体は、使用前に溶液中に配置され、溶液が組織に送達されうる。二つの溶液が使用される場合には、各溶液に、接触時に互い反応しうる一つ以上の前駆体が含まれうる。溶液は別々に貯蔵され、組織に送達されるときに混合されうる。
【0042】
in situ形成材料系の一部として利用されるいずれの溶液も、有害または有毒の溶媒を含んではならない。ある実施形態では、前駆体(単数または複数)は、緩衝等張食塩水等の生理学的適合性の溶液における適用を可能にするために、水等の溶媒において実質的に可溶性でありうる。水溶性コーティングは薄膜を形成しうるが、ある実施形態では、厚みの制御された三次元ゲルを形成してもよい。ゲルも、身体から回収される必要がないように生分解可能でありうる。本明細書で用いられるところの「生分解可能」という用語は、生体吸収性材料および生体再吸収性材料の両者を含むものと定義される。生分解可能とは、分解生成物が排出可能または身体に吸収可能であるように、材料が分離し、または身体環境下で構造的完全性を失うこと(例えば酵素的分解または加水分解)、または体内の生理学的条件下で崩壊させられる(物理的または化学的に)ことを意味する。
【0043】
様々な用途で、ヒドロゲルの異なる特徴が必要とされうる。一般に、ヒドロゲル前駆体は、示される生体適合性および毒性の欠如をもとに選択されなければならない。
【0044】
ある実施形態では、ヒドロゲルは、(例えばフリーラジカル重合により架橋できる)少なくとも一つの反応性前駆体と、少なくとも一つの開始性前駆体とから形成され、または、前駆体の一つ以上が架橋に参加してin situ形成材料を形成する、三つ以上の前駆体により作られうる。
【0045】
ヒドロゲル形成の前に、開始性前駆体、ある実施形態では直鎖状PEGアクリレートが、約7〜約11、ある実施形態では約8〜約10のpHを有する高pHのバッファー、例えばホウ酸ナトリウム中で再構成されうる。開始性前駆体、ある実施形態では求電子性官能基を有するマルチアームPEGが、約3〜約6、ある実施形態では約4〜約5のpHを有するリン酸ナトリウム等の低pHのバッファーにより再構成されうる。
【0046】
ある実施形態では、直鎖状PEGアクリレートが開始性前駆体として使用されうる。したがってある実施形態では、第一反応性ヒドロゲル前駆体、第二反応性ヒドロゲル前駆体および開始性前駆体を接触させることにより、ヒドロゲルが形成されうる。第一反応性前駆体および第二反応性前駆体の反応時に、ヒドロゲルが形成しうる。開始性前駆体を架橋し、これによってより高密度のヒドロゲルを作製するために、成分が開始剤に曝露されてもよい。
【0047】
ある実施形態では、もたらされるヒドロゲルが、相互貫通ネットワークを形成しうる。ある実施形態では、相互貫通ネットワークは、二つのヒドロゲルネットワーク、すなわち開始性前駆体と組み合わされた少なくとも二つの反応性前駆体により形成されるヒドロゲルより形成されうる。他の実施形態においては、相互貫通ネットワークは、反応基も有する開始性前駆体から形成されうる。このような前駆体は、他の反応性前駆体と反応できるとともに、開始剤への曝露時に反応開始されうる。
【0048】
例えば、ある実施形態では、マルチアームPEGとトリリジンの間に第一ヒドロゲルが形成しうる。エチレン性不飽和のモノマーを開始剤に曝露することにより、第二ヒドロゲルが形成されうる。これらの二つのヒドロゲルが、開始剤への曝露の前に組み合わされうる。これらのヒドロゲルの開始剤への曝露から、ヒドロゲルの相互貫通ネットワークがもたらされ、その各々が様々な分解速度等、別々の性質を有しうる。さらに、反応性前駆体および開始性前駆体の量を変化させることにより、もたらされる組成物の性質が異なりうる。
【0049】
他の実施形態においては、マルチアームPEGがビニル基により官能基化され、トリリジンと反応させられて第一ヒドロゲルが形成されうる。ビニル基により官能基化されたPEGを開始剤により反応開始させることにより、ビニル基の架橋によりヒドロゲルの架橋が増加し得、これにより相互貫通ネットワークが形成されうる。他の実施形態においては、ビニル基により官能化されたマルチアームPEGが、限定的にアミンと反応し、その後開始剤が加えられてビニル基の架橋が増加されうる。
【0050】
反応性前駆体が第一ヒドロゲルを形成し、開始性前駆体が第二ヒドロゲルを形成し、二つのヒドロゲルが合わさって相互貫通ネットワークを形成する場合、ある実施形態では、反応性前駆体から形成される第一ヒドロゲルが、開始性前駆体から形成される第二ヒドロゲルよりも急速に分解し、これにより、例えば組織内部成長、血管新生、それらの組み合わせなどによる治癒を可能にする空間を形成しうる。
【0051】
ある実施形態では、様々な分解度の相互貫通(interpretation)ネットワークを有する本開示のヒドロゲルは、組織足場として働き、これにより組織集積/内部成長の手段を提供しうる。組織足場は、成長および発達成分を伴う細胞も提供できる。したがって、本開示のヒドロゲルが組織足場として利用される場合には、それは、必要な栄養分および生物活性剤を周囲組織に提供することにより本来の組織の再成長を助けうる。いくつかの実施形態においては、本明細書に記載のように、ヒドロゲル自体がコラーゲン、ゼラチン、ヒアルロン酸、それらの組み合わせなど等の天然成分を含み得、したがって、組織足場が分解するに伴い天然成分が放出され、あるいは移植部位で分解しうる。
【0052】
他の実施形態においては、本開示のヒドロゲル組成物は、一方が他方の中に分散された、二つのヒドロゲルを有しうる。例えば、ある実施形態では、本開示の組成物は、反応性前駆体から形成される第一ヒドロゲルを含み得、当該第一ヒドロゲルの中には少なくとも一つの分散領域を伴い、当該分散領域が、開始性前駆体から形成される第二ヒドロゲルにより形成される。他の実施形態においては、反応性前駆体で形成される第一ヒドロゲルが、開始性前駆体から形成される第二ヒドロゲルの中に、少なくとも一つの分散領域を形成しうる。一つのヒドロゲルにより形成される分散領域が、第二ヒドロゲル中に一つの領域、例えば中心領域またはコアを形成し得、または一つのヒドロゲルにより形成される分散領域が、第二ヒドロゲル中にたくさんの小領域を形成しうる。
【0053】
反応性前駆体および開始性前駆体の濃度を変化させることにより、もたらされるヒドロゲルの性質が異なりうる。例えば、ある実施形態では、溶液が、約200g/モル〜約50,000g/モル、ある実施形態では約500g/モル〜約35,000g/モルの分子量を有するアクリレートを、約5g/ml〜約40g/ml、ある実施形態では約10g/ml〜約20g/mlの濃度で含みうる。溶液は、約5mg/ml〜約100mg/ml、ある実施形態では約10mg/ml〜約20mg/mlの濃度で、光開始剤も含みうる。光開始剤は、例えば、4,4’−ビス(ジエチルアミノ)ベンゾフェノン、2,2−ジメトキシ−2−フェニルアセトフェノン、カンファーキノン/4−ジメチルアミノ安息香酸、エオシン、アゾビスイソブチロニトリル(AIBN)、ジメトキシベンゾフェノン、それらの組み合わせなどでありうる。アクリレート/光開始剤溶液は約4.25%〜約17%、ある実施形態では約6%〜約14%、ある実施形態では約8.5%の濃度を有しうる。ある実施形態では、アクリレート/光開始剤溶液は、約0.05g/ml〜約2g/ml、ある実施形態では約0.1g/ml〜約1g/ml、ある実施形態では約0.26g/mlの濃度でリン酸ナトリウムバッファー中にありうるマルチアームPEGと組み合わせられうる。これらの溶液が反応して、本開示のヒドロゲルを形成しうる。
【0054】
先述のように、反応性前駆体への開始性前駆体の付加およびその後の開始剤への曝露により、もたらされるヒドロゲルの性質が変更されうる。さらに、反応性前駆体に対する開始性前駆体の比が、機械的性質に影響しうる。図4にグラフで描写され、下表1にリストされるように、反応性前駆体および開始性前駆体の混合物中に存在する開始性前駆体の割合が、反応性ヒドロゲルの架橋後のヒドロゲルの強度に大きく影響する。
【0055】
【表1】

したがって、本開示によれば、反応性前駆体の反応と開始性前駆体の開始という、二つの異なる機構によりヒドロゲルが形成されうる。したがって、もたらされるヒドロゲルは、同様に二つの異なるヒドロゲルで作られうる。例えば、第一ヒドロゲルが反応性前駆体から形成されうる一方で、第二ヒドロゲルが開始性前駆体から形成されうる。
【0056】
第一ヒドロゲルは、約10%〜約30%、ある実施形態では約15%〜約25%の量の第一反応性前駆体と、約70%〜約90%、ある実施形態では約75%〜約85%の量の第二反応性前駆体とを含みうる。他の実施形態においては、第一ヒドロゲルは、約70%〜約90%、ある実施形態では約75%〜約85%の量の第一反応性前駆体と、約10%〜約30%、ある実施形態では約15%〜約25%の量の第二反応性前駆体とを含みうる。
【0057】
本開示の組成物を形成するために利用される材料のモジュラスは、組成物の最終用途に依存しうる。例えば、組織足場として使用するために組織に適用される組成物は、医療デバイスを組織に付着させるための使用を目的とする組成物よりもずっと低いモジュラスを有しうる。
【0058】
ある実施形態では、反応性前駆体から形成される第一ヒドロゲルは、約5キロパスカル(kPa)〜約90kPa、ある実施形態では約10kPa〜約50kPaのモジュラスを有し、開始性前駆体から形成される第二ヒドロゲルは、約50kPa〜約5,000kPa、ある実施形態では約100kPa〜約4,000kPaのモジュラスを有しうる。
【0059】
もたらされるヒドロゲルの分解速度に応じて、反応性前駆体により形成されるヒドロゲルの部分が、開始性前駆体により形成されるヒドロゲルの部分よりも急速に分解し得、これにより、組織内部成長、視覚化などを可能にしうる空間がヒドロゲル中に形成されうる。ある実施形態では、反応性前駆体から形成される第一ヒドロゲルは、約1週〜約12週、ある実施形態では約4週〜約10週の期間にわたり分解しうる一方、開始性前駆体から形成される第二ヒドロゲルは、少なくとも約2週の期間にわたり分解し、ある実施形態では分解しない、すなわち永久に体内に残りうる。いくつかの実施形態において、第二ヒドロゲルは、少なくとも約6ヵ月の期間にわたり分解しうる。いくつかの実施形態において、第二ヒドロゲルは、約6週〜約6ヵ月の期間にわたり分解しうる。
【0060】
第二ヒドロゲルが第一ヒドロゲルの上にバリヤ層を形成する場合には、第一ヒドロゲルは約5kPa〜約60kPa、ある実施形態では約10kPa〜約50kPaのモジュラスを有し得、バリヤ層を形成する第二ヒドロゲルは、約100kPa〜約1,000kPa、ある実施形態では約200kPa〜約900kPaのモジュラスを有しうる。したがって、第一ヒドロゲルは約1日〜約7日、ある実施形態では約2日〜約6日の期間にわたり分解し得、バリヤ層は少なくとも約6ヵ月、ある実施形態では約6ヵ月〜約12ヵ月の期間にわたり分解しうる。
【0061】
ヒドロゲルが相互貫通ネットワークを形成する場合には、第一ヒドロゲルが約5kPa〜約20kPa、ある実施形態では約8kPa〜約17kPaのモジュラスを有し、第二ヒドロゲルは約50kPa〜約500kPa、ある実施形態では約75kPa〜約400kPaのモジュラスを有しうる。
【0062】
ヒドロゲルが医療デバイスを組織に付着させるための付着デバイスを形成するために用いられる場合には、第一前駆体が約10kPa〜約50kPa、ある実施形態では約15kPa〜約45kPaのモジュラスを有し得、第二ヒドロゲルが約60kPa〜約200kPa、ある実施形態では約75kPa〜約175kPaのモジュラスを有しうる。第二ヒドロゲルを形成する開始性前駆体は、付着デバイスの約40重量%〜約90重量%、ある実施形態では付着デバイスの約50重量%〜約75重量%の量で存在しうる。第一ヒドロゲルは約1日〜約7日、ある実施形態では約2日〜約6日の期間にわたり分解し得、第二ヒドロゲルは少なくとも約6ヵ月、ある実施形態では約6ヵ月〜約12ヵ月の期間にわたり分解しうる。
【0063】
本開示の組成物が生物活性剤を送達するために用いられる場合には、第一ヒドロゲルが約5kPa〜約50kPa、ある実施形態では約10kPa〜約40kPaのモジュラスを有し得、第二ヒドロゲルが約10kPa〜約100kPa、ある実施形態では約20kPa〜約80kPaのモジュラスを有しうる。
【0064】
ある実施形態では、一つの反応性前駆体と一つの開始性前駆体が第一溶液中に配置されればよく、第二反応性前駆体および任意の開始性前駆体が第二溶液中に配置されうる。これらの溶液の混合時には、反応性前駆体が架橋してベースヒドロゲルを形成しうるが、開始性前駆体は開始剤に曝露されるまで架橋しえない。他の実施形態においては、一つの反応性前駆体および一つ以上の開始性前駆体(単数または複数)が第一溶液中に配置されればよく、第二反応性前駆体が第二溶液中に配置されうる。
【0065】
反応性前駆体および開始性前駆体の組み合わせからもたらされるヒドロゲルの密度は、ヒドロゲルを形成するために使用される開始剤に基づいて、さらに制御されうる。例えば、NHSでキャップされたマルチアームPEG第一反応性ヒドロゲル前駆体、多官能性アミン第二反応性ヒドロゲル前駆体、および直鎖状PEGアクリレート開始性前駆体からは、未反応アクリレート基を含むヒドロゲルがもたらされうる。開始剤、ある実施形態ではUV光に対する曝露時には、アクリレート基がそれ自体とだけでなくPEGアームの末端と反応しうる。開始剤に対する曝露を制御することにより、このようにある量のアクリレート架橋を用いてヒドロゲルの密度をさらに調整しうる。
【0066】
ヒドロゲル密度の調整は、もたらされるヒドロゲルの浸透性に影響し得、例えば、より高密度のヒドロゲルは浸透性がより低くなりうる。ある実施形態では、開始性前駆体(単数または複数)が高密度に架橋され、その結果、反応性前駆体から形成されるヒドロゲル内または外面上に、浸透性がより低いバリヤ層を形成し、このようにして複合ヒドロゲル組成物が形成されうる。
【0067】
本開示によれば、開始性前駆体から形成されるポリマーは、もたらされる複合ヒドロゲルの約5重量パーセント〜約30重量パーセント、ある実施形態ではもたらされるヒドロゲルの約10重量パーセント〜約20重量パーセントを占めればよく、反応性前駆体から形成されるポリマーが、もたらされるヒドロゲルの約5重量パーセント〜約60重量パーセント、ある実施形態ではもたらされるヒドロゲルの約15重量パーセント〜約40重量パーセントを占めうる。もたらされるヒドロゲルの残部は、液体/水からなる。
【0068】
本開示のヒドロゲルの形成は、in situで起こりうる。他の実施形態においては、ヒドロゲル形成はex vivoで、すなわちin situ配置の前に起こりうる。反応性前駆体の開始性前駆体との組み合わせにより、両方のタイプの架橋前駆体の性質を示すヒドロゲルの形成が可能になる。いくつかの実施形態においては、ヒドロゲルの表面を開始剤に曝露する前に、ヒドロゲルが組織欠損内で望ましい形に成形されうる。
【0069】
In situ形成は、一般に、組織への適用時に活性化されて架橋ヒドロゲルを形成しうるヒドロゲル前駆体を有することにより達成されうる。活性化は、組織への前駆体適用前、適用中、または適用後に行われうる。活性化には、例えば、重合プロセスを誘導するステップ、フリーラジカル重合を開始するステップ、または互いに反応する官能基を有する前駆体を混合するステップを含む。したがって、in situ重合には、化学部分の活性化による共有結合の形成と、材料が患者上、患者内、または患者上および患者内の両方に配置される予定の位置での、不溶性物質、例えばヒドロゲルの作製が含まれる。In situ重合可能ポリマーは、患者内でポリマーを形成するように反応させられうるヒドロゲル前駆体から調製されうる。上記のように、ある実施形態では、反応性前駆体および開始性前駆体の両者からヒドロゲルが形成されうる。
【0070】
前述のように、ヒドロゲル前駆体が使用前に溶液中に配置され、溶液が患者に送達されうる。ある実施形態では、前駆体は、緩衝等張食塩水等の生理学的適合性の溶液における適用を可能にするために、実質的に水溶性でありうる。米国特許第4,874,368号、第4,631,055号;第4,735,616号;第4,359,049号;第4,978,336号;第5,116,315号;第4,902,281号;第4,932,942号;第6,179,862号;第6,673,093号;第6,152,943号;および第7,347,850号に記載されているもの等の二重シリンジまたは類似のデバイスを使用して、前駆体溶液を適用しうる。
【0071】
一般に、二つ以上のヒドロゲル前駆体が、噴霧器を介して組織に適用されて、in situでコーティングが形成されうる。例えば、少なくともうち一つが開始性前駆体を含む二つの反応性前駆体溶液が、噴霧器の別々のチャンバ内に配置されうる。噴霧器が作動されると、出てきたスプレーが組織に接触し、二つの反応性前駆体の混合および架橋が生じて、組織表面にコーティング(例えばヒドロゲル)が形成される。
【0072】
ある実施形態では、噴霧器は、二つ以上の反応性前駆体溶液の各々のための別々のスプレーノズルを含み、各ノズルが別々または共通のガス流出口に囲まれている。反応性前駆体溶液は、別々の区画、例えばマルチシリンダシリンジ中に貯蔵され、圧力下でスプレーノズルに移される。ガス流出口を通るガス流の存在下で、架橋可能溶液が霧化され、ガス流中で混合されてスプレーを形成し、これを用いて組織がコーティングされうる。ある実施形態では、CO2ガスカートリッジが、前駆体の送達を促進するために、可逆的または永久にデバイス上に装備されうる。
【0073】
ある実施形態は、吸引−洗浄装置をヒドロゲル前駆体送達デバイスと組み合わせるステップを含む。このような組み合わせの利点は、凝固血および接着イオジェニック(adhesioniogenic)材料を組織から洗浄でき、組み合わせることにより単一のデバイスを用いたヒドロゲルの配置が可能になりうることである。
【0074】
本開示のヒドロゲルは、例えば接着剤、止血剤、シーラント、移植物、保護バリヤ、薬物送達デバイス、それらの組み合わせなど等の要素を形成するためにも使用されうる。形成されうる移植物には、例えば、マトリックス、人工血管、心臓弁、人工臓器、人工骨、移植可能微小凸レンズ、血管グラフト、ステント、縫合糸、ステープル、クリップ、メッシュ、スリング、ネジ、ピン、ケーブル、軟骨移植物、脊椎移植物およびそれらの組み合わせが含まれる。移植物は、哺乳類の体内の軟組織または硬組織を増強するためにも使用されうる。軟組織増強の用途の例には、括約筋(例えば泌尿器、肛門、食道)増強;人工皮膚としての使用;皮膚のしわの治療;および/または瘢痕の治療が含まれる。硬組織増強の例には、骨および/または軟骨組織の修復および/または置換が含まれる。本開示のヒドロゲルおよび/または移植物で治療できる他の組織欠損には、例えば、胃食道逆流疾患(GERD)を治療するための下部食道括約筋を含む括約筋バルキング;尿失禁を治療するための尿道周囲バルキング;例えばポリープ切除術における、組織解剖および/または切除を助ける組織層間のクッション作製;癒着防止;形成手術において真皮充填材として;唇、乳房、および他の身体組織の欠損の治療;それらの組み合わせなどが含まれる。
【0075】
ある実施形態では、ヒドロゲルを用いて、開始性前駆体により生成されるヒドロゲルにより形成される剛性または高密度の外部と、反応性前駆体により生成されるヒドロゲルにより形成される、より低密度のより可撓性のある内部とを有する、半可撓性の椎間板を形成しうる。ある実施形態では、置換が必要な椎間板に類似する形に作られたテンプレートが用いられうる。テンプレートがヒドロゲル前駆体で満たされて、ヒドロゲルが形成されうる。それから、表面上の開始性前駆体の架橋を誘導するためにヒドロゲルが開始剤に曝露され、これによりヒドロゲル内部を包含する高密度の外層またはバリヤ層が形成されうる。
【0076】
椎間板移植物の形成では、手術中または手術前に移植物が形成されうる。例えば、まずキャリパまたは類似のデバイスを用いて修復される欠損の長さおよび寸法を測定することにより、手術中に適切な移植物サイズが決定されうる。それから外科スタッフは、反応性前駆体および開始性前駆体をテンプレートに導入し、反応性前駆体に第一ヒドロゲルを形成させることにより、上述のテンプレートを利用して、所望のサイズの移植物を形成しうる。それから組成物が開始剤に曝露され、これにより第一ヒドロゲル内部を包含する高密度の外層またはバリヤ層が形成され、これにより椎間板移植物が生成されうる。
【0077】
あるいは、X線、MRIなどを含む放射線撮影技術を用いて、適当な移植物のサイズが術前に決定され、手術前に椎間板移植物が上述のように形成されうる。
【0078】
他の実施形態においては、反応性前駆体が組織欠損に適用され、これにより、その中に第一ヒドロゲルを形成し、開始性前駆体がバリヤ層として機能する第二ヒドロゲルを、組織欠損をカバーする第一ヒドロゲルの表面の少なくとも一部の上に形成しうる。
【0079】
ヒドロゲルを形成するための材料の選択は、本開示のヒドロゲル組成物の最終用途に応じて調整されうる。例えば、タンパク質癒着を防止せねばならない場合にはポリエチレングリコール系ポリマーが所望され得;摺動、滑動および/または潤滑性の強化が望ましい場合にはヒアルロン酸系ポリマーが所望され得;細胞付着のための接着部位を提供するためにはコラーゲン系ポリマーが所望され得;長期および/または永久移植物などには合成ポリマーが所望されうる、などである。
【0080】
ある実施形態では、反応性ヒドロゲル前駆体は、生物活性剤を含むヒドロゲルを形成しうる。開始性前駆体が、反応前または反応後に前駆体に加えられうる。それから、開始性前駆体が反応開始されてバリヤ層を形成しうる。バリヤ層は、反応性前駆体により形成されるヒドロゲルからの生物活性剤のバリヤの方向への拡散を妨げ、これにより、生物活性剤を一方向に、すなわちバリヤ層と反対の方向に投与させる。
【0081】
ある実施形態では、反応性および開始性ヒドロゲル前駆体が、モールドの底の上の層に組み合わせられてもよい。それからベース層が開始剤に曝露されて、底層がさらに架橋されうる。それから前駆体を含む第二層が底層の上に配置され、スクリーンを用いて開始剤に対する第二層の曝露が制限されうる。こうして、遮蔽された部分は架橋しないが、遮蔽されない部分はさらに架橋し、これにより層中に様々な程度の架橋を提供しうる。追加の層は、同じまたは異なるスクリーンを用いて加えられうる。各層が、同じでも異なってもよい生物活性剤を含みうる。様々な量の架橋により、交互の分解速度が提供され、これにより生物活性剤の様々な放出速度が提供されうる。開始剤は、医療デバイスとの接触前または後に、ヒドロゲルと接触させられうる。ヒドロゲルにより組織に付着させられうる医療デバイスには、縫合糸、ステープル、タック、クリップ、リベット、それらの組み合わせなどが含まれる。
【0082】
他の実施形態においては、反応性および開始性ヒドロゲル前駆体の混合物が、メッシュ等の移植物に吹き付けられまたは適用されうる。メッシュは、開始性ヒドロゲルのための開始剤を含むフィラメント状基材でありうる。反応性ヒドロゲルが、メッシュの上にコーティングを形成しうる。コーティングは数日にわたり分解し、これにより接着が防止されうる。コーティングの分解は、メッシュに組織内部成長のための孔をつくるのにも役立ちうる。開始性ヒドロゲルは同様の分解をせず、これにより組織に対するメッシュの接着が維持される。
【0083】
他の実施形態においては、メッシュが反応性前駆体および開始性前駆体(単数または複数)と接触されればよく、反応性前駆体が第一ヒドロゲルを形成し、開始性前駆体が第二ヒドロゲルを形成して、メッシュを組織に固定しうる。ある実施形態では、第一ヒドロゲルが、第二ヒドロゲルの前に形成しうる。他の実施形態においては、第二ヒドロゲルが、第一ヒドロゲルの前に形成されうる。第一ヒドロゲルが第二ヒドロゲルの前に形成するいくつかの実施形態においては、第一ヒドロゲルは、メッシュの組織に対する一時的な接着および配置を許容して、メッシュの組織に対する再配置および再接着を可能にでき、その後に第二ヒドロゲルがメッシュの永久配置のために形成される。このような場合には、第一ヒドロゲルは、メッシュの組織に対する接着および再接着のために少なくとも10分間、ある実施形態では約10分間〜約40分間、ある実施形態では約12分間〜約25分間、粘着性を保たなければならない。この時間以後に、第二ヒドロゲルが形成されうる。
【0084】
ある実施形態では、本開示のメッシュ移植物は、フィラメント状基材の少なくとも一部の上にフィルムコーティングを有する、フィラメント状基材を含みうる。ある実施形態では、フィルムコーティングは、少なくとも一つのビニル基を有する開始性前駆体を含む凍結乾燥組成物を、求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体と求核基を含む第二反応性前駆体とを含む第一ヒドロゲルと組み合わせて含みうる。使用においては、第一ヒドロゲルが再水和されてメッシュが取り外し可能に組織に付着させられ、開始性前駆体が開始剤に曝露されて第二ヒドロゲルが形成され、メッシュが組織にしっかりと固定されうる。第一ヒドロゲルは、体液との接触、食塩水の追加、それらの組み合わせなどの時に再水和されうる。
【0085】
さらに他の実施形態においては、反応性および開始性ヒドロゲル前駆体の混合物が、組み合わせられて組織の表面下に注入されればよく、組織表面上にもプールされうる。こうして形成された組織表面下および組織表面上のヒドロゲルが、縫合糸または他の医療デバイスと接触させられうる。それから医療デバイスがヒドロゲルアンカと接触させられ、これがデバイスを組織に固定するのを助けうる。例えば、縫合糸アンカでは、ヒドロゲルが形成され、縫合糸がそれに通されうる。開始性前駆体からの第二ヒドロゲルの形成の前に、反応性前駆体が第一ヒドロゲルを形成しうる。他の実施形態においては、反応性前駆体から形成されるヒドロゲルの前に、開始性前駆体から形成されるヒドロゲルが形成されうる。
【0086】
他の実施形態においては、反応性および開始性ヒドロゲル前駆体の混合物を用いて、アンカまたはリベット等の移植物付着デバイスが形成されうる。メッシュまたは他の移植物が、前駆体により組織に固定されうる。移植物は、上述の縫合糸アンカと同様に、混合物が押し出される穴を有しうる、すなわちヒドロゲルが組織の表面下に注入され、組織をカバーする移植物の表面上にプールされうる。それから、適所に移植物を保つために反応性ヒドロゲルが形成され、移植の後に、ヒドロゲル混合物が開始剤に曝露され、移植物が組織に固定されうる。
【0087】
例えば、ある実施形態では、求電子基を有するマルチアームポリエーテルを有する第一反応性前駆体と、求核基を有する第二反応性前駆体と、少なくとも一つのビニル基を有する少なくとも一つの開始性前駆体とを含む混合物が形成されうる。メッシュが組織と接触させられ、混合物がメッシュを通して組織に注入されうる。混合物が、メッシュと接触して組織表面下および組織表面上に第一ヒドロゲルを形成しうる。開始性前駆体が開始剤と接触させられて第二ヒドロゲルが形成され、これによりメッシュを組織に付着させるための付着デバイスが形成されうる。
【0088】
ヒドロゲル前駆体(単数または複数)および/またはもたらされるヒドロゲルは、外科的手技の間のその可視性を改善するために、可視化剤を含みうる。可視化剤は、移植可能医療デバイスにおける使用に適する、色素等の様々な非毒性の着色物質から選択されうる。適切な色素は当業者の認識範囲内であり、例えば米国特許第7,009,034号に記載のような、例えばin situで形成されるヒドロゲルの厚さを視覚化するための染料を含みうる。いくつかの実施形態においては、適切な色素には、例えば、FD&Cブルー#1、FD&Cブルー#2、FD&Cブルー#3、FD&Cブルー#6、D&Cグリーン#6、メチレンブルー、インドシアニングリーン、他の着色色素、およびそれらの組み合わせが含まれうる。蛍光化合物(例えばフルオレセイン(flurescein)またはエオシン)、X線造影剤(例えばヨード化合物)、超音波造影剤、およびMRI造影剤(例えばガドリニウム含有化合物)のような追加的な可視化剤が、使用されうると想定される。
【0089】
可視化剤は、ヒドロゲル前駆体溶液中に存在しうる。着色物質は、もたらされるヒドロゲル中に取り込まれても取り込まれなくてもよい。
【0090】
可視化剤は、少量で、ある実施形態では1%重量/体積未満、ある実施形態では0.01%重量/体積未満、ある実施形態では0.001%重量/体積未満の濃度で用いられうる。
【0091】
ヒドロゲル前駆体、ならびにその反応生成物は、薬物療法または生物活性剤の送達にも用いられうる。ある実施形態では、ヒドロゲルが追加の生物活性剤でコーティングされ、またはこれを含みうる。本明細書で用いられるところの「生物活性剤」という用語は、最広義の意味で用いられ、臨床用途を有する任意の物質または物質の混合物を含む。したがって、生物活性剤は、例えば色素のように、それ自体薬理活性を有しても有しなくてもよい。あるいは、生物活性剤は、治療または予防効果を提供する任意の薬剤、組織成長、細胞成長、細胞分化に影響または関与する化合物、癒着防止化合物、免疫応答等の生物学的作用を誘発することが可能でありうる化合物であり得、または一つ以上の生物学的プロセスにおいて他の任意の役割を果たすものでもありうる。生物活性剤は、物質の任意の適切な形、例えばフィルム、粉末、液体、ゲルなどの形でヒドロゲルに適用されうると想定される。
【0092】
上記のように、マルチアームPEGまたはPEGスターを含む実施形態においては、生物活性剤が、PEGのコア、PEGのアーム、またはそれらの組み合わせに取り込まれうる。ある実施形態では、生物活性剤が、PEG鎖の反応基に付着させられうる。生物活性剤は、共有結合的に、非共有結合的に、すなわち静電的に、チオール媒介またはペプチド媒介結合を通して、またはビオチン−アジビン(adivin)化学などを使用して、結合されうる。
【0093】
本開示にしたがって利用されうる生物活性剤のクラスの例には、例えば癒着防止剤;抗菌物質;鎮痛剤;解熱剤;麻酔剤;抗てんかん剤;抗ヒスタミン剤;抗炎症剤;心臓血管薬;診断用剤;交感神経作用剤;コリン性作用剤;抗ムスカリン剤;抗痙攣剤;ホルモン類;成長因子;筋弛緩剤;アドレナリン作動ニューロン遮断剤;抗腫瘍剤;免疫原性剤;免疫抑制剤;胃腸薬;利尿剤;ステロイド類;脂質類;リポ多糖類;多糖類;血小板活性化剤;凝血因子;および酵素が含まれる。生物活性剤の組み合わせが使用されうることも企図される。
【0094】
ヒドロゲル、ある実施形態ではヒドロゲル移植物と、周囲組織との間に癒着が形成するのを防ぐために、癒着防止剤が使用されうる。これらの薬剤のいくつかの例には、ポリ(ビニルピロリドン)、カルボキシメチルセルロース、ヒアルロン酸、ポリエチレンオキシド、ポリビニルアルコール類、およびそれらの組み合わせ等の親水性ポリマーが含まれるがこれに限られない。
【0095】
生物活性剤として含まれうる適切な抗菌剤には、トリクロサン、別名2,4,4’−トリクロロ−2’−ヒドロキシジフェニルエーテル;クロルヘキシジンならびに酢酸クロルヘキシジン、グルコン酸クロルヘキシジン、塩酸クロルヘキシジン、および硫酸クロルヘキシジンを含むその塩類;銀ならびに酢酸銀、安息香酸銀、炭酸銀、クエン酸銀、ヨウ素酸銀、ヨウ化銀、乳酸銀、ラウリン酸銀、硝酸銀、酸化銀、パルミチン酸銀、プロテイン銀およびスルファジアジン銀を含むその塩類;ポリミキシン;テトラサイクリン;トブラマイシンおよびゲンタマイシン、リファンピシン、バシトラシン、ネオマイシン、クロラムフェニコール、およびミコナゾール等のアミノグリコシド類;オキソリン酸、ノルフロキサシン、ナリジキシン酸、ペフロキサシン、エノキサシンおよびシプロフロキサシン等のキノロン類;オキサシリンおよびピプラシル等のペニシリン類;ノノキシノール9;フシジン酸;セファロスポリン類;およびそれらの組み合わせが含まれる。加えて、ウシラクトフェリンおよびラクトフェリシンB等の、抗菌タンパク質類およびペプチド類が、生物活性剤として含まれうる。
【0096】
生物活性剤として含まれうる他の生物活性剤には、局所麻酔剤;非ステロイド性抗受精剤;副交感神経作動剤;精神治療剤;精神安定剤;鬱血除去剤;催眠鎮静剤;ステロイド類;スルホンアミド類;交感神経様作動剤;ワクチン類;ビタミン類;抗マラリア剤;抗片頭痛剤;L−ドーパ等のパーキンソン病治療剤;抗痙攣剤;抗コリン作用剤(例えばオキシブチニン);鎮咳剤;気管支拡張剤;冠状血管拡張剤およびニトログリセリン等の心臓血管剤;アルカロイド類;鎮痛剤;コデイン、ジヒドロコデイノン、メペリジン、モルヒネなど等の麻酔剤;サリチル酸類、アスピリン、アセトアミノフェン、d−プロポキシフェンなど等の非麻酔剤;ナルトレキソンおよびナロキソン等のオピオイド受容体アンタゴニスト類;抗癌剤;抗痙攣剤;制吐剤;抗ヒスタミン剤;ホルモン剤、ヒドロコルチゾン、プレドニソロン、プレドニゾン、非ホルモン剤、アロプリノール、インドメタシン、フェニルブタゾンなど等の抗炎症剤;プロスタグランジン類;細胞毒;化学療法剤、エストロゲン類;抗菌剤;抗生物質;抗真菌薬;抗ウイルス剤;抗凝固剤;抗痙攣剤;抗うつ薬;抗ヒスタミン剤;および免疫学的薬剤が含まれる。
【0097】
ヒドロゲルに含まれうる適切な生物活性剤の他の例には、例えば、ウイルスおよび細胞;ペプチド類、ポリペプチド類、およびタンパク質類、ならびにそのアナログ類、突然変異タンパク質類および活性断片;イムノグロブリン類;抗体類;サイトカイン類(例えばリンホカイン類、モノカイン類、ケモカイン類);血液凝血因子;造血因子;インターロイキン類(IL−2、IL−3、IL−4、IL−6);インターフェロン類(β−IFN、α−IFNおよびγ−IFN);エリスロポエチン;ヌクレアーゼ類;腫瘍壊死因子;コロニー形成刺激因子(例えばGCSF、GM−CSF、MCSF);インシュリン;抗腫瘍剤および腫瘍抑制剤;フィブリン、トロンビン、フィブリノーゲン、合成トロンビン、合成フィブリン、合成フィブリノーゲン等の血液タンパク質類;生殖腺刺激ホルモン類(例えばFSH、LH、CG等);ホルモン類およびホルモンアナログ類(例えば成長ホルモン);ワクチン類(例えば腫瘍、細菌および、ウイルス抗原);ソマトスタチン;抗原;血液凝固因子;成長因子(例えば神経成長因子、インスリン様成長因子);骨形態形成タンパク質類;TGF−B;タンパク質阻害剤;タンパク質アンタゴニスト類;タンパク質アゴニスト類;アンチセンス分子、DNA、RNA、RNAi等の核酸類;オリゴヌクレオチド類;ポリヌクレオチド類;およびリボザイム類が含まれる。
【0098】
生物活性剤は、ボーラスとして、ある期間にわたり、またはその組み合わせにおいてヒドロゲルから放出されうる。反応性前駆体はより浸透性のあるヒドロゲルを形成し、ヒドロゲルからの生物活性剤の拡散を許容しうる。ある実施形態では、開始性前駆体が架橋されて、反応性前駆体から形成されたヒドロゲルの上にバリヤ層を形成し、これにより、そこからの生物活性剤の拡散を減少させうる。
【0099】
次に、本開示の実施形態を、図を参照して記載する。図1Aを参照すると、反応性前駆体が架橋して、in situで組織120上に生物活性剤110を任意に含むヒドロゲル100を形成する。図1Bに示すように、その後ヒドロゲル100がUV光等の開始剤130に曝露されて、中に含まれる開始性前駆体(単数または複数)の反応が開始されうる。図1Cは、ヒドロゲル100上のバリヤ層140の形成を示すが、これは開始性前駆体(単数または複数)により形成され、ヒドロゲルからの生物活性剤110の拡散を妨げる。したがって生物活性剤110は、バリヤ層140の存在により、生物活性剤110を必要とする組織120内に一方向に拡散しうるが、組織120に隣接するいかなる管腔または領域にも拡散しない。生物活性剤の一方向性分布は、例えば、硬膜、肺、または腸への化学療法剤;心臓血管組織への抗凝固薬;心臓への抗不整脈薬;損傷組織への抗炎症剤または鎮痛剤;損傷組織を治療するための止血剤;および同類のもの、ならびにそれらの組み合わせの直接送達に使用されうる。
【0100】
図2Aに示すように、反応性前駆体から椎間板(spinal disc)の形でヒドロゲル200が形成されうる。図2Bはヒドロゲル200の側面図であり、これが開始剤220に曝露されて、ヒドロゲル200中の任意の開始性前駆体がゲル化されうる。図2Cは、反応性前駆体から形成されたヒドロゲル200と開始性前駆体から形成されたより高密度のバリヤ層230とを有する、もたらされるディスクの断面図である。開始性前駆体の反応により表面領域の密度が高められ、これにより、ヒドロゲル200の表面上により高密度のヒドロゲル230の「皮膜」またはバリヤが作製されうる。このような様式で、非分解性椎間板代用物等の移植物が形成されうる。
【0101】
ある実施形態では、二相ヒドロゲル移植物が形成されうる。例えば、テンプレートおよび/またはスクリーンを使用して、二相ヒドロゲル移植物が形成されうる。テンプレートおよびスクリーン(単数または複数)は、任意の形またはサイズでありうる。ある実施形態では、テンプレートは、(実験室ビーカーと同様の)ベースを有するシリンダであり得、スクリーンは、様々なサイズの一連の円形ディスクを含みうる。テンプレートおよびスクリーンを利用して、高密度底層、中間層、および高密度最上層が、テンプレートおよびスクリーン(単数または複数)により形成されうる。例えば、反応性および開始性ヒドロゲル前駆体をテンプレートのベースに適用し、反応性前駆体にヒドロゲルを形成させ、それからヒドロゲルを開始剤に曝露して開始性前駆体(単数または複数)を架橋し、これにより高密度底層を形成することにより、高密度底層が形成されうる。そして、これに反応性前駆体を、開始性前駆体を任意に用いて適用し、それらを反応させることにより、中間層が底層の上に形成されうる。それから、例えば中間層にスクリーンを適用してから反応性および開始性ヒドロゲル前駆体の両方を中間層に適用し、反応性前駆体にヒドロゲル層を形成させることにより、高密度最上層が形成されうる。それから、最上部のヒドロゲルが開始剤に曝露されて、最上部のヒドロゲル中の開始性前駆体(単数または複数)が架橋されて、高密度最上層が形成されうる。スクリーンは、中間層の任意の開始性前駆体の架橋を防ぐ。スクリーンは残存してもよいし、ある実施形態ではスクリーンが除去されうる。したがってもたらされるゲルは、より高密度の最上層およびより高密度の底層、ならびにより低密度の中間層を有する。
【0102】
形成される層の各々が、同じまたは異なるヒドロゲル前駆体を含みうる。加えて、層の各々が、生物活性剤を含みうる。各層中の生物活性剤のタイプおよび量は、同じでも異なってもよい。
【0103】
二相薬物送達ヒドロゲル移植物を形成する方法を、図3を参照してさらに記載する。図3に示すように、ヒドロゲル前駆体の層がテンプレート310内に配置される。反応性前駆体は、互いに曝露された時にヒドロゲル300を形成する。開始性ヒドロゲル前駆体は、架橋を増加させるために開始剤320に曝露され、これにより高密度底層が形成される。図3Bは、様々なサイズのいくつかのスクリーン330を示す。スクリーン330が、ヒドロゲル300上に配置されうる。それから、追加的前駆体がヒドロゲル300の上に加えられ、反応させられ、開始剤320に任意に曝露されて次の層(図示せず)が形成されうる。このプロセスが繰り返されて、前駆体の開始剤への曝露をブロックするスクリーンの存在によってより低密度のコアを有する高密度架橋ゲルが作製されうる。図3Cに示すように、遮蔽された中心350は、ヒドロゲル340のスクリーンによりカバーされない部分よりも低密度のままでありうる。ある実施形態では、異なるサイズおよび/または形のスクリーン330を用いて、異なる中心が形成されうる。もたらされる二相薬物送達ヒドロゲル移植物340は、このようにして、より高密度のヒドロゲル340と、中心部を形成するより低密度のヒドロゲル350を含みうる。
【0104】
in situ配置時には、二相薬物送達ヒドロゲルの中心ヒドロゲル部分350が、より高密度のヒドロゲル340よりも速い速度で分解しうる。したがって、より高密度のヒドロゲル340のより遅い分解速度により、生物活性剤の時間をかけた段階的放出が提供され、ヒドロゲル340が分解した時に、より低密度の中心350からの追加的放出がボーラスとして提供されうる。他の実施形態においては、中心ヒドロゲルが周囲のヒドロゲルよりもゆっくり分解し、ボーラス送達と、その後のより遅い放出維持量が可能になりうる。これは、持続放出の用途で有益であると分かるかもしれない。即時/持続放出薬物送達システムは、例えば麻酔剤、抗凝血剤、抗炎症剤、化学療法剤、ペプチド類、成長因子、それらの組み合わせなどの送達の用途で有用でありうる。
【0105】
移植物を形成するための本開示によるヒドロゲルの別の使用が、図5Aおよび5Bに描写される。移植物400は、メッシュ410を含む。メッシュ410は、過マンガン酸/酢酸、過硫酸アンモニウム/酢酸、過硫酸カリウム/2,2’−アゾビス[2−(2−イミダゾリン(dimidazolin)−2−イル)プロパン]ジヒドロクロリド(2,2’−アゾビス[2−(2−イミダゾリン(dimidazolin)−2−イル)プロパン]ジヒドロクロリドは、VA044(Wako)として市販されている、過硫酸アンモニウム/テトラメチレンジアミン、それらの組み合わせなど等の開始剤でコーティングされうる。PEG−NHSおよびPEG−アクリレート420等の求電子性反応性前駆体および開始性前駆体の混合物が、メッシュ410に噴霧されうる。それからメッシュ410全体が、トリリジン等の求核性反応性前駆体および未反応アクリレート等の追加的な開始性前駆体でコーティングされうる。メッシュ410に接触するPEG−アクリレートが、メッシュおよび架橋430中の過マンガン酸/酢酸により反応開始されうる。PEG−NHSおよびトリリジンも反応して、メッシュ410の孔を含むメッシュ全体の表面全体に、より低密度に架橋したヒドロゲル420を形成しうる。図5Bに描写するように、PEG−NHS−トリリジンヒドロゲル420は、約4日〜約6日の期間にわたり分解して、メッシュ410の孔440を露出させ、これにより組織内部成長のための空間を可能にしうる。このようなメッシュは、例えばヘルニア修復において使用されうる。
【0106】
他の実施形態においては、図6Aに示すように、縫合糸アンカ600を形成するために本開示のヒドロゲルが利用されうる。シリンジ610により、求電子性および求核性(反応性)ヒドロゲル前駆体および開始性ヒドロゲル前駆体の混合物620が組織630の下に注入されて、組織630の表面640の下および上の両方に軟質ヒドロゲル620が形成されうる。図6Bに示すように、軟質ヒドロゲル620がUV光670により反応開始されて、高密度に架橋した縫合糸アンカ650が作製されうる。それから、図6Cに示すように、縫合糸660が縫合糸アンカ650に通されうる。このような縫合糸アンカは、例えば、in situ損傷閉鎖、骨アンカ、腱修復、それらの組み合わせなどのために用いられうる。
【0107】
図にはないが、他の実施形態においては、まず潜在的ヒドロゲル前駆体を反応開始させてから、開始性ヒドロゲルの形成後に反応性前駆体を反応させうる。
【0108】
さらに他の実施形態においては、図7A〜Cに示すように、移植物を組織に接着するために、本開示のヒドロゲルからリベットが形成されうる。ヘルニア修復のために、移植物700が腹膜710に適用されうる。シリンジ720を用いて、腹膜710の下から(または図にはないが上から)、移植物700の穴701、702、703、704、705、706、707、および708を通してヒドロゲル混合物730を注入しうる。ヒドロゲル混合物730は、腹膜の下に軟質ヒドロゲル740を形成し、穴701、702、703、704、705、706、707、および708を満たし、移植物700の非組織側にわずかにプールしうる。それから軟質ヒドロゲル740が開始剤750に曝露されて、高密度に架橋したヒドロゲルリベット760が形成され、これにより、移植物700が腹膜710に接着されうる。
【0109】
上記のように、ある実施形態では、本開示のヒドロゲル組成物は様々なモジュラスを有しうる。当業者は、ある実施形態では、組成物が適用される予定の組織にもとづいて、本開示の組成物を形成するために利用される成分を調整しうる。図10は、様々な組織についての弾性モジュラスを提供し、これを、所望のモジュラスを有する本開示の組成物の調製する際にガイドとして利用しうる。
【0110】
ある実施形態では、図11に描写するように、ヒドロゲル組成物が、組織の欠損を直すために利用されうる。図11は、軟骨下骨の欠損を修復するための、本開示の組成物の使用を描写する。反応性前駆体および開始性前駆体が、軟骨下骨865の欠損820に適用され、これによりその中に第一ヒドロゲル800が形成されうる。放射線源830が、欠損を囲む関節軟骨855に隣接するヒドロゲル800の表面に適用され、これにより、バリヤ層840として機能する第二ヒドロゲルが表面上に形成されうる。
【0111】
上記のように、ある実施形態では、本開示のヒドロゲル組成物は、第二ヒドロゲルに分散された一つのヒドロゲルを含みうる。図12Aに描写するように、分散領域920は、反応性前駆体で形成された第一ヒドロゲル910の中に、開始性前駆体で形成された第二ヒドロゲルで形成されたコアを含みうる。あるいは、図12Bに描写するように、第一ヒドロゲル910の中に多くの分散領域920が形成されうる。図12Aおよび12Bには示されないが、いくつかの実施形態では、開始性前駆体から形成されるバリヤ層が、本開示のヒドロゲル組成物の上に形成されうる。
【0112】
生物活性剤が、第一ヒドロゲル、第二ヒドロゲル、または両方に含まれうる。生物活性剤は、ある実施形態では、リポソーム、ミクロスフェア、微小気泡、それらの組み合わせなどの中にありうる。生物活性剤が第一および第二ヒドロゲル中に存在する場合には、同じまたは異なる生物活性剤がヒドロゲルに含まれうる。第一ヒドロゲルからは約1日〜約6週、ある実施形態では約1週〜約4週の期間にわたり生物活性剤が放出され、第二ヒドロゲルからは約5日〜約12週、ある実施形態では約2週〜約8週の期間にわたり生物活性剤が放出されうる。
【0113】
複数の放出プロフィールを有するヒドロゲルを含む組成物の例には、米国特許出願公開第2009/0047349号に開示されるものが含まれ、その開示の全体が参照により本明細書に組み込まれる。
【0114】
以下の実施例は、本開示の実施形態を例示するために提出される。これらの実施例は、例示だけを目的とし、本開示の範囲を制限することを目的としない。また、別段の定めがない限り、部およびパーセントは重量を基準とする。本明細書で使用されるところの「室温」とは、約20℃〜約30℃の温度をさす。
【実施例】
【0115】
(実施例1)
溶液調製
第一反応性前駆体:リン酸バッファーpH4.04中PEG−ジアクリレートの80%溶液を調製した。この溶液にPEG−NHSを、0.13g/mlの濃度で加えた(3mlのリン酸バッファー中80%ジアクリレート中0.39グラムのPEG−NHS)。
【0116】
第二反応性前駆体:ホウ酸塩バッファー中リジンの0.01g/ml溶液を調製し、pHを8.6に調節した。
【0117】
開始性前駆体:エタノール中4,4’−ビス(ジエチル−アミノ)ベンゾフェノン(励起波長365nm)の10mg/ml溶液を調製した。
【0118】
表2(下)に詳しく記載されるように、様々な量の開始性前駆体溶液を第一反応性前駆体に加えた。
【0119】
第一および第二反応性前駆体の反応
等しい体積の第一および第二反応性前駆体を、別々のシリンジにロードした。シリンジを接続し、溶液を15秒間混合した。次に、ヒドロゲルの完全な架橋を確保するために、溶液を15分間おいた。
【0120】
開始性前駆体の架橋
それから各架橋ヒドロゲルを、それぞれのシリンジから除去し、いくつかのシリンダに切った。それから、架橋ヒドロゲルを様々な量のUV光(表2参照)に曝露して開始性前駆体の架橋を開始させ、開始性ヒドロゲルを形成した。ゲルのシリンダに長い針を貫通させ、UV源の下に配置し、回転させて均一に硬化させた。
【0121】
ヒドロゲル組成物試験
シリンダが硬化したら、各々を12mmのフラットプローブの下に配置し、最初の高さの最大80%まで、または壊れるまで、0.08mm/秒の速度で20グラムのトリガー力および5グラムの破壊感度で圧縮した。各硬化ヒドロゲルについての結果が、表2に記録されている。図8は、表2のデータを示す棒グラフである(サンプルと100マイクロリットルの光開始剤)。図9は、開始性ヒドロゲル(上の線)と非開始性ヒドロゲル(下の線)の比較である。
【0122】
【表2】

(実施例2)
第二ヒドロゲル前駆体中のリジンの代わりにトリリジンを使用して、実施例1の調製を繰り返した。試験の結果が、下表3に提供される。
【0123】
【表3】

上記の実施例で示すように、開始性前駆体の量および開始剤のUV曝露の量を変化させることにより、様々な程度の架橋が達成された。加えて、使用される第一および第二ヒドロゲル前駆体に応じて、UV曝露の前に様々なレベルの架橋が達成された。
【0124】
以上の記載は、多くの詳細を含むが、これらの詳細は、本明細書の開示の範囲に対する制限としてではなく、その特に有用な実施形態の単なる例示として解釈されねばならない。当業者は、添付の請求項に記載の本開示の範囲および精神の範囲内の、他の多くの可能性を思い付くだろう。
【0125】
摘要
本開示は、ヒドロゲル組成物およびそれを使用する方法に関する。ヒドロゲル組成物は、接触時に互いに反応する前駆体ならびに開始剤との接触時に反応する前駆体を含みうる。ある実施形態では、もたらされるヒドロゲルは、様々なレベルの架橋と、より高密度の領域およびより低密度の領域を有しうる。
【特許請求の範囲】
【請求項1】
ヒドロゲルを含む移植物であって、該ヒドロゲルは
求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;
求核基を含む、第二反応性前駆体と;
少なくとも一つのビニル基を含む、少なくとも一つの開始性前駆体と
を含む、移植物。
【請求項2】
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、請求項1に記載の移植物。
【請求項3】
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、請求項1に記載の移植物。
【請求項4】
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、請求項1に記載の移植物。
【請求項5】
生物活性剤をさらに含む、請求項1に記載の移植物。
【請求項6】
前記第一反応性前駆体が前記第二反応性前駆体と反応して第一ヒドロゲルを形成し、前記開始性前駆体が、開始剤との接触時に第二ヒドロゲルを形成する、請求項1に記載の移植物。
【請求項7】
前記開始剤が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される、請求項6に記載の移植物。
【請求項8】
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、請求項7に記載の移植物。
【請求項9】
前記第二ヒドロゲルが、前記第一ヒドロゲルの少なくとも一部の上にバリヤ層を形成する、請求項6に記載の移植物。
【請求項10】
前記第一ヒドロゲルが、組織欠損内に配置され、前記第二ヒドロゲルが、該欠損の上にバリヤ層を提供する、請求項6に記載の移植物。
【請求項11】
前記第一ヒドロゲルが、約5kPa〜約500kPaのモジュラスを有し、前記第二ヒドロゲルが、約50kPa〜約5,000kPaのモジュラスを有する、請求項6に記載の移植物。
【請求項12】
前記第一ヒドロゲルが、約4週〜約10週の期間にわたり分解し、前記第二ヒドロゲルが、約6週〜約6ヵ月の期間にわたり分解する、請求項6に記載の移植物。
【請求項13】
前記移植物が、マトリックス、人工血管、心臓弁、人工臓器、人工骨、移植可能微小凸レンズ、血管グラフト、ステント、縫合糸、ステープル、クリップ、メッシュ、スリング、ネジ、ピン、ケーブル、軟骨移植物、脊椎移植物、およびそれらの組み合わせからなる群より選択される、請求項6に記載の移植物。
【請求項14】
前記移植物が、軟骨移植物を含み、前記第一ヒドロゲルが、軟骨の欠損内にあり、前記第二ヒドロゲルが、該欠損の上にバリヤ層を形成する、請求項13に記載の移植物。
【請求項15】
前記移植物が、前記第二ヒドロゲルにより囲まれた前記第一ヒドロゲルを含む、椎間板移植物を含む、請求項13に記載の移植物。
【請求項16】
前記移植物が、人工皮膚を含む、請求項13に記載の移植物。
【請求項17】
求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体を、求核基を含む第二反応性前駆体と組み合わせて含む、第一ヒドロゲルと;
少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体を含む、第二ヒドロゲルと
を含む、複合ヒドロゲル組成物であり、
該第二ヒドロゲルが、該第一ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成する、複合ヒドロゲル組成物。
【請求項18】
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、請求項17に記載の複合ヒドロゲル組成物。
【請求項19】
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、請求項17に記載の複合ヒドロゲル組成物。
【請求項20】
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、請求項17に記載の複合ヒドロゲル組成物。
【請求項21】
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第二ヒドロゲルをさらに架橋する、請求項17に記載の複合ヒドロゲル組成物。
【請求項22】
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、請求項21に記載の複合ヒドロゲル組成物。
【請求項23】
生物活性剤をさらに含む、請求項17に記載の複合ヒドロゲル組成物。
【請求項24】
前記生物活性剤が、前記第一ヒドロゲル中にある、請求項23に記載の複合ヒドロゲル組成物。
【請求項25】
前記生物活性剤が、約3日〜約6週の期間にわたり前記第一ヒドロゲルから放出される、請求項23に記載の複合ヒドロゲル組成物。
【請求項26】
前記第二ヒドロゲルが、前記複合ヒドロゲル組成物の約5重量%〜約30重量%を構成する、請求項17に記載の複合ヒドロゲル組成物。
【請求項27】
前記第一ヒドロゲル中に少なくとも一つの分散領域を形成する少なくとも一つの開始性前駆体を含む第三ヒドロゲルをさらに含む、請求項17に記載の複合ヒドロゲル組成物。
【請求項28】
前記第二ヒドロゲルおよび前記第三ヒドロゲルが、同じである、請求項27に記載の複合ヒドロゲル組成物。
【請求項29】
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第三ヒドロゲルをさらに架橋する、請求項27に記載の複合ヒドロゲル組成物。
【請求項30】
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、請求項29に記載の複合ヒドロゲル組成物。
【請求項31】
請求項17に記載の前記複合ヒドロゲル組成物を含む、薬物送達デバイス。
【請求項1】
ヒドロゲルを含む移植物であって、該ヒドロゲルは
求電子基を有するマルチアームポリエーテルを含む、第一反応性前駆体と;
求核基を含む、第二反応性前駆体と;
少なくとも一つのビニル基を含む、少なくとも一つの開始性前駆体と
を含む、移植物。
【請求項2】
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、請求項1に記載の移植物。
【請求項3】
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、請求項1に記載の移植物。
【請求項4】
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、請求項1に記載の移植物。
【請求項5】
生物活性剤をさらに含む、請求項1に記載の移植物。
【請求項6】
前記第一反応性前駆体が前記第二反応性前駆体と反応して第一ヒドロゲルを形成し、前記開始性前駆体が、開始剤との接触時に第二ヒドロゲルを形成する、請求項1に記載の移植物。
【請求項7】
前記開始剤が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される、請求項6に記載の移植物。
【請求項8】
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、請求項7に記載の移植物。
【請求項9】
前記第二ヒドロゲルが、前記第一ヒドロゲルの少なくとも一部の上にバリヤ層を形成する、請求項6に記載の移植物。
【請求項10】
前記第一ヒドロゲルが、組織欠損内に配置され、前記第二ヒドロゲルが、該欠損の上にバリヤ層を提供する、請求項6に記載の移植物。
【請求項11】
前記第一ヒドロゲルが、約5kPa〜約500kPaのモジュラスを有し、前記第二ヒドロゲルが、約50kPa〜約5,000kPaのモジュラスを有する、請求項6に記載の移植物。
【請求項12】
前記第一ヒドロゲルが、約4週〜約10週の期間にわたり分解し、前記第二ヒドロゲルが、約6週〜約6ヵ月の期間にわたり分解する、請求項6に記載の移植物。
【請求項13】
前記移植物が、マトリックス、人工血管、心臓弁、人工臓器、人工骨、移植可能微小凸レンズ、血管グラフト、ステント、縫合糸、ステープル、クリップ、メッシュ、スリング、ネジ、ピン、ケーブル、軟骨移植物、脊椎移植物、およびそれらの組み合わせからなる群より選択される、請求項6に記載の移植物。
【請求項14】
前記移植物が、軟骨移植物を含み、前記第一ヒドロゲルが、軟骨の欠損内にあり、前記第二ヒドロゲルが、該欠損の上にバリヤ層を形成する、請求項13に記載の移植物。
【請求項15】
前記移植物が、前記第二ヒドロゲルにより囲まれた前記第一ヒドロゲルを含む、椎間板移植物を含む、請求項13に記載の移植物。
【請求項16】
前記移植物が、人工皮膚を含む、請求項13に記載の移植物。
【請求項17】
求電子基を有するマルチアームポリエーテルを含む第一反応性前駆体を、求核基を含む第二反応性前駆体と組み合わせて含む、第一ヒドロゲルと;
少なくとも一つのビニル基を含む少なくとも一つの開始性前駆体を含む、第二ヒドロゲルと
を含む、複合ヒドロゲル組成物であり、
該第二ヒドロゲルが、該第一ヒドロゲルの表面の少なくとも一部の上にバリヤ層を形成する、複合ヒドロゲル組成物。
【請求項18】
前記第一反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、およびそれらの組み合わせからなる群より選択されるコアを含み、前記第二反応性前駆体が、ポリエチレングリコール、ポリエチレンオキシド、ポリエチレンオキシド−コ−ポリプロピレンオキシド、コ−ポリエチレンオキシドブロックコポリマー、コ−ポリエチレンオキシドランダムコポリマー、ポリビニルアルコール、ポリ(ビニルピロリジノン)、ポリ(アミノ酸類)、デキストラン、キトサン、アルギネート、カルボキシメチルセルロース、酸化セルロース、ヒドロキシエチルセルロース、ヒドロキシメチルセルロース、ヒアルロン酸、アルブミン、コラーゲン、カゼイン、ゼラチン、およびそれらの組み合わせからなる群より選択される成分を含むコアを含む、請求項17に記載の複合ヒドロゲル組成物。
【請求項19】
前記第一反応性前駆体が、N−ヒドロキシスクシンイミド基を有し、前記第二反応性前駆体が、アミン基を有する、請求項17に記載の複合ヒドロゲル組成物。
【請求項20】
前記開始性前駆体が、アクリル酸、メタクリル酸、ホスホリルコリン含有モノマー、フラノン官能性ビニルモノマー、カリウムスルホプロピルアクリレート、カリウムスルホプロピルメタクリレート、n−ビニルピロリドン、ヒドロキシエチルメタクリレート、高屈折率を有するビニルモノマー、シロキサン官能性ビニル化合物、ビニル基を有するポリエチレングリコール−シリコーンコモノマー、トリスアクリレート、ピロール、液晶ビニルモノマー、液晶ビニルポリマー、およびそれらの組み合わせからなる群より選択される、請求項17に記載の複合ヒドロゲル組成物。
【請求項21】
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第二ヒドロゲルをさらに架橋する、請求項17に記載の複合ヒドロゲル組成物。
【請求項22】
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、請求項21に記載の複合ヒドロゲル組成物。
【請求項23】
生物活性剤をさらに含む、請求項17に記載の複合ヒドロゲル組成物。
【請求項24】
前記生物活性剤が、前記第一ヒドロゲル中にある、請求項23に記載の複合ヒドロゲル組成物。
【請求項25】
前記生物活性剤が、約3日〜約6週の期間にわたり前記第一ヒドロゲルから放出される、請求項23に記載の複合ヒドロゲル組成物。
【請求項26】
前記第二ヒドロゲルが、前記複合ヒドロゲル組成物の約5重量%〜約30重量%を構成する、請求項17に記載の複合ヒドロゲル組成物。
【請求項27】
前記第一ヒドロゲル中に少なくとも一つの分散領域を形成する少なくとも一つの開始性前駆体を含む第三ヒドロゲルをさらに含む、請求項17に記載の複合ヒドロゲル組成物。
【請求項28】
前記第二ヒドロゲルおよび前記第三ヒドロゲルが、同じである、請求項27に記載の複合ヒドロゲル組成物。
【請求項29】
前記開始性前駆体が、レドックス開始剤、フリーラジカル開始剤、放射、およびそれらの組み合わせからなる群より選択される開始剤と反応して、前記第三ヒドロゲルをさらに架橋する、請求項27に記載の複合ヒドロゲル組成物。
【請求項30】
前記放射が、熱、可視光、紫外光、ガンマ線、および電子ビームからなる群より選択される、請求項29に記載の複合ヒドロゲル組成物。
【請求項31】
請求項17に記載の前記複合ヒドロゲル組成物を含む、薬物送達デバイス。
【図1A】


【図1B】


【図1C】


【図2A】


【図2B】


【図2C】


【図3A】


【図3B】


【図3C】


【図3D】


【図4】


【図5A】


【図5B】


【図6A】


【図6B】


【図6C】


【図7A】


【図7B】


【図7C】


【図8】


【図9】


【図10】


【図11】


【図12A】


【図12B】




【図1B】


【図1C】


【図2A】


【図2B】


【図2C】


【図3A】


【図3B】


【図3C】


【図3D】


【図4】


【図5A】


【図5B】


【図6A】


【図6B】


【図6C】


【図7A】


【図7B】


【図7C】


【図8】


【図9】


【図10】


【図11】


【図12A】


【図12B】


【公開番号】特開2011−245311(P2011−245311A)
【公開日】平成23年12月8日(2011.12.8)
【国際特許分類】
【外国語出願】
【出願番号】特願2011−119717(P2011−119717)
【出願日】平成23年5月27日(2011.5.27)
【出願人】(507156015)コンフルエント サージカル, インコーポレイテッド (21)
【出願人】(507362281)タイコ ヘルスケア グループ リミテッド パートナーシップ (666)
【Fターム(参考)】
【公開日】平成23年12月8日(2011.12.8)
【国際特許分類】
【出願番号】特願2011−119717(P2011−119717)
【出願日】平成23年5月27日(2011.5.27)
【出願人】(507156015)コンフルエント サージカル, インコーポレイテッド (21)
【出願人】(507362281)タイコ ヘルスケア グループ リミテッド パートナーシップ (666)
【Fターム(参考)】
[ Back to top ]

