樹脂組成物、硬化膜及び光学用部材
【課題】屈折率が高く、透明性に優れ、さらに耐熱性にも優れた特定の構造を有するイミド化重合体を主成分とする硬化膜を与える樹脂組成物を提供する。
【解決手段】(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上、及び(E)有機溶剤を含有するを含む樹脂組成物。

[式(3)中、Rは4価の有機基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100,000の数を示す。]
【解決手段】(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上、及び(E)有機溶剤を含有するを含む樹脂組成物。

[式(3)中、Rは4価の有機基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100,000の数を示す。]
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、樹脂組成物に関する。さらに詳しくは、高屈折率かつ耐熱性に優れた硬化膜を与えるポリアミック酸を含有する樹脂組成物、それから得られる光学用部材に関する。
【背景技術】
【0002】
ポリイミドは複素環や芳香環等の環状構造からなる高次構造を多数有し、高温になっても分子鎖が動き難いこと、二重結合等の高次結合を多数有し、原子間結合エネルギーが大きいこと、複素環や芳香環がポリマー分子内、ポリマー分子間で相互に作用し合いCT(Charge Transfer)錯体を形成し、凝集力が大きい等の理由から、ポリイミドの耐熱性は各種プラスチックの中でも最高位にランクされる。
【0003】
さらに、ポリイミドは耐熱性に優れるだけではなく、高強度・高弾性で機械特性にも優れ、高絶縁・低誘電で電気特性にも優れ、さらには耐薬品性、耐放射線性、難燃性にも優れている。
【0004】
近年では、感光性を有するポリイミドも開発され、超高集積半導体に、強靭で接着力の強いポリイミドは宇宙往還機に、透明性の高いポリイミドは光通信機器に、射出成型性の良いポリイミドは自動車部品を始めとする耐熱摺動部品に使用されている。
【0005】
上記のような特性を有するポリイミドを光学的用途に用いた例として、硫黄原子を含有する二酸無水物と硫黄原子を含有しないジアミンを使用したポリイミドを光導波路として利用した例(特許文献1);硫黄原子を含有しない二酸無水物と硫黄原子を含有するジアミンを使用したポリイミドを液晶配向膜として利用した例(特許文献2);特定の構造を有するポリイミドと酸化チタン粒子の混合物を高屈折率材料として利用した例(特許文献3);及び硫黄原子を含有しないポリアミック酸と酸化チタン粒子及び他の特定の化合物との混合物をポジ型感光性樹脂組成物として利用した例(特許文献4)等が知られている。
【0006】
【特許文献1】特開2004−131684号公報
【特許文献2】特開平5−263077号公報
【特許文献3】特開2001−354853号公報
【特許文献4】特開2005−208465号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
二酸無水物に硫黄を導入した例(特許文献1)では、屈折率が1.67〜1.72であったが可視光(400〜700nm)での透明性が不十分であった。液晶配向膜として利用した例(特許文献2)は、ポリイミドの導電性に着目したものであり、屈折率については記載がない。特許文献3に記載の発明は、特定の構造を有する二酸無水物と特定の構造を有するジアミンとを反応させて得られたポリアミック酸を用いている。特許文献3記載の発明で用いているジアミンは、ベンゼン環の間が主としてエーテル基(−O−)によって結合されており、1つのチオエーテル基(−S−)を有するものが2種類のみ記載されている。
【0008】
本発明は、屈折率が高く、透明性に優れ、さらに耐熱性にも優れた特定の構造を有するイミド化重合体を主成分とする硬化膜を与える樹脂組成物を提供することを目的とする。
【課題を解決するための手段】
【0009】
上記目的を達成するため、本発明者らは鋭意研究を行い、チアンスレン骨格を有するジアミンと、脂肪族又は脂環族テトラカルボン酸二無水物とを組み合わせることにより、高屈折率と高透明性、そして耐熱性に優れたイミド化重合体を与えるポリアミック酸が得られることを見出し、本発明を完成させた。
【0010】
即ち、本発明は、下記の樹脂組成物、それを硬化させてなる硬化膜及びそれからなる光学用部材を提供する。
1.(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上、及び(E)有機溶剤を含有するを含む樹脂組成物。
【化3】

[式(3)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
2.前記Rが、4価の脂肪族基、4価の脂環族基及び4価の芳香族基からなる群から選択される上記1に記載の樹脂組成物。
3.前記Rが、硫黄原子を含む4価の有機基からなる群から選択される上記1又は2に記載の樹脂組成物。
4.さらに、酸化チタン又は酸化ジルコニウムを主成分とする、一次粒子径が1〜100nmの範囲内の粒子を含有する上記1〜3のいずれかに記載の樹脂組成物。
5.前記成分(B)の粒子が、酸化珪素被覆された酸化チタンからなる上記4に記載の樹脂組成物。
6.さらに、(C)界面活性剤を含有する上記1〜5のいずれかに記載の樹脂組成物。
7.さらに、(D)イミド化触媒を含有する上記1〜6のいずれかに記載の樹脂組成物。
8.前記(D)イミド化触媒が、光酸発生剤又は光塩基発生剤である上記7に記載の樹脂組成物。
9.さらに、前記一般式(3)で示される構造を有するポリアミック酸以外のポリアミック酸を含有する上記1〜8のいずれかに記載の樹脂組成物。
10.上記1〜10のいずれかに記載の樹脂組成物を硬化させてなる硬化膜。
11.屈折率が1.60以上である上記10に記載の硬化膜。
12.下記一般式(4)で示される構造を有するイミド化重合体を含む硬化膜。
【化4】

[式(4)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
13.上記10〜12のいずれかに記載の硬化膜からなる光学用部材。
14.固体画像素子の集光材料である上記13に記載の光学用部材。
15.ディスク集光材料である上記13に記載の光学用部材。
【発明の効果】
【0011】
本発明によれば、チアンスレン骨格を有するジアミンを使用することにより、高屈折率(波長633nmにおける屈折率が、最高で1.79)と高耐熱性が達成される。
本発明によれば、高屈折率と高透明性、さらに高耐熱性が要求される光学用部材に適した樹脂組成物を提供することができる。
さらに、本発明の樹脂組成物は、高屈折率ナノ粒子を添加することにより、更なる高屈折率化が可能である。
本発明によれば、屈折率が高く、透明性及び耐熱性に優れた光学用部材を提供することができる。
【発明を実施するための最良の形態】
【0012】
I.樹脂組成物
本発明の樹脂組成物(以下、本発明の組成物という)は、下記成分(A)〜(F)を含み得る。これらの成分のうち、成分(A)及び(E)は必須成分であり、それ以外は必要に応じて添加し得る任意成分である。
(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上
【化5】

(B)周期律表第4族元素の酸化物を主成分とする、一次粒子径が1〜100nmの範囲内の粒子
(C)界面活性剤
(D)イミド化触媒
(E)有機溶剤
(F)添加剤
以下、各成分について説明する。
【0013】
(A)一般式(3)で示される構造を有するポリアミック酸
本発明の組成物の必須成分であるポリアミック酸は、下記一般式(3)で示される構造を有し、それ自体の屈折率(25℃、波長633nm)が非常に高く、高屈折率で、透明性及び耐熱性に優れた硬化膜を形成することができる。
【化6】

【0014】
上記一般式(2)及び(3)中のRは、テトラカルボン酸二無水物から無水物基を除去した残基に相当する4価の有機基を示し、4価の脂肪族基、4価の脂環族基又は4価の芳香族基であることが好ましい。
上記一般式(3)中のR1はそれぞれ独立して炭素数1〜3のアルキル基を示し、a及びbは基R1の置換数を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示す。a及びbは0であることが好ましい。
上記一般式(3)中のmは、1〜100000の数を示し、10〜100000であることが好ましい。
【0015】
(a)上記一般式(3)で示される構造を有するポリアミック酸は、下記一般式(1)で示される新規化合物であるジアミン化合物と、下記一般式(2)で示されるテトラカルボン酸二無水物とを重縮合させることによって得られる。
【化7】

【0016】
【化8】

式(1)及び(2)中の置換基R、R1、a及びbは、上記式(3)において説明した通りである。
【0017】
(b)一般式(1)で示されるジアミンの製造
一般式(1)で示されるジアミン化合物は、次のようにして製造することができる。
工程1:チアンスレン骨格の製造
チアンスレン環の製造方法は公知であり、公知の方法に従って製造することができる。例えば、下記反応式のように、モノハロゲン置換チオフェノール誘導体を、硫酸(発煙硫酸又は濃硫酸)の存在下に縮合させて、ジハロゲン置換チアンスレン誘導体を得る。
【化9】

【0018】
工程2:ジアミン化合物の製造
非プロトン性極性溶剤中、無水炭酸カリウムとモノアミノ置換チオフェノール誘導体とを反応させ、アミノ置換チオフェノール誘導体のカリウム塩を合成する。そこに、上記工程1で製造したジハロゲン置換チアンスレン誘導体を添加することにより、一般式(1)で示されるジアミン化合物を製造することができる。
【化10】

【0019】
一般式(1)で示されるジアミンの例としては、例えば、2,7−ビス(4−アミノフェニレンスルファニル)チアンスレン、2,7−ビス(2−アミノフェニレンスルファニル)チアンスレン、2,7−ビス(3−アミノフェニレンスルファニル)チアンスレン、3,6−ビス(4−アミノフェニレンスルファニル)チアンスレン等が挙げられ、2,7−ビス(4−アミノフェニレンスルファニル)チアンスレンが好ましい。
【0020】
(c)一般式(2)で示されるテトラカルボン酸二無水物
上記一般式(2)で示されるテトラカルボン酸二無水物としては、脂肪族、脂環族又は芳香族テトラカルボン酸二無水物が挙げられ、光学的用途において必要とされる優れた透明性を有する硬化膜が得られることから脂肪族又は脂環族テトラカルボン酸二無水物が好ましい。
【0021】
脂肪族又は脂環族テトラカルボン酸二無水物の具体例としては、例えば、ブタンテトラカルボン酸二無水物、1,2,3,4−シクロブタンテトラカルボン酸二無水物、1,2,3,4−シクロペンタンテトラカルボン酸二無水物、4,10−ジオキサトリシクロ[6.3.1.02,7]ドデカン−3,5,9,11−テトラオン、1,2,4,5−シクロヘキサンテトラカルボン酸二無水物、2,3,5−トリカルボキシシクロペンチル酢酸二水和物、3,5,6−トリカルボキシノルボルナン−2−酢酸二無水物、2,3,4,5−テトラヒドロフランテトラカルボン酸二無水物、1,3,3a,4,5,9b−ヘキサヒドロ−5−テトラヒドロ−2,5−ジオキソ−3−フラニル)−ナフト[1,2−c]−フラン−1,3−ジオン、5−(2,5−ジオキソテトラヒドロフラル)−3−メチル−3−シクロヘキセン−1,2−ジカルボン酸二無水物、ビシクロ[2,2,2]−オクト−7−エン−2,3,5,6−テトラカルボン酸二無水物等の脂肪族及び脂環族テトラカルボン酸二無水物を挙げることができる。これらのうちではブタンテトラカルボン酸二無水物、1,2,3,4−シクロブタンテトラカルボン酸二無水物、4,10−ジオキサトリシクロ[6.3.1.02,7]ドデカン−3,5,9,11−テトラオン、2,3,5−トリカルボキシシクロペンチル酢酸二無水物、5−(2,5−ジオキソテトラヒドロフラル)−3−メチル−3−シクロヘキセン−1,2−ジカルボン酸二無水物及び1,3,3a,4,5,9b−ヘキサヒドロ−5−テトラヒドロ−2,5−ジオキソ−3−フラニル)−ナフト[1,2−c]−フラン−1,3−ジオンが好ましく、1,2,3,4−シクロブタンテトラカルボン酸二無水物、4,10−ジオキサトリシクロ[6.3.1.02,7]ドデカン−3,5,9,11−テトラオン、1,2,4,5−シクロヘキサンテトラカルボン酸二無水物が特に好ましい。
【0022】
芳香族テトラカルボン酸二無水物の具体例としては、ピロメリット酸二無水物、3,3’,4,4’−ベンゾフェノンテトラカルボン酸二無水物、3,3’,4,4’−ビフェニルスルホンテトラカルボン酸二無水物、1,4,5,8−ナフタレンテトラカルボン酸二無水物、2,3,6,7−ナフタレンテトラカルボン酸二無水物、3,3’,4,4’−ビフェニルエーテルテトラカルボン酸二無水物、3,3’,4,4’−ジメチルジフェニルシランテトラカルボン酸二無水物、3,3’,4,4’−テトラフェニルシランテトラカルボン酸二無水物、1,2,3,4−フランテトラカルボン酸二無水物、4,4’−ビス(3,4−ジカルボキシフェノキシ)ジフェニルスルフィド二無水物、4,4’−ビス(3,4−ジカルボキシフェノキシ)ジフェニルスルホン二無水物、4,4’−ビス(3,4−ジカルボキシフェノキシ)ジフェニルプロパン二無水物、4,4’−(ヘキサフルオロイソプロピリデン)ビス(フタル酸)二無水物、3,3’,4,4’−ビフェニルテトラカルボン酸二無水物、ビス(フタル酸)フェニルホスフィンオキサイド二無水物、p−フェニレン−ビス(トリフェニルフタル酸)二無水物、m−フェニレン−ビス(トリフェニルフタル酸)二無水物、ビス(トリフェニルフタル酸)−4,4’−ジフェニルエーテル二無水物、ビス(トリフェニルフタル酸)−4,4’−ジフェニルメタン二無水物等の芳香族テトラカルボン酸二無水物を挙げることができる。これらのうちでは、ピロメリット酸二無水物、3,3’,4,4’−ベンゾフェノンテトラカルボン酸二無水物、3,3’,4,4’−ビフェニルスルホンテトラカルボン酸二無水物、4,4’−(ヘキサフルオロイソプロピリデン)ビス(フタル酸)二無水物及び3,3’,4,4’−ビフェニルテトラカルボン酸二無水物が好ましい。
【0023】
また、より高屈折率のポリアミック酸が得られることから、硫黄原子を含むテトラカルボン酸二無水物を用いることも好ましい。硫黄原子含有酸無水物の例としては、例えば、4,4’−[p−チオビス(フェニレン−スルファニル)]ジフタル酸無水物等が挙げられる。
【0024】
尚、本発明の組成物には、上記一般式(3)で示される構造を有するポリアミック酸以外のポリアミック酸を含有していてもよい。即ち、上記一般式(1)で示されるジアミン化合物の他に、本発明の効果が損なわれない範囲内で、他のジアミンを併用することもできる。このようなジアミン化合物としては、例えばp−フェニレンジアミン、m−フェニレンジアミン、4,4’−ジアミノジフェニルメタン、4,4’−ジアミノジフェニルエタン、4,4’−ジアミノジフェニルスルフィド、4,4’−ジアミノジフェニルスルホン、4,4’−ジアミノジフェニルエーテル、1,5−ジアミノナフタレン、3,3−ジメチル−4,4’−ジアミノビフェニル、4,4’−ジアミノベンズアニリド、3,4’−ジアミノジフェニルエーテル、3,3’−ジアミノベンゾフェノン、3,4’−ジアミノベンゾフェノン、4,4’−ジアミノベンゾフェノン、2,2−ビス[4−(4−アミノフェノキシ)フェニル]プロパン、2,2−ビス[4−(4−アミノフェノキシ)フェニル]ヘキサフルオロプロパン、2,2−ビス(4−アミノフェニル)ヘキサフルオロプロパン、2,2−ビス[4−(4−アミノフェノキシ)フェニル]スルホン、1,4−ビス(4−アミノフェノキシ)ベンゼン、1,3−ビス(4−アミノフェノキシ)ベンゼン、1,3−ビス(3−アミノフェノキシ)ベンゼン、9,9−ビス(4−アミノフェニル)−10−ヒドロアントラセン、9,9−ビス(4−アミノフェニル)フルオレン、4,4’−メチレン−ビス(2−クロロアニリン)、2,2’,5,5’−テトラクロロ−4,4’−ジアミノビフェニル、2,2’−ジクロロ−4,4’−ジアミノ−5,5’−ジメトキシビフェニル、3,3’−ジメトキシ−4,4’−ジアミノビフェニル、4,4’−(p−フェニレンジイソプロピリデン)ビスアニリン、4,4’−(m−フェニレンジイソプロピリデン)ビスアニリンを挙げることができる。
【0025】
また、ジアミノテトラフェニルチオフェン等のヘテロ原子を有する芳香族ジアミン;1,1−メタキシリレンジアミン、1,3−プロパンジアミン、テトラメチレンジアミン、ペンタメチレンジアミン、ヘキサメチレンジアミン、ヘプタメチレンジアミン、オクタメチレンジアミン、ノナメチレンジアミン、4,4−ジアミノヘプタメチレンジアミン、1,4−ジアミノシクロヘキサン、イソホロンジアミン、テトラヒドロジシクロペンタジエニレンジアミン、ヘキサヒドロ−4,7−メタノインダニレンジメチレンジアミン、トリシクロ[6,2,1,02.7]−ウンデシレンジメチルジアミン等の脂肪族又は脂環族ジアミンも挙げることができる。
【0026】
一般式(3)で示される構造を有するポリアミック酸の製造に用いるジアミン類のうち、一般式(1)で示される本発明のジアミン化合物の割合は、50モル%以上であることが好ましく、80モル%以上であることがより好ましく、高屈折率を達成するためには100モル%であることが特に好ましい。
【0027】
一般式(1)で示されるジアミン化合物(以下、単にジアミン化合物ということがある)と、一般式(2)で示されるテトラカルボン酸二無水物(以下、単に酸二無水物ということがある)との重縮合反応は、公知の方法及び条件下に行うことができるが、例えば、下記の方法で行うことが好ましい。
N−メチル−2−ピロリドン等の非プロトン性有機溶媒中において、ジアミン化合物と酸二無水物とを攪拌混合することによって、一般式(3)で示される構造を有するポリアミック酸を溶液として得ることができる。例えば、ジアミン化合物を有機溶媒に溶解し、これに酸二無水物を加えて、攪拌混合してもよく、また、ジアミン化合物と酸二無水物との混合物を有機溶媒に加えて、攪拌混合してもよい。反応は、通常、100℃以下、好ましくは、80℃以下の温度で、常圧下に行われる。しかし、反応は、必要に応じて、加圧下又は減圧下に行ってもよい。反応時間は、用いるジアミン化合物と酸二無水物や、有機溶媒、反応温度等によって異なるが、通常、4〜24時間の範囲である。
【0028】
本発明の組成物中における成分(A)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常10〜100重量%、好ましくは20〜80重量%、より好ましくは30〜70重量%の範囲内である。成分(A)の配合量が10重量%未満では、十分な屈折率や耐熱性が発現できないおそれがある。
尚、本発明の組成物の必須成分は成分(A)のみであるが、通常は、成分(A)の製造に用いられる有機溶剤を含み、組成物の塗工性等の観点からも有機溶剤を含有することが好ましい。
【0029】
(B)周期律表第4族元素の酸化物を主成分とする、一次粒子径が1〜100nmの範囲内の粒子
成分(B)は周期律表第4属元素の酸化物粒子である。屈折率の高い粒子成分を添加することにより、得られる硬化膜の屈折率をさらに高めることができる。
成分(B)の粒子の一次粒子径は、1〜100nmの範囲内であることが必要であり、1〜50nmの範囲内であることが好ましく、5〜15nmの範囲内であることがより好ましい。粒子の一次粒子径が1nm未満であると、二次凝集が起こり易く硬化膜が白化するおそれがあり、100nmを超えると、薄膜形成時の面均一性が損なわれるおそれがある。ここで、一次粒子径は、光散乱法によって測定することができる。
【0030】
成分(B)の粒子として用いることができる酸化物粒子としては、酸化チタン、酸化ジルコニウム、酸化ハフニウム及びこれらの金属酸化物と酸化ケイ素や酸化スズの複合粒子が挙げられ、得られる硬化膜の屈折率を高める効果の点から、酸化チタン及び酸化ジルコニウムが好ましい。
【0031】
尚、酸化チタンは、光触媒活性が有るため、そのままでは光学用途に用いることは難しいため、粒子表面を酸化ケイ素で被覆することが好ましい。
また、酸化チタンには、結晶型の違いにより、アナターゼ型とルチル型が存在するが、屈折率が高く、耐光性に優れることからルチル型が好ましい。
【0032】
成分(B)として用いる酸化物粒子は、粉体状であってもよいし、溶媒分散ゾルであってもよい。分散媒としては、例えば、メタノール、メチルエチルケトン、メチルイソブチルケトン、シクロヘキサノン、N−メチル−2−ピロリドン、プロピレングレコールモノメチルエーテル等が挙げられる。
【0033】
成分(B)として用いることができる粒子の市販品の例としては、例えば、酸化ケイ素被覆アナターゼ型酸化チタン−メタノール分散ゾル(触媒化成工業社製、オプトレイクシリーズ)、酸化ケイ素被覆−酸化スズ含有ルチル型酸化チタン−メタノール分散ゾル(テイカ社製、TSシリーズ)、酸化ジルコニウム−メチルエチルケトン分散ゾル(大阪セメント社製、HXU−120JC)等が挙げられる。
【0034】
本発明の組成物中における成分(B)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常0〜90重量%、好ましくは20〜80重量%、より好ましくは40〜60重量%の範囲内である。成分(B)の配合量が90重量%を超えると、十分な耐熱性が得られないおそれがある。
尚、成分(B)が溶媒分散ゾルである場合には、成分(B)の配合量には分散媒を含まない。
【0035】
(C)界面活性剤
本発明の組成物をスピンコートによって基材等に塗布する場合には、均一な塗膜が得られることから、界面活性剤を配合することが好ましい。
本発明で用いることができる界面活性剤の種類としては、ポリジメチルシロキサン系界面活性剤、フッ素系界面活性剤等が挙げられ、ポリジメチルシロキサン系界面活性剤が好ましい。
【0036】
ポリジメチルシロキサン系の界面活性剤の例としては、例えば、SH28PA(東レダウコーニング社製、ジメチルポリシロキサンポリオキシアルキレン共重合体)、ペインタッド19、54(東レダウコーニング社製、ジメチルポリシロキサンポリオキシアルキレン共重合体)、FM0411(サイラプレーン、チッソ社製)、SF8428(東レダウコーニング社製、ジメチルポリシロキサンポリオキシアルキレン共重合体(側鎖OH含有))、BYK UV3510(ビックケミー・ジャパン社製、ジメチルポリシロキサン−ポリオキシアルキレン共重合体)、DC57(東レ・ダウコーニング・シリコーン社製、ジメチルポリシロキサン−ポリオキシアルキレン共重合体)、DC190(東レ・ダウコーニング・シリコーン社製、ジメチルポリシロキサン−ポリオキシアルキレン共重合体)、サイラプレーンFM−4411、FM−4421、FM−4425、FM−7711、FM−7721、FM−7725、FM−0411、FM−0421、FM−0425、FM−DA11、FM−DA21、FM−DA26、FM0711、FM0721、FM−0725、TM−0701、TM−0701T(チッソ社製)、UV3500、UV3510、UV3530(ビックケミー・ジャパン社製)、BY16−004、SF8428(東レ・ダウコーニング・シリコーン社製)、VPS−1001(和光純薬製)等が挙げられる。特にサイラプレーンFM−7711、FM−7721、FM−7725、FM−0411、FM−0421、FM−0425、FM0711、FM0721、FM−0725、VPS−1001等を挙げることができる。また、エチレン性不飽和基を有する当該シリコーン化合物の市販品としては、例えば、Tego Rad 2300、2200N、テゴ・ケミー社等を挙げることができる。
【0037】
フッ素系の界面活性剤の例として、例えば、メガファックF−114、F410、F411、F450、F493、F494、F443、F444、F445、F446、F470、F471、F472SF、F474、F475、R30、F477、F478、F479、F480SF、F482、F483、F484、F486、F487、F172D、F178K、F178RM、ESM−1、MCF350SF、BL20、R08、R61、R90(大日本インキ化学工業社製)が挙げられる。
【0038】
本発明の組成物中における成分(C)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常0〜10重量%、好ましくは0.1〜5重量%、より好ましくは0.5〜3重量%の範囲内である。成分(C)の配合量が10重量%を超えると、屈折率が低下するおそれがある。
【0039】
(D)イミド化触媒
本発明の組成物は、加熱によって成分(A)のポリアミック酸がイミド化重合体となることにより硬化するものであるが、この熱硬化反応を促進するためにイミド化触媒を添加することもできる。
【0040】
イミド化触媒としては、例えば、無水酢酸−ピリジン混合溶液等が挙げられる。また、無水酢酸−トリエチルアミン混合溶液や、無水トリフルオロ酢酸、ジシクロヘキシルカルボジイミドも使用できる。
【0041】
また、成分(D)として、光の照射によって酸又は塩基を発生させる化合物である光酸発生剤又は光塩基発生剤を用いることにより、本発明の組成物をパターニング可能な材料とすることができる。これにより、本発明の組成物を固体撮像素子の集光部材等のパターニング工程を必要とする光学用部材の製造に用いることが可能となる。
光塩基発生剤としては、例えば、カルバマート型光塩基発生剤等が挙げられる。具体的には、下記のような構造式で示される化合物が光塩基発生剤の例として挙げられる。
【化11】

【0042】
本発明の組成物中における成分(D)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常0〜20重量%、好ましくは1〜10重量%、より好ましくは1〜5重量%の範囲内である。成分(D)の配合量が20重量%を超えると、貯蔵安定性が低下するおそれがある。
【0043】
(E)有機溶剤
本発明の組成物は、通常、成分(A)のポリアミック酸製造の際に用いる溶剤を含有する。また、成分(B)の酸化物粒子として粒子の溶媒分散ゾルを用いる場合には、その分散媒も本発明の組成物中に含有される。その他、組成物の粘度を調整し、均一な塗膜を形成するための組成物の塗布性を改善するために、別途、有機溶剤を添加することができる。
【0044】
本発明で用いる有機溶剤としては、特に制限されないが、非プロトン系有機溶剤が好ましい。非プロトン系有機溶剤としては、例えば、N−メチル−2−ピロリドン(NMP)、ジメチルホルムアミド(DMF)、シクロヘキサノン、N,N−ジメチルアセトアミド(DMAc)等が好ましい。これら以外にもN,N−ジメチルホルムアミド、N、N−ジエチルアセトアミド、N,N−ジメトキシアセトアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルカプロラクタム、1,2−ジメトキシエタン、1,2−ジメトキシエタン、ビス(2−メトキシエチル)エーテル、1,2−ビス(2−メトキシエトキシ)エタン、ビス〔2−(2−メトキシエトキシ)エチル〕エーテル、テトラヒドロフラン、1,3−ジオキサン、1,4−ジオキサン、ピロリン、ピコリン、ジメチルスルホキシド、ジメチルスルホン、テトラメチル尿素、ヘキサメチルホスホルアミド、フェノール、o−クレゾール、m−クレゾール、p−クレゾール、m−クレゾール酸、p−クロロフェノール、アニソール、ベンゼン、トルエン、キシレン等を挙げることができる。これらの有機溶剤は単独で、又は2種類以上の混合物として用いられる。
【0045】
本発明の組成物中における成分(E)有機溶剤の配合量は、有機溶剤を除く固形分全量100重量部に対して、通常100〜9900重量部、好ましくは300〜1900重量部、より好ましくは400〜1900重量部の範囲内である。有機溶剤の配合量が100重量部未満では、スピンコート塗布ができなくなるおそれがあり、9900重量部を超えると、必要膜厚が発現できないおそれがある。
尚、成分(E)の配合量には、成分(A)のポリアミック酸溶液に由来する溶剤及び成分(B)の酸化物粒子分散ゾルの分散媒として持ち込まれる溶剤を含む。
【0046】
(F)添加剤
本発明の組成物には、本発明の効果を損なわない範囲内で、各種の添加剤を配合することができる。このような添加剤としては、例えば、上記成分以外の硬化性化合物、酸化防止剤等が挙げられる。
【0047】
硬化性化合物には、熱硬化性化合物及び光硬化性化合物を含む。これらの化合物を配合することにより、得られる硬化膜の硬度を高めることができる。
熱硬化性化合物としては、例えば、メラミン化合物、アルコキシシラン等が挙げられる。
光硬化性化合物としては、例えば、(メタ)アクリロイル基を有する化合物、ビニル基を有する化合物等が挙げられる。
【0048】
II.硬化膜
本発明の硬化膜は、下記一般式(4)で示される構造を有するイミド化重合体を含むことを特徴とする。一般式(4)で示される構造を有するイミド化重合体は、前記一般式(3)で示される構造を有するポリアミック酸をイミド化することによって得られる。
【化12】

式(4)中、R、R1、a、b及びmは、上記一般式(3)と同様であるためここでは説明を省略する。
【0049】
本発明の硬化膜は、上記本発明の組成物を基材等に塗布後、窒素雰囲気下で80〜300℃の温度で、1〜5時間加熱することによって、組成物中の(A)ポリアミック酸がイミド化されて、上記一般式(4)で示される構造を有するイミド化重合体となり硬化する。
【0050】
本発明の硬化膜は、成分(B)の酸化物粒子を含有しない場合であっても、波長633nmにおける屈折率が、通常1.60以上であり、好ましくは1.68以上、より好ましくは1.70以上である。
本発明の硬化膜の膜厚は、用途によって適宜選択すべきであるが、通常0.1〜5μm、好ましくは0.1〜2μm、透明性の観点からより好ましくは0.1〜1μmの範囲内である。0.1μm未満では製膜が困難となるおそれがあり、5μmを超えると、硫黄原子に起因する着色が見られ、透明性が低下するおそれがある。
【0051】
本発明の硬化膜は、高い屈折率、優れた透明性及び優れた耐熱性を必要とする光学用部材として好適である。本発明の硬化膜からなる光学用部材としては、例えば、固体撮像素子の集光材料、記録用ディスクの集光材料等が挙げられる。
本発明の組成物にイミド化触媒として光酸発生剤又は光塩基発生剤を配合することにより、パターニングが可能となり、例えば、マイクロレンズを製造することも可能である。パターニングによるマイクロレンズの製造方法は従来公知の方法で行うことができる。
【実施例】
【0052】
以下、本発明を実施例によってさらに具体的に説明するが、本発明は、これらの実施例によって何ら限定されるものではない。
【0053】
製造例1
2,7−ジフルオロチアンスレン
【化13】

攪拌機、還流冷却器及び窒素導入管を備えた反応容器に、p−フルオロチオフェノール(9.613g、75mmol)に発煙硫酸10〜50mLを加え、40〜80℃で12〜24時間反応させた。反応液を冷水に注ぎ、析出物を濾取し水洗した。得られた黄色の個体はエタノールを用いて再結晶し精製した。
融点:156.2℃(DSC)
FT−IR(KBr、cm−1):1592.9、1454.1、1253.5、1207.2、894.8、856.2、802.2
1H−NMR(300MHz、DMSO−d6、ppm):6.96−7.03(m、2H)、7.22−7.25(m、2H)、7.41−7.45(m、2H)
【0054】
製造例2
2,7−ビス(4−アミノフェニレンスルファニル)チアンスレンの合成
【化14】

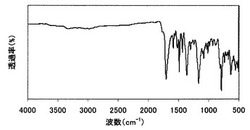
攪拌機、還流冷却器、Dean−Starkトラップ及び窒素導入管を備えた反応容器に、p−アミノチオフェノール(9.389g、75mmol)と無水炭酸カリウム(5.39g、39mmol)、そしてN−メチル−2−ピロリドン(30mL、以下、NMP)とトルエン(50mL)を加え、140〜145℃で4時間反応させた。Dean−Starkトラップで水を除去し、トルエンも減圧留去した。反応液を120℃まで冷却し、製造例1で製造した2,7−ジフルオロチアンスレン(7.569g、30mmol)とNMP(15mL)を加えた。その後、反応液を170℃で12時間反応させた。反応液を室温まで戻し、反応液を冷水(500mL)に注ぎ、黄色の析出物を濾取し水洗した。得られた黄色の個体はエタノールを用いて再結晶し精製した。得られた化合物のIRチャート、1H−NMR及び13C−NMRチャートをそれぞれ図1〜図3に示す。
【0055】
収量:10.34g
収率:74.5%
融点:185.2℃(DSC)
FT−IR(KBr、cm−1):3428.8、3332.4、2360.4、1619.9、1592.9、1565.9、1492.6、1442.5、1361.5、1292.1、1176.4、1103.1、817.7
1H−NMR(300MHz、DMSO−d6、ppm):5.49(s、4H)、6.61−6.64(d、4H)、6.94−6.98(d、4H)、7.06(s、2H)、7.14−7.17(d、4H)、7.36−7.38(d、2H)
13C−NMR(300MHz、DMSO−d6、ppm):151.2、142.2、137.5、136.7、131.0、129.9、126.2、125.9、115.8、114.3
元素分析:計算値 C24H18N2S4:C、62.31%;H、3.92%;N、6.05%
測定値 C、62.22%;H、3.96%;N、6.01%
【0056】
製造例3
4,4’−[p−チオビス(フェニレン−スルファニル)]ジフタル酸無水物
【化15】

攪拌機、還流冷却器及び窒素導入管を備えた反応容器に、4,4’−チオビスベンゼンチオール(5.00g、0.02mol)と4−ブロモフタル酸無水物(10.00g、0.044mol)、無水炭酸カリウム(6.08g、0.044mol)、そしてN,N−ジメチルホルムアミド(DMF)(100mL)を加え、120℃で12時間反応させた。反応液を室温に戻し、白色の固体を濾取し、160℃で24時間減圧乾燥した。得られた白色の固体に蒸留水(100mL)と濃塩酸(100mL)を加え、3時間の間、加熱攪拌した。得られた白色の固体を濾取し、180〜190℃で3時間加熱し黄色の固体を得た。
【0057】
収量:7.8g
収率:71.9%
融点:175.2℃(DSC)
FT−IR(KBr、cm−1):1847.5、1778.0、1604.4、1473.3、1326.8、1257.4、902.5、817.7、732.0
1H−NMR(300MHz、DMSO−d6、ppm):7.45−7.49(d、4H)、7.52−7.55(d、4H)、7.56(s、2H)、7.60−7.63(d、2H)、7.83−7.85(d、2H)
元素分析:計算値 C28H14O6S3:C、61.98%;H、2.60%
測定値 C、62.23%;H、2.97%
【0058】
<粒子成分を含まない組成物の製造例>
実施例1
窒素導入管を備えた反応容器に、2,7−ビス(4−アミノフェニレンスルファニル)チアンスレン(18.51g、40mmol)(以下、APTTという)にN−メチル−2−ピロリドン(80g)(以下、NMPという)を加え、室温で攪拌し完全に溶解させた。次に、1,2,3,4−シクロブタンテトラカルボン酸二無水物(7.84g、40mmol)(以下、CBDAという)とNMP(25g)を添加し、室温で24時間攪拌して、ポリアミック酸のNMP溶液Aを得た。得られたポリアミック酸のIRチャートを図4に示す。
【0059】
実施例2〜6
実施例1で用いたCBDAの代わりに、下記表1に示す酸無水物を用いた他は、実施例1と同様の方法で重合を行い、各ポリアミック酸のNMP溶液を得た。
【0060】
比較例1
窒素導入管を備えた反応容器に、ビス(p−アミノフェニル)エーテル(8.01g、40mmol)(以下、ODAという)にN−メチル−2−ピロリドン(80g)(NMP)を加え、室温で攪拌し完全に溶解させた。次に、CBDA(7.84g、40mmol)とNMP(25g)を添加し、室温で24時間攪拌して、ポリアミック酸のNMP溶液を得た。
【0061】
<硬化膜の作成>
3インチ径3mm厚の溶融石英基板上に実施例1〜6及び比較例1で製造したポリアミック酸のNMP溶液をディスペンスし、厚さが約8〜12μmになるようにスピンコート塗布し、窒素雰囲気下280℃で1.5時間加熱し、硬化膜を得た。
実施例1で得られた硬化膜中のイミド化重合体のIRチャートを図5、実施例3〜6で得られた硬化膜中の各イミド化重合体のIRチャートを図6に示す。
【0062】
<硬化膜の特性評価>
上記で得られた硬化膜について下記特性を評価した。結果を表1に示す。
【0063】
(1)屈折率
Metricon社のPC−2000型プリズムカプラーを使用して、上記で得られた硬化膜の、波長633nmにおける屈折率を測定した。
【0064】
(2)透過率
日立製作所社製のU−3500型自記分光光度計を使用して、上記で得られた硬化膜の膜厚1μm当たりの波長400nm及び450nmにおける透過率(%)を測定した。
【0065】
(3)耐熱性
セイコーインスツル社製のDSC6300(昇温速度10℃/分、窒素気流下)を使用して、上記で得られた硬化膜の5%重量減少温度を測定した。5%重量減少温度が400℃以上の場合を耐熱性合格(○)と評価した。
【0066】
【表1】

【0067】
表1中の略号は下記のものを表す。
APTT:2,7−ビス(4−アミノフェニレンスルファニル)チアンスレン;実施例1で製造
ODA:ビス(p−アミノフェニル)エーテル
CBDA:1,2,3,4−シクロブタンテトラカルボン酸二無水物
CHDA:1,2,4,5−シクロヘキサンテトラカルボン酸二無水物
sBPDA:3,3’,4,4’−ビフェニルテトラカルボン酸二無水物
aBPDA:2,3’,3,4’−ビフェニルテトラカルボン酸二無水物
ODPA:4,4’−オキシジフタル酸二無水物
3SDEA:4,4’−[p−チオビス(フェニレン−スルファニル)]ジフタル酸無水物;製造例1で製造
【0068】
表1の結果から、一般式(3)で示される構造を有するポリアミック酸は、屈折率が高く、透明性に優れ、さらに耐熱性にも優れた一般式(4)で示される構造を有するイミド化重合体与えることがわかる。
【0069】
<粒子成分を含む組成物の製造例>
実施例7
窒素導入管を備えた反応容器に、実施例1で製造したポリアミック酸のNMP溶液(ポリアミック酸含有量20重量%)28.88gに、シクロヘキサノン、乳酸エチル、2−ブトキシエタノールの混合溶剤(重量比:3/0.5/0.5)59.53gとジメチルポリシロキサンポリオキシアルキレン共重合体(東レダウコーニング社製SH28PA)0.11gを加え溶解させた。次に酸化ケイ素被覆−酸化スズ含有ルチル型酸化チタンのメタノールゾル(テイカ社製TSシリーズ、粒子含量20重量%)23.62gを滴下した。その後、室温で1時間攪拌し高屈折率樹脂組成物を得た。
【0070】
実施例8〜11及び比較例2
表2に示す組成とした以外は、実施例7と同様の方法で調製を行い、各高屈折率樹脂組成物を得た。
【0071】
<硬化膜の作製>
4インチ径のシリコンウエハ基板上に実施例24〜31及び比較例2で調整した高屈折率樹脂組成物をディスペンスし、厚さ約0.3μmになるようにスピンコート塗布し、窒素雰囲気下280℃×1.5時間で製膜した。
【0072】
<硬化膜の特性評価>
上記のようにして作製した硬化膜について、下記特性を測定、評価した。結果を表2に示す。
【0073】
(1)屈折率
N&K Technology社のN&K Analyzerを使用して、波長633nmにおける屈折率を測定した。
【0074】
(2)透過率
JASCO社製のV−570型分光光度計を使用して、波長400nmにおける透過率を測定した。
【0075】
【表2】

【0076】
表2中の略号等は下記のものを示す。
酸化ケイ素被覆−酸化スズ含有ルチル型酸化チタン:テイカ社製の粒子メタノールゾル、TSシリーズ、一次粒子径5〜15nm、粒子含量20重量%
酸化ジルコニウム:住友大阪セメント社製の粒子メチルエチルケトンゾル、HXU−120JC、一次粒子径5〜15nm、粒子含量40重量%
酸化ケイ素被覆アナターゼ型酸化チタン:触媒化成工業社製の粒子メタノールゾル、オプトレイク、一次粒子径5〜20nm、粒子含量25重量%
SH28PA:東レダウコーニング社製界面活性剤、ジメチルポリシロキサンポリオキシアルキレン共重合体
【0077】
表2の結果から、(B)粒子成分を配合することにより、さらに屈折率が1.756〜1.864と非常に高く、光学用部材に必要な高い透過率も有する硬化膜が得られることがわかる。
【図面の簡単な説明】
【0078】
【図1】製造例2で得られたジアミン化合物のIRチャートである。
【図2】製造例2で得られたジアミン化合物の1H−NMRチャートである。
【図3】製造例2で得られたジアミン化合物の13C−NMRチャートである。
【図4】実施例1で得られたポリアミック酸のIRチャートである。
【図5】実施例1で得られたポリアミック酸をイミド化したイミド化重合体のIRチャートである。
【図6】実施例2で得られたポリアミック酸のIRチャートである。
【図7】実施例2で得られたイミド化重合体のIRデータである。
【図8】実施例3で得られたポリアミック酸のIRチャートである。
【図9】実施例4で得られたポリアミック酸のIRチャートである。
【図10】実施例5で得られたポリアミック酸のIRチャートである。
【図11】実施例6で得られたポリアミック酸のIRチャートである。
【図12】実施例3〜6で得られた各ポリアミック酸をイミド化したイミド化重合体(PI−3〜6)のIRチャートである。
【技術分野】
【0001】
本発明は、樹脂組成物に関する。さらに詳しくは、高屈折率かつ耐熱性に優れた硬化膜を与えるポリアミック酸を含有する樹脂組成物、それから得られる光学用部材に関する。
【背景技術】
【0002】
ポリイミドは複素環や芳香環等の環状構造からなる高次構造を多数有し、高温になっても分子鎖が動き難いこと、二重結合等の高次結合を多数有し、原子間結合エネルギーが大きいこと、複素環や芳香環がポリマー分子内、ポリマー分子間で相互に作用し合いCT(Charge Transfer)錯体を形成し、凝集力が大きい等の理由から、ポリイミドの耐熱性は各種プラスチックの中でも最高位にランクされる。
【0003】
さらに、ポリイミドは耐熱性に優れるだけではなく、高強度・高弾性で機械特性にも優れ、高絶縁・低誘電で電気特性にも優れ、さらには耐薬品性、耐放射線性、難燃性にも優れている。
【0004】
近年では、感光性を有するポリイミドも開発され、超高集積半導体に、強靭で接着力の強いポリイミドは宇宙往還機に、透明性の高いポリイミドは光通信機器に、射出成型性の良いポリイミドは自動車部品を始めとする耐熱摺動部品に使用されている。
【0005】
上記のような特性を有するポリイミドを光学的用途に用いた例として、硫黄原子を含有する二酸無水物と硫黄原子を含有しないジアミンを使用したポリイミドを光導波路として利用した例(特許文献1);硫黄原子を含有しない二酸無水物と硫黄原子を含有するジアミンを使用したポリイミドを液晶配向膜として利用した例(特許文献2);特定の構造を有するポリイミドと酸化チタン粒子の混合物を高屈折率材料として利用した例(特許文献3);及び硫黄原子を含有しないポリアミック酸と酸化チタン粒子及び他の特定の化合物との混合物をポジ型感光性樹脂組成物として利用した例(特許文献4)等が知られている。
【0006】
【特許文献1】特開2004−131684号公報
【特許文献2】特開平5−263077号公報
【特許文献3】特開2001−354853号公報
【特許文献4】特開2005−208465号公報
【発明の開示】
【発明が解決しようとする課題】
【0007】
二酸無水物に硫黄を導入した例(特許文献1)では、屈折率が1.67〜1.72であったが可視光(400〜700nm)での透明性が不十分であった。液晶配向膜として利用した例(特許文献2)は、ポリイミドの導電性に着目したものであり、屈折率については記載がない。特許文献3に記載の発明は、特定の構造を有する二酸無水物と特定の構造を有するジアミンとを反応させて得られたポリアミック酸を用いている。特許文献3記載の発明で用いているジアミンは、ベンゼン環の間が主としてエーテル基(−O−)によって結合されており、1つのチオエーテル基(−S−)を有するものが2種類のみ記載されている。
【0008】
本発明は、屈折率が高く、透明性に優れ、さらに耐熱性にも優れた特定の構造を有するイミド化重合体を主成分とする硬化膜を与える樹脂組成物を提供することを目的とする。
【課題を解決するための手段】
【0009】
上記目的を達成するため、本発明者らは鋭意研究を行い、チアンスレン骨格を有するジアミンと、脂肪族又は脂環族テトラカルボン酸二無水物とを組み合わせることにより、高屈折率と高透明性、そして耐熱性に優れたイミド化重合体を与えるポリアミック酸が得られることを見出し、本発明を完成させた。
【0010】
即ち、本発明は、下記の樹脂組成物、それを硬化させてなる硬化膜及びそれからなる光学用部材を提供する。
1.(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上、及び(E)有機溶剤を含有するを含む樹脂組成物。
【化3】

[式(3)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
2.前記Rが、4価の脂肪族基、4価の脂環族基及び4価の芳香族基からなる群から選択される上記1に記載の樹脂組成物。
3.前記Rが、硫黄原子を含む4価の有機基からなる群から選択される上記1又は2に記載の樹脂組成物。
4.さらに、酸化チタン又は酸化ジルコニウムを主成分とする、一次粒子径が1〜100nmの範囲内の粒子を含有する上記1〜3のいずれかに記載の樹脂組成物。
5.前記成分(B)の粒子が、酸化珪素被覆された酸化チタンからなる上記4に記載の樹脂組成物。
6.さらに、(C)界面活性剤を含有する上記1〜5のいずれかに記載の樹脂組成物。
7.さらに、(D)イミド化触媒を含有する上記1〜6のいずれかに記載の樹脂組成物。
8.前記(D)イミド化触媒が、光酸発生剤又は光塩基発生剤である上記7に記載の樹脂組成物。
9.さらに、前記一般式(3)で示される構造を有するポリアミック酸以外のポリアミック酸を含有する上記1〜8のいずれかに記載の樹脂組成物。
10.上記1〜10のいずれかに記載の樹脂組成物を硬化させてなる硬化膜。
11.屈折率が1.60以上である上記10に記載の硬化膜。
12.下記一般式(4)で示される構造を有するイミド化重合体を含む硬化膜。
【化4】

[式(4)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
13.上記10〜12のいずれかに記載の硬化膜からなる光学用部材。
14.固体画像素子の集光材料である上記13に記載の光学用部材。
15.ディスク集光材料である上記13に記載の光学用部材。
【発明の効果】
【0011】
本発明によれば、チアンスレン骨格を有するジアミンを使用することにより、高屈折率(波長633nmにおける屈折率が、最高で1.79)と高耐熱性が達成される。
本発明によれば、高屈折率と高透明性、さらに高耐熱性が要求される光学用部材に適した樹脂組成物を提供することができる。
さらに、本発明の樹脂組成物は、高屈折率ナノ粒子を添加することにより、更なる高屈折率化が可能である。
本発明によれば、屈折率が高く、透明性及び耐熱性に優れた光学用部材を提供することができる。
【発明を実施するための最良の形態】
【0012】
I.樹脂組成物
本発明の樹脂組成物(以下、本発明の組成物という)は、下記成分(A)〜(F)を含み得る。これらの成分のうち、成分(A)及び(E)は必須成分であり、それ以外は必要に応じて添加し得る任意成分である。
(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上
【化5】

(B)周期律表第4族元素の酸化物を主成分とする、一次粒子径が1〜100nmの範囲内の粒子
(C)界面活性剤
(D)イミド化触媒
(E)有機溶剤
(F)添加剤
以下、各成分について説明する。
【0013】
(A)一般式(3)で示される構造を有するポリアミック酸
本発明の組成物の必須成分であるポリアミック酸は、下記一般式(3)で示される構造を有し、それ自体の屈折率(25℃、波長633nm)が非常に高く、高屈折率で、透明性及び耐熱性に優れた硬化膜を形成することができる。
【化6】

【0014】
上記一般式(2)及び(3)中のRは、テトラカルボン酸二無水物から無水物基を除去した残基に相当する4価の有機基を示し、4価の脂肪族基、4価の脂環族基又は4価の芳香族基であることが好ましい。
上記一般式(3)中のR1はそれぞれ独立して炭素数1〜3のアルキル基を示し、a及びbは基R1の置換数を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示す。a及びbは0であることが好ましい。
上記一般式(3)中のmは、1〜100000の数を示し、10〜100000であることが好ましい。
【0015】
(a)上記一般式(3)で示される構造を有するポリアミック酸は、下記一般式(1)で示される新規化合物であるジアミン化合物と、下記一般式(2)で示されるテトラカルボン酸二無水物とを重縮合させることによって得られる。
【化7】

【0016】
【化8】

式(1)及び(2)中の置換基R、R1、a及びbは、上記式(3)において説明した通りである。
【0017】
(b)一般式(1)で示されるジアミンの製造
一般式(1)で示されるジアミン化合物は、次のようにして製造することができる。
工程1:チアンスレン骨格の製造
チアンスレン環の製造方法は公知であり、公知の方法に従って製造することができる。例えば、下記反応式のように、モノハロゲン置換チオフェノール誘導体を、硫酸(発煙硫酸又は濃硫酸)の存在下に縮合させて、ジハロゲン置換チアンスレン誘導体を得る。
【化9】

【0018】
工程2:ジアミン化合物の製造
非プロトン性極性溶剤中、無水炭酸カリウムとモノアミノ置換チオフェノール誘導体とを反応させ、アミノ置換チオフェノール誘導体のカリウム塩を合成する。そこに、上記工程1で製造したジハロゲン置換チアンスレン誘導体を添加することにより、一般式(1)で示されるジアミン化合物を製造することができる。
【化10】

【0019】
一般式(1)で示されるジアミンの例としては、例えば、2,7−ビス(4−アミノフェニレンスルファニル)チアンスレン、2,7−ビス(2−アミノフェニレンスルファニル)チアンスレン、2,7−ビス(3−アミノフェニレンスルファニル)チアンスレン、3,6−ビス(4−アミノフェニレンスルファニル)チアンスレン等が挙げられ、2,7−ビス(4−アミノフェニレンスルファニル)チアンスレンが好ましい。
【0020】
(c)一般式(2)で示されるテトラカルボン酸二無水物
上記一般式(2)で示されるテトラカルボン酸二無水物としては、脂肪族、脂環族又は芳香族テトラカルボン酸二無水物が挙げられ、光学的用途において必要とされる優れた透明性を有する硬化膜が得られることから脂肪族又は脂環族テトラカルボン酸二無水物が好ましい。
【0021】
脂肪族又は脂環族テトラカルボン酸二無水物の具体例としては、例えば、ブタンテトラカルボン酸二無水物、1,2,3,4−シクロブタンテトラカルボン酸二無水物、1,2,3,4−シクロペンタンテトラカルボン酸二無水物、4,10−ジオキサトリシクロ[6.3.1.02,7]ドデカン−3,5,9,11−テトラオン、1,2,4,5−シクロヘキサンテトラカルボン酸二無水物、2,3,5−トリカルボキシシクロペンチル酢酸二水和物、3,5,6−トリカルボキシノルボルナン−2−酢酸二無水物、2,3,4,5−テトラヒドロフランテトラカルボン酸二無水物、1,3,3a,4,5,9b−ヘキサヒドロ−5−テトラヒドロ−2,5−ジオキソ−3−フラニル)−ナフト[1,2−c]−フラン−1,3−ジオン、5−(2,5−ジオキソテトラヒドロフラル)−3−メチル−3−シクロヘキセン−1,2−ジカルボン酸二無水物、ビシクロ[2,2,2]−オクト−7−エン−2,3,5,6−テトラカルボン酸二無水物等の脂肪族及び脂環族テトラカルボン酸二無水物を挙げることができる。これらのうちではブタンテトラカルボン酸二無水物、1,2,3,4−シクロブタンテトラカルボン酸二無水物、4,10−ジオキサトリシクロ[6.3.1.02,7]ドデカン−3,5,9,11−テトラオン、2,3,5−トリカルボキシシクロペンチル酢酸二無水物、5−(2,5−ジオキソテトラヒドロフラル)−3−メチル−3−シクロヘキセン−1,2−ジカルボン酸二無水物及び1,3,3a,4,5,9b−ヘキサヒドロ−5−テトラヒドロ−2,5−ジオキソ−3−フラニル)−ナフト[1,2−c]−フラン−1,3−ジオンが好ましく、1,2,3,4−シクロブタンテトラカルボン酸二無水物、4,10−ジオキサトリシクロ[6.3.1.02,7]ドデカン−3,5,9,11−テトラオン、1,2,4,5−シクロヘキサンテトラカルボン酸二無水物が特に好ましい。
【0022】
芳香族テトラカルボン酸二無水物の具体例としては、ピロメリット酸二無水物、3,3’,4,4’−ベンゾフェノンテトラカルボン酸二無水物、3,3’,4,4’−ビフェニルスルホンテトラカルボン酸二無水物、1,4,5,8−ナフタレンテトラカルボン酸二無水物、2,3,6,7−ナフタレンテトラカルボン酸二無水物、3,3’,4,4’−ビフェニルエーテルテトラカルボン酸二無水物、3,3’,4,4’−ジメチルジフェニルシランテトラカルボン酸二無水物、3,3’,4,4’−テトラフェニルシランテトラカルボン酸二無水物、1,2,3,4−フランテトラカルボン酸二無水物、4,4’−ビス(3,4−ジカルボキシフェノキシ)ジフェニルスルフィド二無水物、4,4’−ビス(3,4−ジカルボキシフェノキシ)ジフェニルスルホン二無水物、4,4’−ビス(3,4−ジカルボキシフェノキシ)ジフェニルプロパン二無水物、4,4’−(ヘキサフルオロイソプロピリデン)ビス(フタル酸)二無水物、3,3’,4,4’−ビフェニルテトラカルボン酸二無水物、ビス(フタル酸)フェニルホスフィンオキサイド二無水物、p−フェニレン−ビス(トリフェニルフタル酸)二無水物、m−フェニレン−ビス(トリフェニルフタル酸)二無水物、ビス(トリフェニルフタル酸)−4,4’−ジフェニルエーテル二無水物、ビス(トリフェニルフタル酸)−4,4’−ジフェニルメタン二無水物等の芳香族テトラカルボン酸二無水物を挙げることができる。これらのうちでは、ピロメリット酸二無水物、3,3’,4,4’−ベンゾフェノンテトラカルボン酸二無水物、3,3’,4,4’−ビフェニルスルホンテトラカルボン酸二無水物、4,4’−(ヘキサフルオロイソプロピリデン)ビス(フタル酸)二無水物及び3,3’,4,4’−ビフェニルテトラカルボン酸二無水物が好ましい。
【0023】
また、より高屈折率のポリアミック酸が得られることから、硫黄原子を含むテトラカルボン酸二無水物を用いることも好ましい。硫黄原子含有酸無水物の例としては、例えば、4,4’−[p−チオビス(フェニレン−スルファニル)]ジフタル酸無水物等が挙げられる。
【0024】
尚、本発明の組成物には、上記一般式(3)で示される構造を有するポリアミック酸以外のポリアミック酸を含有していてもよい。即ち、上記一般式(1)で示されるジアミン化合物の他に、本発明の効果が損なわれない範囲内で、他のジアミンを併用することもできる。このようなジアミン化合物としては、例えばp−フェニレンジアミン、m−フェニレンジアミン、4,4’−ジアミノジフェニルメタン、4,4’−ジアミノジフェニルエタン、4,4’−ジアミノジフェニルスルフィド、4,4’−ジアミノジフェニルスルホン、4,4’−ジアミノジフェニルエーテル、1,5−ジアミノナフタレン、3,3−ジメチル−4,4’−ジアミノビフェニル、4,4’−ジアミノベンズアニリド、3,4’−ジアミノジフェニルエーテル、3,3’−ジアミノベンゾフェノン、3,4’−ジアミノベンゾフェノン、4,4’−ジアミノベンゾフェノン、2,2−ビス[4−(4−アミノフェノキシ)フェニル]プロパン、2,2−ビス[4−(4−アミノフェノキシ)フェニル]ヘキサフルオロプロパン、2,2−ビス(4−アミノフェニル)ヘキサフルオロプロパン、2,2−ビス[4−(4−アミノフェノキシ)フェニル]スルホン、1,4−ビス(4−アミノフェノキシ)ベンゼン、1,3−ビス(4−アミノフェノキシ)ベンゼン、1,3−ビス(3−アミノフェノキシ)ベンゼン、9,9−ビス(4−アミノフェニル)−10−ヒドロアントラセン、9,9−ビス(4−アミノフェニル)フルオレン、4,4’−メチレン−ビス(2−クロロアニリン)、2,2’,5,5’−テトラクロロ−4,4’−ジアミノビフェニル、2,2’−ジクロロ−4,4’−ジアミノ−5,5’−ジメトキシビフェニル、3,3’−ジメトキシ−4,4’−ジアミノビフェニル、4,4’−(p−フェニレンジイソプロピリデン)ビスアニリン、4,4’−(m−フェニレンジイソプロピリデン)ビスアニリンを挙げることができる。
【0025】
また、ジアミノテトラフェニルチオフェン等のヘテロ原子を有する芳香族ジアミン;1,1−メタキシリレンジアミン、1,3−プロパンジアミン、テトラメチレンジアミン、ペンタメチレンジアミン、ヘキサメチレンジアミン、ヘプタメチレンジアミン、オクタメチレンジアミン、ノナメチレンジアミン、4,4−ジアミノヘプタメチレンジアミン、1,4−ジアミノシクロヘキサン、イソホロンジアミン、テトラヒドロジシクロペンタジエニレンジアミン、ヘキサヒドロ−4,7−メタノインダニレンジメチレンジアミン、トリシクロ[6,2,1,02.7]−ウンデシレンジメチルジアミン等の脂肪族又は脂環族ジアミンも挙げることができる。
【0026】
一般式(3)で示される構造を有するポリアミック酸の製造に用いるジアミン類のうち、一般式(1)で示される本発明のジアミン化合物の割合は、50モル%以上であることが好ましく、80モル%以上であることがより好ましく、高屈折率を達成するためには100モル%であることが特に好ましい。
【0027】
一般式(1)で示されるジアミン化合物(以下、単にジアミン化合物ということがある)と、一般式(2)で示されるテトラカルボン酸二無水物(以下、単に酸二無水物ということがある)との重縮合反応は、公知の方法及び条件下に行うことができるが、例えば、下記の方法で行うことが好ましい。
N−メチル−2−ピロリドン等の非プロトン性有機溶媒中において、ジアミン化合物と酸二無水物とを攪拌混合することによって、一般式(3)で示される構造を有するポリアミック酸を溶液として得ることができる。例えば、ジアミン化合物を有機溶媒に溶解し、これに酸二無水物を加えて、攪拌混合してもよく、また、ジアミン化合物と酸二無水物との混合物を有機溶媒に加えて、攪拌混合してもよい。反応は、通常、100℃以下、好ましくは、80℃以下の温度で、常圧下に行われる。しかし、反応は、必要に応じて、加圧下又は減圧下に行ってもよい。反応時間は、用いるジアミン化合物と酸二無水物や、有機溶媒、反応温度等によって異なるが、通常、4〜24時間の範囲である。
【0028】
本発明の組成物中における成分(A)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常10〜100重量%、好ましくは20〜80重量%、より好ましくは30〜70重量%の範囲内である。成分(A)の配合量が10重量%未満では、十分な屈折率や耐熱性が発現できないおそれがある。
尚、本発明の組成物の必須成分は成分(A)のみであるが、通常は、成分(A)の製造に用いられる有機溶剤を含み、組成物の塗工性等の観点からも有機溶剤を含有することが好ましい。
【0029】
(B)周期律表第4族元素の酸化物を主成分とする、一次粒子径が1〜100nmの範囲内の粒子
成分(B)は周期律表第4属元素の酸化物粒子である。屈折率の高い粒子成分を添加することにより、得られる硬化膜の屈折率をさらに高めることができる。
成分(B)の粒子の一次粒子径は、1〜100nmの範囲内であることが必要であり、1〜50nmの範囲内であることが好ましく、5〜15nmの範囲内であることがより好ましい。粒子の一次粒子径が1nm未満であると、二次凝集が起こり易く硬化膜が白化するおそれがあり、100nmを超えると、薄膜形成時の面均一性が損なわれるおそれがある。ここで、一次粒子径は、光散乱法によって測定することができる。
【0030】
成分(B)の粒子として用いることができる酸化物粒子としては、酸化チタン、酸化ジルコニウム、酸化ハフニウム及びこれらの金属酸化物と酸化ケイ素や酸化スズの複合粒子が挙げられ、得られる硬化膜の屈折率を高める効果の点から、酸化チタン及び酸化ジルコニウムが好ましい。
【0031】
尚、酸化チタンは、光触媒活性が有るため、そのままでは光学用途に用いることは難しいため、粒子表面を酸化ケイ素で被覆することが好ましい。
また、酸化チタンには、結晶型の違いにより、アナターゼ型とルチル型が存在するが、屈折率が高く、耐光性に優れることからルチル型が好ましい。
【0032】
成分(B)として用いる酸化物粒子は、粉体状であってもよいし、溶媒分散ゾルであってもよい。分散媒としては、例えば、メタノール、メチルエチルケトン、メチルイソブチルケトン、シクロヘキサノン、N−メチル−2−ピロリドン、プロピレングレコールモノメチルエーテル等が挙げられる。
【0033】
成分(B)として用いることができる粒子の市販品の例としては、例えば、酸化ケイ素被覆アナターゼ型酸化チタン−メタノール分散ゾル(触媒化成工業社製、オプトレイクシリーズ)、酸化ケイ素被覆−酸化スズ含有ルチル型酸化チタン−メタノール分散ゾル(テイカ社製、TSシリーズ)、酸化ジルコニウム−メチルエチルケトン分散ゾル(大阪セメント社製、HXU−120JC)等が挙げられる。
【0034】
本発明の組成物中における成分(B)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常0〜90重量%、好ましくは20〜80重量%、より好ましくは40〜60重量%の範囲内である。成分(B)の配合量が90重量%を超えると、十分な耐熱性が得られないおそれがある。
尚、成分(B)が溶媒分散ゾルである場合には、成分(B)の配合量には分散媒を含まない。
【0035】
(C)界面活性剤
本発明の組成物をスピンコートによって基材等に塗布する場合には、均一な塗膜が得られることから、界面活性剤を配合することが好ましい。
本発明で用いることができる界面活性剤の種類としては、ポリジメチルシロキサン系界面活性剤、フッ素系界面活性剤等が挙げられ、ポリジメチルシロキサン系界面活性剤が好ましい。
【0036】
ポリジメチルシロキサン系の界面活性剤の例としては、例えば、SH28PA(東レダウコーニング社製、ジメチルポリシロキサンポリオキシアルキレン共重合体)、ペインタッド19、54(東レダウコーニング社製、ジメチルポリシロキサンポリオキシアルキレン共重合体)、FM0411(サイラプレーン、チッソ社製)、SF8428(東レダウコーニング社製、ジメチルポリシロキサンポリオキシアルキレン共重合体(側鎖OH含有))、BYK UV3510(ビックケミー・ジャパン社製、ジメチルポリシロキサン−ポリオキシアルキレン共重合体)、DC57(東レ・ダウコーニング・シリコーン社製、ジメチルポリシロキサン−ポリオキシアルキレン共重合体)、DC190(東レ・ダウコーニング・シリコーン社製、ジメチルポリシロキサン−ポリオキシアルキレン共重合体)、サイラプレーンFM−4411、FM−4421、FM−4425、FM−7711、FM−7721、FM−7725、FM−0411、FM−0421、FM−0425、FM−DA11、FM−DA21、FM−DA26、FM0711、FM0721、FM−0725、TM−0701、TM−0701T(チッソ社製)、UV3500、UV3510、UV3530(ビックケミー・ジャパン社製)、BY16−004、SF8428(東レ・ダウコーニング・シリコーン社製)、VPS−1001(和光純薬製)等が挙げられる。特にサイラプレーンFM−7711、FM−7721、FM−7725、FM−0411、FM−0421、FM−0425、FM0711、FM0721、FM−0725、VPS−1001等を挙げることができる。また、エチレン性不飽和基を有する当該シリコーン化合物の市販品としては、例えば、Tego Rad 2300、2200N、テゴ・ケミー社等を挙げることができる。
【0037】
フッ素系の界面活性剤の例として、例えば、メガファックF−114、F410、F411、F450、F493、F494、F443、F444、F445、F446、F470、F471、F472SF、F474、F475、R30、F477、F478、F479、F480SF、F482、F483、F484、F486、F487、F172D、F178K、F178RM、ESM−1、MCF350SF、BL20、R08、R61、R90(大日本インキ化学工業社製)が挙げられる。
【0038】
本発明の組成物中における成分(C)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常0〜10重量%、好ましくは0.1〜5重量%、より好ましくは0.5〜3重量%の範囲内である。成分(C)の配合量が10重量%を超えると、屈折率が低下するおそれがある。
【0039】
(D)イミド化触媒
本発明の組成物は、加熱によって成分(A)のポリアミック酸がイミド化重合体となることにより硬化するものであるが、この熱硬化反応を促進するためにイミド化触媒を添加することもできる。
【0040】
イミド化触媒としては、例えば、無水酢酸−ピリジン混合溶液等が挙げられる。また、無水酢酸−トリエチルアミン混合溶液や、無水トリフルオロ酢酸、ジシクロヘキシルカルボジイミドも使用できる。
【0041】
また、成分(D)として、光の照射によって酸又は塩基を発生させる化合物である光酸発生剤又は光塩基発生剤を用いることにより、本発明の組成物をパターニング可能な材料とすることができる。これにより、本発明の組成物を固体撮像素子の集光部材等のパターニング工程を必要とする光学用部材の製造に用いることが可能となる。
光塩基発生剤としては、例えば、カルバマート型光塩基発生剤等が挙げられる。具体的には、下記のような構造式で示される化合物が光塩基発生剤の例として挙げられる。
【化11】

【0042】
本発明の組成物中における成分(D)の配合量は、有機溶剤を除く固形分全量を100重量%としたときに、通常0〜20重量%、好ましくは1〜10重量%、より好ましくは1〜5重量%の範囲内である。成分(D)の配合量が20重量%を超えると、貯蔵安定性が低下するおそれがある。
【0043】
(E)有機溶剤
本発明の組成物は、通常、成分(A)のポリアミック酸製造の際に用いる溶剤を含有する。また、成分(B)の酸化物粒子として粒子の溶媒分散ゾルを用いる場合には、その分散媒も本発明の組成物中に含有される。その他、組成物の粘度を調整し、均一な塗膜を形成するための組成物の塗布性を改善するために、別途、有機溶剤を添加することができる。
【0044】
本発明で用いる有機溶剤としては、特に制限されないが、非プロトン系有機溶剤が好ましい。非プロトン系有機溶剤としては、例えば、N−メチル−2−ピロリドン(NMP)、ジメチルホルムアミド(DMF)、シクロヘキサノン、N,N−ジメチルアセトアミド(DMAc)等が好ましい。これら以外にもN,N−ジメチルホルムアミド、N、N−ジエチルアセトアミド、N,N−ジメトキシアセトアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルカプロラクタム、1,2−ジメトキシエタン、1,2−ジメトキシエタン、ビス(2−メトキシエチル)エーテル、1,2−ビス(2−メトキシエトキシ)エタン、ビス〔2−(2−メトキシエトキシ)エチル〕エーテル、テトラヒドロフラン、1,3−ジオキサン、1,4−ジオキサン、ピロリン、ピコリン、ジメチルスルホキシド、ジメチルスルホン、テトラメチル尿素、ヘキサメチルホスホルアミド、フェノール、o−クレゾール、m−クレゾール、p−クレゾール、m−クレゾール酸、p−クロロフェノール、アニソール、ベンゼン、トルエン、キシレン等を挙げることができる。これらの有機溶剤は単独で、又は2種類以上の混合物として用いられる。
【0045】
本発明の組成物中における成分(E)有機溶剤の配合量は、有機溶剤を除く固形分全量100重量部に対して、通常100〜9900重量部、好ましくは300〜1900重量部、より好ましくは400〜1900重量部の範囲内である。有機溶剤の配合量が100重量部未満では、スピンコート塗布ができなくなるおそれがあり、9900重量部を超えると、必要膜厚が発現できないおそれがある。
尚、成分(E)の配合量には、成分(A)のポリアミック酸溶液に由来する溶剤及び成分(B)の酸化物粒子分散ゾルの分散媒として持ち込まれる溶剤を含む。
【0046】
(F)添加剤
本発明の組成物には、本発明の効果を損なわない範囲内で、各種の添加剤を配合することができる。このような添加剤としては、例えば、上記成分以外の硬化性化合物、酸化防止剤等が挙げられる。
【0047】
硬化性化合物には、熱硬化性化合物及び光硬化性化合物を含む。これらの化合物を配合することにより、得られる硬化膜の硬度を高めることができる。
熱硬化性化合物としては、例えば、メラミン化合物、アルコキシシラン等が挙げられる。
光硬化性化合物としては、例えば、(メタ)アクリロイル基を有する化合物、ビニル基を有する化合物等が挙げられる。
【0048】
II.硬化膜
本発明の硬化膜は、下記一般式(4)で示される構造を有するイミド化重合体を含むことを特徴とする。一般式(4)で示される構造を有するイミド化重合体は、前記一般式(3)で示される構造を有するポリアミック酸をイミド化することによって得られる。
【化12】

式(4)中、R、R1、a、b及びmは、上記一般式(3)と同様であるためここでは説明を省略する。
【0049】
本発明の硬化膜は、上記本発明の組成物を基材等に塗布後、窒素雰囲気下で80〜300℃の温度で、1〜5時間加熱することによって、組成物中の(A)ポリアミック酸がイミド化されて、上記一般式(4)で示される構造を有するイミド化重合体となり硬化する。
【0050】
本発明の硬化膜は、成分(B)の酸化物粒子を含有しない場合であっても、波長633nmにおける屈折率が、通常1.60以上であり、好ましくは1.68以上、より好ましくは1.70以上である。
本発明の硬化膜の膜厚は、用途によって適宜選択すべきであるが、通常0.1〜5μm、好ましくは0.1〜2μm、透明性の観点からより好ましくは0.1〜1μmの範囲内である。0.1μm未満では製膜が困難となるおそれがあり、5μmを超えると、硫黄原子に起因する着色が見られ、透明性が低下するおそれがある。
【0051】
本発明の硬化膜は、高い屈折率、優れた透明性及び優れた耐熱性を必要とする光学用部材として好適である。本発明の硬化膜からなる光学用部材としては、例えば、固体撮像素子の集光材料、記録用ディスクの集光材料等が挙げられる。
本発明の組成物にイミド化触媒として光酸発生剤又は光塩基発生剤を配合することにより、パターニングが可能となり、例えば、マイクロレンズを製造することも可能である。パターニングによるマイクロレンズの製造方法は従来公知の方法で行うことができる。
【実施例】
【0052】
以下、本発明を実施例によってさらに具体的に説明するが、本発明は、これらの実施例によって何ら限定されるものではない。
【0053】
製造例1
2,7−ジフルオロチアンスレン
【化13】

攪拌機、還流冷却器及び窒素導入管を備えた反応容器に、p−フルオロチオフェノール(9.613g、75mmol)に発煙硫酸10〜50mLを加え、40〜80℃で12〜24時間反応させた。反応液を冷水に注ぎ、析出物を濾取し水洗した。得られた黄色の個体はエタノールを用いて再結晶し精製した。
融点:156.2℃(DSC)
FT−IR(KBr、cm−1):1592.9、1454.1、1253.5、1207.2、894.8、856.2、802.2
1H−NMR(300MHz、DMSO−d6、ppm):6.96−7.03(m、2H)、7.22−7.25(m、2H)、7.41−7.45(m、2H)
【0054】
製造例2
2,7−ビス(4−アミノフェニレンスルファニル)チアンスレンの合成
【化14】

攪拌機、還流冷却器、Dean−Starkトラップ及び窒素導入管を備えた反応容器に、p−アミノチオフェノール(9.389g、75mmol)と無水炭酸カリウム(5.39g、39mmol)、そしてN−メチル−2−ピロリドン(30mL、以下、NMP)とトルエン(50mL)を加え、140〜145℃で4時間反応させた。Dean−Starkトラップで水を除去し、トルエンも減圧留去した。反応液を120℃まで冷却し、製造例1で製造した2,7−ジフルオロチアンスレン(7.569g、30mmol)とNMP(15mL)を加えた。その後、反応液を170℃で12時間反応させた。反応液を室温まで戻し、反応液を冷水(500mL)に注ぎ、黄色の析出物を濾取し水洗した。得られた黄色の個体はエタノールを用いて再結晶し精製した。得られた化合物のIRチャート、1H−NMR及び13C−NMRチャートをそれぞれ図1〜図3に示す。
【0055】
収量:10.34g
収率:74.5%
融点:185.2℃(DSC)
FT−IR(KBr、cm−1):3428.8、3332.4、2360.4、1619.9、1592.9、1565.9、1492.6、1442.5、1361.5、1292.1、1176.4、1103.1、817.7
1H−NMR(300MHz、DMSO−d6、ppm):5.49(s、4H)、6.61−6.64(d、4H)、6.94−6.98(d、4H)、7.06(s、2H)、7.14−7.17(d、4H)、7.36−7.38(d、2H)
13C−NMR(300MHz、DMSO−d6、ppm):151.2、142.2、137.5、136.7、131.0、129.9、126.2、125.9、115.8、114.3
元素分析:計算値 C24H18N2S4:C、62.31%;H、3.92%;N、6.05%
測定値 C、62.22%;H、3.96%;N、6.01%
【0056】
製造例3
4,4’−[p−チオビス(フェニレン−スルファニル)]ジフタル酸無水物
【化15】

攪拌機、還流冷却器及び窒素導入管を備えた反応容器に、4,4’−チオビスベンゼンチオール(5.00g、0.02mol)と4−ブロモフタル酸無水物(10.00g、0.044mol)、無水炭酸カリウム(6.08g、0.044mol)、そしてN,N−ジメチルホルムアミド(DMF)(100mL)を加え、120℃で12時間反応させた。反応液を室温に戻し、白色の固体を濾取し、160℃で24時間減圧乾燥した。得られた白色の固体に蒸留水(100mL)と濃塩酸(100mL)を加え、3時間の間、加熱攪拌した。得られた白色の固体を濾取し、180〜190℃で3時間加熱し黄色の固体を得た。
【0057】
収量:7.8g
収率:71.9%
融点:175.2℃(DSC)
FT−IR(KBr、cm−1):1847.5、1778.0、1604.4、1473.3、1326.8、1257.4、902.5、817.7、732.0
1H−NMR(300MHz、DMSO−d6、ppm):7.45−7.49(d、4H)、7.52−7.55(d、4H)、7.56(s、2H)、7.60−7.63(d、2H)、7.83−7.85(d、2H)
元素分析:計算値 C28H14O6S3:C、61.98%;H、2.60%
測定値 C、62.23%;H、2.97%
【0058】
<粒子成分を含まない組成物の製造例>
実施例1
窒素導入管を備えた反応容器に、2,7−ビス(4−アミノフェニレンスルファニル)チアンスレン(18.51g、40mmol)(以下、APTTという)にN−メチル−2−ピロリドン(80g)(以下、NMPという)を加え、室温で攪拌し完全に溶解させた。次に、1,2,3,4−シクロブタンテトラカルボン酸二無水物(7.84g、40mmol)(以下、CBDAという)とNMP(25g)を添加し、室温で24時間攪拌して、ポリアミック酸のNMP溶液Aを得た。得られたポリアミック酸のIRチャートを図4に示す。
【0059】
実施例2〜6
実施例1で用いたCBDAの代わりに、下記表1に示す酸無水物を用いた他は、実施例1と同様の方法で重合を行い、各ポリアミック酸のNMP溶液を得た。
【0060】
比較例1
窒素導入管を備えた反応容器に、ビス(p−アミノフェニル)エーテル(8.01g、40mmol)(以下、ODAという)にN−メチル−2−ピロリドン(80g)(NMP)を加え、室温で攪拌し完全に溶解させた。次に、CBDA(7.84g、40mmol)とNMP(25g)を添加し、室温で24時間攪拌して、ポリアミック酸のNMP溶液を得た。
【0061】
<硬化膜の作成>
3インチ径3mm厚の溶融石英基板上に実施例1〜6及び比較例1で製造したポリアミック酸のNMP溶液をディスペンスし、厚さが約8〜12μmになるようにスピンコート塗布し、窒素雰囲気下280℃で1.5時間加熱し、硬化膜を得た。
実施例1で得られた硬化膜中のイミド化重合体のIRチャートを図5、実施例3〜6で得られた硬化膜中の各イミド化重合体のIRチャートを図6に示す。
【0062】
<硬化膜の特性評価>
上記で得られた硬化膜について下記特性を評価した。結果を表1に示す。
【0063】
(1)屈折率
Metricon社のPC−2000型プリズムカプラーを使用して、上記で得られた硬化膜の、波長633nmにおける屈折率を測定した。
【0064】
(2)透過率
日立製作所社製のU−3500型自記分光光度計を使用して、上記で得られた硬化膜の膜厚1μm当たりの波長400nm及び450nmにおける透過率(%)を測定した。
【0065】
(3)耐熱性
セイコーインスツル社製のDSC6300(昇温速度10℃/分、窒素気流下)を使用して、上記で得られた硬化膜の5%重量減少温度を測定した。5%重量減少温度が400℃以上の場合を耐熱性合格(○)と評価した。
【0066】
【表1】

【0067】
表1中の略号は下記のものを表す。
APTT:2,7−ビス(4−アミノフェニレンスルファニル)チアンスレン;実施例1で製造
ODA:ビス(p−アミノフェニル)エーテル
CBDA:1,2,3,4−シクロブタンテトラカルボン酸二無水物
CHDA:1,2,4,5−シクロヘキサンテトラカルボン酸二無水物
sBPDA:3,3’,4,4’−ビフェニルテトラカルボン酸二無水物
aBPDA:2,3’,3,4’−ビフェニルテトラカルボン酸二無水物
ODPA:4,4’−オキシジフタル酸二無水物
3SDEA:4,4’−[p−チオビス(フェニレン−スルファニル)]ジフタル酸無水物;製造例1で製造
【0068】
表1の結果から、一般式(3)で示される構造を有するポリアミック酸は、屈折率が高く、透明性に優れ、さらに耐熱性にも優れた一般式(4)で示される構造を有するイミド化重合体与えることがわかる。
【0069】
<粒子成分を含む組成物の製造例>
実施例7
窒素導入管を備えた反応容器に、実施例1で製造したポリアミック酸のNMP溶液(ポリアミック酸含有量20重量%)28.88gに、シクロヘキサノン、乳酸エチル、2−ブトキシエタノールの混合溶剤(重量比:3/0.5/0.5)59.53gとジメチルポリシロキサンポリオキシアルキレン共重合体(東レダウコーニング社製SH28PA)0.11gを加え溶解させた。次に酸化ケイ素被覆−酸化スズ含有ルチル型酸化チタンのメタノールゾル(テイカ社製TSシリーズ、粒子含量20重量%)23.62gを滴下した。その後、室温で1時間攪拌し高屈折率樹脂組成物を得た。
【0070】
実施例8〜11及び比較例2
表2に示す組成とした以外は、実施例7と同様の方法で調製を行い、各高屈折率樹脂組成物を得た。
【0071】
<硬化膜の作製>
4インチ径のシリコンウエハ基板上に実施例24〜31及び比較例2で調整した高屈折率樹脂組成物をディスペンスし、厚さ約0.3μmになるようにスピンコート塗布し、窒素雰囲気下280℃×1.5時間で製膜した。
【0072】
<硬化膜の特性評価>
上記のようにして作製した硬化膜について、下記特性を測定、評価した。結果を表2に示す。
【0073】
(1)屈折率
N&K Technology社のN&K Analyzerを使用して、波長633nmにおける屈折率を測定した。
【0074】
(2)透過率
JASCO社製のV−570型分光光度計を使用して、波長400nmにおける透過率を測定した。
【0075】
【表2】

【0076】
表2中の略号等は下記のものを示す。
酸化ケイ素被覆−酸化スズ含有ルチル型酸化チタン:テイカ社製の粒子メタノールゾル、TSシリーズ、一次粒子径5〜15nm、粒子含量20重量%
酸化ジルコニウム:住友大阪セメント社製の粒子メチルエチルケトンゾル、HXU−120JC、一次粒子径5〜15nm、粒子含量40重量%
酸化ケイ素被覆アナターゼ型酸化チタン:触媒化成工業社製の粒子メタノールゾル、オプトレイク、一次粒子径5〜20nm、粒子含量25重量%
SH28PA:東レダウコーニング社製界面活性剤、ジメチルポリシロキサンポリオキシアルキレン共重合体
【0077】
表2の結果から、(B)粒子成分を配合することにより、さらに屈折率が1.756〜1.864と非常に高く、光学用部材に必要な高い透過率も有する硬化膜が得られることがわかる。
【図面の簡単な説明】
【0078】
【図1】製造例2で得られたジアミン化合物のIRチャートである。
【図2】製造例2で得られたジアミン化合物の1H−NMRチャートである。
【図3】製造例2で得られたジアミン化合物の13C−NMRチャートである。
【図4】実施例1で得られたポリアミック酸のIRチャートである。
【図5】実施例1で得られたポリアミック酸をイミド化したイミド化重合体のIRチャートである。
【図6】実施例2で得られたポリアミック酸のIRチャートである。
【図7】実施例2で得られたイミド化重合体のIRデータである。
【図8】実施例3で得られたポリアミック酸のIRチャートである。
【図9】実施例4で得られたポリアミック酸のIRチャートである。
【図10】実施例5で得られたポリアミック酸のIRチャートである。
【図11】実施例6で得られたポリアミック酸のIRチャートである。
【図12】実施例3〜6で得られた各ポリアミック酸をイミド化したイミド化重合体(PI−3〜6)のIRチャートである。
【特許請求の範囲】
【請求項1】
(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上、及び(E)有機溶剤を含有する樹脂組成物。
【化1】

[式(3)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
【請求項2】
前記Rが、4価の脂肪族基、4価の脂環族基及び4価の芳香族基からなる群から選択される請求項1に記載の樹脂組成物。
【請求項3】
前記Rが、硫黄原子を含む4価の有機基からなる群から選択される請求項1又は2に記載の樹脂組成物。
【請求項4】
さらに、酸化チタン又は酸化ジルコニウムを主成分とする、一次粒子径が1〜100nmの範囲内の粒子を含有する請求項1〜3のいずれか1項に記載の樹脂組成物。
【請求項5】
前記成分(B)の粒子が、酸化珪素被覆された酸化チタンからなる請求項4に記載の樹脂組成物。
【請求項6】
さらに、(C)界面活性剤を含有する請求項1〜5のいずれか1項に記載の樹脂組成物。
【請求項7】
さらに、(D)イミド化触媒を含有する請求項1〜6のいずれか1項に記載の樹脂組成物。
【請求項8】
前記(D)イミド化触媒が、光酸発生剤又は光塩基発生剤である請求項7に記載の樹脂組成物。
【請求項9】
さらに、前記一般式(3)で示される構造を有するポリアミック酸以外のポリアミック酸を含有する請求項1〜8のいずれか1項に記載の樹脂組成物。
【請求項10】
請求項1〜9のいずれか1項に記載の樹脂組成物を加熱して得られる硬化膜。
【請求項11】
屈折率が1.60以上である請求項10に記載の硬化膜。
【請求項12】
下記一般式(4)で示される構造を有するイミド化重合体を含む硬化膜。
【化2】

[式(4)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
【請求項13】
請求項10〜12のいずれか1項に記載の硬化膜からなる光学用部材。
【請求項14】
固体画像素子の集光材料である請求項13に記載の光学用部材。
【請求項15】
ディスク集光材料である請求項13に記載の光学用部材。
【請求項1】
(A)下記一般式(3)で示される構造を有するポリアミック酸の1種以上、及び(E)有機溶剤を含有する樹脂組成物。
【化1】

[式(3)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
【請求項2】
前記Rが、4価の脂肪族基、4価の脂環族基及び4価の芳香族基からなる群から選択される請求項1に記載の樹脂組成物。
【請求項3】
前記Rが、硫黄原子を含む4価の有機基からなる群から選択される請求項1又は2に記載の樹脂組成物。
【請求項4】
さらに、酸化チタン又は酸化ジルコニウムを主成分とする、一次粒子径が1〜100nmの範囲内の粒子を含有する請求項1〜3のいずれか1項に記載の樹脂組成物。
【請求項5】
前記成分(B)の粒子が、酸化珪素被覆された酸化チタンからなる請求項4に記載の樹脂組成物。
【請求項6】
さらに、(C)界面活性剤を含有する請求項1〜5のいずれか1項に記載の樹脂組成物。
【請求項7】
さらに、(D)イミド化触媒を含有する請求項1〜6のいずれか1項に記載の樹脂組成物。
【請求項8】
前記(D)イミド化触媒が、光酸発生剤又は光塩基発生剤である請求項7に記載の樹脂組成物。
【請求項9】
さらに、前記一般式(3)で示される構造を有するポリアミック酸以外のポリアミック酸を含有する請求項1〜8のいずれか1項に記載の樹脂組成物。
【請求項10】
請求項1〜9のいずれか1項に記載の樹脂組成物を加熱して得られる硬化膜。
【請求項11】
屈折率が1.60以上である請求項10に記載の硬化膜。
【請求項12】
下記一般式(4)で示される構造を有するイミド化重合体を含む硬化膜。
【化2】

[式(4)中、Rは4価の脂肪族基、4価の脂環族基又は4価の芳香族基を示し、R1はそれぞれ独立して炭素数1〜3のアルキル基を示し、aはそれぞれ独立して0〜4の整数を示し、bはそれぞれ独立して0〜3の整数を示し、mは1〜100000の数を示す。]
【請求項13】
請求項10〜12のいずれか1項に記載の硬化膜からなる光学用部材。
【請求項14】
固体画像素子の集光材料である請求項13に記載の光学用部材。
【請求項15】
ディスク集光材料である請求項13に記載の光学用部材。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2008−274229(P2008−274229A)
【公開日】平成20年11月13日(2008.11.13)
【国際特許分類】
【出願番号】特願2008−59601(P2008−59601)
【出願日】平成20年3月10日(2008.3.10)
【出願人】(000004178)JSR株式会社 (3,320)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【Fターム(参考)】
【公開日】平成20年11月13日(2008.11.13)
【国際特許分類】
【出願日】平成20年3月10日(2008.3.10)
【出願人】(000004178)JSR株式会社 (3,320)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【Fターム(参考)】
[ Back to top ]

