歯周病と歯髄疾患の治療剤と治療方法
【課題】本発明の目的は、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法を提供することである。
【解決手段】神経栄養因子を有効成分とする、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法。神経栄養因子は、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5である。
【解決手段】神経栄養因子を有効成分とする、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法。神経栄養因子は、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法に関するものである。
【背景技術】
【0002】
歯肉、歯槽骨、歯周靱帯(歯根膜)、セメント質、歯髄等で構成される歯周組織は、歯牙を植立させ、咀嚼や咬合等の機能を維持させるための重要な組織であり、その損傷や破壊は歯の喪失につながる。例えば、日本国内に約3000万人の患者が存在するといわれる歯周病においては、病気の進行と共に歯周組織の損傷や破壊が進み、歯を喪失する大きな原因となっている。損傷あるいは破壊された歯髄を含む歯周組織の治療には、医薬品投与や外科手術等、様々な方法が試みられているが、いずれの薬剤や治療方法も、損傷あるいは破壊された歯髄を含む歯周組織を再生させる効果は十分とはいえない。
【0003】
神経栄養因子には脳由来神経栄養因子(Brain-derived neurotrophic factor、BDNF)、神経成長因子(Nerve growth factor、NGF)、ニューロトロフィン3(Neurotrophin 3、NT-3)、およびニューロトロフィン4/5(Neurotrophin 4/5、NT-4/5)があり、神経細胞の分化促進や生存維持、再生促進、機能維持に関与する。BDNFとNT-4/5はTrkB(tropomyosin receptor kinase B)、NGFはTrkA、NT-3はTrkCという高親和性レセプターに特異的に結合する。
【0004】
BDNF、NGF、NT-3は、主として脳内に存在する神経栄養因子であり、BDNFとNGFは運動神経障害モデル、パーキンソン病モデル、アルツハイマー病モデルなど、各種の疾患モデル動物を用いた実験で、有効性が証明されている。中でも、BDNFは、運動・末梢神経疾患として筋萎縮性側索硬化症(ALS)、糖尿病や化学療法剤による末梢神経障害など、また中枢神経系疾患としてアルツハイマー病、パーキンソン病、網膜関連疾患などの治療薬としての開発が期待されている。
【0005】
これらの神経栄養因子は、中枢神経系のみならず末梢神経系においても重要な役割を果たしていると言われている。マウス肋骨の骨折治癒過程においてBDNF、NGF、NT-3、TrkC、TrkAの発現が増加した(K. Asaumiら、Bone Vol 26, No.6, 625-633, 2000)、BDNF、NGF、NT-3がマウス歯周靱帯細胞の増殖を促進した(Y. Tsuboiら、J Dent Res 80, (3), 881-886, 2001)等の報告もある。しかし、歯周組織や歯髄組織におけるこれらの神経栄養因子の働きについての詳しい報告はない。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】K. Asaumiら、Bone Vol 26, No.6, 625-633, 2000
【非特許文献2】Y. Tsuboiら、J Dent Res 80, (3), 881-886, 2001
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明の目的は、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法を提供することである。
【課題を解決するための手段】
【0008】
本発明者らは、上記課題を解決するために鋭意研究した結果、神経栄養因子が、ヒト歯周靱帯由来線維芽細胞の増殖を促進し、骨関連タンパク質のmRNA発現を促進すること、イヌの根分岐部病変モデルにおいて歯周組織の再生を促進することを知得し、本発明を完成するに至った。
【0009】
すなわち、本発明によれば、神経栄養因子を有効成分とする、歯周病の治療剤が提供される。
本発明の治療剤が、歯周組織を再生させることが好ましい。
【0010】
本発明の治療剤が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
本発明の治療剤が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
【0011】
本発明の治療剤が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。
本発明の治療剤において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
【0012】
本発明の別の側面によれば、神経栄養因子を含有する歯周組織再生用移植材が提供される。
本発明の移植材が、歯周組織を再生させることが好ましい。
【0013】
本発明の移植材が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
本発明の移植材が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
【0014】
本発明の移植材が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。
本発明の移植材において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
【0015】
本発明のさらに別の側面によれば、神経栄養因子を使用する歯周組織の再生方法が提供される。
本発明の再生方法が、歯周組織を再生させることが好ましい。
【0016】
本発明の再生方法が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
本発明の再生方法が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
【0017】
本発明の再生方法において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
本発明の別の側面によれば、歯周病の治療方法であって、そうした状態に罹患しているまたは罹患しやすい対象に治療有効量の神経栄養因子を投与することを含む、歯周病の治療法が提供される。
【0018】
本発明の治療法が、歯周組織を再生させることが好ましい。
本発明の治療法が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
【0019】
本発明の治療法が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
本発明の治療法が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。
【0020】
本発明の治療法において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
本発明のさらに別の側面によれば、歯周病の治療に使用する薬剤を製造するための神経栄養因子の使用が提供される。
【0021】
この薬剤が、歯周組織を再生させることが好ましく、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。この薬剤が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。この薬剤が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
【0022】
本発明のさらに別の側面によれば、神経栄養因子を有効成分とする、修復象牙質の形成促進剤が提供される。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。修復象牙質が歯髄腔の内壁に添加されることが好ましい。
【0023】
本発明の別の側面によれば、歯髄疾患の治療方法であって、そうした疾患に罹患しているまたは罹患しやすい対象に、修復象牙質の形成を促進するために治療有効量の神経栄養因子を投与することを含む、歯髄疾患の治療法が提供される。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。修復象牙質が歯髄腔の内壁へ添加されることが好ましい。
【0024】
本発明のさらに別の側面によれば、修復象牙質の形成を促進するために使用する薬剤を製造するための神経栄養因子の使用が提供される。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。修復象牙質が歯髄腔の内壁へ添加されることが好ましい。
【図面の簡単な説明】
【0025】
【図1】HPL細胞およびヒト歯周靭帯における、BDNFとTrkBとのmRNA発現を示す電気泳動図である。各電気泳動図の、左端のレーンはマーカーである。(A)は、ヒト歯周靭帯およびHPL 細胞におけるグリセルアルデヒド-3-リン酸脱水素酵素(GAPDH)のmRNA(613bp)の発現を示す。(B)は、ヒト歯周靭帯におけるBDNFのmRNA(438bp)とTrkBのmRNA(434bp)の発現を示す。(C)は、HPL 細胞におけるBDNFとTrkBとのmRNA発現を示す。
【図2A】HPL 細胞における、BDNFの作用時間とALPaseのmRNA(381bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を1としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図2B】HPL 細胞における、BDNFの作用時間とOPNのmRNA(532bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を1としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図2C】HPL 細胞における、BDNFの作用時間と、BMP-2のmRNA(440bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を1としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図2D】HPL 細胞における、BDNFの作用時間とGAPDHのmRNAの発現量との関係を示す電気泳動図である。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。
【図3A】HPL 細胞における、BDNFの作用時間とBMP-4のmRNA(339bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図3B】HPL 細胞における、BDNFの作用時間とOPGのmRNA(736bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図4A】HPL 細胞における、BDNFの投与量とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。各濃度のBDNFを、HPL 細胞に24時間作用させた。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF投与量0のときのmRNA発現量を1とした場合の、各投与量におけるmRNAの発現量の割合を示す。横軸は、BDNFの濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図4B】HPL 細胞における、BDNFの投与量とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。各濃度のBDNFを、HPL 細胞に12時間作用させた。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF投与量0のときのmRNA発現量を1とした場合の、各投与量におけるmRNAの発現量の割合を示す。横軸は、BDNFの濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図4C】HPL 細胞における、BDNFの投与量とBMP-2のmRNAの発現量との関係を示す電気泳動図とグラフである。各濃度のBDNFを、HPL 細胞に24時間作用させた。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF投与量0のときのmRNA発現量を1とした場合の、各投与量におけるmRNAの発現量の割合を示す。横軸は、BDNFの濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。
【図4D】HPL 細胞における、BDNFの投与量とGAPDHのmRNA(613bp)発現量との関係を示す電気泳動図である。
【図5】(A)は、HPL 細胞における、BDNFの投与量とOPNの分泌量の関係を示すグラフである。各濃度のBDNFを、HPL 細胞に12時間作用させた。縦軸にOPNの分泌量(ng/ml)、横軸にBDNFの濃度(ng/ml)を示す。(B)は、HPL 細胞における、BDNFの投与量とBMP-2の分泌量の関係を示すグラフである。各濃度のBDNFを、HPL 細胞に、24時間作用させた。縦軸にBMP-2の分泌量(pg/ml)、横軸にBDNFの濃度(ng/ml)を示す。(C)は、HPL 細胞における、BDNFの作用時間とBMP-2の分泌量の関係を示すグラフである。細胞は最終濃度50ng/mlのBDNFで処理した。縦軸にBMP-2の分泌量(pg/ml)、横軸にBDNFの作用時間を示す。(A)〜(C)の各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図6】BDNFの投与量とHPL 細胞およびHGKのDNA合成能との関係を示すグラフである。各濃度のBDNFを、HPL 細胞およびHGKに24時間作用させた。各グラフの縦軸は、BDNFあるいはbFGF非投与(つまりBDNF濃度0あるいはbFGF濃度0)のときのDNA合成能を100としたときの、各投与量におけるDNA合成能の割合を示している。横軸はBDNFまたはbFGF濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。(A)はHPL 細胞におけるDNA合成能を示し、(B)はHGKにおけるDNA合成能を示す。
【図7】(A)は、HPL 細胞における、BDNFの投与量とI型コラーゲンの合成量との関係を示すグラフである。各濃度のBDNFを、HPL 細胞に24時間作用させた。縦軸にI型コラーゲンの合成量(μg/ml)、横軸にBDNFの濃度(ng/ml)を示す。(B)は、HPL 細胞における、BDNFの作用時間とI型コラーゲン合成量の関係を示すグラフである。細胞は最終濃度50ng/mlのBDNFで処理した。縦軸にI型コラーゲン合成量(μg/ml)、横軸にBDNFの作用時間を示す。(A)、(B)の各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。
【図8】イヌの3級根分岐部病変モデルにおける、BDNFの投与量とセメント質および歯槽骨の再生との関係を示すグラフである。縦軸にセメント質再生率(%)または骨再生率(%)を示し、横軸にBDNFの濃度(μg/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。(A)はセメント質再生率との関係を示し、(B)は骨再生率との関係を示す。
【図9A】実施例2で作成された、BDNFを含まないテルプラグを填塞した根分岐部骨欠損部位(対照群)のヘマトキシリン・エオジン染色標本の光学顕微鏡像(倍率20倍)である。
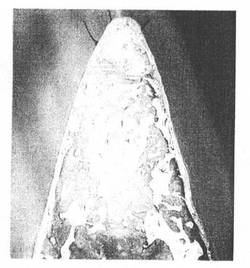
【図9B】実施例2で作成された、BDNF(5μg/ml)を含む移植材を填塞した分岐部骨欠損部位の顕微鏡像(倍率20倍)である。
【図10】図9Bの根分岐部直下の部分拡大像である(倍率200倍)。根分岐部直下において、裸出させた歯根面のほとんどの部分でコラーゲン線維を埋入したセメント質が再生しており、上皮の進入も見られなかった。
【図11A】HPL細胞における、NGFのmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量に対するNGFのmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図11B】HPL細胞における、TrkAのmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量に対するTrkAのmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図12】HPL 細胞におけるOPNのmRNA発現量に及ぼす、NGFの影響を示すグラフである。(A)はNGFの経時効果の測定結果を示すグラフであり、グラフ縦軸は、NGF作用時間0におけるmRNA発現量を1としたときの、各作用時間におけるOPNのmRNA発現量の割合を示す。グラフ横軸はNGFの作用時間を示す。すべて最終濃度100ng/mlのNGFで処理した。(B)は濃度効果の測定結果を示すグラフである。グラフ縦軸は、NGF濃度0におけるmRNA発現量を1としたときの、各濃度におけるOPNのmRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。NGFはすべて24時間作用させた。
【図13】HPL 細胞におけるALPaseのmRNA発現量に及ぼす、NGFの影響を示すグラフである。(A)はNGFの経時効果の測定結果を示すグラフであり、グラフ縦軸は、NGF作用時間0におけるALPaseのmRNA発現量を1としたときの、各作用時間におけるALPaseのmRNA発現量の割合を示す。グラフ横軸はNGFの作用時間を示す。(B)は濃度効果の測定結果を示すグラフである。グラフ縦軸は、NGF濃度0におけるALPaseのmRNA発現量を1としたときの、各濃度におけるALPaseのmRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。
【図14】HPL 細胞におけるBMP-2のmRNA発現量に及ぼす、NGFの影響を示すグラフである。(A)はNGFの経時効果の測定結果を示すグラフであり、グラフ縦軸は、NGF作用時間0におけるBMP-2のmRNA発現量を1としたときの、各作用時間におけるBMP-2のmRNA発現量の割合を示す。グラフ横軸はNGFの作用時間を示す。(B)は濃度効果の測定結果を示すグラフである。グラフ縦軸は、NGF濃度0におけるBMP-2のmRNA発現量を1としたときの、各濃度におけるBMP-2のmRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。
【図15】NGFの投与量とHPL 細胞およびHGKのDNA合成能との関係を示すグラフである。各濃度のNGFを、HPL 細胞およびHGKに24時間作用させた。各グラフの縦軸は、NGF濃度0におけるDNA合成能を100としたときの、NGF各投与量におけるDNA合成能の割合を示している。横軸はNGF濃度(ng/ml)を示す。(A)はHPL 細胞におけるDNA合成能を示し、(B)はHGKにおけるDNA合成能を示す。
【図16A】HPL細胞における、NT-3のmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量を1としたときのNT-3のmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図16B】HPL細胞における、TrkCのmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量を1としたときのTrkCのmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図17】HPL細胞における、NT-3の投与量とALPase活性との関係を示すグラフである。グラフ縦軸はALPase活性(nmol/ウェル)を示し、横軸はNT-3濃度(ng/ml)を示す。
【図18】HPL 細胞における、NT-3の投与量とHPL細胞のDNA合成能との関係を示すグラフである。グラフの縦軸は、NT-3各濃度におけるHPL細胞のDNA合成能を吸光度で比較したものである。横軸はNT-3濃度(ng/ml)を示す。
【図19A】HPL細胞における、NT-4/5の作用時間とOPN、OCNのmRNAの発現量との関係を示す電気泳動図とグラフである。NT-4/5の最終濃度は50ng/mlとした。電気泳動図の左端のレーンはマーカーである。各グラフ縦軸は、NT-4/5の作用時間0のときの各mRNA発現量を100としたときの、各作用時間における各mRNAの発現量の割合を示す。横軸は、NT-4/5の作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【図19B】HPL細胞における、NT-4/5の作用時間とBMP-2、BMP-7のmRNAの発現量との関係を示す電気泳動図とグラフである。NT-4/5の最終濃度は50ng/mlとした。電気泳動図の左端のレーンはマーカーである。各グラフ縦軸は、NT-4/5の作用時間0のときの各mRNA発現量を100としたときの、各作用時間における各mRNAの発現量の割合を示す。横軸は、NT-4/5の作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【図19C】HPL 細胞におけるNT-4/5の作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフ、およびNT-4/5の作用時間とGAPDHの発現量との関係を示す電気泳動図である。NT-4/5の最終濃度は50ng/mlとした。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-4/5の作用時間0のときのmRNA発現量を100としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、NT-4/5の作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05を表す(統計学的検定はt-testによる)。
【図20】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、OPN、OCN)のmRNA発現に対する、NGFの濃度効果の測定結果を示すグラフである。NGFの作用時間は24時間である。各グラフ縦軸は、NGF濃度0におけるmRNA発現量を1としたときの、各濃度における各mRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図21】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、I型コラーゲン、OPN、OCN)のmRNA発現に対する、BDNFの濃度効果の測定結果を示すグラフである。各グラフ縦軸は、BDNF濃度0における各mRNA発現量を1としたときの、各濃度におけるmRNA発現量の割合を示す。横軸はBDNF濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図22】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、OPN、OCN)のmRNA発現に対する、NT-3の濃度効果の測定結果を示すグラフである。各グラフ縦軸は、NT-3濃度0におけるmRNA発現量を1としたときの、各濃度における各mRNA発現量の割合を示す。横軸はNT-3濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図23】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、I型コラーゲン、OPN、OCN)のmRNA発現に対する、NT-4/5の濃度効果の測定結果を示すグラフである。各グラフ縦軸は、NT-4/5濃度0におけるmRNA発現量を1としたときの、各濃度における各mRNA発現量の割合を示す。横軸はNT-4/5濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図24】各神経栄養因子(NGF、BDNF、NT-3、NT-4/5)の投与量とHP 細胞のDNA合成能との関係を示すグラフである。各濃度の神経栄養因子を、HP 細胞に24時間作用させた。各グラフの縦軸は、神経栄養因子非投与(つまり神経栄養因子の濃度0)のときの吸光度を100としたときの、各投与量における吸光度の割合を示している。横軸は各神経栄養因子の濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図25A】HMS 細胞における、NGFの作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。コントロールであるGAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25B】HMS 細胞における、NGFの作用時間とOCNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25C】HMS 細胞における、NGFの作用時間とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25D】HMS 細胞における、NGFの作用時間とBSPのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25E】HMS 細胞における、NGFの作用時間とI型コラーゲンのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図26A】HMS 細胞における、BDNFの作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26B】HMS 細胞における、BDNFの作用時間とOCNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26C】HMS 細胞における、BDNFの作用時間とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26D】HMS 細胞における、BDNFの作用時間とBSPのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26E】HMS 細胞における、BDNFの作用時間とI型コラーゲンのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図27A】HMS 細胞における、NT-3の作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27B】HMS 細胞における、NT-3の作用時間とOCNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27C】HMS 細胞における、NT-3の作用時間とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27D】HMS 細胞における、NT-3の作用時間とBSPのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27E】HMS 細胞における、NT-3の作用時間とI型コラーゲンのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図28】HMS細胞の増殖に及ぼすアスコルビン酸(Aa)、NGF、BDNF、NT-3の効果を示すグラフである。グラフの縦軸は、対照群に対する試験群の吸光度の百分率を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【図29A】実施例8で作成された、NGF(100μg/ml)を含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像(倍率20倍)である。
【図29B】実施例8で作成された、NT-3(100μg/ml)を含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像(倍率20倍)である。
【発明を実施するための形態】
【0026】
以下、本発明のより具体的な態様、並びに本発明を実施するための方法につき説明する。
本明細書において「歯周組織」とは、歯肉、歯槽骨、歯周靱帯(歯根膜)、セメント質で構成される組織を意味する。
【0027】
「歯肉」とは、歯頚部と歯槽骨の一部を被覆している軟組織で、歯肉上皮と歯肉固有層とからなる。
「歯周靭帯」とは、歯槽骨とセメント質の間に介在している結合組織のことであり、歯根膜とも呼ばれる。
【0028】
「歯槽骨」は、歯根を取り巻いている歯槽壁の緻密質の部分に相当する固有歯槽骨と、さらにその外側に位置する海綿質と緻密質の部分からなる支持歯槽骨とに区分される。
「セメント質」は、歯根の最表層の硬組織であり、セメント細胞を有する有細胞性セメント質とセメント細胞を有さない無細胞性セメント質とに区分される。
【0029】
「歯髄」は、歯の生活反応を司る組織で、生理的、病的刺激に反応して、象牙質を形成する。歯髄細胞、神経線維、細胞外基質、血管などから構成される。
「再生(regeneration)」とは、喪失組織、破壊された組織や損傷組織の再構成(reconstruction)および再構築(reproduction)のことであり、「歯周組織の再生」とは、歯周組織を元の状態に回復させ機能させることである。
【0030】
「修復(repair)」とは、創傷部の構造と機能がいまだ完全な状態では回復していない組織の治癒のことであり、「歯周組織の修復」には、歯根表面への上皮性付着などが含まれる。
【0031】
「歯肉上皮の歯根面根尖方向への進入を防止する」とは、歯肉上皮細胞が歯根面に沿って根尖側に向かって増殖していくことを防ぐことを意味する。
「歯周組織再生用移植材」とは、歯周組織の再生を促す材料のことである。BDNF等の神経栄養因子を所定の生体部位(歯槽骨の欠損部位など)に一定の濃度で作用させるためには、何らかの足場(scaffold)が必要である。こうした足場となる材料とBDNF等の神経栄養因子を組合わせたものが本願の移植材である。
【0032】
「歯周病」とは、局所の細菌等を原因として起こる歯周組織の炎症性疾患を意味する。
「修復象牙質」とは、外来刺激を受けた結果形成された象牙質を意味する。
「歯髄疾患」とは、歯髄の炎症性疾患、退行変性などを意味する。
【0033】
本発明は、ヒトなどの温血動物において、特に好ましくはヒトに適用される。
本発明に使用する神経栄養因子、BDNF、NGF、NT-3、NT-4/5等は、遺伝子組換えや化学合成などで人工的に製造したものでも天然型(native)でもよい。
【0034】
本発明の歯周病治療剤は、外用剤などによる局所投与が好ましい。シリンジ等に充填し、歯周ポケット内に注入してもよい。また、歯周外科治療の際に、歯周組織の欠損部に投与することも可能である。その場合には、長時間一定の濃度で作用させるために、本発明の治療剤をシートやスポンジなどに吸収させて使用することも好ましい。感染した歯周組織を除去してから投与することが好ましい。本発明の治療剤は注射により局所投与することも可能である。例えば、歯周ポケット部の歯肉に注射してもよいし、歯槽骨頂付近の歯根膜腔に注射してもよい。根尖部付近に注射してもよい。
【0035】
本発明の修復象牙質形成促進剤は、外用剤などによる局所投与が好ましい。例えば、露髄部に、液状、クリーム状、ペースト状などの修復象牙質形成促進剤を適用しても良いし、断髄や抜髄に適用しても良い。活性成分を吸収させたシートやスポンジを適用し、一定期間仮封しても良い。あるいは外傷等で脱落した歯牙を再植する際に根尖部等に適用しても良い。
【0036】
本発明の歯周病治療剤と修復象牙質形成促進剤の剤型としては、通常の製剤方法により、製剤的に許容しうる担体または希釈剤などを使用して製造されるクリーム剤、軟膏剤、ローション剤等の外用剤の他、例えば水系の溶剤を主成分とした注射剤などが挙げられる。粉末状の剤型として、使用直前に精製水などの溶解液に溶解して使用することも可能である。
【0037】
本発明の歯周病治療剤と修復象牙質形成促進剤の投与量は、投与対象の年齢、性別、症状等により異なるが、局所投与においては、通常1歯あたり、神経栄養因子として1×10−12g〜1×10−3 g、特に1×10−11g〜1×10−7 g、さらに特に1×10−10g〜1×10−8 gであることが好ましい。一般に、注射で局所投与する場合は外用薬よりも少ない投与量でよい。
【0038】
本発明の移植材は、1つの根分岐部欠損に使用する量あたり、1×10−12g〜1×10−3 g、特に1×10−11g〜1×10−8 g、さらに特に1×10−10g〜1×10−9 gの神経栄養因子を含むことが好ましい。
【0039】
本発明の歯周病治療剤、修復象牙質形成促進剤や移植材は、その有効性を妨げない限り、他の薬剤と組合わせて使用してもよい。BDNF、NGF、NT-3、NT-4/5を互いに組合わせて使用してもよい。骨髄由来間葉系幹細胞(MSC)、歯周靱帯由来線維芽細胞、歯肉線維芽細胞、血管内皮細胞等と組み合わせて使用してもよい。水酸化カルシウム製剤、抗菌剤などと併用してもよい。
【0040】
本発明の移植材において神経栄養因子と組合わせる材料としては、神経栄養因子を投与局所に維持できる生体為害性のない材料であればよいが、例えば、多孔性のシートやスポンジなどが好ましい。生体分解性タンパク材料(コラーゲン、ゼラチン、アルブミン、プレートレット・リッチ・プラズマ(PRP))や組織吸収性材料(ポリグリコール酸(PGA)、ポリ乳酸(PLA)、乳酸グリコール酸共重合体(PLGA)、ヒアルロン酸(HA)、三リン酸カルシウム(TPC))であれば、後に摘出する必要がないためさらに好ましい。例えば、テルプラグ(商品名)(テルモ株式会社)、ジーシーメンブレン(商品名)(株式会社ジーシー)、オスフェリオン(商品名)(オリンパス株式会社)等がある。
【0041】
以下の実施例により本発明をさらに詳細に説明する。
【実施例1】
【0042】
ヒト歯周靱帯由来線維芽細胞(human periodontal ligament cell、HPL 細胞)およびヒト歯肉上皮細胞(human gingival keratinocyte、HGK)に及ぼすBDNFの影響を検討した。
(1)使用細胞
(i) ヒト歯周靱帯由来線維芽細胞(HPL 細胞)
矯正治療のために便宜的に抜歯された健全なヒト小臼歯の歯周靭帯から、HPL 細胞を分離した。歯周靭帯周囲の他の結合組織からの細胞の混入を防ぐため、抜去ヒト小臼歯の歯頚部、根尖部を除く歯根中央部の健康な歯周靭帯を、メスを用いて剥離し、細切した。細切した組織を、直径60mmの細胞培養用シャーレ(CORNING、NY)に貼り付け、37℃、5%CO2気相条件で培養した。培地は、10%FBS(GIBCO、Buffalo、NY)、ペニシリン(100ユニット/ml)(明治製菓、東京)、ストレプトマイシン(100μg/ml)(明治製菓)、およびアンホテリシンB(1μg/ml)(GIBCO)を添加したダルベッコ変法イーグル培地(DMEM、日水製薬、東京)を使用した(ここで使用した培地を「培地A」と記す)。4〜8代継代したHPL 細胞を以下の実験に供した。
【0043】
(ii) ヒト歯肉上皮細胞(HGK)
ヒト培養細胞を用いた実験の必要性および歯肉の使用目的などを患者に十分説明し、患者の同意を得た後に、歯肉の提供を受けた。智歯周囲炎の患者から、原因となった智歯を抜歯する際に、余剰の歯肉弁から歯肉片を獲得した。得られた歯肉片を、4℃で一昼夜、0.01%エチレンジアミン4酢酸(EDTA)と0.025%トリプシンを含むダルベッコPBS(−)(PBS(−),日水製薬)で処理して、HGKを分離した。ウシインシュリン(10μg/ml)(Sigma、St. Rouis, MO, USA)、ヒトトランスフェリン(5μg/ml)(Sigma)、2-メルカプトエタノール(10μM)、2-アミノエタノール(10μM)、亜セレン酸ナトリウム(10μM)、牛下垂体抽出液(50μg/ml)、ペニシリン(100ユニット/ml)、ストレプトマイシン(100μg/ml)およびアンホテリシンB(50ng/ml)を含むMCDB153培地(Sigma)で初代培養を行った(ここで使用した培地を「培地C」と記す)。培養は、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1、住友ベークライト、東京)を用いて、37℃、5%CO2気相条件で行った。3〜4代継代したHGKを以下の実験に供した。
【0044】
(2)HPL細胞におけるBDNFとそのレセプターの発現
HPL細胞およびヒト歯周靭帯におけるBDNFとTrkBのmRNA発現を、1st Strand cDNA Synthesis Kit for RT-PCR(Roche、Indianapolis)を使用して、逆転写PCR法で調べた。
【0045】
上記(1)(i)で得られたHPL 細胞がコンフルエントになった時点で細胞を回収し、ISOGEN(ニッポンジーン、東京)にて細胞を溶解させた後、クロロホルムを加えて遠心分離し、得られた水相にイソプロパノールを加えて総RNAを抽出した。
【0046】
上記(1)(i)で得られたヒト歯周靭帯をISOGEN中でホモジナイズした後、クロロホルムを加えて遠心分離し、得られた水相にイソプロパノールを加えて総RNAを抽出した。
精製した総RNAのうち1μgの各RNAを、オリゴdTプライマ−を用いて逆転写し、得られたcDNAをPCR反応30サイクルにて増幅させた後、1.5%アガロースゲルに泳動した。コントロールとしてはグリセルアルデヒド-3-リン酸脱水素酵素(GAPDH)を使用した。
【0047】
結果を図1に示す。コントロールとしてはグリセルアルデヒド-3-リン酸脱水素酵素(GAPDH)を使用した。図から明らかなように、ヒト歯周靭帯においてBDNFとTrkBのmRNAの発現がみられ、そのヒト歯周靱帯より分離、培養したHPL 細胞においても、BDNFとTrkBのmRNAが発現していることが確認された。
【0048】
(3)細胞のBDNFでの処理
(i) HPL 細胞
上記(1)(i)で得られたHPL 細胞を、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1)に、1シャーレあたり3.5×105個で、50μg/mlのL-アスコルビン酸を含む培地Aを用いて、37℃、5%CO2気相条件で13日間培養した(ここで使用した培地を「培地B」と記す)。培地は2日に1回交換した。14日目の培養終了前0、3、6、12または24時間において、細胞をDMEMで2回洗浄し、最終濃度0、1、10、50または100ng/mlのBDNF(Recombinant Human BDNF、R & D system、Minneapolis、 USA)を含む無血清培地(ペニシリン(100ユニット/ml)、ストレプトマイシン(100μg/ml)、アンホテリシンB(1μg/ml)(GIBCO)、およびL-アスコルビン酸(50μg/ml)を添加したDMEM)(ここで使用した培地を「培地D」と記す)に交換した。
【0049】
(ii) HGK
上記(1)(ii)で得られたHGKを、ウシI型コラーゲンがコートされた96穴プレート(SUMILON セルタイトC-1プレート96F、住友ベークライト)に、2×103個/ウェルで接種し、37℃、5%CO2気相条件で、培地Cを用いて培養した。培地は2日に1回交換した。細胞増殖期にあたる培養4〜5日目に、プレートの細胞をMCDB153培地で2回洗浄し、最終濃度0、1、10、25、50または100ng/mlのBDNFを含む培地(牛下垂体抽出液を含まないこと以外は培地Cと同一の組成の培地)に交換し、24時間培養した。
【0050】
(4)HPL細胞における骨関連タンパク質の発現
(i) mRNAの発現
上記(3)(i)に記載の方法と同様にして、最終濃度0、1、10、50または100ng/mlのBDNFで処理したHPL 細胞から、ISOGENを用いて総RNAを抽出し、精製した。アルカリホスファターゼ(ALPase)、骨形成タンパク-2(bone morphogenetic protein-2、BMP-2)、骨形成タンパク-4(bone morphogenetic protein-4、BMP-4)、オステオポンチン(osteopontin、OPN)、オステオプロテジェリン(osteoprotegerin、OPG)のmRNA発現量は、ABI PRISM7700 (Applied Biosystems、東京)を用いて、PCRプロダクトの生成過程をリアルタイムでモニタリングし、定量的に解析した(Real-time PCR法)。コントロールとしてはGAPDHを使用した。
【0051】
各骨関連タンパク質のmRNA発現に対する、BDNFの経時効果測定の結果を図2A〜2C、3A、3Bに、濃度効果測定の結果を図4A〜4Cに示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【0052】
これらの図から明らかなように、BDNFはOPG、BMP-4のmRNA発現に影響を及ぼさなかったが、ALPase、BMP-2、OPNのmRNA発現量を濃度および時間依存的に増加させた。
(ii) タンパク質の発現
上記(1)(i)で得られたHPL 細胞を、ウシI型コラーゲンがコートされた48穴プレート(SUMILON セルタイトC-1プレート 48F、住友ベークライト)に、1×104個/ウェルで播種し、培地Bを用いて13日間培養した。培地は2日に1回交換した。14日目の培養終了24時間前に、プレートの細胞をDMEMで2回洗浄し、最終濃度0、1、10、25、50または100ng/mlのBDNFを含む無血清培地Dに交換した。培養終了後に、上清を回収し、上清中の分泌OPN量、分泌BMP-2量を、ELISA法で測定した。分泌OPN量の測定にはサンドイッチELISAキット(IBL、群馬)を、分泌BMP-2量の測定にはサンドイッチELISAキット(R & D system)を使用した。
【0053】
図5に、HPL 細胞の分泌OPN量と分泌BMP-2量に対する、BDNFの経時効果測定および濃度効果測定の結果を示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。図5から明らかなように、BDNFは、HPL細胞におけるOPNとBMP-2の分泌を促進した。
【0054】
(5)HPL細胞とHGKの増殖
HPL細胞とHGKのDNA合成能に及ぼすBDNFの影響を、Cell Proliferation ELISA system, version 2(アマシャムファルマシアバイオテク)を用いて、ELISA法で測定した。
【0055】
上記(1)(i)で得られたHPL細胞を、ウシI型コラーゲンがコートされた96穴プレート(SUMILON セルタイトC-1プレート96F)に、5×103個/ウェルで播種し、培地Bを用いて10日間培養した。細胞をDMEMで2回洗浄し、10%FBSの代わりに0.3%FBSを添加した培地Bで24時間培養した後、同じ培地にBDNFを最終濃度0、1、10、25、50又は100ng/mlとなるように添加して調製した培地と交換し、さらに24時間培養した。培養終了の2時間前(つまりにBDNF添加の22時間後)に、ブロモデオキシウリジン(BrdU)を10ng/mlの濃度で各ウェルに添加して、細胞に取り込ませた。培養は37℃、5%CO2気相条件下で行った。
【0056】
上記(1)(ii)で得られたHGKを、上記(3)(ii)と同一の方法で培養し、BDNFで処理した。培養終了の2時間前(つまりにBDNF添加の22時間後)に、ブロモデオキシウリジン(BrdU)を10ng/mlの濃度で各ウェルに添加して、細胞に取り込ませた。
【0057】
培養終了後、HPL細胞とHGKを固定した後、ブロッキングを行い、ペルオキシダーゼ標識抗BrdU抗体を室温で2時間作用させ、TMB(3,3',5,5'-テトラメチルベンシジン)基質を加え、波長450nmにおける吸光度を吸光度計(MICRO PLATE READER、TOSOH)で測定した。コントロールとして、塩基性線維芽細胞成長因子(bFGF)を最終濃度0、0.3、1、3、5、10ng/mlで24時間作用させた細胞を同様に処理して、DNA合成能を測定した。
【0058】
結果を図6に示す。(A)はHPL細胞に対する効果を示すグラフであり、(B)はHGKに対する効果を示すグラフである。なお、各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【0059】
図6から明らかなように、BDNFはHPL細胞のDNA合成能を促進させたのに対し、HGKのDNA合成能には影響を及ぼさなかった。
(6)HPL細胞のコラーゲン合成
上記(1)(i)で得られたHPL細胞をウシI型コラーゲンをコートした48穴プレートに播種し、培地Bを用いて13日間培養した。培地は2日に1回交換した。14日目の培養終了前0、3、6、12または24時間、プレートの細胞をDMEMで2回洗浄し、最終濃度0、1、10、25、50または100ng/mlのBDNFを含む無血清培地Dに交換した。
【0060】
Procollagen type I C-peptide (PIP)EIA kit(TAKARA)を使用して、ELISA法でHPL細胞のコラーゲン合成量を測定した。I型プロコラーゲンC末端プロペプチド(PIP)に特異的なモノクローナル抗体(ペルオキシダーゼ標識)を用いて、HPL細胞培養上清中のコラーゲン合成量を、波長450nmにおける吸光度を吸光度計(MICRO PLATE READER)で測定した。
【0061】
結果を図7に示す。(A)はBDNFのI型コラーゲン合成への濃度効果測定の結果を示し、(B)は経時効果測定の結果を示す。図7から明らかなように、BDNFはHPL細胞のI型コラーゲン合成量を増加させた。
【実施例2】
【0062】
ビーグル犬の3級根分岐部病変モデルにおけるBDNFの効果を検討した。
直径8mm×5mmのテルプラグ(商品名)(テルモ)に、濃度5、25、50μg/mlのBDNF溶液(滅菌生理食塩液中)の25μlをしみこませ、移植材とした。
【0063】
7頭の雌ビーグル犬(12〜20ヵ月齢、体重10〜14kg)を、ドミトール(明治製菓)筋注による鎮静下に、全顎的にハンドスケーラーでスケーリングを行った。以後2日に1回の割合でブラッシングとポビドンヨードを有効成分とする含嗽薬であるイソジン(商品名)(明治製菓)による口腔清掃とを1ヵ月行い、臨床的に健康な歯周組織の状態を確立した。
【0064】
これらのビーグル犬に、ペントバルビタール系麻酔剤の静脈内注射により、全身麻酔を施し、左右両側下顎頬側歯肉に浸潤麻酔を行い、第一小臼歯遠心から第一大臼歯近心にかけての歯肉溝切開を行い、歯肉を剥離し粘膜骨膜弁を形成した。次いで、左右両側第二、第三、第四小臼歯の根分岐部歯槽骨をラウンドバーと骨ノミで削除し、根分岐部3級(Lindhe & Nymanの分類による)の骨欠損を作成した。骨欠損の大きさは、未処置の根分岐部直下から約4mm根尖側寄りまでとした。
【0065】
露出させた歯根面の残存セメント質をハンドスケーラーで除去した後、根分岐部骨欠損内を生理食塩液で十分洗浄して削片を洗い流し、1ヵ所あたり直径8mm×5mmのテルプラグ移植材を填塞した。BDNFを含まない、滅菌生理食塩液25μlのみをしみこませた直径8mm×5mmのテルプラグ移植材を填塞して、コントロールとした。
【0066】
手術6週間後に、ペントバルビタール系麻酔剤の静脈内注射による全身麻酔下で、4%パラホルムアルデヒドで全身を灌流固定した。灌流固定後、下顎を切断し、処理した歯及び歯周組織を一塊として摘出した。得られた標本を、4%パラホルムアルデヒドで1日浸漬固定後、10%EDTAにて脱灰を行い、通法に従いアルコール脱水しパラフィンに包埋した。この標本から、近遠心方向に歯軸と平行な切片(厚さ約5μm)を作製し、ヘマトキシリン・エオジン染色を施した。
【0067】
作成した組織標本のなかで、近遠心方向歯軸に平行でしかも根中央付近で薄切された標本を選択し、光学顕微鏡(ECLIPSE E600、NIKON)で組織観察と計測を行った。骨再生率は、裸出させた根分岐部欠損の面積に対する再生歯槽骨の面積の割合(百分率)として表した。セメント質再生率は、裸出させた歯根面の長さに対する、再生セメント質の長さの割合(百分率)として表した。
【0068】
結果を図8、9A、9B、10に示す。図8の(A)はセメント質再生へのBDNFの効果の測定結果を示し、図8の(B)は歯槽骨再生へのBDNFの効果の測定結果を示す。図9AはBDNF非投与(コントロール)の根分岐部骨欠損部のヘマトキシリン・エオジン染色標本であり、図9Bは、BDNFを投与した(BDNF(5μg/ml)を含む移植材を填塞)根分岐部骨欠損部の光学顕微鏡像である(倍率20倍)。図10は図9Bの根分岐部直下の部分拡大像である(倍率200倍)。
【0069】
図8から明らかなように、BDNFの投与により、イヌの3級根分岐部病変モデルにおいて、セメント質の再生と歯槽骨の再生が認められた。
図9Aのコントロール標本においては、セメント質、歯槽骨、歯周靱帯の再生がいくらか観察されたものの、骨欠損底部から歯冠側方向のほぼ1/2に留まっていた。根分岐部直下の欠損部にはセメント質再生、歯槽骨再生は認められず、上皮の進入も認められ、線維芽細胞、コラーゲン線維、血管を主体とした結合組織で埋めつくされていた。
【0070】
図9Bおよび図10のBDNFを投与した根分岐部骨欠損部の標本では、裸出させた歯根面のほとんどの部分でセメント質が再生しており、上皮の進入も見られなかった。また、再生セメント質と再生歯槽骨の間には一定の幅を維持した歯周靱帯も観察された。
【実施例3】
【0071】
HPL 細胞およびHGKに及ぼすNGFの影響を検討した。
(1)HPL細胞におけるNGFとそのレセプターの発現
上記実施例1(2)と同一の方法でHPL細胞から総RNAを回収し、精製した。得られた総RNAを試料として、NGFとTrkAとのmRNA発現をノーザンブロット法で測定した。コントロールとしてはGAPDHを使用した。
【0072】
結果を図11A、11Bに示す。図11AはNGFのmRNA発現を示し、図11BはTrkAのmRNA発現を示す。図から明らかなように、HPL 細胞においてNGFのmRNAとTrkAのmRNAとが発現していることが確認された。
【0073】
(2)HPL細胞における骨関連タンパク質の発現
HPL 細胞の骨関連タンパク質のmRNA発現に及ぼすNGFの影響を測定した。
HPL 細胞を、最終濃度0、5、10、25、50または100ng/mlのNGF(Recombinant Human NGF、R & D system、Minneapolis、USA)をBDNFの代わりに使用すること以外は、実施例1(4)(i)と同一の方法で処理した。NGF処理したHPL 細胞のALPase、BMP-2、OPNの各mRNA発現量を、実施例1(4)(i)と同一の方法で測定した。
【0074】
図12、13、14に、それぞれ、OPN、ALPase、BMP-2のmRNA発現に対する、NGFの経時効果測定および濃度効果測定の結果を示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す。検定はt-testによる。
【0075】
図12、13、14から明らかなように、NGFは、ALPase、BMP-2、OPNのmRNA発現量を濃度および時間依存的に増加させた。
(3)HPL細胞とHGKの増殖
HPL細胞とHGKのDNA合成能に及ぼすNGFの影響を測定した。
【0076】
HPL細胞とHGKを、最終濃度0、5、10、25、50または100ng/mlのNGFをBDNFの代わりに使用すること以外は、実施例1(5)と同一の方法で処理した。NGF処理したHPL細胞とHGKのDNA合成能を、実施例1(5)と同一の方法で測定した。
【0077】
結果を図15に示す。NGF作用時間はすべて24時間である。(A)はHPL細胞に対する効果を示し、(B)はHGKに対する効果を示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す。検定はt-testによる。
【0078】
図15から明らかなように、NGFはHPL細胞のDNA合成能を促進させたのに対し、HGKのDNA合成能を低下させた。
【実施例4】
【0079】
HPL 細胞およびHGKに及ぼすNT-3の影響を検討した。
(1)HPL細胞におけるNT-3とそのレセプターの発現
上記実施例1(2)と同一の方法でHPL細胞から総RNAを回収し、精製した。得られた総RNAを試料として、NT-3とTrkCのmRNA発現を、ノーザンブロット法で測定した。コントロールとしてはGAPDHを使用した。
【0080】
結果を図16A、16Bに示す。図16AはNT-3のmRNA発現を示し、16BはTrkCのmRNA発現を示す。これらの図から明らかなように、HPL 細胞においてNT-3のmRNAとTrkCのmRNAとが発現していることが確認された。
【0081】
(2)HPL細胞における骨関連タンパク質の発現
HPL 細胞のALPase活性に及ぼすNT-3の影響を測定した。
HPL 細胞を、最終濃度0、1、10または50ng/mlのNT-3(Recombinant Human NT-3、R & D system、Minneapolis、USA)をBDNFの代わりに使用すること以外は実施例1(3)(i)と同一の方法で処理し、そのALPase活性をBessey-Lowry法に従って定量した。すなわち、NT-3処理したHPL 細胞をリン酸緩衝液で3回洗浄し、10mMトリス塩酸緩衝液を加えた後、氷冷下で超音波処理を行い、試料を調製した。p-ニトロフェニルリン酸を基質とするALPase測定キット(和光純業)を使用して、試料中のALPaseの活性を測定した。
【0082】
図17に、ALPase活性に対するNT-3の濃度効果測定の結果を示す。NT-3作用時間はすべて24時間である。図から明らかなように、NT-3は、ALPase活性に対してそれほど影響が見られなかった。
【0083】
(3)HPL細胞の増殖
実施例1(1)と同一の方法で分離したHPL細胞を、最終濃度0、1、5、10、50または100ng/mlのNT-3をBDNFの代わりに使用すること以外は、実施例1(5)と同一の方法で処理し、そのDNA合成能を、実施例1(5)と同一の方法で測定した。
【0084】
結果を図18に示す。NT-3作用時間はすべて24時間である。本グラフにおいて、*はp<0.05、**はp<0.01を表す。検定はt-testによる。図から明らかなように、NT-3はHPL細胞のDNA合成能を促進させた。
【実施例5】
【0085】
ヒト歯周靱帯由来線維芽細胞(human periodontal ligament cell、HPL 細胞)におけるNT-4/5による骨関連タンパク質のmRNA発現を調べた。
(1)HPL細胞のNT-4/5での処理
上記実施例1(1)(i)で得られたHPL細胞を、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1)に、1シャーレあたり3.5×105個で、50μg/mlの培地Bを用いて、37℃、5%CO2気相条件で13日間培養した。培地は2日に1回交換した。14日目の培養終了前0、3、6、12または24時間において、細胞をDMEMで2回洗浄し、最終濃度50ng/mlのNT-4/5(R&D)を含む培地Dに交換した。
【0086】
(2)HPL細胞におけるmRNAの発現
上記(3)(i)に記載の方法と同様にして、最終濃度50ng/mlのNT-4/5で処理したHPL 細胞から、ISOGENを用いて総RNAを抽出し、精製した。ALPase、BMP-2、OPN、オステオカルシン(OCN)、BMP-7、BMP-4、OPGのmRNA発現量は、ABI PRISM7700 (Applied Biosystems、東京)を用いて、PCRプロダクトの生成過程をリアルタイムでモニタリングし、定量的に解析した(Real-time PCR法)。コントロールとしてはGAPDHを使用した。
【0087】
各骨関連タンパク質のmRNA発現に対する、NT-4/5の経時効果測定の結果を図19A、19B、19Cに示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。図から明らかなように、HPL 細胞において、NT-4/5は、OPN、BMP-2、ALPase、OCN、BMP-7のmRNA発現を促進した。しかし、BMP-4、OPGの発現には影響を与えなかった(データは示さず)。
【実施例6】
【0088】
ヒト歯髄細胞(human pulp cell、HP 細胞)に及ぼすNGF、BDNF、NT-3、NT-4/5の影響を検討した。
(1)使用細胞
便宜的歯髄除去時に得られた健全歯髄を細切した。細切した組織を、直径60mmの細胞培養用シャーレ(コーニング、NY)に貼り付け、37℃、5%CO2気相条件で培地Aにて培養した。4〜8代継代したHP細胞を以下の実験に供した。
【0089】
(2)細胞のNGF、BDNF、NT-3、NT-4/5での処理
NGF、BDNF、NT-3またはNT-4/5を培地Dに最終濃度0、5、10、25、50、100ng/mlで加えて、各種濃度の神経栄養因子含有培地を用意した。上記(2)で得られたHP 細胞を、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1)に、1シャーレあたり3.5×105個で、培地Bを用いて、37℃、5%CO2気相条件で13日間培養した。培地は2日に1回交換した。14日目の培養終了前24時間において、細胞をDMEMで2回洗浄し、いずれかの神経栄養因子含有培地に交換した。
【0090】
(3)HP細胞におけるmRNAの発現
上記(1)で、各濃度のNGF、BDNF、NT-3、またはNT-4/5で24時間処理したHP細胞から、ISOGENを用いて総RNAを抽出し、精製した。ALPase、BMP-2、象牙質シアロタンパク(DSPP)、I型コラーゲン(collagen)、OPN、OCNのmRNA発現量は、ABI PRISM7700 (Applied Biosystems、東京)を用いて、PCRプロダクトの生成過程をリアルタイムでモニタリングし、定量的に解析した(Real-time PCR法)。コントロールとしてはGAPDHを使用した。
【0091】
NGF、BDNF、NT-3、NT-4/5の各骨関連タンパク質のmRNA発現に対する濃度効果の測定結果を、それぞれ、図20、21、22、23に示す。図から明らかなように、NGF、BDNF、NT-3、NT-4/5は、HP細胞において、ALPase、BMP-2、DSPP、OPN、OCNのmRNA発現を促進した。BDNFとNT-4/5は、I型コラーゲンのmRNA発現も促進した。
【0092】
(4)HP細胞の増殖
HP細胞のDNA合成能に及ぼすNGF、BDNF、NT-3、NT-4/5の影響を、Cell Proliferation ELISA system, version 2(アマシャムファルマシアバイオテク)を用いて、ELISA法で測定した。
【0093】
NGF、BDNF、NT-3、NT-4/5のそれぞれを、10%FBSの代わりに0.3%FBSを添加した培地Bに、最終濃度0、5、10、25、50又は100ng/mlとなるように添加して、各種神経培養因子含有培地を調製した。
【0094】
上記(1)で得られたHP細胞を、ウシI型コラーゲンがコートされた96穴プレート(SUMILON セルタイトC-1プレート96F)に、5×103個/ウェルで播種し、培地Bを用いて10日間培養した。細胞をDMEMで2回洗浄し、10%FBSの代わりに0.3%FBSを添加した培地Bで24時間培養した後、上記の各種神経培養因子含有培地と交換し、さらに24時間培養した。培養終了の2時間前(つまりに神経培養因子添加の22時間後)に、ブロモデオキシウリジン(BrdU)を10ng/mlの濃度で各ウェルに添加して、細胞に取り込ませた。培養は37℃、5%CO2気相条件下で行った。
【0095】
培養終了後、HP細胞を固定後、ブロッキングを行い、ペルオキシダーゼ標識抗BrdU抗体を室温で2時間作用させ、TMB(3,3',5,5'-テトラメチルベンシジン)基質を加え、波長450nmにおける吸光度を吸光度計(MICRO PLATE READER、TOSOH)で測定した。
【0096】
結果を図24に示す。図から明らかなように、NGF、BDNF、NT-3、NT-4/5はHP細胞のDNA合成能を促進させた。
【実施例7】
【0097】
ヒト間葉系幹細胞(human mesenchymal stem cell、HMS細胞)に及ぼすNGF、BDNF、NT-3、アスコルビン酸の影響を検討した。
(1)使用細胞
HMS細胞の分離は堤ら(S.Tsutsumi:BBRC, 26, 288(2), 2001)の方法に準じて行った。すなわち、十分なインフォームドコンセントを得た患者の智歯抜去時に下顎骨骨髄腔へ穿刺し、骨髄液を得た。得られた骨髄液をヘパリンナトリウム(200 U/ml,シグマ、米国)を含むダルベッコ変法イーグル培地(DMEM、シグマ、米国)と速やかに混合し,遠心分離(150g,5 min)を行った。遠心分離後、上清を除去し、得られた細胞成分を10%のウシ胎児血清(FCS, Biological Industries, イスラエル)、100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含むDMEMに懸濁し、骨髄液が200〜500 μl/dish、培地が10 ml/dishとなるように、直径100 mmの細胞培養用シャーレ(コーニング、米国)に播種した。培養は37℃,5%CO2気相条件で行った。以後4日毎に培地交換を行った。増殖した細胞がコンフルエントに達する直前に、0.05% トリプシン(ディフコ、米国)、0.02% EDTA(片山化学、大阪)、100 units/mlのペニシリン,100 μg/mlのストレプトマイシンを含むリン酸緩衝生理食塩液(PBS,日水製薬,東京)を用いて細胞を分散させた。分散させた細胞は20% FCS、10%のジメチルスルホキシド(DMSO,片山化学,大阪)、100 units/mlのペニシリン、100 μg/mlのストレプトマイシンを含むDMEMに、細胞密度が1.0 x 106細胞/mlとなるよう懸濁し、セラムチューブ(住友ベークライト,東京)に1 mlずつ分注した後に−20℃で2時間、−80℃で通夜冷却した後に、液体窒素中に保存した。
【0098】
(2)HMS細胞における骨関連タンパク質のmRNAの発現
(i) 細胞のNGF、BDNF、NT-3での処理
上記(1)で得られたHMS細胞を、10%FCSを含むDMEM(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に懸濁し、1.0 x 105 細胞/ウエルの密度で6穴細胞培養プレートに播種した。細胞を1週間培養し、細胞がコンフルエントになる直前の時点で培地をFCSを含まないDMEM(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に交換し、NGF、BDNF、NT-3のいずれかをそれぞれ100 ng/mlの濃度で12時間および24時間作用させた。培養終了後,ISOGEN(商品名)を用いて総RNAの抽出を行った。
【0099】
(ii) mRNAの発現
ALPase、OCN、OPN、骨シアロタンパク(BSP)、I型コラーゲンに特異的なプライマーを用いてPCRを行った。PCR反応は、94℃で2分間変性を行った後、94℃、15秒間、アニーリング30秒間、72℃、50秒間を30サイクル(BSPのみ35サイクル)繰り返し、その後72℃、7分間の伸長によって行った。得られたPCR産物は0.002%臭化エチジウムを含む2%アガロースゲルを用いて電気泳動を行った。電気泳動後のバンドの濃さをNIH imageを用いて測定した。
【0100】
結果を図25A〜E、26A〜E27および27A〜Eに示す。図から明らかなように、NGFについては、HMS細胞のALPase、OCN、OPN、BSP、I型コラーゲンのいずれのmRNA発現に対しても著明な作用は認められなかった。BDNFは、ALPase、OPN、BSP、BMP-2のmRNA発現を強く促進させ、OCNの遺伝子発現をいくらか促進させた。NT-3は、ALPaseおよびI型コラーゲンのmRNA発現を促進させた。
【0101】
(3)HMS細胞の増殖に及ぼすアスコルビン酸、NGF、BDNF、NT-3の影響
上記(1)で得られたHMS細胞を、10%FCSを含むDMEM(日水製薬製)(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に懸濁し、96穴細胞培養プレート(コーニング、米国)上に5.0 x 103細胞/ウエルの密度で播種した。試験群については、培養開始24時間後から50 μg/mlのアスコルビン酸(シグマ、米国)、100 ng/mlのNGF(フナコシ,東京)、100 ng/mlのBDNF(フナコシ,東京)、あるいは100 ng/mlのNT-3(フナコシ、東京)をそれぞれ単独で培地に添加し、さらに7日間培養した。培地交換は4日目に行った。対照群は10%FCSを含むDMEM(日水製薬製です)(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)で培養したものとした。7日間培養後、培地を全て10%FCS を含むDMEM(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に交換し、CellTiter 96(商品名)AQueous One Solution Cell Proliferation Assay Kit(Promega、米国)を用いて490 nmにおける吸光度を測定することにより、生細胞数を計測した。
【0102】
結果を図28に示す。グラフの縦軸は、対照群に対する試験群の吸光度の百分率を示す。*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。図から明らかなように、アスコルビン酸、NGF、BDNF、NT-3のいずれかを添加した培地で培養したHMS細胞は、コントロールと比べて有意に高い細胞増殖を示した。特に、アスコルビン酸、BDNF、NT-3の増殖促進作用はNGFに比べ強かった。
【実施例8】
【0103】
ビーグル犬の3級根分岐部病変モデルにおけるNGFとNT-3の効果を検討した。
直径8mm×5mmのテルプラグに、濃度5、25、50μg/mlのBDNF溶液(滅菌生理食塩液中)の25μlの代わりに濃度100μg/mlのNGF溶液(滅菌生理食塩液中)の25μlをしみこませたものと、濃度100μg/mlのNT-3溶液(滅菌生理食塩液中)の25μlをしみこませたものを、移植材として用いたこと以外は、実施例2と同様に実験を行った。作成した組織標本(ヘマトキシリン・エオジン染色)から、近遠心方向歯軸に平行でしかも根中央付近で薄切された標本を選択し、光学顕微鏡(ECLIPSE E600、NIKON)で観察した。
【0104】
図29AはNGFを含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像であり、図29Bは、NT-3を含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像である(倍率20倍)。図から明らかなように、NGFあるいはNT-3の投与により、イヌの3級根分岐部病変モデルにおいて再生骨が観察された。
【産業上の利用可能性】
【0105】
本発明の歯周病治療剤、修復象牙質形成促進剤、治療方法、歯周組織再生用移植材、歯周組織の再生方法は、歯周病治療や歯内療法において有効と成り得る可能性がある。
【技術分野】
【0001】
本発明は、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法に関するものである。
【背景技術】
【0002】
歯肉、歯槽骨、歯周靱帯(歯根膜)、セメント質、歯髄等で構成される歯周組織は、歯牙を植立させ、咀嚼や咬合等の機能を維持させるための重要な組織であり、その損傷や破壊は歯の喪失につながる。例えば、日本国内に約3000万人の患者が存在するといわれる歯周病においては、病気の進行と共に歯周組織の損傷や破壊が進み、歯を喪失する大きな原因となっている。損傷あるいは破壊された歯髄を含む歯周組織の治療には、医薬品投与や外科手術等、様々な方法が試みられているが、いずれの薬剤や治療方法も、損傷あるいは破壊された歯髄を含む歯周組織を再生させる効果は十分とはいえない。
【0003】
神経栄養因子には脳由来神経栄養因子(Brain-derived neurotrophic factor、BDNF)、神経成長因子(Nerve growth factor、NGF)、ニューロトロフィン3(Neurotrophin 3、NT-3)、およびニューロトロフィン4/5(Neurotrophin 4/5、NT-4/5)があり、神経細胞の分化促進や生存維持、再生促進、機能維持に関与する。BDNFとNT-4/5はTrkB(tropomyosin receptor kinase B)、NGFはTrkA、NT-3はTrkCという高親和性レセプターに特異的に結合する。
【0004】
BDNF、NGF、NT-3は、主として脳内に存在する神経栄養因子であり、BDNFとNGFは運動神経障害モデル、パーキンソン病モデル、アルツハイマー病モデルなど、各種の疾患モデル動物を用いた実験で、有効性が証明されている。中でも、BDNFは、運動・末梢神経疾患として筋萎縮性側索硬化症(ALS)、糖尿病や化学療法剤による末梢神経障害など、また中枢神経系疾患としてアルツハイマー病、パーキンソン病、網膜関連疾患などの治療薬としての開発が期待されている。
【0005】
これらの神経栄養因子は、中枢神経系のみならず末梢神経系においても重要な役割を果たしていると言われている。マウス肋骨の骨折治癒過程においてBDNF、NGF、NT-3、TrkC、TrkAの発現が増加した(K. Asaumiら、Bone Vol 26, No.6, 625-633, 2000)、BDNF、NGF、NT-3がマウス歯周靱帯細胞の増殖を促進した(Y. Tsuboiら、J Dent Res 80, (3), 881-886, 2001)等の報告もある。しかし、歯周組織や歯髄組織におけるこれらの神経栄養因子の働きについての詳しい報告はない。
【先行技術文献】
【非特許文献】
【0006】
【非特許文献1】K. Asaumiら、Bone Vol 26, No.6, 625-633, 2000
【非特許文献2】Y. Tsuboiら、J Dent Res 80, (3), 881-886, 2001
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明の目的は、歯周病や歯髄疾患の治療剤と治療方法、歯周組織再生用移植材、歯周組織の再生方法を提供することである。
【課題を解決するための手段】
【0008】
本発明者らは、上記課題を解決するために鋭意研究した結果、神経栄養因子が、ヒト歯周靱帯由来線維芽細胞の増殖を促進し、骨関連タンパク質のmRNA発現を促進すること、イヌの根分岐部病変モデルにおいて歯周組織の再生を促進することを知得し、本発明を完成するに至った。
【0009】
すなわち、本発明によれば、神経栄養因子を有効成分とする、歯周病の治療剤が提供される。
本発明の治療剤が、歯周組織を再生させることが好ましい。
【0010】
本発明の治療剤が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
本発明の治療剤が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
【0011】
本発明の治療剤が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。
本発明の治療剤において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
【0012】
本発明の別の側面によれば、神経栄養因子を含有する歯周組織再生用移植材が提供される。
本発明の移植材が、歯周組織を再生させることが好ましい。
【0013】
本発明の移植材が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
本発明の移植材が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
【0014】
本発明の移植材が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。
本発明の移植材において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
【0015】
本発明のさらに別の側面によれば、神経栄養因子を使用する歯周組織の再生方法が提供される。
本発明の再生方法が、歯周組織を再生させることが好ましい。
【0016】
本発明の再生方法が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
本発明の再生方法が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
【0017】
本発明の再生方法において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
本発明の別の側面によれば、歯周病の治療方法であって、そうした状態に罹患しているまたは罹患しやすい対象に治療有効量の神経栄養因子を投与することを含む、歯周病の治療法が提供される。
【0018】
本発明の治療法が、歯周組織を再生させることが好ましい。
本発明の治療法が、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。
【0019】
本発明の治療法が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。
本発明の治療法が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。
【0020】
本発明の治療法において、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
本発明のさらに別の側面によれば、歯周病の治療に使用する薬剤を製造するための神経栄養因子の使用が提供される。
【0021】
この薬剤が、歯周組織を再生させることが好ましく、セメント質、歯周靭帯、歯槽骨または歯髄を再生させることが好ましい。この薬剤が、歯肉上皮の歯根面根尖方向への進入を防止することが好ましい。この薬剤が、歯髄腔における修復象牙質の産生を促進することが好ましい。また、歯髄腔内壁への修復象牙質の添加を促進することが好ましい。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。
【0022】
本発明のさらに別の側面によれば、神経栄養因子を有効成分とする、修復象牙質の形成促進剤が提供される。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。修復象牙質が歯髄腔の内壁に添加されることが好ましい。
【0023】
本発明の別の側面によれば、歯髄疾患の治療方法であって、そうした疾患に罹患しているまたは罹患しやすい対象に、修復象牙質の形成を促進するために治療有効量の神経栄養因子を投与することを含む、歯髄疾患の治療法が提供される。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。修復象牙質が歯髄腔の内壁へ添加されることが好ましい。
【0024】
本発明のさらに別の側面によれば、修復象牙質の形成を促進するために使用する薬剤を製造するための神経栄養因子の使用が提供される。神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であることが好ましい。修復象牙質が歯髄腔の内壁へ添加されることが好ましい。
【図面の簡単な説明】
【0025】
【図1】HPL細胞およびヒト歯周靭帯における、BDNFとTrkBとのmRNA発現を示す電気泳動図である。各電気泳動図の、左端のレーンはマーカーである。(A)は、ヒト歯周靭帯およびHPL 細胞におけるグリセルアルデヒド-3-リン酸脱水素酵素(GAPDH)のmRNA(613bp)の発現を示す。(B)は、ヒト歯周靭帯におけるBDNFのmRNA(438bp)とTrkBのmRNA(434bp)の発現を示す。(C)は、HPL 細胞におけるBDNFとTrkBとのmRNA発現を示す。
【図2A】HPL 細胞における、BDNFの作用時間とALPaseのmRNA(381bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を1としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図2B】HPL 細胞における、BDNFの作用時間とOPNのmRNA(532bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を1としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図2C】HPL 細胞における、BDNFの作用時間と、BMP-2のmRNA(440bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を1としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図2D】HPL 細胞における、BDNFの作用時間とGAPDHのmRNAの発現量との関係を示す電気泳動図である。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。
【図3A】HPL 細胞における、BDNFの作用時間とBMP-4のmRNA(339bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図3B】HPL 細胞における、BDNFの作用時間とOPGのmRNA(736bp)の発現量との関係を示す電気泳動図とグラフである。HPL 細胞は、すべて最終濃度50ng/mlのBDNFで処理した。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図4A】HPL 細胞における、BDNFの投与量とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。各濃度のBDNFを、HPL 細胞に24時間作用させた。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF投与量0のときのmRNA発現量を1とした場合の、各投与量におけるmRNAの発現量の割合を示す。横軸は、BDNFの濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図4B】HPL 細胞における、BDNFの投与量とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。各濃度のBDNFを、HPL 細胞に12時間作用させた。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF投与量0のときのmRNA発現量を1とした場合の、各投与量におけるmRNAの発現量の割合を示す。横軸は、BDNFの濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図4C】HPL 細胞における、BDNFの投与量とBMP-2のmRNAの発現量との関係を示す電気泳動図とグラフである。各濃度のBDNFを、HPL 細胞に24時間作用させた。電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF投与量0のときのmRNA発現量を1とした場合の、各投与量におけるmRNAの発現量の割合を示す。横軸は、BDNFの濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。
【図4D】HPL 細胞における、BDNFの投与量とGAPDHのmRNA(613bp)発現量との関係を示す電気泳動図である。
【図5】(A)は、HPL 細胞における、BDNFの投与量とOPNの分泌量の関係を示すグラフである。各濃度のBDNFを、HPL 細胞に12時間作用させた。縦軸にOPNの分泌量(ng/ml)、横軸にBDNFの濃度(ng/ml)を示す。(B)は、HPL 細胞における、BDNFの投与量とBMP-2の分泌量の関係を示すグラフである。各濃度のBDNFを、HPL 細胞に、24時間作用させた。縦軸にBMP-2の分泌量(pg/ml)、横軸にBDNFの濃度(ng/ml)を示す。(C)は、HPL 細胞における、BDNFの作用時間とBMP-2の分泌量の関係を示すグラフである。細胞は最終濃度50ng/mlのBDNFで処理した。縦軸にBMP-2の分泌量(pg/ml)、横軸にBDNFの作用時間を示す。(A)〜(C)の各棒グラフのバーは、平均値±標準偏差の範囲を表す。**はp<0.01の統計学的有意差を示す(t-test)。
【図6】BDNFの投与量とHPL 細胞およびHGKのDNA合成能との関係を示すグラフである。各濃度のBDNFを、HPL 細胞およびHGKに24時間作用させた。各グラフの縦軸は、BDNFあるいはbFGF非投与(つまりBDNF濃度0あるいはbFGF濃度0)のときのDNA合成能を100としたときの、各投与量におけるDNA合成能の割合を示している。横軸はBDNFまたはbFGF濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。(A)はHPL 細胞におけるDNA合成能を示し、(B)はHGKにおけるDNA合成能を示す。
【図7】(A)は、HPL 細胞における、BDNFの投与量とI型コラーゲンの合成量との関係を示すグラフである。各濃度のBDNFを、HPL 細胞に24時間作用させた。縦軸にI型コラーゲンの合成量(μg/ml)、横軸にBDNFの濃度(ng/ml)を示す。(B)は、HPL 細胞における、BDNFの作用時間とI型コラーゲン合成量の関係を示すグラフである。細胞は最終濃度50ng/mlのBDNFで処理した。縦軸にI型コラーゲン合成量(μg/ml)、横軸にBDNFの作用時間を示す。(A)、(B)の各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。
【図8】イヌの3級根分岐部病変モデルにおける、BDNFの投与量とセメント質および歯槽骨の再生との関係を示すグラフである。縦軸にセメント質再生率(%)または骨再生率(%)を示し、横軸にBDNFの濃度(μg/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01の統計学的有意差を示す(t-test)。(A)はセメント質再生率との関係を示し、(B)は骨再生率との関係を示す。
【図9A】実施例2で作成された、BDNFを含まないテルプラグを填塞した根分岐部骨欠損部位(対照群)のヘマトキシリン・エオジン染色標本の光学顕微鏡像(倍率20倍)である。
【図9B】実施例2で作成された、BDNF(5μg/ml)を含む移植材を填塞した分岐部骨欠損部位の顕微鏡像(倍率20倍)である。
【図10】図9Bの根分岐部直下の部分拡大像である(倍率200倍)。根分岐部直下において、裸出させた歯根面のほとんどの部分でコラーゲン線維を埋入したセメント質が再生しており、上皮の進入も見られなかった。
【図11A】HPL細胞における、NGFのmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量に対するNGFのmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図11B】HPL細胞における、TrkAのmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量に対するTrkAのmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図12】HPL 細胞におけるOPNのmRNA発現量に及ぼす、NGFの影響を示すグラフである。(A)はNGFの経時効果の測定結果を示すグラフであり、グラフ縦軸は、NGF作用時間0におけるmRNA発現量を1としたときの、各作用時間におけるOPNのmRNA発現量の割合を示す。グラフ横軸はNGFの作用時間を示す。すべて最終濃度100ng/mlのNGFで処理した。(B)は濃度効果の測定結果を示すグラフである。グラフ縦軸は、NGF濃度0におけるmRNA発現量を1としたときの、各濃度におけるOPNのmRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。NGFはすべて24時間作用させた。
【図13】HPL 細胞におけるALPaseのmRNA発現量に及ぼす、NGFの影響を示すグラフである。(A)はNGFの経時効果の測定結果を示すグラフであり、グラフ縦軸は、NGF作用時間0におけるALPaseのmRNA発現量を1としたときの、各作用時間におけるALPaseのmRNA発現量の割合を示す。グラフ横軸はNGFの作用時間を示す。(B)は濃度効果の測定結果を示すグラフである。グラフ縦軸は、NGF濃度0におけるALPaseのmRNA発現量を1としたときの、各濃度におけるALPaseのmRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。
【図14】HPL 細胞におけるBMP-2のmRNA発現量に及ぼす、NGFの影響を示すグラフである。(A)はNGFの経時効果の測定結果を示すグラフであり、グラフ縦軸は、NGF作用時間0におけるBMP-2のmRNA発現量を1としたときの、各作用時間におけるBMP-2のmRNA発現量の割合を示す。グラフ横軸はNGFの作用時間を示す。(B)は濃度効果の測定結果を示すグラフである。グラフ縦軸は、NGF濃度0におけるBMP-2のmRNA発現量を1としたときの、各濃度におけるBMP-2のmRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。
【図15】NGFの投与量とHPL 細胞およびHGKのDNA合成能との関係を示すグラフである。各濃度のNGFを、HPL 細胞およびHGKに24時間作用させた。各グラフの縦軸は、NGF濃度0におけるDNA合成能を100としたときの、NGF各投与量におけるDNA合成能の割合を示している。横軸はNGF濃度(ng/ml)を示す。(A)はHPL 細胞におけるDNA合成能を示し、(B)はHGKにおけるDNA合成能を示す。
【図16A】HPL細胞における、NT-3のmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量を1としたときのNT-3のmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図16B】HPL細胞における、TrkCのmRNA発現量を示す放射活性のバンドとグラフである。グラフ縦軸は、GAPDHのmRNA発現量を1としたときのTrkCのmRNA発現量の割合を示す。グラフ中、HGFは歯肉線維芽細胞、HPCは歯髄細胞、HSFは包皮由来線維芽細胞、HNBはヒト神経芽細胞腫細胞を示す。
【図17】HPL細胞における、NT-3の投与量とALPase活性との関係を示すグラフである。グラフ縦軸はALPase活性(nmol/ウェル)を示し、横軸はNT-3濃度(ng/ml)を示す。
【図18】HPL 細胞における、NT-3の投与量とHPL細胞のDNA合成能との関係を示すグラフである。グラフの縦軸は、NT-3各濃度におけるHPL細胞のDNA合成能を吸光度で比較したものである。横軸はNT-3濃度(ng/ml)を示す。
【図19A】HPL細胞における、NT-4/5の作用時間とOPN、OCNのmRNAの発現量との関係を示す電気泳動図とグラフである。NT-4/5の最終濃度は50ng/mlとした。電気泳動図の左端のレーンはマーカーである。各グラフ縦軸は、NT-4/5の作用時間0のときの各mRNA発現量を100としたときの、各作用時間における各mRNAの発現量の割合を示す。横軸は、NT-4/5の作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【図19B】HPL細胞における、NT-4/5の作用時間とBMP-2、BMP-7のmRNAの発現量との関係を示す電気泳動図とグラフである。NT-4/5の最終濃度は50ng/mlとした。電気泳動図の左端のレーンはマーカーである。各グラフ縦軸は、NT-4/5の作用時間0のときの各mRNA発現量を100としたときの、各作用時間における各mRNAの発現量の割合を示す。横軸は、NT-4/5の作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【図19C】HPL 細胞におけるNT-4/5の作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフ、およびNT-4/5の作用時間とGAPDHの発現量との関係を示す電気泳動図である。NT-4/5の最終濃度は50ng/mlとした。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-4/5の作用時間0のときのmRNA発現量を100としたときの、各作用時間におけるmRNAの発現量の割合を示す。横軸は、NT-4/5の作用時間を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05を表す(統計学的検定はt-testによる)。
【図20】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、OPN、OCN)のmRNA発現に対する、NGFの濃度効果の測定結果を示すグラフである。NGFの作用時間は24時間である。各グラフ縦軸は、NGF濃度0におけるmRNA発現量を1としたときの、各濃度における各mRNA発現量の割合を示す。横軸はNGF濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図21】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、I型コラーゲン、OPN、OCN)のmRNA発現に対する、BDNFの濃度効果の測定結果を示すグラフである。各グラフ縦軸は、BDNF濃度0における各mRNA発現量を1としたときの、各濃度におけるmRNA発現量の割合を示す。横軸はBDNF濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図22】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、OPN、OCN)のmRNA発現に対する、NT-3の濃度効果の測定結果を示すグラフである。各グラフ縦軸は、NT-3濃度0におけるmRNA発現量を1としたときの、各濃度における各mRNA発現量の割合を示す。横軸はNT-3濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図23】HP 細胞の各骨関連タンパク質(ALPase、BMP-2、DSPP、I型コラーゲン、OPN、OCN)のmRNA発現に対する、NT-4/5の濃度効果の測定結果を示すグラフである。各グラフ縦軸は、NT-4/5濃度0におけるmRNA発現量を1としたときの、各濃度における各mRNA発現量の割合を示す。横軸はNT-4/5濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図24】各神経栄養因子(NGF、BDNF、NT-3、NT-4/5)の投与量とHP 細胞のDNA合成能との関係を示すグラフである。各濃度の神経栄養因子を、HP 細胞に24時間作用させた。各グラフの縦軸は、神経栄養因子非投与(つまり神経栄養因子の濃度0)のときの吸光度を100としたときの、各投与量における吸光度の割合を示している。横軸は各神経栄養因子の濃度(ng/ml)を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。
【図25A】HMS 細胞における、NGFの作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。コントロールであるGAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25B】HMS 細胞における、NGFの作用時間とOCNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25C】HMS 細胞における、NGFの作用時間とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25D】HMS 細胞における、NGFの作用時間とBSPのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図25E】HMS 細胞における、NGFの作用時間とI型コラーゲンのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNGFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NGF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NGFの作用時間を示す。
【図26A】HMS 細胞における、BDNFの作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26B】HMS 細胞における、BDNFの作用時間とOCNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26C】HMS 細胞における、BDNFの作用時間とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26D】HMS 細胞における、BDNFの作用時間とBSPのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図26E】HMS 細胞における、BDNFの作用時間とI型コラーゲンのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのBDNFで処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、BDNF作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、BDNFの作用時間を示す。
【図27A】HMS 細胞における、NT-3の作用時間とALPaseのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27B】HMS 細胞における、NT-3の作用時間とOCNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27C】HMS 細胞における、NT-3の作用時間とOPNのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27D】HMS 細胞における、NT-3の作用時間とBSPのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図27E】HMS 細胞における、NT-3の作用時間とI型コラーゲンのmRNAの発現量との関係を示す電気泳動図とグラフである。GAPDHのmRNAの発現量との関係を示す電気泳動図も示す。HMS 細胞は、すべて最終濃度100 ng/mlのNT-3で処理した。各電気泳動図の左端のレーンはマーカーである。グラフ縦軸は、NT-3作用時間0のmRNA発現量を100%としたときの、各作用時間におけるmRNAの発現量の百分率を示す。横軸は、NT-3の作用時間を示す。
【図28】HMS細胞の増殖に及ぼすアスコルビン酸(Aa)、NGF、BDNF、NT-3の効果を示すグラフである。グラフの縦軸は、対照群に対する試験群の吸光度の百分率を示す。各棒グラフのバーは、平均値±標準偏差の範囲を表す。*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【図29A】実施例8で作成された、NGF(100μg/ml)を含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像(倍率20倍)である。
【図29B】実施例8で作成された、NT-3(100μg/ml)を含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像(倍率20倍)である。
【発明を実施するための形態】
【0026】
以下、本発明のより具体的な態様、並びに本発明を実施するための方法につき説明する。
本明細書において「歯周組織」とは、歯肉、歯槽骨、歯周靱帯(歯根膜)、セメント質で構成される組織を意味する。
【0027】
「歯肉」とは、歯頚部と歯槽骨の一部を被覆している軟組織で、歯肉上皮と歯肉固有層とからなる。
「歯周靭帯」とは、歯槽骨とセメント質の間に介在している結合組織のことであり、歯根膜とも呼ばれる。
【0028】
「歯槽骨」は、歯根を取り巻いている歯槽壁の緻密質の部分に相当する固有歯槽骨と、さらにその外側に位置する海綿質と緻密質の部分からなる支持歯槽骨とに区分される。
「セメント質」は、歯根の最表層の硬組織であり、セメント細胞を有する有細胞性セメント質とセメント細胞を有さない無細胞性セメント質とに区分される。
【0029】
「歯髄」は、歯の生活反応を司る組織で、生理的、病的刺激に反応して、象牙質を形成する。歯髄細胞、神経線維、細胞外基質、血管などから構成される。
「再生(regeneration)」とは、喪失組織、破壊された組織や損傷組織の再構成(reconstruction)および再構築(reproduction)のことであり、「歯周組織の再生」とは、歯周組織を元の状態に回復させ機能させることである。
【0030】
「修復(repair)」とは、創傷部の構造と機能がいまだ完全な状態では回復していない組織の治癒のことであり、「歯周組織の修復」には、歯根表面への上皮性付着などが含まれる。
【0031】
「歯肉上皮の歯根面根尖方向への進入を防止する」とは、歯肉上皮細胞が歯根面に沿って根尖側に向かって増殖していくことを防ぐことを意味する。
「歯周組織再生用移植材」とは、歯周組織の再生を促す材料のことである。BDNF等の神経栄養因子を所定の生体部位(歯槽骨の欠損部位など)に一定の濃度で作用させるためには、何らかの足場(scaffold)が必要である。こうした足場となる材料とBDNF等の神経栄養因子を組合わせたものが本願の移植材である。
【0032】
「歯周病」とは、局所の細菌等を原因として起こる歯周組織の炎症性疾患を意味する。
「修復象牙質」とは、外来刺激を受けた結果形成された象牙質を意味する。
「歯髄疾患」とは、歯髄の炎症性疾患、退行変性などを意味する。
【0033】
本発明は、ヒトなどの温血動物において、特に好ましくはヒトに適用される。
本発明に使用する神経栄養因子、BDNF、NGF、NT-3、NT-4/5等は、遺伝子組換えや化学合成などで人工的に製造したものでも天然型(native)でもよい。
【0034】
本発明の歯周病治療剤は、外用剤などによる局所投与が好ましい。シリンジ等に充填し、歯周ポケット内に注入してもよい。また、歯周外科治療の際に、歯周組織の欠損部に投与することも可能である。その場合には、長時間一定の濃度で作用させるために、本発明の治療剤をシートやスポンジなどに吸収させて使用することも好ましい。感染した歯周組織を除去してから投与することが好ましい。本発明の治療剤は注射により局所投与することも可能である。例えば、歯周ポケット部の歯肉に注射してもよいし、歯槽骨頂付近の歯根膜腔に注射してもよい。根尖部付近に注射してもよい。
【0035】
本発明の修復象牙質形成促進剤は、外用剤などによる局所投与が好ましい。例えば、露髄部に、液状、クリーム状、ペースト状などの修復象牙質形成促進剤を適用しても良いし、断髄や抜髄に適用しても良い。活性成分を吸収させたシートやスポンジを適用し、一定期間仮封しても良い。あるいは外傷等で脱落した歯牙を再植する際に根尖部等に適用しても良い。
【0036】
本発明の歯周病治療剤と修復象牙質形成促進剤の剤型としては、通常の製剤方法により、製剤的に許容しうる担体または希釈剤などを使用して製造されるクリーム剤、軟膏剤、ローション剤等の外用剤の他、例えば水系の溶剤を主成分とした注射剤などが挙げられる。粉末状の剤型として、使用直前に精製水などの溶解液に溶解して使用することも可能である。
【0037】
本発明の歯周病治療剤と修復象牙質形成促進剤の投与量は、投与対象の年齢、性別、症状等により異なるが、局所投与においては、通常1歯あたり、神経栄養因子として1×10−12g〜1×10−3 g、特に1×10−11g〜1×10−7 g、さらに特に1×10−10g〜1×10−8 gであることが好ましい。一般に、注射で局所投与する場合は外用薬よりも少ない投与量でよい。
【0038】
本発明の移植材は、1つの根分岐部欠損に使用する量あたり、1×10−12g〜1×10−3 g、特に1×10−11g〜1×10−8 g、さらに特に1×10−10g〜1×10−9 gの神経栄養因子を含むことが好ましい。
【0039】
本発明の歯周病治療剤、修復象牙質形成促進剤や移植材は、その有効性を妨げない限り、他の薬剤と組合わせて使用してもよい。BDNF、NGF、NT-3、NT-4/5を互いに組合わせて使用してもよい。骨髄由来間葉系幹細胞(MSC)、歯周靱帯由来線維芽細胞、歯肉線維芽細胞、血管内皮細胞等と組み合わせて使用してもよい。水酸化カルシウム製剤、抗菌剤などと併用してもよい。
【0040】
本発明の移植材において神経栄養因子と組合わせる材料としては、神経栄養因子を投与局所に維持できる生体為害性のない材料であればよいが、例えば、多孔性のシートやスポンジなどが好ましい。生体分解性タンパク材料(コラーゲン、ゼラチン、アルブミン、プレートレット・リッチ・プラズマ(PRP))や組織吸収性材料(ポリグリコール酸(PGA)、ポリ乳酸(PLA)、乳酸グリコール酸共重合体(PLGA)、ヒアルロン酸(HA)、三リン酸カルシウム(TPC))であれば、後に摘出する必要がないためさらに好ましい。例えば、テルプラグ(商品名)(テルモ株式会社)、ジーシーメンブレン(商品名)(株式会社ジーシー)、オスフェリオン(商品名)(オリンパス株式会社)等がある。
【0041】
以下の実施例により本発明をさらに詳細に説明する。
【実施例1】
【0042】
ヒト歯周靱帯由来線維芽細胞(human periodontal ligament cell、HPL 細胞)およびヒト歯肉上皮細胞(human gingival keratinocyte、HGK)に及ぼすBDNFの影響を検討した。
(1)使用細胞
(i) ヒト歯周靱帯由来線維芽細胞(HPL 細胞)
矯正治療のために便宜的に抜歯された健全なヒト小臼歯の歯周靭帯から、HPL 細胞を分離した。歯周靭帯周囲の他の結合組織からの細胞の混入を防ぐため、抜去ヒト小臼歯の歯頚部、根尖部を除く歯根中央部の健康な歯周靭帯を、メスを用いて剥離し、細切した。細切した組織を、直径60mmの細胞培養用シャーレ(CORNING、NY)に貼り付け、37℃、5%CO2気相条件で培養した。培地は、10%FBS(GIBCO、Buffalo、NY)、ペニシリン(100ユニット/ml)(明治製菓、東京)、ストレプトマイシン(100μg/ml)(明治製菓)、およびアンホテリシンB(1μg/ml)(GIBCO)を添加したダルベッコ変法イーグル培地(DMEM、日水製薬、東京)を使用した(ここで使用した培地を「培地A」と記す)。4〜8代継代したHPL 細胞を以下の実験に供した。
【0043】
(ii) ヒト歯肉上皮細胞(HGK)
ヒト培養細胞を用いた実験の必要性および歯肉の使用目的などを患者に十分説明し、患者の同意を得た後に、歯肉の提供を受けた。智歯周囲炎の患者から、原因となった智歯を抜歯する際に、余剰の歯肉弁から歯肉片を獲得した。得られた歯肉片を、4℃で一昼夜、0.01%エチレンジアミン4酢酸(EDTA)と0.025%トリプシンを含むダルベッコPBS(−)(PBS(−),日水製薬)で処理して、HGKを分離した。ウシインシュリン(10μg/ml)(Sigma、St. Rouis, MO, USA)、ヒトトランスフェリン(5μg/ml)(Sigma)、2-メルカプトエタノール(10μM)、2-アミノエタノール(10μM)、亜セレン酸ナトリウム(10μM)、牛下垂体抽出液(50μg/ml)、ペニシリン(100ユニット/ml)、ストレプトマイシン(100μg/ml)およびアンホテリシンB(50ng/ml)を含むMCDB153培地(Sigma)で初代培養を行った(ここで使用した培地を「培地C」と記す)。培養は、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1、住友ベークライト、東京)を用いて、37℃、5%CO2気相条件で行った。3〜4代継代したHGKを以下の実験に供した。
【0044】
(2)HPL細胞におけるBDNFとそのレセプターの発現
HPL細胞およびヒト歯周靭帯におけるBDNFとTrkBのmRNA発現を、1st Strand cDNA Synthesis Kit for RT-PCR(Roche、Indianapolis)を使用して、逆転写PCR法で調べた。
【0045】
上記(1)(i)で得られたHPL 細胞がコンフルエントになった時点で細胞を回収し、ISOGEN(ニッポンジーン、東京)にて細胞を溶解させた後、クロロホルムを加えて遠心分離し、得られた水相にイソプロパノールを加えて総RNAを抽出した。
【0046】
上記(1)(i)で得られたヒト歯周靭帯をISOGEN中でホモジナイズした後、クロロホルムを加えて遠心分離し、得られた水相にイソプロパノールを加えて総RNAを抽出した。
精製した総RNAのうち1μgの各RNAを、オリゴdTプライマ−を用いて逆転写し、得られたcDNAをPCR反応30サイクルにて増幅させた後、1.5%アガロースゲルに泳動した。コントロールとしてはグリセルアルデヒド-3-リン酸脱水素酵素(GAPDH)を使用した。
【0047】
結果を図1に示す。コントロールとしてはグリセルアルデヒド-3-リン酸脱水素酵素(GAPDH)を使用した。図から明らかなように、ヒト歯周靭帯においてBDNFとTrkBのmRNAの発現がみられ、そのヒト歯周靱帯より分離、培養したHPL 細胞においても、BDNFとTrkBのmRNAが発現していることが確認された。
【0048】
(3)細胞のBDNFでの処理
(i) HPL 細胞
上記(1)(i)で得られたHPL 細胞を、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1)に、1シャーレあたり3.5×105個で、50μg/mlのL-アスコルビン酸を含む培地Aを用いて、37℃、5%CO2気相条件で13日間培養した(ここで使用した培地を「培地B」と記す)。培地は2日に1回交換した。14日目の培養終了前0、3、6、12または24時間において、細胞をDMEMで2回洗浄し、最終濃度0、1、10、50または100ng/mlのBDNF(Recombinant Human BDNF、R & D system、Minneapolis、 USA)を含む無血清培地(ペニシリン(100ユニット/ml)、ストレプトマイシン(100μg/ml)、アンホテリシンB(1μg/ml)(GIBCO)、およびL-アスコルビン酸(50μg/ml)を添加したDMEM)(ここで使用した培地を「培地D」と記す)に交換した。
【0049】
(ii) HGK
上記(1)(ii)で得られたHGKを、ウシI型コラーゲンがコートされた96穴プレート(SUMILON セルタイトC-1プレート96F、住友ベークライト)に、2×103個/ウェルで接種し、37℃、5%CO2気相条件で、培地Cを用いて培養した。培地は2日に1回交換した。細胞増殖期にあたる培養4〜5日目に、プレートの細胞をMCDB153培地で2回洗浄し、最終濃度0、1、10、25、50または100ng/mlのBDNFを含む培地(牛下垂体抽出液を含まないこと以外は培地Cと同一の組成の培地)に交換し、24時間培養した。
【0050】
(4)HPL細胞における骨関連タンパク質の発現
(i) mRNAの発現
上記(3)(i)に記載の方法と同様にして、最終濃度0、1、10、50または100ng/mlのBDNFで処理したHPL 細胞から、ISOGENを用いて総RNAを抽出し、精製した。アルカリホスファターゼ(ALPase)、骨形成タンパク-2(bone morphogenetic protein-2、BMP-2)、骨形成タンパク-4(bone morphogenetic protein-4、BMP-4)、オステオポンチン(osteopontin、OPN)、オステオプロテジェリン(osteoprotegerin、OPG)のmRNA発現量は、ABI PRISM7700 (Applied Biosystems、東京)を用いて、PCRプロダクトの生成過程をリアルタイムでモニタリングし、定量的に解析した(Real-time PCR法)。コントロールとしてはGAPDHを使用した。
【0051】
各骨関連タンパク質のmRNA発現に対する、BDNFの経時効果測定の結果を図2A〜2C、3A、3Bに、濃度効果測定の結果を図4A〜4Cに示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【0052】
これらの図から明らかなように、BDNFはOPG、BMP-4のmRNA発現に影響を及ぼさなかったが、ALPase、BMP-2、OPNのmRNA発現量を濃度および時間依存的に増加させた。
(ii) タンパク質の発現
上記(1)(i)で得られたHPL 細胞を、ウシI型コラーゲンがコートされた48穴プレート(SUMILON セルタイトC-1プレート 48F、住友ベークライト)に、1×104個/ウェルで播種し、培地Bを用いて13日間培養した。培地は2日に1回交換した。14日目の培養終了24時間前に、プレートの細胞をDMEMで2回洗浄し、最終濃度0、1、10、25、50または100ng/mlのBDNFを含む無血清培地Dに交換した。培養終了後に、上清を回収し、上清中の分泌OPN量、分泌BMP-2量を、ELISA法で測定した。分泌OPN量の測定にはサンドイッチELISAキット(IBL、群馬)を、分泌BMP-2量の測定にはサンドイッチELISAキット(R & D system)を使用した。
【0053】
図5に、HPL 細胞の分泌OPN量と分泌BMP-2量に対する、BDNFの経時効果測定および濃度効果測定の結果を示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。図5から明らかなように、BDNFは、HPL細胞におけるOPNとBMP-2の分泌を促進した。
【0054】
(5)HPL細胞とHGKの増殖
HPL細胞とHGKのDNA合成能に及ぼすBDNFの影響を、Cell Proliferation ELISA system, version 2(アマシャムファルマシアバイオテク)を用いて、ELISA法で測定した。
【0055】
上記(1)(i)で得られたHPL細胞を、ウシI型コラーゲンがコートされた96穴プレート(SUMILON セルタイトC-1プレート96F)に、5×103個/ウェルで播種し、培地Bを用いて10日間培養した。細胞をDMEMで2回洗浄し、10%FBSの代わりに0.3%FBSを添加した培地Bで24時間培養した後、同じ培地にBDNFを最終濃度0、1、10、25、50又は100ng/mlとなるように添加して調製した培地と交換し、さらに24時間培養した。培養終了の2時間前(つまりにBDNF添加の22時間後)に、ブロモデオキシウリジン(BrdU)を10ng/mlの濃度で各ウェルに添加して、細胞に取り込ませた。培養は37℃、5%CO2気相条件下で行った。
【0056】
上記(1)(ii)で得られたHGKを、上記(3)(ii)と同一の方法で培養し、BDNFで処理した。培養終了の2時間前(つまりにBDNF添加の22時間後)に、ブロモデオキシウリジン(BrdU)を10ng/mlの濃度で各ウェルに添加して、細胞に取り込ませた。
【0057】
培養終了後、HPL細胞とHGKを固定した後、ブロッキングを行い、ペルオキシダーゼ標識抗BrdU抗体を室温で2時間作用させ、TMB(3,3',5,5'-テトラメチルベンシジン)基質を加え、波長450nmにおける吸光度を吸光度計(MICRO PLATE READER、TOSOH)で測定した。コントロールとして、塩基性線維芽細胞成長因子(bFGF)を最終濃度0、0.3、1、3、5、10ng/mlで24時間作用させた細胞を同様に処理して、DNA合成能を測定した。
【0058】
結果を図6に示す。(A)はHPL細胞に対する効果を示すグラフであり、(B)はHGKに対する効果を示すグラフである。なお、各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。
【0059】
図6から明らかなように、BDNFはHPL細胞のDNA合成能を促進させたのに対し、HGKのDNA合成能には影響を及ぼさなかった。
(6)HPL細胞のコラーゲン合成
上記(1)(i)で得られたHPL細胞をウシI型コラーゲンをコートした48穴プレートに播種し、培地Bを用いて13日間培養した。培地は2日に1回交換した。14日目の培養終了前0、3、6、12または24時間、プレートの細胞をDMEMで2回洗浄し、最終濃度0、1、10、25、50または100ng/mlのBDNFを含む無血清培地Dに交換した。
【0060】
Procollagen type I C-peptide (PIP)EIA kit(TAKARA)を使用して、ELISA法でHPL細胞のコラーゲン合成量を測定した。I型プロコラーゲンC末端プロペプチド(PIP)に特異的なモノクローナル抗体(ペルオキシダーゼ標識)を用いて、HPL細胞培養上清中のコラーゲン合成量を、波長450nmにおける吸光度を吸光度計(MICRO PLATE READER)で測定した。
【0061】
結果を図7に示す。(A)はBDNFのI型コラーゲン合成への濃度効果測定の結果を示し、(B)は経時効果測定の結果を示す。図7から明らかなように、BDNFはHPL細胞のI型コラーゲン合成量を増加させた。
【実施例2】
【0062】
ビーグル犬の3級根分岐部病変モデルにおけるBDNFの効果を検討した。
直径8mm×5mmのテルプラグ(商品名)(テルモ)に、濃度5、25、50μg/mlのBDNF溶液(滅菌生理食塩液中)の25μlをしみこませ、移植材とした。
【0063】
7頭の雌ビーグル犬(12〜20ヵ月齢、体重10〜14kg)を、ドミトール(明治製菓)筋注による鎮静下に、全顎的にハンドスケーラーでスケーリングを行った。以後2日に1回の割合でブラッシングとポビドンヨードを有効成分とする含嗽薬であるイソジン(商品名)(明治製菓)による口腔清掃とを1ヵ月行い、臨床的に健康な歯周組織の状態を確立した。
【0064】
これらのビーグル犬に、ペントバルビタール系麻酔剤の静脈内注射により、全身麻酔を施し、左右両側下顎頬側歯肉に浸潤麻酔を行い、第一小臼歯遠心から第一大臼歯近心にかけての歯肉溝切開を行い、歯肉を剥離し粘膜骨膜弁を形成した。次いで、左右両側第二、第三、第四小臼歯の根分岐部歯槽骨をラウンドバーと骨ノミで削除し、根分岐部3級(Lindhe & Nymanの分類による)の骨欠損を作成した。骨欠損の大きさは、未処置の根分岐部直下から約4mm根尖側寄りまでとした。
【0065】
露出させた歯根面の残存セメント質をハンドスケーラーで除去した後、根分岐部骨欠損内を生理食塩液で十分洗浄して削片を洗い流し、1ヵ所あたり直径8mm×5mmのテルプラグ移植材を填塞した。BDNFを含まない、滅菌生理食塩液25μlのみをしみこませた直径8mm×5mmのテルプラグ移植材を填塞して、コントロールとした。
【0066】
手術6週間後に、ペントバルビタール系麻酔剤の静脈内注射による全身麻酔下で、4%パラホルムアルデヒドで全身を灌流固定した。灌流固定後、下顎を切断し、処理した歯及び歯周組織を一塊として摘出した。得られた標本を、4%パラホルムアルデヒドで1日浸漬固定後、10%EDTAにて脱灰を行い、通法に従いアルコール脱水しパラフィンに包埋した。この標本から、近遠心方向に歯軸と平行な切片(厚さ約5μm)を作製し、ヘマトキシリン・エオジン染色を施した。
【0067】
作成した組織標本のなかで、近遠心方向歯軸に平行でしかも根中央付近で薄切された標本を選択し、光学顕微鏡(ECLIPSE E600、NIKON)で組織観察と計測を行った。骨再生率は、裸出させた根分岐部欠損の面積に対する再生歯槽骨の面積の割合(百分率)として表した。セメント質再生率は、裸出させた歯根面の長さに対する、再生セメント質の長さの割合(百分率)として表した。
【0068】
結果を図8、9A、9B、10に示す。図8の(A)はセメント質再生へのBDNFの効果の測定結果を示し、図8の(B)は歯槽骨再生へのBDNFの効果の測定結果を示す。図9AはBDNF非投与(コントロール)の根分岐部骨欠損部のヘマトキシリン・エオジン染色標本であり、図9Bは、BDNFを投与した(BDNF(5μg/ml)を含む移植材を填塞)根分岐部骨欠損部の光学顕微鏡像である(倍率20倍)。図10は図9Bの根分岐部直下の部分拡大像である(倍率200倍)。
【0069】
図8から明らかなように、BDNFの投与により、イヌの3級根分岐部病変モデルにおいて、セメント質の再生と歯槽骨の再生が認められた。
図9Aのコントロール標本においては、セメント質、歯槽骨、歯周靱帯の再生がいくらか観察されたものの、骨欠損底部から歯冠側方向のほぼ1/2に留まっていた。根分岐部直下の欠損部にはセメント質再生、歯槽骨再生は認められず、上皮の進入も認められ、線維芽細胞、コラーゲン線維、血管を主体とした結合組織で埋めつくされていた。
【0070】
図9Bおよび図10のBDNFを投与した根分岐部骨欠損部の標本では、裸出させた歯根面のほとんどの部分でセメント質が再生しており、上皮の進入も見られなかった。また、再生セメント質と再生歯槽骨の間には一定の幅を維持した歯周靱帯も観察された。
【実施例3】
【0071】
HPL 細胞およびHGKに及ぼすNGFの影響を検討した。
(1)HPL細胞におけるNGFとそのレセプターの発現
上記実施例1(2)と同一の方法でHPL細胞から総RNAを回収し、精製した。得られた総RNAを試料として、NGFとTrkAとのmRNA発現をノーザンブロット法で測定した。コントロールとしてはGAPDHを使用した。
【0072】
結果を図11A、11Bに示す。図11AはNGFのmRNA発現を示し、図11BはTrkAのmRNA発現を示す。図から明らかなように、HPL 細胞においてNGFのmRNAとTrkAのmRNAとが発現していることが確認された。
【0073】
(2)HPL細胞における骨関連タンパク質の発現
HPL 細胞の骨関連タンパク質のmRNA発現に及ぼすNGFの影響を測定した。
HPL 細胞を、最終濃度0、5、10、25、50または100ng/mlのNGF(Recombinant Human NGF、R & D system、Minneapolis、USA)をBDNFの代わりに使用すること以外は、実施例1(4)(i)と同一の方法で処理した。NGF処理したHPL 細胞のALPase、BMP-2、OPNの各mRNA発現量を、実施例1(4)(i)と同一の方法で測定した。
【0074】
図12、13、14に、それぞれ、OPN、ALPase、BMP-2のmRNA発現に対する、NGFの経時効果測定および濃度効果測定の結果を示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す。検定はt-testによる。
【0075】
図12、13、14から明らかなように、NGFは、ALPase、BMP-2、OPNのmRNA発現量を濃度および時間依存的に増加させた。
(3)HPL細胞とHGKの増殖
HPL細胞とHGKのDNA合成能に及ぼすNGFの影響を測定した。
【0076】
HPL細胞とHGKを、最終濃度0、5、10、25、50または100ng/mlのNGFをBDNFの代わりに使用すること以外は、実施例1(5)と同一の方法で処理した。NGF処理したHPL細胞とHGKのDNA合成能を、実施例1(5)と同一の方法で測定した。
【0077】
結果を図15に示す。NGF作用時間はすべて24時間である。(A)はHPL細胞に対する効果を示し、(B)はHGKに対する効果を示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す。検定はt-testによる。
【0078】
図15から明らかなように、NGFはHPL細胞のDNA合成能を促進させたのに対し、HGKのDNA合成能を低下させた。
【実施例4】
【0079】
HPL 細胞およびHGKに及ぼすNT-3の影響を検討した。
(1)HPL細胞におけるNT-3とそのレセプターの発現
上記実施例1(2)と同一の方法でHPL細胞から総RNAを回収し、精製した。得られた総RNAを試料として、NT-3とTrkCのmRNA発現を、ノーザンブロット法で測定した。コントロールとしてはGAPDHを使用した。
【0080】
結果を図16A、16Bに示す。図16AはNT-3のmRNA発現を示し、16BはTrkCのmRNA発現を示す。これらの図から明らかなように、HPL 細胞においてNT-3のmRNAとTrkCのmRNAとが発現していることが確認された。
【0081】
(2)HPL細胞における骨関連タンパク質の発現
HPL 細胞のALPase活性に及ぼすNT-3の影響を測定した。
HPL 細胞を、最終濃度0、1、10または50ng/mlのNT-3(Recombinant Human NT-3、R & D system、Minneapolis、USA)をBDNFの代わりに使用すること以外は実施例1(3)(i)と同一の方法で処理し、そのALPase活性をBessey-Lowry法に従って定量した。すなわち、NT-3処理したHPL 細胞をリン酸緩衝液で3回洗浄し、10mMトリス塩酸緩衝液を加えた後、氷冷下で超音波処理を行い、試料を調製した。p-ニトロフェニルリン酸を基質とするALPase測定キット(和光純業)を使用して、試料中のALPaseの活性を測定した。
【0082】
図17に、ALPase活性に対するNT-3の濃度効果測定の結果を示す。NT-3作用時間はすべて24時間である。図から明らかなように、NT-3は、ALPase活性に対してそれほど影響が見られなかった。
【0083】
(3)HPL細胞の増殖
実施例1(1)と同一の方法で分離したHPL細胞を、最終濃度0、1、5、10、50または100ng/mlのNT-3をBDNFの代わりに使用すること以外は、実施例1(5)と同一の方法で処理し、そのDNA合成能を、実施例1(5)と同一の方法で測定した。
【0084】
結果を図18に示す。NT-3作用時間はすべて24時間である。本グラフにおいて、*はp<0.05、**はp<0.01を表す。検定はt-testによる。図から明らかなように、NT-3はHPL細胞のDNA合成能を促進させた。
【実施例5】
【0085】
ヒト歯周靱帯由来線維芽細胞(human periodontal ligament cell、HPL 細胞)におけるNT-4/5による骨関連タンパク質のmRNA発現を調べた。
(1)HPL細胞のNT-4/5での処理
上記実施例1(1)(i)で得られたHPL細胞を、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1)に、1シャーレあたり3.5×105個で、50μg/mlの培地Bを用いて、37℃、5%CO2気相条件で13日間培養した。培地は2日に1回交換した。14日目の培養終了前0、3、6、12または24時間において、細胞をDMEMで2回洗浄し、最終濃度50ng/mlのNT-4/5(R&D)を含む培地Dに交換した。
【0086】
(2)HPL細胞におけるmRNAの発現
上記(3)(i)に記載の方法と同様にして、最終濃度50ng/mlのNT-4/5で処理したHPL 細胞から、ISOGENを用いて総RNAを抽出し、精製した。ALPase、BMP-2、OPN、オステオカルシン(OCN)、BMP-7、BMP-4、OPGのmRNA発現量は、ABI PRISM7700 (Applied Biosystems、東京)を用いて、PCRプロダクトの生成過程をリアルタイムでモニタリングし、定量的に解析した(Real-time PCR法)。コントロールとしてはGAPDHを使用した。
【0087】
各骨関連タンパク質のmRNA発現に対する、NT-4/5の経時効果測定の結果を図19A、19B、19Cに示す。各グラフにおいて、*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。図から明らかなように、HPL 細胞において、NT-4/5は、OPN、BMP-2、ALPase、OCN、BMP-7のmRNA発現を促進した。しかし、BMP-4、OPGの発現には影響を与えなかった(データは示さず)。
【実施例6】
【0088】
ヒト歯髄細胞(human pulp cell、HP 細胞)に及ぼすNGF、BDNF、NT-3、NT-4/5の影響を検討した。
(1)使用細胞
便宜的歯髄除去時に得られた健全歯髄を細切した。細切した組織を、直径60mmの細胞培養用シャーレ(コーニング、NY)に貼り付け、37℃、5%CO2気相条件で培地Aにて培養した。4〜8代継代したHP細胞を以下の実験に供した。
【0089】
(2)細胞のNGF、BDNF、NT-3、NT-4/5での処理
NGF、BDNF、NT-3またはNT-4/5を培地Dに最終濃度0、5、10、25、50、100ng/mlで加えて、各種濃度の神経栄養因子含有培地を用意した。上記(2)で得られたHP 細胞を、ウシI型コラーゲンがコートされた直径60mmのシャーレ(SUMILON セルタイトC-1)に、1シャーレあたり3.5×105個で、培地Bを用いて、37℃、5%CO2気相条件で13日間培養した。培地は2日に1回交換した。14日目の培養終了前24時間において、細胞をDMEMで2回洗浄し、いずれかの神経栄養因子含有培地に交換した。
【0090】
(3)HP細胞におけるmRNAの発現
上記(1)で、各濃度のNGF、BDNF、NT-3、またはNT-4/5で24時間処理したHP細胞から、ISOGENを用いて総RNAを抽出し、精製した。ALPase、BMP-2、象牙質シアロタンパク(DSPP)、I型コラーゲン(collagen)、OPN、OCNのmRNA発現量は、ABI PRISM7700 (Applied Biosystems、東京)を用いて、PCRプロダクトの生成過程をリアルタイムでモニタリングし、定量的に解析した(Real-time PCR法)。コントロールとしてはGAPDHを使用した。
【0091】
NGF、BDNF、NT-3、NT-4/5の各骨関連タンパク質のmRNA発現に対する濃度効果の測定結果を、それぞれ、図20、21、22、23に示す。図から明らかなように、NGF、BDNF、NT-3、NT-4/5は、HP細胞において、ALPase、BMP-2、DSPP、OPN、OCNのmRNA発現を促進した。BDNFとNT-4/5は、I型コラーゲンのmRNA発現も促進した。
【0092】
(4)HP細胞の増殖
HP細胞のDNA合成能に及ぼすNGF、BDNF、NT-3、NT-4/5の影響を、Cell Proliferation ELISA system, version 2(アマシャムファルマシアバイオテク)を用いて、ELISA法で測定した。
【0093】
NGF、BDNF、NT-3、NT-4/5のそれぞれを、10%FBSの代わりに0.3%FBSを添加した培地Bに、最終濃度0、5、10、25、50又は100ng/mlとなるように添加して、各種神経培養因子含有培地を調製した。
【0094】
上記(1)で得られたHP細胞を、ウシI型コラーゲンがコートされた96穴プレート(SUMILON セルタイトC-1プレート96F)に、5×103個/ウェルで播種し、培地Bを用いて10日間培養した。細胞をDMEMで2回洗浄し、10%FBSの代わりに0.3%FBSを添加した培地Bで24時間培養した後、上記の各種神経培養因子含有培地と交換し、さらに24時間培養した。培養終了の2時間前(つまりに神経培養因子添加の22時間後)に、ブロモデオキシウリジン(BrdU)を10ng/mlの濃度で各ウェルに添加して、細胞に取り込ませた。培養は37℃、5%CO2気相条件下で行った。
【0095】
培養終了後、HP細胞を固定後、ブロッキングを行い、ペルオキシダーゼ標識抗BrdU抗体を室温で2時間作用させ、TMB(3,3',5,5'-テトラメチルベンシジン)基質を加え、波長450nmにおける吸光度を吸光度計(MICRO PLATE READER、TOSOH)で測定した。
【0096】
結果を図24に示す。図から明らかなように、NGF、BDNF、NT-3、NT-4/5はHP細胞のDNA合成能を促進させた。
【実施例7】
【0097】
ヒト間葉系幹細胞(human mesenchymal stem cell、HMS細胞)に及ぼすNGF、BDNF、NT-3、アスコルビン酸の影響を検討した。
(1)使用細胞
HMS細胞の分離は堤ら(S.Tsutsumi:BBRC, 26, 288(2), 2001)の方法に準じて行った。すなわち、十分なインフォームドコンセントを得た患者の智歯抜去時に下顎骨骨髄腔へ穿刺し、骨髄液を得た。得られた骨髄液をヘパリンナトリウム(200 U/ml,シグマ、米国)を含むダルベッコ変法イーグル培地(DMEM、シグマ、米国)と速やかに混合し,遠心分離(150g,5 min)を行った。遠心分離後、上清を除去し、得られた細胞成分を10%のウシ胎児血清(FCS, Biological Industries, イスラエル)、100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含むDMEMに懸濁し、骨髄液が200〜500 μl/dish、培地が10 ml/dishとなるように、直径100 mmの細胞培養用シャーレ(コーニング、米国)に播種した。培養は37℃,5%CO2気相条件で行った。以後4日毎に培地交換を行った。増殖した細胞がコンフルエントに達する直前に、0.05% トリプシン(ディフコ、米国)、0.02% EDTA(片山化学、大阪)、100 units/mlのペニシリン,100 μg/mlのストレプトマイシンを含むリン酸緩衝生理食塩液(PBS,日水製薬,東京)を用いて細胞を分散させた。分散させた細胞は20% FCS、10%のジメチルスルホキシド(DMSO,片山化学,大阪)、100 units/mlのペニシリン、100 μg/mlのストレプトマイシンを含むDMEMに、細胞密度が1.0 x 106細胞/mlとなるよう懸濁し、セラムチューブ(住友ベークライト,東京)に1 mlずつ分注した後に−20℃で2時間、−80℃で通夜冷却した後に、液体窒素中に保存した。
【0098】
(2)HMS細胞における骨関連タンパク質のmRNAの発現
(i) 細胞のNGF、BDNF、NT-3での処理
上記(1)で得られたHMS細胞を、10%FCSを含むDMEM(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に懸濁し、1.0 x 105 細胞/ウエルの密度で6穴細胞培養プレートに播種した。細胞を1週間培養し、細胞がコンフルエントになる直前の時点で培地をFCSを含まないDMEM(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に交換し、NGF、BDNF、NT-3のいずれかをそれぞれ100 ng/mlの濃度で12時間および24時間作用させた。培養終了後,ISOGEN(商品名)を用いて総RNAの抽出を行った。
【0099】
(ii) mRNAの発現
ALPase、OCN、OPN、骨シアロタンパク(BSP)、I型コラーゲンに特異的なプライマーを用いてPCRを行った。PCR反応は、94℃で2分間変性を行った後、94℃、15秒間、アニーリング30秒間、72℃、50秒間を30サイクル(BSPのみ35サイクル)繰り返し、その後72℃、7分間の伸長によって行った。得られたPCR産物は0.002%臭化エチジウムを含む2%アガロースゲルを用いて電気泳動を行った。電気泳動後のバンドの濃さをNIH imageを用いて測定した。
【0100】
結果を図25A〜E、26A〜E27および27A〜Eに示す。図から明らかなように、NGFについては、HMS細胞のALPase、OCN、OPN、BSP、I型コラーゲンのいずれのmRNA発現に対しても著明な作用は認められなかった。BDNFは、ALPase、OPN、BSP、BMP-2のmRNA発現を強く促進させ、OCNの遺伝子発現をいくらか促進させた。NT-3は、ALPaseおよびI型コラーゲンのmRNA発現を促進させた。
【0101】
(3)HMS細胞の増殖に及ぼすアスコルビン酸、NGF、BDNF、NT-3の影響
上記(1)で得られたHMS細胞を、10%FCSを含むDMEM(日水製薬製)(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に懸濁し、96穴細胞培養プレート(コーニング、米国)上に5.0 x 103細胞/ウエルの密度で播種した。試験群については、培養開始24時間後から50 μg/mlのアスコルビン酸(シグマ、米国)、100 ng/mlのNGF(フナコシ,東京)、100 ng/mlのBDNF(フナコシ,東京)、あるいは100 ng/mlのNT-3(フナコシ、東京)をそれぞれ単独で培地に添加し、さらに7日間培養した。培地交換は4日目に行った。対照群は10%FCSを含むDMEM(日水製薬製です)(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)で培養したものとした。7日間培養後、培地を全て10%FCS を含むDMEM(100 units/mlのペニシリン(明治製菓、東京)、100 μg/mlのストレプトマイシン(明治製菓,東京)、1μg/mlのアンホテリシンB(ギブコ、米国)を含む)に交換し、CellTiter 96(商品名)AQueous One Solution Cell Proliferation Assay Kit(Promega、米国)を用いて490 nmにおける吸光度を測定することにより、生細胞数を計測した。
【0102】
結果を図28に示す。グラフの縦軸は、対照群に対する試験群の吸光度の百分率を示す。*はp<0.05、**はp<0.01を表す(統計学的検定はt-testによる)。図から明らかなように、アスコルビン酸、NGF、BDNF、NT-3のいずれかを添加した培地で培養したHMS細胞は、コントロールと比べて有意に高い細胞増殖を示した。特に、アスコルビン酸、BDNF、NT-3の増殖促進作用はNGFに比べ強かった。
【実施例8】
【0103】
ビーグル犬の3級根分岐部病変モデルにおけるNGFとNT-3の効果を検討した。
直径8mm×5mmのテルプラグに、濃度5、25、50μg/mlのBDNF溶液(滅菌生理食塩液中)の25μlの代わりに濃度100μg/mlのNGF溶液(滅菌生理食塩液中)の25μlをしみこませたものと、濃度100μg/mlのNT-3溶液(滅菌生理食塩液中)の25μlをしみこませたものを、移植材として用いたこと以外は、実施例2と同様に実験を行った。作成した組織標本(ヘマトキシリン・エオジン染色)から、近遠心方向歯軸に平行でしかも根中央付近で薄切された標本を選択し、光学顕微鏡(ECLIPSE E600、NIKON)で観察した。
【0104】
図29AはNGFを含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像であり、図29Bは、NT-3を含む移植材を填塞した根分岐部骨欠損部の光学顕微鏡像である(倍率20倍)。図から明らかなように、NGFあるいはNT-3の投与により、イヌの3級根分岐部病変モデルにおいて再生骨が観察された。
【産業上の利用可能性】
【0105】
本発明の歯周病治療剤、修復象牙質形成促進剤、治療方法、歯周組織再生用移植材、歯周組織の再生方法は、歯周病治療や歯内療法において有効と成り得る可能性がある。
【特許請求の範囲】
【請求項1】
神経栄養因子を有効成分とする、歯周病の治療剤であって、神経栄養因子が脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であり、治療剤が歯周組織を再生させることを特徴とする、前記治療剤。
【請求項2】
歯肉上皮の歯根面根尖方向への進入を防止することを特徴とする、請求項1に記載の治療剤。
【請求項3】
セメント質を再生させることを特徴とする、請求項1または2に記載の治療剤。
【請求項4】
歯周靭帯を再生させることを特徴とする、請求項1〜3の何れか1項に記載の治療剤。
【請求項5】
歯槽骨を再生させることを特徴とする、請求項1〜4の何れか1項に記載の治療剤。
【請求項6】
歯髄を再生させることを特徴とする、請求項1〜5の何れか1項に記載の治療剤。
【請求項7】
歯髄腔における修復象牙質の産生を促進することを特徴とする、請求項1〜6の何れか1項に記載の治療剤。
【請求項8】
神経栄養因子が、脳由来神経栄養因子である、請求項1に記載の治療剤。
【請求項9】
神経栄養因子が、神経成長因子である、請求項1に記載の治療剤。
【請求項10】
神経栄養因子が、脳由来神経栄養因子である、請求項6に記載の治療剤。
【請求項11】
神経栄養因子が、神経成長因子である、請求項6に記載の治療剤。
【請求項12】
神経栄養因子が、脳由来神経栄養因子である、請求項2〜5のいずれか1項に記載の治療剤。
【請求項13】
神経栄養因子を含有する歯周組織再生用移植材であって、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5である、前記歯周組織再生用移植材。
【請求項14】
(a) セメント質を再生するため;
(b) 歯槽骨を再生するため;
(c) 歯肉上皮の歯根面根尖方向への進入を防止するため;
(d) 歯髄を再生するため;または
(e) 歯髄腔における修復象牙質の産生を促進するため
に使用する、請求項13に記載の歯周組織再生用移植材。
【請求項15】
歯周靭帯を再生するために使用する、請求項13に記載の歯周組織再生用移植材。
【請求項16】
神経栄養因子が、脳由来神経栄養因子である、請求項13〜15の何れか1項に記載の歯周組織再生用移植材。
【請求項17】
(a) セメント質を再生するため;及び
(b) 歯槽骨を再生するため;及び
(c) 歯肉上皮の歯根面根尖方向への進入を防止するため
に使用する、請求項16に記載の歯周組織再生用移植材。
【請求項18】
神経栄養因子を有効成分とする、修復象牙質の形成促進剤であって、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5である、前記修復象牙質の形成促進剤。
【請求項1】
神経栄養因子を有効成分とする、歯周病の治療剤であって、神経栄養因子が脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5であり、治療剤が歯周組織を再生させることを特徴とする、前記治療剤。
【請求項2】
歯肉上皮の歯根面根尖方向への進入を防止することを特徴とする、請求項1に記載の治療剤。
【請求項3】
セメント質を再生させることを特徴とする、請求項1または2に記載の治療剤。
【請求項4】
歯周靭帯を再生させることを特徴とする、請求項1〜3の何れか1項に記載の治療剤。
【請求項5】
歯槽骨を再生させることを特徴とする、請求項1〜4の何れか1項に記載の治療剤。
【請求項6】
歯髄を再生させることを特徴とする、請求項1〜5の何れか1項に記載の治療剤。
【請求項7】
歯髄腔における修復象牙質の産生を促進することを特徴とする、請求項1〜6の何れか1項に記載の治療剤。
【請求項8】
神経栄養因子が、脳由来神経栄養因子である、請求項1に記載の治療剤。
【請求項9】
神経栄養因子が、神経成長因子である、請求項1に記載の治療剤。
【請求項10】
神経栄養因子が、脳由来神経栄養因子である、請求項6に記載の治療剤。
【請求項11】
神経栄養因子が、神経成長因子である、請求項6に記載の治療剤。
【請求項12】
神経栄養因子が、脳由来神経栄養因子である、請求項2〜5のいずれか1項に記載の治療剤。
【請求項13】
神経栄養因子を含有する歯周組織再生用移植材であって、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5である、前記歯周組織再生用移植材。
【請求項14】
(a) セメント質を再生するため;
(b) 歯槽骨を再生するため;
(c) 歯肉上皮の歯根面根尖方向への進入を防止するため;
(d) 歯髄を再生するため;または
(e) 歯髄腔における修復象牙質の産生を促進するため
に使用する、請求項13に記載の歯周組織再生用移植材。
【請求項15】
歯周靭帯を再生するために使用する、請求項13に記載の歯周組織再生用移植材。
【請求項16】
神経栄養因子が、脳由来神経栄養因子である、請求項13〜15の何れか1項に記載の歯周組織再生用移植材。
【請求項17】
(a) セメント質を再生するため;及び
(b) 歯槽骨を再生するため;及び
(c) 歯肉上皮の歯根面根尖方向への進入を防止するため
に使用する、請求項16に記載の歯周組織再生用移植材。
【請求項18】
神経栄養因子を有効成分とする、修復象牙質の形成促進剤であって、神経栄養因子が、脳由来神経栄養因子、神経成長因子、ニューロトロフィン3、またはニューロトロフィン4/5である、前記修復象牙質の形成促進剤。
【図5】


【図6】


【図7】


【図8】


【図1】


【図2A】


【図2B】


【図2C】


【図2D】


【図3A】


【図3B】


【図4A】


【図4B】


【図4C】


【図4D】


【図9A】


【図9B】


【図10】


【図11A】


【図11B】


【図12】


【図13】


【図14】


【図15】


【図16A】


【図16B】


【図17】


【図18】


【図19A】


【図19B】


【図19C】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25A】


【図25B】


【図25C】


【図25D】


【図25E】


【図26A】


【図26B】


【図26C】


【図26D】


【図26E】


【図27A】


【図27B】


【図27C】


【図27D】


【図27E】


【図28】


【図29A】


【図29B】




【図6】


【図7】


【図8】


【図1】


【図2A】


【図2B】


【図2C】


【図2D】


【図3A】


【図3B】


【図4A】


【図4B】


【図4C】


【図4D】


【図9A】


【図9B】


【図10】


【図11A】


【図11B】


【図12】


【図13】


【図14】


【図15】


【図16A】


【図16B】


【図17】


【図18】


【図19A】


【図19B】


【図19C】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25A】


【図25B】


【図25C】


【図25D】


【図25E】


【図26A】


【図26B】


【図26C】


【図26D】


【図26E】


【図27A】


【図27B】


【図27C】


【図27D】


【図27E】


【図28】


【図29A】


【図29B】


【公開番号】特開2010−215661(P2010−215661A)
【公開日】平成22年9月30日(2010.9.30)
【国際特許分類】
【出願番号】特願2010−143538(P2010−143538)
【出願日】平成22年6月24日(2010.6.24)
【分割の表示】特願2005−513867(P2005−513867)の分割
【原出願日】平成16年9月8日(2004.9.8)
【出願人】(503328193)株式会社ツーセル (24)
【出願人】(503328469)
【Fターム(参考)】
【公開日】平成22年9月30日(2010.9.30)
【国際特許分類】
【出願日】平成22年6月24日(2010.6.24)
【分割の表示】特願2005−513867(P2005−513867)の分割
【原出願日】平成16年9月8日(2004.9.8)
【出願人】(503328193)株式会社ツーセル (24)
【出願人】(503328469)

【Fターム(参考)】
[ Back to top ]

