殺生剤としてのハロゲン化アミドによるバイオフィルムの制御
固着微生物を制御し、水性系または水分含有系からバイオフィルムを除去する方法を提供する。該方法は、系を、有効量の式(I)(式中、X、RおよびR1は本開示で定義する通りである)の化合物で処理することを含む。水性系または水分含有系における微生物を制御する方法は、水性系または水分含有系を、有効量の式(I):(式I)(式中、Xはハロゲンであり;そしてRおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、またはRおよびR1は、それぞれ、水素および式:(式II)のアミド基である)の化合物で処理することを含み、制御される微生物が固着微生物である。


【発明の詳細な説明】
【技術分野】
【0001】
関連出願の相互参照
本件は、米国仮出願整理番号第61/179,161号(2009年5月18日出願)(その全部を参照により本明細書に組入れる)の利益を主張する。
【0002】
発明の分野
本発明は、水性系または水分含有系において、系をハロゲン化アミド殺生剤で処理することによってバイオフィルムを制御する方法に関する。
【背景技術】
【0003】
発明の背景
バイオフィルムは、微生物、水分、栄養、および表面の組合せが存在する殆どのあらゆる環境中で生育する。工業において、バイオフィルムは水系プロセス(例えば水の処理および分配)において生じる。微生物生育によって形成されるバイオフィルムは、設備およびパイプラインの腐食、系の閉塞、製品不良、およびエネルギー損失により、工業における甚大な経済的損失の原因となる。バイオフィルムは、自己成長高分子マトリクス内に被包された構造群を占める微生物の層の蓄積によって形成される。バイオフィルム内の微生物は、固着微生物として公知であり、一方、フリーの浮遊する非バイオフィルム微生物はプランクトン様である。
【0004】
バイオフィルム内での生育により、固着微生物は抗微生物処理に対して、より耐性である。例えば、2,2−ジブロモ−3−ニトリロプロピオンアミド(「DBNPA」)はプランクトン様微生物を殺すのに極めて有効な市販で入手可能な殺生剤である。しかし、バイオフィルム処理に用いる場合、これはそれほど有効ではない。主な原因は、その急速な加水分解、およびその結果の、バイオフィルム内の固着バクテリアとの短い接触時間である。
【0005】
バイオフィルム関連微生物に対する有効性を示す殺生剤は、汚染された表面からバイオフィルムを除去するのに必ずしも有効ではない。バイオフィルムの残余物(例えばエキソ多糖類および死んだバクテリアの細胞)の物理的な存在は、腐食を生じさせる金属表面に対する酸素の一様でない可用性をなお招来する。よって、バイオフィルムを表面から除去することなくバイオフィルム内の微生物を殺すことは、腐食の問題を常に解決できるわけではない。
【0006】
プランクトン様および固着の細胞の両者に対して高い有効性を有し、そして汚染された表面からバイオフィルムを除去する高い能力を有する殺生剤を提供することは工業において大きな利点である。
【発明の概要】
【課題を解決するための手段】
【0007】
発明の簡単な要約
本発明は、水性系または水分含有系における固着微生物およびバイオフィルムを制御する方法を提供する。該方法は、水性系または水分含有系を、有効量の式(I):
【0008】
【化1】

【0009】
(式中、Xはハロゲンであり;そして
RおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、または
RおよびR1は、それぞれ、水素および式:
【0010】
【化2】

【0011】
のアミド基である)
の化合物で処理することを含む。
【図面の簡単な説明】
【0012】
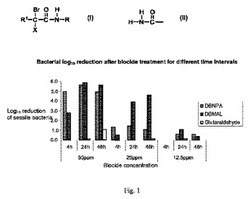
【図1】図1は、種々の時間間隔について殺生剤処理後の生存固着バクテリアの低減を示す棒グラフである。
【図2】図2は、バイオフィルムの除去での殺生剤の有効性を示す棒グラフである。
【発明を実施するための形態】
【0013】
発明の詳細な説明
上記のように、本発明は、水性系または水分含有系におけるバイオフィルムを制御する方法を提供する。該方法は、水性系または水分含有系を有効量の式(I)の化合物で処理することを含む。本発明者らは、驚くべきことに、式(I)の化合物が、固着細胞の制御に有効であることを発見した。加えて、該化合物はまた、水性系または水分含有系において(例えば系において操作する設備表面から)既に形成されたバイオフィルムの除去にも有効である。
【0014】
式(I)の化合物は、以下の化学構造:
【0015】
【化3】

【0016】
(式中、Xは、ハロゲンであり;そしてRおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、または、RおよびR1は、それぞれ、水素および式:
【0017】
【化4】

【0018】
のアミド基である)
を有する。
【0019】
好ましくは、式(I)の化合物中のXは、ブロモ、クロロ、またはヨードであり、より好ましくはブロモである。
【0020】
式(I)の好ましい化合物は、2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミドである。
【0021】
式(I)の更に好ましい化合物は、2,2−ジブロモマロンアミドである。用語「2,2−ジブロモマロンアミド」は、下記式:
【0022】
【化5】

【0023】
の化合物を意味する。
【0024】
式(I)の化合物は、当業者によって、周知の文献の方法を用いて調製できる。
【0025】
バイオフィルムに対するこれらの全体的な有効性に加え、本発明の化合物はまた、驚くべきことに、ほぼ中性〜アルカリ性のpHでの加水分解に対して、他の殺生剤よりも耐性である。例えば、以下の例は、pH6.9で、2,2−ジブロモマロンアミド(DBMAL)、本発明の例の化合物が、特筆すべきことに、DBNPA(比較殺生剤)よりも安定であることを示す。DBMALの損失は、96時間に亘って検出されず、一方84%のDBNPAが、この同じ時間枠にて同一条件で損失する。
【0026】
よって、更なる態様において、式(I)の化合物は、水性系または水分含有系における固着微生物およびバイオフィルムを制御する方法であって水性成分または水分含有成分がpH5以上を有する方法において使用される。幾つかの態様において、pHは6以上である。更なる態様において、pHは7以上である。更なる態様において、pHは8以上である。
【0027】
本発明の化合物で処理できる水性系または水分含有系としては、これらに限定するものではないが、パルプおよび紙の工場、冷却塔操作、熱交換器、金属作動流体、逆浸透水加工、油田およびガス田の注入水、破砕水および生成水、油井およびガス井および貯留槽、脱気塔、油およびガスの操作系および輸送系、油およびガスの分離系および貯蔵タンク、油およびガスのパイプライン、ガス容器、便器、水泳プール、家庭排水、家庭用品表面、プロセス設備、下水道系、廃水および処理系、他の工業プロセス水、ボイラー系、バラスト水、ならびにこれらの系における設備、パイプ、チューブおよび他の表面が挙げられる。好ましい水性系または水分系は、紙およびパルプの工場、冷却塔操作、逆浸透水加工、油田およびガス田の操作系、分離系、輸送系および貯蔵系、パイプライン、ガス容器、金属作動流体ならびに膜系濾過システムである。
【0028】
代表的な膜系濾過システムとしては、1つ以上の半透膜を含むものが挙げられ、これらに限定するものではないが:精密濾過膜、限外濾過膜、ナノ濾過膜、逆浸透膜およびイオン交換膜が挙げられる。適用可能な系としては、単一種の膜を含むもの(例えば、精密濾過)、および複数種の膜を含むもの(例えば、限外濾過および逆浸透)が挙げられる。例えば、膜系濾過システムは、上流の精密濾過膜または限外濾過膜および下流のナノ濾過膜または逆浸透膜を含むことができる。
【0029】
主題の殺生物化合物は、濾過前(例えば、処理されることになる供給物溶液を収容する貯蔵タンクまたは貯蔵池に添加する)、または濾過中(例えば、濾過中に、加圧した供給物溶液中に投入する)に供給物溶液に添加できる。更に、主題の殺生物化合物は、膜に接触する、洗浄溶液または貯蔵溶液に添加できる。この記載の目的のために、系の膜に接触する任意の水性溶液(例えば、原料供給水、洗浄溶液、膜貯蔵溶液等)を「供給物溶液」という。
【0030】
精密濾過膜または限外濾過膜およびナノ濾過膜または逆浸透膜の両者を有する系において使用する場合には、主題の殺生物化合物は、各膜(例えば、上流および下流の膜の両者)に対して殺生物効果を与える。
【0031】
1つまたは複数の膜によって拒絶される殺生物化合物の部分は、後続の処理で用いるために、濃縮物流から回収して再循環させることができる(例えば貯蔵タンクに直接戻すか、または入ってくる供給物中に投入する)。殺生物化合物の再循環は間欠または連続のプロセスの一部であることができる。
【0032】
多くの膜系濾過システムにおいて、供給物溶液のpHは少なくとも7、しばしば少なくとも8、幾つかの態様では少なくとも9、および他の態様では少なくとも10である。このような膜系システムの例は、第US6,537,456号および第US7,442,309号に記載されている。更に、多くの系の膜は、一般的に、pH値が少なくとも11、および幾つかの態様では少なくとも12である供給物溶液で洗浄または貯蔵する。DBNPA(第WO2008/091453号に記載されるような)とは異なり、主題の殺生物化合物は、このような中性およびアルカリ性の条件下で有効であり続ける。結果として、主題の殺生物化合物は、より広い範囲の供給物溶液(例えば、pHが調製された水性供給物、水性洗浄溶液、水性貯蔵溶液)(膜系濾過システムに関して用いるもの)に添加できる。
【0033】
このような系で用いる膜の種類は特に限定されず、フラットシート、チューブ状および中空状の繊維が挙げられる。膜の1つの好ましい分類としては、薄膜コンポジットポリアミド膜(ナノ濾過および逆浸透の用途で一般的に用いるもの)が挙げられる(一般的に、第US4,277,344号;第US2007/0251883号;および第US2008/0185332号に記載される通り)。このようなナノ濾過膜および/または逆浸透膜は、一般的に、らせん巻き構造でのフラットシートとして提供される。精密濾過膜および限外濾過膜の非限定例としては、種々の物質(例えばポリスルホン、ポリエーテルスルホン、ポリアミド、ポリプロピレンおよびポリフッ化ビニリデン)から形成される多孔質膜が挙げられる。このような精密濾過膜および限外濾過膜は、一般的には中空繊維として提供される。
【0034】
当業者は、過度の実験を伴わずに、任意の特定用途において用いるべき式(I)の化合物の有効量を容易に決定できる。例えば、少なくとも1ppm、代替として少なくとも5質量ppm、代替として少なくとも10ppm、または少なくとも50ppmの量が一般的に適切である。幾つかの態様において、該量は、1000ppm以下、代替として500ppm以下、または300ppm以下、または200ppm以下、または100ppm以下である。更なる態様において、該量は約20〜約30ppmである。
【0035】
式(I)の化合物は、水性系または水分含有系において、他の添加剤(例えば、これらに限定するものではないが、界面活性剤、イオン性/非イオン性ポリマー、ならびにスケール防止剤および腐食防止剤、酸素捕捉剤、ならびに/または追加の殺生剤)とともに使用できる。
【0036】
式(I)の化合物は、広範囲の微生物を制御するのに有用である。一態様において、微生物はレジオネラ種のバクテリア(例えばアメーバ内で継代して数が増殖するようなバクテリア)である。このレジオネラ態様に対して好ましい殺生剤は、2,2−ジブロモマロンアミドである。
【0037】
レジオネラバクテリアは、レジオネラ症およびポンティアック熱(包括的にレジオネラ症として知られている)の原因とみなされてきた。レジオネラ症の多くの発生は、感染用量を与える蒸発冷却系に影響してきた。レジオネラは、アメーバ内に寄生して生息するという比較的特異な生存能力を示し、最終的にはその宿主細胞を溶解させ、成熟した感染型として外に出る。この機構は、天然および人工の水系におけるレジオネラ数の増殖およびその増大した毒性の主要な手段として提案されてきた。レジオネラ(例えばアメーバ内で継代することによってより感染性になるレジオネラの型)を有効に制御できる殺生剤が高度に望ましい。例によって示すように、式(I)の化合物,例えば2,2−ジブロモマロンアミドはこのようなバクテリア制御に対して有効である。
【0038】
本開示で記載される化合物は、驚くべきことに、固着/バイオフィルム微生物の制御で、他の殺生剤(例えば市販化合物DBNPA)よりも有効であり、従って工業に大きな利点を与える。
【0039】
本明細書の目的のために、「微生物」はバクテリア、藻類、またはウイルスを意味する。用語「制御」および「制御する」は、固着微生物の生育または増殖を阻害すること、固着微生物を殺すこと、消毒、および/または防腐という、その意味を包含しそれに限定することのないように広く解釈すべきである。「制御」および「制御する」はまた、固着微生物のバイオフィルムの、これが少なくとも部分的に付着いている表面からの部分的または完全な除去を網羅する。
【0040】
「ヒドロキシアルキル」は、アルキル基(すなわち、直鎖および分岐鎖の脂肪族基)であって1〜6個の炭素原子を有し、水酸基で置換されているものを意味する。例としては、これらに限定するものではないが、ヒドロキシメチル、ヒドロキシエチル、2−ヒドロキシプロピル、3−ヒドロキシプロピル等が挙げられる。
【0041】
「ハロゲン」はフルオロ、クロロ、ブロモ、またはヨードを意味する。
【0042】
特記がない限り、本開示で用いる比、パーセント、部等は質量基準である。
【0043】
以下の例は本発明の例示であるがその範囲の限定を意図しない。
【0044】
例
以下の組成物を例において評価する:
2,2−ジブロモ−3−ニトリロプロピオンアミド(「DBNPA」)はThe Dow Chemical Companyから得る。
【0045】
2,2−ジブロモマロンアミド(「DBMAL」)は、Johnson Matheyから得る。
【0046】
グルタルアルデヒドは、The Dow Chemical Companyから得る。
【0047】
CMIT/MIT(5−クロロ−2−メチル−4−イソチアゾリン−3−オンおよび2−メチル−4−イソチアゾリン−3−オン)はThe Dow Chemical Companyから得る。
【0048】
ジオクチルジメチルアンモニウムクロリドは、Lonza Inc.から得る。
【0049】
例1
2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミド(DBCHA)の調製
0.1モルの3−アミノ−1−プロパノール(7.51g)を、0.1モルのメチルシアノアセテート(10.1g)の溶液(メタノール中(40g))に添加する。混合物を撹拌して60℃まで30分間加熱する。メタノール溶媒を反応生成物から減圧ストリップする。反応生成物を、任意の更なる精製を必要とせず、水中に溶解させ、0.1モルの臭素(16.0g)および0.03モルの臭素酸ナトリウム(5.0g)と反応させる。反応温度は30℃未満に保つ。臭素および臭素酸ナトリウムの添加が完了した後、反応混合物を30分間撹拌した後、pH3〜4まで、希薄水酸化ナトリウムで中和する。収量は0.09モルの2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミド(28g)である。
【0050】
例2
加水分解に対する安定性:DBMALおよびDBNPAの比較
希薄溶液(0.5質量%未満)のDBMALおよびDBNPAを3つの異なるpHで調製する。標準緩衝溶液を用いて、pH6.9、8.0および9.0にて、pHを設定および維持する。次いで、これらの溶液を一定温度で、−1℃または30℃のいずれかで保持する。定期的に、分割量をHPLCによって分析して、残存するDBMALまたはDBNPAのレベルを評価する。結果を表1に示す。
【0051】
【表1】

【0052】
表1は、中性近傍条件(pH=6.9)および温度30℃であっても、DBMALが、DBNPA(比較殺生剤)よりも顕著に安定であることを示す。DBMALの損失は、96時間に亘って検出されず、一方84%のDBNPAがこの同じ時間枠にて同じ条件で損失する。
【0053】
例3
バイオフィルム関連バクテリアに対する有効性
P.aeruginosa ATCC 10145のバイオフィルムを、Calgaryバイオフィルム装置(Innovotech,Alberta,Canada)内で42時間生育させる。トリプチケースソイ培地(TSB)をバイオフィルム装置内で培地として用いる。培養時間後、緩く結合した細胞を、滅菌0.85%NaClでリンスすることによって、浸漬したペグの表面上に生育するバイオフィルムから除去する。次いで、バイオフィルムをDBMAL(発明殺生剤)、グルタルアルデヒド(比較殺生剤)、またはDBNPA(比較殺生剤)で処理する。希薄塩溶液を、有効性検討用の試験媒体として用いる。該塩溶液は(脱イオン水1リットル当たりのグラム単位で)CaCl2,0.2203g;MgSO4,0.1847g;およびNaHCO3,0.2033gを含有する。溶液の最終pHは8.5に調整する。
【0054】
試験する各活性物質の濃度は、塩溶液中、100ppm、50ppm、25ppm、12.5ppmであり、接触時間は、それぞれ4時間、24時間、および48時間である。全ての場合で、培養温度は37℃である。滅菌脱イオン水を、非殺生剤処理対照として用いる。各接触時間後、滅菌0.85%NaClでペグを洗浄し、バクテリアを各ペグの表面のバイオフィルムから滅菌0.85%NaCl中に超音波処理で放出させる(Ceriら,Journal of Clinical Microbiology 1999,37:1771−1776参照)。次いで、生存バクテリアをTSB中で、連続希釈法を用いて計数する。DBMALをDBNPAおよびグルタルアルデヒドと比較するデータを図1に示す。
【0055】
一般的に、DBMAL(発明殺生剤)は、DBNPA(比較殺生剤)よりも、固着バクテリアに対して有効である。グルタルアルデヒドは、50ppm活性物質濃度で、48時間処理後に低い有効性を示すのみである。活性物質濃度25ppmでは、DBMALは極めて有効な殺生剤であり、その有効性は接触時間とともに増大する。
【0056】
例4
バイオフィルム除去評価
Calgaryバイオフィルム装置を用いて、P.aeruginosa ATCC 10145のバイオフィルムを得る。TSBを培地として用い、バイオフィルムを42時間に亘って生育させる。次いで、表面上に生育するバイオフィルムを有するペグを、滅菌0.85%NaClで洗浄し、次いでDBMAL(発明殺生剤)またはDBNPA(比較殺生剤)で処理する。試験する活性物質の濃度は、試験媒体としての滅菌希釈塩溶液中、25ppm、50ppm、100ppmである。処理を37℃で4時間および24時間それぞれ実施する。滅菌脱イオン水を非処理対照として用いる。処理後、ペグを滅菌0.85%NaClで洗浄し、次いで各ペグ上のバイオマス/バイオフィルムを測定する(Stepanovicら,Journal of Microbiological Methods,2000,40,175−179参照)。まず、バイオフィルムを99%メタノールで固定し、風乾後、ペグを2%(w/v)クリスタルバイオレットで染色し、水道水で洗浄する。次いでペグを風乾し、バイオフィルムに結合したクリスタルバイオレットを33%氷酢酸で抽出する。抽出された溶液の光学密度(OD)を580nmで測定する。結果を図2に示す。
【0057】
データから分かるように、DBMAL(発明殺生剤)は、DBNPA(比較殺生剤)よりも全体的により良好なバイオフィルム除去を示す。バイオフィルム除去の有効性は、両物質について、より長い時間で(24時間を4時間と比べ)改善する。
【0058】
例5
アメーバ増殖レジオネラの制御
レジオネラは天然および人工の系中(例えば冷却塔)で、アメーバを経て継代することで増殖するため、このようなアメーバに栄養を受けたレジオネラ形の根絶は、より重要で当面関連する。この例は、アメーバに栄養を受けたLegionella pneumophila(AfLp)を評価において好適な殺生剤として使用する。
【0059】
レジオネラは、アメーバ(Acanthamoeba polypohaga)内で、低い多重度の感染から始まって、感染および生育させることができる(1レジオネラを100アメーバ細胞に対して)。このような継代をもう1度繰り返すことで、これらの支配的な生理学としてのより伝染性の型が、種々の濃度の殺生剤への曝露前に定着する。評価は、2時間および24時間の曝露後に実施する。殺生剤の適切な中和を、生存物の計数前に行う。下記の表6は、AfLpおよびフリーの通常生育レジオネラ細胞の両者に対する種々の殺生剤の有効性を比較する。
【0060】
【表2】

【0061】
データは、試験した全ての殺生剤について、AfLpを殺すのに必要な量が、フリーのレジオネラを殺すのに必要な量よりも大きいことを示す。しかし、レジオネラ制御に必要なDBMALの量は、他の試験した殺生剤,例えばDBNPAよりも大幅に低い。これは予期しない驚くべき知見である。6logの殺生物を与えるのに必要なDBMALのレベルは、対応する時点でフリーの細胞を制御するのに必要なものの約2倍に過ぎない。DBMALは、より伝染性の型のAfLpを、他の一般的に使用される殺生剤と比べたときにより低用量で制御する手段を与える。
【0062】
本発明をその好ましい態様に従って上記してきたが、本開示の精神および範囲の中で変更可能である。従って本件は、本開示で記載される一般原理を用いた本発明の任意の変更、使用または適合を網羅することを意図する。更に、本件は本発明が属する分野で公知または一般的な実施の範囲となる本開示からの逸脱を網羅し、これが特許請求の範囲の限定の範囲内となることを意図する。
【技術分野】
【0001】
関連出願の相互参照
本件は、米国仮出願整理番号第61/179,161号(2009年5月18日出願)(その全部を参照により本明細書に組入れる)の利益を主張する。
【0002】
発明の分野
本発明は、水性系または水分含有系において、系をハロゲン化アミド殺生剤で処理することによってバイオフィルムを制御する方法に関する。
【背景技術】
【0003】
発明の背景
バイオフィルムは、微生物、水分、栄養、および表面の組合せが存在する殆どのあらゆる環境中で生育する。工業において、バイオフィルムは水系プロセス(例えば水の処理および分配)において生じる。微生物生育によって形成されるバイオフィルムは、設備およびパイプラインの腐食、系の閉塞、製品不良、およびエネルギー損失により、工業における甚大な経済的損失の原因となる。バイオフィルムは、自己成長高分子マトリクス内に被包された構造群を占める微生物の層の蓄積によって形成される。バイオフィルム内の微生物は、固着微生物として公知であり、一方、フリーの浮遊する非バイオフィルム微生物はプランクトン様である。
【0004】
バイオフィルム内での生育により、固着微生物は抗微生物処理に対して、より耐性である。例えば、2,2−ジブロモ−3−ニトリロプロピオンアミド(「DBNPA」)はプランクトン様微生物を殺すのに極めて有効な市販で入手可能な殺生剤である。しかし、バイオフィルム処理に用いる場合、これはそれほど有効ではない。主な原因は、その急速な加水分解、およびその結果の、バイオフィルム内の固着バクテリアとの短い接触時間である。
【0005】
バイオフィルム関連微生物に対する有効性を示す殺生剤は、汚染された表面からバイオフィルムを除去するのに必ずしも有効ではない。バイオフィルムの残余物(例えばエキソ多糖類および死んだバクテリアの細胞)の物理的な存在は、腐食を生じさせる金属表面に対する酸素の一様でない可用性をなお招来する。よって、バイオフィルムを表面から除去することなくバイオフィルム内の微生物を殺すことは、腐食の問題を常に解決できるわけではない。
【0006】
プランクトン様および固着の細胞の両者に対して高い有効性を有し、そして汚染された表面からバイオフィルムを除去する高い能力を有する殺生剤を提供することは工業において大きな利点である。
【発明の概要】
【課題を解決するための手段】
【0007】
発明の簡単な要約
本発明は、水性系または水分含有系における固着微生物およびバイオフィルムを制御する方法を提供する。該方法は、水性系または水分含有系を、有効量の式(I):
【0008】
【化1】

【0009】
(式中、Xはハロゲンであり;そして
RおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、または
RおよびR1は、それぞれ、水素および式:
【0010】
【化2】

【0011】
のアミド基である)
の化合物で処理することを含む。
【図面の簡単な説明】
【0012】
【図1】図1は、種々の時間間隔について殺生剤処理後の生存固着バクテリアの低減を示す棒グラフである。
【図2】図2は、バイオフィルムの除去での殺生剤の有効性を示す棒グラフである。
【発明を実施するための形態】
【0013】
発明の詳細な説明
上記のように、本発明は、水性系または水分含有系におけるバイオフィルムを制御する方法を提供する。該方法は、水性系または水分含有系を有効量の式(I)の化合物で処理することを含む。本発明者らは、驚くべきことに、式(I)の化合物が、固着細胞の制御に有効であることを発見した。加えて、該化合物はまた、水性系または水分含有系において(例えば系において操作する設備表面から)既に形成されたバイオフィルムの除去にも有効である。
【0014】
式(I)の化合物は、以下の化学構造:
【0015】
【化3】

【0016】
(式中、Xは、ハロゲンであり;そしてRおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、または、RおよびR1は、それぞれ、水素および式:
【0017】
【化4】

【0018】
のアミド基である)
を有する。
【0019】
好ましくは、式(I)の化合物中のXは、ブロモ、クロロ、またはヨードであり、より好ましくはブロモである。
【0020】
式(I)の好ましい化合物は、2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミドである。
【0021】
式(I)の更に好ましい化合物は、2,2−ジブロモマロンアミドである。用語「2,2−ジブロモマロンアミド」は、下記式:
【0022】
【化5】

【0023】
の化合物を意味する。
【0024】
式(I)の化合物は、当業者によって、周知の文献の方法を用いて調製できる。
【0025】
バイオフィルムに対するこれらの全体的な有効性に加え、本発明の化合物はまた、驚くべきことに、ほぼ中性〜アルカリ性のpHでの加水分解に対して、他の殺生剤よりも耐性である。例えば、以下の例は、pH6.9で、2,2−ジブロモマロンアミド(DBMAL)、本発明の例の化合物が、特筆すべきことに、DBNPA(比較殺生剤)よりも安定であることを示す。DBMALの損失は、96時間に亘って検出されず、一方84%のDBNPAが、この同じ時間枠にて同一条件で損失する。
【0026】
よって、更なる態様において、式(I)の化合物は、水性系または水分含有系における固着微生物およびバイオフィルムを制御する方法であって水性成分または水分含有成分がpH5以上を有する方法において使用される。幾つかの態様において、pHは6以上である。更なる態様において、pHは7以上である。更なる態様において、pHは8以上である。
【0027】
本発明の化合物で処理できる水性系または水分含有系としては、これらに限定するものではないが、パルプおよび紙の工場、冷却塔操作、熱交換器、金属作動流体、逆浸透水加工、油田およびガス田の注入水、破砕水および生成水、油井およびガス井および貯留槽、脱気塔、油およびガスの操作系および輸送系、油およびガスの分離系および貯蔵タンク、油およびガスのパイプライン、ガス容器、便器、水泳プール、家庭排水、家庭用品表面、プロセス設備、下水道系、廃水および処理系、他の工業プロセス水、ボイラー系、バラスト水、ならびにこれらの系における設備、パイプ、チューブおよび他の表面が挙げられる。好ましい水性系または水分系は、紙およびパルプの工場、冷却塔操作、逆浸透水加工、油田およびガス田の操作系、分離系、輸送系および貯蔵系、パイプライン、ガス容器、金属作動流体ならびに膜系濾過システムである。
【0028】
代表的な膜系濾過システムとしては、1つ以上の半透膜を含むものが挙げられ、これらに限定するものではないが:精密濾過膜、限外濾過膜、ナノ濾過膜、逆浸透膜およびイオン交換膜が挙げられる。適用可能な系としては、単一種の膜を含むもの(例えば、精密濾過)、および複数種の膜を含むもの(例えば、限外濾過および逆浸透)が挙げられる。例えば、膜系濾過システムは、上流の精密濾過膜または限外濾過膜および下流のナノ濾過膜または逆浸透膜を含むことができる。
【0029】
主題の殺生物化合物は、濾過前(例えば、処理されることになる供給物溶液を収容する貯蔵タンクまたは貯蔵池に添加する)、または濾過中(例えば、濾過中に、加圧した供給物溶液中に投入する)に供給物溶液に添加できる。更に、主題の殺生物化合物は、膜に接触する、洗浄溶液または貯蔵溶液に添加できる。この記載の目的のために、系の膜に接触する任意の水性溶液(例えば、原料供給水、洗浄溶液、膜貯蔵溶液等)を「供給物溶液」という。
【0030】
精密濾過膜または限外濾過膜およびナノ濾過膜または逆浸透膜の両者を有する系において使用する場合には、主題の殺生物化合物は、各膜(例えば、上流および下流の膜の両者)に対して殺生物効果を与える。
【0031】
1つまたは複数の膜によって拒絶される殺生物化合物の部分は、後続の処理で用いるために、濃縮物流から回収して再循環させることができる(例えば貯蔵タンクに直接戻すか、または入ってくる供給物中に投入する)。殺生物化合物の再循環は間欠または連続のプロセスの一部であることができる。
【0032】
多くの膜系濾過システムにおいて、供給物溶液のpHは少なくとも7、しばしば少なくとも8、幾つかの態様では少なくとも9、および他の態様では少なくとも10である。このような膜系システムの例は、第US6,537,456号および第US7,442,309号に記載されている。更に、多くの系の膜は、一般的に、pH値が少なくとも11、および幾つかの態様では少なくとも12である供給物溶液で洗浄または貯蔵する。DBNPA(第WO2008/091453号に記載されるような)とは異なり、主題の殺生物化合物は、このような中性およびアルカリ性の条件下で有効であり続ける。結果として、主題の殺生物化合物は、より広い範囲の供給物溶液(例えば、pHが調製された水性供給物、水性洗浄溶液、水性貯蔵溶液)(膜系濾過システムに関して用いるもの)に添加できる。
【0033】
このような系で用いる膜の種類は特に限定されず、フラットシート、チューブ状および中空状の繊維が挙げられる。膜の1つの好ましい分類としては、薄膜コンポジットポリアミド膜(ナノ濾過および逆浸透の用途で一般的に用いるもの)が挙げられる(一般的に、第US4,277,344号;第US2007/0251883号;および第US2008/0185332号に記載される通り)。このようなナノ濾過膜および/または逆浸透膜は、一般的に、らせん巻き構造でのフラットシートとして提供される。精密濾過膜および限外濾過膜の非限定例としては、種々の物質(例えばポリスルホン、ポリエーテルスルホン、ポリアミド、ポリプロピレンおよびポリフッ化ビニリデン)から形成される多孔質膜が挙げられる。このような精密濾過膜および限外濾過膜は、一般的には中空繊維として提供される。
【0034】
当業者は、過度の実験を伴わずに、任意の特定用途において用いるべき式(I)の化合物の有効量を容易に決定できる。例えば、少なくとも1ppm、代替として少なくとも5質量ppm、代替として少なくとも10ppm、または少なくとも50ppmの量が一般的に適切である。幾つかの態様において、該量は、1000ppm以下、代替として500ppm以下、または300ppm以下、または200ppm以下、または100ppm以下である。更なる態様において、該量は約20〜約30ppmである。
【0035】
式(I)の化合物は、水性系または水分含有系において、他の添加剤(例えば、これらに限定するものではないが、界面活性剤、イオン性/非イオン性ポリマー、ならびにスケール防止剤および腐食防止剤、酸素捕捉剤、ならびに/または追加の殺生剤)とともに使用できる。
【0036】
式(I)の化合物は、広範囲の微生物を制御するのに有用である。一態様において、微生物はレジオネラ種のバクテリア(例えばアメーバ内で継代して数が増殖するようなバクテリア)である。このレジオネラ態様に対して好ましい殺生剤は、2,2−ジブロモマロンアミドである。
【0037】
レジオネラバクテリアは、レジオネラ症およびポンティアック熱(包括的にレジオネラ症として知られている)の原因とみなされてきた。レジオネラ症の多くの発生は、感染用量を与える蒸発冷却系に影響してきた。レジオネラは、アメーバ内に寄生して生息するという比較的特異な生存能力を示し、最終的にはその宿主細胞を溶解させ、成熟した感染型として外に出る。この機構は、天然および人工の水系におけるレジオネラ数の増殖およびその増大した毒性の主要な手段として提案されてきた。レジオネラ(例えばアメーバ内で継代することによってより感染性になるレジオネラの型)を有効に制御できる殺生剤が高度に望ましい。例によって示すように、式(I)の化合物,例えば2,2−ジブロモマロンアミドはこのようなバクテリア制御に対して有効である。
【0038】
本開示で記載される化合物は、驚くべきことに、固着/バイオフィルム微生物の制御で、他の殺生剤(例えば市販化合物DBNPA)よりも有効であり、従って工業に大きな利点を与える。
【0039】
本明細書の目的のために、「微生物」はバクテリア、藻類、またはウイルスを意味する。用語「制御」および「制御する」は、固着微生物の生育または増殖を阻害すること、固着微生物を殺すこと、消毒、および/または防腐という、その意味を包含しそれに限定することのないように広く解釈すべきである。「制御」および「制御する」はまた、固着微生物のバイオフィルムの、これが少なくとも部分的に付着いている表面からの部分的または完全な除去を網羅する。
【0040】
「ヒドロキシアルキル」は、アルキル基(すなわち、直鎖および分岐鎖の脂肪族基)であって1〜6個の炭素原子を有し、水酸基で置換されているものを意味する。例としては、これらに限定するものではないが、ヒドロキシメチル、ヒドロキシエチル、2−ヒドロキシプロピル、3−ヒドロキシプロピル等が挙げられる。
【0041】
「ハロゲン」はフルオロ、クロロ、ブロモ、またはヨードを意味する。
【0042】
特記がない限り、本開示で用いる比、パーセント、部等は質量基準である。
【0043】
以下の例は本発明の例示であるがその範囲の限定を意図しない。
【0044】
例
以下の組成物を例において評価する:
2,2−ジブロモ−3−ニトリロプロピオンアミド(「DBNPA」)はThe Dow Chemical Companyから得る。
【0045】
2,2−ジブロモマロンアミド(「DBMAL」)は、Johnson Matheyから得る。
【0046】
グルタルアルデヒドは、The Dow Chemical Companyから得る。
【0047】
CMIT/MIT(5−クロロ−2−メチル−4−イソチアゾリン−3−オンおよび2−メチル−4−イソチアゾリン−3−オン)はThe Dow Chemical Companyから得る。
【0048】
ジオクチルジメチルアンモニウムクロリドは、Lonza Inc.から得る。
【0049】
例1
2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミド(DBCHA)の調製
0.1モルの3−アミノ−1−プロパノール(7.51g)を、0.1モルのメチルシアノアセテート(10.1g)の溶液(メタノール中(40g))に添加する。混合物を撹拌して60℃まで30分間加熱する。メタノール溶媒を反応生成物から減圧ストリップする。反応生成物を、任意の更なる精製を必要とせず、水中に溶解させ、0.1モルの臭素(16.0g)および0.03モルの臭素酸ナトリウム(5.0g)と反応させる。反応温度は30℃未満に保つ。臭素および臭素酸ナトリウムの添加が完了した後、反応混合物を30分間撹拌した後、pH3〜4まで、希薄水酸化ナトリウムで中和する。収量は0.09モルの2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミド(28g)である。
【0050】
例2
加水分解に対する安定性:DBMALおよびDBNPAの比較
希薄溶液(0.5質量%未満)のDBMALおよびDBNPAを3つの異なるpHで調製する。標準緩衝溶液を用いて、pH6.9、8.0および9.0にて、pHを設定および維持する。次いで、これらの溶液を一定温度で、−1℃または30℃のいずれかで保持する。定期的に、分割量をHPLCによって分析して、残存するDBMALまたはDBNPAのレベルを評価する。結果を表1に示す。
【0051】
【表1】

【0052】
表1は、中性近傍条件(pH=6.9)および温度30℃であっても、DBMALが、DBNPA(比較殺生剤)よりも顕著に安定であることを示す。DBMALの損失は、96時間に亘って検出されず、一方84%のDBNPAがこの同じ時間枠にて同じ条件で損失する。
【0053】
例3
バイオフィルム関連バクテリアに対する有効性
P.aeruginosa ATCC 10145のバイオフィルムを、Calgaryバイオフィルム装置(Innovotech,Alberta,Canada)内で42時間生育させる。トリプチケースソイ培地(TSB)をバイオフィルム装置内で培地として用いる。培養時間後、緩く結合した細胞を、滅菌0.85%NaClでリンスすることによって、浸漬したペグの表面上に生育するバイオフィルムから除去する。次いで、バイオフィルムをDBMAL(発明殺生剤)、グルタルアルデヒド(比較殺生剤)、またはDBNPA(比較殺生剤)で処理する。希薄塩溶液を、有効性検討用の試験媒体として用いる。該塩溶液は(脱イオン水1リットル当たりのグラム単位で)CaCl2,0.2203g;MgSO4,0.1847g;およびNaHCO3,0.2033gを含有する。溶液の最終pHは8.5に調整する。
【0054】
試験する各活性物質の濃度は、塩溶液中、100ppm、50ppm、25ppm、12.5ppmであり、接触時間は、それぞれ4時間、24時間、および48時間である。全ての場合で、培養温度は37℃である。滅菌脱イオン水を、非殺生剤処理対照として用いる。各接触時間後、滅菌0.85%NaClでペグを洗浄し、バクテリアを各ペグの表面のバイオフィルムから滅菌0.85%NaCl中に超音波処理で放出させる(Ceriら,Journal of Clinical Microbiology 1999,37:1771−1776参照)。次いで、生存バクテリアをTSB中で、連続希釈法を用いて計数する。DBMALをDBNPAおよびグルタルアルデヒドと比較するデータを図1に示す。
【0055】
一般的に、DBMAL(発明殺生剤)は、DBNPA(比較殺生剤)よりも、固着バクテリアに対して有効である。グルタルアルデヒドは、50ppm活性物質濃度で、48時間処理後に低い有効性を示すのみである。活性物質濃度25ppmでは、DBMALは極めて有効な殺生剤であり、その有効性は接触時間とともに増大する。
【0056】
例4
バイオフィルム除去評価
Calgaryバイオフィルム装置を用いて、P.aeruginosa ATCC 10145のバイオフィルムを得る。TSBを培地として用い、バイオフィルムを42時間に亘って生育させる。次いで、表面上に生育するバイオフィルムを有するペグを、滅菌0.85%NaClで洗浄し、次いでDBMAL(発明殺生剤)またはDBNPA(比較殺生剤)で処理する。試験する活性物質の濃度は、試験媒体としての滅菌希釈塩溶液中、25ppm、50ppm、100ppmである。処理を37℃で4時間および24時間それぞれ実施する。滅菌脱イオン水を非処理対照として用いる。処理後、ペグを滅菌0.85%NaClで洗浄し、次いで各ペグ上のバイオマス/バイオフィルムを測定する(Stepanovicら,Journal of Microbiological Methods,2000,40,175−179参照)。まず、バイオフィルムを99%メタノールで固定し、風乾後、ペグを2%(w/v)クリスタルバイオレットで染色し、水道水で洗浄する。次いでペグを風乾し、バイオフィルムに結合したクリスタルバイオレットを33%氷酢酸で抽出する。抽出された溶液の光学密度(OD)を580nmで測定する。結果を図2に示す。
【0057】
データから分かるように、DBMAL(発明殺生剤)は、DBNPA(比較殺生剤)よりも全体的により良好なバイオフィルム除去を示す。バイオフィルム除去の有効性は、両物質について、より長い時間で(24時間を4時間と比べ)改善する。
【0058】
例5
アメーバ増殖レジオネラの制御
レジオネラは天然および人工の系中(例えば冷却塔)で、アメーバを経て継代することで増殖するため、このようなアメーバに栄養を受けたレジオネラ形の根絶は、より重要で当面関連する。この例は、アメーバに栄養を受けたLegionella pneumophila(AfLp)を評価において好適な殺生剤として使用する。
【0059】
レジオネラは、アメーバ(Acanthamoeba polypohaga)内で、低い多重度の感染から始まって、感染および生育させることができる(1レジオネラを100アメーバ細胞に対して)。このような継代をもう1度繰り返すことで、これらの支配的な生理学としてのより伝染性の型が、種々の濃度の殺生剤への曝露前に定着する。評価は、2時間および24時間の曝露後に実施する。殺生剤の適切な中和を、生存物の計数前に行う。下記の表6は、AfLpおよびフリーの通常生育レジオネラ細胞の両者に対する種々の殺生剤の有効性を比較する。
【0060】
【表2】

【0061】
データは、試験した全ての殺生剤について、AfLpを殺すのに必要な量が、フリーのレジオネラを殺すのに必要な量よりも大きいことを示す。しかし、レジオネラ制御に必要なDBMALの量は、他の試験した殺生剤,例えばDBNPAよりも大幅に低い。これは予期しない驚くべき知見である。6logの殺生物を与えるのに必要なDBMALのレベルは、対応する時点でフリーの細胞を制御するのに必要なものの約2倍に過ぎない。DBMALは、より伝染性の型のAfLpを、他の一般的に使用される殺生剤と比べたときにより低用量で制御する手段を与える。
【0062】
本発明をその好ましい態様に従って上記してきたが、本開示の精神および範囲の中で変更可能である。従って本件は、本開示で記載される一般原理を用いた本発明の任意の変更、使用または適合を網羅することを意図する。更に、本件は本発明が属する分野で公知または一般的な実施の範囲となる本開示からの逸脱を網羅し、これが特許請求の範囲の限定の範囲内となることを意図する。
【特許請求の範囲】
【請求項1】
水性系または水分含有系における微生物を制御する方法であって、水性系または水分含有系を、有効量の式(I):
【化1】

(式中、Xはハロゲンであり;そして
RおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、または
RおよびR1は、それぞれ、水素および式:
【化2】

のアミド基である)
の化合物で処理することを含み、
制御される微生物が固着微生物である、方法。
【請求項2】
Xがブロモである、請求項1に記載の方法。
【請求項3】
式(I)の化合物が:2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミド;2,2−ジブロモマロンアミド;またはこれらの混合物である、請求項1〜2に記載の方法。
【請求項4】
該水性系または水分含有系が、pH5以上を有する、請求項1〜3に記載の方法。
【請求項5】
該水性系または水分含有系が、パルプおよび紙の工場、冷却塔操作、熱交換器、金属作動流体、逆浸透水加工、油田およびガス田の注入水、破砕水および生成水、油井およびガス井および貯留槽、脱気塔、油およびガスの操作系および輸送系、油およびガスの分離系および貯蔵タンク、油およびガスのパイプライン、ガス容器、便器、水泳プール、家庭排水、家庭用品表面、プロセス設備、下水道系、廃水および処理系、他の工業プロセス水、ボイラー系、バラスト水、ならびにこれらの系における設備、パイプ、チューブおよび他の表面である、請求項1〜4に記載の方法。
【請求項6】
該微生物が、バクテリアである、請求項1〜5に記載の方法。
【請求項7】
該微生物が、バクテリアである、請求項1〜6のいずれか1項に記載の方法。
【請求項8】
該微生物が、レジオネラ属の種である、請求項1〜7のいずれか1項に記載の方法。
【請求項9】
該微生物が、生存アメーバ内で増殖したレジオネラ種である、請求項1〜8のいずれか1項に記載の方法。
【請求項10】
系が、精密濾過膜、限外濾過膜、ナノ濾過膜、逆浸透膜およびイオン交換膜の少なくとも1つから選択される少なくとも1つの半透膜を含む膜系濾過システムを含み;該方法が、式(I)の化合物を供給物溶液に添加し、次いで該供給物溶液を該半透膜と接触させることを含む、請求項1〜9に記載の方法。
【請求項11】
該膜系濾過システムが、少なくとも:i)1つの精密濾過膜または限外濾過膜およびii)少なくとも1つのナノ濾過膜または逆浸透膜;を含む、請求項1〜10に記載の方法。
【請求項12】
該供給物溶液が、pH少なくとも9を有する、請求項1〜11に記載の方法。
【請求項13】
該供給物溶液が、pH少なくとも11を有する、請求項1〜12に記載の方法。
【請求項1】
水性系または水分含有系における微生物を制御する方法であって、水性系または水分含有系を、有効量の式(I):
【化1】

(式中、Xはハロゲンであり;そして
RおよびR1は、それぞれ、ヒドロキシアルキル基およびシアノ基(−C≡N)であり、または
RおよびR1は、それぞれ、水素および式:
【化2】

のアミド基である)
の化合物で処理することを含み、
制御される微生物が固着微生物である、方法。
【請求項2】
Xがブロモである、請求項1に記載の方法。
【請求項3】
式(I)の化合物が:2,2−ジブロモ−2−シアノ−N−(3−ヒドロキシプロピル)アセトアミド;2,2−ジブロモマロンアミド;またはこれらの混合物である、請求項1〜2に記載の方法。
【請求項4】
該水性系または水分含有系が、pH5以上を有する、請求項1〜3に記載の方法。
【請求項5】
該水性系または水分含有系が、パルプおよび紙の工場、冷却塔操作、熱交換器、金属作動流体、逆浸透水加工、油田およびガス田の注入水、破砕水および生成水、油井およびガス井および貯留槽、脱気塔、油およびガスの操作系および輸送系、油およびガスの分離系および貯蔵タンク、油およびガスのパイプライン、ガス容器、便器、水泳プール、家庭排水、家庭用品表面、プロセス設備、下水道系、廃水および処理系、他の工業プロセス水、ボイラー系、バラスト水、ならびにこれらの系における設備、パイプ、チューブおよび他の表面である、請求項1〜4に記載の方法。
【請求項6】
該微生物が、バクテリアである、請求項1〜5に記載の方法。
【請求項7】
該微生物が、バクテリアである、請求項1〜6のいずれか1項に記載の方法。
【請求項8】
該微生物が、レジオネラ属の種である、請求項1〜7のいずれか1項に記載の方法。
【請求項9】
該微生物が、生存アメーバ内で増殖したレジオネラ種である、請求項1〜8のいずれか1項に記載の方法。
【請求項10】
系が、精密濾過膜、限外濾過膜、ナノ濾過膜、逆浸透膜およびイオン交換膜の少なくとも1つから選択される少なくとも1つの半透膜を含む膜系濾過システムを含み;該方法が、式(I)の化合物を供給物溶液に添加し、次いで該供給物溶液を該半透膜と接触させることを含む、請求項1〜9に記載の方法。
【請求項11】
該膜系濾過システムが、少なくとも:i)1つの精密濾過膜または限外濾過膜およびii)少なくとも1つのナノ濾過膜または逆浸透膜;を含む、請求項1〜10に記載の方法。
【請求項12】
該供給物溶液が、pH少なくとも9を有する、請求項1〜11に記載の方法。
【請求項13】
該供給物溶液が、pH少なくとも11を有する、請求項1〜12に記載の方法。
【図1】


【図2】




【図2】


【公表番号】特表2012−527352(P2012−527352A)
【公表日】平成24年11月8日(2012.11.8)
【国際特許分類】
【出願番号】特願2012−511914(P2012−511914)
【出願日】平成22年5月14日(2010.5.14)
【国際出願番号】PCT/US2010/034939
【国際公開番号】WO2010/135195
【国際公開日】平成22年11月25日(2010.11.25)
【出願人】(502141050)ダウ グローバル テクノロジーズ エルエルシー (1,383)
【Fターム(参考)】
【公表日】平成24年11月8日(2012.11.8)
【国際特許分類】
【出願日】平成22年5月14日(2010.5.14)
【国際出願番号】PCT/US2010/034939
【国際公開番号】WO2010/135195
【国際公開日】平成22年11月25日(2010.11.25)
【出願人】(502141050)ダウ グローバル テクノロジーズ エルエルシー (1,383)
【Fターム(参考)】
[ Back to top ]

