治療用細胞フラグメント回収用基材およびそれを用いた治療用細胞フラグメントの製造方法、ならびに、継代用細胞フラグメント回収用基材およびそれを用いた継代用細胞フラグメントの製造方法
【課題】本発明は、治療効果を再現性良く発揮できる治療用細胞フラグメントを得ることができる治療用細胞フラグメント回収用基材を提供することを主目的とする。
【解決手段】本発明は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域の周囲が、上記細胞非接着領域により囲まれていることを特徴とする治療用細胞フラグメント回収用基材を提供することにより、上記目的を達成する。
【解決手段】本発明は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域の周囲が、上記細胞非接着領域により囲まれていることを特徴とする治療用細胞フラグメント回収用基材を提供することにより、上記目的を達成する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、治療効果を再現性良く発揮できる治療用細胞フラグメントを得ること、および、継代操作時に細胞を安定的に培養できる継代用細胞フラグメントを容易に得ることができる細胞フラグメント回収用基材に関するものである。
【背景技術】
【0002】
近年、細胞フラグメントが、再生医療などでしばしば用いられるようになってきている。
ここで、細胞フラグメントとは、細胞間結合で細胞同士が少なくとも単層で連結された細胞集合体である。
【0003】
このような細胞フラグメントの作製方法としては、支持体上に細胞を播種・培養し形成された細胞シートに、トリプシン等のタンパク質分解酵素を作用させ、支持体−細胞間および細胞−細胞間の結合が切断された細胞フラグメントを回収する方法や、支持体上に細胞を播種・培養し形成された細胞シートに金属製の網を押し当て、上記細胞シートを所定のサイズに分断する方法が開示されている(非特許文献1)。
しかしながら、このような方法で得られた細胞フラグメントを前臨床研究において実験動物への移植に用いた場合には、細胞間結合を物理的に切断しているため侵襲的であるだけでなく、サイズの不揃いなフラグメントしか得られず実験結果がばらつくといった問題があった。
【0004】
また、細胞の継代操作時に、タンパク質分解酵素を用いて培養容器等の支持体から細胞を剥離し、新しい支持体に剥離した細胞を植え継ぐ作業が行われる。
しかしながら、このようなタンパク質分解酵素を用いる方法では、タンパク質分解酵素の滴下、反応停止等の作業が必要であり作業が煩雑であるといった問題や、タンパク質分解酵素により細胞がダメージを受け、その後の増殖に悪影響が出る等の問題があった。また、タンパク質分解酵素の濃度、処理時間を厳密に管理できていない場合には、継代操作毎に細胞増殖速度にばらつきが出るといった問題があった。
【先行技術文献】
【非特許文献】
【0005】
【非特許文献1】Cardiovascular Reserch(2008)77,515-524
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明は、上記問題点に鑑みてなされたものであり、治療効果を再現性良く発揮できる細胞フラグメントを得ること、および、継代操作時に細胞を安定的に培養できる継代用細胞フラグメントを容易に得ることができる細胞フラグメント回収用基材を提供することを主目的とする。
【課題を解決するための手段】
【0007】
本発明者等は、上記課題を解決すべく研究を重ねた結果、従来のトリプシン等のタンパク質分解酵素を用いる方法や、金網等で細胞シートを分断する方法では、サイズや形状が不揃いな細胞フラグメントなり、このようなサイズおよび形状の不揃いな細胞フラグメントを用いた場合には、上記細胞フラグメントを前臨床研究における実験動物への移植に用いた際に細胞間結合を物理的に切断しているため侵襲的であるだけでなく、サイズの不揃いなフラグメントしか得られず実験結果がばらつくことを見出した。
また、継代操作時に、トリプシン等のタンパク質分解酵素により細胞−細胞間の結合を切断するが、このような処理により形成される細胞フラグメントのサイズおよび形状が不揃いなことにより、その後の細胞増殖にばらつきがでること、および、細胞が効率よく増殖できる細胞フラグメントのサイズ、すなわち、一つの細胞フラグメントに含まれる細胞の数が細胞毎に異なるものであることを見出し、本発明を完成させるに至ったのである。
【0008】
すなわち、本発明は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域が、上記細胞非接着領域により囲まれていることを特徴とする治療用細胞フラグメント回収用基材を提供する。
【0009】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域への刺激の付与により、任意のサイズおよび形状に制御された治療用細胞フラグメントを容易に回収することができる。
また、サイズおよび形状が制御されているため、このような治療用細胞フラグメントを用いた移植等による治療効果を再現性良く発揮することができる。
【0010】
本発明は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域が、上記細胞非接着領域により囲まれていることを特徴とする継代用細胞フラグメント回収用基材を提供する。
【0011】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域への刺激の付与により、任意のサイズおよび形状に制御された継代用細胞フラグメントを容易に回収することができる。このため、継代操作を簡便なものとすることができる。また、トリプシン等のタンパク質分解酵素の使用を不要とすることができるため、上記細胞を安定的に増殖させることができる。
また、サイズおよび形状が制御されているため、このような継代用細胞フラグメントを用いて継代した場合には、上記細胞の増殖を精度良くコントロールでき、安定的に培養することができる。
このようなことから、例えば、自動培養装置においてこのような継代用細胞フラグメント回収用基材を用いた場合には、安定的に細胞を増殖、培養することができる。
【0012】
本発明においては、上記刺激応答性領域が、温度変化により細胞接着性が変化する温度応答性材料を含むことが好ましい。刺激の付与が容易だからである。
【0013】
本発明においては、上記温度応答性材料が、ポリイソプロピルアクリルアミドであることが好ましい。細胞の培養に適した温度において細胞接着性を有し、細胞へのダメージの少ない温度で細胞非接着性を発現することから、上記細胞フラグメントを安定的に回収することができるからである。
【0014】
本発明は、上述の治療用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記治療用細胞フラグメントを回収する回収工程と、を有することを特徴とする治療用細胞フラグメントの製造方法を提供する。
また、本発明は、上述の継代用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる継代用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記継代用細胞フラグメントを回収する回収工程と、を有することを特徴とする継代用細胞フラグメントの製造方法を提供する。
【0015】
本発明によれば、上記治療用細胞フラグメント回収用基材および継代用細胞フラグメント回収用基材を用いることにより、サイズおよび形状が制御された上記治療用細胞フラグメントおよび継代用細胞フラグメントを容易に製造することができる。
【発明の効果】
【0016】
本発明は、治療効果を再現性良く発揮できる治療用細胞フラグメントを得ること、および、継代操作時に細胞を安定的に培養できる継代用細胞フラグメントを容易に得ることができる細胞フラグメント回収用基材を提供できるといった効果を奏する。
【図面の簡単な説明】
【0017】
【図1】本発明の治療用細胞フラグメント回収用基材の一例を示す概略平面図である。
【図2】図1のA−A線断面図である。
【図3】本発明の治療用細胞フラグメント回収用基材の他の例を示す概略平面図である。
【図4】本発明の治療用細胞フラグメント回収用基材の他の例を示す概略平面図である。
【図5】本発明の治療用細胞フラグメント回収用基材の他の例を示す概略断面図である。
【図6】本発明の治療用細胞フラグメントの製造方法の一例を示す工程図である。
【発明を実施するための形態】
【0018】
本発明は、治療用細胞フラグメント回収用基材およびそれを用いた治療用細胞フラグメントの製造方法、ならびに、継代用細胞フラグメント回収用基材およびそれを用いた継代用細胞フラグメントの製造方法に関するものである。
以下、本発明の治療用細胞フラグメント回収用基材、継代用細胞フラグメント回収用基材、治療用細胞フラグメントの製造方法、および継代用細胞フラグメントの製造方法について詳細に説明する。
【0019】
A.治療用細胞フラグメント回収用基材
まず、本発明の治療用細胞フラグメント回収用基材について説明する。
本発明の治療用細胞フラグメント回収用基材は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域が、上記細胞非接着領域により囲まれていることを特徴とするものである。
【0020】
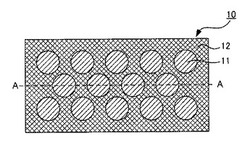
このような本発明の治療用細胞フラグメント回収用基材について図を参照して説明する。図1は、本発明の治療用細胞フラグメント回収用基材の一例を示す概略平面図であり、図2は、図1のA−A線断面図である。
図1および2に例示するように、本発明の治療用細胞フラグメント回収用基材10は、刺激により細胞接着性が変化する刺激応答性材料を含む刺激応答性層1と、細胞非接着性を有する細胞非接着材料を含む細胞非接着層2と、を有し、上記刺激応答性層1の露出表面である刺激応答性領域11が上記細胞非接着層2の露出表面である細胞非接着領域12により囲まれているものである。また、上記刺激応答性層1および細胞非接着性層2を支持する基材3を有するものである。
【0021】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域に細胞を播種し、培養することにより治療用細胞フラグメントを形成した後に、上記刺激応答性領域へ刺激を付与することにより、任意のサイズおよび形状に制御された治療用細胞フラグメントを上記刺激応答性領域から容易に剥離し回収することができる。
また、サイズおよび形状が制御されているため、このような治療用細胞フラグメントを用いた場合には、従来のトリプシン等のタンパク質分解酵素や、金網を押し付ける方法により得られる細胞フラグメントを用いる場合と比較し、前臨床研究における実験動物への移植等の際に、サイズの揃ったフラグメントが得られるため実験の再現性が向上する効果が得られる。
【0022】
本発明の治療用細胞フラグメント回収用基材は、刺激応答性領域および細胞非接着性領域を少なくとも有するものである。
以下、本発明の治療用細胞フラグメント回収用基材の各構成について詳細に説明する。
【0023】
1.刺激応答性領域
本発明における刺激応答性領域は、刺激応答性材料を含む刺激応答性層の表面のうち、露出した範囲であり、上記細胞非接着領域により囲まれるものである。
【0024】
(1)刺激応答性領域
本発明における刺激応答性領域は、上記細胞非接着領域により囲まれているものであり、刺激により細胞接着性を変化させることにより培養する細胞の接着および剥離を行なうことができるものである。
【0025】
本発明における刺激応答性領域は、特定の刺激により細胞接着性が良好な細胞接着性を発現している状態から、細胞の接着性が低い性質である細胞非接着性を発現している状態に変化し得るものである。
ここで、上記刺激応答性領域が細胞接着性を発現しているとは、上記刺激応答性領域上で、細胞が接着、伸展しやすく、細胞接着伸展率が高い状態であることをいうものである。本発明において、このような細胞接着伸展率が高い状態としては、具体的には、細胞接着伸展率が60%以上である状態とすることができる。
本発明においては、なかでも、80%以上であることが好ましい。効率的に細胞を培養し、治療用細胞フラグメントを形成させることができるからである。
なお、本発明における細胞接着伸展率は、播種密度が4000cells/cm2以上30000cells/cm2未満の範囲内でウシ血管内皮細胞を播種し、37℃インキュベーター内(CO2濃度5%)に保管し、3時間以上経過し、倍加時間前に接着伸展している細胞の割合({(接着している細胞数)/(播種した細胞数)}×100(%))を表すものである。
また、上記細胞の播種は、10%FBS(血清)入りDMEM培地に懸濁させて培養基材上に播種し、その後、上記細胞ができるだけ均一に分布するよう、上記細胞が播種された培養基材をゆっくりと振とうすることにより行うものである。
さらに、細胞接着伸展率の測定は、測定直前に培地交換を行って接着していない細胞を除去した後に行い、細胞接着伸展率の測定個所としては、細胞の存在密度が特異的になりやすい箇所(例えば、存在密度が高くなりやすい所定領域の中央、存在密度が低くなりやすい所定領域の周縁)を除いて測定を行うものである。
【0026】
また、上記刺激応答性領域が細胞非接着性を発現している場合とは、上記刺激応答性領域上で細胞が接着、伸展しにくく、細胞接着伸展率が低い状態であることをいうものである。本発明において、このような細胞接着伸展率が低い状態としては、具体的には、上記細胞接着伸展率が5%以下である状態とすることができる。本発明においては、なかでも2%以下であることが好ましい。
したがって、上記刺激応答性領域に細胞を播種すると、細胞接着性を発現している際には細胞が上記刺激応答性領域に接着し、容易に治療用細胞フラグメントを形成することができ、細胞非接着性を発現している際には細胞が上記刺激応答性領域に接着することを阻害されるため、上記刺激応答性領域に接着していた治療用細胞フラグメントを容易に剥離し、回収することができるのである。
【0027】
本発明に用いられる刺激応答性領域の形状としては、安定的に治療用細胞フラグメントを回収することができるものであれば特に限定されるものではなく、例えば、既に説明した図1に示すような円形状や楕円形状、図3に例示するような多角形状、ライン状、格子状、星型等であってもよい。また、複数の形状を組み合わせたものであってもよい。
本発明においては、なかでも、円形状または六角形状以上の多角形であることが好ましく、特に、円形状であることが好ましい。上記刺激応答性領域に刺激を与えた際に、上記治療用細胞フラグメントを上記刺激応答性領域から安定的に剥離することができるからである。
【0028】
本発明に用いられる刺激応答性領域の一つあたりの面積としては、少なくとも1以上の細胞が接着することができ、上記治療用細胞フラグメントを安定的に回収できるものであれば特に限定されるものではないが、具体的には、200μm2〜100000μm2の範囲内であることが好ましく、1000μm2〜50000μm2の範囲内であることが好ましく、10000μm2〜40000μm2の範囲内であることが好ましい。上記刺激応答性領域に刺激を付与することにより、上記治療用細胞フラグメントを安定的に剥離し、回収することができるからである。
【0029】
本発明に用いられる刺激応答性領域の配置としては、上記治療用細胞フラグメントを安定的に回収することができるものであれば特に限定されるものではないが、上記治療用細胞フラグメントを安定的に得られる範囲で、最も多くの治療用細胞フラグメントを形成できるものであることが好ましい。一回の操作で、効率的に上記治療用細胞フラグメントを得ることができるからである。
【0030】
本発明に用いられる刺激応答性領域が占める割合としては、本発明の治療用細胞フラグメント回収用基材内の底面を100%とした場合に少なくとも50%以上含まれるものであれば特に限定されるものではないが、50%〜95%の範囲内であることが好ましく、なかでも、70%〜90%の範囲内であることが好ましい。
サイズおよび形状が制御された治療用細胞フラグメントを得ることができるとの本発明の効果をより効果的に発揮することができるからである。
【0031】
本発明に用いられる刺激応答性領域の種類としては、1種類のみであっても良く、異なる刺激に応答する複数の刺激応答性領域を含むものであっても良い。
【0032】
本発明に用いられる刺激応答性領域は、上記細胞非接着領域により囲まれるもの、すなわち、上記細胞非接着領域が上記刺激応答性領域の周囲に配置され、外周に上記細胞非接着領域との境界である非接着境界を有するものである。
ここで、上記非接着境界は、上記刺激応答性領域に刺激を与えた際に、上記非接着境界に沿って、上記治療用細胞フラグメントを上記刺激応答性領域から剥離させることができるものであれば特に限定されるものではない。
このような非接着境界は、通常、平面視上、上記細胞非接着領域と接しているが、例えば、上記刺激応答性領域および細胞非接着領域の間に、上記刺激応答性領域に刺激を与えた際に、上記非接着境界に沿って、上記治療用細胞フラグメントを剥離させることができる程度の幅で形成された細胞接着領域等の他の領域が存在する箇所も含むものである。
本発明においては、なかでも、平面視上、上記細胞非接着領域と接する箇所であること、すなわち、上記刺激応答性領域および細胞非接着領域の間に他の領域を含まない箇所であることが好ましい。上記治療用細胞フラグメントを安定的に形成することができるからである。
【0033】
本発明における刺激応答性領域の外周に形成される非接着境界の位置としては、上記刺激応答性領域に刺激を与えた際に、上記治療用細胞フラグメントを上記刺激応答性領域から安定的に剥離できるものであれば良く、上記刺激応答性領域の外周の少なくとも一部に形成されるものとすることができる。
本発明においては、なかでも、上記刺激応答性領域の全外周に形成されるものであることが好ましい。上記治療用細胞フラグメントを上記刺激応答性領域の形状で安定的に剥離することができるからである。
【0034】
本発明に用いられる刺激応答性領域の上記細胞非接着領域に対する高さとしては、上記細胞フラグメントを安定的に形成可能であれば特に限定されるものではないが、上記刺激応答性領域および細胞非接着領域が同一の高さ、すなわち同一平面上に形成されるものであっても良く、異なるものであっても良い。
【0035】
(2)刺激応答性層
本発明に用いられる刺激応答性層は、上記刺激応答性材料を含み、平面視上、露出した表面である刺激応答性領域を有するものである。
【0036】
(a)刺激応答性材料
本発明に用いられる刺激応答性材料としては、刺激の有無により細胞接着性が変化し、培養する細胞の接着および剥離を行なうことができる刺激応答性材料を含むものであれば特に限定されるものではなく、例えば、温度、光、pH、電位および磁力によりそれぞれ細胞接着性が変化する温度応答性材料、光応答性材料、pH応答性材料、電位応答性材料、および磁力応答性材料等を挙げることができる。
本発明においては、なかでも、温度応答性材料であることが好ましい。刺激の付与が容易だからである。
【0037】
本発明に用いられる刺激応答性材料の細胞接着性の変化としては、少なくとも、細胞接着性を有する状態から細胞非接着性を有する状態に変化することができるものであれば特に限定されるものではなく、可逆的に変化するものであっても良く、非可逆的に変化するものであっても良く、用途によって選択されるものである。
【0038】
本発明に用いられる刺激応答性材料の上記刺激応答性層中の含有量としては、刺激により上記刺激応答性層の表面である刺激応答性領域に所望の接着性の変化を得られるものであれば特に限定されるものではなく、上記材料の種類等によって異なるものである。
【0039】
本発明において刺激応答性層に含まれる刺激応答性材料の種類としては、1種類であっても良く、2種以上含むものであっても良い。
【0040】
本発明に用いられる温度応答性材料は、温度変化により、細胞接着性が変化するものであれば特に限定されるものではない。
本発明においては、上記温度応答性材料の細胞接着性を発揮する温度領域が、10℃〜45℃の範囲内であることが好ましく、なかでも、33℃〜40℃の範囲内であることが好ましい。上記温度領域が上述の範囲内であることにより、細胞を安定的に培養することができるからである。
【0041】
本発明における温度応答性材料の細胞非接着性を発揮する温度領域が、1℃〜36℃の範囲内であることが好ましく、なかでも、4℃〜32℃の範囲内であることが好ましい。上記温度領域が上述の範囲内であることにより、細胞へのダメージの少ないものとすることができるからである。
【0042】
このような本発明に用いられる温度応答性材料としては、具体的には、ポリ−N−イソプロピルアクリルアミド(PIPAAm)、ポリ−N−n−プロピルアクリルアミド、ポリ−N−n−プロピルメタクリルアミド、ポリ−N−エトキシエチルアクリルアミド、ポリ−N−テトラヒドロフルフリルアクリルアミド、ポリ−N−テトラヒドロフルフリルメタクリルアミド、及び、ポリ−N,N−ジエチルアクリルアミド等を挙げることができ、なかでもPIPAAm、ポリーN−n―プロピルメタクリルアミド、ポリーN,N−ジエチルアクリルアミドを好ましく用いることができ、特に、PIPAAmを好ましく用いることができる。細胞の培養に適した温度において細胞接着性を有し、細胞へのダメージの少ない温度で細胞非接着性を発現することから、上記細胞フラグメントを安定的に回収することができるからである。
また、本発明においては、上記温度応答性材料が1種類のみからなるものであっても良く、2種類以上含むものであっても良い。また、温度領域の調整するため、上記温度応答性材料同士および/またはその他のポリマーと共重合したものを用いるものであっても良い。
【0043】
本発明に用いられる光応答性材料としては、光照射の有無により細胞接着性が変化するものであれば特に限定されるものではなく、例えば、特開2005−210936号公報に開示されるような、光触媒や、アゾベンゼン、ジアリールエテン、スピロピラン、スピロオキサジン、フルギドおよびロイコ色素等の光応答成分を含むものを用いることができる。
【0044】
本発明に用いられる電位応答性材料としては、電位の印加により、細胞接着性が変化するものであれば特に限定されるものではなく、例えば、特開2008−295382号公報に開示されるような、電極と、RGD配列を含むペプチド等の細胞接着性部分を有し、上記電極表面にチオレートを介して結合するアルカンチオール、システイン、アルカンジスルフィド等のスペーサ物質とを有するものを挙げることができる。
【0045】
本発明に用いられる磁力応答性材料としては、磁力の付与・除去により細胞接着性が変化するものであれば特に限定されるものではなく、例えば、特開2005−312386号公報に開示されるような、フェライト等の磁性粒子を正電荷リポソームに封入した磁性粒子封入正電荷リポソームを挙げることができる。
【0046】
(b)刺激応答性層
本発明に用いられる刺激応答性層は、少なくとも上記刺激応答性材料を含むものである。
本発明においては、上記刺激応答性を阻害しない範囲内において、必要に応じて、レベリング剤、可塑剤、界面活性剤、消泡剤、増感剤等の添加剤や、ポリビニルアルコール、不飽和ポリエステル、アクリル樹脂、ポリエチレン、ジアリルフタレート、エチレンプロピレンジエンモノマー、エポキシ樹脂、フェノール樹脂、ポリウレタン、メラミン樹脂、ポリカーボネート、ポリ塩化ビニル、ポリアミド、ポリイミド、スチレンブタジエンゴム、クロロプレンゴム、ポリプロピレン、ポリブチレン、ポリスチレン、ポリ酢酸ビニル、ナイロン、ポリエステル、ポリブタジエン、ポリベンズイミダゾール、ポリアクリルニトリル、エピクロルヒドリン、ポリサルファイド、ポリイソプレンや、ポリエチレングリコール、MPCポリマー(商品名)等の両性イオン高分子等のバインダー樹脂を含むものであっても良い。
【0047】
本発明に用いられる刺激応答性層の膜厚としては、刺激応答性を発揮することができるものであれば特に限定されるものではなく、具体的には、0.5nm〜 300nmの範囲内であることが好ましく、なかでも1nm〜100nmの範囲内であることが好ましい。
【0048】
本発明に用いられる刺激応答性層の形成方法としては、所望のパターンに形成可能であれば特に限定されるものではない。
具体的には、上記刺激応答性材料を含む刺激応答性材料組成物をスピンコート等の公知の塗布方法を用いて塗布し、フォトリソ法によりパターニングする方法や、グラビア印刷やフレキソ印刷、スクリーン印刷、インクジェット法などの公知のパターン塗布法を用いて上記刺激応答性材料組成物をパターン状に塗布する方法を挙げることができる。
また、上記刺激応答性層が、刺激応答性材料として光触媒等の無機物のみからなるものである場合には、スパッタリング法、CVD法、真空蒸着法等の真空製膜法を用いる方法を挙げることができる。均一な膜厚の層とすることができるからである。
【0049】
2.細胞非接着領域
本発明に用いられる細胞非接着領域は、上記細胞非接着材料を含む細胞非接着層の表面のうち、露出した範囲であり、細胞非接着性を有するものである。
【0050】
(1)細胞非接着領域
本発明に用いられる細胞非接着領域は、少なくとも上記刺激応答性領域を囲むものを含むものである。
【0051】
このような細胞非接着領域の細胞接着性の程度としては、所望の細胞非接着性を示すものであれば特に限定されるものではなく、上記刺激応答性領域が細胞非接着性を発現している場合の細胞接着性と同様とすることができる。
【0052】
本発明に用いられる細胞非接着領域の形成箇所としては、少なくとも上記刺激応答性領域を囲む箇所を含むものであれば特に限定されるものではなく、例えば、図4に例示するように、上記刺激応答性領域内に形成されるものであっても良い。
なお、図4中の符号については、図1のものと同一の部材を示すものであるので、ここでの説明は省略する。
【0053】
本発明に用いられる細胞非接着領域の種類としては、1種類のみであっても良く、異なる細胞非接着材料を含む複数の細胞非接着領域を含むものであっても良い。
【0054】
本発明に用いられる細胞非接着領域の上記刺激応答性領域との非接着境界からの幅としては、上記刺激応答性領域の形状に細胞を接着させ培養することができるものであれば良く、例えば、5μm以上であることが好ましく、なかでも、10μm以上であることが好ましい。上記幅が上述の範囲であることにより、上記細胞非接着領域上に細胞が増殖することを安定的に抑制することができるからである。
【0055】
(2)細胞非接着層
本発明に用いられる細胞非接着層は、細胞非接着材料を含むものである。
このような細胞非接着材料としては、細胞と非接着性を有するものであれば良く、例えば、撥水性または撥油性を有する材料や、超親水性を有する材料も用いることができる。具体的には、ジエチレングリコール、トリエチレングリコール、テトラエチレングリコール、ポリエチレングリコール、ポリエチレングリコールジアクリレート、ポリエチレングリコールメタクリレート等を用いたエチレングリコール系材料、デシルメトキシシランなどの長鎖アルキル系材料、フルオロアルキルシランなどのフッ素系材料、シリコンなどの撥水性材料、ポリビニルアルコール(PVA)、ポリアクリルアミドなどの親水性材料、MPCポリマー等のリン脂質材料、BSAタンパク等が挙げられる。
本発明においては、なかでも、エチレングリコール系材料を好ましく用いることができる。細胞との優れた細胞非接着性および細胞毒性をほとんど示さないことにより、上記治療用細胞フラグメントをパターン精度良く形成することができるからである。
【0056】
本発明に用いられる細胞非接着層が含有可能な添加剤やバインダー樹脂、ならびに膜厚および形成方法としては、上記「1.刺激応答性領域」の項に記載の内容と同様とすることができる。
【0057】
3.治療用細胞フラグメント
本発明の治療用細胞フラグメント回収用基材により上記刺激応答性領域上で形成される治療用細胞フラグメントは、上記細胞同士が結合しているものであり、上記刺激応答性領域から剥離した場合であっても、上記細胞同士が結合した状態を維持できるものである。
また、このよう治療用細胞フラグメントを構成する細胞としては、血球系等の非接着性細胞、細胞間結合の弱い細胞以外なら、生体に存在するあらゆる組織とそれに由来する細胞を用いることができる。
具体的には、生体内の各組織、臓器を構成する上皮細胞や内皮細胞、収縮性を示す骨格筋細胞、平滑筋細胞、心筋細胞、神経系を構成するニューロン、グリア細胞、線維芽細胞、歯根膜細胞、子宮内膜由来細胞、血管系細胞、軟骨細胞、骨細胞、生体の代謝に関係する肝実質細胞、非肝実質細胞や脂肪細胞、がん細胞、分化能を有する細胞として、種々組織に存在する幹細胞、さらには骨髄細胞、ES細胞、iPS細胞、幹細胞、各種前駆細胞、ES細胞やiPS細胞から分化誘導した種種の細胞等を用いることができる。
その中でも、ヒト由来の間葉系幹細胞を使用するのが好ましい。ヒト由来の間葉系幹細胞は再生医療の標準的なモデル細胞としてよく利用されることが多いためである。
【0058】
4.治療用細胞フラグメント回収用基材
本発明の治療用細胞フラグメント回収用基材は、少なくとも、上記刺激応答性領域および細胞非接着領域を含むものである。
本発明においては、既に説明した図2に示すように、上記刺激応答性領域および細胞非接着領域を構成する刺激応答性層および細胞非接着層を支持する基材等のその他の構成を含むものであっても良い。
【0059】
このような基材としては、上記刺激応答性層および細胞非接着層等を支持することができるものであれば特に限定されるものではない。
本発明において上記基材の材料としては、ポリエチレンテレフタレート(PET)、ポリスチレン(PS)、ポリカーボネート(PC)、TAC(トリアセチルセルロース)、ポリイミド(PI)、ナイロン(Ny)、低密度ポリエチレン(LDPE)、中密度ポリエチレン(MDPE)、塩化ビニル、塩化ビニリデン、ポリフェニレンサルファイド、ポリエーテルサルフォン、ポリエチレンナフタレート、ポリプロピレン、ウレタンアクリレートなどのアクリル系材料、セルロース、ガラス等が挙げられる。ポリ乳酸、ポリグリコール酸、ポリカプロラクタン、もしくはその共重合体のような生分解性ポリマーであってもよい。また、基材が多孔質なものであってもよい。
本発明においては、なかでも、ポリエチレンテレフタレート、ポリスチレン、ポリカーボネートを好ましく用いることができ、特に、ポリエチレンテレフタレートを好ましく用いることができる。透明性、寸法安定性、機械的性質、電気的性質、耐薬品性等の性質に優れているからである。
【0060】
本発明における基材の膜厚としては、上記刺激応答性層等を安定的に支持することができるものであれば特に限定されるものではないが、例えば、10μm〜1000μmの範囲内、好ましくは、50μm〜200μmの範囲内である。
【0061】
また、本発明における基材の形状としては、板状であっても良く、ペトリディッシュやマルチウェルプレートのような凹状であっても良い。
【0062】
また、図5に例示するように、上記刺激応答性層1が、上記細胞非接着層2を支持する基材として用いられるように、上記刺激応答性層または上記細胞非接着層が、他の層を支持する基材とするものであっても良い。
【0063】
さらに、必要に応じて、上記各層を接着する接着層等の露出表面を有さない他の層や、他の領域となる露出表面を有する他の層を含むものであっても良い。
【0064】
本発明の治療用細胞フラグメント回収用基材の製造方法としては、上記刺激応答性領域等を安定的に形成できる方法であれば特に限定されるものではなく、例えば、上記基材上に、上記刺激応答性層および細胞非接着層をこの順で形成する方法を挙げることができる。
【0065】
本発明の治療用細胞フラグメント回収用基材の用途としては、移植等の治療用の細胞フラグメントの製造に用いられ、なかでも、サイズおよび形状が制御されることが要求される治療用の細胞フラグメントの製造に好適に用いることができる。
【0066】
B.継代用細胞フラグメント回収用基材
次に、本発明の継代用細胞フラグメント回収用基材について説明する。
本発明の継代用細胞フラグメント回収用基材は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域の周囲が、上記細胞非接着領域により囲まれていることを特徴とするものである。
【0067】
このような継代用細胞フラグメント回収用基材を図を参照して説明する。本発明の継代用細胞フラグメント回収用基材としては、既に説明した図1および2に示すものと同様とすることができる。
【0068】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域への刺激の付与により、任意のサイズおよび形状に制御された継代用細胞フラグメントを容易に回収することができる。このため、継代操作を簡便なものとすることができる。また、トリプシン等のタンパク質分解酵素の使用を不要とすることができるため、上記細胞を安定的に増殖させることができる。
また、サイズおよび形状が制御されているため、このような継代用細胞フラグメントを用いて継代した場合には、上記細胞の増殖を精度良くコントロールでき、安定的に培養することができる。
このようなことから、例えば、自動培養装置においてこのような継代用細胞フラグメント回収用基材を用いた場合には、安定的に細胞を増殖、培養することができる。
【0069】
本発明の継代用細胞フラグメント回収用基材は上記刺激応答性領域および細胞非接着領域を少なくとも含むものである。
なお、このような刺激応答性領域、細胞非接着領域、得られる継代用細胞フラグメント、その他の構成、製造方法等については、上記「A.治療用細胞フラグメント回収用基材」の項に記載の内容と同様とすることができるので、ここでの説明は省略する。
【0070】
本発明の継代用細胞フラグメント回収用基材の用途としては、細胞の培養・増殖に用いられ、なかでも、簡便性および安定性が要求される細胞の培養・増殖や、自動培養装置等に好適に用いられる。
【0071】
C.治療用細胞フラグメントの製造方法
次に、本発明の治療用細胞フラグメントの製造方法について説明する。
本発明の治療用細胞フラグメントの製造方法は、上述の治療用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記治療用細胞フラグメントを回収する回収工程と、を有することを特徴とするものである。
【0072】
このような本発明の治療用細胞フラグメントの製造方法について図を参照して説明する。図6は、本発明の治療用細胞フラグメントの製造方法の一例を示す工程図である。図6に例示するように、本発明の治療用細胞フラグメントの製造方法は、上記治療用細胞フラグメント回収用基材10を準備し、上記刺激応答性層1の露出した表面である刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し(図6(a))、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメント21を形成し(図6(b))、上記刺激応答性領域に刺激を与え細胞非接着性を発現させ(図6(c))、上記刺激応答性領域から剥離した上記治療用細胞フラグメント21を回収するものである(図6(d))。
なお、この例において、図6(a)および(b)が細胞フラグメント形成工程であり、図6(c)が刺激付与工程であり、図6(d)が回収工程である。
【0073】
本発明によれば、上記治療用細胞フラグメント回収用基材を用いることにより、サイズおよび形状が制御された治療用細胞フラグメントを容易に得ることができる。したがって、治療等の効果を再現性良く発揮することができる。
【0074】
本発明の治療用細胞フラグメントの製造方法は、細胞フラグメント形成工程、刺激付与工程および回収工程を少なくとも有するものである。
以下、本発明の治療用細胞フラグメントの製造方法の各工程について詳細に説明する。
【0075】
1.細胞フラグメント形成工程
本発明における細胞フラグメント形成工程は、上述の治療用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する工程である。
【0076】
本工程において、上記刺激応答性領域に細胞接着性を発現させる方法としては、上記刺激応答性領域を構成する刺激応答性材料の種類により異なるものであり、上述の細胞接着性を発現させることができる方法であれば特に限定されるものではない。
具体的には、上記刺激応答性材料がPIPAAmである場合には、上記刺激応答性領域を32℃より高い温度条件とする方法が挙げられる。
【0077】
本工程において上記細胞を播種する方法としては、上記刺激応答性領域上に均一に細胞を播種する方法であれば特に限定されるものではなく、一般的な播種方法を用いることができる。例えば、上記治療用細胞フラグメント回収用基材を培地中に浸漬させた状態で、上記細胞を播種する方法を挙げることができる。
【0078】
本工程において上記細胞を培養する方法としては、上記刺激応答性領域に接着した1以上の細胞からなる治療用細胞フラグメントを形成することができる方法であれば特に限定されるものではなく、一般的な培養方法を用いることができる。
【0079】
本工程において形成される治療用細胞フラグメントとしては、上記「A.治療用細胞フラグメント回収用基材」の項に記載の内容と同様とすることができる。
【0080】
2.刺激付与工程
本発明における刺激付与工程は、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる工程である。
【0081】
本工程において上記刺激応答性領域に刺激を与え、細胞非接着性を発現させる方法としては、上記刺激応答性領域に細胞非接着性を発現させ、上記刺激応答性領域から上記治療用細胞フラグメントを剥離させることができる方法であれば良く、上記刺激応答性領域の種類により異なるものである。
具体的には、上記刺激応答性材料がPIPAAmである場合には、上記治療用細胞フラグメントが付着した治療用細胞フラグメント回収用基材を、32℃以下の温度に設定されたインキュベーター内に静置する方法等を用いることができる。
【0082】
また、本工程においては、上記刺激応答性領域に刺激を与えた後に、上記刺激応答性領域にピペッティング等の外部応力を加える処理を行うものであっても良い。上記治療用細胞フラグメントをより安定的に剥離させることができるからである。
【0083】
3.回収工程
本発明における回収工程は、上記刺激応答性領域から剥離した上記治療用細胞フラグメントを回収する工程である。
【0084】
本工程において、上記治療用細胞フラグメントを回収する方法としては、上記治療用細胞フラグメント回収用基材と、上記治療用細胞フラグメントと、をそれぞれ分離することができる方法であれば良く、例えば、上記治療用細胞フラグメントが接着可能な回収用基材に上記刺激応答性領域から剥離した治療用細胞フラグメントを接着させる方法や、上記治療用細胞フラグメントを培地と共に吸引する方法等を挙げることができる。
本発明においては、なかでも、上記治療用細胞フラグメントを培地と共に吸引する方法であることが好ましい。培地に懸濁した懸濁液として回収できるため、移植等の治療への利用が容易だからである。
【0085】
4.その他
本発明の治療用細胞フラグメントの製造方法は、細胞フラグメント形成工程、刺激付与工程および回収工程を少なくとも有する。
【0086】
D.継代用細胞フラグメントの製造方法
次に、継代用細胞フラグメントの製造方法について説明する。
本発明の継代用細胞フラグメントの製造方法は、上述の継代用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる継代用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記継代用細胞フラグメントを回収する回収工程と、を有することを特徴とするものである。
【0087】
このような本発明の継代用細胞フラグメントの製造方法としては、例えば、既に説明した図6と同様とすることができる。
【0088】
本発明によれば、上記継代用細胞フラグメント回収用基材を用いることにより、サイズおよび形状が制御された継代用細胞フラグメントを容易に得ることができる。
【0089】
本発明の継代用細胞フラグメントの製造方法は、細胞フラグメント形成工程、刺激付与工程および回収工程を少なくとも有するものである。
なお、本発明の継代用細胞フラグメントの製造方法に含まれる各工程については、上記「C.治療用細胞フラグメントの製造方法」の項に記載の内容と同様であるので、ここでの説明は省略する。
【0090】
なお、本発明は、上記実施形態に限定されるものではない。上記実施形態は、例示であり、本発明の特許請求の範囲に記載された技術的思想と実質的に同一な構成を有し、同様な作用効果を奏するものは、いかなるものであっても本発明の技術的範囲に包含される。
【実施例】
【0091】
以下、本発明について実施例および比較例を用いて具体的に説明する。
【0092】
[実施例1]
(1)温度応答性フィルムの作製
N−イソプロピルアクリルアミドを、最終濃度20重量%になるようにイソプロピルアルコール(IPA)に溶解させた。市販の易接着性ポリエチレンテレフタレートフィルム(三光産業社より入手、透明50−Fセパ1090)(以下において「易接着PET」と略することがある)を調達し、これを10cm角に切断した。ここに前記溶液を、易接着PETの易接着面に展開し、ミヤバーでコーティングした。電子線照射装置(岩崎電気社製)を用いて該サンプル上に電子線照射を行い、該溶液をグラフト重合した。このときの電子線照射線量は300kGyであった。
【0093】
(2)細胞非接着層の形成
メタクリロキシシラン(モメンティブパフォーマンスマテリアルズ社より入手、TSL8370)を用意し、これをイソプロピルアルコール(IPA)で0.1重量%になるように希釈した。
前記で得られた温度応答性フィルムを、ガラスにテープで固定し、スピンナー(ミカサ製)を用いて、メタクリロキシシランをコーティングし、シラン処理を行った。
【0094】
次いで、ポリエチレングリコールジアクリレート(分子量300、アルドリッチ社より入手)が最終濃度50重量%になるように、純水で希釈し、ここに、重合開始剤として、2−ヒドロキシ−4‘−(2−ヒドロオキシエトキシ)−2−メチルプロピオフェノン(アルドリッチ社より入手)を最終濃度1重量%になるように加えた。この溶液をスターラーで15分間攪拌した。
これをシラン処理した温度応答性フィルム上に1mL展開し、下記表の条件でスピンコートを実施した。その後、フォトマスクを用いて、露光装置で150mJのエネルギーで処理した。フォトマスクデザインは、刺激応答性領域(温度応答性領域)が200μm角のパッチが間隔200μmで配列するように設計されたものを使用した。
その後、シラン処理基材上に、細胞非接着層としてポリエリレングリコールジアクリレートが固定化されていることを目視で確認した。
【0095】
(3)細胞フラグメント回収用基材の作製
このようにして得られた培養支持体ツールを、20mmφに切り出し、粘着層を露出させ、35mmφポリスチレンディッシュ(ベクトンディッキンソン社製)底面に貼り付け、細胞フラグメント回収用基材とした。
【0096】
(4)細胞フラグメントの形成
実施例で得られた細胞フラグメント回収用基材を70%エタノールにて滅菌した。滅菌時間は1時間とした。
その後、ヒト由来間葉系幹細胞(hMSC)を4×105cells/cm2播種し、7日間培養した。7日後に、位相差顕微鏡で観察したところ、200μm角の複数の細胞からなる細胞フラグメントが間隔200μmで得られることを確認した。また、接眼10倍、対物4倍の倍率で、200μm角の細胞フラグメントが1視野に16個含まれるように位相差像を取得し、それぞれのフラグメントに含まれる細胞数を計測したところ平均7.5個(標準偏差0.9)であった。
【0097】
(5)細胞フラグメントの回収
その後、上記細胞フラグメント回収用基材を37度インキュベーターから25度の低温インキュベーターに移し、25分静置後、ピペッティングを10回程度実施することにより、上記刺激応答性領域(温度応答性領域)に刺激を与え、上記細胞フラグメントを回収した。得られた、細胞フラグメントについて、位相差顕微鏡を用いて測定した結果、フラグメントのサイズは30μmφであり、サイズおよび形状がほぼ同一の細胞フラグメントが回収できたことが確認できた。
【0098】
[比較例1]
(1)温度応答性フィルムの作製
N−イソプロピルアクリルアミドを、最終濃度20重量%になるようにイソプロピルアルコール(IPA)に溶解させた。市販の易接着性ポリエチレンテレフタレートフィルム(三光産業社より入手、透明50−Fセパ1090)(以下において「易接着PET」と略することがある)を調達し、これを10cm角に切断した。ここに前記溶液を、易接着PETの易接着面に展開し、ミヤバーでコーティングした。電子線照射装置(岩崎電気社製)を用いて該サンプル上に電子線照射を行い、該溶液をグラフト重合した。このときの電子線照射線量は300kGyであった。
【0099】
(2)細胞フラグメント回収用基材の作製
このようにして得られた培養支持体ツールを、20mmφに切り出し、粘着層を露出させ、35mmφポリスチレンディッシュ(ベクトンディッキンソン社製)底面に貼り付け、細胞フラグメント回収用基材とした。
【0100】
(3)細胞シートの形成
実施例で得られた細胞フラグメント回収用基材を70%エタノールにて滅菌した。滅菌時間は1時間とした。
その後、ヒト由来間葉系幹細胞(hMSC)を4×105cells/cm2播種し、7日間培養した。7日後に、位相差顕微鏡で観察したところ、hMSCがシート状で得られることを確認した。
【0101】
(4)細胞フラグメントの回収
クリーンベンチ内で、培養液を吸引しhMSCシートの上に滅菌された金網を押し当て、その後培養液を加え、室温で25分静置した後にピペッティングを10回実施することにより、上記刺激応答性領域(温度応答性領域)に刺激を与え、上記細胞フラグメントを回収した。得られた、細胞フラグメントについて、位相差顕微鏡を用いて測定した結果、フラグメントのサイズは15μmφ〜150μmφであり、細胞フラグメントのサイズおよび形状は不揃いであった。
【0102】
[比較例2]
(1)温度応答性フィルムの作製
N−イソプロピルアクリルアミドを、最終濃度20重量%になるようにイソプロピルアルコール(IPA)に溶解させた。市販の易接着性ポリエチレンテレフタレートフィルム(三光産業社より入手、透明50−Fセパ1090)(以下において「易接着PET」と略することがある)を調達し、これを10cm角に切断した。ここに前記溶液を、易接着PETの易接着面に展開し、ミヤバーでコーティングした。電子線照射装置(岩崎電気社製)を用いて該サンプル上に電子線照射を行い、該溶液をグラフト重合した。このときの電子線照射線量は300kGyであった。
【0103】
(2)細胞非接着層の形成
メタクリロキシシラン(モメンティブパフォーマンスマテリアルズ社より入手、TSL8370)を用意し、これをイソプロピルアルコール(IPA)で0.1重量%になるように希釈した。
前記で得られた温度応答性フィルムを、ガラスにテープで固定し、スピンナー(ミカサ製)を用いて、メタクリロキシシランをコーティングし、シラン処理を行った。
次いで、ポリエチレングリコールジアクリレート(分子量300、アルドリッチ社より入手)が最終濃度50重量%になるように、純水で希釈し、ここに、重合開始剤として、2−ヒドロキシ−4‘−(2−ヒドロオキシエトキシ)−2−メチルプロピオフェノン(アルドリッチ社より入手)を最終濃度1重量%になるように加えた。この溶液をスターラーで15分間攪拌した。
これをシラン処理した温度応答性フィルム上に1mL展開し、下記表の条件でスピンコートを実施した。その後、フォトマスクを用いて、露光装置で150mJのエネルギーで処理した。フォトマスクデザインは、刺激応答性領域(温度応答性領域)が200μm角のパッチが間隔200μmで配列するように設計されたものを使用した。
その後、シラン処理基材上に、細胞非接着層としてポリエリレングリコールジアクリレートが固定化されていることを目視で確認した。
【0104】
(3)細胞フラグメント回収用基材の作製
このようにして得られた培養支持体ツールを、20mmφに切り出し、粘着層を露出させ、35mmφポリスチレンディッシュ(ベクトンディッキンソン社製)底面に貼り付け、細胞フラグメント回収用基材とした。
【0105】
(4)細胞シートの形成
実施例で得られた細胞フラグメント回収用基材を70%エタノールにて滅菌した。滅菌時間は1時間とした。
その後、ヒト由来間葉系幹細胞(hMSC)を4×105cells/cm2播種し、7日間培養した。7日後に、位相差顕微鏡で観察したところ、200μm角の複数の細胞からなる細胞フラグメントが間隔200μmで得られることを確認した。また、接眼10倍、対物4倍の倍率で、200μm角の細胞フラグメントが1視野に16個含まれるように位相差像を取得し、それぞれのフラグメントに含まれる細胞数を計測したところ平均7.5個(標準偏差0.9)であった。
【0106】
(5)細胞フラグメントの回収
クリーンベンチ内で、培養液を吸引し、0.25%トリプシン-EDTA溶液を加え室温で5分処理した。その後位相差顕微鏡を用いて観察した結果、hMSCが細胞間接着が切断され、シングルセルとしてトリプシン溶液中に浮遊している様子が観察され、サイズおよび形状の揃った細胞フラグメントを得ることはできなかった。
【符号の説明】
【0107】
1 … 刺激応答性層
2 … 細胞非接着層
3 … 基材
10 … 細胞フラグメント回収用基材
11 … 刺激応答性領域
12 … 細胞非接着領域
21 … 細胞フラグメント
【技術分野】
【0001】
本発明は、治療効果を再現性良く発揮できる治療用細胞フラグメントを得ること、および、継代操作時に細胞を安定的に培養できる継代用細胞フラグメントを容易に得ることができる細胞フラグメント回収用基材に関するものである。
【背景技術】
【0002】
近年、細胞フラグメントが、再生医療などでしばしば用いられるようになってきている。
ここで、細胞フラグメントとは、細胞間結合で細胞同士が少なくとも単層で連結された細胞集合体である。
【0003】
このような細胞フラグメントの作製方法としては、支持体上に細胞を播種・培養し形成された細胞シートに、トリプシン等のタンパク質分解酵素を作用させ、支持体−細胞間および細胞−細胞間の結合が切断された細胞フラグメントを回収する方法や、支持体上に細胞を播種・培養し形成された細胞シートに金属製の網を押し当て、上記細胞シートを所定のサイズに分断する方法が開示されている(非特許文献1)。
しかしながら、このような方法で得られた細胞フラグメントを前臨床研究において実験動物への移植に用いた場合には、細胞間結合を物理的に切断しているため侵襲的であるだけでなく、サイズの不揃いなフラグメントしか得られず実験結果がばらつくといった問題があった。
【0004】
また、細胞の継代操作時に、タンパク質分解酵素を用いて培養容器等の支持体から細胞を剥離し、新しい支持体に剥離した細胞を植え継ぐ作業が行われる。
しかしながら、このようなタンパク質分解酵素を用いる方法では、タンパク質分解酵素の滴下、反応停止等の作業が必要であり作業が煩雑であるといった問題や、タンパク質分解酵素により細胞がダメージを受け、その後の増殖に悪影響が出る等の問題があった。また、タンパク質分解酵素の濃度、処理時間を厳密に管理できていない場合には、継代操作毎に細胞増殖速度にばらつきが出るといった問題があった。
【先行技術文献】
【非特許文献】
【0005】
【非特許文献1】Cardiovascular Reserch(2008)77,515-524
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明は、上記問題点に鑑みてなされたものであり、治療効果を再現性良く発揮できる細胞フラグメントを得ること、および、継代操作時に細胞を安定的に培養できる継代用細胞フラグメントを容易に得ることができる細胞フラグメント回収用基材を提供することを主目的とする。
【課題を解決するための手段】
【0007】
本発明者等は、上記課題を解決すべく研究を重ねた結果、従来のトリプシン等のタンパク質分解酵素を用いる方法や、金網等で細胞シートを分断する方法では、サイズや形状が不揃いな細胞フラグメントなり、このようなサイズおよび形状の不揃いな細胞フラグメントを用いた場合には、上記細胞フラグメントを前臨床研究における実験動物への移植に用いた際に細胞間結合を物理的に切断しているため侵襲的であるだけでなく、サイズの不揃いなフラグメントしか得られず実験結果がばらつくことを見出した。
また、継代操作時に、トリプシン等のタンパク質分解酵素により細胞−細胞間の結合を切断するが、このような処理により形成される細胞フラグメントのサイズおよび形状が不揃いなことにより、その後の細胞増殖にばらつきがでること、および、細胞が効率よく増殖できる細胞フラグメントのサイズ、すなわち、一つの細胞フラグメントに含まれる細胞の数が細胞毎に異なるものであることを見出し、本発明を完成させるに至ったのである。
【0008】
すなわち、本発明は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域が、上記細胞非接着領域により囲まれていることを特徴とする治療用細胞フラグメント回収用基材を提供する。
【0009】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域への刺激の付与により、任意のサイズおよび形状に制御された治療用細胞フラグメントを容易に回収することができる。
また、サイズおよび形状が制御されているため、このような治療用細胞フラグメントを用いた移植等による治療効果を再現性良く発揮することができる。
【0010】
本発明は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域が、上記細胞非接着領域により囲まれていることを特徴とする継代用細胞フラグメント回収用基材を提供する。
【0011】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域への刺激の付与により、任意のサイズおよび形状に制御された継代用細胞フラグメントを容易に回収することができる。このため、継代操作を簡便なものとすることができる。また、トリプシン等のタンパク質分解酵素の使用を不要とすることができるため、上記細胞を安定的に増殖させることができる。
また、サイズおよび形状が制御されているため、このような継代用細胞フラグメントを用いて継代した場合には、上記細胞の増殖を精度良くコントロールでき、安定的に培養することができる。
このようなことから、例えば、自動培養装置においてこのような継代用細胞フラグメント回収用基材を用いた場合には、安定的に細胞を増殖、培養することができる。
【0012】
本発明においては、上記刺激応答性領域が、温度変化により細胞接着性が変化する温度応答性材料を含むことが好ましい。刺激の付与が容易だからである。
【0013】
本発明においては、上記温度応答性材料が、ポリイソプロピルアクリルアミドであることが好ましい。細胞の培養に適した温度において細胞接着性を有し、細胞へのダメージの少ない温度で細胞非接着性を発現することから、上記細胞フラグメントを安定的に回収することができるからである。
【0014】
本発明は、上述の治療用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記治療用細胞フラグメントを回収する回収工程と、を有することを特徴とする治療用細胞フラグメントの製造方法を提供する。
また、本発明は、上述の継代用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる継代用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記継代用細胞フラグメントを回収する回収工程と、を有することを特徴とする継代用細胞フラグメントの製造方法を提供する。
【0015】
本発明によれば、上記治療用細胞フラグメント回収用基材および継代用細胞フラグメント回収用基材を用いることにより、サイズおよび形状が制御された上記治療用細胞フラグメントおよび継代用細胞フラグメントを容易に製造することができる。
【発明の効果】
【0016】
本発明は、治療効果を再現性良く発揮できる治療用細胞フラグメントを得ること、および、継代操作時に細胞を安定的に培養できる継代用細胞フラグメントを容易に得ることができる細胞フラグメント回収用基材を提供できるといった効果を奏する。
【図面の簡単な説明】
【0017】
【図1】本発明の治療用細胞フラグメント回収用基材の一例を示す概略平面図である。
【図2】図1のA−A線断面図である。
【図3】本発明の治療用細胞フラグメント回収用基材の他の例を示す概略平面図である。
【図4】本発明の治療用細胞フラグメント回収用基材の他の例を示す概略平面図である。
【図5】本発明の治療用細胞フラグメント回収用基材の他の例を示す概略断面図である。
【図6】本発明の治療用細胞フラグメントの製造方法の一例を示す工程図である。
【発明を実施するための形態】
【0018】
本発明は、治療用細胞フラグメント回収用基材およびそれを用いた治療用細胞フラグメントの製造方法、ならびに、継代用細胞フラグメント回収用基材およびそれを用いた継代用細胞フラグメントの製造方法に関するものである。
以下、本発明の治療用細胞フラグメント回収用基材、継代用細胞フラグメント回収用基材、治療用細胞フラグメントの製造方法、および継代用細胞フラグメントの製造方法について詳細に説明する。
【0019】
A.治療用細胞フラグメント回収用基材
まず、本発明の治療用細胞フラグメント回収用基材について説明する。
本発明の治療用細胞フラグメント回収用基材は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域が、上記細胞非接着領域により囲まれていることを特徴とするものである。
【0020】
このような本発明の治療用細胞フラグメント回収用基材について図を参照して説明する。図1は、本発明の治療用細胞フラグメント回収用基材の一例を示す概略平面図であり、図2は、図1のA−A線断面図である。
図1および2に例示するように、本発明の治療用細胞フラグメント回収用基材10は、刺激により細胞接着性が変化する刺激応答性材料を含む刺激応答性層1と、細胞非接着性を有する細胞非接着材料を含む細胞非接着層2と、を有し、上記刺激応答性層1の露出表面である刺激応答性領域11が上記細胞非接着層2の露出表面である細胞非接着領域12により囲まれているものである。また、上記刺激応答性層1および細胞非接着性層2を支持する基材3を有するものである。
【0021】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域に細胞を播種し、培養することにより治療用細胞フラグメントを形成した後に、上記刺激応答性領域へ刺激を付与することにより、任意のサイズおよび形状に制御された治療用細胞フラグメントを上記刺激応答性領域から容易に剥離し回収することができる。
また、サイズおよび形状が制御されているため、このような治療用細胞フラグメントを用いた場合には、従来のトリプシン等のタンパク質分解酵素や、金網を押し付ける方法により得られる細胞フラグメントを用いる場合と比較し、前臨床研究における実験動物への移植等の際に、サイズの揃ったフラグメントが得られるため実験の再現性が向上する効果が得られる。
【0022】
本発明の治療用細胞フラグメント回収用基材は、刺激応答性領域および細胞非接着性領域を少なくとも有するものである。
以下、本発明の治療用細胞フラグメント回収用基材の各構成について詳細に説明する。
【0023】
1.刺激応答性領域
本発明における刺激応答性領域は、刺激応答性材料を含む刺激応答性層の表面のうち、露出した範囲であり、上記細胞非接着領域により囲まれるものである。
【0024】
(1)刺激応答性領域
本発明における刺激応答性領域は、上記細胞非接着領域により囲まれているものであり、刺激により細胞接着性を変化させることにより培養する細胞の接着および剥離を行なうことができるものである。
【0025】
本発明における刺激応答性領域は、特定の刺激により細胞接着性が良好な細胞接着性を発現している状態から、細胞の接着性が低い性質である細胞非接着性を発現している状態に変化し得るものである。
ここで、上記刺激応答性領域が細胞接着性を発現しているとは、上記刺激応答性領域上で、細胞が接着、伸展しやすく、細胞接着伸展率が高い状態であることをいうものである。本発明において、このような細胞接着伸展率が高い状態としては、具体的には、細胞接着伸展率が60%以上である状態とすることができる。
本発明においては、なかでも、80%以上であることが好ましい。効率的に細胞を培養し、治療用細胞フラグメントを形成させることができるからである。
なお、本発明における細胞接着伸展率は、播種密度が4000cells/cm2以上30000cells/cm2未満の範囲内でウシ血管内皮細胞を播種し、37℃インキュベーター内(CO2濃度5%)に保管し、3時間以上経過し、倍加時間前に接着伸展している細胞の割合({(接着している細胞数)/(播種した細胞数)}×100(%))を表すものである。
また、上記細胞の播種は、10%FBS(血清)入りDMEM培地に懸濁させて培養基材上に播種し、その後、上記細胞ができるだけ均一に分布するよう、上記細胞が播種された培養基材をゆっくりと振とうすることにより行うものである。
さらに、細胞接着伸展率の測定は、測定直前に培地交換を行って接着していない細胞を除去した後に行い、細胞接着伸展率の測定個所としては、細胞の存在密度が特異的になりやすい箇所(例えば、存在密度が高くなりやすい所定領域の中央、存在密度が低くなりやすい所定領域の周縁)を除いて測定を行うものである。
【0026】
また、上記刺激応答性領域が細胞非接着性を発現している場合とは、上記刺激応答性領域上で細胞が接着、伸展しにくく、細胞接着伸展率が低い状態であることをいうものである。本発明において、このような細胞接着伸展率が低い状態としては、具体的には、上記細胞接着伸展率が5%以下である状態とすることができる。本発明においては、なかでも2%以下であることが好ましい。
したがって、上記刺激応答性領域に細胞を播種すると、細胞接着性を発現している際には細胞が上記刺激応答性領域に接着し、容易に治療用細胞フラグメントを形成することができ、細胞非接着性を発現している際には細胞が上記刺激応答性領域に接着することを阻害されるため、上記刺激応答性領域に接着していた治療用細胞フラグメントを容易に剥離し、回収することができるのである。
【0027】
本発明に用いられる刺激応答性領域の形状としては、安定的に治療用細胞フラグメントを回収することができるものであれば特に限定されるものではなく、例えば、既に説明した図1に示すような円形状や楕円形状、図3に例示するような多角形状、ライン状、格子状、星型等であってもよい。また、複数の形状を組み合わせたものであってもよい。
本発明においては、なかでも、円形状または六角形状以上の多角形であることが好ましく、特に、円形状であることが好ましい。上記刺激応答性領域に刺激を与えた際に、上記治療用細胞フラグメントを上記刺激応答性領域から安定的に剥離することができるからである。
【0028】
本発明に用いられる刺激応答性領域の一つあたりの面積としては、少なくとも1以上の細胞が接着することができ、上記治療用細胞フラグメントを安定的に回収できるものであれば特に限定されるものではないが、具体的には、200μm2〜100000μm2の範囲内であることが好ましく、1000μm2〜50000μm2の範囲内であることが好ましく、10000μm2〜40000μm2の範囲内であることが好ましい。上記刺激応答性領域に刺激を付与することにより、上記治療用細胞フラグメントを安定的に剥離し、回収することができるからである。
【0029】
本発明に用いられる刺激応答性領域の配置としては、上記治療用細胞フラグメントを安定的に回収することができるものであれば特に限定されるものではないが、上記治療用細胞フラグメントを安定的に得られる範囲で、最も多くの治療用細胞フラグメントを形成できるものであることが好ましい。一回の操作で、効率的に上記治療用細胞フラグメントを得ることができるからである。
【0030】
本発明に用いられる刺激応答性領域が占める割合としては、本発明の治療用細胞フラグメント回収用基材内の底面を100%とした場合に少なくとも50%以上含まれるものであれば特に限定されるものではないが、50%〜95%の範囲内であることが好ましく、なかでも、70%〜90%の範囲内であることが好ましい。
サイズおよび形状が制御された治療用細胞フラグメントを得ることができるとの本発明の効果をより効果的に発揮することができるからである。
【0031】
本発明に用いられる刺激応答性領域の種類としては、1種類のみであっても良く、異なる刺激に応答する複数の刺激応答性領域を含むものであっても良い。
【0032】
本発明に用いられる刺激応答性領域は、上記細胞非接着領域により囲まれるもの、すなわち、上記細胞非接着領域が上記刺激応答性領域の周囲に配置され、外周に上記細胞非接着領域との境界である非接着境界を有するものである。
ここで、上記非接着境界は、上記刺激応答性領域に刺激を与えた際に、上記非接着境界に沿って、上記治療用細胞フラグメントを上記刺激応答性領域から剥離させることができるものであれば特に限定されるものではない。
このような非接着境界は、通常、平面視上、上記細胞非接着領域と接しているが、例えば、上記刺激応答性領域および細胞非接着領域の間に、上記刺激応答性領域に刺激を与えた際に、上記非接着境界に沿って、上記治療用細胞フラグメントを剥離させることができる程度の幅で形成された細胞接着領域等の他の領域が存在する箇所も含むものである。
本発明においては、なかでも、平面視上、上記細胞非接着領域と接する箇所であること、すなわち、上記刺激応答性領域および細胞非接着領域の間に他の領域を含まない箇所であることが好ましい。上記治療用細胞フラグメントを安定的に形成することができるからである。
【0033】
本発明における刺激応答性領域の外周に形成される非接着境界の位置としては、上記刺激応答性領域に刺激を与えた際に、上記治療用細胞フラグメントを上記刺激応答性領域から安定的に剥離できるものであれば良く、上記刺激応答性領域の外周の少なくとも一部に形成されるものとすることができる。
本発明においては、なかでも、上記刺激応答性領域の全外周に形成されるものであることが好ましい。上記治療用細胞フラグメントを上記刺激応答性領域の形状で安定的に剥離することができるからである。
【0034】
本発明に用いられる刺激応答性領域の上記細胞非接着領域に対する高さとしては、上記細胞フラグメントを安定的に形成可能であれば特に限定されるものではないが、上記刺激応答性領域および細胞非接着領域が同一の高さ、すなわち同一平面上に形成されるものであっても良く、異なるものであっても良い。
【0035】
(2)刺激応答性層
本発明に用いられる刺激応答性層は、上記刺激応答性材料を含み、平面視上、露出した表面である刺激応答性領域を有するものである。
【0036】
(a)刺激応答性材料
本発明に用いられる刺激応答性材料としては、刺激の有無により細胞接着性が変化し、培養する細胞の接着および剥離を行なうことができる刺激応答性材料を含むものであれば特に限定されるものではなく、例えば、温度、光、pH、電位および磁力によりそれぞれ細胞接着性が変化する温度応答性材料、光応答性材料、pH応答性材料、電位応答性材料、および磁力応答性材料等を挙げることができる。
本発明においては、なかでも、温度応答性材料であることが好ましい。刺激の付与が容易だからである。
【0037】
本発明に用いられる刺激応答性材料の細胞接着性の変化としては、少なくとも、細胞接着性を有する状態から細胞非接着性を有する状態に変化することができるものであれば特に限定されるものではなく、可逆的に変化するものであっても良く、非可逆的に変化するものであっても良く、用途によって選択されるものである。
【0038】
本発明に用いられる刺激応答性材料の上記刺激応答性層中の含有量としては、刺激により上記刺激応答性層の表面である刺激応答性領域に所望の接着性の変化を得られるものであれば特に限定されるものではなく、上記材料の種類等によって異なるものである。
【0039】
本発明において刺激応答性層に含まれる刺激応答性材料の種類としては、1種類であっても良く、2種以上含むものであっても良い。
【0040】
本発明に用いられる温度応答性材料は、温度変化により、細胞接着性が変化するものであれば特に限定されるものではない。
本発明においては、上記温度応答性材料の細胞接着性を発揮する温度領域が、10℃〜45℃の範囲内であることが好ましく、なかでも、33℃〜40℃の範囲内であることが好ましい。上記温度領域が上述の範囲内であることにより、細胞を安定的に培養することができるからである。
【0041】
本発明における温度応答性材料の細胞非接着性を発揮する温度領域が、1℃〜36℃の範囲内であることが好ましく、なかでも、4℃〜32℃の範囲内であることが好ましい。上記温度領域が上述の範囲内であることにより、細胞へのダメージの少ないものとすることができるからである。
【0042】
このような本発明に用いられる温度応答性材料としては、具体的には、ポリ−N−イソプロピルアクリルアミド(PIPAAm)、ポリ−N−n−プロピルアクリルアミド、ポリ−N−n−プロピルメタクリルアミド、ポリ−N−エトキシエチルアクリルアミド、ポリ−N−テトラヒドロフルフリルアクリルアミド、ポリ−N−テトラヒドロフルフリルメタクリルアミド、及び、ポリ−N,N−ジエチルアクリルアミド等を挙げることができ、なかでもPIPAAm、ポリーN−n―プロピルメタクリルアミド、ポリーN,N−ジエチルアクリルアミドを好ましく用いることができ、特に、PIPAAmを好ましく用いることができる。細胞の培養に適した温度において細胞接着性を有し、細胞へのダメージの少ない温度で細胞非接着性を発現することから、上記細胞フラグメントを安定的に回収することができるからである。
また、本発明においては、上記温度応答性材料が1種類のみからなるものであっても良く、2種類以上含むものであっても良い。また、温度領域の調整するため、上記温度応答性材料同士および/またはその他のポリマーと共重合したものを用いるものであっても良い。
【0043】
本発明に用いられる光応答性材料としては、光照射の有無により細胞接着性が変化するものであれば特に限定されるものではなく、例えば、特開2005−210936号公報に開示されるような、光触媒や、アゾベンゼン、ジアリールエテン、スピロピラン、スピロオキサジン、フルギドおよびロイコ色素等の光応答成分を含むものを用いることができる。
【0044】
本発明に用いられる電位応答性材料としては、電位の印加により、細胞接着性が変化するものであれば特に限定されるものではなく、例えば、特開2008−295382号公報に開示されるような、電極と、RGD配列を含むペプチド等の細胞接着性部分を有し、上記電極表面にチオレートを介して結合するアルカンチオール、システイン、アルカンジスルフィド等のスペーサ物質とを有するものを挙げることができる。
【0045】
本発明に用いられる磁力応答性材料としては、磁力の付与・除去により細胞接着性が変化するものであれば特に限定されるものではなく、例えば、特開2005−312386号公報に開示されるような、フェライト等の磁性粒子を正電荷リポソームに封入した磁性粒子封入正電荷リポソームを挙げることができる。
【0046】
(b)刺激応答性層
本発明に用いられる刺激応答性層は、少なくとも上記刺激応答性材料を含むものである。
本発明においては、上記刺激応答性を阻害しない範囲内において、必要に応じて、レベリング剤、可塑剤、界面活性剤、消泡剤、増感剤等の添加剤や、ポリビニルアルコール、不飽和ポリエステル、アクリル樹脂、ポリエチレン、ジアリルフタレート、エチレンプロピレンジエンモノマー、エポキシ樹脂、フェノール樹脂、ポリウレタン、メラミン樹脂、ポリカーボネート、ポリ塩化ビニル、ポリアミド、ポリイミド、スチレンブタジエンゴム、クロロプレンゴム、ポリプロピレン、ポリブチレン、ポリスチレン、ポリ酢酸ビニル、ナイロン、ポリエステル、ポリブタジエン、ポリベンズイミダゾール、ポリアクリルニトリル、エピクロルヒドリン、ポリサルファイド、ポリイソプレンや、ポリエチレングリコール、MPCポリマー(商品名)等の両性イオン高分子等のバインダー樹脂を含むものであっても良い。
【0047】
本発明に用いられる刺激応答性層の膜厚としては、刺激応答性を発揮することができるものであれば特に限定されるものではなく、具体的には、0.5nm〜 300nmの範囲内であることが好ましく、なかでも1nm〜100nmの範囲内であることが好ましい。
【0048】
本発明に用いられる刺激応答性層の形成方法としては、所望のパターンに形成可能であれば特に限定されるものではない。
具体的には、上記刺激応答性材料を含む刺激応答性材料組成物をスピンコート等の公知の塗布方法を用いて塗布し、フォトリソ法によりパターニングする方法や、グラビア印刷やフレキソ印刷、スクリーン印刷、インクジェット法などの公知のパターン塗布法を用いて上記刺激応答性材料組成物をパターン状に塗布する方法を挙げることができる。
また、上記刺激応答性層が、刺激応答性材料として光触媒等の無機物のみからなるものである場合には、スパッタリング法、CVD法、真空蒸着法等の真空製膜法を用いる方法を挙げることができる。均一な膜厚の層とすることができるからである。
【0049】
2.細胞非接着領域
本発明に用いられる細胞非接着領域は、上記細胞非接着材料を含む細胞非接着層の表面のうち、露出した範囲であり、細胞非接着性を有するものである。
【0050】
(1)細胞非接着領域
本発明に用いられる細胞非接着領域は、少なくとも上記刺激応答性領域を囲むものを含むものである。
【0051】
このような細胞非接着領域の細胞接着性の程度としては、所望の細胞非接着性を示すものであれば特に限定されるものではなく、上記刺激応答性領域が細胞非接着性を発現している場合の細胞接着性と同様とすることができる。
【0052】
本発明に用いられる細胞非接着領域の形成箇所としては、少なくとも上記刺激応答性領域を囲む箇所を含むものであれば特に限定されるものではなく、例えば、図4に例示するように、上記刺激応答性領域内に形成されるものであっても良い。
なお、図4中の符号については、図1のものと同一の部材を示すものであるので、ここでの説明は省略する。
【0053】
本発明に用いられる細胞非接着領域の種類としては、1種類のみであっても良く、異なる細胞非接着材料を含む複数の細胞非接着領域を含むものであっても良い。
【0054】
本発明に用いられる細胞非接着領域の上記刺激応答性領域との非接着境界からの幅としては、上記刺激応答性領域の形状に細胞を接着させ培養することができるものであれば良く、例えば、5μm以上であることが好ましく、なかでも、10μm以上であることが好ましい。上記幅が上述の範囲であることにより、上記細胞非接着領域上に細胞が増殖することを安定的に抑制することができるからである。
【0055】
(2)細胞非接着層
本発明に用いられる細胞非接着層は、細胞非接着材料を含むものである。
このような細胞非接着材料としては、細胞と非接着性を有するものであれば良く、例えば、撥水性または撥油性を有する材料や、超親水性を有する材料も用いることができる。具体的には、ジエチレングリコール、トリエチレングリコール、テトラエチレングリコール、ポリエチレングリコール、ポリエチレングリコールジアクリレート、ポリエチレングリコールメタクリレート等を用いたエチレングリコール系材料、デシルメトキシシランなどの長鎖アルキル系材料、フルオロアルキルシランなどのフッ素系材料、シリコンなどの撥水性材料、ポリビニルアルコール(PVA)、ポリアクリルアミドなどの親水性材料、MPCポリマー等のリン脂質材料、BSAタンパク等が挙げられる。
本発明においては、なかでも、エチレングリコール系材料を好ましく用いることができる。細胞との優れた細胞非接着性および細胞毒性をほとんど示さないことにより、上記治療用細胞フラグメントをパターン精度良く形成することができるからである。
【0056】
本発明に用いられる細胞非接着層が含有可能な添加剤やバインダー樹脂、ならびに膜厚および形成方法としては、上記「1.刺激応答性領域」の項に記載の内容と同様とすることができる。
【0057】
3.治療用細胞フラグメント
本発明の治療用細胞フラグメント回収用基材により上記刺激応答性領域上で形成される治療用細胞フラグメントは、上記細胞同士が結合しているものであり、上記刺激応答性領域から剥離した場合であっても、上記細胞同士が結合した状態を維持できるものである。
また、このよう治療用細胞フラグメントを構成する細胞としては、血球系等の非接着性細胞、細胞間結合の弱い細胞以外なら、生体に存在するあらゆる組織とそれに由来する細胞を用いることができる。
具体的には、生体内の各組織、臓器を構成する上皮細胞や内皮細胞、収縮性を示す骨格筋細胞、平滑筋細胞、心筋細胞、神経系を構成するニューロン、グリア細胞、線維芽細胞、歯根膜細胞、子宮内膜由来細胞、血管系細胞、軟骨細胞、骨細胞、生体の代謝に関係する肝実質細胞、非肝実質細胞や脂肪細胞、がん細胞、分化能を有する細胞として、種々組織に存在する幹細胞、さらには骨髄細胞、ES細胞、iPS細胞、幹細胞、各種前駆細胞、ES細胞やiPS細胞から分化誘導した種種の細胞等を用いることができる。
その中でも、ヒト由来の間葉系幹細胞を使用するのが好ましい。ヒト由来の間葉系幹細胞は再生医療の標準的なモデル細胞としてよく利用されることが多いためである。
【0058】
4.治療用細胞フラグメント回収用基材
本発明の治療用細胞フラグメント回収用基材は、少なくとも、上記刺激応答性領域および細胞非接着領域を含むものである。
本発明においては、既に説明した図2に示すように、上記刺激応答性領域および細胞非接着領域を構成する刺激応答性層および細胞非接着層を支持する基材等のその他の構成を含むものであっても良い。
【0059】
このような基材としては、上記刺激応答性層および細胞非接着層等を支持することができるものであれば特に限定されるものではない。
本発明において上記基材の材料としては、ポリエチレンテレフタレート(PET)、ポリスチレン(PS)、ポリカーボネート(PC)、TAC(トリアセチルセルロース)、ポリイミド(PI)、ナイロン(Ny)、低密度ポリエチレン(LDPE)、中密度ポリエチレン(MDPE)、塩化ビニル、塩化ビニリデン、ポリフェニレンサルファイド、ポリエーテルサルフォン、ポリエチレンナフタレート、ポリプロピレン、ウレタンアクリレートなどのアクリル系材料、セルロース、ガラス等が挙げられる。ポリ乳酸、ポリグリコール酸、ポリカプロラクタン、もしくはその共重合体のような生分解性ポリマーであってもよい。また、基材が多孔質なものであってもよい。
本発明においては、なかでも、ポリエチレンテレフタレート、ポリスチレン、ポリカーボネートを好ましく用いることができ、特に、ポリエチレンテレフタレートを好ましく用いることができる。透明性、寸法安定性、機械的性質、電気的性質、耐薬品性等の性質に優れているからである。
【0060】
本発明における基材の膜厚としては、上記刺激応答性層等を安定的に支持することができるものであれば特に限定されるものではないが、例えば、10μm〜1000μmの範囲内、好ましくは、50μm〜200μmの範囲内である。
【0061】
また、本発明における基材の形状としては、板状であっても良く、ペトリディッシュやマルチウェルプレートのような凹状であっても良い。
【0062】
また、図5に例示するように、上記刺激応答性層1が、上記細胞非接着層2を支持する基材として用いられるように、上記刺激応答性層または上記細胞非接着層が、他の層を支持する基材とするものであっても良い。
【0063】
さらに、必要に応じて、上記各層を接着する接着層等の露出表面を有さない他の層や、他の領域となる露出表面を有する他の層を含むものであっても良い。
【0064】
本発明の治療用細胞フラグメント回収用基材の製造方法としては、上記刺激応答性領域等を安定的に形成できる方法であれば特に限定されるものではなく、例えば、上記基材上に、上記刺激応答性層および細胞非接着層をこの順で形成する方法を挙げることができる。
【0065】
本発明の治療用細胞フラグメント回収用基材の用途としては、移植等の治療用の細胞フラグメントの製造に用いられ、なかでも、サイズおよび形状が制御されることが要求される治療用の細胞フラグメントの製造に好適に用いることができる。
【0066】
B.継代用細胞フラグメント回収用基材
次に、本発明の継代用細胞フラグメント回収用基材について説明する。
本発明の継代用細胞フラグメント回収用基材は、刺激により細胞接着性が変化する刺激応答性領域と、細胞非接着性を有する細胞非接着領域と、を有し、上記刺激応答性領域の周囲が、上記細胞非接着領域により囲まれていることを特徴とするものである。
【0067】
このような継代用細胞フラグメント回収用基材を図を参照して説明する。本発明の継代用細胞フラグメント回収用基材としては、既に説明した図1および2に示すものと同様とすることができる。
【0068】
本発明によれば、上記細胞非接着領域により囲まれている刺激応答性領域を有することにより、上記刺激応答性領域への刺激の付与により、任意のサイズおよび形状に制御された継代用細胞フラグメントを容易に回収することができる。このため、継代操作を簡便なものとすることができる。また、トリプシン等のタンパク質分解酵素の使用を不要とすることができるため、上記細胞を安定的に増殖させることができる。
また、サイズおよび形状が制御されているため、このような継代用細胞フラグメントを用いて継代した場合には、上記細胞の増殖を精度良くコントロールでき、安定的に培養することができる。
このようなことから、例えば、自動培養装置においてこのような継代用細胞フラグメント回収用基材を用いた場合には、安定的に細胞を増殖、培養することができる。
【0069】
本発明の継代用細胞フラグメント回収用基材は上記刺激応答性領域および細胞非接着領域を少なくとも含むものである。
なお、このような刺激応答性領域、細胞非接着領域、得られる継代用細胞フラグメント、その他の構成、製造方法等については、上記「A.治療用細胞フラグメント回収用基材」の項に記載の内容と同様とすることができるので、ここでの説明は省略する。
【0070】
本発明の継代用細胞フラグメント回収用基材の用途としては、細胞の培養・増殖に用いられ、なかでも、簡便性および安定性が要求される細胞の培養・増殖や、自動培養装置等に好適に用いられる。
【0071】
C.治療用細胞フラグメントの製造方法
次に、本発明の治療用細胞フラグメントの製造方法について説明する。
本発明の治療用細胞フラグメントの製造方法は、上述の治療用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記治療用細胞フラグメントを回収する回収工程と、を有することを特徴とするものである。
【0072】
このような本発明の治療用細胞フラグメントの製造方法について図を参照して説明する。図6は、本発明の治療用細胞フラグメントの製造方法の一例を示す工程図である。図6に例示するように、本発明の治療用細胞フラグメントの製造方法は、上記治療用細胞フラグメント回収用基材10を準備し、上記刺激応答性層1の露出した表面である刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し(図6(a))、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメント21を形成し(図6(b))、上記刺激応答性領域に刺激を与え細胞非接着性を発現させ(図6(c))、上記刺激応答性領域から剥離した上記治療用細胞フラグメント21を回収するものである(図6(d))。
なお、この例において、図6(a)および(b)が細胞フラグメント形成工程であり、図6(c)が刺激付与工程であり、図6(d)が回収工程である。
【0073】
本発明によれば、上記治療用細胞フラグメント回収用基材を用いることにより、サイズおよび形状が制御された治療用細胞フラグメントを容易に得ることができる。したがって、治療等の効果を再現性良く発揮することができる。
【0074】
本発明の治療用細胞フラグメントの製造方法は、細胞フラグメント形成工程、刺激付与工程および回収工程を少なくとも有するものである。
以下、本発明の治療用細胞フラグメントの製造方法の各工程について詳細に説明する。
【0075】
1.細胞フラグメント形成工程
本発明における細胞フラグメント形成工程は、上述の治療用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する工程である。
【0076】
本工程において、上記刺激応答性領域に細胞接着性を発現させる方法としては、上記刺激応答性領域を構成する刺激応答性材料の種類により異なるものであり、上述の細胞接着性を発現させることができる方法であれば特に限定されるものではない。
具体的には、上記刺激応答性材料がPIPAAmである場合には、上記刺激応答性領域を32℃より高い温度条件とする方法が挙げられる。
【0077】
本工程において上記細胞を播種する方法としては、上記刺激応答性領域上に均一に細胞を播種する方法であれば特に限定されるものではなく、一般的な播種方法を用いることができる。例えば、上記治療用細胞フラグメント回収用基材を培地中に浸漬させた状態で、上記細胞を播種する方法を挙げることができる。
【0078】
本工程において上記細胞を培養する方法としては、上記刺激応答性領域に接着した1以上の細胞からなる治療用細胞フラグメントを形成することができる方法であれば特に限定されるものではなく、一般的な培養方法を用いることができる。
【0079】
本工程において形成される治療用細胞フラグメントとしては、上記「A.治療用細胞フラグメント回収用基材」の項に記載の内容と同様とすることができる。
【0080】
2.刺激付与工程
本発明における刺激付与工程は、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる工程である。
【0081】
本工程において上記刺激応答性領域に刺激を与え、細胞非接着性を発現させる方法としては、上記刺激応答性領域に細胞非接着性を発現させ、上記刺激応答性領域から上記治療用細胞フラグメントを剥離させることができる方法であれば良く、上記刺激応答性領域の種類により異なるものである。
具体的には、上記刺激応答性材料がPIPAAmである場合には、上記治療用細胞フラグメントが付着した治療用細胞フラグメント回収用基材を、32℃以下の温度に設定されたインキュベーター内に静置する方法等を用いることができる。
【0082】
また、本工程においては、上記刺激応答性領域に刺激を与えた後に、上記刺激応答性領域にピペッティング等の外部応力を加える処理を行うものであっても良い。上記治療用細胞フラグメントをより安定的に剥離させることができるからである。
【0083】
3.回収工程
本発明における回収工程は、上記刺激応答性領域から剥離した上記治療用細胞フラグメントを回収する工程である。
【0084】
本工程において、上記治療用細胞フラグメントを回収する方法としては、上記治療用細胞フラグメント回収用基材と、上記治療用細胞フラグメントと、をそれぞれ分離することができる方法であれば良く、例えば、上記治療用細胞フラグメントが接着可能な回収用基材に上記刺激応答性領域から剥離した治療用細胞フラグメントを接着させる方法や、上記治療用細胞フラグメントを培地と共に吸引する方法等を挙げることができる。
本発明においては、なかでも、上記治療用細胞フラグメントを培地と共に吸引する方法であることが好ましい。培地に懸濁した懸濁液として回収できるため、移植等の治療への利用が容易だからである。
【0085】
4.その他
本発明の治療用細胞フラグメントの製造方法は、細胞フラグメント形成工程、刺激付与工程および回収工程を少なくとも有する。
【0086】
D.継代用細胞フラグメントの製造方法
次に、継代用細胞フラグメントの製造方法について説明する。
本発明の継代用細胞フラグメントの製造方法は、上述の継代用細胞フラグメント回収用基材を準備し、上記刺激応答性領域が細胞接着性を発現している状態で、上記刺激応答性領域上に細胞を播種・培養し、上記刺激応答性領域に接着した少なくとも1以上の細胞からなる継代用細胞フラグメントを形成する細胞フラグメント形成工程と、上記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、上記刺激応答性領域から剥離した上記継代用細胞フラグメントを回収する回収工程と、を有することを特徴とするものである。
【0087】
このような本発明の継代用細胞フラグメントの製造方法としては、例えば、既に説明した図6と同様とすることができる。
【0088】
本発明によれば、上記継代用細胞フラグメント回収用基材を用いることにより、サイズおよび形状が制御された継代用細胞フラグメントを容易に得ることができる。
【0089】
本発明の継代用細胞フラグメントの製造方法は、細胞フラグメント形成工程、刺激付与工程および回収工程を少なくとも有するものである。
なお、本発明の継代用細胞フラグメントの製造方法に含まれる各工程については、上記「C.治療用細胞フラグメントの製造方法」の項に記載の内容と同様であるので、ここでの説明は省略する。
【0090】
なお、本発明は、上記実施形態に限定されるものではない。上記実施形態は、例示であり、本発明の特許請求の範囲に記載された技術的思想と実質的に同一な構成を有し、同様な作用効果を奏するものは、いかなるものであっても本発明の技術的範囲に包含される。
【実施例】
【0091】
以下、本発明について実施例および比較例を用いて具体的に説明する。
【0092】
[実施例1]
(1)温度応答性フィルムの作製
N−イソプロピルアクリルアミドを、最終濃度20重量%になるようにイソプロピルアルコール(IPA)に溶解させた。市販の易接着性ポリエチレンテレフタレートフィルム(三光産業社より入手、透明50−Fセパ1090)(以下において「易接着PET」と略することがある)を調達し、これを10cm角に切断した。ここに前記溶液を、易接着PETの易接着面に展開し、ミヤバーでコーティングした。電子線照射装置(岩崎電気社製)を用いて該サンプル上に電子線照射を行い、該溶液をグラフト重合した。このときの電子線照射線量は300kGyであった。
【0093】
(2)細胞非接着層の形成
メタクリロキシシラン(モメンティブパフォーマンスマテリアルズ社より入手、TSL8370)を用意し、これをイソプロピルアルコール(IPA)で0.1重量%になるように希釈した。
前記で得られた温度応答性フィルムを、ガラスにテープで固定し、スピンナー(ミカサ製)を用いて、メタクリロキシシランをコーティングし、シラン処理を行った。
【0094】
次いで、ポリエチレングリコールジアクリレート(分子量300、アルドリッチ社より入手)が最終濃度50重量%になるように、純水で希釈し、ここに、重合開始剤として、2−ヒドロキシ−4‘−(2−ヒドロオキシエトキシ)−2−メチルプロピオフェノン(アルドリッチ社より入手)を最終濃度1重量%になるように加えた。この溶液をスターラーで15分間攪拌した。
これをシラン処理した温度応答性フィルム上に1mL展開し、下記表の条件でスピンコートを実施した。その後、フォトマスクを用いて、露光装置で150mJのエネルギーで処理した。フォトマスクデザインは、刺激応答性領域(温度応答性領域)が200μm角のパッチが間隔200μmで配列するように設計されたものを使用した。
その後、シラン処理基材上に、細胞非接着層としてポリエリレングリコールジアクリレートが固定化されていることを目視で確認した。
【0095】
(3)細胞フラグメント回収用基材の作製
このようにして得られた培養支持体ツールを、20mmφに切り出し、粘着層を露出させ、35mmφポリスチレンディッシュ(ベクトンディッキンソン社製)底面に貼り付け、細胞フラグメント回収用基材とした。
【0096】
(4)細胞フラグメントの形成
実施例で得られた細胞フラグメント回収用基材を70%エタノールにて滅菌した。滅菌時間は1時間とした。
その後、ヒト由来間葉系幹細胞(hMSC)を4×105cells/cm2播種し、7日間培養した。7日後に、位相差顕微鏡で観察したところ、200μm角の複数の細胞からなる細胞フラグメントが間隔200μmで得られることを確認した。また、接眼10倍、対物4倍の倍率で、200μm角の細胞フラグメントが1視野に16個含まれるように位相差像を取得し、それぞれのフラグメントに含まれる細胞数を計測したところ平均7.5個(標準偏差0.9)であった。
【0097】
(5)細胞フラグメントの回収
その後、上記細胞フラグメント回収用基材を37度インキュベーターから25度の低温インキュベーターに移し、25分静置後、ピペッティングを10回程度実施することにより、上記刺激応答性領域(温度応答性領域)に刺激を与え、上記細胞フラグメントを回収した。得られた、細胞フラグメントについて、位相差顕微鏡を用いて測定した結果、フラグメントのサイズは30μmφであり、サイズおよび形状がほぼ同一の細胞フラグメントが回収できたことが確認できた。
【0098】
[比較例1]
(1)温度応答性フィルムの作製
N−イソプロピルアクリルアミドを、最終濃度20重量%になるようにイソプロピルアルコール(IPA)に溶解させた。市販の易接着性ポリエチレンテレフタレートフィルム(三光産業社より入手、透明50−Fセパ1090)(以下において「易接着PET」と略することがある)を調達し、これを10cm角に切断した。ここに前記溶液を、易接着PETの易接着面に展開し、ミヤバーでコーティングした。電子線照射装置(岩崎電気社製)を用いて該サンプル上に電子線照射を行い、該溶液をグラフト重合した。このときの電子線照射線量は300kGyであった。
【0099】
(2)細胞フラグメント回収用基材の作製
このようにして得られた培養支持体ツールを、20mmφに切り出し、粘着層を露出させ、35mmφポリスチレンディッシュ(ベクトンディッキンソン社製)底面に貼り付け、細胞フラグメント回収用基材とした。
【0100】
(3)細胞シートの形成
実施例で得られた細胞フラグメント回収用基材を70%エタノールにて滅菌した。滅菌時間は1時間とした。
その後、ヒト由来間葉系幹細胞(hMSC)を4×105cells/cm2播種し、7日間培養した。7日後に、位相差顕微鏡で観察したところ、hMSCがシート状で得られることを確認した。
【0101】
(4)細胞フラグメントの回収
クリーンベンチ内で、培養液を吸引しhMSCシートの上に滅菌された金網を押し当て、その後培養液を加え、室温で25分静置した後にピペッティングを10回実施することにより、上記刺激応答性領域(温度応答性領域)に刺激を与え、上記細胞フラグメントを回収した。得られた、細胞フラグメントについて、位相差顕微鏡を用いて測定した結果、フラグメントのサイズは15μmφ〜150μmφであり、細胞フラグメントのサイズおよび形状は不揃いであった。
【0102】
[比較例2]
(1)温度応答性フィルムの作製
N−イソプロピルアクリルアミドを、最終濃度20重量%になるようにイソプロピルアルコール(IPA)に溶解させた。市販の易接着性ポリエチレンテレフタレートフィルム(三光産業社より入手、透明50−Fセパ1090)(以下において「易接着PET」と略することがある)を調達し、これを10cm角に切断した。ここに前記溶液を、易接着PETの易接着面に展開し、ミヤバーでコーティングした。電子線照射装置(岩崎電気社製)を用いて該サンプル上に電子線照射を行い、該溶液をグラフト重合した。このときの電子線照射線量は300kGyであった。
【0103】
(2)細胞非接着層の形成
メタクリロキシシラン(モメンティブパフォーマンスマテリアルズ社より入手、TSL8370)を用意し、これをイソプロピルアルコール(IPA)で0.1重量%になるように希釈した。
前記で得られた温度応答性フィルムを、ガラスにテープで固定し、スピンナー(ミカサ製)を用いて、メタクリロキシシランをコーティングし、シラン処理を行った。
次いで、ポリエチレングリコールジアクリレート(分子量300、アルドリッチ社より入手)が最終濃度50重量%になるように、純水で希釈し、ここに、重合開始剤として、2−ヒドロキシ−4‘−(2−ヒドロオキシエトキシ)−2−メチルプロピオフェノン(アルドリッチ社より入手)を最終濃度1重量%になるように加えた。この溶液をスターラーで15分間攪拌した。
これをシラン処理した温度応答性フィルム上に1mL展開し、下記表の条件でスピンコートを実施した。その後、フォトマスクを用いて、露光装置で150mJのエネルギーで処理した。フォトマスクデザインは、刺激応答性領域(温度応答性領域)が200μm角のパッチが間隔200μmで配列するように設計されたものを使用した。
その後、シラン処理基材上に、細胞非接着層としてポリエリレングリコールジアクリレートが固定化されていることを目視で確認した。
【0104】
(3)細胞フラグメント回収用基材の作製
このようにして得られた培養支持体ツールを、20mmφに切り出し、粘着層を露出させ、35mmφポリスチレンディッシュ(ベクトンディッキンソン社製)底面に貼り付け、細胞フラグメント回収用基材とした。
【0105】
(4)細胞シートの形成
実施例で得られた細胞フラグメント回収用基材を70%エタノールにて滅菌した。滅菌時間は1時間とした。
その後、ヒト由来間葉系幹細胞(hMSC)を4×105cells/cm2播種し、7日間培養した。7日後に、位相差顕微鏡で観察したところ、200μm角の複数の細胞からなる細胞フラグメントが間隔200μmで得られることを確認した。また、接眼10倍、対物4倍の倍率で、200μm角の細胞フラグメントが1視野に16個含まれるように位相差像を取得し、それぞれのフラグメントに含まれる細胞数を計測したところ平均7.5個(標準偏差0.9)であった。
【0106】
(5)細胞フラグメントの回収
クリーンベンチ内で、培養液を吸引し、0.25%トリプシン-EDTA溶液を加え室温で5分処理した。その後位相差顕微鏡を用いて観察した結果、hMSCが細胞間接着が切断され、シングルセルとしてトリプシン溶液中に浮遊している様子が観察され、サイズおよび形状の揃った細胞フラグメントを得ることはできなかった。
【符号の説明】
【0107】
1 … 刺激応答性層
2 … 細胞非接着層
3 … 基材
10 … 細胞フラグメント回収用基材
11 … 刺激応答性領域
12 … 細胞非接着領域
21 … 細胞フラグメント
【特許請求の範囲】
【請求項1】
刺激により細胞接着性が変化する刺激応答性領域と、
細胞非接着性を有する細胞非接着領域と、
を有し、
前記刺激応答性領域が、前記細胞非接着領域により囲まれていることを特徴とする治療用細胞フラグメント回収用基材。
【請求項2】
前記刺激応答性材料が、温度変化により細胞剥離性を発現する温度応答性材料であることを特徴とする請求項1に記載の治療用細胞フラグメント回収用基材。
【請求項3】
前記温度応答性材料が、ポリ−N−イソプロピルアクリルアミド(PIPAAm)であることを特徴とする請求項2に記載の治療用細胞フラグメント回収用基材。
【請求項4】
刺激により細胞接着性が変化する刺激応答性領域と、
細胞非接着性を有する細胞非接着領域と、
を有し、
前記刺激応答性領域が、前記細胞非接着領域により囲まれていることを特徴とする継代用細胞フラグメント回収用基材。
【請求項5】
前記刺激応答性材料が、温度変化により細胞剥離性を発現する温度応答性材料であることを特徴とする請求項4に記載の継代用細胞フラグメント回収用基材。
【請求項6】
前記温度応答性材料が、ポリ−N−イソプロピルアクリルアミド(PIPAAm)であることを特徴とする請求項5に記載の継代用細胞フラグメント回収用基材。
【請求項7】
請求項1から請求項3までのいずれかの請求項に記載の治療用細胞フラグメント回収用基材を準備し、
前記刺激応答性領域が細胞接着性を発現している状態で、前記刺激応答性領域上に細胞を播種・培養し、前記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する細胞フラグメント形成工程と、
前記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、
前記刺激応答性領域から剥離した前記治療用細胞フラグメントを回収する回収工程と、
を有することを特徴とする治療用細胞フラグメントの製造方法。
【請求項8】
請求項4から請求項6までのいずれかの請求項に記載の継代用細胞フラグメント回収用基材を準備し、
前記刺激応答性領域が細胞接着性を発現している状態で、前記刺激応答性領域上に細胞を播種・培養し、前記刺激応答性領域に接着した少なくとも1以上の細胞からなる継代用細胞フラグメントを形成する細胞フラグメント形成工程と、
前記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、
前記刺激応答性領域から剥離した前記継代用細胞フラグメントを回収する回収工程と、
を有することを特徴とする継代用細胞フラグメントの製造方法。
【請求項1】
刺激により細胞接着性が変化する刺激応答性領域と、
細胞非接着性を有する細胞非接着領域と、
を有し、
前記刺激応答性領域が、前記細胞非接着領域により囲まれていることを特徴とする治療用細胞フラグメント回収用基材。
【請求項2】
前記刺激応答性材料が、温度変化により細胞剥離性を発現する温度応答性材料であることを特徴とする請求項1に記載の治療用細胞フラグメント回収用基材。
【請求項3】
前記温度応答性材料が、ポリ−N−イソプロピルアクリルアミド(PIPAAm)であることを特徴とする請求項2に記載の治療用細胞フラグメント回収用基材。
【請求項4】
刺激により細胞接着性が変化する刺激応答性領域と、
細胞非接着性を有する細胞非接着領域と、
を有し、
前記刺激応答性領域が、前記細胞非接着領域により囲まれていることを特徴とする継代用細胞フラグメント回収用基材。
【請求項5】
前記刺激応答性材料が、温度変化により細胞剥離性を発現する温度応答性材料であることを特徴とする請求項4に記載の継代用細胞フラグメント回収用基材。
【請求項6】
前記温度応答性材料が、ポリ−N−イソプロピルアクリルアミド(PIPAAm)であることを特徴とする請求項5に記載の継代用細胞フラグメント回収用基材。
【請求項7】
請求項1から請求項3までのいずれかの請求項に記載の治療用細胞フラグメント回収用基材を準備し、
前記刺激応答性領域が細胞接着性を発現している状態で、前記刺激応答性領域上に細胞を播種・培養し、前記刺激応答性領域に接着した少なくとも1以上の細胞からなる治療用細胞フラグメントを形成する細胞フラグメント形成工程と、
前記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、
前記刺激応答性領域から剥離した前記治療用細胞フラグメントを回収する回収工程と、
を有することを特徴とする治療用細胞フラグメントの製造方法。
【請求項8】
請求項4から請求項6までのいずれかの請求項に記載の継代用細胞フラグメント回収用基材を準備し、
前記刺激応答性領域が細胞接着性を発現している状態で、前記刺激応答性領域上に細胞を播種・培養し、前記刺激応答性領域に接着した少なくとも1以上の細胞からなる継代用細胞フラグメントを形成する細胞フラグメント形成工程と、
前記刺激応答性領域に刺激を与え細胞非接着性を発現させる刺激付与工程と、
前記刺激応答性領域から剥離した前記継代用細胞フラグメントを回収する回収工程と、
を有することを特徴とする継代用細胞フラグメントの製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2013−13368(P2013−13368A)
【公開日】平成25年1月24日(2013.1.24)
【国際特許分類】
【出願番号】特願2011−148437(P2011−148437)
【出願日】平成23年7月4日(2011.7.4)
【出願人】(000002897)大日本印刷株式会社 (14,506)
【出願人】(591173198)学校法人東京女子医科大学 (48)
【出願人】(501345220)株式会社セルシード (39)
【Fターム(参考)】
【公開日】平成25年1月24日(2013.1.24)
【国際特許分類】
【出願日】平成23年7月4日(2011.7.4)
【出願人】(000002897)大日本印刷株式会社 (14,506)
【出願人】(591173198)学校法人東京女子医科大学 (48)
【出願人】(501345220)株式会社セルシード (39)
【Fターム(参考)】
[ Back to top ]

