治療的処置のための粘液腫ウイルスとラパマイシンの組み合わせの使用
【課題】腫瘍細胞を選択的に標的とする一方で、健常な細胞に対する毒性をより低くして、健常細胞が影響を受けないままでいる可能性をより高くする新しい抗癌療法を提供する。
【解決手段】本発明は、ラパマイシンとの併用など、粘液腫ウイルスを組み合わせて治療上使用することに関係する。ラパマイシンによる処理は、インターフェロンに応答しない細胞など、先天的な抗ウイルス応答が欠損した細胞に粘液腫ウイルスが選択的に感染する能力を増進させる。ラパマイシンと粘液腫ウイルスの組み合わせを利用して、前記細胞が存在することを特徴とする、癌などの病気を治療することができる。また、本発明は、機能的M135Rを発現しない粘液腫ウイルスを治療上使用することにも関係する。
【解決手段】本発明は、ラパマイシンとの併用など、粘液腫ウイルスを組み合わせて治療上使用することに関係する。ラパマイシンによる処理は、インターフェロンに応答しない細胞など、先天的な抗ウイルス応答が欠損した細胞に粘液腫ウイルスが選択的に感染する能力を増進させる。ラパマイシンと粘液腫ウイルスの組み合わせを利用して、前記細胞が存在することを特徴とする、癌などの病気を治療することができる。また、本発明は、機能的M135Rを発現しない粘液腫ウイルスを治療上使用することにも関係する。
【発明の詳細な説明】
【技術分野】
【0001】
(関連出願の引用)
本出願は、米国仮特許出願第60/658,816号(2005年3月7日出願)の優先権を主張し、その内容は、本明細書中で参考として援用される。
【0002】
(発明の分野)
本発明は、一般的には、粘液腫ウイルスとラパマイシンの治療的利用に関する。
【背景技術】
【0003】
(発明の背景)
さまざまな種類の癌を治療するために使用される現在の治療法は、癌細胞を毒殺または死滅させることによって効果を発揮するというものになりがちである。残念なことに、癌細胞に対して毒性のある治療法は、健常な細胞にも有毒になりがちである。さらに、腫瘍の異質性が、依然として有効な癌治療が得られないことの主な理由の一つとなっている。化学療法や放射線療法など、現在主流の治療法は、狭い治療毒性濃度域内で使用されがちである。多様な種類の腫瘍細胞があり、これらの治療法を行うことができる濃度域が限られているため、この種の療法は、切れ味の鈍い手段と見なされている。
【0004】
現在開発中の新しい抗癌療法は、腫瘍細胞を選択的に標的とする一方で、健常な細胞に対する毒性をより低くして、健常細胞が影響を受けないままでいる可能性をより高くしようと試みている。
【0005】
腫瘍退縮性ウイルス療法が、腫瘍細胞と正常細胞との細胞間の違いを利用することを目的とする方法の一つである。この療法は、複製能のある腫瘍選択的なウイルスベクターを抗癌剤として使用する。腫瘍退縮性ウイルスは、感染のために癌細胞を特異的に標的するか、または、正常細胞よりも癌細胞において効率的に複製するのに適している。これら複製能のある腫瘍退縮性ウイルスは、不均一な腫瘍集団を標的する非常に選択的かつ強力な手段となる天然または遺伝子操作されている。複製選択的な腫瘍退縮性ウイルスは、正常な細胞では効率的に複製しないため、特に、放射線療法や化学療法のような伝統的な療法と比較して患者に対する毒性が低いはずである。
【0006】
数多くの研究で、さまざまなウイルス株について腫瘍退縮活性が報告されているが、最も有望な腫瘍退縮性ウイルスは、天然または遺伝子改変されたアデノウイルス、単純ヘルペスウイルス1型(「HSV1」)、レオウイルス、ワクシニアウイルス、水疱性口内炎ウイルス(「VSV」)、またはポリオウイルスである。抗癌剤として現在検討されている改変型腫瘍退縮性ウイルスは、HSV、アデノウイルス、ニューカッスル病ウイルス(「NDV」)、レオウイルス、およびワクシニアウイルス、麻疹、VSV、およびポリオウイルスなどである。さまざまな腫瘍退縮性ウイルスが、第一相および第二相で臨床試験されており、いくつかは持続した効能を示している。しかし、どのウイルスが、持続的複製、特異的かつ強力な退縮活性という目標をもっともよく達成するかは分かっていない。腫瘍退縮性ウイルスベクターの完全に効率的な候補は、生活環が短く、すぐに成熟したビリオンを形成し、細胞から細胞へ効率的に伝播し、すぐに挿入可能なゲノムをもつものである。その上、初期の先天的な免疫応答を阻害し、Th1応答の発達を遅延させることが、腫瘍退縮療法の有効性にとって重要なことが、証拠によって示唆されている。腫瘍退縮性ウイルスの開発用に想定されているウイルスの多くに対して正常な集団で見られる大量の抗体およびT細胞反応から見て、ヒトのウイルスが非常に免疫原性であることは明らかである。
【0007】
臨床実験によって、現在の腫瘍退縮性ウイルスは実際に安全であるが、単剤療法として臨床上十分に有効であるとするほど強力でではない。腫瘍細胞への不十分または不効率な感染が普通に見られるため、現在の動きは、候補ウイルスの効率を上げるために、それらを遺伝子操作して治療用の導入遺伝子を発現させることによりそれらを武装させようとするものである。上記した腫瘍退縮性ウイルスのほとんどは、他の一般的な腫瘍退縮療法と組み合わせてテストされている。
【0008】
アデノウイルスは、容易に遺伝子操作することができ、よく知られた関連するウイルスタンパク質機能を持っており、また、非常に軽度の病態に関連している。ONYX−015ヒトアデノウイルス(Onyx Pharmaceuticals Inc.)は、最も広範に試験されている。臨床使用用に最適化された腫瘍退縮性ウイルスであり、p53陰性腫瘍の中で選択的に複製すると考えられて、頭頸部癌患者での臨床試験において可能性を見せている。しかし、報告によれば、ONYX−015は、治療した患者の14%で客観的な臨床反応を示しているにすぎない(非特許文献1)。
【0009】
特許文献1と特許文献2は、腫瘍細胞の増殖を阻害し、神経細胞に特異的な変異型腫瘍退縮性HSVを記載している。さらなる利点は、HSVは簡単に遺伝子改変することができ、不要なウイルス増殖を止める薬剤が存在していることである。しかし、一般の集団はこのウイルスに曝露されて免疫反応を獲得していて、このウイルスの腫瘍退縮効果が弱まっていると考えられるため、このような普遍的ヒト病原体の使用には限界がある。また、HSVは、重大な副作用または死に至る可能性がある病気を引き起こす可能性もある。
【0010】
III型レオウイルスは、比較的軽度な病気と関連し、そのウイルス遺伝子の機能がかなり十分に理解されている。III型レオウイルスは、変異型ras発癌遺伝子を発現する細胞において増進された複製特性を示し、かつPKR −/−細胞の中で選択的に増殖する癌治療剤として、現在、Oncolytic Biotech社によって開発されているところである(非特許文献2)。しかし、レオウイルスは、遺伝子操作することが難しく、そのウイルス複製を簡単に止めることができない。
【0011】
VSVは、比較的軽度な病気に関連しており、よく知られたウイルス遺伝子機能をもっている。WO99/04026には、さまざまな疾患に広く治療効果を表すためにVSVをベクターとして遺伝子治療法に使用することが記載されている。しかし、VSVは、遺伝子操作が困難であり、また、そのウイルス複製を簡単に止めることができないという点で、レオウイルスと同じ問題を抱えている。
【0012】
ワクシニアウイルスおよびポリオウイルスは、当技術分野において記載のある別の腫瘍退縮性ウイルス候補であるが、重大であるか、または死に至る可能性がある病気と関連している。
【0013】
特許文献3は、ヒト腫瘍細胞に対してガンマインターフェロンとIFNγの断片を使用することを開示している。特許文献4は、病気の細胞がインターフェロンが介在する抗ウイルス応答に欠損をもつヒトの病気を治療する方法であって、治療上有効な量のインターフェロン感受性で複製能をもつクローンウイルスをヒトに投与することを含む方法を開示している。具体的には、VSV粒子が腫瘍細胞に対して毒性活性を有するが、インターフェロン存在下では、正常細胞においてVSVによる細胞毒性の改善が起こることを開示している。また、特許文献4は、インターフェロン処理された腫瘍細胞でNDVに誘導された感受性が見られたが、正常な細胞にインターフェロンを加えると、これらの細胞はNDVに対して抵抗性になることも開示している。この方法は、細胞にインターフェロン感受性のウイルスを感染させることによって、それらをインターフェロン感受性にすることを目的としている。
【先行技術文献】
【特許文献】
【0014】
【特許文献1】国際公開第96/03997号パンフレット
【特許文献2】国際公開第97/26904号パンフレット
【特許文献3】米国特許第4,806,347号明細書
【特許文献4】国際公開第99/18799号パンフレット
【非特許文献】
【0015】
【非特許文献1】Nemunaitis J,Khuri F,Ganly I5 Arseneau J,Posner M,Vokes E,Kuhn J,McCarty T,Landers S,Blackburn A,Romel L,Randlev B,Kaye S,およびKirn D.,J.Clin. Oncol,2001年1月15日,第19巻,第2号,p.289−98
【非特許文献2】Strong J.E.およびP.W.Lee.,J.Virology,1996年,第70巻,p.612−616
【発明の概要】
【課題を解決するための手段】
【0016】
(発明の要旨)
本発明は、機能的なM135Rタンパク質を発現しない新規の粘液腫ウイルスを含む、ウサギ粘液腫ウイルスが、インターフェロンに対して非反応性の細胞など、先天的な抗ウイルス応答を欠損した、ヒト腫瘍細胞などの細胞に選択的に感染することができ、このような感染が、薬剤であるラパマイシンで前記細胞を処理することにより促進されるという予想外の発見に基づいている。これと関連して使用される場合、「先天的」という用語は、非抗原特異的な免疫反応を表している。粘液腫ウイルスは、正常なヒト細胞では効率的に複製できないため、インターフェロンに対して非感受性の細胞など、先天的な抗ウイルス応答を欠損した細胞を特徴とするさまざまな疾患および症状に対する治療法として、例えば、癌に対する腫瘍退縮治療法として、このウイルスを使用することができる。また、このウイルスを、先天的な抗ウイルス応答を欠損した細胞を同定するため、また、これらの細胞をインビボで画像化するために使用することもできる。
【0017】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害する方法であって、粘液腫ウイルスとラパマイシンを組み合わせたものの有効量を細胞に投与することを含む方法を提供する。
【0018】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に粘液腫ウイルスとラパマイシンを組み合わせたものの有効量を投与することを含む方法を提供する。
【0019】
本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害するため、および、先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤を製造するための、有効量の粘液腫ウイルスとラパマイシンの合剤の使用をさらに提供する。
【0020】
本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする患者の病状を治療するため、および患者におけるそのような病状を治療するための薬剤を製造するための、有効量の粘液腫ウイルスとラパマイシンの合剤の使用をさらに提供する。
【0021】
別の態様において、本発明は、粘液腫ウイルスとラパマイシンを含む医薬組成物を提供する。この医薬組成物は、先天的な抗ウイルス応答を欠損した細胞を阻害するため、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するために役立つことができる。
【0022】
別の態様において、本発明は、粘液腫ウイルス、ラパマイシン、および先天的な抗ウイルス応答を欠損した細胞を阻害するため、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための説明書を含むキットを提供する。この病状は、癌および慢性ウイルス感染症を含む。
【0023】
本発明は、先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、細胞集団を、粘液腫ウイルスとラパマイシンの混合物に曝露すること、ウイルスを、先天的な抗ウイルス応答を欠損した細胞に感染させること、および細胞集団のどの細胞が粘液腫ウイルスに感染したかを決定することを含む方法を提供する。
【0024】
本発明は、さらに、ウサギ粘液腫ウイルスタンパク質M135Rが、ウサギにおける免疫応答を誘発するのに関与していること、および機能的なM135Rを発現しない粘液腫ウイルス株は、インビトロで細胞を死滅させることができるが、動物では粘液腫症を引き起こさないという予想外の発見に基づいている。このようなウイルス株は、薬剤であるラパマイシンと併用して投与される治療法など、インターフェロンに対して非感受性の細胞を含む、先天的な抗ウイルス応答を欠損した細胞を処理するために使用することができ、ウイルスの混入を増加させる必要がないため、安全性を向上させる結果となる。
【0025】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害する方法であって、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して細胞に投与することを含む方法を提供する。
【0026】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して投与することを含む方法を提供する。
【0027】
本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害するために、および先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤を製造する際に、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して使用することをさらに提供する。
【0028】
本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする患者の病状を治療するために、および患者におけるそのような病状を治療するための薬剤を製造する際に、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して使用することをさらに提供する。
【0029】
さらなる態様において、本発明は、機能的なM135Rを発現しない粘液腫ウイルスを提供する。
【0030】
別の態様において、本発明は、機能的なM135Rを発現しない粘液腫ウイルスを含む医薬組成物を提供する。この医薬組成物は、先天的な抗ウイルス応答を欠損した細胞を阻害するか、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする患者の病状を治療するのに役立ちうる。この医薬組成物は、ラパマイシンをさらに含むことができる。
【0031】
別の態様において、本発明は、機能的なM135Rを発現しない粘液腫ウイルス、および先天的な抗ウイルス応答を欠損した細胞を阻害するため、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための説明書を含むキットを提供する。このキットは、さらにラパマイシンを含むことが可能である。この病状は、癌および慢性ウイルス感染症を含む。
【0032】
本発明は、先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、細胞集団を、機能的なM135Rを発現しない粘液腫ウイルスに、任意にはラパマイシンとの混合物に曝露すること、ウイルスを、先天的な抗ウイルス応答を欠損した細胞に感染させること、および細胞集団のどの細胞が粘液腫ウイルスに感染したかを決定することを含む方法を提供する。
【0033】
以下の発明の具体的態様の説明を、添付の図面とともに検討すれば、本発明のその他の態様および特徴が当業者に明らかとなろう。しかし、当然ながら、本発明の主旨と範囲に含まれる多様な改変および修正が、詳細な説明から当業者に明らかとなるのであるから、詳細な説明および具体的実施例は、本発明の好適な実施態様を示しつつも、例示のためだけに提示されていると理解されるべきである。
本発明はまた、以下の項目を提供する。
(項目1)
先天的な抗ウイルス応答を欠損した細胞を阻害する方法であって、該細胞に有効量の粘液腫ウイルスとラパマイシンの配合物を投与することを含む方法。
(項目2)
上記細胞がインターフェロンに非応答性である、項目1記載の方法。
(項目3)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目2記載の方法。
(項目4)
上記細胞がヒト癌細胞である、項目3記載の方法。
(項目5)
上記粘液腫ウイルスが野生型ウイルスである、項目4記載の方法。
(項目6)
上記粘液腫ウイルスが遺伝子改変されている、項目4記載の方法。
(項目7)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目6記載の方法。
(項目8)
上記細胞が肺癌細胞、黒色腫細胞、卵巣癌細胞、前立腺癌細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目4記載の方法。
(項目9)
上記細胞が慢性的にウイルスに感染したヒト細胞である、項目1記載の方法。
(項目10)
先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に有効量の粘液腫ウイルスとラパマイシンの配合物を投与することを含む方法。
(項目11)
上記病状が癌である、項目10記載の方法。
(項目12)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目11記載の方法。
(項目13)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目11記載の方法。
(項目14)
上記患者がヒトである、項目13記載の方法。
(項目15)
上記粘液腫ウイルスが野生型ウイルスである、項目14記載の方法。
(項目16)
上記粘液腫ウイルスが遺伝子改変されている、項目14記載の方法。
(項目17)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目16記載の方法。
(項目18)
上記ウイルスと上記ラパマイシンは注射によって上記癌の部位に投与される、項目14記載の方法。
(項目19)
上記ウイルスと上記ラパマイシンは全身に投与される、項目14記載の方法。
(項目20)
上記病状が慢性ウイルス感染症である、項目10記載の方法。
(項目21)
先天的な抗ウイルス応答を欠損した細胞を阻害するための有効量の粘液腫ウイルスとラパマイシンの配合物の使用。
(項目22)
先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤の製造における、有効量の粘液腫ウイルスとラパマイシンの配合物の使用。
(項目23)
上記細胞がインターフェロン非応答性である、項目21または22記載の使用。
(項目24)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目23記載の使用。
(項目25)
上記細胞が慢性的にウイルスに感染している、項目24記載の使用。
(項目26)
上記細胞がヒト癌細胞である、項目24記載の使用。
(項目27)
上記細胞が肺癌細胞、黒色腫細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目26記載の使用。
(項目28)
上記粘液腫ウイルスが野生型ウイルスである、項目20から27のいずれか一項記載の使用。
(項目29)
上記粘液腫ウイルスが遺伝子改変されている、項目20から27のいずれか一項記載の使用。
(項目30)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目29記載の使用。
(項目31)
患者における病状を治療するための有効量の粘液腫ウイルスとラパマイシンの配合物の使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする、使用。
(項目32)
患者における病状を治療するための薬剤の製造における有効量の粘液腫ウイルスとラパマイシンの配合物の使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が患者に存在することを特徴とする、使用。
(項目33)
上記病状が癌である、項目31または32記載の使用。
(項目34)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目33記載の使用。
(項目35)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目33記載の使用。
(項目36)
上記病状が慢性ウイルス感染症である、項目31または32記載の使用。
(項目37)
上記患者がヒトである、項目31から36のいずれか一項記載の使用。
(項目38)
上記粘液腫ウイルスが野生型ウイルスである、項目31から37のいずれか一項記載の使用。
(項目39)
上記粘液腫ウイルスが遺伝子改変されている、項目31から37のいずれか一項記載の使用。
(項目40)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目39記載の使用。
(項目41)
粘液腫ウイルスとラパマイシンを含む医薬組成物。
(項目42)
さらに付加的治療薬を含む、項目41記載の医薬組成物。
(項目43)
上記付加的治療薬が化学療法薬である、項目42記載の医薬組成物。
(項目44)
先天的な抗ウイルス応答を欠損した細胞を阻害するため、または先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための、粘液腫ウイルス、ラパマイシンおよび使用説明書を含むキット。
(項目45)
先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、粘液腫ウイルスとラパマイシンの配合物に細胞の集団を曝露する工程、先天的な抗ウイルス応答を欠損した細胞に該ウイルスを感染させる工程、および該細胞集団のどの細胞が粘液腫ウイルスに感染したかを判定する工程を含む方法。
(項目46)
上記細胞集団が患者の体内にあり、上記曝露工程が、上記粘液腫ウイルスとラパマイシンの配合物を該患者に投与することを含み、該粘液腫ウイルスが、検出可能なマーカーを発現するよう遺伝子改変されており、かつ、上記判定工程が、該患者の中で該検出可能なマーカーを発現する細胞を検出することを含む、項目45記載の方法。
(項目47)
上記細胞集団が培養されている、項目45記載の方法。
(項目48)
機能的なM135Rを発現しない有効量の粘液腫ウイルスを、随意で有効量のラパマイシンと組み合わせて細胞に投与することを含む、先天的な抗ウイルス応答を欠損した細胞を阻害する方法。
(項目49)
上記細胞がインターフェロンに非応答性である、項目48記載の方法。
(項目50)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目49記載の方法。
(項目51)
上記細胞がヒト癌細胞である、項目50記載の方法。
(項目52)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目51記載の方法。
(項目53)
上記細胞が肺癌細胞、黒色腫細胞、卵巣癌細胞、前立腺癌細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目51記載の方法。
(項目54)
上記細胞が慢性的にウイルスに感染しているヒト細胞である、項目48記載の方法。
(項目55)
先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に機能的なM135Rを発現しない有効量の粘液腫ウイルスを投与することを含む方法。
(項目56)
さらに、有効量のラパマイシンを上記患者に投与することを含む、項目55記載の方法。
(項目57)
上記病状が癌である、項目55または56記載の方法。
(項目58)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目57記載の方法。
(項目59)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目57記載の方法。
(項目60)
上記患者がヒトである、項目59記載の方法。
(項目61)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目59記載の方法。
(項目62)
上記癌の部位に注射することによって上記投与が行われる、項目55または56記載の方法。
(項目63)
上記投与が全身性である、項目55または56記載の方法。
(項目64)
上記病状が慢性ウイルス感染症である、項目55記載の方法。
(項目65)
機能的なM135Rを発現しない粘液腫ウイルスの有効量の使用。
(項目66)
有効量のラパマイシンをさらに配合する、項目65記載の使用。
(項目67)
先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤を製造するための、機能的なM135Rを発現しない粘液腫ウイルスの有効量の使用。
(項目68)
薬剤が、有効量のラパマイシンと配合して投与されるように処方されている、項目67記載の使用。
(項目69)
上記細胞がインターフェロンに非応答性である、項目65から68のいずれか一項記載の使用。
(項目70)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目69記載の使用。
(項目71)
上記細胞が慢性的にウイルスに感染している、項目70記載の使用。
(項目72)
上記細胞がヒト癌細胞である、項目70記載の使用。
(項目73)
上記細胞が肺癌細胞、黒色腫細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目72記載の使用。
(項目74)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目65から73のいずれか一項記載の使用。
(項目75)
患者における病状を治療するための、機能的なM135Rを発現しない有効量の粘液腫ウイルスの使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が患者に存在することを特徴とする、使用。
(項目76)
有効量のラパマイシンをさらに含む、項目75記載の使用。
(項目77)
上記患者における病状を治療するための薬剤の製造のための、機能的なM135Rを発現しない有効量の粘液腫ウイルスの使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする、使用。
(項目78)
上記薬剤が、有効量のラパマイシンと配合して投与されるように処方されている、項目77記載の使用。
(項目79)
上記病状が癌である、項目75から78のいずれか一項記載の使用。
(項目80)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目79記載の使用。
(項目81)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目79記載の使用。
(項目82)
上記病状が慢性ウイルス感染症である、項目75から78のいずれか一項記載の使用。
(項目83)
上記患者がヒトである、項目75から82のいずれか一項記載の使用。
(項目84)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目75から83のいずれか一項記載の使用。
(項目85)
機能的なM135Rを発現しない粘液腫ウイルス。
(項目86)
機能的なM135Rを発現しない粘液腫ウイルスを含む医薬組成物。
(項目87)
さらにラパマイシンを含む、項目86記載の医薬組成物。
(項目88)
さらに付加的治療薬を含む、項目86記載の医薬組成物。
(項目89)
上記付加的治療薬が化学療法薬である、項目86記載の医薬組成物。
(項目90)
先天的な抗ウイルス応答を欠損した細胞を阻害するため、または先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための、機能的なM135Rを発現しない粘液腫ウイルスおよび使用説明書を含むキット。
(項目91)
さらにラパマイシンを含む、項目90記載のキット。
(項目92)
先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、機能的なM135Rを発現しない粘液腫ウイルスに細胞の集団を曝露する工程、先天的な抗ウイルス応答を欠損した細胞に該ウイルスを感染させる工程、および該細胞集団のどの細胞が該粘液腫ウイルスに感染したかを判定する工程を含む方法。
(項目93)
上記細胞集団が患者の体内にあり、上記曝露工程が、上記機能的なM135Rを発現しない粘液腫ウイルスを該患者に投与することを含み、該機能的なM135Rを発現しない粘液腫ウイルスが、検出可能なマーカーを発現するよう遺伝子改変されており、かつ、上記判定工程が、該患者の中で該検出可能なマーカーを発現する細胞を検出することを含む、項目92記載の方法。
(項目94)
ラパマイシンと組み合わせて上記曝露が行われる、項目92または93記載の方法。
(項目95)
上記細胞集団が培養されている、項目92記載の方法。
【図面の簡単な説明】
【0034】
図面は、本発明の実施態様が具体的に説明されているが、あくまで例示のためのものである。
【図1】細胞にウイルスが感染すると誘導される、インターフェロンによって誘導抗ウイルスシグナル伝達スキームの概略図である。
【図2】粘液腫ウイルスに曝露された後の非許容性の野生型マウス胎仔線維芽細胞(「MEF」)の位相差顕微鏡写真であり、インターフェロンα/βを中和抗体で阻害した後にMEF細胞が許容性になることを示している。
【図3】粘液腫ウイルス感染後のSTAT1およびSTAT2のリン酸化(活性化)状態を示すウエスタンブロットであり、MEF細胞への非許容感染(nonpermissive infections)は、STAT1およびSTAT2のリン酸化と関連することを示している。
【図4】粘液腫ウイルス感染後のSTAT3、STAT4、STAT5およびST6のリン酸化(活性化)状態を示すウエスタンブロットであり、MEF細胞への非許容感染は、これらの分子種のいずれも活性化しないことを示している
【図5】粘液腫ウイルス感染後のINFα/β R−/−型MEFおよびSTAT1−/−型MEFの位相差顕微鏡写真であり、IFN/STAT/JAKシグナル伝達の不活性化は、細胞を粘液腫ウイルスに対して許容性にすることを示している。
【図6】粘液腫ウイルス感染後の非許容性野生型MEFにおけるPKRのリン酸化状態を示すウエスタンブロットであり、PRKは粘液腫ウイルス感染によって活性化されないことを示している。
【図7】模擬感染したか、粘液腫ウイルスに前感染した野生型MEFにおけるPKRのリン酸化状態を示すウエスタンブロットであり、粘液腫ウイルスが、MEF細胞におけるPKR活性化を阻止することを示している。
【図8】粘液腫ウイルス感染後の野生型MEFにおけるPEKRのリン酸化状態を示すウエスタンブロットであり、粘液腫ウイルスが、MEF細胞におけるPEKRの活性化を阻止することを示している。
【図9】粘液腫ウイルスに曝露した後のPKR−/−、RNaseL−/−、およびMx1−/−という三重のノックアウトの位相差顕微鏡写真であり、MEF細胞における抗ウイルス状態は別の経路によってもたらされていることを示している。
【図10】粘液腫ウイルスに曝露した後のPKR−/−、RNaseL−/−、およびMx1−/−の三重ノックアウトの位相差顕微鏡写真である。
【図11】INFα/βに対する中和抗体で処理した後、および粘液腫ウイルスに曝露した後のPKR−/−、RNase L−/−、およびMx1−/−という三重のノックアウトの位相差顕微鏡写真である。
【図12】INFα/βに対する中和抗体で処理した後、および粘液腫ウイルスに曝露した後の非許容性MEFにおけるeIF2αおよびPKRのリン酸化レベルを示すウエスタンブロットであり、非応答性細胞におけるeIF2αのリン酸化は、PKR非依存的経路によって触媒されることを示している。
【図13】粘液腫ウイルス感染後のPKR−/−、RNaseL−/−、およびMx1−/−三重のノックアウトにおけるSTAT1のリン酸化状態を示すウエスタンブロットであり、正常なIFN誘導シグナル応答を示している。
【図14】感染12時間後の非許容性PKR−/−+RNaseL−/−+Mx1−/−細胞におけるチロシンリン酸化型STAT1の細胞内の局在を示す位相差顕微鏡写真であり、正常なIFN/STATシグナル応答で予測されたように、活性化されたSTAT1は核に局在することを示している。
【図15】模擬感染させたか、GFPを発現する死菌または生菌の粘液腫ウイルスに感染させた、頭蓋骨内に神経膠腫を有するヌードマウスの脳の蛍光画像であり、粘液腫ウイルスが神経膠腫細胞を標的とすることを示している。
【図16】GFPを発現する粘液腫ウイルスに感染したマウスの薄層切片の蛍光画像および写真であり、粘液腫ウイルスが腫瘍細胞だけで複製することを示している。
【図17】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したHT29ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における非許容感染の例を示すものである。
【図18】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したHOP92ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における許容感染の例を示すものである。
【図19】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したOVCAR4ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における許容感染の例を示すものである。
【図20】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したSK−MEL3ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における許容感染の例を示すものである。
【図21】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したSK−MEL28ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における半許容感染の例を示すものである。
【図22】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したBGMK細胞の位相差顕微鏡写真であり、典型的な許容性対照感染の例を示すものである。
【図23】LacZタンパク質を発現する粘液腫ウイルスの高濃度液を感染させた陽性対照BGMK細胞、およびヒト腫瘍細胞株U87、A172、およびU373を、X−Galで染色したものの位相差顕微鏡写真であり、これらのヒト神経膠腫はすべて、粘液腫ウイルスの複製に対して許容性であったことを示している。
【図24】高濃度の粘液腫ウイルスに感染させたBGMK、U87、A172、およびU373の各細胞の感染72時間後の生存率を示す図であり、粘液腫ウイルスがこれらの細胞をすべて死滅させることができることを示している。
【図25】MV GFPに感染させたSF04 1585星状細胞腫細胞の位相差顕微鏡写真および蛍光画像であり、初代ヒト神経膠腫細胞で感染が起きたことを示している。
【図26】LacZタンパク質を発現する粘液腫ウイルスに感染させたU373神経膠腫細胞をX−Galで染色したものの位相差顕微鏡写真であり、これらのヒト腫瘍細胞で感染が起きたことを示している。
【図27】MV GFPに感染させたSF04 1585細胞の感染48時間後の生存率を示す図であり、これらの感染ヒト腫瘍細胞が死滅したことを示している。
【図28】GFPを発現する粘液腫ウイルスに感染させたDaoy髄芽細胞およびD384髄芽細胞の蛍光顕微鏡写真であり、これらのヒト腫瘍細胞で感染が起きたことを示している。
【図29−1】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−2】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−3】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−4】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−5】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図30】vMyxLacまたはvMyxLacT5−のいずれかに感染させたウイルス感染細胞株の写真である。
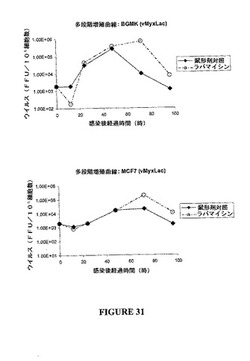
【図31−1】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株(BGMK;A9;MCF−7;MDA−MB−435;M14;およびCOLO205)におけるウイルス産生速度をグラフ表示したものである。
【図31−2】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株(BGMK;A9;MCF−7;MDA−MB−435;M14;およびCOLO205)におけるウイルス産生速度をグラフ表示したものである。
【図31−3】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株(BGMK;A9;MCF−7;MDA−MB−435;M14;およびCOLO205)におけるウイルス産生速度をグラフ表示したものである。
【図32】(A)粘液腫ウイルスタンパク質M135Rおよびワクシニアウイルスタンパク質B18Rのアラインメントの略図である。(B)M135Rと、B18Rの最初の179アミノ酸のアミノ酸配列アラインメントである。
【図33】(A)粘液腫ウイルスのローザンヌ(Lausanne)株(vMyxLau)に感染させたBGMK細胞で発現したM135Rのウエスタンブロット。(B)vMyxLauに感染させ、araC、ツニカマイシン、またはたモネンシンで処理したBGMK細胞で発現したM135Rのウエスタンブロット。
【図34】(A)模擬感染させたか、粘液腫ウイルスに感染させ、M135Rについて染色したBGMK細胞の蛍光画像。(B)野生型粘液腫ウイルス(vMyxgfp)またはM135Rノックアウト株(vMyx135KO)に感染させた細胞の免疫沈殿物または細胞可溶化物に対する、抗M135R抗体を用いたウエスタンブロット。
【図35】(A)vMyx135KOを作出するためのクローニング法の概略図。(B)PCR挿入配列産物のアガロースゲル。(C)野生型粘液腫ウイルスおよびM135Rノックアウト粘液腫ウイルスに感染させた細胞のウエスタンブロット。
【図36】vMyxgfpまたはvMyx135KOに感染させたBGMK細胞におけるウイルス増殖巣の増殖曲線である。
【図37】vMyxgfpまたはvMyx135KOに感染させたウサギ胚線維芽細胞の光学顕微鏡写真と蛍光顕微鏡写真である。
【図38】vMyxgfpまたはvMyx135KOに感染させたウサギHIG82線維芽細胞の光学顕微鏡写真と蛍光顕微鏡写真である。
【図39】vMyxgfpまたはvMyx135KOに感染させたヒト初代線維芽細胞の光学顕微鏡写真と蛍光顕微鏡写真である。
【図40】vMyxLauまたはvMyx135KOに感染させたウサギの体温のグラフである。
【図41】模擬感染させたか、またはvMyxgfpもしくはvMyx135KOに感染させ、125Iで標識したウサギインターフェロンα/βで処理した細胞の125I放射のグラフである。
【図42】感染させる24時間前にウサギインターフェロンα/βで処理するか、無処理のままで、RK13細胞またはBGMK細胞にvMyxgfpもしくはvMyx135KOを感染させることによって形成された増殖巣のグラフである。
【図43】20nMラパマイシン(R)、または賦形剤対照(D)で予め処理した786−0ヒト癌細胞の細胞可溶化物を用い、図に示したタンパク質に対する抗体を用いてプローブ検索したウエスタンブロットの写真である。
【発明を実施するための形態】
【0035】
(詳細な説明)
これまでに、本発明者らは、通常はウサギに感染するウイルスである野生型の粘液腫ウイルスが、その全体が参照されて本明細書に組み込まれるPCT/CA2004/000341に記載されているように、例えば、インターフェロンに非応答性の細胞など、先天的な抗ウイルス応答を欠損した、ヒト細胞などの細胞に選択的に感染して死滅させうることを発見した。粘液腫ウイルスは、正常なヒト細胞の中では効率的に複製しない。多くの病気または症状が、インターフェロンに対して応答性でない細胞、例えば、癌など、先天的な抗ウイルス応答を欠損している細胞が存在することを特徴としているため、正常な健常細胞に対する毒性が低い粘液腫ウイルスを使用して、癌を含むそのような病気および症状を治療することができる。また、慢性的に感染した細胞は、先天的な抗ウイルス応答を欠損しているため、粘液腫ウイルスを使用して、そのような細胞を治療することができる。例えば、多くのウイルスが、細胞の抗ウイルス性インターフェロン応答を阻害するように機能する遺伝子産物をコードするが、粘液腫ウイルスはそのような細胞に選択的に感染することができる。
【0036】
粘液腫ウイルス(「MV」)は、ウサギの粘液腫症の病原因子である。MVは、DNAウイルスの中で最大のポックスウイルス科のレポリポックスウイルス属に属している。MVは、その自然宿主であるアメリカ大陸のワタオウサギ(Sylvilagus rabbit)において良性の病気を引き起こす。しかし、それは、全身に見られるが、特に粘膜部周辺に見られる病変部を特徴とする、欧州大陸のウサギにおいては致命的な病気を引き起こす、病原性かつ宿主特異的なポックスウイルスである(Cameron C, Hota−Mitchell S, Chen L, Barrett J, Cao JX, Macaulay C, Willer D, Evans D, McFadden G. Virology 1999, 264(2): 298−318; Kerr P & McFadden G. Viral Immunology 2002, 15(2): 229−246)。
【0037】
MVは、感染細胞の細胞質の中で複製する163kbの二本鎖DNAゲノムを持つ大型のウイルスである(B. N. Fields, D. M. Knipe, P. M. Howley, Eds., Virology Lippincott Raven Press, New York, 2nd ed., 1996)。MVは、宿主の免疫反応および炎症反応の下方制御ならびにウイルス感染細胞のアポトーシスに関与するとされてきた、多様な細胞結合型タンパク質および細胞分泌型タンパク質をコードすることが知られている。MVは全てのヒト体細胞に取り込まれることができる。しかし、細胞が先天的な抗ウイルス応答性を持っている場合、正常なウサギ体細胞以外には、ウイルスは細胞に増殖できる形で感染することができないが、このことは、ウイルスが複製して
細胞死を引き起こすことができないことを意味している。
【0038】
インターフェロン(「INF」)は、多様な刺激に反応して分泌されるサイトカインのファミリーである。インターフェロンは細胞表面受容体に結合して、抗ウイルス応答、ならびに増殖阻害シグナルおよび/またはアポトーシスシグナルの誘導など、細胞応答を導くシグナル伝達カスケードを活性化させる。インターフェロンはI型またはII型に分類される。I型インターフェロンはIFN−α、IFN−β、IFN−τ、およびIFN−ωなどであり、これらはすべて単量体であるが、唯一のII型IFNはIFN−γであり、二量体である。IFN−αの12種の異なったサブタイプは、14の遺伝子によって産生されるが、他のIFNはすべて一遺伝子性のものである(Arduini et al., 1999)。IFNは、癌遺伝子発現を調節することによって、直接的な抗腫瘍活性を発揮する。増殖促進性癌遺伝子が過剰発現されるか、または腫瘍抑制癌遺伝子の発現が消失すると、悪性の形質転換が生じることがある。癌の発生に関係する癌遺伝子には、p53、Rb、PC、NFl、WTl、DCCがある。
【0039】
粘液腫ウイルス、また、レオウイルスおよびVSVなど、その他の腫瘍退縮性ウイルスは、細胞の中で複製できるようになるためには、正常な健常細胞に存在する抗ウイルス防御を迂回する必要がある。MVおよびその他の腫瘍退縮性ウイルスはインターフェロン産生を誘導し、かつ、IFN経路の抗ウイルス効果に対して、通常は感受性である。IFNの抗ウイルス応答によって生じた関連タンパク質であって、主にウイルス増殖に影響を及ぼすものはPKR、OASシンテターゼおよびリボヌクレアーゼLヌクレアーゼなどである。PKRはeIF2αを活性化させ、その結果、翻訳の阻害とアポトーシスの誘導をもたらす。図1にIFN応答経路の概略を示す。正常な細胞においては、MVは、直接PKRおよびeIF2αによる影響を受ける。
【0040】
抗ウイルス応答経路は、しばしば癌細胞の中で破壊されている。例えば、IFNに対する応答の低下または欠損は、形質転換または腫瘍発生の過程でしばしば生じる遺伝子欠損である。腫瘍細胞株の80%以上がインターフェロンに応答しないか、応答低下を示す(Stojdl et al., Cancer Cell (2003) 4: 263−275 and references cited therein; Wong et al. J Biol Chem. (1997) 272(45):28779−85; Sun et al. Blood. (1998) 91(2):570−6; Matin et al. Cancer Res. (2001) 61(5):2261−6; Balachandran et al Cancer Cell (2004) 5(l):51−65)。PCT/CA2004/000341で既に開示されているように、MVはヒト腫瘍細胞などの癌細胞に感染して死滅させることができ、また、これらの細胞は先天的な抗ウイルス応答を欠損しているために、MVはそれらに感染することができると、特定の理論に制約されることなく考えられている。
【0041】
初期先天性免疫応答を阻害すること、およびThl応答の発生を遅くすることが腫瘍退縮療法の有効性に重要であることが、証拠から示唆されている。粘液腫ウイルスは毒性ウイルスであるが、宿主特異的で宿主域が非常に狭いため、ヒトまたはマウスには感染しない。特定の理論に拘泥することなく、粘液腫ウイルスは非ヒトウイルスであるために、ヒトの既存の免疫認識と出会うはずがないと考えられる。したがって、その腫瘍退縮性ウイルスとしての可能性は、より障害をもたらしにくいため、天然のヒトウイルスよりも粘液腫ウイルスの方が、許容性腫瘍細胞により強く感染して、癌に対する有効な腫瘍退縮治療を行うことができるはずである。
【0042】
粘液腫ウイルスの宿主域遺伝子M−T5は、粘液腫ウイルスが多くのヒト腫瘍細胞株に感染する際に決定的な役割を果たしているように見える(Sypula et al, (2004) Gene Ther. Mol. Biol. 8:103)。このMT−5遺伝子は、ウサギリンパ球において粘液腫が複製するために必要とされるアンキリン反復タンパク質をコードし、MT−5遺伝子を欠失した粘液腫ウイルスは、感受性のウサギにおいても粘液腫症を発症させることができない(Mossman et al, (1996) J. Virol. 70: 4394)。入手可能な証拠から、感染ヒト細胞の中での細胞内シグナル伝達における違いが、粘液腫ウイルスの感染および増殖複製に対して許容性のあるヒト腫瘍細胞を区別するのに決定的であることが示唆されている(Johnston et al, (2003) J. Virol. 11: 5877)。
【0043】
さらに、粘液腫ウイルスは、インターフェロンα/β受容体(「IFNα/β−R」)のアミノ末端部分に相同性を示すM135Rタンパク質を持っている。M135Rは、宿主の抗ウイルス応答を開始させないために、宿主のINFα/β−Rを模倣することが示唆されている(Barrett et al., Seminars in Immunology (2001)13:73−84)。この予測は、ワクシニアウイルスB18R由来のウイルスINFα/β−Rとの配列相同性に基づくものであり、ワクシニアウイルス(「VV」)がそのような免疫回避戦略を採ることが実証されている。しかし、M135Rは、VVB18R、およびその他配列決定されたポックスウイルス由来のINFα/β−R相同体の大きさの半分しかないため、すべての場合で、相同体のアミノ末端側の半分だけにしかアラインメントされない。
【0044】
本発明者らは、免疫蛍光法の結果はM135Rが細胞表面に局在していることを示唆しているにもかかわらず、M135RがINFα/βと相互作用できることを実証する試みは否定的であったことを発見した。このような結果にも関わらず、本発明者らは、M135Rの欠失は、粘液腫ウイルスが宿主動物において病気を引き起こす能力を大幅に減弱させるが、一方、このような欠失をもつ粘液腫ウイルスは、野生型MVとインビトロで比較すると、細胞に感染して死滅させるのに同等の効果をもつことを発見した。このように、一つの態様において、本発明は、治療を受けている患者に尋常でない封じ込めストラテジーを行う必要がなく、粘液腫ウイルスを腫瘍退縮性ウイルス治療のためのより安全な代替法として提供できるため、機能的なM135Rを発現しない粘液腫ウイルスは、腫瘍退縮性の研究など、先天的な抗ウイルス応答を欠損した細胞を処理する上で有用であるという発見に関する。
【0045】
別の態様において、本発明は、粘液腫ウイルス感染に許容性のあるヒト腫瘍細胞において、抗癌剤であるラパマイシンが粘液腫ウイルスの感染力のレベルを高める働きをするという発見、および、ラパマイシンが存在しなければ、粘液腫ウイルスのある株の複製を制限するヒト腫瘍細胞において、ラパマイシンがあれば粘液腫ウイルスの一定の株の複製が可能となるという発見に関する。粘液腫ウイルス感染に許容性のある細胞とは、このウイルスが入り込むことができ、かつその中でウイルスが増殖的に繁殖できる細胞である。許容細胞は、タンパク質PTEN、PDK、AKT、GSK、Raf、mTORまたはP70S6Kを含む1つ以上の経路に欠損また変異があってもよい。制限細胞は、一定の条件下でのみ粘液腫ウイルスに対して許容的であるが、その他の条件下では増殖性感染を許容しない。例えば、制限細胞は、このウイルスの野生株に許容性があるが、変異型粘液腫株、例えば、MT−5遺伝子をノックアウトされた株は増殖的に繁殖させない。別の例において、粘液腫ウイルスに対して制限的な細胞は、粘液腫ウイルス単独での増殖的な感染を許容しないかもしれないが、ラパマイシンで処理すると、同じ粘液腫ウイルスが細胞に増殖的に感染することができるようになる。非増殖性の細胞株は、粘液腫ウイルス感染に対し非許容性であって、すなわち、ウイルスは細胞に入り込むことはできるかもしれないが、細胞に増殖的に感染はしないことを意味している。
【0046】
このように、ラパマイシンは、粘液腫ウイルスと併用すると、先天的な抗ウイルス応答を欠損した細胞に対する粘液腫ウイルスの感染力を高める。本発明は、先天的な抗ウイルス応答を欠損した細胞を処理するために、ラパマイシンを粘液腫ウイルスと併用することに関する。
【0047】
ラパマイシンは、土壌細菌であるストレプトマイセス・ヒグロスコピカス(Streptomyces hygroscopicus)から精製された活性抗真菌化合物であることが示されている大環状ラクトンである。本明細書において、ラパマイシンは、FKBP12と複合体を形成してmTORを阻害することができるラパマイシン(シロリムスとも称される)およびそのアナログまたは誘導体を意味し、アナログであるCCI−779(細胞周期阻害剤−779またはラパマイシン−42,2,2−ビス(ヒドロキシメチル)−プロピオン酸とも称される)およびRAD001(エベロリムスまたは40−Ο−(2−ヒドロキシエチル)−ラパマイシンとも称される)などを含む。ラパマイシン、CCI−779およびRAD001は市販されており、ラパマイシンは、Wyeth−Ayerstから商標Rapamuneという名称で購入可能である。ラパマイシンという用語は、さらに、ラパマイシンの医薬上許容される塩およびエステル、その水和物、溶媒和物、多形体、アナログまたは誘導体、ならびに、使用される過程、例えば、患者に投与されると、代謝または転換されてラパマイシンまたはそのアナログもしくは誘導体となるプロドラッグまたは前駆体も含む。
【0048】
細胞内シグナル伝達阻害剤としてのラパマイシンは極めて特異的であり、細胞に入り込んで、FKBP12として知られる細胞タンパク質に結合する。次に、ラパマイシン/FKBP12複合体は特異的な細胞内標的mTOR(哺乳類のラパマイシン標的)に結合する。多くの癌が、P13Kなどのシグナル伝達分子の過活性、または腫瘍抑制遺伝子PTENの欠如から発生することが示されている。これらの分子はどちらもmTORの上流に存在する。mTORは、細胞の増殖、成長、分化、遊走および生存の中心的調節因子であることが示されており、そのため、癌細胞の非制御成長を阻止する上で理想的な標的である。ラパマイシンに感受性の癌細胞株は、通常、mTORを介した経路の活性化の結果生じたものである。
【0049】
ラパマイシンは、シクロスポリン治療の代替治療または補完治療として、主に臓器移植患者に使用されている。臓器移植患者において、ラパマイシン治療は、一般にシクロポリンAまたはFK506よりも副作用が少ない。加えて、ラパマイシン治療を受けた患者のほうが一般に、癌の発生が少なく、かつCMV(ヘルペスウイルスであるサイトメガロウイルス)の発生率が低いことが、遡及研究によって示されている。したがって、特に、CMV複製がラパマイシンによって減少するはずであると仮定する研究を考慮すると、ラパマイシン治療によって粘液腫ウイルスの癌細胞への感染が促進されるのは意外なことである(Ponticelliによる“The pleiotropic effects of mTOR inhibitors” in J Nephrology 2004; 17: 762のレビュー)。特定の理論に制限されなくても、粘液腫ウイルスが、これらの細胞の腫瘍性表現型に関係しているかもしれないmTOR経路を介する異常なシグナル伝達を利用している可能性がある。そうであれば、mTOR阻害剤によってこの経路を操作することは、このウイルスにとって選択的な利益となるかもしれない。
【0050】
このようにして、先天的な抗ウイルス応答を欠損した細胞を阻害するための方法であって、このような細胞に有効量の粘液腫ウイルスを投与することを含む方法が提供される。さらなる実施態様において、このウイルスを、有効量のラパマイシンと併用して投与する。
【0051】
この粘液腫ウイルスは、ポックスウイルスのレポリポックスウイルス属に属する、複製可能なウイルスであればよい。この粘液腫ウイルスは粘液腫ウイルスの野生株でよく、または、粘液腫のMT−5ノックアウト株のように、遺伝子改変された粘液腫ウイルス株でもよい。この粘液腫ウイルスは、下記のように、機能的M135Rタンパク質を発現しない株など、ウサギにおいて弱毒化された効果を示し、その結果、病気のリスクが低くなっている株であってもよい。
【0052】
特定の実施態様において、粘液腫ウイルスは、機能的M135Rを発現しない粘液腫ウイルスである。
【0053】
機能的M135Rを発現しない粘液腫ウイルスは、遺伝子産物、安定型遺伝子産物、または機能的遺伝子産物が発現されないように欠失、置換または中断されたM135Rをコードするオープンリーディングフレームの一部または全部を持つ粘液腫ウイルスを含む。このようなウイルスは、M135Rをコードする遺伝子からタンパク質が発現されることがないように欠失、置換または中断された、M135Rの遺伝子調節領域の一部または全部を有する粘液腫ウイルスも含む。機能的M135Rタンパク質とは、転写され、翻訳され、折り畳まれ、翻訳後に修飾され、細胞の内部に局在化されるM135Rであり、粘液腫ウイルスが感染した宿主の中で粘液腫症を引き起こすことを可能にするものである。M135Rタンパク質が、全く、または適正に、または十分に転写されず、翻訳されず、折り畳まれず、翻訳後に修飾されず、細胞内に局在化されないために、感染した宿主が粘液腫症を発生しなければ、その時には、機能的M135Rが細胞内で発現されていない。
【0054】
さらなる実施態様において、細胞はインターフェロンに対して非応答性である。
【0055】
特定の実施態様において、細胞は哺乳動物の癌細胞である。一つの実施態様において、細胞は、ヒト固形腫瘍などのヒト癌細胞である。
【0056】
別の実施態様において、細胞はウイルスに慢性的に感染している。
【0057】
ラパマイシンと粘液腫ウイルスの投与するための「併用」は、同一の投薬形態で一緒に処方するか、または別々の投与形態で処方することができ、別々の投与形態の場合には、同じ様式で投与するため、または異なった投与様式で投与するために同じ形であっても、異なった形であってもよい。さらに、同じ投薬形態で一緒に投与しない場合に、ラパマイシンと粘液腫ウイルスを併用して投与するとは、ラパマイシンおよび粘液腫ウイルスを治療中の哺乳動物に同時に投与することを意味し、同時に、または任意の順序で連続的に、または異なった時点で投与することができることを意味する。このように、ラパマイシンと粘液腫ウイルスを別々に投与することも可能であるが、望ましい治療効果をもたらすよう時間的に十分近接させて投与することができる。
【0058】
本明細書において「有効量」という用語は、所望の結果を得るのに必要な投薬形態または期間において有効な量を意味する。
【0059】
本明細書において「先天的な抗ウイルス応答を欠損した細胞」という用語は、ウイルスに曝露されるか、ウイルスの侵入を受けた場合に、ウイルスの複製、インターフェロンの産生、インターフェロン応答経路の誘導、およびインターフェロンが介在しているか否かに関わらないアポトーシスなどの抗ウイルス防御機構を誘導せず、そのため、MVが、単独で、またはラパマイシン療法と併用すると感染することができる細胞を意味する。この用語は、ウイルスに曝露または感染したときに、正常な細胞、例えば、非感染細胞または非癌細胞と比較すると、先天的な抗ウイルス応答が低下または欠損している細胞を含む。これは、インターフェロンに対して非応答性である細胞、およびアポトーシス応答またはアポトーシス経路誘導が低下もしくは欠損している細胞を含む。この欠損は、感染、遺伝
子欠損、または環境ストレスなど、さまざまな原因によって生じうる。しかしながら、この欠損が既存の感染によって生じている場合、MVによる重感染は排除され、当業者はそのような例を容易に同定することができる。当業者は、過度の実験を行うことなく、いずれか所定の細胞型が先天的な抗ウイルス応答を欠損しているために、単独の、またはラパマイシン治療と併用した粘液腫ウイルスによって感染されうるか否かを容易に決定することができる。例えば、VSVを普通に用いて、細胞の抗ウイルス応答を測定することができる。
【0060】
所定の細胞型、例えば、所定の癌細胞型が先天性抗ウイルス応答不全であるか否かを評価するために、当業者は外植片を採取し、インビトロでこれらの細胞のいくつかを培養して、VSVによる、あるいは、ラパマイシンと併用した粘液腫ウイルスを含む粘液腫ウイルスによる感染の可能性を測定することができる。
【0061】
本明細書を通して、「インターフェロンに対して非応答性である細胞」という用語は、インターフェロンの活性、例えば、インターフェロンの抗ウイルス活性もしくは抗腫瘍活性に応答しない細胞、または異常なインターフェロン応答、例えば、インターフェロンに対する低下した、もしくは無効な応答を示すか、または、例えば、転写因子、例えば、STATlなどのシグナル伝達分子のリン酸化もしくは活性化によって測定すると異常なインターフェロンシグナル伝達を示す細胞を意味する。例えば、制限はないが、この細胞は、インターフェロンに対して応答性である細胞の中でそのような応答を誘導するのに十分な濃度のインターフェロンに曝露されても、増殖を阻害されず、または、死滅しないかもしれない。インターフェロンに対して非応答性の細胞は、細胞内シグナル伝達経路、または通常は応答性細胞の中で活性化されている経路に欠損があるかもしれない。典型的には、VSVによる感染に対する感受性は、インターフェロンに対する非応答性の指標であり、当業者は、インターフェロン存在下でVSV感染を阻止することができるか、またはその能力を欠いているかによって、あるいは、当技術分野において周知のインターフェロン活性のマーカーとなる他のもの、例えば、PKR、STAT、OAS、MXのように、INFによって刺激される遺伝子の発現レベルを用いて、特定の細胞がインターフェロンに対して非応答性であるか否かを簡単に判定することができる。
【0062】
本明細書を通して、「複製能がある」という用語は、特定の宿主の内部で感染および複製することができるウイルスを意味する。これは、特定の宿主の中では単独で複製を制限されているが、宿主細胞をラパマイシンで処理すると、ウイルスがその細胞に増殖的に感染することができるウイルスを含む。
【0063】
本明細書において、「細胞」という用語は、単一細胞および複数の細胞または細胞群を含む。細胞に薬剤を投与するとは、インビトロおよびインビボにおける投与を含む。
【0064】
本明細書において、「動物」という用語は、動物界の全生物を含み、具体的には哺乳動物、特にヒトを含む。
【0065】
先天的な抗ウイルス応答を欠損した細胞を「阻害する」という用語は、細胞を成長もしくは分裂できないようにすること、または細胞の増殖または分裂を低下もしくは遅延させることに加えて、溶解またはアポトーシスまたはその他の細胞死機構による細胞死を含む。
【0066】
当業者に周知で、例えば、Sambrook et al. ((2001) Molecular Cloning: a Laboratory Manual, 3rd ed., Cold Spring Harbour Laboratory Press)に記載されている標準的な分子生物学技術を用いて、粘液腫ウイルスのゲノムを容易に改変して、1つ以上の治療用導入遺伝子を発現させることができる。当業者は、粘液腫ウイルスのどの部分を欠失させれば、そのウイルスが依然として増殖性感染できるかを容易に決めることができるようになる。例えば、公表されたウイルスのゲノム配列を、特徴がはっきりした他のウイルスのゲノムと比較して、欠失させることができるウイルスゲノムの非必須領域を推定することができる(例えば、C. Cameron, S. Hota−Mitchell, L. Chen, J. Barrett, J.−X. Cao, C. Macaulay, D. Willer, D. Evans, and G. McFadden, Virology (1999) 264: 298−318)参照)。
【0067】
本明細書において、「治療用遺伝子」または「治療導入遺伝子」という用語は、その発現が所望の結果、例えば、抗癌作用をもたらす任意の遺伝子を広く説明しようとするものである。例えば、このウイルスを改変して、ウイルス治療の抗癌作用を増進する遺伝子を担持させることができる。このような遺伝子は、アポトーシスを開始させることに関与するか、または免疫を破壊するために感染細胞を標的とすることに関与する遺伝子であり、例えば、インターフェロンに対する応答の欠如を修復する遺伝子、または、細菌の細胞表面の抗原など、抗体の応答を刺激する細胞表面マーカーの発現をもたらす遺伝子などである。また、このウイルスを改変して、腫瘍性細胞または癌細胞の増殖および成長を遮断して、細胞が分裂できなくなることに関与する遺伝子を発現させることもできる。さらに、このウイルスを改変して、化学治療剤の合成に関与する遺伝子のような治療用遺伝子を含ませることができ、または、例えば、ヒト細胞など、阻害されるか死滅させられる細胞が由来する特定の生物種の細胞における複製量が増加するよう改変することができる。粘液腫ウイルスに挿入されて、その抗癌作用を高めることができる遺伝子の具体例は、TRAILタンパク質に関するヒト遺伝子、またはE4 orf4ポリペプチドをコードするアデノウイルス遺伝子などであるが、これらのタンパク質はいずれもヒト腫瘍細胞を死滅させることに関与する。
【0068】
当然のことながら、ラパマイシンと併用して使用される場合を含め、粘液腫ウイルスの治療効果は、このウイルスによる細胞溶解によって、またはこのウイルスによる治療薬の送達によって達成することができる。粘液腫ウイルスと併用してラパマイシンが含まれることによって、粘液腫ウイルス単独の効果を増強することが可能になるはずである。すなわち、粘液腫ウイルスは、ラパマイシンと併用して投与すると、粘液腫ウイルス単独のときよりも多数の標的細胞に増殖的に感染することができるか、またはラパマイシン不在下では粘液腫ウイルスによる増殖的感染を制限する、先天的な抗ウイルス応答を欠損した標的細胞に増殖的に感染することができるはずである。
【0069】
このウイルスは、当技術分野において周知の標準的な技術を用いて調製することができる。例えば、培養ウサギ細胞に使用すべき粘液腫ウイルス株を感染させてウイルスを調製することができ、感染を進行させて、ウイルスが培養細胞の中で複製し、当技術分野において既知の標準的な細胞表面破砕法によって細胞表面を崩壊させるとウイルスが遊離できるようにし、それによって、回収のためウイルス粒子を放出させることができる。ウイルスを回収したところで、ウサギ細胞のコンフルエントな細胞層に感染させてから、プラークアッセイを行なうことによって、ウイルス力価を測定することができる(Mossman et al. (1996) Virology 215:17−30参照)。
【0070】
また、先天的な抗ウイルス応答が欠損した細胞が存在することを特徴とする病状を治療するための方法であって、有効量の粘液腫ウイルスを、任意にはラパマイシンと併用して患者に投与することを含む方法が、そのような治療を必要とする患者に提供される。患者は、ヒトを含む哺乳動物など、任意の動物であってよい。
【0071】
本明細書において、「先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状」とは、先天的な抗ウイルス応答を欠損した細胞であって、これらの細胞を死滅させることによって病気、疾患、病状、もしくはその症状を治療することができる細胞が存在することに付随、関連、またはそれを特徴とする病気、疾患もしくは病状を意味する。例えば、病気の状態は癌であってよい。病気の状態はウイルスによる慢性感染症も含む。
【0072】
病状を「治療すること」は、臨床結果など、有益または所望の結果を得るための方法を意味する。有益または所望の臨床結果は、1つ以上の症状もしくは病状を緩和もしくは改善すること、病気の範囲が縮小すること、病状が安定すること、病気の発生を予防すること、病気の広がりを予防すること、病気の進行を遅延もしくは緩徐化すること、発病を遅延もしくは緩徐化すること、病状を改善もしくは緩和すること、ならびに(部分的もしくは全体的な)寛解を含むが、これらに限定されるものではない。「治療する」とは、治療を行わない場合に予想された生存期間を超えて患者の生存期間を伸ばすことを意味することも可能である。また、「治療する」とは、病気が進行するのを阻害して、病気の進行を一時的に緩徐化することを意味することも可能であるが、より好ましくは、病気の進行を永続的に停止させることを含む。
【0073】
一つの実施態様において、病状は癌である。癌は、必ずしも細胞の全部である必要はないが、細胞の少なくとも一部が先天的な抗ウイルス応答を欠損した任意の型の細胞であればよい。一つの実施態様において、癌は、細胞の少なくとも一部がインターフェロンに対して非応答性である癌であればよい。本明細書において、「腫瘍」、「腫瘍細胞」、「癌」および「癌細胞」という用語は(互換的に使用され)、細胞増殖の調節が顕著に失われることを特徴とする、異常な増殖を示す細胞または不死化している細胞を意味する。「癌」または「腫瘍」という用語は、転移性および非転移性の癌もしくは腫瘍を含む。本明細書において、「腫瘍性」または「腫瘍」という用語は、正常な増殖抑制機構なしに増殖する単一または複数の細胞を広く意味し、したがって、癌および異形成細胞もしくは過形成細胞に加えて、良性腫瘍を含む。
【0074】
癌は、悪性腫瘍の存在など、当技術分野において一般に受け入れられている診断基準を用いて診断することができる。
【0075】
本発明に従って治療することができる癌の型は、白血病、リンパ腫などの造血細胞癌、大腸癌、肺癌、腎癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮癌、前立腺癌、乳癌、子宮頸癌、直腸結腸癌、黒色腫およびその他の腫瘍を含むが、これらに限定されない。肉腫および癌腫などの固形腫瘍は、線維肉腫、粘液肉腫、脂肪肉腫、軟骨肉腫、骨原性肉腫、およびその他の肉腫、滑液腫瘍、中皮腫、ユーイング腫瘍、平滑筋肉腫、横紋筋肉腫、結腸癌、リンパ性腫瘍、膵癌、乳癌、肺癌、卵巣癌、前立腺癌、肝細胞癌、扁平上皮癌、基底細胞腫、腺癌、汗腺癌、脂腺癌、乳頭癌、乳頭腺癌、髄様癌、気管支原性肺癌、腎細胞癌、肺細胞腫、胆管癌、絨毛癌、ウィルムス腫瘍、子宮頸癌、精巣腫瘍、膀胱癌、およびCNS腫瘍(神経膠腫、星細胞腫、髄芽腫、頭蓋咽頭腫、上衣細胞腫、松果体腫、血管芽細胞腫、聴神経腫、乏突起膠腫、髄膜腫、黒色腫、神経芽細胞腫および網膜芽細胞腫など)を含むが、これらに限定されない。
【0076】
別の実施態様において、病状は慢性ウイルス感染症である。
【0077】
慢性的に感染するウイルスは、長期間にわたり持続的な形で動物の細胞内で感染および複製して、病態を引き起こすような任意のウイルスであってもよい。慢性感染ウイルスは、癌の発生と付随または関連するウイルスであってもよい。
【0078】
ウイルスの慢性感染症は、当技術分野において周知の標準的な方法を用いて診断することができる。例えば、慢性ウイルス感染症は、患者に抗ウイルス抗体が存在することによって、または患者の細胞の中にウイルスのRNAもしくはDNAが存在するかについて陽性試験することによって検出することができる。
【0079】
患者に投与する場合、有効量の粘液腫ウイルス、および任意には粘液腫ウイルスとラパマイシンを併用したものが、その投薬量または十分な期間において、このウイルスが病気を軽減、改善、緩和、寛解させ、その広がりを抑制し、その進行を緩徐もしくは遅延させ、または治療するのに必要とされる量である。例えば、癌性細胞または腫瘍細胞の数を減らしたり、破壊したりする効果、またはウイルスに慢性的に感染した細胞の数を減らしたり、破壊したりする効果、またはそのような細胞の成長および/または増殖を阻止する効果を達成するのに十分な量であろう。
【0080】
患者に投与すべき有効量は、粘液腫ウイルスおよび任意にはラパマイシンの薬力学的特性、投与方式、患者の年齢、健康状態および体重、病状の性質および範囲、治療頻度および、行っているならば、併用治療の種類、ならびにウイルスの毒性ならびに力価など、多くの因子に依存して変わりうる。
【0081】
当業者は、上記の因子に基づいて、投与する粘液腫ウイルスの適正な量を決定することができる。まず、患者の臨床反応に応じて、必要に応じて調整を加えることができる適当量にして、このウイルスを投与することができる。ウイルスの有効量は経験的に決定してもよく、それは安全に投与することができるウイルスの最大量、および所望の結果を生むウイルスの最小量に依存する。
【0082】
粘液腫ウイルスは、標準的な投与法を用いて患者に投与することができる。一つの実施態様において、このウイルスを全身的に投与する。別の実施態様において、このウイルスを病気の部位に投与する。特定の実施態様において、この病状は固形腫瘍であり、この腫瘍部位に注射によってウイルスを投与する。さまざまな実施態様において、ウイルスは、経口的もしくは非経口的に投与するか、または当技術分野において周知の標準的な方法によって投与することが可能である。
【0083】
全身にウイルスを投与する場合に、病気の部位にウイルスを注射することにより達成される効果と同じ臨床効果をもたらすためには、かなり高用量のウイルスを投与することが必要とされるであろう。しかし、適切な服用レベルは、所望の結果を得る最少量のはずである。
【0084】
投与するウイルスの濃度は、投与すべき粘液腫の具体的な株の毒性、および標的となる細胞の性質に応じて変わる。一つの実施態様において、約109プラーク形成単位(「pfu」)よりも少ない量をヒト患者に投与する。さまざまな実施態様において、約102から約109pfuの間、約102から約107pfuの間、約103から約106pfuの間、または約104から約105pfuの間を単一用量にして投与することができる。
【0085】
当業者は、上記の因子を用いて、患者に投与するラパマイシンの適正量を決定することができる。ラパマイシンの有効量は経験的に決定することができ、投与されるウイルスの量と株、安全に投与することができるウイルスの最大量、および粘液腫ウイルスの感染力の増強を実現するために投与することができるラパマイシンの最小量に応じて変わる。
【0086】
ラパマイシンは、標準的な投与法を用いて患者に投与することができる。一つの実施態様において、パマイシンを全身に投与する。別の実施態様において、ラパマイシンを病気の部位に注射して投与する。特定の実施態様において、病状は固形腫瘍であり、ラパマイシンをその腫瘍部位に注射によって投与する。さまざまな実施態様において、ラパマイシンを経口的もしくは非経口的に投与するか、または当技術分野において周知のいずれかの標準的な方法によって投与することができる。
【0087】
ラパマイシンの全量を単一用量にして、または1日または数日間にわたる多回用量にして投与することができる。用量の投与頻度および期間は容易に決定することができる。投薬計画は、粘液腫ウイルスを投与する期間に応じて決まる。例えば、ラパマイシンは、患者に単一回投与することもでき、または1日あたり2〜4回投与することもできる。
【0088】
さまざまな実施態様において、ラパマイシンの用量は1日あたり体重1kgにつき約0.01〜約250mg、1日あたり体重1kgにつき約0.01〜50mg、1日あたり体重1kgにつき約0.05〜10mg、1日あたり体重1kgにつき約0.1〜7.5mgであろう。
【0089】
有効量の粘液腫ウイルスとラパマイシンの併用剤を、初期治療計画の効果に基づいて、繰り返し投与してよい。投与は、典型的には、任意の反応をモニターしながら定期的に行われる。上記した用量よりも少ないかまたは多い用量を、選択された投与計画または経路に応じて投与してもよいと当業者は認識していよう。
【0090】
粘液腫ウイルスを、任意にはラパマイシンと併用して、単独療法として投与することができ、または、化学療法、放射線療法またはその他の抗ウイルス療法など、他の療法と併用して投与することができる。例えば、原発腫瘍の摘出手術の前もしくは後に、または、放射線療法もしくは従来型化学療法剤を投与するなどの治療の前、同時もしくは後に、粘液腫ウイルスを、任意には、ラパマイシンと併用して投与することができる。一つの実施態様において、その他の腫瘍退縮性ウイルスであって、多様な腫瘍細胞型に対して特異性を示しうるようなウイルスと組み合わせて、または逐次的に、粘液腫ウイルスを、任意にはラパマイシンと併用して投与することもできる。
【0091】
投与を容易にするために、粘液腫ウイルスを、任意には、ラパマイシンと併用して、医薬組成物の成分として調製することができる。したがって、さらなる実施態様において、粘液腫ウイルス、および任意にはラパマイシン、ならびに薬学的に許容される希釈剤を含む医薬組成物が提供される。したがって、本発明は、一つの態様において、先天的な抗ウイルス応答を欠損した細胞を阻害する際、または先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する際に使用するための医薬組成物も含む。この組成物は、薬学的に許容される濃度の塩、緩衝剤、防腐剤、およびさまざまな適合担体を通常含むことができる。すべての送達形態について、組換え粘液腫ウイルスを生理食塩水内で処方することができる。
【0092】
この医薬組成物は、追加的な抗癌剤など、別の治療薬をさらに含むことが可能である。一つの実施態様において、この組成物は化学療法剤を含む。この化学療法剤は、例えば、患者の癌細胞または腫瘍細胞に対して腫瘍退縮効果を示すが、粘液腫ウイルスの腫瘍殺傷効果を阻害または低下させないものであれば、実質的にいずれの薬剤であってもよい。例えば、化学療法剤は、アントラサイクリン、アルキル化剤、スルホン酸アルキル、アジリジン、エチレンイミン、メチルメラミン、ナイトロジェンマスタード、ニトロソ尿素、抗生物質、代謝拮抗剤、葉酸アナログ、プリンアナログ、ピリミジンアナログ、酵素、ポドフィロトキシン、白金含有剤またはサイトカインであってよいが、これらに限定されるものではない。好ましくは、化学療法剤は、癌性または腫瘍性である特定の細胞型に対して有効であることが知られているものである。
【0093】
医薬上許容される希釈剤の比率および同一性は、選択された投与経路、生ウイルスとの適合性、および適用可能な場合には、ラパマイシンの化学的安定性との適合性、ならびに標準的な薬学的実施慣行によって決定される。通常、医薬組成物は、生きた粘液腫ウイルスの生物学的特性を顕著には損なわず、ラパマイシンが含まれている場合には、その分解をもたらしたり、その安定性または効力を低下させたりしない成分とともに処方される。
【0094】
この医薬組成物は、有効な量の単一または複数の活性物質を医薬上許容される賦形剤との混合物として併用されるよう、患者に投与するのに適した医薬上許容される組成物を調製するための周知の方法によって調製することができる。適当な賦形剤は、例えば、Remington’s Pharmaceutical Sciences (Remington’s Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., USA 1985)に記載されている。これに基づいて、組成物は、一つ以上の医薬上許容される賦形剤または希釈剤とともに、適当なpHおよび生理液と等張の緩衝液に含まれている、任意にはラパマイシンが入った粘液腫ウイルス溶液を、これらに限定されずに含む。
【0095】
当業者には当然のことながら、医薬組成物は、選択された投与経路に応じて、さまざまな形で患者に投与することができる。経口的または非経口的に、本発明の組成物を投与することができる。非経口投与は、静脈内、腹腔内、皮下、筋肉内、経上皮、経鼻、肺内、くも膜下腔内、直腸および局所的な投与方式を含む。非経口投与は、選択された期間にわたる持続注入によるものであってもよい。
【0096】
医薬組成物は、例えば、不活性希釈剤または同化可能な担体とともに経口投与することができ、または、硬ゼラチンカプセルまたは軟ゼラチンカプセルの中に封入することができ、または、圧縮して錠剤にすることもできる。経口的に治療薬として投与するには、粘液腫ウイルスを、任意にはラパマイシンと一緒に、賦形剤に取り込み、消化可能な錠剤、口腔錠、トローチ、カプセル、エリキシル剤、懸濁剤、ウエハースなどの形態にして使用することができる。
【0097】
粘液腫ウイルス溶液を、任意にはラパマイシンと一緒に、生理学的に適した緩衝剤の中で調製することができる。通常の保存および使用条件下では、これらの調製物は微生物の増殖を阻止するための保存剤を含むが、それで生ウイルスが不活化されることはない。当業者ならば、適当な処方剤の調製法を知っているであろう。適当な処方剤を選択および調製するための従来の手順および成分については、例えば、1999年に出版されたRemington’s Pharmaceutical SciencesおよびThe United States Pharmacopeia: The National Formulary (USP 24 NF19)に記載されている。
【0098】
さまざまな実施態様において、組成物は、腫瘍部位など病気の部位に直接(皮下、静脈内、筋肉内などに)注射によって投与されるか、または経口投与、あるいは、経皮投与によって投与される。
【0099】
注射液として使用するのに適した医薬組成物の形態は、無菌の水溶液もしくは分散液、ならびに無菌の注射用の溶液または分散液を即時調製するための無菌粉末などであるが、ここで、無菌という用語は、投与される粘液腫ウイルス自体には及ばない。すべての場合において、剤形は無菌でなければならず、そして容易に注射できる程度に流動性でなければならない。
【0100】
使用される医薬組成物の用量は、治療中の特定の症状、症状の重症度、年齢、体調、体格および体重など個々の患者のパラメーター、治療継続期間、(もしあれば)併用療法の性質、具体的な投与経路、ならびに医療専門家の知識および専門技術範囲内にあるその他の類似要素なに応じて変わる。これらの要素は、当業者に周知のものであり、最小限の日常的実験作業によって扱うことができる。
【0101】
また、任意にはラパマイシンと併用される粘液腫ウイルス、または粘液腫ウイルスおよびラパマイシンを含む医薬組成物は、同じ処方剤の中で一緒に、または異なる処方剤にして、キットとしてパッケージにすることもでき、このキットは、それを必要とする患者に、粘液腫ウイルスを使用して、もしくはラパマイシンとともに粘液腫ウイルスを使用して、先天的な抗ウイルス応答を欠損した細胞を阻害するため、または粘液腫ウイルスを使用して、もしくはラパマイシンとともに粘液腫ウイルスを使用して、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するためなど、粘液腫ウイルスおよびラパマイシンを使用するための説明書を含む。この病状は癌、または慢性ウイルス感染症であってよい。それを必要とする患者において、
また、本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害するために、粘液腫ウイルスを、任意にはラパマイシンと併用して使用することを想定している。一つの実施態様において、細胞はインターフェロンに対して非応答性である。先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するために、それを必要とする患者に、粘液腫ウイルスを、任意にはラパマイシンと併用して使用することがさらに提供されている。一つの実施態様において、病状は癌である。また、薬剤の製造において、先天的な抗ウイルス応答を欠損した細胞を阻害するため、またはそれを必要とする患者において先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するために、粘液腫ウイルスを、任意にはラパマイシンと併用して使用すること提供されている。
【0102】
MVは、MVの自然宿主以外の動物の細胞、またはそれらに由来する細胞、すなわち、先天的な抗ウイルス応答を欠損している細胞集団に由来する細胞に選択的に感染することができる。MVにこのような能力があるため、培養中の、または動物の体内にある細胞の集団から、インターフェロンに対して非応答性の細胞など、先天的な抗ウイルス応答を欠失した細胞を検出する際にMVを使用することができる。このような細胞、例えば、蝕知可能な腫瘤にまで進行していないか、または動物の中で顕著な症状を誘起していない一定の癌細胞は、別の方法では容易に検出できないかもしれない。
【0103】
したがって、一つの実施態様において、患者の中で先天的な抗ウイルス応答を欠損した細胞を検出するための方法であって、検出可能なマーカーを発現するように改変された粘液腫ウイルスを、任意にはラパマイシンと併用して患者に投与すること;患者の中で、先天的な抗ウイルス応答を欠損した細胞にこのウイルス感染させること;および、患者の中で検出マーカーを発現する細胞を検出することを含む方法が提供される。
【0104】
感染細胞は、診断画像を視覚化するための従来の方法を用いて検出することができる。この検出法は、使用する具体的な検出用マーカーによって決まる。例えば、蛍光タンパク質を発現するように遺伝子改変された粘液腫ウイルスに感染した細胞は、蛍光デジタル画像顕微鏡を使用して検出することができる。その他の方法は、コンピュータ断層撮影法(CT)、陽電子放出撮影法(PET)などの全身走査法、核磁気共鳴影像法(MRI)、および超音波検査法などである。当業者は、具体的な検出マーカーを検出するための適切な方法を決めることができるだろう。
【0105】
検出可能なマーカーには、改変ウイルスに感染した細胞の内部で、マーカーの発現または合成が起きるように、それを発現または合成する遺伝子を粘液腫ゲノムに挿入することができる任意のマーカーがあるが、これらに限定されるものではない。例えば、一つの実施態様において、検出可能なマーカーは蛍光タンパク質でもよい。感染細胞は、改変ウイルスが先天的な抗ウイルス応答を欠損した細胞に感染して、検出可能マーカーをそのような細胞の中で検出可能なレベルで発現させることができるようにするため、改変ウイルスを患者に投与した後適当な時間をおいて検出することができる。例えば、蛍光タンパク質を発現するように遺伝子改変したウイルスを患者に投与した後、2〜20日間のいずれかの時点で検出することができる。
【0106】
先天的な抗ウイルス応答を欠損した細胞が患者に存在することをモニターするために、その患者において、間隔をおきながら繰り返し検出法を実施することができる。例えば、粘液腫ウイルスを用いて、そのような細胞を検出する方法は、先天的な抗ウイルス応答を欠損した細胞の性質、および患者の体内にそのような細胞が存在する結果として引き起こされたいずれかの病状の性質に基づき、必要に応じて、6ケ月、1年または2年の間隔で実施することができる。ある期間にわたりこの方法を繰り返すと、病状の進行もしくは寛解、または患者の体内での病気の広がりをモニターすることが可能になる。
【0107】
粘液腫ウイルスは、先天的な抗ウイルス応答を欠損した細胞に選択的に感染する能力があるため、細胞におけるそのような欠損の指示薬として使用することができる。したがって、本発明の方法を用いて、先天的な抗ウイルス応答の欠損について、患者から摘出した細胞をアッセイすることができる。このような測定法は、他の指示薬と併用すると、その患者が特定の病状、例えば、癌に罹患していることを表示することができる。
【0108】
したがって、一つの実施態様において、試料中で先天的な抗ウイルス応答を欠損した細胞を検出するための方法であって、細胞を培養すること、培養細胞を、任意にはラパマイシンと併用した粘液腫ウイルスに曝露すること、および粘液腫ウイルスによる細胞の感染力を測定することを含む方法が提供される。
【0109】
周知の生検法を用いて、ヒト被験者など、被験対象から細胞を取り出すことができる。生検法は、検査すべき細胞の存在する場所およびその型に応じて決められる。
【0110】
周知の培養技術に従って細胞を培養してから、培養液に生きた粘液腫ウイルス、および任意にはラパマイシンを添加することにより、細胞をMVに、任意にはラパマイシンに曝露する。粘液腫ウイルスをラパマイシンと併用して添加する場合、ウイルスとラパマイシンは、同時または経時的に添加することができる。ラパマイシンが存在する場合など、感染多重度(「MOI」)を変えて、所定の細胞型、密度および培養技術、および具体的なラパマイシン濃度に対して最適なMOIを、MVに曝露すると感染することが知られている陽性対照細胞の培養物を用いて決定することができる。
【0111】
ラパマイシンの量、ならびにラパマイシンおよび粘液腫ウイルスを培養細胞に添加するタイミングは、細胞型、培養方法、およびウイルス株に応じて変えることができる。このようなパラメーターは、常法を用いた最小限の検査法によって試験および調整することができる。
【0112】
MVの細胞死を引き起こす能力など、ラパマイシンが存在する場合も含んだMVによる培養細胞への感染力は、当業者に周知のさまざまな方法によって決定することができる。また、これは、ウイルスの発現産物との酵素反応または化学反応を完了させるために、細胞培養液に試薬を添加することも含むかもしれない。ウイルス発現産物は、MVゲノムに挿入されたレポーター遺伝子から発現されたものであってもよい。
【0113】
一つの実施態様において、MVを改変して、感染状態を検出するのを容易にすることができる。例えば、MVを遺伝子改変して、位相差顕微鏡、蛍光顕微鏡、または放射性イメージングによって容易に検出することができるマーカーを発現させることができる。このマーカーは、発現された蛍光タンパク質、または比色反応または放射標識反応に関与する可能性のある発現酵素であってもよい。別の実施態様において、このマーカーは、試験されている細胞の特定の機能を妨害または阻害する遺伝子産物であってもよい。
【0114】
本発明は、以下の非限定的な実施例によってさらに具体的に説明される。
【実施例】
【0115】
(実施例1:粘液腫ウイルスによるマウス細胞株およびヒト細胞株への感染)
(ウイルス株)
使用したウイルス株は、野生型MV、緑色蛍光タンパク質(「GFP」)またはβ−ガラクトシダーゼ(「LacZ」)を発現するように改変されたMV、および死滅(「不活化」)ウイルスを含む。標準的な技術を用いて、ウイルスを調製し滴定した。
【0116】
(細胞株)
野生型マウス、および以下のノックアウトマウスに由来するマウス胚線維芽細胞(「MEF」)を使用して、マウス実験を行った。すなわち、IFNα/β受容体ホモ接合ノックアウト、STATlホモ接合ノックアウト、PKRヘテロ接合ノックアウト、RNase Lヘテロ接合ノックアウト、Mx1ヘテロ接合ノックアウト、PKR/RNaseL/Mx1ホモ接合三重ノックアウト。
【0117】
Stojdl et al.,Cancer Cell(2003)4:263−275に記載されているように、BGMK対照細胞および以下のヒト腫瘍細胞株に対してヒトに関する実験を行った。すなわち、HT29、HOP92、OVCAR5、SK−MEL3、SK−MEL28、M14、SKOV3、PC3、DU145、CAKI−1、786−0、T47D、MDAMB435、SF04、U87、A172、U373、DaoyおよびD384。
【0118】
(方法)
一般的には、Lalani et al. Virology (1999) 256: 233−245; Johnston et al. J Virology (2003) 77(13): 7682−7688; and Sypula et al. Gen Ther Mol Biol (2004) 8: 103の記載に従って、アッセイ法および実験を行った。
【0119】
インビボでのマウス研究では、ヒト頭蓋内神経膠腫U87をヌードマウスに移植した。移植後15日目に、生きたMV GFPまたは不活化MV GFPを5×106の力価でマウスの腫瘍内に注射するか、擬似感染させた。感染後72時間目に、動物を殺してから、その脳を摘出してOCT(至適温度化合物)の中に埋め込み、凍結切片を切り出した。蛍光顕微鏡によって全脳切片の中で粘液腫GFPを可視化した。その後、切片を固定し、H&E(ヘモトキシリンおよびエオシン)を用いて染色して、腫瘍を可視化した。
【0120】
ヒト腫瘍細胞アッセイ法では、手術後直ちに、腫瘍をトリプシン処理して平板培養し、翌日、MOI0.1、1.0または10でウイルスに感染させた。感染後24時間目および48時間目に、位相差顕微鏡法および蛍光顕微鏡法を用いて、それぞれ細胞毒性およびウイルス発現に関するデータを集めた。黄色テトラゾリウム塩MTTを用いるアッセイ法を行って、感染後48、72または96時間目の細胞生存率(%)(擬似感染後生存していた細胞に対するパーセンテージ)を定量した。
【0121】
ヒト小児髄芽腫細胞株DaoyおよびD384を、10M.O.I.の粘液腫GFPに感染させた。感染後72時間目に、MTTを用いて細胞生存率を測定した。
【0122】
(結果:マウス細胞株の感染)
従来の研究では、ケモカイン受容体でトランスフェクトされたマウス3T3細胞のいくつかのクローンに、粘液腫ウイルスを感染させることができたが、その他のクローンには感染させることができなかったことが示されていた。他のマウス細胞において粘液腫ウイルス指向性がいずれか特定の受容体に依存しているか否かを調べるために、本発明者らは、野生型(WT)マウスおよび多様な遺伝子ノックアウト由来の初代マウス胚線維芽細胞(MEF)を利用した。
【0123】
IFNは抗ウイルス応答を開始する上で重要な役割を果たしているため、本発明者らはこの制限的な表現型(restrictive phenotype)が、IFNを介した「抗ウイルス状態」に関係があると仮定した。IFN系の事象の連鎖を断つか、抗体によって循環INFを中和するか、またはIFN受容体陰性マウスもしくは細胞内シグナル伝達経路の遺伝子を欠失したマウスを作成すると、通常は正常なマウス細胞には感染しない粘液腫ウイルスに対する宿主の抵抗性が著しく損なわれると考えた。
【0124】
この仮説を検証するために、本発明者らは、非許容性細胞における粘液腫ウイルスの非感染性がIFNの抗ウイルス活性のせいであるか否かを明らかにする必要があった。細胞内IFNシグナル応答に関与する1つ以上のタンパク質をノックアウトしたさまざまなMEF細胞型について、IFN経路に対するMV感染の効果を調べた。
【0125】
初代MEFに対して行われた実験によって、野生型(「WT」)MEFは粘液腫ウイルスによって感染可能ではないことが実証された。INF経路がINFα/βに対する中和抗体によってブロックされた場合、前記MEFは粘液腫ウイルスによって完全に感染可能になる(図2)。しかし、INFγに対する中和抗体に曝露されたMEFは非許容性のままであった。このことは、粘液腫ウイルスがインビトロでMEFに感染するのを許容する環境を作り出すことに、IFNγではなくIFNα/βが重要であることが大まかに示している。INFα/βおよびINFγに対するさまざまな細胞内シグナル伝達経路が文献中で同定されてきた。しかし、INFα/βおよびINFγはともに、培養された線維芽細胞とは異なり、感染宿主中において重要な役割を果たしている可能性が高い。本発明者らは、INFα/βおよび/またはINFγの経路のいずれかを欠損したヒト腫瘍がインビボでの粘液腫ウイルス感染に感受性になるものと予想している。
【0126】
本発明者らは、MVに感染した非許容性WT MEFの中でSTAT1およびSTAT2の活性を調べた。図3に示す結果は、STAT1およびSTAT2が活性化されることを示した。さらなる研究によって、STAT3、STAT4およびSTAT5は活性化されないことが示された(図4)。
【0127】
MEFの非許容性状態を維持する上でIFNα/β細胞内経路が重要性であることを確認するために、遺伝子欠失実験を行って、INFα/β受容体および細胞内カスケードを破壊したものを用意した。INF受容体またはJAK1もしくはSTAT1の遺伝子を欠失させ、MVを使用して、WT MEF、IFNα/β R−/−MEFおよびSTAT1−/−MEFを感染させた。IFNα/β R−/−MEFおよびSTAT1−/−MEFはMVに対して許容性であり、INFα/βおよびSTAT1カスケードがMV感染にとって重大な意味を持つことを明らかにした(図5)。
【0128】
プリテインキナーゼR(PKR)は、さまざまな細胞の中でINFα/βによって誘導される酵素である。このキナーゼは、dsRNAの存在下で自己リン酸化を受け、次に、リン酸化によってタンパク質翻訳およびアポトーシスの阻害を誘導することができる、真核生物のタンパク質合成開始因子(eIF−2α)など、いくつかの細胞タンパク質をリン酸化する。また、PKRはRNaseLの活性化にも示される。本発明者らは、MV感染後、非許容性MEFにおけるPKRの活性化を調べた。抗ウイルス状態が十分に確立している非許容性MEFでは、PKRはリン酸化されない(図6)。さらに、MV感染によって、PKRのリン酸化が阻害される(図7)。また、PERK(PKR様のERキナーゼ)は、粘液腫ウイルス感染後の初期の野生型MEF内でリン酸化されない(図8)。
【0129】
MVを用いて、PKR、RNaseLまたはMx1の単一遺伝子ノックアウトを有するMEFに感染させた(図9)。PKR、RNaseLまたはMx1は、粘液腫ウイルス感染に対する非許容性を維持するためには非必須であることが発見された。PKR、RNaseLおよびMx1の役割が必須でないことをさらに確かめるために、MEFにおいてPKR−/−、RNaseL−/−およびMx1−/−という三重ノックアウトを行った。PKR−/−、RNaseL−/−およびMx1−/−の三重ノックアウトは、MV感染を支持しない(図10)が、しかし、インターフェロンα/βに対する中和抗体で処理された、PKR、RNaseLおよびMx1の三重ノックアウトMEFは粘液腫ウイルス感染に対して許容性となる(図10および11を比較せよ)。これらの実験は、MVに対するMEFの非許容性をもたらす上で、PKR、RNaseLおよびMx1は必須ではないことを示している。
【0130】
さらなる実験を行って、MV感染後の非許容性野生型MEFおよび許容性のINFα/β R−/−MEFならびにSTAT1−/−MEFにおけるeIF2αおよびPKRの活性化を調べた。MV感染後に、eIF2αは非許容性MEFおよび許容性MEFの中でリン酸化されるが、PKRはどちらの場合においてもリン酸化されない(図12)。このことは、PKRおよびPERKの関与がなくても、eIF2αリン酸化を引き起こす別の経路によって、抗ウイルス状態がもたらされることを示している。
【0131】
STAT1は、非許容性のPKR、RNaseおよびMx1の三重ノックアウトMEFにおいて、MV感染後にセリンおよびチロシンのリン酸化を受ける(図13)。また、粘液腫ウイルス感染後の非許容性PKR−/−+RNaseL−/−+Mx1−/−MEFにおけるチロシンリン酸化STAT1の細胞内局在化も示されている(図14)。
【0132】
要約すれば、これらの結果は、IFN/STAT1を含む並行したPKR/PERK非依存的な抗ウイルス経路が、ポックスウイルス指向性にとって重大な意味を持つことを示している。さらに、eIF2αのリン酸化は、INFによる抗ウイルス作用の最良のマーカーである。
【0133】
(結果:ヒト腫瘍研究)
本発明者らは、MVがインビボ系の中でヒト腫瘍細胞に感染することができるかを調べた。ヌードマウスにヒト神経膠腫細胞を注射したところ、引き続いて、頭蓋内神経膠腫を発症した。生ウイルスは、これらのヒト腫瘍細胞に感染することができたが、周囲の細胞には感染しなかった(図15)。GFP由来の蛍光シグナルが腫瘍に局在化することを図16に示す。
【0134】
多くのヒト腫瘍がインターフェロンに対して非応答性であること、および、正常なヒト細胞の中に存在するINFシグナル伝達カスケードと比較すると、これらの腫瘍細胞は正常なINFシグナル伝達カスケードを持たないことから、ヒト腫瘍に対する粘液腫ウイルスの効果を調べるために実験を行った。結果を下記に要約する。
【0135】
最初に、粘液腫ウイルスを用いて、さまざまな対照腫瘍細胞株およびヒト腫瘍細胞株であるBGMK、HT29、HOP92、OVCAR4、SK−MEL3、およびSK−MEL28に対する感染力および細胞溶解性効果を調べた。MVは多様な感染力および細胞溶解作用の結果を示した:HT29(図17)、HOP92(図18)、OVCAR4(図19)、SK−MEL3(図20)、SK−MEL28(図21)およびBGMK(図22)。
【0136】
さらなる腫瘍細胞を検査し、下記の表1は、検査した多様な腫瘍型を許容性および非許容性に分類している。
【0137】
(表1 粘液腫ウイルスのヒト腫瘍細胞に対する指向性)
【0138】
【表1】

MV−LacZの濃度を増加させて感染させると、多様なヒト腫瘍株がさまざまな反応性を示した。例えば、U373細胞では、U87において低いウイルス力価で行われた細胞殺傷のレベルを達成するのに高いウイルス力価を必要とした(図23および図24)。粘液腫は星状細胞腫細胞(図25)および神経膠腫細胞(図26)を効率的に感染させた。粘液腫は感染48時間後、死滅したヒト星状細胞種および髄芽細胞腫において効率的だった。
【0139】
(実施例2:制限細胞株におけるにおける粘液腫ウイルス複製の動態に対するラパマイシンの効果)
(ウイルス株)
使用されたウイルス株は、野生型MV(「vMyxLac」)、およびMT−5遺伝子がノックアウトされるよう改変されたMV(「vMyxLacT5−」)を含む。標準的な技術を用いて、ウイルスを調製および滴定した。
【0140】
(細胞株)
ヒトに関する実験を、BGMK霊長類対照細胞、RK−13ウサギ対照細胞、および正常なヒト線維芽細胞A9、制限ヒト腫瘍細胞株786−0(腎臓癌)、ACHN(腎臓癌)、HCT116(結腸癌)、MCF−7(乳癌)、MDA−MB−435(乳癌)、M14(黒色腫)およびCOLO205(結腸癌)に対して行った。
【0141】
(方法)
一般的に、Lalani et al. Virology (1999) 256: 233−245; Johnston et al. J Virology (2003) 77(13): 7682−7688;およびSypula et al. Gen Ther MoI Biol (2004) 8: 103に記載されているとおりに、アッセイ法および実験を行った。
【0142】
ウイルスの増殖曲線には、細胞をインビトロで単層に増殖させ、ウイルスに感染させる前に20nMのラパマイシンまたは対照(DMSOを1:5000に希釈したもの)で処理した。
【0143】
表示されたウイルス株に感染した表示された細胞株の試料を、感染後72時間目に集めて、溶解させた。細胞溶解物の中に含まれるウイルスを滴定して、BGMKの単層を感染させるのに使用した。感染後48時間目に細胞を固定して、X−galを用いて染色した。
【0144】
(結果)
粘液腫ウイルスは多くの種類のヒト腫瘍細胞に感染して複製できることが、本発明者らによって既に明らかにされている(Sypula et al. (2004) Gene Ther. Mol. Biol. 8:103)。このウサギ特異的ウイルスは、NCI参照用コレクションに由来するヒト癌細胞株の大多数(約70%)に選択的に感染することができる。また、宿主域遺伝子M−T5が、これら多くの細胞株に粘液腫ウイルスが感染する際に重大な役割を果たすことが分かっている。
【0145】
ヒト腫瘍細胞の内部で粘液腫ウイルスが選択的に複製する能力に影響を与えることができる細胞内分子の可能性があるものを今回調査した際に、ラパマイシンの効果を調べた。
【0146】
図29から分かるように、低多重度感染(MOI)の後、粘液腫ウイルスが複製および拡散できることを、多段階増殖曲線を用い、BGMK(対照用霊長類細胞株);RK−13およびRL5(対照用ウサギ細胞株);4TlおよびB16F10(マウス癌細胞株);HOSおよびPC3(許容性ヒト細胞株)、786−0、HCT116、およびACHN(制限ヒト癌細胞株)、MCF−7、M14ならびにCOLO205(不全型ヒト癌細胞)を用いて行うことができる。野生型vMyxLacと、M−T5ノックアウトウイルスvMyxT5KOの両方を試験して、ラパマイシンによる予備処理した場合としない場合に、この2つのウイルスが単層全体に感染して拡散することができるかを調べた。BGMK細胞上で病巣形成させて、ウイルスの力価を測定した。感染させる6時間前に、20nMのラパマイシンまたは適当な賦形剤対照(DMSOを1:5000に希釈したもの)で細胞を事前処理した。
【0147】
実証されているように、ラパマイシンは、対照BGMK細胞に対しても、MT−5ノックアウトウイルスに対して非許容的なRL−5細胞を含む試験したウサギ細胞株のいずれに対しても何の効果も示さない。しかし、ラパマイシンは、マウス腫瘍細胞株の中では粘液腫ウイルスの複製を促進し、PC−3などの許容性(I型)細胞株の中では僅かに促進する。ラパマイシンは、HOS細胞のように非常に許容的な細胞に対しては効果が少ないが、それは、このような細胞株は既に粘液腫ウイルスに対して最大限許容的であるという事実による可能性が高い。ラパマイシンによる最大の効果は、制限性(II型)細胞株(786−0、HCT116およびACHN)で観察されたが、これらは、野生型ウイルスに対しては許容性があるが、vMyxT5KO株に対しては非許容性である。不全型(III型)細胞株であるMCF−7およびCOLO205においてさえもいくらかの効果が見られたが、不全型細胞株M14では見られなかった。
【0148】
次に、BGMKおよび786−0の感染細胞の試料を回収して溶解し、単離したウイルスを用いて、BGMK細胞の単層を感染させた(図30)。X−Gal染色を用いて、ウイルス感染した細胞を可視化した。
【0149】
粘液腫ウイルス感染に対して「制限的」な腫瘍細胞、すなわち、野生型粘液腫ウイルスの複製は許容するが、MT−5ノックアウトウイルスの複製は許容しない細胞をラパマイシンで処理すると、粘液腫ウイルスが、腎臓癌、結腸癌、および卵巣癌の細胞株を含む癌細胞株において複製する能力を回復する結果となった(図29および30)。
【0150】
さらに、ラパマイシンで処理すると、野生型ウイルスがこれらと同じ細胞の中では複製する能力は増強されたが、対照であるウサギ細胞または霊長類細胞では増強されなかった。これらの結果は、ラパマイシンが粘液腫ウイルスの感染を促進するように作用することを示している。また、ラパマイシンは、このウイルスに感染されにくい癌細胞がウイルス複製を許容する能力に影響を与えると考えられる。
【0151】
その後の実験で、野生型粘液腫ウイルスの感染を支持することができなかったヒト腫瘍細胞に対するラパマイシン処理の効果を調べた(図31)。この事前処理は、対照である霊長類細胞や正常なヒト線維芽細胞に対してほとんど効果を示さなかったが、乳癌細胞株MCF−7など、いくつかの細胞株におけるウイルスの感染力を増強することができた。ヒト腫瘍細胞のいくつかが、対照細胞株と同じように、ラパマイシン処理に対して抵抗性のままであったため、ラパマイシン処理によって、粘液腫ウイルスが、非形質転換組織に増殖性感染できるようになったとは考えにくい。
【0152】
(実施例3:改良型腫瘍退縮性ウイルス候補としての粘液腫ウイルスM135KO変異型。)
(M135Rは、初期遺伝子として粘液腫ウイルスから発現される)
粘液腫ウイルスは、MVゲノムの配列決定から同定されたタンパク質(M135R)をコードし(Cameron et al. Virology (1999) 264: 298−318)、宿主のIFNα/β受容体を模倣し、IFNα/βが宿主の抗ウイルス応答を開始させないようにしていると予測されている (Barrett et al. Seminars in Immunology (2001) 13:73−84)。この予測は、そのような免疫回避戦略を採ることが明らかになっている(Symons et al. Cell (1995) 81 :551−560)ワクシニアウイルス(B18R)に由来するウイルスIFNα/β受容体のホモログに対する配列相同性に基づいている。しかし、M135Rは、VVB18R、およびその他配列決定されたポックスウイルス由来のINFα/β−R相同体の大きさの半分しかないため、すべての場合で、ポックスウイルスIFNα/β−Rの相同体のアミノ末端側の半分だけにしかアラインメントされない。図32は、MVのM135RとVVのB18Rの間で予測された構造および配列の類似性を示している。B18Rの最初の179アミノ酸残基だけが、配列アラインメントで示されている。表2は、M145Rと、表示されたポックスウイルスIFNα/β−Rの相同体との一致率(%)を示している。対角線の上の数字は、一致率(%)を表し、対角線の下の数字は、2つの種間における類似性(%)を表している。上部を横切る括弧内の数字は、推定されたタンパク質のアミノ酸数を表している。予測されたM135R(178アミノ酸)の全長コピーと各相同体の最初の178残基だけの間で比較を行った。
【0153】
(表2 M135Rと他のポックスウイルス相同体との比較)
【0154】
【表2】

M135Rの推定免疫原領域に対するペプチドを合成して、ウエスタンブロット解析、免疫沈殿、および免疫蛍光法で使用したポリクローナル抗体をウサギの中で作製した。免疫ブロッティングによって、M135Rが、感染後早くも3時間でその発現を検出できる初期遺伝子として合成されていることを確認した(図33A;レーン1:模擬感染BGMK細胞;レーン2〜6:それぞれ感染後0、3、6、18、および36時間目のvMyxLauに感染したBGMK細胞)。感染細胞をAraCで処理すると、M135Rの合成は、後期のタンパク質発現を阻害しても変化することがないため、これは初期遺伝子であることが示される(図33B)。しかし、ツニカマイシンで処理すると、おそらく、配列から予測された単一の部位で、M135RはN結合型グリコシル化されていることが示される(図33B)。モネンシン処理によって、O結合型グルコシル化は存在しないことが示唆されている。図33に示されている結果について、BGMKには、moi10で粘液腫ウイルスを感染させた。40μg/mlの濃度のAraC、1μg/mlのツニカマイシン、および1μg/mlのモネンシンで、表示された時間に細胞を処理したか、処理しなかった。ペプチド抗体を用いてM135Rを検出した。
【0155】
(M135Rはシグナル配列をコードするが分泌されない)
M135Rの配列解析によって、推定シグナル配列が存在することが示されている(図32B)。しかし、カルボキシ末端には膜貫通ドメインと推定されるものもある(図32B)。感染BGMK細胞から得た上清の免疫ブロットは、M135Rが分泌されないことを示している。しかし、M135Rは、全細胞溶解液の中で簡単に検出される(図33)。シグナル配列が、M135Rを細胞表面に追いやるよう機能したか否かを調べるために、本発明者らは、膜貫通ドメインを欠失させ、この変異体をバキュロウイルス発現系にクローニングした。Ac135RとAc135ΔTMに感染した上清を比較したところ、全長のM135Rが細胞溶解液中に見られ、分泌された証拠はない。これに対し、Ac135ΔTMは分泌され、シグナル配列がM135Rを細胞外環境に追いやるよう機能していることが確認できる(データは示さず)。
【0156】
(M135Rタンパク質は、感染細胞の表面に局在する)
M135Rが機能的なシグナル配列と膜貫通ドメインをもつという観察結果から、本発明者らは、急いでM135Rの局在を調べた。2つの証拠が、M135Rが細胞表面に局在することを示している。まず、BGMKをカバーガラスの上に播種して、24時間vMyxLau(moiは10)に感染させると、アフィニティー精製された抗M135R、次いでFITC結合二次抗体による免疫染色でM135Rが検出された(図34A)。M135Rの染色パターンは、感染した細胞の細胞表面への局在を示している。vMyxLauは、β−gal遺伝子やEGFP遺伝子の挿入によって改変されていない真正な粘液腫ウイルスの野生型である。
【0157】
第二の証拠は、M135Rが、vMyzgfpまたはvMyx135KOのどちらかに感染したGHOST細胞の細胞表面タンパク質のビオチン化に付随することである。感染後24時間で細胞溶解液を調製した。ストレプトアビジンアガロースビーズを、細胞溶解液から得た全細胞タンパク質500μgと45分間混合した。このビーズを洗浄して、15%SDS−PAGEゲルで分離してから、抗M135Rでプローブした。感染した細胞の溶解液から得た50μgの全細胞タンパク質を対照として泳動した。ビオチン化した表面タンパク質を免疫沈殿すると、m135Rが感染した細胞の表面に存在することが示される(図34B)。
【0158】
(M135Rはインビトロにおける粘液腫ウイルスの複製に必須ではない)
M135Rが病原性因子として作用することができるかを調べるために、本発明者らは、M135Rを欠失し、VV早期/後期プロモーター下でEGFPおよびgptをコードするカセット(460ヌクレオチド、すなわちorfの86%が欠失している)で置換されている組換えウイルスを構築した。クローニング法およびカセットを図35Aに示す。EGFPを発現するウイルスクローンを選択して、組換体をプラーク精製した。組換体の精製度をPCRで確認した(図35B;レーン1は1Kb+DNAラダー、レーン2および3は、2つの精製vMyx135KOクローンからのPCR産物。PCR産物は、M135Rのコード領域が欠失されて、EGFP/gptマーカーが挿入されている領域を表している。レーン2はプラーク1であり、レーン3はプラーク2である。レーン4は、同じ領域を示し、本来の切断されていないM135R遺伝子座をカバーしている)。vMyxLauまたはvMyx135KOのいずれかに感染したBGMK細胞の免疫ブロッティングによって、vMyx135KOがM135R発現を失ってしまったことが確認された(図35C;M135Rの発現の経時変化:レーン1は未感染のBGMK細胞。レーン2〜6は、感染後0時間(レーン2)、3時間(レーン3)、6時間(レーン4)、18時間(レーン5)、および36時間(レーン6)における、vMyx135KOに感染したBGMK細胞を示している。レーン7および8は、感染後6時間(レーン7)および18時間(レーン8)における、vMyx135KOに感染したBGMK細胞を示している。レーン9は、AcNPVで発現するM135Rをもつ陽性対照である)。
【0159】
一段階増殖曲線を用いて、vMyx135KOがBGMK細胞の中で複製できるかを調べた。BGMK細胞を、moi5でvMyxgfpまたはvMyx135KOに感染させ、表示された時間に細胞を回収した。ウイルスの力価をBGMK細胞上で測定した。vMyxgfpとvMyx135KOの間で複製パターンの違いはなかった(図36)。これらの結果は、M135Rがインビトロでの複製には必要でないことを示している。
【0160】
粘液腫ウイルスの別の遺伝子が、ウサギの初代胚線維芽細胞(REF)における粘液腫ウイルスの複製に影響できないかを調べた本発明者らの実験の際に、ノックアウト対照としてvMyx135KOを用いたが、奇妙な現象を観察した。REFにvMyxgfpを感染させると、正常な感染病巣が生じたが、vMyx135KOは、感染のプラーク様ゾーンを生じさせた(図37)。本発明者らが、この表現型を確認するために別の細胞を調べたとき、別のウサギ線維芽細胞(HIG−82、図38)およびヒト初代線維芽細胞(ccd922−sk、図39)では、プラーク形成を反復させることができた。
【0161】
(M135Rはウサギにおける病原性に対する重大な病原因子である)
次に、本発明者らは、vMyx135KOが実験用ウサギの中で粘液腫を発生させることができるかを調べた。vMyxLauまたはvMyxgfpを感染させて、感染後9から10日の安楽死させなければならない動物とは対照的に、vMyx135KOを注射されたウサギは完全に回復した(表3)。M135Rの消失がvMyx135KOの弱毒化をもたらすことを確認するために、本発明者らは、M135Rが回復された復帰変異体ウイルスを作製し、この復帰変異体(vMyx135REV)が、粘液腫を生じさせる能力を回復することができるかを調べた。4つのウサギの処理グループはすべて、各ウイルスを注射してから最初の6日間は同じように応答した(表3)。本発明者らは、感染後4日目までは、すべての処理グループで、注射した部位に大きく赤い盛り上がった病変部ができるのを観察した。しかし、6日目に始まり、その後引き続き3〜4日間にわたって、さまざまなウイルスの間の違いが明らかになった。野生型または復帰変異型ウイルスを注射した動物は、耳、眼、および鼻に、vMyx135KOを注射した動物には見られなかった数多くの二次的病変部を持っていた(表3)。本発明者らは、動物モデルにおいて、M135Rの消失は劇的にMVを弱毒化すると結論づけ、M135Rが重大な病原因子であることを示している。
【0162】
(表3 野生型対照と比較したときのvMyx135KOの病原性)
【0163】
【表3】

実験前の3日間、ウサギの体温を毎日測った。これを動物の基礎体温と見なした。実験の間中、各動物の体温を毎日測り続けた。しかし、処理グループ間に体温の違いはなかった(図40)。これは、M135Rが、感染動物の発熱反応に関与していないことを示唆するものである。
【0164】
(M135RはウサギIFNα/βに結合または阻害しない)
M135Rの配列は、IFNα/β受容体の模倣体であるワクシニアB18Rに類似している。本発明者らは、M135Rがウサギの1型IFNに結合できるかを調べた。まず、ウサギIFN(5μg、ヨードビーズを用いて)をヨウ素化して、vMyx135KOに感染した細胞が、vMyxgfpを(moi10で)感染させた細胞と比較して、125I−ウサギIFNに結合できるかを調べた。細胞を回収して、洗浄し、ガンマ線計測装置で計測した。M135Rの欠失は、感染細胞へのIFNα/βの結合に影響せず、RK13細胞またはBGMK細胞のいずれかの細胞表面に結合しているIFNの量に差異は見られなかった(図41)。また、RK13細胞またはBGMK細胞を外来性のウサギ1型IFNで処理しても、vMyx135KOによる細胞への感染には影響を与えなかった(図42;細胞を12穴培養皿に播種し、表示されたウイルスにmoi0.01で感染させた;感染後72〜96時間目に蛍光巣の数を数えた;200ユニットのウサギIFNα/βを、感染させる24時間前に添加するか、細胞を処理しなかった)。この同じ結果が、感染させる24時間前に事前処理して、細胞の中で抗ウイルス状態を誘導したときにも見られた。RK13細胞またはBGMK細胞のいずれかで感染後に形成される巣に顕著な違いがあることに気づかなかった(データは示さず)。また、この現象は、細胞をヒトIFNA/Dで処理した場合にも当てはまる(データは示さず)。また、Ac135ΔTMの上清を、BIAcoreチップに付着させたウサギIFNα/βに適用すると、結合を全く観察できなくなった(データは示さず)。
【0165】
(実施例3:粘液腫ウイルス感染に関連してmTORを阻害することの分子的影響)
ラパマイシンが粘液腫ウイルス感染を促進するII型癌細胞株である786−0細胞の細胞溶解液を用いてウエスタンブロット解析を行った(図43)。vMyxLacまたはvMyxT5KOのいずれかをMOI3で感染させたか、ウイルス感染させないままで16時間経過した後に溶解液を回収した。表示したレーンには、感染前6時間20nMのラパマイシン(Rと命名)、または適当な賦形剤対照(DMSOを1:5000で希釈したもの、Dと命名)で事前処理した細胞からのタンパク質を含む。表示したタンパク質に対する一次抗体を用いてブロットをプローブした。
【0166】
実証されたように、粘液腫ウイルス感染は、ラパマイシンの生理学的標的であるmTORに収束する多くのシグナル伝達経路に影響を与える。ラパマイシンがウイルス複製に大して有利な効果をもつ、野生型ウイルス(vMyxLac)またはMT−5欠損型ウイルス(vMyxT5KO)のいずれかによる感染に関しては、ラパマイシン単独処理に基づいては予測しえなかった広範囲の効果が、これらのシグナル伝達分子の多くで見られた(模擬感染レーンを参照)。これらの効果には、AKT−1、Raf−1、GSK−3β、およびmTOR自身のキナーゼ活性が増加すること、ならびにPTENおよびp70S6Kのキナーゼ活性が低下することが含まれる。このデータは、これらの経路が、ヒト癌細胞株における粘液腫ウイルスの許容性に関与している可能性を示している。
【0167】
当業者には理解できるように、本明細書に記載した例示的な実施態様に多くの変更を加えることが可能である。それどころか、本発明は、請求項に記載されているように、そのような変更もすべてその範囲に含もうとするものである。
【0168】
本発明のさまざまな実施態様が本明細書に開示されているが、当技術分野における技術常識に従って、多くの適応および変更を本発明の範囲内で行うことができる。そのような変更には、同じ結果を実質的に同じ方法で得るために、本発明の何らかの態様について同等物であることが知られているものと置換することを含む。本明細書で使用される科学技術用語はすべて、別段の記載がない限り、本発明の技術分野における当業者に広く理解されている意味と同じ意味を有する。
【0169】
本明細書で引用されている参考文献はすべて参照されて、全部が組み込まれる。
【技術分野】
【0001】
(関連出願の引用)
本出願は、米国仮特許出願第60/658,816号(2005年3月7日出願)の優先権を主張し、その内容は、本明細書中で参考として援用される。
【0002】
(発明の分野)
本発明は、一般的には、粘液腫ウイルスとラパマイシンの治療的利用に関する。
【背景技術】
【0003】
(発明の背景)
さまざまな種類の癌を治療するために使用される現在の治療法は、癌細胞を毒殺または死滅させることによって効果を発揮するというものになりがちである。残念なことに、癌細胞に対して毒性のある治療法は、健常な細胞にも有毒になりがちである。さらに、腫瘍の異質性が、依然として有効な癌治療が得られないことの主な理由の一つとなっている。化学療法や放射線療法など、現在主流の治療法は、狭い治療毒性濃度域内で使用されがちである。多様な種類の腫瘍細胞があり、これらの治療法を行うことができる濃度域が限られているため、この種の療法は、切れ味の鈍い手段と見なされている。
【0004】
現在開発中の新しい抗癌療法は、腫瘍細胞を選択的に標的とする一方で、健常な細胞に対する毒性をより低くして、健常細胞が影響を受けないままでいる可能性をより高くしようと試みている。
【0005】
腫瘍退縮性ウイルス療法が、腫瘍細胞と正常細胞との細胞間の違いを利用することを目的とする方法の一つである。この療法は、複製能のある腫瘍選択的なウイルスベクターを抗癌剤として使用する。腫瘍退縮性ウイルスは、感染のために癌細胞を特異的に標的するか、または、正常細胞よりも癌細胞において効率的に複製するのに適している。これら複製能のある腫瘍退縮性ウイルスは、不均一な腫瘍集団を標的する非常に選択的かつ強力な手段となる天然または遺伝子操作されている。複製選択的な腫瘍退縮性ウイルスは、正常な細胞では効率的に複製しないため、特に、放射線療法や化学療法のような伝統的な療法と比較して患者に対する毒性が低いはずである。
【0006】
数多くの研究で、さまざまなウイルス株について腫瘍退縮活性が報告されているが、最も有望な腫瘍退縮性ウイルスは、天然または遺伝子改変されたアデノウイルス、単純ヘルペスウイルス1型(「HSV1」)、レオウイルス、ワクシニアウイルス、水疱性口内炎ウイルス(「VSV」)、またはポリオウイルスである。抗癌剤として現在検討されている改変型腫瘍退縮性ウイルスは、HSV、アデノウイルス、ニューカッスル病ウイルス(「NDV」)、レオウイルス、およびワクシニアウイルス、麻疹、VSV、およびポリオウイルスなどである。さまざまな腫瘍退縮性ウイルスが、第一相および第二相で臨床試験されており、いくつかは持続した効能を示している。しかし、どのウイルスが、持続的複製、特異的かつ強力な退縮活性という目標をもっともよく達成するかは分かっていない。腫瘍退縮性ウイルスベクターの完全に効率的な候補は、生活環が短く、すぐに成熟したビリオンを形成し、細胞から細胞へ効率的に伝播し、すぐに挿入可能なゲノムをもつものである。その上、初期の先天的な免疫応答を阻害し、Th1応答の発達を遅延させることが、腫瘍退縮療法の有効性にとって重要なことが、証拠によって示唆されている。腫瘍退縮性ウイルスの開発用に想定されているウイルスの多くに対して正常な集団で見られる大量の抗体およびT細胞反応から見て、ヒトのウイルスが非常に免疫原性であることは明らかである。
【0007】
臨床実験によって、現在の腫瘍退縮性ウイルスは実際に安全であるが、単剤療法として臨床上十分に有効であるとするほど強力でではない。腫瘍細胞への不十分または不効率な感染が普通に見られるため、現在の動きは、候補ウイルスの効率を上げるために、それらを遺伝子操作して治療用の導入遺伝子を発現させることによりそれらを武装させようとするものである。上記した腫瘍退縮性ウイルスのほとんどは、他の一般的な腫瘍退縮療法と組み合わせてテストされている。
【0008】
アデノウイルスは、容易に遺伝子操作することができ、よく知られた関連するウイルスタンパク質機能を持っており、また、非常に軽度の病態に関連している。ONYX−015ヒトアデノウイルス(Onyx Pharmaceuticals Inc.)は、最も広範に試験されている。臨床使用用に最適化された腫瘍退縮性ウイルスであり、p53陰性腫瘍の中で選択的に複製すると考えられて、頭頸部癌患者での臨床試験において可能性を見せている。しかし、報告によれば、ONYX−015は、治療した患者の14%で客観的な臨床反応を示しているにすぎない(非特許文献1)。
【0009】
特許文献1と特許文献2は、腫瘍細胞の増殖を阻害し、神経細胞に特異的な変異型腫瘍退縮性HSVを記載している。さらなる利点は、HSVは簡単に遺伝子改変することができ、不要なウイルス増殖を止める薬剤が存在していることである。しかし、一般の集団はこのウイルスに曝露されて免疫反応を獲得していて、このウイルスの腫瘍退縮効果が弱まっていると考えられるため、このような普遍的ヒト病原体の使用には限界がある。また、HSVは、重大な副作用または死に至る可能性がある病気を引き起こす可能性もある。
【0010】
III型レオウイルスは、比較的軽度な病気と関連し、そのウイルス遺伝子の機能がかなり十分に理解されている。III型レオウイルスは、変異型ras発癌遺伝子を発現する細胞において増進された複製特性を示し、かつPKR −/−細胞の中で選択的に増殖する癌治療剤として、現在、Oncolytic Biotech社によって開発されているところである(非特許文献2)。しかし、レオウイルスは、遺伝子操作することが難しく、そのウイルス複製を簡単に止めることができない。
【0011】
VSVは、比較的軽度な病気に関連しており、よく知られたウイルス遺伝子機能をもっている。WO99/04026には、さまざまな疾患に広く治療効果を表すためにVSVをベクターとして遺伝子治療法に使用することが記載されている。しかし、VSVは、遺伝子操作が困難であり、また、そのウイルス複製を簡単に止めることができないという点で、レオウイルスと同じ問題を抱えている。
【0012】
ワクシニアウイルスおよびポリオウイルスは、当技術分野において記載のある別の腫瘍退縮性ウイルス候補であるが、重大であるか、または死に至る可能性がある病気と関連している。
【0013】
特許文献3は、ヒト腫瘍細胞に対してガンマインターフェロンとIFNγの断片を使用することを開示している。特許文献4は、病気の細胞がインターフェロンが介在する抗ウイルス応答に欠損をもつヒトの病気を治療する方法であって、治療上有効な量のインターフェロン感受性で複製能をもつクローンウイルスをヒトに投与することを含む方法を開示している。具体的には、VSV粒子が腫瘍細胞に対して毒性活性を有するが、インターフェロン存在下では、正常細胞においてVSVによる細胞毒性の改善が起こることを開示している。また、特許文献4は、インターフェロン処理された腫瘍細胞でNDVに誘導された感受性が見られたが、正常な細胞にインターフェロンを加えると、これらの細胞はNDVに対して抵抗性になることも開示している。この方法は、細胞にインターフェロン感受性のウイルスを感染させることによって、それらをインターフェロン感受性にすることを目的としている。
【先行技術文献】
【特許文献】
【0014】
【特許文献1】国際公開第96/03997号パンフレット
【特許文献2】国際公開第97/26904号パンフレット
【特許文献3】米国特許第4,806,347号明細書
【特許文献4】国際公開第99/18799号パンフレット
【非特許文献】
【0015】
【非特許文献1】Nemunaitis J,Khuri F,Ganly I5 Arseneau J,Posner M,Vokes E,Kuhn J,McCarty T,Landers S,Blackburn A,Romel L,Randlev B,Kaye S,およびKirn D.,J.Clin. Oncol,2001年1月15日,第19巻,第2号,p.289−98
【非特許文献2】Strong J.E.およびP.W.Lee.,J.Virology,1996年,第70巻,p.612−616
【発明の概要】
【課題を解決するための手段】
【0016】
(発明の要旨)
本発明は、機能的なM135Rタンパク質を発現しない新規の粘液腫ウイルスを含む、ウサギ粘液腫ウイルスが、インターフェロンに対して非反応性の細胞など、先天的な抗ウイルス応答を欠損した、ヒト腫瘍細胞などの細胞に選択的に感染することができ、このような感染が、薬剤であるラパマイシンで前記細胞を処理することにより促進されるという予想外の発見に基づいている。これと関連して使用される場合、「先天的」という用語は、非抗原特異的な免疫反応を表している。粘液腫ウイルスは、正常なヒト細胞では効率的に複製できないため、インターフェロンに対して非感受性の細胞など、先天的な抗ウイルス応答を欠損した細胞を特徴とするさまざまな疾患および症状に対する治療法として、例えば、癌に対する腫瘍退縮治療法として、このウイルスを使用することができる。また、このウイルスを、先天的な抗ウイルス応答を欠損した細胞を同定するため、また、これらの細胞をインビボで画像化するために使用することもできる。
【0017】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害する方法であって、粘液腫ウイルスとラパマイシンを組み合わせたものの有効量を細胞に投与することを含む方法を提供する。
【0018】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に粘液腫ウイルスとラパマイシンを組み合わせたものの有効量を投与することを含む方法を提供する。
【0019】
本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害するため、および、先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤を製造するための、有効量の粘液腫ウイルスとラパマイシンの合剤の使用をさらに提供する。
【0020】
本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする患者の病状を治療するため、および患者におけるそのような病状を治療するための薬剤を製造するための、有効量の粘液腫ウイルスとラパマイシンの合剤の使用をさらに提供する。
【0021】
別の態様において、本発明は、粘液腫ウイルスとラパマイシンを含む医薬組成物を提供する。この医薬組成物は、先天的な抗ウイルス応答を欠損した細胞を阻害するため、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するために役立つことができる。
【0022】
別の態様において、本発明は、粘液腫ウイルス、ラパマイシン、および先天的な抗ウイルス応答を欠損した細胞を阻害するため、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための説明書を含むキットを提供する。この病状は、癌および慢性ウイルス感染症を含む。
【0023】
本発明は、先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、細胞集団を、粘液腫ウイルスとラパマイシンの混合物に曝露すること、ウイルスを、先天的な抗ウイルス応答を欠損した細胞に感染させること、および細胞集団のどの細胞が粘液腫ウイルスに感染したかを決定することを含む方法を提供する。
【0024】
本発明は、さらに、ウサギ粘液腫ウイルスタンパク質M135Rが、ウサギにおける免疫応答を誘発するのに関与していること、および機能的なM135Rを発現しない粘液腫ウイルス株は、インビトロで細胞を死滅させることができるが、動物では粘液腫症を引き起こさないという予想外の発見に基づいている。このようなウイルス株は、薬剤であるラパマイシンと併用して投与される治療法など、インターフェロンに対して非感受性の細胞を含む、先天的な抗ウイルス応答を欠損した細胞を処理するために使用することができ、ウイルスの混入を増加させる必要がないため、安全性を向上させる結果となる。
【0025】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害する方法であって、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して細胞に投与することを含む方法を提供する。
【0026】
一つの態様において、本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して投与することを含む方法を提供する。
【0027】
本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害するために、および先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤を製造する際に、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して使用することをさらに提供する。
【0028】
本発明は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする患者の病状を治療するために、および患者におけるそのような病状を治療するための薬剤を製造する際に、機能的なM135Rを発現しない粘液腫ウイルスの有効量を、任意には、有効量のラパマイシンと併用して使用することをさらに提供する。
【0029】
さらなる態様において、本発明は、機能的なM135Rを発現しない粘液腫ウイルスを提供する。
【0030】
別の態様において、本発明は、機能的なM135Rを発現しない粘液腫ウイルスを含む医薬組成物を提供する。この医薬組成物は、先天的な抗ウイルス応答を欠損した細胞を阻害するか、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする患者の病状を治療するのに役立ちうる。この医薬組成物は、ラパマイシンをさらに含むことができる。
【0031】
別の態様において、本発明は、機能的なM135Rを発現しない粘液腫ウイルス、および先天的な抗ウイルス応答を欠損した細胞を阻害するため、または、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための説明書を含むキットを提供する。このキットは、さらにラパマイシンを含むことが可能である。この病状は、癌および慢性ウイルス感染症を含む。
【0032】
本発明は、先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、細胞集団を、機能的なM135Rを発現しない粘液腫ウイルスに、任意にはラパマイシンとの混合物に曝露すること、ウイルスを、先天的な抗ウイルス応答を欠損した細胞に感染させること、および細胞集団のどの細胞が粘液腫ウイルスに感染したかを決定することを含む方法を提供する。
【0033】
以下の発明の具体的態様の説明を、添付の図面とともに検討すれば、本発明のその他の態様および特徴が当業者に明らかとなろう。しかし、当然ながら、本発明の主旨と範囲に含まれる多様な改変および修正が、詳細な説明から当業者に明らかとなるのであるから、詳細な説明および具体的実施例は、本発明の好適な実施態様を示しつつも、例示のためだけに提示されていると理解されるべきである。
本発明はまた、以下の項目を提供する。
(項目1)
先天的な抗ウイルス応答を欠損した細胞を阻害する方法であって、該細胞に有効量の粘液腫ウイルスとラパマイシンの配合物を投与することを含む方法。
(項目2)
上記細胞がインターフェロンに非応答性である、項目1記載の方法。
(項目3)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目2記載の方法。
(項目4)
上記細胞がヒト癌細胞である、項目3記載の方法。
(項目5)
上記粘液腫ウイルスが野生型ウイルスである、項目4記載の方法。
(項目6)
上記粘液腫ウイルスが遺伝子改変されている、項目4記載の方法。
(項目7)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目6記載の方法。
(項目8)
上記細胞が肺癌細胞、黒色腫細胞、卵巣癌細胞、前立腺癌細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目4記載の方法。
(項目9)
上記細胞が慢性的にウイルスに感染したヒト細胞である、項目1記載の方法。
(項目10)
先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に有効量の粘液腫ウイルスとラパマイシンの配合物を投与することを含む方法。
(項目11)
上記病状が癌である、項目10記載の方法。
(項目12)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目11記載の方法。
(項目13)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目11記載の方法。
(項目14)
上記患者がヒトである、項目13記載の方法。
(項目15)
上記粘液腫ウイルスが野生型ウイルスである、項目14記載の方法。
(項目16)
上記粘液腫ウイルスが遺伝子改変されている、項目14記載の方法。
(項目17)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目16記載の方法。
(項目18)
上記ウイルスと上記ラパマイシンは注射によって上記癌の部位に投与される、項目14記載の方法。
(項目19)
上記ウイルスと上記ラパマイシンは全身に投与される、項目14記載の方法。
(項目20)
上記病状が慢性ウイルス感染症である、項目10記載の方法。
(項目21)
先天的な抗ウイルス応答を欠損した細胞を阻害するための有効量の粘液腫ウイルスとラパマイシンの配合物の使用。
(項目22)
先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤の製造における、有効量の粘液腫ウイルスとラパマイシンの配合物の使用。
(項目23)
上記細胞がインターフェロン非応答性である、項目21または22記載の使用。
(項目24)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目23記載の使用。
(項目25)
上記細胞が慢性的にウイルスに感染している、項目24記載の使用。
(項目26)
上記細胞がヒト癌細胞である、項目24記載の使用。
(項目27)
上記細胞が肺癌細胞、黒色腫細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目26記載の使用。
(項目28)
上記粘液腫ウイルスが野生型ウイルスである、項目20から27のいずれか一項記載の使用。
(項目29)
上記粘液腫ウイルスが遺伝子改変されている、項目20から27のいずれか一項記載の使用。
(項目30)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目29記載の使用。
(項目31)
患者における病状を治療するための有効量の粘液腫ウイルスとラパマイシンの配合物の使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする、使用。
(項目32)
患者における病状を治療するための薬剤の製造における有効量の粘液腫ウイルスとラパマイシンの配合物の使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が患者に存在することを特徴とする、使用。
(項目33)
上記病状が癌である、項目31または32記載の使用。
(項目34)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目33記載の使用。
(項目35)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目33記載の使用。
(項目36)
上記病状が慢性ウイルス感染症である、項目31または32記載の使用。
(項目37)
上記患者がヒトである、項目31から36のいずれか一項記載の使用。
(項目38)
上記粘液腫ウイルスが野生型ウイルスである、項目31から37のいずれか一項記載の使用。
(項目39)
上記粘液腫ウイルスが遺伝子改変されている、項目31から37のいずれか一項記載の使用。
(項目40)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目39記載の使用。
(項目41)
粘液腫ウイルスとラパマイシンを含む医薬組成物。
(項目42)
さらに付加的治療薬を含む、項目41記載の医薬組成物。
(項目43)
上記付加的治療薬が化学療法薬である、項目42記載の医薬組成物。
(項目44)
先天的な抗ウイルス応答を欠損した細胞を阻害するため、または先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための、粘液腫ウイルス、ラパマイシンおよび使用説明書を含むキット。
(項目45)
先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、粘液腫ウイルスとラパマイシンの配合物に細胞の集団を曝露する工程、先天的な抗ウイルス応答を欠損した細胞に該ウイルスを感染させる工程、および該細胞集団のどの細胞が粘液腫ウイルスに感染したかを判定する工程を含む方法。
(項目46)
上記細胞集団が患者の体内にあり、上記曝露工程が、上記粘液腫ウイルスとラパマイシンの配合物を該患者に投与することを含み、該粘液腫ウイルスが、検出可能なマーカーを発現するよう遺伝子改変されており、かつ、上記判定工程が、該患者の中で該検出可能なマーカーを発現する細胞を検出することを含む、項目45記載の方法。
(項目47)
上記細胞集団が培養されている、項目45記載の方法。
(項目48)
機能的なM135Rを発現しない有効量の粘液腫ウイルスを、随意で有効量のラパマイシンと組み合わせて細胞に投与することを含む、先天的な抗ウイルス応答を欠損した細胞を阻害する方法。
(項目49)
上記細胞がインターフェロンに非応答性である、項目48記載の方法。
(項目50)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目49記載の方法。
(項目51)
上記細胞がヒト癌細胞である、項目50記載の方法。
(項目52)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目51記載の方法。
(項目53)
上記細胞が肺癌細胞、黒色腫細胞、卵巣癌細胞、前立腺癌細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目51記載の方法。
(項目54)
上記細胞が慢性的にウイルスに感染しているヒト細胞である、項目48記載の方法。
(項目55)
先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する方法であって、それを必要とする患者に機能的なM135Rを発現しない有効量の粘液腫ウイルスを投与することを含む方法。
(項目56)
さらに、有効量のラパマイシンを上記患者に投与することを含む、項目55記載の方法。
(項目57)
上記病状が癌である、項目55または56記載の方法。
(項目58)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目57記載の方法。
(項目59)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目57記載の方法。
(項目60)
上記患者がヒトである、項目59記載の方法。
(項目61)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目59記載の方法。
(項目62)
上記癌の部位に注射することによって上記投与が行われる、項目55または56記載の方法。
(項目63)
上記投与が全身性である、項目55または56記載の方法。
(項目64)
上記病状が慢性ウイルス感染症である、項目55記載の方法。
(項目65)
機能的なM135Rを発現しない粘液腫ウイルスの有効量の使用。
(項目66)
有効量のラパマイシンをさらに配合する、項目65記載の使用。
(項目67)
先天的な抗ウイルス応答を欠損した細胞を阻害するための薬剤を製造するための、機能的なM135Rを発現しない粘液腫ウイルスの有効量の使用。
(項目68)
薬剤が、有効量のラパマイシンと配合して投与されるように処方されている、項目67記載の使用。
(項目69)
上記細胞がインターフェロンに非応答性である、項目65から68のいずれか一項記載の使用。
(項目70)
上記細胞が異常なインターフェロンシグナル伝達を示す、項目69記載の使用。
(項目71)
上記細胞が慢性的にウイルスに感染している、項目70記載の使用。
(項目72)
上記細胞がヒト癌細胞である、項目70記載の使用。
(項目73)
上記細胞が肺癌細胞、黒色腫細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、項目72記載の使用。
(項目74)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目65から73のいずれか一項記載の使用。
(項目75)
患者における病状を治療するための、機能的なM135Rを発現しない有効量の粘液腫ウイルスの使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が患者に存在することを特徴とする、使用。
(項目76)
有効量のラパマイシンをさらに含む、項目75記載の使用。
(項目77)
上記患者における病状を治療するための薬剤の製造のための、機能的なM135Rを発現しない有効量の粘液腫ウイルスの使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする、使用。
(項目78)
上記薬剤が、有効量のラパマイシンと配合して投与されるように処方されている、項目77記載の使用。
(項目79)
上記病状が癌である、項目75から78のいずれか一項記載の使用。
(項目80)
上記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、項目79記載の使用。
(項目81)
上記癌が肺癌、黒色腫、卵巣癌、前立腺癌、腎臓癌、神経膠腫、または星状細胞腫である、項目79記載の使用。
(項目82)
上記病状が慢性ウイルス感染症である、項目75から78のいずれか一項記載の使用。
(項目83)
上記患者がヒトである、項目75から82のいずれか一項記載の使用。
(項目84)
上記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、項目75から83のいずれか一項記載の使用。
(項目85)
機能的なM135Rを発現しない粘液腫ウイルス。
(項目86)
機能的なM135Rを発現しない粘液腫ウイルスを含む医薬組成物。
(項目87)
さらにラパマイシンを含む、項目86記載の医薬組成物。
(項目88)
さらに付加的治療薬を含む、項目86記載の医薬組成物。
(項目89)
上記付加的治療薬が化学療法薬である、項目86記載の医薬組成物。
(項目90)
先天的な抗ウイルス応答を欠損した細胞を阻害するため、または先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための、機能的なM135Rを発現しない粘液腫ウイルスおよび使用説明書を含むキット。
(項目91)
さらにラパマイシンを含む、項目90記載のキット。
(項目92)
先天的な抗ウイルス応答を欠損した細胞を検出する方法であって、機能的なM135Rを発現しない粘液腫ウイルスに細胞の集団を曝露する工程、先天的な抗ウイルス応答を欠損した細胞に該ウイルスを感染させる工程、および該細胞集団のどの細胞が該粘液腫ウイルスに感染したかを判定する工程を含む方法。
(項目93)
上記細胞集団が患者の体内にあり、上記曝露工程が、上記機能的なM135Rを発現しない粘液腫ウイルスを該患者に投与することを含み、該機能的なM135Rを発現しない粘液腫ウイルスが、検出可能なマーカーを発現するよう遺伝子改変されており、かつ、上記判定工程が、該患者の中で該検出可能なマーカーを発現する細胞を検出することを含む、項目92記載の方法。
(項目94)
ラパマイシンと組み合わせて上記曝露が行われる、項目92または93記載の方法。
(項目95)
上記細胞集団が培養されている、項目92記載の方法。
【図面の簡単な説明】
【0034】
図面は、本発明の実施態様が具体的に説明されているが、あくまで例示のためのものである。
【図1】細胞にウイルスが感染すると誘導される、インターフェロンによって誘導抗ウイルスシグナル伝達スキームの概略図である。
【図2】粘液腫ウイルスに曝露された後の非許容性の野生型マウス胎仔線維芽細胞(「MEF」)の位相差顕微鏡写真であり、インターフェロンα/βを中和抗体で阻害した後にMEF細胞が許容性になることを示している。
【図3】粘液腫ウイルス感染後のSTAT1およびSTAT2のリン酸化(活性化)状態を示すウエスタンブロットであり、MEF細胞への非許容感染(nonpermissive infections)は、STAT1およびSTAT2のリン酸化と関連することを示している。
【図4】粘液腫ウイルス感染後のSTAT3、STAT4、STAT5およびST6のリン酸化(活性化)状態を示すウエスタンブロットであり、MEF細胞への非許容感染は、これらの分子種のいずれも活性化しないことを示している
【図5】粘液腫ウイルス感染後のINFα/β R−/−型MEFおよびSTAT1−/−型MEFの位相差顕微鏡写真であり、IFN/STAT/JAKシグナル伝達の不活性化は、細胞を粘液腫ウイルスに対して許容性にすることを示している。
【図6】粘液腫ウイルス感染後の非許容性野生型MEFにおけるPKRのリン酸化状態を示すウエスタンブロットであり、PRKは粘液腫ウイルス感染によって活性化されないことを示している。
【図7】模擬感染したか、粘液腫ウイルスに前感染した野生型MEFにおけるPKRのリン酸化状態を示すウエスタンブロットであり、粘液腫ウイルスが、MEF細胞におけるPKR活性化を阻止することを示している。
【図8】粘液腫ウイルス感染後の野生型MEFにおけるPEKRのリン酸化状態を示すウエスタンブロットであり、粘液腫ウイルスが、MEF細胞におけるPEKRの活性化を阻止することを示している。
【図9】粘液腫ウイルスに曝露した後のPKR−/−、RNaseL−/−、およびMx1−/−という三重のノックアウトの位相差顕微鏡写真であり、MEF細胞における抗ウイルス状態は別の経路によってもたらされていることを示している。
【図10】粘液腫ウイルスに曝露した後のPKR−/−、RNaseL−/−、およびMx1−/−の三重ノックアウトの位相差顕微鏡写真である。
【図11】INFα/βに対する中和抗体で処理した後、および粘液腫ウイルスに曝露した後のPKR−/−、RNase L−/−、およびMx1−/−という三重のノックアウトの位相差顕微鏡写真である。
【図12】INFα/βに対する中和抗体で処理した後、および粘液腫ウイルスに曝露した後の非許容性MEFにおけるeIF2αおよびPKRのリン酸化レベルを示すウエスタンブロットであり、非応答性細胞におけるeIF2αのリン酸化は、PKR非依存的経路によって触媒されることを示している。
【図13】粘液腫ウイルス感染後のPKR−/−、RNaseL−/−、およびMx1−/−三重のノックアウトにおけるSTAT1のリン酸化状態を示すウエスタンブロットであり、正常なIFN誘導シグナル応答を示している。
【図14】感染12時間後の非許容性PKR−/−+RNaseL−/−+Mx1−/−細胞におけるチロシンリン酸化型STAT1の細胞内の局在を示す位相差顕微鏡写真であり、正常なIFN/STATシグナル応答で予測されたように、活性化されたSTAT1は核に局在することを示している。
【図15】模擬感染させたか、GFPを発現する死菌または生菌の粘液腫ウイルスに感染させた、頭蓋骨内に神経膠腫を有するヌードマウスの脳の蛍光画像であり、粘液腫ウイルスが神経膠腫細胞を標的とすることを示している。
【図16】GFPを発現する粘液腫ウイルスに感染したマウスの薄層切片の蛍光画像および写真であり、粘液腫ウイルスが腫瘍細胞だけで複製することを示している。
【図17】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したHT29ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における非許容感染の例を示すものである。
【図18】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したHOP92ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における許容感染の例を示すものである。
【図19】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したOVCAR4ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における許容感染の例を示すものである。
【図20】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したSK−MEL3ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における許容感染の例を示すものである。
【図21】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したSK−MEL28ヒト腫瘍細胞の位相差顕微鏡写真であり、ヒト細胞における半許容感染の例を示すものである。
【図22】粘液腫ウイルスに感染した後にX−Galまたはクリスタルバイオレットのいずれかで染色したBGMK細胞の位相差顕微鏡写真であり、典型的な許容性対照感染の例を示すものである。
【図23】LacZタンパク質を発現する粘液腫ウイルスの高濃度液を感染させた陽性対照BGMK細胞、およびヒト腫瘍細胞株U87、A172、およびU373を、X−Galで染色したものの位相差顕微鏡写真であり、これらのヒト神経膠腫はすべて、粘液腫ウイルスの複製に対して許容性であったことを示している。
【図24】高濃度の粘液腫ウイルスに感染させたBGMK、U87、A172、およびU373の各細胞の感染72時間後の生存率を示す図であり、粘液腫ウイルスがこれらの細胞をすべて死滅させることができることを示している。
【図25】MV GFPに感染させたSF04 1585星状細胞腫細胞の位相差顕微鏡写真および蛍光画像であり、初代ヒト神経膠腫細胞で感染が起きたことを示している。
【図26】LacZタンパク質を発現する粘液腫ウイルスに感染させたU373神経膠腫細胞をX−Galで染色したものの位相差顕微鏡写真であり、これらのヒト腫瘍細胞で感染が起きたことを示している。
【図27】MV GFPに感染させたSF04 1585細胞の感染48時間後の生存率を示す図であり、これらの感染ヒト腫瘍細胞が死滅したことを示している。
【図28】GFPを発現する粘液腫ウイルスに感染させたDaoy髄芽細胞およびD384髄芽細胞の蛍光顕微鏡写真であり、これらのヒト腫瘍細胞で感染が起きたことを示している。
【図29−1】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−2】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−3】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−4】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図29−5】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株におけるウイルス産生速度をグラフ表示したものである:BGMK(初代対照用細胞株);RK−13およびRL5(ウサギ対照細胞株);4TlおよびB16F10(マウス癌細胞株);HOS、PC3、786−0、HCTl16、ACHN、MCF−7、M14ならびにCOLO205(ヒト癌細胞)、野生型ウイルスをvMyxLac、M−T5ノックアウトウイルスをvMyxT5KOとして表示する。
【図30】vMyxLacまたはvMyxLacT5−のいずれかに感染させたウイルス感染細胞株の写真である。
【図31−1】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株(BGMK;A9;MCF−7;MDA−MB−435;M14;およびCOLO205)におけるウイルス産生速度をグラフ表示したものである。
【図31−2】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株(BGMK;A9;MCF−7;MDA−MB−435;M14;およびCOLO205)におけるウイルス産生速度をグラフ表示したものである。
【図31−3】ラパマイシンで事前処理した場合としない場合のさまざまな細胞株(BGMK;A9;MCF−7;MDA−MB−435;M14;およびCOLO205)におけるウイルス産生速度をグラフ表示したものである。
【図32】(A)粘液腫ウイルスタンパク質M135Rおよびワクシニアウイルスタンパク質B18Rのアラインメントの略図である。(B)M135Rと、B18Rの最初の179アミノ酸のアミノ酸配列アラインメントである。
【図33】(A)粘液腫ウイルスのローザンヌ(Lausanne)株(vMyxLau)に感染させたBGMK細胞で発現したM135Rのウエスタンブロット。(B)vMyxLauに感染させ、araC、ツニカマイシン、またはたモネンシンで処理したBGMK細胞で発現したM135Rのウエスタンブロット。
【図34】(A)模擬感染させたか、粘液腫ウイルスに感染させ、M135Rについて染色したBGMK細胞の蛍光画像。(B)野生型粘液腫ウイルス(vMyxgfp)またはM135Rノックアウト株(vMyx135KO)に感染させた細胞の免疫沈殿物または細胞可溶化物に対する、抗M135R抗体を用いたウエスタンブロット。
【図35】(A)vMyx135KOを作出するためのクローニング法の概略図。(B)PCR挿入配列産物のアガロースゲル。(C)野生型粘液腫ウイルスおよびM135Rノックアウト粘液腫ウイルスに感染させた細胞のウエスタンブロット。
【図36】vMyxgfpまたはvMyx135KOに感染させたBGMK細胞におけるウイルス増殖巣の増殖曲線である。
【図37】vMyxgfpまたはvMyx135KOに感染させたウサギ胚線維芽細胞の光学顕微鏡写真と蛍光顕微鏡写真である。
【図38】vMyxgfpまたはvMyx135KOに感染させたウサギHIG82線維芽細胞の光学顕微鏡写真と蛍光顕微鏡写真である。
【図39】vMyxgfpまたはvMyx135KOに感染させたヒト初代線維芽細胞の光学顕微鏡写真と蛍光顕微鏡写真である。
【図40】vMyxLauまたはvMyx135KOに感染させたウサギの体温のグラフである。
【図41】模擬感染させたか、またはvMyxgfpもしくはvMyx135KOに感染させ、125Iで標識したウサギインターフェロンα/βで処理した細胞の125I放射のグラフである。
【図42】感染させる24時間前にウサギインターフェロンα/βで処理するか、無処理のままで、RK13細胞またはBGMK細胞にvMyxgfpもしくはvMyx135KOを感染させることによって形成された増殖巣のグラフである。
【図43】20nMラパマイシン(R)、または賦形剤対照(D)で予め処理した786−0ヒト癌細胞の細胞可溶化物を用い、図に示したタンパク質に対する抗体を用いてプローブ検索したウエスタンブロットの写真である。
【発明を実施するための形態】
【0035】
(詳細な説明)
これまでに、本発明者らは、通常はウサギに感染するウイルスである野生型の粘液腫ウイルスが、その全体が参照されて本明細書に組み込まれるPCT/CA2004/000341に記載されているように、例えば、インターフェロンに非応答性の細胞など、先天的な抗ウイルス応答を欠損した、ヒト細胞などの細胞に選択的に感染して死滅させうることを発見した。粘液腫ウイルスは、正常なヒト細胞の中では効率的に複製しない。多くの病気または症状が、インターフェロンに対して応答性でない細胞、例えば、癌など、先天的な抗ウイルス応答を欠損している細胞が存在することを特徴としているため、正常な健常細胞に対する毒性が低い粘液腫ウイルスを使用して、癌を含むそのような病気および症状を治療することができる。また、慢性的に感染した細胞は、先天的な抗ウイルス応答を欠損しているため、粘液腫ウイルスを使用して、そのような細胞を治療することができる。例えば、多くのウイルスが、細胞の抗ウイルス性インターフェロン応答を阻害するように機能する遺伝子産物をコードするが、粘液腫ウイルスはそのような細胞に選択的に感染することができる。
【0036】
粘液腫ウイルス(「MV」)は、ウサギの粘液腫症の病原因子である。MVは、DNAウイルスの中で最大のポックスウイルス科のレポリポックスウイルス属に属している。MVは、その自然宿主であるアメリカ大陸のワタオウサギ(Sylvilagus rabbit)において良性の病気を引き起こす。しかし、それは、全身に見られるが、特に粘膜部周辺に見られる病変部を特徴とする、欧州大陸のウサギにおいては致命的な病気を引き起こす、病原性かつ宿主特異的なポックスウイルスである(Cameron C, Hota−Mitchell S, Chen L, Barrett J, Cao JX, Macaulay C, Willer D, Evans D, McFadden G. Virology 1999, 264(2): 298−318; Kerr P & McFadden G. Viral Immunology 2002, 15(2): 229−246)。
【0037】
MVは、感染細胞の細胞質の中で複製する163kbの二本鎖DNAゲノムを持つ大型のウイルスである(B. N. Fields, D. M. Knipe, P. M. Howley, Eds., Virology Lippincott Raven Press, New York, 2nd ed., 1996)。MVは、宿主の免疫反応および炎症反応の下方制御ならびにウイルス感染細胞のアポトーシスに関与するとされてきた、多様な細胞結合型タンパク質および細胞分泌型タンパク質をコードすることが知られている。MVは全てのヒト体細胞に取り込まれることができる。しかし、細胞が先天的な抗ウイルス応答性を持っている場合、正常なウサギ体細胞以外には、ウイルスは細胞に増殖できる形で感染することができないが、このことは、ウイルスが複製して
細胞死を引き起こすことができないことを意味している。
【0038】
インターフェロン(「INF」)は、多様な刺激に反応して分泌されるサイトカインのファミリーである。インターフェロンは細胞表面受容体に結合して、抗ウイルス応答、ならびに増殖阻害シグナルおよび/またはアポトーシスシグナルの誘導など、細胞応答を導くシグナル伝達カスケードを活性化させる。インターフェロンはI型またはII型に分類される。I型インターフェロンはIFN−α、IFN−β、IFN−τ、およびIFN−ωなどであり、これらはすべて単量体であるが、唯一のII型IFNはIFN−γであり、二量体である。IFN−αの12種の異なったサブタイプは、14の遺伝子によって産生されるが、他のIFNはすべて一遺伝子性のものである(Arduini et al., 1999)。IFNは、癌遺伝子発現を調節することによって、直接的な抗腫瘍活性を発揮する。増殖促進性癌遺伝子が過剰発現されるか、または腫瘍抑制癌遺伝子の発現が消失すると、悪性の形質転換が生じることがある。癌の発生に関係する癌遺伝子には、p53、Rb、PC、NFl、WTl、DCCがある。
【0039】
粘液腫ウイルス、また、レオウイルスおよびVSVなど、その他の腫瘍退縮性ウイルスは、細胞の中で複製できるようになるためには、正常な健常細胞に存在する抗ウイルス防御を迂回する必要がある。MVおよびその他の腫瘍退縮性ウイルスはインターフェロン産生を誘導し、かつ、IFN経路の抗ウイルス効果に対して、通常は感受性である。IFNの抗ウイルス応答によって生じた関連タンパク質であって、主にウイルス増殖に影響を及ぼすものはPKR、OASシンテターゼおよびリボヌクレアーゼLヌクレアーゼなどである。PKRはeIF2αを活性化させ、その結果、翻訳の阻害とアポトーシスの誘導をもたらす。図1にIFN応答経路の概略を示す。正常な細胞においては、MVは、直接PKRおよびeIF2αによる影響を受ける。
【0040】
抗ウイルス応答経路は、しばしば癌細胞の中で破壊されている。例えば、IFNに対する応答の低下または欠損は、形質転換または腫瘍発生の過程でしばしば生じる遺伝子欠損である。腫瘍細胞株の80%以上がインターフェロンに応答しないか、応答低下を示す(Stojdl et al., Cancer Cell (2003) 4: 263−275 and references cited therein; Wong et al. J Biol Chem. (1997) 272(45):28779−85; Sun et al. Blood. (1998) 91(2):570−6; Matin et al. Cancer Res. (2001) 61(5):2261−6; Balachandran et al Cancer Cell (2004) 5(l):51−65)。PCT/CA2004/000341で既に開示されているように、MVはヒト腫瘍細胞などの癌細胞に感染して死滅させることができ、また、これらの細胞は先天的な抗ウイルス応答を欠損しているために、MVはそれらに感染することができると、特定の理論に制約されることなく考えられている。
【0041】
初期先天性免疫応答を阻害すること、およびThl応答の発生を遅くすることが腫瘍退縮療法の有効性に重要であることが、証拠から示唆されている。粘液腫ウイルスは毒性ウイルスであるが、宿主特異的で宿主域が非常に狭いため、ヒトまたはマウスには感染しない。特定の理論に拘泥することなく、粘液腫ウイルスは非ヒトウイルスであるために、ヒトの既存の免疫認識と出会うはずがないと考えられる。したがって、その腫瘍退縮性ウイルスとしての可能性は、より障害をもたらしにくいため、天然のヒトウイルスよりも粘液腫ウイルスの方が、許容性腫瘍細胞により強く感染して、癌に対する有効な腫瘍退縮治療を行うことができるはずである。
【0042】
粘液腫ウイルスの宿主域遺伝子M−T5は、粘液腫ウイルスが多くのヒト腫瘍細胞株に感染する際に決定的な役割を果たしているように見える(Sypula et al, (2004) Gene Ther. Mol. Biol. 8:103)。このMT−5遺伝子は、ウサギリンパ球において粘液腫が複製するために必要とされるアンキリン反復タンパク質をコードし、MT−5遺伝子を欠失した粘液腫ウイルスは、感受性のウサギにおいても粘液腫症を発症させることができない(Mossman et al, (1996) J. Virol. 70: 4394)。入手可能な証拠から、感染ヒト細胞の中での細胞内シグナル伝達における違いが、粘液腫ウイルスの感染および増殖複製に対して許容性のあるヒト腫瘍細胞を区別するのに決定的であることが示唆されている(Johnston et al, (2003) J. Virol. 11: 5877)。
【0043】
さらに、粘液腫ウイルスは、インターフェロンα/β受容体(「IFNα/β−R」)のアミノ末端部分に相同性を示すM135Rタンパク質を持っている。M135Rは、宿主の抗ウイルス応答を開始させないために、宿主のINFα/β−Rを模倣することが示唆されている(Barrett et al., Seminars in Immunology (2001)13:73−84)。この予測は、ワクシニアウイルスB18R由来のウイルスINFα/β−Rとの配列相同性に基づくものであり、ワクシニアウイルス(「VV」)がそのような免疫回避戦略を採ることが実証されている。しかし、M135Rは、VVB18R、およびその他配列決定されたポックスウイルス由来のINFα/β−R相同体の大きさの半分しかないため、すべての場合で、相同体のアミノ末端側の半分だけにしかアラインメントされない。
【0044】
本発明者らは、免疫蛍光法の結果はM135Rが細胞表面に局在していることを示唆しているにもかかわらず、M135RがINFα/βと相互作用できることを実証する試みは否定的であったことを発見した。このような結果にも関わらず、本発明者らは、M135Rの欠失は、粘液腫ウイルスが宿主動物において病気を引き起こす能力を大幅に減弱させるが、一方、このような欠失をもつ粘液腫ウイルスは、野生型MVとインビトロで比較すると、細胞に感染して死滅させるのに同等の効果をもつことを発見した。このように、一つの態様において、本発明は、治療を受けている患者に尋常でない封じ込めストラテジーを行う必要がなく、粘液腫ウイルスを腫瘍退縮性ウイルス治療のためのより安全な代替法として提供できるため、機能的なM135Rを発現しない粘液腫ウイルスは、腫瘍退縮性の研究など、先天的な抗ウイルス応答を欠損した細胞を処理する上で有用であるという発見に関する。
【0045】
別の態様において、本発明は、粘液腫ウイルス感染に許容性のあるヒト腫瘍細胞において、抗癌剤であるラパマイシンが粘液腫ウイルスの感染力のレベルを高める働きをするという発見、および、ラパマイシンが存在しなければ、粘液腫ウイルスのある株の複製を制限するヒト腫瘍細胞において、ラパマイシンがあれば粘液腫ウイルスの一定の株の複製が可能となるという発見に関する。粘液腫ウイルス感染に許容性のある細胞とは、このウイルスが入り込むことができ、かつその中でウイルスが増殖的に繁殖できる細胞である。許容細胞は、タンパク質PTEN、PDK、AKT、GSK、Raf、mTORまたはP70S6Kを含む1つ以上の経路に欠損また変異があってもよい。制限細胞は、一定の条件下でのみ粘液腫ウイルスに対して許容的であるが、その他の条件下では増殖性感染を許容しない。例えば、制限細胞は、このウイルスの野生株に許容性があるが、変異型粘液腫株、例えば、MT−5遺伝子をノックアウトされた株は増殖的に繁殖させない。別の例において、粘液腫ウイルスに対して制限的な細胞は、粘液腫ウイルス単独での増殖的な感染を許容しないかもしれないが、ラパマイシンで処理すると、同じ粘液腫ウイルスが細胞に増殖的に感染することができるようになる。非増殖性の細胞株は、粘液腫ウイルス感染に対し非許容性であって、すなわち、ウイルスは細胞に入り込むことはできるかもしれないが、細胞に増殖的に感染はしないことを意味している。
【0046】
このように、ラパマイシンは、粘液腫ウイルスと併用すると、先天的な抗ウイルス応答を欠損した細胞に対する粘液腫ウイルスの感染力を高める。本発明は、先天的な抗ウイルス応答を欠損した細胞を処理するために、ラパマイシンを粘液腫ウイルスと併用することに関する。
【0047】
ラパマイシンは、土壌細菌であるストレプトマイセス・ヒグロスコピカス(Streptomyces hygroscopicus)から精製された活性抗真菌化合物であることが示されている大環状ラクトンである。本明細書において、ラパマイシンは、FKBP12と複合体を形成してmTORを阻害することができるラパマイシン(シロリムスとも称される)およびそのアナログまたは誘導体を意味し、アナログであるCCI−779(細胞周期阻害剤−779またはラパマイシン−42,2,2−ビス(ヒドロキシメチル)−プロピオン酸とも称される)およびRAD001(エベロリムスまたは40−Ο−(2−ヒドロキシエチル)−ラパマイシンとも称される)などを含む。ラパマイシン、CCI−779およびRAD001は市販されており、ラパマイシンは、Wyeth−Ayerstから商標Rapamuneという名称で購入可能である。ラパマイシンという用語は、さらに、ラパマイシンの医薬上許容される塩およびエステル、その水和物、溶媒和物、多形体、アナログまたは誘導体、ならびに、使用される過程、例えば、患者に投与されると、代謝または転換されてラパマイシンまたはそのアナログもしくは誘導体となるプロドラッグまたは前駆体も含む。
【0048】
細胞内シグナル伝達阻害剤としてのラパマイシンは極めて特異的であり、細胞に入り込んで、FKBP12として知られる細胞タンパク質に結合する。次に、ラパマイシン/FKBP12複合体は特異的な細胞内標的mTOR(哺乳類のラパマイシン標的)に結合する。多くの癌が、P13Kなどのシグナル伝達分子の過活性、または腫瘍抑制遺伝子PTENの欠如から発生することが示されている。これらの分子はどちらもmTORの上流に存在する。mTORは、細胞の増殖、成長、分化、遊走および生存の中心的調節因子であることが示されており、そのため、癌細胞の非制御成長を阻止する上で理想的な標的である。ラパマイシンに感受性の癌細胞株は、通常、mTORを介した経路の活性化の結果生じたものである。
【0049】
ラパマイシンは、シクロスポリン治療の代替治療または補完治療として、主に臓器移植患者に使用されている。臓器移植患者において、ラパマイシン治療は、一般にシクロポリンAまたはFK506よりも副作用が少ない。加えて、ラパマイシン治療を受けた患者のほうが一般に、癌の発生が少なく、かつCMV(ヘルペスウイルスであるサイトメガロウイルス)の発生率が低いことが、遡及研究によって示されている。したがって、特に、CMV複製がラパマイシンによって減少するはずであると仮定する研究を考慮すると、ラパマイシン治療によって粘液腫ウイルスの癌細胞への感染が促進されるのは意外なことである(Ponticelliによる“The pleiotropic effects of mTOR inhibitors” in J Nephrology 2004; 17: 762のレビュー)。特定の理論に制限されなくても、粘液腫ウイルスが、これらの細胞の腫瘍性表現型に関係しているかもしれないmTOR経路を介する異常なシグナル伝達を利用している可能性がある。そうであれば、mTOR阻害剤によってこの経路を操作することは、このウイルスにとって選択的な利益となるかもしれない。
【0050】
このようにして、先天的な抗ウイルス応答を欠損した細胞を阻害するための方法であって、このような細胞に有効量の粘液腫ウイルスを投与することを含む方法が提供される。さらなる実施態様において、このウイルスを、有効量のラパマイシンと併用して投与する。
【0051】
この粘液腫ウイルスは、ポックスウイルスのレポリポックスウイルス属に属する、複製可能なウイルスであればよい。この粘液腫ウイルスは粘液腫ウイルスの野生株でよく、または、粘液腫のMT−5ノックアウト株のように、遺伝子改変された粘液腫ウイルス株でもよい。この粘液腫ウイルスは、下記のように、機能的M135Rタンパク質を発現しない株など、ウサギにおいて弱毒化された効果を示し、その結果、病気のリスクが低くなっている株であってもよい。
【0052】
特定の実施態様において、粘液腫ウイルスは、機能的M135Rを発現しない粘液腫ウイルスである。
【0053】
機能的M135Rを発現しない粘液腫ウイルスは、遺伝子産物、安定型遺伝子産物、または機能的遺伝子産物が発現されないように欠失、置換または中断されたM135Rをコードするオープンリーディングフレームの一部または全部を持つ粘液腫ウイルスを含む。このようなウイルスは、M135Rをコードする遺伝子からタンパク質が発現されることがないように欠失、置換または中断された、M135Rの遺伝子調節領域の一部または全部を有する粘液腫ウイルスも含む。機能的M135Rタンパク質とは、転写され、翻訳され、折り畳まれ、翻訳後に修飾され、細胞の内部に局在化されるM135Rであり、粘液腫ウイルスが感染した宿主の中で粘液腫症を引き起こすことを可能にするものである。M135Rタンパク質が、全く、または適正に、または十分に転写されず、翻訳されず、折り畳まれず、翻訳後に修飾されず、細胞内に局在化されないために、感染した宿主が粘液腫症を発生しなければ、その時には、機能的M135Rが細胞内で発現されていない。
【0054】
さらなる実施態様において、細胞はインターフェロンに対して非応答性である。
【0055】
特定の実施態様において、細胞は哺乳動物の癌細胞である。一つの実施態様において、細胞は、ヒト固形腫瘍などのヒト癌細胞である。
【0056】
別の実施態様において、細胞はウイルスに慢性的に感染している。
【0057】
ラパマイシンと粘液腫ウイルスの投与するための「併用」は、同一の投薬形態で一緒に処方するか、または別々の投与形態で処方することができ、別々の投与形態の場合には、同じ様式で投与するため、または異なった投与様式で投与するために同じ形であっても、異なった形であってもよい。さらに、同じ投薬形態で一緒に投与しない場合に、ラパマイシンと粘液腫ウイルスを併用して投与するとは、ラパマイシンおよび粘液腫ウイルスを治療中の哺乳動物に同時に投与することを意味し、同時に、または任意の順序で連続的に、または異なった時点で投与することができることを意味する。このように、ラパマイシンと粘液腫ウイルスを別々に投与することも可能であるが、望ましい治療効果をもたらすよう時間的に十分近接させて投与することができる。
【0058】
本明細書において「有効量」という用語は、所望の結果を得るのに必要な投薬形態または期間において有効な量を意味する。
【0059】
本明細書において「先天的な抗ウイルス応答を欠損した細胞」という用語は、ウイルスに曝露されるか、ウイルスの侵入を受けた場合に、ウイルスの複製、インターフェロンの産生、インターフェロン応答経路の誘導、およびインターフェロンが介在しているか否かに関わらないアポトーシスなどの抗ウイルス防御機構を誘導せず、そのため、MVが、単独で、またはラパマイシン療法と併用すると感染することができる細胞を意味する。この用語は、ウイルスに曝露または感染したときに、正常な細胞、例えば、非感染細胞または非癌細胞と比較すると、先天的な抗ウイルス応答が低下または欠損している細胞を含む。これは、インターフェロンに対して非応答性である細胞、およびアポトーシス応答またはアポトーシス経路誘導が低下もしくは欠損している細胞を含む。この欠損は、感染、遺伝
子欠損、または環境ストレスなど、さまざまな原因によって生じうる。しかしながら、この欠損が既存の感染によって生じている場合、MVによる重感染は排除され、当業者はそのような例を容易に同定することができる。当業者は、過度の実験を行うことなく、いずれか所定の細胞型が先天的な抗ウイルス応答を欠損しているために、単独の、またはラパマイシン治療と併用した粘液腫ウイルスによって感染されうるか否かを容易に決定することができる。例えば、VSVを普通に用いて、細胞の抗ウイルス応答を測定することができる。
【0060】
所定の細胞型、例えば、所定の癌細胞型が先天性抗ウイルス応答不全であるか否かを評価するために、当業者は外植片を採取し、インビトロでこれらの細胞のいくつかを培養して、VSVによる、あるいは、ラパマイシンと併用した粘液腫ウイルスを含む粘液腫ウイルスによる感染の可能性を測定することができる。
【0061】
本明細書を通して、「インターフェロンに対して非応答性である細胞」という用語は、インターフェロンの活性、例えば、インターフェロンの抗ウイルス活性もしくは抗腫瘍活性に応答しない細胞、または異常なインターフェロン応答、例えば、インターフェロンに対する低下した、もしくは無効な応答を示すか、または、例えば、転写因子、例えば、STATlなどのシグナル伝達分子のリン酸化もしくは活性化によって測定すると異常なインターフェロンシグナル伝達を示す細胞を意味する。例えば、制限はないが、この細胞は、インターフェロンに対して応答性である細胞の中でそのような応答を誘導するのに十分な濃度のインターフェロンに曝露されても、増殖を阻害されず、または、死滅しないかもしれない。インターフェロンに対して非応答性の細胞は、細胞内シグナル伝達経路、または通常は応答性細胞の中で活性化されている経路に欠損があるかもしれない。典型的には、VSVによる感染に対する感受性は、インターフェロンに対する非応答性の指標であり、当業者は、インターフェロン存在下でVSV感染を阻止することができるか、またはその能力を欠いているかによって、あるいは、当技術分野において周知のインターフェロン活性のマーカーとなる他のもの、例えば、PKR、STAT、OAS、MXのように、INFによって刺激される遺伝子の発現レベルを用いて、特定の細胞がインターフェロンに対して非応答性であるか否かを簡単に判定することができる。
【0062】
本明細書を通して、「複製能がある」という用語は、特定の宿主の内部で感染および複製することができるウイルスを意味する。これは、特定の宿主の中では単独で複製を制限されているが、宿主細胞をラパマイシンで処理すると、ウイルスがその細胞に増殖的に感染することができるウイルスを含む。
【0063】
本明細書において、「細胞」という用語は、単一細胞および複数の細胞または細胞群を含む。細胞に薬剤を投与するとは、インビトロおよびインビボにおける投与を含む。
【0064】
本明細書において、「動物」という用語は、動物界の全生物を含み、具体的には哺乳動物、特にヒトを含む。
【0065】
先天的な抗ウイルス応答を欠損した細胞を「阻害する」という用語は、細胞を成長もしくは分裂できないようにすること、または細胞の増殖または分裂を低下もしくは遅延させることに加えて、溶解またはアポトーシスまたはその他の細胞死機構による細胞死を含む。
【0066】
当業者に周知で、例えば、Sambrook et al. ((2001) Molecular Cloning: a Laboratory Manual, 3rd ed., Cold Spring Harbour Laboratory Press)に記載されている標準的な分子生物学技術を用いて、粘液腫ウイルスのゲノムを容易に改変して、1つ以上の治療用導入遺伝子を発現させることができる。当業者は、粘液腫ウイルスのどの部分を欠失させれば、そのウイルスが依然として増殖性感染できるかを容易に決めることができるようになる。例えば、公表されたウイルスのゲノム配列を、特徴がはっきりした他のウイルスのゲノムと比較して、欠失させることができるウイルスゲノムの非必須領域を推定することができる(例えば、C. Cameron, S. Hota−Mitchell, L. Chen, J. Barrett, J.−X. Cao, C. Macaulay, D. Willer, D. Evans, and G. McFadden, Virology (1999) 264: 298−318)参照)。
【0067】
本明細書において、「治療用遺伝子」または「治療導入遺伝子」という用語は、その発現が所望の結果、例えば、抗癌作用をもたらす任意の遺伝子を広く説明しようとするものである。例えば、このウイルスを改変して、ウイルス治療の抗癌作用を増進する遺伝子を担持させることができる。このような遺伝子は、アポトーシスを開始させることに関与するか、または免疫を破壊するために感染細胞を標的とすることに関与する遺伝子であり、例えば、インターフェロンに対する応答の欠如を修復する遺伝子、または、細菌の細胞表面の抗原など、抗体の応答を刺激する細胞表面マーカーの発現をもたらす遺伝子などである。また、このウイルスを改変して、腫瘍性細胞または癌細胞の増殖および成長を遮断して、細胞が分裂できなくなることに関与する遺伝子を発現させることもできる。さらに、このウイルスを改変して、化学治療剤の合成に関与する遺伝子のような治療用遺伝子を含ませることができ、または、例えば、ヒト細胞など、阻害されるか死滅させられる細胞が由来する特定の生物種の細胞における複製量が増加するよう改変することができる。粘液腫ウイルスに挿入されて、その抗癌作用を高めることができる遺伝子の具体例は、TRAILタンパク質に関するヒト遺伝子、またはE4 orf4ポリペプチドをコードするアデノウイルス遺伝子などであるが、これらのタンパク質はいずれもヒト腫瘍細胞を死滅させることに関与する。
【0068】
当然のことながら、ラパマイシンと併用して使用される場合を含め、粘液腫ウイルスの治療効果は、このウイルスによる細胞溶解によって、またはこのウイルスによる治療薬の送達によって達成することができる。粘液腫ウイルスと併用してラパマイシンが含まれることによって、粘液腫ウイルス単独の効果を増強することが可能になるはずである。すなわち、粘液腫ウイルスは、ラパマイシンと併用して投与すると、粘液腫ウイルス単独のときよりも多数の標的細胞に増殖的に感染することができるか、またはラパマイシン不在下では粘液腫ウイルスによる増殖的感染を制限する、先天的な抗ウイルス応答を欠損した標的細胞に増殖的に感染することができるはずである。
【0069】
このウイルスは、当技術分野において周知の標準的な技術を用いて調製することができる。例えば、培養ウサギ細胞に使用すべき粘液腫ウイルス株を感染させてウイルスを調製することができ、感染を進行させて、ウイルスが培養細胞の中で複製し、当技術分野において既知の標準的な細胞表面破砕法によって細胞表面を崩壊させるとウイルスが遊離できるようにし、それによって、回収のためウイルス粒子を放出させることができる。ウイルスを回収したところで、ウサギ細胞のコンフルエントな細胞層に感染させてから、プラークアッセイを行なうことによって、ウイルス力価を測定することができる(Mossman et al. (1996) Virology 215:17−30参照)。
【0070】
また、先天的な抗ウイルス応答が欠損した細胞が存在することを特徴とする病状を治療するための方法であって、有効量の粘液腫ウイルスを、任意にはラパマイシンと併用して患者に投与することを含む方法が、そのような治療を必要とする患者に提供される。患者は、ヒトを含む哺乳動物など、任意の動物であってよい。
【0071】
本明細書において、「先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状」とは、先天的な抗ウイルス応答を欠損した細胞であって、これらの細胞を死滅させることによって病気、疾患、病状、もしくはその症状を治療することができる細胞が存在することに付随、関連、またはそれを特徴とする病気、疾患もしくは病状を意味する。例えば、病気の状態は癌であってよい。病気の状態はウイルスによる慢性感染症も含む。
【0072】
病状を「治療すること」は、臨床結果など、有益または所望の結果を得るための方法を意味する。有益または所望の臨床結果は、1つ以上の症状もしくは病状を緩和もしくは改善すること、病気の範囲が縮小すること、病状が安定すること、病気の発生を予防すること、病気の広がりを予防すること、病気の進行を遅延もしくは緩徐化すること、発病を遅延もしくは緩徐化すること、病状を改善もしくは緩和すること、ならびに(部分的もしくは全体的な)寛解を含むが、これらに限定されるものではない。「治療する」とは、治療を行わない場合に予想された生存期間を超えて患者の生存期間を伸ばすことを意味することも可能である。また、「治療する」とは、病気が進行するのを阻害して、病気の進行を一時的に緩徐化することを意味することも可能であるが、より好ましくは、病気の進行を永続的に停止させることを含む。
【0073】
一つの実施態様において、病状は癌である。癌は、必ずしも細胞の全部である必要はないが、細胞の少なくとも一部が先天的な抗ウイルス応答を欠損した任意の型の細胞であればよい。一つの実施態様において、癌は、細胞の少なくとも一部がインターフェロンに対して非応答性である癌であればよい。本明細書において、「腫瘍」、「腫瘍細胞」、「癌」および「癌細胞」という用語は(互換的に使用され)、細胞増殖の調節が顕著に失われることを特徴とする、異常な増殖を示す細胞または不死化している細胞を意味する。「癌」または「腫瘍」という用語は、転移性および非転移性の癌もしくは腫瘍を含む。本明細書において、「腫瘍性」または「腫瘍」という用語は、正常な増殖抑制機構なしに増殖する単一または複数の細胞を広く意味し、したがって、癌および異形成細胞もしくは過形成細胞に加えて、良性腫瘍を含む。
【0074】
癌は、悪性腫瘍の存在など、当技術分野において一般に受け入れられている診断基準を用いて診断することができる。
【0075】
本発明に従って治療することができる癌の型は、白血病、リンパ腫などの造血細胞癌、大腸癌、肺癌、腎癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮癌、前立腺癌、乳癌、子宮頸癌、直腸結腸癌、黒色腫およびその他の腫瘍を含むが、これらに限定されない。肉腫および癌腫などの固形腫瘍は、線維肉腫、粘液肉腫、脂肪肉腫、軟骨肉腫、骨原性肉腫、およびその他の肉腫、滑液腫瘍、中皮腫、ユーイング腫瘍、平滑筋肉腫、横紋筋肉腫、結腸癌、リンパ性腫瘍、膵癌、乳癌、肺癌、卵巣癌、前立腺癌、肝細胞癌、扁平上皮癌、基底細胞腫、腺癌、汗腺癌、脂腺癌、乳頭癌、乳頭腺癌、髄様癌、気管支原性肺癌、腎細胞癌、肺細胞腫、胆管癌、絨毛癌、ウィルムス腫瘍、子宮頸癌、精巣腫瘍、膀胱癌、およびCNS腫瘍(神経膠腫、星細胞腫、髄芽腫、頭蓋咽頭腫、上衣細胞腫、松果体腫、血管芽細胞腫、聴神経腫、乏突起膠腫、髄膜腫、黒色腫、神経芽細胞腫および網膜芽細胞腫など)を含むが、これらに限定されない。
【0076】
別の実施態様において、病状は慢性ウイルス感染症である。
【0077】
慢性的に感染するウイルスは、長期間にわたり持続的な形で動物の細胞内で感染および複製して、病態を引き起こすような任意のウイルスであってもよい。慢性感染ウイルスは、癌の発生と付随または関連するウイルスであってもよい。
【0078】
ウイルスの慢性感染症は、当技術分野において周知の標準的な方法を用いて診断することができる。例えば、慢性ウイルス感染症は、患者に抗ウイルス抗体が存在することによって、または患者の細胞の中にウイルスのRNAもしくはDNAが存在するかについて陽性試験することによって検出することができる。
【0079】
患者に投与する場合、有効量の粘液腫ウイルス、および任意には粘液腫ウイルスとラパマイシンを併用したものが、その投薬量または十分な期間において、このウイルスが病気を軽減、改善、緩和、寛解させ、その広がりを抑制し、その進行を緩徐もしくは遅延させ、または治療するのに必要とされる量である。例えば、癌性細胞または腫瘍細胞の数を減らしたり、破壊したりする効果、またはウイルスに慢性的に感染した細胞の数を減らしたり、破壊したりする効果、またはそのような細胞の成長および/または増殖を阻止する効果を達成するのに十分な量であろう。
【0080】
患者に投与すべき有効量は、粘液腫ウイルスおよび任意にはラパマイシンの薬力学的特性、投与方式、患者の年齢、健康状態および体重、病状の性質および範囲、治療頻度および、行っているならば、併用治療の種類、ならびにウイルスの毒性ならびに力価など、多くの因子に依存して変わりうる。
【0081】
当業者は、上記の因子に基づいて、投与する粘液腫ウイルスの適正な量を決定することができる。まず、患者の臨床反応に応じて、必要に応じて調整を加えることができる適当量にして、このウイルスを投与することができる。ウイルスの有効量は経験的に決定してもよく、それは安全に投与することができるウイルスの最大量、および所望の結果を生むウイルスの最小量に依存する。
【0082】
粘液腫ウイルスは、標準的な投与法を用いて患者に投与することができる。一つの実施態様において、このウイルスを全身的に投与する。別の実施態様において、このウイルスを病気の部位に投与する。特定の実施態様において、この病状は固形腫瘍であり、この腫瘍部位に注射によってウイルスを投与する。さまざまな実施態様において、ウイルスは、経口的もしくは非経口的に投与するか、または当技術分野において周知の標準的な方法によって投与することが可能である。
【0083】
全身にウイルスを投与する場合に、病気の部位にウイルスを注射することにより達成される効果と同じ臨床効果をもたらすためには、かなり高用量のウイルスを投与することが必要とされるであろう。しかし、適切な服用レベルは、所望の結果を得る最少量のはずである。
【0084】
投与するウイルスの濃度は、投与すべき粘液腫の具体的な株の毒性、および標的となる細胞の性質に応じて変わる。一つの実施態様において、約109プラーク形成単位(「pfu」)よりも少ない量をヒト患者に投与する。さまざまな実施態様において、約102から約109pfuの間、約102から約107pfuの間、約103から約106pfuの間、または約104から約105pfuの間を単一用量にして投与することができる。
【0085】
当業者は、上記の因子を用いて、患者に投与するラパマイシンの適正量を決定することができる。ラパマイシンの有効量は経験的に決定することができ、投与されるウイルスの量と株、安全に投与することができるウイルスの最大量、および粘液腫ウイルスの感染力の増強を実現するために投与することができるラパマイシンの最小量に応じて変わる。
【0086】
ラパマイシンは、標準的な投与法を用いて患者に投与することができる。一つの実施態様において、パマイシンを全身に投与する。別の実施態様において、ラパマイシンを病気の部位に注射して投与する。特定の実施態様において、病状は固形腫瘍であり、ラパマイシンをその腫瘍部位に注射によって投与する。さまざまな実施態様において、ラパマイシンを経口的もしくは非経口的に投与するか、または当技術分野において周知のいずれかの標準的な方法によって投与することができる。
【0087】
ラパマイシンの全量を単一用量にして、または1日または数日間にわたる多回用量にして投与することができる。用量の投与頻度および期間は容易に決定することができる。投薬計画は、粘液腫ウイルスを投与する期間に応じて決まる。例えば、ラパマイシンは、患者に単一回投与することもでき、または1日あたり2〜4回投与することもできる。
【0088】
さまざまな実施態様において、ラパマイシンの用量は1日あたり体重1kgにつき約0.01〜約250mg、1日あたり体重1kgにつき約0.01〜50mg、1日あたり体重1kgにつき約0.05〜10mg、1日あたり体重1kgにつき約0.1〜7.5mgであろう。
【0089】
有効量の粘液腫ウイルスとラパマイシンの併用剤を、初期治療計画の効果に基づいて、繰り返し投与してよい。投与は、典型的には、任意の反応をモニターしながら定期的に行われる。上記した用量よりも少ないかまたは多い用量を、選択された投与計画または経路に応じて投与してもよいと当業者は認識していよう。
【0090】
粘液腫ウイルスを、任意にはラパマイシンと併用して、単独療法として投与することができ、または、化学療法、放射線療法またはその他の抗ウイルス療法など、他の療法と併用して投与することができる。例えば、原発腫瘍の摘出手術の前もしくは後に、または、放射線療法もしくは従来型化学療法剤を投与するなどの治療の前、同時もしくは後に、粘液腫ウイルスを、任意には、ラパマイシンと併用して投与することができる。一つの実施態様において、その他の腫瘍退縮性ウイルスであって、多様な腫瘍細胞型に対して特異性を示しうるようなウイルスと組み合わせて、または逐次的に、粘液腫ウイルスを、任意にはラパマイシンと併用して投与することもできる。
【0091】
投与を容易にするために、粘液腫ウイルスを、任意には、ラパマイシンと併用して、医薬組成物の成分として調製することができる。したがって、さらなる実施態様において、粘液腫ウイルス、および任意にはラパマイシン、ならびに薬学的に許容される希釈剤を含む医薬組成物が提供される。したがって、本発明は、一つの態様において、先天的な抗ウイルス応答を欠損した細胞を阻害する際、または先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療する際に使用するための医薬組成物も含む。この組成物は、薬学的に許容される濃度の塩、緩衝剤、防腐剤、およびさまざまな適合担体を通常含むことができる。すべての送達形態について、組換え粘液腫ウイルスを生理食塩水内で処方することができる。
【0092】
この医薬組成物は、追加的な抗癌剤など、別の治療薬をさらに含むことが可能である。一つの実施態様において、この組成物は化学療法剤を含む。この化学療法剤は、例えば、患者の癌細胞または腫瘍細胞に対して腫瘍退縮効果を示すが、粘液腫ウイルスの腫瘍殺傷効果を阻害または低下させないものであれば、実質的にいずれの薬剤であってもよい。例えば、化学療法剤は、アントラサイクリン、アルキル化剤、スルホン酸アルキル、アジリジン、エチレンイミン、メチルメラミン、ナイトロジェンマスタード、ニトロソ尿素、抗生物質、代謝拮抗剤、葉酸アナログ、プリンアナログ、ピリミジンアナログ、酵素、ポドフィロトキシン、白金含有剤またはサイトカインであってよいが、これらに限定されるものではない。好ましくは、化学療法剤は、癌性または腫瘍性である特定の細胞型に対して有効であることが知られているものである。
【0093】
医薬上許容される希釈剤の比率および同一性は、選択された投与経路、生ウイルスとの適合性、および適用可能な場合には、ラパマイシンの化学的安定性との適合性、ならびに標準的な薬学的実施慣行によって決定される。通常、医薬組成物は、生きた粘液腫ウイルスの生物学的特性を顕著には損なわず、ラパマイシンが含まれている場合には、その分解をもたらしたり、その安定性または効力を低下させたりしない成分とともに処方される。
【0094】
この医薬組成物は、有効な量の単一または複数の活性物質を医薬上許容される賦形剤との混合物として併用されるよう、患者に投与するのに適した医薬上許容される組成物を調製するための周知の方法によって調製することができる。適当な賦形剤は、例えば、Remington’s Pharmaceutical Sciences (Remington’s Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., USA 1985)に記載されている。これに基づいて、組成物は、一つ以上の医薬上許容される賦形剤または希釈剤とともに、適当なpHおよび生理液と等張の緩衝液に含まれている、任意にはラパマイシンが入った粘液腫ウイルス溶液を、これらに限定されずに含む。
【0095】
当業者には当然のことながら、医薬組成物は、選択された投与経路に応じて、さまざまな形で患者に投与することができる。経口的または非経口的に、本発明の組成物を投与することができる。非経口投与は、静脈内、腹腔内、皮下、筋肉内、経上皮、経鼻、肺内、くも膜下腔内、直腸および局所的な投与方式を含む。非経口投与は、選択された期間にわたる持続注入によるものであってもよい。
【0096】
医薬組成物は、例えば、不活性希釈剤または同化可能な担体とともに経口投与することができ、または、硬ゼラチンカプセルまたは軟ゼラチンカプセルの中に封入することができ、または、圧縮して錠剤にすることもできる。経口的に治療薬として投与するには、粘液腫ウイルスを、任意にはラパマイシンと一緒に、賦形剤に取り込み、消化可能な錠剤、口腔錠、トローチ、カプセル、エリキシル剤、懸濁剤、ウエハースなどの形態にして使用することができる。
【0097】
粘液腫ウイルス溶液を、任意にはラパマイシンと一緒に、生理学的に適した緩衝剤の中で調製することができる。通常の保存および使用条件下では、これらの調製物は微生物の増殖を阻止するための保存剤を含むが、それで生ウイルスが不活化されることはない。当業者ならば、適当な処方剤の調製法を知っているであろう。適当な処方剤を選択および調製するための従来の手順および成分については、例えば、1999年に出版されたRemington’s Pharmaceutical SciencesおよびThe United States Pharmacopeia: The National Formulary (USP 24 NF19)に記載されている。
【0098】
さまざまな実施態様において、組成物は、腫瘍部位など病気の部位に直接(皮下、静脈内、筋肉内などに)注射によって投与されるか、または経口投与、あるいは、経皮投与によって投与される。
【0099】
注射液として使用するのに適した医薬組成物の形態は、無菌の水溶液もしくは分散液、ならびに無菌の注射用の溶液または分散液を即時調製するための無菌粉末などであるが、ここで、無菌という用語は、投与される粘液腫ウイルス自体には及ばない。すべての場合において、剤形は無菌でなければならず、そして容易に注射できる程度に流動性でなければならない。
【0100】
使用される医薬組成物の用量は、治療中の特定の症状、症状の重症度、年齢、体調、体格および体重など個々の患者のパラメーター、治療継続期間、(もしあれば)併用療法の性質、具体的な投与経路、ならびに医療専門家の知識および専門技術範囲内にあるその他の類似要素なに応じて変わる。これらの要素は、当業者に周知のものであり、最小限の日常的実験作業によって扱うことができる。
【0101】
また、任意にはラパマイシンと併用される粘液腫ウイルス、または粘液腫ウイルスおよびラパマイシンを含む医薬組成物は、同じ処方剤の中で一緒に、または異なる処方剤にして、キットとしてパッケージにすることもでき、このキットは、それを必要とする患者に、粘液腫ウイルスを使用して、もしくはラパマイシンとともに粘液腫ウイルスを使用して、先天的な抗ウイルス応答を欠損した細胞を阻害するため、または粘液腫ウイルスを使用して、もしくはラパマイシンとともに粘液腫ウイルスを使用して、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するためなど、粘液腫ウイルスおよびラパマイシンを使用するための説明書を含む。この病状は癌、または慢性ウイルス感染症であってよい。それを必要とする患者において、
また、本発明は、先天的な抗ウイルス応答を欠損した細胞を阻害するために、粘液腫ウイルスを、任意にはラパマイシンと併用して使用することを想定している。一つの実施態様において、細胞はインターフェロンに対して非応答性である。先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するために、それを必要とする患者に、粘液腫ウイルスを、任意にはラパマイシンと併用して使用することがさらに提供されている。一つの実施態様において、病状は癌である。また、薬剤の製造において、先天的な抗ウイルス応答を欠損した細胞を阻害するため、またはそれを必要とする患者において先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するために、粘液腫ウイルスを、任意にはラパマイシンと併用して使用すること提供されている。
【0102】
MVは、MVの自然宿主以外の動物の細胞、またはそれらに由来する細胞、すなわち、先天的な抗ウイルス応答を欠損している細胞集団に由来する細胞に選択的に感染することができる。MVにこのような能力があるため、培養中の、または動物の体内にある細胞の集団から、インターフェロンに対して非応答性の細胞など、先天的な抗ウイルス応答を欠失した細胞を検出する際にMVを使用することができる。このような細胞、例えば、蝕知可能な腫瘤にまで進行していないか、または動物の中で顕著な症状を誘起していない一定の癌細胞は、別の方法では容易に検出できないかもしれない。
【0103】
したがって、一つの実施態様において、患者の中で先天的な抗ウイルス応答を欠損した細胞を検出するための方法であって、検出可能なマーカーを発現するように改変された粘液腫ウイルスを、任意にはラパマイシンと併用して患者に投与すること;患者の中で、先天的な抗ウイルス応答を欠損した細胞にこのウイルス感染させること;および、患者の中で検出マーカーを発現する細胞を検出することを含む方法が提供される。
【0104】
感染細胞は、診断画像を視覚化するための従来の方法を用いて検出することができる。この検出法は、使用する具体的な検出用マーカーによって決まる。例えば、蛍光タンパク質を発現するように遺伝子改変された粘液腫ウイルスに感染した細胞は、蛍光デジタル画像顕微鏡を使用して検出することができる。その他の方法は、コンピュータ断層撮影法(CT)、陽電子放出撮影法(PET)などの全身走査法、核磁気共鳴影像法(MRI)、および超音波検査法などである。当業者は、具体的な検出マーカーを検出するための適切な方法を決めることができるだろう。
【0105】
検出可能なマーカーには、改変ウイルスに感染した細胞の内部で、マーカーの発現または合成が起きるように、それを発現または合成する遺伝子を粘液腫ゲノムに挿入することができる任意のマーカーがあるが、これらに限定されるものではない。例えば、一つの実施態様において、検出可能なマーカーは蛍光タンパク質でもよい。感染細胞は、改変ウイルスが先天的な抗ウイルス応答を欠損した細胞に感染して、検出可能マーカーをそのような細胞の中で検出可能なレベルで発現させることができるようにするため、改変ウイルスを患者に投与した後適当な時間をおいて検出することができる。例えば、蛍光タンパク質を発現するように遺伝子改変したウイルスを患者に投与した後、2〜20日間のいずれかの時点で検出することができる。
【0106】
先天的な抗ウイルス応答を欠損した細胞が患者に存在することをモニターするために、その患者において、間隔をおきながら繰り返し検出法を実施することができる。例えば、粘液腫ウイルスを用いて、そのような細胞を検出する方法は、先天的な抗ウイルス応答を欠損した細胞の性質、および患者の体内にそのような細胞が存在する結果として引き起こされたいずれかの病状の性質に基づき、必要に応じて、6ケ月、1年または2年の間隔で実施することができる。ある期間にわたりこの方法を繰り返すと、病状の進行もしくは寛解、または患者の体内での病気の広がりをモニターすることが可能になる。
【0107】
粘液腫ウイルスは、先天的な抗ウイルス応答を欠損した細胞に選択的に感染する能力があるため、細胞におけるそのような欠損の指示薬として使用することができる。したがって、本発明の方法を用いて、先天的な抗ウイルス応答の欠損について、患者から摘出した細胞をアッセイすることができる。このような測定法は、他の指示薬と併用すると、その患者が特定の病状、例えば、癌に罹患していることを表示することができる。
【0108】
したがって、一つの実施態様において、試料中で先天的な抗ウイルス応答を欠損した細胞を検出するための方法であって、細胞を培養すること、培養細胞を、任意にはラパマイシンと併用した粘液腫ウイルスに曝露すること、および粘液腫ウイルスによる細胞の感染力を測定することを含む方法が提供される。
【0109】
周知の生検法を用いて、ヒト被験者など、被験対象から細胞を取り出すことができる。生検法は、検査すべき細胞の存在する場所およびその型に応じて決められる。
【0110】
周知の培養技術に従って細胞を培養してから、培養液に生きた粘液腫ウイルス、および任意にはラパマイシンを添加することにより、細胞をMVに、任意にはラパマイシンに曝露する。粘液腫ウイルスをラパマイシンと併用して添加する場合、ウイルスとラパマイシンは、同時または経時的に添加することができる。ラパマイシンが存在する場合など、感染多重度(「MOI」)を変えて、所定の細胞型、密度および培養技術、および具体的なラパマイシン濃度に対して最適なMOIを、MVに曝露すると感染することが知られている陽性対照細胞の培養物を用いて決定することができる。
【0111】
ラパマイシンの量、ならびにラパマイシンおよび粘液腫ウイルスを培養細胞に添加するタイミングは、細胞型、培養方法、およびウイルス株に応じて変えることができる。このようなパラメーターは、常法を用いた最小限の検査法によって試験および調整することができる。
【0112】
MVの細胞死を引き起こす能力など、ラパマイシンが存在する場合も含んだMVによる培養細胞への感染力は、当業者に周知のさまざまな方法によって決定することができる。また、これは、ウイルスの発現産物との酵素反応または化学反応を完了させるために、細胞培養液に試薬を添加することも含むかもしれない。ウイルス発現産物は、MVゲノムに挿入されたレポーター遺伝子から発現されたものであってもよい。
【0113】
一つの実施態様において、MVを改変して、感染状態を検出するのを容易にすることができる。例えば、MVを遺伝子改変して、位相差顕微鏡、蛍光顕微鏡、または放射性イメージングによって容易に検出することができるマーカーを発現させることができる。このマーカーは、発現された蛍光タンパク質、または比色反応または放射標識反応に関与する可能性のある発現酵素であってもよい。別の実施態様において、このマーカーは、試験されている細胞の特定の機能を妨害または阻害する遺伝子産物であってもよい。
【0114】
本発明は、以下の非限定的な実施例によってさらに具体的に説明される。
【実施例】
【0115】
(実施例1:粘液腫ウイルスによるマウス細胞株およびヒト細胞株への感染)
(ウイルス株)
使用したウイルス株は、野生型MV、緑色蛍光タンパク質(「GFP」)またはβ−ガラクトシダーゼ(「LacZ」)を発現するように改変されたMV、および死滅(「不活化」)ウイルスを含む。標準的な技術を用いて、ウイルスを調製し滴定した。
【0116】
(細胞株)
野生型マウス、および以下のノックアウトマウスに由来するマウス胚線維芽細胞(「MEF」)を使用して、マウス実験を行った。すなわち、IFNα/β受容体ホモ接合ノックアウト、STATlホモ接合ノックアウト、PKRヘテロ接合ノックアウト、RNase Lヘテロ接合ノックアウト、Mx1ヘテロ接合ノックアウト、PKR/RNaseL/Mx1ホモ接合三重ノックアウト。
【0117】
Stojdl et al.,Cancer Cell(2003)4:263−275に記載されているように、BGMK対照細胞および以下のヒト腫瘍細胞株に対してヒトに関する実験を行った。すなわち、HT29、HOP92、OVCAR5、SK−MEL3、SK−MEL28、M14、SKOV3、PC3、DU145、CAKI−1、786−0、T47D、MDAMB435、SF04、U87、A172、U373、DaoyおよびD384。
【0118】
(方法)
一般的には、Lalani et al. Virology (1999) 256: 233−245; Johnston et al. J Virology (2003) 77(13): 7682−7688; and Sypula et al. Gen Ther Mol Biol (2004) 8: 103の記載に従って、アッセイ法および実験を行った。
【0119】
インビボでのマウス研究では、ヒト頭蓋内神経膠腫U87をヌードマウスに移植した。移植後15日目に、生きたMV GFPまたは不活化MV GFPを5×106の力価でマウスの腫瘍内に注射するか、擬似感染させた。感染後72時間目に、動物を殺してから、その脳を摘出してOCT(至適温度化合物)の中に埋め込み、凍結切片を切り出した。蛍光顕微鏡によって全脳切片の中で粘液腫GFPを可視化した。その後、切片を固定し、H&E(ヘモトキシリンおよびエオシン)を用いて染色して、腫瘍を可視化した。
【0120】
ヒト腫瘍細胞アッセイ法では、手術後直ちに、腫瘍をトリプシン処理して平板培養し、翌日、MOI0.1、1.0または10でウイルスに感染させた。感染後24時間目および48時間目に、位相差顕微鏡法および蛍光顕微鏡法を用いて、それぞれ細胞毒性およびウイルス発現に関するデータを集めた。黄色テトラゾリウム塩MTTを用いるアッセイ法を行って、感染後48、72または96時間目の細胞生存率(%)(擬似感染後生存していた細胞に対するパーセンテージ)を定量した。
【0121】
ヒト小児髄芽腫細胞株DaoyおよびD384を、10M.O.I.の粘液腫GFPに感染させた。感染後72時間目に、MTTを用いて細胞生存率を測定した。
【0122】
(結果:マウス細胞株の感染)
従来の研究では、ケモカイン受容体でトランスフェクトされたマウス3T3細胞のいくつかのクローンに、粘液腫ウイルスを感染させることができたが、その他のクローンには感染させることができなかったことが示されていた。他のマウス細胞において粘液腫ウイルス指向性がいずれか特定の受容体に依存しているか否かを調べるために、本発明者らは、野生型(WT)マウスおよび多様な遺伝子ノックアウト由来の初代マウス胚線維芽細胞(MEF)を利用した。
【0123】
IFNは抗ウイルス応答を開始する上で重要な役割を果たしているため、本発明者らはこの制限的な表現型(restrictive phenotype)が、IFNを介した「抗ウイルス状態」に関係があると仮定した。IFN系の事象の連鎖を断つか、抗体によって循環INFを中和するか、またはIFN受容体陰性マウスもしくは細胞内シグナル伝達経路の遺伝子を欠失したマウスを作成すると、通常は正常なマウス細胞には感染しない粘液腫ウイルスに対する宿主の抵抗性が著しく損なわれると考えた。
【0124】
この仮説を検証するために、本発明者らは、非許容性細胞における粘液腫ウイルスの非感染性がIFNの抗ウイルス活性のせいであるか否かを明らかにする必要があった。細胞内IFNシグナル応答に関与する1つ以上のタンパク質をノックアウトしたさまざまなMEF細胞型について、IFN経路に対するMV感染の効果を調べた。
【0125】
初代MEFに対して行われた実験によって、野生型(「WT」)MEFは粘液腫ウイルスによって感染可能ではないことが実証された。INF経路がINFα/βに対する中和抗体によってブロックされた場合、前記MEFは粘液腫ウイルスによって完全に感染可能になる(図2)。しかし、INFγに対する中和抗体に曝露されたMEFは非許容性のままであった。このことは、粘液腫ウイルスがインビトロでMEFに感染するのを許容する環境を作り出すことに、IFNγではなくIFNα/βが重要であることが大まかに示している。INFα/βおよびINFγに対するさまざまな細胞内シグナル伝達経路が文献中で同定されてきた。しかし、INFα/βおよびINFγはともに、培養された線維芽細胞とは異なり、感染宿主中において重要な役割を果たしている可能性が高い。本発明者らは、INFα/βおよび/またはINFγの経路のいずれかを欠損したヒト腫瘍がインビボでの粘液腫ウイルス感染に感受性になるものと予想している。
【0126】
本発明者らは、MVに感染した非許容性WT MEFの中でSTAT1およびSTAT2の活性を調べた。図3に示す結果は、STAT1およびSTAT2が活性化されることを示した。さらなる研究によって、STAT3、STAT4およびSTAT5は活性化されないことが示された(図4)。
【0127】
MEFの非許容性状態を維持する上でIFNα/β細胞内経路が重要性であることを確認するために、遺伝子欠失実験を行って、INFα/β受容体および細胞内カスケードを破壊したものを用意した。INF受容体またはJAK1もしくはSTAT1の遺伝子を欠失させ、MVを使用して、WT MEF、IFNα/β R−/−MEFおよびSTAT1−/−MEFを感染させた。IFNα/β R−/−MEFおよびSTAT1−/−MEFはMVに対して許容性であり、INFα/βおよびSTAT1カスケードがMV感染にとって重大な意味を持つことを明らかにした(図5)。
【0128】
プリテインキナーゼR(PKR)は、さまざまな細胞の中でINFα/βによって誘導される酵素である。このキナーゼは、dsRNAの存在下で自己リン酸化を受け、次に、リン酸化によってタンパク質翻訳およびアポトーシスの阻害を誘導することができる、真核生物のタンパク質合成開始因子(eIF−2α)など、いくつかの細胞タンパク質をリン酸化する。また、PKRはRNaseLの活性化にも示される。本発明者らは、MV感染後、非許容性MEFにおけるPKRの活性化を調べた。抗ウイルス状態が十分に確立している非許容性MEFでは、PKRはリン酸化されない(図6)。さらに、MV感染によって、PKRのリン酸化が阻害される(図7)。また、PERK(PKR様のERキナーゼ)は、粘液腫ウイルス感染後の初期の野生型MEF内でリン酸化されない(図8)。
【0129】
MVを用いて、PKR、RNaseLまたはMx1の単一遺伝子ノックアウトを有するMEFに感染させた(図9)。PKR、RNaseLまたはMx1は、粘液腫ウイルス感染に対する非許容性を維持するためには非必須であることが発見された。PKR、RNaseLおよびMx1の役割が必須でないことをさらに確かめるために、MEFにおいてPKR−/−、RNaseL−/−およびMx1−/−という三重ノックアウトを行った。PKR−/−、RNaseL−/−およびMx1−/−の三重ノックアウトは、MV感染を支持しない(図10)が、しかし、インターフェロンα/βに対する中和抗体で処理された、PKR、RNaseLおよびMx1の三重ノックアウトMEFは粘液腫ウイルス感染に対して許容性となる(図10および11を比較せよ)。これらの実験は、MVに対するMEFの非許容性をもたらす上で、PKR、RNaseLおよびMx1は必須ではないことを示している。
【0130】
さらなる実験を行って、MV感染後の非許容性野生型MEFおよび許容性のINFα/β R−/−MEFならびにSTAT1−/−MEFにおけるeIF2αおよびPKRの活性化を調べた。MV感染後に、eIF2αは非許容性MEFおよび許容性MEFの中でリン酸化されるが、PKRはどちらの場合においてもリン酸化されない(図12)。このことは、PKRおよびPERKの関与がなくても、eIF2αリン酸化を引き起こす別の経路によって、抗ウイルス状態がもたらされることを示している。
【0131】
STAT1は、非許容性のPKR、RNaseおよびMx1の三重ノックアウトMEFにおいて、MV感染後にセリンおよびチロシンのリン酸化を受ける(図13)。また、粘液腫ウイルス感染後の非許容性PKR−/−+RNaseL−/−+Mx1−/−MEFにおけるチロシンリン酸化STAT1の細胞内局在化も示されている(図14)。
【0132】
要約すれば、これらの結果は、IFN/STAT1を含む並行したPKR/PERK非依存的な抗ウイルス経路が、ポックスウイルス指向性にとって重大な意味を持つことを示している。さらに、eIF2αのリン酸化は、INFによる抗ウイルス作用の最良のマーカーである。
【0133】
(結果:ヒト腫瘍研究)
本発明者らは、MVがインビボ系の中でヒト腫瘍細胞に感染することができるかを調べた。ヌードマウスにヒト神経膠腫細胞を注射したところ、引き続いて、頭蓋内神経膠腫を発症した。生ウイルスは、これらのヒト腫瘍細胞に感染することができたが、周囲の細胞には感染しなかった(図15)。GFP由来の蛍光シグナルが腫瘍に局在化することを図16に示す。
【0134】
多くのヒト腫瘍がインターフェロンに対して非応答性であること、および、正常なヒト細胞の中に存在するINFシグナル伝達カスケードと比較すると、これらの腫瘍細胞は正常なINFシグナル伝達カスケードを持たないことから、ヒト腫瘍に対する粘液腫ウイルスの効果を調べるために実験を行った。結果を下記に要約する。
【0135】
最初に、粘液腫ウイルスを用いて、さまざまな対照腫瘍細胞株およびヒト腫瘍細胞株であるBGMK、HT29、HOP92、OVCAR4、SK−MEL3、およびSK−MEL28に対する感染力および細胞溶解性効果を調べた。MVは多様な感染力および細胞溶解作用の結果を示した:HT29(図17)、HOP92(図18)、OVCAR4(図19)、SK−MEL3(図20)、SK−MEL28(図21)およびBGMK(図22)。
【0136】
さらなる腫瘍細胞を検査し、下記の表1は、検査した多様な腫瘍型を許容性および非許容性に分類している。
【0137】
(表1 粘液腫ウイルスのヒト腫瘍細胞に対する指向性)
【0138】
【表1】

MV−LacZの濃度を増加させて感染させると、多様なヒト腫瘍株がさまざまな反応性を示した。例えば、U373細胞では、U87において低いウイルス力価で行われた細胞殺傷のレベルを達成するのに高いウイルス力価を必要とした(図23および図24)。粘液腫は星状細胞腫細胞(図25)および神経膠腫細胞(図26)を効率的に感染させた。粘液腫は感染48時間後、死滅したヒト星状細胞種および髄芽細胞腫において効率的だった。
【0139】
(実施例2:制限細胞株におけるにおける粘液腫ウイルス複製の動態に対するラパマイシンの効果)
(ウイルス株)
使用されたウイルス株は、野生型MV(「vMyxLac」)、およびMT−5遺伝子がノックアウトされるよう改変されたMV(「vMyxLacT5−」)を含む。標準的な技術を用いて、ウイルスを調製および滴定した。
【0140】
(細胞株)
ヒトに関する実験を、BGMK霊長類対照細胞、RK−13ウサギ対照細胞、および正常なヒト線維芽細胞A9、制限ヒト腫瘍細胞株786−0(腎臓癌)、ACHN(腎臓癌)、HCT116(結腸癌)、MCF−7(乳癌)、MDA−MB−435(乳癌)、M14(黒色腫)およびCOLO205(結腸癌)に対して行った。
【0141】
(方法)
一般的に、Lalani et al. Virology (1999) 256: 233−245; Johnston et al. J Virology (2003) 77(13): 7682−7688;およびSypula et al. Gen Ther MoI Biol (2004) 8: 103に記載されているとおりに、アッセイ法および実験を行った。
【0142】
ウイルスの増殖曲線には、細胞をインビトロで単層に増殖させ、ウイルスに感染させる前に20nMのラパマイシンまたは対照(DMSOを1:5000に希釈したもの)で処理した。
【0143】
表示されたウイルス株に感染した表示された細胞株の試料を、感染後72時間目に集めて、溶解させた。細胞溶解物の中に含まれるウイルスを滴定して、BGMKの単層を感染させるのに使用した。感染後48時間目に細胞を固定して、X−galを用いて染色した。
【0144】
(結果)
粘液腫ウイルスは多くの種類のヒト腫瘍細胞に感染して複製できることが、本発明者らによって既に明らかにされている(Sypula et al. (2004) Gene Ther. Mol. Biol. 8:103)。このウサギ特異的ウイルスは、NCI参照用コレクションに由来するヒト癌細胞株の大多数(約70%)に選択的に感染することができる。また、宿主域遺伝子M−T5が、これら多くの細胞株に粘液腫ウイルスが感染する際に重大な役割を果たすことが分かっている。
【0145】
ヒト腫瘍細胞の内部で粘液腫ウイルスが選択的に複製する能力に影響を与えることができる細胞内分子の可能性があるものを今回調査した際に、ラパマイシンの効果を調べた。
【0146】
図29から分かるように、低多重度感染(MOI)の後、粘液腫ウイルスが複製および拡散できることを、多段階増殖曲線を用い、BGMK(対照用霊長類細胞株);RK−13およびRL5(対照用ウサギ細胞株);4TlおよびB16F10(マウス癌細胞株);HOSおよびPC3(許容性ヒト細胞株)、786−0、HCT116、およびACHN(制限ヒト癌細胞株)、MCF−7、M14ならびにCOLO205(不全型ヒト癌細胞)を用いて行うことができる。野生型vMyxLacと、M−T5ノックアウトウイルスvMyxT5KOの両方を試験して、ラパマイシンによる予備処理した場合としない場合に、この2つのウイルスが単層全体に感染して拡散することができるかを調べた。BGMK細胞上で病巣形成させて、ウイルスの力価を測定した。感染させる6時間前に、20nMのラパマイシンまたは適当な賦形剤対照(DMSOを1:5000に希釈したもの)で細胞を事前処理した。
【0147】
実証されているように、ラパマイシンは、対照BGMK細胞に対しても、MT−5ノックアウトウイルスに対して非許容的なRL−5細胞を含む試験したウサギ細胞株のいずれに対しても何の効果も示さない。しかし、ラパマイシンは、マウス腫瘍細胞株の中では粘液腫ウイルスの複製を促進し、PC−3などの許容性(I型)細胞株の中では僅かに促進する。ラパマイシンは、HOS細胞のように非常に許容的な細胞に対しては効果が少ないが、それは、このような細胞株は既に粘液腫ウイルスに対して最大限許容的であるという事実による可能性が高い。ラパマイシンによる最大の効果は、制限性(II型)細胞株(786−0、HCT116およびACHN)で観察されたが、これらは、野生型ウイルスに対しては許容性があるが、vMyxT5KO株に対しては非許容性である。不全型(III型)細胞株であるMCF−7およびCOLO205においてさえもいくらかの効果が見られたが、不全型細胞株M14では見られなかった。
【0148】
次に、BGMKおよび786−0の感染細胞の試料を回収して溶解し、単離したウイルスを用いて、BGMK細胞の単層を感染させた(図30)。X−Gal染色を用いて、ウイルス感染した細胞を可視化した。
【0149】
粘液腫ウイルス感染に対して「制限的」な腫瘍細胞、すなわち、野生型粘液腫ウイルスの複製は許容するが、MT−5ノックアウトウイルスの複製は許容しない細胞をラパマイシンで処理すると、粘液腫ウイルスが、腎臓癌、結腸癌、および卵巣癌の細胞株を含む癌細胞株において複製する能力を回復する結果となった(図29および30)。
【0150】
さらに、ラパマイシンで処理すると、野生型ウイルスがこれらと同じ細胞の中では複製する能力は増強されたが、対照であるウサギ細胞または霊長類細胞では増強されなかった。これらの結果は、ラパマイシンが粘液腫ウイルスの感染を促進するように作用することを示している。また、ラパマイシンは、このウイルスに感染されにくい癌細胞がウイルス複製を許容する能力に影響を与えると考えられる。
【0151】
その後の実験で、野生型粘液腫ウイルスの感染を支持することができなかったヒト腫瘍細胞に対するラパマイシン処理の効果を調べた(図31)。この事前処理は、対照である霊長類細胞や正常なヒト線維芽細胞に対してほとんど効果を示さなかったが、乳癌細胞株MCF−7など、いくつかの細胞株におけるウイルスの感染力を増強することができた。ヒト腫瘍細胞のいくつかが、対照細胞株と同じように、ラパマイシン処理に対して抵抗性のままであったため、ラパマイシン処理によって、粘液腫ウイルスが、非形質転換組織に増殖性感染できるようになったとは考えにくい。
【0152】
(実施例3:改良型腫瘍退縮性ウイルス候補としての粘液腫ウイルスM135KO変異型。)
(M135Rは、初期遺伝子として粘液腫ウイルスから発現される)
粘液腫ウイルスは、MVゲノムの配列決定から同定されたタンパク質(M135R)をコードし(Cameron et al. Virology (1999) 264: 298−318)、宿主のIFNα/β受容体を模倣し、IFNα/βが宿主の抗ウイルス応答を開始させないようにしていると予測されている (Barrett et al. Seminars in Immunology (2001) 13:73−84)。この予測は、そのような免疫回避戦略を採ることが明らかになっている(Symons et al. Cell (1995) 81 :551−560)ワクシニアウイルス(B18R)に由来するウイルスIFNα/β受容体のホモログに対する配列相同性に基づいている。しかし、M135Rは、VVB18R、およびその他配列決定されたポックスウイルス由来のINFα/β−R相同体の大きさの半分しかないため、すべての場合で、ポックスウイルスIFNα/β−Rの相同体のアミノ末端側の半分だけにしかアラインメントされない。図32は、MVのM135RとVVのB18Rの間で予測された構造および配列の類似性を示している。B18Rの最初の179アミノ酸残基だけが、配列アラインメントで示されている。表2は、M145Rと、表示されたポックスウイルスIFNα/β−Rの相同体との一致率(%)を示している。対角線の上の数字は、一致率(%)を表し、対角線の下の数字は、2つの種間における類似性(%)を表している。上部を横切る括弧内の数字は、推定されたタンパク質のアミノ酸数を表している。予測されたM135R(178アミノ酸)の全長コピーと各相同体の最初の178残基だけの間で比較を行った。
【0153】
(表2 M135Rと他のポックスウイルス相同体との比較)
【0154】
【表2】

M135Rの推定免疫原領域に対するペプチドを合成して、ウエスタンブロット解析、免疫沈殿、および免疫蛍光法で使用したポリクローナル抗体をウサギの中で作製した。免疫ブロッティングによって、M135Rが、感染後早くも3時間でその発現を検出できる初期遺伝子として合成されていることを確認した(図33A;レーン1:模擬感染BGMK細胞;レーン2〜6:それぞれ感染後0、3、6、18、および36時間目のvMyxLauに感染したBGMK細胞)。感染細胞をAraCで処理すると、M135Rの合成は、後期のタンパク質発現を阻害しても変化することがないため、これは初期遺伝子であることが示される(図33B)。しかし、ツニカマイシンで処理すると、おそらく、配列から予測された単一の部位で、M135RはN結合型グリコシル化されていることが示される(図33B)。モネンシン処理によって、O結合型グルコシル化は存在しないことが示唆されている。図33に示されている結果について、BGMKには、moi10で粘液腫ウイルスを感染させた。40μg/mlの濃度のAraC、1μg/mlのツニカマイシン、および1μg/mlのモネンシンで、表示された時間に細胞を処理したか、処理しなかった。ペプチド抗体を用いてM135Rを検出した。
【0155】
(M135Rはシグナル配列をコードするが分泌されない)
M135Rの配列解析によって、推定シグナル配列が存在することが示されている(図32B)。しかし、カルボキシ末端には膜貫通ドメインと推定されるものもある(図32B)。感染BGMK細胞から得た上清の免疫ブロットは、M135Rが分泌されないことを示している。しかし、M135Rは、全細胞溶解液の中で簡単に検出される(図33)。シグナル配列が、M135Rを細胞表面に追いやるよう機能したか否かを調べるために、本発明者らは、膜貫通ドメインを欠失させ、この変異体をバキュロウイルス発現系にクローニングした。Ac135RとAc135ΔTMに感染した上清を比較したところ、全長のM135Rが細胞溶解液中に見られ、分泌された証拠はない。これに対し、Ac135ΔTMは分泌され、シグナル配列がM135Rを細胞外環境に追いやるよう機能していることが確認できる(データは示さず)。
【0156】
(M135Rタンパク質は、感染細胞の表面に局在する)
M135Rが機能的なシグナル配列と膜貫通ドメインをもつという観察結果から、本発明者らは、急いでM135Rの局在を調べた。2つの証拠が、M135Rが細胞表面に局在することを示している。まず、BGMKをカバーガラスの上に播種して、24時間vMyxLau(moiは10)に感染させると、アフィニティー精製された抗M135R、次いでFITC結合二次抗体による免疫染色でM135Rが検出された(図34A)。M135Rの染色パターンは、感染した細胞の細胞表面への局在を示している。vMyxLauは、β−gal遺伝子やEGFP遺伝子の挿入によって改変されていない真正な粘液腫ウイルスの野生型である。
【0157】
第二の証拠は、M135Rが、vMyzgfpまたはvMyx135KOのどちらかに感染したGHOST細胞の細胞表面タンパク質のビオチン化に付随することである。感染後24時間で細胞溶解液を調製した。ストレプトアビジンアガロースビーズを、細胞溶解液から得た全細胞タンパク質500μgと45分間混合した。このビーズを洗浄して、15%SDS−PAGEゲルで分離してから、抗M135Rでプローブした。感染した細胞の溶解液から得た50μgの全細胞タンパク質を対照として泳動した。ビオチン化した表面タンパク質を免疫沈殿すると、m135Rが感染した細胞の表面に存在することが示される(図34B)。
【0158】
(M135Rはインビトロにおける粘液腫ウイルスの複製に必須ではない)
M135Rが病原性因子として作用することができるかを調べるために、本発明者らは、M135Rを欠失し、VV早期/後期プロモーター下でEGFPおよびgptをコードするカセット(460ヌクレオチド、すなわちorfの86%が欠失している)で置換されている組換えウイルスを構築した。クローニング法およびカセットを図35Aに示す。EGFPを発現するウイルスクローンを選択して、組換体をプラーク精製した。組換体の精製度をPCRで確認した(図35B;レーン1は1Kb+DNAラダー、レーン2および3は、2つの精製vMyx135KOクローンからのPCR産物。PCR産物は、M135Rのコード領域が欠失されて、EGFP/gptマーカーが挿入されている領域を表している。レーン2はプラーク1であり、レーン3はプラーク2である。レーン4は、同じ領域を示し、本来の切断されていないM135R遺伝子座をカバーしている)。vMyxLauまたはvMyx135KOのいずれかに感染したBGMK細胞の免疫ブロッティングによって、vMyx135KOがM135R発現を失ってしまったことが確認された(図35C;M135Rの発現の経時変化:レーン1は未感染のBGMK細胞。レーン2〜6は、感染後0時間(レーン2)、3時間(レーン3)、6時間(レーン4)、18時間(レーン5)、および36時間(レーン6)における、vMyx135KOに感染したBGMK細胞を示している。レーン7および8は、感染後6時間(レーン7)および18時間(レーン8)における、vMyx135KOに感染したBGMK細胞を示している。レーン9は、AcNPVで発現するM135Rをもつ陽性対照である)。
【0159】
一段階増殖曲線を用いて、vMyx135KOがBGMK細胞の中で複製できるかを調べた。BGMK細胞を、moi5でvMyxgfpまたはvMyx135KOに感染させ、表示された時間に細胞を回収した。ウイルスの力価をBGMK細胞上で測定した。vMyxgfpとvMyx135KOの間で複製パターンの違いはなかった(図36)。これらの結果は、M135Rがインビトロでの複製には必要でないことを示している。
【0160】
粘液腫ウイルスの別の遺伝子が、ウサギの初代胚線維芽細胞(REF)における粘液腫ウイルスの複製に影響できないかを調べた本発明者らの実験の際に、ノックアウト対照としてvMyx135KOを用いたが、奇妙な現象を観察した。REFにvMyxgfpを感染させると、正常な感染病巣が生じたが、vMyx135KOは、感染のプラーク様ゾーンを生じさせた(図37)。本発明者らが、この表現型を確認するために別の細胞を調べたとき、別のウサギ線維芽細胞(HIG−82、図38)およびヒト初代線維芽細胞(ccd922−sk、図39)では、プラーク形成を反復させることができた。
【0161】
(M135Rはウサギにおける病原性に対する重大な病原因子である)
次に、本発明者らは、vMyx135KOが実験用ウサギの中で粘液腫を発生させることができるかを調べた。vMyxLauまたはvMyxgfpを感染させて、感染後9から10日の安楽死させなければならない動物とは対照的に、vMyx135KOを注射されたウサギは完全に回復した(表3)。M135Rの消失がvMyx135KOの弱毒化をもたらすことを確認するために、本発明者らは、M135Rが回復された復帰変異体ウイルスを作製し、この復帰変異体(vMyx135REV)が、粘液腫を生じさせる能力を回復することができるかを調べた。4つのウサギの処理グループはすべて、各ウイルスを注射してから最初の6日間は同じように応答した(表3)。本発明者らは、感染後4日目までは、すべての処理グループで、注射した部位に大きく赤い盛り上がった病変部ができるのを観察した。しかし、6日目に始まり、その後引き続き3〜4日間にわたって、さまざまなウイルスの間の違いが明らかになった。野生型または復帰変異型ウイルスを注射した動物は、耳、眼、および鼻に、vMyx135KOを注射した動物には見られなかった数多くの二次的病変部を持っていた(表3)。本発明者らは、動物モデルにおいて、M135Rの消失は劇的にMVを弱毒化すると結論づけ、M135Rが重大な病原因子であることを示している。
【0162】
(表3 野生型対照と比較したときのvMyx135KOの病原性)
【0163】
【表3】

実験前の3日間、ウサギの体温を毎日測った。これを動物の基礎体温と見なした。実験の間中、各動物の体温を毎日測り続けた。しかし、処理グループ間に体温の違いはなかった(図40)。これは、M135Rが、感染動物の発熱反応に関与していないことを示唆するものである。
【0164】
(M135RはウサギIFNα/βに結合または阻害しない)
M135Rの配列は、IFNα/β受容体の模倣体であるワクシニアB18Rに類似している。本発明者らは、M135Rがウサギの1型IFNに結合できるかを調べた。まず、ウサギIFN(5μg、ヨードビーズを用いて)をヨウ素化して、vMyx135KOに感染した細胞が、vMyxgfpを(moi10で)感染させた細胞と比較して、125I−ウサギIFNに結合できるかを調べた。細胞を回収して、洗浄し、ガンマ線計測装置で計測した。M135Rの欠失は、感染細胞へのIFNα/βの結合に影響せず、RK13細胞またはBGMK細胞のいずれかの細胞表面に結合しているIFNの量に差異は見られなかった(図41)。また、RK13細胞またはBGMK細胞を外来性のウサギ1型IFNで処理しても、vMyx135KOによる細胞への感染には影響を与えなかった(図42;細胞を12穴培養皿に播種し、表示されたウイルスにmoi0.01で感染させた;感染後72〜96時間目に蛍光巣の数を数えた;200ユニットのウサギIFNα/βを、感染させる24時間前に添加するか、細胞を処理しなかった)。この同じ結果が、感染させる24時間前に事前処理して、細胞の中で抗ウイルス状態を誘導したときにも見られた。RK13細胞またはBGMK細胞のいずれかで感染後に形成される巣に顕著な違いがあることに気づかなかった(データは示さず)。また、この現象は、細胞をヒトIFNA/Dで処理した場合にも当てはまる(データは示さず)。また、Ac135ΔTMの上清を、BIAcoreチップに付着させたウサギIFNα/βに適用すると、結合を全く観察できなくなった(データは示さず)。
【0165】
(実施例3:粘液腫ウイルス感染に関連してmTORを阻害することの分子的影響)
ラパマイシンが粘液腫ウイルス感染を促進するII型癌細胞株である786−0細胞の細胞溶解液を用いてウエスタンブロット解析を行った(図43)。vMyxLacまたはvMyxT5KOのいずれかをMOI3で感染させたか、ウイルス感染させないままで16時間経過した後に溶解液を回収した。表示したレーンには、感染前6時間20nMのラパマイシン(Rと命名)、または適当な賦形剤対照(DMSOを1:5000で希釈したもの、Dと命名)で事前処理した細胞からのタンパク質を含む。表示したタンパク質に対する一次抗体を用いてブロットをプローブした。
【0166】
実証されたように、粘液腫ウイルス感染は、ラパマイシンの生理学的標的であるmTORに収束する多くのシグナル伝達経路に影響を与える。ラパマイシンがウイルス複製に大して有利な効果をもつ、野生型ウイルス(vMyxLac)またはMT−5欠損型ウイルス(vMyxT5KO)のいずれかによる感染に関しては、ラパマイシン単独処理に基づいては予測しえなかった広範囲の効果が、これらのシグナル伝達分子の多くで見られた(模擬感染レーンを参照)。これらの効果には、AKT−1、Raf−1、GSK−3β、およびmTOR自身のキナーゼ活性が増加すること、ならびにPTENおよびp70S6Kのキナーゼ活性が低下することが含まれる。このデータは、これらの経路が、ヒト癌細胞株における粘液腫ウイルスの許容性に関与している可能性を示している。
【0167】
当業者には理解できるように、本明細書に記載した例示的な実施態様に多くの変更を加えることが可能である。それどころか、本発明は、請求項に記載されているように、そのような変更もすべてその範囲に含もうとするものである。
【0168】
本発明のさまざまな実施態様が本明細書に開示されているが、当技術分野における技術常識に従って、多くの適応および変更を本発明の範囲内で行うことができる。そのような変更には、同じ結果を実質的に同じ方法で得るために、本発明の何らかの態様について同等物であることが知られているものと置換することを含む。本明細書で使用される科学技術用語はすべて、別段の記載がない限り、本発明の技術分野における当業者に広く理解されている意味と同じ意味を有する。
【0169】
本明細書で引用されている参考文献はすべて参照されて、全部が組み込まれる。
【特許請求の範囲】
【請求項1】
先天的な抗ウイルス応答を欠損した細胞を阻害するための組成物であって、該細胞に有効量の機能的なM135Rを発現しない粘液腫ウイルスを含む組成物。
【請求項2】
前記細胞がインターフェロンに非応答性である、請求項1記載の組成物。
【請求項3】
前記細胞が異常なインターフェロンシグナル伝達を示す、請求項1記載の組成物。
【請求項4】
前記細胞がヒト癌細胞である、請求項1記載の組成物。
【請求項5】
前記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、請求項1記載の組成物。
【請求項6】
前記細胞が肺癌細胞、黒色腫細胞、卵巣癌細胞、前立腺癌細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、請求項4記載の組成物。
【請求項7】
前記細胞が慢性的にウイルスに感染したヒト細胞である、請求項1記載の組成物。
【請求項8】
先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための、請求項1〜7のいずれか1項記載の組成物であって、有効量の機能的なM135Rを発現しない粘液腫ウイルスを含み、投与に適することを特徴とする、組成物。
【請求項9】
前記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、請求項4または8記載の組成物。
【請求項10】
前記癌の部位への注射による投与に適したものである、請求項8記載の組成物。
【請求項11】
全身投与に適したものである、請求項8記載の組成物。
【請求項12】
機能的なM135Rを発現しない有効量の粘液腫ウイルスの使用。
【請求項13】
先天的な抗ウイルス応答を欠損した細胞を阻害するための医薬の製造のための、請求項12記載の使用。
【請求項14】
前記細胞がインターフェロンに非応答性である、請求項12〜13のいずれか1項記載の使用。
【請求項15】
前記細胞が異常なインターフェロンシグナル伝達を示す、請求項13記載の使用。
【請求項16】
前記細胞が慢性的にウイルスに感染している、請求項13記載の使用。
【請求項17】
前記細胞がヒト癌細胞である、請求項13記載の使用。
【請求項18】
前記細胞が肺癌細胞、黒色腫細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、請求項17記載の使用。
【請求項19】
前記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、請求項12〜18いずれか1項記載の使用。
【請求項20】
患者における病状を治療するための薬剤の製造のための請求項13〜19のうちのいずれか1項記載の使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする、使用。
【請求項21】
前記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、請求項17または20記載の使用。
【請求項22】
機能的なM135Rを発現しない粘液腫ウイルスを含む医薬組成物。
【請求項23】
さらに付加的治療薬を含む、請求項22記載の医薬組成物。
【請求項24】
前記付加的治療薬が化学療法薬である、請求項23記載の医薬組成物。
【請求項1】
先天的な抗ウイルス応答を欠損した細胞を阻害するための組成物であって、該細胞に有効量の機能的なM135Rを発現しない粘液腫ウイルスを含む組成物。
【請求項2】
前記細胞がインターフェロンに非応答性である、請求項1記載の組成物。
【請求項3】
前記細胞が異常なインターフェロンシグナル伝達を示す、請求項1記載の組成物。
【請求項4】
前記細胞がヒト癌細胞である、請求項1記載の組成物。
【請求項5】
前記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、請求項1記載の組成物。
【請求項6】
前記細胞が肺癌細胞、黒色腫細胞、卵巣癌細胞、前立腺癌細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、請求項4記載の組成物。
【請求項7】
前記細胞が慢性的にウイルスに感染したヒト細胞である、請求項1記載の組成物。
【請求項8】
先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする病状を治療するための、請求項1〜7のいずれか1項記載の組成物であって、有効量の機能的なM135Rを発現しない粘液腫ウイルスを含み、投与に適することを特徴とする、組成物。
【請求項9】
前記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、請求項4または8記載の組成物。
【請求項10】
前記癌の部位への注射による投与に適したものである、請求項8記載の組成物。
【請求項11】
全身投与に適したものである、請求項8記載の組成物。
【請求項12】
機能的なM135Rを発現しない有効量の粘液腫ウイルスの使用。
【請求項13】
先天的な抗ウイルス応答を欠損した細胞を阻害するための医薬の製造のための、請求項12記載の使用。
【請求項14】
前記細胞がインターフェロンに非応答性である、請求項12〜13のいずれか1項記載の使用。
【請求項15】
前記細胞が異常なインターフェロンシグナル伝達を示す、請求項13記載の使用。
【請求項16】
前記細胞が慢性的にウイルスに感染している、請求項13記載の使用。
【請求項17】
前記細胞がヒト癌細胞である、請求項13記載の使用。
【請求項18】
前記細胞が肺癌細胞、黒色腫細胞、腎臓癌細胞、神経膠腫細胞、または星状細胞腫細胞である、請求項17記載の使用。
【請求項19】
前記粘液腫ウイルスが、治療用遺伝子を発現するよう遺伝子改変されている、請求項12〜18いずれか1項記載の使用。
【請求項20】
患者における病状を治療するための薬剤の製造のための請求項13〜19のうちのいずれか1項記載の使用であって、該病状は、先天的な抗ウイルス応答を欠損した細胞が存在することを特徴とする、使用。
【請求項21】
前記癌が固形癌、造血細胞癌、結腸癌、肺癌、腎臓癌、膵臓癌、子宮内膜癌、甲状腺癌、口腔癌、卵巣癌、喉頭癌、肝細胞癌、胆管癌、扁平上皮細胞癌、前立腺癌、乳癌、子宮頸癌、結腸直腸癌または黒色腫である、請求項17または20記載の使用。
【請求項22】
機能的なM135Rを発現しない粘液腫ウイルスを含む医薬組成物。
【請求項23】
さらに付加的治療薬を含む、請求項22記載の医薬組成物。
【請求項24】
前記付加的治療薬が化学療法薬である、請求項23記載の医薬組成物。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29−1】


【図29−2】


【図29−3】


【図29−4】


【図29−5】


【図30】


【図31−1】


【図31−2】


【図31−3】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29−1】


【図29−2】


【図29−3】


【図29−4】


【図29−5】


【図30】


【図31−1】


【図31−2】


【図31−3】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【公開番号】特開2012−236860(P2012−236860A)
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【外国語出願】
【出願番号】特願2012−197457(P2012−197457)
【出願日】平成24年9月7日(2012.9.7)
【分割の表示】特願2008−500016(P2008−500016)の分割
【原出願日】平成18年3月6日(2006.3.6)
【出願人】(505310530)ロバーツ リサーチ インスティテュート (6)
【Fターム(参考)】
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願番号】特願2012−197457(P2012−197457)
【出願日】平成24年9月7日(2012.9.7)
【分割の表示】特願2008−500016(P2008−500016)の分割
【原出願日】平成18年3月6日(2006.3.6)
【出願人】(505310530)ロバーツ リサーチ インスティテュート (6)
【Fターム(参考)】
[ Back to top ]

