活性化部分トロンボプラスチン時間測定試薬、活性化部分トロンボプラスチン時間測定方法、及び血液凝固抑制物質の有無の判定方法
【課題】
簡便で正確に、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなくAPTT測定を行うことが可能な、APTT測定試薬、及びそれを用いたAPTT測定方法を提供する。簡便で正確に、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく血液凝固抑制物質の有無を判定する方法を提供する。
【解決手段】
本発明の活性化部分トロンボプラスチン時間測定試薬は、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む。
簡便で正確に、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなくAPTT測定を行うことが可能な、APTT測定試薬、及びそれを用いたAPTT測定方法を提供する。簡便で正確に、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく血液凝固抑制物質の有無を判定する方法を提供する。
【解決手段】
本発明の活性化部分トロンボプラスチン時間測定試薬は、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、活性化部分トロンボプラスチン時間測定試薬、活性化部分トロンボプラスチン時間測定方法、及び血液凝固抑制物質の有無の判定方法に関する。
【背景技術】
【0002】
血液凝固検査の対象となる患者の中には、血栓の治療薬としてヘパリンの投与を受けている患者が存在する。また、点滴を行う際に、カテーテル内の血液凝固反応を防止することを目的として、カテーテル内にヘパリンを用いた生理食塩水を充填するヘパリンロックを施したカテーテルを使用している患者がいる。これらの患者から採取した被検血漿には、外的要因のヘパリンが含まれる場合がある。この被検血漿を使用して、活性化部分トロンボプラスチン時間(APTT)を測定すると、ヘパリンの影響により血液凝固時間が延長してしまう。
【0003】
特許文献1には、被検血漿中に含まれる外的要因のヘパリンによるAPTT測定への影響を除く方法が開示されている。この方法では、被検血漿をヘパリン中和剤で中和してからAPTTを測定することにより、被検血漿に含まれるヘパリンの影響を除去している。しかし、特許文献1に記載の方法では、予め被検血漿中にヘパリン中和剤を添加する必要が有る。そのため、APTT測定の工程が煩雑であった。また、特許文献1に記載の方法では、APTT測定を行う際に、被検血漿にヘパリンが存在する可能性を常に意識する必要があった。特に、医療現場において、緊急にAPTT測定を行う際は、被検血漿中の外的要因のヘパリンの有無を確認せず、APTT測定が行われてしまう場合がある。
【0004】
また、近年、APTT測定試薬を用いるクロスミキシング試験においても、被検血漿中に含まれる外的要因のヘパリンの影響が問題になっている(非特許文献1)。クロスミキシング試験は、被検血漿と正常血漿との混合血漿の血液凝固時間を測定することで、患者の凝固因子欠損や、被検血漿中の血液凝固抑制物質の存在を検査する試験である。上述のように、被検血漿に外的要因のヘパリンが含まれると血液凝固時間が延長してしまう。そのため、クロスミキシング試験においても、被検血漿中に含まれる外的要因のヘパリンが含まれると、内的要因の血液凝固抑制物質の存在が正確に検査できないおそれがある。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特表平5−507297号公報
【非特許文献】
【0006】
【非特許文献1】検査と技術 vol.34 no.8 2006年8月 p.738−739
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、APTT測定試薬を提供することを目的とする。
【0008】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、APTT測定試薬を提供することを目的とする。
【0009】
本発明は、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後にAPTTを測定するために用いられる試薬であって、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、試薬を提供することを目的とする。
【0010】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、APTT測定方法を提供することを目的とする。
【0011】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、血液凝固抑制物質の有無を判定する方法を提供することを目的とする。
【課題を解決するための手段】
【0012】
本発明者らは、APTT測定試薬に予めヘパリン中和剤を含有させることで、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことができることを見出し、本発明を完成させた。
【0013】
本発明の第1の局面の活性化部分トロンボプラスチン時間測定試薬は、ヘパリン中和剤を含む。
本発明の第2の局面の活性化部分トロンボプラスチン時間測定試薬は、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む。
本発明の第3の局面の試薬は、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後に、活性化部分トロンボプラスチン時間を測定するために用いられる試薬であって、ヘパリン中和剤及びカルシウム塩を含有する。
本発明の第4の局面の活性化部分トロンボプラスチン時間測定方法は、被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、第2混合工程で得られた試料の凝固時間を測定する工程と、を含む。
本発明の第5の局面の被検血漿に含まれる血液凝固抑制物質の有無の判定方法は、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する調整工程と、調製工程で得られたそれぞれの測定試料とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、第1混合工程で得られたそれぞれの試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、第2混合工程で得られたそれぞれの試料の凝固時間を測定する工程と、測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する工程と、を含む。
【発明の効果】
【0014】
本発明の第1の局面の活性化部分トロンボプラスチン時間測定試薬によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、APTT測定試薬を提供することができる。
【0015】
本発明の第2の局面の活性化部分トロンボプラスチン時間測定試薬によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、APTT測定試薬を提供することができる。
【0016】
本発明の第3の局面の試薬によれば、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後にAPTTを測定するために用いられる試薬であって、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、試薬を提供することができる。
【0017】
本発明の第4の局面の活性化部分トロンボプラスチン時間測定方法によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、APTT測定方法を提供することができる。
【0018】
本発明の第5の局面の被検血漿に含まれる血液凝固抑制物質の有無の判定方法によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、血液凝固抑制物質の有無を判定する方法を提供することができる。
【図面の簡単な説明】
【0019】
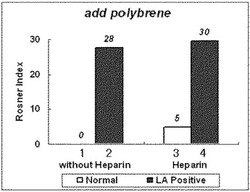
【図1】ポリブレンを含むカルシウム溶液を用いた活性化部分トロンボプラスチン時間(APTT)測定で得られたAPTTから算出したロスナーインデックス値を棒グラフで示している図である。
【図2】ポリブレンを含まないカルシウム溶液を用いた活性化部分トロンボプラスチン時間(APTT)測定で得られたAPTTから算出したロスナーインデックス値を棒グラフで示している図である。
【発明を実施するための形態】
【0020】
本実施形態における活性化部分トロンボプラスチン時間(APTT)測定試薬は、ヘパリン中和剤を含む。APTT測定試薬は、例えば、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む構成であってもよいし、リン脂質及び活性化剤を含む第1試薬と、カルシウム塩を含む第2試薬と、ヘパリン中和剤を含む第3試薬と、を含む構成であってもよい。ここで、第3試薬は、第1試薬の添加後で第2試薬の添加前、に添加されてもよいし、第1試薬と第2試薬を添加した後、に添加されてもよい。
【0021】
なお、本発明者らは、APTT測定試薬において、カルシウム塩を含む試薬にヘパリン中和剤を添加することで、沈殿を生ずることなく、且つ被検血漿中に含まれるヘパリンの影響を受けずに、APTT測定を行うことができることを見出した。そのため、本実施形態では、ヘパリン中和剤を含むAPTT測定試薬の構成としては、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む構成であることが好ましい。
【0022】
本実施形態における活性化部分トロンボプラスチン時間(APTT)測定試薬は、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む。
【0023】
第1試薬中のリン脂質は、APTT測定試薬に一般的に用いることができるリン脂質であれば特に制限されない。例えば、ホスファチジルセリン、ホスファチジルエタノールアミン、ホスファチジルコリン、及びホスファチジルグリセロールなどが挙げられる。また、リン脂質は、ウシ脳由来、ウサギ脳由来、ヒト胎盤由来、大豆由来、及び卵黄由来などの天然のもの、又は合成リン脂質のいずれであってもよい。好ましくは、ウサギ脳由来セファリン、大豆由来セファリン及び合成リン脂質等が挙げられる。
【0024】
第1試薬中のリン脂質の濃度としては、リン脂質の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第1試薬中のリン脂質の濃度として、20〜200μg/mLが挙げられ、50〜150μg/mLが好ましい。リン脂質としてウサギ脳由来セファリン、大豆由来セファリン又は合成リン脂質を用いる場合の、第1試薬中のリン脂質の濃度としては、20〜200μg/mLが好ましく、50〜150μg/mLがより好ましい。
【0025】
第1試薬中の活性化剤は、接触因子系を活性化する物質であれば特に制限されない。例えば、エラグ酸、カオリン、セライト、コロイダルシリカ、及び無水ケイ酸等からなる群より選択される少なくとも1種を用いることができる。本実施形態における好ましい活性化剤としては、エラグ酸、及びコロイダルシリカが挙げられる。
【0026】
第1試薬中の活性化剤の濃度としては、活性化剤の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第1試薬中の活性化剤の濃度としては、5〜1000μg/mLが挙げられ、20〜500μg/mLが好ましい。活性化剤としてエラグ酸を用いる場合の、第1試薬中の活性化剤の濃度としては、5〜100μg/mLが好ましく、20〜50μg/mLがより好ましい。
【0027】
また、第1試薬は、リン脂質及び活性化剤の他に、APTT測定試薬に添加可能な、他の成分をさらに含んでも良い。ここで、他の成分としては、例えば、緩衝剤、防腐剤、及び抗酸化剤などが挙げられる。
【0028】
ここで、緩衝剤は、APTT測定試薬に用いられる公知の緩衝剤であれば、特に制限されない。緩衝剤としては、例えば、HEPES、TRIS、及びMOPSなどが挙げられる。なお、第1試薬のpHは、pHが5〜9が好ましく、より好ましくは6〜8である。この第1試薬のpHを、上記の緩衝剤を用いて調整することができる。
【0029】
また、防腐剤は、APTT測定試薬に用いられる公知の防腐剤であれば、特に制限されない。防腐剤としては、例えば、アジ化ナトリウム、フェノール及び抗生物質(シプロフロキサシン)などが挙げられ、フェノールが好ましい。第1試薬中の防腐剤の濃度は、適宜調整すれば良く、特に制限されないが、例えば、1〜5mg/mLが挙げられる。
【0030】
また、抗酸化剤は、APTT測定試薬に用いられる公知の抗酸化剤であれば、特に制限されない。抗酸化剤としては、例えば、ブチルヒドロキシアニソールなどが挙げられる。
【0031】
本実施形態における、第2試薬中のヘパリン中和剤は、APTT測定に影響を及ぼさない公知のヘパリン中和剤であればよく、特に制限されない。例えば、ポリブレン、硫酸プロタミン、及びヘパリナーゼ等からなる群より選択される少なくとも1種を、ヘパリン中和剤として用いることができる。本実施形態におけるヘパリン中和剤としては、ポリブレンが好ましい。
【0032】
ここで、第2試薬中のヘパリン中和剤の濃度としては、ヘパリン中和剤の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第2試薬中のヘパリン中和剤の濃度としては、0.5〜100μg/mLが挙げられる。ヘパリン中和剤としてポリブレンを用いる場合、第2試薬中のポリブレンの濃度は、5〜50μg/mLが好ましく、10〜20μg/mLがより好ましい。
【0033】
ここで、第2試薬中のカルシウム塩は、APTT測定試薬に一般的に用いることができるカルシウム塩であれば特に制限されない。例えば、無機酸とカルシウムとの塩、及び有機酸とカルシウムの塩のいずれも使用することができる。無機酸とカルシウムとの塩としては、塩化カルシウム、亜硝酸カルシウム、硫酸カルシウム、及び炭酸カルシウム等が挙げられる。有機酸とカルシウムの塩としては、乳酸カルシウム、及び酒石酸カルシウム等が挙げられる。第2試薬中のカルシウム塩としては無機酸とカルシウムとの塩が好ましく、特に塩化カルシウムが好ましい。
【0034】
第2試薬中のカルシウムの濃度としては、カルシウム塩の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第2試薬中のカルシウム塩の濃度として、15〜50mMが挙げられ、20〜30mMが好ましい。カルシウム塩として塩化カルシウムを用いる場合の、第2試薬中のカルシウム塩の濃度としては、15〜30mMが好ましく、20〜25mMがより好ましい。
【0035】
また、第2試薬は、ヘパリン中和剤及びカルシウム塩の他に、APTT測定試薬に添加可能な、他の成分をさらに含んでも良い。ここで、他の成分としては、例えば、緩衝剤、及び防腐剤が挙げられる。
【0036】
ここで、緩衝剤としては、上記第1試薬と同様の緩衝剤を用いることができる。なお、第2試薬のpHは、pHが5〜9が好ましく、より好ましくは6〜8である。この第2試薬のpHも、第1試薬と同様に、上記の緩衝剤を用いて調整することができる。
【0037】
また、防腐剤としては、上記第1試薬と同様の緩衝剤を用いることができる。なお第2試薬中の防腐剤の濃度は、適宜調整すれば良く、特に制限されないが、例えば、1〜5mg/mLが挙げられる。
【0038】
本実施形態における、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後に、活性化部分トロンボプラスチン時間を測定するために用いられる試薬であって、ヘパリン中和剤及びカルシウム塩を含有する試薬は、上記の本実施形態のAPTT測定試薬の第2試薬と同様である。
【0039】
本実施形態における活性化部分トロンボプラスチン時間(APTT)測定方法は、上記の本実施形態のAPTT測定試薬を用いて行われる。すなわち、本実施形態におけるAPTT測定方法は、被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程、第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程、第2混合工程で得られた試料の凝固時間を測定する工程、を含む。
【0040】
第1混合工程は、被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する工程であればよく、被験血漿及び第1試薬との添加の順序は制限されない。
【0041】
ここで、被検血漿は、患者の全血から得られた血液中から血球を取り除いた部分であれば良く、特に制限されない。被検血漿を取得する方法は公知である。例えば、被検血漿を取得する方法として、患者から取得した血液に血液凝固阻止剤を加えて遠心した後、上清を取ることで被検血漿を得る方法が挙げられる。また、被検血漿は上記方法で得たもの以外にも市販の血漿を用いることもできる。市販の血漿としては、正常血漿、血液凝固因子を欠損している血漿、及び血液凝固抑制物質を含有している血漿等が挙げられる。正常血漿としては、コアグトロールN(シスメックス社製)、血液凝固試験用標準ヒト血漿(シスメックス社製)などが挙げられる。血液凝固因子を欠損している血漿としては第VIII因子欠乏血漿(シスメックス社製)、及び第IX因子欠乏血漿(シスメックス社製)などが挙げられる。血液凝固抑制物質を含有している血漿としては、LA陽性血漿(ジョージキング社製)、及びFACTOR VIII DEFICIENT PLASMA WITH INHIBITOR(ジョージキング社製)などが挙げられる。また上記被検血漿はAPTTの測定条件等に応じて適宜希釈して用いてもよい。
【0042】
なお、第1混合工程で用いる第1試薬は、上記の本実施形態のAPTT測定試薬の第1試薬と同様である。
【0043】
第1混合工程における反応温度は、被検血漿と第1試薬との混合割合や被検血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、25℃〜45℃が挙げられ、好ましくは、30℃〜40℃、より好ましくは、35℃〜38℃である。
【0044】
また、第1混合工程における反応時間も、被検血漿と第1試薬との混合割合や被検血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、1分〜15分が挙げられ、好ましくは、2分〜10分、より好ましくは、3分〜5分である。
【0045】
第1混合工程における、被検血漿と第1試薬との混合割合は、被検血漿の希釈割合や第1試薬の組成等に応じて適宜設定すればよく、特に制限されない。例えば、被検血漿と第1試薬との混合割合は容量比で、8:2〜2:8が挙げられ、好ましくは6:4〜4:6、より好ましくは5:5である。
【0046】
第2混合工程は、第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する工程であればよく、第1混合工程で得られた試料及び第2試薬との添加の順序は制限されない。
【0047】
なお、第2混合工程で用いる第2試薬は、上記の本実施形態のAPTT測定試薬の第2試薬と同様である。
【0048】
第2混合工程における反応温度としては、第1混合工程で得られた試料と第2試薬との混合割合や被検血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、20℃〜45℃が挙げられ、好ましくは、30℃〜40℃、より好ましくは、35℃〜38℃である。
【0049】
第2混合工程における、第1混合工程で得られた試料と第2試薬との混合割合は、被検血漿と第1試薬との混合割合や第2試薬の組成等に応じて適宜設定すればよく、特に制限されない。例えば、第1混合工程で得られた試料と第2試薬との混合割合は容量比で、8:2〜5:5が挙げられ、好ましくは7:3〜6:4、より好ましくは2:1である。
【0050】
測定工程は、一般的にAPTT測定で用いられる公知の凝固時間の測定方法により、第2混合工程で得られた試料の凝固時間を測定すればよい。ここで、試料の凝固時間の測定方法としては、例えば、人が目視によりストップウォッチ等を用いて試料が凝固するまでの時間を測定する方法や、光学的情報を測定する装置により試料の凝固時間を測定する方法等が挙げられる。なお、試料の凝固時間を測定するための市販の血液凝固測定装置を用いることもできる。市販の血液凝固測定装置としては、例えば、シスメックス社製のCS−2000i及びCS−2100i等が挙げられる。
【0051】
本実施形態における被検血漿に含まれる血液凝固抑制物質の有無の判定方法は、上記の本実施形態のAPTT測定方法を用いたクロスミキシング試験により行われる。すなわち、本実施形態における判定方法は、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する調整工程、調製工程で得られたそれぞれの測定試料とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程、第1混合工程で得られたそれぞれの試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程、第2混合工程で得られたそれぞれの試料の凝固時間を測定する工程、測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する工程、を含む。
【0052】
調製工程は、一般的なクロスミキシング試験に用いる測定試料を調製する工程であればよい。すなわち、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する工程である。なお、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿との添加の順序は制限されない。
【0053】
ここで、血液凝固抑制物質は、被検血漿に含まれる、ヘパリン以外の血液凝固抑制物質であれば良い。より具体的な血液凝固抑制物質としては、例えば、ループスアンチコアグラント(LA)、後天性血友病、凝固因子インヒビター、及びC1インアクチベーター等が挙げられる。
【0054】
なお、被検血漿は、上記の本実施形態のAPTT測定方法で用いる被検血漿と同様の被検血漿である。
【0055】
ここで、正常血漿は、健常者の全血から得られた血液中から血球を取り除いた部分であれば良く、特に制限されない。正常血漿を取得する方法は公知である。例えば、正常血漿を取得する方法として、健常者から取得した血液に血液凝固阻止剤を加えて遠心した後、上清を取ることで正常血漿を得る方法が挙げられる。また、正常血漿は上記方法で得たもの以外にも市販の正常血漿を用いることもできる。市販の正常血漿としては、コアグトロールN(シスメックス社製)、血液凝固試験用標準ヒト血漿(シスメックス社製)などが挙げられる。また上記正常血漿はAPTTの測定条件等に応じて適宜希釈して用いてもよい。
【0056】
ここで、調製工程で調製される、被検血漿と正常血漿との混合割合が異なる測定試料の数としては、3つ以上であればよく、特に制限されない。なお、測定試料の数を増やすことで、本実施形態の判定方法の精度を向上させることができる。本実施形態における測定試料の数としては、3〜6が挙げられる。
【0057】
また、調製工程で調製される測定試料における、被検血漿と正常血漿との混合割合は、一般的なクロスミキシング試験に用いられる測定試料の被検血漿と正常血漿の混合割合であればよい。すなわち、混合割合としては、被検血漿:正常血漿が0:10〜10:0の容量比が挙げられる。つまり、調製工程における、被検血漿と正常血漿との混合には、被検血漿又は正常血漿の混合割合が0の混合も含まれる。例えば、調製工程で調製される被検血漿と正常血漿との混合割合が異なる測定試料の数が3つの場合、被検血漿と正常血漿とを10:0、1:1、及び0:10の3つの異なる容量比で混合することができる。
【0058】
調製工程における反応温度としては、判定対象である血液凝固抑制物質の種類、被検血漿の希釈割合、及び正常血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、25℃〜45℃が挙げられ、好ましくは、30℃〜40℃、より好ましくは、35℃〜38℃である。
【0059】
また、調製工程における反応時間は、判定対象である血液凝固抑制物質の種類、被検血漿の希釈割合、及び正常血漿の希釈割合等に応じて、適宜設定すればよい。例えば、被検血漿中の判定したい血液凝固物質がループスアンチコアグラント(LA)等の即時的に血液凝固反応を阻害する物質の場合、調製工程における反応時間としては1分〜15分が挙げられ、好ましくは1分〜5分、より好ましくは1分である。また、被検血漿中の判定したい血液凝固物質が後天性血友病等の比較的緩やかに血液凝固反応を阻害する物質の場合は、調製工程における反応時間としては0.2時間〜5時間が挙げられ、好ましくは0.5時間〜4時間、より好ましくは1時間〜3時間である。
【0060】
なお、本実施形態の被検血漿に含まれる血液凝固抑制物質の有無の判定方法において、第1混合工程、第2混合工程、及び測定工程は、調製工程で調製された測定試料に対し、それぞれ上記の本実施形態のAPTT測定方法の第1混合工程、第2混合工程、及び測定工程と同様の処理を行う。
【0061】
判定工程は、クロスミキシング試験において、測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する、公知の方法を用いればよく、特に制限されない。例えば、混合比及び凝固時間のグラフの形状や、ロスナーインデックス値を用いた判定方法等が挙げられる。より具体的には、混合比及び凝固時間のグラフの形状を用いた判定方法の場合、被検血漿と正常血漿との混合比を横軸にし、試料の凝固時間を縦軸にしたグラフを作成し、グラフの形が凹型であれば血液凝固抑制物質が有ると判定し、凹型でなければ血液凝固抑制物質が無いと判定することができる。また、ロスナーインデックス値を用いた判定方法の場合、ロスナーインデックス値に閾値を設定しておき、試料の凝固時間から算出されたロスナーインデックス値が閾値より高い場合、血液凝固抑制物質が有ると判定し、試料の凝固時間から算出されたロスナーインデックス値が閾値より低い場合、血液凝固抑制物質が無いと判定することができる。
【0062】
なお、ロスナーインデックス値とは、下記の式(1)より算出される値である。
ロスナーインデックス値=((被検血漿と正常血漿との混合割合が1:1の試料のAPTT)−(正常血漿のAPTT))/(被検血漿のAPTT) ×100・・・式(1)
【0063】
以下、実施例を挙げて本発明を詳細に説明するが、本発明はこれらに限定されるものではない。
【実施例】
【0064】
<実験例1>
[APTT測定試薬へのポリブレンの添加]
(試薬1)
トロンボチェックAPTT−SLA(シスメックス社製)のリン脂質及び活性化剤を含む試薬3mLに、10mg/mLのポリブレン溶液(10mg ポリブレン(ナカライテスク社製)、1mL 精製水)を3μL添加し、試薬1を調整した。
(試薬2)
アクチンFSL(シスメックス社製)3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬2を調整した。
(試薬3)
ヒーモスアイエルAPTT−SP(三菱化学メディエンス社製)のリン脂質及び活性化剤を含む試薬3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬3を調整した。
(試薬4)
ヒーモスアイエルシンサシルAPTT(三菱化学メディエンス社製)のリン脂質及び活性化剤を含む試薬3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬4を調整した。
(試薬5)
25mMのカルシウム溶液(278mg 塩化カルシウム、100mL 精製水)3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬5を調整した。
【0065】
なお、トロンボチェックAPTT−SLA、アクチンFSL、ヒーモスアイエルAPTT−SP、及びヒーモスアイエルシンサシルAPTTの、それぞれのリン脂質及び活性化剤の種類を表1に示す。
【0066】
【表1】

【0067】
[APTT測定試薬へのポリブレンの添加の影響の観察]
試薬1〜5の、6時間経過後の沈殿の有無を、目視により観察した。観察結果を表2に示す。
【0068】
【表2】

+:沈殿あり
−:沈殿なし
【0069】
表2から明らかなように、APTT測定試薬のリン脂質及び活性化剤を含む試薬は、リン脂質の種類や活性化剤の種類に係わらず、ポリブレンの添加により沈殿が生じることが分かる。一方、APTT測定試薬のカルシウム溶液は、ポリブレンを添加しても、沈殿が生じないことが明らかとなった。
【0070】
<実験例2>
[測定試料の調整]
(測定試料1)
コアグトロールN(シスメックス社製)を、37℃で1分間加温して、測定試料1とした。
(測定試料2)
ジョージキング社製のループスアンチコアグラント(LA)陽性血漿を、37℃で1分間加温して、測定試料2とした。
(測定試料3)
正常血漿として、コアグトロールNを用いた。また、被検血漿として、ジョージキング社製のLA陽性血漿を用いた。そして、正常血漿と、被検血漿とを、1:1で混合し、37℃で2分間加温して、測定試料3を調製した。
(測定試料4)
コアグトロールNにノボ・ヘパリン注(ノボノルディスクA/S社製)を0.5U/mLとなるように添加したものを、37℃で2分間加温して、測定試料4とした。
(測定試料5)
正常血漿として、コアグトロールNを用いた。被検血漿として、コアグトロールNにノボ・ヘパリン注(ノボノルディスクA/S社製)を0.5U/mLとなるように添加したものを用いた。そして、正常血漿と、被検血漿とを、1:1で混合し、37℃で2分間加温して、測定試料5を調製した。
(測定試料6)
ジョージキング社製のLA陽性血漿にノボ・ヘパリン注(ノボノルディスクA/S社製)を0.5U/mLとなるように添加したものを、37℃で2分間加温して、測定試料6とした。
(測定試料7)
正常血漿として、コアグトロールNを用いた。また、被検血漿として、ジョージキング社製のLA陽性血漿にノボ・ヘパリン注を0.5U/mLとなるように添加したものを用いた。そして、正常血漿と、被検血漿とを、1:1で混合し、37℃で2分間加温して、測定試料7を調製した。
【0071】
[APTT測定]
50μLの測定試料1をキュベットに分注した。次いで、50μLのトロンボチェックAPTT−SLAのリン脂質及び活性化剤を含む試薬を、キュベットに添加し、37℃で3分間加温した。その後、ポリブレンを含むカルシウム溶液である上記の試薬5を50μL添加し、試料が凝固するまでの時間を全自動血液凝固測定装置CS−2000i(シスメックス社製)で測定し、測定値1を得た。
【0072】
測定試料1に代えて、測定試料2、測定試料3、測定試料4、測定試料5、測定試料6、又は測定試料7を用いた以外、測定試料1のAPTT測定と同様の操作により、測定試料2〜7の凝固時間を測定し、それぞれ測定値2〜7を得た。
【0073】
[ロスナーインデックス値によるクロスミキシング試験の解析]
測定試料1〜7の凝固時間の測定値(APTT)を用い算出したロスナーインデックス値によるクロスミキシング試験の解析結果を図1に示す。ここで、ロスナーインデックス値は上述の式(1)を用いて算出した。なお、式(1)中、正常血漿のAPTTとして、測定値1を用いた。具体的な算出式を式(2)に示す。
ロスナーインデックス値=((混合血漿の測定値)−(測定値1))/(被検血漿の測定値) ×100・・・式(2)
【0074】
図1における、棒グラフ1及び棒グラフ2は、ヘパリンを含まない血漿を用いた際の、ロスナーインデックス値を示す。ここで、棒グラフ1は、式(2)において、(被検血漿の測定値)及び(混合血漿の測定値)として、測定値1を代入した際の、ロスナーインデックス値を示す。棒グラフ2は、(被検血漿の測定値)として測定値2、(混合血漿の測定値)として測定値3を代入した際の、ロスナーインデックス値を示す。
【0075】
図1における、棒グラフ3及び棒グラフ4は、ヘパリンを含む血漿を用いた際の、ロスナーインデックス値を示す。ここで、棒グラフ3は、式(2)において、(被検血漿の測定値)として測定値4、(混合血漿の測定値)として測定値5を代入した際の、ロスナーインデックス値を示す。棒グラフ4は、(被検血漿の測定値)として測定値6、(混合血漿の測定値)として測定値7を代入した際の、ロスナーインデックス値を示す。
【0076】
<実験例3>
実験例2のポリブレンを含むカルシウム溶液である試薬5に代えて、ポリブレンを含まない25mM カルシウム溶液(278mg 塩化カルシウム、100mL 精製水)を用いた以外、実験例2と同様の操作で、APTT測定及びロスナーインデックス値によるクロスミキシング試験の解析を行った。クロスミキシング試験の解析結果を図2に示す。なお、図2における、棒グラフ1〜4は、上記図1の棒グラフ1〜4と同じく、棒グラフ1及び棒グラフ2は、ヘパリンを含まない血漿を用いた際のロスナーインデックス値を示し、棒グラフ3及び棒グラフ4は、ヘパリンを含む血漿を用いた際のロスナーインデックス値を示す。
【0077】
図1及び図2の棒グラフ1及び2から、ポリブレンを含むカルシウム溶液を用いたAPTT測定でも、ポリブレンを含まないカルシウム溶液を用いたAPTT測定と同様のロスナーインデックス値が得られることが明らかになった。このことから、カルシウム溶液へのポリブレンの添加は、APTT測定に影響を与えないことが示唆された。
【0078】
また、図2の棒グラフ3及び棒グラフ4から明らかなように、ポリブレンを含まないカルシウム溶液を用い、外因性のヘパリンを含む血漿のAPTT測定を行った場合、正常血漿とLA陽性血漿のロスナーインデックス値の差が無くなり、LAが陽性か陰性かの判断が困難になることが分かる。一方、図1の棒グラフ3及び棒グラフ4から明らかなように、ポリブレンを含むカルシウム溶液を用いた場合、外因性のヘパリンの影響が軽減され、外因性のヘパリンを含む血漿であっても、LAが陽性か陰性かの判断が可能であることが分かる。
【0079】
上述の結果から、ポリブレンを含むカルシウム溶液を用いても、APTT測定自体に影響を及ぼすことがないことが分かった。また、ポリブレンを含むカルシウム溶液を用いることで、外因性のヘパリンを含む血漿であっても、正確にAPTT測定を行うことが可能となることが分かった。
【技術分野】
【0001】
本発明は、活性化部分トロンボプラスチン時間測定試薬、活性化部分トロンボプラスチン時間測定方法、及び血液凝固抑制物質の有無の判定方法に関する。
【背景技術】
【0002】
血液凝固検査の対象となる患者の中には、血栓の治療薬としてヘパリンの投与を受けている患者が存在する。また、点滴を行う際に、カテーテル内の血液凝固反応を防止することを目的として、カテーテル内にヘパリンを用いた生理食塩水を充填するヘパリンロックを施したカテーテルを使用している患者がいる。これらの患者から採取した被検血漿には、外的要因のヘパリンが含まれる場合がある。この被検血漿を使用して、活性化部分トロンボプラスチン時間(APTT)を測定すると、ヘパリンの影響により血液凝固時間が延長してしまう。
【0003】
特許文献1には、被検血漿中に含まれる外的要因のヘパリンによるAPTT測定への影響を除く方法が開示されている。この方法では、被検血漿をヘパリン中和剤で中和してからAPTTを測定することにより、被検血漿に含まれるヘパリンの影響を除去している。しかし、特許文献1に記載の方法では、予め被検血漿中にヘパリン中和剤を添加する必要が有る。そのため、APTT測定の工程が煩雑であった。また、特許文献1に記載の方法では、APTT測定を行う際に、被検血漿にヘパリンが存在する可能性を常に意識する必要があった。特に、医療現場において、緊急にAPTT測定を行う際は、被検血漿中の外的要因のヘパリンの有無を確認せず、APTT測定が行われてしまう場合がある。
【0004】
また、近年、APTT測定試薬を用いるクロスミキシング試験においても、被検血漿中に含まれる外的要因のヘパリンの影響が問題になっている(非特許文献1)。クロスミキシング試験は、被検血漿と正常血漿との混合血漿の血液凝固時間を測定することで、患者の凝固因子欠損や、被検血漿中の血液凝固抑制物質の存在を検査する試験である。上述のように、被検血漿に外的要因のヘパリンが含まれると血液凝固時間が延長してしまう。そのため、クロスミキシング試験においても、被検血漿中に含まれる外的要因のヘパリンが含まれると、内的要因の血液凝固抑制物質の存在が正確に検査できないおそれがある。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特表平5−507297号公報
【非特許文献】
【0006】
【非特許文献1】検査と技術 vol.34 no.8 2006年8月 p.738−739
【発明の概要】
【発明が解決しようとする課題】
【0007】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、APTT測定試薬を提供することを目的とする。
【0008】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、APTT測定試薬を提供することを目的とする。
【0009】
本発明は、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後にAPTTを測定するために用いられる試薬であって、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、試薬を提供することを目的とする。
【0010】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、APTT測定方法を提供することを目的とする。
【0011】
本発明は、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、血液凝固抑制物質の有無を判定する方法を提供することを目的とする。
【課題を解決するための手段】
【0012】
本発明者らは、APTT測定試薬に予めヘパリン中和剤を含有させることで、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことができることを見出し、本発明を完成させた。
【0013】
本発明の第1の局面の活性化部分トロンボプラスチン時間測定試薬は、ヘパリン中和剤を含む。
本発明の第2の局面の活性化部分トロンボプラスチン時間測定試薬は、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む。
本発明の第3の局面の試薬は、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後に、活性化部分トロンボプラスチン時間を測定するために用いられる試薬であって、ヘパリン中和剤及びカルシウム塩を含有する。
本発明の第4の局面の活性化部分トロンボプラスチン時間測定方法は、被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、第2混合工程で得られた試料の凝固時間を測定する工程と、を含む。
本発明の第5の局面の被検血漿に含まれる血液凝固抑制物質の有無の判定方法は、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する調整工程と、調製工程で得られたそれぞれの測定試料とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、第1混合工程で得られたそれぞれの試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、第2混合工程で得られたそれぞれの試料の凝固時間を測定する工程と、測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する工程と、を含む。
【発明の効果】
【0014】
本発明の第1の局面の活性化部分トロンボプラスチン時間測定試薬によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、APTT測定試薬を提供することができる。
【0015】
本発明の第2の局面の活性化部分トロンボプラスチン時間測定試薬によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、APTT測定試薬を提供することができる。
【0016】
本発明の第3の局面の試薬によれば、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後にAPTTを測定するために用いられる試薬であって、被検血漿中に含まれる外的要因のヘパリンの影響を受けることなく、簡便で、正確にAPTT測定を行うことが可能な、安定性の高い、試薬を提供することができる。
【0017】
本発明の第4の局面の活性化部分トロンボプラスチン時間測定方法によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、APTT測定方法を提供することができる。
【0018】
本発明の第5の局面の被検血漿に含まれる血液凝固抑制物質の有無の判定方法によれば、被検血漿中に含まれる外的要因のヘパリンの影響を受けることがなく、簡便で、正確であり、かつ、試薬の安定性が高い、血液凝固抑制物質の有無を判定する方法を提供することができる。
【図面の簡単な説明】
【0019】
【図1】ポリブレンを含むカルシウム溶液を用いた活性化部分トロンボプラスチン時間(APTT)測定で得られたAPTTから算出したロスナーインデックス値を棒グラフで示している図である。
【図2】ポリブレンを含まないカルシウム溶液を用いた活性化部分トロンボプラスチン時間(APTT)測定で得られたAPTTから算出したロスナーインデックス値を棒グラフで示している図である。
【発明を実施するための形態】
【0020】
本実施形態における活性化部分トロンボプラスチン時間(APTT)測定試薬は、ヘパリン中和剤を含む。APTT測定試薬は、例えば、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む構成であってもよいし、リン脂質及び活性化剤を含む第1試薬と、カルシウム塩を含む第2試薬と、ヘパリン中和剤を含む第3試薬と、を含む構成であってもよい。ここで、第3試薬は、第1試薬の添加後で第2試薬の添加前、に添加されてもよいし、第1試薬と第2試薬を添加した後、に添加されてもよい。
【0021】
なお、本発明者らは、APTT測定試薬において、カルシウム塩を含む試薬にヘパリン中和剤を添加することで、沈殿を生ずることなく、且つ被検血漿中に含まれるヘパリンの影響を受けずに、APTT測定を行うことができることを見出した。そのため、本実施形態では、ヘパリン中和剤を含むAPTT測定試薬の構成としては、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む構成であることが好ましい。
【0022】
本実施形態における活性化部分トロンボプラスチン時間(APTT)測定試薬は、リン脂質及び活性化剤を含む第1試薬と、ヘパリン中和剤及びカルシウム塩を含む第2試薬と、を含む。
【0023】
第1試薬中のリン脂質は、APTT測定試薬に一般的に用いることができるリン脂質であれば特に制限されない。例えば、ホスファチジルセリン、ホスファチジルエタノールアミン、ホスファチジルコリン、及びホスファチジルグリセロールなどが挙げられる。また、リン脂質は、ウシ脳由来、ウサギ脳由来、ヒト胎盤由来、大豆由来、及び卵黄由来などの天然のもの、又は合成リン脂質のいずれであってもよい。好ましくは、ウサギ脳由来セファリン、大豆由来セファリン及び合成リン脂質等が挙げられる。
【0024】
第1試薬中のリン脂質の濃度としては、リン脂質の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第1試薬中のリン脂質の濃度として、20〜200μg/mLが挙げられ、50〜150μg/mLが好ましい。リン脂質としてウサギ脳由来セファリン、大豆由来セファリン又は合成リン脂質を用いる場合の、第1試薬中のリン脂質の濃度としては、20〜200μg/mLが好ましく、50〜150μg/mLがより好ましい。
【0025】
第1試薬中の活性化剤は、接触因子系を活性化する物質であれば特に制限されない。例えば、エラグ酸、カオリン、セライト、コロイダルシリカ、及び無水ケイ酸等からなる群より選択される少なくとも1種を用いることができる。本実施形態における好ましい活性化剤としては、エラグ酸、及びコロイダルシリカが挙げられる。
【0026】
第1試薬中の活性化剤の濃度としては、活性化剤の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第1試薬中の活性化剤の濃度としては、5〜1000μg/mLが挙げられ、20〜500μg/mLが好ましい。活性化剤としてエラグ酸を用いる場合の、第1試薬中の活性化剤の濃度としては、5〜100μg/mLが好ましく、20〜50μg/mLがより好ましい。
【0027】
また、第1試薬は、リン脂質及び活性化剤の他に、APTT測定試薬に添加可能な、他の成分をさらに含んでも良い。ここで、他の成分としては、例えば、緩衝剤、防腐剤、及び抗酸化剤などが挙げられる。
【0028】
ここで、緩衝剤は、APTT測定試薬に用いられる公知の緩衝剤であれば、特に制限されない。緩衝剤としては、例えば、HEPES、TRIS、及びMOPSなどが挙げられる。なお、第1試薬のpHは、pHが5〜9が好ましく、より好ましくは6〜8である。この第1試薬のpHを、上記の緩衝剤を用いて調整することができる。
【0029】
また、防腐剤は、APTT測定試薬に用いられる公知の防腐剤であれば、特に制限されない。防腐剤としては、例えば、アジ化ナトリウム、フェノール及び抗生物質(シプロフロキサシン)などが挙げられ、フェノールが好ましい。第1試薬中の防腐剤の濃度は、適宜調整すれば良く、特に制限されないが、例えば、1〜5mg/mLが挙げられる。
【0030】
また、抗酸化剤は、APTT測定試薬に用いられる公知の抗酸化剤であれば、特に制限されない。抗酸化剤としては、例えば、ブチルヒドロキシアニソールなどが挙げられる。
【0031】
本実施形態における、第2試薬中のヘパリン中和剤は、APTT測定に影響を及ぼさない公知のヘパリン中和剤であればよく、特に制限されない。例えば、ポリブレン、硫酸プロタミン、及びヘパリナーゼ等からなる群より選択される少なくとも1種を、ヘパリン中和剤として用いることができる。本実施形態におけるヘパリン中和剤としては、ポリブレンが好ましい。
【0032】
ここで、第2試薬中のヘパリン中和剤の濃度としては、ヘパリン中和剤の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第2試薬中のヘパリン中和剤の濃度としては、0.5〜100μg/mLが挙げられる。ヘパリン中和剤としてポリブレンを用いる場合、第2試薬中のポリブレンの濃度は、5〜50μg/mLが好ましく、10〜20μg/mLがより好ましい。
【0033】
ここで、第2試薬中のカルシウム塩は、APTT測定試薬に一般的に用いることができるカルシウム塩であれば特に制限されない。例えば、無機酸とカルシウムとの塩、及び有機酸とカルシウムの塩のいずれも使用することができる。無機酸とカルシウムとの塩としては、塩化カルシウム、亜硝酸カルシウム、硫酸カルシウム、及び炭酸カルシウム等が挙げられる。有機酸とカルシウムの塩としては、乳酸カルシウム、及び酒石酸カルシウム等が挙げられる。第2試薬中のカルシウム塩としては無機酸とカルシウムとの塩が好ましく、特に塩化カルシウムが好ましい。
【0034】
第2試薬中のカルシウムの濃度としては、カルシウム塩の種類やAPTTの測定条件等に応じて、適宜設定すればよく、特に制限されない。例えば、第2試薬中のカルシウム塩の濃度として、15〜50mMが挙げられ、20〜30mMが好ましい。カルシウム塩として塩化カルシウムを用いる場合の、第2試薬中のカルシウム塩の濃度としては、15〜30mMが好ましく、20〜25mMがより好ましい。
【0035】
また、第2試薬は、ヘパリン中和剤及びカルシウム塩の他に、APTT測定試薬に添加可能な、他の成分をさらに含んでも良い。ここで、他の成分としては、例えば、緩衝剤、及び防腐剤が挙げられる。
【0036】
ここで、緩衝剤としては、上記第1試薬と同様の緩衝剤を用いることができる。なお、第2試薬のpHは、pHが5〜9が好ましく、より好ましくは6〜8である。この第2試薬のpHも、第1試薬と同様に、上記の緩衝剤を用いて調整することができる。
【0037】
また、防腐剤としては、上記第1試薬と同様の緩衝剤を用いることができる。なお第2試薬中の防腐剤の濃度は、適宜調整すれば良く、特に制限されないが、例えば、1〜5mg/mLが挙げられる。
【0038】
本実施形態における、被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後に、活性化部分トロンボプラスチン時間を測定するために用いられる試薬であって、ヘパリン中和剤及びカルシウム塩を含有する試薬は、上記の本実施形態のAPTT測定試薬の第2試薬と同様である。
【0039】
本実施形態における活性化部分トロンボプラスチン時間(APTT)測定方法は、上記の本実施形態のAPTT測定試薬を用いて行われる。すなわち、本実施形態におけるAPTT測定方法は、被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程、第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程、第2混合工程で得られた試料の凝固時間を測定する工程、を含む。
【0040】
第1混合工程は、被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する工程であればよく、被験血漿及び第1試薬との添加の順序は制限されない。
【0041】
ここで、被検血漿は、患者の全血から得られた血液中から血球を取り除いた部分であれば良く、特に制限されない。被検血漿を取得する方法は公知である。例えば、被検血漿を取得する方法として、患者から取得した血液に血液凝固阻止剤を加えて遠心した後、上清を取ることで被検血漿を得る方法が挙げられる。また、被検血漿は上記方法で得たもの以外にも市販の血漿を用いることもできる。市販の血漿としては、正常血漿、血液凝固因子を欠損している血漿、及び血液凝固抑制物質を含有している血漿等が挙げられる。正常血漿としては、コアグトロールN(シスメックス社製)、血液凝固試験用標準ヒト血漿(シスメックス社製)などが挙げられる。血液凝固因子を欠損している血漿としては第VIII因子欠乏血漿(シスメックス社製)、及び第IX因子欠乏血漿(シスメックス社製)などが挙げられる。血液凝固抑制物質を含有している血漿としては、LA陽性血漿(ジョージキング社製)、及びFACTOR VIII DEFICIENT PLASMA WITH INHIBITOR(ジョージキング社製)などが挙げられる。また上記被検血漿はAPTTの測定条件等に応じて適宜希釈して用いてもよい。
【0042】
なお、第1混合工程で用いる第1試薬は、上記の本実施形態のAPTT測定試薬の第1試薬と同様である。
【0043】
第1混合工程における反応温度は、被検血漿と第1試薬との混合割合や被検血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、25℃〜45℃が挙げられ、好ましくは、30℃〜40℃、より好ましくは、35℃〜38℃である。
【0044】
また、第1混合工程における反応時間も、被検血漿と第1試薬との混合割合や被検血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、1分〜15分が挙げられ、好ましくは、2分〜10分、より好ましくは、3分〜5分である。
【0045】
第1混合工程における、被検血漿と第1試薬との混合割合は、被検血漿の希釈割合や第1試薬の組成等に応じて適宜設定すればよく、特に制限されない。例えば、被検血漿と第1試薬との混合割合は容量比で、8:2〜2:8が挙げられ、好ましくは6:4〜4:6、より好ましくは5:5である。
【0046】
第2混合工程は、第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する工程であればよく、第1混合工程で得られた試料及び第2試薬との添加の順序は制限されない。
【0047】
なお、第2混合工程で用いる第2試薬は、上記の本実施形態のAPTT測定試薬の第2試薬と同様である。
【0048】
第2混合工程における反応温度としては、第1混合工程で得られた試料と第2試薬との混合割合や被検血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、20℃〜45℃が挙げられ、好ましくは、30℃〜40℃、より好ましくは、35℃〜38℃である。
【0049】
第2混合工程における、第1混合工程で得られた試料と第2試薬との混合割合は、被検血漿と第1試薬との混合割合や第2試薬の組成等に応じて適宜設定すればよく、特に制限されない。例えば、第1混合工程で得られた試料と第2試薬との混合割合は容量比で、8:2〜5:5が挙げられ、好ましくは7:3〜6:4、より好ましくは2:1である。
【0050】
測定工程は、一般的にAPTT測定で用いられる公知の凝固時間の測定方法により、第2混合工程で得られた試料の凝固時間を測定すればよい。ここで、試料の凝固時間の測定方法としては、例えば、人が目視によりストップウォッチ等を用いて試料が凝固するまでの時間を測定する方法や、光学的情報を測定する装置により試料の凝固時間を測定する方法等が挙げられる。なお、試料の凝固時間を測定するための市販の血液凝固測定装置を用いることもできる。市販の血液凝固測定装置としては、例えば、シスメックス社製のCS−2000i及びCS−2100i等が挙げられる。
【0051】
本実施形態における被検血漿に含まれる血液凝固抑制物質の有無の判定方法は、上記の本実施形態のAPTT測定方法を用いたクロスミキシング試験により行われる。すなわち、本実施形態における判定方法は、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する調整工程、調製工程で得られたそれぞれの測定試料とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程、第1混合工程で得られたそれぞれの試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程、第2混合工程で得られたそれぞれの試料の凝固時間を測定する工程、測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する工程、を含む。
【0052】
調製工程は、一般的なクロスミキシング試験に用いる測定試料を調製する工程であればよい。すなわち、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する工程である。なお、血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿との添加の順序は制限されない。
【0053】
ここで、血液凝固抑制物質は、被検血漿に含まれる、ヘパリン以外の血液凝固抑制物質であれば良い。より具体的な血液凝固抑制物質としては、例えば、ループスアンチコアグラント(LA)、後天性血友病、凝固因子インヒビター、及びC1インアクチベーター等が挙げられる。
【0054】
なお、被検血漿は、上記の本実施形態のAPTT測定方法で用いる被検血漿と同様の被検血漿である。
【0055】
ここで、正常血漿は、健常者の全血から得られた血液中から血球を取り除いた部分であれば良く、特に制限されない。正常血漿を取得する方法は公知である。例えば、正常血漿を取得する方法として、健常者から取得した血液に血液凝固阻止剤を加えて遠心した後、上清を取ることで正常血漿を得る方法が挙げられる。また、正常血漿は上記方法で得たもの以外にも市販の正常血漿を用いることもできる。市販の正常血漿としては、コアグトロールN(シスメックス社製)、血液凝固試験用標準ヒト血漿(シスメックス社製)などが挙げられる。また上記正常血漿はAPTTの測定条件等に応じて適宜希釈して用いてもよい。
【0056】
ここで、調製工程で調製される、被検血漿と正常血漿との混合割合が異なる測定試料の数としては、3つ以上であればよく、特に制限されない。なお、測定試料の数を増やすことで、本実施形態の判定方法の精度を向上させることができる。本実施形態における測定試料の数としては、3〜6が挙げられる。
【0057】
また、調製工程で調製される測定試料における、被検血漿と正常血漿との混合割合は、一般的なクロスミキシング試験に用いられる測定試料の被検血漿と正常血漿の混合割合であればよい。すなわち、混合割合としては、被検血漿:正常血漿が0:10〜10:0の容量比が挙げられる。つまり、調製工程における、被検血漿と正常血漿との混合には、被検血漿又は正常血漿の混合割合が0の混合も含まれる。例えば、調製工程で調製される被検血漿と正常血漿との混合割合が異なる測定試料の数が3つの場合、被検血漿と正常血漿とを10:0、1:1、及び0:10の3つの異なる容量比で混合することができる。
【0058】
調製工程における反応温度としては、判定対象である血液凝固抑制物質の種類、被検血漿の希釈割合、及び正常血漿の希釈割合等に応じて、適宜設定すればよく、特に制限されないが、例えば、25℃〜45℃が挙げられ、好ましくは、30℃〜40℃、より好ましくは、35℃〜38℃である。
【0059】
また、調製工程における反応時間は、判定対象である血液凝固抑制物質の種類、被検血漿の希釈割合、及び正常血漿の希釈割合等に応じて、適宜設定すればよい。例えば、被検血漿中の判定したい血液凝固物質がループスアンチコアグラント(LA)等の即時的に血液凝固反応を阻害する物質の場合、調製工程における反応時間としては1分〜15分が挙げられ、好ましくは1分〜5分、より好ましくは1分である。また、被検血漿中の判定したい血液凝固物質が後天性血友病等の比較的緩やかに血液凝固反応を阻害する物質の場合は、調製工程における反応時間としては0.2時間〜5時間が挙げられ、好ましくは0.5時間〜4時間、より好ましくは1時間〜3時間である。
【0060】
なお、本実施形態の被検血漿に含まれる血液凝固抑制物質の有無の判定方法において、第1混合工程、第2混合工程、及び測定工程は、調製工程で調製された測定試料に対し、それぞれ上記の本実施形態のAPTT測定方法の第1混合工程、第2混合工程、及び測定工程と同様の処理を行う。
【0061】
判定工程は、クロスミキシング試験において、測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する、公知の方法を用いればよく、特に制限されない。例えば、混合比及び凝固時間のグラフの形状や、ロスナーインデックス値を用いた判定方法等が挙げられる。より具体的には、混合比及び凝固時間のグラフの形状を用いた判定方法の場合、被検血漿と正常血漿との混合比を横軸にし、試料の凝固時間を縦軸にしたグラフを作成し、グラフの形が凹型であれば血液凝固抑制物質が有ると判定し、凹型でなければ血液凝固抑制物質が無いと判定することができる。また、ロスナーインデックス値を用いた判定方法の場合、ロスナーインデックス値に閾値を設定しておき、試料の凝固時間から算出されたロスナーインデックス値が閾値より高い場合、血液凝固抑制物質が有ると判定し、試料の凝固時間から算出されたロスナーインデックス値が閾値より低い場合、血液凝固抑制物質が無いと判定することができる。
【0062】
なお、ロスナーインデックス値とは、下記の式(1)より算出される値である。
ロスナーインデックス値=((被検血漿と正常血漿との混合割合が1:1の試料のAPTT)−(正常血漿のAPTT))/(被検血漿のAPTT) ×100・・・式(1)
【0063】
以下、実施例を挙げて本発明を詳細に説明するが、本発明はこれらに限定されるものではない。
【実施例】
【0064】
<実験例1>
[APTT測定試薬へのポリブレンの添加]
(試薬1)
トロンボチェックAPTT−SLA(シスメックス社製)のリン脂質及び活性化剤を含む試薬3mLに、10mg/mLのポリブレン溶液(10mg ポリブレン(ナカライテスク社製)、1mL 精製水)を3μL添加し、試薬1を調整した。
(試薬2)
アクチンFSL(シスメックス社製)3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬2を調整した。
(試薬3)
ヒーモスアイエルAPTT−SP(三菱化学メディエンス社製)のリン脂質及び活性化剤を含む試薬3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬3を調整した。
(試薬4)
ヒーモスアイエルシンサシルAPTT(三菱化学メディエンス社製)のリン脂質及び活性化剤を含む試薬3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬4を調整した。
(試薬5)
25mMのカルシウム溶液(278mg 塩化カルシウム、100mL 精製水)3mLに、10mg/mLのポリブレン溶液を3μL添加し、試薬5を調整した。
【0065】
なお、トロンボチェックAPTT−SLA、アクチンFSL、ヒーモスアイエルAPTT−SP、及びヒーモスアイエルシンサシルAPTTの、それぞれのリン脂質及び活性化剤の種類を表1に示す。
【0066】
【表1】

【0067】
[APTT測定試薬へのポリブレンの添加の影響の観察]
試薬1〜5の、6時間経過後の沈殿の有無を、目視により観察した。観察結果を表2に示す。
【0068】
【表2】

+:沈殿あり
−:沈殿なし
【0069】
表2から明らかなように、APTT測定試薬のリン脂質及び活性化剤を含む試薬は、リン脂質の種類や活性化剤の種類に係わらず、ポリブレンの添加により沈殿が生じることが分かる。一方、APTT測定試薬のカルシウム溶液は、ポリブレンを添加しても、沈殿が生じないことが明らかとなった。
【0070】
<実験例2>
[測定試料の調整]
(測定試料1)
コアグトロールN(シスメックス社製)を、37℃で1分間加温して、測定試料1とした。
(測定試料2)
ジョージキング社製のループスアンチコアグラント(LA)陽性血漿を、37℃で1分間加温して、測定試料2とした。
(測定試料3)
正常血漿として、コアグトロールNを用いた。また、被検血漿として、ジョージキング社製のLA陽性血漿を用いた。そして、正常血漿と、被検血漿とを、1:1で混合し、37℃で2分間加温して、測定試料3を調製した。
(測定試料4)
コアグトロールNにノボ・ヘパリン注(ノボノルディスクA/S社製)を0.5U/mLとなるように添加したものを、37℃で2分間加温して、測定試料4とした。
(測定試料5)
正常血漿として、コアグトロールNを用いた。被検血漿として、コアグトロールNにノボ・ヘパリン注(ノボノルディスクA/S社製)を0.5U/mLとなるように添加したものを用いた。そして、正常血漿と、被検血漿とを、1:1で混合し、37℃で2分間加温して、測定試料5を調製した。
(測定試料6)
ジョージキング社製のLA陽性血漿にノボ・ヘパリン注(ノボノルディスクA/S社製)を0.5U/mLとなるように添加したものを、37℃で2分間加温して、測定試料6とした。
(測定試料7)
正常血漿として、コアグトロールNを用いた。また、被検血漿として、ジョージキング社製のLA陽性血漿にノボ・ヘパリン注を0.5U/mLとなるように添加したものを用いた。そして、正常血漿と、被検血漿とを、1:1で混合し、37℃で2分間加温して、測定試料7を調製した。
【0071】
[APTT測定]
50μLの測定試料1をキュベットに分注した。次いで、50μLのトロンボチェックAPTT−SLAのリン脂質及び活性化剤を含む試薬を、キュベットに添加し、37℃で3分間加温した。その後、ポリブレンを含むカルシウム溶液である上記の試薬5を50μL添加し、試料が凝固するまでの時間を全自動血液凝固測定装置CS−2000i(シスメックス社製)で測定し、測定値1を得た。
【0072】
測定試料1に代えて、測定試料2、測定試料3、測定試料4、測定試料5、測定試料6、又は測定試料7を用いた以外、測定試料1のAPTT測定と同様の操作により、測定試料2〜7の凝固時間を測定し、それぞれ測定値2〜7を得た。
【0073】
[ロスナーインデックス値によるクロスミキシング試験の解析]
測定試料1〜7の凝固時間の測定値(APTT)を用い算出したロスナーインデックス値によるクロスミキシング試験の解析結果を図1に示す。ここで、ロスナーインデックス値は上述の式(1)を用いて算出した。なお、式(1)中、正常血漿のAPTTとして、測定値1を用いた。具体的な算出式を式(2)に示す。
ロスナーインデックス値=((混合血漿の測定値)−(測定値1))/(被検血漿の測定値) ×100・・・式(2)
【0074】
図1における、棒グラフ1及び棒グラフ2は、ヘパリンを含まない血漿を用いた際の、ロスナーインデックス値を示す。ここで、棒グラフ1は、式(2)において、(被検血漿の測定値)及び(混合血漿の測定値)として、測定値1を代入した際の、ロスナーインデックス値を示す。棒グラフ2は、(被検血漿の測定値)として測定値2、(混合血漿の測定値)として測定値3を代入した際の、ロスナーインデックス値を示す。
【0075】
図1における、棒グラフ3及び棒グラフ4は、ヘパリンを含む血漿を用いた際の、ロスナーインデックス値を示す。ここで、棒グラフ3は、式(2)において、(被検血漿の測定値)として測定値4、(混合血漿の測定値)として測定値5を代入した際の、ロスナーインデックス値を示す。棒グラフ4は、(被検血漿の測定値)として測定値6、(混合血漿の測定値)として測定値7を代入した際の、ロスナーインデックス値を示す。
【0076】
<実験例3>
実験例2のポリブレンを含むカルシウム溶液である試薬5に代えて、ポリブレンを含まない25mM カルシウム溶液(278mg 塩化カルシウム、100mL 精製水)を用いた以外、実験例2と同様の操作で、APTT測定及びロスナーインデックス値によるクロスミキシング試験の解析を行った。クロスミキシング試験の解析結果を図2に示す。なお、図2における、棒グラフ1〜4は、上記図1の棒グラフ1〜4と同じく、棒グラフ1及び棒グラフ2は、ヘパリンを含まない血漿を用いた際のロスナーインデックス値を示し、棒グラフ3及び棒グラフ4は、ヘパリンを含む血漿を用いた際のロスナーインデックス値を示す。
【0077】
図1及び図2の棒グラフ1及び2から、ポリブレンを含むカルシウム溶液を用いたAPTT測定でも、ポリブレンを含まないカルシウム溶液を用いたAPTT測定と同様のロスナーインデックス値が得られることが明らかになった。このことから、カルシウム溶液へのポリブレンの添加は、APTT測定に影響を与えないことが示唆された。
【0078】
また、図2の棒グラフ3及び棒グラフ4から明らかなように、ポリブレンを含まないカルシウム溶液を用い、外因性のヘパリンを含む血漿のAPTT測定を行った場合、正常血漿とLA陽性血漿のロスナーインデックス値の差が無くなり、LAが陽性か陰性かの判断が困難になることが分かる。一方、図1の棒グラフ3及び棒グラフ4から明らかなように、ポリブレンを含むカルシウム溶液を用いた場合、外因性のヘパリンの影響が軽減され、外因性のヘパリンを含む血漿であっても、LAが陽性か陰性かの判断が可能であることが分かる。
【0079】
上述の結果から、ポリブレンを含むカルシウム溶液を用いても、APTT測定自体に影響を及ぼすことがないことが分かった。また、ポリブレンを含むカルシウム溶液を用いることで、外因性のヘパリンを含む血漿であっても、正確にAPTT測定を行うことが可能となることが分かった。
【特許請求の範囲】
【請求項1】
ヘパリン中和剤を含む活性化部分トロンボプラスチン時間測定試薬。
【請求項2】
リン脂質及び活性化剤を含む第1試薬と、
ヘパリン中和剤及びカルシウム塩を含む第2試薬と、
を含む、活性化部分トロンボプラスチン時間測定試薬。
【請求項3】
ヘパリン中和剤がポリブレンである請求項1又は2に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項4】
カルシウム塩が塩化カルシウムである請求項2又は3に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項5】
活性化剤がエラグ酸、コロイダルシリカ、及び無水ケイ酸の少なくとも一つである請求項2〜4のいずれか1項に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項6】
リン脂質がホスファチジルセリン、ホスファチジルエタノールアミン、ホスファチジルコリン、及びホスファチジルグリセロールの少なくとも一つである請求項2〜5のいずれか1項に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項7】
被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後に、活性化部分トロンボプラスチン時間を測定するために用いられる試薬であって、
ヘパリン中和剤及びカルシウム塩を含有する試薬。
【請求項8】
ヘパリン中和剤がポリブレンである請求項7に記載の試薬。
【請求項9】
被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、
第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、
第2混合工程で得られた試料の凝固時間を測定する工程と、
を含む、活性化部分トロンボプラスチン時間測定方法。
【請求項10】
ヘパリン中和剤がポリブレンである請求項9に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項11】
カルシウム塩が塩化カルシウムである請求項9又は10に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項12】
活性化剤がエラグ酸、コロイダルシリカ、及び無水ケイ酸の少なくとも一つである請求項9〜11のいずれか1項に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項13】
リン脂質がホスファチジルセリン、ホスファチジルエタノールアミン、ホスファチジルコリン、及びホスファチジルグリセロールの少なくとも一つである請求項9〜12のいずれか1項に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項14】
血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する調整工程と、
調製工程で得られたそれぞれの測定試料とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、
第1混合工程で得られたそれぞれの試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、
第2混合工程で得られたそれぞれの試料の凝固時間を測定する工程と、
測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する工程と、
を含む、被検血漿に含まれる血液凝固抑制物質の有無の判定方法。
【請求項15】
判定工程が、測定工程で得られた、それぞれの試料の凝固時間に基づいて、ロスナーインデックス値を取得し、取得したロスナーインデックス値に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する、請求項14に記載の方法。
【請求項16】
血液凝固抑制物質が、ループスアンチコアグラント、後天性血友病、凝固因子インヒビター、又はC1インアクチベーターである請求項14又は15に記載の方法。
【請求項17】
ヘパリン中和剤がポリブレンである請求項14〜16のいずれか1項に記載の方法。
【請求項1】
ヘパリン中和剤を含む活性化部分トロンボプラスチン時間測定試薬。
【請求項2】
リン脂質及び活性化剤を含む第1試薬と、
ヘパリン中和剤及びカルシウム塩を含む第2試薬と、
を含む、活性化部分トロンボプラスチン時間測定試薬。
【請求項3】
ヘパリン中和剤がポリブレンである請求項1又は2に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項4】
カルシウム塩が塩化カルシウムである請求項2又は3に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項5】
活性化剤がエラグ酸、コロイダルシリカ、及び無水ケイ酸の少なくとも一つである請求項2〜4のいずれか1項に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項6】
リン脂質がホスファチジルセリン、ホスファチジルエタノールアミン、ホスファチジルコリン、及びホスファチジルグリセロールの少なくとも一つである請求項2〜5のいずれか1項に記載の活性化部分トロンボプラスチン時間測定試薬。
【請求項7】
被検血漿とリン脂質及び活性化剤を含む試薬とを混合した後に、活性化部分トロンボプラスチン時間を測定するために用いられる試薬であって、
ヘパリン中和剤及びカルシウム塩を含有する試薬。
【請求項8】
ヘパリン中和剤がポリブレンである請求項7に記載の試薬。
【請求項9】
被検血漿とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、
第1混合工程で得られた試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、
第2混合工程で得られた試料の凝固時間を測定する工程と、
を含む、活性化部分トロンボプラスチン時間測定方法。
【請求項10】
ヘパリン中和剤がポリブレンである請求項9に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項11】
カルシウム塩が塩化カルシウムである請求項9又は10に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項12】
活性化剤がエラグ酸、コロイダルシリカ、及び無水ケイ酸の少なくとも一つである請求項9〜11のいずれか1項に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項13】
リン脂質がホスファチジルセリン、ホスファチジルエタノールアミン、ホスファチジルコリン、及びホスファチジルグリセロールの少なくとも一つである請求項9〜12のいずれか1項に記載の活性化部分トロンボプラスチン時間測定方法。
【請求項14】
血液凝固抑制物質の存在が疑われる被検血漿及び正常血漿を、少なくとも3つの異なる割合で混合し測定試料を調整する調整工程と、
調製工程で得られたそれぞれの測定試料とリン脂質及び活性化剤を含む第1試薬とを混合する第1混合工程と、
第1混合工程で得られたそれぞれの試料とヘパリン中和剤及びカルシウム塩を含む第2試薬とを混合する第2混合工程と、
第2混合工程で得られたそれぞれの試料の凝固時間を測定する工程と、
測定工程で得られた、それぞれの試料の凝固時間に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する工程と、
を含む、被検血漿に含まれる血液凝固抑制物質の有無の判定方法。
【請求項15】
判定工程が、測定工程で得られた、それぞれの試料の凝固時間に基づいて、ロスナーインデックス値を取得し、取得したロスナーインデックス値に基づいて、被検血漿に含まれる血液凝固抑制物質の有無を判定する、請求項14に記載の方法。
【請求項16】
血液凝固抑制物質が、ループスアンチコアグラント、後天性血友病、凝固因子インヒビター、又はC1インアクチベーターである請求項14又は15に記載の方法。
【請求項17】
ヘパリン中和剤がポリブレンである請求項14〜16のいずれか1項に記載の方法。
【図1】


【図2】




【図2】


【公開番号】特開2011−133396(P2011−133396A)
【公開日】平成23年7月7日(2011.7.7)
【国際特許分類】
【出願番号】特願2009−294107(P2009−294107)
【出願日】平成21年12月25日(2009.12.25)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
【公開日】平成23年7月7日(2011.7.7)
【国際特許分類】
【出願日】平成21年12月25日(2009.12.25)
【出願人】(390014960)シスメックス株式会社 (810)
【Fターム(参考)】
[ Back to top ]

