活性酸素の定量法
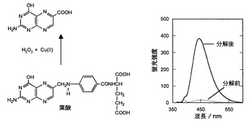
【課題】 新しい活性酸素の定量法を提供する。
【解決手段】 一般式1〔R1は−OH、−OR、−R、−H、−NHR又は‐NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示し、前記Rは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕のビタミンB又はその誘導体を、金属イオンと活性酸素生成物質の存在下で分解して、一般式2(R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)のプテリジン類を生成し、当該プテリジン類の蛍光強度を測定する活性酸素の定量法。
【解決手段】 一般式1〔R1は−OH、−OR、−R、−H、−NHR又は‐NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示し、前記Rは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕のビタミンB又はその誘導体を、金属イオンと活性酸素生成物質の存在下で分解して、一般式2(R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)のプテリジン類を生成し、当該プテリジン類の蛍光強度を測定する活性酸素の定量法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、特定のビタミンB又はその誘導体を活性酸素(例えば過酸化水素)との反応により蛍光性物質を生成させて活性酸素を定量する方法に係わる。
【背景技術】
【0002】
活性酸素は、発がん性物質の酸化還元反応、光触媒反応、光増感反応、細胞内の酸化系や還元系の還元又は励起によって生成し、細胞毒性の原因となる。また、活性酸素は蛋白質、低分子細胞成分、低分子化合物の自動酸化によっても生成することが知られている。また、活性酸素は蛋白質、低分子細胞成分、低分子化合物の自動酸化によっても生成することが知られている。
【0003】
例えば、酸化チタンの光触媒作用で酸化された糖の酸化物と生体内金属イオンとの反応で活性酸素の一種である過酸化水素が生成し、DNA損傷が引き起こされることが非特許文献1に報告されている。
【0004】
細胞毒性に関する場合、低い濃度の活性酸素でも大きな影響を示すことがある。この他、SUS管、銅管内で活性酸素が生成すると腐食を生じ、種々の水処理上のトラブルを生じることとなる。一方、活性酸素は利用の仕方如何では殺菌剤、殺藻剤、除草剤として用いることもできる。従って、活性酸素を高い感度で容易に定量することは各種産業分野において極めて重要なことである。
【0005】
従来、活性酸素の検出方法としては次のような方法が提案されている。
酸化還元色素であるNBT(Nitro Blue Tetrazolium)と活性酸素の反応により生じるホルマザンを銅電極と照合電極とを浸漬し、両電極間の電位差を測定して活性酸素を定量する方法が特許文献1に開示されている。しかし、100ml程度の多量の試料が必要である。また、原理上、電極の使用が不可能な試料への適用が不可能である。
【0006】
活性酸素によって酸化されると強い蛍光を有するフルオレセインやローダミンが生成することにより、蛍光強度の測定から活性酸素を検出する方法が、特許文献2に提案されている。しかし、これらの化合物は高価である。
【0007】
一方、分解反応により蛍光強度が増強する化合物として、ビタミンBの一種である葉酸が報告されている。葉酸は、プテリジン環をもち、プテリジン化合物は、強い蛍光をもつものが多いが、葉酸からの蛍光はほとんど観測されない。それは、葉酸の分子内のアミノベンゾイル残基により励起状態が失活するためである。葉酸は、紫外線の照射で分解し、強い蛍光を有するプテリン−6−カルボン酸が生成することが、非特許文献2に報告されている。
【0008】
即ち、非特許文献2には、式(3′):
【化9】

で示される、ビタミンBの一種である葉酸に紫外線を作用させると、その葉酸が加水分解されて、化学式(1′):
【化10】

で示される、可視光の蛍光を発するプテリジン化合物が生成し、このプテリジン化合物(プテリン−6−カルボン酸)が光化学反応でDNA損傷を引き起こすことが報告されている。
【0009】
しかし、前記の葉酸が紫外線以外の手段によって分解されて、蛍光を有するプテリジン類を生成することについては、非特許文献2を含めこれまでまったく記載されていない。
【0010】
また、葉酸の誘導体であるアメトプテリンが紫外線の照射で分解し、強い蛍光を有する2,4−ジアミノ−6−ヒドロキシメチルプテリジンを生成することが、非特許文献3に報告されている。
【0011】
このアメトプテリンもプテリジン環をもつが、アメトプテリンからの蛍光はほとんど観測されない。葉酸と同様にアメトプテリンの分子内のアミノベンゾイル残基により励起状態が失活するためであるが、その分解により2,4−ジアミノ−6−ヒドロキシメチルプテリジンが生成すると強い蛍光を示すようになる。この非特許文献3には、アメトプテリンの紫外線による分解で生成した2,4−ジアミノ−6−ヒドロキシメチルプテリジンが光化学反応でDNA損傷を引き起こすことが報告されている。
【0012】
即ち、非特許文献3には、化学式(4):
【化11】

で示されるビタミンBの一種である葉酸の誘導体であるメトトレキサート(アメトプテリンの別名、Methotrexateともいう。)に紫外線を作用させると、化学式2:
【化12】

で示される、可視光の蛍光を有するプテリジン化合物が生成し、このプテリジン化合物が光化学反応でDNA損傷を引き起こすことが開示されている。
【0013】
しかし、葉酸の誘導体であるこのアメトプテリンが紫外線の照射以外で分解され、強い蛍光を有する2,4−ジアミノ−6−ヒドロキシメチルプテリジンを生成することはこれまで知られていない。
【0014】
一方、金属イオンの存在下で、過酸化水素が生成することは、発がん性物質セミカルバジドと銅(II)イオンとの反応で過酸化水素が生成し、DNA損傷が引き起こされること(非特許文献4)、酸化チタン光触媒により酸化された糖と銅(II)イオンとの反応で過酸化水素を生成し、DNA損傷が引き起されること(非特許文献1)、銅(II)イオンの触媒作用によるベンゼンジオールの自動酸化反応により過酸化水素が生成し、DNA損傷を引き起こすことが報告されている(非特許文献5)。しかし、このような過酸化水素で葉酸やアメトプテリンが分解され強い蛍光を有するプテリジン化合物が生成することや、さらにこの蛍光物質を分解に関与した過酸化水素の定量に利用できることは知られていなかった。
【0015】
【特許文献1】特開平07−301618号
【特許文献2】特開2000−321262号
【非特許文献1】光化学討論会 講演要旨集 2003年11月22日(土)〜24日(月) 3D06
【非特許文献2】K. Hirakawa et al. Archives of Biochemistry and Biophysics 410巻, 261-268頁, 2003年.
【非特許文献3】K. Hirakawa et al. Photochemistry and Photobiology, 76巻, 467-472頁, 2002年.
【非特許文献4】K. Hirakawa, et al. Mutation Research 536巻, 91-101頁, 2003年.
【非特許文献5】K. Hirakawa et al. Chemical Research in Toxicology 15巻, 76-82頁, 2002年.
【発明の開示】
【発明が解決しようとする課題】
【0016】
本発明は、例えば、生体内で生成する過酸化水素などの活性酸素は、DNA損傷に関与するなど、その検出・定量は重要であることから、新しい活性酸素の定量法を提供することを目的としている。
【0017】
上記従来法のうち、蛍光プローブの利用では、高価な試薬が必要であり、また、多量の試料が必要である。また、原理上、電極の使用が不可能な試料への適用が不可能である。
【0018】
従って、本発明は、上記の従来の定量法における問題点を解決し、活性酸素を高価な試薬を用いることなく、容易に定量する方法を提供することを目的としている。
【課題を解決するための手段】
【0019】
(1)一般式1:
【化13】

〔但し、式中、R1は−OH、−OR、−R、−H、−NHR又は‐NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕で示されるビタミンB又はその誘導体と金属イオンおよび活性酸素生成物質を含有する試料の存在下で、活性酸素により、当該ビタミンB又はその誘導体を酸化分解して、
【0020】
【化14】

(但し、式中、R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)で示される可視光の蛍光を有するプテリジン類を生成させ、当該プテリジン類の蛍光強度を測定することによって活性酸素を定量することを特徴とする活性酸素の定量法に関する。
【0021】
(2)本発明は、ビタミンB又はその誘導体が、一般式3:
【化15】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−OHで示されるものである、(1)に記載の活性酸素の定量法に関する。
【0022】
(3)本発明は、ビタミンB又はその誘導体が、一般式4:
【化16】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−NH2で示されるものである(1)に記載の活性酸素の定量法に関する。
【0023】
(4)本発明は、金属イオンが二価または三価の金属イオンである(1)に記載の活性酸素の定量法に関する。
【0024】
(5)本発明は、金属イオンが二価の銅イオンである(1)に記載の活性酸素の定量法に関する。
【0025】
(6)本発明は、活性酸素が過酸化水素である(1)に記載の活性酸素の定量法に関する。
【0026】
(7)ビタミンB又はその誘導体が、一般式5:
【化17】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、
【0027】
プテリジン類が、化学式1:
【化18】

で示される化合物である(1)に記載の活性酸素の定量法に関する。
【0028】
(8)ビタミンB又はその誘導体が、一般式6:
【化19】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、
【0029】
プテリジン類が、化学式2:
【化20】

である(1)に記載の活性酸素の定量法に関する。
【0030】
(9)本発明は、(1)〜(8)のいずれか一つに記載の活性酸素定量法から、活性酸素生成物質の量を測定する、活性酸素生成物質定量法に関する。
【発明の効果】
【0031】
活性酸素を高価な試薬を用いることなく、金属イオン、特に銅(II)イオン存在下で、ビタミンBまたはその誘導体を用いて活性酸素の定量が可能となった。
【発明を実施するための最良の形態】
【0032】
本発明は、
【化21】

〔但し、式中、R1は−OH、−OR、−R、−H、−NHR又は‐NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕で示されるビタミンB又はその誘導体を用いて、金属イオンの存在下に、活性酸素生成物質を含有する試料と反応させることによって、一般式1で示されるビタミンB又はその誘導体を分解して、
【0033】
【化22】

(但し、上記一般式2において、R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)で示される可視光の蛍光を示すプテリジン類を生成させ、その蛍光の強度を測定することによって活性酸素を定量することを特徴とする活性酸素の定量法に関する。
【0034】
即ち、本発明は、例えば、次の反応式1に示すように、ビタミンBの一種である葉酸(化学式3′)を、二価の銅イオンの存在下に、過酸化水素を含有する水溶液(試料)に添加して、前記の葉酸を酸化分解して、強い可視光蛍光を示すプテリジン(化学式1′)を生成させるものである。この反応において、過酸化水素は、ヒドロキシルラジカルおよび銅酸素錯体(Cu(I)OOH)を生成して、一般式1で示されるビタミンB又はその誘導体を酸化分解して蛍光物質を生成していると考えられる(非特許文献4および5)。
【0035】
【化23】

【0036】
尚、本発明において、ビタミンBの一種である葉酸は、次の反応式2に示すような、平衡反応により、異性体(一般式3と一般式3′で示される異性体)であっても、その混合物であってもよく、また化学式1で示されるプテリジン類も同様に異性体もしくはその混合物(化学式1と化学式1′で示される異性体)であってもよいので、本発明における一般式1で示されるビタミンBとその誘導体及び一般式2で示されるプテリジン類もまた、R1が−OHである場合には、同様な異性体、またはその混合物であってもよい。このことは、一般式5で示されるビタミンBとその誘導体においてもいえることである。
【0037】
【化24】

【0038】
本発明において用いる、上記一般式1で示されるビタミンB又はその誘導体とは、例えば、一般式3、一般式4で示されるものを好適に挙げることができ、特に、好ましくは、一般式5、一般式6で示されるものを挙げることができ、さらに好ましいのは、一般式5におけるR3が−Hであり、一般式6におけるR3が−H又は炭素数1〜3のアルキル基であるものを挙げることができ、そして、最も好ましいのは、葉酸、アメトプテリン、4−[N−(2,4−ジアミノ−6−プテリジニルメチル)−N−メチルアミノ]安息香酸、アミノプテリン、N10−(トリフルオロアセチル)プテロイック酸、プテロイック酸、プテロイルアスパルチック酸などである。各一般式における置換基は一般式1と同様である。
【0039】
本発明において用いる、上記一般式中のRは、炭素数が1〜8、特に1〜6の炭化水素基で、例えば、アルキル基、アリル基、アルキルカルボキシル基、カルボニル基、カルバモイル基などが挙げられ、Xのハロゲンは,フッ素(F)、塩素(Cl)、臭素(Br)ヨウ素(I)などが挙げられる。
【0040】
本発明において用いる、金属イオンには、二価の銅イオン、二価の鉄イオン、三価のロジウムイオン、二価のパラジウムイオン、二価のニッケルイオン、二価のマンガンイオン、二価の銀イオンなどを挙げることができ、またテトラクロロ金(III)酸四水和物、ヘキサクロロ白金(IV)酸六水和物、塩化金(III)などの金化合物も含めるが、二価の銅イオン、二価の鉄イオンが好ましく、二価の銅イオンが最も好ましい。
【0041】
本発明における活性酸素生成物質とは、上記金属イオンの存在下に活性酸素を生成させる物質であればどのような物質でも良いが、例えば、酸化されたグルコース、酸化されたガラクトース、セミカルバジド、ベンゼンジオール、ヒドラジン、ヒドララジン、メチルヒドラジン,メチルヒドロキノン、オルト−アミノフェノール、ケルセチン、イソチオシアン酸アリル、イソチオシアン酸ベンジル、イソチオシアン酸フェネチル、2−アミノ−1−メチル−6−フェニルイミダゾ[4,5−b]ピリミジン、ヒドラゾベンゼン、N−ヒドロキシ−4−アミノアゾベンゼン、N−アセチルシステイン、レチノール、レチナール、没食子酸などが挙げられる。ここで、活性酸素とは、反応性の強い酸素の分子種で、過酸化水素、ヒドロキルラジカル、スーパーオキシドアニオン、一重項酸素、一酸化窒素、オゾンなどが挙げられるが、上記一般式1のビタンミンB又はその誘導体を酸化分解して上記一般式2の蛍光物質であるプテリジン類を生成することができれば、いずれの活性酸素の形態であってもよい。好ましい活性酸素は、過酸化水素、ヒドロキルラジカルなどである。
【0042】
本発明において用いる、可視光の蛍光とは、人間の目に見える400nm〜700nmの波長の蛍光のことを意味する。
【0043】
本発明においては、蛍光の強度の測定において、励起波長および蛍光の検出波長は、それぞれ葉酸が吸収する波長および蛍光スペクトルの範囲の波長を利用できる。本実施例では、360nmの励起光で試料を励起し、380〜600nmの範囲で蛍光スペクトルを測定した。蛍光の極大波長である450nmにおける蛍光強度で評価した。この蛍光強度の測定は、通常の蛍光光度測定装置を用いて測定でき、例えば、前述のビタミンB又はその誘導体、金属イオン、活性酸素生成物質を含有する試料を水溶液中で混合して、試料溶液を石英製の蛍光用セルに入れ、島津RF−1500、RF−5300などの蛍光光度計を使用して測定できるが、これに限定されるものではない。
【0044】
本発明において、ビタミンB又はその誘導体を酸化分解反応における反応温度は0℃〜50℃程度、特に5℃〜40℃程度であればよく、即ち、常温(23℃)付近であればよく、圧力が常圧(1気圧)であればよい。前記酸化分解反応において、溶媒は、水溶液または水を主として(水50重量%以上)含む溶液であることが好ましく、その溶液には、必要であれば、リン酸緩衝液、炭酸緩衝液、トリス塩酸緩衝液などの緩衝液が含有されていてもよい。更に、前記の酸化分解反応において、測定時間は、1分〜100分程度、特に、5分〜60分程度であればよい。
【0045】
本発明において、活性酸素生成物質の定量とは、本発明の方法により定量された過酸化水素の量から金属イオンの存在下で活性酸素を生成させた物質の量を表すことが出来るということを意味する。例えば、試料中に発がん性物質セミカルバジドが含まれており、ある量の過酸化水素が発生していれば、その過酸化水素量を測定することで実施例4及び5の計算式(3)または図5の検量線より発がん性物質セミカルバジドの量を知ることが出来るという意味である。さらに、試料中の活性酸素生成物質が未知の場合であっても、その過酸化水素量を測定することでその過酸化水素量を発生させるのに必要な活性酸素生成物質の量を、例えば実施例4及び5の計算式(3)もしくは図5または図7の検量線より得られた発がん性物質セミカルバジドまたは1,4−ベンゼンジオールの量として未知の活性酸素生成物質の量を表すこともできるという意味である。必要であれば、未知の活性酸素生成物質の量を他の先に記載した活性酸素生成物質のいずれかとして表すことも出来る。
【実施例1】
【0046】
葉酸の酸化分解前後での蛍光スペクトル
10μM葉酸(和光純薬工業株式会社)、20μM銅(II)イオン(塩化銅(II)二水和物(和光純薬工業株式会社))を含む1.0mLの10mMリン酸緩衝液(pH7.6)を分解前の試料とした。10μM葉酸、20μM銅(II)イオン、50μM過酸化水素を含む1.0mLの10mMリン酸緩衝液(pH7.6)を1.5mLのマイクロチューブ中、37℃で1時間反応させたものを分解後の試料とした。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−5300)を使用し、励起波長360nmで測定した。
【0047】
化学式1で示されるプテリジンは、図1の分解後で示すような可視光蛍光の強度を有している。
本発明におけるビタミンB又は誘導体は、プテリジン環をもつが、プテリジン由来の蛍光はほとんど観測されなかった(図1分解前)。酸化分解によって、プテリジン環の部分がアミノベンゾイル残基から離れることにより、強い蛍光が観測された。
【0048】
葉酸の蛍光は、図1に示すように非常に弱いが、過酸化水素と銅(II)イオンとの反応により酸化分解するとプテリジン化合物由来の非常に強い蛍光が観測される。また、アメトプテリン(メトトレキサート(アルドリッチ))においても葉酸と同様に過酸化水素による酸化分解で強い蛍光が観察された(図には示していない)。
【実施例2】
【0049】
銅(II)イオン存在下での過酸化水素の定量
ビタミンBの一種である葉酸を使用し、金属イオンとして銅(II)イオンを用い、活性酸素である過酸化水素の定量を行った。
【0050】
本実施例1において、10μM葉酸、20μM銅(II)イオンを含む1.0mLの10mMリン酸緩衝液(pH7.6)と過酸化水素を1.5mLのマイクロチューブ中で加え、37℃で1時間反応させた。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
過酸化水素の濃度は、0.1μMから100μMで変化させた。
【0051】
この実施例2において、銅(II)イオンと過酸化水素の添加により試料の蛍光強度は増大した。
蛍光スペクトルは、プテリン−6−カルボン酸の蛍光スペクトルと一致し、蛍光物質としてプテリジン化合物の生成を示している。銅(II)イオン存在下、過酸化水素濃度の増大に従って蛍光強度が増大した。
試料の蛍光強度は、図2(黒丸)に示す通りである。
【0052】
比較におけるコントロール試料として、葉酸、銅(II)イオンを含み、過酸化水素を含まない溶液および葉酸と過酸化水素を含み、銅(II)イオンを含まない溶液を用いて、実施例2と同様に行った。
銅(II)イオンを添加していない場合には、蛍光の増強は観測されなかった。
試料の蛍光強度は、図2(白丸)に示す通りである。
【0053】
なお、実施例2と同様の方法で過酸化水素濃度に対する葉酸の蛍光強度の検量線を作成し、濃度未知の過酸化水素水に含まれる過酸化水素濃度を求めたところ、同試料に含まれる過酸化水素濃度を過マンガン酸カリウムを用いた酸化還元滴定により求めた値と一致した。過マンガン酸カリウムを用いた酸化還元滴定は、文献(化学実験第3版、東京大学教養学部化学教室化学教育研究会編、東京大学出版会、81〜83頁)の方法に従った。
【実施例3】
【0054】
他の金属イオン存在下での過酸化水素の定量
本実施例3では、葉酸、他の金属イオンを用い、活性酸素として過酸化水素の定量を行った。
即ち、本実施例3において、10μM葉酸、金属イオンとして20μM鉄(II)イオン(塩化鉄(II)四水和物(和光純薬工業株式会社))、20μMテトラクロロ金(III)酸四水和物(和光純薬工業株式会社)、20μMヘキサクロロ白金(IV)酸六水和物(和光純薬工業株式会社)、20μM硝酸銀のいずれかひとつを含む1.0mLの10mMリン酸緩衝液(pH7.6)と過酸化水素を1.5mLのマイクロチューブ中で加え、37℃で1時間反応した。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
【0055】
過酸化水素の濃度は、0.1μMから5μMで変化させた。
試料の蛍光強度は、図3(黒丸)に示す通りである。
図3によれば、鉄(II)イオンにより、過酸化水素が存在しない場合にも蛍光強度が増大した。
過酸化水素との反応による葉酸の蛍光強度の増大は、銅(II)イオンを用いた場合の方が鉄(II)イオンを用いた場合よりも感度が高い。
【0056】
比較は、コントロール試料として、葉酸、金属イオンとして鉄(II)イオン、テトラクロロ金(III)酸四水和物、ヘキサクロロ白金(IV)酸六水和物、硝酸銀のいずれかひとつを含み、過酸化水素を含まない溶液および葉酸と過酸化水素を含み、金属イオンを含まない溶液を用いて、実施例3と同様にして定量を行った。
鉄(II)イオンの結果を図3(白丸)に示す。同様に、テトラクロロ金(III)酸四水和物、ヘキサクロロ白金(IV)酸六水和物にも弱いながら効果が認められたが、硝酸銀ではその効果はほとんど認められなかった(図には示していない)。
【実施例4】
【0057】
葉酸の蛍光強度と過酸化水素濃度との関係
この実施例においては、葉酸の蛍光強度の増大の時間変化を測定した。
10μM葉酸、20μM銅(II)イオンを含む1.0mLの10mMリン酸緩衝液(pH7.6)と過酸化水素を1.5mLのマイクロチューブ中で加え、37℃で反応した。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
結果は、図4に示す通りである。
【0058】
反応時間に比例した蛍光強度の増大が観測された。蛍光強度の増大速度は、過酸化水素濃度に依存した。図4の傾きから蛍光強度の増大速度を計算すると過酸化水素濃度に比例した。
【0059】
比較におけるコントロール試料として、葉酸、銅(II)イオンを含み、過酸化水素を含まない溶液を用いて、実施例4と同様に行った。
その結果を図4(黒三角)に示す。
【0060】
従って、コントロール試料と過酸化水素を含む試料の蛍光強度を比較し、その増大量(ΔI)を反応時間で割り蛍光強度の増大速度を求めることができ、さらに過酸化水素濃度を計算で求めることができることを示している。
過酸化水素濃度を[H2O2]、比例定数をkと表すとΔI/反応時間=k×[H2O2]の式(式1)で表すことができる。
図4の傾きから蛍光強度の増大速度を求め、過酸化水素濃度に対してプロットし、得られた直線の傾きからkが求められる。
本実施例の条件では、kは、1.5μM-1min-1である。kは、使用する分光光度計の機種によっても異なり、濃度既知の過酸化水素を用いた測定によりあらかじめ求めることにより、未知濃度の過酸化水素の定量に利用できる。
【実施例5】
【0061】
セミカルバジドにより生成する過酸化水素の定量
発がん性物質セミカルバジドと銅(II)イオンとの反応で過酸化水素が生成し、DNA損傷が引き起こされることが報告されている(非特許文献4)。
葉酸の蛍光強度の測定により、セミカルバジドと銅(II)イオンとの反応で生成する過酸化水素の定量を行った。
【0062】
10μM葉酸、20μM銅(II)イオンとセミカルバジド(セミカルバジド塩酸塩(和光純薬工業株式会社))含む1.0mLの10mMリン酸緩衝液(pH7.6)を1.5mLのマイクロチューブ中で混合し、37℃で1時間反応させた。
セミカルバジドの濃度は、1μMから50μMで変化させた。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
その結果を、図5(黒丸)に示す。
【0063】
比較において、コントロール試料として、葉酸、セミカルバジドを含み、銅(II)イオンを含まない溶液を用いて、実施例5に準じて行った。
その結果を図5(白丸)に示す。
結果は、図5に示す通り、銅(II)イオン存在下、セミカルバジドの濃度の増大に従い、蛍光強度が増大した。一方、銅(II)イオンを含まない試料では変化はなかった。
【0064】
カタラーゼをあらかじめ添加すると蛍光の増大は完全に抑制された。カタラーゼは、過酸化水素をすみやかに水と酸素に分解する酵素であるため、葉酸の蛍光強度の増大は、過酸化水素によることが示された(図には示していない)。
比較におけるコントロール試料の蛍光強度と比較した蛍光の増大量から過酸化水素の生成速度を計算した。セミカルバジドと銅(II)イオンとの反応で過酸化水素が生成し、葉酸の酸化分解が起こり、蛍光強度の増大が起こるとき、ΔI=∫0Tk(T−t)rH2O2dtの式(式2)で蛍光強度の増大を表すことができる。
【0065】
この式で、ΔIおよびkは、式1に記載のものである。Tは、反応時間、tは任意の時間、rH2O2は、過酸化水素の生成速度を表している。セミカルバジドと銅(II)イオンとの反応時間に比例して過酸化水素が生成すると仮定すると、式2からrH2O2=2ΔI/kT2の式(式3)を求めることができる。上記の測定条件では、Tは、60分、kは、1.5μM-1min-1であり、図5に示す蛍光強度のデータからμM min-1単位の過酸化水素生成速度を計算することができる。
計算結果は、図5(白四角)に示す通りで、過酸化水素の生成速度がセミカルバジドの濃度の増大に従って大きくなることが示された。これにより、蛍光強度から試料中の過酸化水素生成速度およびセミカルバジド濃度が明らかとなる。
【実施例6】
【0066】
酸化された糖により生成する過酸化水素の定量
酸化チタン光触媒により酸化された糖と銅(II)イオンとの反応で過酸化水素を生成し、DNA損傷を引き起こすことが報告されている(非特許文献1)。
本発明を利用し、糖の酸化物から生成した過酸化水素量を求めた。
本実施例6では、1.5mLのマイクロチューブ中に酸化チタン(Degussa P-25、日本アエロジル株式会社),0.8mg mL-1)と10mMの糖(グルコース(和光純薬工業株式会社)、ガラクトース(和光純薬工業株式会社))を含む0.2mLの10mMリン酸緩衝液(pH7.6)を調製し、光照射(365nm,5Jcm-2)で、グルコースとガラクトースの酸化物を調製した。
【0067】
遠心分離(10,000回転/分、5分)で酸化チタン粒子を沈降させた後、糖の酸化物を含む上澄み液を糖濃度が図6の横軸に示す濃度になるように1.0mLの10mMリン酸緩衝液(pH7.6)中で10μM葉酸と20μM銅(II)イオンを含む溶液を調製した。37℃で1時間反応させ、実施例1と同様に蛍光測定した。
蛍光強度は、葉酸と反応させた糖の濃度の増大に従って増大した。蛍光強度の増大は、カタラーゼの添加で完全に抑制されたことから過酸化水素の生成が確認された(図には示していない)。
【0068】
上記と同様に式3を用いて、過酸化水素の生成速度(単位μM min-1)を計算した。さらに、過酸化水素の生成速度に反応時間をかけるとその反応時間の内に生成した過酸化水素量を計算することができる。反応時間1時間(60分)後の過酸化水素量を求めた例を図6に示す。
【実施例7】
【0069】
ベンゼンジオールにより生成する過酸化水素の測定
銅(II)イオンの触媒作用によるベンゼンジオールの自動酸化反応により過酸化水素が生成し、DNA損傷を引き起こすことが報告されている(非特許文献5)。
1,4−ベンゼンジオールの方が1,2−ベンゼンジオールよりも自動酸化速度が著しく速いことが報告されている。
本発明を利用し、葉酸の蛍光強度の増大から計算したベンゼンジオールの自動酸化による過酸化水素生成速度を求めた。
1.5mLのマイクロチューブ中で10μM葉酸、20μM銅(II)イオン、ベンゼンジオール(1,2−ベンゼンジオールには、カテコール(和光純薬工業株式会社)を使用し、1,4−ベンゼンジオールにはヒドロキノン(和光純薬工業株式会社)を使用した)を含む1.0mLの10mMリン酸緩衝液(pH7.6)を調製し、37℃で1時間反応させた。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
銅(II)イオンを添加しない場合には、蛍光強度の増大は観測されなかった(図には示していない)。
【0070】
図7に示す通り、銅(II)イオン存在下、1,4−ベンゼンジオールを含む試料では、蛍光強度の増大が観測された。カタラーゼの添加で蛍光強度の増大が完全に抑制されたことから、過酸化水素による葉酸の酸化分解であることが確認された(図には示していない)。
1,2−ベンゼンジオールを含む試料では、蛍光強度の増大はほとんど観測されなかった。
この結果は、これまで報告されたDNA損傷の程度および自動酸化速度の違いとよく対応している。銅(II)イオンを添加していない場合には、蛍光の増強は観測されなかった。葉酸の蛍光強度の増大量から上記と同様に式3を用いて、過酸化水素の生成速度を計算した。計算結果を図7に示す。これにより、蛍光強度から試料中の過酸化水素生成速度および1,4−ベンゼンジオール濃度が明らかとなる。
【産業上の利用可能性】
【0071】
本発明の活性酸素の検出方法によれば、高価な試薬を用いることなく、安価な試薬と蛍光光度計とを用いて、高い感度で試料中の活性酸素の定量を行う検出試薬の開発が可能となる。本発明の方法によれば、活性酸素生成物質の探索及び定量、生成した活性酸素の定量を容易に実施することができる。さらに、生体内で生成する活性酸素検出用プローブとしての利用も可能である。そして、活性酸素生成物質の測定値を活性酸素生成等を介した酸化ストレスや生体分子損傷作用の簡便な評価法として利用できる。
【図面の簡単な説明】
【0072】
【図1】葉酸の酸化分解前後の蛍光スペクトルである。
【図2】実施例2における銅(II)イオン存在下、葉酸の酸化分解による蛍光強度の過酸化水素濃度依存性を示す。
【図3】実施例3における鉄(II)イオン存在下、葉酸の酸化分解による蛍光強度の過酸化水素濃度依存性を示す。
【図4】実施例4における銅(II)イオン存在下、過酸化水素による葉酸の蛍光強度の時間変化を示す。
【図5】実施例5におけるセミカルバジドとの反応による葉酸の蛍光強度及び蛍光強度から計算した過酸化水素生成速度とセミカルバジドの濃度との関係を示す。
【図6】実施例6における葉酸の蛍光強度の増大から計算した糖の酸化物から生成した過酸化水素生成量との関係を示す。
【図7】実施例7におけるベンゼンジオールとの反応による葉酸の蛍光強度及び蛍光強度から計算した過酸化水素生成速度とベンゼンジオールの濃度との関係を示す。
【技術分野】
【0001】
本発明は、特定のビタミンB又はその誘導体を活性酸素(例えば過酸化水素)との反応により蛍光性物質を生成させて活性酸素を定量する方法に係わる。
【背景技術】
【0002】
活性酸素は、発がん性物質の酸化還元反応、光触媒反応、光増感反応、細胞内の酸化系や還元系の還元又は励起によって生成し、細胞毒性の原因となる。また、活性酸素は蛋白質、低分子細胞成分、低分子化合物の自動酸化によっても生成することが知られている。また、活性酸素は蛋白質、低分子細胞成分、低分子化合物の自動酸化によっても生成することが知られている。
【0003】
例えば、酸化チタンの光触媒作用で酸化された糖の酸化物と生体内金属イオンとの反応で活性酸素の一種である過酸化水素が生成し、DNA損傷が引き起こされることが非特許文献1に報告されている。
【0004】
細胞毒性に関する場合、低い濃度の活性酸素でも大きな影響を示すことがある。この他、SUS管、銅管内で活性酸素が生成すると腐食を生じ、種々の水処理上のトラブルを生じることとなる。一方、活性酸素は利用の仕方如何では殺菌剤、殺藻剤、除草剤として用いることもできる。従って、活性酸素を高い感度で容易に定量することは各種産業分野において極めて重要なことである。
【0005】
従来、活性酸素の検出方法としては次のような方法が提案されている。
酸化還元色素であるNBT(Nitro Blue Tetrazolium)と活性酸素の反応により生じるホルマザンを銅電極と照合電極とを浸漬し、両電極間の電位差を測定して活性酸素を定量する方法が特許文献1に開示されている。しかし、100ml程度の多量の試料が必要である。また、原理上、電極の使用が不可能な試料への適用が不可能である。
【0006】
活性酸素によって酸化されると強い蛍光を有するフルオレセインやローダミンが生成することにより、蛍光強度の測定から活性酸素を検出する方法が、特許文献2に提案されている。しかし、これらの化合物は高価である。
【0007】
一方、分解反応により蛍光強度が増強する化合物として、ビタミンBの一種である葉酸が報告されている。葉酸は、プテリジン環をもち、プテリジン化合物は、強い蛍光をもつものが多いが、葉酸からの蛍光はほとんど観測されない。それは、葉酸の分子内のアミノベンゾイル残基により励起状態が失活するためである。葉酸は、紫外線の照射で分解し、強い蛍光を有するプテリン−6−カルボン酸が生成することが、非特許文献2に報告されている。
【0008】
即ち、非特許文献2には、式(3′):
【化9】

で示される、ビタミンBの一種である葉酸に紫外線を作用させると、その葉酸が加水分解されて、化学式(1′):
【化10】

で示される、可視光の蛍光を発するプテリジン化合物が生成し、このプテリジン化合物(プテリン−6−カルボン酸)が光化学反応でDNA損傷を引き起こすことが報告されている。
【0009】
しかし、前記の葉酸が紫外線以外の手段によって分解されて、蛍光を有するプテリジン類を生成することについては、非特許文献2を含めこれまでまったく記載されていない。
【0010】
また、葉酸の誘導体であるアメトプテリンが紫外線の照射で分解し、強い蛍光を有する2,4−ジアミノ−6−ヒドロキシメチルプテリジンを生成することが、非特許文献3に報告されている。
【0011】
このアメトプテリンもプテリジン環をもつが、アメトプテリンからの蛍光はほとんど観測されない。葉酸と同様にアメトプテリンの分子内のアミノベンゾイル残基により励起状態が失活するためであるが、その分解により2,4−ジアミノ−6−ヒドロキシメチルプテリジンが生成すると強い蛍光を示すようになる。この非特許文献3には、アメトプテリンの紫外線による分解で生成した2,4−ジアミノ−6−ヒドロキシメチルプテリジンが光化学反応でDNA損傷を引き起こすことが報告されている。
【0012】
即ち、非特許文献3には、化学式(4):
【化11】

で示されるビタミンBの一種である葉酸の誘導体であるメトトレキサート(アメトプテリンの別名、Methotrexateともいう。)に紫外線を作用させると、化学式2:
【化12】

で示される、可視光の蛍光を有するプテリジン化合物が生成し、このプテリジン化合物が光化学反応でDNA損傷を引き起こすことが開示されている。
【0013】
しかし、葉酸の誘導体であるこのアメトプテリンが紫外線の照射以外で分解され、強い蛍光を有する2,4−ジアミノ−6−ヒドロキシメチルプテリジンを生成することはこれまで知られていない。
【0014】
一方、金属イオンの存在下で、過酸化水素が生成することは、発がん性物質セミカルバジドと銅(II)イオンとの反応で過酸化水素が生成し、DNA損傷が引き起こされること(非特許文献4)、酸化チタン光触媒により酸化された糖と銅(II)イオンとの反応で過酸化水素を生成し、DNA損傷が引き起されること(非特許文献1)、銅(II)イオンの触媒作用によるベンゼンジオールの自動酸化反応により過酸化水素が生成し、DNA損傷を引き起こすことが報告されている(非特許文献5)。しかし、このような過酸化水素で葉酸やアメトプテリンが分解され強い蛍光を有するプテリジン化合物が生成することや、さらにこの蛍光物質を分解に関与した過酸化水素の定量に利用できることは知られていなかった。
【0015】
【特許文献1】特開平07−301618号
【特許文献2】特開2000−321262号
【非特許文献1】光化学討論会 講演要旨集 2003年11月22日(土)〜24日(月) 3D06
【非特許文献2】K. Hirakawa et al. Archives of Biochemistry and Biophysics 410巻, 261-268頁, 2003年.
【非特許文献3】K. Hirakawa et al. Photochemistry and Photobiology, 76巻, 467-472頁, 2002年.
【非特許文献4】K. Hirakawa, et al. Mutation Research 536巻, 91-101頁, 2003年.
【非特許文献5】K. Hirakawa et al. Chemical Research in Toxicology 15巻, 76-82頁, 2002年.
【発明の開示】
【発明が解決しようとする課題】
【0016】
本発明は、例えば、生体内で生成する過酸化水素などの活性酸素は、DNA損傷に関与するなど、その検出・定量は重要であることから、新しい活性酸素の定量法を提供することを目的としている。
【0017】
上記従来法のうち、蛍光プローブの利用では、高価な試薬が必要であり、また、多量の試料が必要である。また、原理上、電極の使用が不可能な試料への適用が不可能である。
【0018】
従って、本発明は、上記の従来の定量法における問題点を解決し、活性酸素を高価な試薬を用いることなく、容易に定量する方法を提供することを目的としている。
【課題を解決するための手段】
【0019】
(1)一般式1:
【化13】

〔但し、式中、R1は−OH、−OR、−R、−H、−NHR又は‐NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕で示されるビタミンB又はその誘導体と金属イオンおよび活性酸素生成物質を含有する試料の存在下で、活性酸素により、当該ビタミンB又はその誘導体を酸化分解して、
【0020】
【化14】

(但し、式中、R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)で示される可視光の蛍光を有するプテリジン類を生成させ、当該プテリジン類の蛍光強度を測定することによって活性酸素を定量することを特徴とする活性酸素の定量法に関する。
【0021】
(2)本発明は、ビタミンB又はその誘導体が、一般式3:
【化15】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−OHで示されるものである、(1)に記載の活性酸素の定量法に関する。
【0022】
(3)本発明は、ビタミンB又はその誘導体が、一般式4:
【化16】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−NH2で示されるものである(1)に記載の活性酸素の定量法に関する。
【0023】
(4)本発明は、金属イオンが二価または三価の金属イオンである(1)に記載の活性酸素の定量法に関する。
【0024】
(5)本発明は、金属イオンが二価の銅イオンである(1)に記載の活性酸素の定量法に関する。
【0025】
(6)本発明は、活性酸素が過酸化水素である(1)に記載の活性酸素の定量法に関する。
【0026】
(7)ビタミンB又はその誘導体が、一般式5:
【化17】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、
【0027】
プテリジン類が、化学式1:
【化18】

で示される化合物である(1)に記載の活性酸素の定量法に関する。
【0028】
(8)ビタミンB又はその誘導体が、一般式6:
【化19】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、
【0029】
プテリジン類が、化学式2:
【化20】

である(1)に記載の活性酸素の定量法に関する。
【0030】
(9)本発明は、(1)〜(8)のいずれか一つに記載の活性酸素定量法から、活性酸素生成物質の量を測定する、活性酸素生成物質定量法に関する。
【発明の効果】
【0031】
活性酸素を高価な試薬を用いることなく、金属イオン、特に銅(II)イオン存在下で、ビタミンBまたはその誘導体を用いて活性酸素の定量が可能となった。
【発明を実施するための最良の形態】
【0032】
本発明は、
【化21】

〔但し、式中、R1は−OH、−OR、−R、−H、−NHR又は‐NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕で示されるビタミンB又はその誘導体を用いて、金属イオンの存在下に、活性酸素生成物質を含有する試料と反応させることによって、一般式1で示されるビタミンB又はその誘導体を分解して、
【0033】
【化22】

(但し、上記一般式2において、R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)で示される可視光の蛍光を示すプテリジン類を生成させ、その蛍光の強度を測定することによって活性酸素を定量することを特徴とする活性酸素の定量法に関する。
【0034】
即ち、本発明は、例えば、次の反応式1に示すように、ビタミンBの一種である葉酸(化学式3′)を、二価の銅イオンの存在下に、過酸化水素を含有する水溶液(試料)に添加して、前記の葉酸を酸化分解して、強い可視光蛍光を示すプテリジン(化学式1′)を生成させるものである。この反応において、過酸化水素は、ヒドロキシルラジカルおよび銅酸素錯体(Cu(I)OOH)を生成して、一般式1で示されるビタミンB又はその誘導体を酸化分解して蛍光物質を生成していると考えられる(非特許文献4および5)。
【0035】
【化23】

【0036】
尚、本発明において、ビタミンBの一種である葉酸は、次の反応式2に示すような、平衡反応により、異性体(一般式3と一般式3′で示される異性体)であっても、その混合物であってもよく、また化学式1で示されるプテリジン類も同様に異性体もしくはその混合物(化学式1と化学式1′で示される異性体)であってもよいので、本発明における一般式1で示されるビタミンBとその誘導体及び一般式2で示されるプテリジン類もまた、R1が−OHである場合には、同様な異性体、またはその混合物であってもよい。このことは、一般式5で示されるビタミンBとその誘導体においてもいえることである。
【0037】
【化24】

【0038】
本発明において用いる、上記一般式1で示されるビタミンB又はその誘導体とは、例えば、一般式3、一般式4で示されるものを好適に挙げることができ、特に、好ましくは、一般式5、一般式6で示されるものを挙げることができ、さらに好ましいのは、一般式5におけるR3が−Hであり、一般式6におけるR3が−H又は炭素数1〜3のアルキル基であるものを挙げることができ、そして、最も好ましいのは、葉酸、アメトプテリン、4−[N−(2,4−ジアミノ−6−プテリジニルメチル)−N−メチルアミノ]安息香酸、アミノプテリン、N10−(トリフルオロアセチル)プテロイック酸、プテロイック酸、プテロイルアスパルチック酸などである。各一般式における置換基は一般式1と同様である。
【0039】
本発明において用いる、上記一般式中のRは、炭素数が1〜8、特に1〜6の炭化水素基で、例えば、アルキル基、アリル基、アルキルカルボキシル基、カルボニル基、カルバモイル基などが挙げられ、Xのハロゲンは,フッ素(F)、塩素(Cl)、臭素(Br)ヨウ素(I)などが挙げられる。
【0040】
本発明において用いる、金属イオンには、二価の銅イオン、二価の鉄イオン、三価のロジウムイオン、二価のパラジウムイオン、二価のニッケルイオン、二価のマンガンイオン、二価の銀イオンなどを挙げることができ、またテトラクロロ金(III)酸四水和物、ヘキサクロロ白金(IV)酸六水和物、塩化金(III)などの金化合物も含めるが、二価の銅イオン、二価の鉄イオンが好ましく、二価の銅イオンが最も好ましい。
【0041】
本発明における活性酸素生成物質とは、上記金属イオンの存在下に活性酸素を生成させる物質であればどのような物質でも良いが、例えば、酸化されたグルコース、酸化されたガラクトース、セミカルバジド、ベンゼンジオール、ヒドラジン、ヒドララジン、メチルヒドラジン,メチルヒドロキノン、オルト−アミノフェノール、ケルセチン、イソチオシアン酸アリル、イソチオシアン酸ベンジル、イソチオシアン酸フェネチル、2−アミノ−1−メチル−6−フェニルイミダゾ[4,5−b]ピリミジン、ヒドラゾベンゼン、N−ヒドロキシ−4−アミノアゾベンゼン、N−アセチルシステイン、レチノール、レチナール、没食子酸などが挙げられる。ここで、活性酸素とは、反応性の強い酸素の分子種で、過酸化水素、ヒドロキルラジカル、スーパーオキシドアニオン、一重項酸素、一酸化窒素、オゾンなどが挙げられるが、上記一般式1のビタンミンB又はその誘導体を酸化分解して上記一般式2の蛍光物質であるプテリジン類を生成することができれば、いずれの活性酸素の形態であってもよい。好ましい活性酸素は、過酸化水素、ヒドロキルラジカルなどである。
【0042】
本発明において用いる、可視光の蛍光とは、人間の目に見える400nm〜700nmの波長の蛍光のことを意味する。
【0043】
本発明においては、蛍光の強度の測定において、励起波長および蛍光の検出波長は、それぞれ葉酸が吸収する波長および蛍光スペクトルの範囲の波長を利用できる。本実施例では、360nmの励起光で試料を励起し、380〜600nmの範囲で蛍光スペクトルを測定した。蛍光の極大波長である450nmにおける蛍光強度で評価した。この蛍光強度の測定は、通常の蛍光光度測定装置を用いて測定でき、例えば、前述のビタミンB又はその誘導体、金属イオン、活性酸素生成物質を含有する試料を水溶液中で混合して、試料溶液を石英製の蛍光用セルに入れ、島津RF−1500、RF−5300などの蛍光光度計を使用して測定できるが、これに限定されるものではない。
【0044】
本発明において、ビタミンB又はその誘導体を酸化分解反応における反応温度は0℃〜50℃程度、特に5℃〜40℃程度であればよく、即ち、常温(23℃)付近であればよく、圧力が常圧(1気圧)であればよい。前記酸化分解反応において、溶媒は、水溶液または水を主として(水50重量%以上)含む溶液であることが好ましく、その溶液には、必要であれば、リン酸緩衝液、炭酸緩衝液、トリス塩酸緩衝液などの緩衝液が含有されていてもよい。更に、前記の酸化分解反応において、測定時間は、1分〜100分程度、特に、5分〜60分程度であればよい。
【0045】
本発明において、活性酸素生成物質の定量とは、本発明の方法により定量された過酸化水素の量から金属イオンの存在下で活性酸素を生成させた物質の量を表すことが出来るということを意味する。例えば、試料中に発がん性物質セミカルバジドが含まれており、ある量の過酸化水素が発生していれば、その過酸化水素量を測定することで実施例4及び5の計算式(3)または図5の検量線より発がん性物質セミカルバジドの量を知ることが出来るという意味である。さらに、試料中の活性酸素生成物質が未知の場合であっても、その過酸化水素量を測定することでその過酸化水素量を発生させるのに必要な活性酸素生成物質の量を、例えば実施例4及び5の計算式(3)もしくは図5または図7の検量線より得られた発がん性物質セミカルバジドまたは1,4−ベンゼンジオールの量として未知の活性酸素生成物質の量を表すこともできるという意味である。必要であれば、未知の活性酸素生成物質の量を他の先に記載した活性酸素生成物質のいずれかとして表すことも出来る。
【実施例1】
【0046】
葉酸の酸化分解前後での蛍光スペクトル
10μM葉酸(和光純薬工業株式会社)、20μM銅(II)イオン(塩化銅(II)二水和物(和光純薬工業株式会社))を含む1.0mLの10mMリン酸緩衝液(pH7.6)を分解前の試料とした。10μM葉酸、20μM銅(II)イオン、50μM過酸化水素を含む1.0mLの10mMリン酸緩衝液(pH7.6)を1.5mLのマイクロチューブ中、37℃で1時間反応させたものを分解後の試料とした。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−5300)を使用し、励起波長360nmで測定した。
【0047】
化学式1で示されるプテリジンは、図1の分解後で示すような可視光蛍光の強度を有している。
本発明におけるビタミンB又は誘導体は、プテリジン環をもつが、プテリジン由来の蛍光はほとんど観測されなかった(図1分解前)。酸化分解によって、プテリジン環の部分がアミノベンゾイル残基から離れることにより、強い蛍光が観測された。
【0048】
葉酸の蛍光は、図1に示すように非常に弱いが、過酸化水素と銅(II)イオンとの反応により酸化分解するとプテリジン化合物由来の非常に強い蛍光が観測される。また、アメトプテリン(メトトレキサート(アルドリッチ))においても葉酸と同様に過酸化水素による酸化分解で強い蛍光が観察された(図には示していない)。
【実施例2】
【0049】
銅(II)イオン存在下での過酸化水素の定量
ビタミンBの一種である葉酸を使用し、金属イオンとして銅(II)イオンを用い、活性酸素である過酸化水素の定量を行った。
【0050】
本実施例1において、10μM葉酸、20μM銅(II)イオンを含む1.0mLの10mMリン酸緩衝液(pH7.6)と過酸化水素を1.5mLのマイクロチューブ中で加え、37℃で1時間反応させた。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
過酸化水素の濃度は、0.1μMから100μMで変化させた。
【0051】
この実施例2において、銅(II)イオンと過酸化水素の添加により試料の蛍光強度は増大した。
蛍光スペクトルは、プテリン−6−カルボン酸の蛍光スペクトルと一致し、蛍光物質としてプテリジン化合物の生成を示している。銅(II)イオン存在下、過酸化水素濃度の増大に従って蛍光強度が増大した。
試料の蛍光強度は、図2(黒丸)に示す通りである。
【0052】
比較におけるコントロール試料として、葉酸、銅(II)イオンを含み、過酸化水素を含まない溶液および葉酸と過酸化水素を含み、銅(II)イオンを含まない溶液を用いて、実施例2と同様に行った。
銅(II)イオンを添加していない場合には、蛍光の増強は観測されなかった。
試料の蛍光強度は、図2(白丸)に示す通りである。
【0053】
なお、実施例2と同様の方法で過酸化水素濃度に対する葉酸の蛍光強度の検量線を作成し、濃度未知の過酸化水素水に含まれる過酸化水素濃度を求めたところ、同試料に含まれる過酸化水素濃度を過マンガン酸カリウムを用いた酸化還元滴定により求めた値と一致した。過マンガン酸カリウムを用いた酸化還元滴定は、文献(化学実験第3版、東京大学教養学部化学教室化学教育研究会編、東京大学出版会、81〜83頁)の方法に従った。
【実施例3】
【0054】
他の金属イオン存在下での過酸化水素の定量
本実施例3では、葉酸、他の金属イオンを用い、活性酸素として過酸化水素の定量を行った。
即ち、本実施例3において、10μM葉酸、金属イオンとして20μM鉄(II)イオン(塩化鉄(II)四水和物(和光純薬工業株式会社))、20μMテトラクロロ金(III)酸四水和物(和光純薬工業株式会社)、20μMヘキサクロロ白金(IV)酸六水和物(和光純薬工業株式会社)、20μM硝酸銀のいずれかひとつを含む1.0mLの10mMリン酸緩衝液(pH7.6)と過酸化水素を1.5mLのマイクロチューブ中で加え、37℃で1時間反応した。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
【0055】
過酸化水素の濃度は、0.1μMから5μMで変化させた。
試料の蛍光強度は、図3(黒丸)に示す通りである。
図3によれば、鉄(II)イオンにより、過酸化水素が存在しない場合にも蛍光強度が増大した。
過酸化水素との反応による葉酸の蛍光強度の増大は、銅(II)イオンを用いた場合の方が鉄(II)イオンを用いた場合よりも感度が高い。
【0056】
比較は、コントロール試料として、葉酸、金属イオンとして鉄(II)イオン、テトラクロロ金(III)酸四水和物、ヘキサクロロ白金(IV)酸六水和物、硝酸銀のいずれかひとつを含み、過酸化水素を含まない溶液および葉酸と過酸化水素を含み、金属イオンを含まない溶液を用いて、実施例3と同様にして定量を行った。
鉄(II)イオンの結果を図3(白丸)に示す。同様に、テトラクロロ金(III)酸四水和物、ヘキサクロロ白金(IV)酸六水和物にも弱いながら効果が認められたが、硝酸銀ではその効果はほとんど認められなかった(図には示していない)。
【実施例4】
【0057】
葉酸の蛍光強度と過酸化水素濃度との関係
この実施例においては、葉酸の蛍光強度の増大の時間変化を測定した。
10μM葉酸、20μM銅(II)イオンを含む1.0mLの10mMリン酸緩衝液(pH7.6)と過酸化水素を1.5mLのマイクロチューブ中で加え、37℃で反応した。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
結果は、図4に示す通りである。
【0058】
反応時間に比例した蛍光強度の増大が観測された。蛍光強度の増大速度は、過酸化水素濃度に依存した。図4の傾きから蛍光強度の増大速度を計算すると過酸化水素濃度に比例した。
【0059】
比較におけるコントロール試料として、葉酸、銅(II)イオンを含み、過酸化水素を含まない溶液を用いて、実施例4と同様に行った。
その結果を図4(黒三角)に示す。
【0060】
従って、コントロール試料と過酸化水素を含む試料の蛍光強度を比較し、その増大量(ΔI)を反応時間で割り蛍光強度の増大速度を求めることができ、さらに過酸化水素濃度を計算で求めることができることを示している。
過酸化水素濃度を[H2O2]、比例定数をkと表すとΔI/反応時間=k×[H2O2]の式(式1)で表すことができる。
図4の傾きから蛍光強度の増大速度を求め、過酸化水素濃度に対してプロットし、得られた直線の傾きからkが求められる。
本実施例の条件では、kは、1.5μM-1min-1である。kは、使用する分光光度計の機種によっても異なり、濃度既知の過酸化水素を用いた測定によりあらかじめ求めることにより、未知濃度の過酸化水素の定量に利用できる。
【実施例5】
【0061】
セミカルバジドにより生成する過酸化水素の定量
発がん性物質セミカルバジドと銅(II)イオンとの反応で過酸化水素が生成し、DNA損傷が引き起こされることが報告されている(非特許文献4)。
葉酸の蛍光強度の測定により、セミカルバジドと銅(II)イオンとの反応で生成する過酸化水素の定量を行った。
【0062】
10μM葉酸、20μM銅(II)イオンとセミカルバジド(セミカルバジド塩酸塩(和光純薬工業株式会社))含む1.0mLの10mMリン酸緩衝液(pH7.6)を1.5mLのマイクロチューブ中で混合し、37℃で1時間反応させた。
セミカルバジドの濃度は、1μMから50μMで変化させた。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
その結果を、図5(黒丸)に示す。
【0063】
比較において、コントロール試料として、葉酸、セミカルバジドを含み、銅(II)イオンを含まない溶液を用いて、実施例5に準じて行った。
その結果を図5(白丸)に示す。
結果は、図5に示す通り、銅(II)イオン存在下、セミカルバジドの濃度の増大に従い、蛍光強度が増大した。一方、銅(II)イオンを含まない試料では変化はなかった。
【0064】
カタラーゼをあらかじめ添加すると蛍光の増大は完全に抑制された。カタラーゼは、過酸化水素をすみやかに水と酸素に分解する酵素であるため、葉酸の蛍光強度の増大は、過酸化水素によることが示された(図には示していない)。
比較におけるコントロール試料の蛍光強度と比較した蛍光の増大量から過酸化水素の生成速度を計算した。セミカルバジドと銅(II)イオンとの反応で過酸化水素が生成し、葉酸の酸化分解が起こり、蛍光強度の増大が起こるとき、ΔI=∫0Tk(T−t)rH2O2dtの式(式2)で蛍光強度の増大を表すことができる。
【0065】
この式で、ΔIおよびkは、式1に記載のものである。Tは、反応時間、tは任意の時間、rH2O2は、過酸化水素の生成速度を表している。セミカルバジドと銅(II)イオンとの反応時間に比例して過酸化水素が生成すると仮定すると、式2からrH2O2=2ΔI/kT2の式(式3)を求めることができる。上記の測定条件では、Tは、60分、kは、1.5μM-1min-1であり、図5に示す蛍光強度のデータからμM min-1単位の過酸化水素生成速度を計算することができる。
計算結果は、図5(白四角)に示す通りで、過酸化水素の生成速度がセミカルバジドの濃度の増大に従って大きくなることが示された。これにより、蛍光強度から試料中の過酸化水素生成速度およびセミカルバジド濃度が明らかとなる。
【実施例6】
【0066】
酸化された糖により生成する過酸化水素の定量
酸化チタン光触媒により酸化された糖と銅(II)イオンとの反応で過酸化水素を生成し、DNA損傷を引き起こすことが報告されている(非特許文献1)。
本発明を利用し、糖の酸化物から生成した過酸化水素量を求めた。
本実施例6では、1.5mLのマイクロチューブ中に酸化チタン(Degussa P-25、日本アエロジル株式会社),0.8mg mL-1)と10mMの糖(グルコース(和光純薬工業株式会社)、ガラクトース(和光純薬工業株式会社))を含む0.2mLの10mMリン酸緩衝液(pH7.6)を調製し、光照射(365nm,5Jcm-2)で、グルコースとガラクトースの酸化物を調製した。
【0067】
遠心分離(10,000回転/分、5分)で酸化チタン粒子を沈降させた後、糖の酸化物を含む上澄み液を糖濃度が図6の横軸に示す濃度になるように1.0mLの10mMリン酸緩衝液(pH7.6)中で10μM葉酸と20μM銅(II)イオンを含む溶液を調製した。37℃で1時間反応させ、実施例1と同様に蛍光測定した。
蛍光強度は、葉酸と反応させた糖の濃度の増大に従って増大した。蛍光強度の増大は、カタラーゼの添加で完全に抑制されたことから過酸化水素の生成が確認された(図には示していない)。
【0068】
上記と同様に式3を用いて、過酸化水素の生成速度(単位μM min-1)を計算した。さらに、過酸化水素の生成速度に反応時間をかけるとその反応時間の内に生成した過酸化水素量を計算することができる。反応時間1時間(60分)後の過酸化水素量を求めた例を図6に示す。
【実施例7】
【0069】
ベンゼンジオールにより生成する過酸化水素の測定
銅(II)イオンの触媒作用によるベンゼンジオールの自動酸化反応により過酸化水素が生成し、DNA損傷を引き起こすことが報告されている(非特許文献5)。
1,4−ベンゼンジオールの方が1,2−ベンゼンジオールよりも自動酸化速度が著しく速いことが報告されている。
本発明を利用し、葉酸の蛍光強度の増大から計算したベンゼンジオールの自動酸化による過酸化水素生成速度を求めた。
1.5mLのマイクロチューブ中で10μM葉酸、20μM銅(II)イオン、ベンゼンジオール(1,2−ベンゼンジオールには、カテコール(和光純薬工業株式会社)を使用し、1,4−ベンゼンジオールにはヒドロキノン(和光純薬工業株式会社)を使用した)を含む1.0mLの10mMリン酸緩衝液(pH7.6)を調製し、37℃で1時間反応させた。これらの試料の蛍光スペクトルを蛍光分光光度計(島津製作所RF−1500)を使用し、励起波長360nmで測定した。
銅(II)イオンを添加しない場合には、蛍光強度の増大は観測されなかった(図には示していない)。
【0070】
図7に示す通り、銅(II)イオン存在下、1,4−ベンゼンジオールを含む試料では、蛍光強度の増大が観測された。カタラーゼの添加で蛍光強度の増大が完全に抑制されたことから、過酸化水素による葉酸の酸化分解であることが確認された(図には示していない)。
1,2−ベンゼンジオールを含む試料では、蛍光強度の増大はほとんど観測されなかった。
この結果は、これまで報告されたDNA損傷の程度および自動酸化速度の違いとよく対応している。銅(II)イオンを添加していない場合には、蛍光の増強は観測されなかった。葉酸の蛍光強度の増大量から上記と同様に式3を用いて、過酸化水素の生成速度を計算した。計算結果を図7に示す。これにより、蛍光強度から試料中の過酸化水素生成速度および1,4−ベンゼンジオール濃度が明らかとなる。
【産業上の利用可能性】
【0071】
本発明の活性酸素の検出方法によれば、高価な試薬を用いることなく、安価な試薬と蛍光光度計とを用いて、高い感度で試料中の活性酸素の定量を行う検出試薬の開発が可能となる。本発明の方法によれば、活性酸素生成物質の探索及び定量、生成した活性酸素の定量を容易に実施することができる。さらに、生体内で生成する活性酸素検出用プローブとしての利用も可能である。そして、活性酸素生成物質の測定値を活性酸素生成等を介した酸化ストレスや生体分子損傷作用の簡便な評価法として利用できる。
【図面の簡単な説明】
【0072】
【図1】葉酸の酸化分解前後の蛍光スペクトルである。
【図2】実施例2における銅(II)イオン存在下、葉酸の酸化分解による蛍光強度の過酸化水素濃度依存性を示す。
【図3】実施例3における鉄(II)イオン存在下、葉酸の酸化分解による蛍光強度の過酸化水素濃度依存性を示す。
【図4】実施例4における銅(II)イオン存在下、過酸化水素による葉酸の蛍光強度の時間変化を示す。
【図5】実施例5におけるセミカルバジドとの反応による葉酸の蛍光強度及び蛍光強度から計算した過酸化水素生成速度とセミカルバジドの濃度との関係を示す。
【図6】実施例6における葉酸の蛍光強度の増大から計算した糖の酸化物から生成した過酸化水素生成量との関係を示す。
【図7】実施例7におけるベンゼンジオールとの反応による葉酸の蛍光強度及び蛍光強度から計算した過酸化水素生成速度とベンゼンジオールの濃度との関係を示す。
【特許請求の範囲】
【請求項1】
一般式1:
【化1】

〔但し、式中、R1は−OH、−OR、−R、−H、−NHR又は−NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕で示されるビタミンB又はその誘導体と金属イオンおよび活性酸素生成物質を含有する試料の存在下で、活性酸素により、当該ビタミンB又はその誘導体を酸化分解して、
一般式2:
【化2】

(但し、式中、R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)で示される可視光の蛍光を有するプテリジン類を生成させ、当該プテリジン類の蛍光強度を測定することによって活性酸素を定量することを特徴とする活性酸素の定量法。
【請求項2】
ビタミンB又はその誘導体が、一般式3:
【化3】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)、及び前記のRは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−OHで示されるものである、請求項1に記載の活性酸素の定量法。
【請求項3】
ビタミンB又はその誘導体が、一般式4:
【化4】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)及び前記のRは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−NH2で示されるものである請求項1に記載の活性酸素の定量法。
【請求項4】
金属イオンが二価または三価の金属イオンである請求項1に記載の活性酸素の定量法。
【請求項5】
金属イオンが二価の銅イオンである請求項1に記載の活性酸素の定量法。
【請求項6】
活性酸素が過酸化水素である請求項1に記載の活性酸素の定量法。
【請求項7】
ビタミンB又はその誘導体が、一般式5:
【化5】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、プテリジン類が、化学式1:
【化6】

で示される化合物である請求項1に記載の活性酸素の定量法。
【請求項8】
ビタミンB又はその誘導体が、一般式6:
【化7】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、プテリジン類が、化学式2:
【化8】

である、請求項1に記載の活性酸素の定量法。
【請求項9】
請求項1〜8のいずれか一項記載の活性酸素定量法から、活性酸素生成物質の量を測定する、活性酸素生成物質定量法。
【請求項1】
一般式1:
【化1】

〔但し、式中、R1は−OH、−OR、−R、−H、−NHR又は−NH2、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕で示されるビタミンB又はその誘導体と金属イオンおよび活性酸素生成物質を含有する試料の存在下で、活性酸素により、当該ビタミンB又はその誘導体を酸化分解して、
一般式2:
【化2】

(但し、式中、R1及びR2は前記と同じ意味を示し、R5は−COOH、−CHO又は−CH2OHを示す。)で示される可視光の蛍光を有するプテリジン類を生成させ、当該プテリジン類の蛍光強度を測定することによって活性酸素を定量することを特徴とする活性酸素の定量法。
【請求項2】
ビタミンB又はその誘導体が、一般式3:
【化3】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)、及び前記のRは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−OHで示されるものである、請求項1に記載の活性酸素の定量法。
【請求項3】
ビタミンB又はその誘導体が、一般式4:
【化4】

〔但し、式中、R2は−NH2、−OR、−R、−H又は−NHR、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)及び前記のRは炭素数1〜8の炭化水素基を示し、Xはハロゲンを示す。〕であって、プテリジン類に係わる一般式2におけるR1が−NH2で示されるものである請求項1に記載の活性酸素の定量法。
【請求項4】
金属イオンが二価または三価の金属イオンである請求項1に記載の活性酸素の定量法。
【請求項5】
金属イオンが二価の銅イオンである請求項1に記載の活性酸素の定量法。
【請求項6】
活性酸素が過酸化水素である請求項1に記載の活性酸素の定量法。
【請求項7】
ビタミンB又はその誘導体が、一般式5:
【化5】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、プテリジン類が、化学式1:
【化6】

で示される化合物である請求項1に記載の活性酸素の定量法。
【請求項8】
ビタミンB又はその誘導体が、一般式6:
【化7】

〔但し、式中、R3は−H、−COR、−COCX3又は−R、R4は−COOH、−CONHR、−COR、−COOR、−CONHCH(COOH)(CH2COOH)、−CONHCH(COOH)(CH2CH2COOH)又は−CONHCH(COOH)(CH2CH2PO(OH)CH(COOH)(CH2CH2COOH)を示す。前記のRは炭素数1〜8の炭化水素基を示す。Xはハロゲンを示す。〕であると共に、プテリジン類が、化学式2:
【化8】

である、請求項1に記載の活性酸素の定量法。
【請求項9】
請求項1〜8のいずれか一項記載の活性酸素定量法から、活性酸素生成物質の量を測定する、活性酸素生成物質定量法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2006−119085(P2006−119085A)
【公開日】平成18年5月11日(2006.5.11)
【国際特許分類】
【出願番号】特願2004−309573(P2004−309573)
【出願日】平成16年10月25日(2004.10.25)
【出願人】(304023318)国立大学法人静岡大学 (416)
【Fターム(参考)】
【公開日】平成18年5月11日(2006.5.11)
【国際特許分類】
【出願日】平成16年10月25日(2004.10.25)
【出願人】(304023318)国立大学法人静岡大学 (416)
【Fターム(参考)】
[ Back to top ]

