浸透圧薬物送達システム
経口浸透圧薬物送達システムは、基本的な浸透圧ポンプ送達システムで製剤化する場合に不規則又は不完全な放出プロファイルを示す高水溶性薬物、及び少なくとも1つの放出増強剤を含む。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、水への溶解度は高いが、例えば剤形の他の構成成分の存在下で溶解度が低下するために、不規則又は不完全な放出、例えば基本的な浸透圧ポンプ(EOP)送達システムからの放出を示す治療用化合物の経口浸透圧送達に関する。剤形の他の構成成分の存在下で溶解度が制限されることにより、不完全放出となることも多い。他の構成成分の存在下で溶解度の低下を示す薬剤には、完全放出を達成するために、剤形中の放出増強剤(放出促進剤としても知られている)が有用である。本発明は、元々溶解度は高いが、浸透圧剤形からの放出が制限されているすべての治療薬に対する経口浸透圧薬物送達システムに関する。
【背景技術】
【0002】
半透膜によって包囲された浸透圧活性薬物コアを有する持続放出錠は、当該技術分野において既知である。こうした浸透圧剤形は、胃液又は腸液由来の水を半透膜から通過させ、コア中の活性成分を溶解させることによって機能して、膜内の1つ又は複数の経路を通って活性成分を放出することができる。基本的な浸透圧ポンプ(EOP)送達システムは、制御された且つ予測可能な様式で送達されるために、薬物が溶解して存在することを必要とする。溶解した薬物は、半透膜を隔てて生成する浸透圧勾配に起因して送り出される。
【0003】
水性媒体への薬物の溶解度は通常、コア製剤において可溶化剤が必要かどうかを評価するための基準として使用される。難溶性薬剤の制限された溶解度という難題を克服するために、幾つかの薬物送達プラットフォームが開発された。薬物が不溶性である場合、基本的な浸透圧ポンプシステムは、適切に機能しない。水性溶媒に不溶な医薬を送達するための1つの手法が、Kuczynski et al.(米国特許第5,545,413号)によって開発された。彼らの手法において、錠剤又はカプセル剤の内側は、一方が医薬を(錠剤又はカプセル剤の壁にある、開口部又は孔を通ってさらに放出されるように)含有し、他方が水と接触すると膨潤する材料の層である2つのコア層によって特徴付けられる。水又は他の体液に曝されると平衡状態まで膨潤又は膨張する材料は、「オスモポリマー」と称される。この体積膨張を使用して、製造中に壁、シェル又はコーティング内に形成された開口部から医薬が物理的に押し出される。医薬は主に不溶性粒子(そのため、バイオアベイラビリティが制限されている)の形態で放出される。この方法は、一般的に「プッシュ/プル」手法と称されている。例えば、米国特許第5,422,123号;同第4,783,337号;同第4,765,989号;同第4,612,008号;及び同第4,327,725号を参照されたい。特許文献には、制御速度で且つ長時間、十分用量の広範な薬物を送達するこの手法が教示されている。
【0004】
他の浸透圧送達システムも記載されている。例えば、米国特許第4,609,374号;同第4,036,228号;同第4,992,278号;同第4,160,020号;及び同第4,615,698号を参照されたい。これらのタイプのシステムで使用されるオスモポリマーは、水及び水性液と相互作用すると膨潤することがその機能である構成成分である。これらの特許において、この膨潤効果は、液体を吸収して、非常に高度に膨張する(通常、2倍〜50倍の体積増加を示す)性質と定義されている。
【0005】
Rudnic et al.(米国特許第6,110,498号;同第6,284,276号;同第6,361,796号、及び同第6,514,532号)は、ラウリル硫酸ナトリウム及び他の可溶化剤を使用することにより、難溶性薬物であるグリピジドの溶解度を増大させて、基本タイプの浸透圧システムからグリピジドを持続的な様式で送達した。このRudnicのシステムは、(a)薬物送達の間、その完全性を維持し、且つそれを通る少なくとも1つの経路を有する半透壁;(b)当該壁内の単一、均一な組成物であって、本質的に(i)薬学的活性剤、(ii)薬学的活性剤の溶解度を増大させる少なくとも1つの非膨潤可溶化剤、(iii)少なくとも1つの非膨潤浸透圧剤、及び必要に応じて(iv)薬学的活性剤と入ってくる水性液との接触表面積を増加させる、組成物全体に分散した非膨潤ウィッキング剤から本質的に成る組成物から構成される。
【0006】
Thombre et al.(米国特許第5,697,922号)は、グリピジドの可溶化剤としてメグルミンを使用した。この特許では、メグルミンを半透性ポリマーフィルムでコーティングして、コアからの可溶化剤の放出を持続することが示唆されている。Thombre et al.は、カプセル化されていない可溶化剤が先にコアを離れて、薬物が未溶解形態で残ると主張した。この可溶化剤の減少は、不規則放出又は全く放出しないという結果をもたらす。本手法の課題は、錠剤の製造中に可溶化賦形剤のコーティングを伴うため、非常に複雑なことである。このプロセスでは、実用上の意義が制限される。また、この手法で使用される可溶化賦形剤の量は極めて多い。グリピジドを送達する浸透圧剤形における90%メグルミン(別名、N−メチルグルカミン)の使用を開示している、米国特許第5,698,220号も参照されたい。
【0007】
この先行技術は、単独で試験すると高水溶性であるが、浸透圧剤形の他の構成成分の存在下で、溶解度の制限、及び不規則又は不完全な放出が顕在化する薬物に対処していない。
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明は、先行技術の、高水溶性であるが、浸透圧剤形からの放出に難がある薬剤の送達における欠点を克服する。浸透圧送達システムにおいて難溶性薬物の送達を取り扱う幾つかの手法がある一方で、これらの手法のいずれも、高水溶性であるが、剤形の他の構成成分の存在下で溶解度及び放出が制限された薬剤の不完全且つ不規則な放出という課題に対処していない。このような薬物は、肺高血圧、肺動脈高血圧(PAH)、末梢血管疾患(PVD)、虚血性疾患(例えば、末梢血管疾患、レイノー現象、強皮症、心筋虚血、虚血性脳梗塞、腎不全)、心不全(鬱血性心不全を含む)、抗凝血を必要とする病態(例えば、MI後、心臓手術後)、血栓性微小血管症、体外循環、網膜中心静脈閉塞症、アテローム性動脈硬化症、炎症性疾患(例えば、乾癬)、高血圧、癌、又は細胞増殖が無秩序な他の病態、細胞/組織保存、及びプロスタサイクリン治療が有益な役割を有すると思われる他の新興治療領域の/ための治療で使用される価値の高い薬理学的活性化合物であるプロスタサイクリンによって例示され得る。
【0009】
プロスタサイクリンは、数分〜数時間の範囲の非常に短い半減期を特徴とし、これにより、本化合物の持続性経口送達が課題の多いものとなっている。プロスタサイクリンの化学的に安定なアナログであるトレプロスチニルは、先行技術による持続性経口送達での課題を提示している。トレプロスチニルナトリウム(Remodulin(登録商標))は、米国食品医薬品局(FDA)によって皮下投与及び静脈内投与が承認されているが、遊離酸としてのトレプロスチニルの絶対的経口バイオアベイラビリティは10%未満である。トレプロスチニルの経口製剤が開示されている(例えば、米国特許出願第20050165111号及び同第20050282903号、並びに米国特許第5153222号、同第5028628号、及び同第6054486号)が、これらの刊行物のいずれも経口制御放出剤形からのトレプロスチニルの不規則/不完全な放出の問題を扱っていない。Pharesに対する米国特許公開第20050282901号では、プロスタサイクリン(トレプロシニル(treprosinil))、及びトレプロスチニルの経口バイオアベイラビリティを増大させるさらなる心血管作動薬を含む組成物が開示されている。しかしながら、トレプロスチニルを唯一の活性剤として有する浸透圧徐放高バイオアベイラビリティ製剤についていかなる教示も示唆されていない。
【課題を解決するための手段】
【0010】
発明の要約
したがって、トレプロスチニル又はその塩若しくは誘導体を、経口投与によって完全且つ持続的に送達する安全且つ有効な方法に臨床的関心がある。本発明は、放出促進剤(単数又は複数)(放出増強剤)を組み込んで、このような薬剤の完全且つ予測可能な放出を達成する浸透圧薬物送達システムに関する。さらに、特に徐放固形剤形での、プロスタサイクリン、トレプロスチニルの経口送達方法に関する。
【0011】
本発明は、浸透圧制御/徐放剤形、即ち、標準的な浸透圧送達システムからの放出が不規則且つ/又は不完全であり、水への溶解度が少なくとも30mg/ml以上の、水への溶解度が高い薬剤(したがって、溶解度増強剤(単数又は複数)を無視しない)の完全且つ予測可能な放出を提供する。本発明のため、不規則放出は、同様の組成を有する錠剤間で一致しない放出と定義し(放出される平均(n=6)の%が25%超異なる)、不完全放出は、1日2回投与される薬物に関しては、10時間〜12時間で完全放出未満(80%以下)、1日1回投与される薬物に関しては、16時間〜24時間で80%以下と定義する。
【0012】
これらの不規則且つ/又は不完全な放出は、常法に従って、例えば、図に記載されるUSP溶出法によって測定されるin vitroでの放出を指す。
【0013】
本明細書中の「標準的な浸透圧送達システム」とは、基本的な浸透圧ポンプ(elementary osmotic pump; EOP)システムを意味する。EOPは、当業者には非常によく知られている。本システムを使用して、定義のように、「不規則」であるか、又は不完全な放出プロファイルを与える薬物を試験することができる。例えば、Felix Theeuwes著「基本的な浸透圧ポンプ(Elementary Osmotic Pump)」(Journal of Pharmaceutical Sciences, Vol. 64, No. 12, Pp 1987-1991, December 1975)を参照されたい。
【0014】
本発明で使用される放出増強剤(放出促進剤とも呼ばれる)は、制御された且つ所定の速度で薬物を送達しながら、薬剤の放出を促進する。本発明はまた、ここではトレプロスチニル又はその塩若しくは誘導体によって例示される、数分〜最大3時間の範囲の非常に短い半減期を示すプロスタサイクリン等、一群の薬剤の制御された且つ持続的な放出を提供する。
【0015】
本発明は、特定の治療目標を満足させるために、制御された且つ予測可能な様式でのこのような薬剤の経口送達に関する。好ましくは、本発明は、in vivoでの放出プロファイル(CMAX及び/又はAUC及び/又はTMAX)を標準的なin vitroでの溶出プロファイルから精度よく予測することができる、例えば、所望のin vivoでのプロファイルを日常的に達成するのに十分な信頼性を有する、薬物及びシステムを提供する。
【0016】
本発明の他の目的、特徴、及び利点は、以下の詳細な説明から明らかとなる。しかしながら、本発明の趣旨及び範囲内の各種変形形態及び変更形態が、詳細な説明から当業者に明らかとなるので、詳細な説明及び特定の実施例は、本発明の好ましい実施の形態を示す一方、単なる例示目的で示されていると理解されるべきである。
【0017】
本発明の各種特徴及び付随する利点は、添付の図面と関連付けて考えると、よりよく理解されるため、より完全に理解される。それらの図面では、同様の参照文字により、幾つかの図面全体にわたって同一又は類似の部分が指定される。
【発明を実施するための最良の形態】
【0018】
本発明は、水への溶解度が高く(少なくとも30mg/ml)、好ましくは、先行技術のような溶解度増強剤が必要ないか又は有用でないが、他のコア賦形剤の存在下での溶解度がかなり予測不可能な医薬の制御放出浸透圧送達の課題を解決するための代替案を提供する。コア製剤における予測不可能且つ不規則な溶解度の結果生じる薬物放出は、予測不可能であり且つかなり程度が小さい。コアにおけるこのような不規則な溶解度はまた、剤形からの薬物放出の速度及び程度に対する、pH、攪拌、及びイオン強度等の外部環境変数の効果を増幅させる。こうした溶解度及び送達の難点は、コア環境とは関係なく、コアにおける薬物の溶解度を増大させ、かつ、浸透圧システムからのこのような薬物の完全放出が可能になるように選択された放出増強剤を本発明の浸透圧送達システムに組み込むことによって克服される。したがって、本発明の浸透圧送達システムは、(a)浸透圧剤形に製剤化する場合に制限された且つ/又は不規則かつ予測不可能な放出を示す、水への溶解度が高い少なくとも1つの薬剤;(b)少なくとも1つの放出増強剤;(c)少なくとも1つの浸透圧剤;(d)必要に応じて、錠剤化を補助するための結合剤;(e)必要に応じて、錠剤化プロセスを補助するための少なくとも1つの滑沢剤;(f)典型的には少なくとも1つのコーティングポリマー;(g)必要に応じて、少なくとも1つの可塑剤を含む。
【0019】
本出願のため、以下の用語の定義が与えられる:
「錯化剤」及び「ミセル形成剤」という用語は、「レミントンの製薬の科学と実践(Remington's The Science and Practice of Pharmacy)」(第20版、Lippincott, Williams and Williams, 2000)第20版の第14章及び第20章にそれぞれ記載されるように本明細書中で使用される。
【0020】
ウィッキング剤は、送達剤形のネットワークに水を吸い込む能力を有する任意の材料と定義される。そうすることにより、ウィッキング剤は、主として可溶化形態になっている医薬の流路を増大させる。
【0021】
好適な放出増強剤としては、高HLB界面活性剤(例えば、Tween20、Tween60又はTween80)等のウィッキング剤;エチレンオキサイド−プロピレンオキサイドブロック共重合体(別名、Pluronics(登録商標))、ラウリル硫酸ナトリウム、ソディウムドキュセート等のイオン性界面活性剤、非膨潤親水性ポリマー(セルロースエーテル等)、及びポリエチレングリコール(PEG);ポリビニルピロリドン、シクロデキストリン等の錯化剤、及び非イオン性界面活性剤;並びにTween(ポリエチレンオキサイド変性ソルビタンモノエステル)、Span(脂肪酸ソルビタンエステル)、ラウリル硫酸ナトリウム、及びソディウムドキュセート等の界面活性剤であり得る、ミセル形成剤が挙げられる。
【0022】
放出増強剤は、コア錠剤処方に組み込まれ、処方の0.5重量%〜90重量%、好ましくは1重量%〜50重量%を構成する。より好ましくは、放出増強剤は、製剤の1重量%〜20重量%を構成する。それらは、造粒中又は造粒後に組み込むことができる。放出増強剤(単数又は複数)は、固体粉末の形態で添加することができ、また造粒中の液体に溶解させ、造粒中に噴霧することができる。薬物(単数又は複数)との均質混合を達成するために、放出増強剤は、他の賦形剤を組み込む前に薬物単独と混合することができる。代替的には、放出増強剤(単数又は複数)及び薬物は、造粒中の液体に溶解させ、造粒中に噴霧することができる。さらに別の方法において、放出増強剤(単数又は複数)及び薬物は、溶媒に溶解させることができ、溶液を乾燥させる場合には、そうして得られる固体塊を粉砕し、その後さらなる加工のために賦形剤の残りと混合することができる。
【0023】
浸透圧剤は当業者によく知られている。本発明に好適な浸透圧剤は、スクロース、キシリトール、グルコース、ラクトース等の単純な糖;塩化ナトリウム、塩化カリウム等の塩;セルロースエーテル、マルトデキストリン、及びシクロデキストリン等の低分子量親水性ポリマーである。本発明の製剤に組み込むことができる浸透圧剤の量は1重量%〜90重量%、好ましくは5重量%〜80重量%、最も好ましくは10重量%〜80重量%である。典型的には、浸透圧剤は造粒中に処方に組み込むことができる。
【0024】
また、顆粒は、所望の剤形:錠剤、カプセル剤又はペレットの製造を補助するために、他の賦形剤と混合することができる。錠剤は、標準的な回転式錠剤プレス上で圧縮される。
【0025】
典型的には、コア錠剤は少なくとも1つの可塑剤を含有する半透膜でコーティングされる。コーティングポリマーは、少なくとも1つの可塑剤と共に、適切な溶媒又は溶媒の混合物中に溶解させ、コーティングのために錠剤上に噴霧する。コーティングポリマーとしては、限定するものではないが、酢酸セルロースが挙げられる。コーティング膜は好ましくは、コートの柔軟性及び耐久性を向上させる少なくとも1つの可塑剤も含有する。このような可塑剤としては、限定するものではないが、クエン酸トリエチル(TEC)、プロピレングリコール(PG)、又はTECとPGとの比が25:75〜75:25の範囲であるそれらの混合物;Tween80、ポリエチレングリコール(PEG);他のポリオキシエチレンソルビタンエステル、トリアセチン、フタル酸ジエチル、鉱油、セバシン酸トリブチル、及びグリセロールが挙げられる。コーティングレベルは、1重量%〜25重量%、好ましくは2重量%〜20重量%、最も好ましくは3重量%〜10重量%で変動し得る。
【0026】
半透壁はまた、薬物(単数又は複数)の浸透圧送達を提供するための少なくとも1つの開口部を含む。概して、少なくとも1つの開口部の直径は50μm〜1000μm、好ましくは100μm〜800μmである。開口部は、レーザー又は任意の他の適切な穿孔システムを使用して穿孔することによって形成される。開口部は任意の形状であり得る。本発明について考慮される各種形状としては、限定するものではないが、丸形、十字形、長方形、菱形、星形、及び四角形が挙げられる。投与単位(浸透圧錠)が水を吸収すると、放出増強剤が溶液中に入り、薬物が溶出する環境を提供する。コア錠剤中の浸透圧剤(単数又は複数)は、水をコア錠剤へ吸い込み、半透膜を隔てた浸透圧勾配を作り出す。浸透圧勾配により、レーザーで穿孔した孔を通じて溶液中に薬物が押し出される。
【0027】
本発明は錠剤等の特定の剤形に限定されない。適切な放出増強剤を含有する剤形は、例えば、カプセル剤又はペレットの形態で調製することができる。薬物、放出増強剤、及び賦形剤の適切な組合せでカプセルを充填してすぐに、半透膜でコーティングされる。少なくとも1つの開口部が半透膜を通して穿孔されて、薬物放出が可能となる。
【0028】
本発明の経口浸透圧送達システムは、水への溶解度は高いが、標準的な浸透圧製剤からの放出が不完全又は不規則な薬物の完全且つ予測可能な放出を提供する。この完全且つ予測可能な放出は、少なくとも1つの放出増強剤を製剤に組み込むことによって達成される。本発明の製剤からのこのような薬物の放出は、pH及びイオン強度等のコア環境変数によって影響を受けない。このような放出は攪拌の程度にも依存しない。したがって、本発明の剤形は強固であり、薬剤の予測可能な放出を提供する。剤形はまた、in vitroでの放出プロファイルに基づいて予測することができるin vivoでの放出プロファイルを提供する。本発明による剤形はさらに、1日2回〜1回の投与を可能にして治療的価値を達成する薬剤の制御放出を提供する。このような投与は患者のコンプライアンスを向上させる。薬剤の制御送達は、薬剤の血中濃度におけるスパイクに関連する副作用を低減させる本質的にフラットな薬物動態プロファイルを生じる。
【0029】
本発明は、先行技術により課題が提示されていた、特に経口送達しにくく、且つ半減期の短い薬物であるトレプロスチニルによって例示される。トレプロスチニルは、プロスタサイクリンの化学的に安定なアナログであり、皮下投与及び静脈内投与が米国食品医薬品局(FDA)によって承認されており、特殊なポンプを使用して薬物が長期間にわたって送達される。本ポンプにより、制御された速度での患者への薬物の送達が可能となる。この型の投与の欠点は、複雑、高価であり、注射部位で反応を生じることである。本発明は、フラットな薬物動態プロファイルを生じる、制御された速度での本薬物の経口送達を提供する。注射による制御徐放経口投与の利点は当業者にとって価値が高い。特に、本発明は、約2時間〜8時間の時間、Cmin(0.1ng/ml〜0.2ng/ml)〜トレプロスチニルの最高血漿中濃度(約0.5ng/ml〜約2ng/ml)の間で変動する血漿中濃度を生じるのに有効な、経口投与されるトレプロスチニル徐放製剤を提供する。製剤は、1日2回のレジメンで、薬物の所望の定常状態での血中レベルが提供されるように設計され得る。またさらに、製剤は、所望の治療的に有効な血漿中薬物濃度プロファイルも提供する、持続放出製剤でのトレプロスチニルの1日1回の投薬に調整され得る。
【0030】
本発明はまた、プロスタサイクリン及びとりわけトレプロスチニルを使用する、肺高血圧、肺動脈高血圧(PAH)、虚血性疾患、心不全、抗凝血を必要とする病態、血栓性微小血管症、体外循環、網膜中心静脈閉塞症、アテローム性動脈硬化症、末梢血管疾患、炎症性疾患、高血圧、癌、又は細胞増殖が無秩序な他の病態、細胞/組織保存、及び他のプロスタサイクリン治療が有益な役割を有すると思われる新興治療領域の治療方法に関する。本発明の好ましい実施形態は、薬学的有効量のプロスタサイクリンアナログを徐放浸透圧投与製剤で経口投与することを含む、被験者における肺動脈高血圧及び/又は末梢血管疾患の治療方法である。
【0031】
プロスタサイクリンに加えて、本発明は、他の治療薬に有用である。それらは、高水溶性薬剤、例えば、塩酸シタロプラム、塩酸フルオキセチン、及びプロトリプチリン等の抗うつ薬;塩酸モリンドン及び塩酸クロルプロマジン等の抗精神病薬;塩酸トリフルペラジン(trifluperazine HCl)及びクロラゼプ酸二カリウム等の抗不安薬;硫酸ブレオマイシン及び塩酸クリンダマイシン等の抗生物質;アテノロール、リシノプリル、コハク酸メトプロロール、フマル酸ビソプロロール、ヒドロクロロチアジド、塩酸キナプリル、塩酸プロプラノロール、ペリンドプリルエルブミン、マレイン酸エナラプリル、及びとりわけカプトプリル等の降圧薬;塩酸テラゾシン及びクエン酸タモキシフェン等の抗悪性腫瘍薬;パーキンソン病の治療に使用される薬物、例えば、塩酸ビペリジン(biperidine HCl);ガバペンチン及び塩酸チアギャビン等の抗てんかん薬;グリコピロレート及び塩化トロスピウム等の抗コリン作動薬;塩酸プロメタジン等の抗アレルギー薬;二硝酸イソソルビド及びナドロール等の抗狭心症薬;塩酸ミドドリン等、起立性低血圧を治療するための薬物;アンフェタミン等の注意欠陥多動性障害(ADHD)薬;塩酸ヒドロモルホン、リン酸コデイン、及び塩酸メペリジン等の疼痛管理薬、並びに標準的な浸透圧剤形からのその完全放出が達成されていない上述されていない任意の他の高水溶性薬物によって表すことができる。他に規定しない限り、「a」又は「an」は、「1又はそれ以上」を意味する。また、当業者によって理解されるように、例えば「最大(up to)」、「少なくとも(at least)」、「より大きい(greater than)」、「未満(less than)」、「超(more than)」等のすべての語は、列挙される数を含み、且つ上記で説明したように、続けて部分範囲に分割することができる範囲を指す。同様に、本明細書中で開示されるすべての比は、より広範な比の範囲内にあるすべての部分比も含む。さらに、当業者はまた、成員がマーカッシュグループ等、一般的な様式で相互にグループ化される場合に、本発明が、全体として列記されたグループ全体だけでなく、個々にグループの各成員及び主要グループの考えられ得るすべてのサブグループを包含することを容易に認識する。本発明の他の目的、特徴、及び利点は、以下の実施例から明らかとなる。しかしながら、本発明の趣旨及び範囲内の各種変形形態及び変更形態が、詳細な説明から当業者に明らかとなるので、詳細な説明及び特定の実施例は、本発明の好ましい実施の形態を示す一方、単なる例示目的で示されていると理解されるべきである。
【実施例】
【0032】
本発明をよりよく理解することができるように、以下の実施例を記載する。これらの実施例は単なる例示目的であり、いかなる方法によっても本発明の範囲を限定するものと解釈されるべきではない。本発明の多数の他の変形形態は、本明細書中の開示内容を鑑みて、当業者によって理解される。示される正確な組成物、調製方法、及び実施形態は本発明の限定事項ではなく、任意の明白な変更形態が当業者には明らかである。
【0033】
[実施例1]
放出増強剤としてラウリル硫酸ナトリウム及びメグルミンを含有するトレプロスチニル浸透圧製剤の造粒
第1表は、放出増強剤を含む及び含まないトレプロスチニル浸透圧錠コアの組成を示す:
【0034】
【表1】

【0035】
すべての成分を、造粒前に18メッシュの篩いを通して篩い分けした。顆粒を、Glattの流動床造粒機(GPCG−1又はGPCG−15(Glatt(登録商標)、Air Techniques Inc.、ニュージャージー州ラムジー(Ramsey)))内で、トップスプレー(top spray)造粒によって製造した。2つの噴霧溶液を調製した。1つの溶液は、Maltrin M150(結合剤として使用する)及び薬物であるトレプロスチニルを含有した。第2の溶液は、Maltrin M150のみを含有した。予め篩い分けした成分を流動床造粒機に入れた。最初に噴霧溶液1、続いて噴霧溶液2を噴霧した。第2表に、造粒加工パラメータを示す。すべての噴霧溶液を噴霧してすぐに、顆粒を、水分レベルをモニタリングしながら流動床造粒機内で乾燥させた。3%未満の水分レベルを許容可能と見なした。乾燥した顆粒を18メッシュの篩いを通して篩い分けした。
【0036】
【表2】

【0037】
[実施例2]
実施例1による顆粒の錠剤化
実施例1による篩い分けした顆粒を、V型混合機内で3分〜5分間、ステアリン酸マグネシウムと混合した。混合物を、5/16インチの丸形標準凹状工具(concave tooling)(穿孔機及び金型)を使用して回転式錠剤プレス上で錠剤化した。錠剤の重量、硬さ、及び厚さを、圧縮操作を通じてモニタリングした。また、アッセイ及び含量均一性に関して錠剤を分析した。
【0038】
第3表は、トレプロスチニルコア錠剤の組成を示す:
【0039】
【表3】

【0040】
[実施例3]
実施例2による錠剤のコーティング
実施例1によるコア錠剤を、ポリマーとしての酢酸セルロース、及び可塑剤としてのポリエチレングリコール3350(PEG3350)を含有するコーティングシステムでコーティングした。コーティングは、LDCS−IIIパンコーター(Vector Corporation、アイオワ州マリオン(Marion))内で実施した。所望のコーティングレベルを達成するまで、コーティング溶液を、回転する有孔パン(perforated pan)内で錠剤上に噴霧した。
【0041】
[実施例4]
レーザー錠剤穿孔システムを使用する、実施例3によるコーティングした錠剤の穿孔
Lumonicsレーザー錠剤穿孔システム(Resonetics Inc、ニューハンプシャー州ナシュア(Nashua))を使用して、実施例3による錠剤のコーティング上に穿孔した。レーザー出力及びビーム直径を調整して所望の孔径を達成する。アッセイ、含量均一性及び溶出に関して、穿孔した錠剤を評価した。
【0042】
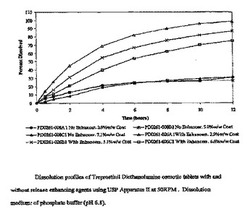
図1は、実施例5による錠剤の溶出プロファイルを示す。溶出は、USP装置IIを使用してパドル速度50RPMで行った。溶出媒体は、50mMリン酸緩衝液(pH6.8)であった。放出増強剤(単数又は複数)を含有する浸透圧錠からのトレプロスチニルの放出は、T10(10%放出までの時間)=0.25時間〜1時間;T50(50%放出までの時間)=2時間〜5時間、及びT80(80%放出までの時間)=6時間〜12時間で記述することができる。
【0043】
[実施例5]
放出増強剤としてラウリル硫酸ナトリウム(SLS)を含有する製剤の造粒及び錠剤化
【0044】
【表4】

【0045】
第4表は、顆粒及び錠剤の組成を示す。顆粒は、流動床造粒機(2kgスケール用GPCG−1及び10kgスケールバッチ用GPCG−15)内で、トップスプレー造粒によって製造した。2つの噴霧溶液を調製した。1つの溶液は、Maltrin M150(結合剤として使用する)及びトレプロスチニルジエタノールアミンを含有した。第2の溶液は、Maltrin M150のみを含有した。すべての成分を、18メッシュの篩いを通して篩い分けした。篩い分けした成分を流動床造粒機に入れた。最初に噴霧溶液1、続いて噴霧溶液2を噴霧した。第2表に、造粒加工パラメータを示す。すべての噴霧溶液を噴霧してすぐに、顆粒を、水分レベルをモニタリングしながら流動床造粒機内で乾燥させた。3%未満の水分レベルを許容可能と見なした。乾燥した顆粒を18メッシュの篩いを通して篩い分けした。乾燥顆粒を、適切なサイズのシェルが付いたPK V型混合機内で、ステアリン酸マグネシウムと混合した。混合時間は3分〜5分であった。その後、混合物を、標準的な5/16インチの凹状工具を使用して、回転式錠剤プレス上で圧縮した。錠剤の重量、硬さ、及び厚さを、圧縮操作を通じてモニタリングした。
【0046】
[実施例6]
実施例5による錠剤のコーティング及び穿孔
【0047】
【表5】

【0048】
第6表は、錠剤のコーティング加工パラメータを示す。
【0049】
【表6】

【0050】
錠剤をパンコーターに入れ、軽くゆすって温めた。排気温度をモニタリングしながら、コーティング溶液を噴霧した。錠剤を、各種コーティングレベル(重量基準)までコーティングした。第6表は、使用したコーティング加工パラメータを示す。コーティングした錠剤を、実施例2と同様に穿孔し、溶出に関して、穿孔した錠剤を試験した。本実施例で作製した錠剤の溶出プロファイルを、図2〜図5に示す。
【0051】
得られた溶出プロファイルは、T10(10%放出までの時間)=0.25時間〜1時間;T50(50%放出までの時間)=2時間〜5時間、及びT80(80%放出までの時間)=6時間〜12時間で記述することができる。図2は、浸透圧トレプロスチニル錠からのトレプロスチニルの放出に対する溶出条件(パドル速度、溶出媒体のイオン強度、溶出媒体のpH)の効果を示す。図3は、浸透圧トレプロスチニル錠からのトレプロスチニルの放出に対するコーティングレベル(重量基準)の効果を示す。図4は、トレプロスチニルの放出に対する開口直径の効果を示す。図5は、様々な量の活性薬物を含有する浸透圧トレプロスチニル錠の溶出プロファイルである。
【0052】
[実施例7]
実施例6によるトレプロスチニル浸透圧錠のヒトでの薬物動態研究
健常者において、12時間トレプロスチニル浸透圧錠製剤(lot# B05005)の安全性及びPKプロファイルを、8時間徐放(SR)錠製剤と比較することを目的とした。被験者(n=10)は、絶食状態又は摂食状態(標準的なFDA食)のいずれかで、単回用量(1mg)の浸透圧製剤を摂取した。そして被験者は、7日間の休薬期間を置いて、診療所に戻り、クロスオーバー処置(crossover treatment)を受けた。投薬日には、投薬後24時間までPK試料を採取し、診療所から退院するまで安全性を評価した。PK試料を、バリデートしたLC/MS/MSアッセイで分析した。図7に、薬物動態プロファイルを示す。結果からは、浸透圧錠製剤が、8時間SR(徐放)錠製剤と比較して、全身曝露を持続させることが示される。
【0053】
[実施例8]
浸透圧トレプロスチニル錠によるトレプロスチニルの薬物動態に対する食事の効果
健常者における摂食状態及び絶食状態での、12時間トレプロスチニル浸透圧錠製剤(lot# B05005)の安全性及びPKプロファイルを比較することを目的とした。被験者(n=10)は、絶食状態又は摂食状態(標準的なFDA食)のいずれかで、単回用量(1mg)の浸透圧製剤を摂取した。そして被験者は、7日間の休薬期間をおいて、診療所に戻り、クロスオーバー処置を受けた。投薬日には、投薬後24時間までPK試料を採取し、診療所から退院するまで安全性を評価した。PK試料を、バリデートしたLC/MS/MSアッセイで分析した。図7に、薬物動態プロファイルを示す。そこで示される結果は、摂食状態と絶食状態との間でPKプロファイルが異なり、摂食状態の方がトレプロスチニル全身曝露の持続期間が長いことを示す。摂食状態と絶食状態との間で安全性パラメータは類似しており、全体的な耐容性が非常に良好である。
【0054】
さらに詳述しなくても、当業者は先の説明を使用して、本発明を最大限に利用することができると考えられる。したがって、先の好ましい特定の実施形態は、単に例示であるに過ぎず、決して本開示内容の残り部分を限定するものではないと解釈される。
【0055】
上記及び本実施例において、特に明示しない限り、温度はすべて、℃でそのまま記載され、すべての部及び%は重量基準である。
【0056】
本明細書中に引用されるすべての出願、特許、及び刊行物の開示内容全体は、本明細書中に参照により援用される。
【0057】
先の実施例は、本発明の包括的又は具体的に記載した反応剤及び/又は操作条件を、先の実施例で使用したものの代わりに用いることによって、同様に首尾よく反復することができる。
【0058】
上記明細書から、当業者は、本発明の本質的特徴を容易に確定することができ、その趣旨及び範囲を逸脱することなく、本発明の各種変形形態及び変更形態を各種使用方法及び条件に適合させるようにすることができる。
【図面の簡単な説明】
【0059】
【図1】コア製剤が放出増強剤を含む場合及び放出増強剤を含まない場合の、トレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイルを表す。図1.USP装置IIを50RPMで使用する、トレプロスチニルジエタノールアミン浸透圧錠(放出増強剤あり及び放出増強剤なし)の溶出プロファイル。溶出媒体:リン酸緩衝液(pH6.8)。
【図2】トレプロスチニルジエタノールアミン浸透圧錠からのトレプロスチニルの放出に対する溶出条件の効果を示す。図2.USP装置IIを使用する、各種溶出条件(溶出媒体、パドル速度)下でのトレプロスチニルジエタノールアミン浸透圧錠の溶出。
【図3】トレプロスチニルジエタノールアミン浸透圧錠からのトレプロスチニルの放出に対する、コーティングレベル(重量基準)の効果を示す。図3.各種コーティングレベルまでコーティングしたトレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイル。
【図4】トレプロスチニルジエタノールアミン浸透圧錠からのトレプロスチニルの放出に対する孔径の効果を示す。図4.3重量%増加するまでコーティングし、各種孔径に穿孔したトレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイル。
【図5】様々な量の活性薬物(1mg、5mg、及び10mg)を含有するトレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイルを示す。図5.トレプロスチニルジエタノールアミン浸透圧錠1mg、5mg、及び10mgの溶出プロファイル。
【図6】経口液剤に対する、トレプロスチニルジエタノールアミン浸透圧錠及び対照用錠剤製剤のヒトでの薬物動態プロファイルを示す。図6.トレプロスチニルの経口液剤に対する、トレプロスチニルジエタノールアミン浸透圧錠及び比較物の薬物動態プロファイル。
【図7】食事を与えた場合及び食事を与えなかった場合の、トレプロスチニルジエタノールアミン浸透圧錠の薬物動態プロファイルを示す図である。図7.摂食条件及び絶食条件下での、トレプロスチニルジエタノールアミン浸透圧錠1mgの薬物動態プロファイル。
【技術分野】
【0001】
本発明は、水への溶解度は高いが、例えば剤形の他の構成成分の存在下で溶解度が低下するために、不規則又は不完全な放出、例えば基本的な浸透圧ポンプ(EOP)送達システムからの放出を示す治療用化合物の経口浸透圧送達に関する。剤形の他の構成成分の存在下で溶解度が制限されることにより、不完全放出となることも多い。他の構成成分の存在下で溶解度の低下を示す薬剤には、完全放出を達成するために、剤形中の放出増強剤(放出促進剤としても知られている)が有用である。本発明は、元々溶解度は高いが、浸透圧剤形からの放出が制限されているすべての治療薬に対する経口浸透圧薬物送達システムに関する。
【背景技術】
【0002】
半透膜によって包囲された浸透圧活性薬物コアを有する持続放出錠は、当該技術分野において既知である。こうした浸透圧剤形は、胃液又は腸液由来の水を半透膜から通過させ、コア中の活性成分を溶解させることによって機能して、膜内の1つ又は複数の経路を通って活性成分を放出することができる。基本的な浸透圧ポンプ(EOP)送達システムは、制御された且つ予測可能な様式で送達されるために、薬物が溶解して存在することを必要とする。溶解した薬物は、半透膜を隔てて生成する浸透圧勾配に起因して送り出される。
【0003】
水性媒体への薬物の溶解度は通常、コア製剤において可溶化剤が必要かどうかを評価するための基準として使用される。難溶性薬剤の制限された溶解度という難題を克服するために、幾つかの薬物送達プラットフォームが開発された。薬物が不溶性である場合、基本的な浸透圧ポンプシステムは、適切に機能しない。水性溶媒に不溶な医薬を送達するための1つの手法が、Kuczynski et al.(米国特許第5,545,413号)によって開発された。彼らの手法において、錠剤又はカプセル剤の内側は、一方が医薬を(錠剤又はカプセル剤の壁にある、開口部又は孔を通ってさらに放出されるように)含有し、他方が水と接触すると膨潤する材料の層である2つのコア層によって特徴付けられる。水又は他の体液に曝されると平衡状態まで膨潤又は膨張する材料は、「オスモポリマー」と称される。この体積膨張を使用して、製造中に壁、シェル又はコーティング内に形成された開口部から医薬が物理的に押し出される。医薬は主に不溶性粒子(そのため、バイオアベイラビリティが制限されている)の形態で放出される。この方法は、一般的に「プッシュ/プル」手法と称されている。例えば、米国特許第5,422,123号;同第4,783,337号;同第4,765,989号;同第4,612,008号;及び同第4,327,725号を参照されたい。特許文献には、制御速度で且つ長時間、十分用量の広範な薬物を送達するこの手法が教示されている。
【0004】
他の浸透圧送達システムも記載されている。例えば、米国特許第4,609,374号;同第4,036,228号;同第4,992,278号;同第4,160,020号;及び同第4,615,698号を参照されたい。これらのタイプのシステムで使用されるオスモポリマーは、水及び水性液と相互作用すると膨潤することがその機能である構成成分である。これらの特許において、この膨潤効果は、液体を吸収して、非常に高度に膨張する(通常、2倍〜50倍の体積増加を示す)性質と定義されている。
【0005】
Rudnic et al.(米国特許第6,110,498号;同第6,284,276号;同第6,361,796号、及び同第6,514,532号)は、ラウリル硫酸ナトリウム及び他の可溶化剤を使用することにより、難溶性薬物であるグリピジドの溶解度を増大させて、基本タイプの浸透圧システムからグリピジドを持続的な様式で送達した。このRudnicのシステムは、(a)薬物送達の間、その完全性を維持し、且つそれを通る少なくとも1つの経路を有する半透壁;(b)当該壁内の単一、均一な組成物であって、本質的に(i)薬学的活性剤、(ii)薬学的活性剤の溶解度を増大させる少なくとも1つの非膨潤可溶化剤、(iii)少なくとも1つの非膨潤浸透圧剤、及び必要に応じて(iv)薬学的活性剤と入ってくる水性液との接触表面積を増加させる、組成物全体に分散した非膨潤ウィッキング剤から本質的に成る組成物から構成される。
【0006】
Thombre et al.(米国特許第5,697,922号)は、グリピジドの可溶化剤としてメグルミンを使用した。この特許では、メグルミンを半透性ポリマーフィルムでコーティングして、コアからの可溶化剤の放出を持続することが示唆されている。Thombre et al.は、カプセル化されていない可溶化剤が先にコアを離れて、薬物が未溶解形態で残ると主張した。この可溶化剤の減少は、不規則放出又は全く放出しないという結果をもたらす。本手法の課題は、錠剤の製造中に可溶化賦形剤のコーティングを伴うため、非常に複雑なことである。このプロセスでは、実用上の意義が制限される。また、この手法で使用される可溶化賦形剤の量は極めて多い。グリピジドを送達する浸透圧剤形における90%メグルミン(別名、N−メチルグルカミン)の使用を開示している、米国特許第5,698,220号も参照されたい。
【0007】
この先行技術は、単独で試験すると高水溶性であるが、浸透圧剤形の他の構成成分の存在下で、溶解度の制限、及び不規則又は不完全な放出が顕在化する薬物に対処していない。
【発明の開示】
【発明が解決しようとする課題】
【0008】
本発明は、先行技術の、高水溶性であるが、浸透圧剤形からの放出に難がある薬剤の送達における欠点を克服する。浸透圧送達システムにおいて難溶性薬物の送達を取り扱う幾つかの手法がある一方で、これらの手法のいずれも、高水溶性であるが、剤形の他の構成成分の存在下で溶解度及び放出が制限された薬剤の不完全且つ不規則な放出という課題に対処していない。このような薬物は、肺高血圧、肺動脈高血圧(PAH)、末梢血管疾患(PVD)、虚血性疾患(例えば、末梢血管疾患、レイノー現象、強皮症、心筋虚血、虚血性脳梗塞、腎不全)、心不全(鬱血性心不全を含む)、抗凝血を必要とする病態(例えば、MI後、心臓手術後)、血栓性微小血管症、体外循環、網膜中心静脈閉塞症、アテローム性動脈硬化症、炎症性疾患(例えば、乾癬)、高血圧、癌、又は細胞増殖が無秩序な他の病態、細胞/組織保存、及びプロスタサイクリン治療が有益な役割を有すると思われる他の新興治療領域の/ための治療で使用される価値の高い薬理学的活性化合物であるプロスタサイクリンによって例示され得る。
【0009】
プロスタサイクリンは、数分〜数時間の範囲の非常に短い半減期を特徴とし、これにより、本化合物の持続性経口送達が課題の多いものとなっている。プロスタサイクリンの化学的に安定なアナログであるトレプロスチニルは、先行技術による持続性経口送達での課題を提示している。トレプロスチニルナトリウム(Remodulin(登録商標))は、米国食品医薬品局(FDA)によって皮下投与及び静脈内投与が承認されているが、遊離酸としてのトレプロスチニルの絶対的経口バイオアベイラビリティは10%未満である。トレプロスチニルの経口製剤が開示されている(例えば、米国特許出願第20050165111号及び同第20050282903号、並びに米国特許第5153222号、同第5028628号、及び同第6054486号)が、これらの刊行物のいずれも経口制御放出剤形からのトレプロスチニルの不規則/不完全な放出の問題を扱っていない。Pharesに対する米国特許公開第20050282901号では、プロスタサイクリン(トレプロシニル(treprosinil))、及びトレプロスチニルの経口バイオアベイラビリティを増大させるさらなる心血管作動薬を含む組成物が開示されている。しかしながら、トレプロスチニルを唯一の活性剤として有する浸透圧徐放高バイオアベイラビリティ製剤についていかなる教示も示唆されていない。
【課題を解決するための手段】
【0010】
発明の要約
したがって、トレプロスチニル又はその塩若しくは誘導体を、経口投与によって完全且つ持続的に送達する安全且つ有効な方法に臨床的関心がある。本発明は、放出促進剤(単数又は複数)(放出増強剤)を組み込んで、このような薬剤の完全且つ予測可能な放出を達成する浸透圧薬物送達システムに関する。さらに、特に徐放固形剤形での、プロスタサイクリン、トレプロスチニルの経口送達方法に関する。
【0011】
本発明は、浸透圧制御/徐放剤形、即ち、標準的な浸透圧送達システムからの放出が不規則且つ/又は不完全であり、水への溶解度が少なくとも30mg/ml以上の、水への溶解度が高い薬剤(したがって、溶解度増強剤(単数又は複数)を無視しない)の完全且つ予測可能な放出を提供する。本発明のため、不規則放出は、同様の組成を有する錠剤間で一致しない放出と定義し(放出される平均(n=6)の%が25%超異なる)、不完全放出は、1日2回投与される薬物に関しては、10時間〜12時間で完全放出未満(80%以下)、1日1回投与される薬物に関しては、16時間〜24時間で80%以下と定義する。
【0012】
これらの不規則且つ/又は不完全な放出は、常法に従って、例えば、図に記載されるUSP溶出法によって測定されるin vitroでの放出を指す。
【0013】
本明細書中の「標準的な浸透圧送達システム」とは、基本的な浸透圧ポンプ(elementary osmotic pump; EOP)システムを意味する。EOPは、当業者には非常によく知られている。本システムを使用して、定義のように、「不規則」であるか、又は不完全な放出プロファイルを与える薬物を試験することができる。例えば、Felix Theeuwes著「基本的な浸透圧ポンプ(Elementary Osmotic Pump)」(Journal of Pharmaceutical Sciences, Vol. 64, No. 12, Pp 1987-1991, December 1975)を参照されたい。
【0014】
本発明で使用される放出増強剤(放出促進剤とも呼ばれる)は、制御された且つ所定の速度で薬物を送達しながら、薬剤の放出を促進する。本発明はまた、ここではトレプロスチニル又はその塩若しくは誘導体によって例示される、数分〜最大3時間の範囲の非常に短い半減期を示すプロスタサイクリン等、一群の薬剤の制御された且つ持続的な放出を提供する。
【0015】
本発明は、特定の治療目標を満足させるために、制御された且つ予測可能な様式でのこのような薬剤の経口送達に関する。好ましくは、本発明は、in vivoでの放出プロファイル(CMAX及び/又はAUC及び/又はTMAX)を標準的なin vitroでの溶出プロファイルから精度よく予測することができる、例えば、所望のin vivoでのプロファイルを日常的に達成するのに十分な信頼性を有する、薬物及びシステムを提供する。
【0016】
本発明の他の目的、特徴、及び利点は、以下の詳細な説明から明らかとなる。しかしながら、本発明の趣旨及び範囲内の各種変形形態及び変更形態が、詳細な説明から当業者に明らかとなるので、詳細な説明及び特定の実施例は、本発明の好ましい実施の形態を示す一方、単なる例示目的で示されていると理解されるべきである。
【0017】
本発明の各種特徴及び付随する利点は、添付の図面と関連付けて考えると、よりよく理解されるため、より完全に理解される。それらの図面では、同様の参照文字により、幾つかの図面全体にわたって同一又は類似の部分が指定される。
【発明を実施するための最良の形態】
【0018】
本発明は、水への溶解度が高く(少なくとも30mg/ml)、好ましくは、先行技術のような溶解度増強剤が必要ないか又は有用でないが、他のコア賦形剤の存在下での溶解度がかなり予測不可能な医薬の制御放出浸透圧送達の課題を解決するための代替案を提供する。コア製剤における予測不可能且つ不規則な溶解度の結果生じる薬物放出は、予測不可能であり且つかなり程度が小さい。コアにおけるこのような不規則な溶解度はまた、剤形からの薬物放出の速度及び程度に対する、pH、攪拌、及びイオン強度等の外部環境変数の効果を増幅させる。こうした溶解度及び送達の難点は、コア環境とは関係なく、コアにおける薬物の溶解度を増大させ、かつ、浸透圧システムからのこのような薬物の完全放出が可能になるように選択された放出増強剤を本発明の浸透圧送達システムに組み込むことによって克服される。したがって、本発明の浸透圧送達システムは、(a)浸透圧剤形に製剤化する場合に制限された且つ/又は不規則かつ予測不可能な放出を示す、水への溶解度が高い少なくとも1つの薬剤;(b)少なくとも1つの放出増強剤;(c)少なくとも1つの浸透圧剤;(d)必要に応じて、錠剤化を補助するための結合剤;(e)必要に応じて、錠剤化プロセスを補助するための少なくとも1つの滑沢剤;(f)典型的には少なくとも1つのコーティングポリマー;(g)必要に応じて、少なくとも1つの可塑剤を含む。
【0019】
本出願のため、以下の用語の定義が与えられる:
「錯化剤」及び「ミセル形成剤」という用語は、「レミントンの製薬の科学と実践(Remington's The Science and Practice of Pharmacy)」(第20版、Lippincott, Williams and Williams, 2000)第20版の第14章及び第20章にそれぞれ記載されるように本明細書中で使用される。
【0020】
ウィッキング剤は、送達剤形のネットワークに水を吸い込む能力を有する任意の材料と定義される。そうすることにより、ウィッキング剤は、主として可溶化形態になっている医薬の流路を増大させる。
【0021】
好適な放出増強剤としては、高HLB界面活性剤(例えば、Tween20、Tween60又はTween80)等のウィッキング剤;エチレンオキサイド−プロピレンオキサイドブロック共重合体(別名、Pluronics(登録商標))、ラウリル硫酸ナトリウム、ソディウムドキュセート等のイオン性界面活性剤、非膨潤親水性ポリマー(セルロースエーテル等)、及びポリエチレングリコール(PEG);ポリビニルピロリドン、シクロデキストリン等の錯化剤、及び非イオン性界面活性剤;並びにTween(ポリエチレンオキサイド変性ソルビタンモノエステル)、Span(脂肪酸ソルビタンエステル)、ラウリル硫酸ナトリウム、及びソディウムドキュセート等の界面活性剤であり得る、ミセル形成剤が挙げられる。
【0022】
放出増強剤は、コア錠剤処方に組み込まれ、処方の0.5重量%〜90重量%、好ましくは1重量%〜50重量%を構成する。より好ましくは、放出増強剤は、製剤の1重量%〜20重量%を構成する。それらは、造粒中又は造粒後に組み込むことができる。放出増強剤(単数又は複数)は、固体粉末の形態で添加することができ、また造粒中の液体に溶解させ、造粒中に噴霧することができる。薬物(単数又は複数)との均質混合を達成するために、放出増強剤は、他の賦形剤を組み込む前に薬物単独と混合することができる。代替的には、放出増強剤(単数又は複数)及び薬物は、造粒中の液体に溶解させ、造粒中に噴霧することができる。さらに別の方法において、放出増強剤(単数又は複数)及び薬物は、溶媒に溶解させることができ、溶液を乾燥させる場合には、そうして得られる固体塊を粉砕し、その後さらなる加工のために賦形剤の残りと混合することができる。
【0023】
浸透圧剤は当業者によく知られている。本発明に好適な浸透圧剤は、スクロース、キシリトール、グルコース、ラクトース等の単純な糖;塩化ナトリウム、塩化カリウム等の塩;セルロースエーテル、マルトデキストリン、及びシクロデキストリン等の低分子量親水性ポリマーである。本発明の製剤に組み込むことができる浸透圧剤の量は1重量%〜90重量%、好ましくは5重量%〜80重量%、最も好ましくは10重量%〜80重量%である。典型的には、浸透圧剤は造粒中に処方に組み込むことができる。
【0024】
また、顆粒は、所望の剤形:錠剤、カプセル剤又はペレットの製造を補助するために、他の賦形剤と混合することができる。錠剤は、標準的な回転式錠剤プレス上で圧縮される。
【0025】
典型的には、コア錠剤は少なくとも1つの可塑剤を含有する半透膜でコーティングされる。コーティングポリマーは、少なくとも1つの可塑剤と共に、適切な溶媒又は溶媒の混合物中に溶解させ、コーティングのために錠剤上に噴霧する。コーティングポリマーとしては、限定するものではないが、酢酸セルロースが挙げられる。コーティング膜は好ましくは、コートの柔軟性及び耐久性を向上させる少なくとも1つの可塑剤も含有する。このような可塑剤としては、限定するものではないが、クエン酸トリエチル(TEC)、プロピレングリコール(PG)、又はTECとPGとの比が25:75〜75:25の範囲であるそれらの混合物;Tween80、ポリエチレングリコール(PEG);他のポリオキシエチレンソルビタンエステル、トリアセチン、フタル酸ジエチル、鉱油、セバシン酸トリブチル、及びグリセロールが挙げられる。コーティングレベルは、1重量%〜25重量%、好ましくは2重量%〜20重量%、最も好ましくは3重量%〜10重量%で変動し得る。
【0026】
半透壁はまた、薬物(単数又は複数)の浸透圧送達を提供するための少なくとも1つの開口部を含む。概して、少なくとも1つの開口部の直径は50μm〜1000μm、好ましくは100μm〜800μmである。開口部は、レーザー又は任意の他の適切な穿孔システムを使用して穿孔することによって形成される。開口部は任意の形状であり得る。本発明について考慮される各種形状としては、限定するものではないが、丸形、十字形、長方形、菱形、星形、及び四角形が挙げられる。投与単位(浸透圧錠)が水を吸収すると、放出増強剤が溶液中に入り、薬物が溶出する環境を提供する。コア錠剤中の浸透圧剤(単数又は複数)は、水をコア錠剤へ吸い込み、半透膜を隔てた浸透圧勾配を作り出す。浸透圧勾配により、レーザーで穿孔した孔を通じて溶液中に薬物が押し出される。
【0027】
本発明は錠剤等の特定の剤形に限定されない。適切な放出増強剤を含有する剤形は、例えば、カプセル剤又はペレットの形態で調製することができる。薬物、放出増強剤、及び賦形剤の適切な組合せでカプセルを充填してすぐに、半透膜でコーティングされる。少なくとも1つの開口部が半透膜を通して穿孔されて、薬物放出が可能となる。
【0028】
本発明の経口浸透圧送達システムは、水への溶解度は高いが、標準的な浸透圧製剤からの放出が不完全又は不規則な薬物の完全且つ予測可能な放出を提供する。この完全且つ予測可能な放出は、少なくとも1つの放出増強剤を製剤に組み込むことによって達成される。本発明の製剤からのこのような薬物の放出は、pH及びイオン強度等のコア環境変数によって影響を受けない。このような放出は攪拌の程度にも依存しない。したがって、本発明の剤形は強固であり、薬剤の予測可能な放出を提供する。剤形はまた、in vitroでの放出プロファイルに基づいて予測することができるin vivoでの放出プロファイルを提供する。本発明による剤形はさらに、1日2回〜1回の投与を可能にして治療的価値を達成する薬剤の制御放出を提供する。このような投与は患者のコンプライアンスを向上させる。薬剤の制御送達は、薬剤の血中濃度におけるスパイクに関連する副作用を低減させる本質的にフラットな薬物動態プロファイルを生じる。
【0029】
本発明は、先行技術により課題が提示されていた、特に経口送達しにくく、且つ半減期の短い薬物であるトレプロスチニルによって例示される。トレプロスチニルは、プロスタサイクリンの化学的に安定なアナログであり、皮下投与及び静脈内投与が米国食品医薬品局(FDA)によって承認されており、特殊なポンプを使用して薬物が長期間にわたって送達される。本ポンプにより、制御された速度での患者への薬物の送達が可能となる。この型の投与の欠点は、複雑、高価であり、注射部位で反応を生じることである。本発明は、フラットな薬物動態プロファイルを生じる、制御された速度での本薬物の経口送達を提供する。注射による制御徐放経口投与の利点は当業者にとって価値が高い。特に、本発明は、約2時間〜8時間の時間、Cmin(0.1ng/ml〜0.2ng/ml)〜トレプロスチニルの最高血漿中濃度(約0.5ng/ml〜約2ng/ml)の間で変動する血漿中濃度を生じるのに有効な、経口投与されるトレプロスチニル徐放製剤を提供する。製剤は、1日2回のレジメンで、薬物の所望の定常状態での血中レベルが提供されるように設計され得る。またさらに、製剤は、所望の治療的に有効な血漿中薬物濃度プロファイルも提供する、持続放出製剤でのトレプロスチニルの1日1回の投薬に調整され得る。
【0030】
本発明はまた、プロスタサイクリン及びとりわけトレプロスチニルを使用する、肺高血圧、肺動脈高血圧(PAH)、虚血性疾患、心不全、抗凝血を必要とする病態、血栓性微小血管症、体外循環、網膜中心静脈閉塞症、アテローム性動脈硬化症、末梢血管疾患、炎症性疾患、高血圧、癌、又は細胞増殖が無秩序な他の病態、細胞/組織保存、及び他のプロスタサイクリン治療が有益な役割を有すると思われる新興治療領域の治療方法に関する。本発明の好ましい実施形態は、薬学的有効量のプロスタサイクリンアナログを徐放浸透圧投与製剤で経口投与することを含む、被験者における肺動脈高血圧及び/又は末梢血管疾患の治療方法である。
【0031】
プロスタサイクリンに加えて、本発明は、他の治療薬に有用である。それらは、高水溶性薬剤、例えば、塩酸シタロプラム、塩酸フルオキセチン、及びプロトリプチリン等の抗うつ薬;塩酸モリンドン及び塩酸クロルプロマジン等の抗精神病薬;塩酸トリフルペラジン(trifluperazine HCl)及びクロラゼプ酸二カリウム等の抗不安薬;硫酸ブレオマイシン及び塩酸クリンダマイシン等の抗生物質;アテノロール、リシノプリル、コハク酸メトプロロール、フマル酸ビソプロロール、ヒドロクロロチアジド、塩酸キナプリル、塩酸プロプラノロール、ペリンドプリルエルブミン、マレイン酸エナラプリル、及びとりわけカプトプリル等の降圧薬;塩酸テラゾシン及びクエン酸タモキシフェン等の抗悪性腫瘍薬;パーキンソン病の治療に使用される薬物、例えば、塩酸ビペリジン(biperidine HCl);ガバペンチン及び塩酸チアギャビン等の抗てんかん薬;グリコピロレート及び塩化トロスピウム等の抗コリン作動薬;塩酸プロメタジン等の抗アレルギー薬;二硝酸イソソルビド及びナドロール等の抗狭心症薬;塩酸ミドドリン等、起立性低血圧を治療するための薬物;アンフェタミン等の注意欠陥多動性障害(ADHD)薬;塩酸ヒドロモルホン、リン酸コデイン、及び塩酸メペリジン等の疼痛管理薬、並びに標準的な浸透圧剤形からのその完全放出が達成されていない上述されていない任意の他の高水溶性薬物によって表すことができる。他に規定しない限り、「a」又は「an」は、「1又はそれ以上」を意味する。また、当業者によって理解されるように、例えば「最大(up to)」、「少なくとも(at least)」、「より大きい(greater than)」、「未満(less than)」、「超(more than)」等のすべての語は、列挙される数を含み、且つ上記で説明したように、続けて部分範囲に分割することができる範囲を指す。同様に、本明細書中で開示されるすべての比は、より広範な比の範囲内にあるすべての部分比も含む。さらに、当業者はまた、成員がマーカッシュグループ等、一般的な様式で相互にグループ化される場合に、本発明が、全体として列記されたグループ全体だけでなく、個々にグループの各成員及び主要グループの考えられ得るすべてのサブグループを包含することを容易に認識する。本発明の他の目的、特徴、及び利点は、以下の実施例から明らかとなる。しかしながら、本発明の趣旨及び範囲内の各種変形形態及び変更形態が、詳細な説明から当業者に明らかとなるので、詳細な説明及び特定の実施例は、本発明の好ましい実施の形態を示す一方、単なる例示目的で示されていると理解されるべきである。
【実施例】
【0032】
本発明をよりよく理解することができるように、以下の実施例を記載する。これらの実施例は単なる例示目的であり、いかなる方法によっても本発明の範囲を限定するものと解釈されるべきではない。本発明の多数の他の変形形態は、本明細書中の開示内容を鑑みて、当業者によって理解される。示される正確な組成物、調製方法、及び実施形態は本発明の限定事項ではなく、任意の明白な変更形態が当業者には明らかである。
【0033】
[実施例1]
放出増強剤としてラウリル硫酸ナトリウム及びメグルミンを含有するトレプロスチニル浸透圧製剤の造粒
第1表は、放出増強剤を含む及び含まないトレプロスチニル浸透圧錠コアの組成を示す:
【0034】
【表1】

【0035】
すべての成分を、造粒前に18メッシュの篩いを通して篩い分けした。顆粒を、Glattの流動床造粒機(GPCG−1又はGPCG−15(Glatt(登録商標)、Air Techniques Inc.、ニュージャージー州ラムジー(Ramsey)))内で、トップスプレー(top spray)造粒によって製造した。2つの噴霧溶液を調製した。1つの溶液は、Maltrin M150(結合剤として使用する)及び薬物であるトレプロスチニルを含有した。第2の溶液は、Maltrin M150のみを含有した。予め篩い分けした成分を流動床造粒機に入れた。最初に噴霧溶液1、続いて噴霧溶液2を噴霧した。第2表に、造粒加工パラメータを示す。すべての噴霧溶液を噴霧してすぐに、顆粒を、水分レベルをモニタリングしながら流動床造粒機内で乾燥させた。3%未満の水分レベルを許容可能と見なした。乾燥した顆粒を18メッシュの篩いを通して篩い分けした。
【0036】
【表2】

【0037】
[実施例2]
実施例1による顆粒の錠剤化
実施例1による篩い分けした顆粒を、V型混合機内で3分〜5分間、ステアリン酸マグネシウムと混合した。混合物を、5/16インチの丸形標準凹状工具(concave tooling)(穿孔機及び金型)を使用して回転式錠剤プレス上で錠剤化した。錠剤の重量、硬さ、及び厚さを、圧縮操作を通じてモニタリングした。また、アッセイ及び含量均一性に関して錠剤を分析した。
【0038】
第3表は、トレプロスチニルコア錠剤の組成を示す:
【0039】
【表3】

【0040】
[実施例3]
実施例2による錠剤のコーティング
実施例1によるコア錠剤を、ポリマーとしての酢酸セルロース、及び可塑剤としてのポリエチレングリコール3350(PEG3350)を含有するコーティングシステムでコーティングした。コーティングは、LDCS−IIIパンコーター(Vector Corporation、アイオワ州マリオン(Marion))内で実施した。所望のコーティングレベルを達成するまで、コーティング溶液を、回転する有孔パン(perforated pan)内で錠剤上に噴霧した。
【0041】
[実施例4]
レーザー錠剤穿孔システムを使用する、実施例3によるコーティングした錠剤の穿孔
Lumonicsレーザー錠剤穿孔システム(Resonetics Inc、ニューハンプシャー州ナシュア(Nashua))を使用して、実施例3による錠剤のコーティング上に穿孔した。レーザー出力及びビーム直径を調整して所望の孔径を達成する。アッセイ、含量均一性及び溶出に関して、穿孔した錠剤を評価した。
【0042】
図1は、実施例5による錠剤の溶出プロファイルを示す。溶出は、USP装置IIを使用してパドル速度50RPMで行った。溶出媒体は、50mMリン酸緩衝液(pH6.8)であった。放出増強剤(単数又は複数)を含有する浸透圧錠からのトレプロスチニルの放出は、T10(10%放出までの時間)=0.25時間〜1時間;T50(50%放出までの時間)=2時間〜5時間、及びT80(80%放出までの時間)=6時間〜12時間で記述することができる。
【0043】
[実施例5]
放出増強剤としてラウリル硫酸ナトリウム(SLS)を含有する製剤の造粒及び錠剤化
【0044】
【表4】

【0045】
第4表は、顆粒及び錠剤の組成を示す。顆粒は、流動床造粒機(2kgスケール用GPCG−1及び10kgスケールバッチ用GPCG−15)内で、トップスプレー造粒によって製造した。2つの噴霧溶液を調製した。1つの溶液は、Maltrin M150(結合剤として使用する)及びトレプロスチニルジエタノールアミンを含有した。第2の溶液は、Maltrin M150のみを含有した。すべての成分を、18メッシュの篩いを通して篩い分けした。篩い分けした成分を流動床造粒機に入れた。最初に噴霧溶液1、続いて噴霧溶液2を噴霧した。第2表に、造粒加工パラメータを示す。すべての噴霧溶液を噴霧してすぐに、顆粒を、水分レベルをモニタリングしながら流動床造粒機内で乾燥させた。3%未満の水分レベルを許容可能と見なした。乾燥した顆粒を18メッシュの篩いを通して篩い分けした。乾燥顆粒を、適切なサイズのシェルが付いたPK V型混合機内で、ステアリン酸マグネシウムと混合した。混合時間は3分〜5分であった。その後、混合物を、標準的な5/16インチの凹状工具を使用して、回転式錠剤プレス上で圧縮した。錠剤の重量、硬さ、及び厚さを、圧縮操作を通じてモニタリングした。
【0046】
[実施例6]
実施例5による錠剤のコーティング及び穿孔
【0047】
【表5】

【0048】
第6表は、錠剤のコーティング加工パラメータを示す。
【0049】
【表6】

【0050】
錠剤をパンコーターに入れ、軽くゆすって温めた。排気温度をモニタリングしながら、コーティング溶液を噴霧した。錠剤を、各種コーティングレベル(重量基準)までコーティングした。第6表は、使用したコーティング加工パラメータを示す。コーティングした錠剤を、実施例2と同様に穿孔し、溶出に関して、穿孔した錠剤を試験した。本実施例で作製した錠剤の溶出プロファイルを、図2〜図5に示す。
【0051】
得られた溶出プロファイルは、T10(10%放出までの時間)=0.25時間〜1時間;T50(50%放出までの時間)=2時間〜5時間、及びT80(80%放出までの時間)=6時間〜12時間で記述することができる。図2は、浸透圧トレプロスチニル錠からのトレプロスチニルの放出に対する溶出条件(パドル速度、溶出媒体のイオン強度、溶出媒体のpH)の効果を示す。図3は、浸透圧トレプロスチニル錠からのトレプロスチニルの放出に対するコーティングレベル(重量基準)の効果を示す。図4は、トレプロスチニルの放出に対する開口直径の効果を示す。図5は、様々な量の活性薬物を含有する浸透圧トレプロスチニル錠の溶出プロファイルである。
【0052】
[実施例7]
実施例6によるトレプロスチニル浸透圧錠のヒトでの薬物動態研究
健常者において、12時間トレプロスチニル浸透圧錠製剤(lot# B05005)の安全性及びPKプロファイルを、8時間徐放(SR)錠製剤と比較することを目的とした。被験者(n=10)は、絶食状態又は摂食状態(標準的なFDA食)のいずれかで、単回用量(1mg)の浸透圧製剤を摂取した。そして被験者は、7日間の休薬期間を置いて、診療所に戻り、クロスオーバー処置(crossover treatment)を受けた。投薬日には、投薬後24時間までPK試料を採取し、診療所から退院するまで安全性を評価した。PK試料を、バリデートしたLC/MS/MSアッセイで分析した。図7に、薬物動態プロファイルを示す。結果からは、浸透圧錠製剤が、8時間SR(徐放)錠製剤と比較して、全身曝露を持続させることが示される。
【0053】
[実施例8]
浸透圧トレプロスチニル錠によるトレプロスチニルの薬物動態に対する食事の効果
健常者における摂食状態及び絶食状態での、12時間トレプロスチニル浸透圧錠製剤(lot# B05005)の安全性及びPKプロファイルを比較することを目的とした。被験者(n=10)は、絶食状態又は摂食状態(標準的なFDA食)のいずれかで、単回用量(1mg)の浸透圧製剤を摂取した。そして被験者は、7日間の休薬期間をおいて、診療所に戻り、クロスオーバー処置を受けた。投薬日には、投薬後24時間までPK試料を採取し、診療所から退院するまで安全性を評価した。PK試料を、バリデートしたLC/MS/MSアッセイで分析した。図7に、薬物動態プロファイルを示す。そこで示される結果は、摂食状態と絶食状態との間でPKプロファイルが異なり、摂食状態の方がトレプロスチニル全身曝露の持続期間が長いことを示す。摂食状態と絶食状態との間で安全性パラメータは類似しており、全体的な耐容性が非常に良好である。
【0054】
さらに詳述しなくても、当業者は先の説明を使用して、本発明を最大限に利用することができると考えられる。したがって、先の好ましい特定の実施形態は、単に例示であるに過ぎず、決して本開示内容の残り部分を限定するものではないと解釈される。
【0055】
上記及び本実施例において、特に明示しない限り、温度はすべて、℃でそのまま記載され、すべての部及び%は重量基準である。
【0056】
本明細書中に引用されるすべての出願、特許、及び刊行物の開示内容全体は、本明細書中に参照により援用される。
【0057】
先の実施例は、本発明の包括的又は具体的に記載した反応剤及び/又は操作条件を、先の実施例で使用したものの代わりに用いることによって、同様に首尾よく反復することができる。
【0058】
上記明細書から、当業者は、本発明の本質的特徴を容易に確定することができ、その趣旨及び範囲を逸脱することなく、本発明の各種変形形態及び変更形態を各種使用方法及び条件に適合させるようにすることができる。
【図面の簡単な説明】
【0059】
【図1】コア製剤が放出増強剤を含む場合及び放出増強剤を含まない場合の、トレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイルを表す。図1.USP装置IIを50RPMで使用する、トレプロスチニルジエタノールアミン浸透圧錠(放出増強剤あり及び放出増強剤なし)の溶出プロファイル。溶出媒体:リン酸緩衝液(pH6.8)。
【図2】トレプロスチニルジエタノールアミン浸透圧錠からのトレプロスチニルの放出に対する溶出条件の効果を示す。図2.USP装置IIを使用する、各種溶出条件(溶出媒体、パドル速度)下でのトレプロスチニルジエタノールアミン浸透圧錠の溶出。
【図3】トレプロスチニルジエタノールアミン浸透圧錠からのトレプロスチニルの放出に対する、コーティングレベル(重量基準)の効果を示す。図3.各種コーティングレベルまでコーティングしたトレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイル。
【図4】トレプロスチニルジエタノールアミン浸透圧錠からのトレプロスチニルの放出に対する孔径の効果を示す。図4.3重量%増加するまでコーティングし、各種孔径に穿孔したトレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイル。
【図5】様々な量の活性薬物(1mg、5mg、及び10mg)を含有するトレプロスチニルジエタノールアミン浸透圧錠の溶出プロファイルを示す。図5.トレプロスチニルジエタノールアミン浸透圧錠1mg、5mg、及び10mgの溶出プロファイル。
【図6】経口液剤に対する、トレプロスチニルジエタノールアミン浸透圧錠及び対照用錠剤製剤のヒトでの薬物動態プロファイルを示す。図6.トレプロスチニルの経口液剤に対する、トレプロスチニルジエタノールアミン浸透圧錠及び比較物の薬物動態プロファイル。
【図7】食事を与えた場合及び食事を与えなかった場合の、トレプロスチニルジエタノールアミン浸透圧錠の薬物動態プロファイルを示す図である。図7.摂食条件及び絶食条件下での、トレプロスチニルジエタノールアミン浸透圧錠1mgの薬物動態プロファイル。
【特許請求の範囲】
【請求項1】
標準的な浸透圧送達システムで製剤化する場合に不規則又は不完全な放出プロファイルを示す高水溶性薬物、及び少なくとも1つの放出増強剤を含む、経口浸透圧薬物送達システム。
【請求項2】
前記薬物の水への溶解度が少なくとも約30mg/mlである、請求項1に記載の経口浸透圧薬物送達システム。
【請求項3】
in vitroでの放出プロファイルから予測され得るin vivoでの放出プロファイルを示す、請求項1に記載の経口浸透圧薬物送達システム。
【請求項4】
前記経口浸透圧薬物送達システムが徐放送達システムである、請求項2に記載の経口浸透圧薬物送達システム。
【請求項5】
前記薬物が短い半減期を有する、請求項4に記載の経口浸透圧薬物送達システム。
【請求項6】
前記半減期が数分〜3時間の範囲である、請求項5に記載の経口浸透圧薬物送達システム。
【請求項7】
前記薬物がプロスタサイクリンである、請求項6に記載の経口浸透圧薬物送達システム。
【請求項8】
前記プロスタサイクリンがトレプロスチニル又はその誘導体若しくは塩である、請求項7に記載の経口浸透圧薬物送達システム。
【請求項9】
トレプロスチニル又はその薬学的に許容される誘導体の量が、トレプロスチニルの治療的に有効な血漿中濃度を生じるのに十分である、請求項8に記載の経口浸透圧薬物送達システム。
【請求項10】
前記トレプロスチニルの治療的に有効な血漿中濃度のCminが0.1ng/ml〜0.2ng/mlである、請求項9に記載の経口浸透圧薬物送達システム。
【請求項11】
前記トレプロスチニルの治療的に有効な血漿中濃度のCmaxが0.5ng/ml〜2ng/mlである、請求項9に記載の経口浸透圧薬物送達システム。
【請求項12】
前記トレプロスチニルの治療的に有効な血漿中濃度のTmax(Cmaxに到達するまでの時間)が2時間〜8時間である、請求項11に記載の経口浸透圧薬物送達システム。
【請求項13】
前記トレプロスチニルの治療的に有効な血漿中濃度が、1日2回〜1日1回の投与が可能となるように維持される、請求項9に記載の経口浸透圧薬物送達システム。
【請求項14】
前記トレプロスチニルの治療的に有効な血漿中濃度が副作用の低減を生じる、請求項9に記載の経口浸透圧薬物送達システム。
【請求項15】
前記放出増強剤が、0.5重量%〜90重量%の範囲の濃度で前記剤形中に存在する、請求項1に記載の経口浸透圧薬物送達システム。
【請求項16】
前記放出増強剤が、ウィッキング剤、錯化剤、及びミセル形成剤から成る群より選択される、請求項1に記載の経口浸透圧薬物送達システム。
【請求項17】
前記ウィッキング剤が、高HLB界面活性剤、イオン性界面活性剤、及び非膨潤親水性ポリマーを含む群より選択される、請求項16に記載の経口浸透圧薬物送達システム。
【請求項18】
前記非膨潤親水性ポリマーが、ポリエチレンオキサイド−ポリプロピレンオキサイドブロック共重合体、セルロースエーテル、及びポリエチレングリコールから成る群より選択される、請求項17に記載の経口浸透圧薬物送達システム。
【請求項19】
前記錯化剤が、ポリビニルピロリドン、シクロデキストリン、及び非イオン性界面活性剤を含む群より選択される、請求項16に記載の経口浸透圧薬物送達システム。
【請求項20】
前記ミセル形成剤が、ポリエチレンオキサイド変性ソルビタンモノエステル、脂肪酸ソルビタンエステル、ラウリル硫酸ナトリウム、及びソディウムドキュセートを含む群より選択される、請求項16に記載の経口浸透圧薬物送達システム。
【請求項21】
前記形態が、錠剤、カプセル剤、及びペレットから成る群より選択される、請求項1に記載の経口浸透圧薬物送達システム。
【請求項22】
プロスタサイクリン及び少なくとも1つの放出増強剤を含む徐放経口浸透圧薬物送達システムを、患者に投与することを含む、プロスタサイクリンの経口送達方法。
【請求項23】
前記放出増強剤が、ウィッキング剤、錯化剤、及びミセル形成剤から成る群より選択される、請求項22に記載の方法。
【請求項24】
前記ウィッキング剤が、高HLB界面活性剤、イオン性界面活性剤、及び非膨潤親水性ポリマーを含む群より選択される、請求項23に記載の方法。
【請求項25】
前記非膨潤親水性ポリマーが、ポリエチレンオキサイド−ポリプロピレンオキサイドブロック共重合体、セルロースエーテル、及びポリエチレングリコールから成る群より選択される、請求項24に記載の方法。
【請求項26】
前記錯化剤が、ポリビニルピロリドン、シクロデキストリン、及び非イオン性界面活性剤を含む群より選択される、請求項23に記載の方法。
【請求項27】
前記ミセル形成剤が、ポリエチレンオキサイド変性ソルビタンモノエステル、脂肪酸ソルビタンエステル、ラウリル硫酸ナトリウム、及びソディウムドキュセートを含む群より選択される、請求項23に記載の方法。
【請求項28】
前記プロスタサイクリンが短い半減期を有する、請求項22に記載の方法。
【請求項29】
前記プロスタサイクリンの半減期が数分〜最大3時間の範囲である、請求項28に記載の方法。
【請求項30】
前記プロスタサイクリンがトレプロスチニル又はその誘導体若しくは塩である、請求項29に記載の方法。
【請求項31】
トレプロスチニル又はその薬学的に許容される塩の量が、トレプロスチニルの治療的に有効な血漿中濃度を生じるのに十分である、請求項30に記載の方法。
【請求項32】
前記トレプロスチニルの治療的に有効な血漿中濃度のCminが0.1ng/ml〜0.2ng/mlである、請求項31に記載の方法。
【請求項33】
前記トレプロスチニルの治療的に有効な血漿中濃度のCmaxが0.5ng/ml〜2ng/mlである、請求項31に記載の方法。
【請求項34】
前記トレプロスチニルの治療的に有効な血漿中濃度のTmax(Cmaxに到達するまでの時間)が2時間〜8時間である、請求項33に記載の方法。
【請求項35】
前記トレプロスチニルの治療的に有効な血漿中濃度が、1日2回〜1日1回の投与が可能となるように維持される、請求項31に記載の方法。
【請求項36】
有効薬物の投与による疾患の治療方法であって、該薬物を含有する請求項1に記載の浸透圧薬物送達システムを経口投与することを含む、有効薬物の投与による疾患の治療方法。
【請求項37】
前記経口浸透圧薬物送達システムが徐放送達システムである、請求項36に記載の方法。
【請求項38】
前記薬物の水への溶解度が少なくとも約30mg/mlである、請求項37に記載の方法。
【請求項39】
前記薬物が短い半減期を有する、請求項37に記載の方法。
【請求項40】
前記薬物の半減期が数分〜3時間の範囲である、請求項39に記載の方法。
【請求項41】
前記薬物がプロスタサイクリンである、請求項40に記載の方法。
【請求項42】
前記薬物がトレプロスチニル又はその誘導体若しくは塩である、請求項41に記載の方法。
【請求項43】
前記徐放浸透圧薬物送達システムが1日2回〜1日1回の投与に好適である、請求項42に記載の方法。
【請求項44】
前記疾患が、肺高血圧、肺動脈高血圧(PAH)、末梢血管疾患(PVD)、虚血性疾患、心不全、抗凝血を必要とする病態、血栓性微小血管症、体外循環、網膜中心静脈閉塞症、アテローム性動脈硬化症、炎症性疾患、高血圧、癌、又は細胞増殖が無秩序な他の病態を含む群より選択される、請求項41に記載の方法。
【請求項45】
前記放出増強剤が、ウィッキング剤、錯化剤、及びミセル形成剤から成る群より選択される、請求項36に記載の方法。
【請求項46】
前記ウィッキング剤が、高HLB界面活性剤、イオン性界面活性剤、及び非膨潤親水性ポリマーを含む群より選択される、請求項45に記載の方法。
【請求項47】
前記非膨潤親水性ポリマーが、ポリエチレンオキサイド−ポリプロピレンオキサイドブロック共重合体、セルロースエーテル、及びポリエチレングリコールから成る群より選択される、請求項46に記載の方法。
【請求項48】
前記錯化剤が、ポリビニルピロリドン、シクロデキストリン、及び非イオン性界面活性剤を含む群より選択される、請求項45に記載の方法。
【請求項49】
前記ミセル形成剤が、ポリエチレンオキサイド変性ソルビタンモノエステル、脂肪酸ソルビタンエステル、ラウリル硫酸ナトリウム、及びソディウムドキュセートを含む群より選択される、請求項45に記載の方法。
【請求項1】
標準的な浸透圧送達システムで製剤化する場合に不規則又は不完全な放出プロファイルを示す高水溶性薬物、及び少なくとも1つの放出増強剤を含む、経口浸透圧薬物送達システム。
【請求項2】
前記薬物の水への溶解度が少なくとも約30mg/mlである、請求項1に記載の経口浸透圧薬物送達システム。
【請求項3】
in vitroでの放出プロファイルから予測され得るin vivoでの放出プロファイルを示す、請求項1に記載の経口浸透圧薬物送達システム。
【請求項4】
前記経口浸透圧薬物送達システムが徐放送達システムである、請求項2に記載の経口浸透圧薬物送達システム。
【請求項5】
前記薬物が短い半減期を有する、請求項4に記載の経口浸透圧薬物送達システム。
【請求項6】
前記半減期が数分〜3時間の範囲である、請求項5に記載の経口浸透圧薬物送達システム。
【請求項7】
前記薬物がプロスタサイクリンである、請求項6に記載の経口浸透圧薬物送達システム。
【請求項8】
前記プロスタサイクリンがトレプロスチニル又はその誘導体若しくは塩である、請求項7に記載の経口浸透圧薬物送達システム。
【請求項9】
トレプロスチニル又はその薬学的に許容される誘導体の量が、トレプロスチニルの治療的に有効な血漿中濃度を生じるのに十分である、請求項8に記載の経口浸透圧薬物送達システム。
【請求項10】
前記トレプロスチニルの治療的に有効な血漿中濃度のCminが0.1ng/ml〜0.2ng/mlである、請求項9に記載の経口浸透圧薬物送達システム。
【請求項11】
前記トレプロスチニルの治療的に有効な血漿中濃度のCmaxが0.5ng/ml〜2ng/mlである、請求項9に記載の経口浸透圧薬物送達システム。
【請求項12】
前記トレプロスチニルの治療的に有効な血漿中濃度のTmax(Cmaxに到達するまでの時間)が2時間〜8時間である、請求項11に記載の経口浸透圧薬物送達システム。
【請求項13】
前記トレプロスチニルの治療的に有効な血漿中濃度が、1日2回〜1日1回の投与が可能となるように維持される、請求項9に記載の経口浸透圧薬物送達システム。
【請求項14】
前記トレプロスチニルの治療的に有効な血漿中濃度が副作用の低減を生じる、請求項9に記載の経口浸透圧薬物送達システム。
【請求項15】
前記放出増強剤が、0.5重量%〜90重量%の範囲の濃度で前記剤形中に存在する、請求項1に記載の経口浸透圧薬物送達システム。
【請求項16】
前記放出増強剤が、ウィッキング剤、錯化剤、及びミセル形成剤から成る群より選択される、請求項1に記載の経口浸透圧薬物送達システム。
【請求項17】
前記ウィッキング剤が、高HLB界面活性剤、イオン性界面活性剤、及び非膨潤親水性ポリマーを含む群より選択される、請求項16に記載の経口浸透圧薬物送達システム。
【請求項18】
前記非膨潤親水性ポリマーが、ポリエチレンオキサイド−ポリプロピレンオキサイドブロック共重合体、セルロースエーテル、及びポリエチレングリコールから成る群より選択される、請求項17に記載の経口浸透圧薬物送達システム。
【請求項19】
前記錯化剤が、ポリビニルピロリドン、シクロデキストリン、及び非イオン性界面活性剤を含む群より選択される、請求項16に記載の経口浸透圧薬物送達システム。
【請求項20】
前記ミセル形成剤が、ポリエチレンオキサイド変性ソルビタンモノエステル、脂肪酸ソルビタンエステル、ラウリル硫酸ナトリウム、及びソディウムドキュセートを含む群より選択される、請求項16に記載の経口浸透圧薬物送達システム。
【請求項21】
前記形態が、錠剤、カプセル剤、及びペレットから成る群より選択される、請求項1に記載の経口浸透圧薬物送達システム。
【請求項22】
プロスタサイクリン及び少なくとも1つの放出増強剤を含む徐放経口浸透圧薬物送達システムを、患者に投与することを含む、プロスタサイクリンの経口送達方法。
【請求項23】
前記放出増強剤が、ウィッキング剤、錯化剤、及びミセル形成剤から成る群より選択される、請求項22に記載の方法。
【請求項24】
前記ウィッキング剤が、高HLB界面活性剤、イオン性界面活性剤、及び非膨潤親水性ポリマーを含む群より選択される、請求項23に記載の方法。
【請求項25】
前記非膨潤親水性ポリマーが、ポリエチレンオキサイド−ポリプロピレンオキサイドブロック共重合体、セルロースエーテル、及びポリエチレングリコールから成る群より選択される、請求項24に記載の方法。
【請求項26】
前記錯化剤が、ポリビニルピロリドン、シクロデキストリン、及び非イオン性界面活性剤を含む群より選択される、請求項23に記載の方法。
【請求項27】
前記ミセル形成剤が、ポリエチレンオキサイド変性ソルビタンモノエステル、脂肪酸ソルビタンエステル、ラウリル硫酸ナトリウム、及びソディウムドキュセートを含む群より選択される、請求項23に記載の方法。
【請求項28】
前記プロスタサイクリンが短い半減期を有する、請求項22に記載の方法。
【請求項29】
前記プロスタサイクリンの半減期が数分〜最大3時間の範囲である、請求項28に記載の方法。
【請求項30】
前記プロスタサイクリンがトレプロスチニル又はその誘導体若しくは塩である、請求項29に記載の方法。
【請求項31】
トレプロスチニル又はその薬学的に許容される塩の量が、トレプロスチニルの治療的に有効な血漿中濃度を生じるのに十分である、請求項30に記載の方法。
【請求項32】
前記トレプロスチニルの治療的に有効な血漿中濃度のCminが0.1ng/ml〜0.2ng/mlである、請求項31に記載の方法。
【請求項33】
前記トレプロスチニルの治療的に有効な血漿中濃度のCmaxが0.5ng/ml〜2ng/mlである、請求項31に記載の方法。
【請求項34】
前記トレプロスチニルの治療的に有効な血漿中濃度のTmax(Cmaxに到達するまでの時間)が2時間〜8時間である、請求項33に記載の方法。
【請求項35】
前記トレプロスチニルの治療的に有効な血漿中濃度が、1日2回〜1日1回の投与が可能となるように維持される、請求項31に記載の方法。
【請求項36】
有効薬物の投与による疾患の治療方法であって、該薬物を含有する請求項1に記載の浸透圧薬物送達システムを経口投与することを含む、有効薬物の投与による疾患の治療方法。
【請求項37】
前記経口浸透圧薬物送達システムが徐放送達システムである、請求項36に記載の方法。
【請求項38】
前記薬物の水への溶解度が少なくとも約30mg/mlである、請求項37に記載の方法。
【請求項39】
前記薬物が短い半減期を有する、請求項37に記載の方法。
【請求項40】
前記薬物の半減期が数分〜3時間の範囲である、請求項39に記載の方法。
【請求項41】
前記薬物がプロスタサイクリンである、請求項40に記載の方法。
【請求項42】
前記薬物がトレプロスチニル又はその誘導体若しくは塩である、請求項41に記載の方法。
【請求項43】
前記徐放浸透圧薬物送達システムが1日2回〜1日1回の投与に好適である、請求項42に記載の方法。
【請求項44】
前記疾患が、肺高血圧、肺動脈高血圧(PAH)、末梢血管疾患(PVD)、虚血性疾患、心不全、抗凝血を必要とする病態、血栓性微小血管症、体外循環、網膜中心静脈閉塞症、アテローム性動脈硬化症、炎症性疾患、高血圧、癌、又は細胞増殖が無秩序な他の病態を含む群より選択される、請求項41に記載の方法。
【請求項45】
前記放出増強剤が、ウィッキング剤、錯化剤、及びミセル形成剤から成る群より選択される、請求項36に記載の方法。
【請求項46】
前記ウィッキング剤が、高HLB界面活性剤、イオン性界面活性剤、及び非膨潤親水性ポリマーを含む群より選択される、請求項45に記載の方法。
【請求項47】
前記非膨潤親水性ポリマーが、ポリエチレンオキサイド−ポリプロピレンオキサイドブロック共重合体、セルロースエーテル、及びポリエチレングリコールから成る群より選択される、請求項46に記載の方法。
【請求項48】
前記錯化剤が、ポリビニルピロリドン、シクロデキストリン、及び非イオン性界面活性剤を含む群より選択される、請求項45に記載の方法。
【請求項49】
前記ミセル形成剤が、ポリエチレンオキサイド変性ソルビタンモノエステル、脂肪酸ソルビタンエステル、ラウリル硫酸ナトリウム、及びソディウムドキュセートを含む群より選択される、請求項45に記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公表番号】特表2009−535337(P2009−535337A)
【公表日】平成21年10月1日(2009.10.1)
【国際特許分類】
【出願番号】特願2009−507767(P2009−507767)
【出願日】平成19年4月26日(2007.4.26)
【国際出願番号】PCT/US2007/009969
【国際公開番号】WO2007/127216
【国際公開日】平成19年11月8日(2007.11.8)
【出願人】(506339316)スパーナス ファーマシューティカルズ インコーポレイテッド (23)
【Fターム(参考)】
【公表日】平成21年10月1日(2009.10.1)
【国際特許分類】
【出願日】平成19年4月26日(2007.4.26)
【国際出願番号】PCT/US2007/009969
【国際公開番号】WO2007/127216
【国際公開日】平成19年11月8日(2007.11.8)
【出願人】(506339316)スパーナス ファーマシューティカルズ インコーポレイテッド (23)
【Fターム(参考)】
[ Back to top ]

