液滴アクチュエータ装置、システム、および方法
【課題】本発明は、流動性の充填流体による1つの液滴から別の液滴への汚染物質の移動を減少または排除するための特定の新規アプローチに関する。
【解決手段】1つの適用において、液滴アクチュエータは、ポリメラーゼ連鎖反応(PCR)技術を用いて遺伝子解析を実施するために使用される。本発明は、サンプル標的の最適な増幅および検出を与える液滴アクチュエータでPCRを実施する方法を改良するための必要性を扱う。本発明は、サンプル中の標的核酸を増幅および/または検出する方法を提供する。その方法は、核酸増幅反応液滴のセットを提供する工程を含んでもよい。各液滴はサンプルの一部を含んでもよい。その方法は、標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理して、増幅核酸を有する増幅液滴の対応するサブセットを得る工程を含んでもよい。
【解決手段】1つの適用において、液滴アクチュエータは、ポリメラーゼ連鎖反応(PCR)技術を用いて遺伝子解析を実施するために使用される。本発明は、サンプル標的の最適な増幅および検出を与える液滴アクチュエータでPCRを実施する方法を改良するための必要性を扱う。本発明は、サンプル中の標的核酸を増幅および/または検出する方法を提供する。その方法は、核酸増幅反応液滴のセットを提供する工程を含んでもよい。各液滴はサンプルの一部を含んでもよい。その方法は、標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理して、増幅核酸を有する増幅液滴の対応するサブセットを得る工程を含んでもよい。
【発明の詳細な説明】
【技術分野】
【0001】
(1.関連出願)
本出願は、2008年10月28日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/108,880号、2008年11月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/115,654号、2009年2月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/153,598号、2008年5月13日に出願された「Reducing Droplet Cross−contamination in a Droplet Actuator」という発明の名称の米国特許出願第61/052,885号、2008年9月22日に出願された「Reducing Droplet Cross−contamination in a Droplet Actuator」という発明の名称の米国特許出願第61/098,860号、2009年3月16日に出願された「Reducing Droplet Cross−contamination in a Droplet Actuator」という発明の名称の米国特許出願第61/160,607号、2008年10月7日に出願された「Nucleic Acid Handling on a Droplet Actuator」という発明の名称の米国特許出願第61/103,332号、2008年12月31日に出願された「Sample Preparation and Assay Execution on a Droplet Actuator」という発明の名称の米国特許出願第61/141,820号に対する優先権を主張し、これらの出願の各々の全開示は参照として本明細書に援用される。
【0002】
(2.政府の利益)
本発明は、米国の国立衛生研究所によって与えられたAI065169−01およびAI066590−02のもとで、政府の支援によってなされたものである。米国政府は、本発明において特定の権利を有する。
【0003】
AI065169−01のもとの政府の支援に関する上述の声明は、2008年10月28日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/108,880号、2008年11月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/115,654号、2009年2月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/153,598号に起因する本出願において記載され、特許請求される本発明のこれらの態様のみに適用し、AI066590−02のもとの政府の支援に関する上述の声明は、2008年10月7日に出願された「Nucleic Acid Handling on a Droplet Actuator」という発明の名称の米国特許出願第61/103,332号、2008年12月31日に出願された「Sample Preparation and Assay Execution on a Droplet Actuator」という発明の名称の米国特許出願第61/141,820号に起因する本出願において記載され、特許請求される本発明のこれらの態様のみに適用する。
【0004】
本発明は、液滴アクチュエータ装置、システム、および方法に関する。
【背景技術】
【0005】
(3.背景)
液滴アクチュエータは、多種多様の液滴操作を実施するために使用される。液滴アクチュエータは、典型的に、液滴操作間隙によって隔てられる2つの基板を備える。基板は、液滴操作を実施するための電極を備える。基板間の液滴操作間隙は、典型的に、液滴操作に供される流体と混ざらない流動性の充填流体で満たされる。液滴操作は、基板の1つまたは両方と結合する電極によって制御される。液滴の成分は、一部の場合において、充填流体中の液滴から出ていくことがある。充填流体からのそのような成分は他の液滴を汚染する場合がある。
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明は、流動性の充填流体を介して液滴アクチュエータ上のある液滴から別の液滴への汚染の移動を減少または除去するための特定の新規のアプローチに関する。1つの適用において、液滴アクチュエータは、ポリメラーゼ連鎖反応(PCR)技術を用いて遺伝子解析を実施するために使用される。標的サンプルの最適な増幅および検出を提供する液滴アクチュエータ上でPCRを実施する改良された方法についての必要性が存在する。
【課題を解決するための手段】
【0007】
(4 本発明の詳細な説明)
本発明は、サンプル中の標的核酸を増幅および/または検出する方法を提供する。その方法は、核酸増幅反応液滴のセットを提供する工程を含んでもよい。各液滴はサンプルの一部を含んでもよい。その方法は、標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理して、増幅核酸を有する増幅液滴の対応するサブセットを得る工程を含んでもよい。増幅反応液滴の各サブセットは、1つ以上の増幅反応液滴を含んでもよい。増幅反応液滴の各サブセットは、標的核酸を増幅するための異なる条件下で処理されてもよい。その方法は、検出するための増幅液滴を調製する工程を含んでもよい。その方法は、増幅液滴からシグナルを検出する工程を含んでもよい。その方法はまた、増幅液滴および/またはサンプルに存在する増幅核酸の量および/または識別を決定する工程を含んでもよい。核酸増幅反応液滴のセットを提供する工程は、サンプル液滴から核酸増幅液滴のセットを分配する工程を含んでもよい。サンプル液滴は、液滴アクチュエータの液滴操作間隙に提供されてもよく、分配は電極により媒介されてもよい。サンプル液滴は、液滴アクチュエータのリザーバーに提供されてもよい。液滴アクチュエータは、リザーバーから液滴操作間隙内への液体経路を備えてもよい。核酸増幅液滴のセットを分配する工程は、液体経路を通して液滴操作間隙内にサンプル液滴を流動させる工程、および液滴操作間隙中に増幅反応液滴を分配するために電極を使用する工程を含んでもよい。核酸増幅反応液滴のセットを提供する工程は、サンプル液滴を提供する工程と、サンプル液滴を複数のサンプル小液滴に分裂する工程と、各サンプル小液滴と、増幅試薬を含み得る1つ以上の液滴とを混合して、増幅反応液滴を生じる工程とを含んでもよい。本明細書に記載される方法の任意の1つ以上の工程は、電極によって媒介される液滴操作を用いて液滴アクチュエータの液滴操作間隙中で行われてもよい。本明細書に記載される方法の任意の1つ以上の工程は、電極によって媒介される液滴操作を用いて行われてもよい。サンプル液滴、複数の小液滴および1つ以上の液滴は、増幅試薬を含んでもよい。増幅反応液滴は、液滴操作間隙に配置され、少なくとも部分的に流動性の充填流体によって囲まれてもよい。核酸増幅反応液滴のセットを提供する工程は、以下の工程を含んでもよい:サンプル液滴を提供する工程;サンプル液滴と、増幅試薬を含み得る1つ以上の液滴とを混合して、増幅準備液滴を生じる工程;および増幅準備液滴を分裂して、増幅反応液滴を生じる工程。サンプル液滴、1つ以上の液滴は、増幅試薬、親増幅反応液滴を含んでもよく、増幅反応液滴は、液滴アクチュエータの液滴操作間隙に配置されてもよく、流動性の充填流体に少なくとも部分的に囲まれてもよい。その方法は、標的核酸がサンプル中に存在する場合、各増幅反応液滴が標的核酸を含むことを確実にするために増幅準備液滴中で十分に増幅された核酸を得るために選択される条件下で増幅準備液滴を処理する工程を含んでもよい。増幅準備液滴を処理する工程は、1〜50サイクル、1〜40サイクル、1〜30サイクル、1〜20サイクル、または1〜10サイクル、または1〜5サイクルについて増幅準備液滴を熱サイクルすることを含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、液滴アクチュエータの液滴操作間隙中の複数の電極経路に沿って液滴を輸送することによって2つ以上の熱領域の間で増幅反応液滴をサイクルする工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、液滴アクチュエータの液滴操作間隙内の共通の電極経路に沿って各サブセットにおける液滴を輸送することによって2つ以上の熱領域の間で2つ以上の増幅反応液滴のサブセットをサイクルする工程を含んでもよい。一部の場合において、1つ以上の電極経路は、2つ以上の熱領域の間に1つ以上のループ経路を規定する。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、電極経路ループの周りに複数の増幅反応液滴を輸送する工程を含んでもよい。その方法は、その所定数のサイクルが完了した場合、各増幅液滴を電極経路ループから除去する工程を含んでもよい。各増幅液滴を電極経路ループから除去する工程は、増幅反応液滴を液滴操作間隙の別の領域に輸送するために電極により媒介される液滴操作を含んでもよい。液滴操作間隙の領域は、まだ検出されていない増幅液滴を保存するために選択される温度を有する温度制御領域を備えてもよい。各増幅液滴を電極経路ループから除去する工程は、各増幅液滴を液滴アクチュエータの液滴操作間隙から除去する工程を含んでもよい。他の場合において、電極経路は、2つ以上の熱領域の間で曲がっている。電極経路上の1つの電極から電極経路上の隣接する電極への輸送時間は、隣接する電極の各対に関して実質的に均一であってもよく、熱領域内の滞留時間は、熱領域に存在する電極経路の各曲がり角の電極の数によって規定されてもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、並行して熱領域の間に増幅反応液滴の2つ以上のサブセットを輸送する工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、増幅反応液滴の2つ以上のサブセットを熱領域内に連続して輸送する工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、増幅反応液滴の第1のサブセットを第1の熱領域内に輸送するが、増幅反応液滴の第2のサブセットを第2の熱領域内に輸送する工程と、増幅反応試薬液滴の第1のサブセットを第2の熱領域に輸送するが、増幅反応試薬の第2のサブセットを第1の熱領域に輸送する工程を含んでもよい。連続して熱サイクルされた増幅反応液滴のサブセットは、共通の電極経路に沿って熱サイクルされてもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、並行して2つ以上のサブセットを増幅させる工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、全ての増幅反応試薬に関して熱的に同時に熱サイクルする工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、全ての増幅反応試薬に関して熱的に同時でなくてもよい熱サイクルする工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、液滴アクチュエータの熱サイクル領域を加熱および冷却することによって行われ得ることを含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、1回以上、熱サイクルするサイクル数で熱領域における増幅反応液滴の滞留時間を変化させる工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、増幅液滴からシグナルを検出する前に増幅反応液滴の全てのサブセットに関して完了されてもよい。一部の場合において、増幅液滴からシグナルを検出する工程は、第2のセットの液滴について標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する前に第1のサブセットの液滴について完了されてもよい。検出するための増幅液滴を調製する工程は、2つ以上の増幅液滴のセットに対して標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する前に、液滴アクチュエータの熱サイクル範囲から離れた位置、または熱サイクル領域から離れた位置に2つ以上の増幅液滴のセットを輸送する工程を含んでもよい。増幅液滴は、増幅液滴からシグナルを検出するのに適切な温度を有する熱領域に輸送されてもよい。検出するための増幅液滴を調製する工程は、配置された増幅液滴の各々のそのようなサブセットに対して増幅液滴からシグナルを検出する前に熱サイクル領域から離れた位置に増幅液滴のサブセットを少なくとも配置する工程を含んでもよい。検出するための増幅液滴を調製する工程は、増幅核酸から未結合の検出試薬を分離する工程を含んでもよい。検出するための増幅液滴を調製する工程は、増幅液滴における増幅を実質的に停止する工程を含んでもよい。検出するための増幅液滴を調製する工程は、1つの液滴アクチュエータから別の液滴アクチュエータに増幅液滴を輸送する工程を含んでもよい。増幅液滴における増幅を実質的に停止する工程は、増幅反応を実質的に停止するために液滴温度を調節する工程を含んでもよい。増幅液滴における増幅を実質的に停止する工程は、増幅反応を実質的に停止するために試薬を増幅液滴に添加する工程を含んでもよい。試薬を増幅液滴に添加する工程は、増幅液滴と試薬液滴とを混合する工程を含んでもよく、試薬液滴は、増幅反応を実質的に停止するために選択される試薬を含んでもよい。増幅反応を実質的に停止するために選択される試薬は、ポリメラーゼ活性を妨げること、ポリメラーゼ補因子活性を妨げること、核酸に結合すること、および/または鉄イオンを放出することによって増幅反応を実質的に停止する試薬を含んでもよい。特定の実施形態において、増幅反応液滴は検出試薬を欠く。検出するための増幅液滴を調製する工程は、検出試薬を増幅液滴に添加する工程を含んでもよい。検出試薬を増幅液滴に添加する工程は、各々の増幅液滴と検出試薬を含む液滴とを混合する工程を含んでもよい。検出するための増幅液滴を調製する工程は、各々の増幅液滴と1つ以上の検出試薬を含む液滴とを混合する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、検出試薬によって媒介されるシグナルに基づいて増幅を検出する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、そのような液滴の検出ウィンドウへの輸送後に各々の増幅液滴からシグナルを検出する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、増幅液滴の1つ以上のサブセットのセットを、検出するための検出ウィンドウに輸送する工程を含んでもよい。特定の実施形態において、標的核酸を増幅するための条件下で増幅反応試薬の2つ以上のサブセットを処理する工程は、液滴アクチュエータの液滴操作間隙内で達成されてもよく、検出するための増幅液滴を調製する工程および/または増幅液滴からシグナルを検出する工程は、液滴操作間隙の外側で達成されてもよい。従って、検出するための増幅液滴を調製する工程は、検出するための液滴操作間隙の外側に1つ以上の増幅液滴を輸送する工程を含んでもよい。一部の場合において、増幅液滴からシグナルを検出する工程は、液滴アクチュエータの液滴操作間隙の外側のリザーバーで行われてもよい。検出するための増幅液滴を調製する工程は、増幅液滴のサブセットを、少ないサイクル数のサブセットで開始する検出ウィンドウに輸送する工程、および高いサイクル数のサブセットまで処理する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、増幅液滴のアレイを走査する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、増幅液滴のアレイを画像化する工程を含んでもよい。特定の実施形態において、標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、複数のサブセットに関して並行して開始し、検出するための増幅液滴を調製する工程は、連続して開始し、各サブセットは以前のサブセットの開始後に開始し、増幅液滴からシグナルを検出する工程は連続して開始し、各サブセットは以前のサブセットの開始後に開始する。一部の場合において、検出するための増幅液滴を調製する工程は連続して開始し、各サブセットは以前のサブセットの開始後に開始する。一部の場合において、増幅液滴からシグナルを検出する工程は連続して開始し、各サブセットは以前のサブセットの完了後に開始する。
【0008】
一部の場合において、増幅液滴からシグナルを検出する工程は、液滴が装置の領域を通って移動する場合、その液滴を追跡し、その液滴からシグナルを測定する画像化装置を用いて達成される。一部の場合において、検出するための増幅液滴を調製する工程は並行して開始し、各サブセットはほぼ同じ時間でプロセスを開始する。一部の場合において、増幅液滴からシグナルを検出する工程は並行して開始し、各サブセットはほぼ同じ時間でプロセスを開始する。その方法は、増幅液滴のサブセットの各々についての熱サイクルエンドポイントにてシグナルの増加または減少を決定することによって増幅液滴に存在する増幅核酸の量を決定する工程を含んでもよい。増幅液滴および/またはサンプルに存在する増幅核酸の量を検出する工程は、サンプル液滴に存在する標的核酸の量を決定するために増幅液滴に存在する増幅核酸の量を使用する工程を含んでもよい。増幅液滴および/またはサンプルに存在する増幅核酸の量を決定する工程は、サンプル液滴に存在する標的核酸の量を決定するために異なる数の熱サイクルの後に増幅液滴に存在する増幅核酸の量を使用する工程を含んでもよい。標的核酸を増幅するための異なる条件は、増幅反応液滴の各サブセットについての異なる数の熱サイクルを含んでもよい。増幅反応液滴は検出試薬を含んでもよい。他の場合において、増幅反応液滴は有意な量の検出試薬を含まなくてもよい。増幅試薬を含む1つ以上の液滴はさらに、検出試薬を含んでもよい。他の場合において、増幅試薬を含む1つ以上の液滴は、有意な量の検出試薬を含まなくてもよい。検出試薬は核酸結合剤を含んでもよい。一部の場合において、核酸結合剤は核酸増幅の割合を有意に阻害できる。核酸結合剤は挿入剤を含んでもよい。挿入剤は蛍光色素を含んでもよい。標的核酸は、遺伝性疾患または感染病の指標であってもよい。標的核酸は、生物学的集団由来の個体または個体のサブグループの同定の指標であってもよい。一部の実施形態において、核酸増幅反応液滴の1つ以上は、標的核酸を増幅するための条件下で、増幅反応液滴の2つ以上のサブセットを処理する工程、および増幅液滴に存在する増幅核酸の量を決定する工程の前に、初期検出工程に供されてもよく、ならびに/あるいはサンプルは、初期検出工程において検出されるシグナルと、増幅液滴から検出されるシグナルとの間の比較物を含んでもよい。サンプル中の標的核酸を検出する方法は、十分なデータが所定の範囲の統計的確実性内で開始サンプルに存在する標的核酸を定量化するために収集された場合、方法を停止する工程を含んでもよい。その方法は、選択されるサイクル数の各々についての増幅液滴および/またはサンプルに存在する増幅核酸の量を決定するための十分なデータを提供するために予想される第1のセットのサイクル数を選択する工程、1つ以上の増幅反応液滴のサブセットを増幅させる工程に供する工程、調製する工程、検出する工程、および決定する工程、ならびに十分なデータが、所定の範囲の統計的確実性内でサンプルに存在する核酸を同定または定量化するために収集されているかどうかを決定する工程を含んでもよい。十分なデータが、所定の範囲の統計的確実性内で開始サンプルに存在する標的核酸を同定または定量化するために収集されるまで、あるいは十分なデータが、標的核酸がサンプルに存在しない所定の範囲の統計的確実性内で決定するために収集されるまで、工程は新しいセットのサイクル数で繰り返されてもよい。十分なデータが収集されるかどうかを決定する工程は、十分なデータが、所定の範囲の統計的確実性内でサンプルに存在する標的核酸を同定するために収集されるかどうかを決定する工程を含んでもよい。十分なデータが収集されるかどうかを決定する工程は、十分なデータが、所定の範囲の統計的確実性内でサンプルに存在する標的核酸を定量化するために収集されるかどうかを決定する工程を含む。
【0009】
本発明はサンプル中の標的核酸の増加をモニターする方法を提供する。その方法は、核酸増幅反応液滴のセットを提供する工程を含んでもよく、各液滴はサンプルの一部を含む。その方法は、増幅された二本鎖核酸を有する増幅液滴を得るために標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを熱サイクルする工程を含んでもよい。増幅反応液滴の各サブセットは、1つ以上の増幅反応液滴を含んでもよい。増幅反応液滴の各サブセットは、異なる数のサイクルについて熱サイクルされてもよい。増幅反応液滴の各サブセットは、各サブセットについての所定数のサイクルの完了前に検出に供されなくてもよい。その方法は、検出準備プロトコルを実行する工程を含んでもよく、その検出準備プロトコルは、増幅液滴の各々と、増幅核酸の検出用の検出試薬とを混合して、検出準備液滴を生じる工程を含んでもよい。その方法は、検出準備液滴からシグナルを検出する工程を含んでもよい。その方法は、増幅液滴および/またはサンプルに存在する増幅核酸のシグナル、存在および/または量に基づいて決定する工程を含んでもよい。
【0010】
本発明は、予め組み込まれている液滴アクチュエータカートリッジを提供する。予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を形成する1つ以上の基板、およびその1つ以上の基板に結合され、かつ液滴操作間隙内で液滴操作を媒介するように配置される電極を含んでもよい。予め組み込まれている液滴アクチュエータカートリッジは、増幅試薬を含み、検出試薬を欠く1つ以上の液滴を含む第1のリザーバー、および1つ以上の検出試薬を含む第2のリザーバーを含んでもよい。予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を有する第1のリザーバーおよび第2のリザーバーに流動的に接続される1つ以上の流体経路を含んでもよい。例えば、予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を有する第1のリザーバーに流動的に接続される流体経路を備えてもよい。同様に、予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を有する第2のリザーバーに流動的に接続される流体経路を備えてもよい。予め組み込まれている液滴アクチュエータカートリッジは、サンプルを液滴操作間隙に負荷するための手段を備えてもよい。サンプルを液滴操作間隙に負荷するための手段は、例えば、サンプル負荷リザーバーおよび液滴操作間隙を有するサンプル負荷リザーバーに流動的に接続される流体経路を含んでもよい。本発明は、予め組み込まれている液滴アクチュエータカートリッジを含むキットを提供する。キットはまた、カートリッジを用いて増幅プロトコルを実行するためのソフトウェアを含んでもよい。本発明の物理的実施形態のいずれかは、物理的実施形態を含むそのようなキットおよび物理的実施形態を制御するためのソフトウェア含んでもよい。
【0011】
本発明は検体を検出する方法を提供する。その方法は、検出ウィンドウ内に液滴を提供する工程を含んでもよい。液滴は、検体の存在および/または量の指標であるシグナル生成物質を含んでもよい。液滴は、シグナル生成物質によって生成されたシグナルを妨げることができる1つ以上の磁性反応ビーズを含んでもよい。その方法は、検出ウィンドウ内の液滴を輸送および/または抑制している間、検出ウィンドウから磁性反応ビーズを磁性的に除去するため、および/または磁性反応ビーズが検出ウィンドウに侵入することを磁性的に抑制するための磁場を使用する工程を含んでもよい。その方法は、磁性反応ビーズから実質的に妨げられないシグナル生成物質によって生成されるシグナルを検出する工程を含んでもよい。同様に、本発明は、検出ウィンドウに液滴を提供する工程を含む検体を検出する方法を提供し、ここで、液滴は、検体および/または実質的に磁性反応ではなく、シグナル生成物質によって生成されたシグナルを妨げることができる1つ以上のビーズの存在および/または量の指標であるシグナル生成物質を含む。その方法は、検出ウィンドウ内に液滴を輸送および/または保有している間、ビーズが検出ウィンドウに侵入することを防ぐ物理的障壁を使用する工程を含んでもよい。その方法は、ビーズから実質的に妨げられないシグナル生成物質によって生成されたシグナルを検出する工程を含んでもよい。この物理的障壁アプローチは、ビーズが磁性反応であるか否かに関わらず、使用されてもよいことは理解されるだろう。検体を検出するこれらの方法において、液滴は、液滴アクチュエータの液滴操作間隙内に提供されてもよい。検出ウィンドウは、液滴アクチュエータの基板内に開口部またはウィンドウを備えてもよい。実質的に非磁性反応ビーズを利用する実施形態に関して、磁場を使用する工程は、検出ウィンドウに近接する固定磁石を提供する工程を含んでもよい。検出ウィンドウ内に液滴を輸送する工程は、磁性反応ビーズを、ビーズが検出ウィンドウから離れた位置へ引き付けられ得るか、および/またはビーズが検出ウィンドウに侵入することを抑制され得る、固定磁石に十分に近接する位置に送達できる。物理的障壁を利用する実施形態に関して、液滴を検出ウィンドウに輸送する工程は、ビーズが物理的障壁によって検出ウィンドウ内に侵入することを抑制している間に達成されてもよい。このビーズが検出ウィンドウに侵入することを抑制することは、液滴から磁性反応ビーズを除去して、または除去せずに達成されてもよい。磁場を利用する本発明のこれらおよび任意の他の実施形態において、磁場は、任意の適切な磁場源によって生成されてもよい。例えば、磁場源は、固定永久磁石、移動可能な永久磁石、および/または電磁石を備えてもよい。磁場は、液滴の端部に磁性反応ビーズを凝集させるために配置されてもよい。磁場は、検出ウィンドウの外側であり得る液滴の領域内に磁性反応ビーズを凝集させるために配置されてもよい。一部の場合において、磁場は、液滴から離れた位置に磁性反応ビーズを分裂させるために選択される。例えば、磁場は、液滴が所定の位置に保持され得る間、および/または電極により媒介される力によって移動され得る間、磁性反応ビーズを液滴から離れた位置に分裂させることができる。一部の場合において、液滴が検出ウィンドウ内に少なくとも部分的に存在し得る場合、磁場は、磁性反応ビーズを液滴の端部に引き付ける方法で磁性反応ビーズを引き付ける。一部の場合において、液滴が磁石上を通過する場合、磁場は液滴の外側に磁性反応ビーズを引き付ける。一部の場合において、液滴が磁石の近くに近づく場合、磁場は液滴の外側に磁性反応ビーズを引き付ける。一部の場合において、液滴が検出ウィンドウに近づく場合、磁場は液滴の外側に磁性反応ビーズを引き付ける。一部の場合において、液滴が検出ウィンドウ内に輸送され得る場合、磁場は、実質的に全てのビーズが検出ウィンドウに侵入するか、または再侵入することを抑制する方法で磁性反応ビーズを引き付ける。検出ウィンドウは、液滴アクチュエータ装置の表面に設けられてもよい。液滴アクチュエータは、例えば、液滴操作表面に結合される電極の複数の経路、検出ウィンドウに結合される各々の経路、ならびに検出ウィンドウ内に液滴を輸送および/または保有している間、対応する検出ウィンドウから磁性反応ビーズを磁性的に除去するように、および/または磁性反応ビーズが対応する検出ウィンドウに侵入することを磁性的に抑制するように配置される経路に近接する磁場を備える。液滴は、1つ以上の検体の存在、非存在および/または量の指標であるシグナルを放出できる。例えば、1つ以上の検体は増幅核酸を含んでもよい。検出ウィンドウは液滴アクチュエータの表面に配置されてもよく、液滴アクチュエータは、熱サイクル反応を実施するための電極の経路に沿った温度制御ゾーンを備えてもよい。そのような液滴アクチュエータを使用する方法は、増幅液滴を得るために増幅準備液滴を熱サイクルする工程、および増幅液滴を検出ウィンドウに輸送する工程を含んでもよい。その方法は、1以上の熱サイクルの後、電極の経路から少なくとも部分的に電極の経路に沿って磁性反応ビーズを含み得る液滴を、検出ウィンドウ内に輸送する工程を含んでもよい。
【0012】
本発明はまた、液滴を熱サイクルする方法を提供する。その方法は、充填流体によって少なくとも部分的に囲まれた液滴を提供する工程を含んでもよい。液滴は、潜在的に標的核酸を含んでもよい。液滴は、標的核酸の存在下で増幅を生じるのに十分な試薬を含んでもよく、試薬は、熱サイクルプロトコルを実施している間、充填流体中で有意に分離しないフルオロフォアを含んでもよい。その方法は、標的核酸の存在下で増幅を誘導するために熱サイクルプロトコルに従って液滴の温度を調節する工程を含んでもよい。フルオロフォアは極性フルオロフォアを含んでもよい。フルオロフォアは細胞膜に実質的に不浸透性であってもよい。フルオロフォアは細胞膜に完全に不浸透性であってもよい。フルオロフォアはEVAGREEN(登録商標)フルオロフォアを含んでもよい。フルオロフォアはTO−PRO1フルオロフォアを含んでもよい。充填流体は、本質的にシリコーンオイルから構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、10〜20の炭素オイルから構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、15〜20の炭素オイルから本質的に構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、ヘキサデカンオイルから本質的に構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、実質的な脱気水から本質的に構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。液滴を提供する工程は、液滴を液滴アクチュエータの液滴操作間隙に提供する工程を含んでもよい。熱サイクルプロトコルに従って液滴の温度を調節する工程は、液滴アクチュエータの液滴操作間隙の液滴を加熱および/または冷却する工程を含んでもよい。熱サイクルプロトコルに従って液滴の温度を調節する工程は、電極により媒介される液滴操作を用いて液滴操作間隙内の熱領域の間に液滴を輸送する工程を含んでもよい。
【0013】
本発明は、液滴アクチュエータでプロトコルを実行する方法を含む。その方法は、不動態化剤を含み得る液滴を有する領域内で1つ以上の電極で液滴操作を実施することによって液滴アクチュエータの1つ以上の領域を処理する工程、および液滴アクチュエータの1つ以上の処理された領域を用いてプロトコルを実施する工程を含む。そのプロトコルは、標的核酸の解析における工程を含んでもよく、不動態化剤は標的核酸でなくてもよい核酸を含んでもよい。そのプロトコルは核酸増幅プロトコルを含んでもよい。そのプロトコルは熱サイクルプロトコルを含んでもよい。少し例を挙げると、不動態化剤は、核酸、ポリビニルピロリドン、ポリエチレングリコール、界面活性剤、トゥイーン(tween)、アルブミン、血清アルブミン、ウシ血清アルブミン、および/または色素を含んでもよい。不動態化剤は、液滴アクチュエータの表面上に吸着するように選択されてもよい。不動態化剤は、充填流体内に吸着するように選択されてもよい。1つ以上の液滴は、十分な不動態化剤を実質的に飽和する可能性のある不動態化部位に送達してもよい。そのプロトコルは、不動態化剤を含む液滴を用いて実施されてもよい。一例として、そのプロトコルは、核酸増幅プロトコルを含んでもよい。核酸増幅プロトコルおよび処理する工程は、核酸増幅試薬および不動態化剤を含む液滴を用いて同時に実施されてもよい。
【0014】
本発明はまた、高温で液滴操作を実施するための液滴アクチュエータを提供する。液滴アクチュエータは、液滴操作基板および液滴操作表面とカバーとの間に液滴操作間隙を形成するために液滴操作表面に隣接し、液滴操作表面から離れているカバーを備えてもよく、液滴操作間隙は少なくとも250μmの高さを有する。液滴アクチュエータは、液滴操作基板および/またはカバーに結合され、熱サイクルプロトコルに従って熱領域の間に液滴を輸送するように配置される電極の経路を備えてもよい。液滴アクチュエータは、液滴操作間隙内の1つ以上の熱領域を規定するように配置される温度制御素子を備えてもよい。一部の場合において、液滴操作間隙は、実質的に球状の形状の単一のサイズの液滴を与えるように選択される高さを有してもよい。例えば、特定の実施形態において、約250μm〜約500μm、または約275μm〜約450μm、または約300μm〜約400μm、または約320μm〜約375μm、または約320μm〜約350μmの範囲の高さを有してもよい。特定の実施形態において、電極はピッチを有してもよく、液滴操作間隙は、約7:1〜約2.8:1、または約6:1〜約3:1、または約4.3:1〜約3.4:1の範囲の比のピッチ:高さを規定する高さを有してもよい。特定の実施形態において、液滴操作間隙は、熱サイクルプロトコルを受ける液滴から完全な熱サイクルプロトコルについて5%未満、または完全な熱サイクルプロトコルについて1%未満、または完全な熱サイクルプロトコルについて0.01%未満の容積減少を維持するように選択される高さを有する。特定の実施形態において、液滴操作間隙は、熱サイクルプロトコルを受ける液滴から1回の熱サイクルにつき0.1%未満、または1回の熱サイクルにつき0.01%未満、または1回の熱サイクルにつき0.001%未満の容積減少を維持するように選択される高さを有する。一部の場合において、液滴操作間隙は、熱サイクルプロトコルの間、実質的に容積減少を排除するように選択される高さを有する。本発明はまた、熱サイクル反応を実施する方法を提供し、その方法は、本発明のこの態様の液滴アクチュエータを提供する工程、電極の経路に沿って、磁性反応ビーズを含み得る液滴を、検出ウィンドウ内の少なくとも部分的に電極の経路に輸送する工程であって、その結果、磁石が、1つ以上のビーズが検出ウィンドウに侵入することを抑制する方法で磁性反応ビーズを引き付ける、工程、および液滴からのシグナルを検出するためにセンサーを使用する工程を含んでもよい。
【0015】
本発明は、解析用のサンプルを調製する方法を提供する。その方法は、液滴操作基板、基板の液滴操作表面上で液滴操作を実施するように配置される電極、液滴操作表面に隣接し、液滴操作表面とカバーとの間に液滴操作間隙を形成するために液滴操作表面から離れているカバー、上部基板に結合され、1つ以上の標的検体および/または1つ以上の標的検体を含み得る物質に対する親和性を有するビーズを含み得るリザーバー、リザーバーから液滴操作間隙内に延びる液体経路、液滴操作基板に結合され、磁性反応ビーズを引き付けるのに十分な磁場を生じるように構成される磁場源を備える液滴アクチュエータを提供する工程を含んでもよい。その方法は、サンプルをリザーバーに供給する工程を含んでもよい。サンプルは1つ以上の標的物質を含んでもよい。その方法は、液滴経路を通して液滴操作間隙に磁性反応ビーズとともにサンプルを流動させる工程を含んでもよい。その方法は、磁石で磁性反応ビーズを凝集させる工程を含んでもよい。その方法は、磁性反応ビーズを有する液滴操作間隙内のサンプル液滴を得るために、磁場を除去する工程または磁場からビーズを除去する工程を含んでもよい。一部の場合において、液体経路は、(より湾曲した液体経路とは対照的に)基板における穴または開口部などの実質的に真っ直ぐな液体経路であってもよい。磁石は、リザーバーから液滴操作間隙内に1つ以上のビーズを引き付けるのに十分な磁場の強さを有してもよい。液滴アクチュエータは、液滴操作基板に結合され、液体経路を介して液滴操作間隙に侵入する流体を受容するように配置されるリザーバー電極を備えてもよい。磁石は液体経路に対してリザーバー電極の反対側に配置されてもよい。磁石は、電磁石または永久磁石などの適切な磁場を生成するための任意の要素または要素の組み合わせであってもよい。磁石は空間的に調節可能である。磁石は、第1の位置において液滴操作間隙内の永久磁石の磁場をブロックまたは妨げることができるか、あるいは第2の位置において液滴操作間隙内の永久磁石の磁場をブロックまたは妨げることができない可動式磁気シールドに結合されてもよい。液滴アクチュエータは、リザーバー内のサンプル流体を撹拌するように配置される撹拌器を備えてもよく、その方法は、リザーバー内のサンプルを撹拌する工程を含んでもよい。液滴アクチュエータは、音波エネルギーをリザーバー内のサンプル流体に与えるように配置される超音波処理器を備えてもよく、その方法は、リザーバー内のサンプルを超音波処理する工程を含んでもよい。液滴アクチュエータはまた、1つ以上の電極に結合される第2の磁石を備えてもよい。物質は、ビーズが親和性を有する1つ以上の標的検体を含んでもよい。一実施形態において、標的検体は細胞を含み、その方法は、細胞を溶解または分解する工程を含む。例えば、細胞を溶解する工程は、溶解試薬を、細胞を含む液滴に加えることによって達成されてもよい。一例として、溶解試薬を加える工程は、磁性反応ビーズを含む液滴操作間隙内のサンプル液滴と、細胞溶解試薬を含む溶解液滴とを混合する工程を含む。混合した液滴は超音波処理されてもよいか、あるいは混合するために攪拌または振盪されてもよい。その方法は、一部の場合、磁性反応ビーズを固定するために磁場を再印加する工程を含んでもよい。その方法は、固定された磁性反応ビーズから離れた位置に液滴を輸送する工程を含んでもよい。その方法は、磁性反応ビーズから離れた位置に液滴の一部を輸送する工程を含んでもよい。その方法は、離れた位置に輸送された液滴または液滴の一部と、1つ以上の標的検体に対する親和性を有するビーズを含む液滴とを混合する工程を含んでもよい。その方法は、1つ以上の標的検体に対する親和性を有するビーズを洗浄するための洗浄プロトコルを実施する工程であって、実質的に精製された標的検体を含むビーズを有する液滴を生じる工程を含んでもよい。その方法は、実質的に精製された標的検体を含むビーズを有する液滴を用いて解析プロトコルを実施する工程を含んでもよい。解析プロトコルの工程は、液滴操作間隙内または液滴操作間隙外で達成されてもよい。解析プロトコルの工程は、液滴アクチュエータ上、別の液滴アクチュエータ上、または液滴アクチュエータを使用せずに達成されてもよい。例えば、ビーズおよび実質的に精製された標的検体を含む液滴は、解析プロトコルを実施する前に液滴操作間隙から除去されてもよい。その方法は、液滴操作間隙間から実質的に精製された標的検体を有するビーズを除去する工程を含んでもよい。その方法は、ビーズから1つ以上の標的検体を溶出する工程を含んでもよい。溶出する工程は、実質的に精製された標的検体を含むビーズを含む液滴と、溶出バッファーを含む液滴とを混合する工程であって、ビーズを含む液滴および溶出された1つ以上の標的検体を生じる工程を含んでもよい。その方法は、実質的に精製された標的検体を含み、かつ実質的にビーズを含まない液滴を得るために、ビーズおよび溶出された1つ以上の標的検体を含む液滴からビーズを除去する工程を含んでもよい。除去する工程は、例えば、磁場および/または物理的障壁を用いて行われてもよい。その方法は、実質的に精製された標的検体を含み、かつ実質的にビーズを含まない液滴を、液滴操作間隙から除去する工程を含んでもよい。その方法は、実質的に精製された標的検体を含み、かつ実質的にビーズを含まない液滴を用いて解析プロトコルを実施する工程を含んでもよい。そのプロトコルは、液滴操作間隙内または外において、液滴アクチュエータ上で、または液滴アクチュエータ外で行われてもよい。本明細書に記載されるアッセイプロトコルのいずれかは、解析プロトコルの結果のアウトプット指標を提供する工程を含んでもよい。その方法の工程の1つ以上は、その方法の工程の1つ以上を実行するようにプログラムされた液滴アクチュエータおよびプロセッサを含むシステムによって実行されてもよい。その方法は、解析プロトコルの結果のユーザーが判読可能なアウトプット指標をアウトプットする工程を含んでもよい。標的検体は、核酸、タンパク質またはペプチド、抗体、小有機分子などを含んでもよい。液滴操作間隙は流動性の充填流体で満たされてもよい。
【0016】
本発明は液滴アクチュエータを操作する方法を提供する。本発明は、内部液滴操作間隙を形成するように構成される1つ以上の基板を備える液滴アクチュエータ装置を提供する工程を含んでもよい。その方法は、液滴操作間隙内に流動性の充填流体を提供する工程を含んでもよい。その方法は、液滴操作間隙内の充填流体中で液滴プロトコルを実行する工程を含んでもよい。その方法は、液滴操作間隙内の充填流体を置き換える工程を含んでもよい。一旦、充填流体が置き換えられると、その方法は、液滴操作間隙内の充填流体中で別の液滴プロトコルを実行する工程を含んでもよい。本発明は、共通の液滴アクチュエータ上で、液滴プロトコル実行の間に充填流体の交換が実施される複数の液滴プロトコルを提供する。従って、例えば、本発明は、充填−実行−再充填パターンの使用を含んでもよく、実行−再充填は、数回、例えば2、5、10、20、50、100またはそれ以上繰り返される。同様に、本発明は、充填−実行−実行−再充填パターンの使用を含んでもよく、実行−実行−再充填は、数回、例えば2、5、10、20、50、100またはそれ以上繰り返される。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙を通して充填流体をフラッシングする工程を含んでもよい。液滴操作間隙を通して充填流体をフラッシング工程は、所定量のフラッシングが達成するまで続けてもよい。液滴操作間隙を通して充填流体をフラッシングする工程は、洗浄の指標(例えば除去された充填流体中で測定される汚染)が所定のレベルに到達するまで続けてもよい。フラッシングの量は自動化されてもよい。液滴プロトコルは、例えば、標的検体の存在および/または量を測定するためのプロトコルを含んでもよい。例えば、プロトコルは診断的プロトコルであってもよい。少しの例を挙げると、液滴プロトコルは、核酸増幅プロトコル、核酸シークエンシングプロトコル、免疫学的検定プロトコル、および/または酵素アッセイプロトコルであってもよい。一部の実施形態において、流動性の充填流体は、充填流体を置き換える間、汚染について試験されてもよく、別のプロトコルの実行が、所定のレベルの汚染の減少が達成された後に行われてもよい。このプロセスは自動化されてもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙を通して、および液滴操作間隙の外側に、流動性の充填流体源から流動性の充填流体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える前に、液滴操作間隙を通して洗浄流体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を交換する前に、液滴操作間隙を通して充填流体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える前に、液滴操作間隙を通して加熱された洗浄液体を流動させる工程を含んでもよい。加熱された洗浄液体は、汚染物質を分解するように選択される温度を有してもよい。例えば、種々の実施形態において、温度は、約30℃〜約125℃、または約60℃〜約115℃、または約75℃〜約105℃、または約90℃以上、または約100℃以上、または約125℃以上、または約150℃以上の範囲である。温度は、典型的に、液滴アクチュエータの1つ以上の構成要素が過度な損傷、すなわち、液滴アクチュエータ装置にその意図される使用に対する損傷を受ける温度未満である。充填流体などの冷却液体は、加熱された洗浄後に、適切または操作可能な温度を設定するために液滴アクチュエータ間隙を通して流されてもよい。加熱された洗浄液体は、例えば、充填流体、オイル、溶媒、および/または水性洗浄液体を含んでもよい。洗浄液体は、親油性物質が可溶性であり得る成分および親水性物質が可溶性であり得る成分を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える前に、液滴アクチュエータ間隙を乾燥させるために、液滴アクチュエータ間隙を通してガスを流動させる工程を含んでもよい。ガスは空気または別のガスであってもよい。ガスは、洗浄液体の温度と比較して、加熱または冷却されてもよい。ガスは、例えば、約50℃以上、約75℃以上、約100℃以上、約125℃以上、または約150℃以上の温度を有してもよい。温度は、典型的に、液滴アクチュエータの1つ以上の構成要素が過度な損傷、すなわち、液滴アクチュエータ装置にその意図される使用に対する損傷を受ける温度未満である。液滴操作間隙内の充填流体を置き換える工程は、液滴アクチュエータ間隙を通してガスを流動させる工程の前に、液滴アクチュエータ間隙を通して洗浄液体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内に存在する少なくとも約50%の充填流体、または液滴操作間隙内に存在する少なくとも約75%の充填流体、または液滴操作間隙に存在する少なくとも約90%の充填流体、または液滴操作間隙に存在する少なくとも約95%の充填流体、または液滴操作間隙に存在する少なくとも約99%の充填流体、または液滴操作間隙に存在する少なくとも約99.9%の充填流体、または液滴操作間隙に存在する実質的に全ての充填流体を置き換える工程を含んでもよい。液滴操作間隙の1つ以上の表面はコーティングを含んでもよく、洗浄液体はコーティングの層を除去するために選択されてもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える工程の前に所定の温度を設定するために、液滴操作間隙を通して冷却液体を流動させる工程を含んでもよい。洗浄流体は溶媒を含んでもよい。洗浄流体は水溶液を含んでもよい。洗浄流体は、新油性化合物を溶解する1つ以上の成分および親水性化合物を溶解する1つ以上の成分を含んでもよい。本発明は、本発明の充填流体を置き換える方法を実行するための命令を有するプログラムを有するコンピューターにより読取可能な媒体を提供する。本発明は、内部液滴操作間隙を形成するように構成される1つ以上の基板、流動性の充填流体源に流動的に接続される液滴操作間隙内の開口部、その開口部を通して、液滴操作間隙内に充填流体源から充填流体の流れを制御するように構成される1つ以上の弁および/またはポンプ、ならびに本発明の充填流体の交換および/または洗浄のいずれかを実行するようにプログラムされる1つ以上のポンプおよび/または弁を制御するプロセッサを備える液滴アクチュエータ装置を有するシステムを提供する。
【0017】
本発明は、液滴操作間隙を形成する1つ以上の基板を備える液滴アクチュエータを提供する。液滴操作間隙は、液体経路によって流動的に結合される少なくとも2つの温度制御リザーバーを規定する熱サイクル経路および1つ以上の障壁、ならびに1つまたは両方の基板に結合され、温度制御リザーバーの間に液滴を輸送するように構成される電極を備えてもよい。液滴アクチュエータは2つ以上のこのような熱サイクル経路を備えてもよい。
【0018】
本発明は、液滴アクチュエータ上での液滴間の二次汚染を阻害する方法を提供する。その方法は、液滴操作間隙を形成する1つ以上の基板、複数の実質的に平行な液滴輸送経路を規定する1つ以上の基板に結合される電極、および液滴操作間隙を実質的に充填する流動性の充填流体を有する液滴アクチュエータを提供する工程を含んでもよい。その方法は、第1のサブセットの複数の実質的に平行な液滴輸送経路上に複数のアッセイ液滴を輸送する工程を含んでもよい。その方法は、第2のサブセットの複数の実質的に平行な液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよく、その第2のサブセットの各々の液滴輸送経路は、第1のサブセットの2つの液滴輸送経路の間に存在してもよい。アッセイ液滴を輸送する工程および液滴を洗浄する工程は同時に行われてもよい。2つ以上の洗浄液滴は、第2のサブセットの各々の液滴輸送経路上に提供/輸送されてもよい。洗浄液滴は、液滴または液滴スラグ(細長い液滴)の形態で提供されてもよい。その方法は、第1のサブセットの液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよい。その方法は、第1のサブセットの液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよい。その方法は、第1の洗浄液滴に対してアッセイ液滴の反対側の第1のサブセットの液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよい。アッセイ液滴は核酸増幅液滴を含んでもよい。その方法は、増幅を行うために2つの熱領域の間にアッセイ液滴を輸送する工程を含んでもよい。
【0019】
本発明はまた、液滴操作間隙を設けるように配置される1つ以上の基板、複数の実質的に平行な液滴輸送経路を規定する1つ以上の基板に結合される電極、液滴操作間隙を実質的に充填する流動性の充填流体、ならびに液滴輸送経路の各々の間にあり、1つの液滴操作経路と結合される充填流体が、他の液滴操作経路と結合される充填流体と接触することを防ぐ障壁を有する液滴アクチュエータを提供する。液滴アクチュエータは、2つ以上の液滴輸送経路上にアッセイ液滴を含んでもよい。アッセイ液滴は、核酸を増幅するための試薬およびサンプルを含んでもよい。
【0020】
本発明は、液滴アクチュエータ上の液滴間の二次汚染を減少させる方法を提供する。その方法は、内部液滴操作間隙および液滴操作間隙内のオイルベースの充填流体を含み得る液滴アクチュエータを提供する工程、ならびに液滴操作間隙内に水性液滴を提供する工程を含んでもよい。液滴は、オイルベースの充填流体によって少なくとも部分的に囲まれてもよい。液滴は界面活性剤−酵素複合体を含んでもよく、その複合体は、潜在的な汚染物質を分解するように選択される酵素に結合された界面活性剤を含んでもよい。適切な酵素のいくつかの非限定的な例としては、ヌクレアーゼ、エンドヌクレアーゼ、エキソヌクレアーゼ、および/またはプロテイナーゼが挙げられる。界面活性剤に関して、任意の適切な界面活性剤が使用されてもよい。例としては、ポリエチレン(PEG)−アルキル界面活性剤などのポリアルカレン(PAG)−アルキル界面活性剤が挙げられる。界面活性剤−酵素複合体は、酵素−PAG−アルキル複合体を含んでもよい。界面活性剤は、例えば、酵素のアミノ部分に結合されてもよい。界面活性剤−酵素複合体は、液滴内で実質的に不活性であるように十分に低く、液滴から形成され得る、微小液滴、マイクロ液滴またはナノ液滴内で活性であるように十分に高い量で液滴に存在してもよい。一部の場合において、その量は、約10μL未満、または約1μL未満、または約0.01μL未満、または約0.001μL未満であり得る平均容積を有する微小液滴内で活性であるように選択される。一部の場合において、平均液滴サイズ対平均微小液滴サイズの比は、約1000対約1未満、または約1000対約0.1未満、または約1000対約0.01未満、または約1000対約0.001未満であり得る。潜在的な汚染物質としては、例えば、タンパク質、核酸、または試薬が挙げられ得る。特定の実施形態において、界面活性剤−酵素複合体の実質的に全ては、液滴の表面に捕捉されてもよい。充填流体は、シリコンオイルなどのオイルを含んでもよい。液滴は、充填流体によって部分的に囲まれてもよい。液滴は、充填流体によって実質的に囲まれてもよい。液滴は、充填流体によって完全に囲まれてもよい。
【0021】
本発明は、デジタル増幅法を提供する。その方法は、標的核酸、および必要に応じて増幅試薬を含むサンプル液滴を提供する工程を含んでもよい。その方法は、サンプル液滴から小液滴を分配する工程、および増幅試薬がサンプル液滴に存在し得ない場合、増幅準備液滴を得るために各々の小液滴と増幅試薬とを混合する工程を含んでもよい。その方法は、各々の小液滴を、標的核酸を増幅するために選択される熱サイクルプロトコルに供する工程を含んでもよい。その方法は、各々の小液滴内の増幅産物を検出する工程を含んでもよい。その方法は、サンプル部を含む小液滴の数を決定する工程を含んでもよく、そのサンプル部から上記増幅産物が形成されてもよい。典型的に、上記小液滴の少なくとも1つは、少なくとも1つの標的核酸分子を含む。増幅試薬は、増幅標的分子に対してハイブリダイズし、ハイブリダイゼーションの際に変化するか、またはハイブリダイゼーションの結果として変化する蛍光特性を有する少なくとも1つのプローブを含んでもよい。その方法は、サンプル部を含む小液滴の数を決定する工程を含んでもよく、そのサンプル部から上記増幅産物が形成される。一部の場合において、決定する工程は、上記少なくとも1つのプローブのハイブリダイゼーションに起因する蛍光変化を検出する工程を含んでもよい。上記増幅産物が形成され得るサンプル部を含む小液滴の数を決定する工程は、全ての小液滴を一緒に画像化する工程を含んでもよい。上記増幅産物が形成され得るサンプル部を含む小液滴の数を決定する工程は、検出ウィンドウを通して一つずつまたは小液滴内の液滴を輸送する工程を含んでもよい。小液滴は、約1μL未満、または約1μL以上〜約1000μLの範囲、または約100μL以上〜約500μLの容積を有してもよい。この1つ以上の系統および本発明の他の方法は、液滴アクチュエータの液滴操作間隙内で実施されてもよい。小液滴は、液滴操作間隙内の2つの基板の間で平らまたはディスク形状の構造に圧縮されてもよい。液滴操作間隙は、約50μm〜約1000μm、または約100μm以上〜約500μmの範囲の高さを有してもよい。熱サイクルは、1つの熱領域から別の熱領域へ液滴を輸送することによって行われてもよい。特定の実施形態において、液滴アクチュエータはサンプルチャンバを欠く。特定の実施形態において、液滴アクチュエータは流路チャネルを欠く。特定の実施形態において、サンプル液滴から小液滴を分配する工程は、流路チャネルからサンプルを配置する配置流体を用いずに行われてもよい。特定の実施形態において、標的核酸を含むサンプル液滴はまた、増幅試薬を含んでもよい。特定の実施形態において、増幅試薬はサンプル液滴に存在しなくてもよく、その方法は、各々の小液滴と増幅試薬とを混合して増幅準備試薬を生じる工程を含んでもよい。特定の実施形態において、各々の小液滴中の増幅産物を検出する工程は、液滴を検出に供する前に、増幅液滴と1つ以上の検出試薬を含む液滴とを混合する工程を含んでもよい。
【0022】
本発明のこれらの態様および多くの他の態様は、本明細書の残りの段落および添付の特許請求の範囲から明らかになるだろう。
【0023】
(5.定義)
本明細書で使用する場合、以下の用語は示される意味を有する。
【0024】
1つ以上の電極に関して「活性化する」とは、液滴の存在下において、1つ以上の電極の電気状態の変化を与えることにより、液滴操作を生じさせることを意味する。
【0025】
液滴アクチュエータ上のビーズに関して「ビーズ」とは、液滴アクチュエータ上で、または液滴アクチュエータと近接して、液滴と相互作用できる任意のビーズまたは粒子を意味する。ビーズは、球形、ほぼ球形、卵形、円盤形状、立方体および他の三次元形状などの様々な形状のいずれかであってもよい。ビーズは、例えば、液滴アクチュエータ上の液滴中で輸送され得るか、あるいは液滴アクチュエータ上の液滴が、液滴アクチュエータ上および/または液滴アクチュエータの外でビーズと接触できる方法で液滴アクチュエータに対して構成され得る。ビーズは、例えば、樹脂およびポリマーを含む、様々な材料を用いて製造されてもよい。ビーズは、例えば、マイクロビーズ、マイクロ粒子、ナノビーズおよびナノ粒子を含む、任意の適切なサイズであってもよい。一部の場合において、ビーズは磁性反応であり、他の場合において、ビーズは、著しく磁性反応でなくてもよい。磁性反応ビーズに関して、磁性反応材料は、ビーズの実質的に全てまたはビーズの1つの成分のみを構成してもよい。ビーズの残りは、特に、アッセイ試薬の結合を可能にするポリマー性の材料、コーティング、および部分を含んでもよい。適切な磁性反応ビーズの例は、2005年11月24日に公開された「Multiplex flow assays preferably with magnetic particles as solid phase」という発明の名称の米国特許出願公開第2005−0260686号に記載されており、その全開示は、磁性反応材料およびビーズに関するその教示のために本明細書に参照として援用される。流体は、1つ以上の磁性反応ビーズおよび/または非磁性反応ビーズを含んでもよい。磁性反応ビーズおよび/または非磁性反応ビーズを固定するための液滴アクチュエータ技術ならびに/あるいはビーズを用いて液滴操作プロトコルを実施するための液滴アクチュエータ技術の例は、2006年12月15日に出願された「Droplet−Based Particle Sorting」という発明の名称の米国特許出願公開第11/639,566号;2008年3月25日に出願された「Multiplexing Bead Detection in a Single Droplet」という発明の名称の米国特許出願公開第61/039,183号;2008年4月25日に出願された「Droplet Actuator Devices and Droplet Operations Using Beads」という発明の名称の米国特許出願公開第61/047,789号;2008年8月5日に出願された「Droplet Actuator Devices and Methods for Manipulating Beads」という発明の名称の米国特許出願公開第61/086,183号;2008年2月11日に出願された「Droplet Actuator Devices and Methods Employing Magnetic Beads」という発明の名称の国際特許出願第PCT/US2008/053545号;2008年3月24日に出願された「Bead−based Multiplexed Analytical Methods and Instrumentation」という発明の名称の国際特許出願第PCT/US2008/058018号;2008年3月23日に出願された「Bead Sorting on a Droplet Actuator」という発明の名称の国際特許出願第PCT/US2008/058047号;および2006年12月11日に出願された「Droplet−based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/047486号に記載されており、その全開示は本明細書に参照により援用される。
【0026】
「液滴」とは、充填流体に少なくとも部分的に結合される液滴アクチュエータ上の液体の量を意味する。例えば、液滴は充填流体によって完全に囲まれてもよいか、または充填流体および液滴アクチュエータの1つ以上の表面に結合されてもよい。液滴は、例えば、水溶性であっても、非水溶性であってもよいか、または水溶性および非水溶性成分を含む混合物もしくはエマルションであってもよい。液滴は様々な形状をとってもよく、非限定的な例として、ほぼ円盤形状、スラグ形状、切頭球体、楕円、球形、部分的に圧縮された球形、半球形、卵形、円筒形、および液滴アクチュエータの1つ以上の表面と、そのような形状との接触の結果として融合または分裂または形成されるなどの液滴操作の間に形成された種々の形状が挙げられる。本発明のアプローチを用いて液滴操作に供され得る液滴流体の例に関しては、2006年12月11日に出願された「Droplet−Based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/47486号を参照のこと。種々の実施形態において、液滴は、全血、リンパ液、血清、血漿、汗、涙、唾液、痰、脳脊髄液、羊水、精液、膣排出液、漿液、滑液、心膜液、腹水、胸膜液、浸出液、滲出液、嚢胞液、胆汁、尿、胃液、腸液、糞便試料、単細胞または多細胞を含む液体、細胞小器官を含む液体、流動組織、流動器官、多細胞生物を含む液体、生物学的スワブおよび生物学的洗浄液などの生物学的サンプルを含んでもよい。さらに、液滴は、水、脱イオン水、生理的食塩水、酸性溶液、塩基性溶液、清浄液および/または緩衝液などの試薬を含んでもよい。液滴内容物の他の例としては、核酸増幅プロトコル、親和性ベースアッセイプロトコル、酵素アッセイプロトコル、シークエンシングプロトコル、および/または生物学的流体の解析のためのプロトコルなどの生物学的プロトコルのための試薬などの試薬が挙げられる。
【0027】
「液滴アクチュエータ」とは、液滴を操作するための装置を意味する。液滴アクチュエータの例に関しては、Pamulaらによる2005年6月28日に発行された「Apparatus for Manipulating Droplets by Electrowetting−Based Techniques」という発明の名称の米国特許第6,911,132号;2006年1月30日に出願された「Apparatuses and Methods for Manipulating Droplets on a Printed Circuit Board」という発明の名称の米国特許出願公開第11/343,284号;両方、Shenderovらによる、2004年8月10日に発行された「Electrostatic Actuators for Microfluidics and Methods for Using Same」という発明の名称の米国特許第6,773,566号および2000年1月24日に発行された「Actuators for Microfluidics Without Moving Parts」という発明の名称の同第6,565,727号;Pollackら、2006年12月11日に出願された「Droplet−Based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/047486号;ならびにRouxら、2005年8月18日に公開された「Device for Controlling the Displacement of a Drop Between two or Several Solid Substrates」という発明の名称の米国特許出願公開第20050179746号を参照のこと(これらの開示は本明細書に参照として援用される)。特定の液滴アクチュエータは、基板、基板に結合された液滴操作電極、液滴操作表面を形成する基板および/または電極の上の1つ以上の誘電層および/または疎水性層、ならびに必要に応じて、液滴操作間隙によって液滴操作表面から分離された上部基板を備える。1つ以上の参照電極が、上部または底部の基板ならびに/あるいは液滴操作間隙内に設けられてもよい。種々の実施形態において、液滴アクチュエータによる液滴の操作は、電極により媒介、例えばエレクトロウェッティングにより媒介、または誘電泳動により媒介、またはクーロン力により媒介されてもよい。本発明の液滴アクチュエータに使用され得る液体の流れを制御する他の方法の例としては、機械的原理(例えば外部シリンジポンプ、空気圧膜ポンプ、振動膜ポンプ、真空装置、遠心力、圧電/超音波ポンプおよび音響力);電気または磁気的原理(例えば電気浸透流、動電学的ポンプ、磁性流体プラグ、電気流体力学ポンプ、磁場を用いる引力または斥力および電磁流体力学的ポンプ);熱力学的原理(例えば気泡生成/相変化誘発体積膨張);他の種類の表面湿潤原理(例えばエレクトロウェッティングおよびオプトエレクトロウェッティング、ならびに化学的、熱的、構造的、および放射活性的に誘発される表面張力勾配);重力;表面張力(例えば毛細管現象);静電気力(例えば電気浸透流);遠心力を利用した流れ(コンパクトディスクに配置され、回転される基板);磁場(例えば周期的に振動するイオンが流れを引き起こす);電磁流体力学的力;ならびに真空または圧力差に基づいて操作するものなどの流体力学的流体圧力を含む装置が挙げられる。特定の実施形態において、2つ以上の上述の技術の組み合わせが、本発明の液滴アクチュエータに利用されてもよい。
【0028】
「液滴アクチュエータ」とは、液滴アクチュエータ上での液滴の任意の操作を意味する。液滴操作としては、例えば、液滴アクチュエータに液滴を負荷すること、液滴源から1つ以上の液滴を分配すること、1つの液滴を2つ以上の液滴に分裂、分離、または分割すること、任意の方向において液滴を1つの位置から別の位置に輸送すること、2つ以上の液滴を単一の液滴に融合または混合すること、液滴を希釈すること、液滴を混合すること、液滴を攪拌すること、液滴を変形させること、液滴を所定の位置に保持すること、液滴をインキュベートすること、液滴を加熱すること、液滴を蒸発させること、液滴を冷却すること、液滴を配置すること、液滴アクチュエータの外部へ液滴を輸送すること、本明細書に記載される他の液滴操作、および/または上述の任意の組み合わせが挙げられ得る。用語「融合する」、「融合している」、「混合する」、「混合している」などは、2つ以上の液滴から1つの液滴を生成することを述べるのに使用される。そのような用語が、2つ以上の液滴に関して使用される場合、2つ以上の液滴の1つの液滴への混合を生じるのに十分な液滴操作の任意の組み合わせが使用されてもよいことは理解されるべきである。例えば、「液滴Aと液滴Bとを融合する」ことは、液滴Aを静止液滴Bと接触するように輸送すること、液滴Bを静止液滴Aと接触するように輸送すること、または液滴AおよびBを互いに接触するように輸送することによって達成され得る。用語「分裂している」、「分離している」、「分割している」とは、得られる液滴の容積に対する任意の特定の結果、または得られる液滴の数に対する任意の特定の結果を表すことを意図しない(すなわち得られる液滴の容積は同じであっても、異なっていてもよいか、あるいは得られる液滴の数は2、3、4、5またはそれ以上であってもよい)。用語「混合する」とは、液滴内の1つ以上の成分のより均一な分布を生じる液滴操作を指す。液滴を「負荷する」操作の例としては、微小透析負荷、圧力支援による負荷、ロボットによる負荷、不動態による負荷、およびピペットによる負荷が挙げられる。液滴操作は電極により媒介されてもよい。一部の場合において、液滴操作は、表面上の親水性および/または疎水性領域の使用によって、ならびに/あるいは物理的障壁によってさらに容易にされる。
【0029】
「充填流体」とは、液滴アクチュエータの液滴操作基板に結合する液体を意味し、その液体は、液滴相が電極により媒介される液滴操作を受けるように液滴相と十分に混ざらない。充填流体は、例えば、シリコーンオイルなどの低粘度のオイルであってもよい。充填流体の他の例は、2006年12月11日に出願された「Droplet−Based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/047486号;2008年8月8日に出願された「Use of additives for enhancing droplet actuation」という発明の名称の国際特許出願第PCT/US2008/072604号;および2007年5月17日に出願された「Electrowetting Devices」という発明の名称の米国特許出願公開第20080283414号(その全開示は本明細書に参照として援用される)に提供される。充填流体は、液滴アクチュエータの間隙全体を満たしてもよいか、または液滴アクチュエータの1つ以上の表面を覆ってもよい。充填流体は、導電性であっても、または非導電性であってもよい。「充填物質」は、凝固または硬化されたワックス、油脂またはオイルなどの凝固または硬化された充填流体である。
【0030】
磁性反応ビーズに関して「固定する」とは、ビーズが、液滴アクチュエータ上の液滴または充填流体内の所定の位置に実質的に保持されることを意味する。例えば、一実施形態において、固定されるビーズは、液滴上での分裂操作の実施を可能にするために、所定の位置に実質的に保持され、実質的に全てのビーズを有する1つの液滴およびビーズを実質的に欠く1つの液滴を生じる。
【0031】
「液体経路」とは、液体を誘導または流動させるのに適切な経路を意味する。液体経路は、管基板(例えば毛細管)内の内腔経路または固体基板内のチャネル、管、導管、穴、開口部、溝またはくぼみの経路など、基板内に規定されてもよい。液体経路は、開いていても(例えば液体が流れる表面内の溝またはくぼみ)、閉じていてもよい(例えば管)。多くの場合、液体経路は、液体リザーバーから、液体経路を通して、液滴アクチュエータの液滴操作間隙内、または液体リザーバーから、液滴経路を通して、第2の液体経路内などのように、1つのチャンバから別のチャンバへ液体を流すように規定される。
【0032】
「磁性反応」とは、磁場に対する反応を意味する。「磁性反応ビーズ」は、磁性反応物質を含むか、または磁性反応物質から構成される。磁性反応物質の例としては、常磁性体、強磁性体、フェリ磁性体、およびメタ磁性体が挙げられる。適切な常磁性体の例としては、鉄、ニッケルおよびコバルト、ならびにFe3O4、BaFe12O19、CoO、NiO、Mn2O3、Cr2O3、およびCoMnPなどの金属酸化物が挙げられる。
【0033】
磁性反応ビーズを洗浄することに関して、「洗浄する」とは、磁性反応ビーズと接触するか、または磁性反応ビーズと接触する液滴から磁性反応ビーズに曝露される1つ以上の物質の量および/または濃度を減少させることを意味する。物質の量および/または濃度の減少は、部分的、実質的に完全または均一に完全であってもよい。物質は、様々な物質の任意のものであってもよい。例としては、さらなる解析のための標的物質、ならびにサンプル、汚染物質、および/または過剰な試薬の成分などの不要な物質が挙げられる。一部の実施形態において、洗浄操作は磁性反応ビーズと接触する開始液滴で始まり、その液滴は物質の初期量および初期濃度を含む。洗浄操作は種々の液滴操作を用いて進行されてもよい。洗浄操作により、磁性反応ビーズを含む液滴が生じ得、その液滴は、物質の初期量および/または濃度未満の物質の全量および/または濃度を有する。適切な洗浄技術の例は、Pamulaら,2008年10月21日に付与された「Droplet−Based Surface Modification and Washing」という発明の名称の米国特許第7,439,014号(その全開示は本明細書に参照として援用される)に記載されている。
【0034】
用語「上部」、「底部」、「上」、「下」および「上に」は、液滴アクチュエータの上部および底部基板の相対的位置などの液滴アクチュエータの構成要素の相対的位置に関して本明細書全体を通して使用される。液滴アクチュエータは空間の方向に関わらず機能的であることは理解されるだろう。
【0035】
任意の形態の液体(例えば、移動しているか、または静止しているかに関わらず、液滴または連続体)が、電極、アレイ、表面のマトリクス「の上に」、「において」または「より上に」存在していると記載される場合、そのような液体は、電極/アレイ/マトリクス/表面と直接接触してもよいか、または液体と電極/アレイ/マトリクス/表面との間に入り込む1つ以上の層もしくは薄膜と接触してもよいかのいずかである。
【0036】
液滴が、液滴アクチュエータ「の上に」または「の上に負荷される」と記載される場合、液滴が、液滴アクチュエータを用いて液滴上での1つ以上の液滴操作を実施することを容易にする方法で液滴アクチュエータ上に配置され、液滴は、液滴からの特性またはシグナルの検出を容易にする方法で液滴アクチュエータ上に配置され、および/または液滴は液滴アクチュエータ上で液滴操作に供されることは理解されるべきである。
【図面の簡単な説明】
【0037】
(6.図面の簡単な説明)
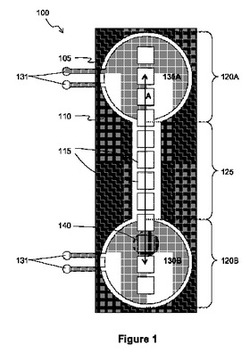
【図1】図1は、液滴アクチュエータ基板上の熱サイクル経路を示す。
【図2】図2は、液滴アクチュエータ基板上に規定された一連の熱サイクル経路を示す。
【図3】図3は、液滴アクチュエータについての別の熱サイクルの配置を示す。
【図4】図4は、液滴間の二次汚染を減少または除去するための技術を示す。
【図5】図5は、複数の洗浄液滴がサンプル液滴間の経路に置かれることを除いて、図4に示す技術と実質的に同様の技術を示す。
【図6】図6は、洗浄液滴がサンプル液滴に対して1つの電極によってオフセットされることを除いて、図5に示す技術と実質的に同様の技術を示す。
【図7】図7は、洗浄液滴が細長いスラグ形状の洗浄液滴と置き換えられることを除いて、図4および5に示す技術と実質的に同様の技術を示す。
【図8】図8は、細長い洗浄スラグが、サンプル液滴の前後のサンプル液滴経路において洗浄液滴でさらに補われることを除いて、図7に示す技術と実質的に同様の技術を示す。
【図9】図9は、洗浄液滴が、サンプル液滴の前後に水平形状の洗浄液滴として提供されることを除いて、先行技術と実質的に同様の技術を示す。
【図10】図10は、経路間の充填流体の交換または充填流体の構成を防止する、細長い物理的障壁が、サンプル経路間に備えられることを除いて、図2に示す実施形態と同様の実施形態を示す。
【図11】図11は、充填流体が、保存温度で実質的に凝固し、操作に必要とされる温度で加熱器の近くで融解する物質として提供される実施形態を示す。
【図12】図12Aおよび12Bは、液滴間の二次汚染を減少または除去するための別の技術を示す。
【図13】図13は、液滴間の二次汚染を減少または除去するための別の技術を示す。
【図14】図14は、液滴アクチュエータ上の反応を開始するために表面積対体積比の原理ならびに図12Aおよび12Bに示す表面活性酵素複合体を使用する実施形態を示す。
【図15】図15は、充填流体を置き換える流路を構成する液滴アクチュエータの断面図を示す。
【図16】図16は、充填流体を置き換える流路を構成する図15に示すものと同様の液滴アクチュエータの上面図(図16A)および断面図(図16B)を示す。
【図17】図17は、充填流体を置き換える流路を構成する液滴アクチュエータの断面図を示す。
【図18】図18は、熱領域間で液滴を循環させるように配置される電極経路を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図19】図19は、本発明の液滴アクチュエータの電極の構成を示し、液滴が温度制御素子から離れて滞留され得るように、特定の経路が延長されることを除いて、図18に示す電極の構成と同様である。
【図20】図20は、本発明の液滴アクチュエータの電極の構成を示し、液滴を検出ウィンドウの存在下に輸送させることができるように配置される電極経路に沿って検出ウィンドウが提供されることを除いて、図19に示す構成と同様である。
【図21】図21は、2つ以上の熱領域を通る曲がった蛇行している電極経路を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図22】図22は、曲がった電極経路から液滴を輸送するように構成されるさらなる電極経路を含む2つ以上の熱領域を通る曲がった蛇行している電極経路を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図23】図23は、各々の熱領域内の曲がっている電極経路が、その領域内の液滴の滞留時間を長くするか、または短くするために、どのように延びているか、または短縮しているかを示す、本発明の液滴アクチュエータの電極の構成を示す。
【図24】図24は、曲がっている経路を含む、本発明の液滴アクチュエータの電極の構成を示し、曲がっている経路の1つ以上の曲がり角はアクセス経路に結合される。
【図25】図25は、図25の電極の構成と同じ電極の構成を示すが、電極の活性化を必要とせずに検出前に液滴を保存するための液滴滞留領域も含む。
【図26】図26は、熱制御領域の間に液滴を輸送するための電極経路のループを形成するように配置される電極を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図27】図27は、複数の電極経路のループを含む、本発明の液滴アクチュエータの電極の構成を示す。
【図28】図28は、電極経路のループおよび電極経路のサブループを含む、本発明の液滴アクチュエータの電極の構成を示す。
【図29】図29は、流路の熱サイクルの構成を例示する本発明の液滴アクチュエータの電極の構成を示し、小液滴は検出のためのより大きな液滴から分裂される。
【図30】図30は、電極アレイおよび電極アレイに配置されるサブサンプルの液滴を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図31】図31は、サンプル液滴が熱サイクルされ、nサイクルごとの後、サブサンプル液滴が分配され、検出のために離れた位置に輸送される、本発明の実施形態を示す。
【図32】図32は、どのように小液滴が離れた位置に輸送され、配置されて、その後検出器によって操作され得るかを示す、実施形態を示す。
【図33】図33は、電極の構成が、反応液滴を配置するために使用される、実施形態を示す。
【図34】図34は、熱サイクル経路が半径方向に配置される、本発明の液滴アクチュエータの電極の構成を示す。
【図35】図35は、液滴輸送経路の複数のセットを有する電極アレイによって接続される複数の温度制御素子を有する電極の構成を示す。
【図36】図36は、先細の電極である電極の構成を示し、温度制御素子の間に液滴を輸送するために使用される。
【図37】図37は、本発明の液滴アクチュエータカートリッジの基板底部の写真である。
【図38】図38は、図37に示す基板底部の配置の図である。
【図39】図39は、カートリッジ上の増幅についての生のデータおよび正規化されたデータを示す。
【図40】図40は、BioRadIQ5からの正規化されたデータと比較した本発明のカートリッジからの正規化されたデータを示す。
【図41】図41は、1つの液滴アクチュエータ上の12の同時増幅反応の結果を示す。
【図42】図42は、図37および38に示されるカートリッジの配置を用いた別の熱サイクル実験の結果を示す。
【図43】図43は、増幅が検出と分離される実験に使用される液滴プロトコルを示す。
【図44】図44は、図43に関して記載される実験の結果を示す。
【図45】図45は、ビーズが、検出の間、検出ウィンドウに曝露されないように、磁性反応ビーズが、細長い液滴内の端側に引き付けられる本発明の実施形態を示す。
【図46A】図46Aは、液滴アクチュエータの領域の上面図を示し、検体の検出を向上するための磁性反応ビーズを操作する方法の特定の工程を一緒に示す。
【図46B】図46Bは、液滴アクチュエータの領域の上面図を示し、検体の検出を向上するための磁性反応ビーズを操作する方法の特定の工程を一緒に示す。
【図46C】図46Cは、液滴アクチュエータの領域の上面図を示し、検体の検出を向上するための磁性反応ビーズを操作する方法の特定の工程を一緒に示す。
【図46D】図46Dは、熱サイクル反応から得たリアルタイムPCRデータのプロットを示す。
【図47】図47A〜47Iは液滴アクチュエータの領域の断面図を示し、核酸増幅および検体についてのサンプル流体からの標的核酸の濃縮および回収プロセスにおける磁性反応捕捉ビーズの使用例を提供する。
【図48】図48Aおよび48Bは、加熱バーおよび挿入される加熱バーの側面図を示す。
【発明を実施するための形態】
【0038】
(7.詳細)
本発明は、液滴アクチュエータ装置、液滴アクチュエータを製造および使用するための技術ならびにシステムを提供する。本発明の実施形態は、液滴操作を実施するのに有用である。本発明の実施形態は、核酸を増幅するための液滴の熱サイクルなどの液滴の熱サイクルを利用するアッセイを実施するのに有用である。本発明の種々の熱サイクルプロトコルは、当該技術分野に対して様々な利点を有する。一部の場合において、そのプロトコルは、加熱器または液滴アクチュエータが熱サイクルされることを必要としない。他の場合において、同時または同じ部位で発生する核酸増幅および検出を必ずしも必要としない。さらに他の場合において、熱サイクルの間の反応に存在すべき検出試薬を必ずしも必要としなくてもよい。例えば、検出試薬は、熱サイクルされた液滴と、検出試薬を含む液滴とを混合することなどによって熱サイクルの後に加えられてもよい。一部の実施形態において、熱サイクルの間に生じる検出を必ずしも必要としない。すなわち、検出は、熱サイクルの完了の際、または熱サイクル後に生じてもよい。さらに他の場合において、測定されるべき1つより多い個々の反応からのシグナルを必ずしも必要としない。さらに、任意の特定の順序で決定されるべき任意の特定の数のサイクルと関連するシグナルを必ずしも必要としなくてもよい。本発明の任意の特定の熱サイクルプロトコルは、これらおよび他の利点のうちの1つ以上を有してもよい。
【0039】
本発明は、液滴アクチュエータおよび液滴アクチュエータ上でのPCRなどの核酸解析を実施する改良された方法を提供する。例えば、本発明は、増幅された標的物(例えば核酸)の検出を改良するために磁性反応ビーズを操作する方法を提供する。本発明はまた、増幅された標的物の検出を改良するために、液滴アクチュエータにより駆動される増幅プロトコルにおいて極性蛍光色素分子の使用を提供する。本発明はまた、液滴操作の間の核酸標的物およびPCR試薬の損失を実質的に減少および/または除去するための方法(例えば不動態化)を提供する。本発明はまた、液滴操作の間の液滴の安定性を改良するために、増加した間隙サイズを有する液滴アクチュエータを提供する。本発明はまた、増幅反応液滴間のキャリーオーバーおよび二次汚染を減少させる方法を提供する。本発明はさらに、サンプル流体から標的核酸を濃縮および収集するための方法を提供する。
【0040】
特定の実施形態において、実質的に同一の組成を含む複数の液滴が熱サイクルプロトコルに供されてもよく、異なる液滴または異なる液滴のセットが異なる数のサイクルに供される。液滴または液滴のセットが所定数のサイクルを完了すると、液滴は、その液滴に存在する増幅産物の量を決定するために検出に供されてもよい。曲線が、異なる熱サイクルのエンドポイントにおいて液滴の検出に基づいて生成され、オリジナルのサンプルに存在する標的物を定量化するために使用されてもよい。多くの代替が、本明細書に開示される本発明を考慮して本発明の範囲内で可能である。
【0041】
本発明の装置、技術およびシステムは、限定されないが、液滴アクチュエータ上の液滴と、他の液滴、充填流体、および/または液滴アクチュエータ表面との間の二次汚染の減少または除去、汚染を減少または除去するために使用する液滴アクチュエータ間の清浄を含む、当該技術分野に対する多くの利点を有する。
【0042】
(7.1 二次汚染の減少)
本発明は、液滴アクチュエータ装置および液滴操作を実施するための方法を提供する。本発明は、液滴アクチュエータ上の液滴と、他の液滴、充填流体、および/または液滴アクチュエータ表面との間の二次汚染ならびにキャリーオーバーを実質的に減少または除去することができる。本発明は、汚染を減少または除去するために使用する液滴アクチュエータ間の清浄を提供することができる。本発明は概して、PCRなどの核酸増幅反応を参照して記載されるが、その方法は、液滴間の二次汚染またはキャリーオーバーが問題となる任意の種類のアッセイに適切であることは理解されるだろう。
【0043】
図1は、液滴アクチュエータ基板上の熱サイクル経路100を示す。熱サイクル経路100は液滴操作領域105を備える。液滴操作領域105は第1の基板上に規定され、第1の基板に対してほぼ平行な様式で配置され、液滴操作を実施するための液滴操作間隙をその間に生成するように第2の基板も含んでもよい。液滴操作領域105は、液滴操作領域105に侵入するか、またはそこから出ていく汚染を防止するためにガスケット110により囲まれる。第1および第2の基板が存在する場合、ガスケット110は液滴操作間隙に設けられてもよい。ガスケット110は、液滴操作領域105において充填流体を保有するためのシールとして、および/または液滴操作領域105の液滴操作間隙の高さを規定するためのスペーサーとして役立ってもよい。
【0044】
ガスケット110が液滴操作領域105において流動性の充填流体を保有する場合、ガスケット110は、充填流体の汚染が液滴アクチュエータ表面上の他の液滴操作領域を汚染することを防ぐ。従って、第1および第2の基板が存在する場合、ガスケット110は液滴操作間隙に設けられ、液滴操作領域105における充填流体が、第1および第2の基板ならびにガスケットによって完全に囲まれるように配置されてもよい。種々のポートが、液滴操作領域105まで/から流体を負荷する/取り出す(非負荷する)ために、液滴操作間隙から液滴アクチュエータの外側、または液滴アクチュエータの別の領域まで任意の経路に沿って設けられてもよい。
【0045】
図示するように、液滴操作領域105は、2つの温度制御領域120Aおよび120B、ならびに遷移領域125を備える。温度制御領域120は、温度制御素子130Aおよび130Bに結合される。温度制御素子130は、それらの近くで充填流体の温度を制御する素子である。温度制御素子130は、電気を温度制御素子130に供給するために電気接点131に電気的に接続されてもよい。適切な温度制御素子130の例としては、加熱器およびヒートシンクが挙げられる。図示するように、2つの温度制御領域120Aおよび120Bが存在するが、任意の数の温度制御領域120が備えられてもよいことは理解されるだろう。
【0046】
温度制御領域120は遷移領域125に接続される。遷移領域125における電極115は、温度制御領域間の液滴を往復させるために利用されてもよい。一部の実施形態において、遷移領域125は、温度制御領域120の間の流体の循環を最小化するために、温度制御領域120より狭くてもよい。図示するように、単一の遷移領域125は2つの温度制御領域120に接続するが、温度制御領域120が複数の遷移領域125の接続を有してもよいことは理解されるだろう。さらに、任意の数の温度制御領域120が、任意の数の遷移領域125によって接続されてもよい。
【0047】
液滴操作領域105は、第1および第2の基板の1つまたは両方に結合される電極115を備える。電極115は1つ以上の液滴操作を実施するように構成される。電極115は、例えば矢印Aによって示される方向で、例えば液滴140を温度領域120Aと120Bとの間で前後に往復させるために使用されてもよい。
【0048】
図2は、液滴アクチュエータ基板上に規定される連続した熱サイクル経路100を示す。温度制御素子130は、連続して一緒に電気的に接続される連続したほぼディスク形状の加熱器として示される。しかしながら、温度制御素子130は、電源または別個の電源に並行に接続されてもよいことは理解されるだろう。さらに、温度制御素子130は組み合わされてもよい。例えば、素子130Aは、各々の温度制御領域120Aと結合される単一の温度制御素子130と置き換えられてもよい。同様に、素子130Bは、各々の温度制御領域120Bと結合される単一の温度制御素子130と置き換えられてもよい。
【0049】
図3は、液滴アクチュエータのための別の熱サイクルの配置300を示す。熱サイクルの配置300は、図1および2における熱サイクル経路100を規定する配置と同様である。しかしながら、熱制御素子305は、複数の液滴往復経路310A−310Bにわたる温度制御領域320Aおよび320Bを規定する。液滴往復経路310は、概して図1を参照して記載されるように、1つ以上の液滴操作を実施するように構成される液滴操作電極315から構成される。特に、液滴往復経路310は、矢印Aによって示される方向において熱領域320Aと320Bとの間で液滴340を往復させるために液滴操作電極315を利用する。熱サイクルの配置300はまた、熱領域320Aと320Bとの間で充填流体の循環を減少させるように構成される物理的障壁を備えてもよい。
【0050】
図4は、液滴間の二次汚染を減少または除去するための技術を示す。液滴往復経路105A、105B、105C、105Dおよび105Eが、液滴アクチュエータ基板上に設けられる。液滴は、矢印Aによって示される方向において熱領域(図示せず)の間で往復する。経路105A、105Cおよび105Eは、PCR液滴としてここで示されるサンプル液滴を含む。洗浄液滴Wは、サンプル液滴を含む経路間の経路105Bおよび105D上に置かれる。サンプル液滴が温度領域間で往復する場合、洗浄液滴はサンプル液滴経路間で往復する。洗浄液滴WはDNA分解酵素などの汚染物質を分解する化合物を含んでもよい。洗浄液滴Wは、DNA結合ビーズなどの汚染物質に結合する成分を含んでもよい。洗浄液滴Wは、サンプル液滴に対して同じ方向または反対方向において往復してもよい。それらは、サンプル液滴にすぐ隣接する位置および/またはサンプル液滴に対してオフセットする位置において往復してもよい。洗浄液滴Wは、必要に応じて、核酸増幅試薬を含んでもよく、それによって、それらはまた、洗浄液滴内で増幅された核酸の検出が、汚染物質が洗浄液滴内で検出可能であるという指標を与えるネガティブ反応コントロールとして機能する。
【0051】
図5は、複数の洗浄液滴がサンプル液滴間の経路に置かれることを除いて、図4に示す技術と実質的に同様の技術を示す。代替の実施形態において、複数の洗浄液滴経路は、各々の洗浄液滴経路において1つ以上の洗浄液滴を有するサンプル液滴経路間に配置される。
【0052】
図6は、洗浄液滴が、サンプル液滴に対して1つの電極によってオフセットすることを除いて、図5に示す技術と実質的に同様の技術を示す。
【0053】
図7は、洗浄液滴が細長いスラグ形状の洗浄液滴と置き換えられることを除いて、図4および5に示す技術と実質的に同様の技術を示す。
【0054】
図8は、細長い洗浄スラグがさらに、サンプル液滴の前後でサンプル液滴経路において洗浄液滴で補われることを除いて、図7に示す技術と実質的に同様の技術を示す。同様に、サンプル液滴の前後のサンプル液滴経路における洗浄液滴はまた、図1〜7のいずれかに含まれ得る。
【0055】
図9は、洗浄液滴が、サンプル液滴の前後で水平形状の洗浄液滴として与えられることを除いて、先行技術と実質的に同様の技術を示す。同様の実施形態において、洗浄液滴のスラグは、2X、3X、4X、5X、6X、7X、8X、9Xまたはそれより大きい液滴の任意の形状と置き換えられてもよい。
【0056】
図10は、経路または領域間の充填流体の交換または充填流体の構成を防止する、細長い物理的障壁1010A、1010B、1010Cおよび1010Dが、サンプル経路1005A、1005B、1005C、1005Dおよび1005Eの間に備えられることを除いて、図2に示す実施形態と同様の実施形態を示す。
【0057】
図11は、充填流体が、保存温度で実質的に凝固し、操作に必要とされる温度で加熱器の近くで融解する物質として与えられる実施形態を示す。加熱器1130は、所望の液滴操作経路1105の形状とほぼ対応する形状を有するように与えられる。4つの液滴操作経路1105A、1105B、1105Cおよび1105Dをここで示すが、任意の数の経路が設けられてもよいことは理解されるだろう。実質的に凝固した充填物質を加熱する際に、一部の充填物質は融解して、実質的に固体のままである充填物質により囲まれる流体が充填した液滴操作経路1105を形成し、それにより、汚染物質が1つの液滴操作経路1105から別の経路まで流動性の充填流体を介して移動することの障壁1120として役立つ。一実施形態において、充填物質は、核酸増幅を実施するのに必要とされる温度以下の温度で固体のままであり、核酸増幅を実施するのに必要とされる温度で融解するように選択される。
【0058】
図12Aおよび12Bは、液滴間の二次汚染を減少または除去するための別の技術を示す。液滴操作電極1210の経路またはアレイは、液滴アクチュエータ基板上に設けられる。液滴操作電極1210は1つ以上の液滴操作を実施するように構成される。図12Aに示すように、例えば、液滴操作電極1210は、液滴1220を輸送するために使用されてもよい。液滴1220は、汚染物質を潜在的に含む任意の液体であってもよい。すなわち、物質は別の液滴を汚染する可能性がある。例えば、液滴1220は、免疫学的検定、シークエンシングアッセイ、核酸増幅アッセイ、および/または酵素アッセイの液滴に使用される液滴などのアッセイ液滴であってもよい。汚染物質は、例えば、核酸増幅反応における核酸などの標的物質、免疫学的検定サンプルにおける非標的タンパク質などの非標的物質、および/または酵素などの試薬であってもよい。
【0059】
液滴1220は、多量の界面活性剤−酵素複合体1224を含んでもよい。一例において、複合体1224は、界面活性剤−DNase複合体(すなわち、DNA分解複合体)であってもよい。界面活性剤部分のために、実質的に全ての複合体1224は、液滴1220の表面に閉じ込められる。多量の複合体1224は、酵素部分(例えばDNase)の濃度が十分に低く、それによって、液滴1220中で実質的に不活性であるように選択されてもよい。
【0060】
液滴操作電極1210に沿った液滴1220の移動は、図12Bに示すように、特定の液滴操作電極1210上に残ったままになり得る微小液滴1226の形成を生じる場合がある。微小液滴1226は、DNAおよび複合体1224などの液滴1220の全ての成分を含んでもよい。結果として、微小液滴1226は、液滴操作電極1210に沿って生じ得る、後の液滴操作におけるDNA汚染の源となり得る。
【0061】
例えば、微小液滴1226は、液滴1220の直径の1/100であってもよい。より小さい直径の微小液滴1226は、十分により高い(例えば100倍高い)表面積対体積比を与える。高い表面積対体積比は、微小液滴1226中により高い濃度(例えば100倍高い)の複合体1224を与え得る。しかしながら、微小液滴1226中の複合体1224の高い濃度のために、微小液滴1226中でのDNAの急速な分解が達成され得、微小液滴1226によって引き起こされる二次汚染を実質的に防止または減少する。
【0062】
例として、酵素は、PAG−アルキルポリマーのポリアルカレングリコール(PAG)部分(例えばポリエチレングリコール(PEG)、ポリプロピレングリコールなど)に結合されてもよい。そのような結合を達成するための種々の方法は当該分野において公知である:米国特許第4,088,538号は、PEGに共有結合された酵素の酵素的に活性なポリマー−酵素結合体を記載し、米国特許第4,496,689号は、α−1プロテアーゼ阻害剤と、PEGまたはメトキシポリ(エチレングリコール)などのポリマーとの共有結合した複合体を記載し、Abuchowskiら,J.Biol.Chem.252:3578(1977)は、ウシ血清アルブミンのアミン基に対するmPEGの共有結合を記載し、米国特許第4,414,147号は、ポリ(エチレン無水コハク酸)などのジカルボン酸の無水物に対するインターフェロンの結合を記載し、国際特許公開第1987/00056は、インターフェロン−β、インターロイキン−2および抗毒素などのタンパク質に対するPEGおよびポリ(オキシエチル化)ポリオールの結合を記載している。このような文献の各々の全開示は参照により本明細書に援用される。
【0063】
酵素にPEGを結合する別の様式は、ペプチド上のグリコシル残基の酸化による。酸化された糖は、ペプチドにPEG部分を結合するための部位として利用される。例えば、国際特許公開第1994/05332号は、PEGを糖タンパク質に付加するためにヒドラジンまたはアミノ−PEGの使用を記載している。グリコシル部分は、後でアミノ−PEGに結合される、対応するアルデヒドに酸化される。国際特許公開第1996/40731号は、免疫グロブリン上のグリカンを酵素的に酸化し、次いで、グリカンとアミノ−PEG分子とを接触することによって免疫グロブリン分子に対するPEGの結合を記載している。界面活性剤は、結合が酵素の活性を過度に阻害しない、酵素の1つ以上の分子にて結合される。
【0064】
図13は、液滴間の二次汚染を減少または除去するための別の技術を示す。この実施形態において、液滴操作経路1310A、1310Bおよび1310Cは、液滴アクチュエータ基板上に設けられる。3つの液滴操作経路1310A、1310Bおよび1310Cをここで示すが、任意の数の経路が設けられてもよいことは理解されるだろう。経路1310A、1310Bおよび1310Cは、ここで、PCR液滴として示されるサンプル液滴を含む。液滴は、例えば矢印Aによって示される方向において熱領域間(図示せず)を往復する。液滴の往復は、充填流体1316中に分散され得る微小液滴1314の形成を生じ得る。微小液滴1314はDNAを含んでもよく、従って、他の液滴操作経路に対する汚染の源であってもよい。
【0065】
充填流体1316は多量の界面活性剤−酵素複合体1320を含む。この例において、複合体1320は、DNAを分解するために使用される界面活性剤−DNase複合体であってもよい。複合体1320は、経路1310A、1310Bおよび1310C間に障壁を与え、それによって、複合体1320は微小液滴1314中でDNAを分解し、その後、経路間の二次汚染を実質的に防止または減少する。
【0066】
代替の実施形態において、図12A、12Bおよび13に示す実施例は、液滴アクチュエータにおける他の物質の二次汚染を減少させるために適用されてもよい。例えば、界面活性剤−プロテアーゼ複合体は、液滴操作中のタンパク質のキャリーオーバーを実質的に防止または減少させるために使用されてもよい。
【0067】
図14は、表面積対体積比ならびに液滴アクチュエータ上での反応を開始するために図12Aおよび12Bに示す表面活性酵素複合体の原理を使用する実施形態を示す。
【0068】
この例において、リザーバー電極1410および液滴操作電極1412の経路またはアレイは、液滴アクチュエータ基板上に設けられる。多量の界面活性剤−酵素複合体1418を含む多量のサンプル流体1416は、リザーバー電極1410に与えられる。界面活性剤部分のために、実質的に全ての複合体1418は、サンプル流体1416の表面に閉じ込められる。多量の複合体1418は、酵素部分の濃度が十分に低く、それによって、サンプル流体1416中で実質的に不活性であるように選択されてもよい。
【0069】
リザーバー電極1410は、液滴操作電極1412上に単一のサイズの液滴1420を分配するように構成される。液滴操作電極1412は、単一のサイズの液滴1420を処理するために1つ以上の液滴操作を実施するように構成される。
【0070】
リザーバー電極1410上のサンプル流体1416の体積は、単一のサイズの液滴1420の体積より実質的に大きい。例えば、サンプル流体1416の体積は、単一のサイズの液滴1420の体積より約10倍〜約1,000倍大きくてもよい。サンプル流体1416と比べて、単一のサイズの液滴1420のより小さい体積は、実質的により高い表面積対体積比を与える。高い表面積対体積比は、単一のサイズの液滴1420中により高い濃度の複合体1418を与えることができる。単一のサイズの液滴1420中の高い濃度の複合体1418は、反応を開始するのに十分である。
【0071】
代替の実施形態において、リザーバー電極1410は他の液滴操作電極1412と置き換えられる。この例において、多量の界面活性剤−酵素複合体を含むサンプル液滴は、液滴操作を用いて分裂されて、その表面積対体積比を変化させて反応を開始してもよい。
【0072】
一部の実施形態において、液滴アクチュエータは、充填流体を置き換えるように構成される。一部の適用において、液滴アクチュエータの反復された使用を与えることは有用である。充填流体の汚染が問題となる場合、アッセイが作動している間に液滴アクチュエータにおける充填流体の一部または全てを置き換えることは有用であり得る。この技術は、例えば、増幅、シークエンシング、免疫学的検定、酵素アッセイなどのためのプロトコルを含む、広範な液滴プロトコルで有用であり得る。一実施形態において、充填流体は実質的に完全に置き換えられる。置き換えは自動化されてもよい。充填流体は各々の作動後に試験されてもよく、所定レベルの汚染が検出される場合、充填流体は置き換えられてもよい。置き換えは自動化されてもよい。一部の場合において、置き換えは、周期的、例えば1、2、3、4、5またはそれ以上の作動ごとの後に発生してもよい。
【0073】
図15は、充填流体を置き換える流路が構成される液滴アクチュエータ1500の断面図を示す。液滴アクチュエータ1500は、1つ以上の液滴操作を実施するように構成される電極1510を含む基礎基板1505を備える。液滴アクチュエータ1500はまた、液滴操作間隙1520を生じるように基礎基板1505から分離した上部基板1515を備える。液滴アクチュエータ1500は、液滴操作間隙1520を通して充填流体を流動するための側方開口部1525を備える。側方開口部1525は、外部の充填流体源または充填流体の送達位置上の1つ以上の対応する調整具1535と適合するように構成される調整具1530を備えてもよい。調整具1535は、外部の充填流体源(図示せず)から、導管1540を通り、調整具1530および1535を通り、液滴操作間隙1520への液体経路を規定する導管1540と結合されてもよい。調整具1535は、液滴操作間隙1520から、調整具1530および1535を通り、導管1540を通り、外部の充填流体の送達位置(図示せず)への液体経路を規定する導管と結合されてもよい。
【0074】
図16は、充填流体を置き換える流路が構成される同様の液滴アクチュエータ1600の上面図(図16A)および断面図(図16B)を示す。液滴アクチュエータ1600は、1つ以上の液滴操作を実施するように構成される電極1610を含む基礎基板1605を備える。液滴アクチュエータ1600はまた、液滴操作間隙1620を生じるように基礎基板1605から分離される上部基板1615を備える。液滴アクチュエータ1600は、液滴操作間隙を通して充填流体を流動するための側方開口部1625を備える。側方開口部1625は、導管1640から液滴操作間隙に、および/または液滴操作間隙から導管1640に液体を流動するように構成されるマニホルド1660に結合されてもよい。マニホルド1660は、外部の充填流体源から、導管1640を通り、マニホルド1660を通り、液滴操作間隙へと液体経路を規定するように、導管1640および流動性の充填流体源(図示せず)を備えて構成されてもよい。マニホルド1660は、液滴操作間隙から、マニホルド1660を通り、導管1640を通り、流動性の充填流体の送達位置へと液体経路を規定するように、導管1640および流動性の充填流体の送達位置(図示せず)を備えて構成されてもよい。マニホルド1660は、直接または間接的に導管1640に結合するのに適切な開口部1662を備えてもよい。マニホルド1660は、直接または間接的に液滴アクチュエータに結合するのに適切な開口部1664を備えてもよい。理想的には、開口部1664および開口部1625は、液滴操作間隙1620における充填流体を完全に置き換えることを容易にするために液滴操作間隙1620の断面と実質的に同様の形状を有する。1つ以上の通気口は、再充填の間に液滴操作間隙1620内に導入され得る気泡が放出できるように、液滴アクチュエータ1600の基板に、および/または基板間(例えばガスケット中)に存在してもよい。矢印xは、導管1640、マニホルド1660を通り、液滴操作間隙1620へ流れる流れの方向を示す。
【0075】
図17は、充填流体を置き換える流路が構成される液滴アクチュエータ1700の断面図を示す。液滴アクチュエータ1700は、液滴アクチュエータを通して流体を流動するための開口部が、液滴アクチュエータの底部に配置されることを除いて、液滴アクチュエータ1500と同様である。この配置構成は、液滴操作間隙を通して液体を流動するための構成要素を備えるシステムにおいて液滴アクチュエータの取り付けを容易にするために有用である。液滴アクチュエータ1700は、1つ以上の液滴操作を実施するのに構成される電極1710を含む基礎基板1705を備える。液滴アクチュエータ1700はまた、液滴操作間隙1720を生じるために基礎基板1705から分離された上部基板1715を備える。ガスケット1707は液滴操作間隙を密閉する。液滴アクチュエータ1700は、液滴操作間隙1720を通って充填流体を流動するための底開口部1725を備える。底開口部1725は、外部の充填流体源および/または充填流体の送達位置のための液体経路と結合する1つ以上の対応する調整具1735と適合するように構成される調整具1730を備えてもよい。一例として、適切なチップ−管の接続としては、NANOPORT(商標)アセンブリ(IDEX Corporation,Oak Harbor,WA)が挙げられる。1つ以上の調整具1735は、外部の充填流体源(図示せず)から、導管1740を通り、調整具1730および1735を通り、液滴操作間隙1720への液体経路を規定する導管1740と結合されてもよい。1つ以上の調整具1735は、液滴操作間隙1720から、調整具1730および1735を通り、導管1740を通り、外部の充填流体の送達位置(図示せず)への液体経路を規定する導管と結合されてもよい。
【0076】
本発明の種々の態様において、このように充填流体は、充填流体源から、液体経路を通り、液滴操作間隙を通って流動し、かつ、第2の液体経路中の液滴操作間隙から流動性の充填流体の送達位置まで出ていく。このように、充填流体は、少なくとも部分的に置き換えられてもよい。液滴操作間隙を通る充填流体の流れは、液滴操作間隙に最初に存在する充填流体と実質的に置き換えられてもよい。一部の場合において、充填流体は、液滴操作間隙中の充填流体を置き換えるのに十分な量で液滴操作間隙に流れてもよい。他の場合において、充填流体は、液滴操作間隙をフラッシュするために液滴操作によって流さてもよい。フラッシングの完了の際に、液滴操作間隙は、充填流体で充填されたままであり、操作しやすくなっている。特定の実施形態において、液滴操作間隙をフラッシュするのに使用される充填流体は、液滴操作間隙における清浄を高めるために加熱されてもよい。別の実施形態において、液滴操作間隙における汚染は、充填流体のフラッシングの間にモニターされてもよく、適切なレベルの清浄が達成されると、フラッシングは停止されてもよい。
【0077】
本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約50%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約75%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約90%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約95%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約99%を置き換えるために使用されてもよい。
【0078】
本発明の他の態様において、洗浄流体は、液滴アクチュエータを洗浄するために液滴操作間隙を通って流されてもよい。洗浄後、新鮮な充填流体が液滴操作間隙に流されてもよい。例えば、溶媒が、新鮮な充填流体を液滴操作間隙に流す前に、液滴アクチュエータを洗浄するために液滴操作間隙を通して流されてもよい。液滴操作間隙の表面を過度に損傷せずに充填流体を除去するのに適切である溶媒が、選択されてもよい。一部の場合において、液滴操作間隙を充填流体に再充填する前に、液滴アクチュエータ間隙を乾燥することが望まれてもよい。一部の場合において、空気などの気体が、液滴操作間隙を充填流体で再充填する前に、液滴操作間隙を乾燥するために、液滴操作間隙を通して流されてもよい。
【0079】
種々の液体が、本発明の方法における洗浄流体として使用されてもよい。一態様において、選択され得る洗浄液体(その中で油および水の両方が可溶性である)は低沸点を有するものが良好な洗浄剤である。高沸点洗浄流体または洗浄流体成分もまた、使用されてもよい。一実施形態において、高沸点洗浄流体が使用され、その後、より低い沸点でリンスされる。冷却流体は、液滴アクチュエータを操作温度に戻すために、充填流体を充填する前に、液滴操作間隙を通して流されてもよい。
【0080】
適切な洗浄液体の例としては、アセトン、イソプロピルアルコール、エタノール、メタノール、テトラヒドロフラン、アセトニトリル、およびそれらの成分の1つ以上を含む混合物などの極性液体が挙げられる。これらの溶媒の混合物もまた、使用されてもよい。水溶性シリコーン油誘導体もまた、使用されてもよい。水ベースの洗浄液体もまた、使用されてもよい。好ましくは、カートリッジは、水ベースの洗浄液体の使用後、再充填する前に乾燥される。多成分混合物もまた、使用されてもよい。一実施形態において、洗浄液体は、水溶性を有する1つ以上の成分および油溶性を有する1つ以上の成分を含む。洗浄流体はまた、種々の触媒または酵素を含んでもよい。例えば、特定の汚染物質を分解する酵素が含まれてもよい。一部の場合において、油は空気または水と置き換えられ、次いで、液滴操作間隙が充填流体で再充填される。
【0081】
フラッシュアッセイにおいて、液滴輸送経路を洗浄するために誘因溶液を含む洗浄液滴を使用することは有用であり得る。基板を輸送するために使用されている電極経路は、同じ領域の一部または全てにわたって1つ以上の洗浄液滴を輸送することによって洗浄されてもよい。洗浄液滴はフラッシュ酵素を含んでもよい。例えば、洗浄液滴はルシフェラーゼまたはルシフェラーゼとATPを含んでもよい。一例として、アクリジニウムエステル(AE)が、本発明のフラッシュアッセイにおける化学発光標識として使用されてもよい。AEシグナルは、誘因溶液の添加時に、典型的に約10、9、8、7、6、5、4、3、2または1秒未満で高い値まで急速に上昇する。シグナルは、典型的に約60、30、20または10秒未満で非常に低い値まで低下する。これにより、検出ループおよび検出スポットでの汚染が除去され得る。しかしながら、汚染物質は洗浄経路および同じ経路上で実施されるその後のアッセイに潜在的に影響を与える可能性があるAEで結合された遊離の二次抗体によるインキュベーション領域にさらに存在する場合がある。AEで結合された抗体で汚染されている電極にわたるAE誘因溶液の1、2、3、4、5、6、7、8、9、10またはそれ以上の液滴を輸送することは、急速に減少する化学発光を生成し、実質的にAE汚染を除去する。
【0082】
種々の場合において洗浄流体は、酸性または塩基性、例えば高いpHに関してエタノール中の水酸化ナトリウムまたは水酸化カリウム、あるいは低いpHに関して酢酸または希塩酸であってもよい。一実施形態において、水に対する溶解度を有する溶媒、続いて第1の溶媒に対する溶解度を有する液体で開始する、多段階の洗浄手順が与えられる。
【0083】
加熱した溶媒が洗浄流体として使用されてもよい。温度は、液滴アクチュエータに対する過度な損傷を引き起こさずに、洗浄を高めるために選択されてもよい。好ましい温度は使用される物質に依存して変化する。一部の場合において、温度は、約30℃〜約125℃、好ましくは約60℃〜約115℃、より好ましくは約75℃〜約105℃の範囲である。好ましい温度は、使用される物質に依存して変化する。ポリカーボネートの上部基板が使用される場合、現在、最大温度は100℃近くである。ガラスの上部基板が使用される場合、最大温度は、例えば150℃以上のように非常に高くてもよい。
【0084】
一部の場合において、1つ以上の液滴アクチュエータの表面はコーティングを備え、洗浄液体は、洗浄の間にコーティングの非常に薄い層を除去するように選択される。例えば、1つ以上の液滴アクチュエータの表面は疎水性コーティングを備え、洗浄液滴は、洗浄の間に疎水性コーティングの非常に薄い層を除去するように選択される。従って、洗浄液体として使用するために選択され得る液体は、疎水性コーティングに対して非常にわずかな溶解度を有する。例えば、疎水性コーティングはフッ素化ポリマーを含んでもよい。洗浄液体は、完全にフッ素化された溶媒または部分的にフッ素化された溶媒などのフッ素化溶媒を含んでもよい。洗浄液体は、非常に低い濃度で別の溶媒に分散される完全にフッ素化された溶媒を含んでもよい。洗浄液体は、他の有機溶媒に対する溶解度を有する部分的にフッ素化された液体を含んでもよい。洗浄液体はまた、既存の疎水性コーティング上にさらなる薄い疎水性コーティングを堆積させるように選択されてもよい。薄層を除去することによって、またはさらなる量の薄層を堆積させることによって、洗浄液体が疎水性コーティングを変化させるかに関わらず、いずれの場合においてもその効果は、疎水性コーティングをその元の状態まで「再び新しくする」ことである。
【0085】
(7.2 並行流路)
図18は、本発明の液滴アクチュエータの一部の電極構成1800を示す。電極構成1800は、液滴アクチュエータの表面で液滴操作を実施するように構成される電極1805を備える。本発明の全ての電極構成と同様である電極構成1800は、より広範囲の電極構成および/またはより広範囲のマイクロ流体ネットワークの一部として提供され得る。液滴アクチュエータは、例えば、単一のサンプル液滴(図示せず)または別の液体源から同一のサブサンプル液滴を分配することによって、一連の同一の反応液滴1820を用いて液滴操作表面で他の液滴操作を分配および実施するために使用されてもよい。液滴操作電極1805は、一連の液滴輸送経路1806を提供するように構成されてもよい。液滴操作電極1805は、反応液滴1820をいくつかの液滴輸送経路1806の1つに輸送するために使用されてもよい。
【0086】
電極構成1800はまた、加熱器および/またはヒートシンクなどの1つ以上の温度制御素子1810と結合されてもよい。温度制御素子1810は、液滴作動表面で液滴を加熱および/または冷却するのに適切な任意の方法で構成されてもよい。温度制御素子1810は、液滴操作表面で温度領域を規定するために使用されてもよい。液滴アクチュエータが、液滴操作を実施するための液滴操作間隙を形成するために離間した2つの基板を備える場合、温度制御素子1810は、液滴操作間隙内に温度領域を規定するように構成されてもよい。液滴操作間隙が、流動性の充填流体で充填される場合、温度制御素子1810は、液滴操作間隙内の充填流体の種々の領域内に温度領域を規定するように構成されてもよい。液滴操作輸送経路1806において、液滴は、1つ以上の温度制御素子1810によって規定される温度領域の中で、液滴操作電極1805によって媒介される液滴操作を用いて輸送されてもよい。
【0087】
本発明の任意の実施形態はシステムの一部として構成されてもよい。例えば、システムは、本発明の任意の電極構成の電極の活性化を制御することによって、液滴アクチュエータで液滴操作を制御するコンピューターを備えてもよい。図18の液滴アクチュエータを備えるシステムは、異なる所定数のサイクルについて、各経路における液滴をサイクルするようにプログラムされてもよい。検出は熱サイクル経路自体でなされてもよいか、または液滴は検出のために別の場所に輸送されてもよい。例示した実施形態において、液滴は、その液滴にわたってセンサを走査することによる検出のためにAと印した経路に滞留される。各経路における熱サイクルが完了した場合に、検出がなされてもよい。あるいは、液滴の一部または全ては熱サイクル後に滞留され、センサは、Aと印した経路に沿って次々に液滴を走査してもよい。他の適切な検出アプローチが本明細書に記載される。
【0088】
図19は、本発明の液滴アクチュエータの電極構成1900を示す。構成1900は、液滴が温度制御素子1810から離れて滞留され得るように、経路1806が延長されていることを除いて、構成1800および図18と同様である。示した例において、上部の経路における液滴は5回のサイクルに供され、次の経路における液滴は10回のサイクルに供されるなどで、底部までで液滴は35回のサイクルに供される。任意の数の経路が設けられてもよく、各経路1806における液滴1820は、温度領域間で任意の数のサイクルの輸送に供されてもよい。所定数のサイクルの完了時に、各液滴は、検出に供され得る場合、Aと印した経路に沿って、そのそれぞれの経路1806における位置まで輸送されてもよい。検出は、例えば液滴からのシグナルの感知を含む。シグナル強度は、液滴における増幅された核酸を定量化するために使用されてもよい。各液滴は、その所定数のサイクルの完了時に迅速に検出に供されてもよい。あるいは、液滴は滞留されて、検出のためのセンサによって後の時間に走査されてもよい。
【0089】
図20は、本発明の液滴アクチュエータの電極構成2000を示す。電極構成2000は、検出ウィンドウ2005が、液滴が各経路1806から検出ウィンドウ内に輸送できるように配置される電極経路2010に沿って与えられることを除いて、概して図19に示す構成1900と同一である。検出ウィンドウは、液滴が検出のために輸送され得る任意の電極経路または任意の位置に配置されてもよい。図20はまた、3つの温度制御素子1810を備える実施形態を示す。もちろん、任意の数の温度制御素子が使用されてもよい。
【0090】
操作において、各液滴がその所定数のサイクルを完了すると、液滴は検出のための検出ウィンドウに輸送される。同様の実施形態において、各液滴がその所定数のサイクルを完了すると、液滴は滞留される。滞留は、液滴を所定の位置に輸送すること、および液滴をその位置に保存することを含む。その位置は、熱サイクル領域に対して液滴アクチュエータの別の領域であってもよい。その後、各液滴は検出のための検出ウィンドウに輸送される。センサは、検出ウィンドウに配置される液滴からシグナルを検出するように配置されてもよい。センサは、各液滴の1つ以上のシグナルを定量化するのに適切であり得る。検出ウィンドウは物理的ウィンドウを必要としない。その最も簡単な形態において、それは単にセンサの近くの領域であり、ウィンドウ内に部分的または完全に配置される液滴はセンサによる検出に感受性がある。
【0091】
一例において、温度領域はPCR混合物などの核酸増幅混合物の熱サイクルを実施するように規定される。増幅液滴は、サンプルに潜在的に存在する標的核酸を増幅するのに適切な試薬とともに核酸サンプルを含む。各々の経路は異なる数のサイクルについて熱サイクルに供される。液滴が所定数のサイクルに到達すると、その液滴は、例えば本明細書に記載される種々のスキームに従って、検出に供されてもよい。例えば、液滴は、増幅産物の検出のためのセンサに輸送されてもよい。
【0092】
一部の場合において、液滴のセットが連続して次々に熱サイクルされる。他の場合において、セット内の液滴が連続して熱サイクルされ、セット外の液滴が並行して熱サイクルされる。各セットは1つ以上の液滴を含んでもよい。適切なデータが、所定の許容可能な程度の確実性で開始サンプルに存在する増幅産物を定量化するために収集されると、熱サイクル反応は終了する。標的核酸がサンプルに存在しないか、または増幅されていないことが統計的に明らかである場合、熱サイクルを停止してもよい。増幅反応が、例えば異なる試薬または異なる液滴アクチュエータを用いて再び作動され得るように、新しいセットのサブサンプルの液滴がサンプルから得られてもよい。他の場合において、熱サイクル液滴のセットからの熱サイクルエンドポイントのセットが十分な曲線を示す場合、生成物を含む(曲線に従う)はずの1つ以上のサブサンプル液滴における生成物の欠如を示すが、新しいサブサンプルの液滴が分配され、熱サイクルプロトコルが、一部または全てのデータポイントについて繰り返されてもよい。
【0093】
並行アッセイとして図18〜20に示すようなアッセイにおいて、複数の液滴が並行に熱サイクルされる。言い換えれば、特定のグループにおける全てのサブサンプルの液滴は、同時に同じ熱領域に存在する。しかしながら、より簡単な実施形態において、全てまたは1つ以上のサブセットの液滴が、連続して熱サイクルされてもよいことは理解されるだろう。一部の場合において、サブセットの各メンバーは、以前のサブセットのメンバーの増幅の完了後に増幅されるが、異なるサブセットが並行して熱サイクルされる。
【0094】
例えば、単一の経路の熱サイクラーが設けられてもよい。第1の液滴は、5回、経路で熱サイクルされ、次いで検出に供されてもよく、第2の液滴は、10回、熱サイクルされ、次いで検出に供されてもよいなどである。十分なデータポイントのセットが、曲線を規定するために得られるまで、プロセスは繰り返されてもよく、その曲線から、サンプルにおける標的核酸の量が計算されてもよい。同様に、第1の液滴は35回、第2の液滴は30回、第3の液滴は25回などで熱サイクルされるなどで、第1の液滴は5回までサイクルされる。あるいは、全ての液滴は滞留されて、後の時間に連続または同時検出に供されてもよい。曲線はデータポイントから生成されることができ、サンプルにおける標的核酸の量はその曲線に基づいて計算され得る。一実施形態において、標的核酸が第1の液滴に検出される場合に限り、長いサイクルを最初に、次に短いサイクルの液滴を実施することは有用であり得る。
【0095】
同様の実施形態において、多くの熱サイクル経路は、熱サイクルのために選択される液滴の総数より少なく与えられてもよい。サブサンプルの液滴はセット内で処理されてもよい。セット内の各液滴は、ほぼ並行して熱サイクルされてもよいが、複数のセットが連続して熱サイクルされてもよい。例えば、5つの経路を備える液滴アクチュエータが、5セットにおいて35のサブサンプルの液滴、1、2、3...35を処理するために使用されてもよい。例えば、第1のセットの5つの液滴は、1サイクル、2サイクル、3サイクル、4サイクルおよび5サイクルについてのサブサンプルの液滴を含んでもよく、第2のセットの5つの液滴は、6サイクル、7サイクル、8サイクル、9サイクルおよび10サイクルについてのサブサンプルの液滴を処理してもよく、その後のセットは、11〜15サイクル、16〜20サイクル、21〜25サイクル、26〜30サイクルなどでサブサンプルの液滴を処理してもよい。
【0096】
代替の実施形態において、第1のセットの5つの液滴は、5、15、25、35および40サイクルについてのサブサンプルの液滴を含んでもよく、第2のセットの5つの液滴は、8、10、20、30および38サンプルについてのサブサンプルの液滴を含んでもよい。他のセットは、以前に実行した数の間のサイクル数で満たしてもよい。さらに、データはセットの間で解析されてもよく、十分なデータが、所定の範囲の統計的確実性までサンプル中の標的核酸を定量化するために得られると、サイクルは終了してもよい。同様に、標的核酸が存在しないか、またはサブサンプルの液滴中で増幅されないことが明らかな場合、サイクルは終了してもよい。後者の場合において、熱サイクルは、例えば異なる液滴アクチュエータおよび/または異なる試薬を用いて繰り返されてもよい。
【0097】
並行流路のサイクル技術において、全ての経路がサブサンプルの液滴に負荷されてもよい。液滴は、一体となって移動されてもよく、液滴が移動するのに正確な一体化が必要とされなくてもよい。例えば、一部の液滴は反対方向に移動されてもよい。液滴における増幅反応は、概して、異なる回数で停止されるが、一部の液滴は同じ回数サイクルされ、同時に停止されて、繰り返されてもよいことは理解されるだろう。反応は、温度制御領域(例えば図18に示す)において停止されてもよいか、または温度制御領域(図19および20に示す)から離れた位置に輸送されてもよい。液滴が検出領域にわたって輸送される場合、より少ないサイクル数を最初に受けて、続いて、より多いサイクル数を受けた液滴を輸送することは有用であり得る。このアプローチは、高濃度の標的核酸を含む液滴によって引き起こされる可能性がより高い、二次汚染の結果を防止または軽減するのに役立つ。
【0098】
並行流路の熱サイクル技術の種々の実施形態において、液滴が負荷され、滞留されてもよい。次いで、熱サイクルが同時に開始され、各サブセットの液滴について各液滴がその所定数のサイクルを終える場合、連続して終了されてもよい。別の実施形態において、液滴は負荷され、滞留されてもよく、各液滴または各サブセットの液滴についての熱サイクルは、連続して開始され、同時に終了されてもよい。プロトコルにおいて、1つ以上のサブセットの液滴がサブセットと一緒に開始し、連続して終了するが、液滴の他のサブセットは、連続して開始し、サブセットがまた、本発明の範囲内で可能である場合、それらの熱サイクルを完了する。さらに別の実施形態において、液滴または液滴のサブセットは、その液滴が負荷される場合、連続して負荷され、連続して開始されてもよく、液滴が熱サイクルを例えば連続してまたはグループにおいて完了する場合、終了してもよい。さらに別の実施形態において、液滴は分配され、並行して負荷される。
【0099】
別の実施形態において、液滴は、同時に熱サイクルを開始し、異なる数のサイクルを同時に完了することができる。このアプローチは、熱領域内または熱領域間の輸送速度および/または滞留時間を調整することを含み、その結果、液滴はそれらの異なる数のサイクルを同時に完了する。同様の実施形態において、液滴の種々のサブセットは、それらの異なる数のサイクルを同時に完了する。例えば、サイクル数1〜5は同時に完了されてもよく、サイクル数6〜10は同時に完了されてもよいなどである。
【0100】
さらに別の実施形態において、滞留時間は、個々の液滴の熱サイクルプロファイル内で異なるサイクル数で異なってもよい。例えば、初期サイクルはよりゆっくりでもよいが、後のサイクルはより速くてもよいか、またはその逆でもよい。さらに例示するために、液滴は35回サイクルされてもよく、各サイクルは前のサイクルよりわずかに速くてもよい。あるいは別の例として、液滴は35回サイクルされてもよく、サイクル1〜10は第1の速度で開始されてもよいが、サイクル10〜20は第2の速度で開始されるなどである。
【0101】
別の実施形態において、複数のサイクルが効果的な経路の使用のために経路の中で分配されてもよい。例えば、4つの利用可能な経路を備える熱サイクル液滴アクチュエータにおいて、液滴は以下のようにサイクルされてもよい。
・経路1:7
・経路2:1,6
・経路3:2,5
・経路4:3,4
【0102】
このように、経路1において、単一の液滴が7回サイクルされる。経路2において、第1の液滴は1回サイクルされ、続いて第2の液滴は6回サイクルされる。経路3において、第1の液滴は2回サイクルされ、第2の液滴は5回サイクルされる。最後に、経路4において、第1の液滴は3回サイクルされ、第2の液滴は4回サイクルされる。各経路は正確に7サイクル実施し、経路空間が効率的に利用され、液滴の全てをサイクルするのに必要とされる全時間を最小化する。さらに、例示において、少ないサイクル数を受けた液滴が最初に処理され、続いて多いサイクル数を受けた液滴が処理される。この方法において、少ない数のコピーの液滴は、同じ液滴アクチュエータの実際の場所で多い数のコピーの液滴に先行する。このアプローチは、第1の液滴によって残される残留物によって引き起こされる二次汚染の可能性を減少させる。もちろん、これは単純な例であり、本明細書を考慮して当業者によって理解されるように、任意の数の経路が任意の数の液滴とともに使用され、同様に組み合わされてもよい。
【0103】
(7.3 曲がっている流路)
図21は、本発明の液滴アクチュエータの電極構成2100を示す。電極構成2100は、供給源(示さず)からの液滴1815が、2以上の温度領域の間の前後で電極経路に沿って輸送できる方法で構成される電極1805を備える電極経路2105を備える。以前の例のように、温度領域は、加熱器またはヒートシンクなどの温度制御素子1810によって規定される。液滴1815は、温度制御素子1810によって規定される温度領域の間で前後に曲がっているか、または巻いている電極経路2105に沿って蛇行する。他の実施形態のように、液滴アクチュエータは、液滴操作を制御するシステムの一部として与えられてもよい。そのシステムは、熱サイクル領域を通して、検出のための位置に液滴を輸送するようにプログラムされてもよい。
【0104】
図22は、本発明の液滴アクチュエータの電極構成2200を示す。電極構成2200は、図21の電極構成2100と同様である。しかしながら、電極構成2200は、検出のための熱サイクル領域から離れた位置に液滴を輸送するための電極経路2205を備える。電極経路2205は、曲がっている電極経路2005から液滴を輸送するように構成される。
【0105】
各液滴は所定数のサイクルに関して温度領域を通してサイクルされてもよく、次いで検出のために離れた位置に輸送されてもよい。液滴は滞留されてもよく、次いでセンサによって走査されてもよい。例えば、液滴は線Aに沿って滞留されてもよく、センサは液滴を走査できる。あるいは、液滴は検出のために検出ウィンドウ2220に輸送されてもよい。センサは検出ウィンドウに配置される液滴を検出するように配置されてもよい。センサは、各液滴からシグナルを検出するのに適切であり得る。別の実施形態において、CCDカメラまたはLED−フォトダイオード対のアレイなどのアレイ検出器が、複数の液滴を同時に検出するために使用されてもよい。
【0106】
このように、一例において、PCR混合物などの核酸増幅混合物を含む液滴1815、および標的核酸を潜在的に含むサンプルが、電極1805によって規定される曲がっている経路2205に沿って分配され、輸送されてもよい。液滴1815は、温度制御素子1810によって規定される温度領域の間の前後を通る曲がっている経路2205に沿って液滴1815を輸送することによって熱サイクルされてもよい。
【0107】
各液滴は、所定数の回数、サイクルされてもよく、各液滴がその所定数のサイクルを完了する場合、各液滴は検出のための熱サイクル温度領域から離れた位置に輸送されてもよい。別の実施形態において、各液滴がその所定数のサイクルを完了する場合、各液滴は、熱サイクル温度領域の1つに、または検出のための液滴を維持するのに適切な温度を有する別の熱サイクル温度領域に輸送されてもよい。種々の実施形態において、液滴は滞留され、センサによって走査されてもよい。別の実施形態において、各液滴は検出ウィンドウに輸送されてもよい。このプロセスは液滴のセットを生成し、その各々は、所定の回数、熱サイクルされる。例えば、第1の液滴は5回熱サイクルされてもよく、第2の液滴は10回熱サイクルされてもよく、第4の液滴は15回熱サイクルされてもよい、などである。他の例のように、このプロセスは、標的物質を定量化するために適切なデータが得られると、停止されてもよい。
【0108】
曲がっている経路は、本質的に、温度領域間の前後またはジグザグに曲がっているか、または蛇行している任意の種々の形状をとってもよい。例えば、電極経路は、図4および6に示すように直角に沿って前後に蛇行してもよい。その経路は電極のより大きなアレイの一部を形成してもよく、その電極から曲がっているか、または蛇行している経路が選択されてもよい。曲がっている経路は、ジグザグ形状または曲線形状をとってもよい。曲がっている経路の各曲がり角はほぼ同じサイズであってもよいか、または曲がり角は異なるサイズであってもよい。
【0109】
液滴は経路の一端で曲がっている経路に継続的に注ぎ込まれてもよく、他端まで流れてもよい。一部の実施形態において、電極経路は、液滴を曲がっている経路上に、または曲がっている経路外に導くように配置されてもよい。例えば、一実施形態において、経路のあらゆる湾曲または曲がり角は、経路から液滴を取り除くため、および/または経路まで液滴を導入するための少なくとも1つの利用可能な電極経路を備える。一部の場合において、液滴は、利用可能な電極経路を通して経路に沿った異なる点で経路に供給されてもよい。一部の場合において、液滴は、利用可能な電極経路を通して経路に沿った異なる点で経路から除去されてもよい。他の実施形態において、液滴は、上部の基板、底部の基板、および/または上部基板と底基板との間の液滴操作間隙内の横方向の開口部などの任意の液滴アクチュエータ基板の開口部を通して経路上に導入され、および/または経路から除去されてもよい。
【0110】
一部の実施形態において、反応を同時に行うことは有用であり得る。そのような実施形態において、液滴は輸送サイクル時間と等しい速度で供給されてもよい。この実施形態において、進行中の反応の数は各輸送サイクルにて1つ増加する。この実施形態において、同時に行うとは、全ての液滴が同時に熱サイクルの同じ部分にあることを意味する。液滴の同時に行うことにより、輸送速度を変更させることが可能となる。液滴は、同時に熱サイクルの同じ部分内で停止され、インキュベートされてもよい。
【0111】
種々の実施形態において、液滴が、高サイクル数の液滴、すなわち高濃度の標的核酸を有すると予想され得る液滴によって以前に占められた電極を横切らないことを確実にすることは有用であり得る。
【0112】
一部の実施形態において、液滴の検出は曲がっている経路上の所定の位置で起こる。他の実施形態において、液滴は検出のために他の場所に輸送される。一部の実施形態において、検出のポイントまで曲がっている経路に沿って液滴を輸送することは有用であり得る。そのような実施形態において、一旦、全ての液滴の熱サイクルが完了すると、温度制御素子は、継続した熱サイクルを必要とせず、曲がっている電極経路に沿って液滴の輸送を可能にするように調節されてもよい。例えば、核酸変性加熱器は、最も低い起こり得る核酸変性温度以下までその温度を低下させることができる。この方法において、液滴は、増幅プロセスを継続せずに曲がっている経路に沿って蛇行し続けてもよい。キャリーオーバーが懸念される場合、液滴の流れの方向を反転させることが有用であり得る。すなわち、最初に少ないサイクル数を有する液滴を除去し、次に多いサイクル数を有する液滴を除去する。この方法において、液滴は、以前に受け入れられた多いサイクル数の液滴を有する電極を通過しない。
【0113】
別の実施形態において、反応は、それらが、増幅しない熱サイクル温度により輸送され続けることができるように不活性化されてもよい。あるいは、上記のように、液滴は、利用可能な電極経路を通して、検出のための液滴アクチュエータ上の別の位置に輸送されてもよい。
【0114】
図23は、本発明の液滴アクチュエータの電極構成2300を示す。電極構成2300は、温度制御素子1810によって規定される各熱領域内の曲がっている電極経路が、その領域における液滴の保持時間を長くまたは短くするために、どのように長く、または短くすることができるかを示す。
【0115】
例えば、一実施形態において、熱領域における曲がっている経路の曲がり角の長さ(すなわち熱領域における電極の数)は、液滴の進行方向において徐々に短くなってもよく、それによって、液滴が、電極から電極まで一定の速度で経路に沿って輸送される場合、サイクルは加速する。同様に、熱領域における曲がっている経路の曲がり角の長さ(すなわち、熱領域における電極の数)は、液滴の進行方向において徐々に長くなってもよく、それによって、液滴が電極から電極まで一定の速度で経路に沿って輸送される場合、サイクルは減速する。別の実施形態において、熱領域における曲がっている経路の曲がり角の長さ(すなわち熱領域における電極の数)は、第1のサイクルなどの特定のサイクル数にてより長いインキュベーション時間を与えるように変化させてもよい。
【0116】
従って、液滴は、2つの温度領域間の曲がっている経路に継続的に供給されてもよく、固定および一定の速度で輸送されてもよい。温度領域における滞留時間は、温度領域を通過するために横切らなければならない液滴の電極の数によって決定されてもよい。この実施形態において、異なる液滴が同時に温度サイクルの異なる段階で存在することができるという意味において、液滴は熱的に同時に行われなくてもよい。この実施形態は、実際の場所をより少なくする方法で液滴アクチュエータ上に電極を配置することによって液滴アクチュエータのサイズを減少させるのに有用であり得る。
【0117】
本明細書に記載される曲がっている電極構成または他の流路の構成は、概して、2つの温度領域を有するように例示されているが、任意の数の温度領域を有してもよいこともまた、留意されるべきである。
【0118】
図24は、本発明の液滴アクチュエータの電極構成2400を示す。電極構成2400は曲がっている経路2425を備える実施形態を示し、曲がっている経路2425の1つ以上の曲がり角はアクセス経路2420を備える。例示した実施形態において、アクセス経路2420は、曲がっている経路2425から、温度制御素子2405によって規定される温度制御領域に液滴を輸送するように構成される。温度制御素子2405は、例えば、検出前に増幅した液滴を維持するように構成されてもよい。例えば、液滴は、室温または検出前に液滴成分を保存するために選択された温度で維持されてもよい。このように、操作において、一連の液滴は、熱領域1810間に液滴を輸送するために長い曲がっている経路2425に輸送されてもよい。各液滴に関して、所定数のサイクルが達成されると、液滴はアクセス経路2420を通して曲がっている経路2425から外側へ輸送されてもよく、検出のため、または未検出物を保持するための保存領域に輸送されてもよい。
【0119】
図25は、本発明の液滴アクチュエータの電極構成2500を示す。電極構成2500は、構成2500が、電極の活性化を必要とせずに、検出前に液滴を保存するための滞留領域2505を備えるということを除いて、図24の電極構成2400と同様である。滞留領域2505は、例えば、種々の化学および/または物理的特性により規定されてもよい。例えば、滞留領域2505は、液滴操作間隙内または上部の基板または底部の基板(例えば障壁、壁、くぼみおよび/または突起)の物理的特性、および親水性領域などの化学特性により規定されてもよい。物理および/または化学的特性は、検出の間および/または検出に係る間に、所定の場所に液滴1815を保持するために共同してもよい。このように、操作において、一連の液滴は、熱領域(図示せず)の間に液滴を輸送するために長い曲がっている経路2425に輸送されてもよい。各液滴1815に関して、所定数のサイクルが達成されると、液滴1815は、アクセス経路2420を通して曲がっている経路2425から外側に輸送され、未検出物を保持するための滞留領域2505に輸送されてもよい。
【0120】
(7.4 ループ流路)
図26は、本発明の液滴アクチュエータの電極構成2600を示す。電極構成2600は電極ループ2605を形成するように配置される電極1805を備える。液滴1815は、熱サイクルを行うために熱領域を通ってループ中の電極経路に沿って輸送される。液滴は、ループに侵入し、所定の回数、ループの周りを回ることができ、次いでループから出ていく。入口および出口は、例えば、電極経路(図示せず)にアクセスすることによって、および/または液滴アクチュエータの外部から1つ以上の開口部を通して(例えば上部または底部の基板あるいは液滴アクチュエータ内の任意の他の経路を通して)与えられてもよい。
【0121】
輸送は一定であってもよい。すなわち、液滴は、一定の速度でループの周りを継続的に移動するか、または液滴は、異なる速度だが、実質的に同一の平均速度で移動することができる。一定の輸送の実施形態に関して、電極の配置は、各熱領域における必要な滞留時間を規定するように構成されてもよい。輸送は周期的であってもよい。すなわち、液滴は、一定の期間、熱領域に保持されてもよく、次いでループを通して他の熱領域に輸送されてもよい。
【0122】
ループは様々な液滴を効率的に収容でき、必要な場合、熱サイクルプロトコルの一部または全プロトコルについての最大数の液滴を負荷できる。ループの周りの液滴の輸送は、一方向であってもよいか、または二方向であってもよい(すなわち液滴輸送の方向は可逆的であってもよい)。検出はループ自体でなされてもよいか、または液滴は検出のためのループから離れた位置に輸送されてもよい。一定の循環は、液滴内の混合および熱均一性を増加でき、同じ経路を通る各液滴の循環は、熱領域内の空間の温度変化に起因する変動性を減少できる。
【0123】
図27は、本発明の液滴アクチュエータの電極構成2700を示す。電極構成2700は複数の電極経路ループ2705を備える。電極構成2700はまた、電極経路ループ2705上に、および/または電極経路ループ2705から液滴を輸送するためのアクセス電極経路2710を備える。熱サイクルプロトコルは1つ以上のループ2705を備えてもよい。例えば、一連の4つのループ2705は、複数の液滴が各ループでサイクルされる熱サイクルプロトコルを実施するために使用されてもよい。一般的に、液滴は、ループ上の1または2の空の電極部位によって分離されるべきであり、それによって、各ループ上の液滴の最大数は1/2nまたは1/3nと等しく、ここでnはループにおける電極の総数であり、nはループにおける電極の数である。検出はリアルタイムであってもよいか、またはサイクルの各々からのエンドポイントデータは、サンプルにおける産物を定量化するために使用される曲線を規定するように使用されてもよい。
【0124】
図28は、本発明の液滴アクチュエータの電極構成2800を示す。電極構成2800は電極経路ループ2805、および電極経路サブループ2810を備える。電極経路サブループ2810は、熱領域における液滴のための保持領域を与えるように構成される。構成2810および同様の構成において、プロトコルが実行でき、ここで、1つ以上の液滴は、輸送速度のみに基づいた有効な滞留時間より長い一定の期間、熱領域内に維持されることを必要とする。ループ2810の電極経路は、分岐構造または他の種類のループと置き換えられてもよいことは理解されるだろう。
【0125】
ループが存在する場合、特定の液滴がアクセスされるまで、保存がサブループ2810の周りに液滴を回転させることによってなされてもよい。次いで、特定の液滴は、電極経路ループ2805を通して他の熱領域に輸送されてもよい。他の熱領域において、特定の液滴は、ループ上に保存されてもよいか、またはループを通過し、出発熱領域に戻るように方向付けられてもよい。電極経路ループ2805および電極経路サブループ2810の周りの移動は、一方向であってもよいか、または二方向であってもよい。図18〜20に例示されるような直線状の電極経路を備える他の実施形態もまた、熱領域内にループ電極経路または分岐電極経路を備えてもよいこともまた、理解されるだろう。
【0126】
(7.5 等分している流路サイクル)
図29は、本発明の液滴アクチュエータの電極構成2900を示す。電極構成2900は熱サイクルの流路の構成を示し、ここで、小液滴は検出のためのより大きな液滴から分裂される。電極経路2900は、熱制御素子110によって規定される熱領域の間の前後に熱サイクル液滴2910を輸送するように構成される電極2907を備える第1の電極経路2905を備える。電極経路2905は、本明細書に記載されるような1つ以上の電極経路ループおよび/または曲がっている流路の電極配置と置き換えられてもよいことは理解されるだろう。電極構成2900はまた、熱サイクル液滴2910から小液滴2912を分配するように構成される電極2917を備える第2の電極経路2915を備える。電極2907は、概して、電極2917より大きく、従って、比較的大きな体積の液滴2910を支持し、その液滴2910から複数の小さな液滴の小液滴2912が分配されてもよい。電極経路Aは、熱サイクルの間の液滴2910が、熱制御素子1810によって規定される熱領域の間に輸送されることを示す。電極経路Bは操作を分配する部分を示し、ここで、液滴2910は、電極経路2915に近接する電極経路2905の電極上に位置する。電極経路2915上の電極2917は活性化され、それによって、液滴2910から細長い延長部の形成を引き起こす。電極経路Cは、電極経路2915上の小液滴2912の形成を引き起こすための1つ以上の中間電極2917の不活性化を示す。小液滴2912は検出に供されてもよく、ここで、小液滴2912は形成され、および/または検出のために離れて輸送されてもよい。
【0127】
一般的に、等分している流路アプローチにおいて、熱サイクル液滴2910のサイズは、検出のために取り除かれる小液滴2912のサイズの数倍である。一部の実施形態において、新しい液滴が、検出のための小液滴の除去後、熱サイクルしている液滴に追加されてもよい。例えば、追加された液滴は、熱サイクル反応のためのバッファーまたは1つ以上のさらなる試薬を含んでもよい。この方法において、熱サイクル液滴は一定の体積で維持されてもよい。図29に示す実施形態において、熱サイクル液滴2910由来の小液滴から分配するために使用される電極2917は、より小さい小液滴2912を収容するために、熱サイクル電極2907より小さい。しかしながら、代替の構成において、小液滴から分配するために使用される液滴は、熱サイクル液滴を輸送するために使用される液滴と同じサイズであってもよい。一部の場合において、熱サイクル液滴は、細長いスラグ形状の液滴として輸送されてもよく、小液滴は、例えばスラグの下にある中間電極を不活性化することによってスラグ形状の液滴の端部から分配されてもよい。
【0128】
関連したアプローチにおいて、サンプル液滴のセットが熱サイクルされ、小液滴が各サイクル後、そのセットの1つのメンバーから除去される。このアプローチにおいて、セットにnのサンプル液滴が存在する場合、小液滴はnサイクル毎に液滴から除去されてもよい。このアプローチは、より小さい種類の液滴サイズを用いて熱サイクルプロトコルを支持するという利点を有する。例えば、4倍数の液滴の10の並行反応が、40の熱サイクルのエンドポイントを与えるために使用されてもよい。
【0129】
別の関連した実施形態において、より大きな液滴が、上記のように熱サイクルされ得るより小さな液滴に分裂される前に、数回、熱サイクルされてもよい。このアプローチは、複数の小液滴の熱サイクルを含む本明細書に記載される任意の実施形態において有用であり得る。この方法において、産物の開始濃度(例えば核酸産物)が規定されてもよく、それによって、各々の小液滴は、小液滴における増幅を確実にするための十分な産物を含む。従って、本発明は、電極の複数のパッドが、図29に示す電極経路2905および2915の結合と同様の方法で互いに結合される、種々の実施形態を含む。例えば、一実施形態において、電極経路には、大きな電極を有する第1の経路と、中間のサイズの電極を有する第2の経路と、小さなサイズの電極を有する第3の経路が備えられる。別の例として、配置は、大きなサイズの電極を有する第1の電極経路を備えてもよい。この第1の電極経路は、同様のサイズの電極を有する2つ以上の第2の電極経路と結合されてもよい。第2の電極経路の各々は、さらに小さなサイズの電極を有する1つ以上の第3の電極経路と結合されてもよい。最初に、大きな液滴は第1の電極経路上で熱サイクルされ、次いで2つ以上の第2の電極経路上に分配されてもよい。2つ以上の第2の電極経路から、液滴は、検出のための1つ以上の第3の電極経路上に分配されてもよい。第2の電極経路上の液滴は熱サイクルされてもよく、続いて各々の所定数の熱サイクルがされ、小液滴は検出のための1つ以上の第3の電極経路上に分配されてもよい。
【0130】
(7.6 バッチサイクル)
一実施形態において、本発明は一連の検出バッチ熱サイクル技術を与える。このアプローチにおいて、サブサンプル液滴はサンプルから生成され、温度制御領域に配置されてもよい。温度制御素子は、所定の熱サイクルプロトコルに従って温度制御領域において温度をサイクルすることができる。1つの液滴は、所定数のサイクル毎の後に検出されてもよい。このように、例えば一実施形態において、異なる液滴が各サイクルの後に検出される。この方法において、各液滴は一度のみ検出に供される。データは、サンプルに存在する標的物質を定量化するのに適切な曲線を生成するために使用されてもよい。
【0131】
図30は、本発明の液滴アクチュエータの電極構成3000を示す。液滴アクチュエータ3000は電極アレイ3005と、電極アレイ3005に配置されるサブサンプル液滴3010を備える。サブサンプル液滴3010は、単一のサンプル液滴(図示せず)から分配されてもよい。サブサンプル液滴3010は、(存在する場合)液滴操作間隙の外部まで電極経路(図示せず)または多くの開口部(図示せず)のうちの1つを通して電極アレイ3005上に負荷されてもよい。
【0132】
1つ以上の熱サイクル温度制御素子3015は、例えばアレイの下および/またはアレイの上にある、アレイ3005に結合される。熱サイクル温度制御素子3015は、電極アレイ3005上の熱サイクル液滴3010を加熱し、能動的または受動的に冷却する。熱サイクルの間、センサは液滴3010からの信号を検出するために液滴3010上を通過する。例えばセンサは、各サイクル後、単一の液滴を検出するのに十分な速度で液滴3010上を通過してもよい。一般的に、センサは、nサイクル毎に単一の液滴を検出するのに十分な速度で液滴3010を通過してもよい。ここで、nは、所定のレベルの統計的有意性にて液滴中の標的産物を定量化するのに有用な曲線を生成するために十分なエンドポイントを達成するのに選択される数である。代替の実施形態において、2つ以上のセンサが使用されてもよい。さらに別の実施形態において、CCDカメラなどのアレイ検出器、またはLED−フォトダイオード対のアレイが、複数の液滴を同時に検出するために使用されてもよい。
【0133】
同様の実施形態において、サブサンプル液滴は温度制御領域に配置されるサンプルから生成されてもよい。温度制御素子は、所定の熱サイクルプロトコルに従って温度制御領域において温度をサイクルすることができる。熱サイクルの各nラウンド後、1つ以上の液滴が検出のための温度制御領域から離れた位置に輸送されてもよい。例えば、輸送は電極経路に沿って液滴操作によって実施されてもよい。液滴は、それらが温度制御領域から離れるか、またはそれらが後の時間での解析のために滞留され得る場合、検出されてもよい。
【0134】
関連したアプローチにおいて、液滴は、n回の熱サイクル毎の時間に1回以上、熱サイクルユニット上に連続して輸送されてもよい。次いで、検出は最後のサイクルの後に実施されてもよい。例えば、液滴のアレイは、連続して、同時にまたは最後のサイクルの後にサブセットにおいて画像化されてもよく、検出からのデータは、元のサンプル中の標的産物を定量化するための曲線を生成するために使用されてもよい。
【0135】
図31は、本発明の別の電極構成3100を示し、ここで、サンプル液滴は熱サイクルされ、nサイクル毎の後、サブサンプルの液滴は分配され、検出のために離れた位置に輸送される。例示した実施形態において、リザーバー3105はガスケット3110によって規定される。温度制御素子3115はリザーバー3105の下部にある。ガスケット3110における開口部3120は、リザーバー3105から離れてサブサンプル液滴3130を輸送するための液体経路を与える。電極経路3125は、サンプル液滴3135からサブサンプル液滴3130を分配するための手段を与える。分配されたサブサンプル液滴3130は検出に供されてもよい。例えば、それらは、形成時にすぐ検出に供されてもよいか、またはそれらは後の時間での検出のために離れた位置に輸送されてもよい。
【0136】
同様の実施形態において、液滴3135は、液滴アクチュエータの液滴操作間隙に対して外側のリザーバーに与えられてもよい。液滴3135はリザーバー内で熱サイクルされてもよく、小液滴3130は、任意の種々の液滴分配技術を用いてリザーバーから液滴操作間隙内に分配されてもよい。例えばリザーバーは、リザーバーから、1つ以上の電極に近接する液滴操作間隙に延びる液体経路に結合されてもよい。電極は、熱サイクルの各nサイクルの後、液滴を液滴操作間隙に分配するために使用されてもよい。次いで、分配された液滴は、さらなるアッセイ工程および/または検出に供されてもよい。
【0137】
図32は、図31の電極構成3100と同様の実施形態を示す。電極構成3200は、小液滴3130が、どのように、離れた位置に輸送され、配置され、続いて検出器によって操作され得るかを示す。例えば、検出器は、Aと印した経路などの経路に沿って連続して各液滴を検出してもよい。あるいは、本明細書に記載されるこの実施形態および他の実施形態において、全ての液滴は、例えばCCDカメラまたはLED−フォトダイオード対のアレイなどのアレイ検出器を用いて一緒に画像化されてもよい。
【0138】
(7.7 反応クエンチング技術)
図33は、電極構成3300が、反応液滴3305を配置するために使用される実施形態を示す。反応液滴3305は、本明細書の特定の他の実施例に示されるように、熱サイクル液滴(例えば増幅準備液滴)であってもよいか、または反応が経時的に生じる一部の他の反応であってもよい。温度制御素子3310は熱サイクルまたは反応液滴3305の温度制御を与えられてもよい。反応クエンチング液滴3315は、反応液滴3305と接触するように輸送されてもよい。反応クエンチング液滴3315は、反応液滴3305において生じる反応をクエンチ、または後でクエンチするための1つ以上の試薬を含んでもよい。一実施形態において、反応液滴3305における反応は実質的に同時に開始され、反応液滴3305は連続して反応クエンチング液滴3315と混合される。クエンチング後、混合された液滴は、反応速度論の曲線の指標を生成するためのさらなるアッセイ工程および/または検出に供されてもよい。別の実施形態において、反応液滴3305における反応は連続して開始され、反応液滴3305は反応クエンチング液滴3315と実質的に同時に混合される。同様に、クエンチング後、混合された液滴は、反応速度論の曲線の指標を生成するためのさらなるアッセイ工程および/または検出に供されてもよい。中間プロセスにおいて、反応は連続して開始され、連続してクエンチされる。
【0139】
反応液滴が反応クエンチング液滴と混合される本発明の任意の種々の実施形態において、反応液滴は反応クエンチング液滴と接触するように輸送されてもよく、反応クエンチング液滴は反応液滴と接触するように輸送されてもよく、ならびに/または反応液滴および反応クエンチング液滴は互いに輸送されてもよい。クエンチング液滴は必要な場合、送達されてもよいか、または反応液滴とともに配置され、所定の計時プロトコルに従って混合されてもよい。
【0140】
熱サイクル増幅プロトコルにおけるこのアプローチの1つの利点は、クエンチ後、液滴が熱サイクルに供され続け得るが、増幅はクエンチング液滴との混合の結果として停止することである。
【0141】
関連した実施形態において、出願人は、核酸増幅などの特定の反応が、静電場を用いてクエンチされ得ることを発見した。例えば、反応は、電圧信号を下部の電極または液滴に近接する別の電極に印加することによって停止されてもよい。印加される電圧信号は、反応を停止または実質的に停止するのに十分であるように選択されてもよい。例えば、増幅反応を停止するのに必要とされる電圧信号は、1つの電極から次の電極に液滴輸送を実施するのに必要とされる電圧信号に関する電圧信号を単に維持されてもよい。従って、例えば核酸増幅反応は、核酸増幅液滴の輸送を停止させ、反応を停止させるのに十分な期間、活性化された電極上に液滴を保持することによって停止されてもよい。電圧レベル、サイクルおよび/または電圧の種類もまた、増幅反応が実質的に停止されるまで、調節されてもよい。一部の場合において、電極構成は特異的不活性化部位を含んでもよく、その部位に電極が存在し、反応を不活性化するように選択される特性を有する。さらに、増幅が電極に配置される液滴を用いて実施される実施形態において、一部の場合において、増幅の間に増幅準備液滴の下部にある電極上の電圧を不活性化または制御することは有用であり得、それによって、電極は液滴の継続している増幅を過度に妨げない。
【0142】
別の関連した実施形態において、液滴アクチュエータは、液滴操作電極に近接して位置する1つ以上の阻害剤を含んでもよい。例えば、阻害剤は液滴アクチュエータの表面で乾燥された乾燥阻害試薬であってもよい。別の例として、阻害剤はPCRを阻害することが知られている白金または窒化物などの物質であってもよい。例えば、阻害剤は、液滴が反応を停止させるためにパッドまたはワイヤと接触して輸送され得るように配置される白金パッドまたはワイヤに曝露されてもよい。一部の実施形態において、阻害剤は、液滴アクチュエータ上の種々の電極部位に配置されてもよい。
【0143】
操作において、反応液滴は、連続して、阻害剤と接触して輸送されてもよく、液滴は、連続して、反応が停止される時間における反応のエンドポイントの曲線の指標を生成するためにさらなるアッセイ工程および/または検出工程に供されてもよい。同様に、反応は連続して開始され、阻害剤のアレイと接触して同時に輸送されてもよい。別の実施形態において、反応は連続して開始されてもよく、液滴は、阻害剤と接触して連続して輸送されてもよい。任意の事象において、液滴は異なる反応時間または熱サイクルを受ける液滴を含み、液滴中の反応産物は、時間またはサイクルに関する反応の進行の曲線の指標を生成するために、さらなるアッセイ工程および/または検出工程に供されてもよい。
【0144】
(7.8 反応時間経過のサンプリング)
本発明は、液滴アクチュエータが提供され、反応液滴が液滴アクチュエータ上に提供される、関連する実施形態を提供する。反応液滴は、1つ以上の反応が反応液滴内で起こるという特徴がある。例えば、反応としては、化学反応、生化学反応および/または生物学的反応が挙げられる。反応が進行する場合、1つ以上の小液滴は反応液滴から分配される。各々のこのような小液滴は、反応を停止させる方法で処理されてもよい。例えば、小液滴の温度は、反応が停止または実質的に停止する温度に調節されてもよい。別の例として、各々の小液滴は、反応をクエンチする試薬を含む試薬液滴と混合されてもよい。各々の小液滴は異なる時間で親反応の液滴から除去されてもよく、小液滴は、反応の時間経過を示す曲線を生成するためにさらなる解析に供されてもよい。関連した実施形態において、小液滴における反応はクエンチされないが、各々の小液滴は、親反応の液滴から分配された後、迅速に検出に供される。さらに別の実施形態において、親液滴は多数の小液滴に細分されてもよく、小液滴は、各々の小液滴が異なる時間で検出に供される検出プロトコルに供されてもよい。収集したデータは、反応速度論の曲線の指標を生成するために使用されてもよい。一実施形態において、小液滴の分配は、電極、例えばエレクトロウェッティング媒介、誘電泳動現象媒介液滴分配によって媒介される。
【0145】
関連した実施形態において、反応速度は、異なる時間で一連の反応を開始するために液滴アクチュエータ上の液滴を混合し、続いて、同時に液滴を画像化し、反応速度論の曲線の指標を生成するためにデータを用いることによって測定される。さらに別の関連した実施形態において、反応速度は、異なる時間で一連の反応を開始するために液滴アクチュエータ上の試薬液滴を混合し、続いて、異なる時間でセンサを用いて反応液滴を走査し、反応速度の異なる反応時間の指標に基づいて曲線を生成することによって測定される。これらの任意の実施形態において、特定の問題のある反応の必要性に依存して、反応は検出前に停止されても、されなくてもよい。
【0146】
(7.9 さらなる熱サイクルの実施形態)
種々の特性を有するさらなる様々な実施形態は、本発明の範囲内であり得る。少しの例を以下に示す。
【0147】
図34は、本発明の液滴アクチュエータの電極構成3400を示し、ここで、熱サイクル経路3425は半径方向に配置される。中心の温度制御素子3410は環状である。温度制御素子3410は、ディスク形状、六角形、八角形などの様々な代替の形状であってもよい。例示した実施形態において、熱サイクル経路3405は温度制御素子3410から外側に放射状に広がる。外側の温度制御素子3415もまた設けられる。電極経路3425は、中心の温度制御素子3410から外側の温度制御素子3415まで延びる。電極構成3400は、より大きな電極構成の一部として与えられてもよい。液滴は、液滴アクチュエータの外部に対する開口部を介して、および/または他の電極経路(図示せず)を介して電極経路3425に導入されてもよいか、あるいは上部の基板を欠く開口系において、液滴は単に液滴操作表面上に配置されてもよい。外側の温度制御素子3415は、ワイヤ3416によって接続される個々の温度制御素子として例示される。しかしながら、外側温度制御素子3415は異なる形状であってもよく、例えば外側温度制御素子3415は、単一の環状の外側温度制御素子、例えば円形、六角形、八角形、または他の環構造を有する環と置き換えられてもよいことは理解されるだろう。
【0148】
図35は、複数のセットの液滴輸送経路3515を有する電極アレイによって接続される複数の温度制御素子3510を有する電極構成3500を示す。リザーバー電極3520もまた、液滴輸送経路3515に隣接して与えられる。温度制御素子3510は同じであってもよいか、または異なっていてもよい。温度制御素子3510は温度制御領域を規定するために使用されてもよい。温度制御領域における温度は同じであってもよいか、または異なっていてもよい。
【0149】
図36は、電極構成3600を示し、ここで、先細(例えば細長い三角形または楔形)の電極3610および3615が、温度制御素子3620と3526との間に液滴を輸送するために使用される。電極3615は不活性化されるが、電極3610の活性化により、温度制御素子3620に対して液滴が輸送される。電極3615の活性化および電極3610の不活性化により、温度制御素子3620から温度制御素子3625に戻るように液滴が輸送される。この種の電極構成または2008年10月17日に出願された「Droplet Actuator Structures」という発明の名称の国際特許出願第PCT/US2008/80275(その全開示は本明細書に参照として援用される)に記載されるもののような電場勾配を利用する他の構成も使用されてもよい。
【0150】
図37は、本発明の液滴アクチュエータカートリッジの底部基板3700の写真である。この配置(プリントされた回路基板上の銅)は、サンプルおよび試薬を分配するためのリザーバー電極3710を備える。この配置は、温度領域3740の間に液滴を循環させるための電極ループ3716を備える。この配置は、試薬および/またはサンプル液滴を用いて液滴操作を実施するための輸送経路3720を備える。例えば、輸送経路3720は、リザーバー電極3710と電極ループ3716および/またはサンプル調製操作および/または他の液滴操作との間の試薬および/またはサンプル液滴を輸送するために使用されてもよい。この配置は検出電極3718を備える。検出電極3718は、電極ループ3716および輸送経路3720から構成される他の液滴操作電極より大きい。液滴アクチュエータカートリッジは、電極の構成を覆い、液滴操作を実施するのに適切な液滴操作間隙を形成するために底部基板から分離される上部の基板(図示せず)を備えてもよい。上部の基板は、液滴操作間隙における液滴に対して電気的に露出される参照電極または接地電極を備えてもよい。適切な上部基板の例としては、9月4日,3708に出願された「Droplet Actuator with Improved top Substrate」という発明の名称の国際特許出願第PCT/US2008/075160号に記載されるものが挙げられる。液滴操作間隙は、液滴操作に供される液滴と混合する流動性の充填流体などの流動性の充填流体で充填されてもよい。
【0151】
図38は、図37に示される底部基板3700の配置の図である。この図は、カートリッジ上に熱サイクル温度領域を作製するのに使用される加熱バー3808の配置を示す。
【0152】
図39〜43は、図37および38に示すカートリッジ配置を用いた熱サイクル実験の実施の結果を示す。
・MRSA/Eva Greenシステム:
標的物:mecA遺伝子の176bpフラグメント(遺伝子1つにつき8〜10のコピー)
サンプル:バッファー中のメチシリン耐性黄色ブドウ球菌(MRSA) gDNA(ATCC#700699D−5)
・定量実験:
100,000〜1コピーのMRSAゲノム(反応物中に300pg〜3fg gDNA)
同じ量のDNAを、660nLの液滴アクチュエータ反応物およびBioRad 50μl反応物(75倍の濃度差)に加えた。
・PCR混合物:
Eva Green色素
白金Taq
・充填流体
ヘキサデカン
・熱プログラム(典型的):
Hotstart:60s@95、
40サイクル:(10s 95C、20s@60C)
【0153】
比較実験を、液滴アクチュエータおよび市販のリアルタイムPCRシステム(BioRad IQ5)で実施した。インプットゲノムDNAの量は、1〜100,000MRSA細胞におけるDNAの量と対応するように変化させた。CT値は以下のようであった。
【0154】
【表1】

【0155】
図39は、カートリッジ上での増幅にいての生のデータおよび正規化したデータを示す。
【0156】
図40は、BioRadIQ5からの正規化したデータと比較した本発明のカートリッジからの正規化したデータを示す。
【0157】
図41は、1つの液滴アクチュエータでの12の併発反応(4つの濃度の各々の3つの複製)の結果を示す。各セットの複製を単一のループで増幅させた。
【0158】
図42は、図37および38に示すカートリッジ配置を用いる別の熱サイクル実験の結果を示す。実験の詳細は以下の通りである。
・Candida albicans/Taq Manシステム
−標的物:18SリボソームRNA遺伝子の172bpフラグメント(1つのゲノムにつき70〜100コピー)
−サンプル:Candida albicans gDNA(ATCC#10232D−5)
・PCR混合物
−TaqManプローブ(FAM−BHQ)
−Bio−Rad iTaq
・充填流体
−シリコーン油
・熱プログラム
−Hotstart:120s@95C
−40サイクル(15s 95C、60s@60C)
図42における定量は、gDNAのインプット量の生物またはゲノム等価物の数による。
【0159】
図43は、増幅が検出から分離される実験に使用される液滴プロトコルを示す。同一の液滴の集団は色素を用いずに熱サイクルした。周期的に、1つの液滴を除去し、色素液滴と合わせ、検出に供し、次いで廃棄リザーバーに輸送した。上記のMRSAシステムを、87,000コピーおよび5サイクルの間隔で使用した。工程1において、6つの液滴を、図37および38に示す液滴アクチュエータの熱サイクルループ上に分配し、輸送した。液滴は増幅試薬を含んだが、検出試薬は含まなかった。工程2において、3つの液滴を各温度制御領域に配置した。工程3において、液滴を、熱サイクルを行うためにループの周りに回転させた。工程4において、n回の熱サイクルの後、液滴を熱サイクルループから取り除いた。工程5において、取り除いた液滴を熱領域から離れた位置へ輸送した。工程6において、除去した液滴を検出液滴と合わせ、検出に供し、処分した。工程4、5および6を後の液滴について繰り返した。
【0160】
図44は、図43に対して記載される実験の結果を示す。その結果は、増幅が検出から分離され、個々の小サンプル液滴のセットが異なって熱サイクルされて、単一のリアルタイム増幅曲線を生成するプロトコルを用いて生成され得る増幅曲線を示す。
【0161】
(7.10 反応の停止)
核酸増幅反応をクエンチまたは実質的に停止することが所望される本明細書の種々の実施形態において、増幅反応を停止することが公知である種々の試薬が使用されてもよい。例えば、試薬は、例えばポリメラーゼを変性および/または分解するために結合することによって、ポリメラーゼ活性を妨げることができる。さらなる例を以下の表に与える。
【0162】
【表2】

【0163】
(7.11 デジタルPCR)
デジタルPCRは、サンプル中の正確な数のテンプレートコピーを測定するのに高度に定量的な方法として報告されている。サンプル液滴は、複数のナノリットルサイズのサブユニットに分配されるか、または分裂されてもよい。ほとんどの娘液滴は、0または1つのコピーを含む(一部はポアソン分布に起因して2つ以上のコピーを有する場合がある)。本発明は、液滴アクチュエータ上でデジタルPCRを実施するための技術を提供する。小さなユニットサイズの電極が好ましい。一実施形態において、電極は約200×200μmの電極である。液滴操作間隙の高さも調節されてもよい。200×200μmの電極を備える約100μmの液滴操作間隙の高さは、約4nLの体積を有する液滴を規定する。多くのこのような液滴は、種々の液滴分配技術を用いて生成されてもよい。一例において、一連の電極は細長い鎖を生成するように活性化され、次いで活性化された電極の散在された群は不活性化され、活性化された電極上でナノリットルのサイズの娘液滴を生じる。従来の分配および輸送技術もまた、一連の娘液滴を形成するために使用されてもよい。液滴アクチュエータ全体は増幅を実施するために熱サイクルされてもよいか、または個々の液滴は、熱サイクルを行うために熱制御領域を通してサイクルされてもよい。液滴は、液滴アクチュエータ表面上に、電圧、化学的または物理的パターニングによって反応全体にわたって所定の位置に維持されてもよい。増幅核酸の存在は液滴中で検出されてもよく、標的核酸の量が決定されてもよい。
【0164】
従って、例えば、本発明は、標的核酸、および必要に応じて増幅試薬を含むサンプル液滴を提供する工程と、サンプル液滴から小液滴を分配する工程であって、増幅試薬がサンプル液滴に存在しない場合、増幅試薬を含む各々の小液滴を混合して、増幅準備液滴を生じる工程と、各々の小液滴を、標的核酸を増幅するために選択される熱サイクルプロトコルに供する工程と、各々の小液滴中の増幅産物を検出する工程と、前記増幅産物が生成されるサンプルの一部を含む小液滴の数を決定する工程とを含む方法を提供する。一部の実施形態において、前記小液滴のうちの少なくとも1つは少なくとも1つの標的核酸分子を含む。増幅試薬は標的物を増幅するのに適切な任意の試薬を含んでもよい。一部の場合において、増幅試薬は、増幅標的分子とハイブリダイズし、ハイブリダイゼーションの際に変化するか、またはハイブリダイゼーションの結果として蛍光特性を有する少なくとも1つのプローブを含む。前記増幅産物が生成されるサンプルの一部を含む小液滴の数を決定する工程は、前記少なくとも1つのプローブのハイブリダイゼーションの結果としての蛍光変化を検出することを含んでもよい。前記増幅産物が生成されるサンプルの一部を含む小液滴の数を決定する工程は、全ての小液滴を一緒に画像化すること、あるいは例えば液滴を一度に輸送することによって、または検出ウィンドウを通してサブグループ内の個々の液滴もしくは液滴のグループを連続して画像化することを含む。小液滴は約1μL未満の体積を有してもよい。他の実施形態において、小液滴は、約1μLより大きい範囲から約1000μL、または約100μより大きい範囲から約500μLの体積を有する。この方法の種々の工程は、液滴アクチュエータの液滴操作間隙中、または液滴操作表面上で実施されてもよい。一部の場合において、小液滴は、液滴操作間隙の2つの基板間で平らまたはディスク形状の構造に圧縮される。液滴操作間隙が設けられる場合、それは、必要とされる液滴操作を実施するのに適切な任意の高さを有してもよい。一部の場合において、液滴操作間隙は、約50μm〜約1000μmの範囲、または約100μmより大きい範囲〜約500μの高さを有する。特定の実施形態において、熱サイクルは、1つの熱領域から別の熱領域へ液滴を輸送することによってなされる。特定の実施形態において、液滴アクチュエータはサンプルチャンバを欠き、および/または流路チャネルを欠く。特定の実施形態において、サンプル液滴から小液滴を分配する工程は、流路チャンネルからサンプルを置き換える置き換え流体を用いずになされる。サンプル液滴は増幅試薬とともに与えられてもよいか、または増幅試薬は、増幅準備液滴を得るために、例えば各小液滴と増幅試薬とを混合することによって、液滴操作を用いて加えられてもよい。サンプル液滴は検出試薬とともに与えられてもよいか、または検出試薬は、検出準備液滴を得るために例えば各小液滴と検出試薬とを混合することによって、液滴操作を用いて加えられてもよい。検出試薬は増幅の前後に加えられてもよい。
【0165】
関連した実施形態に加えて、サンプル液滴がナノリットルの娘液滴のセットに分裂された後、異なるセットのプライマーが、特定の核酸配列についてのPCRを実施するために各娘液滴と混合されてもよい。このアプローチは、液滴アクチュエータで同時に複数の核酸の発現レベルの評価を容易にする。
【0166】
(7.12 検出のための磁性反応ビーズの操作)
液滴アクチュエータベースのPCR(例えば、定量的リアルタイムPCR(QRT−PCR))において、標的核酸は増幅反応のために磁性反応ビーズに固定されてもよい。増幅産物を定量化するために、磁性反応ビーズを含む反応液滴は、液滴操作を用いて液滴アクチュエータ上の検出ウィンドウに輸送されてもよい。一部の例(例えばQRT−PCR)において、増幅産物の検出は、増幅産物の量を定量化するためにSybrGreenなどの蛍光色素を利用してもよい。しかしながら、サンプル液滴内に分散される磁性反応ビーズは、検出装置(例えば蛍光光度計)から蛍光を遮断することによって蛍光色素の検出を妨げる場合がある。
【0167】
磁場が、(a)組み込まれていない標識ヌクレオチドの検出のために増幅液滴から磁性ビーズを取り除くため、または(b)組み込まれていない標識ヌクレオチドの検出のために増幅液滴内の側へ液滴を引き付けるために使用されてもよい。
【0168】
図45は、ビーズが細長い液滴内の端側へ引き付けられ、それによってビーズが検出の間、検出ウィンドウに曝露されない本発明の実施形態を示す。磁石は、もちろん、液滴操作表面または液滴操作に対して様々な配置で与えられてもよい。例えば、図45に示すように、磁石は液滴操作表面の下に配置される。しかしながら、磁石は、代替として、液滴アクチュエータ間隙において、および/または部分的に液滴アクチュエータを形成する1つ以上の基板上において、液滴アクチュエータの側方に隣接して、液滴アクチュエータの上に配置されてもよい。つまり、磁石は、検出ウィンドウの外側または少なくとも実質的に外側である液滴の領域にビーズを引き付ける任意の位置に与えられてもよい。
【0169】
代替の実施形態において、磁石は、検出に供される液滴の完全に外側にビーズを引き付けてもよい。例えば、液滴アクチュエータは、ビーズ除去のために規定される液滴アクチュエータの領域に強力な磁石を備えてもよい。磁石の力は、液滴アクチュエータのビーズ除去領域に移動される任意の液滴の外側に磁性ビーズを引き付けるように選択されてもよい。一部の場合において、ビーズの除去は効果的に不可逆的であってもよい。
【0170】
図46A、46B、および46Cは液滴アクチュエータの領域の上面図を示し、検体検出を改良するために、磁性反応ビーズを操作する方法および結果を示す。液滴アクチュエータ4600は、PCRなどの増幅反応などの核酸ベースのアッセイに必要とされる液滴操作を実施するように構成される液滴操作電極4610(例えばエレクトロウェッティング電極)の経路またはアレイを備えてもよい。特に、検出ウィンドウ4612は液滴操作表面に与えられる。検出ウィンドウ4612は特定の液滴操作電極4610Dに配置されてもよいか、あるいは液滴が、必要に応じて親水性表面または上部基板および/もしくは底部基板の形状のバリエーションなどの他の輸送機構を備える液滴操作電極を用いて輸送され得る領域であってもよい。液滴アクチュエータ4600は、液滴操作を介して液滴操作電極4610に沿って輸送され得るサンプル液滴4620を備えてもよい。サンプル液滴4620は、解析される標的核酸についての親和性を有する磁性反応ビーズ4624などの一定量のビーズを備えてもよい。
【0171】
図46Aにおいて示すように、ビーズ4624をその中に有するサンプル液滴4620が、検出ウィンドウ4612の領域内にある液滴操作電極4610Dに配置される。検出ウィンドウ4612は典型的に、サンプル液滴4620より小さい直径である。磁性反応ビーズ4624は、検出ウィンドウ4612によって占められる領域を含むサンプル液滴4620内に分散され、分散された読み取りおよびバックグラウンドノイズを生じる、検出装置(すなわち蛍光光度計)からの蛍光を遮断することによって、増幅シグナル、例えば蛍光色素の検出を妨げる場合がある。
【0172】
図46Bに示すように、磁石4630はサンプル液滴4620に近接して配置される。磁石4630は永久磁石または電磁石であってもよい。磁石4630は、サンプル液滴4620の実質的に端部で、かつ検出ウィンドウ4612から実質的に離れた位置に磁性反応ビーズ4624を引き付け、集めるのに十分な磁場を提供するために操作電極4610Dおよびサンプル液滴4620から一定の距離で配置される。一部の場合において、磁石4630によって与えられる磁場の強さは、ビーズ4624が密接な凝集を形成しないものであり、後の液滴操作において容易に再分配されてもよい。他の場合において、ビーズの除去が本質的に永続的であると意図される場合、凝集は問題ではない。
【0173】
図46Cに示すように、磁石4630は、サンプル液滴4620から磁性反応ビーズ4624を分離するために使用されてもよい。十分な数の熱サイクル反応(例えば約10サイクル)の後、PCR液滴の液相における増幅核酸の量は、磁性反応ビーズの非存在下で正確に検出されるのに十分な量であってもよい。液滴操作を用いて、サンプル液滴4620は、液滴操作を介して、磁石4630の磁場内および磁場外に輸送されてもよい。サンプル液滴4620が磁石4630から離れた位置に輸送される場合、ビーズ4626の集合は、液滴操作電極4610Mに配置されたままになる。ビーズ液滴4626の量は、十分に多い封入ビーズ4624であってもよい。ここで、サンプル液滴4620は磁性反応ビーズを実質的に含まず、蛍光検出はビーズ干渉物の非存在下で進行されてもよい。
【0174】
図46Dは、図46Bの方法(すなわち磁石によって凝集される磁性反応ビーズ)および図46Cの方法(磁性反応ビーズを含まないPCR液滴)を用いて熱サイクル反応から得られるリアルタイムPCRデータのプロットを示す。図46Dは、蛍光シグナルの検出の間の磁性反応ビーズの干渉から生じ得る検出シグナルにおける不安定性およびバックグランドノイズを示す。磁性反応ビーズが、例えば熱サイクル11(矢印で示す)で除去される場合、検出シグナルは十分に安定である。
【0175】
(7.13 極性蛍光色素分子)
核酸増幅方法は熱サイクルを使用する。すなわち、規定された一連の温度変化によってサンプルおよび増幅試薬を含む液滴を交互に加熱および冷却する。液滴アクチュエータベースの増幅(例えば電極によって媒介される液滴操作などの液滴操作を用いて実施されるPCR)において、温度制御素子(例えばペルチェユニット、加熱ブロック、冷却ユニットなど)が、液滴アクチュエータ表面上、または液滴アクチュエータ間隙内の充填流体の温度を制御するために使用されてもよい。しかしながら、熱サイクルに必要とされる高温は、蛍光増強が、検出法および検出色素として使用されるSybrGreenなどの蛍光色素(すなわち蛍光色素分子)として使用される場合、検出シグナルの損失を生じる場合がある。SYBR(登録商標)Green dyeなどの細胞透過性蛍光色素分子は、疎水性相(例えば油性充填流体)において十分な溶解性を有することができ、水性PCR液滴から充填流体に、特に熱サイクルの間に発生するものなどの高温で分配することができる。
【0176】
細胞透過性蛍光色素分子に対する代替として、極性または細胞不透過性蛍光色素分子が使用されてもよい。例えば、EVAGREEN(登録商標)極性蛍光色素分子が、蛍光検出シグナルを著しく損失せずにPCRに使用されてもよい。EVAGREEN(登録商標)極性蛍光色素分子(Biotium,Hayward,CAから入手可能)およびTO−PRO1などの多くの異なる極性蛍光色素分子が、増幅産物を検出するためにPCRに使用されてもよい。
【0177】
(7.14 不動態化)
核酸増幅は、反応液滴内に含まれる核酸テンプレート、オリゴヌクレオチドプライマー、試薬および酵素などの多くの異なる反応成分を含むいくつかの工程を必要とする。核酸、タンパク質(すなわち酵素)、および/または色素(例えば蛍光色素)などの増幅液滴のこれらの成分の多くは、基板表面(例えば液滴操作電極)上に吸収され得、および/または液滴アクチュエータの充填流体(例えば油性充填流体)内に分配され得る可能性がある。液滴アクチュエータの基板表面および/または充填流体に対するこれらの重要な成分の損失は、PCR反応の低減した効果および/またはPCR反応の失敗を生じる場合がある。一実施形態において、本発明は、物質がその物質を一緒に使用する前に他の物質に対して「不動態」となる表面安定化技術を提供する。本発明の表面安定化技術は、増幅液滴から液滴アクチュエータの表面までの重要な成分の損失を低減および/または取り除くことができる。
【0178】
不動態化試薬(すなわち遮断剤)は、基板表面に対する核酸テンプレートおよび/またはオリゴヌクレオチドプライマーの結合ならびに/あるいは充填流体含有の損失を減少および/または防ぐように選択されてもよい。実施例は、非標的DNA分子などの他の核酸分子および/またはさらなる量のオリゴヌクレオチドプライマーを含む。
【0179】
不動態化試薬(すなわち遮断剤)は、基板表面に対するタンパク質の結合および/または充填流体の損失を減少および/または防ぐように選択されてもよい。例としては、限定されないが、ポリビニルピロリドン(PVP)、ポリエチレングリコール(PEG)、トゥイーン(Tween)などの界面活性剤、およびウシ血清アルブミン(BSA)などの種々のポリマーが挙げられる。
【0180】
一例において、液滴アクチュエータの表面は、前処理液滴内に含まれる一定量の不動態化剤で前処理される。前処理液滴は、1つ以上の反応サイクルを介して液滴アクチュエータの1つ以上のPCR経路に沿って輸送されてもよい。前処理液滴がPCR経路内にサイクルされる場合、核酸、タンパク質(すなわち酵素)、および/または色素(例えば蛍光色素)などの不動態化剤が、基板表面(例えば液滴操作電極)上に吸着されてもよく、ならびに/あるいは充填流体(例えば油性充填流体)に分配されてもよく、PCR液滴内の成分の次の結合からの潜在的な吸収部位を効果的に飽和させる。別の例において、一定量の不動態化剤は、PCR液滴内に直接加えられてもよい(すなわち動的不動態化)。この例において、PCR液滴内の不動態化剤は、液滴アクチュエータの基板表面および/または充填流体上の利用可能な吸収部位に対して反応成分と効果的に競合し得る。
【0181】
(7.15 間隙の高さ)
PCRを実施するのに使用される液滴アクチュエータは、液滴操作間隙によって隔てられる底部基板および上部基板を備えてもよい。表面張力は温度の増加に伴い減少するため、表面張力が非常に低い場合、液滴は、高い温度で分裂または砕け得る。従って、室温で十分に作用することができる間隙の高さの構成は高温で作用しなくてもよい。なぜなら、表面張力は効果的に減少するからである。本発明は、この効果がより大きな間隙を用いることによって埋め合わされてもよいことが発見されている。表面張力(エネルギー)はより大きな間隙について同じであるが、領域はより大きいので、多くの総エネルギーが、砕くために液滴に必要とされる。典型的に、熱サイクルを実施するのに使用される液滴アクチュエータにおける液滴操作間隙の高さは約200μmであってもよい。しかしながら、非常に小さな間隙の高さは、熱サイクル領域の間に液滴を往復させるときなどの液滴操作の間に増幅液滴の分裂を生じる場合がある。PCR液滴の分裂は、標的核酸および試薬成分の損失を生じる場合がある。これらの重要な成分の損失は、増幅反応の実質的に低減した効果および/または増幅反応の失敗を生じる場合がある。
【0182】
液滴操作間隙の高さは、単一のサイズの電極および単一のサイズの液滴の量に対して選択されてもよく、それによって液滴は実質的に球形である。より低いアスペクト比の液滴は球形のサイズにより近く、より高いアスペクト比の液滴はよりディスク形状である。本発明者らは、ディスク形状の液滴が、液滴輸送、分配および分裂などの液滴操作に関してより低い電圧を必要とするが、それらはまた、より球状の液滴より容易に微小液滴を形成する傾向があることを発見した。実質的に球状の液滴は、同じ液滴操作に関してより高い電圧を必要とするが、それらは液滴操作の間に微小液滴を形成する傾向がより低い。高温に供される液滴を必要とするアッセイにおいて、微小液滴形成は増加する。一例において、本発明者らは、4:1または3:1の電極ピッチ:ギャップ高さ比(約1200μmの電極ピッチおよび約300μmまたは約400μmの液滴操作間隙の高さと等しい)が、微小液滴の形成を実質的に減少させることを見出した。
【0183】
本発明は、液滴操作の間の液滴の安定性(例えばPCR液滴の分裂を実質的に減少させる)を改良するために、高い間隙の高さを有する液滴アクチュエータを提供する。例えば、約320μm〜約350μmの液滴操作間隙の高さは、液滴操作を介して輸送されたPCR液滴の向上した安定性を提供する。
【0184】
一実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約250μmより大きい。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は、約250μm〜約500μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約275μm〜約450μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約300μm〜約400μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約320μm〜約375μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は、約320μm〜約350μmの範囲の高さを有する。
【0185】
一実施形態において、本発明は、約7:1〜約2.8:1の範囲の電極ピッチ:間隙の高さの比を有する液滴アクチュエータを提供する。別の実施形態において、本発明は、約6:1〜約3:1の範囲の電極ピッチ:間隙の高さの比を有する液滴アクチュエータを提供する。さらに別の実施形態において、本発明は、約4.3:1〜約3.4:1の範囲の電極ピッチ:間隙の高さの比を有する液滴アクチュエータを提供する。
【0186】
別の実施形態において、本発明は、約1200μmの電極ピッチおよび約175μm(約7:1のアスペクト比)〜約450μm(約2.8:1のアスペクト比)の範囲の液滴操作間隙の高さを有する液滴アクチュエータを提供する。さらに別の実施形態において、本発明は、約1200μmの電極ピッチおよび約200μm(約6:1のアスペクト比)〜約400μm(約3:1のアスペクト比)の範囲の液滴操作間隙の高さを有する液滴アクチュエータを提供する。さらに別の実施形態において、本発明は、約1200μmの電極ピッチおよび約280μm(4.3:1)〜約350μm(3.4:1)の範囲の液滴操作間隙の高さを有する液滴アクチュエータを提供する。
【0187】
液滴アクチュエータにおける間隙の高さは、例えば、低部と上部の液滴アクチュエータ表面間に適切な厚さのスペーサー材料を「挟み込むこと」によって制御されてもよい。あるいは、材料の層は、2つの基板の少なくとも一部の間に適切な厚さの間隙空間を規定する絶縁材を提供するように上部または低部の基板のいずれかの内面に接着されてもよい。あるいは、絶縁材は1つまたは両方の基板の一体部分、射出成形または他の形成プロセスの間に、基板に成形または形成される例えば突起柱または他の構造であってもよい。所望の高いアスペクト比を達成するための間隙の高さを制御する種々のさらなる手段は当業者に容易に理解されるだろう。
【0188】
(7.16 キャリーオーバー汚染の減少)
液滴アクチュエータでの液滴ベースの核酸増幅は、熱反応領域と検出器との間で電極によって媒介される液滴操作を用いて増幅準備液滴が往復される、一連の液滴操作を含む。このプロセスが共通の経路または近接する経路に沿う複数の液滴の移動に関する場合、増幅液滴からの残留成分は、1つの液滴から別の液滴に移動する場合があり、一連の液滴操作におけるその後の増幅液滴を汚染する。本発明は、油内の増幅液滴を使用する増幅液滴の間の二次汚染を減少させるための液滴アクチュエータおよび方法を提供する。
【0189】
本発明の液滴アクチュエータは、液滴操作間隙によって分離される底部基板と上部基板とを備えてもよい。液滴アクチュエータの指定された領域において、液滴操作間隙は、油状の充填流体などの流動性の充填流体を含んでもよい。液滴アクチュエータの他の指定された領域において、液滴操作間隙間は空気などの気体状の充填流体を充填されてもよい。
【0190】
油に囲まれた液滴は、例えば、油でサンプルリザーバーを充填し、続いてリザーバーに水性サンプル、例えばPCRサンプルを負荷し、油層に囲まれる水性PCR液滴を分配または「ピンチオフ(pinch off)」するために液滴操作を用いることによって形成されてもよい。油に囲まれたPCR液滴の形成を促進するために、高い表面張力を有する高粘性油が使用されてもよい。適切な油の例としては、限定されないが、ヘプタデカンまたはオクタデカン油が挙げられる。油に囲まれたPCR液滴が分配される場合、それは、その後のPCR反応のために液滴操作を用いて、油を含まない液滴アクチュエータの領域(すなわち間隙が空気に充填されている)に輸送されてもよい。
【0191】
高粘性油は室温(すなわち約22℃〜28℃)で部分的な固体または固体であってもよい。例えば、ヘプタデカン、オクタデカン、ノナデカン、およびエイコサン油の融点は、それぞれ、20〜22℃、26〜29℃、30〜34℃および35〜37℃である。液滴アクチュエータベースの増幅に関して、オイルは異なる増幅のためにその融点に基づいて選択されてもよい。例えば、液滴アクチュエータの輸送が必要とされる製造観点から、リザーバーは、選択される油の融点以上の温度で油を充填され、次いで液滴アクチュエータにおいて冷却および凝固させてもよい。液滴アクチュエータベースのPCRは典型的に、約60℃以上で操作するため、選択される油は液相内にあり、油で囲まれたPCR液滴の形成が可能になる。
【0192】
(7.17 標的核酸の濃縮および収集)
液滴アクチュエータベースの核酸増幅の一部の適用において、PCR解析の前にサンプル流体中の検体(例えば細菌、ウイルス、真菌、および/または核酸)を濃縮することが必要な場合がある。例えば、最適な解析を与えるために、サンプル流体の量は非常に多く、および/または検体の濃度は非常に小さくてもよい。
【0193】
図47Aおよび図47Iは、液滴アクチュエータ4700の領域の断面図を示し、核酸増幅および検出のためのサンプル流体由来の標的核酸の濃縮および収集プロセスにおける磁性反応捕捉ビーズの使用を示す。
【0194】
図47Aに示されるように、検出アクチュエータ4700は底基板4710を備え得る。底部基板4710は、液滴操作間隙4716によって上部基板4714から分離されてもよい。リザーバー電極4718は底部基板4710上に配置されてもよい。リザーバー電極4718は、液滴操作電極4720(例えばエレクトロウェッティング電極)の経路またはアレイと結合して配置されてもよく、それによって、液滴は、液滴操作電極4720の経路またはアレイ上にリザーバー電極4718から配置されてもよい。誘電体が電極を覆ってもよい。疎水性層が電極を覆ってもよい(または疎水性誘電体が選択されてもよい)。リザーバー4730は、電極が液体経路を通して流される液体と相互作用できるように、リザーバー4730から間隙4716への液体経路を規定し、リザーバー電極4718に十分に近接する上部基板4714に設けられる。リザーバー4730は、例えば約1ミリリットル(ml)以上のサンプル流体を含むのに十分なサイズであってもよい。リザーバー4730は一定量の磁性反応捕捉ビーズ4734を含む。磁性反応捕捉ビーズ4734は、例えば、一次捕捉抗体、またはオリゴヌクレオチド配列、あるいは結合および捕捉事象を与える特異的標的検体に対する親和性を有する任意の結合タンパク質を含むビーズであってもよい。リザーバー4730は隔壁4738によって密閉される。隔壁4738は、望まれない物質によるリザーバー4730の汚染に対する障壁を与える。
【0195】
磁石4740は液滴アクチュエータ4700に結合される。磁石は、リザーバー電極4718が磁石4740の磁場内にあるように配置される。例えば、磁場4740は永久磁石または電磁石であってもよい。一例において、磁石4740は、リザーバー電極4718の近接内、またはリザーバー電極4718から離れた位置に移動され得るように位置が調節される永久磁石である。磁石4740は、例えば、磁性反応捕捉ビーズ4734を引き付けおよび/または固定するように使用されてもよい。操作において、磁石4740は、磁性反応捕捉ビーズ4734に結合される標的検体を濃縮するプロセスを補助するように使用されてもよい。
【0196】
超音波処理器4742は液滴アクチュエータ4700に結合される。超音波処理器4742は、流体内の粒子を攪拌するために、音波エネルギー(例えば超音波)をリザーバー4730内のサンプル流体に与えるように使用されてもよい。別の例において、超音波処理器4742はサンプル流体内の粒子を穏やかに攪拌し、再懸濁するために使用されてもよい。別の例において、超音波処理器4742はサンプル流体内の粒子を激しく攪拌するために使用されてもよい。一部の適用において、強力な超音波処理が、細胞膜を破壊し、細胞内容物を放出するために使用されてもよい。さらに、リザーバー4730に対する超音波処理器4742の位置は変化させてもよい。
【0197】
第2の磁石4744は液滴アクチュエータ4700に結合される。磁石4744は、例えば、永久磁石または電磁石であってもよい。磁石4744は、1つ以上の液滴操作電極4720が磁石4744の磁場内にあるように配置される。磁石4744は、さらに標的核酸を濃縮および精製するために、例えば、磁性反応ビーズを用いて第2の捕捉事象に磁場を与えるように使用されてもよい。
【0198】
サンプル流体由来の標的核酸を濃縮および収集するために、磁性反応捕捉ビーズを用いるプロセスの例としては、限定されないが、以下の工程が挙げられる。
【0199】
図47Bは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける第1の工程を示す。この工程において、負荷装置4750(例えば、シリンジおよびニードル、マイクロピペット)は、一定量のサンプル流体4752をリザーバー4730に入れておくために使用される。サンプル流体4752は、例えば、約1ml以上の体積の血液サンプルまたは鼻咽頭洗浄サンプルであってもよい。サンプル流体4752は一定量の標的検体4754を含んでもよい。標的検体4754は、例えば、磁性反応捕捉ビーズ4734に対する親和性を有する細菌、ウイルス、および/または真菌標的物であってもよい。リザーバー電極4718は活性化されず、磁石4740の一部は、実質的にリザーバー電極4718に存在する磁場がないため、サンプル流体4752はリザーバー4730に保持される。
【0200】
図47Cは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、超音波処理器4742は、活性化(例えば低エネルギー操作)され、穏やかに攪拌するために使用され、サンプル流体4752中の磁性反応捕捉ビーズ4734を再懸濁する。超音波処理器4742は、磁性反応捕捉ビーズ4734に対する標的検体4754の最適な混合および結合(すなわち一次捕捉)を与えるために、十分な時間、活性化されてもよい。
【0201】
図47Dは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、超音波処理器4742はスイッチが切られ、磁石4740の位置は、液滴アクチュエータ4700のリザーバー4718に特定の磁場が存在し、リザーバー電極4718が活性化されるようにある。リザーバー電極4718の磁場および活性化の結果として、結合された標的検体4754を含む磁性反応捕捉ビーズ4734がリザーバー4718に定着し、サンプル流体4752内で効果的に濃縮する。
【0202】
図47Eは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、磁石4740は液滴アクチュエータ4700から離れた位置に物理的に移動され、その結果、リザーバー電極4718に実質的に磁場は存在しない。磁場の除去の結果として、磁性反応捕捉ビーズ4734はリザーバー電極4718の表面に長く固定されず、間隙4716内のサンプル体積に分配される。この例において、標的検体4754が、例えば細菌、ウイルスおよび/または真菌である場合、溶解試薬液滴4756が輸送され、液滴操作を用いて間隙4716内でサンプル体積と融合される。1つ以上の溶解試薬液滴4756が、標的検体4754の十分な溶解および標的核酸の放出を提供するために使用されてもよい。
【0203】
図47Fは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、超音波処理器4742は活性化されるリザーバー4718の近接に物理的に移動される。超音波処理器4742は活性化され(例えば高エネルギー操作)、激しく攪拌し、サンプル流体4752を混合するために使用される。超音波処理器4742は、標的検体4754の最適な溶解および核酸の放出を提供するのに十分な時間、活性化されてもよい。別の実施形態において、単一の超音波処理器は、液滴操作間隙における液滴およびリザーバー内の流体の同時超音波処理を可能にする方法で戦略的に配置されてもよい。さらに別の実施形態において、1つより多い超音波処理器が設けられてもよい。
【0204】
一例において、化学試薬および/または酵素溶解試薬(すなわち溶解試薬液滴4756)と組み合わせた強力な超音波処理が、真菌病原体を含む生物学的サンプルに有用であり得る。
【0205】
図47Gは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、磁石4740の位置は、液滴アクチュエータ4700のリザーバー電極4718に特定の磁場が存在するような位置である。磁場の結果として、結合される標的検体4754を有する磁性反応捕捉ビーズ4734はリザーバー電極4718に定着される。標的検体4754は溶解されるため、核酸はサンプル流体4752に放出される。一定量の標的核酸4760(例えばDNAまたはRNA)を含む1つ以上の溶解液滴4758は、液滴操作を用いて、磁石4744に対して液滴操作電極4720の経路に沿ってリザーバー電極4718から離れた位置に輸送される。
【0206】
図47Hは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、一定量の磁性反応捕捉ビーズ4764を含む捕捉液滴4762は、液滴操作を用いて第2の磁石4744に配置される。捕捉ビーズ4764は、溶解液滴4758中の捕捉標的核酸4760をアニールするために使用される一定量のオリゴヌクレオチド配列を含む。液滴操作を用いて、1つ以上の溶解液滴4758は、捕捉液滴4762に輸送され、融合される。この工程において、標的核酸4760はさらに濃縮され、精製される。
【0207】
図47Iは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、捕捉液滴4762は、未結合の物質を除去するために一連の液滴操作を用いて洗浄される。捕捉液滴4762中の結合された核酸4760は、ここでPCR用に準備される。
【0208】
別の実施形態において、標的検体4754が核酸である場合、溶解工程(すなわち図47Eおよび47F)は必要でなくてもよい。
【0209】
(7.18 サンプル)
本発明の種々の実施形態において、本発明は核酸サンプルを使用する。核酸サンプルは、標的分子、細胞または生物などの標的物質に直接または間接的に結合される標的核酸または核酸を少なくとも潜在的に含むサンプルである。特定の実施形態において、核酸サンプルはサブサンプルに細分化されてもよい。例えば、サブサンプル液滴はサンプル液滴から液滴操作を用いて分配されてもよい。
【0210】
個々のサブサンプルは、一連のエンドポイント測定を生成するための所定数のサイクルのために増幅されてもよい。エンドポイント測定は、特定の所定数の増幅サイクルの後、または終わりに得られるサブサンプル(および/またはサブサンプルのセット)の各々の測定を含んでもよい。異なるサブサンプルのエンドポイント測定は、生物サンプルに存在する標的核酸を定量化するために使用され得る曲線を生成するために使用されてもよい。例えば、異なるサブサンプル液滴のエンドポイント測定は、サンプル液滴、またはサンプル液滴が誘導されるオリジナルのサンプルに存在する標的核酸を定量化するために使用され得る曲線を生成するために使用されてもよい。
【0211】
核酸サンプルは、対象物、コントロール、標準物または複製物由来のサンプルであってもよい。核酸は、目的の実際の検体である標的分子などの別の物質に結合されてもよい。種々の実施形態において、プロトコルは、1つ以上の対象物のサンプル由来の物質の増幅、ならびに1つ以上のコントロールおよび/または複製物の増幅を含んでもよい。特定の実施形態において、特定のサブサンプルは、単一のデータポイントのみを生成するために使用される。他の実施形態において、複数の同一のサブサンプル液滴は、増幅サイクルの数の関数として検出される増幅シグナルの量を示す一連のデータポイントを生成するように異なって増幅されてもよい。
【0212】
核酸サンプルは、例えば、空気サンプル、水サンプル、土壌サンプルなどの環境サンプル;髪の毛のサンプル、皮膚細胞、および他の法医学的残留物などの法医学サンプル;ならびに全血、リンパ液、血清、血漿、汗、涙、唾液、痰、脳脊髄液、羊膜液、精液、膣分泌物、漿液、滑液、心膜液、腹膜液、胸膜液、浸出液、滲出液、嚢胞液、胆液、尿、胃液、腸液、糞便試料、単細胞および多細胞を含む液体、細胞小器官を含む液体、流動組織、流動器官、多細胞生物を含む液体、生物学的スワブまたは洗浄物などの他の生物学的サンプル由来であってもよい。
【0213】
(7.19 検出)
増幅を検出するための種々のアプローチが本発明の実施に使用されてもよい。例えば、一実施形態において、各サブサンプル液滴は所定の波長で蛍光強度測定に供される。一実施形態において、検出は増幅反応と同時に達成される。言い換えれば、複数のサブサンプル液滴が増幅される間、各サブサンプル液滴はその所定数のサイクルを達成するため、検出に供されてもよい。1つの液滴が検出に供されている間、他の液滴は増幅され続けてもよい。特定の実施形態において、液滴のグループがほぼ同時に達成され、各n回のサイクル後に、少なくとも1つの液滴が検出に供される。各検出工程の間のサイクルの数は、特定のアッセイに必要なデータに基づいて選択されてもよい。一般に、より正確な定量化は、多数または少数の全増幅サイクルの検出を必要とする。
【0214】
検出は、サブサンプル液滴が利用可能になると、すなわち、所定数のサイクルが完了すると、ほぼ達成され得る。サブサンプル液滴は所定の位置で試験されてもよいか、または後の検出のために他の場所に輸送もしくは移動されてもよい。後のアプローチは、増幅と検出の機能を分けるのに有用であり得る。例えば、サブサンプル液滴は、液滴アクチュエータ上の他の場所に輸送され、それらが検出を待っている間、滞留されてもよい。サブサンプル液滴が検出のために準備されている場合、センサが、液滴が各液滴を測定するために滞留される領域を走査してもよい。あるいは、サブサンプル液滴は、検出のためのセンサの存在下で一定の時間に1つ以上輸送されてもよい。例えば、各サブサンプル液滴は、検出ウィンドウを通して輸送されてもよく、測定は、各液滴が検出ウィンドウに存在している間、その各液滴についてセンサによって得られてもよい。
【0215】
液滴は種々の技術を用いて検出に供されてもよい。一実施形態において、液滴は検出の存在下で輸送されてもよい。この実施形態において、1つ以上の固定センサが、検出を達成するために使用されてもよい。このような構成は機器のコストおよび複雑性を減少させる。別の実施形態において、センサは検出のための液滴の存在下で移動される。液滴は、後の時間での検出のために液滴アクチュエータに配置されてもよいか、液滴アクチュエータから除去されてもよい。配置された液滴はセンサによって走査されてもよいか、または画像化されてもよい。例えば、配置された液滴は、CCDまたはLED/フォトダイオードアレイなどのアレイ検出器によって画像化されてもよい。液滴は、CCDもしくはLED/フォトダイオードアレイの存在下で移動されてもよく、および/またはCCDもしくはLED/フォトダイオードアレイは、液滴の存在下で移動されてもよい。
【0216】
すでに述べたように、特定の実施形態において、検出における増幅は分けられてもよい。この利点は、経時的な同じ反応の複数の測定よりむしろ、複数のエンドポイント反応の使用によって促進される。このアプローチはまた、検出前であるが増幅後の検出試薬の添加を促進する。熱サイクルおよび検出の分離は、核酸増幅を実施できる液滴アクチュエータを設計する場合、より大きな設計の柔軟性を提供する。
【0217】
種々の実施形態において、検出試薬は、検出前または間であるが、増幅後に各サブサンプル液滴に加えられる。例えば、挿入色素(SYBR Green)および/または分子指標を含む液滴が、増幅後にサブサンプル液滴に加えられてもよい。この実施形態は、増幅が完了した後に試薬が加えられるため、増幅を阻害できる試薬の使用を促進する。試薬は、検出前または間に加えられてもよい。別の実施形態において、増幅サイクルの一部は、検出試薬の検出前に実施されてもよい。言い換えれば、検出試薬は、1つ以上の最後のサイクルの間または前に加えられてもよい。このアプローチは、Taqman(r)試薬などの、重合の間に存在する検出試薬を必要とする化学物質を検出するのに有用であり得る。
【0218】
示されるように、増幅および検出の分離は、検出アクチュエータおよび液滴アクチュエータを操作するのに必要とされる機器についての設計の柔軟性を改良する。例えば、検出器モジュールおよび加熱器モジュールは、それらのそれぞれの機能を実施する位置を交換することができる。このアプローチは、加熱器が検出を妨げずに液滴アクチュエータの両側に配置されることを可能にする。別の例において、分離面が熱サイクルおよび検出のために設けられてもよい。
【0219】
検出は数秒で達成され得るが、熱サイクルは数分〜1時間までを必要とする場合がある。従って、1つの検出機器は、複数の液滴アクチュエータで熱サイクルを制御するために使用される機器において複数の熱サイクルまたは熱サイクルのブランクを支持するために使用されてもよい。例えば、機器は、熱サイクルのための複数のスロット、および検出のための1つまたは少数のスロットのみを有するように設けられてもよい。液滴アクチュエータは、使用者、ロボット手段または他の手段によってスロットを検出するために熱サイクルスロットから移動されてもよい。
【0220】
液滴が検出のために準備されている場合、それらは、使用される検出の形態に適切な任意の方法で配置されてもよい。例えば、それらは、単一のファイルに並べられてもよいか、または密度の濃いアレイにパッケージされてもよい。検出のための空間および構成は、熱サイクルの必要性によって抑制されない。液滴を密な1−Dアレイに配置する能力により、走査検出器のコストおよび複雑性が減少する。センサについての全移動は、直線状で、1軸の方向のみに低減され得る。同様に、より小さいCCDまたはLED/フォトダイオードアレイが使用されてもよい。
【0221】
他の設計の利点は、熱サイクルおよび検出についての異なる必要性から生じる。例えば、光透過性が検出の一部の形態に必要とされてもよいが、特定の熱サイクルの構成に必要とされなくてもよい。熱特性は液滴アクチュエータの熱サイクル領域について最適化されてもよいが、光学特性は液滴アクチュエータの検出領域に最適化されてもよい。さらに、本発明の液滴アクチュエータは、後の時間に再試験するために液滴アレイを保存するために使用されてもよい。
【0222】
他の利点の中で、本発明の熱サイクル技術は、増幅の間、液滴に存在する結合剤などの検出剤を必要とせずに液滴の増幅を促進する。示されるように、一部の場合において、小液滴は熱サイクルを受ける液滴から分配されてもよい。小液滴は熱サイクルプロセスから出ていってもよく、適切な検出試薬と混合され、次いで検出に供されてもよい。本明細書に記載されるエンドポイント検出スキームもまた、この技術を利用してもよい。各小液滴は、熱サイクルプロセスの完了後に結合剤を含む液滴と混合されてもよい。
【0223】
特定の実施形態において、本発明の方法は、サンプルおよび結合剤を一緒に含む増幅反応混合物の熱サイクルを省略する。特定の実施形態において、本発明の技術は、特に、増幅反応が進行中の間に、蛍光シグナルを検出するために操作される検出器を除外してもよい。
【0224】
種々の実施形態において、検出剤が熱サイクルの後に加えられる場合、他に核酸増幅を妨げる薬剤が利用されてもよい。例えば、増幅の間に存在する場合、熱サイクルを阻害する結合剤が、その結合剤が増幅後に加えられる本発明の技術に使用されてもよい。従って、特定の実施形態において、本発明は、核酸増幅の速度および増幅のための試薬を特異的に阻害する結合剤を利用する。
【0225】
他の実施形態において、検出は標識ヌクレオチドを用いて達成されてもよい。テンプレートはビーズに結合され、蛍光ヌクレオチドなどの標識ヌクレオチドを用いて増幅されてもよい。標識ヌクレオチドは増幅鎖に導入されてもよく、検出は、(a)液滴からの標識核酸の喪失、および/または(b)標識核酸の増幅鎖への導入に基づいてもよい。特定の実施形態において、「Droplet−based Surface Modification and Washing」という発明の名称の米国特許第7,439,014号に記載されるものなどのビーズ洗浄技術が、増幅鎖に導入される標識ヌクレオチドの検出のために未結合の標識ヌクレオチドから離れて洗浄するために使用されてもよい。この技術は、内部蛍光を有する捕捉ビーズとともに蛍光ヌクレオチドを用いることによって高められてもよく、ビーズは蛍光ヌクレオチドの蛍光を増幅する。
【0226】
さらに別の実施形態において、DNA合成は、ピロリン酸塩の生成に基づいて測定されてもよい。各サイクルにて、デオキシトリヌクレオチドの導入は、ピロリン酸塩の分子を遊離させる。遊離されるピロリン酸塩の量は、単位複製配列の長さマイナスプライマーの長さに比例する。各サイクルの終わりに、化学的方法がピロリン酸塩を検出するために使用されてもよい。一部の場合において、小液滴は、熱サイクルを受け、ピロリン酸塩遊離についての試験に供される液滴から分配されてもよい。小液滴は、熱サイクルプロセスから出ていき、ピロリン酸塩検出プロトコルに供されてもよい。
【0227】
本明細書に記載されるエンドポイント検出スキームはまた、この技術を利用してもよい。液滴は、熱サイクルプロセスの完了後にピロリン酸塩検出プロトコルに供されてもよい。いずれの場合においても、ピロリン酸塩検出プロトコルは、2007年、10月25日に公開された「Droplet−Based Pyrosequencing」という発明の名称の国際公開第2007/120240号に記載されるものなどの液滴操作を用いて達成されてもよい。
【0228】
本明細書に記載される種々の検出アプローチは、通常、以下に記載される任意の実施形態とともに使用されてもよいことは理解されるだろう。
【0229】
(7.20 加熱バー)
本明細書に記載され、図48Aおよび48Bに示されるように、加熱バー4800は、十分な熱伝導率のために、アルミニウムバー4802などのアルミニウムから構成されてもよい。2つの抵抗器4804(各々15Ω)は、均一な加熱を与えるように底側の2つの端部に取り付けられる。サーミスタプローブ4806は、加熱器PID制御因子に温度測定を与えるために加熱バーの中央に取り付けられてもよい。加熱バーは、位置決めねじ4810を用いてカートリッジデッキ4808に配置され、下部のスプリング4812によって支持されてもよい。スプリング力は、加熱バー表面と加熱されるPCBカートリッジ4814との間の密な接触を確実にする。スプリングにより留められた加熱バーはカートリッジデッキに接触せず、デッキに移動される望まれない加熱器は最小化される。
【0230】
(7.21 システム)
当業者によって理解されるように、本発明は、方法、システムまたはコンピュータープログラム製品として具現化されてもよい。従って、本発明の種々の態様は、ハードウェア実施形態、ソフトウェア実施形態(ファームウェア、常駐ソフトウェア、マイクロコードなどを含む)、または「回路」、「モジュール」もしくは「システム」として本明細書においてほぼ全て参照され得るソフトウェアおよびハードウェアの態様を組み合わせた実施形態の形態をとってもよい。さらに、本発明の方法は、媒体において具現化されるコンピューターにより使用可能なプログラムコードを有するコンピューターにより使用可能な記録媒体上でコンピュータープログラム製品の形態をとってもよい。
【0231】
任意の適切なコンピューターにより使用可能な媒体は、本発明のソフトウェアの態様で利用されてもよい。コンピューターにより使用可能またはコンピューターにより読み取り可能な媒体は、例えば限定されないが、電子、磁気、光学、電磁気、赤外線、または半導体のシステム、装置、デバイス、または伝搬媒質であり得る。コンピューターにより読み取り可能な媒体のより具体的な例(限定的なリスト)としては、以下の一部または全てが挙げられる:1つ以上のワイヤを有する電気的接続、携帯型フロッピー(登録商標)ディスク、ハードディスク、ランダムアクセスメモリ(RAM)、リードオンリメモリ(ROM)、消去可能なプログラム可能なリードオンリメモリ(EPROMまたはフラッシュメモリ)、光ファイバー、携帯型コンパクトディスクリードオンリメモリ(CD−ROM)、光学式記憶デバイス、インターネットもしくはイントラネットをサポートするものなどの伝送媒体、または磁気記憶デバイス。コンピューターにより使用可能またはコンピューターにより読み取り可能な媒体はさらに、紙または別の適切な媒体であってもよく、例えば紙または他の媒体の光学走査によって、プログラムが電子的に捕捉され得るように、その上にプログラムがプリントされ、次いで、必要な場合、適切な方法でコンパイル、読み取り、または処理され、次いで、コンピューターメモリに保存されることに留意すべきである。この文書の文脈において、コンピューターにより使用可能またはコンピューターにより読み取り可能な媒体は、命令実行システム、装置、もしくはデバイスによって、またはそれらと併せて使用するためのプログラムを含有し、保存し、通信し、伝播し、または輸送できる任意の媒体であってもよい。
【0232】
本発明の操作を実行するためのコンピュータープログラムコードは、Java(登録商標)、Smalltalk、C++などのオブジェクト指向のプログラミング言語で書かれてもよい。しかし、本発明の操作を実行するためのコンピュータープログラムコードはまた、「C」プログラミング言語または同様のプログラミング言語などの従来の手続きプログラミング言語で書かれてもよい。プログラムコードは、使用者のコンピューター上で部分的に、リモートコンピューターで部分的に、またはリモーターコンピューターもしくはサーバーで完全に、スタンドアロンソフトウェアパッケージとして、使用者のコンピューター上で完全に、または使用者のコンピューター上で部分的に実行できる。後者の状況において、リモートコンピューターは、ローカルエリアネットワーク(LAN)または広域ネットワーク(WAN)を介して使用者のコンピューターに接続されてもよいか、その接続は外部コンピューターに対してなされてもよい(例えば、インターネットサービスプロバイダーを使用するインターネットを介して)。
【0233】
本発明の特定の態様は、種々の方法および方法の工程に対する参照とともに記載される。各方法の工程は、コンピュータープログラム命令によって実行され得ることは理解されるだろう。これらのコンピュータープログラム命令は、機械を生成するために、汎用コンピューター、専用コンピューター、または他のプログラム可能なデータプロセス装置のプロセッサに与えられてもよく、それによって、コンピューターまたは他のプログラム可能なデータプロセス装置のプロセッサを介して実行する命令は、この方法で指定される機能/作用を実行するための手段を作成する。
【0234】
コンピュータープログラム命令はまた、特定の方法で機能するように、コンピューターまたは他のプログラム可能なデータプロセス装置を指示し得るコンピューター読み取り可能メモリに保存されてもよく、それによって、コンピューター読み取り可能メモリに保存される命令は、この方法の工程の様々な態様を実行する命令手段を含む製造物品を生成する。
【0235】
コンピュータープログラム命令はまた、コンピューターまたは他のプログラム可能なデータプロセス装置にロードされて、コンピューターにより実行されるプロセスを生成するためにコンピューターまたは他のプログラム可能な装置で実施されるべき一連の操作工程を生じることができ、それによって、コンピューターまたは他のプログラム可能な装置で実行する命令は、本発明の方法において指定される様々な機能/作用を実行するための工程を提供する。
【0236】
(8 結びの見解)
上述の実施形態の詳細な説明は、本発明の特定の実施形態を例示する添付の図面を参照する。異なる構造および操作を有する他の実施形態も本発明の範囲から逸脱しない。用語「本発明」などは、本明細書に記載される本出願人の発明の多くの代替の工程または実施形態の特定の具体例に対する参照とともに使用され、その使用が存在してもしなくても、本出願人の発明の範囲または特許請求の範囲を限定することを意図しない。本明細書は、読み手のみの簡便さのためにセクションに分けられる。見出しは本発明の範囲を限定すると解釈されるべきではない。その定義は本発明の詳細の一部と意図される。本発明の様々な詳細は、本発明の範囲から逸脱せずに変更されてもよいことは理解されるだろう。さらに、上述の詳細は例示のみの目的のためであり、限定を目的とせず、本発明は添付の特許請求の範囲によって定義される。
【技術分野】
【0001】
(1.関連出願)
本出願は、2008年10月28日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/108,880号、2008年11月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/115,654号、2009年2月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/153,598号、2008年5月13日に出願された「Reducing Droplet Cross−contamination in a Droplet Actuator」という発明の名称の米国特許出願第61/052,885号、2008年9月22日に出願された「Reducing Droplet Cross−contamination in a Droplet Actuator」という発明の名称の米国特許出願第61/098,860号、2009年3月16日に出願された「Reducing Droplet Cross−contamination in a Droplet Actuator」という発明の名称の米国特許出願第61/160,607号、2008年10月7日に出願された「Nucleic Acid Handling on a Droplet Actuator」という発明の名称の米国特許出願第61/103,332号、2008年12月31日に出願された「Sample Preparation and Assay Execution on a Droplet Actuator」という発明の名称の米国特許出願第61/141,820号に対する優先権を主張し、これらの出願の各々の全開示は参照として本明細書に援用される。
【0002】
(2.政府の利益)
本発明は、米国の国立衛生研究所によって与えられたAI065169−01およびAI066590−02のもとで、政府の支援によってなされたものである。米国政府は、本発明において特定の権利を有する。
【0003】
AI065169−01のもとの政府の支援に関する上述の声明は、2008年10月28日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/108,880号、2008年11月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/115,654号、2009年2月18日に出願された「Droplet Thermal Cycling Techniques」という発明の名称の米国特許出願第61/153,598号に起因する本出願において記載され、特許請求される本発明のこれらの態様のみに適用し、AI066590−02のもとの政府の支援に関する上述の声明は、2008年10月7日に出願された「Nucleic Acid Handling on a Droplet Actuator」という発明の名称の米国特許出願第61/103,332号、2008年12月31日に出願された「Sample Preparation and Assay Execution on a Droplet Actuator」という発明の名称の米国特許出願第61/141,820号に起因する本出願において記載され、特許請求される本発明のこれらの態様のみに適用する。
【0004】
本発明は、液滴アクチュエータ装置、システム、および方法に関する。
【背景技術】
【0005】
(3.背景)
液滴アクチュエータは、多種多様の液滴操作を実施するために使用される。液滴アクチュエータは、典型的に、液滴操作間隙によって隔てられる2つの基板を備える。基板は、液滴操作を実施するための電極を備える。基板間の液滴操作間隙は、典型的に、液滴操作に供される流体と混ざらない流動性の充填流体で満たされる。液滴操作は、基板の1つまたは両方と結合する電極によって制御される。液滴の成分は、一部の場合において、充填流体中の液滴から出ていくことがある。充填流体からのそのような成分は他の液滴を汚染する場合がある。
【発明の概要】
【発明が解決しようとする課題】
【0006】
本発明は、流動性の充填流体を介して液滴アクチュエータ上のある液滴から別の液滴への汚染の移動を減少または除去するための特定の新規のアプローチに関する。1つの適用において、液滴アクチュエータは、ポリメラーゼ連鎖反応(PCR)技術を用いて遺伝子解析を実施するために使用される。標的サンプルの最適な増幅および検出を提供する液滴アクチュエータ上でPCRを実施する改良された方法についての必要性が存在する。
【課題を解決するための手段】
【0007】
(4 本発明の詳細な説明)
本発明は、サンプル中の標的核酸を増幅および/または検出する方法を提供する。その方法は、核酸増幅反応液滴のセットを提供する工程を含んでもよい。各液滴はサンプルの一部を含んでもよい。その方法は、標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理して、増幅核酸を有する増幅液滴の対応するサブセットを得る工程を含んでもよい。増幅反応液滴の各サブセットは、1つ以上の増幅反応液滴を含んでもよい。増幅反応液滴の各サブセットは、標的核酸を増幅するための異なる条件下で処理されてもよい。その方法は、検出するための増幅液滴を調製する工程を含んでもよい。その方法は、増幅液滴からシグナルを検出する工程を含んでもよい。その方法はまた、増幅液滴および/またはサンプルに存在する増幅核酸の量および/または識別を決定する工程を含んでもよい。核酸増幅反応液滴のセットを提供する工程は、サンプル液滴から核酸増幅液滴のセットを分配する工程を含んでもよい。サンプル液滴は、液滴アクチュエータの液滴操作間隙に提供されてもよく、分配は電極により媒介されてもよい。サンプル液滴は、液滴アクチュエータのリザーバーに提供されてもよい。液滴アクチュエータは、リザーバーから液滴操作間隙内への液体経路を備えてもよい。核酸増幅液滴のセットを分配する工程は、液体経路を通して液滴操作間隙内にサンプル液滴を流動させる工程、および液滴操作間隙中に増幅反応液滴を分配するために電極を使用する工程を含んでもよい。核酸増幅反応液滴のセットを提供する工程は、サンプル液滴を提供する工程と、サンプル液滴を複数のサンプル小液滴に分裂する工程と、各サンプル小液滴と、増幅試薬を含み得る1つ以上の液滴とを混合して、増幅反応液滴を生じる工程とを含んでもよい。本明細書に記載される方法の任意の1つ以上の工程は、電極によって媒介される液滴操作を用いて液滴アクチュエータの液滴操作間隙中で行われてもよい。本明細書に記載される方法の任意の1つ以上の工程は、電極によって媒介される液滴操作を用いて行われてもよい。サンプル液滴、複数の小液滴および1つ以上の液滴は、増幅試薬を含んでもよい。増幅反応液滴は、液滴操作間隙に配置され、少なくとも部分的に流動性の充填流体によって囲まれてもよい。核酸増幅反応液滴のセットを提供する工程は、以下の工程を含んでもよい:サンプル液滴を提供する工程;サンプル液滴と、増幅試薬を含み得る1つ以上の液滴とを混合して、増幅準備液滴を生じる工程;および増幅準備液滴を分裂して、増幅反応液滴を生じる工程。サンプル液滴、1つ以上の液滴は、増幅試薬、親増幅反応液滴を含んでもよく、増幅反応液滴は、液滴アクチュエータの液滴操作間隙に配置されてもよく、流動性の充填流体に少なくとも部分的に囲まれてもよい。その方法は、標的核酸がサンプル中に存在する場合、各増幅反応液滴が標的核酸を含むことを確実にするために増幅準備液滴中で十分に増幅された核酸を得るために選択される条件下で増幅準備液滴を処理する工程を含んでもよい。増幅準備液滴を処理する工程は、1〜50サイクル、1〜40サイクル、1〜30サイクル、1〜20サイクル、または1〜10サイクル、または1〜5サイクルについて増幅準備液滴を熱サイクルすることを含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、液滴アクチュエータの液滴操作間隙中の複数の電極経路に沿って液滴を輸送することによって2つ以上の熱領域の間で増幅反応液滴をサイクルする工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、液滴アクチュエータの液滴操作間隙内の共通の電極経路に沿って各サブセットにおける液滴を輸送することによって2つ以上の熱領域の間で2つ以上の増幅反応液滴のサブセットをサイクルする工程を含んでもよい。一部の場合において、1つ以上の電極経路は、2つ以上の熱領域の間に1つ以上のループ経路を規定する。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、電極経路ループの周りに複数の増幅反応液滴を輸送する工程を含んでもよい。その方法は、その所定数のサイクルが完了した場合、各増幅液滴を電極経路ループから除去する工程を含んでもよい。各増幅液滴を電極経路ループから除去する工程は、増幅反応液滴を液滴操作間隙の別の領域に輸送するために電極により媒介される液滴操作を含んでもよい。液滴操作間隙の領域は、まだ検出されていない増幅液滴を保存するために選択される温度を有する温度制御領域を備えてもよい。各増幅液滴を電極経路ループから除去する工程は、各増幅液滴を液滴アクチュエータの液滴操作間隙から除去する工程を含んでもよい。他の場合において、電極経路は、2つ以上の熱領域の間で曲がっている。電極経路上の1つの電極から電極経路上の隣接する電極への輸送時間は、隣接する電極の各対に関して実質的に均一であってもよく、熱領域内の滞留時間は、熱領域に存在する電極経路の各曲がり角の電極の数によって規定されてもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、並行して熱領域の間に増幅反応液滴の2つ以上のサブセットを輸送する工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、増幅反応液滴の2つ以上のサブセットを熱領域内に連続して輸送する工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、増幅反応液滴の第1のサブセットを第1の熱領域内に輸送するが、増幅反応液滴の第2のサブセットを第2の熱領域内に輸送する工程と、増幅反応試薬液滴の第1のサブセットを第2の熱領域に輸送するが、増幅反応試薬の第2のサブセットを第1の熱領域に輸送する工程を含んでもよい。連続して熱サイクルされた増幅反応液滴のサブセットは、共通の電極経路に沿って熱サイクルされてもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、並行して2つ以上のサブセットを増幅させる工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、全ての増幅反応試薬に関して熱的に同時に熱サイクルする工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、全ての増幅反応試薬に関して熱的に同時でなくてもよい熱サイクルする工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、液滴アクチュエータの熱サイクル領域を加熱および冷却することによって行われ得ることを含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、1回以上、熱サイクルするサイクル数で熱領域における増幅反応液滴の滞留時間を変化させる工程を含んでもよい。標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、増幅液滴からシグナルを検出する前に増幅反応液滴の全てのサブセットに関して完了されてもよい。一部の場合において、増幅液滴からシグナルを検出する工程は、第2のセットの液滴について標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する前に第1のサブセットの液滴について完了されてもよい。検出するための増幅液滴を調製する工程は、2つ以上の増幅液滴のセットに対して標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する前に、液滴アクチュエータの熱サイクル範囲から離れた位置、または熱サイクル領域から離れた位置に2つ以上の増幅液滴のセットを輸送する工程を含んでもよい。増幅液滴は、増幅液滴からシグナルを検出するのに適切な温度を有する熱領域に輸送されてもよい。検出するための増幅液滴を調製する工程は、配置された増幅液滴の各々のそのようなサブセットに対して増幅液滴からシグナルを検出する前に熱サイクル領域から離れた位置に増幅液滴のサブセットを少なくとも配置する工程を含んでもよい。検出するための増幅液滴を調製する工程は、増幅核酸から未結合の検出試薬を分離する工程を含んでもよい。検出するための増幅液滴を調製する工程は、増幅液滴における増幅を実質的に停止する工程を含んでもよい。検出するための増幅液滴を調製する工程は、1つの液滴アクチュエータから別の液滴アクチュエータに増幅液滴を輸送する工程を含んでもよい。増幅液滴における増幅を実質的に停止する工程は、増幅反応を実質的に停止するために液滴温度を調節する工程を含んでもよい。増幅液滴における増幅を実質的に停止する工程は、増幅反応を実質的に停止するために試薬を増幅液滴に添加する工程を含んでもよい。試薬を増幅液滴に添加する工程は、増幅液滴と試薬液滴とを混合する工程を含んでもよく、試薬液滴は、増幅反応を実質的に停止するために選択される試薬を含んでもよい。増幅反応を実質的に停止するために選択される試薬は、ポリメラーゼ活性を妨げること、ポリメラーゼ補因子活性を妨げること、核酸に結合すること、および/または鉄イオンを放出することによって増幅反応を実質的に停止する試薬を含んでもよい。特定の実施形態において、増幅反応液滴は検出試薬を欠く。検出するための増幅液滴を調製する工程は、検出試薬を増幅液滴に添加する工程を含んでもよい。検出試薬を増幅液滴に添加する工程は、各々の増幅液滴と検出試薬を含む液滴とを混合する工程を含んでもよい。検出するための増幅液滴を調製する工程は、各々の増幅液滴と1つ以上の検出試薬を含む液滴とを混合する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、検出試薬によって媒介されるシグナルに基づいて増幅を検出する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、そのような液滴の検出ウィンドウへの輸送後に各々の増幅液滴からシグナルを検出する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、増幅液滴の1つ以上のサブセットのセットを、検出するための検出ウィンドウに輸送する工程を含んでもよい。特定の実施形態において、標的核酸を増幅するための条件下で増幅反応試薬の2つ以上のサブセットを処理する工程は、液滴アクチュエータの液滴操作間隙内で達成されてもよく、検出するための増幅液滴を調製する工程および/または増幅液滴からシグナルを検出する工程は、液滴操作間隙の外側で達成されてもよい。従って、検出するための増幅液滴を調製する工程は、検出するための液滴操作間隙の外側に1つ以上の増幅液滴を輸送する工程を含んでもよい。一部の場合において、増幅液滴からシグナルを検出する工程は、液滴アクチュエータの液滴操作間隙の外側のリザーバーで行われてもよい。検出するための増幅液滴を調製する工程は、増幅液滴のサブセットを、少ないサイクル数のサブセットで開始する検出ウィンドウに輸送する工程、および高いサイクル数のサブセットまで処理する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、増幅液滴のアレイを走査する工程を含んでもよい。増幅液滴からシグナルを検出する工程は、増幅液滴のアレイを画像化する工程を含んでもよい。特定の実施形態において、標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを処理する工程は、複数のサブセットに関して並行して開始し、検出するための増幅液滴を調製する工程は、連続して開始し、各サブセットは以前のサブセットの開始後に開始し、増幅液滴からシグナルを検出する工程は連続して開始し、各サブセットは以前のサブセットの開始後に開始する。一部の場合において、検出するための増幅液滴を調製する工程は連続して開始し、各サブセットは以前のサブセットの開始後に開始する。一部の場合において、増幅液滴からシグナルを検出する工程は連続して開始し、各サブセットは以前のサブセットの完了後に開始する。
【0008】
一部の場合において、増幅液滴からシグナルを検出する工程は、液滴が装置の領域を通って移動する場合、その液滴を追跡し、その液滴からシグナルを測定する画像化装置を用いて達成される。一部の場合において、検出するための増幅液滴を調製する工程は並行して開始し、各サブセットはほぼ同じ時間でプロセスを開始する。一部の場合において、増幅液滴からシグナルを検出する工程は並行して開始し、各サブセットはほぼ同じ時間でプロセスを開始する。その方法は、増幅液滴のサブセットの各々についての熱サイクルエンドポイントにてシグナルの増加または減少を決定することによって増幅液滴に存在する増幅核酸の量を決定する工程を含んでもよい。増幅液滴および/またはサンプルに存在する増幅核酸の量を検出する工程は、サンプル液滴に存在する標的核酸の量を決定するために増幅液滴に存在する増幅核酸の量を使用する工程を含んでもよい。増幅液滴および/またはサンプルに存在する増幅核酸の量を決定する工程は、サンプル液滴に存在する標的核酸の量を決定するために異なる数の熱サイクルの後に増幅液滴に存在する増幅核酸の量を使用する工程を含んでもよい。標的核酸を増幅するための異なる条件は、増幅反応液滴の各サブセットについての異なる数の熱サイクルを含んでもよい。増幅反応液滴は検出試薬を含んでもよい。他の場合において、増幅反応液滴は有意な量の検出試薬を含まなくてもよい。増幅試薬を含む1つ以上の液滴はさらに、検出試薬を含んでもよい。他の場合において、増幅試薬を含む1つ以上の液滴は、有意な量の検出試薬を含まなくてもよい。検出試薬は核酸結合剤を含んでもよい。一部の場合において、核酸結合剤は核酸増幅の割合を有意に阻害できる。核酸結合剤は挿入剤を含んでもよい。挿入剤は蛍光色素を含んでもよい。標的核酸は、遺伝性疾患または感染病の指標であってもよい。標的核酸は、生物学的集団由来の個体または個体のサブグループの同定の指標であってもよい。一部の実施形態において、核酸増幅反応液滴の1つ以上は、標的核酸を増幅するための条件下で、増幅反応液滴の2つ以上のサブセットを処理する工程、および増幅液滴に存在する増幅核酸の量を決定する工程の前に、初期検出工程に供されてもよく、ならびに/あるいはサンプルは、初期検出工程において検出されるシグナルと、増幅液滴から検出されるシグナルとの間の比較物を含んでもよい。サンプル中の標的核酸を検出する方法は、十分なデータが所定の範囲の統計的確実性内で開始サンプルに存在する標的核酸を定量化するために収集された場合、方法を停止する工程を含んでもよい。その方法は、選択されるサイクル数の各々についての増幅液滴および/またはサンプルに存在する増幅核酸の量を決定するための十分なデータを提供するために予想される第1のセットのサイクル数を選択する工程、1つ以上の増幅反応液滴のサブセットを増幅させる工程に供する工程、調製する工程、検出する工程、および決定する工程、ならびに十分なデータが、所定の範囲の統計的確実性内でサンプルに存在する核酸を同定または定量化するために収集されているかどうかを決定する工程を含んでもよい。十分なデータが、所定の範囲の統計的確実性内で開始サンプルに存在する標的核酸を同定または定量化するために収集されるまで、あるいは十分なデータが、標的核酸がサンプルに存在しない所定の範囲の統計的確実性内で決定するために収集されるまで、工程は新しいセットのサイクル数で繰り返されてもよい。十分なデータが収集されるかどうかを決定する工程は、十分なデータが、所定の範囲の統計的確実性内でサンプルに存在する標的核酸を同定するために収集されるかどうかを決定する工程を含んでもよい。十分なデータが収集されるかどうかを決定する工程は、十分なデータが、所定の範囲の統計的確実性内でサンプルに存在する標的核酸を定量化するために収集されるかどうかを決定する工程を含む。
【0009】
本発明はサンプル中の標的核酸の増加をモニターする方法を提供する。その方法は、核酸増幅反応液滴のセットを提供する工程を含んでもよく、各液滴はサンプルの一部を含む。その方法は、増幅された二本鎖核酸を有する増幅液滴を得るために標的核酸を増幅するための条件下で増幅反応液滴の2つ以上のサブセットを熱サイクルする工程を含んでもよい。増幅反応液滴の各サブセットは、1つ以上の増幅反応液滴を含んでもよい。増幅反応液滴の各サブセットは、異なる数のサイクルについて熱サイクルされてもよい。増幅反応液滴の各サブセットは、各サブセットについての所定数のサイクルの完了前に検出に供されなくてもよい。その方法は、検出準備プロトコルを実行する工程を含んでもよく、その検出準備プロトコルは、増幅液滴の各々と、増幅核酸の検出用の検出試薬とを混合して、検出準備液滴を生じる工程を含んでもよい。その方法は、検出準備液滴からシグナルを検出する工程を含んでもよい。その方法は、増幅液滴および/またはサンプルに存在する増幅核酸のシグナル、存在および/または量に基づいて決定する工程を含んでもよい。
【0010】
本発明は、予め組み込まれている液滴アクチュエータカートリッジを提供する。予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を形成する1つ以上の基板、およびその1つ以上の基板に結合され、かつ液滴操作間隙内で液滴操作を媒介するように配置される電極を含んでもよい。予め組み込まれている液滴アクチュエータカートリッジは、増幅試薬を含み、検出試薬を欠く1つ以上の液滴を含む第1のリザーバー、および1つ以上の検出試薬を含む第2のリザーバーを含んでもよい。予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を有する第1のリザーバーおよび第2のリザーバーに流動的に接続される1つ以上の流体経路を含んでもよい。例えば、予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を有する第1のリザーバーに流動的に接続される流体経路を備えてもよい。同様に、予め組み込まれている液滴アクチュエータカートリッジは、液滴操作間隙を有する第2のリザーバーに流動的に接続される流体経路を備えてもよい。予め組み込まれている液滴アクチュエータカートリッジは、サンプルを液滴操作間隙に負荷するための手段を備えてもよい。サンプルを液滴操作間隙に負荷するための手段は、例えば、サンプル負荷リザーバーおよび液滴操作間隙を有するサンプル負荷リザーバーに流動的に接続される流体経路を含んでもよい。本発明は、予め組み込まれている液滴アクチュエータカートリッジを含むキットを提供する。キットはまた、カートリッジを用いて増幅プロトコルを実行するためのソフトウェアを含んでもよい。本発明の物理的実施形態のいずれかは、物理的実施形態を含むそのようなキットおよび物理的実施形態を制御するためのソフトウェア含んでもよい。
【0011】
本発明は検体を検出する方法を提供する。その方法は、検出ウィンドウ内に液滴を提供する工程を含んでもよい。液滴は、検体の存在および/または量の指標であるシグナル生成物質を含んでもよい。液滴は、シグナル生成物質によって生成されたシグナルを妨げることができる1つ以上の磁性反応ビーズを含んでもよい。その方法は、検出ウィンドウ内の液滴を輸送および/または抑制している間、検出ウィンドウから磁性反応ビーズを磁性的に除去するため、および/または磁性反応ビーズが検出ウィンドウに侵入することを磁性的に抑制するための磁場を使用する工程を含んでもよい。その方法は、磁性反応ビーズから実質的に妨げられないシグナル生成物質によって生成されるシグナルを検出する工程を含んでもよい。同様に、本発明は、検出ウィンドウに液滴を提供する工程を含む検体を検出する方法を提供し、ここで、液滴は、検体および/または実質的に磁性反応ではなく、シグナル生成物質によって生成されたシグナルを妨げることができる1つ以上のビーズの存在および/または量の指標であるシグナル生成物質を含む。その方法は、検出ウィンドウ内に液滴を輸送および/または保有している間、ビーズが検出ウィンドウに侵入することを防ぐ物理的障壁を使用する工程を含んでもよい。その方法は、ビーズから実質的に妨げられないシグナル生成物質によって生成されたシグナルを検出する工程を含んでもよい。この物理的障壁アプローチは、ビーズが磁性反応であるか否かに関わらず、使用されてもよいことは理解されるだろう。検体を検出するこれらの方法において、液滴は、液滴アクチュエータの液滴操作間隙内に提供されてもよい。検出ウィンドウは、液滴アクチュエータの基板内に開口部またはウィンドウを備えてもよい。実質的に非磁性反応ビーズを利用する実施形態に関して、磁場を使用する工程は、検出ウィンドウに近接する固定磁石を提供する工程を含んでもよい。検出ウィンドウ内に液滴を輸送する工程は、磁性反応ビーズを、ビーズが検出ウィンドウから離れた位置へ引き付けられ得るか、および/またはビーズが検出ウィンドウに侵入することを抑制され得る、固定磁石に十分に近接する位置に送達できる。物理的障壁を利用する実施形態に関して、液滴を検出ウィンドウに輸送する工程は、ビーズが物理的障壁によって検出ウィンドウ内に侵入することを抑制している間に達成されてもよい。このビーズが検出ウィンドウに侵入することを抑制することは、液滴から磁性反応ビーズを除去して、または除去せずに達成されてもよい。磁場を利用する本発明のこれらおよび任意の他の実施形態において、磁場は、任意の適切な磁場源によって生成されてもよい。例えば、磁場源は、固定永久磁石、移動可能な永久磁石、および/または電磁石を備えてもよい。磁場は、液滴の端部に磁性反応ビーズを凝集させるために配置されてもよい。磁場は、検出ウィンドウの外側であり得る液滴の領域内に磁性反応ビーズを凝集させるために配置されてもよい。一部の場合において、磁場は、液滴から離れた位置に磁性反応ビーズを分裂させるために選択される。例えば、磁場は、液滴が所定の位置に保持され得る間、および/または電極により媒介される力によって移動され得る間、磁性反応ビーズを液滴から離れた位置に分裂させることができる。一部の場合において、液滴が検出ウィンドウ内に少なくとも部分的に存在し得る場合、磁場は、磁性反応ビーズを液滴の端部に引き付ける方法で磁性反応ビーズを引き付ける。一部の場合において、液滴が磁石上を通過する場合、磁場は液滴の外側に磁性反応ビーズを引き付ける。一部の場合において、液滴が磁石の近くに近づく場合、磁場は液滴の外側に磁性反応ビーズを引き付ける。一部の場合において、液滴が検出ウィンドウに近づく場合、磁場は液滴の外側に磁性反応ビーズを引き付ける。一部の場合において、液滴が検出ウィンドウ内に輸送され得る場合、磁場は、実質的に全てのビーズが検出ウィンドウに侵入するか、または再侵入することを抑制する方法で磁性反応ビーズを引き付ける。検出ウィンドウは、液滴アクチュエータ装置の表面に設けられてもよい。液滴アクチュエータは、例えば、液滴操作表面に結合される電極の複数の経路、検出ウィンドウに結合される各々の経路、ならびに検出ウィンドウ内に液滴を輸送および/または保有している間、対応する検出ウィンドウから磁性反応ビーズを磁性的に除去するように、および/または磁性反応ビーズが対応する検出ウィンドウに侵入することを磁性的に抑制するように配置される経路に近接する磁場を備える。液滴は、1つ以上の検体の存在、非存在および/または量の指標であるシグナルを放出できる。例えば、1つ以上の検体は増幅核酸を含んでもよい。検出ウィンドウは液滴アクチュエータの表面に配置されてもよく、液滴アクチュエータは、熱サイクル反応を実施するための電極の経路に沿った温度制御ゾーンを備えてもよい。そのような液滴アクチュエータを使用する方法は、増幅液滴を得るために増幅準備液滴を熱サイクルする工程、および増幅液滴を検出ウィンドウに輸送する工程を含んでもよい。その方法は、1以上の熱サイクルの後、電極の経路から少なくとも部分的に電極の経路に沿って磁性反応ビーズを含み得る液滴を、検出ウィンドウ内に輸送する工程を含んでもよい。
【0012】
本発明はまた、液滴を熱サイクルする方法を提供する。その方法は、充填流体によって少なくとも部分的に囲まれた液滴を提供する工程を含んでもよい。液滴は、潜在的に標的核酸を含んでもよい。液滴は、標的核酸の存在下で増幅を生じるのに十分な試薬を含んでもよく、試薬は、熱サイクルプロトコルを実施している間、充填流体中で有意に分離しないフルオロフォアを含んでもよい。その方法は、標的核酸の存在下で増幅を誘導するために熱サイクルプロトコルに従って液滴の温度を調節する工程を含んでもよい。フルオロフォアは極性フルオロフォアを含んでもよい。フルオロフォアは細胞膜に実質的に不浸透性であってもよい。フルオロフォアは細胞膜に完全に不浸透性であってもよい。フルオロフォアはEVAGREEN(登録商標)フルオロフォアを含んでもよい。フルオロフォアはTO−PRO1フルオロフォアを含んでもよい。充填流体は、本質的にシリコーンオイルから構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、10〜20の炭素オイルから構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、15〜20の炭素オイルから本質的に構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、ヘキサデカンオイルから本質的に構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。充填流体は、実質的な脱気水から本質的に構成されてもよく、必要に応じて1つ以上の添加剤でドープされてもよい。液滴を提供する工程は、液滴を液滴アクチュエータの液滴操作間隙に提供する工程を含んでもよい。熱サイクルプロトコルに従って液滴の温度を調節する工程は、液滴アクチュエータの液滴操作間隙の液滴を加熱および/または冷却する工程を含んでもよい。熱サイクルプロトコルに従って液滴の温度を調節する工程は、電極により媒介される液滴操作を用いて液滴操作間隙内の熱領域の間に液滴を輸送する工程を含んでもよい。
【0013】
本発明は、液滴アクチュエータでプロトコルを実行する方法を含む。その方法は、不動態化剤を含み得る液滴を有する領域内で1つ以上の電極で液滴操作を実施することによって液滴アクチュエータの1つ以上の領域を処理する工程、および液滴アクチュエータの1つ以上の処理された領域を用いてプロトコルを実施する工程を含む。そのプロトコルは、標的核酸の解析における工程を含んでもよく、不動態化剤は標的核酸でなくてもよい核酸を含んでもよい。そのプロトコルは核酸増幅プロトコルを含んでもよい。そのプロトコルは熱サイクルプロトコルを含んでもよい。少し例を挙げると、不動態化剤は、核酸、ポリビニルピロリドン、ポリエチレングリコール、界面活性剤、トゥイーン(tween)、アルブミン、血清アルブミン、ウシ血清アルブミン、および/または色素を含んでもよい。不動態化剤は、液滴アクチュエータの表面上に吸着するように選択されてもよい。不動態化剤は、充填流体内に吸着するように選択されてもよい。1つ以上の液滴は、十分な不動態化剤を実質的に飽和する可能性のある不動態化部位に送達してもよい。そのプロトコルは、不動態化剤を含む液滴を用いて実施されてもよい。一例として、そのプロトコルは、核酸増幅プロトコルを含んでもよい。核酸増幅プロトコルおよび処理する工程は、核酸増幅試薬および不動態化剤を含む液滴を用いて同時に実施されてもよい。
【0014】
本発明はまた、高温で液滴操作を実施するための液滴アクチュエータを提供する。液滴アクチュエータは、液滴操作基板および液滴操作表面とカバーとの間に液滴操作間隙を形成するために液滴操作表面に隣接し、液滴操作表面から離れているカバーを備えてもよく、液滴操作間隙は少なくとも250μmの高さを有する。液滴アクチュエータは、液滴操作基板および/またはカバーに結合され、熱サイクルプロトコルに従って熱領域の間に液滴を輸送するように配置される電極の経路を備えてもよい。液滴アクチュエータは、液滴操作間隙内の1つ以上の熱領域を規定するように配置される温度制御素子を備えてもよい。一部の場合において、液滴操作間隙は、実質的に球状の形状の単一のサイズの液滴を与えるように選択される高さを有してもよい。例えば、特定の実施形態において、約250μm〜約500μm、または約275μm〜約450μm、または約300μm〜約400μm、または約320μm〜約375μm、または約320μm〜約350μmの範囲の高さを有してもよい。特定の実施形態において、電極はピッチを有してもよく、液滴操作間隙は、約7:1〜約2.8:1、または約6:1〜約3:1、または約4.3:1〜約3.4:1の範囲の比のピッチ:高さを規定する高さを有してもよい。特定の実施形態において、液滴操作間隙は、熱サイクルプロトコルを受ける液滴から完全な熱サイクルプロトコルについて5%未満、または完全な熱サイクルプロトコルについて1%未満、または完全な熱サイクルプロトコルについて0.01%未満の容積減少を維持するように選択される高さを有する。特定の実施形態において、液滴操作間隙は、熱サイクルプロトコルを受ける液滴から1回の熱サイクルにつき0.1%未満、または1回の熱サイクルにつき0.01%未満、または1回の熱サイクルにつき0.001%未満の容積減少を維持するように選択される高さを有する。一部の場合において、液滴操作間隙は、熱サイクルプロトコルの間、実質的に容積減少を排除するように選択される高さを有する。本発明はまた、熱サイクル反応を実施する方法を提供し、その方法は、本発明のこの態様の液滴アクチュエータを提供する工程、電極の経路に沿って、磁性反応ビーズを含み得る液滴を、検出ウィンドウ内の少なくとも部分的に電極の経路に輸送する工程であって、その結果、磁石が、1つ以上のビーズが検出ウィンドウに侵入することを抑制する方法で磁性反応ビーズを引き付ける、工程、および液滴からのシグナルを検出するためにセンサーを使用する工程を含んでもよい。
【0015】
本発明は、解析用のサンプルを調製する方法を提供する。その方法は、液滴操作基板、基板の液滴操作表面上で液滴操作を実施するように配置される電極、液滴操作表面に隣接し、液滴操作表面とカバーとの間に液滴操作間隙を形成するために液滴操作表面から離れているカバー、上部基板に結合され、1つ以上の標的検体および/または1つ以上の標的検体を含み得る物質に対する親和性を有するビーズを含み得るリザーバー、リザーバーから液滴操作間隙内に延びる液体経路、液滴操作基板に結合され、磁性反応ビーズを引き付けるのに十分な磁場を生じるように構成される磁場源を備える液滴アクチュエータを提供する工程を含んでもよい。その方法は、サンプルをリザーバーに供給する工程を含んでもよい。サンプルは1つ以上の標的物質を含んでもよい。その方法は、液滴経路を通して液滴操作間隙に磁性反応ビーズとともにサンプルを流動させる工程を含んでもよい。その方法は、磁石で磁性反応ビーズを凝集させる工程を含んでもよい。その方法は、磁性反応ビーズを有する液滴操作間隙内のサンプル液滴を得るために、磁場を除去する工程または磁場からビーズを除去する工程を含んでもよい。一部の場合において、液体経路は、(より湾曲した液体経路とは対照的に)基板における穴または開口部などの実質的に真っ直ぐな液体経路であってもよい。磁石は、リザーバーから液滴操作間隙内に1つ以上のビーズを引き付けるのに十分な磁場の強さを有してもよい。液滴アクチュエータは、液滴操作基板に結合され、液体経路を介して液滴操作間隙に侵入する流体を受容するように配置されるリザーバー電極を備えてもよい。磁石は液体経路に対してリザーバー電極の反対側に配置されてもよい。磁石は、電磁石または永久磁石などの適切な磁場を生成するための任意の要素または要素の組み合わせであってもよい。磁石は空間的に調節可能である。磁石は、第1の位置において液滴操作間隙内の永久磁石の磁場をブロックまたは妨げることができるか、あるいは第2の位置において液滴操作間隙内の永久磁石の磁場をブロックまたは妨げることができない可動式磁気シールドに結合されてもよい。液滴アクチュエータは、リザーバー内のサンプル流体を撹拌するように配置される撹拌器を備えてもよく、その方法は、リザーバー内のサンプルを撹拌する工程を含んでもよい。液滴アクチュエータは、音波エネルギーをリザーバー内のサンプル流体に与えるように配置される超音波処理器を備えてもよく、その方法は、リザーバー内のサンプルを超音波処理する工程を含んでもよい。液滴アクチュエータはまた、1つ以上の電極に結合される第2の磁石を備えてもよい。物質は、ビーズが親和性を有する1つ以上の標的検体を含んでもよい。一実施形態において、標的検体は細胞を含み、その方法は、細胞を溶解または分解する工程を含む。例えば、細胞を溶解する工程は、溶解試薬を、細胞を含む液滴に加えることによって達成されてもよい。一例として、溶解試薬を加える工程は、磁性反応ビーズを含む液滴操作間隙内のサンプル液滴と、細胞溶解試薬を含む溶解液滴とを混合する工程を含む。混合した液滴は超音波処理されてもよいか、あるいは混合するために攪拌または振盪されてもよい。その方法は、一部の場合、磁性反応ビーズを固定するために磁場を再印加する工程を含んでもよい。その方法は、固定された磁性反応ビーズから離れた位置に液滴を輸送する工程を含んでもよい。その方法は、磁性反応ビーズから離れた位置に液滴の一部を輸送する工程を含んでもよい。その方法は、離れた位置に輸送された液滴または液滴の一部と、1つ以上の標的検体に対する親和性を有するビーズを含む液滴とを混合する工程を含んでもよい。その方法は、1つ以上の標的検体に対する親和性を有するビーズを洗浄するための洗浄プロトコルを実施する工程であって、実質的に精製された標的検体を含むビーズを有する液滴を生じる工程を含んでもよい。その方法は、実質的に精製された標的検体を含むビーズを有する液滴を用いて解析プロトコルを実施する工程を含んでもよい。解析プロトコルの工程は、液滴操作間隙内または液滴操作間隙外で達成されてもよい。解析プロトコルの工程は、液滴アクチュエータ上、別の液滴アクチュエータ上、または液滴アクチュエータを使用せずに達成されてもよい。例えば、ビーズおよび実質的に精製された標的検体を含む液滴は、解析プロトコルを実施する前に液滴操作間隙から除去されてもよい。その方法は、液滴操作間隙間から実質的に精製された標的検体を有するビーズを除去する工程を含んでもよい。その方法は、ビーズから1つ以上の標的検体を溶出する工程を含んでもよい。溶出する工程は、実質的に精製された標的検体を含むビーズを含む液滴と、溶出バッファーを含む液滴とを混合する工程であって、ビーズを含む液滴および溶出された1つ以上の標的検体を生じる工程を含んでもよい。その方法は、実質的に精製された標的検体を含み、かつ実質的にビーズを含まない液滴を得るために、ビーズおよび溶出された1つ以上の標的検体を含む液滴からビーズを除去する工程を含んでもよい。除去する工程は、例えば、磁場および/または物理的障壁を用いて行われてもよい。その方法は、実質的に精製された標的検体を含み、かつ実質的にビーズを含まない液滴を、液滴操作間隙から除去する工程を含んでもよい。その方法は、実質的に精製された標的検体を含み、かつ実質的にビーズを含まない液滴を用いて解析プロトコルを実施する工程を含んでもよい。そのプロトコルは、液滴操作間隙内または外において、液滴アクチュエータ上で、または液滴アクチュエータ外で行われてもよい。本明細書に記載されるアッセイプロトコルのいずれかは、解析プロトコルの結果のアウトプット指標を提供する工程を含んでもよい。その方法の工程の1つ以上は、その方法の工程の1つ以上を実行するようにプログラムされた液滴アクチュエータおよびプロセッサを含むシステムによって実行されてもよい。その方法は、解析プロトコルの結果のユーザーが判読可能なアウトプット指標をアウトプットする工程を含んでもよい。標的検体は、核酸、タンパク質またはペプチド、抗体、小有機分子などを含んでもよい。液滴操作間隙は流動性の充填流体で満たされてもよい。
【0016】
本発明は液滴アクチュエータを操作する方法を提供する。本発明は、内部液滴操作間隙を形成するように構成される1つ以上の基板を備える液滴アクチュエータ装置を提供する工程を含んでもよい。その方法は、液滴操作間隙内に流動性の充填流体を提供する工程を含んでもよい。その方法は、液滴操作間隙内の充填流体中で液滴プロトコルを実行する工程を含んでもよい。その方法は、液滴操作間隙内の充填流体を置き換える工程を含んでもよい。一旦、充填流体が置き換えられると、その方法は、液滴操作間隙内の充填流体中で別の液滴プロトコルを実行する工程を含んでもよい。本発明は、共通の液滴アクチュエータ上で、液滴プロトコル実行の間に充填流体の交換が実施される複数の液滴プロトコルを提供する。従って、例えば、本発明は、充填−実行−再充填パターンの使用を含んでもよく、実行−再充填は、数回、例えば2、5、10、20、50、100またはそれ以上繰り返される。同様に、本発明は、充填−実行−実行−再充填パターンの使用を含んでもよく、実行−実行−再充填は、数回、例えば2、5、10、20、50、100またはそれ以上繰り返される。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙を通して充填流体をフラッシングする工程を含んでもよい。液滴操作間隙を通して充填流体をフラッシング工程は、所定量のフラッシングが達成するまで続けてもよい。液滴操作間隙を通して充填流体をフラッシングする工程は、洗浄の指標(例えば除去された充填流体中で測定される汚染)が所定のレベルに到達するまで続けてもよい。フラッシングの量は自動化されてもよい。液滴プロトコルは、例えば、標的検体の存在および/または量を測定するためのプロトコルを含んでもよい。例えば、プロトコルは診断的プロトコルであってもよい。少しの例を挙げると、液滴プロトコルは、核酸増幅プロトコル、核酸シークエンシングプロトコル、免疫学的検定プロトコル、および/または酵素アッセイプロトコルであってもよい。一部の実施形態において、流動性の充填流体は、充填流体を置き換える間、汚染について試験されてもよく、別のプロトコルの実行が、所定のレベルの汚染の減少が達成された後に行われてもよい。このプロセスは自動化されてもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙を通して、および液滴操作間隙の外側に、流動性の充填流体源から流動性の充填流体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える前に、液滴操作間隙を通して洗浄流体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を交換する前に、液滴操作間隙を通して充填流体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える前に、液滴操作間隙を通して加熱された洗浄液体を流動させる工程を含んでもよい。加熱された洗浄液体は、汚染物質を分解するように選択される温度を有してもよい。例えば、種々の実施形態において、温度は、約30℃〜約125℃、または約60℃〜約115℃、または約75℃〜約105℃、または約90℃以上、または約100℃以上、または約125℃以上、または約150℃以上の範囲である。温度は、典型的に、液滴アクチュエータの1つ以上の構成要素が過度な損傷、すなわち、液滴アクチュエータ装置にその意図される使用に対する損傷を受ける温度未満である。充填流体などの冷却液体は、加熱された洗浄後に、適切または操作可能な温度を設定するために液滴アクチュエータ間隙を通して流されてもよい。加熱された洗浄液体は、例えば、充填流体、オイル、溶媒、および/または水性洗浄液体を含んでもよい。洗浄液体は、親油性物質が可溶性であり得る成分および親水性物質が可溶性であり得る成分を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える前に、液滴アクチュエータ間隙を乾燥させるために、液滴アクチュエータ間隙を通してガスを流動させる工程を含んでもよい。ガスは空気または別のガスであってもよい。ガスは、洗浄液体の温度と比較して、加熱または冷却されてもよい。ガスは、例えば、約50℃以上、約75℃以上、約100℃以上、約125℃以上、または約150℃以上の温度を有してもよい。温度は、典型的に、液滴アクチュエータの1つ以上の構成要素が過度な損傷、すなわち、液滴アクチュエータ装置にその意図される使用に対する損傷を受ける温度未満である。液滴操作間隙内の充填流体を置き換える工程は、液滴アクチュエータ間隙を通してガスを流動させる工程の前に、液滴アクチュエータ間隙を通して洗浄液体を流動させる工程を含んでもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内に存在する少なくとも約50%の充填流体、または液滴操作間隙内に存在する少なくとも約75%の充填流体、または液滴操作間隙に存在する少なくとも約90%の充填流体、または液滴操作間隙に存在する少なくとも約95%の充填流体、または液滴操作間隙に存在する少なくとも約99%の充填流体、または液滴操作間隙に存在する少なくとも約99.9%の充填流体、または液滴操作間隙に存在する実質的に全ての充填流体を置き換える工程を含んでもよい。液滴操作間隙の1つ以上の表面はコーティングを含んでもよく、洗浄液体はコーティングの層を除去するために選択されてもよい。液滴操作間隙内の充填流体を置き換える工程は、液滴操作間隙内の充填流体を置き換える工程の前に所定の温度を設定するために、液滴操作間隙を通して冷却液体を流動させる工程を含んでもよい。洗浄流体は溶媒を含んでもよい。洗浄流体は水溶液を含んでもよい。洗浄流体は、新油性化合物を溶解する1つ以上の成分および親水性化合物を溶解する1つ以上の成分を含んでもよい。本発明は、本発明の充填流体を置き換える方法を実行するための命令を有するプログラムを有するコンピューターにより読取可能な媒体を提供する。本発明は、内部液滴操作間隙を形成するように構成される1つ以上の基板、流動性の充填流体源に流動的に接続される液滴操作間隙内の開口部、その開口部を通して、液滴操作間隙内に充填流体源から充填流体の流れを制御するように構成される1つ以上の弁および/またはポンプ、ならびに本発明の充填流体の交換および/または洗浄のいずれかを実行するようにプログラムされる1つ以上のポンプおよび/または弁を制御するプロセッサを備える液滴アクチュエータ装置を有するシステムを提供する。
【0017】
本発明は、液滴操作間隙を形成する1つ以上の基板を備える液滴アクチュエータを提供する。液滴操作間隙は、液体経路によって流動的に結合される少なくとも2つの温度制御リザーバーを規定する熱サイクル経路および1つ以上の障壁、ならびに1つまたは両方の基板に結合され、温度制御リザーバーの間に液滴を輸送するように構成される電極を備えてもよい。液滴アクチュエータは2つ以上のこのような熱サイクル経路を備えてもよい。
【0018】
本発明は、液滴アクチュエータ上での液滴間の二次汚染を阻害する方法を提供する。その方法は、液滴操作間隙を形成する1つ以上の基板、複数の実質的に平行な液滴輸送経路を規定する1つ以上の基板に結合される電極、および液滴操作間隙を実質的に充填する流動性の充填流体を有する液滴アクチュエータを提供する工程を含んでもよい。その方法は、第1のサブセットの複数の実質的に平行な液滴輸送経路上に複数のアッセイ液滴を輸送する工程を含んでもよい。その方法は、第2のサブセットの複数の実質的に平行な液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよく、その第2のサブセットの各々の液滴輸送経路は、第1のサブセットの2つの液滴輸送経路の間に存在してもよい。アッセイ液滴を輸送する工程および液滴を洗浄する工程は同時に行われてもよい。2つ以上の洗浄液滴は、第2のサブセットの各々の液滴輸送経路上に提供/輸送されてもよい。洗浄液滴は、液滴または液滴スラグ(細長い液滴)の形態で提供されてもよい。その方法は、第1のサブセットの液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよい。その方法は、第1のサブセットの液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよい。その方法は、第1の洗浄液滴に対してアッセイ液滴の反対側の第1のサブセットの液滴輸送経路上に1つ以上のバッファー液滴を輸送する工程を含んでもよい。アッセイ液滴は核酸増幅液滴を含んでもよい。その方法は、増幅を行うために2つの熱領域の間にアッセイ液滴を輸送する工程を含んでもよい。
【0019】
本発明はまた、液滴操作間隙を設けるように配置される1つ以上の基板、複数の実質的に平行な液滴輸送経路を規定する1つ以上の基板に結合される電極、液滴操作間隙を実質的に充填する流動性の充填流体、ならびに液滴輸送経路の各々の間にあり、1つの液滴操作経路と結合される充填流体が、他の液滴操作経路と結合される充填流体と接触することを防ぐ障壁を有する液滴アクチュエータを提供する。液滴アクチュエータは、2つ以上の液滴輸送経路上にアッセイ液滴を含んでもよい。アッセイ液滴は、核酸を増幅するための試薬およびサンプルを含んでもよい。
【0020】
本発明は、液滴アクチュエータ上の液滴間の二次汚染を減少させる方法を提供する。その方法は、内部液滴操作間隙および液滴操作間隙内のオイルベースの充填流体を含み得る液滴アクチュエータを提供する工程、ならびに液滴操作間隙内に水性液滴を提供する工程を含んでもよい。液滴は、オイルベースの充填流体によって少なくとも部分的に囲まれてもよい。液滴は界面活性剤−酵素複合体を含んでもよく、その複合体は、潜在的な汚染物質を分解するように選択される酵素に結合された界面活性剤を含んでもよい。適切な酵素のいくつかの非限定的な例としては、ヌクレアーゼ、エンドヌクレアーゼ、エキソヌクレアーゼ、および/またはプロテイナーゼが挙げられる。界面活性剤に関して、任意の適切な界面活性剤が使用されてもよい。例としては、ポリエチレン(PEG)−アルキル界面活性剤などのポリアルカレン(PAG)−アルキル界面活性剤が挙げられる。界面活性剤−酵素複合体は、酵素−PAG−アルキル複合体を含んでもよい。界面活性剤は、例えば、酵素のアミノ部分に結合されてもよい。界面活性剤−酵素複合体は、液滴内で実質的に不活性であるように十分に低く、液滴から形成され得る、微小液滴、マイクロ液滴またはナノ液滴内で活性であるように十分に高い量で液滴に存在してもよい。一部の場合において、その量は、約10μL未満、または約1μL未満、または約0.01μL未満、または約0.001μL未満であり得る平均容積を有する微小液滴内で活性であるように選択される。一部の場合において、平均液滴サイズ対平均微小液滴サイズの比は、約1000対約1未満、または約1000対約0.1未満、または約1000対約0.01未満、または約1000対約0.001未満であり得る。潜在的な汚染物質としては、例えば、タンパク質、核酸、または試薬が挙げられ得る。特定の実施形態において、界面活性剤−酵素複合体の実質的に全ては、液滴の表面に捕捉されてもよい。充填流体は、シリコンオイルなどのオイルを含んでもよい。液滴は、充填流体によって部分的に囲まれてもよい。液滴は、充填流体によって実質的に囲まれてもよい。液滴は、充填流体によって完全に囲まれてもよい。
【0021】
本発明は、デジタル増幅法を提供する。その方法は、標的核酸、および必要に応じて増幅試薬を含むサンプル液滴を提供する工程を含んでもよい。その方法は、サンプル液滴から小液滴を分配する工程、および増幅試薬がサンプル液滴に存在し得ない場合、増幅準備液滴を得るために各々の小液滴と増幅試薬とを混合する工程を含んでもよい。その方法は、各々の小液滴を、標的核酸を増幅するために選択される熱サイクルプロトコルに供する工程を含んでもよい。その方法は、各々の小液滴内の増幅産物を検出する工程を含んでもよい。その方法は、サンプル部を含む小液滴の数を決定する工程を含んでもよく、そのサンプル部から上記増幅産物が形成されてもよい。典型的に、上記小液滴の少なくとも1つは、少なくとも1つの標的核酸分子を含む。増幅試薬は、増幅標的分子に対してハイブリダイズし、ハイブリダイゼーションの際に変化するか、またはハイブリダイゼーションの結果として変化する蛍光特性を有する少なくとも1つのプローブを含んでもよい。その方法は、サンプル部を含む小液滴の数を決定する工程を含んでもよく、そのサンプル部から上記増幅産物が形成される。一部の場合において、決定する工程は、上記少なくとも1つのプローブのハイブリダイゼーションに起因する蛍光変化を検出する工程を含んでもよい。上記増幅産物が形成され得るサンプル部を含む小液滴の数を決定する工程は、全ての小液滴を一緒に画像化する工程を含んでもよい。上記増幅産物が形成され得るサンプル部を含む小液滴の数を決定する工程は、検出ウィンドウを通して一つずつまたは小液滴内の液滴を輸送する工程を含んでもよい。小液滴は、約1μL未満、または約1μL以上〜約1000μLの範囲、または約100μL以上〜約500μLの容積を有してもよい。この1つ以上の系統および本発明の他の方法は、液滴アクチュエータの液滴操作間隙内で実施されてもよい。小液滴は、液滴操作間隙内の2つの基板の間で平らまたはディスク形状の構造に圧縮されてもよい。液滴操作間隙は、約50μm〜約1000μm、または約100μm以上〜約500μmの範囲の高さを有してもよい。熱サイクルは、1つの熱領域から別の熱領域へ液滴を輸送することによって行われてもよい。特定の実施形態において、液滴アクチュエータはサンプルチャンバを欠く。特定の実施形態において、液滴アクチュエータは流路チャネルを欠く。特定の実施形態において、サンプル液滴から小液滴を分配する工程は、流路チャネルからサンプルを配置する配置流体を用いずに行われてもよい。特定の実施形態において、標的核酸を含むサンプル液滴はまた、増幅試薬を含んでもよい。特定の実施形態において、増幅試薬はサンプル液滴に存在しなくてもよく、その方法は、各々の小液滴と増幅試薬とを混合して増幅準備試薬を生じる工程を含んでもよい。特定の実施形態において、各々の小液滴中の増幅産物を検出する工程は、液滴を検出に供する前に、増幅液滴と1つ以上の検出試薬を含む液滴とを混合する工程を含んでもよい。
【0022】
本発明のこれらの態様および多くの他の態様は、本明細書の残りの段落および添付の特許請求の範囲から明らかになるだろう。
【0023】
(5.定義)
本明細書で使用する場合、以下の用語は示される意味を有する。
【0024】
1つ以上の電極に関して「活性化する」とは、液滴の存在下において、1つ以上の電極の電気状態の変化を与えることにより、液滴操作を生じさせることを意味する。
【0025】
液滴アクチュエータ上のビーズに関して「ビーズ」とは、液滴アクチュエータ上で、または液滴アクチュエータと近接して、液滴と相互作用できる任意のビーズまたは粒子を意味する。ビーズは、球形、ほぼ球形、卵形、円盤形状、立方体および他の三次元形状などの様々な形状のいずれかであってもよい。ビーズは、例えば、液滴アクチュエータ上の液滴中で輸送され得るか、あるいは液滴アクチュエータ上の液滴が、液滴アクチュエータ上および/または液滴アクチュエータの外でビーズと接触できる方法で液滴アクチュエータに対して構成され得る。ビーズは、例えば、樹脂およびポリマーを含む、様々な材料を用いて製造されてもよい。ビーズは、例えば、マイクロビーズ、マイクロ粒子、ナノビーズおよびナノ粒子を含む、任意の適切なサイズであってもよい。一部の場合において、ビーズは磁性反応であり、他の場合において、ビーズは、著しく磁性反応でなくてもよい。磁性反応ビーズに関して、磁性反応材料は、ビーズの実質的に全てまたはビーズの1つの成分のみを構成してもよい。ビーズの残りは、特に、アッセイ試薬の結合を可能にするポリマー性の材料、コーティング、および部分を含んでもよい。適切な磁性反応ビーズの例は、2005年11月24日に公開された「Multiplex flow assays preferably with magnetic particles as solid phase」という発明の名称の米国特許出願公開第2005−0260686号に記載されており、その全開示は、磁性反応材料およびビーズに関するその教示のために本明細書に参照として援用される。流体は、1つ以上の磁性反応ビーズおよび/または非磁性反応ビーズを含んでもよい。磁性反応ビーズおよび/または非磁性反応ビーズを固定するための液滴アクチュエータ技術ならびに/あるいはビーズを用いて液滴操作プロトコルを実施するための液滴アクチュエータ技術の例は、2006年12月15日に出願された「Droplet−Based Particle Sorting」という発明の名称の米国特許出願公開第11/639,566号;2008年3月25日に出願された「Multiplexing Bead Detection in a Single Droplet」という発明の名称の米国特許出願公開第61/039,183号;2008年4月25日に出願された「Droplet Actuator Devices and Droplet Operations Using Beads」という発明の名称の米国特許出願公開第61/047,789号;2008年8月5日に出願された「Droplet Actuator Devices and Methods for Manipulating Beads」という発明の名称の米国特許出願公開第61/086,183号;2008年2月11日に出願された「Droplet Actuator Devices and Methods Employing Magnetic Beads」という発明の名称の国際特許出願第PCT/US2008/053545号;2008年3月24日に出願された「Bead−based Multiplexed Analytical Methods and Instrumentation」という発明の名称の国際特許出願第PCT/US2008/058018号;2008年3月23日に出願された「Bead Sorting on a Droplet Actuator」という発明の名称の国際特許出願第PCT/US2008/058047号;および2006年12月11日に出願された「Droplet−based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/047486号に記載されており、その全開示は本明細書に参照により援用される。
【0026】
「液滴」とは、充填流体に少なくとも部分的に結合される液滴アクチュエータ上の液体の量を意味する。例えば、液滴は充填流体によって完全に囲まれてもよいか、または充填流体および液滴アクチュエータの1つ以上の表面に結合されてもよい。液滴は、例えば、水溶性であっても、非水溶性であってもよいか、または水溶性および非水溶性成分を含む混合物もしくはエマルションであってもよい。液滴は様々な形状をとってもよく、非限定的な例として、ほぼ円盤形状、スラグ形状、切頭球体、楕円、球形、部分的に圧縮された球形、半球形、卵形、円筒形、および液滴アクチュエータの1つ以上の表面と、そのような形状との接触の結果として融合または分裂または形成されるなどの液滴操作の間に形成された種々の形状が挙げられる。本発明のアプローチを用いて液滴操作に供され得る液滴流体の例に関しては、2006年12月11日に出願された「Droplet−Based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/47486号を参照のこと。種々の実施形態において、液滴は、全血、リンパ液、血清、血漿、汗、涙、唾液、痰、脳脊髄液、羊水、精液、膣排出液、漿液、滑液、心膜液、腹水、胸膜液、浸出液、滲出液、嚢胞液、胆汁、尿、胃液、腸液、糞便試料、単細胞または多細胞を含む液体、細胞小器官を含む液体、流動組織、流動器官、多細胞生物を含む液体、生物学的スワブおよび生物学的洗浄液などの生物学的サンプルを含んでもよい。さらに、液滴は、水、脱イオン水、生理的食塩水、酸性溶液、塩基性溶液、清浄液および/または緩衝液などの試薬を含んでもよい。液滴内容物の他の例としては、核酸増幅プロトコル、親和性ベースアッセイプロトコル、酵素アッセイプロトコル、シークエンシングプロトコル、および/または生物学的流体の解析のためのプロトコルなどの生物学的プロトコルのための試薬などの試薬が挙げられる。
【0027】
「液滴アクチュエータ」とは、液滴を操作するための装置を意味する。液滴アクチュエータの例に関しては、Pamulaらによる2005年6月28日に発行された「Apparatus for Manipulating Droplets by Electrowetting−Based Techniques」という発明の名称の米国特許第6,911,132号;2006年1月30日に出願された「Apparatuses and Methods for Manipulating Droplets on a Printed Circuit Board」という発明の名称の米国特許出願公開第11/343,284号;両方、Shenderovらによる、2004年8月10日に発行された「Electrostatic Actuators for Microfluidics and Methods for Using Same」という発明の名称の米国特許第6,773,566号および2000年1月24日に発行された「Actuators for Microfluidics Without Moving Parts」という発明の名称の同第6,565,727号;Pollackら、2006年12月11日に出願された「Droplet−Based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/047486号;ならびにRouxら、2005年8月18日に公開された「Device for Controlling the Displacement of a Drop Between two or Several Solid Substrates」という発明の名称の米国特許出願公開第20050179746号を参照のこと(これらの開示は本明細書に参照として援用される)。特定の液滴アクチュエータは、基板、基板に結合された液滴操作電極、液滴操作表面を形成する基板および/または電極の上の1つ以上の誘電層および/または疎水性層、ならびに必要に応じて、液滴操作間隙によって液滴操作表面から分離された上部基板を備える。1つ以上の参照電極が、上部または底部の基板ならびに/あるいは液滴操作間隙内に設けられてもよい。種々の実施形態において、液滴アクチュエータによる液滴の操作は、電極により媒介、例えばエレクトロウェッティングにより媒介、または誘電泳動により媒介、またはクーロン力により媒介されてもよい。本発明の液滴アクチュエータに使用され得る液体の流れを制御する他の方法の例としては、機械的原理(例えば外部シリンジポンプ、空気圧膜ポンプ、振動膜ポンプ、真空装置、遠心力、圧電/超音波ポンプおよび音響力);電気または磁気的原理(例えば電気浸透流、動電学的ポンプ、磁性流体プラグ、電気流体力学ポンプ、磁場を用いる引力または斥力および電磁流体力学的ポンプ);熱力学的原理(例えば気泡生成/相変化誘発体積膨張);他の種類の表面湿潤原理(例えばエレクトロウェッティングおよびオプトエレクトロウェッティング、ならびに化学的、熱的、構造的、および放射活性的に誘発される表面張力勾配);重力;表面張力(例えば毛細管現象);静電気力(例えば電気浸透流);遠心力を利用した流れ(コンパクトディスクに配置され、回転される基板);磁場(例えば周期的に振動するイオンが流れを引き起こす);電磁流体力学的力;ならびに真空または圧力差に基づいて操作するものなどの流体力学的流体圧力を含む装置が挙げられる。特定の実施形態において、2つ以上の上述の技術の組み合わせが、本発明の液滴アクチュエータに利用されてもよい。
【0028】
「液滴アクチュエータ」とは、液滴アクチュエータ上での液滴の任意の操作を意味する。液滴操作としては、例えば、液滴アクチュエータに液滴を負荷すること、液滴源から1つ以上の液滴を分配すること、1つの液滴を2つ以上の液滴に分裂、分離、または分割すること、任意の方向において液滴を1つの位置から別の位置に輸送すること、2つ以上の液滴を単一の液滴に融合または混合すること、液滴を希釈すること、液滴を混合すること、液滴を攪拌すること、液滴を変形させること、液滴を所定の位置に保持すること、液滴をインキュベートすること、液滴を加熱すること、液滴を蒸発させること、液滴を冷却すること、液滴を配置すること、液滴アクチュエータの外部へ液滴を輸送すること、本明細書に記載される他の液滴操作、および/または上述の任意の組み合わせが挙げられ得る。用語「融合する」、「融合している」、「混合する」、「混合している」などは、2つ以上の液滴から1つの液滴を生成することを述べるのに使用される。そのような用語が、2つ以上の液滴に関して使用される場合、2つ以上の液滴の1つの液滴への混合を生じるのに十分な液滴操作の任意の組み合わせが使用されてもよいことは理解されるべきである。例えば、「液滴Aと液滴Bとを融合する」ことは、液滴Aを静止液滴Bと接触するように輸送すること、液滴Bを静止液滴Aと接触するように輸送すること、または液滴AおよびBを互いに接触するように輸送することによって達成され得る。用語「分裂している」、「分離している」、「分割している」とは、得られる液滴の容積に対する任意の特定の結果、または得られる液滴の数に対する任意の特定の結果を表すことを意図しない(すなわち得られる液滴の容積は同じであっても、異なっていてもよいか、あるいは得られる液滴の数は2、3、4、5またはそれ以上であってもよい)。用語「混合する」とは、液滴内の1つ以上の成分のより均一な分布を生じる液滴操作を指す。液滴を「負荷する」操作の例としては、微小透析負荷、圧力支援による負荷、ロボットによる負荷、不動態による負荷、およびピペットによる負荷が挙げられる。液滴操作は電極により媒介されてもよい。一部の場合において、液滴操作は、表面上の親水性および/または疎水性領域の使用によって、ならびに/あるいは物理的障壁によってさらに容易にされる。
【0029】
「充填流体」とは、液滴アクチュエータの液滴操作基板に結合する液体を意味し、その液体は、液滴相が電極により媒介される液滴操作を受けるように液滴相と十分に混ざらない。充填流体は、例えば、シリコーンオイルなどの低粘度のオイルであってもよい。充填流体の他の例は、2006年12月11日に出願された「Droplet−Based Biochemistry」という発明の名称の国際特許出願第PCT/US2006/047486号;2008年8月8日に出願された「Use of additives for enhancing droplet actuation」という発明の名称の国際特許出願第PCT/US2008/072604号;および2007年5月17日に出願された「Electrowetting Devices」という発明の名称の米国特許出願公開第20080283414号(その全開示は本明細書に参照として援用される)に提供される。充填流体は、液滴アクチュエータの間隙全体を満たしてもよいか、または液滴アクチュエータの1つ以上の表面を覆ってもよい。充填流体は、導電性であっても、または非導電性であってもよい。「充填物質」は、凝固または硬化されたワックス、油脂またはオイルなどの凝固または硬化された充填流体である。
【0030】
磁性反応ビーズに関して「固定する」とは、ビーズが、液滴アクチュエータ上の液滴または充填流体内の所定の位置に実質的に保持されることを意味する。例えば、一実施形態において、固定されるビーズは、液滴上での分裂操作の実施を可能にするために、所定の位置に実質的に保持され、実質的に全てのビーズを有する1つの液滴およびビーズを実質的に欠く1つの液滴を生じる。
【0031】
「液体経路」とは、液体を誘導または流動させるのに適切な経路を意味する。液体経路は、管基板(例えば毛細管)内の内腔経路または固体基板内のチャネル、管、導管、穴、開口部、溝またはくぼみの経路など、基板内に規定されてもよい。液体経路は、開いていても(例えば液体が流れる表面内の溝またはくぼみ)、閉じていてもよい(例えば管)。多くの場合、液体経路は、液体リザーバーから、液体経路を通して、液滴アクチュエータの液滴操作間隙内、または液体リザーバーから、液滴経路を通して、第2の液体経路内などのように、1つのチャンバから別のチャンバへ液体を流すように規定される。
【0032】
「磁性反応」とは、磁場に対する反応を意味する。「磁性反応ビーズ」は、磁性反応物質を含むか、または磁性反応物質から構成される。磁性反応物質の例としては、常磁性体、強磁性体、フェリ磁性体、およびメタ磁性体が挙げられる。適切な常磁性体の例としては、鉄、ニッケルおよびコバルト、ならびにFe3O4、BaFe12O19、CoO、NiO、Mn2O3、Cr2O3、およびCoMnPなどの金属酸化物が挙げられる。
【0033】
磁性反応ビーズを洗浄することに関して、「洗浄する」とは、磁性反応ビーズと接触するか、または磁性反応ビーズと接触する液滴から磁性反応ビーズに曝露される1つ以上の物質の量および/または濃度を減少させることを意味する。物質の量および/または濃度の減少は、部分的、実質的に完全または均一に完全であってもよい。物質は、様々な物質の任意のものであってもよい。例としては、さらなる解析のための標的物質、ならびにサンプル、汚染物質、および/または過剰な試薬の成分などの不要な物質が挙げられる。一部の実施形態において、洗浄操作は磁性反応ビーズと接触する開始液滴で始まり、その液滴は物質の初期量および初期濃度を含む。洗浄操作は種々の液滴操作を用いて進行されてもよい。洗浄操作により、磁性反応ビーズを含む液滴が生じ得、その液滴は、物質の初期量および/または濃度未満の物質の全量および/または濃度を有する。適切な洗浄技術の例は、Pamulaら,2008年10月21日に付与された「Droplet−Based Surface Modification and Washing」という発明の名称の米国特許第7,439,014号(その全開示は本明細書に参照として援用される)に記載されている。
【0034】
用語「上部」、「底部」、「上」、「下」および「上に」は、液滴アクチュエータの上部および底部基板の相対的位置などの液滴アクチュエータの構成要素の相対的位置に関して本明細書全体を通して使用される。液滴アクチュエータは空間の方向に関わらず機能的であることは理解されるだろう。
【0035】
任意の形態の液体(例えば、移動しているか、または静止しているかに関わらず、液滴または連続体)が、電極、アレイ、表面のマトリクス「の上に」、「において」または「より上に」存在していると記載される場合、そのような液体は、電極/アレイ/マトリクス/表面と直接接触してもよいか、または液体と電極/アレイ/マトリクス/表面との間に入り込む1つ以上の層もしくは薄膜と接触してもよいかのいずかである。
【0036】
液滴が、液滴アクチュエータ「の上に」または「の上に負荷される」と記載される場合、液滴が、液滴アクチュエータを用いて液滴上での1つ以上の液滴操作を実施することを容易にする方法で液滴アクチュエータ上に配置され、液滴は、液滴からの特性またはシグナルの検出を容易にする方法で液滴アクチュエータ上に配置され、および/または液滴は液滴アクチュエータ上で液滴操作に供されることは理解されるべきである。
【図面の簡単な説明】
【0037】
(6.図面の簡単な説明)
【図1】図1は、液滴アクチュエータ基板上の熱サイクル経路を示す。
【図2】図2は、液滴アクチュエータ基板上に規定された一連の熱サイクル経路を示す。
【図3】図3は、液滴アクチュエータについての別の熱サイクルの配置を示す。
【図4】図4は、液滴間の二次汚染を減少または除去するための技術を示す。
【図5】図5は、複数の洗浄液滴がサンプル液滴間の経路に置かれることを除いて、図4に示す技術と実質的に同様の技術を示す。
【図6】図6は、洗浄液滴がサンプル液滴に対して1つの電極によってオフセットされることを除いて、図5に示す技術と実質的に同様の技術を示す。
【図7】図7は、洗浄液滴が細長いスラグ形状の洗浄液滴と置き換えられることを除いて、図4および5に示す技術と実質的に同様の技術を示す。
【図8】図8は、細長い洗浄スラグが、サンプル液滴の前後のサンプル液滴経路において洗浄液滴でさらに補われることを除いて、図7に示す技術と実質的に同様の技術を示す。
【図9】図9は、洗浄液滴が、サンプル液滴の前後に水平形状の洗浄液滴として提供されることを除いて、先行技術と実質的に同様の技術を示す。
【図10】図10は、経路間の充填流体の交換または充填流体の構成を防止する、細長い物理的障壁が、サンプル経路間に備えられることを除いて、図2に示す実施形態と同様の実施形態を示す。
【図11】図11は、充填流体が、保存温度で実質的に凝固し、操作に必要とされる温度で加熱器の近くで融解する物質として提供される実施形態を示す。
【図12】図12Aおよび12Bは、液滴間の二次汚染を減少または除去するための別の技術を示す。
【図13】図13は、液滴間の二次汚染を減少または除去するための別の技術を示す。
【図14】図14は、液滴アクチュエータ上の反応を開始するために表面積対体積比の原理ならびに図12Aおよび12Bに示す表面活性酵素複合体を使用する実施形態を示す。
【図15】図15は、充填流体を置き換える流路を構成する液滴アクチュエータの断面図を示す。
【図16】図16は、充填流体を置き換える流路を構成する図15に示すものと同様の液滴アクチュエータの上面図(図16A)および断面図(図16B)を示す。
【図17】図17は、充填流体を置き換える流路を構成する液滴アクチュエータの断面図を示す。
【図18】図18は、熱領域間で液滴を循環させるように配置される電極経路を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図19】図19は、本発明の液滴アクチュエータの電極の構成を示し、液滴が温度制御素子から離れて滞留され得るように、特定の経路が延長されることを除いて、図18に示す電極の構成と同様である。
【図20】図20は、本発明の液滴アクチュエータの電極の構成を示し、液滴を検出ウィンドウの存在下に輸送させることができるように配置される電極経路に沿って検出ウィンドウが提供されることを除いて、図19に示す構成と同様である。
【図21】図21は、2つ以上の熱領域を通る曲がった蛇行している電極経路を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図22】図22は、曲がった電極経路から液滴を輸送するように構成されるさらなる電極経路を含む2つ以上の熱領域を通る曲がった蛇行している電極経路を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図23】図23は、各々の熱領域内の曲がっている電極経路が、その領域内の液滴の滞留時間を長くするか、または短くするために、どのように延びているか、または短縮しているかを示す、本発明の液滴アクチュエータの電極の構成を示す。
【図24】図24は、曲がっている経路を含む、本発明の液滴アクチュエータの電極の構成を示し、曲がっている経路の1つ以上の曲がり角はアクセス経路に結合される。
【図25】図25は、図25の電極の構成と同じ電極の構成を示すが、電極の活性化を必要とせずに検出前に液滴を保存するための液滴滞留領域も含む。
【図26】図26は、熱制御領域の間に液滴を輸送するための電極経路のループを形成するように配置される電極を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図27】図27は、複数の電極経路のループを含む、本発明の液滴アクチュエータの電極の構成を示す。
【図28】図28は、電極経路のループおよび電極経路のサブループを含む、本発明の液滴アクチュエータの電極の構成を示す。
【図29】図29は、流路の熱サイクルの構成を例示する本発明の液滴アクチュエータの電極の構成を示し、小液滴は検出のためのより大きな液滴から分裂される。
【図30】図30は、電極アレイおよび電極アレイに配置されるサブサンプルの液滴を含む、本発明の液滴アクチュエータの電極の構成を示す。
【図31】図31は、サンプル液滴が熱サイクルされ、nサイクルごとの後、サブサンプル液滴が分配され、検出のために離れた位置に輸送される、本発明の実施形態を示す。
【図32】図32は、どのように小液滴が離れた位置に輸送され、配置されて、その後検出器によって操作され得るかを示す、実施形態を示す。
【図33】図33は、電極の構成が、反応液滴を配置するために使用される、実施形態を示す。
【図34】図34は、熱サイクル経路が半径方向に配置される、本発明の液滴アクチュエータの電極の構成を示す。
【図35】図35は、液滴輸送経路の複数のセットを有する電極アレイによって接続される複数の温度制御素子を有する電極の構成を示す。
【図36】図36は、先細の電極である電極の構成を示し、温度制御素子の間に液滴を輸送するために使用される。
【図37】図37は、本発明の液滴アクチュエータカートリッジの基板底部の写真である。
【図38】図38は、図37に示す基板底部の配置の図である。
【図39】図39は、カートリッジ上の増幅についての生のデータおよび正規化されたデータを示す。
【図40】図40は、BioRadIQ5からの正規化されたデータと比較した本発明のカートリッジからの正規化されたデータを示す。
【図41】図41は、1つの液滴アクチュエータ上の12の同時増幅反応の結果を示す。
【図42】図42は、図37および38に示されるカートリッジの配置を用いた別の熱サイクル実験の結果を示す。
【図43】図43は、増幅が検出と分離される実験に使用される液滴プロトコルを示す。
【図44】図44は、図43に関して記載される実験の結果を示す。
【図45】図45は、ビーズが、検出の間、検出ウィンドウに曝露されないように、磁性反応ビーズが、細長い液滴内の端側に引き付けられる本発明の実施形態を示す。
【図46A】図46Aは、液滴アクチュエータの領域の上面図を示し、検体の検出を向上するための磁性反応ビーズを操作する方法の特定の工程を一緒に示す。
【図46B】図46Bは、液滴アクチュエータの領域の上面図を示し、検体の検出を向上するための磁性反応ビーズを操作する方法の特定の工程を一緒に示す。
【図46C】図46Cは、液滴アクチュエータの領域の上面図を示し、検体の検出を向上するための磁性反応ビーズを操作する方法の特定の工程を一緒に示す。
【図46D】図46Dは、熱サイクル反応から得たリアルタイムPCRデータのプロットを示す。
【図47】図47A〜47Iは液滴アクチュエータの領域の断面図を示し、核酸増幅および検体についてのサンプル流体からの標的核酸の濃縮および回収プロセスにおける磁性反応捕捉ビーズの使用例を提供する。
【図48】図48Aおよび48Bは、加熱バーおよび挿入される加熱バーの側面図を示す。
【発明を実施するための形態】
【0038】
(7.詳細)
本発明は、液滴アクチュエータ装置、液滴アクチュエータを製造および使用するための技術ならびにシステムを提供する。本発明の実施形態は、液滴操作を実施するのに有用である。本発明の実施形態は、核酸を増幅するための液滴の熱サイクルなどの液滴の熱サイクルを利用するアッセイを実施するのに有用である。本発明の種々の熱サイクルプロトコルは、当該技術分野に対して様々な利点を有する。一部の場合において、そのプロトコルは、加熱器または液滴アクチュエータが熱サイクルされることを必要としない。他の場合において、同時または同じ部位で発生する核酸増幅および検出を必ずしも必要としない。さらに他の場合において、熱サイクルの間の反応に存在すべき検出試薬を必ずしも必要としなくてもよい。例えば、検出試薬は、熱サイクルされた液滴と、検出試薬を含む液滴とを混合することなどによって熱サイクルの後に加えられてもよい。一部の実施形態において、熱サイクルの間に生じる検出を必ずしも必要としない。すなわち、検出は、熱サイクルの完了の際、または熱サイクル後に生じてもよい。さらに他の場合において、測定されるべき1つより多い個々の反応からのシグナルを必ずしも必要としない。さらに、任意の特定の順序で決定されるべき任意の特定の数のサイクルと関連するシグナルを必ずしも必要としなくてもよい。本発明の任意の特定の熱サイクルプロトコルは、これらおよび他の利点のうちの1つ以上を有してもよい。
【0039】
本発明は、液滴アクチュエータおよび液滴アクチュエータ上でのPCRなどの核酸解析を実施する改良された方法を提供する。例えば、本発明は、増幅された標的物(例えば核酸)の検出を改良するために磁性反応ビーズを操作する方法を提供する。本発明はまた、増幅された標的物の検出を改良するために、液滴アクチュエータにより駆動される増幅プロトコルにおいて極性蛍光色素分子の使用を提供する。本発明はまた、液滴操作の間の核酸標的物およびPCR試薬の損失を実質的に減少および/または除去するための方法(例えば不動態化)を提供する。本発明はまた、液滴操作の間の液滴の安定性を改良するために、増加した間隙サイズを有する液滴アクチュエータを提供する。本発明はまた、増幅反応液滴間のキャリーオーバーおよび二次汚染を減少させる方法を提供する。本発明はさらに、サンプル流体から標的核酸を濃縮および収集するための方法を提供する。
【0040】
特定の実施形態において、実質的に同一の組成を含む複数の液滴が熱サイクルプロトコルに供されてもよく、異なる液滴または異なる液滴のセットが異なる数のサイクルに供される。液滴または液滴のセットが所定数のサイクルを完了すると、液滴は、その液滴に存在する増幅産物の量を決定するために検出に供されてもよい。曲線が、異なる熱サイクルのエンドポイントにおいて液滴の検出に基づいて生成され、オリジナルのサンプルに存在する標的物を定量化するために使用されてもよい。多くの代替が、本明細書に開示される本発明を考慮して本発明の範囲内で可能である。
【0041】
本発明の装置、技術およびシステムは、限定されないが、液滴アクチュエータ上の液滴と、他の液滴、充填流体、および/または液滴アクチュエータ表面との間の二次汚染の減少または除去、汚染を減少または除去するために使用する液滴アクチュエータ間の清浄を含む、当該技術分野に対する多くの利点を有する。
【0042】
(7.1 二次汚染の減少)
本発明は、液滴アクチュエータ装置および液滴操作を実施するための方法を提供する。本発明は、液滴アクチュエータ上の液滴と、他の液滴、充填流体、および/または液滴アクチュエータ表面との間の二次汚染ならびにキャリーオーバーを実質的に減少または除去することができる。本発明は、汚染を減少または除去するために使用する液滴アクチュエータ間の清浄を提供することができる。本発明は概して、PCRなどの核酸増幅反応を参照して記載されるが、その方法は、液滴間の二次汚染またはキャリーオーバーが問題となる任意の種類のアッセイに適切であることは理解されるだろう。
【0043】
図1は、液滴アクチュエータ基板上の熱サイクル経路100を示す。熱サイクル経路100は液滴操作領域105を備える。液滴操作領域105は第1の基板上に規定され、第1の基板に対してほぼ平行な様式で配置され、液滴操作を実施するための液滴操作間隙をその間に生成するように第2の基板も含んでもよい。液滴操作領域105は、液滴操作領域105に侵入するか、またはそこから出ていく汚染を防止するためにガスケット110により囲まれる。第1および第2の基板が存在する場合、ガスケット110は液滴操作間隙に設けられてもよい。ガスケット110は、液滴操作領域105において充填流体を保有するためのシールとして、および/または液滴操作領域105の液滴操作間隙の高さを規定するためのスペーサーとして役立ってもよい。
【0044】
ガスケット110が液滴操作領域105において流動性の充填流体を保有する場合、ガスケット110は、充填流体の汚染が液滴アクチュエータ表面上の他の液滴操作領域を汚染することを防ぐ。従って、第1および第2の基板が存在する場合、ガスケット110は液滴操作間隙に設けられ、液滴操作領域105における充填流体が、第1および第2の基板ならびにガスケットによって完全に囲まれるように配置されてもよい。種々のポートが、液滴操作領域105まで/から流体を負荷する/取り出す(非負荷する)ために、液滴操作間隙から液滴アクチュエータの外側、または液滴アクチュエータの別の領域まで任意の経路に沿って設けられてもよい。
【0045】
図示するように、液滴操作領域105は、2つの温度制御領域120Aおよび120B、ならびに遷移領域125を備える。温度制御領域120は、温度制御素子130Aおよび130Bに結合される。温度制御素子130は、それらの近くで充填流体の温度を制御する素子である。温度制御素子130は、電気を温度制御素子130に供給するために電気接点131に電気的に接続されてもよい。適切な温度制御素子130の例としては、加熱器およびヒートシンクが挙げられる。図示するように、2つの温度制御領域120Aおよび120Bが存在するが、任意の数の温度制御領域120が備えられてもよいことは理解されるだろう。
【0046】
温度制御領域120は遷移領域125に接続される。遷移領域125における電極115は、温度制御領域間の液滴を往復させるために利用されてもよい。一部の実施形態において、遷移領域125は、温度制御領域120の間の流体の循環を最小化するために、温度制御領域120より狭くてもよい。図示するように、単一の遷移領域125は2つの温度制御領域120に接続するが、温度制御領域120が複数の遷移領域125の接続を有してもよいことは理解されるだろう。さらに、任意の数の温度制御領域120が、任意の数の遷移領域125によって接続されてもよい。
【0047】
液滴操作領域105は、第1および第2の基板の1つまたは両方に結合される電極115を備える。電極115は1つ以上の液滴操作を実施するように構成される。電極115は、例えば矢印Aによって示される方向で、例えば液滴140を温度領域120Aと120Bとの間で前後に往復させるために使用されてもよい。
【0048】
図2は、液滴アクチュエータ基板上に規定される連続した熱サイクル経路100を示す。温度制御素子130は、連続して一緒に電気的に接続される連続したほぼディスク形状の加熱器として示される。しかしながら、温度制御素子130は、電源または別個の電源に並行に接続されてもよいことは理解されるだろう。さらに、温度制御素子130は組み合わされてもよい。例えば、素子130Aは、各々の温度制御領域120Aと結合される単一の温度制御素子130と置き換えられてもよい。同様に、素子130Bは、各々の温度制御領域120Bと結合される単一の温度制御素子130と置き換えられてもよい。
【0049】
図3は、液滴アクチュエータのための別の熱サイクルの配置300を示す。熱サイクルの配置300は、図1および2における熱サイクル経路100を規定する配置と同様である。しかしながら、熱制御素子305は、複数の液滴往復経路310A−310Bにわたる温度制御領域320Aおよび320Bを規定する。液滴往復経路310は、概して図1を参照して記載されるように、1つ以上の液滴操作を実施するように構成される液滴操作電極315から構成される。特に、液滴往復経路310は、矢印Aによって示される方向において熱領域320Aと320Bとの間で液滴340を往復させるために液滴操作電極315を利用する。熱サイクルの配置300はまた、熱領域320Aと320Bとの間で充填流体の循環を減少させるように構成される物理的障壁を備えてもよい。
【0050】
図4は、液滴間の二次汚染を減少または除去するための技術を示す。液滴往復経路105A、105B、105C、105Dおよび105Eが、液滴アクチュエータ基板上に設けられる。液滴は、矢印Aによって示される方向において熱領域(図示せず)の間で往復する。経路105A、105Cおよび105Eは、PCR液滴としてここで示されるサンプル液滴を含む。洗浄液滴Wは、サンプル液滴を含む経路間の経路105Bおよび105D上に置かれる。サンプル液滴が温度領域間で往復する場合、洗浄液滴はサンプル液滴経路間で往復する。洗浄液滴WはDNA分解酵素などの汚染物質を分解する化合物を含んでもよい。洗浄液滴Wは、DNA結合ビーズなどの汚染物質に結合する成分を含んでもよい。洗浄液滴Wは、サンプル液滴に対して同じ方向または反対方向において往復してもよい。それらは、サンプル液滴にすぐ隣接する位置および/またはサンプル液滴に対してオフセットする位置において往復してもよい。洗浄液滴Wは、必要に応じて、核酸増幅試薬を含んでもよく、それによって、それらはまた、洗浄液滴内で増幅された核酸の検出が、汚染物質が洗浄液滴内で検出可能であるという指標を与えるネガティブ反応コントロールとして機能する。
【0051】
図5は、複数の洗浄液滴がサンプル液滴間の経路に置かれることを除いて、図4に示す技術と実質的に同様の技術を示す。代替の実施形態において、複数の洗浄液滴経路は、各々の洗浄液滴経路において1つ以上の洗浄液滴を有するサンプル液滴経路間に配置される。
【0052】
図6は、洗浄液滴が、サンプル液滴に対して1つの電極によってオフセットすることを除いて、図5に示す技術と実質的に同様の技術を示す。
【0053】
図7は、洗浄液滴が細長いスラグ形状の洗浄液滴と置き換えられることを除いて、図4および5に示す技術と実質的に同様の技術を示す。
【0054】
図8は、細長い洗浄スラグがさらに、サンプル液滴の前後でサンプル液滴経路において洗浄液滴で補われることを除いて、図7に示す技術と実質的に同様の技術を示す。同様に、サンプル液滴の前後のサンプル液滴経路における洗浄液滴はまた、図1〜7のいずれかに含まれ得る。
【0055】
図9は、洗浄液滴が、サンプル液滴の前後で水平形状の洗浄液滴として与えられることを除いて、先行技術と実質的に同様の技術を示す。同様の実施形態において、洗浄液滴のスラグは、2X、3X、4X、5X、6X、7X、8X、9Xまたはそれより大きい液滴の任意の形状と置き換えられてもよい。
【0056】
図10は、経路または領域間の充填流体の交換または充填流体の構成を防止する、細長い物理的障壁1010A、1010B、1010Cおよび1010Dが、サンプル経路1005A、1005B、1005C、1005Dおよび1005Eの間に備えられることを除いて、図2に示す実施形態と同様の実施形態を示す。
【0057】
図11は、充填流体が、保存温度で実質的に凝固し、操作に必要とされる温度で加熱器の近くで融解する物質として与えられる実施形態を示す。加熱器1130は、所望の液滴操作経路1105の形状とほぼ対応する形状を有するように与えられる。4つの液滴操作経路1105A、1105B、1105Cおよび1105Dをここで示すが、任意の数の経路が設けられてもよいことは理解されるだろう。実質的に凝固した充填物質を加熱する際に、一部の充填物質は融解して、実質的に固体のままである充填物質により囲まれる流体が充填した液滴操作経路1105を形成し、それにより、汚染物質が1つの液滴操作経路1105から別の経路まで流動性の充填流体を介して移動することの障壁1120として役立つ。一実施形態において、充填物質は、核酸増幅を実施するのに必要とされる温度以下の温度で固体のままであり、核酸増幅を実施するのに必要とされる温度で融解するように選択される。
【0058】
図12Aおよび12Bは、液滴間の二次汚染を減少または除去するための別の技術を示す。液滴操作電極1210の経路またはアレイは、液滴アクチュエータ基板上に設けられる。液滴操作電極1210は1つ以上の液滴操作を実施するように構成される。図12Aに示すように、例えば、液滴操作電極1210は、液滴1220を輸送するために使用されてもよい。液滴1220は、汚染物質を潜在的に含む任意の液体であってもよい。すなわち、物質は別の液滴を汚染する可能性がある。例えば、液滴1220は、免疫学的検定、シークエンシングアッセイ、核酸増幅アッセイ、および/または酵素アッセイの液滴に使用される液滴などのアッセイ液滴であってもよい。汚染物質は、例えば、核酸増幅反応における核酸などの標的物質、免疫学的検定サンプルにおける非標的タンパク質などの非標的物質、および/または酵素などの試薬であってもよい。
【0059】
液滴1220は、多量の界面活性剤−酵素複合体1224を含んでもよい。一例において、複合体1224は、界面活性剤−DNase複合体(すなわち、DNA分解複合体)であってもよい。界面活性剤部分のために、実質的に全ての複合体1224は、液滴1220の表面に閉じ込められる。多量の複合体1224は、酵素部分(例えばDNase)の濃度が十分に低く、それによって、液滴1220中で実質的に不活性であるように選択されてもよい。
【0060】
液滴操作電極1210に沿った液滴1220の移動は、図12Bに示すように、特定の液滴操作電極1210上に残ったままになり得る微小液滴1226の形成を生じる場合がある。微小液滴1226は、DNAおよび複合体1224などの液滴1220の全ての成分を含んでもよい。結果として、微小液滴1226は、液滴操作電極1210に沿って生じ得る、後の液滴操作におけるDNA汚染の源となり得る。
【0061】
例えば、微小液滴1226は、液滴1220の直径の1/100であってもよい。より小さい直径の微小液滴1226は、十分により高い(例えば100倍高い)表面積対体積比を与える。高い表面積対体積比は、微小液滴1226中により高い濃度(例えば100倍高い)の複合体1224を与え得る。しかしながら、微小液滴1226中の複合体1224の高い濃度のために、微小液滴1226中でのDNAの急速な分解が達成され得、微小液滴1226によって引き起こされる二次汚染を実質的に防止または減少する。
【0062】
例として、酵素は、PAG−アルキルポリマーのポリアルカレングリコール(PAG)部分(例えばポリエチレングリコール(PEG)、ポリプロピレングリコールなど)に結合されてもよい。そのような結合を達成するための種々の方法は当該分野において公知である:米国特許第4,088,538号は、PEGに共有結合された酵素の酵素的に活性なポリマー−酵素結合体を記載し、米国特許第4,496,689号は、α−1プロテアーゼ阻害剤と、PEGまたはメトキシポリ(エチレングリコール)などのポリマーとの共有結合した複合体を記載し、Abuchowskiら,J.Biol.Chem.252:3578(1977)は、ウシ血清アルブミンのアミン基に対するmPEGの共有結合を記載し、米国特許第4,414,147号は、ポリ(エチレン無水コハク酸)などのジカルボン酸の無水物に対するインターフェロンの結合を記載し、国際特許公開第1987/00056は、インターフェロン−β、インターロイキン−2および抗毒素などのタンパク質に対するPEGおよびポリ(オキシエチル化)ポリオールの結合を記載している。このような文献の各々の全開示は参照により本明細書に援用される。
【0063】
酵素にPEGを結合する別の様式は、ペプチド上のグリコシル残基の酸化による。酸化された糖は、ペプチドにPEG部分を結合するための部位として利用される。例えば、国際特許公開第1994/05332号は、PEGを糖タンパク質に付加するためにヒドラジンまたはアミノ−PEGの使用を記載している。グリコシル部分は、後でアミノ−PEGに結合される、対応するアルデヒドに酸化される。国際特許公開第1996/40731号は、免疫グロブリン上のグリカンを酵素的に酸化し、次いで、グリカンとアミノ−PEG分子とを接触することによって免疫グロブリン分子に対するPEGの結合を記載している。界面活性剤は、結合が酵素の活性を過度に阻害しない、酵素の1つ以上の分子にて結合される。
【0064】
図13は、液滴間の二次汚染を減少または除去するための別の技術を示す。この実施形態において、液滴操作経路1310A、1310Bおよび1310Cは、液滴アクチュエータ基板上に設けられる。3つの液滴操作経路1310A、1310Bおよび1310Cをここで示すが、任意の数の経路が設けられてもよいことは理解されるだろう。経路1310A、1310Bおよび1310Cは、ここで、PCR液滴として示されるサンプル液滴を含む。液滴は、例えば矢印Aによって示される方向において熱領域間(図示せず)を往復する。液滴の往復は、充填流体1316中に分散され得る微小液滴1314の形成を生じ得る。微小液滴1314はDNAを含んでもよく、従って、他の液滴操作経路に対する汚染の源であってもよい。
【0065】
充填流体1316は多量の界面活性剤−酵素複合体1320を含む。この例において、複合体1320は、DNAを分解するために使用される界面活性剤−DNase複合体であってもよい。複合体1320は、経路1310A、1310Bおよび1310C間に障壁を与え、それによって、複合体1320は微小液滴1314中でDNAを分解し、その後、経路間の二次汚染を実質的に防止または減少する。
【0066】
代替の実施形態において、図12A、12Bおよび13に示す実施例は、液滴アクチュエータにおける他の物質の二次汚染を減少させるために適用されてもよい。例えば、界面活性剤−プロテアーゼ複合体は、液滴操作中のタンパク質のキャリーオーバーを実質的に防止または減少させるために使用されてもよい。
【0067】
図14は、表面積対体積比ならびに液滴アクチュエータ上での反応を開始するために図12Aおよび12Bに示す表面活性酵素複合体の原理を使用する実施形態を示す。
【0068】
この例において、リザーバー電極1410および液滴操作電極1412の経路またはアレイは、液滴アクチュエータ基板上に設けられる。多量の界面活性剤−酵素複合体1418を含む多量のサンプル流体1416は、リザーバー電極1410に与えられる。界面活性剤部分のために、実質的に全ての複合体1418は、サンプル流体1416の表面に閉じ込められる。多量の複合体1418は、酵素部分の濃度が十分に低く、それによって、サンプル流体1416中で実質的に不活性であるように選択されてもよい。
【0069】
リザーバー電極1410は、液滴操作電極1412上に単一のサイズの液滴1420を分配するように構成される。液滴操作電極1412は、単一のサイズの液滴1420を処理するために1つ以上の液滴操作を実施するように構成される。
【0070】
リザーバー電極1410上のサンプル流体1416の体積は、単一のサイズの液滴1420の体積より実質的に大きい。例えば、サンプル流体1416の体積は、単一のサイズの液滴1420の体積より約10倍〜約1,000倍大きくてもよい。サンプル流体1416と比べて、単一のサイズの液滴1420のより小さい体積は、実質的により高い表面積対体積比を与える。高い表面積対体積比は、単一のサイズの液滴1420中により高い濃度の複合体1418を与えることができる。単一のサイズの液滴1420中の高い濃度の複合体1418は、反応を開始するのに十分である。
【0071】
代替の実施形態において、リザーバー電極1410は他の液滴操作電極1412と置き換えられる。この例において、多量の界面活性剤−酵素複合体を含むサンプル液滴は、液滴操作を用いて分裂されて、その表面積対体積比を変化させて反応を開始してもよい。
【0072】
一部の実施形態において、液滴アクチュエータは、充填流体を置き換えるように構成される。一部の適用において、液滴アクチュエータの反復された使用を与えることは有用である。充填流体の汚染が問題となる場合、アッセイが作動している間に液滴アクチュエータにおける充填流体の一部または全てを置き換えることは有用であり得る。この技術は、例えば、増幅、シークエンシング、免疫学的検定、酵素アッセイなどのためのプロトコルを含む、広範な液滴プロトコルで有用であり得る。一実施形態において、充填流体は実質的に完全に置き換えられる。置き換えは自動化されてもよい。充填流体は各々の作動後に試験されてもよく、所定レベルの汚染が検出される場合、充填流体は置き換えられてもよい。置き換えは自動化されてもよい。一部の場合において、置き換えは、周期的、例えば1、2、3、4、5またはそれ以上の作動ごとの後に発生してもよい。
【0073】
図15は、充填流体を置き換える流路が構成される液滴アクチュエータ1500の断面図を示す。液滴アクチュエータ1500は、1つ以上の液滴操作を実施するように構成される電極1510を含む基礎基板1505を備える。液滴アクチュエータ1500はまた、液滴操作間隙1520を生じるように基礎基板1505から分離した上部基板1515を備える。液滴アクチュエータ1500は、液滴操作間隙1520を通して充填流体を流動するための側方開口部1525を備える。側方開口部1525は、外部の充填流体源または充填流体の送達位置上の1つ以上の対応する調整具1535と適合するように構成される調整具1530を備えてもよい。調整具1535は、外部の充填流体源(図示せず)から、導管1540を通り、調整具1530および1535を通り、液滴操作間隙1520への液体経路を規定する導管1540と結合されてもよい。調整具1535は、液滴操作間隙1520から、調整具1530および1535を通り、導管1540を通り、外部の充填流体の送達位置(図示せず)への液体経路を規定する導管と結合されてもよい。
【0074】
図16は、充填流体を置き換える流路が構成される同様の液滴アクチュエータ1600の上面図(図16A)および断面図(図16B)を示す。液滴アクチュエータ1600は、1つ以上の液滴操作を実施するように構成される電極1610を含む基礎基板1605を備える。液滴アクチュエータ1600はまた、液滴操作間隙1620を生じるように基礎基板1605から分離される上部基板1615を備える。液滴アクチュエータ1600は、液滴操作間隙を通して充填流体を流動するための側方開口部1625を備える。側方開口部1625は、導管1640から液滴操作間隙に、および/または液滴操作間隙から導管1640に液体を流動するように構成されるマニホルド1660に結合されてもよい。マニホルド1660は、外部の充填流体源から、導管1640を通り、マニホルド1660を通り、液滴操作間隙へと液体経路を規定するように、導管1640および流動性の充填流体源(図示せず)を備えて構成されてもよい。マニホルド1660は、液滴操作間隙から、マニホルド1660を通り、導管1640を通り、流動性の充填流体の送達位置へと液体経路を規定するように、導管1640および流動性の充填流体の送達位置(図示せず)を備えて構成されてもよい。マニホルド1660は、直接または間接的に導管1640に結合するのに適切な開口部1662を備えてもよい。マニホルド1660は、直接または間接的に液滴アクチュエータに結合するのに適切な開口部1664を備えてもよい。理想的には、開口部1664および開口部1625は、液滴操作間隙1620における充填流体を完全に置き換えることを容易にするために液滴操作間隙1620の断面と実質的に同様の形状を有する。1つ以上の通気口は、再充填の間に液滴操作間隙1620内に導入され得る気泡が放出できるように、液滴アクチュエータ1600の基板に、および/または基板間(例えばガスケット中)に存在してもよい。矢印xは、導管1640、マニホルド1660を通り、液滴操作間隙1620へ流れる流れの方向を示す。
【0075】
図17は、充填流体を置き換える流路が構成される液滴アクチュエータ1700の断面図を示す。液滴アクチュエータ1700は、液滴アクチュエータを通して流体を流動するための開口部が、液滴アクチュエータの底部に配置されることを除いて、液滴アクチュエータ1500と同様である。この配置構成は、液滴操作間隙を通して液体を流動するための構成要素を備えるシステムにおいて液滴アクチュエータの取り付けを容易にするために有用である。液滴アクチュエータ1700は、1つ以上の液滴操作を実施するのに構成される電極1710を含む基礎基板1705を備える。液滴アクチュエータ1700はまた、液滴操作間隙1720を生じるために基礎基板1705から分離された上部基板1715を備える。ガスケット1707は液滴操作間隙を密閉する。液滴アクチュエータ1700は、液滴操作間隙1720を通って充填流体を流動するための底開口部1725を備える。底開口部1725は、外部の充填流体源および/または充填流体の送達位置のための液体経路と結合する1つ以上の対応する調整具1735と適合するように構成される調整具1730を備えてもよい。一例として、適切なチップ−管の接続としては、NANOPORT(商標)アセンブリ(IDEX Corporation,Oak Harbor,WA)が挙げられる。1つ以上の調整具1735は、外部の充填流体源(図示せず)から、導管1740を通り、調整具1730および1735を通り、液滴操作間隙1720への液体経路を規定する導管1740と結合されてもよい。1つ以上の調整具1735は、液滴操作間隙1720から、調整具1730および1735を通り、導管1740を通り、外部の充填流体の送達位置(図示せず)への液体経路を規定する導管と結合されてもよい。
【0076】
本発明の種々の態様において、このように充填流体は、充填流体源から、液体経路を通り、液滴操作間隙を通って流動し、かつ、第2の液体経路中の液滴操作間隙から流動性の充填流体の送達位置まで出ていく。このように、充填流体は、少なくとも部分的に置き換えられてもよい。液滴操作間隙を通る充填流体の流れは、液滴操作間隙に最初に存在する充填流体と実質的に置き換えられてもよい。一部の場合において、充填流体は、液滴操作間隙中の充填流体を置き換えるのに十分な量で液滴操作間隙に流れてもよい。他の場合において、充填流体は、液滴操作間隙をフラッシュするために液滴操作によって流さてもよい。フラッシングの完了の際に、液滴操作間隙は、充填流体で充填されたままであり、操作しやすくなっている。特定の実施形態において、液滴操作間隙をフラッシュするのに使用される充填流体は、液滴操作間隙における清浄を高めるために加熱されてもよい。別の実施形態において、液滴操作間隙における汚染は、充填流体のフラッシングの間にモニターされてもよく、適切なレベルの清浄が達成されると、フラッシングは停止されてもよい。
【0077】
本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約50%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約75%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約90%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約95%を置き換えるために使用されてもよい。本発明の方法は、液滴操作間隙に最初に存在する充填流体の少なくとも約99%を置き換えるために使用されてもよい。
【0078】
本発明の他の態様において、洗浄流体は、液滴アクチュエータを洗浄するために液滴操作間隙を通って流されてもよい。洗浄後、新鮮な充填流体が液滴操作間隙に流されてもよい。例えば、溶媒が、新鮮な充填流体を液滴操作間隙に流す前に、液滴アクチュエータを洗浄するために液滴操作間隙を通して流されてもよい。液滴操作間隙の表面を過度に損傷せずに充填流体を除去するのに適切である溶媒が、選択されてもよい。一部の場合において、液滴操作間隙を充填流体に再充填する前に、液滴アクチュエータ間隙を乾燥することが望まれてもよい。一部の場合において、空気などの気体が、液滴操作間隙を充填流体で再充填する前に、液滴操作間隙を乾燥するために、液滴操作間隙を通して流されてもよい。
【0079】
種々の液体が、本発明の方法における洗浄流体として使用されてもよい。一態様において、選択され得る洗浄液体(その中で油および水の両方が可溶性である)は低沸点を有するものが良好な洗浄剤である。高沸点洗浄流体または洗浄流体成分もまた、使用されてもよい。一実施形態において、高沸点洗浄流体が使用され、その後、より低い沸点でリンスされる。冷却流体は、液滴アクチュエータを操作温度に戻すために、充填流体を充填する前に、液滴操作間隙を通して流されてもよい。
【0080】
適切な洗浄液体の例としては、アセトン、イソプロピルアルコール、エタノール、メタノール、テトラヒドロフラン、アセトニトリル、およびそれらの成分の1つ以上を含む混合物などの極性液体が挙げられる。これらの溶媒の混合物もまた、使用されてもよい。水溶性シリコーン油誘導体もまた、使用されてもよい。水ベースの洗浄液体もまた、使用されてもよい。好ましくは、カートリッジは、水ベースの洗浄液体の使用後、再充填する前に乾燥される。多成分混合物もまた、使用されてもよい。一実施形態において、洗浄液体は、水溶性を有する1つ以上の成分および油溶性を有する1つ以上の成分を含む。洗浄流体はまた、種々の触媒または酵素を含んでもよい。例えば、特定の汚染物質を分解する酵素が含まれてもよい。一部の場合において、油は空気または水と置き換えられ、次いで、液滴操作間隙が充填流体で再充填される。
【0081】
フラッシュアッセイにおいて、液滴輸送経路を洗浄するために誘因溶液を含む洗浄液滴を使用することは有用であり得る。基板を輸送するために使用されている電極経路は、同じ領域の一部または全てにわたって1つ以上の洗浄液滴を輸送することによって洗浄されてもよい。洗浄液滴はフラッシュ酵素を含んでもよい。例えば、洗浄液滴はルシフェラーゼまたはルシフェラーゼとATPを含んでもよい。一例として、アクリジニウムエステル(AE)が、本発明のフラッシュアッセイにおける化学発光標識として使用されてもよい。AEシグナルは、誘因溶液の添加時に、典型的に約10、9、8、7、6、5、4、3、2または1秒未満で高い値まで急速に上昇する。シグナルは、典型的に約60、30、20または10秒未満で非常に低い値まで低下する。これにより、検出ループおよび検出スポットでの汚染が除去され得る。しかしながら、汚染物質は洗浄経路および同じ経路上で実施されるその後のアッセイに潜在的に影響を与える可能性があるAEで結合された遊離の二次抗体によるインキュベーション領域にさらに存在する場合がある。AEで結合された抗体で汚染されている電極にわたるAE誘因溶液の1、2、3、4、5、6、7、8、9、10またはそれ以上の液滴を輸送することは、急速に減少する化学発光を生成し、実質的にAE汚染を除去する。
【0082】
種々の場合において洗浄流体は、酸性または塩基性、例えば高いpHに関してエタノール中の水酸化ナトリウムまたは水酸化カリウム、あるいは低いpHに関して酢酸または希塩酸であってもよい。一実施形態において、水に対する溶解度を有する溶媒、続いて第1の溶媒に対する溶解度を有する液体で開始する、多段階の洗浄手順が与えられる。
【0083】
加熱した溶媒が洗浄流体として使用されてもよい。温度は、液滴アクチュエータに対する過度な損傷を引き起こさずに、洗浄を高めるために選択されてもよい。好ましい温度は使用される物質に依存して変化する。一部の場合において、温度は、約30℃〜約125℃、好ましくは約60℃〜約115℃、より好ましくは約75℃〜約105℃の範囲である。好ましい温度は、使用される物質に依存して変化する。ポリカーボネートの上部基板が使用される場合、現在、最大温度は100℃近くである。ガラスの上部基板が使用される場合、最大温度は、例えば150℃以上のように非常に高くてもよい。
【0084】
一部の場合において、1つ以上の液滴アクチュエータの表面はコーティングを備え、洗浄液体は、洗浄の間にコーティングの非常に薄い層を除去するように選択される。例えば、1つ以上の液滴アクチュエータの表面は疎水性コーティングを備え、洗浄液滴は、洗浄の間に疎水性コーティングの非常に薄い層を除去するように選択される。従って、洗浄液体として使用するために選択され得る液体は、疎水性コーティングに対して非常にわずかな溶解度を有する。例えば、疎水性コーティングはフッ素化ポリマーを含んでもよい。洗浄液体は、完全にフッ素化された溶媒または部分的にフッ素化された溶媒などのフッ素化溶媒を含んでもよい。洗浄液体は、非常に低い濃度で別の溶媒に分散される完全にフッ素化された溶媒を含んでもよい。洗浄液体は、他の有機溶媒に対する溶解度を有する部分的にフッ素化された液体を含んでもよい。洗浄液体はまた、既存の疎水性コーティング上にさらなる薄い疎水性コーティングを堆積させるように選択されてもよい。薄層を除去することによって、またはさらなる量の薄層を堆積させることによって、洗浄液体が疎水性コーティングを変化させるかに関わらず、いずれの場合においてもその効果は、疎水性コーティングをその元の状態まで「再び新しくする」ことである。
【0085】
(7.2 並行流路)
図18は、本発明の液滴アクチュエータの一部の電極構成1800を示す。電極構成1800は、液滴アクチュエータの表面で液滴操作を実施するように構成される電極1805を備える。本発明の全ての電極構成と同様である電極構成1800は、より広範囲の電極構成および/またはより広範囲のマイクロ流体ネットワークの一部として提供され得る。液滴アクチュエータは、例えば、単一のサンプル液滴(図示せず)または別の液体源から同一のサブサンプル液滴を分配することによって、一連の同一の反応液滴1820を用いて液滴操作表面で他の液滴操作を分配および実施するために使用されてもよい。液滴操作電極1805は、一連の液滴輸送経路1806を提供するように構成されてもよい。液滴操作電極1805は、反応液滴1820をいくつかの液滴輸送経路1806の1つに輸送するために使用されてもよい。
【0086】
電極構成1800はまた、加熱器および/またはヒートシンクなどの1つ以上の温度制御素子1810と結合されてもよい。温度制御素子1810は、液滴作動表面で液滴を加熱および/または冷却するのに適切な任意の方法で構成されてもよい。温度制御素子1810は、液滴操作表面で温度領域を規定するために使用されてもよい。液滴アクチュエータが、液滴操作を実施するための液滴操作間隙を形成するために離間した2つの基板を備える場合、温度制御素子1810は、液滴操作間隙内に温度領域を規定するように構成されてもよい。液滴操作間隙が、流動性の充填流体で充填される場合、温度制御素子1810は、液滴操作間隙内の充填流体の種々の領域内に温度領域を規定するように構成されてもよい。液滴操作輸送経路1806において、液滴は、1つ以上の温度制御素子1810によって規定される温度領域の中で、液滴操作電極1805によって媒介される液滴操作を用いて輸送されてもよい。
【0087】
本発明の任意の実施形態はシステムの一部として構成されてもよい。例えば、システムは、本発明の任意の電極構成の電極の活性化を制御することによって、液滴アクチュエータで液滴操作を制御するコンピューターを備えてもよい。図18の液滴アクチュエータを備えるシステムは、異なる所定数のサイクルについて、各経路における液滴をサイクルするようにプログラムされてもよい。検出は熱サイクル経路自体でなされてもよいか、または液滴は検出のために別の場所に輸送されてもよい。例示した実施形態において、液滴は、その液滴にわたってセンサを走査することによる検出のためにAと印した経路に滞留される。各経路における熱サイクルが完了した場合に、検出がなされてもよい。あるいは、液滴の一部または全ては熱サイクル後に滞留され、センサは、Aと印した経路に沿って次々に液滴を走査してもよい。他の適切な検出アプローチが本明細書に記載される。
【0088】
図19は、本発明の液滴アクチュエータの電極構成1900を示す。構成1900は、液滴が温度制御素子1810から離れて滞留され得るように、経路1806が延長されていることを除いて、構成1800および図18と同様である。示した例において、上部の経路における液滴は5回のサイクルに供され、次の経路における液滴は10回のサイクルに供されるなどで、底部までで液滴は35回のサイクルに供される。任意の数の経路が設けられてもよく、各経路1806における液滴1820は、温度領域間で任意の数のサイクルの輸送に供されてもよい。所定数のサイクルの完了時に、各液滴は、検出に供され得る場合、Aと印した経路に沿って、そのそれぞれの経路1806における位置まで輸送されてもよい。検出は、例えば液滴からのシグナルの感知を含む。シグナル強度は、液滴における増幅された核酸を定量化するために使用されてもよい。各液滴は、その所定数のサイクルの完了時に迅速に検出に供されてもよい。あるいは、液滴は滞留されて、検出のためのセンサによって後の時間に走査されてもよい。
【0089】
図20は、本発明の液滴アクチュエータの電極構成2000を示す。電極構成2000は、検出ウィンドウ2005が、液滴が各経路1806から検出ウィンドウ内に輸送できるように配置される電極経路2010に沿って与えられることを除いて、概して図19に示す構成1900と同一である。検出ウィンドウは、液滴が検出のために輸送され得る任意の電極経路または任意の位置に配置されてもよい。図20はまた、3つの温度制御素子1810を備える実施形態を示す。もちろん、任意の数の温度制御素子が使用されてもよい。
【0090】
操作において、各液滴がその所定数のサイクルを完了すると、液滴は検出のための検出ウィンドウに輸送される。同様の実施形態において、各液滴がその所定数のサイクルを完了すると、液滴は滞留される。滞留は、液滴を所定の位置に輸送すること、および液滴をその位置に保存することを含む。その位置は、熱サイクル領域に対して液滴アクチュエータの別の領域であってもよい。その後、各液滴は検出のための検出ウィンドウに輸送される。センサは、検出ウィンドウに配置される液滴からシグナルを検出するように配置されてもよい。センサは、各液滴の1つ以上のシグナルを定量化するのに適切であり得る。検出ウィンドウは物理的ウィンドウを必要としない。その最も簡単な形態において、それは単にセンサの近くの領域であり、ウィンドウ内に部分的または完全に配置される液滴はセンサによる検出に感受性がある。
【0091】
一例において、温度領域はPCR混合物などの核酸増幅混合物の熱サイクルを実施するように規定される。増幅液滴は、サンプルに潜在的に存在する標的核酸を増幅するのに適切な試薬とともに核酸サンプルを含む。各々の経路は異なる数のサイクルについて熱サイクルに供される。液滴が所定数のサイクルに到達すると、その液滴は、例えば本明細書に記載される種々のスキームに従って、検出に供されてもよい。例えば、液滴は、増幅産物の検出のためのセンサに輸送されてもよい。
【0092】
一部の場合において、液滴のセットが連続して次々に熱サイクルされる。他の場合において、セット内の液滴が連続して熱サイクルされ、セット外の液滴が並行して熱サイクルされる。各セットは1つ以上の液滴を含んでもよい。適切なデータが、所定の許容可能な程度の確実性で開始サンプルに存在する増幅産物を定量化するために収集されると、熱サイクル反応は終了する。標的核酸がサンプルに存在しないか、または増幅されていないことが統計的に明らかである場合、熱サイクルを停止してもよい。増幅反応が、例えば異なる試薬または異なる液滴アクチュエータを用いて再び作動され得るように、新しいセットのサブサンプルの液滴がサンプルから得られてもよい。他の場合において、熱サイクル液滴のセットからの熱サイクルエンドポイントのセットが十分な曲線を示す場合、生成物を含む(曲線に従う)はずの1つ以上のサブサンプル液滴における生成物の欠如を示すが、新しいサブサンプルの液滴が分配され、熱サイクルプロトコルが、一部または全てのデータポイントについて繰り返されてもよい。
【0093】
並行アッセイとして図18〜20に示すようなアッセイにおいて、複数の液滴が並行に熱サイクルされる。言い換えれば、特定のグループにおける全てのサブサンプルの液滴は、同時に同じ熱領域に存在する。しかしながら、より簡単な実施形態において、全てまたは1つ以上のサブセットの液滴が、連続して熱サイクルされてもよいことは理解されるだろう。一部の場合において、サブセットの各メンバーは、以前のサブセットのメンバーの増幅の完了後に増幅されるが、異なるサブセットが並行して熱サイクルされる。
【0094】
例えば、単一の経路の熱サイクラーが設けられてもよい。第1の液滴は、5回、経路で熱サイクルされ、次いで検出に供されてもよく、第2の液滴は、10回、熱サイクルされ、次いで検出に供されてもよいなどである。十分なデータポイントのセットが、曲線を規定するために得られるまで、プロセスは繰り返されてもよく、その曲線から、サンプルにおける標的核酸の量が計算されてもよい。同様に、第1の液滴は35回、第2の液滴は30回、第3の液滴は25回などで熱サイクルされるなどで、第1の液滴は5回までサイクルされる。あるいは、全ての液滴は滞留されて、後の時間に連続または同時検出に供されてもよい。曲線はデータポイントから生成されることができ、サンプルにおける標的核酸の量はその曲線に基づいて計算され得る。一実施形態において、標的核酸が第1の液滴に検出される場合に限り、長いサイクルを最初に、次に短いサイクルの液滴を実施することは有用であり得る。
【0095】
同様の実施形態において、多くの熱サイクル経路は、熱サイクルのために選択される液滴の総数より少なく与えられてもよい。サブサンプルの液滴はセット内で処理されてもよい。セット内の各液滴は、ほぼ並行して熱サイクルされてもよいが、複数のセットが連続して熱サイクルされてもよい。例えば、5つの経路を備える液滴アクチュエータが、5セットにおいて35のサブサンプルの液滴、1、2、3...35を処理するために使用されてもよい。例えば、第1のセットの5つの液滴は、1サイクル、2サイクル、3サイクル、4サイクルおよび5サイクルについてのサブサンプルの液滴を含んでもよく、第2のセットの5つの液滴は、6サイクル、7サイクル、8サイクル、9サイクルおよび10サイクルについてのサブサンプルの液滴を処理してもよく、その後のセットは、11〜15サイクル、16〜20サイクル、21〜25サイクル、26〜30サイクルなどでサブサンプルの液滴を処理してもよい。
【0096】
代替の実施形態において、第1のセットの5つの液滴は、5、15、25、35および40サイクルについてのサブサンプルの液滴を含んでもよく、第2のセットの5つの液滴は、8、10、20、30および38サンプルについてのサブサンプルの液滴を含んでもよい。他のセットは、以前に実行した数の間のサイクル数で満たしてもよい。さらに、データはセットの間で解析されてもよく、十分なデータが、所定の範囲の統計的確実性までサンプル中の標的核酸を定量化するために得られると、サイクルは終了してもよい。同様に、標的核酸が存在しないか、またはサブサンプルの液滴中で増幅されないことが明らかな場合、サイクルは終了してもよい。後者の場合において、熱サイクルは、例えば異なる液滴アクチュエータおよび/または異なる試薬を用いて繰り返されてもよい。
【0097】
並行流路のサイクル技術において、全ての経路がサブサンプルの液滴に負荷されてもよい。液滴は、一体となって移動されてもよく、液滴が移動するのに正確な一体化が必要とされなくてもよい。例えば、一部の液滴は反対方向に移動されてもよい。液滴における増幅反応は、概して、異なる回数で停止されるが、一部の液滴は同じ回数サイクルされ、同時に停止されて、繰り返されてもよいことは理解されるだろう。反応は、温度制御領域(例えば図18に示す)において停止されてもよいか、または温度制御領域(図19および20に示す)から離れた位置に輸送されてもよい。液滴が検出領域にわたって輸送される場合、より少ないサイクル数を最初に受けて、続いて、より多いサイクル数を受けた液滴を輸送することは有用であり得る。このアプローチは、高濃度の標的核酸を含む液滴によって引き起こされる可能性がより高い、二次汚染の結果を防止または軽減するのに役立つ。
【0098】
並行流路の熱サイクル技術の種々の実施形態において、液滴が負荷され、滞留されてもよい。次いで、熱サイクルが同時に開始され、各サブセットの液滴について各液滴がその所定数のサイクルを終える場合、連続して終了されてもよい。別の実施形態において、液滴は負荷され、滞留されてもよく、各液滴または各サブセットの液滴についての熱サイクルは、連続して開始され、同時に終了されてもよい。プロトコルにおいて、1つ以上のサブセットの液滴がサブセットと一緒に開始し、連続して終了するが、液滴の他のサブセットは、連続して開始し、サブセットがまた、本発明の範囲内で可能である場合、それらの熱サイクルを完了する。さらに別の実施形態において、液滴または液滴のサブセットは、その液滴が負荷される場合、連続して負荷され、連続して開始されてもよく、液滴が熱サイクルを例えば連続してまたはグループにおいて完了する場合、終了してもよい。さらに別の実施形態において、液滴は分配され、並行して負荷される。
【0099】
別の実施形態において、液滴は、同時に熱サイクルを開始し、異なる数のサイクルを同時に完了することができる。このアプローチは、熱領域内または熱領域間の輸送速度および/または滞留時間を調整することを含み、その結果、液滴はそれらの異なる数のサイクルを同時に完了する。同様の実施形態において、液滴の種々のサブセットは、それらの異なる数のサイクルを同時に完了する。例えば、サイクル数1〜5は同時に完了されてもよく、サイクル数6〜10は同時に完了されてもよいなどである。
【0100】
さらに別の実施形態において、滞留時間は、個々の液滴の熱サイクルプロファイル内で異なるサイクル数で異なってもよい。例えば、初期サイクルはよりゆっくりでもよいが、後のサイクルはより速くてもよいか、またはその逆でもよい。さらに例示するために、液滴は35回サイクルされてもよく、各サイクルは前のサイクルよりわずかに速くてもよい。あるいは別の例として、液滴は35回サイクルされてもよく、サイクル1〜10は第1の速度で開始されてもよいが、サイクル10〜20は第2の速度で開始されるなどである。
【0101】
別の実施形態において、複数のサイクルが効果的な経路の使用のために経路の中で分配されてもよい。例えば、4つの利用可能な経路を備える熱サイクル液滴アクチュエータにおいて、液滴は以下のようにサイクルされてもよい。
・経路1:7
・経路2:1,6
・経路3:2,5
・経路4:3,4
【0102】
このように、経路1において、単一の液滴が7回サイクルされる。経路2において、第1の液滴は1回サイクルされ、続いて第2の液滴は6回サイクルされる。経路3において、第1の液滴は2回サイクルされ、第2の液滴は5回サイクルされる。最後に、経路4において、第1の液滴は3回サイクルされ、第2の液滴は4回サイクルされる。各経路は正確に7サイクル実施し、経路空間が効率的に利用され、液滴の全てをサイクルするのに必要とされる全時間を最小化する。さらに、例示において、少ないサイクル数を受けた液滴が最初に処理され、続いて多いサイクル数を受けた液滴が処理される。この方法において、少ない数のコピーの液滴は、同じ液滴アクチュエータの実際の場所で多い数のコピーの液滴に先行する。このアプローチは、第1の液滴によって残される残留物によって引き起こされる二次汚染の可能性を減少させる。もちろん、これは単純な例であり、本明細書を考慮して当業者によって理解されるように、任意の数の経路が任意の数の液滴とともに使用され、同様に組み合わされてもよい。
【0103】
(7.3 曲がっている流路)
図21は、本発明の液滴アクチュエータの電極構成2100を示す。電極構成2100は、供給源(示さず)からの液滴1815が、2以上の温度領域の間の前後で電極経路に沿って輸送できる方法で構成される電極1805を備える電極経路2105を備える。以前の例のように、温度領域は、加熱器またはヒートシンクなどの温度制御素子1810によって規定される。液滴1815は、温度制御素子1810によって規定される温度領域の間で前後に曲がっているか、または巻いている電極経路2105に沿って蛇行する。他の実施形態のように、液滴アクチュエータは、液滴操作を制御するシステムの一部として与えられてもよい。そのシステムは、熱サイクル領域を通して、検出のための位置に液滴を輸送するようにプログラムされてもよい。
【0104】
図22は、本発明の液滴アクチュエータの電極構成2200を示す。電極構成2200は、図21の電極構成2100と同様である。しかしながら、電極構成2200は、検出のための熱サイクル領域から離れた位置に液滴を輸送するための電極経路2205を備える。電極経路2205は、曲がっている電極経路2005から液滴を輸送するように構成される。
【0105】
各液滴は所定数のサイクルに関して温度領域を通してサイクルされてもよく、次いで検出のために離れた位置に輸送されてもよい。液滴は滞留されてもよく、次いでセンサによって走査されてもよい。例えば、液滴は線Aに沿って滞留されてもよく、センサは液滴を走査できる。あるいは、液滴は検出のために検出ウィンドウ2220に輸送されてもよい。センサは検出ウィンドウに配置される液滴を検出するように配置されてもよい。センサは、各液滴からシグナルを検出するのに適切であり得る。別の実施形態において、CCDカメラまたはLED−フォトダイオード対のアレイなどのアレイ検出器が、複数の液滴を同時に検出するために使用されてもよい。
【0106】
このように、一例において、PCR混合物などの核酸増幅混合物を含む液滴1815、および標的核酸を潜在的に含むサンプルが、電極1805によって規定される曲がっている経路2205に沿って分配され、輸送されてもよい。液滴1815は、温度制御素子1810によって規定される温度領域の間の前後を通る曲がっている経路2205に沿って液滴1815を輸送することによって熱サイクルされてもよい。
【0107】
各液滴は、所定数の回数、サイクルされてもよく、各液滴がその所定数のサイクルを完了する場合、各液滴は検出のための熱サイクル温度領域から離れた位置に輸送されてもよい。別の実施形態において、各液滴がその所定数のサイクルを完了する場合、各液滴は、熱サイクル温度領域の1つに、または検出のための液滴を維持するのに適切な温度を有する別の熱サイクル温度領域に輸送されてもよい。種々の実施形態において、液滴は滞留され、センサによって走査されてもよい。別の実施形態において、各液滴は検出ウィンドウに輸送されてもよい。このプロセスは液滴のセットを生成し、その各々は、所定の回数、熱サイクルされる。例えば、第1の液滴は5回熱サイクルされてもよく、第2の液滴は10回熱サイクルされてもよく、第4の液滴は15回熱サイクルされてもよい、などである。他の例のように、このプロセスは、標的物質を定量化するために適切なデータが得られると、停止されてもよい。
【0108】
曲がっている経路は、本質的に、温度領域間の前後またはジグザグに曲がっているか、または蛇行している任意の種々の形状をとってもよい。例えば、電極経路は、図4および6に示すように直角に沿って前後に蛇行してもよい。その経路は電極のより大きなアレイの一部を形成してもよく、その電極から曲がっているか、または蛇行している経路が選択されてもよい。曲がっている経路は、ジグザグ形状または曲線形状をとってもよい。曲がっている経路の各曲がり角はほぼ同じサイズであってもよいか、または曲がり角は異なるサイズであってもよい。
【0109】
液滴は経路の一端で曲がっている経路に継続的に注ぎ込まれてもよく、他端まで流れてもよい。一部の実施形態において、電極経路は、液滴を曲がっている経路上に、または曲がっている経路外に導くように配置されてもよい。例えば、一実施形態において、経路のあらゆる湾曲または曲がり角は、経路から液滴を取り除くため、および/または経路まで液滴を導入するための少なくとも1つの利用可能な電極経路を備える。一部の場合において、液滴は、利用可能な電極経路を通して経路に沿った異なる点で経路に供給されてもよい。一部の場合において、液滴は、利用可能な電極経路を通して経路に沿った異なる点で経路から除去されてもよい。他の実施形態において、液滴は、上部の基板、底部の基板、および/または上部基板と底基板との間の液滴操作間隙内の横方向の開口部などの任意の液滴アクチュエータ基板の開口部を通して経路上に導入され、および/または経路から除去されてもよい。
【0110】
一部の実施形態において、反応を同時に行うことは有用であり得る。そのような実施形態において、液滴は輸送サイクル時間と等しい速度で供給されてもよい。この実施形態において、進行中の反応の数は各輸送サイクルにて1つ増加する。この実施形態において、同時に行うとは、全ての液滴が同時に熱サイクルの同じ部分にあることを意味する。液滴の同時に行うことにより、輸送速度を変更させることが可能となる。液滴は、同時に熱サイクルの同じ部分内で停止され、インキュベートされてもよい。
【0111】
種々の実施形態において、液滴が、高サイクル数の液滴、すなわち高濃度の標的核酸を有すると予想され得る液滴によって以前に占められた電極を横切らないことを確実にすることは有用であり得る。
【0112】
一部の実施形態において、液滴の検出は曲がっている経路上の所定の位置で起こる。他の実施形態において、液滴は検出のために他の場所に輸送される。一部の実施形態において、検出のポイントまで曲がっている経路に沿って液滴を輸送することは有用であり得る。そのような実施形態において、一旦、全ての液滴の熱サイクルが完了すると、温度制御素子は、継続した熱サイクルを必要とせず、曲がっている電極経路に沿って液滴の輸送を可能にするように調節されてもよい。例えば、核酸変性加熱器は、最も低い起こり得る核酸変性温度以下までその温度を低下させることができる。この方法において、液滴は、増幅プロセスを継続せずに曲がっている経路に沿って蛇行し続けてもよい。キャリーオーバーが懸念される場合、液滴の流れの方向を反転させることが有用であり得る。すなわち、最初に少ないサイクル数を有する液滴を除去し、次に多いサイクル数を有する液滴を除去する。この方法において、液滴は、以前に受け入れられた多いサイクル数の液滴を有する電極を通過しない。
【0113】
別の実施形態において、反応は、それらが、増幅しない熱サイクル温度により輸送され続けることができるように不活性化されてもよい。あるいは、上記のように、液滴は、利用可能な電極経路を通して、検出のための液滴アクチュエータ上の別の位置に輸送されてもよい。
【0114】
図23は、本発明の液滴アクチュエータの電極構成2300を示す。電極構成2300は、温度制御素子1810によって規定される各熱領域内の曲がっている電極経路が、その領域における液滴の保持時間を長くまたは短くするために、どのように長く、または短くすることができるかを示す。
【0115】
例えば、一実施形態において、熱領域における曲がっている経路の曲がり角の長さ(すなわち熱領域における電極の数)は、液滴の進行方向において徐々に短くなってもよく、それによって、液滴が、電極から電極まで一定の速度で経路に沿って輸送される場合、サイクルは加速する。同様に、熱領域における曲がっている経路の曲がり角の長さ(すなわち、熱領域における電極の数)は、液滴の進行方向において徐々に長くなってもよく、それによって、液滴が電極から電極まで一定の速度で経路に沿って輸送される場合、サイクルは減速する。別の実施形態において、熱領域における曲がっている経路の曲がり角の長さ(すなわち熱領域における電極の数)は、第1のサイクルなどの特定のサイクル数にてより長いインキュベーション時間を与えるように変化させてもよい。
【0116】
従って、液滴は、2つの温度領域間の曲がっている経路に継続的に供給されてもよく、固定および一定の速度で輸送されてもよい。温度領域における滞留時間は、温度領域を通過するために横切らなければならない液滴の電極の数によって決定されてもよい。この実施形態において、異なる液滴が同時に温度サイクルの異なる段階で存在することができるという意味において、液滴は熱的に同時に行われなくてもよい。この実施形態は、実際の場所をより少なくする方法で液滴アクチュエータ上に電極を配置することによって液滴アクチュエータのサイズを減少させるのに有用であり得る。
【0117】
本明細書に記載される曲がっている電極構成または他の流路の構成は、概して、2つの温度領域を有するように例示されているが、任意の数の温度領域を有してもよいこともまた、留意されるべきである。
【0118】
図24は、本発明の液滴アクチュエータの電極構成2400を示す。電極構成2400は曲がっている経路2425を備える実施形態を示し、曲がっている経路2425の1つ以上の曲がり角はアクセス経路2420を備える。例示した実施形態において、アクセス経路2420は、曲がっている経路2425から、温度制御素子2405によって規定される温度制御領域に液滴を輸送するように構成される。温度制御素子2405は、例えば、検出前に増幅した液滴を維持するように構成されてもよい。例えば、液滴は、室温または検出前に液滴成分を保存するために選択された温度で維持されてもよい。このように、操作において、一連の液滴は、熱領域1810間に液滴を輸送するために長い曲がっている経路2425に輸送されてもよい。各液滴に関して、所定数のサイクルが達成されると、液滴はアクセス経路2420を通して曲がっている経路2425から外側へ輸送されてもよく、検出のため、または未検出物を保持するための保存領域に輸送されてもよい。
【0119】
図25は、本発明の液滴アクチュエータの電極構成2500を示す。電極構成2500は、構成2500が、電極の活性化を必要とせずに、検出前に液滴を保存するための滞留領域2505を備えるということを除いて、図24の電極構成2400と同様である。滞留領域2505は、例えば、種々の化学および/または物理的特性により規定されてもよい。例えば、滞留領域2505は、液滴操作間隙内または上部の基板または底部の基板(例えば障壁、壁、くぼみおよび/または突起)の物理的特性、および親水性領域などの化学特性により規定されてもよい。物理および/または化学的特性は、検出の間および/または検出に係る間に、所定の場所に液滴1815を保持するために共同してもよい。このように、操作において、一連の液滴は、熱領域(図示せず)の間に液滴を輸送するために長い曲がっている経路2425に輸送されてもよい。各液滴1815に関して、所定数のサイクルが達成されると、液滴1815は、アクセス経路2420を通して曲がっている経路2425から外側に輸送され、未検出物を保持するための滞留領域2505に輸送されてもよい。
【0120】
(7.4 ループ流路)
図26は、本発明の液滴アクチュエータの電極構成2600を示す。電極構成2600は電極ループ2605を形成するように配置される電極1805を備える。液滴1815は、熱サイクルを行うために熱領域を通ってループ中の電極経路に沿って輸送される。液滴は、ループに侵入し、所定の回数、ループの周りを回ることができ、次いでループから出ていく。入口および出口は、例えば、電極経路(図示せず)にアクセスすることによって、および/または液滴アクチュエータの外部から1つ以上の開口部を通して(例えば上部または底部の基板あるいは液滴アクチュエータ内の任意の他の経路を通して)与えられてもよい。
【0121】
輸送は一定であってもよい。すなわち、液滴は、一定の速度でループの周りを継続的に移動するか、または液滴は、異なる速度だが、実質的に同一の平均速度で移動することができる。一定の輸送の実施形態に関して、電極の配置は、各熱領域における必要な滞留時間を規定するように構成されてもよい。輸送は周期的であってもよい。すなわち、液滴は、一定の期間、熱領域に保持されてもよく、次いでループを通して他の熱領域に輸送されてもよい。
【0122】
ループは様々な液滴を効率的に収容でき、必要な場合、熱サイクルプロトコルの一部または全プロトコルについての最大数の液滴を負荷できる。ループの周りの液滴の輸送は、一方向であってもよいか、または二方向であってもよい(すなわち液滴輸送の方向は可逆的であってもよい)。検出はループ自体でなされてもよいか、または液滴は検出のためのループから離れた位置に輸送されてもよい。一定の循環は、液滴内の混合および熱均一性を増加でき、同じ経路を通る各液滴の循環は、熱領域内の空間の温度変化に起因する変動性を減少できる。
【0123】
図27は、本発明の液滴アクチュエータの電極構成2700を示す。電極構成2700は複数の電極経路ループ2705を備える。電極構成2700はまた、電極経路ループ2705上に、および/または電極経路ループ2705から液滴を輸送するためのアクセス電極経路2710を備える。熱サイクルプロトコルは1つ以上のループ2705を備えてもよい。例えば、一連の4つのループ2705は、複数の液滴が各ループでサイクルされる熱サイクルプロトコルを実施するために使用されてもよい。一般的に、液滴は、ループ上の1または2の空の電極部位によって分離されるべきであり、それによって、各ループ上の液滴の最大数は1/2nまたは1/3nと等しく、ここでnはループにおける電極の総数であり、nはループにおける電極の数である。検出はリアルタイムであってもよいか、またはサイクルの各々からのエンドポイントデータは、サンプルにおける産物を定量化するために使用される曲線を規定するように使用されてもよい。
【0124】
図28は、本発明の液滴アクチュエータの電極構成2800を示す。電極構成2800は電極経路ループ2805、および電極経路サブループ2810を備える。電極経路サブループ2810は、熱領域における液滴のための保持領域を与えるように構成される。構成2810および同様の構成において、プロトコルが実行でき、ここで、1つ以上の液滴は、輸送速度のみに基づいた有効な滞留時間より長い一定の期間、熱領域内に維持されることを必要とする。ループ2810の電極経路は、分岐構造または他の種類のループと置き換えられてもよいことは理解されるだろう。
【0125】
ループが存在する場合、特定の液滴がアクセスされるまで、保存がサブループ2810の周りに液滴を回転させることによってなされてもよい。次いで、特定の液滴は、電極経路ループ2805を通して他の熱領域に輸送されてもよい。他の熱領域において、特定の液滴は、ループ上に保存されてもよいか、またはループを通過し、出発熱領域に戻るように方向付けられてもよい。電極経路ループ2805および電極経路サブループ2810の周りの移動は、一方向であってもよいか、または二方向であってもよい。図18〜20に例示されるような直線状の電極経路を備える他の実施形態もまた、熱領域内にループ電極経路または分岐電極経路を備えてもよいこともまた、理解されるだろう。
【0126】
(7.5 等分している流路サイクル)
図29は、本発明の液滴アクチュエータの電極構成2900を示す。電極構成2900は熱サイクルの流路の構成を示し、ここで、小液滴は検出のためのより大きな液滴から分裂される。電極経路2900は、熱制御素子110によって規定される熱領域の間の前後に熱サイクル液滴2910を輸送するように構成される電極2907を備える第1の電極経路2905を備える。電極経路2905は、本明細書に記載されるような1つ以上の電極経路ループおよび/または曲がっている流路の電極配置と置き換えられてもよいことは理解されるだろう。電極構成2900はまた、熱サイクル液滴2910から小液滴2912を分配するように構成される電極2917を備える第2の電極経路2915を備える。電極2907は、概して、電極2917より大きく、従って、比較的大きな体積の液滴2910を支持し、その液滴2910から複数の小さな液滴の小液滴2912が分配されてもよい。電極経路Aは、熱サイクルの間の液滴2910が、熱制御素子1810によって規定される熱領域の間に輸送されることを示す。電極経路Bは操作を分配する部分を示し、ここで、液滴2910は、電極経路2915に近接する電極経路2905の電極上に位置する。電極経路2915上の電極2917は活性化され、それによって、液滴2910から細長い延長部の形成を引き起こす。電極経路Cは、電極経路2915上の小液滴2912の形成を引き起こすための1つ以上の中間電極2917の不活性化を示す。小液滴2912は検出に供されてもよく、ここで、小液滴2912は形成され、および/または検出のために離れて輸送されてもよい。
【0127】
一般的に、等分している流路アプローチにおいて、熱サイクル液滴2910のサイズは、検出のために取り除かれる小液滴2912のサイズの数倍である。一部の実施形態において、新しい液滴が、検出のための小液滴の除去後、熱サイクルしている液滴に追加されてもよい。例えば、追加された液滴は、熱サイクル反応のためのバッファーまたは1つ以上のさらなる試薬を含んでもよい。この方法において、熱サイクル液滴は一定の体積で維持されてもよい。図29に示す実施形態において、熱サイクル液滴2910由来の小液滴から分配するために使用される電極2917は、より小さい小液滴2912を収容するために、熱サイクル電極2907より小さい。しかしながら、代替の構成において、小液滴から分配するために使用される液滴は、熱サイクル液滴を輸送するために使用される液滴と同じサイズであってもよい。一部の場合において、熱サイクル液滴は、細長いスラグ形状の液滴として輸送されてもよく、小液滴は、例えばスラグの下にある中間電極を不活性化することによってスラグ形状の液滴の端部から分配されてもよい。
【0128】
関連したアプローチにおいて、サンプル液滴のセットが熱サイクルされ、小液滴が各サイクル後、そのセットの1つのメンバーから除去される。このアプローチにおいて、セットにnのサンプル液滴が存在する場合、小液滴はnサイクル毎に液滴から除去されてもよい。このアプローチは、より小さい種類の液滴サイズを用いて熱サイクルプロトコルを支持するという利点を有する。例えば、4倍数の液滴の10の並行反応が、40の熱サイクルのエンドポイントを与えるために使用されてもよい。
【0129】
別の関連した実施形態において、より大きな液滴が、上記のように熱サイクルされ得るより小さな液滴に分裂される前に、数回、熱サイクルされてもよい。このアプローチは、複数の小液滴の熱サイクルを含む本明細書に記載される任意の実施形態において有用であり得る。この方法において、産物の開始濃度(例えば核酸産物)が規定されてもよく、それによって、各々の小液滴は、小液滴における増幅を確実にするための十分な産物を含む。従って、本発明は、電極の複数のパッドが、図29に示す電極経路2905および2915の結合と同様の方法で互いに結合される、種々の実施形態を含む。例えば、一実施形態において、電極経路には、大きな電極を有する第1の経路と、中間のサイズの電極を有する第2の経路と、小さなサイズの電極を有する第3の経路が備えられる。別の例として、配置は、大きなサイズの電極を有する第1の電極経路を備えてもよい。この第1の電極経路は、同様のサイズの電極を有する2つ以上の第2の電極経路と結合されてもよい。第2の電極経路の各々は、さらに小さなサイズの電極を有する1つ以上の第3の電極経路と結合されてもよい。最初に、大きな液滴は第1の電極経路上で熱サイクルされ、次いで2つ以上の第2の電極経路上に分配されてもよい。2つ以上の第2の電極経路から、液滴は、検出のための1つ以上の第3の電極経路上に分配されてもよい。第2の電極経路上の液滴は熱サイクルされてもよく、続いて各々の所定数の熱サイクルがされ、小液滴は検出のための1つ以上の第3の電極経路上に分配されてもよい。
【0130】
(7.6 バッチサイクル)
一実施形態において、本発明は一連の検出バッチ熱サイクル技術を与える。このアプローチにおいて、サブサンプル液滴はサンプルから生成され、温度制御領域に配置されてもよい。温度制御素子は、所定の熱サイクルプロトコルに従って温度制御領域において温度をサイクルすることができる。1つの液滴は、所定数のサイクル毎の後に検出されてもよい。このように、例えば一実施形態において、異なる液滴が各サイクルの後に検出される。この方法において、各液滴は一度のみ検出に供される。データは、サンプルに存在する標的物質を定量化するのに適切な曲線を生成するために使用されてもよい。
【0131】
図30は、本発明の液滴アクチュエータの電極構成3000を示す。液滴アクチュエータ3000は電極アレイ3005と、電極アレイ3005に配置されるサブサンプル液滴3010を備える。サブサンプル液滴3010は、単一のサンプル液滴(図示せず)から分配されてもよい。サブサンプル液滴3010は、(存在する場合)液滴操作間隙の外部まで電極経路(図示せず)または多くの開口部(図示せず)のうちの1つを通して電極アレイ3005上に負荷されてもよい。
【0132】
1つ以上の熱サイクル温度制御素子3015は、例えばアレイの下および/またはアレイの上にある、アレイ3005に結合される。熱サイクル温度制御素子3015は、電極アレイ3005上の熱サイクル液滴3010を加熱し、能動的または受動的に冷却する。熱サイクルの間、センサは液滴3010からの信号を検出するために液滴3010上を通過する。例えばセンサは、各サイクル後、単一の液滴を検出するのに十分な速度で液滴3010上を通過してもよい。一般的に、センサは、nサイクル毎に単一の液滴を検出するのに十分な速度で液滴3010を通過してもよい。ここで、nは、所定のレベルの統計的有意性にて液滴中の標的産物を定量化するのに有用な曲線を生成するために十分なエンドポイントを達成するのに選択される数である。代替の実施形態において、2つ以上のセンサが使用されてもよい。さらに別の実施形態において、CCDカメラなどのアレイ検出器、またはLED−フォトダイオード対のアレイが、複数の液滴を同時に検出するために使用されてもよい。
【0133】
同様の実施形態において、サブサンプル液滴は温度制御領域に配置されるサンプルから生成されてもよい。温度制御素子は、所定の熱サイクルプロトコルに従って温度制御領域において温度をサイクルすることができる。熱サイクルの各nラウンド後、1つ以上の液滴が検出のための温度制御領域から離れた位置に輸送されてもよい。例えば、輸送は電極経路に沿って液滴操作によって実施されてもよい。液滴は、それらが温度制御領域から離れるか、またはそれらが後の時間での解析のために滞留され得る場合、検出されてもよい。
【0134】
関連したアプローチにおいて、液滴は、n回の熱サイクル毎の時間に1回以上、熱サイクルユニット上に連続して輸送されてもよい。次いで、検出は最後のサイクルの後に実施されてもよい。例えば、液滴のアレイは、連続して、同時にまたは最後のサイクルの後にサブセットにおいて画像化されてもよく、検出からのデータは、元のサンプル中の標的産物を定量化するための曲線を生成するために使用されてもよい。
【0135】
図31は、本発明の別の電極構成3100を示し、ここで、サンプル液滴は熱サイクルされ、nサイクル毎の後、サブサンプルの液滴は分配され、検出のために離れた位置に輸送される。例示した実施形態において、リザーバー3105はガスケット3110によって規定される。温度制御素子3115はリザーバー3105の下部にある。ガスケット3110における開口部3120は、リザーバー3105から離れてサブサンプル液滴3130を輸送するための液体経路を与える。電極経路3125は、サンプル液滴3135からサブサンプル液滴3130を分配するための手段を与える。分配されたサブサンプル液滴3130は検出に供されてもよい。例えば、それらは、形成時にすぐ検出に供されてもよいか、またはそれらは後の時間での検出のために離れた位置に輸送されてもよい。
【0136】
同様の実施形態において、液滴3135は、液滴アクチュエータの液滴操作間隙に対して外側のリザーバーに与えられてもよい。液滴3135はリザーバー内で熱サイクルされてもよく、小液滴3130は、任意の種々の液滴分配技術を用いてリザーバーから液滴操作間隙内に分配されてもよい。例えばリザーバーは、リザーバーから、1つ以上の電極に近接する液滴操作間隙に延びる液体経路に結合されてもよい。電極は、熱サイクルの各nサイクルの後、液滴を液滴操作間隙に分配するために使用されてもよい。次いで、分配された液滴は、さらなるアッセイ工程および/または検出に供されてもよい。
【0137】
図32は、図31の電極構成3100と同様の実施形態を示す。電極構成3200は、小液滴3130が、どのように、離れた位置に輸送され、配置され、続いて検出器によって操作され得るかを示す。例えば、検出器は、Aと印した経路などの経路に沿って連続して各液滴を検出してもよい。あるいは、本明細書に記載されるこの実施形態および他の実施形態において、全ての液滴は、例えばCCDカメラまたはLED−フォトダイオード対のアレイなどのアレイ検出器を用いて一緒に画像化されてもよい。
【0138】
(7.7 反応クエンチング技術)
図33は、電極構成3300が、反応液滴3305を配置するために使用される実施形態を示す。反応液滴3305は、本明細書の特定の他の実施例に示されるように、熱サイクル液滴(例えば増幅準備液滴)であってもよいか、または反応が経時的に生じる一部の他の反応であってもよい。温度制御素子3310は熱サイクルまたは反応液滴3305の温度制御を与えられてもよい。反応クエンチング液滴3315は、反応液滴3305と接触するように輸送されてもよい。反応クエンチング液滴3315は、反応液滴3305において生じる反応をクエンチ、または後でクエンチするための1つ以上の試薬を含んでもよい。一実施形態において、反応液滴3305における反応は実質的に同時に開始され、反応液滴3305は連続して反応クエンチング液滴3315と混合される。クエンチング後、混合された液滴は、反応速度論の曲線の指標を生成するためのさらなるアッセイ工程および/または検出に供されてもよい。別の実施形態において、反応液滴3305における反応は連続して開始され、反応液滴3305は反応クエンチング液滴3315と実質的に同時に混合される。同様に、クエンチング後、混合された液滴は、反応速度論の曲線の指標を生成するためのさらなるアッセイ工程および/または検出に供されてもよい。中間プロセスにおいて、反応は連続して開始され、連続してクエンチされる。
【0139】
反応液滴が反応クエンチング液滴と混合される本発明の任意の種々の実施形態において、反応液滴は反応クエンチング液滴と接触するように輸送されてもよく、反応クエンチング液滴は反応液滴と接触するように輸送されてもよく、ならびに/または反応液滴および反応クエンチング液滴は互いに輸送されてもよい。クエンチング液滴は必要な場合、送達されてもよいか、または反応液滴とともに配置され、所定の計時プロトコルに従って混合されてもよい。
【0140】
熱サイクル増幅プロトコルにおけるこのアプローチの1つの利点は、クエンチ後、液滴が熱サイクルに供され続け得るが、増幅はクエンチング液滴との混合の結果として停止することである。
【0141】
関連した実施形態において、出願人は、核酸増幅などの特定の反応が、静電場を用いてクエンチされ得ることを発見した。例えば、反応は、電圧信号を下部の電極または液滴に近接する別の電極に印加することによって停止されてもよい。印加される電圧信号は、反応を停止または実質的に停止するのに十分であるように選択されてもよい。例えば、増幅反応を停止するのに必要とされる電圧信号は、1つの電極から次の電極に液滴輸送を実施するのに必要とされる電圧信号に関する電圧信号を単に維持されてもよい。従って、例えば核酸増幅反応は、核酸増幅液滴の輸送を停止させ、反応を停止させるのに十分な期間、活性化された電極上に液滴を保持することによって停止されてもよい。電圧レベル、サイクルおよび/または電圧の種類もまた、増幅反応が実質的に停止されるまで、調節されてもよい。一部の場合において、電極構成は特異的不活性化部位を含んでもよく、その部位に電極が存在し、反応を不活性化するように選択される特性を有する。さらに、増幅が電極に配置される液滴を用いて実施される実施形態において、一部の場合において、増幅の間に増幅準備液滴の下部にある電極上の電圧を不活性化または制御することは有用であり得、それによって、電極は液滴の継続している増幅を過度に妨げない。
【0142】
別の関連した実施形態において、液滴アクチュエータは、液滴操作電極に近接して位置する1つ以上の阻害剤を含んでもよい。例えば、阻害剤は液滴アクチュエータの表面で乾燥された乾燥阻害試薬であってもよい。別の例として、阻害剤はPCRを阻害することが知られている白金または窒化物などの物質であってもよい。例えば、阻害剤は、液滴が反応を停止させるためにパッドまたはワイヤと接触して輸送され得るように配置される白金パッドまたはワイヤに曝露されてもよい。一部の実施形態において、阻害剤は、液滴アクチュエータ上の種々の電極部位に配置されてもよい。
【0143】
操作において、反応液滴は、連続して、阻害剤と接触して輸送されてもよく、液滴は、連続して、反応が停止される時間における反応のエンドポイントの曲線の指標を生成するためにさらなるアッセイ工程および/または検出工程に供されてもよい。同様に、反応は連続して開始され、阻害剤のアレイと接触して同時に輸送されてもよい。別の実施形態において、反応は連続して開始されてもよく、液滴は、阻害剤と接触して連続して輸送されてもよい。任意の事象において、液滴は異なる反応時間または熱サイクルを受ける液滴を含み、液滴中の反応産物は、時間またはサイクルに関する反応の進行の曲線の指標を生成するために、さらなるアッセイ工程および/または検出工程に供されてもよい。
【0144】
(7.8 反応時間経過のサンプリング)
本発明は、液滴アクチュエータが提供され、反応液滴が液滴アクチュエータ上に提供される、関連する実施形態を提供する。反応液滴は、1つ以上の反応が反応液滴内で起こるという特徴がある。例えば、反応としては、化学反応、生化学反応および/または生物学的反応が挙げられる。反応が進行する場合、1つ以上の小液滴は反応液滴から分配される。各々のこのような小液滴は、反応を停止させる方法で処理されてもよい。例えば、小液滴の温度は、反応が停止または実質的に停止する温度に調節されてもよい。別の例として、各々の小液滴は、反応をクエンチする試薬を含む試薬液滴と混合されてもよい。各々の小液滴は異なる時間で親反応の液滴から除去されてもよく、小液滴は、反応の時間経過を示す曲線を生成するためにさらなる解析に供されてもよい。関連した実施形態において、小液滴における反応はクエンチされないが、各々の小液滴は、親反応の液滴から分配された後、迅速に検出に供される。さらに別の実施形態において、親液滴は多数の小液滴に細分されてもよく、小液滴は、各々の小液滴が異なる時間で検出に供される検出プロトコルに供されてもよい。収集したデータは、反応速度論の曲線の指標を生成するために使用されてもよい。一実施形態において、小液滴の分配は、電極、例えばエレクトロウェッティング媒介、誘電泳動現象媒介液滴分配によって媒介される。
【0145】
関連した実施形態において、反応速度は、異なる時間で一連の反応を開始するために液滴アクチュエータ上の液滴を混合し、続いて、同時に液滴を画像化し、反応速度論の曲線の指標を生成するためにデータを用いることによって測定される。さらに別の関連した実施形態において、反応速度は、異なる時間で一連の反応を開始するために液滴アクチュエータ上の試薬液滴を混合し、続いて、異なる時間でセンサを用いて反応液滴を走査し、反応速度の異なる反応時間の指標に基づいて曲線を生成することによって測定される。これらの任意の実施形態において、特定の問題のある反応の必要性に依存して、反応は検出前に停止されても、されなくてもよい。
【0146】
(7.9 さらなる熱サイクルの実施形態)
種々の特性を有するさらなる様々な実施形態は、本発明の範囲内であり得る。少しの例を以下に示す。
【0147】
図34は、本発明の液滴アクチュエータの電極構成3400を示し、ここで、熱サイクル経路3425は半径方向に配置される。中心の温度制御素子3410は環状である。温度制御素子3410は、ディスク形状、六角形、八角形などの様々な代替の形状であってもよい。例示した実施形態において、熱サイクル経路3405は温度制御素子3410から外側に放射状に広がる。外側の温度制御素子3415もまた設けられる。電極経路3425は、中心の温度制御素子3410から外側の温度制御素子3415まで延びる。電極構成3400は、より大きな電極構成の一部として与えられてもよい。液滴は、液滴アクチュエータの外部に対する開口部を介して、および/または他の電極経路(図示せず)を介して電極経路3425に導入されてもよいか、あるいは上部の基板を欠く開口系において、液滴は単に液滴操作表面上に配置されてもよい。外側の温度制御素子3415は、ワイヤ3416によって接続される個々の温度制御素子として例示される。しかしながら、外側温度制御素子3415は異なる形状であってもよく、例えば外側温度制御素子3415は、単一の環状の外側温度制御素子、例えば円形、六角形、八角形、または他の環構造を有する環と置き換えられてもよいことは理解されるだろう。
【0148】
図35は、複数のセットの液滴輸送経路3515を有する電極アレイによって接続される複数の温度制御素子3510を有する電極構成3500を示す。リザーバー電極3520もまた、液滴輸送経路3515に隣接して与えられる。温度制御素子3510は同じであってもよいか、または異なっていてもよい。温度制御素子3510は温度制御領域を規定するために使用されてもよい。温度制御領域における温度は同じであってもよいか、または異なっていてもよい。
【0149】
図36は、電極構成3600を示し、ここで、先細(例えば細長い三角形または楔形)の電極3610および3615が、温度制御素子3620と3526との間に液滴を輸送するために使用される。電極3615は不活性化されるが、電極3610の活性化により、温度制御素子3620に対して液滴が輸送される。電極3615の活性化および電極3610の不活性化により、温度制御素子3620から温度制御素子3625に戻るように液滴が輸送される。この種の電極構成または2008年10月17日に出願された「Droplet Actuator Structures」という発明の名称の国際特許出願第PCT/US2008/80275(その全開示は本明細書に参照として援用される)に記載されるもののような電場勾配を利用する他の構成も使用されてもよい。
【0150】
図37は、本発明の液滴アクチュエータカートリッジの底部基板3700の写真である。この配置(プリントされた回路基板上の銅)は、サンプルおよび試薬を分配するためのリザーバー電極3710を備える。この配置は、温度領域3740の間に液滴を循環させるための電極ループ3716を備える。この配置は、試薬および/またはサンプル液滴を用いて液滴操作を実施するための輸送経路3720を備える。例えば、輸送経路3720は、リザーバー電極3710と電極ループ3716および/またはサンプル調製操作および/または他の液滴操作との間の試薬および/またはサンプル液滴を輸送するために使用されてもよい。この配置は検出電極3718を備える。検出電極3718は、電極ループ3716および輸送経路3720から構成される他の液滴操作電極より大きい。液滴アクチュエータカートリッジは、電極の構成を覆い、液滴操作を実施するのに適切な液滴操作間隙を形成するために底部基板から分離される上部の基板(図示せず)を備えてもよい。上部の基板は、液滴操作間隙における液滴に対して電気的に露出される参照電極または接地電極を備えてもよい。適切な上部基板の例としては、9月4日,3708に出願された「Droplet Actuator with Improved top Substrate」という発明の名称の国際特許出願第PCT/US2008/075160号に記載されるものが挙げられる。液滴操作間隙は、液滴操作に供される液滴と混合する流動性の充填流体などの流動性の充填流体で充填されてもよい。
【0151】
図38は、図37に示される底部基板3700の配置の図である。この図は、カートリッジ上に熱サイクル温度領域を作製するのに使用される加熱バー3808の配置を示す。
【0152】
図39〜43は、図37および38に示すカートリッジ配置を用いた熱サイクル実験の実施の結果を示す。
・MRSA/Eva Greenシステム:
標的物:mecA遺伝子の176bpフラグメント(遺伝子1つにつき8〜10のコピー)
サンプル:バッファー中のメチシリン耐性黄色ブドウ球菌(MRSA) gDNA(ATCC#700699D−5)
・定量実験:
100,000〜1コピーのMRSAゲノム(反応物中に300pg〜3fg gDNA)
同じ量のDNAを、660nLの液滴アクチュエータ反応物およびBioRad 50μl反応物(75倍の濃度差)に加えた。
・PCR混合物:
Eva Green色素
白金Taq
・充填流体
ヘキサデカン
・熱プログラム(典型的):
Hotstart:60s@95、
40サイクル:(10s 95C、20s@60C)
【0153】
比較実験を、液滴アクチュエータおよび市販のリアルタイムPCRシステム(BioRad IQ5)で実施した。インプットゲノムDNAの量は、1〜100,000MRSA細胞におけるDNAの量と対応するように変化させた。CT値は以下のようであった。
【0154】
【表1】

【0155】
図39は、カートリッジ上での増幅にいての生のデータおよび正規化したデータを示す。
【0156】
図40は、BioRadIQ5からの正規化したデータと比較した本発明のカートリッジからの正規化したデータを示す。
【0157】
図41は、1つの液滴アクチュエータでの12の併発反応(4つの濃度の各々の3つの複製)の結果を示す。各セットの複製を単一のループで増幅させた。
【0158】
図42は、図37および38に示すカートリッジ配置を用いる別の熱サイクル実験の結果を示す。実験の詳細は以下の通りである。
・Candida albicans/Taq Manシステム
−標的物:18SリボソームRNA遺伝子の172bpフラグメント(1つのゲノムにつき70〜100コピー)
−サンプル:Candida albicans gDNA(ATCC#10232D−5)
・PCR混合物
−TaqManプローブ(FAM−BHQ)
−Bio−Rad iTaq
・充填流体
−シリコーン油
・熱プログラム
−Hotstart:120s@95C
−40サイクル(15s 95C、60s@60C)
図42における定量は、gDNAのインプット量の生物またはゲノム等価物の数による。
【0159】
図43は、増幅が検出から分離される実験に使用される液滴プロトコルを示す。同一の液滴の集団は色素を用いずに熱サイクルした。周期的に、1つの液滴を除去し、色素液滴と合わせ、検出に供し、次いで廃棄リザーバーに輸送した。上記のMRSAシステムを、87,000コピーおよび5サイクルの間隔で使用した。工程1において、6つの液滴を、図37および38に示す液滴アクチュエータの熱サイクルループ上に分配し、輸送した。液滴は増幅試薬を含んだが、検出試薬は含まなかった。工程2において、3つの液滴を各温度制御領域に配置した。工程3において、液滴を、熱サイクルを行うためにループの周りに回転させた。工程4において、n回の熱サイクルの後、液滴を熱サイクルループから取り除いた。工程5において、取り除いた液滴を熱領域から離れた位置へ輸送した。工程6において、除去した液滴を検出液滴と合わせ、検出に供し、処分した。工程4、5および6を後の液滴について繰り返した。
【0160】
図44は、図43に対して記載される実験の結果を示す。その結果は、増幅が検出から分離され、個々の小サンプル液滴のセットが異なって熱サイクルされて、単一のリアルタイム増幅曲線を生成するプロトコルを用いて生成され得る増幅曲線を示す。
【0161】
(7.10 反応の停止)
核酸増幅反応をクエンチまたは実質的に停止することが所望される本明細書の種々の実施形態において、増幅反応を停止することが公知である種々の試薬が使用されてもよい。例えば、試薬は、例えばポリメラーゼを変性および/または分解するために結合することによって、ポリメラーゼ活性を妨げることができる。さらなる例を以下の表に与える。
【0162】
【表2】

【0163】
(7.11 デジタルPCR)
デジタルPCRは、サンプル中の正確な数のテンプレートコピーを測定するのに高度に定量的な方法として報告されている。サンプル液滴は、複数のナノリットルサイズのサブユニットに分配されるか、または分裂されてもよい。ほとんどの娘液滴は、0または1つのコピーを含む(一部はポアソン分布に起因して2つ以上のコピーを有する場合がある)。本発明は、液滴アクチュエータ上でデジタルPCRを実施するための技術を提供する。小さなユニットサイズの電極が好ましい。一実施形態において、電極は約200×200μmの電極である。液滴操作間隙の高さも調節されてもよい。200×200μmの電極を備える約100μmの液滴操作間隙の高さは、約4nLの体積を有する液滴を規定する。多くのこのような液滴は、種々の液滴分配技術を用いて生成されてもよい。一例において、一連の電極は細長い鎖を生成するように活性化され、次いで活性化された電極の散在された群は不活性化され、活性化された電極上でナノリットルのサイズの娘液滴を生じる。従来の分配および輸送技術もまた、一連の娘液滴を形成するために使用されてもよい。液滴アクチュエータ全体は増幅を実施するために熱サイクルされてもよいか、または個々の液滴は、熱サイクルを行うために熱制御領域を通してサイクルされてもよい。液滴は、液滴アクチュエータ表面上に、電圧、化学的または物理的パターニングによって反応全体にわたって所定の位置に維持されてもよい。増幅核酸の存在は液滴中で検出されてもよく、標的核酸の量が決定されてもよい。
【0164】
従って、例えば、本発明は、標的核酸、および必要に応じて増幅試薬を含むサンプル液滴を提供する工程と、サンプル液滴から小液滴を分配する工程であって、増幅試薬がサンプル液滴に存在しない場合、増幅試薬を含む各々の小液滴を混合して、増幅準備液滴を生じる工程と、各々の小液滴を、標的核酸を増幅するために選択される熱サイクルプロトコルに供する工程と、各々の小液滴中の増幅産物を検出する工程と、前記増幅産物が生成されるサンプルの一部を含む小液滴の数を決定する工程とを含む方法を提供する。一部の実施形態において、前記小液滴のうちの少なくとも1つは少なくとも1つの標的核酸分子を含む。増幅試薬は標的物を増幅するのに適切な任意の試薬を含んでもよい。一部の場合において、増幅試薬は、増幅標的分子とハイブリダイズし、ハイブリダイゼーションの際に変化するか、またはハイブリダイゼーションの結果として蛍光特性を有する少なくとも1つのプローブを含む。前記増幅産物が生成されるサンプルの一部を含む小液滴の数を決定する工程は、前記少なくとも1つのプローブのハイブリダイゼーションの結果としての蛍光変化を検出することを含んでもよい。前記増幅産物が生成されるサンプルの一部を含む小液滴の数を決定する工程は、全ての小液滴を一緒に画像化すること、あるいは例えば液滴を一度に輸送することによって、または検出ウィンドウを通してサブグループ内の個々の液滴もしくは液滴のグループを連続して画像化することを含む。小液滴は約1μL未満の体積を有してもよい。他の実施形態において、小液滴は、約1μLより大きい範囲から約1000μL、または約100μより大きい範囲から約500μLの体積を有する。この方法の種々の工程は、液滴アクチュエータの液滴操作間隙中、または液滴操作表面上で実施されてもよい。一部の場合において、小液滴は、液滴操作間隙の2つの基板間で平らまたはディスク形状の構造に圧縮される。液滴操作間隙が設けられる場合、それは、必要とされる液滴操作を実施するのに適切な任意の高さを有してもよい。一部の場合において、液滴操作間隙は、約50μm〜約1000μmの範囲、または約100μmより大きい範囲〜約500μの高さを有する。特定の実施形態において、熱サイクルは、1つの熱領域から別の熱領域へ液滴を輸送することによってなされる。特定の実施形態において、液滴アクチュエータはサンプルチャンバを欠き、および/または流路チャネルを欠く。特定の実施形態において、サンプル液滴から小液滴を分配する工程は、流路チャンネルからサンプルを置き換える置き換え流体を用いずになされる。サンプル液滴は増幅試薬とともに与えられてもよいか、または増幅試薬は、増幅準備液滴を得るために、例えば各小液滴と増幅試薬とを混合することによって、液滴操作を用いて加えられてもよい。サンプル液滴は検出試薬とともに与えられてもよいか、または検出試薬は、検出準備液滴を得るために例えば各小液滴と検出試薬とを混合することによって、液滴操作を用いて加えられてもよい。検出試薬は増幅の前後に加えられてもよい。
【0165】
関連した実施形態に加えて、サンプル液滴がナノリットルの娘液滴のセットに分裂された後、異なるセットのプライマーが、特定の核酸配列についてのPCRを実施するために各娘液滴と混合されてもよい。このアプローチは、液滴アクチュエータで同時に複数の核酸の発現レベルの評価を容易にする。
【0166】
(7.12 検出のための磁性反応ビーズの操作)
液滴アクチュエータベースのPCR(例えば、定量的リアルタイムPCR(QRT−PCR))において、標的核酸は増幅反応のために磁性反応ビーズに固定されてもよい。増幅産物を定量化するために、磁性反応ビーズを含む反応液滴は、液滴操作を用いて液滴アクチュエータ上の検出ウィンドウに輸送されてもよい。一部の例(例えばQRT−PCR)において、増幅産物の検出は、増幅産物の量を定量化するためにSybrGreenなどの蛍光色素を利用してもよい。しかしながら、サンプル液滴内に分散される磁性反応ビーズは、検出装置(例えば蛍光光度計)から蛍光を遮断することによって蛍光色素の検出を妨げる場合がある。
【0167】
磁場が、(a)組み込まれていない標識ヌクレオチドの検出のために増幅液滴から磁性ビーズを取り除くため、または(b)組み込まれていない標識ヌクレオチドの検出のために増幅液滴内の側へ液滴を引き付けるために使用されてもよい。
【0168】
図45は、ビーズが細長い液滴内の端側へ引き付けられ、それによってビーズが検出の間、検出ウィンドウに曝露されない本発明の実施形態を示す。磁石は、もちろん、液滴操作表面または液滴操作に対して様々な配置で与えられてもよい。例えば、図45に示すように、磁石は液滴操作表面の下に配置される。しかしながら、磁石は、代替として、液滴アクチュエータ間隙において、および/または部分的に液滴アクチュエータを形成する1つ以上の基板上において、液滴アクチュエータの側方に隣接して、液滴アクチュエータの上に配置されてもよい。つまり、磁石は、検出ウィンドウの外側または少なくとも実質的に外側である液滴の領域にビーズを引き付ける任意の位置に与えられてもよい。
【0169】
代替の実施形態において、磁石は、検出に供される液滴の完全に外側にビーズを引き付けてもよい。例えば、液滴アクチュエータは、ビーズ除去のために規定される液滴アクチュエータの領域に強力な磁石を備えてもよい。磁石の力は、液滴アクチュエータのビーズ除去領域に移動される任意の液滴の外側に磁性ビーズを引き付けるように選択されてもよい。一部の場合において、ビーズの除去は効果的に不可逆的であってもよい。
【0170】
図46A、46B、および46Cは液滴アクチュエータの領域の上面図を示し、検体検出を改良するために、磁性反応ビーズを操作する方法および結果を示す。液滴アクチュエータ4600は、PCRなどの増幅反応などの核酸ベースのアッセイに必要とされる液滴操作を実施するように構成される液滴操作電極4610(例えばエレクトロウェッティング電極)の経路またはアレイを備えてもよい。特に、検出ウィンドウ4612は液滴操作表面に与えられる。検出ウィンドウ4612は特定の液滴操作電極4610Dに配置されてもよいか、あるいは液滴が、必要に応じて親水性表面または上部基板および/もしくは底部基板の形状のバリエーションなどの他の輸送機構を備える液滴操作電極を用いて輸送され得る領域であってもよい。液滴アクチュエータ4600は、液滴操作を介して液滴操作電極4610に沿って輸送され得るサンプル液滴4620を備えてもよい。サンプル液滴4620は、解析される標的核酸についての親和性を有する磁性反応ビーズ4624などの一定量のビーズを備えてもよい。
【0171】
図46Aにおいて示すように、ビーズ4624をその中に有するサンプル液滴4620が、検出ウィンドウ4612の領域内にある液滴操作電極4610Dに配置される。検出ウィンドウ4612は典型的に、サンプル液滴4620より小さい直径である。磁性反応ビーズ4624は、検出ウィンドウ4612によって占められる領域を含むサンプル液滴4620内に分散され、分散された読み取りおよびバックグラウンドノイズを生じる、検出装置(すなわち蛍光光度計)からの蛍光を遮断することによって、増幅シグナル、例えば蛍光色素の検出を妨げる場合がある。
【0172】
図46Bに示すように、磁石4630はサンプル液滴4620に近接して配置される。磁石4630は永久磁石または電磁石であってもよい。磁石4630は、サンプル液滴4620の実質的に端部で、かつ検出ウィンドウ4612から実質的に離れた位置に磁性反応ビーズ4624を引き付け、集めるのに十分な磁場を提供するために操作電極4610Dおよびサンプル液滴4620から一定の距離で配置される。一部の場合において、磁石4630によって与えられる磁場の強さは、ビーズ4624が密接な凝集を形成しないものであり、後の液滴操作において容易に再分配されてもよい。他の場合において、ビーズの除去が本質的に永続的であると意図される場合、凝集は問題ではない。
【0173】
図46Cに示すように、磁石4630は、サンプル液滴4620から磁性反応ビーズ4624を分離するために使用されてもよい。十分な数の熱サイクル反応(例えば約10サイクル)の後、PCR液滴の液相における増幅核酸の量は、磁性反応ビーズの非存在下で正確に検出されるのに十分な量であってもよい。液滴操作を用いて、サンプル液滴4620は、液滴操作を介して、磁石4630の磁場内および磁場外に輸送されてもよい。サンプル液滴4620が磁石4630から離れた位置に輸送される場合、ビーズ4626の集合は、液滴操作電極4610Mに配置されたままになる。ビーズ液滴4626の量は、十分に多い封入ビーズ4624であってもよい。ここで、サンプル液滴4620は磁性反応ビーズを実質的に含まず、蛍光検出はビーズ干渉物の非存在下で進行されてもよい。
【0174】
図46Dは、図46Bの方法(すなわち磁石によって凝集される磁性反応ビーズ)および図46Cの方法(磁性反応ビーズを含まないPCR液滴)を用いて熱サイクル反応から得られるリアルタイムPCRデータのプロットを示す。図46Dは、蛍光シグナルの検出の間の磁性反応ビーズの干渉から生じ得る検出シグナルにおける不安定性およびバックグランドノイズを示す。磁性反応ビーズが、例えば熱サイクル11(矢印で示す)で除去される場合、検出シグナルは十分に安定である。
【0175】
(7.13 極性蛍光色素分子)
核酸増幅方法は熱サイクルを使用する。すなわち、規定された一連の温度変化によってサンプルおよび増幅試薬を含む液滴を交互に加熱および冷却する。液滴アクチュエータベースの増幅(例えば電極によって媒介される液滴操作などの液滴操作を用いて実施されるPCR)において、温度制御素子(例えばペルチェユニット、加熱ブロック、冷却ユニットなど)が、液滴アクチュエータ表面上、または液滴アクチュエータ間隙内の充填流体の温度を制御するために使用されてもよい。しかしながら、熱サイクルに必要とされる高温は、蛍光増強が、検出法および検出色素として使用されるSybrGreenなどの蛍光色素(すなわち蛍光色素分子)として使用される場合、検出シグナルの損失を生じる場合がある。SYBR(登録商標)Green dyeなどの細胞透過性蛍光色素分子は、疎水性相(例えば油性充填流体)において十分な溶解性を有することができ、水性PCR液滴から充填流体に、特に熱サイクルの間に発生するものなどの高温で分配することができる。
【0176】
細胞透過性蛍光色素分子に対する代替として、極性または細胞不透過性蛍光色素分子が使用されてもよい。例えば、EVAGREEN(登録商標)極性蛍光色素分子が、蛍光検出シグナルを著しく損失せずにPCRに使用されてもよい。EVAGREEN(登録商標)極性蛍光色素分子(Biotium,Hayward,CAから入手可能)およびTO−PRO1などの多くの異なる極性蛍光色素分子が、増幅産物を検出するためにPCRに使用されてもよい。
【0177】
(7.14 不動態化)
核酸増幅は、反応液滴内に含まれる核酸テンプレート、オリゴヌクレオチドプライマー、試薬および酵素などの多くの異なる反応成分を含むいくつかの工程を必要とする。核酸、タンパク質(すなわち酵素)、および/または色素(例えば蛍光色素)などの増幅液滴のこれらの成分の多くは、基板表面(例えば液滴操作電極)上に吸収され得、および/または液滴アクチュエータの充填流体(例えば油性充填流体)内に分配され得る可能性がある。液滴アクチュエータの基板表面および/または充填流体に対するこれらの重要な成分の損失は、PCR反応の低減した効果および/またはPCR反応の失敗を生じる場合がある。一実施形態において、本発明は、物質がその物質を一緒に使用する前に他の物質に対して「不動態」となる表面安定化技術を提供する。本発明の表面安定化技術は、増幅液滴から液滴アクチュエータの表面までの重要な成分の損失を低減および/または取り除くことができる。
【0178】
不動態化試薬(すなわち遮断剤)は、基板表面に対する核酸テンプレートおよび/またはオリゴヌクレオチドプライマーの結合ならびに/あるいは充填流体含有の損失を減少および/または防ぐように選択されてもよい。実施例は、非標的DNA分子などの他の核酸分子および/またはさらなる量のオリゴヌクレオチドプライマーを含む。
【0179】
不動態化試薬(すなわち遮断剤)は、基板表面に対するタンパク質の結合および/または充填流体の損失を減少および/または防ぐように選択されてもよい。例としては、限定されないが、ポリビニルピロリドン(PVP)、ポリエチレングリコール(PEG)、トゥイーン(Tween)などの界面活性剤、およびウシ血清アルブミン(BSA)などの種々のポリマーが挙げられる。
【0180】
一例において、液滴アクチュエータの表面は、前処理液滴内に含まれる一定量の不動態化剤で前処理される。前処理液滴は、1つ以上の反応サイクルを介して液滴アクチュエータの1つ以上のPCR経路に沿って輸送されてもよい。前処理液滴がPCR経路内にサイクルされる場合、核酸、タンパク質(すなわち酵素)、および/または色素(例えば蛍光色素)などの不動態化剤が、基板表面(例えば液滴操作電極)上に吸着されてもよく、ならびに/あるいは充填流体(例えば油性充填流体)に分配されてもよく、PCR液滴内の成分の次の結合からの潜在的な吸収部位を効果的に飽和させる。別の例において、一定量の不動態化剤は、PCR液滴内に直接加えられてもよい(すなわち動的不動態化)。この例において、PCR液滴内の不動態化剤は、液滴アクチュエータの基板表面および/または充填流体上の利用可能な吸収部位に対して反応成分と効果的に競合し得る。
【0181】
(7.15 間隙の高さ)
PCRを実施するのに使用される液滴アクチュエータは、液滴操作間隙によって隔てられる底部基板および上部基板を備えてもよい。表面張力は温度の増加に伴い減少するため、表面張力が非常に低い場合、液滴は、高い温度で分裂または砕け得る。従って、室温で十分に作用することができる間隙の高さの構成は高温で作用しなくてもよい。なぜなら、表面張力は効果的に減少するからである。本発明は、この効果がより大きな間隙を用いることによって埋め合わされてもよいことが発見されている。表面張力(エネルギー)はより大きな間隙について同じであるが、領域はより大きいので、多くの総エネルギーが、砕くために液滴に必要とされる。典型的に、熱サイクルを実施するのに使用される液滴アクチュエータにおける液滴操作間隙の高さは約200μmであってもよい。しかしながら、非常に小さな間隙の高さは、熱サイクル領域の間に液滴を往復させるときなどの液滴操作の間に増幅液滴の分裂を生じる場合がある。PCR液滴の分裂は、標的核酸および試薬成分の損失を生じる場合がある。これらの重要な成分の損失は、増幅反応の実質的に低減した効果および/または増幅反応の失敗を生じる場合がある。
【0182】
液滴操作間隙の高さは、単一のサイズの電極および単一のサイズの液滴の量に対して選択されてもよく、それによって液滴は実質的に球形である。より低いアスペクト比の液滴は球形のサイズにより近く、より高いアスペクト比の液滴はよりディスク形状である。本発明者らは、ディスク形状の液滴が、液滴輸送、分配および分裂などの液滴操作に関してより低い電圧を必要とするが、それらはまた、より球状の液滴より容易に微小液滴を形成する傾向があることを発見した。実質的に球状の液滴は、同じ液滴操作に関してより高い電圧を必要とするが、それらは液滴操作の間に微小液滴を形成する傾向がより低い。高温に供される液滴を必要とするアッセイにおいて、微小液滴形成は増加する。一例において、本発明者らは、4:1または3:1の電極ピッチ:ギャップ高さ比(約1200μmの電極ピッチおよび約300μmまたは約400μmの液滴操作間隙の高さと等しい)が、微小液滴の形成を実質的に減少させることを見出した。
【0183】
本発明は、液滴操作の間の液滴の安定性(例えばPCR液滴の分裂を実質的に減少させる)を改良するために、高い間隙の高さを有する液滴アクチュエータを提供する。例えば、約320μm〜約350μmの液滴操作間隙の高さは、液滴操作を介して輸送されたPCR液滴の向上した安定性を提供する。
【0184】
一実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約250μmより大きい。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は、約250μm〜約500μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約275μm〜約450μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約300μm〜約400μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は約320μm〜約375μmの範囲の高さを有する。別の実施形態において、単一のサイズの液滴操作電極の電極ピッチは約1200μmであり、液滴操作間隙は、約320μm〜約350μmの範囲の高さを有する。
【0185】
一実施形態において、本発明は、約7:1〜約2.8:1の範囲の電極ピッチ:間隙の高さの比を有する液滴アクチュエータを提供する。別の実施形態において、本発明は、約6:1〜約3:1の範囲の電極ピッチ:間隙の高さの比を有する液滴アクチュエータを提供する。さらに別の実施形態において、本発明は、約4.3:1〜約3.4:1の範囲の電極ピッチ:間隙の高さの比を有する液滴アクチュエータを提供する。
【0186】
別の実施形態において、本発明は、約1200μmの電極ピッチおよび約175μm(約7:1のアスペクト比)〜約450μm(約2.8:1のアスペクト比)の範囲の液滴操作間隙の高さを有する液滴アクチュエータを提供する。さらに別の実施形態において、本発明は、約1200μmの電極ピッチおよび約200μm(約6:1のアスペクト比)〜約400μm(約3:1のアスペクト比)の範囲の液滴操作間隙の高さを有する液滴アクチュエータを提供する。さらに別の実施形態において、本発明は、約1200μmの電極ピッチおよび約280μm(4.3:1)〜約350μm(3.4:1)の範囲の液滴操作間隙の高さを有する液滴アクチュエータを提供する。
【0187】
液滴アクチュエータにおける間隙の高さは、例えば、低部と上部の液滴アクチュエータ表面間に適切な厚さのスペーサー材料を「挟み込むこと」によって制御されてもよい。あるいは、材料の層は、2つの基板の少なくとも一部の間に適切な厚さの間隙空間を規定する絶縁材を提供するように上部または低部の基板のいずれかの内面に接着されてもよい。あるいは、絶縁材は1つまたは両方の基板の一体部分、射出成形または他の形成プロセスの間に、基板に成形または形成される例えば突起柱または他の構造であってもよい。所望の高いアスペクト比を達成するための間隙の高さを制御する種々のさらなる手段は当業者に容易に理解されるだろう。
【0188】
(7.16 キャリーオーバー汚染の減少)
液滴アクチュエータでの液滴ベースの核酸増幅は、熱反応領域と検出器との間で電極によって媒介される液滴操作を用いて増幅準備液滴が往復される、一連の液滴操作を含む。このプロセスが共通の経路または近接する経路に沿う複数の液滴の移動に関する場合、増幅液滴からの残留成分は、1つの液滴から別の液滴に移動する場合があり、一連の液滴操作におけるその後の増幅液滴を汚染する。本発明は、油内の増幅液滴を使用する増幅液滴の間の二次汚染を減少させるための液滴アクチュエータおよび方法を提供する。
【0189】
本発明の液滴アクチュエータは、液滴操作間隙によって分離される底部基板と上部基板とを備えてもよい。液滴アクチュエータの指定された領域において、液滴操作間隙は、油状の充填流体などの流動性の充填流体を含んでもよい。液滴アクチュエータの他の指定された領域において、液滴操作間隙間は空気などの気体状の充填流体を充填されてもよい。
【0190】
油に囲まれた液滴は、例えば、油でサンプルリザーバーを充填し、続いてリザーバーに水性サンプル、例えばPCRサンプルを負荷し、油層に囲まれる水性PCR液滴を分配または「ピンチオフ(pinch off)」するために液滴操作を用いることによって形成されてもよい。油に囲まれたPCR液滴の形成を促進するために、高い表面張力を有する高粘性油が使用されてもよい。適切な油の例としては、限定されないが、ヘプタデカンまたはオクタデカン油が挙げられる。油に囲まれたPCR液滴が分配される場合、それは、その後のPCR反応のために液滴操作を用いて、油を含まない液滴アクチュエータの領域(すなわち間隙が空気に充填されている)に輸送されてもよい。
【0191】
高粘性油は室温(すなわち約22℃〜28℃)で部分的な固体または固体であってもよい。例えば、ヘプタデカン、オクタデカン、ノナデカン、およびエイコサン油の融点は、それぞれ、20〜22℃、26〜29℃、30〜34℃および35〜37℃である。液滴アクチュエータベースの増幅に関して、オイルは異なる増幅のためにその融点に基づいて選択されてもよい。例えば、液滴アクチュエータの輸送が必要とされる製造観点から、リザーバーは、選択される油の融点以上の温度で油を充填され、次いで液滴アクチュエータにおいて冷却および凝固させてもよい。液滴アクチュエータベースのPCRは典型的に、約60℃以上で操作するため、選択される油は液相内にあり、油で囲まれたPCR液滴の形成が可能になる。
【0192】
(7.17 標的核酸の濃縮および収集)
液滴アクチュエータベースの核酸増幅の一部の適用において、PCR解析の前にサンプル流体中の検体(例えば細菌、ウイルス、真菌、および/または核酸)を濃縮することが必要な場合がある。例えば、最適な解析を与えるために、サンプル流体の量は非常に多く、および/または検体の濃度は非常に小さくてもよい。
【0193】
図47Aおよび図47Iは、液滴アクチュエータ4700の領域の断面図を示し、核酸増幅および検出のためのサンプル流体由来の標的核酸の濃縮および収集プロセスにおける磁性反応捕捉ビーズの使用を示す。
【0194】
図47Aに示されるように、検出アクチュエータ4700は底基板4710を備え得る。底部基板4710は、液滴操作間隙4716によって上部基板4714から分離されてもよい。リザーバー電極4718は底部基板4710上に配置されてもよい。リザーバー電極4718は、液滴操作電極4720(例えばエレクトロウェッティング電極)の経路またはアレイと結合して配置されてもよく、それによって、液滴は、液滴操作電極4720の経路またはアレイ上にリザーバー電極4718から配置されてもよい。誘電体が電極を覆ってもよい。疎水性層が電極を覆ってもよい(または疎水性誘電体が選択されてもよい)。リザーバー4730は、電極が液体経路を通して流される液体と相互作用できるように、リザーバー4730から間隙4716への液体経路を規定し、リザーバー電極4718に十分に近接する上部基板4714に設けられる。リザーバー4730は、例えば約1ミリリットル(ml)以上のサンプル流体を含むのに十分なサイズであってもよい。リザーバー4730は一定量の磁性反応捕捉ビーズ4734を含む。磁性反応捕捉ビーズ4734は、例えば、一次捕捉抗体、またはオリゴヌクレオチド配列、あるいは結合および捕捉事象を与える特異的標的検体に対する親和性を有する任意の結合タンパク質を含むビーズであってもよい。リザーバー4730は隔壁4738によって密閉される。隔壁4738は、望まれない物質によるリザーバー4730の汚染に対する障壁を与える。
【0195】
磁石4740は液滴アクチュエータ4700に結合される。磁石は、リザーバー電極4718が磁石4740の磁場内にあるように配置される。例えば、磁場4740は永久磁石または電磁石であってもよい。一例において、磁石4740は、リザーバー電極4718の近接内、またはリザーバー電極4718から離れた位置に移動され得るように位置が調節される永久磁石である。磁石4740は、例えば、磁性反応捕捉ビーズ4734を引き付けおよび/または固定するように使用されてもよい。操作において、磁石4740は、磁性反応捕捉ビーズ4734に結合される標的検体を濃縮するプロセスを補助するように使用されてもよい。
【0196】
超音波処理器4742は液滴アクチュエータ4700に結合される。超音波処理器4742は、流体内の粒子を攪拌するために、音波エネルギー(例えば超音波)をリザーバー4730内のサンプル流体に与えるように使用されてもよい。別の例において、超音波処理器4742はサンプル流体内の粒子を穏やかに攪拌し、再懸濁するために使用されてもよい。別の例において、超音波処理器4742はサンプル流体内の粒子を激しく攪拌するために使用されてもよい。一部の適用において、強力な超音波処理が、細胞膜を破壊し、細胞内容物を放出するために使用されてもよい。さらに、リザーバー4730に対する超音波処理器4742の位置は変化させてもよい。
【0197】
第2の磁石4744は液滴アクチュエータ4700に結合される。磁石4744は、例えば、永久磁石または電磁石であってもよい。磁石4744は、1つ以上の液滴操作電極4720が磁石4744の磁場内にあるように配置される。磁石4744は、さらに標的核酸を濃縮および精製するために、例えば、磁性反応ビーズを用いて第2の捕捉事象に磁場を与えるように使用されてもよい。
【0198】
サンプル流体由来の標的核酸を濃縮および収集するために、磁性反応捕捉ビーズを用いるプロセスの例としては、限定されないが、以下の工程が挙げられる。
【0199】
図47Bは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける第1の工程を示す。この工程において、負荷装置4750(例えば、シリンジおよびニードル、マイクロピペット)は、一定量のサンプル流体4752をリザーバー4730に入れておくために使用される。サンプル流体4752は、例えば、約1ml以上の体積の血液サンプルまたは鼻咽頭洗浄サンプルであってもよい。サンプル流体4752は一定量の標的検体4754を含んでもよい。標的検体4754は、例えば、磁性反応捕捉ビーズ4734に対する親和性を有する細菌、ウイルス、および/または真菌標的物であってもよい。リザーバー電極4718は活性化されず、磁石4740の一部は、実質的にリザーバー電極4718に存在する磁場がないため、サンプル流体4752はリザーバー4730に保持される。
【0200】
図47Cは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、超音波処理器4742は、活性化(例えば低エネルギー操作)され、穏やかに攪拌するために使用され、サンプル流体4752中の磁性反応捕捉ビーズ4734を再懸濁する。超音波処理器4742は、磁性反応捕捉ビーズ4734に対する標的検体4754の最適な混合および結合(すなわち一次捕捉)を与えるために、十分な時間、活性化されてもよい。
【0201】
図47Dは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、超音波処理器4742はスイッチが切られ、磁石4740の位置は、液滴アクチュエータ4700のリザーバー4718に特定の磁場が存在し、リザーバー電極4718が活性化されるようにある。リザーバー電極4718の磁場および活性化の結果として、結合された標的検体4754を含む磁性反応捕捉ビーズ4734がリザーバー4718に定着し、サンプル流体4752内で効果的に濃縮する。
【0202】
図47Eは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、磁石4740は液滴アクチュエータ4700から離れた位置に物理的に移動され、その結果、リザーバー電極4718に実質的に磁場は存在しない。磁場の除去の結果として、磁性反応捕捉ビーズ4734はリザーバー電極4718の表面に長く固定されず、間隙4716内のサンプル体積に分配される。この例において、標的検体4754が、例えば細菌、ウイルスおよび/または真菌である場合、溶解試薬液滴4756が輸送され、液滴操作を用いて間隙4716内でサンプル体積と融合される。1つ以上の溶解試薬液滴4756が、標的検体4754の十分な溶解および標的核酸の放出を提供するために使用されてもよい。
【0203】
図47Fは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、超音波処理器4742は活性化されるリザーバー4718の近接に物理的に移動される。超音波処理器4742は活性化され(例えば高エネルギー操作)、激しく攪拌し、サンプル流体4752を混合するために使用される。超音波処理器4742は、標的検体4754の最適な溶解および核酸の放出を提供するのに十分な時間、活性化されてもよい。別の実施形態において、単一の超音波処理器は、液滴操作間隙における液滴およびリザーバー内の流体の同時超音波処理を可能にする方法で戦略的に配置されてもよい。さらに別の実施形態において、1つより多い超音波処理器が設けられてもよい。
【0204】
一例において、化学試薬および/または酵素溶解試薬(すなわち溶解試薬液滴4756)と組み合わせた強力な超音波処理が、真菌病原体を含む生物学的サンプルに有用であり得る。
【0205】
図47Gは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、磁石4740の位置は、液滴アクチュエータ4700のリザーバー電極4718に特定の磁場が存在するような位置である。磁場の結果として、結合される標的検体4754を有する磁性反応捕捉ビーズ4734はリザーバー電極4718に定着される。標的検体4754は溶解されるため、核酸はサンプル流体4752に放出される。一定量の標的核酸4760(例えばDNAまたはRNA)を含む1つ以上の溶解液滴4758は、液滴操作を用いて、磁石4744に対して液滴操作電極4720の経路に沿ってリザーバー電極4718から離れた位置に輸送される。
【0206】
図47Hは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、一定量の磁性反応捕捉ビーズ4764を含む捕捉液滴4762は、液滴操作を用いて第2の磁石4744に配置される。捕捉ビーズ4764は、溶解液滴4758中の捕捉標的核酸4760をアニールするために使用される一定量のオリゴヌクレオチド配列を含む。液滴操作を用いて、1つ以上の溶解液滴4758は、捕捉液滴4762に輸送され、融合される。この工程において、標的核酸4760はさらに濃縮され、精製される。
【0207】
図47Iは、サンプル流体由来の標的核酸を濃縮および収集するプロセスにおける別の工程を示す。この工程において、捕捉液滴4762は、未結合の物質を除去するために一連の液滴操作を用いて洗浄される。捕捉液滴4762中の結合された核酸4760は、ここでPCR用に準備される。
【0208】
別の実施形態において、標的検体4754が核酸である場合、溶解工程(すなわち図47Eおよび47F)は必要でなくてもよい。
【0209】
(7.18 サンプル)
本発明の種々の実施形態において、本発明は核酸サンプルを使用する。核酸サンプルは、標的分子、細胞または生物などの標的物質に直接または間接的に結合される標的核酸または核酸を少なくとも潜在的に含むサンプルである。特定の実施形態において、核酸サンプルはサブサンプルに細分化されてもよい。例えば、サブサンプル液滴はサンプル液滴から液滴操作を用いて分配されてもよい。
【0210】
個々のサブサンプルは、一連のエンドポイント測定を生成するための所定数のサイクルのために増幅されてもよい。エンドポイント測定は、特定の所定数の増幅サイクルの後、または終わりに得られるサブサンプル(および/またはサブサンプルのセット)の各々の測定を含んでもよい。異なるサブサンプルのエンドポイント測定は、生物サンプルに存在する標的核酸を定量化するために使用され得る曲線を生成するために使用されてもよい。例えば、異なるサブサンプル液滴のエンドポイント測定は、サンプル液滴、またはサンプル液滴が誘導されるオリジナルのサンプルに存在する標的核酸を定量化するために使用され得る曲線を生成するために使用されてもよい。
【0211】
核酸サンプルは、対象物、コントロール、標準物または複製物由来のサンプルであってもよい。核酸は、目的の実際の検体である標的分子などの別の物質に結合されてもよい。種々の実施形態において、プロトコルは、1つ以上の対象物のサンプル由来の物質の増幅、ならびに1つ以上のコントロールおよび/または複製物の増幅を含んでもよい。特定の実施形態において、特定のサブサンプルは、単一のデータポイントのみを生成するために使用される。他の実施形態において、複数の同一のサブサンプル液滴は、増幅サイクルの数の関数として検出される増幅シグナルの量を示す一連のデータポイントを生成するように異なって増幅されてもよい。
【0212】
核酸サンプルは、例えば、空気サンプル、水サンプル、土壌サンプルなどの環境サンプル;髪の毛のサンプル、皮膚細胞、および他の法医学的残留物などの法医学サンプル;ならびに全血、リンパ液、血清、血漿、汗、涙、唾液、痰、脳脊髄液、羊膜液、精液、膣分泌物、漿液、滑液、心膜液、腹膜液、胸膜液、浸出液、滲出液、嚢胞液、胆液、尿、胃液、腸液、糞便試料、単細胞および多細胞を含む液体、細胞小器官を含む液体、流動組織、流動器官、多細胞生物を含む液体、生物学的スワブまたは洗浄物などの他の生物学的サンプル由来であってもよい。
【0213】
(7.19 検出)
増幅を検出するための種々のアプローチが本発明の実施に使用されてもよい。例えば、一実施形態において、各サブサンプル液滴は所定の波長で蛍光強度測定に供される。一実施形態において、検出は増幅反応と同時に達成される。言い換えれば、複数のサブサンプル液滴が増幅される間、各サブサンプル液滴はその所定数のサイクルを達成するため、検出に供されてもよい。1つの液滴が検出に供されている間、他の液滴は増幅され続けてもよい。特定の実施形態において、液滴のグループがほぼ同時に達成され、各n回のサイクル後に、少なくとも1つの液滴が検出に供される。各検出工程の間のサイクルの数は、特定のアッセイに必要なデータに基づいて選択されてもよい。一般に、より正確な定量化は、多数または少数の全増幅サイクルの検出を必要とする。
【0214】
検出は、サブサンプル液滴が利用可能になると、すなわち、所定数のサイクルが完了すると、ほぼ達成され得る。サブサンプル液滴は所定の位置で試験されてもよいか、または後の検出のために他の場所に輸送もしくは移動されてもよい。後のアプローチは、増幅と検出の機能を分けるのに有用であり得る。例えば、サブサンプル液滴は、液滴アクチュエータ上の他の場所に輸送され、それらが検出を待っている間、滞留されてもよい。サブサンプル液滴が検出のために準備されている場合、センサが、液滴が各液滴を測定するために滞留される領域を走査してもよい。あるいは、サブサンプル液滴は、検出のためのセンサの存在下で一定の時間に1つ以上輸送されてもよい。例えば、各サブサンプル液滴は、検出ウィンドウを通して輸送されてもよく、測定は、各液滴が検出ウィンドウに存在している間、その各液滴についてセンサによって得られてもよい。
【0215】
液滴は種々の技術を用いて検出に供されてもよい。一実施形態において、液滴は検出の存在下で輸送されてもよい。この実施形態において、1つ以上の固定センサが、検出を達成するために使用されてもよい。このような構成は機器のコストおよび複雑性を減少させる。別の実施形態において、センサは検出のための液滴の存在下で移動される。液滴は、後の時間での検出のために液滴アクチュエータに配置されてもよいか、液滴アクチュエータから除去されてもよい。配置された液滴はセンサによって走査されてもよいか、または画像化されてもよい。例えば、配置された液滴は、CCDまたはLED/フォトダイオードアレイなどのアレイ検出器によって画像化されてもよい。液滴は、CCDもしくはLED/フォトダイオードアレイの存在下で移動されてもよく、および/またはCCDもしくはLED/フォトダイオードアレイは、液滴の存在下で移動されてもよい。
【0216】
すでに述べたように、特定の実施形態において、検出における増幅は分けられてもよい。この利点は、経時的な同じ反応の複数の測定よりむしろ、複数のエンドポイント反応の使用によって促進される。このアプローチはまた、検出前であるが増幅後の検出試薬の添加を促進する。熱サイクルおよび検出の分離は、核酸増幅を実施できる液滴アクチュエータを設計する場合、より大きな設計の柔軟性を提供する。
【0217】
種々の実施形態において、検出試薬は、検出前または間であるが、増幅後に各サブサンプル液滴に加えられる。例えば、挿入色素(SYBR Green)および/または分子指標を含む液滴が、増幅後にサブサンプル液滴に加えられてもよい。この実施形態は、増幅が完了した後に試薬が加えられるため、増幅を阻害できる試薬の使用を促進する。試薬は、検出前または間に加えられてもよい。別の実施形態において、増幅サイクルの一部は、検出試薬の検出前に実施されてもよい。言い換えれば、検出試薬は、1つ以上の最後のサイクルの間または前に加えられてもよい。このアプローチは、Taqman(r)試薬などの、重合の間に存在する検出試薬を必要とする化学物質を検出するのに有用であり得る。
【0218】
示されるように、増幅および検出の分離は、検出アクチュエータおよび液滴アクチュエータを操作するのに必要とされる機器についての設計の柔軟性を改良する。例えば、検出器モジュールおよび加熱器モジュールは、それらのそれぞれの機能を実施する位置を交換することができる。このアプローチは、加熱器が検出を妨げずに液滴アクチュエータの両側に配置されることを可能にする。別の例において、分離面が熱サイクルおよび検出のために設けられてもよい。
【0219】
検出は数秒で達成され得るが、熱サイクルは数分〜1時間までを必要とする場合がある。従って、1つの検出機器は、複数の液滴アクチュエータで熱サイクルを制御するために使用される機器において複数の熱サイクルまたは熱サイクルのブランクを支持するために使用されてもよい。例えば、機器は、熱サイクルのための複数のスロット、および検出のための1つまたは少数のスロットのみを有するように設けられてもよい。液滴アクチュエータは、使用者、ロボット手段または他の手段によってスロットを検出するために熱サイクルスロットから移動されてもよい。
【0220】
液滴が検出のために準備されている場合、それらは、使用される検出の形態に適切な任意の方法で配置されてもよい。例えば、それらは、単一のファイルに並べられてもよいか、または密度の濃いアレイにパッケージされてもよい。検出のための空間および構成は、熱サイクルの必要性によって抑制されない。液滴を密な1−Dアレイに配置する能力により、走査検出器のコストおよび複雑性が減少する。センサについての全移動は、直線状で、1軸の方向のみに低減され得る。同様に、より小さいCCDまたはLED/フォトダイオードアレイが使用されてもよい。
【0221】
他の設計の利点は、熱サイクルおよび検出についての異なる必要性から生じる。例えば、光透過性が検出の一部の形態に必要とされてもよいが、特定の熱サイクルの構成に必要とされなくてもよい。熱特性は液滴アクチュエータの熱サイクル領域について最適化されてもよいが、光学特性は液滴アクチュエータの検出領域に最適化されてもよい。さらに、本発明の液滴アクチュエータは、後の時間に再試験するために液滴アレイを保存するために使用されてもよい。
【0222】
他の利点の中で、本発明の熱サイクル技術は、増幅の間、液滴に存在する結合剤などの検出剤を必要とせずに液滴の増幅を促進する。示されるように、一部の場合において、小液滴は熱サイクルを受ける液滴から分配されてもよい。小液滴は熱サイクルプロセスから出ていってもよく、適切な検出試薬と混合され、次いで検出に供されてもよい。本明細書に記載されるエンドポイント検出スキームもまた、この技術を利用してもよい。各小液滴は、熱サイクルプロセスの完了後に結合剤を含む液滴と混合されてもよい。
【0223】
特定の実施形態において、本発明の方法は、サンプルおよび結合剤を一緒に含む増幅反応混合物の熱サイクルを省略する。特定の実施形態において、本発明の技術は、特に、増幅反応が進行中の間に、蛍光シグナルを検出するために操作される検出器を除外してもよい。
【0224】
種々の実施形態において、検出剤が熱サイクルの後に加えられる場合、他に核酸増幅を妨げる薬剤が利用されてもよい。例えば、増幅の間に存在する場合、熱サイクルを阻害する結合剤が、その結合剤が増幅後に加えられる本発明の技術に使用されてもよい。従って、特定の実施形態において、本発明は、核酸増幅の速度および増幅のための試薬を特異的に阻害する結合剤を利用する。
【0225】
他の実施形態において、検出は標識ヌクレオチドを用いて達成されてもよい。テンプレートはビーズに結合され、蛍光ヌクレオチドなどの標識ヌクレオチドを用いて増幅されてもよい。標識ヌクレオチドは増幅鎖に導入されてもよく、検出は、(a)液滴からの標識核酸の喪失、および/または(b)標識核酸の増幅鎖への導入に基づいてもよい。特定の実施形態において、「Droplet−based Surface Modification and Washing」という発明の名称の米国特許第7,439,014号に記載されるものなどのビーズ洗浄技術が、増幅鎖に導入される標識ヌクレオチドの検出のために未結合の標識ヌクレオチドから離れて洗浄するために使用されてもよい。この技術は、内部蛍光を有する捕捉ビーズとともに蛍光ヌクレオチドを用いることによって高められてもよく、ビーズは蛍光ヌクレオチドの蛍光を増幅する。
【0226】
さらに別の実施形態において、DNA合成は、ピロリン酸塩の生成に基づいて測定されてもよい。各サイクルにて、デオキシトリヌクレオチドの導入は、ピロリン酸塩の分子を遊離させる。遊離されるピロリン酸塩の量は、単位複製配列の長さマイナスプライマーの長さに比例する。各サイクルの終わりに、化学的方法がピロリン酸塩を検出するために使用されてもよい。一部の場合において、小液滴は、熱サイクルを受け、ピロリン酸塩遊離についての試験に供される液滴から分配されてもよい。小液滴は、熱サイクルプロセスから出ていき、ピロリン酸塩検出プロトコルに供されてもよい。
【0227】
本明細書に記載されるエンドポイント検出スキームはまた、この技術を利用してもよい。液滴は、熱サイクルプロセスの完了後にピロリン酸塩検出プロトコルに供されてもよい。いずれの場合においても、ピロリン酸塩検出プロトコルは、2007年、10月25日に公開された「Droplet−Based Pyrosequencing」という発明の名称の国際公開第2007/120240号に記載されるものなどの液滴操作を用いて達成されてもよい。
【0228】
本明細書に記載される種々の検出アプローチは、通常、以下に記載される任意の実施形態とともに使用されてもよいことは理解されるだろう。
【0229】
(7.20 加熱バー)
本明細書に記載され、図48Aおよび48Bに示されるように、加熱バー4800は、十分な熱伝導率のために、アルミニウムバー4802などのアルミニウムから構成されてもよい。2つの抵抗器4804(各々15Ω)は、均一な加熱を与えるように底側の2つの端部に取り付けられる。サーミスタプローブ4806は、加熱器PID制御因子に温度測定を与えるために加熱バーの中央に取り付けられてもよい。加熱バーは、位置決めねじ4810を用いてカートリッジデッキ4808に配置され、下部のスプリング4812によって支持されてもよい。スプリング力は、加熱バー表面と加熱されるPCBカートリッジ4814との間の密な接触を確実にする。スプリングにより留められた加熱バーはカートリッジデッキに接触せず、デッキに移動される望まれない加熱器は最小化される。
【0230】
(7.21 システム)
当業者によって理解されるように、本発明は、方法、システムまたはコンピュータープログラム製品として具現化されてもよい。従って、本発明の種々の態様は、ハードウェア実施形態、ソフトウェア実施形態(ファームウェア、常駐ソフトウェア、マイクロコードなどを含む)、または「回路」、「モジュール」もしくは「システム」として本明細書においてほぼ全て参照され得るソフトウェアおよびハードウェアの態様を組み合わせた実施形態の形態をとってもよい。さらに、本発明の方法は、媒体において具現化されるコンピューターにより使用可能なプログラムコードを有するコンピューターにより使用可能な記録媒体上でコンピュータープログラム製品の形態をとってもよい。
【0231】
任意の適切なコンピューターにより使用可能な媒体は、本発明のソフトウェアの態様で利用されてもよい。コンピューターにより使用可能またはコンピューターにより読み取り可能な媒体は、例えば限定されないが、電子、磁気、光学、電磁気、赤外線、または半導体のシステム、装置、デバイス、または伝搬媒質であり得る。コンピューターにより読み取り可能な媒体のより具体的な例(限定的なリスト)としては、以下の一部または全てが挙げられる:1つ以上のワイヤを有する電気的接続、携帯型フロッピー(登録商標)ディスク、ハードディスク、ランダムアクセスメモリ(RAM)、リードオンリメモリ(ROM)、消去可能なプログラム可能なリードオンリメモリ(EPROMまたはフラッシュメモリ)、光ファイバー、携帯型コンパクトディスクリードオンリメモリ(CD−ROM)、光学式記憶デバイス、インターネットもしくはイントラネットをサポートするものなどの伝送媒体、または磁気記憶デバイス。コンピューターにより使用可能またはコンピューターにより読み取り可能な媒体はさらに、紙または別の適切な媒体であってもよく、例えば紙または他の媒体の光学走査によって、プログラムが電子的に捕捉され得るように、その上にプログラムがプリントされ、次いで、必要な場合、適切な方法でコンパイル、読み取り、または処理され、次いで、コンピューターメモリに保存されることに留意すべきである。この文書の文脈において、コンピューターにより使用可能またはコンピューターにより読み取り可能な媒体は、命令実行システム、装置、もしくはデバイスによって、またはそれらと併せて使用するためのプログラムを含有し、保存し、通信し、伝播し、または輸送できる任意の媒体であってもよい。
【0232】
本発明の操作を実行するためのコンピュータープログラムコードは、Java(登録商標)、Smalltalk、C++などのオブジェクト指向のプログラミング言語で書かれてもよい。しかし、本発明の操作を実行するためのコンピュータープログラムコードはまた、「C」プログラミング言語または同様のプログラミング言語などの従来の手続きプログラミング言語で書かれてもよい。プログラムコードは、使用者のコンピューター上で部分的に、リモートコンピューターで部分的に、またはリモーターコンピューターもしくはサーバーで完全に、スタンドアロンソフトウェアパッケージとして、使用者のコンピューター上で完全に、または使用者のコンピューター上で部分的に実行できる。後者の状況において、リモートコンピューターは、ローカルエリアネットワーク(LAN)または広域ネットワーク(WAN)を介して使用者のコンピューターに接続されてもよいか、その接続は外部コンピューターに対してなされてもよい(例えば、インターネットサービスプロバイダーを使用するインターネットを介して)。
【0233】
本発明の特定の態様は、種々の方法および方法の工程に対する参照とともに記載される。各方法の工程は、コンピュータープログラム命令によって実行され得ることは理解されるだろう。これらのコンピュータープログラム命令は、機械を生成するために、汎用コンピューター、専用コンピューター、または他のプログラム可能なデータプロセス装置のプロセッサに与えられてもよく、それによって、コンピューターまたは他のプログラム可能なデータプロセス装置のプロセッサを介して実行する命令は、この方法で指定される機能/作用を実行するための手段を作成する。
【0234】
コンピュータープログラム命令はまた、特定の方法で機能するように、コンピューターまたは他のプログラム可能なデータプロセス装置を指示し得るコンピューター読み取り可能メモリに保存されてもよく、それによって、コンピューター読み取り可能メモリに保存される命令は、この方法の工程の様々な態様を実行する命令手段を含む製造物品を生成する。
【0235】
コンピュータープログラム命令はまた、コンピューターまたは他のプログラム可能なデータプロセス装置にロードされて、コンピューターにより実行されるプロセスを生成するためにコンピューターまたは他のプログラム可能な装置で実施されるべき一連の操作工程を生じることができ、それによって、コンピューターまたは他のプログラム可能な装置で実行する命令は、本発明の方法において指定される様々な機能/作用を実行するための工程を提供する。
【0236】
(8 結びの見解)
上述の実施形態の詳細な説明は、本発明の特定の実施形態を例示する添付の図面を参照する。異なる構造および操作を有する他の実施形態も本発明の範囲から逸脱しない。用語「本発明」などは、本明細書に記載される本出願人の発明の多くの代替の工程または実施形態の特定の具体例に対する参照とともに使用され、その使用が存在してもしなくても、本出願人の発明の範囲または特許請求の範囲を限定することを意図しない。本明細書は、読み手のみの簡便さのためにセクションに分けられる。見出しは本発明の範囲を限定すると解釈されるべきではない。その定義は本発明の詳細の一部と意図される。本発明の様々な詳細は、本発明の範囲から逸脱せずに変更されてもよいことは理解されるだろう。さらに、上述の詳細は例示のみの目的のためであり、限定を目的とせず、本発明は添付の特許請求の範囲によって定義される。
【特許請求の範囲】
【請求項1】
サンプル中の標的核酸を検出する方法であって、前記方法は、
(a)核酸増幅反応液滴のセットを提供する工程であって、各々の液滴は前記サンプルの一部を含む、工程と、
(b)前記標的核酸を増幅するための条件下で前記増幅反応液滴の2つ以上のサブセットを処理して、増幅核酸を含む増幅された液滴の対応するサブセットを得る工程であって、前記増幅反応液滴の各々のサブセットは、
(i)前記増幅反応液滴の1つ以上を含み、
(ii)前記標的核酸を増幅するための異なる条件下で処理される、
工程と、
(c)検出のための前記増幅された液滴を調製する工程と、
(d)前記増幅された液滴からシグナルを検出する工程と、
(e)前記シグナルに基づいて、前記増幅された液滴および/または前記サンプルに存在する前記増幅された核酸の量を決定する工程と、
を含む、方法。
【請求項2】
核酸増幅反応液滴のセットを提供する工程は、サンプル液滴から前記核酸増幅液滴のセットを分配する工程を含む、請求項1に記載の方法。
【請求項3】
前記サンプル液滴は、液滴アクチュエータの液滴操作間隙に提供され、前記分配する工程は電極により媒介される、請求項2に記載の方法。
【請求項4】
(a)前記サンプル液滴は、液滴アクチュエータのリザーバーに提供され、
(b)前記液滴アクチュエータは、前記リザーバーから液滴操作間隙内への液体経路を備え、
(c)前記核酸増幅液滴のセットを分配する工程であって、
(i)前記サンプル液滴を、前記液体経路を通して前記液滴操作間隙内に流動させる工程と、
(ii)前記液滴操作間隙内の前記増幅反応液滴を分配するために電極を用いる工程と、
を含む、請求項2に記載の方法。
【請求項5】
核酸増幅反応液滴のセットを提供する工程は、
(a)サンプル液滴を提供する工程と、
(b)前記サンプル液滴を、複数のサンプル小液滴に分割する工程と、
(c)前記サンプル小液滴の各々と、増幅試薬を含む1つ以上の液滴とを混合して、前記増幅反応液滴を生じる、工程と、
を含む、請求項1に記載の方法。
【請求項6】
請求項5に記載の工程(b)および/または(c)は、電極により媒介される液滴操作を用いて液滴アクチュエータの液滴操作間隙内で実施される、請求項5に記載の方法。
【請求項7】
前記サンプル液滴、前記複数の小液滴、および前記増幅試薬を含む1つ以上の液滴、および前記増幅反応液滴は、
(a)液滴操作間隙内に配置され、
(b)流動性の充填流体によって少なくとも部分的に囲まれる、
請求項5に記載の方法。
【請求項8】
核酸増幅反応液滴のセットを提供する工程は、
(a)サンプル液滴を提供する工程と、
(b)前記サンプル液滴と、増幅試薬を含む1つ以上の液滴とを混合して、増幅準備液滴を生じる工程と、
(c)前記増幅準備液滴を分割して、前記増幅反応液滴を生じる工程と、
を含む、請求項1に記載の方法。
【請求項9】
前記サンプル液滴、前記増幅試薬を含む1つ以上の液滴、親増幅反応液滴、および前記増幅反応液滴は、
(a)液滴アクチュエータの液滴操作間隙内に配置され、
(b)流動性の充填流体によって少なくとも部分的に囲まれる、
請求項8に記載の方法。
【請求項10】
請求項8に記載の工程(b)および/または工程(c)は、電極により媒介される液滴操作を用いて実施される、請求項8に記載の方法。
【請求項11】
標的核酸が前記サンプルに存在する場合、請求項8に記載の工程(c)で生成された前記増幅反応液滴の各々が、前記標的核酸を含むことを確実にするために、前記増幅準備液滴中で十分な増幅核酸を生じるように選択された条件下で、前記増幅準備液滴を処理する工程をさらに含む、請求項8に記載の方法。
【請求項12】
前記増幅準備液滴を処理する工程は、前記増幅準備液滴を1〜20サイクルの間、熱サイクルする工程を含む、請求項11に記載の方法。
【請求項13】
前記増幅準備液滴を処理する工程は、前記増幅準備液滴を1〜10サイクルの間、熱サイクルする工程を含む、請求項11に記載の方法。
【請求項14】
前記増幅準備液滴を処理する工程は、前記増幅準備液滴を1〜5サイクルの間、熱サイクルする工程を含む、請求項11に記載の方法。
【請求項15】
請求項1に記載の工程(b)は、電極により媒介される液滴操作を用いて液滴アクチュエータの液滴操作間隙内で実施される、請求項1〜14のいずれかに記載の方法。
【請求項16】
請求項1に記載の工程(b)は、液滴アクチュエータの液滴操作間隙内の複数の電極経路に沿って前記液滴を輸送することによって、前記増幅反応液滴を2以上の熱領域の間に循環させる工程を含む、請求項1〜15のいずれかに記載の方法。
【請求項17】
請求項1に記載の工程(b)は、液滴アクチュエータの液滴操作間隙内の共通の電極経路に沿って各々のサブセット内の液滴を輸送することによって、2つ以上の前記増幅反応液滴のサブセットを2つ以上の熱領域の間に循環させる工程を含む、請求項1〜16のいずれかに記載の方法。
【請求項18】
前記1つ以上の電極経路は、前記2つ以上の熱領域の間の1つ以上のループ経路を規定する、請求項17に記載の方法。
【請求項19】
請求項18に記載の方法であって、
(a)請求項1に記載の工程(b)は、電極経路のループの周りに複数の増幅反応液滴を輸送する工程を含み、
(b)前記方法は、所定数のサイクルが完了した場合、各々の増幅液滴を前記電極経路のループから除去する工程をさらに含む、方法。
【請求項20】
各々の増幅液滴を前記電極経路のループから除去する工程は、前記増幅反応液滴を前記液滴操作間隙の別の領域に輸送するために、電極により媒介される液滴操作を使用する工程を含む、請求項19に記載の方法。
【請求項21】
前記液滴操作間隙の領域は、検出が未実施の前記増幅液滴を保存するように選択された温度を有する温度制御領域を含む、請求項20に記載の方法。
【請求項22】
各々の増幅液滴を前記電極経路のループから除去する工程は、各々の増幅液滴を前記液滴アクチュエータの前記液滴操作間隙から除去する工程を含む、請求項19に記載の方法。
【請求項23】
前記電極経路は、2つ以上の熱領域の間で曲がっている、請求項17に記載の方法。
【請求項24】
(a)前記電極経路上の1つの電極から前記電極経路上の隣接する電極までの輸送時間は、各々の対の隣接する電極に関して実質的に均一であり、
(b)熱領域における滞留時間は、前記熱領域に存在する前記電極経路の各々の曲がり角における電極の数によって規定される、請求項17に記載の方法。
【請求項25】
請求項1に記載の工程(b)は、並行して熱領域の間に前記増幅反応液滴の2つ以上のサブセットを輸送する工程を含む、請求項1〜24のいずれかに記載の方法。
【請求項26】
請求項1に記載の工程(b)は、前記増幅反応液滴の2つ以上のサブセットを熱領域に連続して輸送する工程を含む、請求項1〜25のいずれかに記載の方法。
【請求項27】
請求項1に記載の工程(b)は、
(a)前記増幅反応液滴の第2のサブセットを第2の熱領域に輸送している間、前記増幅反応液滴の第1のサブセットを、第1の熱領域に輸送する工程と、
(b)前記増幅反応液滴の第2のサブセットを前記第1の熱領域に輸送している間、前記増幅反応液滴の第1のサブセットを前記第2の熱領域に輸送する工程と、
を含む、請求項1〜26のいずれかに記載の方法。
【請求項28】
連続して熱サイクルされた前記増幅反応液滴のサブセットは、共通の電極経路に沿って熱サイクルされる、請求項26に記載の方法。
【請求項29】
請求項1に記載の工程(b)は、並行して2つ以上のサブセットを増幅させる工程をさらに含む、請求項26に記載の方法。
【請求項30】
請求項1に記載の工程(b)は、全ての増幅反応液滴に関して、熱的に同時に行われる熱サイクルを含む、請求項1〜29のいずれかに記載の方法。
【請求項31】
請求項1に記載の工程(b)は、全ての増幅反応液滴に関して、熱的に同時に行われない熱サイクルを含む、請求項1〜30のいずれかに記載の方法。
【請求項32】
請求項1に記載の工程(b)は、液滴アクチュエータの熱サイクル領域を加熱および冷却することによって実施される、請求項1〜31のいずれかに記載の方法。
【請求項33】
請求項1に記載の工程(b)は、1回以上の熱サイクルのサイクル数にて熱領域における増幅反応液滴の滞留時間を変化させる工程を含む、請求項1〜32のいずれかに記載の方法。
【請求項34】
請求項1に記載の工程(d)を開始する前に、増幅反応液滴の全てのサブセットに関して、請求項1に記載の工程(b)を完了する工程を含む、請求項1〜33のいずれかに記載の方法。
【請求項35】
前記増幅反応液滴の第2のサブセットに関して請求項1に記載の工程(b)を完了する前に、増幅液滴の第1のサブセットに関して請求項1に記載の工程(d)を完了する工程を含む、請求項1〜34のいずれかに記載の方法。
【請求項36】
請求項1に記載の工程(c)は、2つ以上の前記増幅液滴のセットに関して、請求項1に記載の工程(d)を開始する前に、2つ以上の前記増幅液滴のセットを、前記液滴アクチュエータの熱サイクル領域から離れた位置に輸送する工程を含む、請求項1〜35のいずれかに記載の方法。
【請求項37】
請求項1に記載の工程(c)は、各々の前記液滴に関して、請求項1に記載の工程(d)を開始する前に、各々の増幅液滴を、熱サイクル領域から離れた位置に輸送する工程を含む、請求項1〜36のいずれかに記載の方法。
【請求項38】
請求項1に記載の工程(c)は、各々の増幅液滴を、請求項1に記載の工程(d)を実施するのに適切な温度を有する熱領域に輸送する工程を含む、請求項1〜37のいずれかに記載の方法。
【請求項39】
請求項1に記載の工程(c)は、配置された増幅液滴の各々の前記サブセットに関して、請求項1に記載の工程(d)を開始する前に、熱サイクル領域から離れた位置に前記増幅液滴の少なくとも1つのサブセットを配置する工程を含む、請求項1〜38のいずれかに記載の方法。
【請求項40】
請求項1に記載の工程(c)は、未結合の検出試薬を前記増幅核酸から分離する工程を含む、請求項1〜39のいずれかに記載の方法。
【請求項41】
請求項1に記載の工程(c)は、前記増幅液滴中の増幅を実質的に停止させる工程を含む、請求項1〜40のいずれかに記載の方法。
【請求項42】
請求項1に記載の工程(c)は、前記増幅液滴を、1つの液滴アクチュエータから別の液滴アクチュエータに輸送する工程を含む、請求項1〜41のいずれかに記載の方法。
【請求項43】
前記増幅液滴中の増幅を実質的に停止させる工程は、前記増幅反応を実質的に停止させるように液滴温度を調節する工程を含む、請求項41に記載の方法。
【請求項44】
前記増幅液滴中の増幅を実質的に停止させる工程は、前記増幅反応を実質的に停止させるように試薬を前記増幅液滴に添加する工程を含む、請求項43に記載の方法。
【請求項45】
試薬を前記増幅液滴に添加する工程は、前記増幅液滴と試薬液滴とを混合する工程を含み、前記試薬液滴は、前記増幅反応を実質的に停止させるように選択された試薬を含む、請求項44に記載の方法。
【請求項46】
前記増幅反応を実質的に停止させるように選択された試薬は、ポリメラーゼ活性を妨げること、ポリメラーゼ補助因子活性を妨げること、核酸に結合すること、および/または鉄イオンを放出することによって、前記増幅反応を実質的に停止させる試薬を含む、請求項45に記載の方法。
【請求項47】
請求項1に記載の工程(c)および請求項1に記載の工程(d)は、前記サブセットの熱サイクルの完了後に、前記増幅液滴のサブセットの各々について実施される、請求項61に記載の方法。
【請求項48】
(a)前記増幅反応液滴は検出試薬を含まず、
(b)請求項1に記載の工程(c)は、検出試薬を前記増幅液滴に添加する工程を含む、請求項1〜47のいずれかに記載の方法。
【請求項49】
検出試薬を前記増幅液滴に添加する工程は、各々の増幅液滴と検出試薬を含む液滴とを混合する工程を含む、請求項48に記載の方法。
【請求項50】
(a)請求項1に記載の工程(c)は、各々の前記増幅液滴と1つ以上の検出試薬を含む液滴とを混合する工程を含み、
(b)請求項1に記載の工程(d)は、前記検出試薬によって媒介されるシグナルに基づいて増幅を検出する工程を含む、請求項1〜49のいずれかに記載の方法。
【請求項51】
請求項1に記載の工程(d)は、前記液滴の検出ウィンドウへの輸送後に、各々の増幅液滴からシグナルを検出する工程を含む、請求項1〜50のいずれかに記載の方法。
【請求項52】
請求項1に記載の工程(c)は、増幅液滴の1つ以上のサブセットのセットを、検出のために検出ウィンドウに輸送する工程を含む、請求項1〜51のいずれかに記載の方法。
【請求項53】
(a)請求項1に記載の工程(b)は、液滴アクチュエータの液滴操作間隙内で達成され、
(b)請求項1に記載の工程(c)は、前記増幅液滴の1つ以上を、検出のために前記液滴操作間隙の外へ輸送する工程を含む、請求項1〜52のいずれかに記載の方法。
【請求項54】
請求項1に記載の工程(d)は、前記液滴アクチュエータの前記液滴操作間隙の外部のリザーバー内で実施される、請求項53に記載の方法。
【請求項55】
請求項1に記載の工程(c)は、増幅液滴のサブセットを検出ウィンドウに輸送し、少ないサイクル数のサブセットで開始し、多いサイクル数のサブセットまで進行させる工程を含む、請求項1〜54のいずれかに記載の方法。
【請求項56】
請求項1に記載の工程(d)は、増幅液滴のアレイを走査する工程を含む、請求項1〜55のいずれかに記載の方法。
【請求項57】
請求項1に記載の工程(d)は、増幅液滴のアレイを画像化する工程を含む、請求項1〜56のいずれかに記載の方法。
【請求項58】
(a)前記増幅反応液滴は、並行して請求項1に記載の工程(b)に入り、
(b)前記増幅液滴は、連続して請求項1に記載の工程(c)に入り、
(c)前記増幅液滴は、連続して請求項1に記載の工程(d)に入る、
請求項1〜57のいずれかに記載の方法。
【請求項59】
(a)前記増幅反応液滴は、並行して請求項1に記載の工程(b)に入り、
(b)前記増幅液滴は、連続して請求項1に記載の工程(c)に入り、
(c)前記増幅液滴は、並行して請求項1に記載の工程(d)に入る、
請求項1〜58のいずれかに記載の方法。
【請求項60】
(a)前記増幅反応液滴は、連続して請求項1に記載の工程(b)に入り、
(b)前記増幅液滴は、並行して請求項1に記載の工程(c)に入る、
請求項1〜59のいずれかに記載の方法。
【請求項61】
請求項1に記載の工程(e)は、前記増幅液滴のサブセットの各々についての熱サイクルエンドポイントにおけるシグナルの増加または減少を決定することによって、前記増幅液滴に存在する前記増幅核酸の量を決定する工程を含む、請求項1〜60のいずれかに記載の方法。
【請求項62】
請求項1に記載の工程(e)は、前記サンプル液滴に存在する前記標的核酸の量を決定するために、前記増幅液滴に存在する前記増幅核酸の量を使用する工程をさらに含む、請求項1〜61のいずれかに記載の方法。
【請求項63】
請求項1に記載の工程(e)は、前記サンプル液滴に存在する前記標的核酸の量を決定するために、異なる数の熱サイクル後に前記増幅液滴に存在する前記増幅核酸の量を使用する工程をさらに含む、請求項1〜62のいずれかに記載の方法。
【請求項64】
前記標的核酸を増幅させるための異なる条件は、前記増幅反応液滴の各々のサブセットについての異なる数の熱サイクルを含む、請求項1〜63のいずれかに記載の方法。
【請求項65】
前記増幅反応液滴は、検出試薬を含む、請求項1〜64のいずれかに記載の方法。
【請求項66】
前記増幅反応液滴は、有意な量の検出試薬を含まない、請求項1〜65のいずれかに記載の方法。
【請求項67】
増幅試薬を含む1つ以上の前記液滴は、検出試薬をさらに含む、請求項1〜66のいずれかに記載の方法。
【請求項68】
増幅試薬を含む1つ以上の前記液滴は、有意な量の検出試薬を含まない、請求項1〜67のいずれかに記載の方法。
【請求項69】
前記検出試薬は、核酸結合剤を含む、請求項1〜68のいずれかに記載の方法。
【請求項70】
前記核酸結合剤は、核酸増幅の割合を有意に阻害する、請求項69に記載の方法。
【請求項71】
前記核酸結合剤は、挿入剤を含む、請求項69および以下の請求項に記載の方法。
【請求項72】
前記挿入剤は、蛍光色素を含む、請求項71に記載の方法。
【請求項73】
前記標的核酸は、遺伝性疾患または感染病の指標である、請求項1〜72のいずれかに記載の方法。
【請求項74】
前記標的核酸は、生物学的集団由来の個体の個々またはサブグループの同定の指標である、請求項1〜73のいずれかに記載の方法。
【請求項75】
(a)前記核酸増幅反応液滴の1つ以上を、請求項1に記載の工程(b)の前に最初の検出工程に供し、
(b)請求項1に記載の工程(e)は、前記最初の検出工程において検出されたシグナルと、請求項1に記載の工程(d)において検出されたシグナルとの間の比較を含む、請求項1〜74のいずれかに記載の方法。
【請求項76】
開始サンプルに存在する前記標的核酸を定量化するために所定の範囲の統計的確実性内の十分なデータが収集された場合、前記方法を停止させる工程をさらに含む、請求項1〜75のいずれかに記載の方法。
【請求項77】
(a)前記増幅液滴および/または前記サンプルに存在する前記増幅核酸の量を決定するための十分なデータを提供すると予想される第1のセットのサイクル数を選択する工程と、
(b)前記選択されたサイクル数の各々に関して、1つ以上の増幅反応液滴のサブセットを、請求項1に記載の工程(b)、請求項1に記載の工程(c)、請求項1に記載の工程(d)および請求項1に記載の工程(e)に供する工程と、
(c)前記サンプルに存在する前記標的核酸を同定または定量するために所定の範囲の統計的確実性内の十分なデータが収集されたか否かを決定する工程と、
(d)(i)前記開始サンプルに存在する前記標的核酸を同定または定量化するために所定の範囲の統計的確実性内の十分なデータが収集されるまで、または(ii)前記標的核酸が前記サンプルに存在しないことを決定するために所定の範囲の統計的確実性内の十分なデータが収集されるまで、新しいセットのサイクル数で工程(a)、(b)および(c)を繰り返す工程と、
をさらに含む、請求項1〜76のいずれかに記載の方法。
【請求項78】
請求項77に記載の工程(c)は、前記サンプルに存在する前記標的核酸を同定するために所定の範囲の統計的確実性内の十分なデータが収集されたか否かを決定する工程を含む、請求項77に記載の方法。
【請求項79】
請求項77に記載の工程(c)は、前記サンプルに存在する前記標的核酸を定量化するために所定の範囲の統計的確実性内の十分なデータが収集されたか否かを決定する工程を含む、請求項77に記載の方法。
【請求項80】
サンプル中の標的核酸の増加をモニターする方法であって、前記方法は、
(a)核酸増幅反応液滴のセットを提供する工程であって、各々の液滴は前記サンプルの一部を含む工程と、
(b)前記標的核酸を増幅するための条件下で、前記増幅反応液滴の2つ以上のサブセットを熱サイクルして、増幅二本鎖核酸を含む増幅液滴を生じる工程であって、前記増幅反応液滴の各々のサブセットは、
(i)前記増幅反応液滴の1つ以上を含み、
(ii)異なる数のサイクル数について熱サイクルされ、
(iii)前記サブセットについての所定数のサイクルの完了前に検出に供されない、工程と、
(c)前記増幅液滴の各々と、増幅核酸を検出するための検出試薬とを混合して、検出準備液滴を生じる工程を含む、検出準備プロコルを実施する工程と、
(d)前記検出準備液滴からシグナルを検出する工程と、
(e)前記シグナルに基づいて、前記増幅液滴および/または前記サンプルに存在する前記増幅核酸の量を決定する工程と、
を含む、方法。
【請求項81】
(a)液滴操作間隙を形成する1つ以上の基板と、
(b)前記1つ以上の基板と結合され、前記液滴操作間隙内で液滴操作を媒介するように配置される電極と、
(c)増幅試薬を含み、検出試薬を含まない1つ以上の液滴を含む第1のリザーバーと、
(d)1つ以上の検出試薬を含む第2のリザーバーと、
(e)前記液滴操作間隙を備える前記第1のリザーバーおよび前記第2のリザーバーと流動的に接続される1つ以上の流体経路と、
(f)サンプルを前記液滴操作間隙内に充填するための手段と、
を備える、予め組み込まれている液滴アクチュエータカートリッジ。
【請求項82】
(a)請求項81に記載の予め組み込まれている液滴アクチュエータカートリッジと、
(b)前記カートリッジを用いて増幅プロトコルを実行するためのソフトウェアと、
を備えるキット。
【請求項83】
検体を検出する方法であって、前記方法は、
(a)(i)検体の存在および/または量の指標であるシグナル生成物質と、(ii)前記シグナル生成物質によって生成されるシグナルを妨げることができる1つ以上の磁性反応ビーズと、を含む液滴を検出ウィンドウ内に提供する工程と、
(b)(i)前記磁性反応ビーズを前記検出ウィンドウから磁性的に除去するため、ならびに/あるいは(ii)前記検出ウィンドウに前記液滴を輸送および/または保持している間、前記磁性反応ビーズが前記検出ウィンドウに侵入することを磁性的に抑制するために、磁場を用いる工程と、
(c)前記シグナル生成物質によって生成されるシグナルを検出する工程と、
を含む、方法。
【請求項84】
(a)前記液滴は、液滴アクチュエータの液滴操作間隙に提供され、
(b)前記検出ウィンドウは、前記液滴アクチュエータの基板内に開口部またはウィンドウを含む、請求項83に記載の方法。
【請求項85】
(a)請求項83に記載の工程(b)は、前記検出ウィンドウに近接する固定磁場を提供する工程を含み、
(b)前記液滴を前記検出ウィンドウに輸送する工程は、前記ビーズが、前記検出ウィンドウから離れた位置に引き付けられ、および/または前記検出ウィンドウに侵入することを抑制する前記固定磁石に十分に近接する位置に前記磁性反応ビーズを送達する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項86】
前記磁場は、固定永久磁石を含む磁場源によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項87】
前記磁場は、移動可能な永久磁石を含む磁場源によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項88】
前記磁場は、電磁石を含む磁場源によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項89】
前記磁場は、前記液滴の端部において前記磁性反応ビーズを凝集する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項90】
前記磁場は、前記検出ウィンドウの外部にある前記液滴の領域内で前記磁性反応ビーズを凝集する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項91】
前記磁場は、前記液滴から離れて前記磁性反応ビーズを分解する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項92】
前記液滴が所定の位置に保持されるか、または電極により媒介される力によって移動される間、前記磁場は、前記液滴から離れて前記磁性反応ビーズを分解する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項93】
前記液滴が少なくとも部分的に前記検出ウィンドウにある間、前記磁場は、前記磁性反応ビーズを前記液滴の端部に引き付ける方法で前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項94】
前記液滴が前記磁石の上を通過する場合、前記磁場は、前記液滴の外側に前記磁性反応ビーズを引き付ける、請求項83に記載の方法。
【請求項95】
前記液滴が前記磁石の近接に近づく場合、前記磁場は、前記液滴の外側に前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項96】
前記液滴が前記検出ウィンドウに近づく場合、前記磁場は、前記液滴の外部へ前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項97】
前記シグナルは、蛍光色素によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項98】
前記液滴が前記検出ウィンドウに輸送される場合、前記ビーズの実質的に全てが、前記検出ウィンドウに侵入または再侵入するのを抑制する方法で、前記磁場は、前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項99】
前記検出ウィンドウは、液滴アクチュエータ装置の基板に設けられる、請求項83および以下の請求項のいずれかに記載の方法。
【請求項100】
前記液滴アクチュエータは、液滴操作基板に結合された電極の複数の経路を備え、各々の経路は、
(a)検出ウィンドウ、ならびに
(b)(i)前記磁性反応ビーズを前記対応する検出ウィンドウから磁性的に除去するように、および/または(ii)前記検出ウィンドウ内に前記液滴を輸送および/または保持している間、前記磁性反応ビーズが前記対応する検出ウィンドウに侵入することを磁性的に抑制するように、配置される前記経路に近接する磁場、
に結合される、請求項99に記載の方法。
【請求項101】
前記液滴は、1つ以上の検体の存在、非存在および/または量のシグナルの指標を放出する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項102】
前記1つ以上の検体は、増幅核酸を含む、請求項101に記載の方法。
【請求項103】
(a)前記検出ウィンドウは、液滴アクチュエータの基板内に位置し、
(b)前記液滴アクチュエータは、熱サイクル反応を実施するための電極の経路に沿って温度制御領域を備え、
(c)前記方法は、(i)増幅準備液滴を熱サイクルして、増幅液滴を生じる工程と、(ii)前記増幅液滴を前記検出ウィンドウに輸送する工程とを含む、
請求項83および以下の請求項のいずれかに記載の方法。
【請求項104】
1以上の熱サイクルの後、前記電極の経路に沿って磁性反応ビーズを含む液滴を、少なくとも部分的に前記検出ウィンドウに輸送する工程を含む、請求項103に記載の方法。
【請求項105】
液滴を熱サイクルする方法であって、前記方法は、
(a)流動性の充填流体によって少なくとも部分的に囲まれた液滴を提供する工程であって、前記液滴は、(i)標的核酸を潜在的に含み、(ii)前記標的核酸の存在下で増幅を生じるのに十分な試薬を含み、熱サイクルプロトコルを実施している間、前記試薬は前記充填流体中で有意に分離しない蛍光色素分子を含む、工程と、
(b)前記標的核酸の存在下で増幅を誘導するために熱サイクルプロトコルに従って前記液滴の温度を調節する工程と、
を含む、方法。
【請求項106】
前記蛍光色素分子は、極性蛍光色素分子を含む、請求項105に記載の方法。
【請求項107】
前記蛍光色素分子は、細胞膜に実質的に不浸透性である、請求項105に記載の方法。
【請求項108】
前記蛍光色素分子は、細胞膜に完全に不浸透性である、請求項105に記載の方法。
【請求項109】
前記蛍光色素分子は、EVAGREEN(登録商標)蛍光色素分子を含む、請求項105に記載の方法。
【請求項110】
前記蛍光色素分子は、TO−PRO1蛍光色素分子を含む、請求項105に記載の方法。
【請求項111】
前記充填流体は、シリコーンオイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項112】
前記充填流体は、10〜20の炭素オイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項113】
前記充填流体は、15〜20の炭素オイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項114】
前記充填流体は、ヘキサデカンオイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項115】
前記充填流体は、脱ガスオイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項116】
液滴を提供する工程は、液滴アクチュエータの液滴操作間隙内に液滴を提供する工程を含む、請求項105および以下の請求項のいずれかに記載の方法。
【請求項117】
熱サイクルプロトコルに従って前記液滴の温度を調節する工程は、前記液滴アクチュエータの液滴操作間隙内の前記液滴を加熱および/または冷却する工程を含む、請求項116および以下の請求項のいずれかに記載の方法。
【請求項118】
熱サイクルプロトコルに従って前記液滴の温度を調節する工程は、電極により媒介される液滴操作を用いて前記液滴操作間隙内の熱領域の間に前記液滴を輸送する工程を含む、請求項116および以下の請求項のいずれかに記載の方法。
【請求項119】
検出アクチュエータでプロトコルを実施する方法であって、前記方法は、
(a)前記液滴アクチュエータの1つ以上の領域を、不動態化剤を含む液滴を有する前記領域内の1つ以上の電極で液滴操作を実施することによって処理する工程と、
(b)前記液滴アクチュエータの前記処理された領域の1つ以上を用いて前記プロトコルを実施する工程と、
を含む、方法。
【請求項120】
(a)前記プロトコルは、標的核酸の検体中での工程を含み、
(b)前記不動態化剤は、前記標的核酸でない核酸を含む、
請求項119に記載の方法。
【請求項121】
前記プロトコルは、核酸増幅プロトコルを含む、請求項120に記載の方法。
【請求項122】
前記プロトコルは、熱サイクルプロトコルを含む、請求項120に記載の方法。
【請求項123】
前記不動態化剤は、核酸を含む、請求項119に記載の方法。
【請求項124】
前記不動態化剤は、ポリビニルピロリドンを含む、請求項119に記載の方法。
【請求項125】
前記不動態化剤は、ポリエチレングリコールを含む、請求項119に記載の方法。
【請求項126】
前記不動態化剤は、界面活性剤を含む、請求項119に記載の方法。
【請求項127】
前記不動態化剤は、トゥイーンを含む、請求項119に記載の方法。
【請求項128】
前記不動態化剤は、アルブミンを含む、請求項119に記載の方法。
【請求項129】
前記不動態化剤は、血清アルブミンを含む、請求項119に記載の方法。
【請求項130】
前記不動態化剤は、ウシ血清アルブミンを含む、請求項119に記載の方法。
【請求項131】
前記不動態化剤は、色素を含む、請求項119に記載の方法。
【請求項132】
前記不動態化剤は、前記液滴アクチュエータの表面上で吸収するように選択される、請求項119に記載の方法。
【請求項133】
前記不動態化剤は、充填流体中で吸収するように選択される、請求項119に記載の方法。
【請求項134】
前記1つ以上の液滴は、十分な不動態化剤を、実質的に飽和した潜在的な不動態化部位へ送達する、請求項119に記載の方法。
【請求項135】
前記プロトコルは、前記不動態化剤を含む液滴を用いて実施される、請求項119に記載の方法。
【請求項136】
(a)前記プロトコルは、核酸増幅プロトコルを含み、
(b)前記核酸増幅プロトコルおよび処理する工程は、液滴を用いて同時に実施され、前記液滴は、(i)核酸増幅試薬、(ii)前記不動態化剤を含む、請求項135に記載の方法。
【請求項137】
(a)液滴操作基板と、
(b)液滴操作表面とカバーとの間に液滴操作間隙を形成するために、前記液滴操作表面に隣接し、前記液滴操作表面から離間しているカバーであって、前記液滴操作間隙は少なくとも250μmの高さを有する、カバーと、
(c)前記液滴操作基板および/またはカバーに結合され、熱サイクルプロトコルに従って熱領域の間に液滴を輸送するように配置された電極の経路と、
(d)前記液滴操作間隙内に1つ以上の熱領域を規定するように配置される温度制御素子と、
を備える、液滴アクチュエータ。
【請求項138】
前記液滴操作間隙は、実質的に球形形状の単一のサイズの液滴を与えるように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項139】
前記液滴操作間隙は、約250μm〜約500μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項140】
前記液滴操作間隙は、約275μm〜約450μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項141】
前記液滴操作間隙は、約300μm〜約400μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項142】
前記液滴操作間隙は、約320μm〜約375μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項143】
前記液滴操作間隙は、約320μm〜約350μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項144】
前記電極はピッチを有し、前記液滴操作間隙は、約7:1〜約2.8:1の範囲のピッチ:高さの比を規定する高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項145】
前記電極はピッチを有し、前記液滴操作間隙は、約6:1〜約3:1の範囲のピッチ:高さの比を規定する高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項146】
前記電極はピッチを有し、前記液滴操作間隙は、約4.3:1〜約3.4:1の範囲のピッチ:高さの比を規定する高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項147】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて5%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項148】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項149】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項150】
前記液滴操作間隙は、1回の熱サイクルにつき0.1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項151】
前記液滴操作間隙は、1回の熱サイクルにつき0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項152】
前記液滴操作間隙は、1回の熱サイクルにつき0.001%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項153】
前記液滴操作間隙は、熱サイクルプロトコルの間、容積減少を実質的に排除するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項154】
熱サイクル反応を実施する方法であって、前記方法は、
(a)(i)液滴操作基板と、(ii)液滴操作表面とカバーとの間に液滴操作間隙を形成するために、前記液滴操作表面に隣接し、前記液滴操作表面から離間しているカバーであって、前記液滴操作間隙は少なくとも250μmの高さを有する、カバーと、(iii)前記液滴操作基板に結合され、および/または熱サイクルプロトコルに従った熱領域の間で液滴を輸送するために覆い、配置される電極の経路と、(iv)前記液滴操作間隙内に1つ以上の熱領域を規定するように配置される温度制御素子と、を備える液滴アクチュエータを提供する工程と、
(b)少なくとも部分的に前記検出ウィンドウに前記電極の経路に沿って磁性反応ビーズを含む液滴を輸送し、1つ以上の前記ビーズが前記検出ウィンドウに侵入することを抑制する方法で、磁石が、前記磁性反応ビーズを引き付ける工程と、
(c)前記液滴からシグナルを検出するためにセンサを使用する工程と、
を含む、方法。
【請求項155】
前記液滴操作間隙は、実質的に球形形状の単一のサイズの液滴を与えるように選択される高さを有する、請求項154に記載の方法。
【請求項156】
前記液滴操作間隙は、約250μm〜約500μmの範囲の高さを有する、請求項154に記載の方法。
【請求項157】
前記液滴操作間隙は、約275μm〜約450μmの範囲の高さを有する、請求項154に記載の方法。
【請求項158】
前記液滴操作間隙は、約300μm〜約400μmの範囲の高さを有する、請求項154に記載の方法。
【請求項159】
前記液滴操作間隙は、約320μm〜約375μmの範囲の高さを有する、請求項154に記載の方法。
【請求項160】
前記液滴操作間隙は、約320μm〜約350μmの範囲の高さを有する、請求項154に記載の方法。
【請求項161】
前記電極はピッチを有し、前記液滴操作間隙は、約7:1〜約2.8:1の範囲のピッチ:高さの比を規定する高さを有する、請求項154に記載の方法。
【請求項162】
前記電極はピッチを有し、前記液滴操作間隙は、約6:1〜約3:1の範囲のピッチ:高さの比を規定する高さを有する、請求項154に記載の方法。
【請求項163】
前記電極はピッチを有し、前記液滴操作間隙は、約4.3:1〜約3.4:1の範囲のピッチ:高さの比を規定する高さを有する、請求項154に記載の方法。
【請求項164】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて5%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項165】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項166】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項167】
前記液滴操作間隙は、1回の熱サイクルにつき0.1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項168】
前記液滴操作間隙は、1回の熱サイクルにつき0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項169】
前記液滴操作間隙は、1回の熱サイクルにつき0.001%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項170】
前記液滴操作間隙は、熱サイクルプロトコルの間、容積減少を実質的に排除するように選択される高さを有する、請求項154に記載の方法。
【請求項171】
解析するためのサンプルを調製する方法であって、前記方法は、
(a)(i)液滴操作基板と、(ii)前記基板の液滴操作表面上で液滴操作を実施するように配置される電極と、(iii)前記液滴操作表面とカバーとの間に液滴操作間隙を形成するために、前記液滴操作表面に隣接し、前記液滴操作表面から離間している、カバーと、(iv)上部の基板に結合され、1つ以上の標的検体および/または1つ以上の標的検体を含む物質に対する親和性を有するビーズを含むリザーバーと、(v)前記リザーバーから前記液滴操作間隙に延在する液体経路と、(vi)前記液滴操作基板に結合され、磁性反応ビーズを引き付けるのに十分な磁場を生成するように構成される磁場源と、を備える液滴アクチュエータを提供する工程と、
(b)前記リザーバー内にサンプルを供給する工程であって、前記サンプルは、前記標的物質のうちの1つ以上を潜在的に含む工程と、
(c)前記液体経路を通して前記液滴操作間隙内に前記磁性ビーズを含むサンプルを流動させる工程と、
(d)前記磁性反応ビーズを磁石で凝集させる工程と、
(e)前記磁場を除去するか、または前記磁場から前記ビーズを除去して、磁性ビーズを含む前記液滴操作間隙内にサンプル液滴を生じさせる工程と、
を含む、方法。
【請求項172】
前記液体経路は、実質的に真っ直ぐな液体経路である、請求項171に記載の方法。
【請求項173】
前記磁石は、前記リザーバーから前記液滴操作間隙内に1つ以上のビーズを引き付けるのに十分な磁場強度を有する、請求項172に記載の方法。
【請求項174】
前記液滴アクチュエータは、前記液滴操作基板に結合され、前記液体経路を通して前記液滴操作間隙に侵入する流体を受容するように配置されるリザーバー電極を備える、請求項171に記載の方法。
【請求項175】
前記磁石は、前記液体経路に対して前記リザーバー電極の反対側に配置される、請求項174に記載の方法。
【請求項176】
前記磁石は、電磁石を含む、請求項171に記載の方法。
【請求項177】
前記磁石は、永久磁石を含む、請求項171に記載の方法。
【請求項178】
前記永久磁石は、空間的に調節可能である、請求項177に記載の方法。
【請求項179】
前記永久磁石は、移動可能な磁気シールドに結合され、前記磁気シールドは、
(a)第1の位置における前記液滴操作間隙内の前記永久磁石の磁場を遮断または妨げることができ、
(b)第2の位置における前記液滴操作間隙内の前記永久磁石の磁場を遮断または妨げることができない、
請求項177に記載の方法。
【請求項180】
前記液滴アクチュエータは、前記リザーバー内のサンプル流体に音波エネルギーを与えるように配置される超音波処理器を備える、請求項171に記載の方法。
【請求項181】
前記リザーバー内の前記サンプルを超音波処理する工程をさらに含む、請求項180に記載の方法。
【請求項182】
前記電極の1つ以上に結合される第2の磁石をさらに備える、請求項171に記載の方法。
【請求項183】
(a)1つ以上の標的検体を含む物質は、細胞を含み、前記ビーズは前記細胞に対して親和性を有し、
(b)前記方法は、請求項171に記載の工程(e)によって生成される磁性ビーズを含む前記液滴操作間隙内の前記サンプル液滴と、細胞溶解試薬を含む溶解液滴とを混合する工程をさらに含む、
請求項171に記載の方法。
【請求項184】
請求項183に記載の(b)において生成された前記混合された液滴を超音波処理する工程を含む、請求項183に記載の方法。
【請求項185】
前記磁場を再印加して、前記磁性ビーズを固定化させる工程をさらに含む、請求項183に記載の方法。
【請求項186】
前記磁性ビーズから離れた位置に前記液滴を輸送する工程をさらに含む、請求項185に記載の方法。
【請求項187】
前記磁性ビーズから離れた位置に前記液滴の一部を輸送する工程をさらに含む、請求項185に記載の方法。
【請求項188】
離れた位置に輸送された前記液滴または前記液滴の一部と、前記1つ以上の標的検体に対する親和性を有するビーズを含む液滴とを混合する工程をさらに含む、請求項186または187に記載の方法。
【請求項189】
前記1つ以上の標的検体に対する親和性を有するビーズを洗浄するために洗浄プロトコルを実施して、実質的に精製された標的検体を含むビーズを含む液滴を生じる工程をさらに含む、請求項188に記載の方法。
【請求項190】
前記実質的に精製された標的検体を含むビーズを含む前記液滴を用いて解析プロトコルを実施する工程をさらに含む、請求項189に記載の方法。
【請求項191】
前記解析プロトコルを実施する工程は、前記液滴操作間隙内で達成される、請求項190に記載の方法。
【請求項192】
前記実質的に精製された標的検体を含むビーズを含む前記液滴は、前記解析プロトコルを実施する前に、前記液滴操作間隙から除去される、請求項190に記載の方法。
【請求項193】
前記解析プロトコルの結果の出力の指標を提供する工程をさらに含む、請求項190に記載の方法。
【請求項194】
前記実質的に精製された標的検体を含むビーズを含む液滴を、前記液滴操作間隙から除去する工程をさらに含む、請求項189に記載の方法。
【請求項195】
前記1つ以上の標的検体を、前記実質的に精製された標的検体を含むビーズから放出する工程をさらに含む、請求項189に記載の方法。
【請求項196】
前記放出する工程は、前記実質的に精製された標的検体を含むビーズを含む液滴と、放出バッファーを含む液滴とを混合して、前記ビーズおよび前記放出された1つ以上の標的検体を含む液滴を生じる工程を含む、請求項195に記載の方法。
【請求項197】
前記ビーズおよび前記放出された1つ以上の標的検体を含む前記液滴から前記ビーズを除去して、実質的に精製された標的検体を含み、実質的にビーズを含まない液滴を生じる工程をさらに含む、請求項196に記載の方法。
【請求項198】
前記実質的に精製された標的検体を含み、実質的にビーズを含まない液滴を、前記液滴操作間隙から除去する工程をさらに含む、請求項197に記載の方法。
【請求項199】
前記実質的に精製された標的検体を含み、実質的にビーズを含まない液滴を用いて検体プロトコルを実施する工程をさらに含む、請求項197に記載の方法。
【請求項200】
前記解析プロトコルの結果の出力の指標を提供する工程をさらに含む、請求項199に記載の方法。
【請求項201】
前記方法の工程の1つ以上は、前記液滴アクチュエータおよび前記方法の工程の1つ以上を実施するようにプログラムされたプロセッサを含むシステムによって実施される、請求項171および以下の請求項のいずれかに記載の方法。
【請求項202】
前記解析プロトコルの結果の、使用者により読み取り可能な出力の指標を出力する工程をさらに含む、請求項201に記載の方法。
【請求項203】
前記標的検体は、核酸を含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項204】
前記標的検体は、タンパク質またはペプチドを含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項205】
前記標的検体は、抗体を含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項206】
前記標的検体は、小有機分子を含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項207】
前記液滴操作間隙は、流動性の充填流体で満たされる、請求項171および以下の請求項のいずれかに記載の方法。
【請求項208】
液滴アクチュエータを操作する方法であって、前記方法は、
(a)内部液滴操作間隙を形成するように構成される1つ以上の基板を備える液滴アクチュエータ装置を提供する工程と、
(b)前記液滴操作間隙内に流動性の充填流体を提供する工程と、
(c)前記液滴操作間隙内の前記充填流体中で液滴プロトコルを実施する工程と、
(d)前記液滴操作間隙内に前記充填流体を再配置する工程と、
(e)同じまたは異なる液滴プロトコルを用いて工程(c)を繰り返す工程と、
を含む、方法。
【請求項209】
請求項208に記載の工程(d)および請求項208に記載の工程(e)を、2回以上繰り返す工程をさらに含む、請求項208に記載の方法。
【請求項210】
請求項208に記載の工程(d)および請求項208に記載の工程(e)を、5回以上繰り返す工程をさらに含む、請求項208に記載の方法。
【請求項211】
請求項208に記載の工程(d)および請求項208に記載の工程(e)を、10回以上繰り返す工程をさらに含む、請求項208に記載の方法。
【請求項212】
請求項208に記載の工程(d)は、前記液滴操作間隙を通して充填流体をフラッシュする工程をさらに含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項213】
前記液滴操作間隙を通して充填流体をフラッシュする工程は、所定量のフラッシングが達成されるまで続けられる、請求項212に記載の方法。
【請求項214】
前記液滴操作間隙を通して充填流体をフラッシュする工程は、洗浄の指標が所定のレベルに到達するまで続けられる、請求項212に記載の方法。
【請求項215】
前記フラッシングの量は、自動化される、請求項213または214に記載の方法。
【請求項216】
請求項208に記載の工程(c)は、診断プロトコルを実施する工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項217】
請求項208に記載の工程(c)は、核酸増幅プロトコル、核酸シークエンシングプロトコル、免疫アッセイプロトコル、および酵素アッセイプロトコルからなる群より選択されるプロトコルを実施する工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項218】
請求項208に記載の工程(c)は、請求項208に記載の工程(d)を実施する前に、2回以上繰り返される、請求項208および以下の請求項のいずれかに記載の方法。
【請求項219】
前記流動性の充填流体は、請求項208に記載の工程(c)の各々の繰り返しの後に汚染物質について試験され、請求項208に記載の工程(d)は所定のレベルの汚染物質が検出された後に実施される、請求項218に記載の方法。
【請求項220】
請求項208に記載の工程(c)の各々の繰り返し後に汚染物質について試験すること、および請求項208に記載の工程(d)への進行の決定は、自動化される、請求項219に記載の方法。
【請求項221】
請求項208に記載の工程(d)は、前記液滴操作間隙を通して、前記液滴操作間隙の外部へ、流動性の充填流体源から前記流動性の充填流体を流動させることを含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項222】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に、前記液滴操作間隙を通して洗浄流体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項223】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に、前記液滴操作間隙を通して充填流体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項224】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に、前記液滴操作間隙を通して加熱された洗浄液体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項225】
前記加熱された洗浄液体は、汚染物質を溶解または分解するように選択された温度を有する、請求項224に記載の方法。
【請求項226】
前記加熱された洗浄液体は、約30℃〜約125℃の範囲の温度を有する、請求項224に記載の方法。
【請求項227】
前記加熱された洗浄液体は、約60℃〜約115℃の範囲の温度を有する、請求項224に記載の方法。
【請求項228】
前記加熱された洗浄液体は、約75℃〜約105℃の範囲の温度を有する、請求項224に記載の方法。
【請求項229】
前記加熱された洗浄液体は、約90℃より高い温度を有する、請求項224に記載の方法。
【請求項230】
前記加熱された洗浄液体は、約100℃より高い温度を有する、請求項224に記載の方法。
【請求項231】
前記加熱された洗浄液体は、約125℃より高い温度を有する、請求項224に記載の方法。
【請求項232】
前記加熱された洗浄液体は、約150℃より高い温度を有する、請求項224に記載の方法。
【請求項233】
前記加熱された洗浄液体は、前記液滴アクチュエータの1つ以上の構成要素が過度に損傷を受ける温度より低い温度を有する、請求項224および以下の請求項のいずれかに記載の方法。
【請求項234】
前記加熱された洗浄液体は、充填流体を含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項235】
前記加熱された洗浄液体は、オイルを含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項236】
前記加熱された洗浄液体は、溶媒を含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項237】
前記加熱された洗浄液体は、水性洗浄液体を含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項238】
前記洗浄液体は、
(a)親油性物質が溶解できる成分と、
(b)親水性物質が溶解できる成分と、
を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項239】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に前記液滴アクチュエータ間隙を乾燥させるために、前記液滴アクチュエータ間隙を通してガスを流動させる工程をさらに含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項240】
前記ガスは、空気を含む、請求項239に記載の方法。
【請求項241】
前記ガスは、約50℃より高い温度を有する、請求項239に記載の方法。
【請求項242】
前記ガスは、約75℃より高い温度を有する、請求項239に記載の方法。
【請求項243】
前記ガスは、約100℃より高い温度を有する、請求項239に記載の方法。
【請求項244】
前記ガスは、約125℃より高い温度を有する、請求項239に記載の方法。
【請求項245】
前記ガスは、約150℃より高い温度を有する、請求項239に記載の方法。
【請求項246】
前記ガスは、前記液滴アクチュエータの1つ以上の成分が過度に損傷を受ける温度より低い温度を有する、請求項239および以下の請求項のいずれかに記載の方法。
【請求項247】
請求項208に記載の工程(d)は、前記液滴アクチュエータ間隙を通して前記ガスを流動させる前に、前記液滴アクチュエータ間隙を通して洗浄液体を流動させる工程を含む、請求項239に記載の方法。
【請求項248】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約50%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項249】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約75%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項250】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約90%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項251】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約95%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項252】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約99%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項253】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約99.9%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項254】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の実質的に全てを置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項255】
(a)前記液滴操作間隙の1つ以上の表面は、コーティングを含み、
(b)前記洗浄液体は、前記コーティングの層を除去するように選択される、
請求項208および以下の請求項のいずれかに記載の方法。
【請求項256】
請求項208に記載の工程(d)は、前記液滴操作間隙内の前記充填流体を置き換える前に、所定の温度を規定するように、前記液滴操作間隙を通して冷却液体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項257】
前記洗浄流体は、溶媒を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項258】
前記洗浄流体は、水溶液を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項259】
前記洗浄流体は、親油性化合物を溶解する1つ以上の成分、および親水性化合物を溶解する1つ以上の成分を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項260】
請求項208および以下の請求項のいずれかに記載の方法を実施するための命令を有するプログラムを含む、コンピューター可読媒体。
【請求項261】
(a)内部液滴操作間隙を形成するように構成される1つ以上の基板を備える液滴アクチュエータ装置と、
(b)流動性の充填流体源に流動的に接続される前記液滴操作間隙内の開口部と、
(c)前記開口部を通して、前記液滴操作間隙内への前記充填流体源からの充填流体の流れを制御するように構成される1つ以上のバルブおよび/またはポンプと、
(d)1つ以上の前記ポンプおよび/またはバルブを制御し、請求項208および以下の請求項のいずれかの方法を実行するようにプログラムされるプロセッサと、
を含む、システム。
【請求項262】
液滴操作間隙を形成するように分離された2つの基板を備える液滴アクチュエータであって、前記液滴操作間隙は、
(a)液体経路に流動的に接続された少なくとも2つの温度制御リザーバーを規定する1つ以上の障壁と、
(b)1つまたは両方の基板と結合され、前記温度制御リザーバーの間に液滴を輸送するように構成される電極と、
を備える熱サイクル経路を備える、液滴アクチュエータ。
【請求項263】
2つ以上の前記熱サイクル経路を備える、請求項262に記載の液滴アクチュエータ。
【請求項264】
液滴アクチュエータ上の液滴間の二次汚染を防止する方法であって、前記方法は、
(a)(i)液滴操作間隙を形成する1つ以上の基板と、(ii)複数の実質的に平行な液滴操作経路を規定する1つ以上に基板に結合された電極と、(iii)前記液滴操作間隙を実質的に充填する流動性の充填流体と、を備える液滴アクチュエータを提供する工程と、
(b)複数の実質的に平行な液滴輸送経路の第1のサブセット上で複数のアッセイ液滴を輸送する工程と、
(c)複数の実質的に平行な液滴輸送経路の第2のサブセット上で1つ以上のバッファー液滴を輸送する工程であって、前記第2のサブセットの各々の液滴輸送経路は、前記第1のサブセットの2つの液滴輸送経路の間にある、工程と、
を含む、方法。
【請求項265】
アッセイ液滴を輸送する工程と、液滴を洗浄する工程は、同時に行われる、請求項264に記載の方法。
【請求項266】
2つ以上の洗浄液滴が、前記第2のサブセットの各々の液滴輸送経路に提供される、請求項264に記載の方法。
【請求項267】
前記洗浄液滴は、液滴スラグの形状で提供される、請求項264に記載の方法。
【請求項268】
前記第1のサブセットの液滴輸送経路に1つ以上のバッファー液滴を輸送する工程をさらに含む、請求項264に記載の方法。
【請求項269】
(a)前記第1のサブセットの液滴輸送経路に1つ以上のバッファー液滴を輸送する工程と、
(b)前記第1の洗浄液滴に対して前記アッセイ液滴の反対側の前記第1のサブセットの液滴輸送経路に1つ以上のバッファー液滴を輸送する工程と、
を含む、請求項264に記載の方法。
【請求項270】
前記アッセイ液滴は、核酸増幅液滴を含む、請求項264および以下の請求項のいずれかに記載の方法。
【請求項271】
前記方法は、増幅を行うために2つの熱領域の間に前記アッセイ液滴を輸送する工程をさらに含む、請求項270に記載の方法。
【請求項272】
(a)液滴アクチュエータ間隙を設けるように配置される1つ以上の基板と、
(b)複数の実質的に平行な液滴輸送経路を規定する前記1つ以上の基板に結合された電極と、
(c)前記液滴操作間隙を実質的に充填する流動性の充填流体と、
(d)前記液滴輸送経路の各々の間にあり、1つの液滴操作経路に結合された充填流体が、他の液滴操作経路に結合された充填流体と接触することを防ぐ、障壁と、
を備える、液滴アクチュエータ。
【請求項273】
2つ以上の前記液滴輸送経路上にアッセイ液滴をさらに含む、請求項272に記載の液滴アクチュエータ。
【請求項274】
前記アッセイ液滴は、核酸を増幅するための試薬およびサンプルを含む、請求項273に記載の液滴アクチュエータ。
【請求項275】
液滴アクチュエータ上の液滴間の二次汚染を減少させる方法であって、前記方法は、
(a)内部液滴操作間隙と、前記液滴操作間隙内にオイルベースの充填流体とを含む液滴アクチュエータを提供する工程と、
(b)前記液滴操作間隙内に水性液滴を提供する工程であって、前記液滴は、(i)前記オイルベースの充填流体によって少なくとも部分的に囲まれ、(ii)界面活性剤−酵素複合体を含み、前記複合体は、潜在的に汚染物質を分解するように選択された酵素に結合された界面活性剤を含む、工程と、
を含む、方法。
【請求項276】
前記酵素は、ヌクレアーゼを含む、請求項275に記載の方法。
【請求項277】
前記酵素は、エンドヌクレアーゼを含む、請求項275に記載の方法。
【請求項278】
前記酵素は、エキソヌクレアーゼを含む、請求項275に記載の方法。
【請求項279】
前記酵素は、プロテイナーゼを含む、請求項275に記載の方法。
【請求項280】
前記界面活性剤は、PAG−アルキル界面活性剤を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項281】
前記界面活性剤−酵素複合体は、酵素−PAG−アルキル複合体を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項282】
前記界面活性剤は、前記酵素のアミノ部分に結合される、請求項275および以下の請求項のいずれかに記載の方法。
【請求項283】
前記界面活性剤−酵素複合体は、前記液滴中で実質的に不活性であるのに十分に低い量、かつ前記液滴から形成される微小液滴中で活性化するのに十分に高い量で前記液滴に存在する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項284】
前記微小液滴は、約10μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項285】
前記微小液滴は、約1μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項286】
前記微小液滴は、約0.01μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項287】
前記微小液滴は、約0.001μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項288】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約1未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項289】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約0.1未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項290】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約0.01未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項291】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約0.001未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項292】
前記潜在的な汚染物質は、タンパク質を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項293】
前記潜在的な汚染物質は、核酸を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項294】
前記潜在的な汚染物質は、試薬を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項295】
前記界面活性剤−酵素複合体の実質的に全ては、前記液滴の表面に閉じ込められる、請求項275および以下の請求項のいずれかに記載の方法。
【請求項296】
前記充填流体は、シリコンオイルを含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項297】
前記液滴は、前記充填流体によって実質的に囲まれる、請求項275および以下の請求項のいずれかに記載の方法。
【請求項298】
前記液滴は、前記充填流体によって完全に囲まれる、請求項275および以下の請求項のいずれかに記載の方法。
【請求項299】
(a)標的核酸を含み、必要に応じて増幅試薬を含む、サンプル液滴を提供する工程と、
(b)前記サンプル液滴から小液滴を分配する工程と、増幅試薬が前記サンプル液滴に存在しない場合、各々の小液滴と増幅試薬とを混合して、増幅準備液滴を生じる工程と、
(c)各々の小液滴を、前記標的核酸を増幅するために選択される熱サイクルプロトコルに供する工程と、
(d)各々の小液滴中の増幅産物を検出する工程と、
(e)前記増幅産物が形成されるサンプル部分を含む小液滴の数を決定する工程と、
を含む、方法。
【請求項300】
前記小液滴の少なくとも1つは、少なくとも1つの標的核酸分子を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項301】
前記増幅試薬は、増幅された標的分子にハイブリダイズし、ハイブリダイゼーション時に変化するか、またはハイブリダイゼーションの結果として変化する蛍光特性を有する少なくとも1つのプローブを含み、前記増幅産物が形成されるサンプル部分を含む前記小液滴の数を決定する工程は、前記少なくとも1つのプローブのハイブリダイゼーションに起因する前記蛍光の変化を検出する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項302】
前記増幅産物が形成されるサンプル部分を含む前記小液滴の数を決定する工程は、全ての小液滴を一緒に画像化する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項303】
前記増幅産物が形成されるサンプル部分を含む前記小液滴の数を決定する工程は、検出ウィンドウを通して1つずつまたはサブグループで液滴を輸送する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項304】
前記小液滴は、約1μL未満の体積を有する、請求項299および以下の請求項のいずれかに記載の方法。
【請求項305】
前記小液滴は、約1μLより大きい範囲から約1000μLの体積を有する、請求項299および以下の請求項(請求項304を除く)に記載の方法。
【請求項306】
前記小液滴は、約100μLより大きい範囲から約500μLの体積を有する、請求項299および以下の請求項(請求項304を除く)に記載の方法。
【請求項307】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、液滴アクチュエータの液滴操作間隙内で実施される、請求項299および以下の請求項のいずれかに記載の方法。
【請求項308】
前記小液滴は、前記液滴操作間隙内の2つの基板の間で平面またはディスク形状の構造に圧縮される、請求項307に記載の方法。
【請求項309】
前記液滴操作間隙は、約50μm〜約1000μmの範囲の高さを有する、請求項307に記載の方法。
【請求項310】
前記液滴操作間隙は、約100μmより大きい範囲から約500μmの範囲の高さを有する、請求項307に記載の方法。
【請求項311】
熱サイクルが、1つの熱領域から別の熱領域へ液滴を輸送することによって行われる、請求項299および以下の請求項のいずれかに記載の方法。
【請求項312】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、サンプルチャンバを欠く液滴アクチュエータの液滴操作間隙内で実施される、請求項299および以下の請求項のいずれかに記載の方法。
【請求項313】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、流路チャネルを欠く液滴アクチュエータの液滴操作間隙内で実施される、請求項299および以下の請求項のいずれかに記載の方法。
【請求項314】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、液滴アクチュエータの液滴操作間隙内で実施され、前記サンプル液滴から小液滴を分配する工程は、流路チャネルからサンプルを配置する配置流体を用いずに行われる、請求項299および以下の請求項のいずれかに記載の方法。
【請求項315】
標的核酸を含む前記サンプル液滴を提供する工程は、増幅試薬も含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項316】
増幅試薬は、前記サンプル液滴に存在せず、前記方法は、各々の小液滴と増幅試薬とを混合して、増幅準備液滴を生じる工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項317】
各々の小液滴中の増幅産物を検出する工程は、前記液滴を検出に供する前に、前記増幅液滴と、1つ以上の検出試薬を含む液滴とを混合する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項1】
サンプル中の標的核酸を検出する方法であって、前記方法は、
(a)核酸増幅反応液滴のセットを提供する工程であって、各々の液滴は前記サンプルの一部を含む、工程と、
(b)前記標的核酸を増幅するための条件下で前記増幅反応液滴の2つ以上のサブセットを処理して、増幅核酸を含む増幅された液滴の対応するサブセットを得る工程であって、前記増幅反応液滴の各々のサブセットは、
(i)前記増幅反応液滴の1つ以上を含み、
(ii)前記標的核酸を増幅するための異なる条件下で処理される、
工程と、
(c)検出のための前記増幅された液滴を調製する工程と、
(d)前記増幅された液滴からシグナルを検出する工程と、
(e)前記シグナルに基づいて、前記増幅された液滴および/または前記サンプルに存在する前記増幅された核酸の量を決定する工程と、
を含む、方法。
【請求項2】
核酸増幅反応液滴のセットを提供する工程は、サンプル液滴から前記核酸増幅液滴のセットを分配する工程を含む、請求項1に記載の方法。
【請求項3】
前記サンプル液滴は、液滴アクチュエータの液滴操作間隙に提供され、前記分配する工程は電極により媒介される、請求項2に記載の方法。
【請求項4】
(a)前記サンプル液滴は、液滴アクチュエータのリザーバーに提供され、
(b)前記液滴アクチュエータは、前記リザーバーから液滴操作間隙内への液体経路を備え、
(c)前記核酸増幅液滴のセットを分配する工程であって、
(i)前記サンプル液滴を、前記液体経路を通して前記液滴操作間隙内に流動させる工程と、
(ii)前記液滴操作間隙内の前記増幅反応液滴を分配するために電極を用いる工程と、
を含む、請求項2に記載の方法。
【請求項5】
核酸増幅反応液滴のセットを提供する工程は、
(a)サンプル液滴を提供する工程と、
(b)前記サンプル液滴を、複数のサンプル小液滴に分割する工程と、
(c)前記サンプル小液滴の各々と、増幅試薬を含む1つ以上の液滴とを混合して、前記増幅反応液滴を生じる、工程と、
を含む、請求項1に記載の方法。
【請求項6】
請求項5に記載の工程(b)および/または(c)は、電極により媒介される液滴操作を用いて液滴アクチュエータの液滴操作間隙内で実施される、請求項5に記載の方法。
【請求項7】
前記サンプル液滴、前記複数の小液滴、および前記増幅試薬を含む1つ以上の液滴、および前記増幅反応液滴は、
(a)液滴操作間隙内に配置され、
(b)流動性の充填流体によって少なくとも部分的に囲まれる、
請求項5に記載の方法。
【請求項8】
核酸増幅反応液滴のセットを提供する工程は、
(a)サンプル液滴を提供する工程と、
(b)前記サンプル液滴と、増幅試薬を含む1つ以上の液滴とを混合して、増幅準備液滴を生じる工程と、
(c)前記増幅準備液滴を分割して、前記増幅反応液滴を生じる工程と、
を含む、請求項1に記載の方法。
【請求項9】
前記サンプル液滴、前記増幅試薬を含む1つ以上の液滴、親増幅反応液滴、および前記増幅反応液滴は、
(a)液滴アクチュエータの液滴操作間隙内に配置され、
(b)流動性の充填流体によって少なくとも部分的に囲まれる、
請求項8に記載の方法。
【請求項10】
請求項8に記載の工程(b)および/または工程(c)は、電極により媒介される液滴操作を用いて実施される、請求項8に記載の方法。
【請求項11】
標的核酸が前記サンプルに存在する場合、請求項8に記載の工程(c)で生成された前記増幅反応液滴の各々が、前記標的核酸を含むことを確実にするために、前記増幅準備液滴中で十分な増幅核酸を生じるように選択された条件下で、前記増幅準備液滴を処理する工程をさらに含む、請求項8に記載の方法。
【請求項12】
前記増幅準備液滴を処理する工程は、前記増幅準備液滴を1〜20サイクルの間、熱サイクルする工程を含む、請求項11に記載の方法。
【請求項13】
前記増幅準備液滴を処理する工程は、前記増幅準備液滴を1〜10サイクルの間、熱サイクルする工程を含む、請求項11に記載の方法。
【請求項14】
前記増幅準備液滴を処理する工程は、前記増幅準備液滴を1〜5サイクルの間、熱サイクルする工程を含む、請求項11に記載の方法。
【請求項15】
請求項1に記載の工程(b)は、電極により媒介される液滴操作を用いて液滴アクチュエータの液滴操作間隙内で実施される、請求項1〜14のいずれかに記載の方法。
【請求項16】
請求項1に記載の工程(b)は、液滴アクチュエータの液滴操作間隙内の複数の電極経路に沿って前記液滴を輸送することによって、前記増幅反応液滴を2以上の熱領域の間に循環させる工程を含む、請求項1〜15のいずれかに記載の方法。
【請求項17】
請求項1に記載の工程(b)は、液滴アクチュエータの液滴操作間隙内の共通の電極経路に沿って各々のサブセット内の液滴を輸送することによって、2つ以上の前記増幅反応液滴のサブセットを2つ以上の熱領域の間に循環させる工程を含む、請求項1〜16のいずれかに記載の方法。
【請求項18】
前記1つ以上の電極経路は、前記2つ以上の熱領域の間の1つ以上のループ経路を規定する、請求項17に記載の方法。
【請求項19】
請求項18に記載の方法であって、
(a)請求項1に記載の工程(b)は、電極経路のループの周りに複数の増幅反応液滴を輸送する工程を含み、
(b)前記方法は、所定数のサイクルが完了した場合、各々の増幅液滴を前記電極経路のループから除去する工程をさらに含む、方法。
【請求項20】
各々の増幅液滴を前記電極経路のループから除去する工程は、前記増幅反応液滴を前記液滴操作間隙の別の領域に輸送するために、電極により媒介される液滴操作を使用する工程を含む、請求項19に記載の方法。
【請求項21】
前記液滴操作間隙の領域は、検出が未実施の前記増幅液滴を保存するように選択された温度を有する温度制御領域を含む、請求項20に記載の方法。
【請求項22】
各々の増幅液滴を前記電極経路のループから除去する工程は、各々の増幅液滴を前記液滴アクチュエータの前記液滴操作間隙から除去する工程を含む、請求項19に記載の方法。
【請求項23】
前記電極経路は、2つ以上の熱領域の間で曲がっている、請求項17に記載の方法。
【請求項24】
(a)前記電極経路上の1つの電極から前記電極経路上の隣接する電極までの輸送時間は、各々の対の隣接する電極に関して実質的に均一であり、
(b)熱領域における滞留時間は、前記熱領域に存在する前記電極経路の各々の曲がり角における電極の数によって規定される、請求項17に記載の方法。
【請求項25】
請求項1に記載の工程(b)は、並行して熱領域の間に前記増幅反応液滴の2つ以上のサブセットを輸送する工程を含む、請求項1〜24のいずれかに記載の方法。
【請求項26】
請求項1に記載の工程(b)は、前記増幅反応液滴の2つ以上のサブセットを熱領域に連続して輸送する工程を含む、請求項1〜25のいずれかに記載の方法。
【請求項27】
請求項1に記載の工程(b)は、
(a)前記増幅反応液滴の第2のサブセットを第2の熱領域に輸送している間、前記増幅反応液滴の第1のサブセットを、第1の熱領域に輸送する工程と、
(b)前記増幅反応液滴の第2のサブセットを前記第1の熱領域に輸送している間、前記増幅反応液滴の第1のサブセットを前記第2の熱領域に輸送する工程と、
を含む、請求項1〜26のいずれかに記載の方法。
【請求項28】
連続して熱サイクルされた前記増幅反応液滴のサブセットは、共通の電極経路に沿って熱サイクルされる、請求項26に記載の方法。
【請求項29】
請求項1に記載の工程(b)は、並行して2つ以上のサブセットを増幅させる工程をさらに含む、請求項26に記載の方法。
【請求項30】
請求項1に記載の工程(b)は、全ての増幅反応液滴に関して、熱的に同時に行われる熱サイクルを含む、請求項1〜29のいずれかに記載の方法。
【請求項31】
請求項1に記載の工程(b)は、全ての増幅反応液滴に関して、熱的に同時に行われない熱サイクルを含む、請求項1〜30のいずれかに記載の方法。
【請求項32】
請求項1に記載の工程(b)は、液滴アクチュエータの熱サイクル領域を加熱および冷却することによって実施される、請求項1〜31のいずれかに記載の方法。
【請求項33】
請求項1に記載の工程(b)は、1回以上の熱サイクルのサイクル数にて熱領域における増幅反応液滴の滞留時間を変化させる工程を含む、請求項1〜32のいずれかに記載の方法。
【請求項34】
請求項1に記載の工程(d)を開始する前に、増幅反応液滴の全てのサブセットに関して、請求項1に記載の工程(b)を完了する工程を含む、請求項1〜33のいずれかに記載の方法。
【請求項35】
前記増幅反応液滴の第2のサブセットに関して請求項1に記載の工程(b)を完了する前に、増幅液滴の第1のサブセットに関して請求項1に記載の工程(d)を完了する工程を含む、請求項1〜34のいずれかに記載の方法。
【請求項36】
請求項1に記載の工程(c)は、2つ以上の前記増幅液滴のセットに関して、請求項1に記載の工程(d)を開始する前に、2つ以上の前記増幅液滴のセットを、前記液滴アクチュエータの熱サイクル領域から離れた位置に輸送する工程を含む、請求項1〜35のいずれかに記載の方法。
【請求項37】
請求項1に記載の工程(c)は、各々の前記液滴に関して、請求項1に記載の工程(d)を開始する前に、各々の増幅液滴を、熱サイクル領域から離れた位置に輸送する工程を含む、請求項1〜36のいずれかに記載の方法。
【請求項38】
請求項1に記載の工程(c)は、各々の増幅液滴を、請求項1に記載の工程(d)を実施するのに適切な温度を有する熱領域に輸送する工程を含む、請求項1〜37のいずれかに記載の方法。
【請求項39】
請求項1に記載の工程(c)は、配置された増幅液滴の各々の前記サブセットに関して、請求項1に記載の工程(d)を開始する前に、熱サイクル領域から離れた位置に前記増幅液滴の少なくとも1つのサブセットを配置する工程を含む、請求項1〜38のいずれかに記載の方法。
【請求項40】
請求項1に記載の工程(c)は、未結合の検出試薬を前記増幅核酸から分離する工程を含む、請求項1〜39のいずれかに記載の方法。
【請求項41】
請求項1に記載の工程(c)は、前記増幅液滴中の増幅を実質的に停止させる工程を含む、請求項1〜40のいずれかに記載の方法。
【請求項42】
請求項1に記載の工程(c)は、前記増幅液滴を、1つの液滴アクチュエータから別の液滴アクチュエータに輸送する工程を含む、請求項1〜41のいずれかに記載の方法。
【請求項43】
前記増幅液滴中の増幅を実質的に停止させる工程は、前記増幅反応を実質的に停止させるように液滴温度を調節する工程を含む、請求項41に記載の方法。
【請求項44】
前記増幅液滴中の増幅を実質的に停止させる工程は、前記増幅反応を実質的に停止させるように試薬を前記増幅液滴に添加する工程を含む、請求項43に記載の方法。
【請求項45】
試薬を前記増幅液滴に添加する工程は、前記増幅液滴と試薬液滴とを混合する工程を含み、前記試薬液滴は、前記増幅反応を実質的に停止させるように選択された試薬を含む、請求項44に記載の方法。
【請求項46】
前記増幅反応を実質的に停止させるように選択された試薬は、ポリメラーゼ活性を妨げること、ポリメラーゼ補助因子活性を妨げること、核酸に結合すること、および/または鉄イオンを放出することによって、前記増幅反応を実質的に停止させる試薬を含む、請求項45に記載の方法。
【請求項47】
請求項1に記載の工程(c)および請求項1に記載の工程(d)は、前記サブセットの熱サイクルの完了後に、前記増幅液滴のサブセットの各々について実施される、請求項61に記載の方法。
【請求項48】
(a)前記増幅反応液滴は検出試薬を含まず、
(b)請求項1に記載の工程(c)は、検出試薬を前記増幅液滴に添加する工程を含む、請求項1〜47のいずれかに記載の方法。
【請求項49】
検出試薬を前記増幅液滴に添加する工程は、各々の増幅液滴と検出試薬を含む液滴とを混合する工程を含む、請求項48に記載の方法。
【請求項50】
(a)請求項1に記載の工程(c)は、各々の前記増幅液滴と1つ以上の検出試薬を含む液滴とを混合する工程を含み、
(b)請求項1に記載の工程(d)は、前記検出試薬によって媒介されるシグナルに基づいて増幅を検出する工程を含む、請求項1〜49のいずれかに記載の方法。
【請求項51】
請求項1に記載の工程(d)は、前記液滴の検出ウィンドウへの輸送後に、各々の増幅液滴からシグナルを検出する工程を含む、請求項1〜50のいずれかに記載の方法。
【請求項52】
請求項1に記載の工程(c)は、増幅液滴の1つ以上のサブセットのセットを、検出のために検出ウィンドウに輸送する工程を含む、請求項1〜51のいずれかに記載の方法。
【請求項53】
(a)請求項1に記載の工程(b)は、液滴アクチュエータの液滴操作間隙内で達成され、
(b)請求項1に記載の工程(c)は、前記増幅液滴の1つ以上を、検出のために前記液滴操作間隙の外へ輸送する工程を含む、請求項1〜52のいずれかに記載の方法。
【請求項54】
請求項1に記載の工程(d)は、前記液滴アクチュエータの前記液滴操作間隙の外部のリザーバー内で実施される、請求項53に記載の方法。
【請求項55】
請求項1に記載の工程(c)は、増幅液滴のサブセットを検出ウィンドウに輸送し、少ないサイクル数のサブセットで開始し、多いサイクル数のサブセットまで進行させる工程を含む、請求項1〜54のいずれかに記載の方法。
【請求項56】
請求項1に記載の工程(d)は、増幅液滴のアレイを走査する工程を含む、請求項1〜55のいずれかに記載の方法。
【請求項57】
請求項1に記載の工程(d)は、増幅液滴のアレイを画像化する工程を含む、請求項1〜56のいずれかに記載の方法。
【請求項58】
(a)前記増幅反応液滴は、並行して請求項1に記載の工程(b)に入り、
(b)前記増幅液滴は、連続して請求項1に記載の工程(c)に入り、
(c)前記増幅液滴は、連続して請求項1に記載の工程(d)に入る、
請求項1〜57のいずれかに記載の方法。
【請求項59】
(a)前記増幅反応液滴は、並行して請求項1に記載の工程(b)に入り、
(b)前記増幅液滴は、連続して請求項1に記載の工程(c)に入り、
(c)前記増幅液滴は、並行して請求項1に記載の工程(d)に入る、
請求項1〜58のいずれかに記載の方法。
【請求項60】
(a)前記増幅反応液滴は、連続して請求項1に記載の工程(b)に入り、
(b)前記増幅液滴は、並行して請求項1に記載の工程(c)に入る、
請求項1〜59のいずれかに記載の方法。
【請求項61】
請求項1に記載の工程(e)は、前記増幅液滴のサブセットの各々についての熱サイクルエンドポイントにおけるシグナルの増加または減少を決定することによって、前記増幅液滴に存在する前記増幅核酸の量を決定する工程を含む、請求項1〜60のいずれかに記載の方法。
【請求項62】
請求項1に記載の工程(e)は、前記サンプル液滴に存在する前記標的核酸の量を決定するために、前記増幅液滴に存在する前記増幅核酸の量を使用する工程をさらに含む、請求項1〜61のいずれかに記載の方法。
【請求項63】
請求項1に記載の工程(e)は、前記サンプル液滴に存在する前記標的核酸の量を決定するために、異なる数の熱サイクル後に前記増幅液滴に存在する前記増幅核酸の量を使用する工程をさらに含む、請求項1〜62のいずれかに記載の方法。
【請求項64】
前記標的核酸を増幅させるための異なる条件は、前記増幅反応液滴の各々のサブセットについての異なる数の熱サイクルを含む、請求項1〜63のいずれかに記載の方法。
【請求項65】
前記増幅反応液滴は、検出試薬を含む、請求項1〜64のいずれかに記載の方法。
【請求項66】
前記増幅反応液滴は、有意な量の検出試薬を含まない、請求項1〜65のいずれかに記載の方法。
【請求項67】
増幅試薬を含む1つ以上の前記液滴は、検出試薬をさらに含む、請求項1〜66のいずれかに記載の方法。
【請求項68】
増幅試薬を含む1つ以上の前記液滴は、有意な量の検出試薬を含まない、請求項1〜67のいずれかに記載の方法。
【請求項69】
前記検出試薬は、核酸結合剤を含む、請求項1〜68のいずれかに記載の方法。
【請求項70】
前記核酸結合剤は、核酸増幅の割合を有意に阻害する、請求項69に記載の方法。
【請求項71】
前記核酸結合剤は、挿入剤を含む、請求項69および以下の請求項に記載の方法。
【請求項72】
前記挿入剤は、蛍光色素を含む、請求項71に記載の方法。
【請求項73】
前記標的核酸は、遺伝性疾患または感染病の指標である、請求項1〜72のいずれかに記載の方法。
【請求項74】
前記標的核酸は、生物学的集団由来の個体の個々またはサブグループの同定の指標である、請求項1〜73のいずれかに記載の方法。
【請求項75】
(a)前記核酸増幅反応液滴の1つ以上を、請求項1に記載の工程(b)の前に最初の検出工程に供し、
(b)請求項1に記載の工程(e)は、前記最初の検出工程において検出されたシグナルと、請求項1に記載の工程(d)において検出されたシグナルとの間の比較を含む、請求項1〜74のいずれかに記載の方法。
【請求項76】
開始サンプルに存在する前記標的核酸を定量化するために所定の範囲の統計的確実性内の十分なデータが収集された場合、前記方法を停止させる工程をさらに含む、請求項1〜75のいずれかに記載の方法。
【請求項77】
(a)前記増幅液滴および/または前記サンプルに存在する前記増幅核酸の量を決定するための十分なデータを提供すると予想される第1のセットのサイクル数を選択する工程と、
(b)前記選択されたサイクル数の各々に関して、1つ以上の増幅反応液滴のサブセットを、請求項1に記載の工程(b)、請求項1に記載の工程(c)、請求項1に記載の工程(d)および請求項1に記載の工程(e)に供する工程と、
(c)前記サンプルに存在する前記標的核酸を同定または定量するために所定の範囲の統計的確実性内の十分なデータが収集されたか否かを決定する工程と、
(d)(i)前記開始サンプルに存在する前記標的核酸を同定または定量化するために所定の範囲の統計的確実性内の十分なデータが収集されるまで、または(ii)前記標的核酸が前記サンプルに存在しないことを決定するために所定の範囲の統計的確実性内の十分なデータが収集されるまで、新しいセットのサイクル数で工程(a)、(b)および(c)を繰り返す工程と、
をさらに含む、請求項1〜76のいずれかに記載の方法。
【請求項78】
請求項77に記載の工程(c)は、前記サンプルに存在する前記標的核酸を同定するために所定の範囲の統計的確実性内の十分なデータが収集されたか否かを決定する工程を含む、請求項77に記載の方法。
【請求項79】
請求項77に記載の工程(c)は、前記サンプルに存在する前記標的核酸を定量化するために所定の範囲の統計的確実性内の十分なデータが収集されたか否かを決定する工程を含む、請求項77に記載の方法。
【請求項80】
サンプル中の標的核酸の増加をモニターする方法であって、前記方法は、
(a)核酸増幅反応液滴のセットを提供する工程であって、各々の液滴は前記サンプルの一部を含む工程と、
(b)前記標的核酸を増幅するための条件下で、前記増幅反応液滴の2つ以上のサブセットを熱サイクルして、増幅二本鎖核酸を含む増幅液滴を生じる工程であって、前記増幅反応液滴の各々のサブセットは、
(i)前記増幅反応液滴の1つ以上を含み、
(ii)異なる数のサイクル数について熱サイクルされ、
(iii)前記サブセットについての所定数のサイクルの完了前に検出に供されない、工程と、
(c)前記増幅液滴の各々と、増幅核酸を検出するための検出試薬とを混合して、検出準備液滴を生じる工程を含む、検出準備プロコルを実施する工程と、
(d)前記検出準備液滴からシグナルを検出する工程と、
(e)前記シグナルに基づいて、前記増幅液滴および/または前記サンプルに存在する前記増幅核酸の量を決定する工程と、
を含む、方法。
【請求項81】
(a)液滴操作間隙を形成する1つ以上の基板と、
(b)前記1つ以上の基板と結合され、前記液滴操作間隙内で液滴操作を媒介するように配置される電極と、
(c)増幅試薬を含み、検出試薬を含まない1つ以上の液滴を含む第1のリザーバーと、
(d)1つ以上の検出試薬を含む第2のリザーバーと、
(e)前記液滴操作間隙を備える前記第1のリザーバーおよび前記第2のリザーバーと流動的に接続される1つ以上の流体経路と、
(f)サンプルを前記液滴操作間隙内に充填するための手段と、
を備える、予め組み込まれている液滴アクチュエータカートリッジ。
【請求項82】
(a)請求項81に記載の予め組み込まれている液滴アクチュエータカートリッジと、
(b)前記カートリッジを用いて増幅プロトコルを実行するためのソフトウェアと、
を備えるキット。
【請求項83】
検体を検出する方法であって、前記方法は、
(a)(i)検体の存在および/または量の指標であるシグナル生成物質と、(ii)前記シグナル生成物質によって生成されるシグナルを妨げることができる1つ以上の磁性反応ビーズと、を含む液滴を検出ウィンドウ内に提供する工程と、
(b)(i)前記磁性反応ビーズを前記検出ウィンドウから磁性的に除去するため、ならびに/あるいは(ii)前記検出ウィンドウに前記液滴を輸送および/または保持している間、前記磁性反応ビーズが前記検出ウィンドウに侵入することを磁性的に抑制するために、磁場を用いる工程と、
(c)前記シグナル生成物質によって生成されるシグナルを検出する工程と、
を含む、方法。
【請求項84】
(a)前記液滴は、液滴アクチュエータの液滴操作間隙に提供され、
(b)前記検出ウィンドウは、前記液滴アクチュエータの基板内に開口部またはウィンドウを含む、請求項83に記載の方法。
【請求項85】
(a)請求項83に記載の工程(b)は、前記検出ウィンドウに近接する固定磁場を提供する工程を含み、
(b)前記液滴を前記検出ウィンドウに輸送する工程は、前記ビーズが、前記検出ウィンドウから離れた位置に引き付けられ、および/または前記検出ウィンドウに侵入することを抑制する前記固定磁石に十分に近接する位置に前記磁性反応ビーズを送達する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項86】
前記磁場は、固定永久磁石を含む磁場源によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項87】
前記磁場は、移動可能な永久磁石を含む磁場源によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項88】
前記磁場は、電磁石を含む磁場源によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項89】
前記磁場は、前記液滴の端部において前記磁性反応ビーズを凝集する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項90】
前記磁場は、前記検出ウィンドウの外部にある前記液滴の領域内で前記磁性反応ビーズを凝集する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項91】
前記磁場は、前記液滴から離れて前記磁性反応ビーズを分解する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項92】
前記液滴が所定の位置に保持されるか、または電極により媒介される力によって移動される間、前記磁場は、前記液滴から離れて前記磁性反応ビーズを分解する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項93】
前記液滴が少なくとも部分的に前記検出ウィンドウにある間、前記磁場は、前記磁性反応ビーズを前記液滴の端部に引き付ける方法で前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項94】
前記液滴が前記磁石の上を通過する場合、前記磁場は、前記液滴の外側に前記磁性反応ビーズを引き付ける、請求項83に記載の方法。
【請求項95】
前記液滴が前記磁石の近接に近づく場合、前記磁場は、前記液滴の外側に前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項96】
前記液滴が前記検出ウィンドウに近づく場合、前記磁場は、前記液滴の外部へ前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項97】
前記シグナルは、蛍光色素によって生成される、請求項83および以下の請求項のいずれかに記載の方法。
【請求項98】
前記液滴が前記検出ウィンドウに輸送される場合、前記ビーズの実質的に全てが、前記検出ウィンドウに侵入または再侵入するのを抑制する方法で、前記磁場は、前記磁性反応ビーズを引き付ける、請求項83および以下の請求項のいずれかに記載の方法。
【請求項99】
前記検出ウィンドウは、液滴アクチュエータ装置の基板に設けられる、請求項83および以下の請求項のいずれかに記載の方法。
【請求項100】
前記液滴アクチュエータは、液滴操作基板に結合された電極の複数の経路を備え、各々の経路は、
(a)検出ウィンドウ、ならびに
(b)(i)前記磁性反応ビーズを前記対応する検出ウィンドウから磁性的に除去するように、および/または(ii)前記検出ウィンドウ内に前記液滴を輸送および/または保持している間、前記磁性反応ビーズが前記対応する検出ウィンドウに侵入することを磁性的に抑制するように、配置される前記経路に近接する磁場、
に結合される、請求項99に記載の方法。
【請求項101】
前記液滴は、1つ以上の検体の存在、非存在および/または量のシグナルの指標を放出する、請求項83および以下の請求項のいずれかに記載の方法。
【請求項102】
前記1つ以上の検体は、増幅核酸を含む、請求項101に記載の方法。
【請求項103】
(a)前記検出ウィンドウは、液滴アクチュエータの基板内に位置し、
(b)前記液滴アクチュエータは、熱サイクル反応を実施するための電極の経路に沿って温度制御領域を備え、
(c)前記方法は、(i)増幅準備液滴を熱サイクルして、増幅液滴を生じる工程と、(ii)前記増幅液滴を前記検出ウィンドウに輸送する工程とを含む、
請求項83および以下の請求項のいずれかに記載の方法。
【請求項104】
1以上の熱サイクルの後、前記電極の経路に沿って磁性反応ビーズを含む液滴を、少なくとも部分的に前記検出ウィンドウに輸送する工程を含む、請求項103に記載の方法。
【請求項105】
液滴を熱サイクルする方法であって、前記方法は、
(a)流動性の充填流体によって少なくとも部分的に囲まれた液滴を提供する工程であって、前記液滴は、(i)標的核酸を潜在的に含み、(ii)前記標的核酸の存在下で増幅を生じるのに十分な試薬を含み、熱サイクルプロトコルを実施している間、前記試薬は前記充填流体中で有意に分離しない蛍光色素分子を含む、工程と、
(b)前記標的核酸の存在下で増幅を誘導するために熱サイクルプロトコルに従って前記液滴の温度を調節する工程と、
を含む、方法。
【請求項106】
前記蛍光色素分子は、極性蛍光色素分子を含む、請求項105に記載の方法。
【請求項107】
前記蛍光色素分子は、細胞膜に実質的に不浸透性である、請求項105に記載の方法。
【請求項108】
前記蛍光色素分子は、細胞膜に完全に不浸透性である、請求項105に記載の方法。
【請求項109】
前記蛍光色素分子は、EVAGREEN(登録商標)蛍光色素分子を含む、請求項105に記載の方法。
【請求項110】
前記蛍光色素分子は、TO−PRO1蛍光色素分子を含む、請求項105に記載の方法。
【請求項111】
前記充填流体は、シリコーンオイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項112】
前記充填流体は、10〜20の炭素オイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項113】
前記充填流体は、15〜20の炭素オイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項114】
前記充填流体は、ヘキサデカンオイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項115】
前記充填流体は、脱ガスオイルから本質的に構成され、必要に応じて1つ以上の添加剤でドープされる、請求項105〜110のいずれかに記載の方法。
【請求項116】
液滴を提供する工程は、液滴アクチュエータの液滴操作間隙内に液滴を提供する工程を含む、請求項105および以下の請求項のいずれかに記載の方法。
【請求項117】
熱サイクルプロトコルに従って前記液滴の温度を調節する工程は、前記液滴アクチュエータの液滴操作間隙内の前記液滴を加熱および/または冷却する工程を含む、請求項116および以下の請求項のいずれかに記載の方法。
【請求項118】
熱サイクルプロトコルに従って前記液滴の温度を調節する工程は、電極により媒介される液滴操作を用いて前記液滴操作間隙内の熱領域の間に前記液滴を輸送する工程を含む、請求項116および以下の請求項のいずれかに記載の方法。
【請求項119】
検出アクチュエータでプロトコルを実施する方法であって、前記方法は、
(a)前記液滴アクチュエータの1つ以上の領域を、不動態化剤を含む液滴を有する前記領域内の1つ以上の電極で液滴操作を実施することによって処理する工程と、
(b)前記液滴アクチュエータの前記処理された領域の1つ以上を用いて前記プロトコルを実施する工程と、
を含む、方法。
【請求項120】
(a)前記プロトコルは、標的核酸の検体中での工程を含み、
(b)前記不動態化剤は、前記標的核酸でない核酸を含む、
請求項119に記載の方法。
【請求項121】
前記プロトコルは、核酸増幅プロトコルを含む、請求項120に記載の方法。
【請求項122】
前記プロトコルは、熱サイクルプロトコルを含む、請求項120に記載の方法。
【請求項123】
前記不動態化剤は、核酸を含む、請求項119に記載の方法。
【請求項124】
前記不動態化剤は、ポリビニルピロリドンを含む、請求項119に記載の方法。
【請求項125】
前記不動態化剤は、ポリエチレングリコールを含む、請求項119に記載の方法。
【請求項126】
前記不動態化剤は、界面活性剤を含む、請求項119に記載の方法。
【請求項127】
前記不動態化剤は、トゥイーンを含む、請求項119に記載の方法。
【請求項128】
前記不動態化剤は、アルブミンを含む、請求項119に記載の方法。
【請求項129】
前記不動態化剤は、血清アルブミンを含む、請求項119に記載の方法。
【請求項130】
前記不動態化剤は、ウシ血清アルブミンを含む、請求項119に記載の方法。
【請求項131】
前記不動態化剤は、色素を含む、請求項119に記載の方法。
【請求項132】
前記不動態化剤は、前記液滴アクチュエータの表面上で吸収するように選択される、請求項119に記載の方法。
【請求項133】
前記不動態化剤は、充填流体中で吸収するように選択される、請求項119に記載の方法。
【請求項134】
前記1つ以上の液滴は、十分な不動態化剤を、実質的に飽和した潜在的な不動態化部位へ送達する、請求項119に記載の方法。
【請求項135】
前記プロトコルは、前記不動態化剤を含む液滴を用いて実施される、請求項119に記載の方法。
【請求項136】
(a)前記プロトコルは、核酸増幅プロトコルを含み、
(b)前記核酸増幅プロトコルおよび処理する工程は、液滴を用いて同時に実施され、前記液滴は、(i)核酸増幅試薬、(ii)前記不動態化剤を含む、請求項135に記載の方法。
【請求項137】
(a)液滴操作基板と、
(b)液滴操作表面とカバーとの間に液滴操作間隙を形成するために、前記液滴操作表面に隣接し、前記液滴操作表面から離間しているカバーであって、前記液滴操作間隙は少なくとも250μmの高さを有する、カバーと、
(c)前記液滴操作基板および/またはカバーに結合され、熱サイクルプロトコルに従って熱領域の間に液滴を輸送するように配置された電極の経路と、
(d)前記液滴操作間隙内に1つ以上の熱領域を規定するように配置される温度制御素子と、
を備える、液滴アクチュエータ。
【請求項138】
前記液滴操作間隙は、実質的に球形形状の単一のサイズの液滴を与えるように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項139】
前記液滴操作間隙は、約250μm〜約500μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項140】
前記液滴操作間隙は、約275μm〜約450μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項141】
前記液滴操作間隙は、約300μm〜約400μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項142】
前記液滴操作間隙は、約320μm〜約375μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項143】
前記液滴操作間隙は、約320μm〜約350μmの範囲の高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項144】
前記電極はピッチを有し、前記液滴操作間隙は、約7:1〜約2.8:1の範囲のピッチ:高さの比を規定する高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項145】
前記電極はピッチを有し、前記液滴操作間隙は、約6:1〜約3:1の範囲のピッチ:高さの比を規定する高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項146】
前記電極はピッチを有し、前記液滴操作間隙は、約4.3:1〜約3.4:1の範囲のピッチ:高さの比を規定する高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項147】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて5%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項148】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項149】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項150】
前記液滴操作間隙は、1回の熱サイクルにつき0.1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項151】
前記液滴操作間隙は、1回の熱サイクルにつき0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項152】
前記液滴操作間隙は、1回の熱サイクルにつき0.001%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項153】
前記液滴操作間隙は、熱サイクルプロトコルの間、容積減少を実質的に排除するように選択される高さを有する、請求項137に記載の液滴アクチュエータ。
【請求項154】
熱サイクル反応を実施する方法であって、前記方法は、
(a)(i)液滴操作基板と、(ii)液滴操作表面とカバーとの間に液滴操作間隙を形成するために、前記液滴操作表面に隣接し、前記液滴操作表面から離間しているカバーであって、前記液滴操作間隙は少なくとも250μmの高さを有する、カバーと、(iii)前記液滴操作基板に結合され、および/または熱サイクルプロトコルに従った熱領域の間で液滴を輸送するために覆い、配置される電極の経路と、(iv)前記液滴操作間隙内に1つ以上の熱領域を規定するように配置される温度制御素子と、を備える液滴アクチュエータを提供する工程と、
(b)少なくとも部分的に前記検出ウィンドウに前記電極の経路に沿って磁性反応ビーズを含む液滴を輸送し、1つ以上の前記ビーズが前記検出ウィンドウに侵入することを抑制する方法で、磁石が、前記磁性反応ビーズを引き付ける工程と、
(c)前記液滴からシグナルを検出するためにセンサを使用する工程と、
を含む、方法。
【請求項155】
前記液滴操作間隙は、実質的に球形形状の単一のサイズの液滴を与えるように選択される高さを有する、請求項154に記載の方法。
【請求項156】
前記液滴操作間隙は、約250μm〜約500μmの範囲の高さを有する、請求項154に記載の方法。
【請求項157】
前記液滴操作間隙は、約275μm〜約450μmの範囲の高さを有する、請求項154に記載の方法。
【請求項158】
前記液滴操作間隙は、約300μm〜約400μmの範囲の高さを有する、請求項154に記載の方法。
【請求項159】
前記液滴操作間隙は、約320μm〜約375μmの範囲の高さを有する、請求項154に記載の方法。
【請求項160】
前記液滴操作間隙は、約320μm〜約350μmの範囲の高さを有する、請求項154に記載の方法。
【請求項161】
前記電極はピッチを有し、前記液滴操作間隙は、約7:1〜約2.8:1の範囲のピッチ:高さの比を規定する高さを有する、請求項154に記載の方法。
【請求項162】
前記電極はピッチを有し、前記液滴操作間隙は、約6:1〜約3:1の範囲のピッチ:高さの比を規定する高さを有する、請求項154に記載の方法。
【請求項163】
前記電極はピッチを有し、前記液滴操作間隙は、約4.3:1〜約3.4:1の範囲のピッチ:高さの比を規定する高さを有する、請求項154に記載の方法。
【請求項164】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて5%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項165】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項166】
前記液滴操作間隙は、完全な熱サイクルプロトコルについて0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項167】
前記液滴操作間隙は、1回の熱サイクルにつき0.1%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項168】
前記液滴操作間隙は、1回の熱サイクルにつき0.01%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項169】
前記液滴操作間隙は、1回の熱サイクルにつき0.001%未満までの熱サイクルプロトコルを受ける液滴からの容積減少を維持するように選択される高さを有する、請求項154に記載の方法。
【請求項170】
前記液滴操作間隙は、熱サイクルプロトコルの間、容積減少を実質的に排除するように選択される高さを有する、請求項154に記載の方法。
【請求項171】
解析するためのサンプルを調製する方法であって、前記方法は、
(a)(i)液滴操作基板と、(ii)前記基板の液滴操作表面上で液滴操作を実施するように配置される電極と、(iii)前記液滴操作表面とカバーとの間に液滴操作間隙を形成するために、前記液滴操作表面に隣接し、前記液滴操作表面から離間している、カバーと、(iv)上部の基板に結合され、1つ以上の標的検体および/または1つ以上の標的検体を含む物質に対する親和性を有するビーズを含むリザーバーと、(v)前記リザーバーから前記液滴操作間隙に延在する液体経路と、(vi)前記液滴操作基板に結合され、磁性反応ビーズを引き付けるのに十分な磁場を生成するように構成される磁場源と、を備える液滴アクチュエータを提供する工程と、
(b)前記リザーバー内にサンプルを供給する工程であって、前記サンプルは、前記標的物質のうちの1つ以上を潜在的に含む工程と、
(c)前記液体経路を通して前記液滴操作間隙内に前記磁性ビーズを含むサンプルを流動させる工程と、
(d)前記磁性反応ビーズを磁石で凝集させる工程と、
(e)前記磁場を除去するか、または前記磁場から前記ビーズを除去して、磁性ビーズを含む前記液滴操作間隙内にサンプル液滴を生じさせる工程と、
を含む、方法。
【請求項172】
前記液体経路は、実質的に真っ直ぐな液体経路である、請求項171に記載の方法。
【請求項173】
前記磁石は、前記リザーバーから前記液滴操作間隙内に1つ以上のビーズを引き付けるのに十分な磁場強度を有する、請求項172に記載の方法。
【請求項174】
前記液滴アクチュエータは、前記液滴操作基板に結合され、前記液体経路を通して前記液滴操作間隙に侵入する流体を受容するように配置されるリザーバー電極を備える、請求項171に記載の方法。
【請求項175】
前記磁石は、前記液体経路に対して前記リザーバー電極の反対側に配置される、請求項174に記載の方法。
【請求項176】
前記磁石は、電磁石を含む、請求項171に記載の方法。
【請求項177】
前記磁石は、永久磁石を含む、請求項171に記載の方法。
【請求項178】
前記永久磁石は、空間的に調節可能である、請求項177に記載の方法。
【請求項179】
前記永久磁石は、移動可能な磁気シールドに結合され、前記磁気シールドは、
(a)第1の位置における前記液滴操作間隙内の前記永久磁石の磁場を遮断または妨げることができ、
(b)第2の位置における前記液滴操作間隙内の前記永久磁石の磁場を遮断または妨げることができない、
請求項177に記載の方法。
【請求項180】
前記液滴アクチュエータは、前記リザーバー内のサンプル流体に音波エネルギーを与えるように配置される超音波処理器を備える、請求項171に記載の方法。
【請求項181】
前記リザーバー内の前記サンプルを超音波処理する工程をさらに含む、請求項180に記載の方法。
【請求項182】
前記電極の1つ以上に結合される第2の磁石をさらに備える、請求項171に記載の方法。
【請求項183】
(a)1つ以上の標的検体を含む物質は、細胞を含み、前記ビーズは前記細胞に対して親和性を有し、
(b)前記方法は、請求項171に記載の工程(e)によって生成される磁性ビーズを含む前記液滴操作間隙内の前記サンプル液滴と、細胞溶解試薬を含む溶解液滴とを混合する工程をさらに含む、
請求項171に記載の方法。
【請求項184】
請求項183に記載の(b)において生成された前記混合された液滴を超音波処理する工程を含む、請求項183に記載の方法。
【請求項185】
前記磁場を再印加して、前記磁性ビーズを固定化させる工程をさらに含む、請求項183に記載の方法。
【請求項186】
前記磁性ビーズから離れた位置に前記液滴を輸送する工程をさらに含む、請求項185に記載の方法。
【請求項187】
前記磁性ビーズから離れた位置に前記液滴の一部を輸送する工程をさらに含む、請求項185に記載の方法。
【請求項188】
離れた位置に輸送された前記液滴または前記液滴の一部と、前記1つ以上の標的検体に対する親和性を有するビーズを含む液滴とを混合する工程をさらに含む、請求項186または187に記載の方法。
【請求項189】
前記1つ以上の標的検体に対する親和性を有するビーズを洗浄するために洗浄プロトコルを実施して、実質的に精製された標的検体を含むビーズを含む液滴を生じる工程をさらに含む、請求項188に記載の方法。
【請求項190】
前記実質的に精製された標的検体を含むビーズを含む前記液滴を用いて解析プロトコルを実施する工程をさらに含む、請求項189に記載の方法。
【請求項191】
前記解析プロトコルを実施する工程は、前記液滴操作間隙内で達成される、請求項190に記載の方法。
【請求項192】
前記実質的に精製された標的検体を含むビーズを含む前記液滴は、前記解析プロトコルを実施する前に、前記液滴操作間隙から除去される、請求項190に記載の方法。
【請求項193】
前記解析プロトコルの結果の出力の指標を提供する工程をさらに含む、請求項190に記載の方法。
【請求項194】
前記実質的に精製された標的検体を含むビーズを含む液滴を、前記液滴操作間隙から除去する工程をさらに含む、請求項189に記載の方法。
【請求項195】
前記1つ以上の標的検体を、前記実質的に精製された標的検体を含むビーズから放出する工程をさらに含む、請求項189に記載の方法。
【請求項196】
前記放出する工程は、前記実質的に精製された標的検体を含むビーズを含む液滴と、放出バッファーを含む液滴とを混合して、前記ビーズおよび前記放出された1つ以上の標的検体を含む液滴を生じる工程を含む、請求項195に記載の方法。
【請求項197】
前記ビーズおよび前記放出された1つ以上の標的検体を含む前記液滴から前記ビーズを除去して、実質的に精製された標的検体を含み、実質的にビーズを含まない液滴を生じる工程をさらに含む、請求項196に記載の方法。
【請求項198】
前記実質的に精製された標的検体を含み、実質的にビーズを含まない液滴を、前記液滴操作間隙から除去する工程をさらに含む、請求項197に記載の方法。
【請求項199】
前記実質的に精製された標的検体を含み、実質的にビーズを含まない液滴を用いて検体プロトコルを実施する工程をさらに含む、請求項197に記載の方法。
【請求項200】
前記解析プロトコルの結果の出力の指標を提供する工程をさらに含む、請求項199に記載の方法。
【請求項201】
前記方法の工程の1つ以上は、前記液滴アクチュエータおよび前記方法の工程の1つ以上を実施するようにプログラムされたプロセッサを含むシステムによって実施される、請求項171および以下の請求項のいずれかに記載の方法。
【請求項202】
前記解析プロトコルの結果の、使用者により読み取り可能な出力の指標を出力する工程をさらに含む、請求項201に記載の方法。
【請求項203】
前記標的検体は、核酸を含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項204】
前記標的検体は、タンパク質またはペプチドを含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項205】
前記標的検体は、抗体を含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項206】
前記標的検体は、小有機分子を含む、請求項171および以下の請求項のいずれかに記載の方法。
【請求項207】
前記液滴操作間隙は、流動性の充填流体で満たされる、請求項171および以下の請求項のいずれかに記載の方法。
【請求項208】
液滴アクチュエータを操作する方法であって、前記方法は、
(a)内部液滴操作間隙を形成するように構成される1つ以上の基板を備える液滴アクチュエータ装置を提供する工程と、
(b)前記液滴操作間隙内に流動性の充填流体を提供する工程と、
(c)前記液滴操作間隙内の前記充填流体中で液滴プロトコルを実施する工程と、
(d)前記液滴操作間隙内に前記充填流体を再配置する工程と、
(e)同じまたは異なる液滴プロトコルを用いて工程(c)を繰り返す工程と、
を含む、方法。
【請求項209】
請求項208に記載の工程(d)および請求項208に記載の工程(e)を、2回以上繰り返す工程をさらに含む、請求項208に記載の方法。
【請求項210】
請求項208に記載の工程(d)および請求項208に記載の工程(e)を、5回以上繰り返す工程をさらに含む、請求項208に記載の方法。
【請求項211】
請求項208に記載の工程(d)および請求項208に記載の工程(e)を、10回以上繰り返す工程をさらに含む、請求項208に記載の方法。
【請求項212】
請求項208に記載の工程(d)は、前記液滴操作間隙を通して充填流体をフラッシュする工程をさらに含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項213】
前記液滴操作間隙を通して充填流体をフラッシュする工程は、所定量のフラッシングが達成されるまで続けられる、請求項212に記載の方法。
【請求項214】
前記液滴操作間隙を通して充填流体をフラッシュする工程は、洗浄の指標が所定のレベルに到達するまで続けられる、請求項212に記載の方法。
【請求項215】
前記フラッシングの量は、自動化される、請求項213または214に記載の方法。
【請求項216】
請求項208に記載の工程(c)は、診断プロトコルを実施する工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項217】
請求項208に記載の工程(c)は、核酸増幅プロトコル、核酸シークエンシングプロトコル、免疫アッセイプロトコル、および酵素アッセイプロトコルからなる群より選択されるプロトコルを実施する工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項218】
請求項208に記載の工程(c)は、請求項208に記載の工程(d)を実施する前に、2回以上繰り返される、請求項208および以下の請求項のいずれかに記載の方法。
【請求項219】
前記流動性の充填流体は、請求項208に記載の工程(c)の各々の繰り返しの後に汚染物質について試験され、請求項208に記載の工程(d)は所定のレベルの汚染物質が検出された後に実施される、請求項218に記載の方法。
【請求項220】
請求項208に記載の工程(c)の各々の繰り返し後に汚染物質について試験すること、および請求項208に記載の工程(d)への進行の決定は、自動化される、請求項219に記載の方法。
【請求項221】
請求項208に記載の工程(d)は、前記液滴操作間隙を通して、前記液滴操作間隙の外部へ、流動性の充填流体源から前記流動性の充填流体を流動させることを含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項222】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に、前記液滴操作間隙を通して洗浄流体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項223】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に、前記液滴操作間隙を通して充填流体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項224】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に、前記液滴操作間隙を通して加熱された洗浄液体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項225】
前記加熱された洗浄液体は、汚染物質を溶解または分解するように選択された温度を有する、請求項224に記載の方法。
【請求項226】
前記加熱された洗浄液体は、約30℃〜約125℃の範囲の温度を有する、請求項224に記載の方法。
【請求項227】
前記加熱された洗浄液体は、約60℃〜約115℃の範囲の温度を有する、請求項224に記載の方法。
【請求項228】
前記加熱された洗浄液体は、約75℃〜約105℃の範囲の温度を有する、請求項224に記載の方法。
【請求項229】
前記加熱された洗浄液体は、約90℃より高い温度を有する、請求項224に記載の方法。
【請求項230】
前記加熱された洗浄液体は、約100℃より高い温度を有する、請求項224に記載の方法。
【請求項231】
前記加熱された洗浄液体は、約125℃より高い温度を有する、請求項224に記載の方法。
【請求項232】
前記加熱された洗浄液体は、約150℃より高い温度を有する、請求項224に記載の方法。
【請求項233】
前記加熱された洗浄液体は、前記液滴アクチュエータの1つ以上の構成要素が過度に損傷を受ける温度より低い温度を有する、請求項224および以下の請求項のいずれかに記載の方法。
【請求項234】
前記加熱された洗浄液体は、充填流体を含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項235】
前記加熱された洗浄液体は、オイルを含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項236】
前記加熱された洗浄液体は、溶媒を含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項237】
前記加熱された洗浄液体は、水性洗浄液体を含む、請求項224および以下の請求項のいずれかに記載の方法。
【請求項238】
前記洗浄液体は、
(a)親油性物質が溶解できる成分と、
(b)親水性物質が溶解できる成分と、
を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項239】
請求項208に記載の工程(d)は、前記充填流体を前記液滴操作間隙内に再配置する前に前記液滴アクチュエータ間隙を乾燥させるために、前記液滴アクチュエータ間隙を通してガスを流動させる工程をさらに含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項240】
前記ガスは、空気を含む、請求項239に記載の方法。
【請求項241】
前記ガスは、約50℃より高い温度を有する、請求項239に記載の方法。
【請求項242】
前記ガスは、約75℃より高い温度を有する、請求項239に記載の方法。
【請求項243】
前記ガスは、約100℃より高い温度を有する、請求項239に記載の方法。
【請求項244】
前記ガスは、約125℃より高い温度を有する、請求項239に記載の方法。
【請求項245】
前記ガスは、約150℃より高い温度を有する、請求項239に記載の方法。
【請求項246】
前記ガスは、前記液滴アクチュエータの1つ以上の成分が過度に損傷を受ける温度より低い温度を有する、請求項239および以下の請求項のいずれかに記載の方法。
【請求項247】
請求項208に記載の工程(d)は、前記液滴アクチュエータ間隙を通して前記ガスを流動させる前に、前記液滴アクチュエータ間隙を通して洗浄液体を流動させる工程を含む、請求項239に記載の方法。
【請求項248】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約50%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項249】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約75%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項250】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約90%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項251】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約95%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項252】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約99%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項253】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の少なくとも約99.9%を置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項254】
請求項208に記載の工程(d)は、請求項208に記載の工程(c)の間に前記液滴操作間隙に存在する前記充填流体の実質的に全てを置き換える、請求項208および以下の請求項のいずれかに記載の方法。
【請求項255】
(a)前記液滴操作間隙の1つ以上の表面は、コーティングを含み、
(b)前記洗浄液体は、前記コーティングの層を除去するように選択される、
請求項208および以下の請求項のいずれかに記載の方法。
【請求項256】
請求項208に記載の工程(d)は、前記液滴操作間隙内の前記充填流体を置き換える前に、所定の温度を規定するように、前記液滴操作間隙を通して冷却液体を流動させる工程を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項257】
前記洗浄流体は、溶媒を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項258】
前記洗浄流体は、水溶液を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項259】
前記洗浄流体は、親油性化合物を溶解する1つ以上の成分、および親水性化合物を溶解する1つ以上の成分を含む、請求項208および以下の請求項のいずれかに記載の方法。
【請求項260】
請求項208および以下の請求項のいずれかに記載の方法を実施するための命令を有するプログラムを含む、コンピューター可読媒体。
【請求項261】
(a)内部液滴操作間隙を形成するように構成される1つ以上の基板を備える液滴アクチュエータ装置と、
(b)流動性の充填流体源に流動的に接続される前記液滴操作間隙内の開口部と、
(c)前記開口部を通して、前記液滴操作間隙内への前記充填流体源からの充填流体の流れを制御するように構成される1つ以上のバルブおよび/またはポンプと、
(d)1つ以上の前記ポンプおよび/またはバルブを制御し、請求項208および以下の請求項のいずれかの方法を実行するようにプログラムされるプロセッサと、
を含む、システム。
【請求項262】
液滴操作間隙を形成するように分離された2つの基板を備える液滴アクチュエータであって、前記液滴操作間隙は、
(a)液体経路に流動的に接続された少なくとも2つの温度制御リザーバーを規定する1つ以上の障壁と、
(b)1つまたは両方の基板と結合され、前記温度制御リザーバーの間に液滴を輸送するように構成される電極と、
を備える熱サイクル経路を備える、液滴アクチュエータ。
【請求項263】
2つ以上の前記熱サイクル経路を備える、請求項262に記載の液滴アクチュエータ。
【請求項264】
液滴アクチュエータ上の液滴間の二次汚染を防止する方法であって、前記方法は、
(a)(i)液滴操作間隙を形成する1つ以上の基板と、(ii)複数の実質的に平行な液滴操作経路を規定する1つ以上に基板に結合された電極と、(iii)前記液滴操作間隙を実質的に充填する流動性の充填流体と、を備える液滴アクチュエータを提供する工程と、
(b)複数の実質的に平行な液滴輸送経路の第1のサブセット上で複数のアッセイ液滴を輸送する工程と、
(c)複数の実質的に平行な液滴輸送経路の第2のサブセット上で1つ以上のバッファー液滴を輸送する工程であって、前記第2のサブセットの各々の液滴輸送経路は、前記第1のサブセットの2つの液滴輸送経路の間にある、工程と、
を含む、方法。
【請求項265】
アッセイ液滴を輸送する工程と、液滴を洗浄する工程は、同時に行われる、請求項264に記載の方法。
【請求項266】
2つ以上の洗浄液滴が、前記第2のサブセットの各々の液滴輸送経路に提供される、請求項264に記載の方法。
【請求項267】
前記洗浄液滴は、液滴スラグの形状で提供される、請求項264に記載の方法。
【請求項268】
前記第1のサブセットの液滴輸送経路に1つ以上のバッファー液滴を輸送する工程をさらに含む、請求項264に記載の方法。
【請求項269】
(a)前記第1のサブセットの液滴輸送経路に1つ以上のバッファー液滴を輸送する工程と、
(b)前記第1の洗浄液滴に対して前記アッセイ液滴の反対側の前記第1のサブセットの液滴輸送経路に1つ以上のバッファー液滴を輸送する工程と、
を含む、請求項264に記載の方法。
【請求項270】
前記アッセイ液滴は、核酸増幅液滴を含む、請求項264および以下の請求項のいずれかに記載の方法。
【請求項271】
前記方法は、増幅を行うために2つの熱領域の間に前記アッセイ液滴を輸送する工程をさらに含む、請求項270に記載の方法。
【請求項272】
(a)液滴アクチュエータ間隙を設けるように配置される1つ以上の基板と、
(b)複数の実質的に平行な液滴輸送経路を規定する前記1つ以上の基板に結合された電極と、
(c)前記液滴操作間隙を実質的に充填する流動性の充填流体と、
(d)前記液滴輸送経路の各々の間にあり、1つの液滴操作経路に結合された充填流体が、他の液滴操作経路に結合された充填流体と接触することを防ぐ、障壁と、
を備える、液滴アクチュエータ。
【請求項273】
2つ以上の前記液滴輸送経路上にアッセイ液滴をさらに含む、請求項272に記載の液滴アクチュエータ。
【請求項274】
前記アッセイ液滴は、核酸を増幅するための試薬およびサンプルを含む、請求項273に記載の液滴アクチュエータ。
【請求項275】
液滴アクチュエータ上の液滴間の二次汚染を減少させる方法であって、前記方法は、
(a)内部液滴操作間隙と、前記液滴操作間隙内にオイルベースの充填流体とを含む液滴アクチュエータを提供する工程と、
(b)前記液滴操作間隙内に水性液滴を提供する工程であって、前記液滴は、(i)前記オイルベースの充填流体によって少なくとも部分的に囲まれ、(ii)界面活性剤−酵素複合体を含み、前記複合体は、潜在的に汚染物質を分解するように選択された酵素に結合された界面活性剤を含む、工程と、
を含む、方法。
【請求項276】
前記酵素は、ヌクレアーゼを含む、請求項275に記載の方法。
【請求項277】
前記酵素は、エンドヌクレアーゼを含む、請求項275に記載の方法。
【請求項278】
前記酵素は、エキソヌクレアーゼを含む、請求項275に記載の方法。
【請求項279】
前記酵素は、プロテイナーゼを含む、請求項275に記載の方法。
【請求項280】
前記界面活性剤は、PAG−アルキル界面活性剤を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項281】
前記界面活性剤−酵素複合体は、酵素−PAG−アルキル複合体を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項282】
前記界面活性剤は、前記酵素のアミノ部分に結合される、請求項275および以下の請求項のいずれかに記載の方法。
【請求項283】
前記界面活性剤−酵素複合体は、前記液滴中で実質的に不活性であるのに十分に低い量、かつ前記液滴から形成される微小液滴中で活性化するのに十分に高い量で前記液滴に存在する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項284】
前記微小液滴は、約10μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項285】
前記微小液滴は、約1μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項286】
前記微小液滴は、約0.01μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項287】
前記微小液滴は、約0.001μL未満である平均体積を有する、請求項275および以下の請求項のいずれかに記載の方法。
【請求項288】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約1未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項289】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約0.1未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項290】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約0.01未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項291】
平均液滴サイズ対平均微小液滴サイズの比は、約1000対約0.001未満である、請求項275および以下の請求項のいずれかに記載の方法。
【請求項292】
前記潜在的な汚染物質は、タンパク質を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項293】
前記潜在的な汚染物質は、核酸を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項294】
前記潜在的な汚染物質は、試薬を含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項295】
前記界面活性剤−酵素複合体の実質的に全ては、前記液滴の表面に閉じ込められる、請求項275および以下の請求項のいずれかに記載の方法。
【請求項296】
前記充填流体は、シリコンオイルを含む、請求項275および以下の請求項のいずれかに記載の方法。
【請求項297】
前記液滴は、前記充填流体によって実質的に囲まれる、請求項275および以下の請求項のいずれかに記載の方法。
【請求項298】
前記液滴は、前記充填流体によって完全に囲まれる、請求項275および以下の請求項のいずれかに記載の方法。
【請求項299】
(a)標的核酸を含み、必要に応じて増幅試薬を含む、サンプル液滴を提供する工程と、
(b)前記サンプル液滴から小液滴を分配する工程と、増幅試薬が前記サンプル液滴に存在しない場合、各々の小液滴と増幅試薬とを混合して、増幅準備液滴を生じる工程と、
(c)各々の小液滴を、前記標的核酸を増幅するために選択される熱サイクルプロトコルに供する工程と、
(d)各々の小液滴中の増幅産物を検出する工程と、
(e)前記増幅産物が形成されるサンプル部分を含む小液滴の数を決定する工程と、
を含む、方法。
【請求項300】
前記小液滴の少なくとも1つは、少なくとも1つの標的核酸分子を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項301】
前記増幅試薬は、増幅された標的分子にハイブリダイズし、ハイブリダイゼーション時に変化するか、またはハイブリダイゼーションの結果として変化する蛍光特性を有する少なくとも1つのプローブを含み、前記増幅産物が形成されるサンプル部分を含む前記小液滴の数を決定する工程は、前記少なくとも1つのプローブのハイブリダイゼーションに起因する前記蛍光の変化を検出する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項302】
前記増幅産物が形成されるサンプル部分を含む前記小液滴の数を決定する工程は、全ての小液滴を一緒に画像化する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項303】
前記増幅産物が形成されるサンプル部分を含む前記小液滴の数を決定する工程は、検出ウィンドウを通して1つずつまたはサブグループで液滴を輸送する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項304】
前記小液滴は、約1μL未満の体積を有する、請求項299および以下の請求項のいずれかに記載の方法。
【請求項305】
前記小液滴は、約1μLより大きい範囲から約1000μLの体積を有する、請求項299および以下の請求項(請求項304を除く)に記載の方法。
【請求項306】
前記小液滴は、約100μLより大きい範囲から約500μLの体積を有する、請求項299および以下の請求項(請求項304を除く)に記載の方法。
【請求項307】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、液滴アクチュエータの液滴操作間隙内で実施される、請求項299および以下の請求項のいずれかに記載の方法。
【請求項308】
前記小液滴は、前記液滴操作間隙内の2つの基板の間で平面またはディスク形状の構造に圧縮される、請求項307に記載の方法。
【請求項309】
前記液滴操作間隙は、約50μm〜約1000μmの範囲の高さを有する、請求項307に記載の方法。
【請求項310】
前記液滴操作間隙は、約100μmより大きい範囲から約500μmの範囲の高さを有する、請求項307に記載の方法。
【請求項311】
熱サイクルが、1つの熱領域から別の熱領域へ液滴を輸送することによって行われる、請求項299および以下の請求項のいずれかに記載の方法。
【請求項312】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、サンプルチャンバを欠く液滴アクチュエータの液滴操作間隙内で実施される、請求項299および以下の請求項のいずれかに記載の方法。
【請求項313】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、流路チャネルを欠く液滴アクチュエータの液滴操作間隙内で実施される、請求項299および以下の請求項のいずれかに記載の方法。
【請求項314】
請求項299に記載の工程(b)、請求項299に記載の工程(c)、請求項299に記載の工程(d)、および請求項299に記載の工程(e)のうちの1つ以上は、液滴アクチュエータの液滴操作間隙内で実施され、前記サンプル液滴から小液滴を分配する工程は、流路チャネルからサンプルを配置する配置流体を用いずに行われる、請求項299および以下の請求項のいずれかに記載の方法。
【請求項315】
標的核酸を含む前記サンプル液滴を提供する工程は、増幅試薬も含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項316】
増幅試薬は、前記サンプル液滴に存在せず、前記方法は、各々の小液滴と増幅試薬とを混合して、増幅準備液滴を生じる工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【請求項317】
各々の小液滴中の増幅産物を検出する工程は、前記液滴を検出に供する前に、前記増幅液滴と、1つ以上の検出試薬を含む液滴とを混合する工程を含む、請求項299および以下の請求項のいずれかに記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12A】


【図12B】


【図13】


【図14】


【図15】


【図16A】


【図16B】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【図46A】


【図46B】


【図46C】


【図46D】


【図47A】


【図47B】


【図47C】


【図47D】


【図47E】


【図47F】


【図47G】


【図47H】


【図47I】


【図48A】


【図48B】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12A】


【図12B】


【図13】


【図14】


【図15】


【図16A】


【図16B】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【図45】


【図46A】


【図46B】


【図46C】


【図46D】


【図47A】


【図47B】


【図47C】


【図47D】


【図47E】


【図47F】


【図47G】


【図47H】


【図47I】


【図48A】


【図48B】


【公表番号】特表2011−520449(P2011−520449A)
【公表日】平成23年7月21日(2011.7.21)
【国際特許分類】
【出願番号】特願2011−509649(P2011−509649)
【出願日】平成21年5月13日(2009.5.13)
【国際出願番号】PCT/US2009/043774
【国際公開番号】WO2009/140373
【国際公開日】平成21年11月19日(2009.11.19)
【出願人】(509225524)アドヴァンスト リキッド ロジック インコーポレイテッド (8)
【Fターム(参考)】
【公表日】平成23年7月21日(2011.7.21)
【国際特許分類】
【出願日】平成21年5月13日(2009.5.13)
【国際出願番号】PCT/US2009/043774
【国際公開番号】WO2009/140373
【国際公開日】平成21年11月19日(2009.11.19)
【出願人】(509225524)アドヴァンスト リキッド ロジック インコーポレイテッド (8)
【Fターム(参考)】
[ Back to top ]

