淡水性発光細菌の培地液及び毒性検査方法並びにバイオセンサー
【課題】塩分を必要とせず、生育pH範囲が広い淡水性発光細菌に注目し、その発光強度を制御する培地液及びこれを用いた毒性検査方法並びにバイオセンサーを提供する。
【解決手段】淡水性発光細菌の発光強度を増加させる培地液であって、水溶液中に、カリウムイオンを0.001〜1.5g/L、マグネウシムイオンを0.1〜1g/L、及び炭酸水素イオンを0.05〜0.1g/L含む。特に、淡水性発光細菌を用いて重金属やBODなどの検査が可能となり、この培地液で培養された淡水性発光細菌を担持膜に担持させることによって、バイオセンサーが形成できる。
【解決手段】淡水性発光細菌の発光強度を増加させる培地液であって、水溶液中に、カリウムイオンを0.001〜1.5g/L、マグネウシムイオンを0.1〜1g/L、及び炭酸水素イオンを0.05〜0.1g/L含む。特に、淡水性発光細菌を用いて重金属やBODなどの検査が可能となり、この培地液で培養された淡水性発光細菌を担持膜に担持させることによって、バイオセンサーが形成できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、淡水性発光細菌(例えば、フォトラブドゥス・ルミネセンス、Photorhabdus luminescens)の発光増大に対して、NH4+、PO3−が負の影響を、K+、Mg2+、Na+、H+、CO32−が正の影響を与えることを見いだし、一般的培地(例えば、Nutrient Broth)を用いて、又はこれらの培地無しで、淡水性発光細菌を発光させる淡水性発光細菌の培地液及びこれらを用いた毒性検査方法並びに毒性検査具(バイオセンサー)に関する。
【背景技術】
【0002】
発光細菌は生物発光を行う細菌のことをいい、迅速簡便な毒性評価等のバイオアッセイ(生物検定や生物学的試験)やバイオセンサーに利用され、比較的容易に発光量を高めることが可能なことから、一般には海洋性のビブリオ・フィシェリ(Vibrio fischeri)等が広く使用されている。なお、発光細菌は以上の毒性評価の他、FMN又はFAD(P)Hを軸とする酵素系の定量、ATPの測定にも応用されている。
【0003】
このビブリオ・フィシェリの培養方法としては、ニュトリエントブロス(Nutrient Broth3%NaClを含む)、マリンブロス(Marine Broth)等の栄養の富んだ液体培地が使用されている。これは、生物発光に、培地の栄養が富んだ状態で菌数が高密度に増殖した場合により強い発光が現れるクオラムセンシング(quorum sensing)が関与しているからである。
特許文献1には、このような目的に使用される発光細菌(ビブリオ・フィシェリ、フォトバクテリウム・レイオグナチ、フォトバクテリウム・フォスフォレウム、フォトラブドゥス・ルミネセンス)が開示されている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2003−310297号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
特許文献1は、効果のクロマトグラフィーによる検出の実用についての従来技術の限界を克服する生物活性物質を検出するための方法及びキットを提供することを目的としており、更に、使用する培地として、ジペプチド、オリゴペプチド、ホウ酸ジエステル等FFのホウ素化合物、キノロン又はN−アシルホモセリンラクトンあるいはそれらの生化学的前駆物質が使用されており、本願発明とは課題が異なると共に、使用する物質についても異なる。更に、特許文献1では、確かにフォトラブドゥス・ルミネセンスの記載はあるが、実施の好適な態様においては、海洋性の発光細菌であるビブリオ・フィシェリが使用されており、淡水性の発光細菌や、この一例であるフォトラブドゥス・ルミネセンスについての具体的な記載はない。
【0006】
更に、ビブリオ・フィシェリは、生育pH範囲が狭いこと、海洋性であるので2〜3質量%の塩分(NaCl)を必要とし、測定する物質の状態(即ち、工場排水等の淡水性の場合)によって、正確な毒性評価が困難であるとういう問題がある。一方、フォトラブドゥス・ルミネセンス等の淡水性発光細菌は、生育に塩分は必要とせず、取り扱いが容易であるものの、発光量がやや低いことに起因して一般にはバイオセンサーの開発は行われていない。また、フォトラブドゥス・ルミネセンス等で代表される淡水性発光バクテリアの実験を種々行った結果、菌濃度の増加は必ずしも発光性の増大に繋がるものではなく、十分な菌濃度が得られても発光強度が低い場合があることや、逆に菌濃度は低くても培養液の状態によっては、発光強度が高い場合があることを知見して、本発明を完成した。
【0007】
本発明は、かかる事情に鑑みてなされたもので、塩分を必要とせず、生育pH範囲が広い淡水性発光細菌に注目し、その発光強度を制御する培地液及びこれらを用いた毒性検査方法並びにバイオセンサーを提供することを目的とする。
【課題を解決するための手段】
【0008】
第1の発明に係る淡水性発光細菌の培地液は、淡水性発光細菌の発光強度を増加させる培地液であって、水溶液中に、カリウムイオンを0.001〜1.5g/L、マグネウシムイオンを0.1〜1g/L、及び炭酸水素イオンを0.05〜0.1g/L含む。
【0009】
第1の発明に係る淡水性発光細菌の培地液において、1)前記カリウムイオン源は塩化カリウム、臭化カリウム、及び硝酸カリウムのいずれか1又は2以上、2)前記マグネシウムイオン源は塩化マグネシウム、臭化マグネシウム、酢酸マグネシウム、及び三塩化カリウムマグネシウムのいずれか1又は2以上、3)前記炭酸水素イオン源は炭酸水素ナトリウム、炭酸水素アンモニウム、及び炭酸水素カリウムのいずれか1又は2以上を使用するのが一般的であるが、淡水性発光細菌に害を有されない化合物であれば、他の化合物であってもよい。なお、カリウムイオン源として、KHCO3を使用すると、カリウムイオンが適正値であっても、炭酸水素イオンが規定値をオーバーする場合は、発光量が低下する。また、淡水性発光細菌に対して毒性を有する他の化合物を混合しないことは当然である。
【0010】
また、本発明の第2の発明に係る淡水性発光細菌の培地液は、淡水性発光細菌の発光強度を増加させる培地液であって、1000mLの水溶液中に、カリウムイオンを0.05〜50mM、マグネウシムイオンを0.05〜50mM、ナトリウムイオン及び炭酸水素イオンをそれぞれ0.01〜50mM含み、pHが3〜8の範囲にある。なお、1000mLの水溶液中に、カリウムイオンを0.05〜50mMは、0.002g〜2g/Lを、マグネウシムイオンを0.05〜50mMは0.0012〜1.2g/Lを、ナトリウムイオン及び炭酸水素イオンをそれぞれ0.01〜50mMは、0.0023〜1.2g/L(Na+)、0.00062〜3.1g/L(HCO3−)をいう。
【0011】
第2の発明に係る淡水性発光細菌の培地液において、前記カリウムイオン源は塩化カリウム、前記マグネシウムイオン源は塩化マグネシウム、前記炭酸水素イオン源は、炭酸水素ナトリウムを用いるのが好ましいが、淡水性発光細菌に害を有されない化合物であれば、他の化合物であってもよい。
【0012】
第1、第2の発明に係る淡水性発光細菌の培地液において、前記水溶液には前記淡水性発光細菌の栄養源(例えば、Nutrient broth)が添加されているのが好ましい。これによって、淡水性発光細菌は菌数を保持又は増加させることができる。
【0013】
第1、第2の発明に係る淡水性発光細菌の培地液において、前記淡水性発光細菌はフォトラブドゥス・ルミネセンスであるのが好ましいが、他の淡水性発光細菌であってもよい。
【0014】
そして、第3の発明に係る淡水性発光細菌を用いた毒性検査方法は、第1、第2の発明に係る淡水性発光細菌の培地液に淡水性発光細菌を含ませて、該淡水性発光細菌の発光強度を増加させて、試験対象物の試験液として使用する。この毒性検査方法は、比較的安価で容易に入手できる化合物を用いて、培地液を構成でき、しかも、この培地液を用いて淡水性発光細菌の発光強度を高めることができる。更に、淡水性発光細菌は、海洋性発光細菌とは異なり、塩分(NaCl)を必要とせず、pH範囲も広いので、より多くの試験対象物に対応でき、毒性試験の対象物を広げることができる。
【0015】
第4の発明に係るバイオセンサーは、第1の発明に係る淡水性発光細菌の培地液に、淡水性発光細菌及び栄養源を加えて、前記淡水性発光細菌を培養した培養液を、透明容器の内側に設けられた担持膜に含ませ無水処理を行っている。
また、第5の発明に係るバイオセンサーは、淡水性発光細菌が担持された担持膜を透明容器の内側底部に設けて構成されている。
【0016】
第4、第5の発明に係るバイオセンサーにおいて、前記担持膜はフィブロイン、アルギン酸、寒天、ゼラチン、又はその他の多孔性で粘性を有する物質からなるのが好ましい。
なお、バイオセンサーの用途としては、例えば淡水での重金属量(例えば、水銀、ニッケル等)又は淡水でのBODの測定に利用できる。
【発明の効果】
【0017】
第1、第2の発明に係る淡水性発光細菌の培地液及びこれを用いた第3の発明に係る毒性検査方法並び第4、第5の発明に係るバイオセンサーは、比較的安価で容易に入手できる化合物を用いて、培地液を構成でき、しかも、この培地液を用いて淡水性発光細菌の発光強度を高めることができる。
更に、淡水性発光細菌は、海洋性発光細菌とは異なり、塩分(NaCl)を必要とせず、pH範囲も広いので、第3の発明に係る毒性検査方法及び第4、第5の発明に係るバイオセンサーは、工場排水や下水処理場等、より多くの試験対象物に対応でき、毒性試験の対象物を広げることができる。
【0018】
特に、第1の発明に係る淡水性発光細菌の培地液において、1)カリウムイオン源は塩化カリウム、臭化カリウム、及び硝酸カリウムのいずれか1又は2以上、2)マグネシウムイオン源は塩化マグネシウム、臭化マグネシウム、酢酸マグネシウム、及び三塩化カリウムマグネシウムのいずれか1又は2以上、3)炭酸水素イオン源は炭酸水素ナトリウム、炭酸水素アンモニウム、及び炭酸水素カリウムのいずれか1又は2以上を使用した場合には、比較的安価に淡水性発光細菌の培地液を製造することができる。
【図面の簡単な説明】
【0019】
【図1】(A)、(B)はそれぞれ培地液の5つの成分のうち1を欠如させた場合の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図2】(A)、(B)はそれぞれ培地液の5つの成分のうち2を欠如させた場合の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図3】(A)、(B)はそれぞれ培地液の5つの成分のうち3を欠如させた場合の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図4】(A)、(B)はそれぞれ培地液の5つの成分の各々の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図5】(A)、(B)、(C)はそれぞれNB培地液を用いた場合の菌体量、発光量、細胞1個当たりの発光量の推移を示すグラフである。
【図6】(A)、(B)、(C)はそれぞれ3エレメント(KCl:0.77g/L、NaHCO3:0.11g/L、MgCl2・6H2O:4.8g/L)の培地液を用いた場合の菌体量、発光量、細胞1個当たりの発光量の推移を示すグラフである。
【図7】(A)、(B)、(C)はそれぞれ更にNBを加えた培地液を用いた場合の菌体量、発光量、細胞1個当たりの発光量の推移を示すグラフである。
【図8】K+の濃度と発光量との関係を示すグラフである。
【図9】Mg2+濃度と発光量との関係を示すグラフである。
【図10】マグネシウム化合物の濃度と発光量の関係を示すグラフである。
【図11】HCO3−濃度と発光量の関係を示すグラフである。
【図12】(A)〜(C)はそれぞれK、Mg、HCO3化合物の種類と発光量との関係を示すグラフである。
【図13】バイオセンサーの説明図である。
【図14】(A)、(B)はそれぞれバイオセンサーの毒性評価を示すグラフである。
【図15】(A)、(B)はそれぞれバイオセンサーのBOD検査評価を示すグラフである。
【図16】バイオセンサーのBOD検査評価を示すグラフである。
【発明を実施するための形態】
【0020】
続いて、添付した図面を参照しながら、本発明を具体化した実施の形態について説明する。
本発明者らは、先に出願した特願2010−268623号において海洋性発光バクテリアの発光制御方法で、海水に含まれるNaCl、KCl、CaCl2、MgCl2・6H2O、NaHCO3、MgSO4・7H2Oについて如何なる成分が発光性に寄与するかを実験して調べた。しかしながら、海洋性発光バクテリアは前述のように、塩分(NaCl)を必須の成分とし、生存するpH範囲が狭いので、実施上支障がある場合があり、塩分を必要としない淡水性発光バクテリアに注目し、如何なる成分が淡水性発光バクテリアの発光度に寄与するかを研究した。
【0021】
実験に当たっては、海水に含まれる成分を参照して選んだ結果、淡水であることから塩分(NaCl)を除く、1)KCl、2)CaCl2、3)MgCl2・6H2O、4)NaHCO3、5)MgSO4・7H2Oの5成分が有効であると推定し、更にこの中でどの成分が淡水性発光バクテリア(細菌)の発光に寄与するかを実験した。
【0022】
この実験液には、1)KClを0.77g/L(10.3mM)、2)CaCl2を1.21g/L(10.9mM)、3)MgCl2・6H2Oを4.8g/L(23.6mM)、4)NaHCO3を0.11g/L(1.3mM)、5)MgSO4・7H2Oを3.50g/L(14.2mM)をそれぞれ単位として、これらの1〜5を欠如させて、欠如させた培地(培地液に同じ)における淡水性発光細菌の菌体量(菌の数)と発光量を測定した。なお、培養時間は18時間とし、以下の実験においては、淡水性発光細菌として、フォトラブドゥス・ルミネセンスを用い、菌体量として、液の濁り(OD)を測定し、発光量については、5分間の積算値で1mL中の発光量をルミノメータで測定した。なお、ここで、「mM」は水1Lに対するモル数を示す。
【0023】
なお、1)KClを0.77g/Lは、K+イオンに換算して0.4g/L、2)MgCl2・6H2Oの4.8gは、Mg2+イオンに換算して0.6g/L、3)NaHCO3の0.11g/LはHCO3−に換算して0.08g/L、4)MgSO4・7H2Oの3.5g/LはMg2+イオンに換算して0.3g/Lとなる(以下、この溶液を「ISS培地」という)。
【0024】
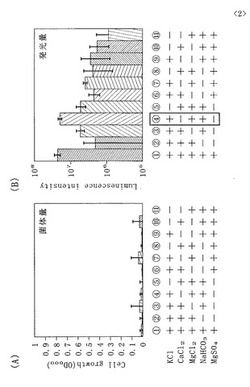
図1(A)、(B)は5成分の1を欠如させたもので、いずれもバクテリアの増殖はみられないが、(3)のNaHCO3欠如、(4)のMgCl2欠如、(6)のKCl欠如のものでは、発光量が他のものより減少していることが判る。
【0025】
図2(A)、(B)は5成分の2を欠如させたもの(即ち、3成分)で、いずれもバクテリアの増殖はみられないが、(4)のKCl、MgCl2・6H2O、NaHCO3を含むものについては、発光量が他のものより多いことが判る。
【0026】
図3(A)、(B)は5成分の3を欠如させたもの(即ち、2成分)で、いずれもバクテリアの増殖はみられない。また、発光量も(1)の全てを含むものに対して、いずれもかなり低くなっている。
【0027】
図4(A)、(B)は5成分の4を欠如させたもの(即ち、1成分)で、いずれもバクテリアの増殖はみられない。また、発光量も(1)の全てを含むものに対して、いずれもかなり低くなっている。
【0028】
図5(A)、(B)、(C)は市販のNB培地(Nutrient broth)を用いて、菌体量、発光量、細胞1個当たりの発光量の時間的推移を詳細に測定したものである。菌体量の増加に伴って、クオラムセンシングにより一時(例えば10〜20時間)は発光量と細胞(菌)の1個当たりの発光量の増加が認められるが、その後は発光量が減少し、その発光量の増加に対して細胞(菌)の1個当たりの発光量が減少していることが判る。
【0029】
図6(A)、(B)、(C)は、KCl(0.77g/L)、MgCl2・6H2O(4.8g/L)、NaHCO3(0.11g/L)のみを培地に溶解させたものを用いて、菌体量、発光量、細胞1個当たりの発光量の時間的推移を測定したものであるが、栄養素が培地にないので、菌体量の増加はない。発光量は15時間経過後位から増加し、細胞1個当たりの発光量も増加している。以上の実験から、フォトラブドゥス・ルミネセンスは栄養源がなく、従って菌体量の増加がない場合であっても、少量のKCl、MgCl2、NaHCO3 が存在すれば、発光することが分かる。
【0030】
図7(A)、(B)、(C)はそれぞれNB培地の場合と、NB培地に更にKCl(0.77g/L)、MgCl2・6H2O( 4.8g/L)、NaHCO3(0.11g/L)を加えた場合との菌体量、発光量、及び細胞1個当たりの発光量の時間的変化を示すが、NB培地に更にKCl(0.77g/L)、MgCl2・6H2O( 4.8g/L)、NaHCO3(0.11g/L)を加えた場合(即ち、栄養源に3エレメントが添加されている場合)の方が、発光量が増すことが判る。
【0031】
以上の実験から以下のことが判る。
(1)カリウムイオン源となるKCl、マグネシウムイオン源となるMgCl2、ナトリウムイオン源及び炭酸水素イオン源となるNaHCO3が欠乏すると、発光量が低下する。
(2)KCl、MgCl2、NaHCO3の3成分で、5成分(KCl、CaCl2、MgCl2、NaHCO3、MgSO4)の発光量と同程度の発光量がある。
(3)NB培地に3成分(KCl、MgCl2、NaHCO3)を添加することによって菌体量、発光量、細胞1つ当たりの発光量が増加する。
(4)以上のことから、3成分(KCl、MgCl2、NaHCO3)が淡水性発光細菌の発光ファクターであるのが判る。なお、この実験では、NaHCO3を使っているので、ナトリウムイオン及び炭酸水素ナトリウムのイオンのいずれか、又は双方が必要であるかについては分からない。
【0032】
上の実験において、カリウムイオン源、マグネシウムイオン源、ナトリウムイオン源、炭酸水素イオン源として、1)KClを0.77g/L(10.3mM)、2)MgCl2・6H2Oを4.8g/L(23.6mM)、3)NaHCO3を0.11g/L(1.3mM)としたが、KClについては、0.05〜50mM(より好ましくは、0.1〜10mM)、MgCl2については、0.05〜50mM(より好ましくは0.1〜10mM)、NaHCO3については0.01〜50mM(より好ましくは、0.1〜5mM)とすることもできる。
【0033】
ここで、KCl、MgCl2、NaHCO3の量が前記した下限値より小さくなると、これらが有効に淡水性発光細菌に作用せず、発光量が下がる。また、KCl、MgCl2、NaHCO3が前記した上限値を超えると、細胞膜に対する浸透圧が高まり、淡水性発光細菌が弱り、発光量が下がる。マグネシウムイオンが過剰であると、淡水性発光細菌に対して毒性がある。炭酸水素ナトリウムが過剰であると、培地液がアルカリ性となる。更に、培地液のpHは3〜8に調整する必要があるが、3成分のみでこのpH範囲に入る。
【0034】
次に、以上の実験に使用したKCl、MgCl2・6H2O、NaHCO3について、更にそのうち、どの成分が有効にフォトラブドゥス・ルミネセンスの発光量に寄与しているかと、それらの成分の適正量を実験を行って調査した。
【0035】
まず、図8に示すように、MgCl2・6H2O( 4.8g/L)、NaHCO3(0.11g/L)は一定にして、かつMgSO4は使用しないで、KClの濃度を変えた場合のKClの濃度と発光量との関係を調べた。実験によると、K+の濃度が微小でもフォトラブドゥス・ルミネセンスの発光性に寄与し、0.001〜1.5g/L(KCl換算で0.0019〜3.62g/L)で発光性が認められた。なお、好ましくはK+の濃度が0.01〜1g/Lある場合、より発光量が増加することが確認されている。
【0036】
そして、KCl、MgCl2・6H2O、NaHCO3 のうち、Mg2+の濃度を変えて、フォトラブドゥス・ルミネセンスの発光量を調査した結果を図9に示す。Mg2+が、0.1〜1g/L(MgCl2・6H2Oに換算すると、0.69〜6.9g/L)の範囲で十分な発光量がある。なお、Mg2+ 濃度が0.86g/L以上では、発光量がやや低下するが1g/L以下であれば使用可能であることが分かった。
【0037】
次に、Mg2+源として、MgCl2 とMgSO4を用いた場合の、濃度と発光量との関係を図10に示す。図10に示すように、MgCl2が5.74g/L(Mg2+換算で、2.3g/L)の場合は、発光量が落ちている。また、MgSO4が同じく5.74g/L(Mg2+換算で1.15g/L)でも発光量が落ちている。なお、同一Mg2+量であっても、硫酸イオンの方が発光量は低い。従って、Mg+イオンが過剰にあるとフォトラブドゥス・ルミネセンスの発光量は減少するものと思慮される。
【0038】
図11には、NaHCO3の量を変えた場合のフォトラブドゥス・ルミネセンスの発光量の変化を示すが、HCO3−が低濃度(0.008〜0.1g/L、より好ましくは、0.05〜0.1g/L)では高い発光を示すが、HCO3−が高濃度(0.12g/L以上)では発光誘導を示さなかった。溶液のpHの影響ではなく、HCO3−の濃度に依存して発光している。
【0039】
図12(A)には、K+イオンに換算して0.4g/Lとして、カリウム源をKNO3、KBr、KHCO3にした場合のフォトラブドゥス・ルミネセンスの発光量を測定した結果を示す。この結果から、K+イオンと結合する陰イオン成分は、NO3、Br等他の成分でもよいことが分かる。ここで、その他の成分については、ISS標準培地(なお、MgSO4・7H2Oは除去している)と同じである。
【0040】
なお、図12(A)において、KHCO3の場合は発光量が減っているが、これはK+イオンを基準とすると、HCO3−イオンが多すぎて、フォトラブドゥス・ルミネセンスに対して発光量を阻外する成分となるからである。ここで、K+イオンの量は低くても発光性があるので、HCO3−イオンを適正値(例えば、0.12g/L未満)とすることによって、フォトラブドゥス・ルミネセンスの発光量は増加する。ここで、ネガティブ(Negative)は、これらのイオンを含まないこと(即ち、ISS標準培地ではない)を意味し、ポジティブ(Positive)はISS標準培地液であることを示す。
【0041】
図12(B)は、他の成分については、ISS標準培地と同一にして、Mg2+と対となる陰イオンの成分を変えた場合の、フォトラブドゥス・ルミネセンスの発光量を示すが、Mg2+と対となる陰イオンが変わった場合、MgBr2、Mg(CH3COO)2、MgKCl3でも高い発光量を示す。
【0042】
図12(C)は、HCO3−イオンについて、対となる陽イオンの成分を変えた場合の、フォトラブドゥス・ルミネセンスの発光量を示すが、陽イオンの種類が変わっても、フォトラブドゥス・ルミネセンスの発光性が維持されることが分かる(例えば、NH4HCO3、KHCO3)。
従って、以上の実験から、フォトラブドゥス・ルミネセンスの細胞密度非依存型の発光誘導においては、K+、Mg2+、HCO3−が必要であることが分かる。
【0043】
淡水性発光細菌を用いた毒性試験を行う場合は、試験液として以上で説明した淡水性発光細菌の培地液(カリウムイオン源、マグネシウムイオン源、炭酸水素イオン源を含む)に淡水性発光細菌を含ませて、淡水性発光細菌の発光強度を増加させて、適当濃度に希釈した試験対象物(例えば、重金属類)を入れ、発光度を測定することによって、試験対象物の毒性が検査できる。この場合、塩分を必要としないこと、pH範囲が広いことから、試験対象物の適用範囲が広がることになる。また、この培地液に適当量の栄養源(例えば、NB)を入れることもできる。
【0044】
続いて、本発明の一実施の形態に係るバイオセンサーについて図13、図14を参照しながら説明する。
図13に示すような、透明の容器の一例である試験管20を用意し、その内側底部に担持膜21を形成する。この担持膜21にはこの実施の形態ではフィブロイン膜を使用しているが、アルギン酸、寒天、ゼラチン又は他の有機性又は無機性の担持膜(多孔性及び粘性を有するもの)を使用することができる。
【0045】
次に、市販のNB液に、KCl、MgCl2・6H2O、NaHCO3を入れて、カリウムイオンを0.001〜1.5g/L(より好ましくは、0.1〜0.8g/L)、マグネウシムイオンを0.1〜1g/L(より好ましくは、0.06〜0.57g/L)、及び炭酸水素イオンを0.05〜0.1g/L(より好ましくは、0.008〜0.08g/L)含むようにした培地液を作り、これにフォトラブドゥス・ルミネセンス(淡水性発光細菌の一例)を少量入れて、温度30℃、攪拌速度70rpm、20時間保持し、フォトラブドゥス・ルミネセンスを一定濃度含むフォトラブドゥス・ルミネセンス試験液(培養液)を作る。
【0046】
このフォトラブドゥス・ルミネセンス試験液2mLを試験管20に入れて、温度30℃で、そのまま3時間放置し、フォトラブドゥス・ルミネセンス試験液を担持膜21に含ませる。この後、イオン交換水2mLで3回洗浄し、水分をキムワイプ(紙製のウエス)で拭き無水処理を行う。これによってバイオセンサー22が完成する。なお、保存する場合は、−30℃以下の冷凍庫に保存する。
【0047】
このバイオセンサー22を使用する場合は、バイオセンサー22を常温(約30℃)に戻した後、対象となる被検査液を入れて、一定時間保持することによって行う。このバイオセンサー22の作用を確認するために、図14(A)に示すように、HgCl2(重金属の一例であるHgイオンを含む)を100ppm、10ppm、1ppm、0.1ppm含む液(2mL)を試験した。そして、5分後と15分後の発光度をルミノメータで確認したが、水銀イオンの検知ができることが分かる。
【0048】
次に、図14(B)に示すように、NiCl2(重金属の一例であるNiイオンを含む)を10000ppm、1000ppm、100ppm、10ppm含む液(2mL)を試験した。そして、5分後と15分後の発光度をルミノメータで確認したが、Niイオンの検知ができることが分かる
【0049】
図15(A)は、同一のバイオセンサー22を用いて、BODの毒性評価を行った結果を示す。まずは、D(+)−グルコース:150mg/L、L−グルタミン酸:150mg/L含み、BODが220±10mg/L含まれているGGA標準液を用いて、濃度と時間(5分と15分)を変えた場合の発光量を確認した。なお、図15(B)に示すように、GGAの濃度を110ppm〜2200ppmとすると、GGAの濃度に比例してフォトラブドゥス・ルミネセンスの発光量が変わる。従って、このバイオセンサー22で、100〜2000ppmのBODの検出がより正確に測定できることかわかる。
【0050】
次に、ニトロフミン酸:4.246mg/L、タンニン酸:4.175mg/L、リグニルスルホン酸ナトリウム:2.427mg/L、アラビアゴム:4.695mg/L、直鎖型アルキルベンゼンスルホン酸:0.942mg/L含み、BODが3.77mg/LのAWW標準液を用いて、バイオセンサー22の作用効果を実験した例を図16に示す。これよっても、フォトラブドゥス・ルミネセンスの発光量が濃度によって異なり、BODの検査にバイオセンサー22が適用できることが分かる。
【0051】
本発明は前記した実施の形態に限定されるものではなく、本発明の要旨を変更しない範囲でその構成を変更することもできる。例えば、淡水性発光細菌として、フォトラブドゥス・ルミネセンス以外の淡水性発光細菌を使用することもできる。
前記実施の形態においては、透明の容器として試験管を用いたが、透光性を有する他の容器(例えば、アンプル等)によって代用できる。
【符号の説明】
【0052】
20:試験管、21:担持膜、22:バイオセンサー
【技術分野】
【0001】
本発明は、淡水性発光細菌(例えば、フォトラブドゥス・ルミネセンス、Photorhabdus luminescens)の発光増大に対して、NH4+、PO3−が負の影響を、K+、Mg2+、Na+、H+、CO32−が正の影響を与えることを見いだし、一般的培地(例えば、Nutrient Broth)を用いて、又はこれらの培地無しで、淡水性発光細菌を発光させる淡水性発光細菌の培地液及びこれらを用いた毒性検査方法並びに毒性検査具(バイオセンサー)に関する。
【背景技術】
【0002】
発光細菌は生物発光を行う細菌のことをいい、迅速簡便な毒性評価等のバイオアッセイ(生物検定や生物学的試験)やバイオセンサーに利用され、比較的容易に発光量を高めることが可能なことから、一般には海洋性のビブリオ・フィシェリ(Vibrio fischeri)等が広く使用されている。なお、発光細菌は以上の毒性評価の他、FMN又はFAD(P)Hを軸とする酵素系の定量、ATPの測定にも応用されている。
【0003】
このビブリオ・フィシェリの培養方法としては、ニュトリエントブロス(Nutrient Broth3%NaClを含む)、マリンブロス(Marine Broth)等の栄養の富んだ液体培地が使用されている。これは、生物発光に、培地の栄養が富んだ状態で菌数が高密度に増殖した場合により強い発光が現れるクオラムセンシング(quorum sensing)が関与しているからである。
特許文献1には、このような目的に使用される発光細菌(ビブリオ・フィシェリ、フォトバクテリウム・レイオグナチ、フォトバクテリウム・フォスフォレウム、フォトラブドゥス・ルミネセンス)が開示されている。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2003−310297号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
特許文献1は、効果のクロマトグラフィーによる検出の実用についての従来技術の限界を克服する生物活性物質を検出するための方法及びキットを提供することを目的としており、更に、使用する培地として、ジペプチド、オリゴペプチド、ホウ酸ジエステル等FFのホウ素化合物、キノロン又はN−アシルホモセリンラクトンあるいはそれらの生化学的前駆物質が使用されており、本願発明とは課題が異なると共に、使用する物質についても異なる。更に、特許文献1では、確かにフォトラブドゥス・ルミネセンスの記載はあるが、実施の好適な態様においては、海洋性の発光細菌であるビブリオ・フィシェリが使用されており、淡水性の発光細菌や、この一例であるフォトラブドゥス・ルミネセンスについての具体的な記載はない。
【0006】
更に、ビブリオ・フィシェリは、生育pH範囲が狭いこと、海洋性であるので2〜3質量%の塩分(NaCl)を必要とし、測定する物質の状態(即ち、工場排水等の淡水性の場合)によって、正確な毒性評価が困難であるとういう問題がある。一方、フォトラブドゥス・ルミネセンス等の淡水性発光細菌は、生育に塩分は必要とせず、取り扱いが容易であるものの、発光量がやや低いことに起因して一般にはバイオセンサーの開発は行われていない。また、フォトラブドゥス・ルミネセンス等で代表される淡水性発光バクテリアの実験を種々行った結果、菌濃度の増加は必ずしも発光性の増大に繋がるものではなく、十分な菌濃度が得られても発光強度が低い場合があることや、逆に菌濃度は低くても培養液の状態によっては、発光強度が高い場合があることを知見して、本発明を完成した。
【0007】
本発明は、かかる事情に鑑みてなされたもので、塩分を必要とせず、生育pH範囲が広い淡水性発光細菌に注目し、その発光強度を制御する培地液及びこれらを用いた毒性検査方法並びにバイオセンサーを提供することを目的とする。
【課題を解決するための手段】
【0008】
第1の発明に係る淡水性発光細菌の培地液は、淡水性発光細菌の発光強度を増加させる培地液であって、水溶液中に、カリウムイオンを0.001〜1.5g/L、マグネウシムイオンを0.1〜1g/L、及び炭酸水素イオンを0.05〜0.1g/L含む。
【0009】
第1の発明に係る淡水性発光細菌の培地液において、1)前記カリウムイオン源は塩化カリウム、臭化カリウム、及び硝酸カリウムのいずれか1又は2以上、2)前記マグネシウムイオン源は塩化マグネシウム、臭化マグネシウム、酢酸マグネシウム、及び三塩化カリウムマグネシウムのいずれか1又は2以上、3)前記炭酸水素イオン源は炭酸水素ナトリウム、炭酸水素アンモニウム、及び炭酸水素カリウムのいずれか1又は2以上を使用するのが一般的であるが、淡水性発光細菌に害を有されない化合物であれば、他の化合物であってもよい。なお、カリウムイオン源として、KHCO3を使用すると、カリウムイオンが適正値であっても、炭酸水素イオンが規定値をオーバーする場合は、発光量が低下する。また、淡水性発光細菌に対して毒性を有する他の化合物を混合しないことは当然である。
【0010】
また、本発明の第2の発明に係る淡水性発光細菌の培地液は、淡水性発光細菌の発光強度を増加させる培地液であって、1000mLの水溶液中に、カリウムイオンを0.05〜50mM、マグネウシムイオンを0.05〜50mM、ナトリウムイオン及び炭酸水素イオンをそれぞれ0.01〜50mM含み、pHが3〜8の範囲にある。なお、1000mLの水溶液中に、カリウムイオンを0.05〜50mMは、0.002g〜2g/Lを、マグネウシムイオンを0.05〜50mMは0.0012〜1.2g/Lを、ナトリウムイオン及び炭酸水素イオンをそれぞれ0.01〜50mMは、0.0023〜1.2g/L(Na+)、0.00062〜3.1g/L(HCO3−)をいう。
【0011】
第2の発明に係る淡水性発光細菌の培地液において、前記カリウムイオン源は塩化カリウム、前記マグネシウムイオン源は塩化マグネシウム、前記炭酸水素イオン源は、炭酸水素ナトリウムを用いるのが好ましいが、淡水性発光細菌に害を有されない化合物であれば、他の化合物であってもよい。
【0012】
第1、第2の発明に係る淡水性発光細菌の培地液において、前記水溶液には前記淡水性発光細菌の栄養源(例えば、Nutrient broth)が添加されているのが好ましい。これによって、淡水性発光細菌は菌数を保持又は増加させることができる。
【0013】
第1、第2の発明に係る淡水性発光細菌の培地液において、前記淡水性発光細菌はフォトラブドゥス・ルミネセンスであるのが好ましいが、他の淡水性発光細菌であってもよい。
【0014】
そして、第3の発明に係る淡水性発光細菌を用いた毒性検査方法は、第1、第2の発明に係る淡水性発光細菌の培地液に淡水性発光細菌を含ませて、該淡水性発光細菌の発光強度を増加させて、試験対象物の試験液として使用する。この毒性検査方法は、比較的安価で容易に入手できる化合物を用いて、培地液を構成でき、しかも、この培地液を用いて淡水性発光細菌の発光強度を高めることができる。更に、淡水性発光細菌は、海洋性発光細菌とは異なり、塩分(NaCl)を必要とせず、pH範囲も広いので、より多くの試験対象物に対応でき、毒性試験の対象物を広げることができる。
【0015】
第4の発明に係るバイオセンサーは、第1の発明に係る淡水性発光細菌の培地液に、淡水性発光細菌及び栄養源を加えて、前記淡水性発光細菌を培養した培養液を、透明容器の内側に設けられた担持膜に含ませ無水処理を行っている。
また、第5の発明に係るバイオセンサーは、淡水性発光細菌が担持された担持膜を透明容器の内側底部に設けて構成されている。
【0016】
第4、第5の発明に係るバイオセンサーにおいて、前記担持膜はフィブロイン、アルギン酸、寒天、ゼラチン、又はその他の多孔性で粘性を有する物質からなるのが好ましい。
なお、バイオセンサーの用途としては、例えば淡水での重金属量(例えば、水銀、ニッケル等)又は淡水でのBODの測定に利用できる。
【発明の効果】
【0017】
第1、第2の発明に係る淡水性発光細菌の培地液及びこれを用いた第3の発明に係る毒性検査方法並び第4、第5の発明に係るバイオセンサーは、比較的安価で容易に入手できる化合物を用いて、培地液を構成でき、しかも、この培地液を用いて淡水性発光細菌の発光強度を高めることができる。
更に、淡水性発光細菌は、海洋性発光細菌とは異なり、塩分(NaCl)を必要とせず、pH範囲も広いので、第3の発明に係る毒性検査方法及び第4、第5の発明に係るバイオセンサーは、工場排水や下水処理場等、より多くの試験対象物に対応でき、毒性試験の対象物を広げることができる。
【0018】
特に、第1の発明に係る淡水性発光細菌の培地液において、1)カリウムイオン源は塩化カリウム、臭化カリウム、及び硝酸カリウムのいずれか1又は2以上、2)マグネシウムイオン源は塩化マグネシウム、臭化マグネシウム、酢酸マグネシウム、及び三塩化カリウムマグネシウムのいずれか1又は2以上、3)炭酸水素イオン源は炭酸水素ナトリウム、炭酸水素アンモニウム、及び炭酸水素カリウムのいずれか1又は2以上を使用した場合には、比較的安価に淡水性発光細菌の培地液を製造することができる。
【図面の簡単な説明】
【0019】
【図1】(A)、(B)はそれぞれ培地液の5つの成分のうち1を欠如させた場合の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図2】(A)、(B)はそれぞれ培地液の5つの成分のうち2を欠如させた場合の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図3】(A)、(B)はそれぞれ培地液の5つの成分のうち3を欠如させた場合の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図4】(A)、(B)はそれぞれ培地液の5つの成分の各々の淡水性発光細菌の菌体量と発光量を示すグラフである。
【図5】(A)、(B)、(C)はそれぞれNB培地液を用いた場合の菌体量、発光量、細胞1個当たりの発光量の推移を示すグラフである。
【図6】(A)、(B)、(C)はそれぞれ3エレメント(KCl:0.77g/L、NaHCO3:0.11g/L、MgCl2・6H2O:4.8g/L)の培地液を用いた場合の菌体量、発光量、細胞1個当たりの発光量の推移を示すグラフである。
【図7】(A)、(B)、(C)はそれぞれ更にNBを加えた培地液を用いた場合の菌体量、発光量、細胞1個当たりの発光量の推移を示すグラフである。
【図8】K+の濃度と発光量との関係を示すグラフである。
【図9】Mg2+濃度と発光量との関係を示すグラフである。
【図10】マグネシウム化合物の濃度と発光量の関係を示すグラフである。
【図11】HCO3−濃度と発光量の関係を示すグラフである。
【図12】(A)〜(C)はそれぞれK、Mg、HCO3化合物の種類と発光量との関係を示すグラフである。
【図13】バイオセンサーの説明図である。
【図14】(A)、(B)はそれぞれバイオセンサーの毒性評価を示すグラフである。
【図15】(A)、(B)はそれぞれバイオセンサーのBOD検査評価を示すグラフである。
【図16】バイオセンサーのBOD検査評価を示すグラフである。
【発明を実施するための形態】
【0020】
続いて、添付した図面を参照しながら、本発明を具体化した実施の形態について説明する。
本発明者らは、先に出願した特願2010−268623号において海洋性発光バクテリアの発光制御方法で、海水に含まれるNaCl、KCl、CaCl2、MgCl2・6H2O、NaHCO3、MgSO4・7H2Oについて如何なる成分が発光性に寄与するかを実験して調べた。しかしながら、海洋性発光バクテリアは前述のように、塩分(NaCl)を必須の成分とし、生存するpH範囲が狭いので、実施上支障がある場合があり、塩分を必要としない淡水性発光バクテリアに注目し、如何なる成分が淡水性発光バクテリアの発光度に寄与するかを研究した。
【0021】
実験に当たっては、海水に含まれる成分を参照して選んだ結果、淡水であることから塩分(NaCl)を除く、1)KCl、2)CaCl2、3)MgCl2・6H2O、4)NaHCO3、5)MgSO4・7H2Oの5成分が有効であると推定し、更にこの中でどの成分が淡水性発光バクテリア(細菌)の発光に寄与するかを実験した。
【0022】
この実験液には、1)KClを0.77g/L(10.3mM)、2)CaCl2を1.21g/L(10.9mM)、3)MgCl2・6H2Oを4.8g/L(23.6mM)、4)NaHCO3を0.11g/L(1.3mM)、5)MgSO4・7H2Oを3.50g/L(14.2mM)をそれぞれ単位として、これらの1〜5を欠如させて、欠如させた培地(培地液に同じ)における淡水性発光細菌の菌体量(菌の数)と発光量を測定した。なお、培養時間は18時間とし、以下の実験においては、淡水性発光細菌として、フォトラブドゥス・ルミネセンスを用い、菌体量として、液の濁り(OD)を測定し、発光量については、5分間の積算値で1mL中の発光量をルミノメータで測定した。なお、ここで、「mM」は水1Lに対するモル数を示す。
【0023】
なお、1)KClを0.77g/Lは、K+イオンに換算して0.4g/L、2)MgCl2・6H2Oの4.8gは、Mg2+イオンに換算して0.6g/L、3)NaHCO3の0.11g/LはHCO3−に換算して0.08g/L、4)MgSO4・7H2Oの3.5g/LはMg2+イオンに換算して0.3g/Lとなる(以下、この溶液を「ISS培地」という)。
【0024】
図1(A)、(B)は5成分の1を欠如させたもので、いずれもバクテリアの増殖はみられないが、(3)のNaHCO3欠如、(4)のMgCl2欠如、(6)のKCl欠如のものでは、発光量が他のものより減少していることが判る。
【0025】
図2(A)、(B)は5成分の2を欠如させたもの(即ち、3成分)で、いずれもバクテリアの増殖はみられないが、(4)のKCl、MgCl2・6H2O、NaHCO3を含むものについては、発光量が他のものより多いことが判る。
【0026】
図3(A)、(B)は5成分の3を欠如させたもの(即ち、2成分)で、いずれもバクテリアの増殖はみられない。また、発光量も(1)の全てを含むものに対して、いずれもかなり低くなっている。
【0027】
図4(A)、(B)は5成分の4を欠如させたもの(即ち、1成分)で、いずれもバクテリアの増殖はみられない。また、発光量も(1)の全てを含むものに対して、いずれもかなり低くなっている。
【0028】
図5(A)、(B)、(C)は市販のNB培地(Nutrient broth)を用いて、菌体量、発光量、細胞1個当たりの発光量の時間的推移を詳細に測定したものである。菌体量の増加に伴って、クオラムセンシングにより一時(例えば10〜20時間)は発光量と細胞(菌)の1個当たりの発光量の増加が認められるが、その後は発光量が減少し、その発光量の増加に対して細胞(菌)の1個当たりの発光量が減少していることが判る。
【0029】
図6(A)、(B)、(C)は、KCl(0.77g/L)、MgCl2・6H2O(4.8g/L)、NaHCO3(0.11g/L)のみを培地に溶解させたものを用いて、菌体量、発光量、細胞1個当たりの発光量の時間的推移を測定したものであるが、栄養素が培地にないので、菌体量の増加はない。発光量は15時間経過後位から増加し、細胞1個当たりの発光量も増加している。以上の実験から、フォトラブドゥス・ルミネセンスは栄養源がなく、従って菌体量の増加がない場合であっても、少量のKCl、MgCl2、NaHCO3 が存在すれば、発光することが分かる。
【0030】
図7(A)、(B)、(C)はそれぞれNB培地の場合と、NB培地に更にKCl(0.77g/L)、MgCl2・6H2O( 4.8g/L)、NaHCO3(0.11g/L)を加えた場合との菌体量、発光量、及び細胞1個当たりの発光量の時間的変化を示すが、NB培地に更にKCl(0.77g/L)、MgCl2・6H2O( 4.8g/L)、NaHCO3(0.11g/L)を加えた場合(即ち、栄養源に3エレメントが添加されている場合)の方が、発光量が増すことが判る。
【0031】
以上の実験から以下のことが判る。
(1)カリウムイオン源となるKCl、マグネシウムイオン源となるMgCl2、ナトリウムイオン源及び炭酸水素イオン源となるNaHCO3が欠乏すると、発光量が低下する。
(2)KCl、MgCl2、NaHCO3の3成分で、5成分(KCl、CaCl2、MgCl2、NaHCO3、MgSO4)の発光量と同程度の発光量がある。
(3)NB培地に3成分(KCl、MgCl2、NaHCO3)を添加することによって菌体量、発光量、細胞1つ当たりの発光量が増加する。
(4)以上のことから、3成分(KCl、MgCl2、NaHCO3)が淡水性発光細菌の発光ファクターであるのが判る。なお、この実験では、NaHCO3を使っているので、ナトリウムイオン及び炭酸水素ナトリウムのイオンのいずれか、又は双方が必要であるかについては分からない。
【0032】
上の実験において、カリウムイオン源、マグネシウムイオン源、ナトリウムイオン源、炭酸水素イオン源として、1)KClを0.77g/L(10.3mM)、2)MgCl2・6H2Oを4.8g/L(23.6mM)、3)NaHCO3を0.11g/L(1.3mM)としたが、KClについては、0.05〜50mM(より好ましくは、0.1〜10mM)、MgCl2については、0.05〜50mM(より好ましくは0.1〜10mM)、NaHCO3については0.01〜50mM(より好ましくは、0.1〜5mM)とすることもできる。
【0033】
ここで、KCl、MgCl2、NaHCO3の量が前記した下限値より小さくなると、これらが有効に淡水性発光細菌に作用せず、発光量が下がる。また、KCl、MgCl2、NaHCO3が前記した上限値を超えると、細胞膜に対する浸透圧が高まり、淡水性発光細菌が弱り、発光量が下がる。マグネシウムイオンが過剰であると、淡水性発光細菌に対して毒性がある。炭酸水素ナトリウムが過剰であると、培地液がアルカリ性となる。更に、培地液のpHは3〜8に調整する必要があるが、3成分のみでこのpH範囲に入る。
【0034】
次に、以上の実験に使用したKCl、MgCl2・6H2O、NaHCO3について、更にそのうち、どの成分が有効にフォトラブドゥス・ルミネセンスの発光量に寄与しているかと、それらの成分の適正量を実験を行って調査した。
【0035】
まず、図8に示すように、MgCl2・6H2O( 4.8g/L)、NaHCO3(0.11g/L)は一定にして、かつMgSO4は使用しないで、KClの濃度を変えた場合のKClの濃度と発光量との関係を調べた。実験によると、K+の濃度が微小でもフォトラブドゥス・ルミネセンスの発光性に寄与し、0.001〜1.5g/L(KCl換算で0.0019〜3.62g/L)で発光性が認められた。なお、好ましくはK+の濃度が0.01〜1g/Lある場合、より発光量が増加することが確認されている。
【0036】
そして、KCl、MgCl2・6H2O、NaHCO3 のうち、Mg2+の濃度を変えて、フォトラブドゥス・ルミネセンスの発光量を調査した結果を図9に示す。Mg2+が、0.1〜1g/L(MgCl2・6H2Oに換算すると、0.69〜6.9g/L)の範囲で十分な発光量がある。なお、Mg2+ 濃度が0.86g/L以上では、発光量がやや低下するが1g/L以下であれば使用可能であることが分かった。
【0037】
次に、Mg2+源として、MgCl2 とMgSO4を用いた場合の、濃度と発光量との関係を図10に示す。図10に示すように、MgCl2が5.74g/L(Mg2+換算で、2.3g/L)の場合は、発光量が落ちている。また、MgSO4が同じく5.74g/L(Mg2+換算で1.15g/L)でも発光量が落ちている。なお、同一Mg2+量であっても、硫酸イオンの方が発光量は低い。従って、Mg+イオンが過剰にあるとフォトラブドゥス・ルミネセンスの発光量は減少するものと思慮される。
【0038】
図11には、NaHCO3の量を変えた場合のフォトラブドゥス・ルミネセンスの発光量の変化を示すが、HCO3−が低濃度(0.008〜0.1g/L、より好ましくは、0.05〜0.1g/L)では高い発光を示すが、HCO3−が高濃度(0.12g/L以上)では発光誘導を示さなかった。溶液のpHの影響ではなく、HCO3−の濃度に依存して発光している。
【0039】
図12(A)には、K+イオンに換算して0.4g/Lとして、カリウム源をKNO3、KBr、KHCO3にした場合のフォトラブドゥス・ルミネセンスの発光量を測定した結果を示す。この結果から、K+イオンと結合する陰イオン成分は、NO3、Br等他の成分でもよいことが分かる。ここで、その他の成分については、ISS標準培地(なお、MgSO4・7H2Oは除去している)と同じである。
【0040】
なお、図12(A)において、KHCO3の場合は発光量が減っているが、これはK+イオンを基準とすると、HCO3−イオンが多すぎて、フォトラブドゥス・ルミネセンスに対して発光量を阻外する成分となるからである。ここで、K+イオンの量は低くても発光性があるので、HCO3−イオンを適正値(例えば、0.12g/L未満)とすることによって、フォトラブドゥス・ルミネセンスの発光量は増加する。ここで、ネガティブ(Negative)は、これらのイオンを含まないこと(即ち、ISS標準培地ではない)を意味し、ポジティブ(Positive)はISS標準培地液であることを示す。
【0041】
図12(B)は、他の成分については、ISS標準培地と同一にして、Mg2+と対となる陰イオンの成分を変えた場合の、フォトラブドゥス・ルミネセンスの発光量を示すが、Mg2+と対となる陰イオンが変わった場合、MgBr2、Mg(CH3COO)2、MgKCl3でも高い発光量を示す。
【0042】
図12(C)は、HCO3−イオンについて、対となる陽イオンの成分を変えた場合の、フォトラブドゥス・ルミネセンスの発光量を示すが、陽イオンの種類が変わっても、フォトラブドゥス・ルミネセンスの発光性が維持されることが分かる(例えば、NH4HCO3、KHCO3)。
従って、以上の実験から、フォトラブドゥス・ルミネセンスの細胞密度非依存型の発光誘導においては、K+、Mg2+、HCO3−が必要であることが分かる。
【0043】
淡水性発光細菌を用いた毒性試験を行う場合は、試験液として以上で説明した淡水性発光細菌の培地液(カリウムイオン源、マグネシウムイオン源、炭酸水素イオン源を含む)に淡水性発光細菌を含ませて、淡水性発光細菌の発光強度を増加させて、適当濃度に希釈した試験対象物(例えば、重金属類)を入れ、発光度を測定することによって、試験対象物の毒性が検査できる。この場合、塩分を必要としないこと、pH範囲が広いことから、試験対象物の適用範囲が広がることになる。また、この培地液に適当量の栄養源(例えば、NB)を入れることもできる。
【0044】
続いて、本発明の一実施の形態に係るバイオセンサーについて図13、図14を参照しながら説明する。
図13に示すような、透明の容器の一例である試験管20を用意し、その内側底部に担持膜21を形成する。この担持膜21にはこの実施の形態ではフィブロイン膜を使用しているが、アルギン酸、寒天、ゼラチン又は他の有機性又は無機性の担持膜(多孔性及び粘性を有するもの)を使用することができる。
【0045】
次に、市販のNB液に、KCl、MgCl2・6H2O、NaHCO3を入れて、カリウムイオンを0.001〜1.5g/L(より好ましくは、0.1〜0.8g/L)、マグネウシムイオンを0.1〜1g/L(より好ましくは、0.06〜0.57g/L)、及び炭酸水素イオンを0.05〜0.1g/L(より好ましくは、0.008〜0.08g/L)含むようにした培地液を作り、これにフォトラブドゥス・ルミネセンス(淡水性発光細菌の一例)を少量入れて、温度30℃、攪拌速度70rpm、20時間保持し、フォトラブドゥス・ルミネセンスを一定濃度含むフォトラブドゥス・ルミネセンス試験液(培養液)を作る。
【0046】
このフォトラブドゥス・ルミネセンス試験液2mLを試験管20に入れて、温度30℃で、そのまま3時間放置し、フォトラブドゥス・ルミネセンス試験液を担持膜21に含ませる。この後、イオン交換水2mLで3回洗浄し、水分をキムワイプ(紙製のウエス)で拭き無水処理を行う。これによってバイオセンサー22が完成する。なお、保存する場合は、−30℃以下の冷凍庫に保存する。
【0047】
このバイオセンサー22を使用する場合は、バイオセンサー22を常温(約30℃)に戻した後、対象となる被検査液を入れて、一定時間保持することによって行う。このバイオセンサー22の作用を確認するために、図14(A)に示すように、HgCl2(重金属の一例であるHgイオンを含む)を100ppm、10ppm、1ppm、0.1ppm含む液(2mL)を試験した。そして、5分後と15分後の発光度をルミノメータで確認したが、水銀イオンの検知ができることが分かる。
【0048】
次に、図14(B)に示すように、NiCl2(重金属の一例であるNiイオンを含む)を10000ppm、1000ppm、100ppm、10ppm含む液(2mL)を試験した。そして、5分後と15分後の発光度をルミノメータで確認したが、Niイオンの検知ができることが分かる
【0049】
図15(A)は、同一のバイオセンサー22を用いて、BODの毒性評価を行った結果を示す。まずは、D(+)−グルコース:150mg/L、L−グルタミン酸:150mg/L含み、BODが220±10mg/L含まれているGGA標準液を用いて、濃度と時間(5分と15分)を変えた場合の発光量を確認した。なお、図15(B)に示すように、GGAの濃度を110ppm〜2200ppmとすると、GGAの濃度に比例してフォトラブドゥス・ルミネセンスの発光量が変わる。従って、このバイオセンサー22で、100〜2000ppmのBODの検出がより正確に測定できることかわかる。
【0050】
次に、ニトロフミン酸:4.246mg/L、タンニン酸:4.175mg/L、リグニルスルホン酸ナトリウム:2.427mg/L、アラビアゴム:4.695mg/L、直鎖型アルキルベンゼンスルホン酸:0.942mg/L含み、BODが3.77mg/LのAWW標準液を用いて、バイオセンサー22の作用効果を実験した例を図16に示す。これよっても、フォトラブドゥス・ルミネセンスの発光量が濃度によって異なり、BODの検査にバイオセンサー22が適用できることが分かる。
【0051】
本発明は前記した実施の形態に限定されるものではなく、本発明の要旨を変更しない範囲でその構成を変更することもできる。例えば、淡水性発光細菌として、フォトラブドゥス・ルミネセンス以外の淡水性発光細菌を使用することもできる。
前記実施の形態においては、透明の容器として試験管を用いたが、透光性を有する他の容器(例えば、アンプル等)によって代用できる。
【符号の説明】
【0052】
20:試験管、21:担持膜、22:バイオセンサー
【特許請求の範囲】
【請求項1】
淡水性発光細菌の発光強度を増加させる培地液であって、水溶液中に、カリウムイオンを0.001〜1.5g/L、マグネウシムイオンを0.1〜1g/L、及び炭酸水素イオンを0.05〜0.1g/L含むことを特徴とする淡水性発光細菌の培地液。
【請求項2】
請求項1記載の培地液において、1)前記カリウムイオン源は塩化カリウム、臭化カリウム、及び硝酸カリウムのいずれか1又は2以上、2)前記マグネシウムイオン源は塩化マグネシウム、臭化マグネシウム、酢酸マグネシウム、及び三塩化カリウムマグネシウムのいずれか1又は2以上、3)前記炭酸水素イオン源は炭酸水素ナトリウム、炭酸水素アンモニウム、及び炭酸水素カリウムのいずれか1又は2以上を使用することを特徴とする淡水性発光細菌の培地液。
【請求項3】
淡水性発光細菌の発光強度を増加させる培地液であって、1000mLの水溶液中に、カリウムイオンを0.05〜50mM、マグネウシムイオンを0.05〜50mM、ナトリウムイオン及び炭酸水素イオンをそれぞれ0.01〜50mM含み、pHが3〜8の範囲にあることを特徴とする淡水性発光細菌の培地液。
【請求項4】
請求項3記載の培地液において、前記カリウムイオン源は塩化カリウム、前記マグネシウムイオン源は塩化マグネシウム、前記ナトリウムイオン源と前記炭酸水素イオン源は、炭酸水素ナトリウムを用いることを特徴とする淡水性発光細菌の培地液。
【請求項5】
請求項1〜4のいずれか1記載の培地液において、前記水溶液には前記淡水性発光細菌の栄養源が添加されていることを特徴とする淡水性発光細菌の培地液。
【請求項6】
請求項1〜5のいずれか1記載の培地液において、前記淡水性発光細菌はフォトラブドゥス・ルミネセンスであることを特徴とする淡水性発光細菌の培地液。
【請求項7】
請求項1〜6のいずれか1記載の淡水性発光細菌の培地液に淡水性発光細菌を含ませて、該淡水性発光細菌の発光強度を増加させて、試験対象物の試験液として使用することを特徴とする淡水性発光細菌を用いた毒性検査方法。
【請求項8】
請求項1又は2記載の淡水性発光細菌の培地液に、淡水性発光細菌及び栄養源を加えて、前記淡水性発光細菌を培養した培養液を、透明容器の内側に設けられた担持膜に含ませ無水処理を行ったことを特徴とするバイオセンサー。
【請求項9】
淡水性発光細菌が担持された担持膜を透明容器の内側底部に設けたことを特徴とするバイオセンサー。
【請求項10】
請求項8又は9記載のバイオセンサーにおいて、前記担持膜はフィブロイン、アルギン酸、寒天、ゼラチン、又はその他の多孔性で粘性を有する物質からなることを特徴とするバイオセンサー。
【請求項1】
淡水性発光細菌の発光強度を増加させる培地液であって、水溶液中に、カリウムイオンを0.001〜1.5g/L、マグネウシムイオンを0.1〜1g/L、及び炭酸水素イオンを0.05〜0.1g/L含むことを特徴とする淡水性発光細菌の培地液。
【請求項2】
請求項1記載の培地液において、1)前記カリウムイオン源は塩化カリウム、臭化カリウム、及び硝酸カリウムのいずれか1又は2以上、2)前記マグネシウムイオン源は塩化マグネシウム、臭化マグネシウム、酢酸マグネシウム、及び三塩化カリウムマグネシウムのいずれか1又は2以上、3)前記炭酸水素イオン源は炭酸水素ナトリウム、炭酸水素アンモニウム、及び炭酸水素カリウムのいずれか1又は2以上を使用することを特徴とする淡水性発光細菌の培地液。
【請求項3】
淡水性発光細菌の発光強度を増加させる培地液であって、1000mLの水溶液中に、カリウムイオンを0.05〜50mM、マグネウシムイオンを0.05〜50mM、ナトリウムイオン及び炭酸水素イオンをそれぞれ0.01〜50mM含み、pHが3〜8の範囲にあることを特徴とする淡水性発光細菌の培地液。
【請求項4】
請求項3記載の培地液において、前記カリウムイオン源は塩化カリウム、前記マグネシウムイオン源は塩化マグネシウム、前記ナトリウムイオン源と前記炭酸水素イオン源は、炭酸水素ナトリウムを用いることを特徴とする淡水性発光細菌の培地液。
【請求項5】
請求項1〜4のいずれか1記載の培地液において、前記水溶液には前記淡水性発光細菌の栄養源が添加されていることを特徴とする淡水性発光細菌の培地液。
【請求項6】
請求項1〜5のいずれか1記載の培地液において、前記淡水性発光細菌はフォトラブドゥス・ルミネセンスであることを特徴とする淡水性発光細菌の培地液。
【請求項7】
請求項1〜6のいずれか1記載の淡水性発光細菌の培地液に淡水性発光細菌を含ませて、該淡水性発光細菌の発光強度を増加させて、試験対象物の試験液として使用することを特徴とする淡水性発光細菌を用いた毒性検査方法。
【請求項8】
請求項1又は2記載の淡水性発光細菌の培地液に、淡水性発光細菌及び栄養源を加えて、前記淡水性発光細菌を培養した培養液を、透明容器の内側に設けられた担持膜に含ませ無水処理を行ったことを特徴とするバイオセンサー。
【請求項9】
淡水性発光細菌が担持された担持膜を透明容器の内側底部に設けたことを特徴とするバイオセンサー。
【請求項10】
請求項8又は9記載のバイオセンサーにおいて、前記担持膜はフィブロイン、アルギン酸、寒天、ゼラチン、又はその他の多孔性で粘性を有する物質からなることを特徴とするバイオセンサー。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【公開番号】特開2013−9666(P2013−9666A)
【公開日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願番号】特願2012−118864(P2012−118864)
【出願日】平成24年5月24日(2012.5.24)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成22年12月4日 社団法人日本生物工学会主催の「第17回 日本生物工学会九州支部 沖縄大会 2010」において文書をもって発表
【出願人】(802000031)公益財団法人北九州産業学術推進機構 (187)
【Fターム(参考)】
【公開日】平成25年1月17日(2013.1.17)
【国際特許分類】
【出願日】平成24年5月24日(2012.5.24)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成22年12月4日 社団法人日本生物工学会主催の「第17回 日本生物工学会九州支部 沖縄大会 2010」において文書をもって発表
【出願人】(802000031)公益財団法人北九州産業学術推進機構 (187)
【Fターム(参考)】
[ Back to top ]

