測定装置、及び、測定プログラム
【課題】 不適当な測定排除して、効率よく生理活性物質と化合物との間の相互作用を測定する。
【解決手段】 ステップS10で、入力された測定条件と同じ測定条件のサンプルデータを抽出し、ステップS12で、抽出されたサンプルデータの各々の参照データG2に着目し、参照データG2が5RU以上の化合物が最も少ないサンプルデータSPを選択し、選択したサンプルデータSPの測定条件を、当該測定のための測定条件として決定する。
【解決手段】 ステップS10で、入力された測定条件と同じ測定条件のサンプルデータを抽出し、ステップS12で、抽出されたサンプルデータの各々の参照データG2に着目し、参照データG2が5RU以上の化合物が最も少ないサンプルデータSPを選択し、選択したサンプルデータSPの測定条件を、当該測定のための測定条件として決定する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、測定装置、及び、測定プログラムに関し、詳しくは、生理活性物質と所定の化合物との相互作用を測定する測定装置、及び、測定プログラムに関するものである。
【背景技術】
【0002】
生理活性物質と所定の化合物との相互作用を測定する装置として、様々なバイオセンサーが提案されている。そのうち、エバネッセント波を利用した測定装置の1つとして、表面プラズモンセンサーが知られている(特許文献1参照)。一般的に、表面プラズモンセンサーは、プリズムと、このプリズムの一面に配置された金属膜と、金属膜上に配置され生理活性物質が固定される固定化膜と、光ビームを発生させる光源と、光ビームをプリズムに対して、プリズムと金属膜との界面で全反射条件が得られるように種々の角度で入射させる光学系と、界面で全反射した光ビームの強度を検出する光検出手段と、を備え、光検出手段の検出結果に基づいて、生理活性物質についての測定を行なうものである。
【0003】
この表面プラズモンセンサーによる測定では、固定化膜の上に固定化された生理活性物質に対して化合物溶液を供給すると共に、金属膜の固定化膜が供給されている側と逆側の面へ光ビームを入射し、その反射光から得られる屈折率の情報に基づいて、生理活性物質と化合物溶液中の化合物との、相互作用が測定される。
【0004】
ところで、表面プラズモンセンサーによる測定では、生理活性物質が固定されている測定部とは別に、生理活性物質が固定されていない参照部を設け、参照部から得られる屈折率の情報で測定部の屈折率の情報を補正することが行われる。ここでの補正は、種類やその他の条件が異なることによる化合物と固定化膜との間の信号変化をキャンセルして、生理活性物質と化合物との間の特異的結合による信号変化のみを測定することが主な目的である。
【0005】
しかしながら、検討対象の化合物が、固定化膜へ大量に吸着(このような吸着を以下「非特異吸着」という)する場合には、生理活性物質と化合物との間の特異的結合が正確に測定されない可能性が高い。
【特許文献1】特許第3294605号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明は上記事実を考慮してなされたものであり、より適切な測定条件を用いて生理活性物質と化合物との間の相互作用を正確に測定する測定装置、及び、測定プログラムを提供することを目的とする。
【課題を解決するための手段】
【0007】
上記課題を解決するために、本発明の測定装置は、固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定する測定装置であって、前記参照データを測定条件及び前記化合物毎に記憶する記憶手段と、前記測定のための測定条件の一部を入力する測定条件入力手段と、前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定する測定条件決定手段と、前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定する測定手段と、前記測定手段により測定された相互作用に関する相互作用データを出力する出力手段と、前記測定手段により得られた参照データを前記測定の際の測定条件と共に前記記憶手段へ記憶させるフィードバック手段と、を備えている。
【0008】
また、本発明の測定プログラムは、固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定するための測定プログラムであって、前記参照データを測定条件及び前記化合物毎に記憶するステップと、前記測定のための測定条件の一部を入力するステップと、前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定するステップと、前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定するステップと、前記測定された相互作用に関する相互作用データを出力するステップと、前記測定により得られた参照データを前記測定の際の測定条件と共に記憶させるステップと、をコンピュータに実行させるものである。
【0009】
ここで、前記生理活性物質とは、日本工業規格(JIS)K3611中に「天然高分子」(記号11001〜11025)として記載されている各物質、生物学データ大百科事典(朝倉書店)中の「1.生体物質概論」に記載されている糖,アミノ酸、ヌクレオチド、脂質、ヘム、キノン、タンパク質、RNA,DNA、リン脂質、多糖、バイオサイエンス辞典(朝倉書店)中の「II.生物物質と代謝」に記載されているタンパク質、アミノ酸、核酸、脂質、糖質、酵素のうちのいずれか1つ以上を含むものを意味する。
【0010】
前記相互作用とは、物理的、化学的、もしくは生化学的な反応における、結合反応の速さ、結合量、または解離反応の速さ、あるいは、上記結合反応の速さ、結合量、および解離反応の速さのうちの2つ以上を組み合わせたものを意味するものである。
【0011】
生理活性物質の固定されている固定化膜と、生理活性物質の固定されていない固定化膜とでは、化合物の非特異吸着量が異なる。したがって、固定化膜への化合物の非特異吸着量が多い場合には、生理活性物質と化合物との相互作用を正しく測定できない可能性が高い。
【0012】
一方、固定化膜への化合物の非特異吸着量は、固定化膜の種類、バッファー液の種類、化合物の種類、化合物濃度、などの測定条件によって異なる。
【0013】
そこで、本発明では、測定のために測定条件の一部のみを入力し、入力された測定条件の一部に対応した参照データに着目する。そして、参照データに基づいて、固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定する。そして、決定された測定条件で生理活性物質と供給される化合物との間の相互作用を測定する。
【0014】
本発明では、非特異的吸着が少なくなるように測定条件が決定され、決定された測定条件で測定が行われるので、より適切な測定条件で正確に測定を行うことができる。
【0015】
また、本発明では、測定により得られた参照データを測定の際の測定条件と共に記憶させるので、測定毎に参照データが蓄積され、測定を重ねることにより多くの参照データに基づいて適切な測定を行うことができる。
【0016】
なお、本発明の測定装置は、前記固定化膜が金属膜上に形成され、前記測定手段が、前記金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、前記生理活性物質及び前記生理活性物質の固定された前記固定化膜と前記化合物との間の相互作用を測定すること、を特徴とすることもできる。
【0017】
また、本発明の測定プログラムは、前記測定が、片面に前記固定化膜の形成された金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、生理活性物質及び生理活性物質の固定された固定化膜と化合物との間の相互作用を測定するものであること、を特徴とすることもできる。
【0018】
上記のような測定としては、表面プラズモンセンサー、漏洩モードセンサによる測定がある。
【発明の効果】
【0019】
上記発明によれば、より適切な測定条件を用いて生理活性物質と化合物との間の相互作用を正確に測定することができる。
【発明を実施するための最良の形態】
【0020】
以下、図面を参照しながら本発明の実施形態について説明する。
【0021】
本実施形態の測定装置としてのバイオセンサー10は、金属膜の表面に発生する表面プラズモンを利用して、生理活性物質Dと化合物との相互作用路を測定する、いわゆる表面プラズモンセンサーである。
【0022】
図1に示すように、バイオセンサー10は、トレイ保持部12、搬送部14、容器載置台16、液体吸排部20、押さえ部26、光学測定部54、及び、制御部60を備えている。
【0023】
トレイ保持部12は、載置台12A、及び、ベルト12Bを含んで構成されている。載置台12Aは、矢印Y方向に架け渡されたベルト12Bに取り付けられており、ベルト12Bの回転により矢印Y方向に移動可能とされている。載置台12A上には、トレイTが2枚、位置決めして載置される。トレイTには、センサースティック40が8本収納されている。センサースティック40は、生理活性物質Dの固定されるチップであり、詳細については後述する。載置台12Aの下には、センサースティック40を後述するスティック保持部材14Cの位置まで押し上げる、押上機構12Dが配置されている。
【0024】
センサースティック40は、図2及び図3に示すように、誘電体ブロック42、流路部材44、保持部材46、接着部材48、及び、蒸発防止部材49、で構成されている。
【0025】
誘電体ブロック42は、光ビームに対して透明な透明樹脂等で構成されており、断面が台形の棒状とされたプリズム部42A、及び、プリズム部42Aの両端部にプリズム部42Aと一体的に形成された被保持部42Bを備えている。プリズム部42Aの互いに平行な2面の内の広い側の上面には、図4にも示すように金属膜50が形成されている。この金属膜50上に、バイオセンサー10で解析する生理活性物質Dが固定される。誘電体ブロック42は、いわゆるプリズムとして機能し、バイオセンサー10での測定の際には、プリズム部42Aの対向する互いに平行でない2つの側面の内の一方から光ビームが入射され、他方から金属膜50との界面で全反射された光ビームが出射される。
【0026】
金属膜50の表面には、図4に示すように、固定化膜50Aが形成されている。固定化膜50Aは、生理活性物質Dを金属膜50上に固定化するためのものである。固定化膜50Aは、固定する生理活性物質Dに応じて選択される。固定化膜50Aとしては、例えばアガロース、デキストラン、カラゲナン、アルギン酸、デンプン、セルロースなどのヒドロゲル、又はこれらの誘導体、例えばカルボキシメチル誘導体、又は水膨潤性有機ポリマー、例えばポリビニルアルコール、ポリアクリル酸、ポリアクリルアミド、ポリエチレングリコールなどを使用することができる。特に、ポリエチレングリコール誘導体、デキストラン誘導体は、生理活性維持の観点から好ましく用いられる。
【0027】
固定化膜50A上には、生理活性物質Dが固定された測定領域E1と、生理活性物質Dが固定されず、測定領域E1の信号測定に際しての参照信号を得るための参照領域E2とが形成される。この参照領域E2は、上述した固定化膜50Aを製膜する際に形成される。形成方法としては、例えば、固定化膜50Aに対して表面処理を施して、生理活性物質Dと結合する結合基を失活させる。これにより、固定化膜50Aの半分が測定領域E1となり、残りの半分が参照領域E2となる。
【0028】
図5にも示すように、液体流路45に露出された固定化膜50Aの、参照領域E2以外の部分には、生理活性物質Dが固定されている。参照領域E2には生理活性物質Dは固定されていない。参照領域E2、及び、参照領域E2よりも上流側に位置する測定領域E1には、各々光ビームL2、L1が入射される。参照領域E2は、生理活性物質Dの固定された測定領域E1から得られるデータを補正するために設けられた領域である。
【0029】
プリズム部42Aの両側面には、上側の端辺に沿って保持部材52と係合される係合凸部42Cが、下側の端辺に沿ってプリズム部42Aの上面と垂直な仮想面の延長上に構成される垂直凸部42Dが、各々7箇所に形成されている。また、誘電体ブロック42の下面の長手方向に沿った中央部には、係合溝42Eが形成されている。
【0030】
流路部材44は、誘電体ブロック42よりもわずかに狭幅の直方体状とされ、図3に示すように、誘電体ブロック42の金属膜50上に6個並べて配置されている。各々の流路部材44の下面には流路溝44Aが形成されており、上面に形成された供給口45A及び排出口45Bと連通されて、金属膜50との間に、液体流路45が構成される。したがって、1本のセンサースティック40には、独立した6個の液体流路45が構成される。流路部材44の側壁には、保持部材46の内側の図示しない凹部に圧入されて保持部材46との密着性を確保するための凸部44Bが形成されている。
【0031】
なお、液体流路45には、蛋白質を含む液体が供給されることが想定されるので、流路部材44への蛋白質の固着を防止するため、流路部材44の材料としては、蛋白質に対する非特異吸着性を有しないことが好ましい。
【0032】
保持部材46は、長尺とされ、上面板46A及び2枚の側面板46Bで構成されている。側面板46Bには、誘電体ブロック42の係合凸部42Cと係合される係合孔46Cが形成されている。保持部材46は、6個の流路部材44を間に挟んで係合孔46Cと係合凸部42Cとが係合されて、誘電体ブロック42に取り付けられる。これにより、流路部材44は、誘電体ブロック42に取り付けられる。上面板46Aには、流路部材44の供給口45A及び排出口45Bと対向する位置に、流路部材44に向けて狭くなるテーパー状のピペット挿入孔46Dが形成されている。また、隣り合うピペット挿入孔46Dとピペット挿入孔46Dとの間には、位置決め用のボス46Eが形成されている。
【0033】
保持部材46の上面には、蒸発防止部材49が接着部材48を介して接着されている。接着部材48のピペット挿入孔46Dと対向する位置にはピペット挿入用の孔48Dが形成され、ボス46Eと対向する位置には位置決め用の孔48Eが形成されている。また、蒸発防止部材49のピペット挿入孔46Dと対向する位置には十字状の切り込みであるスリット49Dが形成され、ボス46Eと対向する位置には位置決め用の孔49Eが形成されている。ボス46Eを孔48E及び49Eに挿通させて、蒸発防止部材49を保持部材52の上面に接着することにより、蒸発防止部材49のスリット49Dと流路部材44の供給口45A及び排出口45Bとが対向するように構成される。ピペットチップCPの非挿入時には、スリット49D部分が供給口45Bを覆い、液体流路45に供給されている液体の蒸発が防止される。
【0034】
図1に示すように、バイオセンサー10の搬送部14は、上部ガイドレール14A、下部ガイドレール14B、及び、スティック保持部材14C、を含んで構成されている。上部ガイドレール14A及び下部ガイドレール14Bは、トレイ保持部12及び光学測定部54の上部で、矢印Y方向と直交する矢印X方向に水平に配置されている。上部ガイドレール14Aには、スティック保持部材14Cが取り付けられている。スティック保持部材14Cは、センサースティック40の両端部の被保持部42Bを保持可能とされていると共に、上部ガイドレール14Aに沿って移動可能とされている。スティック保持部材14Cに保持されたセンサースティック40の係合溝42Eと下部ガイドレール14Bとが係合され、スティック保持部材14Cが矢印X方向に移動することにより、センサースティック40が光学測定部54上の測定部56に搬送される。また、測定部56には、測定時にセンサースティック40を押さえる押さえ部材58が備えられている。押さえ部材58は、図示しない駆動機構によりZ方向に移動可能とされ、測定部56に配置されたセンサースティック40を上側から押圧する。
【0035】
容器載置台16には、化合物溶液プレート17、バッファー液ストック容器18、廃棄液容器19が載置されている。化合物溶液プレート17は、96に区画されており、各種の化合物溶液をストック可能とされている。バッファー液ストック容器18は、容器18A〜18Eで構成されており、バッファー液がストックされている。容器18A〜18Eには、後述するピペットチップCPを挿入可能な開口Kが形成されている。バッファー液としては、例えば公知の緩衝溶液(化学便覧応用編改訂2版、1312頁〜1320頁)を基本に、食塩、界面活性剤(Tween20など)、金属イオン(マグネシウムイオン、カリウムイオン、カルシウムイオンなど)、安定化剤(DTTなど)などを添加したものを用いることができる。特に、PBSバッファー(リン酸バッファー生理食塩水)、Trisバッファー、HEPESバッファーなどが好ましく用いられる。
【0036】
廃棄液容器19は、複数の容器19A〜19Eで構成されており、容器18A〜18Eと同様にピペットチップCPを挿入可能な開口Kが形成されている。
【0037】
液体吸排部20は、上部ガイドレール14A、及び、ガイドレール16Bよりも上方で、矢印Y方向に架け渡された横断レール22、及び、ヘッド24を含んで構成されている。横断レール22は、図示しない駆動機構により、矢印X方向へ移動可能とされている。また、ヘッド24は、横断レール22に取り付けられ、矢印Y方向に移動可能とされている。また、ヘッド24は、図示しない駆動機構により、鉛直方向(矢印Z方向)にも移動可能とされている。ヘッド24は、図6に示すように、2本のピペット部24A、24Bを備えている。ピペット部24A、24Bには、先端部にピペットチップCPが取り付けられ、個々にZ方向の長さを調整可能とされている。ピペットチップCPは、図示しないピペットチップストッカーに多数ストックされており、必要に応じて交換可能とされている。
【0038】
なお、本実施形態においてはセンサースティック40への液体供給はピペットチップCPにより行われるが、ピペットチップの代わりに、一端が上記各溶液プレートに接続され、他端がセンサースティック40に接続可能とされたインジェクションチューブを設け、送液ポンプにより液体の供給を行ってもよい。
【0039】
光学測定部54は、図7に示すように、光源54A、第1光学系54B、第2光学系54C、受光部54D、信号処理部54E、を含んで構成されている。光源54Aからは、発散状態の光ビームLが出射される。光ビームLは、第1光学系54Bを介して、2本の光ビームL1、L2となり、測定部56に配置された誘電体ブロック42の測定領域E1と参照領域E2に入射される。測定領域E1及び参照領域E2において、光ビームL1、L2は、金属膜50と誘電体ブロック42との界面に対して種々の入射角成分を含み、かつ全反射角以上の角度で入射される。光ビームL1、L2は、誘電体ブロック42と金属膜50との界面で全反射される。全反射された光ビームL1、L2も、種々の反射角成分をもって反射される。この全反射された光ビームL1、L2は、第2光学系54Cを経て受光部54Dで受光されて、各々光電変換され、光検出信号が信号処理部54Eへ出力される。信号処理部54Eでは、入力された光検出信号に基づいて所定の処理が行なわれ、測定領域E1の測定データG1、及び、参照領域E2の参照データG2が求められる。この測定データG1、参照データG2が制御部60へ出力される。
【0040】
制御部60は、バイオセンサー10の全体を制御する機能を有し、図7に示すように、光源54A、信号処理部54E、及び、バイオセンサー10の図示しない駆動系と接続されている。制御部60は、図8示すように、バスBを介して互いに接続される、CPU60A、ROM60B、RAM60C、メモリ60D、及び、インターフェースI/F60E、を有し、各種の情報を表示する表示部62、各種の指示、情報を入力するための入力部64、と接続されている。
【0041】
メモリ60Dには、バイオセンサー10を制御するための各種プログラムや、各種データ、非特異吸着データベースHが記憶されている。
【0042】
図9に示すように、非特異吸着データベースHには、固定化膜の種類、バッファーの種類、及び化合物濃度で特定される測定条件毎に、この測定条件における複数の化合物についての参照データG2が記録されている。測定条件毎のデータを、以下、サンプルデータSPという。サンプルデータSPは、バイオセンサー10での測定毎に記録され、増加していく。参照データG2は、固定化膜50Aへの化合物Aの非特異吸着量を含んでおり、生理活性物質Dが固定化されていない固定化膜50A上にランニングバッファーを供給した際に求められる基準点と、化合物Aを供給した際に求められる信号との変化量RUで示されている。
【0043】
次に、バイオセンサー10での、測定について説明する。
【0044】
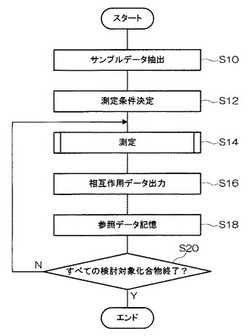
センサースティック40が測定部56へ搬送され、入力部64から測定開始の指示が測定条件の一部(固定化膜の種類、バッファーの種類、及び化合物濃度のうちの2つ)と共に入力されると、制御部60では、図10に示す測定処理が実行される。
【0045】
まず、ステップS10で、入力された一部の測定条件と同じ測定条件のサンプルデータSPを抽出する。例えば、固定化膜がCMD、化合物濃度10μMという条件が入力された場合には、図9に示すサンプルNo.1、3、5のデータが抽出される。
【0046】
ステップS12で、抽出されたサンプルデータの各々の参照データG2に着目し、参照データG2が5RU以上の化合物が最も少ないサンプルデータSPを選択し、選択したサンプルデータSPの測定条件を、当該測定のための測定条件として決定する。例えば、図11に示すように、サンプルNo.1では、化合物No.007、010の2個、サンプルNo.3では、化合物No.007、009の2個、サンプルNo.5では、0個の化合物が5RU以上であるため、サンプルNo.5が選択され、サンプルNo.5の、PBS、Tween20 0.05%がバッファー液として決定される。このようにして決定されたバッファー液が、検討対象となる化合物群の固定化膜への非特異的吸着の少ないものとなる。
【0047】
なお、本実施形態では、閾値を5RUとしたが、5RUに限定されるものではなく、1RU以上でも、2RU以上でもよく、ユーザーが任意の値を設定することができる。
【0048】
次に、ステップS14で、入力及び決定された測定条件での測定が行われる。測定は、図12に示すように、ステップS14−1で、検討対象となっている最初の化合物溶液を液体流路45へ供給し、ステップS14−2で、測定領域E1から測定データG1を取得し、ステップS14−3で参照領域E2から参照データG2を取得する。ステップS14−4で、測定データG1を参照データG2で補正して相互作用データG3を算出することにより行われる。
【0049】
次に、ステップS16で、算出された相互作用データG3を表示部62へ出力する。これにより、表示部62に相互作用データG3が表示される。
【0050】
ステップS18で、取得した参照データG2を測定条件と共にメモリ60Dへ記憶し、ステップS20で、検討対象となっている化合物の測定がすべて終了したかどうかを判断する。判断が否定された場合には、ステップS14へ戻って上記の処理を繰り返す。判断が肯定された場合には、本処理を終了する。
【0051】
上記測定処理によれば、非特異吸着量が少なくなるように測定条件が決定されるので、適切な測定条件により、生理活性物質Dと化合物との間の相互作用を正確に測定することができる。
【0052】
また、測定により得られた参照データG2がメモリ60Dへフィードバックされるので、測定条件毎に非特異吸着量の多い化合物のデータを蓄積することができ、測定を重ねることにより多くの参照データに基づいて適切な測定を行うことができる。
【0053】
なお、本実施形態では、参照データG2が所定値以上の化合物数が最も少ないサンプルデータSPの測定条件を選択したが、参照データG2の値が0の化合物の最も多いサンプルデータSPや、参照データG2が所定値以下となるすべての化合物の参照データG2の合計値が最も小さいサンプルデータSPを、選択するようにしてもよい。
【0054】
また、本実施形態では、バイオセンサーとして、表面プラズモンセンサーを一例として説明したが、バイオセンサーとしては、表面プラズモンセンサーに限定されるものではない。その他の例えば、水晶発振子マイクロバランス(QCM)測定技術、金のコロイド粒子から超微粒子までの機能化表面を使用した光学的測定技術など、あらゆるバイオセンサーを用いた場合における、参照領域で得られる参照データを予めデータベース化して記憶しておき、記憶された参照データにより、測定された測定データを補正するようにすることもできる。
【0055】
また、全反射減衰を利用する他のバイオセンサーとしては、漏洩モード検出器をあげることができる。漏洩モードセンサは、誘電体と、この上に順に層設されたクラッド層と光導波層とによって構成された薄膜とからなり、この薄膜の一方の面がセンサ面となり、他方の面が光入射面となる。光入射面に全反射条件を満たすように光を入射させると、その一部が前記クラッド層を透過して前記光導波層に取り込まれる。そして、この光導波層において、導波モードが励起されると、前記光入射面における反射光が大きく減衰する。導波モードが励起される入射角は、表面プラズモン共鳴角と同様に、センサ面上の媒質の屈折率に応じて変化する。この反射光の減衰を検出することにより、前記センサ面上の反応を測定することができる。
【実施例】
【0056】
次に、上記実施形態で説明した誘電体ブロック上への固定化膜の作成、及び、作成された固定化膜に対する化合物の非特異吸着量の測定について説明する。なお、固定化膜の作成、非特異吸着量の測定については、市販の表面プラズモンセンサーで行った。
【0057】
(1)固定化膜の作成
(固定化膜の作成)
金属膜を製膜した誘電体ブロック上に、以下の方法でヒドロゲル膜で構成される固定化膜を作成した。
【0058】
誘電体ブロックをModel−208UV−オゾンクリーニングシステム(TECHNOVISION INC.)で30分間処理した後、エタノール/水(80/20)で溶解した11−ヒドロキシ−1−ウンデカンチオール(Aldrich社製)の5.0mM溶液を金属膜に接触するように添加し、40℃で30分、さらに25℃で16時間表面処理を行った。その後、エタノールで5回、エタノール/水混合溶媒で1回、水で5回洗浄を行った。
【0059】
次に、11−ヒドロキシ−1−ウンデカンチオールで被覆した表面に10重量%のエピクロロヒドリン溶液(溶媒:0.4M水酸化ナトリウム及びジエチレングリコールジメチルエーテルの1:1混合溶液)を接触させ、25℃の振盪インキュベーター中で4時間反応を進行させた。
【0060】
その後表面をエタノールで2回、水で5回洗浄した。次に、25重量%のデキストラン(T500,Pharmacia)水溶液40.5mlに4.5mlの1M水酸化ナトリウムを添加し、その溶液をエピクロロヒドリン処理表面上に接触させた。次に振盪インキュベーター中で25℃で20時間インキュベートした。表面を50℃の水で10回洗浄した。続いて、ブロモ酢酸3.5gを27gの2M水酸化ナトリウム溶液に溶解した混合物を上記デキストラン処理表面に接触させて、28℃の振盪インキュベーターで16時間インキュベートした。表面を水で洗浄し、その後上述の手順を1回繰り返した。
【0061】
(2)蛋白質の固定
Neutrアビジン(PIERE社製)100μg/ml(酢酸バッファーpH5.0)溶液を調製した。上記測定チップに、1−エチルー2,3ジメチルアミノプロピルカルボジイミド(400mM)とN−ヒドロキシスクシンイミド(100mM)の混合液を添加し、活性化処理を2分、あるいは20分間行った。10mMリン酸バッファーで洗浄した後、上記のNeutrアビジン溶液を添加し、20分静置し、Neutrアビジンをアミンカップリングした。さらに、10mMリン酸バッファーで洗浄後、エタノールアミン・HCl溶液(1M,pH8.5)を測定チップに添加することにより、Neutrアビジンと反応せずに残存したCOOH基をブロッキングした。
【0062】
以上の操作により、Neutrアビジンを測定チップ表面に共有結合で固定した。Neutrアビジン添加前と洗浄後の共鳴シグナル(RU値)変化量をNeutrアビジン固定量(RU値)として、表1に示す。表1から明らかなように、活性化時間を長くする程、Neutrアビジンの固定量も多くなる。
【0063】
(3)化合物の非特異吸着の蛋白固定量依存性
上記のように作成したNeutrアビジンを固定化した測定チップについて、以下の方法で、化合物の非特異吸着性を評価した。
【0064】
下記の化合物Aを0.03mMになるようにPBSバッファー(10mM リン酸ナトリウム, 150mM NaCl, pH7.4)/ DMSO 5%溶液に溶解する。SPR装置に、ランニングバッファーとしてPBSバッファー/DMSO 5%溶液を流し、基準点をとる。次に作成した化合物A溶液を3分間流し、その後、PBSバッファー/DMSO 5%溶液を3分間流す。基準点からのSPR信号の増加分(RU)を非特異吸着量とする。測定結果を表1に示す。
【0065】
Neutrアビジンの固定量が多くなる程、化合物の固定化膜への非特異吸着量が少なくなることが明らかである。
【0066】
【化1】

【0067】
【表1】

【0068】
(5)測定バッファー種と固定化膜への非特異吸着量
化合物Aを、以下のバッファーA、バッファーB、バッファーCに溶解する。化合物濃度については、各々のバッファーについて1μM、10μM、100μM、を用意する。
【0069】
バッファーA:10mM リン酸ナトリウム,150mM NaCl,pH7.4, DMSO 5% ; バッファーB:10mMリン酸ナトリウム,150mM NaCl,Tween20 0.005%,pH 7.4, DMSO 5% ; バッファーC:10mM Tris−HCl,150mM NaCl,pH 8.0,DMSO 5%
SPR装置に、化合物Aを溶解したバッファーと同種のランニングバッファーを流し、基準点をとる。次に作成した化合物Aを3分間流し、その後、化合物Aを溶解したバッファーと同種のランニングバッファーを3分間流す。基準点からのSPR信号の増加分(RU)を非特異吸着量とする。測定結果を表2に示す。
【0070】
【表2】

【0071】
バッファーの組成により、固定化膜に対する低分子化合物の非特異吸着量は顕著に変化する。
【0072】
上記より、固定化膜、バッファー液の構成により、低分子化合物の非特異吸着量が変化することが明らかである。また、蛋白の固定化量によって、固定化膜に吸着する化合物の量にも変化が見られる。したがって、固定化膜、バッファー液の種類毎に化合物の非特異吸着のデータベースが必要である。
【図面の簡単な説明】
【0073】
【図1】本実施形態のバイオセンサーの全体斜視図である。
【図2】本実施形態のセンサースティックの斜視図である。
【図3】本実施形態のセンサースティックの分解斜視図である。
【図4】本実施形態のセンサースティックの1の液体流路部分の断面図である。
【図5】本実施形態のセンサースティックの測定領域、参照領域へ光ビームが入射している状態を示す図である。
【図6】本実施形態の液体供給部を構成するピペット部の側面図である。
【図7】本実施形態のバイオセンサーの光学測定部付近の概略図である。
【図8】本実施形態の制御部とその周辺の概略ブロック図である。
【図9】本実施形態の非特異吸着データベースを示す図である。
【図10】本実施形態の測定処理のフローチャートである。
【図11】本実施形態の測定処理で選択されたサンプルデータの例である。
【図12】本実施形態の測定処理の中の測定についてのフローチャートである。
【符号の説明】
【0074】
10 バイオセンサー
40 センサースティック
45 液体流路
50 金属膜
50A 固定化膜
54 光学測定部
56 測定部
60D メモリ
60 制御部
62 表示部
64 入力部
D 生理活性物質
E1 測定領域
E2 参照領域
G1 測定データ
G2 参照データ
G3 相互作用データ
H 非特異吸着データベース
【技術分野】
【0001】
本発明は、測定装置、及び、測定プログラムに関し、詳しくは、生理活性物質と所定の化合物との相互作用を測定する測定装置、及び、測定プログラムに関するものである。
【背景技術】
【0002】
生理活性物質と所定の化合物との相互作用を測定する装置として、様々なバイオセンサーが提案されている。そのうち、エバネッセント波を利用した測定装置の1つとして、表面プラズモンセンサーが知られている(特許文献1参照)。一般的に、表面プラズモンセンサーは、プリズムと、このプリズムの一面に配置された金属膜と、金属膜上に配置され生理活性物質が固定される固定化膜と、光ビームを発生させる光源と、光ビームをプリズムに対して、プリズムと金属膜との界面で全反射条件が得られるように種々の角度で入射させる光学系と、界面で全反射した光ビームの強度を検出する光検出手段と、を備え、光検出手段の検出結果に基づいて、生理活性物質についての測定を行なうものである。
【0003】
この表面プラズモンセンサーによる測定では、固定化膜の上に固定化された生理活性物質に対して化合物溶液を供給すると共に、金属膜の固定化膜が供給されている側と逆側の面へ光ビームを入射し、その反射光から得られる屈折率の情報に基づいて、生理活性物質と化合物溶液中の化合物との、相互作用が測定される。
【0004】
ところで、表面プラズモンセンサーによる測定では、生理活性物質が固定されている測定部とは別に、生理活性物質が固定されていない参照部を設け、参照部から得られる屈折率の情報で測定部の屈折率の情報を補正することが行われる。ここでの補正は、種類やその他の条件が異なることによる化合物と固定化膜との間の信号変化をキャンセルして、生理活性物質と化合物との間の特異的結合による信号変化のみを測定することが主な目的である。
【0005】
しかしながら、検討対象の化合物が、固定化膜へ大量に吸着(このような吸着を以下「非特異吸着」という)する場合には、生理活性物質と化合物との間の特異的結合が正確に測定されない可能性が高い。
【特許文献1】特許第3294605号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
本発明は上記事実を考慮してなされたものであり、より適切な測定条件を用いて生理活性物質と化合物との間の相互作用を正確に測定する測定装置、及び、測定プログラムを提供することを目的とする。
【課題を解決するための手段】
【0007】
上記課題を解決するために、本発明の測定装置は、固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定する測定装置であって、前記参照データを測定条件及び前記化合物毎に記憶する記憶手段と、前記測定のための測定条件の一部を入力する測定条件入力手段と、前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定する測定条件決定手段と、前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定する測定手段と、前記測定手段により測定された相互作用に関する相互作用データを出力する出力手段と、前記測定手段により得られた参照データを前記測定の際の測定条件と共に前記記憶手段へ記憶させるフィードバック手段と、を備えている。
【0008】
また、本発明の測定プログラムは、固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定するための測定プログラムであって、前記参照データを測定条件及び前記化合物毎に記憶するステップと、前記測定のための測定条件の一部を入力するステップと、前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定するステップと、前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定するステップと、前記測定された相互作用に関する相互作用データを出力するステップと、前記測定により得られた参照データを前記測定の際の測定条件と共に記憶させるステップと、をコンピュータに実行させるものである。
【0009】
ここで、前記生理活性物質とは、日本工業規格(JIS)K3611中に「天然高分子」(記号11001〜11025)として記載されている各物質、生物学データ大百科事典(朝倉書店)中の「1.生体物質概論」に記載されている糖,アミノ酸、ヌクレオチド、脂質、ヘム、キノン、タンパク質、RNA,DNA、リン脂質、多糖、バイオサイエンス辞典(朝倉書店)中の「II.生物物質と代謝」に記載されているタンパク質、アミノ酸、核酸、脂質、糖質、酵素のうちのいずれか1つ以上を含むものを意味する。
【0010】
前記相互作用とは、物理的、化学的、もしくは生化学的な反応における、結合反応の速さ、結合量、または解離反応の速さ、あるいは、上記結合反応の速さ、結合量、および解離反応の速さのうちの2つ以上を組み合わせたものを意味するものである。
【0011】
生理活性物質の固定されている固定化膜と、生理活性物質の固定されていない固定化膜とでは、化合物の非特異吸着量が異なる。したがって、固定化膜への化合物の非特異吸着量が多い場合には、生理活性物質と化合物との相互作用を正しく測定できない可能性が高い。
【0012】
一方、固定化膜への化合物の非特異吸着量は、固定化膜の種類、バッファー液の種類、化合物の種類、化合物濃度、などの測定条件によって異なる。
【0013】
そこで、本発明では、測定のために測定条件の一部のみを入力し、入力された測定条件の一部に対応した参照データに着目する。そして、参照データに基づいて、固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定する。そして、決定された測定条件で生理活性物質と供給される化合物との間の相互作用を測定する。
【0014】
本発明では、非特異的吸着が少なくなるように測定条件が決定され、決定された測定条件で測定が行われるので、より適切な測定条件で正確に測定を行うことができる。
【0015】
また、本発明では、測定により得られた参照データを測定の際の測定条件と共に記憶させるので、測定毎に参照データが蓄積され、測定を重ねることにより多くの参照データに基づいて適切な測定を行うことができる。
【0016】
なお、本発明の測定装置は、前記固定化膜が金属膜上に形成され、前記測定手段が、前記金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、前記生理活性物質及び前記生理活性物質の固定された前記固定化膜と前記化合物との間の相互作用を測定すること、を特徴とすることもできる。
【0017】
また、本発明の測定プログラムは、前記測定が、片面に前記固定化膜の形成された金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、生理活性物質及び生理活性物質の固定された固定化膜と化合物との間の相互作用を測定するものであること、を特徴とすることもできる。
【0018】
上記のような測定としては、表面プラズモンセンサー、漏洩モードセンサによる測定がある。
【発明の効果】
【0019】
上記発明によれば、より適切な測定条件を用いて生理活性物質と化合物との間の相互作用を正確に測定することができる。
【発明を実施するための最良の形態】
【0020】
以下、図面を参照しながら本発明の実施形態について説明する。
【0021】
本実施形態の測定装置としてのバイオセンサー10は、金属膜の表面に発生する表面プラズモンを利用して、生理活性物質Dと化合物との相互作用路を測定する、いわゆる表面プラズモンセンサーである。
【0022】
図1に示すように、バイオセンサー10は、トレイ保持部12、搬送部14、容器載置台16、液体吸排部20、押さえ部26、光学測定部54、及び、制御部60を備えている。
【0023】
トレイ保持部12は、載置台12A、及び、ベルト12Bを含んで構成されている。載置台12Aは、矢印Y方向に架け渡されたベルト12Bに取り付けられており、ベルト12Bの回転により矢印Y方向に移動可能とされている。載置台12A上には、トレイTが2枚、位置決めして載置される。トレイTには、センサースティック40が8本収納されている。センサースティック40は、生理活性物質Dの固定されるチップであり、詳細については後述する。載置台12Aの下には、センサースティック40を後述するスティック保持部材14Cの位置まで押し上げる、押上機構12Dが配置されている。
【0024】
センサースティック40は、図2及び図3に示すように、誘電体ブロック42、流路部材44、保持部材46、接着部材48、及び、蒸発防止部材49、で構成されている。
【0025】
誘電体ブロック42は、光ビームに対して透明な透明樹脂等で構成されており、断面が台形の棒状とされたプリズム部42A、及び、プリズム部42Aの両端部にプリズム部42Aと一体的に形成された被保持部42Bを備えている。プリズム部42Aの互いに平行な2面の内の広い側の上面には、図4にも示すように金属膜50が形成されている。この金属膜50上に、バイオセンサー10で解析する生理活性物質Dが固定される。誘電体ブロック42は、いわゆるプリズムとして機能し、バイオセンサー10での測定の際には、プリズム部42Aの対向する互いに平行でない2つの側面の内の一方から光ビームが入射され、他方から金属膜50との界面で全反射された光ビームが出射される。
【0026】
金属膜50の表面には、図4に示すように、固定化膜50Aが形成されている。固定化膜50Aは、生理活性物質Dを金属膜50上に固定化するためのものである。固定化膜50Aは、固定する生理活性物質Dに応じて選択される。固定化膜50Aとしては、例えばアガロース、デキストラン、カラゲナン、アルギン酸、デンプン、セルロースなどのヒドロゲル、又はこれらの誘導体、例えばカルボキシメチル誘導体、又は水膨潤性有機ポリマー、例えばポリビニルアルコール、ポリアクリル酸、ポリアクリルアミド、ポリエチレングリコールなどを使用することができる。特に、ポリエチレングリコール誘導体、デキストラン誘導体は、生理活性維持の観点から好ましく用いられる。
【0027】
固定化膜50A上には、生理活性物質Dが固定された測定領域E1と、生理活性物質Dが固定されず、測定領域E1の信号測定に際しての参照信号を得るための参照領域E2とが形成される。この参照領域E2は、上述した固定化膜50Aを製膜する際に形成される。形成方法としては、例えば、固定化膜50Aに対して表面処理を施して、生理活性物質Dと結合する結合基を失活させる。これにより、固定化膜50Aの半分が測定領域E1となり、残りの半分が参照領域E2となる。
【0028】
図5にも示すように、液体流路45に露出された固定化膜50Aの、参照領域E2以外の部分には、生理活性物質Dが固定されている。参照領域E2には生理活性物質Dは固定されていない。参照領域E2、及び、参照領域E2よりも上流側に位置する測定領域E1には、各々光ビームL2、L1が入射される。参照領域E2は、生理活性物質Dの固定された測定領域E1から得られるデータを補正するために設けられた領域である。
【0029】
プリズム部42Aの両側面には、上側の端辺に沿って保持部材52と係合される係合凸部42Cが、下側の端辺に沿ってプリズム部42Aの上面と垂直な仮想面の延長上に構成される垂直凸部42Dが、各々7箇所に形成されている。また、誘電体ブロック42の下面の長手方向に沿った中央部には、係合溝42Eが形成されている。
【0030】
流路部材44は、誘電体ブロック42よりもわずかに狭幅の直方体状とされ、図3に示すように、誘電体ブロック42の金属膜50上に6個並べて配置されている。各々の流路部材44の下面には流路溝44Aが形成されており、上面に形成された供給口45A及び排出口45Bと連通されて、金属膜50との間に、液体流路45が構成される。したがって、1本のセンサースティック40には、独立した6個の液体流路45が構成される。流路部材44の側壁には、保持部材46の内側の図示しない凹部に圧入されて保持部材46との密着性を確保するための凸部44Bが形成されている。
【0031】
なお、液体流路45には、蛋白質を含む液体が供給されることが想定されるので、流路部材44への蛋白質の固着を防止するため、流路部材44の材料としては、蛋白質に対する非特異吸着性を有しないことが好ましい。
【0032】
保持部材46は、長尺とされ、上面板46A及び2枚の側面板46Bで構成されている。側面板46Bには、誘電体ブロック42の係合凸部42Cと係合される係合孔46Cが形成されている。保持部材46は、6個の流路部材44を間に挟んで係合孔46Cと係合凸部42Cとが係合されて、誘電体ブロック42に取り付けられる。これにより、流路部材44は、誘電体ブロック42に取り付けられる。上面板46Aには、流路部材44の供給口45A及び排出口45Bと対向する位置に、流路部材44に向けて狭くなるテーパー状のピペット挿入孔46Dが形成されている。また、隣り合うピペット挿入孔46Dとピペット挿入孔46Dとの間には、位置決め用のボス46Eが形成されている。
【0033】
保持部材46の上面には、蒸発防止部材49が接着部材48を介して接着されている。接着部材48のピペット挿入孔46Dと対向する位置にはピペット挿入用の孔48Dが形成され、ボス46Eと対向する位置には位置決め用の孔48Eが形成されている。また、蒸発防止部材49のピペット挿入孔46Dと対向する位置には十字状の切り込みであるスリット49Dが形成され、ボス46Eと対向する位置には位置決め用の孔49Eが形成されている。ボス46Eを孔48E及び49Eに挿通させて、蒸発防止部材49を保持部材52の上面に接着することにより、蒸発防止部材49のスリット49Dと流路部材44の供給口45A及び排出口45Bとが対向するように構成される。ピペットチップCPの非挿入時には、スリット49D部分が供給口45Bを覆い、液体流路45に供給されている液体の蒸発が防止される。
【0034】
図1に示すように、バイオセンサー10の搬送部14は、上部ガイドレール14A、下部ガイドレール14B、及び、スティック保持部材14C、を含んで構成されている。上部ガイドレール14A及び下部ガイドレール14Bは、トレイ保持部12及び光学測定部54の上部で、矢印Y方向と直交する矢印X方向に水平に配置されている。上部ガイドレール14Aには、スティック保持部材14Cが取り付けられている。スティック保持部材14Cは、センサースティック40の両端部の被保持部42Bを保持可能とされていると共に、上部ガイドレール14Aに沿って移動可能とされている。スティック保持部材14Cに保持されたセンサースティック40の係合溝42Eと下部ガイドレール14Bとが係合され、スティック保持部材14Cが矢印X方向に移動することにより、センサースティック40が光学測定部54上の測定部56に搬送される。また、測定部56には、測定時にセンサースティック40を押さえる押さえ部材58が備えられている。押さえ部材58は、図示しない駆動機構によりZ方向に移動可能とされ、測定部56に配置されたセンサースティック40を上側から押圧する。
【0035】
容器載置台16には、化合物溶液プレート17、バッファー液ストック容器18、廃棄液容器19が載置されている。化合物溶液プレート17は、96に区画されており、各種の化合物溶液をストック可能とされている。バッファー液ストック容器18は、容器18A〜18Eで構成されており、バッファー液がストックされている。容器18A〜18Eには、後述するピペットチップCPを挿入可能な開口Kが形成されている。バッファー液としては、例えば公知の緩衝溶液(化学便覧応用編改訂2版、1312頁〜1320頁)を基本に、食塩、界面活性剤(Tween20など)、金属イオン(マグネシウムイオン、カリウムイオン、カルシウムイオンなど)、安定化剤(DTTなど)などを添加したものを用いることができる。特に、PBSバッファー(リン酸バッファー生理食塩水)、Trisバッファー、HEPESバッファーなどが好ましく用いられる。
【0036】
廃棄液容器19は、複数の容器19A〜19Eで構成されており、容器18A〜18Eと同様にピペットチップCPを挿入可能な開口Kが形成されている。
【0037】
液体吸排部20は、上部ガイドレール14A、及び、ガイドレール16Bよりも上方で、矢印Y方向に架け渡された横断レール22、及び、ヘッド24を含んで構成されている。横断レール22は、図示しない駆動機構により、矢印X方向へ移動可能とされている。また、ヘッド24は、横断レール22に取り付けられ、矢印Y方向に移動可能とされている。また、ヘッド24は、図示しない駆動機構により、鉛直方向(矢印Z方向)にも移動可能とされている。ヘッド24は、図6に示すように、2本のピペット部24A、24Bを備えている。ピペット部24A、24Bには、先端部にピペットチップCPが取り付けられ、個々にZ方向の長さを調整可能とされている。ピペットチップCPは、図示しないピペットチップストッカーに多数ストックされており、必要に応じて交換可能とされている。
【0038】
なお、本実施形態においてはセンサースティック40への液体供給はピペットチップCPにより行われるが、ピペットチップの代わりに、一端が上記各溶液プレートに接続され、他端がセンサースティック40に接続可能とされたインジェクションチューブを設け、送液ポンプにより液体の供給を行ってもよい。
【0039】
光学測定部54は、図7に示すように、光源54A、第1光学系54B、第2光学系54C、受光部54D、信号処理部54E、を含んで構成されている。光源54Aからは、発散状態の光ビームLが出射される。光ビームLは、第1光学系54Bを介して、2本の光ビームL1、L2となり、測定部56に配置された誘電体ブロック42の測定領域E1と参照領域E2に入射される。測定領域E1及び参照領域E2において、光ビームL1、L2は、金属膜50と誘電体ブロック42との界面に対して種々の入射角成分を含み、かつ全反射角以上の角度で入射される。光ビームL1、L2は、誘電体ブロック42と金属膜50との界面で全反射される。全反射された光ビームL1、L2も、種々の反射角成分をもって反射される。この全反射された光ビームL1、L2は、第2光学系54Cを経て受光部54Dで受光されて、各々光電変換され、光検出信号が信号処理部54Eへ出力される。信号処理部54Eでは、入力された光検出信号に基づいて所定の処理が行なわれ、測定領域E1の測定データG1、及び、参照領域E2の参照データG2が求められる。この測定データG1、参照データG2が制御部60へ出力される。
【0040】
制御部60は、バイオセンサー10の全体を制御する機能を有し、図7に示すように、光源54A、信号処理部54E、及び、バイオセンサー10の図示しない駆動系と接続されている。制御部60は、図8示すように、バスBを介して互いに接続される、CPU60A、ROM60B、RAM60C、メモリ60D、及び、インターフェースI/F60E、を有し、各種の情報を表示する表示部62、各種の指示、情報を入力するための入力部64、と接続されている。
【0041】
メモリ60Dには、バイオセンサー10を制御するための各種プログラムや、各種データ、非特異吸着データベースHが記憶されている。
【0042】
図9に示すように、非特異吸着データベースHには、固定化膜の種類、バッファーの種類、及び化合物濃度で特定される測定条件毎に、この測定条件における複数の化合物についての参照データG2が記録されている。測定条件毎のデータを、以下、サンプルデータSPという。サンプルデータSPは、バイオセンサー10での測定毎に記録され、増加していく。参照データG2は、固定化膜50Aへの化合物Aの非特異吸着量を含んでおり、生理活性物質Dが固定化されていない固定化膜50A上にランニングバッファーを供給した際に求められる基準点と、化合物Aを供給した際に求められる信号との変化量RUで示されている。
【0043】
次に、バイオセンサー10での、測定について説明する。
【0044】
センサースティック40が測定部56へ搬送され、入力部64から測定開始の指示が測定条件の一部(固定化膜の種類、バッファーの種類、及び化合物濃度のうちの2つ)と共に入力されると、制御部60では、図10に示す測定処理が実行される。
【0045】
まず、ステップS10で、入力された一部の測定条件と同じ測定条件のサンプルデータSPを抽出する。例えば、固定化膜がCMD、化合物濃度10μMという条件が入力された場合には、図9に示すサンプルNo.1、3、5のデータが抽出される。
【0046】
ステップS12で、抽出されたサンプルデータの各々の参照データG2に着目し、参照データG2が5RU以上の化合物が最も少ないサンプルデータSPを選択し、選択したサンプルデータSPの測定条件を、当該測定のための測定条件として決定する。例えば、図11に示すように、サンプルNo.1では、化合物No.007、010の2個、サンプルNo.3では、化合物No.007、009の2個、サンプルNo.5では、0個の化合物が5RU以上であるため、サンプルNo.5が選択され、サンプルNo.5の、PBS、Tween20 0.05%がバッファー液として決定される。このようにして決定されたバッファー液が、検討対象となる化合物群の固定化膜への非特異的吸着の少ないものとなる。
【0047】
なお、本実施形態では、閾値を5RUとしたが、5RUに限定されるものではなく、1RU以上でも、2RU以上でもよく、ユーザーが任意の値を設定することができる。
【0048】
次に、ステップS14で、入力及び決定された測定条件での測定が行われる。測定は、図12に示すように、ステップS14−1で、検討対象となっている最初の化合物溶液を液体流路45へ供給し、ステップS14−2で、測定領域E1から測定データG1を取得し、ステップS14−3で参照領域E2から参照データG2を取得する。ステップS14−4で、測定データG1を参照データG2で補正して相互作用データG3を算出することにより行われる。
【0049】
次に、ステップS16で、算出された相互作用データG3を表示部62へ出力する。これにより、表示部62に相互作用データG3が表示される。
【0050】
ステップS18で、取得した参照データG2を測定条件と共にメモリ60Dへ記憶し、ステップS20で、検討対象となっている化合物の測定がすべて終了したかどうかを判断する。判断が否定された場合には、ステップS14へ戻って上記の処理を繰り返す。判断が肯定された場合には、本処理を終了する。
【0051】
上記測定処理によれば、非特異吸着量が少なくなるように測定条件が決定されるので、適切な測定条件により、生理活性物質Dと化合物との間の相互作用を正確に測定することができる。
【0052】
また、測定により得られた参照データG2がメモリ60Dへフィードバックされるので、測定条件毎に非特異吸着量の多い化合物のデータを蓄積することができ、測定を重ねることにより多くの参照データに基づいて適切な測定を行うことができる。
【0053】
なお、本実施形態では、参照データG2が所定値以上の化合物数が最も少ないサンプルデータSPの測定条件を選択したが、参照データG2の値が0の化合物の最も多いサンプルデータSPや、参照データG2が所定値以下となるすべての化合物の参照データG2の合計値が最も小さいサンプルデータSPを、選択するようにしてもよい。
【0054】
また、本実施形態では、バイオセンサーとして、表面プラズモンセンサーを一例として説明したが、バイオセンサーとしては、表面プラズモンセンサーに限定されるものではない。その他の例えば、水晶発振子マイクロバランス(QCM)測定技術、金のコロイド粒子から超微粒子までの機能化表面を使用した光学的測定技術など、あらゆるバイオセンサーを用いた場合における、参照領域で得られる参照データを予めデータベース化して記憶しておき、記憶された参照データにより、測定された測定データを補正するようにすることもできる。
【0055】
また、全反射減衰を利用する他のバイオセンサーとしては、漏洩モード検出器をあげることができる。漏洩モードセンサは、誘電体と、この上に順に層設されたクラッド層と光導波層とによって構成された薄膜とからなり、この薄膜の一方の面がセンサ面となり、他方の面が光入射面となる。光入射面に全反射条件を満たすように光を入射させると、その一部が前記クラッド層を透過して前記光導波層に取り込まれる。そして、この光導波層において、導波モードが励起されると、前記光入射面における反射光が大きく減衰する。導波モードが励起される入射角は、表面プラズモン共鳴角と同様に、センサ面上の媒質の屈折率に応じて変化する。この反射光の減衰を検出することにより、前記センサ面上の反応を測定することができる。
【実施例】
【0056】
次に、上記実施形態で説明した誘電体ブロック上への固定化膜の作成、及び、作成された固定化膜に対する化合物の非特異吸着量の測定について説明する。なお、固定化膜の作成、非特異吸着量の測定については、市販の表面プラズモンセンサーで行った。
【0057】
(1)固定化膜の作成
(固定化膜の作成)
金属膜を製膜した誘電体ブロック上に、以下の方法でヒドロゲル膜で構成される固定化膜を作成した。
【0058】
誘電体ブロックをModel−208UV−オゾンクリーニングシステム(TECHNOVISION INC.)で30分間処理した後、エタノール/水(80/20)で溶解した11−ヒドロキシ−1−ウンデカンチオール(Aldrich社製)の5.0mM溶液を金属膜に接触するように添加し、40℃で30分、さらに25℃で16時間表面処理を行った。その後、エタノールで5回、エタノール/水混合溶媒で1回、水で5回洗浄を行った。
【0059】
次に、11−ヒドロキシ−1−ウンデカンチオールで被覆した表面に10重量%のエピクロロヒドリン溶液(溶媒:0.4M水酸化ナトリウム及びジエチレングリコールジメチルエーテルの1:1混合溶液)を接触させ、25℃の振盪インキュベーター中で4時間反応を進行させた。
【0060】
その後表面をエタノールで2回、水で5回洗浄した。次に、25重量%のデキストラン(T500,Pharmacia)水溶液40.5mlに4.5mlの1M水酸化ナトリウムを添加し、その溶液をエピクロロヒドリン処理表面上に接触させた。次に振盪インキュベーター中で25℃で20時間インキュベートした。表面を50℃の水で10回洗浄した。続いて、ブロモ酢酸3.5gを27gの2M水酸化ナトリウム溶液に溶解した混合物を上記デキストラン処理表面に接触させて、28℃の振盪インキュベーターで16時間インキュベートした。表面を水で洗浄し、その後上述の手順を1回繰り返した。
【0061】
(2)蛋白質の固定
Neutrアビジン(PIERE社製)100μg/ml(酢酸バッファーpH5.0)溶液を調製した。上記測定チップに、1−エチルー2,3ジメチルアミノプロピルカルボジイミド(400mM)とN−ヒドロキシスクシンイミド(100mM)の混合液を添加し、活性化処理を2分、あるいは20分間行った。10mMリン酸バッファーで洗浄した後、上記のNeutrアビジン溶液を添加し、20分静置し、Neutrアビジンをアミンカップリングした。さらに、10mMリン酸バッファーで洗浄後、エタノールアミン・HCl溶液(1M,pH8.5)を測定チップに添加することにより、Neutrアビジンと反応せずに残存したCOOH基をブロッキングした。
【0062】
以上の操作により、Neutrアビジンを測定チップ表面に共有結合で固定した。Neutrアビジン添加前と洗浄後の共鳴シグナル(RU値)変化量をNeutrアビジン固定量(RU値)として、表1に示す。表1から明らかなように、活性化時間を長くする程、Neutrアビジンの固定量も多くなる。
【0063】
(3)化合物の非特異吸着の蛋白固定量依存性
上記のように作成したNeutrアビジンを固定化した測定チップについて、以下の方法で、化合物の非特異吸着性を評価した。
【0064】
下記の化合物Aを0.03mMになるようにPBSバッファー(10mM リン酸ナトリウム, 150mM NaCl, pH7.4)/ DMSO 5%溶液に溶解する。SPR装置に、ランニングバッファーとしてPBSバッファー/DMSO 5%溶液を流し、基準点をとる。次に作成した化合物A溶液を3分間流し、その後、PBSバッファー/DMSO 5%溶液を3分間流す。基準点からのSPR信号の増加分(RU)を非特異吸着量とする。測定結果を表1に示す。
【0065】
Neutrアビジンの固定量が多くなる程、化合物の固定化膜への非特異吸着量が少なくなることが明らかである。
【0066】
【化1】

【0067】
【表1】

【0068】
(5)測定バッファー種と固定化膜への非特異吸着量
化合物Aを、以下のバッファーA、バッファーB、バッファーCに溶解する。化合物濃度については、各々のバッファーについて1μM、10μM、100μM、を用意する。
【0069】
バッファーA:10mM リン酸ナトリウム,150mM NaCl,pH7.4, DMSO 5% ; バッファーB:10mMリン酸ナトリウム,150mM NaCl,Tween20 0.005%,pH 7.4, DMSO 5% ; バッファーC:10mM Tris−HCl,150mM NaCl,pH 8.0,DMSO 5%
SPR装置に、化合物Aを溶解したバッファーと同種のランニングバッファーを流し、基準点をとる。次に作成した化合物Aを3分間流し、その後、化合物Aを溶解したバッファーと同種のランニングバッファーを3分間流す。基準点からのSPR信号の増加分(RU)を非特異吸着量とする。測定結果を表2に示す。
【0070】
【表2】

【0071】
バッファーの組成により、固定化膜に対する低分子化合物の非特異吸着量は顕著に変化する。
【0072】
上記より、固定化膜、バッファー液の構成により、低分子化合物の非特異吸着量が変化することが明らかである。また、蛋白の固定化量によって、固定化膜に吸着する化合物の量にも変化が見られる。したがって、固定化膜、バッファー液の種類毎に化合物の非特異吸着のデータベースが必要である。
【図面の簡単な説明】
【0073】
【図1】本実施形態のバイオセンサーの全体斜視図である。
【図2】本実施形態のセンサースティックの斜視図である。
【図3】本実施形態のセンサースティックの分解斜視図である。
【図4】本実施形態のセンサースティックの1の液体流路部分の断面図である。
【図5】本実施形態のセンサースティックの測定領域、参照領域へ光ビームが入射している状態を示す図である。
【図6】本実施形態の液体供給部を構成するピペット部の側面図である。
【図7】本実施形態のバイオセンサーの光学測定部付近の概略図である。
【図8】本実施形態の制御部とその周辺の概略ブロック図である。
【図9】本実施形態の非特異吸着データベースを示す図である。
【図10】本実施形態の測定処理のフローチャートである。
【図11】本実施形態の測定処理で選択されたサンプルデータの例である。
【図12】本実施形態の測定処理の中の測定についてのフローチャートである。
【符号の説明】
【0074】
10 バイオセンサー
40 センサースティック
45 液体流路
50 金属膜
50A 固定化膜
54 光学測定部
56 測定部
60D メモリ
60 制御部
62 表示部
64 入力部
D 生理活性物質
E1 測定領域
E2 参照領域
G1 測定データ
G2 参照データ
G3 相互作用データ
H 非特異吸着データベース
【特許請求の範囲】
【請求項1】
固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定する測定装置であって、
前記参照データを測定条件及び前記化合物毎に記憶する記憶手段と、
前記測定のための測定条件の一部を入力する測定条件入力手段と、
前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定する測定条件決定手段と、
前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定する測定手段と、
前記測定手段により測定された相互作用に関する相互作用データを出力する出力手段と、
前記測定手段により得られた参照データを前記測定の際の測定条件と共に前記記憶手段へ記憶させるフィードバック手段と、
を備えた測定装置。
【請求項2】
前記固定化膜は金属膜上に形成され、
前記測定手段は、前記金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、前記生理活性物質及び前記生理活性物質の固定された前記固定化膜と前記化合物との間の相互作用を測定すること、
を特徴とする請求項1に記載の測定装置。
【請求項3】
固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定するための測定プログラムであって、
前記参照データを測定条件及び前記化合物毎に記憶するステップと、
前記測定のための測定条件の一部を入力するステップと、
前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定するステップと、
前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定するステップと、
前記測定された相互作用に関する相互作用データを出力するステップと、
前記測定により得られた参照データを前記測定の際の測定条件と共に記憶させるステップと、
をコンピュータに実行させる測定プログラム。
【請求項4】
前記測定は、片面に前記固定化膜の形成された金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、前記生理活性物質及び前記生理活性物質の固定された前記固定化膜と前記化合物との間の相互作用を測定するものであること、
を特徴とする請求項3に記載の測定プログラム。
【請求項1】
固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定する測定装置であって、
前記参照データを測定条件及び前記化合物毎に記憶する記憶手段と、
前記測定のための測定条件の一部を入力する測定条件入力手段と、
前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定する測定条件決定手段と、
前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定する測定手段と、
前記測定手段により測定された相互作用に関する相互作用データを出力する出力手段と、
前記測定手段により得られた参照データを前記測定の際の測定条件と共に前記記憶手段へ記憶させるフィードバック手段と、
を備えた測定装置。
【請求項2】
前記固定化膜は金属膜上に形成され、
前記測定手段は、前記金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、前記生理活性物質及び前記生理活性物質の固定された前記固定化膜と前記化合物との間の相互作用を測定すること、
を特徴とする請求項1に記載の測定装置。
【請求項3】
固定化膜に生理活性物質が固定された測定領域へ検討対象である化合物を供給して得られる測定データ、及び、前記生理活性物質の固定されていない前記固定化膜で構成された参照領域へ前記化合物を供給して得られ前記固定化膜への前記化合物の非特異吸着量に関する情報を含んだ参照データに基づいて、前記生理活性物質と前記化合物との間の相互作用を測定するための測定プログラムであって、
前記参照データを測定条件及び前記化合物毎に記憶するステップと、
前記測定のための測定条件の一部を入力するステップと、
前記入力された測定条件の一部に対応した前記参照データに基づいて、前記固定化膜と検討対象となる化合物との非特異的吸着が少なくなるように他の測定条件を決定するステップと、
前記決定された測定条件により、前記生理活性物質と供給される化合物との間の相互作用を測定するステップと、
前記測定された相互作用に関する相互作用データを出力するステップと、
前記測定により得られた参照データを前記測定の際の測定条件と共に記憶させるステップと、
をコンピュータに実行させる測定プログラム。
【請求項4】
前記測定は、片面に前記固定化膜の形成された金属膜の前記固定化膜の形成されていない側へ光ビームを入射させることにより発生する全反射減衰を利用して、前記生理活性物質及び前記生理活性物質の固定された前記固定化膜と前記化合物との間の相互作用を測定するものであること、
を特徴とする請求項3に記載の測定プログラム。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【公開番号】特開2007−93301(P2007−93301A)
【公開日】平成19年4月12日(2007.4.12)
【国際特許分類】
【出願番号】特願2005−280834(P2005−280834)
【出願日】平成17年9月27日(2005.9.27)
【出願人】(306037311)富士フイルム株式会社 (25,513)
【Fターム(参考)】
【公開日】平成19年4月12日(2007.4.12)
【国際特許分類】
【出願日】平成17年9月27日(2005.9.27)
【出願人】(306037311)富士フイルム株式会社 (25,513)
【Fターム(参考)】
[ Back to top ]

