測定装置及び測定プログラム
【課題】試薬と撮像素子との間にほこり等が存在する場合においても、精度よく呈色状態を測定することができる。
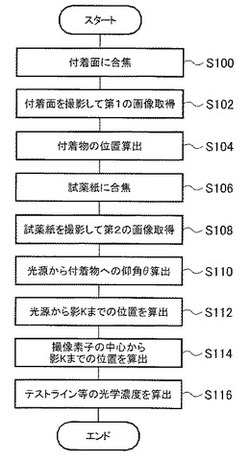
【解決手段】測定装置は、付着物の付着面に合焦して(ステップS100)、付着面を撮影して第1の画像を取得し(ステップS102)、取得した第1の画像に基づいて付着物の位置を算出し(ステップS104)、試薬紙に合焦して(ステップS106)、試薬紙を撮影して第2の画像を取得し(ステップS108)、光源から付着物への仰角を算出し(ステップS110)、光源から影までの位置を算出し(ステップS112)、撮像素子の中心から影までの位置を算出し(ステップS114)、取得した第2の画像に基づいて、影を含む領域を除外してテストライン等の光学濃度を算出する(ステップS116)。
【解決手段】測定装置は、付着物の付着面に合焦して(ステップS100)、付着面を撮影して第1の画像を取得し(ステップS102)、取得した第1の画像に基づいて付着物の位置を算出し(ステップS104)、試薬紙に合焦して(ステップS106)、試薬紙を撮影して第2の画像を取得し(ステップS108)、光源から付着物への仰角を算出し(ステップS110)、光源から影までの位置を算出し(ステップS112)、撮像素子の中心から影までの位置を算出し(ステップS114)、取得した第2の画像に基づいて、影を含む領域を除外してテストライン等の光学濃度を算出する(ステップS116)。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、測定装置及び測定プログラムに係り、特に、クロマトグラフ法を利用したアッセイ用デバイスの測定を行うクロマトグラフ測定装置、特に、被検物質に対する特異的結合物質が固定されたテストラインと測定の終了時を判断するためのコントロールラインの呈色状態を測定して、被検物質を検査する測定装置及び測定プログラムに関する。
【背景技術】
【0002】
近年、被検物質を含有する可能性のある試料(検体溶液)を担体に送液し、免疫学的測定等のアッセイ法を用い、この被検物質について簡便かつ迅速に検査するアッセイ用デバイスが数多く開発されており、体外診断薬や毒物等の検査のための各種デバイスが市販されている。このようなデバイスの一例として、特許文献1に示すようなイムノクロマトグラフ法を利用したものが挙げられる。イムノクロマトグラフ法を利用したデバイスを用いた場合には、その判定・測定に重厚な設備・機器を必要とせず操作が簡便であり、検体溶液を担体上に滴下した後、早いものであれば約5〜10分間静置するだけで測定結果が得られる。そのため、免疫学的測定等のアッセイ法を用いた測定手法は、簡便かつ迅速な特異性の高い測定手法として、多くの場面、例えば病院における臨床検査あるいは研究室における検定試験等で広く使われている。
【0003】
一方、医院や診療所あるいは在宅医療等の診療現場においては、臨床検査の専門家によらず簡便に検査を行うPOCT(Point of Care Testing)診療向けの測定装置として、 イムノクロマトグラフ測定装置(イムノクロマトリーダー)が使用されている。このイムノクロマトグラフ測定装置は、装填されたデバイスの試薬の呈色状態を高感度に測定して、目視判定困難な低呈色状態においても高感度かつ信頼性の高い検査を行うことを可能とする。
【0004】
この試薬の呈色状態を測定する際、測定装置内に入り込んだほこりやゴミ、試薬が収容された試薬ケース等についたほこりやゴミ等からの反射の影響により、誤判定する場合がある。特に、ほこりやゴミ等が試薬の反応ライン上にあり、呈色状態が閾値ぎりぎりの検体の場合、偽陽性、偽陰性となってしまう場合がある。
【0005】
特許文献2には、クロマトグラフィー試験片上に設けた固定化試薬部に測定成分以外のゴミや標識物質の流れ残りなどが残留している場合でも、正確な呈色度を求めて測定成分の濃度を判定できる免疫クロマトグラフィー測定装置が開示されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2008−139297号公報
【特許文献2】特開2009−98080号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
試薬が収容された試薬ケースを測定装置にセットして試薬を撮影し、撮影画像に基づいて試薬の呈色状態を測定する場合、ほこりやゴミの付く場所としては、測定装置の試薬ケースがセットされるガラス面上や、試薬ケースの底面等が考えられる。このほこり等が付着する付着面は、試薬と撮像素子との間に存在するため、これらの付着面にほこり等が付着した場合は、その影が反応ライン上に投影される場合がある。この場合、ほこり等の影が反応ラインの濃度に影響を及ぼし、試薬の呈色状態を精度よく測定できない場合がある。
【0008】
しかしながら、特許文献2に記載された技術は、上記のように試薬と撮像素子との間にほこり等が存在する場合については想定されておらず、精度よく呈色状態を測定するのが困難である、という問題があった。
【0009】
本発明は上記問題点を解決するためになされたものであり、試薬と撮像素子との間にほこり等が存在する場合においても、精度よく呈色状態を測定することができる測定装置及び測定プログラムを提供することを目的とする。
【課題を解決するための手段】
【0010】
上記課題を解決するため、請求項1記載の発明の測定装置は、撮像素子と、試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、前記試薬紙に向けて照射光を照射する光源と、前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御する制御手段と、前記第1の画像に基づいて、前記付着物の位置を算出する付着物位置算出手段と、前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出する影位置算出手段と、前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出する光学濃度算出手段と、を備えたことを特徴とする。
【0011】
この発明によれば、試料が試薬紙に供給された後に、付着面に焦点を合わせて撮像した第1の画像に基づいて付着物の位置を算出し、付着物の位置、光源の位置、付着面の位置、及び試薬紙の位置に基づいて、付着物の試薬紙上の影の位置を算出し、試薬紙に焦点を合わせて撮像した第2の画像に基づいてテストライン領域の光学濃度を算出すると共に、影の位置がテストライン領域内の場合に、テストライン領域のうち影を含む領域を除外してテストライン領域の光学濃度を算出する。このため、試薬と撮像素子との間にほこり等が存在する場合においても、精度よくテストライン領域の呈色状態を測定することができる。
【0012】
なお、請求項2に記載したように、前記制御手段は、前記試料が前記試薬紙に供給された後、前記試薬の反応が終了するまでの間に、前記第1の画像を複数回取得し、前記影位置算出手段は、取得した複数の前記第1の画像に基づいて、前記影の位置を算出するようにしてもよい。
【0013】
請求項3記載の発明の測定プログラムは、コンピュータを、請求項1又は請求項2記載の測定装置を構成する各手段として機能させるための測定プログラムである。
【0014】
請求項4記載の発明の測定方法は、撮像素子と、試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、前記試薬紙に向けて照射光を照射する光源と、を備えた測定装置により実行される測定方法であって、前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御し、前記第1の画像に基づいて、前記付着物の位置を算出し、前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出し、前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出することを特徴とする。
【発明の効果】
【0015】
本発明によれば、試薬と撮像素子との間にほこり等が存在する場合においても、精度よく呈色状態を測定することができる、という効果を有する。
【図面の簡単な説明】
【0016】
【図1】クロマトグラフ測定装置を示す概略斜視図である。
【図2】図1のI−I線におけるクロマトグラフ測定装置の内部を示す概略図である。
【図3】(A)はクロマトグラフ測定装置に装填されるアッセイ用デバイスを示す概略上面図、(B)はクロマトグラフ測定装置に装填されるアッセイ用デバイスを示す概略底面図、(C)は(A)のII−II線におけるアッセイ用デバイスの断面を示す概略断面図である。
【図4】第1の測定部上にセットされたイムノクロマト用デバイスを示す図である。
【図5】試薬紙の平面図である。
【図6】制御部で実行される処理のフローチャートである。
【図7】影の位置の算出について説明するための図である。
【図8】コンピュータの構成図である。
【発明を実施するための形態】
【0017】
以下、本発明の実施形態について図面を用いて説明するが、本発明はこれに限られるものではない。なお、視認しやすくするため、図面中の各構成要素の縮尺等は実際のものとは適宜異ならせてある。
【0018】
(クロマトグラフ測定装置)
【0019】
まず、本実施形態に係るクロマトグラフ測定装置11の構成について説明する。図1は本実施形態に係るクロマトグラフ測定装置11の外観を示す概略斜視図であり、図2はイムノクロマト用デバイス120が装填され、図1におけるI−I線で切断した場合の内部を示す概略図である。また、図3(A)、(B)はそれぞれイムノクロマト用デバイス120の外観を示す概略上面図及び概略底面図、同図(C)は同図(A)のII−II線における概略断面図である。
【0020】
図1及び図2に示すように、クロマトグラフ測定装置11は、筐体110と、筐体110の表面に配置された画面表示部111、画面表示部111に表示されたメニューの操作を行うためのメニュー操作部112及び電源スイッチ113と、イムノクロマト用デバイス120を装置内部に装填するためのデバイス装填部114と、さらに装置1の内部を構成する、イムノクロマト用デバイス120から情報を取得する第1の測定部140及び第2の測定部150と、第1の測定部140により取得された情報に基づいて被検物質の検査結果の有効性判定及び増幅要否判定を行う判定部132と、所定の動作処理を装置に行わせるための動作モードを選択可能とする動作モード選択部134と、処理プログラムや各種データを記憶する記憶部136と、イムノクロマト用デバイス120内の不溶性担体121に増幅溶液を展開する増幅溶液供給部160と、上記第1の測定部140、第2の測定部150、判定部132、動作モード選択部134及び増幅溶液供給部160を制御する制御部130とを備えている。
【0021】
また、図3(A)〜(C)に示すように、イムノクロマト用デバイス120は、2つのテストライン(A及びB)とコントロールラインCとを有する不溶性担体121(試薬)と、不溶性担体121を収容するためのデバイス用筐体122と、不溶性担体121に試薬溶液を注入するための溶液注入口123と、デバイス用筐体122に収容された不溶性担体121の検査部位121aを観察するための観察窓124とを備えており、デバイス用筐体122の表面には情報表示部125が設けられている。なお、観察窓124は、例えばガラスやプラスチック等の透明部材で構成されている。
【0022】
以下、上記測定装置11について説明する。
【0023】
(判定部)
【0024】
クロマトグラフ測定装置11の判定部132は、第1の測定部140により測定された検査部位の呈色状態に基づいて、被検物質の検査結果の有効性判定及び増幅要否判定を行うものである。有効性判定により、検査の進行状態(溶液の展開状態、テストラインにおける被検物質及び標識物質の捕捉状態、及びコントロールラインにおける標識物質の捕捉状態等)が正常であり、その後得られる結果が信頼に足るか否か、または検査が正常に終了しその結果が信頼に足るか否かが判定される。これらの場合において、信頼に足る場合には有効判定が出され、信頼に足らない場合にはエラー判定が出される。一方、増幅要否判定により、検査部位の呈色状態を増幅させる必要があるか否かが判定され、必要がある場合には増幅必要判定が、必要がない場合には増幅不要判定が出される。
【0025】
ここで、テストラインAは、被検出物質Aを検査するテストラインであり、テストラインBは被検出物質Aと異なる被検出物質Bを検査するテストラインであり、コントロールラインCは検査の終了(標識物質が当該地点まで送液されていること)を示すコントロールラインである。そして、テストラインA及びテストラインBはそれぞれ被検物質A及びBが検査されると呈色し、Cラインは被検物質の有無に関わらず、検査が終了すれば呈色する。
【0026】
(有効性判定)
【0027】
検査の進行段階において、判定部132よりエラー判定が出される場合としては、例えば、上記進行状態が正常でない恐れがあるため、何らかの検査結果が得られたとしてもその結果の信頼性が低いと判断された場合等が挙げられる。検査の進行状態が正常でない場合としては、例えばイムノクロマト用デバイス120を再使用しているために検査の初期段階にもかかわらずコントロールラインが呈色していた場合等が挙げられる。検査の終了段階において、判定部132より有効判定が出された場合には、判定部132は当該検査結果が陽性か陰性かの判定も行う。検査の終了段階において、判定部132よりエラー判定が出される場合としては、例えば、上記進行状態が正常でなかったため正常な検査結果を得ることができなかった場合が挙げられる。
【0028】
(増幅要否判定)
【0029】
判定部132より増幅必要判定が出される場合としては、例えば、もともと検体溶液中の被検物質の濃度が低いために、或いは検査ライン(テストライン及びコントロールライン)についての試薬等の性質上当該検査自体の反応完了時間が長いために、検査の進行状態が、そのまま検査を進行させたとしても相当の時間を要しなければ検査結果を得ることができない状態にあると予測された場合が挙げられる。ここで、上記進行状態のどのポイントで増幅要否判定を行うかについては、任意に設定することができる。相当の時間を要するか否かの予測は、経時的に計測した呈色状態の変化に基づいて予測することができ、例えば光学濃度の変化率に基づいて予測することができる。判定部132より増幅不要判定が出される場合としては、例えば、検体溶液中の被検物質の濃度が高いために或いは当該検査自体の反応完了時間が短いために、上記進行状態が、すでに検査結果を得ることができる状態にあると判断された場合、或いは相当の時間を要せずに検査結果を得ることができる状態にあると予測された場合が挙げられる。
【0030】
有効性判定及び増幅要否判定を検査の進行上どのタイミングで行うかは特に制限されないが、最も基本的な検査工程としては、検体溶液注入から所定時間経過後、増幅要否判定、有効性判定の順に判定を行って最終的な検査結果を得るというものである。上記所定時間は、検査目的や検査結果取得の時間短縮等に応じて医師等の使用者によって適宜設定される。例えば、この所定時間を短く設定すれば、早い段階で増幅要否判定を行いかつ必要に応じて増幅工程を行えるため、検査結果を取得するまでの時間を短縮することができる。また、後述するように、検査初期段階における進行状態の異常を検知するために、例えば増幅要否判定の前に別途有効性判定を上記基本的な検査工程に追加することもできる。
【0031】
(動作モード選択部)
【0032】
動作モード選択部134は、予め設定された所定の動作処理を装置に行わせるための動作モードを格納している。そして、格納されている動作モードは制御部130を介して画面表示部111にメニューとして表示され、測定装置11の使用者はメニュー操作部112を操作してこのメニューの中から動作モードを選択することができる。これにより使用者は検査目的に適合した測定を実施することができる。
【0033】
動作モード選択部134は、例えば動作モードとして、検体溶液を不溶性担体に点着してから予め設定された所定時間の経過時に、テストライン及びコントロールラインの光学濃度及び色度を測定手段に測定させ、すべてのラインについての光学濃度及び色度が所定値に達した場合には、判定手段に増幅要否判定を増幅不要と判定させて、増幅を行わず被検物質の検査結果について有効性判定を行わせ、それ以外の場合には、判定手段に増幅要否判定を増幅必要と判定させて、増幅手段に呈色状態を増幅させ、増幅後、判定手段に被検物質の検査結果について有効性判定を行わせる動作モード(第1の動作モード)を格納している。このような動作モードによれば、1つのイムノクロマト用デバイス120に複数のテストラインがある場合に、すべてのテストラインについて信頼性の高い検査を行うことができる。
【0034】
また、イムノクロマト用デバイス120にテストラインが2つ以上ある場合に、測定装置11が、この2つ以上のテストラインの一部を検査対象として指定可能とする指定手段を備えている場合には、動作モード選択部134は、例えば他の動作モードとして、検体溶液を不溶性担体に点着してから予め設定された所定時間の経過時に、テストライン及びコントロールラインの光学濃度及び色度を測定手段に測定させ、指定手段に指定されたテストライン及びコントロールラインについての光学濃度及び色度が所定値に達した場合には、判定手段に増幅要否判定を増幅不要と判定させて、増幅を行わず被検物質の検査結果について判定を行わせ、それ以外の場合には、判定手段に増幅要否判定を増幅必要と判定させて、増幅手段に呈色状態を増幅させ、増幅後、判定手段に被検物質の検査結果について有効性判定を行わせる動作モード(第2の動作モード)を格納している。このような動作モードによれば、無駄な検査時間を低減し、指定したテストラインについて効率よく検査を行うことができる。
【0035】
(測定部)
【0036】
第1の測定部140は、イムノクロマト用デバイス120の観察窓124を通して検査部位121aの呈色状態を測定し、検査部位121aにおける光学的情報を取得するものである。第1の測定部140は、図2に示すように、イメージセンサ142、光源144、及び光学レンズ(図2では図示省略)を含んで構成され、イムノクロマト用デバイス120が測定装置11に装填された際に、これらがイムノクロマト用デバイス120の下方に配して観察窓124に対向するように構成されている。そして、第1の測定部140によって取得された検査部位121aにおける光学的情報、すなわち撮影画像に基づいて、検査部位121aの呈色状態として光学濃度及び色度が算出される。なお、詳細は後述するが、本実施形態では、イメージセンサ142により撮影された撮影画像から、ほこり等の影響を除去した除去画像を求め、求めた除去画像に基づいて、検査部位121aの呈色状態として光学濃度及び色度が算出される。
【0037】
イメージセンサ142は、例えば複数のフォトダイオードがライン状に配列された構成、或いはエリアセンサといった光学センサを備える構成とされており、受光した光の輝度に応じた出力を生じる。イメージセンサ142の受光範囲は、イムノクロマト用デバイス120の長手方向に延びた帯状とされている。光源144は、例えばLEDが内蔵されたモジュールであり、白色光を発するように構成されている。なお、光源144は、増幅前後の色度の区別が付けば例えば単色光を発するものでもよい。また光源144は、モジュールを複数備える場合には、異なる波長の単色光を発する複数のモジュールを用いることもできる。光源144から照射される光は、イムノクロマト用デバイス120の長手方向を照明可能とされている。
【0038】
第2の測定部150は、イムノクロマト用デバイス120の情報表示部125に照明光を照射し、情報表示部125に表示された情報を取得するものである。情報表示部125は、手書きまたはシール添付等により検査に関する情報が表示されている。検査に関する情報とは例えば、被検物質を採取した患者に関する情報(氏名、年齢及び性別等)及び検査に使用される試料・試薬に関する情報(検査対象となる被検物質、洗浄液及び増幅溶液等の名称等)等が挙げられる。情報を取得する方法は、特に制限されず、情報表示部125をそのまま画像化したりバーコード化された情報から読み取ったりすることができる。第2の測定部150は、図2に示すようにイメージセンサ152と光源154とを備え、イムノクロマト用デバイス120が測定装置11に装填された際に、これらがイムノクロマト用デバイス120の上方に配して情報表示部125に対向するように構成されている。そして、第2の測定部150によって取得された検査に関する情報と検査結果とが紐付けされて管理される。イメージセンサ152及び光源154については、上記イメージセンサ142及び光源144とそれぞれ同様である。
【0039】
(光学濃度)
【0040】
光学濃度は、アッセイ用デバイスの検査部位に入射された入射光の強度をI、検査部位からの反射光の強度をIrとしたとき、下記(1)式により定める。
【0041】
光学濃度=−log10(Ir/I) ・・・(1)
【0042】
(色度)
【0043】
また、色度は、色相と彩度を数量的に表示したものであり、イメージセンサで読み取ったRGB輝度信号から算出する。色度の表色系としては、一般的なCIE表色系を用いることができる。
【0044】
(増幅溶液供給部)
【0045】
増幅溶液供給部160は、銀イオン含有化合物を含む増幅溶液を貯蔵する増幅溶液貯蔵ポット162と、増幅溶液貯蔵ポット162から増幅溶液を注入する増幅溶液注入ノズル162aと、上記増幅溶液に含まれる銀イオンを還元する還元剤を貯蔵する還元剤貯蔵ポット164と、還元剤貯蔵ポット164から還元剤を注入する還元剤注入ノズル164aとを備え、増幅溶液貯蔵ポット162及び還元剤貯蔵ポット164のそれぞれに貯蔵された液体を、それぞれの注入ノズル162a・164aを通して装填されたイムノクロマト用デバイス120の溶液注入口123に注入することができるように構成されている。液体の注入は、例えば増幅溶液供給部160を駆動装置により駆動させて順に或いは交互にそれぞれの注入ノズルから別個に注入するようにしてもよく、また2つのノズルを先端部で結合させてそれぞれの貯蔵ポットから供給された液体を同時に注入するようにしてもよい。
【0046】
なお、増幅溶液供給部160は上記構成に限定されるものではない。例えば、それぞれの貯蔵ポットに貯蔵する溶液の組み合わせを増幅溶液及び洗浄液等の組み合わせにしてもよく、また増幅溶液を貯蔵するポット単独で構成してもよい。さらに、溶液を貯蔵する貯蔵ポットは、必ずしも測定装置11の内部に備える必要はない。例えば、貯蔵ポットを測定装置(筐体110)の外部に設け、注入ノズルのみを操作して溶液注入口123に溶液を注入するように構成してもよい。
【0047】
(クロマトグラフ測定方法)
【0048】
次に本発明のクロマトグラフ測定方法について説明する。
【0049】
本実施形態に係る測定方法は、被検物質に対する特異的結合物質が固定されたテストラインと、測定の終了時を判断するためのコントロールラインと、固定化された標識物質とを有する不溶性担体121を備えるイムノクロマト用デバイス120を用意し、このイムノクロマト用デバイス120の溶液注入口123に検査対象である被検物質を含有しうる検体溶液を注入し、不溶性担体121に検体溶液を点着してから所定時間経過後、検査部位121aにおける呈色状態として光学濃度及び色度を測定し、この光学濃度及び色度に基づいて増幅要否判定(第1の判定)を行い、テストライン(A及びB)及びコントロールラインCの少なくとも1つの光学濃度及び色度が所定値に達しなかったため、増幅要否判定の結果、増幅必要判定が出された場合には、不溶性担体121に還元剤(ここで、還元剤は洗浄液としても機能する。)を展開することによりテストライン(A及びB)及びコントロールラインCを洗浄し(洗浄処理)、不溶性担体121に増幅溶液を展開することにより、銀イオンの還元により形成された銀微粒子を標識物質に沈着させて呈色状態を増幅させ(増幅処理)、増幅された呈色状態の光学濃度及び色度を測定して、この光学濃度及び色度に基づいて有効性判定(第2の判定)を行い、それ以外の場合には、上記増幅工程(洗浄処理、増幅処理を含む)を行わず、増幅要否判定(第1の判定)時の光学濃度及び色度に基づいて有効性判定(第2の判定)を行うものである。
【0050】
そして、本発明に係るクロマトグラフ測定方法において、上記所定時間は5分〜20分であることが好ましい。また、第2の判定を第1の判定後1分〜20分以内に行うことが好ましい。つまり、このように時間設定をすることにより、早い段階で増幅の要否が判断できてより迅速に検査結果を得ることができる。
【0051】
検体溶液の展開方向と洗浄液の展開方向との成す角は45度から170度であることが好ましく、不溶性担体は多孔性担体であることが好ましい。
【0052】
(検体溶液)
【0053】
本発明のアッセイ用デバイスを用いて分析することのできる検体溶液としては、被検物質(天然物、毒素、ホルモンまたは農薬等の生理活性物質あるいは環境汚染物質等)を含む可能性のあるものである限り、特に限定されるものではなく、例えば、生物学的試料、特には動物(特にヒト)の体液(例えば、血液、血清、血漿、髄液、涙液、汗、尿、膿、鼻水、又は喀痰)若しくは排泄物(例えば、糞便)、臓器、組織、粘膜や皮膚、それらを含むと考えられる搾過検体(スワブ)、うがい液、又は動植物それ自体若しくはそれらの乾燥体を後述の希釈液で希釈したもの等を挙げることができる。
【0054】
上記検体溶液はそのままで、あるいは、検体溶液を適当な抽出用溶媒を用いて抽出して得られる抽出液の形で、さらには、この抽出液を適当な希釈剤で希釈して得られる希釈液の形、若しくは抽出液を適当な方法で濃縮した形で用いることができる。
【0055】
(標識物質)
【0056】
本発明で使用することができる標識物質としては、一般的なイムノクロマトグラフ法で用いられるような金属微粒子(又は金属コロイド)、着色ラテックス粒子、酵素など、有色で視認できる、または、反応により検査できるようになる標識物であれば特に限定されることなく用いることができるが、標識物質を触媒とした金属イオンの還元反応によって、標識物質への金属の沈着でシグナルを増幅する場合には、その触媒活性の観点から金属微粒子が好ましい。
【0057】
金属微粒子の材料としては、金属単体、金属硫化物、その他金属合金、または金属を含むポリマ−粒子標識を用いることができる。粒子(又はコロイド)の平均粒径は、1nm〜10μmの範囲が好ましい。ここで、平均粒径とは、透過型電子顕微鏡(TEM)により実測された複数の粒子の径(粒子の最長径)の平均値である。より詳細には、金コロイド、銀コロイド、白金コロイド、鉄コロイド、水酸化アルミニウムコロイド、及びこれらの複合コロイドなどが挙げられ、好ましくは、金コロイド、銀コロイド、白金コロイド、及びこれらの複合コロイドであることが望ましい。特に、金コロイドと銀コロイドが適当な粒径において、金コロイドは赤色、銀コロイドは黄色を示し視認度が高いという観点からより好ましい。金コロイドを用いることにより、銀イオン含有化合物を用いた増幅工程を行うことにより増幅の前後で標識の色度が変化する(金コロイドは赤く呈色し、増幅後は還元された銀イオンが金コロイドに沈着し黒くなる)ため、後述するようにこの変化を検査のエラー判定に用いることができるようになる。金属コロイドの平均粒径としては、約1〜500nmが好ましく、さらには1〜100nmがより好ましい。
【0058】
(特異的結合物質)
【0059】
特異的結合物質としては、被検物質に対して親和性を持つものならば特に限定されることはなく例えば、被検物質が抗原である場合には当該抗原に対する抗体、被検物質がたんぱく質、金属イオンまたは低分子量有機化合物である場合にはこれらに対するアプタマー、被検物質がDNAやRNAなど核酸である場合にはこれらに対して相補的な配列を持つDNAやRNA等の核酸分子、被検物質がアビジンである場合にはビオチン、被検物質が特定のペプチドの場合にはこれに特異的に結合する錯体、等を挙げることができる。また、上記した例では特異的結合物質と被検物質との関係を入れ替えることもでき、例えば被検物質が抗体である場合には当該抗体に対する抗原を、特異的結合物質として用いることもできる。さらに、上記のような被検物質に対して親和性を持つ物質を一部に含有する化合物等を特異的結合物質として用いることもできる。
【0060】
上記抗体としては具体的に、その被検物質によって免疫された動物の血清から調製する抗血清、抗血清から精製された免疫グロブリン画分、その被検物質によって免疫された動物の脾臓細胞を用いる細胞融合によって得られるモノクローナル抗体、あるいは、それらの断片[例えば、F(ab’)2、Fab、Fab’、又はFv]を用いることができる。これらの抗体の調製は、常法により行なうことができる。
【0061】
(標識物質のシグナル増幅)
【0062】
標識物質として金属コロイド標識、金属硫化物標識、その他金属合金標識、または金属を含むポリマ−粒子標識を用いるアッセイの場合には、金属系標識の信号を増幅させることができる。具体的には、被検物質と標識物質の複合体の形成後に、無機銀塩、有機銀塩などの銀を含む化合物から供給される銀イオン及び還元剤を接触させ、還元剤によって銀イオンを還元して銀粒子を生成させると、その銀粒子が金属系標識を核として金属系標識上に沈着するので、金属系標識が増幅され、被検物質の分析を高感度に実施することができる。
【0063】
(不溶性担体)
【0064】
不溶性担体121は、検体溶液を滴下する部分である試料添加パッド、被検物質と結合可能な標識物質が固定された標識物質保持パッド、被検物質に対する特異的結合物質が固定された検査部位を有するクロマトグラフ担体、及び送液された検体溶液等を吸収する吸収パッドを有している。検査部位には、それぞれ異なる特異的結合物質が固定された2つのテストラインを設けているが、テストラインの数はこれに限定されず、1つでもよいし3つ以上でもよい。テストラインを複数にすることによって検体溶液に複数の被検物質が含まれる場合に、効率よく一度に複数の被検物質を検査することが可能となる。不溶性担体121の材料は、多孔性であることが好ましく、例えば、ニトロセルロース膜、セルロース膜、アセチルセルロース膜、ポリスルホン膜、ポリエーテルスルホン膜、ナイロン膜、ガラス繊維、不織布、布、または糸等が好ましく挙げられる。
【0065】
クロマトグラフ担体には、被検物質に対する特異的結合物質を固定化させて検査ラインや所望によりコントロール部位が作製される。特異的結合物質は、特異的結合物質をクロマトグラフ担体の一部に物理的または化学的結合により直接固定化させてもよいし、特異的結合物質をラテックス粒子などの微粒子に物理的または化学的に結合させ、この微粒子をクロマトグラフ担体の一部にトラップさせて固定化させてもよい。
【0066】
標識物質保持パッドは、前述の標識物質を含む懸濁液を調製し、その懸濁液を適当なパッド(例えば、グラスファイバーパッド)に塗布した後、それを乾燥することにより調製したものである。これにより、不溶性担体に検体溶液が注入された場合、標識物質が被検物質と共に展開されながら当該被検物質に結合して、検査部位まで流される。
【0067】
試料添加パッドは試料(検体溶液等)を点着する部分であって、試料中の不溶物粒子等を濾過する機能をも兼ねる部分である。なお、分析の際、検体溶液中の被検物質が試料添加部の材質に非特異的に吸着し、分析の精度を低下させることを防止するため、試料添加パッドは予め非特異的吸着防止処理されて用いられることもある。
【0068】
吸収パッドは、添加された試料がクロマト移動により物理的に吸収されると共に、クロマトグラフ担体の検査ラインに不溶化されない未反応標識物質等を吸収除去する部位である。添加された試料のクロマト先端部が吸収部に届いてからのクロマトの速度は、吸収材の材質、大きさなどにより異なるので、その選定により被検物質の測定に合った速度を設定することができる。
【0069】
(増幅溶液)
【0070】
増幅溶液は、含まれる薬剤が標識物質や被検物質の触媒作用によって反応することにより、呈色或いは発光する化合物などを生じ、シグナルの増幅を起こすことができる溶液である。例えば、金属標識上で、物理現像により金属銀の析出を起こす銀イオン溶液である。詳細には、写真化学の分野での一般書物(例えば、「改訂写真工学の基礎-銀塩写真編-」(日本写真学会編、コロナ社)、「写真の化学」(笹井明、写真工業出版社)、「最新処方ハンドブック」(菊池真一他、アミコ出版社))に記載されているような、いわゆる現像液を用いることができる。例えば、増幅溶液として銀イオン含有化合物を含む物理現像液を用いれば、銀イオンの還元剤により液中の銀イオンを、現像の核となるような金属コロイド等を中心に還元させることができる。
【0071】
また別の例としては、酵素反応を用いた例がある。例えば、ペルオキシダーゼ標識と過酸化水素の作用により色素となる、フェニレンジアミン化合物とナフトール化合物の溶液などが挙げられる。さらに、非特許文献「臨床検査 Vol.41 no.9 p.1020 H2O2−POD系を利用した染色」に記載されているような、西洋わさびペルオキシダーゼ検出の発色基質などでもよい。また、特開2009−156612に記載の発色基質は特に好ましく用いることができる。なお、酵素の代わりに白金微粒子などの金属触媒を用いる系でもよい。
【0072】
別の酵素を用いた例としては、アルカリホスファターゼを標識とし、5−ブロモ−4クロロ−3−インドリル−リン酸二ナトリウム塩(BCIP)を基質として発色させるような系もある。以上、呈色する反応を代表に挙げたが、一般的にエンザイムイムノアッセイで用いられるような、酵素と基質の組み合わせであればなんでも良く、化学発光する基質であっても、蛍光を発する基質であってもよい。
【0073】
(銀イオン含有化合物)
【0074】
銀イオン含有化合物としては、有機銀塩、無機銀塩、もしくは銀錯体を用いることができる。好ましくは、水などの溶媒に対して溶解度の高い銀イオン含有化合物であり、硝酸銀、酢酸銀、乳酸銀、酪酸銀、チオ硫酸銀などが挙げられる。特に好ましくは硝酸銀である。銀錯体としては、水酸基やスルホン基など水溶性基を有する配位子に配位された銀錯体が好ましく、ヒドロキシチオエーテル銀等が挙げられる。無機銀塩、もしくは銀錯体は、銀として一般に0.001モル/m2〜0.2モル/m2、好ましくは0.01モル/m2〜0.05モル/m2含有されることが好ましい。
【0075】
(銀イオンの還元剤)
【0076】
銀イオンの還元剤は、銀イオンを銀に還元することができれば、無機・有機のいかなる材料、またはその混合物でも用いることができる。
【0077】
無機還元剤としては、Fe2+、V2+、Ti3+、などの金属イオンで原子価の変化し得る還元性金属塩、還元性金属錯塩を好ましく挙げることができる。無機還元剤を用いる際には、酸化されたイオンを錯形成するか還元して、除去するか無害化する必要がある。例えば、Fe2+を還元剤として用いる系では、クエン酸やEDTAを用いて酸化物であるFe3+の錯体を形成し、無害化することができる。本系ではこのような無機還元剤を用いることが好ましく、より好ましくはFe2+の金属塩が好ましい。
【0078】
なお、本実施形態に係るアッセイ用デバイスを用いて分析することのできる増幅要否判定等の具体例、光学濃度及び色度に基づいた増幅前後の詳細な判定等については詳細な説明は省略するが、例えば本出願人が出願した特願2009−226010号に記載されたものや方法を用いることができる。
【0079】
(ほこり等の影の位置の算出)
【0080】
次に、イメージセンサ142で撮影された撮影画像からほこり等の影の位置を算出し、算出した影の位置に基づいてテストラインの光学濃度を算出する処理について説明する。
【0081】
図4には、第1の測定部140上にイムノクロマト用デバイス120がセットされた状態を示した。図1〜3では図示は省略したが、第1の測定部140のイメージセンサ142及び光学レンズ143の上方はガラス面145で形成されており、このガラス面145上にイムノクロマト用デバイス120がセットされる。
【0082】
なお、光学レンズ143は、制御部130の制御により図4において矢印Y方向に移動可能であり、焦点を試薬紙S(不溶性担体121)、観察窓124、及びガラス面145に合わせることが可能なように構成されている。
【0083】
このような構成の場合、第1の測定部140のガラス面145やイムノクロマト用デバイス120のガラスやプラスチック等の透明部材で構成された観察窓124に微小のほこりやゴミ等の付着物Gが付着する場合がある。この場合、撮影時に光源144から光が照射されると、図4に示すように、付着物Gの影Kが試薬紙S上に投影される。
【0084】
そして、付着物Gの影Kが試薬紙S上に投影された状態で試薬紙Sを撮影すると、図5に示すように、影KがテストラインA、BやコントロールラインC上やその近傍に投影される場合がある。この場合、影Kの影響によって、テストラインA、B、コントロールラインCの呈色状態を判定する際に、誤判定する虞がある。
【0085】
このため、本実施形態では、付着物Gによる影Kの位置を算出し、この影KがテストラインA、BやコントロールラインC上に位置していた場合には、テストラインA、BやコントロールラインCの光学濃度を算出する際に、影Kを含む領域を除外して算出する。
【0086】
次に、制御部130で実行される処理について、図6に示すフローチャートを参照して説明する。
【0087】
なお、図6に示す処理は、イムノクロマト用デバイス120がデバイス装填部114にセットされ、メニュー操作部112が操作されて動作モードが選択されて測定が指示され、検体溶液(試料)が不溶性担体121に点着されてから予め定めた時間の経過後、すなわちテストラインやコントロールラインの呈色状態を適切に測定できる状態になった場合に実行される。
【0088】
まず、ステップS100では、光学レンズ143を移動させ、図7に示すように付着物Gが付着した付着面Fに焦点を合わせる。なお、図7では、イムノクロマト用デバイス120の形状を簡略化して記載し、観察窓124やガラス面145をゴミ等が付着する付着面Fとして表している。
【0089】
ステップS102では、付着面Fをイメージセンサ142により撮影し、撮影画像を第1の画像として取得する。
【0090】
ステップS104では、第1の画像に基づいて、図7に示すように、イメージセンサ142の中心(光学レンズ143の光軸)から付着物Gまでの位置、すなわち距離L5を算出する。このイメージセンサ142の中心から付着物Gまでの距離L5は、以下のようにして得られる。まず、例えば第1の画像に対して二値化処理等の公知の画像処理施して付着物Gを抽出し、抽出した付着物Gの第1の画像の中心(イメージセンサ142の中心)からの画素数を求める。そして、求めた画素数を、画素数を距離に変換する予め定めた変換式により距離に変換する。これにより、イメージセンサ142の中心から付着物Gまでの距離L5を求めることができる。
【0091】
ステップS106では、試薬紙Sに焦点が合うように光学レンズ143を移動させる。
【0092】
ステップS108では、試薬紙Sをイメージセンサ142により撮影し、撮影画像を第2の画像として取得する。
【0093】
ステップS110では、光源144から付着物Gへの仰角θを算出する。仰角θは、図7に示すように、光源144とイメージセンサ142とを結ぶ線と、光源144と付着物Gとを結ぶ線とが成す角度であり、次式により算出することができる。
【0094】
θ=tan−1(L3/(L1−L5)) ・・・(1)
【0095】
ここで、図7に示すように、L1は、イメージセンサ142の中心から光源144までの距離であり、L3は、イメージセンサ142から付着面Fまでの距離であり、L5は、ステップS104で求めたイメージセンサ142の中心から付着物Gまでの距離である。
【0096】
ステップS112では、光源144から影Kまでの距離L2を求める。この距離L2は、次式により算出することができる。
【0097】
L2=L4×tanθ ・・・(2)
【0098】
ここで、L4は、図7に示すように、イメージセンサ142から試薬紙Sまでの距離である。
【0099】
ステップS114では、イメージセンサ142の中心から影Kまでの距離L6を算出する。この距離L6は、次式により算出できる。
【0100】
L6=L1−L2 ・・・(3)
【0101】
ステップS116では、試薬紙Sを撮影した第2の画像に基づいて、テストラインA,B、コントロールラインCの光学濃度を算出する。このとき、図5に示すように、影KがテストラインA,B、コントロールラインC上やその近傍に存在するか否かを判断する。具体的には、ステップS114で算出した影Kの位置、すなわち画像の中心から距離L6に相当する画素数の位置が、テストラインA,BやコントロールラインC上又はその近傍にあるか否かを第2の画像に基づいて判断する。
【0102】
そして、影Kの位置がテストラインA,BやコントロールラインC上又はその近傍に存在する場合には、影Kが存在するラインのうち、影Kを含む領域を除外してそのラインの光学濃度を算出する。
【0103】
例えば図5に示すように、テストラインB上及びその近傍に影Kが存在する場合には、テストラインBが形成された領域のうち、全ての影Kを含む領域Baを、光学濃度を算出する領域から除外する。
【0104】
例えばテストラインAについては影Kが存在しないため、テストラインAが形成された全領域の濃度の例えば平均値をテストラインAの光学濃度とする。
【0105】
テストラインBについては、テストラインBが形成された領域のうち影Kを全て含む領域Baを除外して、その他の領域の光学濃度の例えば平均値をテストラインBの光学濃度とする。
【0106】
コントロールラインCについては、コントロールラインCが形成された領域のうち影Kを含む領域Caを除外して、その他の領域の光学濃度の例えば平均値をコントロールラインCの光学濃度とする。そして、算出した光学濃度に基づいて、各ラインの呈色状態を判定する。
【0107】
このように、本実施形態では、付着面Fに焦点を合わせて撮像した第1の画像に基づいて付着物Gの位置を算出し、付着物Gの位置、光源144の位置、付着面Fの位置、及び試薬紙Sの位置に基づいて、付着物Gの試薬紙S上の影Kの位置を算出し、試薬紙Sに焦点を合わせて撮像した第2の画像に基づいてテストラインA,BやコントロールラインCの光学濃度を算出すると共に、影Kの位置がテストラインA,BやコントロールラインCの領域内(その近傍を含む)の場合に、影Kを含む領域を除外してテストラインA,BやコントロールラインCの光学濃度を算出する。このため、精度よくテストラインやコントロールラインCの呈色状態を判定することができる。
【0108】
なお、付着物Gが付着する付着面Fとしては、本実施形態ではガラス面145及び観察窓124の2つが考えられるため、ガラス面145及び観察窓124の両者について図6に示す処理を実行することが好ましい。これにより、何れの面にほこり等が付着していても、精度よくテストラインやコントロールラインCの呈色状態を判定することができる。
【0109】
また、溶液注入口123に投入された検体溶液(試料)は、図3において左側から右側へ向かって毛細管現象により試薬紙S上を流れていく。このため、流れてくる試料の先端がテストラインA,BやコントロールラインC上に存在するタイミングで第2の画像を撮影すると、これを影と誤判定してしまい、精度よくテストラインA,BやコントロールラインCの呈色状態を判定することができなくなる虞がある。そこで、試料が試薬紙Sに供給された後、テストラインA,BやコントロールラインCの反応が終了するまでの間に、第1の画像を複数回取得し、取得した複数の第1の画像の全てにおいて、同じ位置に存在する同一濃度の領域を影として特定し、その位置を算出するようにしてもよい。これにより、流れてくる試料の先端を影と誤認識してしまうのを防ぐことができる。
【0110】
また、制御部130は、図8に示すようなコンピュータ130で構成できる。コンピュータ130は、CPU(Central Processing Unit)130A、ROM(Read Only Memory)130B、RAM(Random Access Memory)130C、不揮発性メモリ130D、及び入出力インターフェース(I/O)130Eがバス130Fを介して各々接続された構成となっている。この場合、図6に示した処理のプログラムを記憶部136又は不揮発性メモリ130Dに書き込んでおき、これをCPU130Aが読み込んで実行することにより、コンピュータ130が制御部130として機能する。
【0111】
上記実施形態においては、アッセイ法としてイムノクロマトグラフ法について説明したが、本発明のアッセイ法はこれに限定されない。いわゆる免疫反応を用いない系でもよく、例えば、抗体を用いずにDNAやRNAなどの核酸で被検物質を捕捉する系でもよいし、さらには被検物質に対する親和性を持つ別の小分子やペプチド、たんぱく質、錯体形成物質等、によって被検物質を捕捉する系であってもよい。
【符号の説明】
【0112】
11 クロマトグラフ測定装置
114 デバイス装填部
120 イムノクロマト用デバイス
121 不溶性担体
122 デバイス用筐体
124 観察窓
130 制御部
132 判定部
134 動作モード選択部
136 記憶部
140 測定部
142 イメージセンサ
143 光学レンズ
144 光源
145 ガラス面
【技術分野】
【0001】
本発明は、測定装置及び測定プログラムに係り、特に、クロマトグラフ法を利用したアッセイ用デバイスの測定を行うクロマトグラフ測定装置、特に、被検物質に対する特異的結合物質が固定されたテストラインと測定の終了時を判断するためのコントロールラインの呈色状態を測定して、被検物質を検査する測定装置及び測定プログラムに関する。
【背景技術】
【0002】
近年、被検物質を含有する可能性のある試料(検体溶液)を担体に送液し、免疫学的測定等のアッセイ法を用い、この被検物質について簡便かつ迅速に検査するアッセイ用デバイスが数多く開発されており、体外診断薬や毒物等の検査のための各種デバイスが市販されている。このようなデバイスの一例として、特許文献1に示すようなイムノクロマトグラフ法を利用したものが挙げられる。イムノクロマトグラフ法を利用したデバイスを用いた場合には、その判定・測定に重厚な設備・機器を必要とせず操作が簡便であり、検体溶液を担体上に滴下した後、早いものであれば約5〜10分間静置するだけで測定結果が得られる。そのため、免疫学的測定等のアッセイ法を用いた測定手法は、簡便かつ迅速な特異性の高い測定手法として、多くの場面、例えば病院における臨床検査あるいは研究室における検定試験等で広く使われている。
【0003】
一方、医院や診療所あるいは在宅医療等の診療現場においては、臨床検査の専門家によらず簡便に検査を行うPOCT(Point of Care Testing)診療向けの測定装置として、 イムノクロマトグラフ測定装置(イムノクロマトリーダー)が使用されている。このイムノクロマトグラフ測定装置は、装填されたデバイスの試薬の呈色状態を高感度に測定して、目視判定困難な低呈色状態においても高感度かつ信頼性の高い検査を行うことを可能とする。
【0004】
この試薬の呈色状態を測定する際、測定装置内に入り込んだほこりやゴミ、試薬が収容された試薬ケース等についたほこりやゴミ等からの反射の影響により、誤判定する場合がある。特に、ほこりやゴミ等が試薬の反応ライン上にあり、呈色状態が閾値ぎりぎりの検体の場合、偽陽性、偽陰性となってしまう場合がある。
【0005】
特許文献2には、クロマトグラフィー試験片上に設けた固定化試薬部に測定成分以外のゴミや標識物質の流れ残りなどが残留している場合でも、正確な呈色度を求めて測定成分の濃度を判定できる免疫クロマトグラフィー測定装置が開示されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2008−139297号公報
【特許文献2】特開2009−98080号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
試薬が収容された試薬ケースを測定装置にセットして試薬を撮影し、撮影画像に基づいて試薬の呈色状態を測定する場合、ほこりやゴミの付く場所としては、測定装置の試薬ケースがセットされるガラス面上や、試薬ケースの底面等が考えられる。このほこり等が付着する付着面は、試薬と撮像素子との間に存在するため、これらの付着面にほこり等が付着した場合は、その影が反応ライン上に投影される場合がある。この場合、ほこり等の影が反応ラインの濃度に影響を及ぼし、試薬の呈色状態を精度よく測定できない場合がある。
【0008】
しかしながら、特許文献2に記載された技術は、上記のように試薬と撮像素子との間にほこり等が存在する場合については想定されておらず、精度よく呈色状態を測定するのが困難である、という問題があった。
【0009】
本発明は上記問題点を解決するためになされたものであり、試薬と撮像素子との間にほこり等が存在する場合においても、精度よく呈色状態を測定することができる測定装置及び測定プログラムを提供することを目的とする。
【課題を解決するための手段】
【0010】
上記課題を解決するため、請求項1記載の発明の測定装置は、撮像素子と、試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、前記試薬紙に向けて照射光を照射する光源と、前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御する制御手段と、前記第1の画像に基づいて、前記付着物の位置を算出する付着物位置算出手段と、前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出する影位置算出手段と、前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出する光学濃度算出手段と、を備えたことを特徴とする。
【0011】
この発明によれば、試料が試薬紙に供給された後に、付着面に焦点を合わせて撮像した第1の画像に基づいて付着物の位置を算出し、付着物の位置、光源の位置、付着面の位置、及び試薬紙の位置に基づいて、付着物の試薬紙上の影の位置を算出し、試薬紙に焦点を合わせて撮像した第2の画像に基づいてテストライン領域の光学濃度を算出すると共に、影の位置がテストライン領域内の場合に、テストライン領域のうち影を含む領域を除外してテストライン領域の光学濃度を算出する。このため、試薬と撮像素子との間にほこり等が存在する場合においても、精度よくテストライン領域の呈色状態を測定することができる。
【0012】
なお、請求項2に記載したように、前記制御手段は、前記試料が前記試薬紙に供給された後、前記試薬の反応が終了するまでの間に、前記第1の画像を複数回取得し、前記影位置算出手段は、取得した複数の前記第1の画像に基づいて、前記影の位置を算出するようにしてもよい。
【0013】
請求項3記載の発明の測定プログラムは、コンピュータを、請求項1又は請求項2記載の測定装置を構成する各手段として機能させるための測定プログラムである。
【0014】
請求項4記載の発明の測定方法は、撮像素子と、試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、前記試薬紙に向けて照射光を照射する光源と、を備えた測定装置により実行される測定方法であって、前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御し、前記第1の画像に基づいて、前記付着物の位置を算出し、前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出し、前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出することを特徴とする。
【発明の効果】
【0015】
本発明によれば、試薬と撮像素子との間にほこり等が存在する場合においても、精度よく呈色状態を測定することができる、という効果を有する。
【図面の簡単な説明】
【0016】
【図1】クロマトグラフ測定装置を示す概略斜視図である。
【図2】図1のI−I線におけるクロマトグラフ測定装置の内部を示す概略図である。
【図3】(A)はクロマトグラフ測定装置に装填されるアッセイ用デバイスを示す概略上面図、(B)はクロマトグラフ測定装置に装填されるアッセイ用デバイスを示す概略底面図、(C)は(A)のII−II線におけるアッセイ用デバイスの断面を示す概略断面図である。
【図4】第1の測定部上にセットされたイムノクロマト用デバイスを示す図である。
【図5】試薬紙の平面図である。
【図6】制御部で実行される処理のフローチャートである。
【図7】影の位置の算出について説明するための図である。
【図8】コンピュータの構成図である。
【発明を実施するための形態】
【0017】
以下、本発明の実施形態について図面を用いて説明するが、本発明はこれに限られるものではない。なお、視認しやすくするため、図面中の各構成要素の縮尺等は実際のものとは適宜異ならせてある。
【0018】
(クロマトグラフ測定装置)
【0019】
まず、本実施形態に係るクロマトグラフ測定装置11の構成について説明する。図1は本実施形態に係るクロマトグラフ測定装置11の外観を示す概略斜視図であり、図2はイムノクロマト用デバイス120が装填され、図1におけるI−I線で切断した場合の内部を示す概略図である。また、図3(A)、(B)はそれぞれイムノクロマト用デバイス120の外観を示す概略上面図及び概略底面図、同図(C)は同図(A)のII−II線における概略断面図である。
【0020】
図1及び図2に示すように、クロマトグラフ測定装置11は、筐体110と、筐体110の表面に配置された画面表示部111、画面表示部111に表示されたメニューの操作を行うためのメニュー操作部112及び電源スイッチ113と、イムノクロマト用デバイス120を装置内部に装填するためのデバイス装填部114と、さらに装置1の内部を構成する、イムノクロマト用デバイス120から情報を取得する第1の測定部140及び第2の測定部150と、第1の測定部140により取得された情報に基づいて被検物質の検査結果の有効性判定及び増幅要否判定を行う判定部132と、所定の動作処理を装置に行わせるための動作モードを選択可能とする動作モード選択部134と、処理プログラムや各種データを記憶する記憶部136と、イムノクロマト用デバイス120内の不溶性担体121に増幅溶液を展開する増幅溶液供給部160と、上記第1の測定部140、第2の測定部150、判定部132、動作モード選択部134及び増幅溶液供給部160を制御する制御部130とを備えている。
【0021】
また、図3(A)〜(C)に示すように、イムノクロマト用デバイス120は、2つのテストライン(A及びB)とコントロールラインCとを有する不溶性担体121(試薬)と、不溶性担体121を収容するためのデバイス用筐体122と、不溶性担体121に試薬溶液を注入するための溶液注入口123と、デバイス用筐体122に収容された不溶性担体121の検査部位121aを観察するための観察窓124とを備えており、デバイス用筐体122の表面には情報表示部125が設けられている。なお、観察窓124は、例えばガラスやプラスチック等の透明部材で構成されている。
【0022】
以下、上記測定装置11について説明する。
【0023】
(判定部)
【0024】
クロマトグラフ測定装置11の判定部132は、第1の測定部140により測定された検査部位の呈色状態に基づいて、被検物質の検査結果の有効性判定及び増幅要否判定を行うものである。有効性判定により、検査の進行状態(溶液の展開状態、テストラインにおける被検物質及び標識物質の捕捉状態、及びコントロールラインにおける標識物質の捕捉状態等)が正常であり、その後得られる結果が信頼に足るか否か、または検査が正常に終了しその結果が信頼に足るか否かが判定される。これらの場合において、信頼に足る場合には有効判定が出され、信頼に足らない場合にはエラー判定が出される。一方、増幅要否判定により、検査部位の呈色状態を増幅させる必要があるか否かが判定され、必要がある場合には増幅必要判定が、必要がない場合には増幅不要判定が出される。
【0025】
ここで、テストラインAは、被検出物質Aを検査するテストラインであり、テストラインBは被検出物質Aと異なる被検出物質Bを検査するテストラインであり、コントロールラインCは検査の終了(標識物質が当該地点まで送液されていること)を示すコントロールラインである。そして、テストラインA及びテストラインBはそれぞれ被検物質A及びBが検査されると呈色し、Cラインは被検物質の有無に関わらず、検査が終了すれば呈色する。
【0026】
(有効性判定)
【0027】
検査の進行段階において、判定部132よりエラー判定が出される場合としては、例えば、上記進行状態が正常でない恐れがあるため、何らかの検査結果が得られたとしてもその結果の信頼性が低いと判断された場合等が挙げられる。検査の進行状態が正常でない場合としては、例えばイムノクロマト用デバイス120を再使用しているために検査の初期段階にもかかわらずコントロールラインが呈色していた場合等が挙げられる。検査の終了段階において、判定部132より有効判定が出された場合には、判定部132は当該検査結果が陽性か陰性かの判定も行う。検査の終了段階において、判定部132よりエラー判定が出される場合としては、例えば、上記進行状態が正常でなかったため正常な検査結果を得ることができなかった場合が挙げられる。
【0028】
(増幅要否判定)
【0029】
判定部132より増幅必要判定が出される場合としては、例えば、もともと検体溶液中の被検物質の濃度が低いために、或いは検査ライン(テストライン及びコントロールライン)についての試薬等の性質上当該検査自体の反応完了時間が長いために、検査の進行状態が、そのまま検査を進行させたとしても相当の時間を要しなければ検査結果を得ることができない状態にあると予測された場合が挙げられる。ここで、上記進行状態のどのポイントで増幅要否判定を行うかについては、任意に設定することができる。相当の時間を要するか否かの予測は、経時的に計測した呈色状態の変化に基づいて予測することができ、例えば光学濃度の変化率に基づいて予測することができる。判定部132より増幅不要判定が出される場合としては、例えば、検体溶液中の被検物質の濃度が高いために或いは当該検査自体の反応完了時間が短いために、上記進行状態が、すでに検査結果を得ることができる状態にあると判断された場合、或いは相当の時間を要せずに検査結果を得ることができる状態にあると予測された場合が挙げられる。
【0030】
有効性判定及び増幅要否判定を検査の進行上どのタイミングで行うかは特に制限されないが、最も基本的な検査工程としては、検体溶液注入から所定時間経過後、増幅要否判定、有効性判定の順に判定を行って最終的な検査結果を得るというものである。上記所定時間は、検査目的や検査結果取得の時間短縮等に応じて医師等の使用者によって適宜設定される。例えば、この所定時間を短く設定すれば、早い段階で増幅要否判定を行いかつ必要に応じて増幅工程を行えるため、検査結果を取得するまでの時間を短縮することができる。また、後述するように、検査初期段階における進行状態の異常を検知するために、例えば増幅要否判定の前に別途有効性判定を上記基本的な検査工程に追加することもできる。
【0031】
(動作モード選択部)
【0032】
動作モード選択部134は、予め設定された所定の動作処理を装置に行わせるための動作モードを格納している。そして、格納されている動作モードは制御部130を介して画面表示部111にメニューとして表示され、測定装置11の使用者はメニュー操作部112を操作してこのメニューの中から動作モードを選択することができる。これにより使用者は検査目的に適合した測定を実施することができる。
【0033】
動作モード選択部134は、例えば動作モードとして、検体溶液を不溶性担体に点着してから予め設定された所定時間の経過時に、テストライン及びコントロールラインの光学濃度及び色度を測定手段に測定させ、すべてのラインについての光学濃度及び色度が所定値に達した場合には、判定手段に増幅要否判定を増幅不要と判定させて、増幅を行わず被検物質の検査結果について有効性判定を行わせ、それ以外の場合には、判定手段に増幅要否判定を増幅必要と判定させて、増幅手段に呈色状態を増幅させ、増幅後、判定手段に被検物質の検査結果について有効性判定を行わせる動作モード(第1の動作モード)を格納している。このような動作モードによれば、1つのイムノクロマト用デバイス120に複数のテストラインがある場合に、すべてのテストラインについて信頼性の高い検査を行うことができる。
【0034】
また、イムノクロマト用デバイス120にテストラインが2つ以上ある場合に、測定装置11が、この2つ以上のテストラインの一部を検査対象として指定可能とする指定手段を備えている場合には、動作モード選択部134は、例えば他の動作モードとして、検体溶液を不溶性担体に点着してから予め設定された所定時間の経過時に、テストライン及びコントロールラインの光学濃度及び色度を測定手段に測定させ、指定手段に指定されたテストライン及びコントロールラインについての光学濃度及び色度が所定値に達した場合には、判定手段に増幅要否判定を増幅不要と判定させて、増幅を行わず被検物質の検査結果について判定を行わせ、それ以外の場合には、判定手段に増幅要否判定を増幅必要と判定させて、増幅手段に呈色状態を増幅させ、増幅後、判定手段に被検物質の検査結果について有効性判定を行わせる動作モード(第2の動作モード)を格納している。このような動作モードによれば、無駄な検査時間を低減し、指定したテストラインについて効率よく検査を行うことができる。
【0035】
(測定部)
【0036】
第1の測定部140は、イムノクロマト用デバイス120の観察窓124を通して検査部位121aの呈色状態を測定し、検査部位121aにおける光学的情報を取得するものである。第1の測定部140は、図2に示すように、イメージセンサ142、光源144、及び光学レンズ(図2では図示省略)を含んで構成され、イムノクロマト用デバイス120が測定装置11に装填された際に、これらがイムノクロマト用デバイス120の下方に配して観察窓124に対向するように構成されている。そして、第1の測定部140によって取得された検査部位121aにおける光学的情報、すなわち撮影画像に基づいて、検査部位121aの呈色状態として光学濃度及び色度が算出される。なお、詳細は後述するが、本実施形態では、イメージセンサ142により撮影された撮影画像から、ほこり等の影響を除去した除去画像を求め、求めた除去画像に基づいて、検査部位121aの呈色状態として光学濃度及び色度が算出される。
【0037】
イメージセンサ142は、例えば複数のフォトダイオードがライン状に配列された構成、或いはエリアセンサといった光学センサを備える構成とされており、受光した光の輝度に応じた出力を生じる。イメージセンサ142の受光範囲は、イムノクロマト用デバイス120の長手方向に延びた帯状とされている。光源144は、例えばLEDが内蔵されたモジュールであり、白色光を発するように構成されている。なお、光源144は、増幅前後の色度の区別が付けば例えば単色光を発するものでもよい。また光源144は、モジュールを複数備える場合には、異なる波長の単色光を発する複数のモジュールを用いることもできる。光源144から照射される光は、イムノクロマト用デバイス120の長手方向を照明可能とされている。
【0038】
第2の測定部150は、イムノクロマト用デバイス120の情報表示部125に照明光を照射し、情報表示部125に表示された情報を取得するものである。情報表示部125は、手書きまたはシール添付等により検査に関する情報が表示されている。検査に関する情報とは例えば、被検物質を採取した患者に関する情報(氏名、年齢及び性別等)及び検査に使用される試料・試薬に関する情報(検査対象となる被検物質、洗浄液及び増幅溶液等の名称等)等が挙げられる。情報を取得する方法は、特に制限されず、情報表示部125をそのまま画像化したりバーコード化された情報から読み取ったりすることができる。第2の測定部150は、図2に示すようにイメージセンサ152と光源154とを備え、イムノクロマト用デバイス120が測定装置11に装填された際に、これらがイムノクロマト用デバイス120の上方に配して情報表示部125に対向するように構成されている。そして、第2の測定部150によって取得された検査に関する情報と検査結果とが紐付けされて管理される。イメージセンサ152及び光源154については、上記イメージセンサ142及び光源144とそれぞれ同様である。
【0039】
(光学濃度)
【0040】
光学濃度は、アッセイ用デバイスの検査部位に入射された入射光の強度をI、検査部位からの反射光の強度をIrとしたとき、下記(1)式により定める。
【0041】
光学濃度=−log10(Ir/I) ・・・(1)
【0042】
(色度)
【0043】
また、色度は、色相と彩度を数量的に表示したものであり、イメージセンサで読み取ったRGB輝度信号から算出する。色度の表色系としては、一般的なCIE表色系を用いることができる。
【0044】
(増幅溶液供給部)
【0045】
増幅溶液供給部160は、銀イオン含有化合物を含む増幅溶液を貯蔵する増幅溶液貯蔵ポット162と、増幅溶液貯蔵ポット162から増幅溶液を注入する増幅溶液注入ノズル162aと、上記増幅溶液に含まれる銀イオンを還元する還元剤を貯蔵する還元剤貯蔵ポット164と、還元剤貯蔵ポット164から還元剤を注入する還元剤注入ノズル164aとを備え、増幅溶液貯蔵ポット162及び還元剤貯蔵ポット164のそれぞれに貯蔵された液体を、それぞれの注入ノズル162a・164aを通して装填されたイムノクロマト用デバイス120の溶液注入口123に注入することができるように構成されている。液体の注入は、例えば増幅溶液供給部160を駆動装置により駆動させて順に或いは交互にそれぞれの注入ノズルから別個に注入するようにしてもよく、また2つのノズルを先端部で結合させてそれぞれの貯蔵ポットから供給された液体を同時に注入するようにしてもよい。
【0046】
なお、増幅溶液供給部160は上記構成に限定されるものではない。例えば、それぞれの貯蔵ポットに貯蔵する溶液の組み合わせを増幅溶液及び洗浄液等の組み合わせにしてもよく、また増幅溶液を貯蔵するポット単独で構成してもよい。さらに、溶液を貯蔵する貯蔵ポットは、必ずしも測定装置11の内部に備える必要はない。例えば、貯蔵ポットを測定装置(筐体110)の外部に設け、注入ノズルのみを操作して溶液注入口123に溶液を注入するように構成してもよい。
【0047】
(クロマトグラフ測定方法)
【0048】
次に本発明のクロマトグラフ測定方法について説明する。
【0049】
本実施形態に係る測定方法は、被検物質に対する特異的結合物質が固定されたテストラインと、測定の終了時を判断するためのコントロールラインと、固定化された標識物質とを有する不溶性担体121を備えるイムノクロマト用デバイス120を用意し、このイムノクロマト用デバイス120の溶液注入口123に検査対象である被検物質を含有しうる検体溶液を注入し、不溶性担体121に検体溶液を点着してから所定時間経過後、検査部位121aにおける呈色状態として光学濃度及び色度を測定し、この光学濃度及び色度に基づいて増幅要否判定(第1の判定)を行い、テストライン(A及びB)及びコントロールラインCの少なくとも1つの光学濃度及び色度が所定値に達しなかったため、増幅要否判定の結果、増幅必要判定が出された場合には、不溶性担体121に還元剤(ここで、還元剤は洗浄液としても機能する。)を展開することによりテストライン(A及びB)及びコントロールラインCを洗浄し(洗浄処理)、不溶性担体121に増幅溶液を展開することにより、銀イオンの還元により形成された銀微粒子を標識物質に沈着させて呈色状態を増幅させ(増幅処理)、増幅された呈色状態の光学濃度及び色度を測定して、この光学濃度及び色度に基づいて有効性判定(第2の判定)を行い、それ以外の場合には、上記増幅工程(洗浄処理、増幅処理を含む)を行わず、増幅要否判定(第1の判定)時の光学濃度及び色度に基づいて有効性判定(第2の判定)を行うものである。
【0050】
そして、本発明に係るクロマトグラフ測定方法において、上記所定時間は5分〜20分であることが好ましい。また、第2の判定を第1の判定後1分〜20分以内に行うことが好ましい。つまり、このように時間設定をすることにより、早い段階で増幅の要否が判断できてより迅速に検査結果を得ることができる。
【0051】
検体溶液の展開方向と洗浄液の展開方向との成す角は45度から170度であることが好ましく、不溶性担体は多孔性担体であることが好ましい。
【0052】
(検体溶液)
【0053】
本発明のアッセイ用デバイスを用いて分析することのできる検体溶液としては、被検物質(天然物、毒素、ホルモンまたは農薬等の生理活性物質あるいは環境汚染物質等)を含む可能性のあるものである限り、特に限定されるものではなく、例えば、生物学的試料、特には動物(特にヒト)の体液(例えば、血液、血清、血漿、髄液、涙液、汗、尿、膿、鼻水、又は喀痰)若しくは排泄物(例えば、糞便)、臓器、組織、粘膜や皮膚、それらを含むと考えられる搾過検体(スワブ)、うがい液、又は動植物それ自体若しくはそれらの乾燥体を後述の希釈液で希釈したもの等を挙げることができる。
【0054】
上記検体溶液はそのままで、あるいは、検体溶液を適当な抽出用溶媒を用いて抽出して得られる抽出液の形で、さらには、この抽出液を適当な希釈剤で希釈して得られる希釈液の形、若しくは抽出液を適当な方法で濃縮した形で用いることができる。
【0055】
(標識物質)
【0056】
本発明で使用することができる標識物質としては、一般的なイムノクロマトグラフ法で用いられるような金属微粒子(又は金属コロイド)、着色ラテックス粒子、酵素など、有色で視認できる、または、反応により検査できるようになる標識物であれば特に限定されることなく用いることができるが、標識物質を触媒とした金属イオンの還元反応によって、標識物質への金属の沈着でシグナルを増幅する場合には、その触媒活性の観点から金属微粒子が好ましい。
【0057】
金属微粒子の材料としては、金属単体、金属硫化物、その他金属合金、または金属を含むポリマ−粒子標識を用いることができる。粒子(又はコロイド)の平均粒径は、1nm〜10μmの範囲が好ましい。ここで、平均粒径とは、透過型電子顕微鏡(TEM)により実測された複数の粒子の径(粒子の最長径)の平均値である。より詳細には、金コロイド、銀コロイド、白金コロイド、鉄コロイド、水酸化アルミニウムコロイド、及びこれらの複合コロイドなどが挙げられ、好ましくは、金コロイド、銀コロイド、白金コロイド、及びこれらの複合コロイドであることが望ましい。特に、金コロイドと銀コロイドが適当な粒径において、金コロイドは赤色、銀コロイドは黄色を示し視認度が高いという観点からより好ましい。金コロイドを用いることにより、銀イオン含有化合物を用いた増幅工程を行うことにより増幅の前後で標識の色度が変化する(金コロイドは赤く呈色し、増幅後は還元された銀イオンが金コロイドに沈着し黒くなる)ため、後述するようにこの変化を検査のエラー判定に用いることができるようになる。金属コロイドの平均粒径としては、約1〜500nmが好ましく、さらには1〜100nmがより好ましい。
【0058】
(特異的結合物質)
【0059】
特異的結合物質としては、被検物質に対して親和性を持つものならば特に限定されることはなく例えば、被検物質が抗原である場合には当該抗原に対する抗体、被検物質がたんぱく質、金属イオンまたは低分子量有機化合物である場合にはこれらに対するアプタマー、被検物質がDNAやRNAなど核酸である場合にはこれらに対して相補的な配列を持つDNAやRNA等の核酸分子、被検物質がアビジンである場合にはビオチン、被検物質が特定のペプチドの場合にはこれに特異的に結合する錯体、等を挙げることができる。また、上記した例では特異的結合物質と被検物質との関係を入れ替えることもでき、例えば被検物質が抗体である場合には当該抗体に対する抗原を、特異的結合物質として用いることもできる。さらに、上記のような被検物質に対して親和性を持つ物質を一部に含有する化合物等を特異的結合物質として用いることもできる。
【0060】
上記抗体としては具体的に、その被検物質によって免疫された動物の血清から調製する抗血清、抗血清から精製された免疫グロブリン画分、その被検物質によって免疫された動物の脾臓細胞を用いる細胞融合によって得られるモノクローナル抗体、あるいは、それらの断片[例えば、F(ab’)2、Fab、Fab’、又はFv]を用いることができる。これらの抗体の調製は、常法により行なうことができる。
【0061】
(標識物質のシグナル増幅)
【0062】
標識物質として金属コロイド標識、金属硫化物標識、その他金属合金標識、または金属を含むポリマ−粒子標識を用いるアッセイの場合には、金属系標識の信号を増幅させることができる。具体的には、被検物質と標識物質の複合体の形成後に、無機銀塩、有機銀塩などの銀を含む化合物から供給される銀イオン及び還元剤を接触させ、還元剤によって銀イオンを還元して銀粒子を生成させると、その銀粒子が金属系標識を核として金属系標識上に沈着するので、金属系標識が増幅され、被検物質の分析を高感度に実施することができる。
【0063】
(不溶性担体)
【0064】
不溶性担体121は、検体溶液を滴下する部分である試料添加パッド、被検物質と結合可能な標識物質が固定された標識物質保持パッド、被検物質に対する特異的結合物質が固定された検査部位を有するクロマトグラフ担体、及び送液された検体溶液等を吸収する吸収パッドを有している。検査部位には、それぞれ異なる特異的結合物質が固定された2つのテストラインを設けているが、テストラインの数はこれに限定されず、1つでもよいし3つ以上でもよい。テストラインを複数にすることによって検体溶液に複数の被検物質が含まれる場合に、効率よく一度に複数の被検物質を検査することが可能となる。不溶性担体121の材料は、多孔性であることが好ましく、例えば、ニトロセルロース膜、セルロース膜、アセチルセルロース膜、ポリスルホン膜、ポリエーテルスルホン膜、ナイロン膜、ガラス繊維、不織布、布、または糸等が好ましく挙げられる。
【0065】
クロマトグラフ担体には、被検物質に対する特異的結合物質を固定化させて検査ラインや所望によりコントロール部位が作製される。特異的結合物質は、特異的結合物質をクロマトグラフ担体の一部に物理的または化学的結合により直接固定化させてもよいし、特異的結合物質をラテックス粒子などの微粒子に物理的または化学的に結合させ、この微粒子をクロマトグラフ担体の一部にトラップさせて固定化させてもよい。
【0066】
標識物質保持パッドは、前述の標識物質を含む懸濁液を調製し、その懸濁液を適当なパッド(例えば、グラスファイバーパッド)に塗布した後、それを乾燥することにより調製したものである。これにより、不溶性担体に検体溶液が注入された場合、標識物質が被検物質と共に展開されながら当該被検物質に結合して、検査部位まで流される。
【0067】
試料添加パッドは試料(検体溶液等)を点着する部分であって、試料中の不溶物粒子等を濾過する機能をも兼ねる部分である。なお、分析の際、検体溶液中の被検物質が試料添加部の材質に非特異的に吸着し、分析の精度を低下させることを防止するため、試料添加パッドは予め非特異的吸着防止処理されて用いられることもある。
【0068】
吸収パッドは、添加された試料がクロマト移動により物理的に吸収されると共に、クロマトグラフ担体の検査ラインに不溶化されない未反応標識物質等を吸収除去する部位である。添加された試料のクロマト先端部が吸収部に届いてからのクロマトの速度は、吸収材の材質、大きさなどにより異なるので、その選定により被検物質の測定に合った速度を設定することができる。
【0069】
(増幅溶液)
【0070】
増幅溶液は、含まれる薬剤が標識物質や被検物質の触媒作用によって反応することにより、呈色或いは発光する化合物などを生じ、シグナルの増幅を起こすことができる溶液である。例えば、金属標識上で、物理現像により金属銀の析出を起こす銀イオン溶液である。詳細には、写真化学の分野での一般書物(例えば、「改訂写真工学の基礎-銀塩写真編-」(日本写真学会編、コロナ社)、「写真の化学」(笹井明、写真工業出版社)、「最新処方ハンドブック」(菊池真一他、アミコ出版社))に記載されているような、いわゆる現像液を用いることができる。例えば、増幅溶液として銀イオン含有化合物を含む物理現像液を用いれば、銀イオンの還元剤により液中の銀イオンを、現像の核となるような金属コロイド等を中心に還元させることができる。
【0071】
また別の例としては、酵素反応を用いた例がある。例えば、ペルオキシダーゼ標識と過酸化水素の作用により色素となる、フェニレンジアミン化合物とナフトール化合物の溶液などが挙げられる。さらに、非特許文献「臨床検査 Vol.41 no.9 p.1020 H2O2−POD系を利用した染色」に記載されているような、西洋わさびペルオキシダーゼ検出の発色基質などでもよい。また、特開2009−156612に記載の発色基質は特に好ましく用いることができる。なお、酵素の代わりに白金微粒子などの金属触媒を用いる系でもよい。
【0072】
別の酵素を用いた例としては、アルカリホスファターゼを標識とし、5−ブロモ−4クロロ−3−インドリル−リン酸二ナトリウム塩(BCIP)を基質として発色させるような系もある。以上、呈色する反応を代表に挙げたが、一般的にエンザイムイムノアッセイで用いられるような、酵素と基質の組み合わせであればなんでも良く、化学発光する基質であっても、蛍光を発する基質であってもよい。
【0073】
(銀イオン含有化合物)
【0074】
銀イオン含有化合物としては、有機銀塩、無機銀塩、もしくは銀錯体を用いることができる。好ましくは、水などの溶媒に対して溶解度の高い銀イオン含有化合物であり、硝酸銀、酢酸銀、乳酸銀、酪酸銀、チオ硫酸銀などが挙げられる。特に好ましくは硝酸銀である。銀錯体としては、水酸基やスルホン基など水溶性基を有する配位子に配位された銀錯体が好ましく、ヒドロキシチオエーテル銀等が挙げられる。無機銀塩、もしくは銀錯体は、銀として一般に0.001モル/m2〜0.2モル/m2、好ましくは0.01モル/m2〜0.05モル/m2含有されることが好ましい。
【0075】
(銀イオンの還元剤)
【0076】
銀イオンの還元剤は、銀イオンを銀に還元することができれば、無機・有機のいかなる材料、またはその混合物でも用いることができる。
【0077】
無機還元剤としては、Fe2+、V2+、Ti3+、などの金属イオンで原子価の変化し得る還元性金属塩、還元性金属錯塩を好ましく挙げることができる。無機還元剤を用いる際には、酸化されたイオンを錯形成するか還元して、除去するか無害化する必要がある。例えば、Fe2+を還元剤として用いる系では、クエン酸やEDTAを用いて酸化物であるFe3+の錯体を形成し、無害化することができる。本系ではこのような無機還元剤を用いることが好ましく、より好ましくはFe2+の金属塩が好ましい。
【0078】
なお、本実施形態に係るアッセイ用デバイスを用いて分析することのできる増幅要否判定等の具体例、光学濃度及び色度に基づいた増幅前後の詳細な判定等については詳細な説明は省略するが、例えば本出願人が出願した特願2009−226010号に記載されたものや方法を用いることができる。
【0079】
(ほこり等の影の位置の算出)
【0080】
次に、イメージセンサ142で撮影された撮影画像からほこり等の影の位置を算出し、算出した影の位置に基づいてテストラインの光学濃度を算出する処理について説明する。
【0081】
図4には、第1の測定部140上にイムノクロマト用デバイス120がセットされた状態を示した。図1〜3では図示は省略したが、第1の測定部140のイメージセンサ142及び光学レンズ143の上方はガラス面145で形成されており、このガラス面145上にイムノクロマト用デバイス120がセットされる。
【0082】
なお、光学レンズ143は、制御部130の制御により図4において矢印Y方向に移動可能であり、焦点を試薬紙S(不溶性担体121)、観察窓124、及びガラス面145に合わせることが可能なように構成されている。
【0083】
このような構成の場合、第1の測定部140のガラス面145やイムノクロマト用デバイス120のガラスやプラスチック等の透明部材で構成された観察窓124に微小のほこりやゴミ等の付着物Gが付着する場合がある。この場合、撮影時に光源144から光が照射されると、図4に示すように、付着物Gの影Kが試薬紙S上に投影される。
【0084】
そして、付着物Gの影Kが試薬紙S上に投影された状態で試薬紙Sを撮影すると、図5に示すように、影KがテストラインA、BやコントロールラインC上やその近傍に投影される場合がある。この場合、影Kの影響によって、テストラインA、B、コントロールラインCの呈色状態を判定する際に、誤判定する虞がある。
【0085】
このため、本実施形態では、付着物Gによる影Kの位置を算出し、この影KがテストラインA、BやコントロールラインC上に位置していた場合には、テストラインA、BやコントロールラインCの光学濃度を算出する際に、影Kを含む領域を除外して算出する。
【0086】
次に、制御部130で実行される処理について、図6に示すフローチャートを参照して説明する。
【0087】
なお、図6に示す処理は、イムノクロマト用デバイス120がデバイス装填部114にセットされ、メニュー操作部112が操作されて動作モードが選択されて測定が指示され、検体溶液(試料)が不溶性担体121に点着されてから予め定めた時間の経過後、すなわちテストラインやコントロールラインの呈色状態を適切に測定できる状態になった場合に実行される。
【0088】
まず、ステップS100では、光学レンズ143を移動させ、図7に示すように付着物Gが付着した付着面Fに焦点を合わせる。なお、図7では、イムノクロマト用デバイス120の形状を簡略化して記載し、観察窓124やガラス面145をゴミ等が付着する付着面Fとして表している。
【0089】
ステップS102では、付着面Fをイメージセンサ142により撮影し、撮影画像を第1の画像として取得する。
【0090】
ステップS104では、第1の画像に基づいて、図7に示すように、イメージセンサ142の中心(光学レンズ143の光軸)から付着物Gまでの位置、すなわち距離L5を算出する。このイメージセンサ142の中心から付着物Gまでの距離L5は、以下のようにして得られる。まず、例えば第1の画像に対して二値化処理等の公知の画像処理施して付着物Gを抽出し、抽出した付着物Gの第1の画像の中心(イメージセンサ142の中心)からの画素数を求める。そして、求めた画素数を、画素数を距離に変換する予め定めた変換式により距離に変換する。これにより、イメージセンサ142の中心から付着物Gまでの距離L5を求めることができる。
【0091】
ステップS106では、試薬紙Sに焦点が合うように光学レンズ143を移動させる。
【0092】
ステップS108では、試薬紙Sをイメージセンサ142により撮影し、撮影画像を第2の画像として取得する。
【0093】
ステップS110では、光源144から付着物Gへの仰角θを算出する。仰角θは、図7に示すように、光源144とイメージセンサ142とを結ぶ線と、光源144と付着物Gとを結ぶ線とが成す角度であり、次式により算出することができる。
【0094】
θ=tan−1(L3/(L1−L5)) ・・・(1)
【0095】
ここで、図7に示すように、L1は、イメージセンサ142の中心から光源144までの距離であり、L3は、イメージセンサ142から付着面Fまでの距離であり、L5は、ステップS104で求めたイメージセンサ142の中心から付着物Gまでの距離である。
【0096】
ステップS112では、光源144から影Kまでの距離L2を求める。この距離L2は、次式により算出することができる。
【0097】
L2=L4×tanθ ・・・(2)
【0098】
ここで、L4は、図7に示すように、イメージセンサ142から試薬紙Sまでの距離である。
【0099】
ステップS114では、イメージセンサ142の中心から影Kまでの距離L6を算出する。この距離L6は、次式により算出できる。
【0100】
L6=L1−L2 ・・・(3)
【0101】
ステップS116では、試薬紙Sを撮影した第2の画像に基づいて、テストラインA,B、コントロールラインCの光学濃度を算出する。このとき、図5に示すように、影KがテストラインA,B、コントロールラインC上やその近傍に存在するか否かを判断する。具体的には、ステップS114で算出した影Kの位置、すなわち画像の中心から距離L6に相当する画素数の位置が、テストラインA,BやコントロールラインC上又はその近傍にあるか否かを第2の画像に基づいて判断する。
【0102】
そして、影Kの位置がテストラインA,BやコントロールラインC上又はその近傍に存在する場合には、影Kが存在するラインのうち、影Kを含む領域を除外してそのラインの光学濃度を算出する。
【0103】
例えば図5に示すように、テストラインB上及びその近傍に影Kが存在する場合には、テストラインBが形成された領域のうち、全ての影Kを含む領域Baを、光学濃度を算出する領域から除外する。
【0104】
例えばテストラインAについては影Kが存在しないため、テストラインAが形成された全領域の濃度の例えば平均値をテストラインAの光学濃度とする。
【0105】
テストラインBについては、テストラインBが形成された領域のうち影Kを全て含む領域Baを除外して、その他の領域の光学濃度の例えば平均値をテストラインBの光学濃度とする。
【0106】
コントロールラインCについては、コントロールラインCが形成された領域のうち影Kを含む領域Caを除外して、その他の領域の光学濃度の例えば平均値をコントロールラインCの光学濃度とする。そして、算出した光学濃度に基づいて、各ラインの呈色状態を判定する。
【0107】
このように、本実施形態では、付着面Fに焦点を合わせて撮像した第1の画像に基づいて付着物Gの位置を算出し、付着物Gの位置、光源144の位置、付着面Fの位置、及び試薬紙Sの位置に基づいて、付着物Gの試薬紙S上の影Kの位置を算出し、試薬紙Sに焦点を合わせて撮像した第2の画像に基づいてテストラインA,BやコントロールラインCの光学濃度を算出すると共に、影Kの位置がテストラインA,BやコントロールラインCの領域内(その近傍を含む)の場合に、影Kを含む領域を除外してテストラインA,BやコントロールラインCの光学濃度を算出する。このため、精度よくテストラインやコントロールラインCの呈色状態を判定することができる。
【0108】
なお、付着物Gが付着する付着面Fとしては、本実施形態ではガラス面145及び観察窓124の2つが考えられるため、ガラス面145及び観察窓124の両者について図6に示す処理を実行することが好ましい。これにより、何れの面にほこり等が付着していても、精度よくテストラインやコントロールラインCの呈色状態を判定することができる。
【0109】
また、溶液注入口123に投入された検体溶液(試料)は、図3において左側から右側へ向かって毛細管現象により試薬紙S上を流れていく。このため、流れてくる試料の先端がテストラインA,BやコントロールラインC上に存在するタイミングで第2の画像を撮影すると、これを影と誤判定してしまい、精度よくテストラインA,BやコントロールラインCの呈色状態を判定することができなくなる虞がある。そこで、試料が試薬紙Sに供給された後、テストラインA,BやコントロールラインCの反応が終了するまでの間に、第1の画像を複数回取得し、取得した複数の第1の画像の全てにおいて、同じ位置に存在する同一濃度の領域を影として特定し、その位置を算出するようにしてもよい。これにより、流れてくる試料の先端を影と誤認識してしまうのを防ぐことができる。
【0110】
また、制御部130は、図8に示すようなコンピュータ130で構成できる。コンピュータ130は、CPU(Central Processing Unit)130A、ROM(Read Only Memory)130B、RAM(Random Access Memory)130C、不揮発性メモリ130D、及び入出力インターフェース(I/O)130Eがバス130Fを介して各々接続された構成となっている。この場合、図6に示した処理のプログラムを記憶部136又は不揮発性メモリ130Dに書き込んでおき、これをCPU130Aが読み込んで実行することにより、コンピュータ130が制御部130として機能する。
【0111】
上記実施形態においては、アッセイ法としてイムノクロマトグラフ法について説明したが、本発明のアッセイ法はこれに限定されない。いわゆる免疫反応を用いない系でもよく、例えば、抗体を用いずにDNAやRNAなどの核酸で被検物質を捕捉する系でもよいし、さらには被検物質に対する親和性を持つ別の小分子やペプチド、たんぱく質、錯体形成物質等、によって被検物質を捕捉する系であってもよい。
【符号の説明】
【0112】
11 クロマトグラフ測定装置
114 デバイス装填部
120 イムノクロマト用デバイス
121 不溶性担体
122 デバイス用筐体
124 観察窓
130 制御部
132 判定部
134 動作モード選択部
136 記憶部
140 測定部
142 イメージセンサ
143 光学レンズ
144 光源
145 ガラス面
【特許請求の範囲】
【請求項1】
撮像素子と、
試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、
前記試薬紙に向けて照射光を照射する光源と、
前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御する制御手段と、
前記第1の画像に基づいて、前記付着物の位置を算出する付着物位置算出手段と、
前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出する影位置算出手段と、
前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出する光学濃度算出手段と、
を備えた測定装置。
【請求項2】
前記制御手段は、前記試料が前記試薬紙に供給された後、前記試薬の反応が終了するまでの間に、前記第1の画像を複数回取得し、前記影位置算出手段は、取得した複数の前記第1の画像に基づいて、前記影の位置を算出する
請求項1記載の測定装置。
【請求項3】
コンピュータを、請求項1又は請求項2記載の測定装置を構成する各手段として機能させるための測定プログラム。
【請求項4】
撮像素子と、試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、前記試薬紙に向けて照射光を照射する光源と、を備えた測定装置により実行される測定方法であって、
前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御し、
前記第1の画像に基づいて、前記付着物の位置を算出し、
前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出し、
前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出する
測定方法。
【請求項1】
撮像素子と、
試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、
前記試薬紙に向けて照射光を照射する光源と、
前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御する制御手段と、
前記第1の画像に基づいて、前記付着物の位置を算出する付着物位置算出手段と、
前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出する影位置算出手段と、
前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出する光学濃度算出手段と、
を備えた測定装置。
【請求項2】
前記制御手段は、前記試料が前記試薬紙に供給された後、前記試薬の反応が終了するまでの間に、前記第1の画像を複数回取得し、前記影位置算出手段は、取得した複数の前記第1の画像に基づいて、前記影の位置を算出する
請求項1記載の測定装置。
【請求項3】
コンピュータを、請求項1又は請求項2記載の測定装置を構成する各手段として機能させるための測定プログラム。
【請求項4】
撮像素子と、試料に被検物質が含まれるか否かをイムノクロマトグラフ法により判定するための試薬が形成され、かつ、前記試料に前記被検物質が含まれる場合に呈色する特異的結合物質が予め定めたテストライン領域に形成された試薬紙と、前記試薬紙が収容された試薬ケースと前記撮像素子との間の付着物が付着し得る付着面と、の何れかに焦点を合わせる合焦手段と、前記試薬紙に向けて照射光を照射する光源と、を備えた測定装置により実行される測定方法であって、
前記試料が前記試薬紙に供給された後に、前記付着面に焦点を合わせて前記撮像素子により撮像させた第1の画像、及び、前記試薬紙に焦点を合わせて前記撮像素子により撮像させた第2の画像、を取得するように前記合焦手段及び前記撮像素子を制御し、
前記第1の画像に基づいて、前記付着物の位置を算出し、
前記付着物の位置、前記光源の位置、前記付着面の位置、及び前記試薬紙の位置に基づいて、前記付着物の前記試薬紙上の影の位置を算出し、
前記第2の画像に基づいて前記テストライン領域の光学濃度を算出すると共に、前記影の位置が前記テストライン領域内の場合に、前記テストライン領域のうち前記影を含む領域を除外して前記テストライン領域の光学濃度を算出する
測定方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図8】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図8】


【図7】


【公開番号】特開2012−215419(P2012−215419A)
【公開日】平成24年11月8日(2012.11.8)
【国際特許分類】
【出願番号】特願2011−79580(P2011−79580)
【出願日】平成23年3月31日(2011.3.31)
【出願人】(306037311)富士フイルム株式会社 (25,513)
【Fターム(参考)】
【公開日】平成24年11月8日(2012.11.8)
【国際特許分類】
【出願日】平成23年3月31日(2011.3.31)
【出願人】(306037311)富士フイルム株式会社 (25,513)
【Fターム(参考)】
[ Back to top ]

