測定装置
【目的】構造及び使用方法が簡単で、抗原・抗体反応等の特異的反応を利用して迅速に分析対象を測定する装置を提供する。
【構成】フィルター、標識化試薬含有部材、及び1又は複数の反応領域を有する多孔性担体を有する免疫測定装置であって、該多孔性担体がその上流端において該フィルターと該標識化試薬含有部材とにより挟まれており、該反応領域が該フィルター及び該標識化試薬含有部材から離れてその下流に位置し、該標識化試薬含有部材が標識された試薬を含有しており、そして該反応領域に捕捉試薬が固定されていることを特徴とする、特異的反応を用いて分析対象を測定する測定装置。
【構成】フィルター、標識化試薬含有部材、及び1又は複数の反応領域を有する多孔性担体を有する免疫測定装置であって、該多孔性担体がその上流端において該フィルターと該標識化試薬含有部材とにより挟まれており、該反応領域が該フィルター及び該標識化試薬含有部材から離れてその下流に位置し、該標識化試薬含有部材が標識された試薬を含有しており、そして該反応領域に捕捉試薬が固定されていることを特徴とする、特異的反応を用いて分析対象を測定する測定装置。
【発明の詳細な説明】
【0001】
【産業上の利用分野】本発明は、抗原・抗体反応を利用して被検物質を測定するための装置に関する。
【0002】
【従来の技術】医学診断薬の分野での液体試料中に含まれる微量物質の測定法として、種々の分析法が開発されているが、特に高感度測定法として抗原抗体反応を利用した免疫分析法が幅広く用いられている。臨床分野ではこの測定原理を応用した装置を用いて分析している。この免疫反応の原理は、例えば特開昭47-18597、同53-47518、臨床検査 vol.121、NO.1,977等に記載されている。
【0003】更に、医院や一般家庭でもこの免疫反応を利用した簡易測定の必要性も高まり、その目的のための簡易型測定装置の開発も進歩しつつある。これらの装置、方法の中で、例えば特開昭62−501034、同62−501989、同63−118657、同64-463などで開示されている方法、いわゆる「ステイック」法がある。一般にこの方法は個体支持体上に固定化された抗体と試験試料とを反応させた後、この個体支持体を取り出して洗浄し、標識試薬と反応させ検出可能なシグナルを得る。標識が酵素の場合は、さらに発色試薬と反応させる必要がある。もちろん標識試薬と試料中の被検物質とを反応させた後に個体支持体上の抗体と反応させることもできる。しかしいずれの方法も複数の操作手順を必要とし、しかも少なくとも1回の洗浄操作が必要である。
【0004】この点を補うために洗浄操作を省いた装置も考案された。例えば特開昭63−281053、特開平1−299464、同2−12061 、特表平2−500540等に記載されている方法で、いわゆる「膜アッセイ」である。この方法は多孔質膜に抗体を固定化し、この多孔質膜と吸収剤を組み合わせて、試験試料、標識化試薬を順次加えて検出可能なシグナルを得る方法である。この方法では洗浄操作が省かれたものの、まだ数回の操作が必要とされている。
【0005】そのため、操作手順をより簡略化した方法が望まれている。一方、例えば特開昭62-39770、特開平1−123149等には、凝集法を利用した装置が記載されているがこの方法には、複雑な操作手順が必要ないが検出可能なシグナルを得るためには30分から60分の反応時間を必要とし、かつ判定がむずかしい欠点を持つ。これらの欠点を補う装置および方法として、米国特許第 4,235,601及び同 4,361,537に記載されている免疫クロマトグラフィー装置、ならびに測定方法がある。
【0006】この装置および方法は、抗体が固定化されたセルロース濾紙担体に各試薬を予め塗布して置き、試験試料を所定の位置に加える。毛細管現象により濾紙担体上を試料が移動した後、所定の位置に結合した標識試薬を計測する方法であって、抗原抗体反応に不可欠であった洗浄操作、すなわち、未反応物質の除去工程を省略した装置である。その後この装置および方法を改良した多くの公報がある。
【0007】例えば特開昭60−133368には、抗体を固相化し、さらに標識化試薬を保持させた不溶性担体を毛細管へ充填、この毛細管を試験試料につけて試料を毛細管現象で移動させることで測定する装置が記載されている。又、特開昭61−145459には吸収性シートをキャリアーとした免疫クロマトグラフィー法が開示されている。これら吸収性キャリアーを担体とした装置は、特開昭63−159760、同63-96559等にも記載されている。これらの装置の多くは抗体を固相化したクロマトグラフ物質と標識化試薬および必要なら反応に預かるその他の試薬を一体化して、操作手順を極力省いたものである。
【0008】一方、これらの装置のキット化のためにはハウジングを施すのが好ましく、例えば特開昭63−269059、同63−501595、同64-59069等にはハウジングについての記載がある。又、例えば特開平1−503174には多孔質キャリアー上のあるゾーンに抗体を固相化しついで他のゾーンに移動可能な状態で標識化試薬を含ませて、さらに試料受容部をも設け、これをハウジングにより一体化させた装置が考案されている。これを用いることにより、何等複雑な操作手順をふむことなく敏速に、かつ簡便に試験試料中の被検物質を測定できるが、抗原抗体反応が毛細管現象の流体中で起こるために測定感度において十分な効果が得られない。
【0009】また特開平1−244370では試料受容部に標識試薬を含ませる装置が考案されている。この装置は液体試料中の被検物質と標識化試薬との結合反応をインキュベーションにより行うため高感度に測定することが出来るが、しかし、液体試料が血液や尿、とくに尿の場合、これに含まれる不溶物のための試料受容部位が目ずまりを起こし毛管流が停止することがある。このため濾過手段を設けることが好ましいが試料受容部の上部やクロマトグラフィー物質と試料受容部の間に設置してもその効果は十分ではない。そのため、検出までの時間や測定感度の点でさらに改良が必要とされる。
【0010】
【発明が解決しようとする課題】本発明は、分析試料中の分析対象物質(単に、分析対象と言う場合がある)を、抗原・抗体反応を用いて簡単に且つ短時間に測定することができる装置を提供しようとするものである。
【0011】
【課題を解決するための手段】上記の課題を解決するため、本発明は、フィルター、標識化試薬含有部材、及び1又は複数の反応領域を有する多孔性担体を有する免疫測定装置であって、該多孔性担体がその上流端において該フィルターと該標識化試薬含有部材とにより挟まれており、該反応領域が該フィルター及び該標識化試薬含有部材から離れてその下流に位置し、該標識化試薬含有部材が標識された試薬を含有しており、そして該反応領域に捕捉試薬が固定されていることを特徴とする、特異的反応を用いて分析対象を測定する測定装置を提供する。
【0012】
【作用】本発明の装置においては、多孔性担体の一端(上流端と称する)がフィルター及び標識化試薬含有部材により挟まれており、該多孔性担体の下流側には狭い領域に捕捉試薬が固定されている。この領域を反応領域と称する。今、分析対象(例えば抗原)を含有する試料溶液をフィルターに適用すれば、該溶液はフィルターを通過して多孔性担体に移行し、さらに前記標識化試薬部材に入る。この標識化試薬部材には標識された物質(例えば前記抗原に対する抗体)が含まれており、前記分析対象抗原と標識された抗体との免疫複合体が形成される。
【0013】十分量の被検試料液をフィルターに適用すればこの溶液は多孔性担体を毛細管現象により移動し、この際に前記の免疫複合体は該溶液により運搬され、この免疫複合体が前記多孔性フィルター上の反応領域に達すると、該領域に固定されている捕捉試薬(例えば、分析対象抗原に対する第二抗体)と反応し、前記免疫複合体は例えばサンドイッチ状複合体の形で捕捉試薬抗体に捕捉され、こうして捕捉固定された標識が検出される。
【0014】
【効果】本発明の装置を用いる場合、前記のごとく、免疫複合体が反応領域に捕捉濃縮されるので、それに伴って標識物質も濃縮され、分析対象を極めて高感度に、しかも非常に簡単な方法で測定することができる。
【0015】
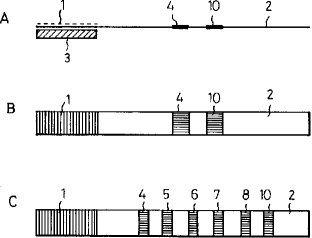
【具体的な説明】本発明の装置の構造の一例を模式的に図1に示す。図1においてAは該装置の横から見た重層構造を示しており、Bはその平面図である。図中1はフィルターを示し、2は多孔性担体を示し、3は標識化試薬含有部材を示し、そして4は反応領域を示す。また10は場合によっては存在するポジティブコントロール用反応領域を示す。
【0016】多孔性担体(2)は、使用時においては通常、細長いテープ状の形状を有している。多孔性担体は、分析試料等の溶液を例えば毛細管現象等の作用により移行させるための媒体として機能するものであり、この様な作用をするものである限りその材質は特に制限されない。この様な材料として、例えばガラス繊維濾紙(例えば、GF/A、 Whatman製)、セルロース膜、ニトロセルロース膜、ナイロン膜等を用いることができる。
【0017】多孔性担体の寸法は特に制限はないが、使用時においては、例えば幅2mm〜10mm、長さ50mm〜 150mm、厚さ20μm〜1000μmのものが用いられる。多孔性担体として幅広いシートを用意しており、使用前にテープに切断して使用することもできる。
【0018】多孔性担体(2)には、前記フィルター(1)及び標識化試薬含有部材(3)より下流であって且つこれらから離れた位置に1個又は複数個の反応領域が設けられており、これらの反応領域には捕捉試薬が固定されている。なお、本発明において「上流」及び「下流」とは、試料溶液等をフィルターに適用した場合に該溶液が多孔性担体中を移行する場合の移動の方向を意味する。
【0019】多孔性担体(2)は1個又は複数個の反応領域を有し、1個の反応領域を有する場合には定性試験又は半定量試験に用いることができ、また複数個の反応領域を有する場合には定量試験に用いることができる。
【0020】1個の反応領域が存在する場合の該反応領域とフィルター(及び標識化試薬含有部材)との間の距離は特に臨界的ではないが5mm〜3cmであり、また複数の反応領域が存在する場合の最上流の反応領域とフィルター(及び標識化試薬含有部材)との間の距離も同様である。複数の反応領域が存在する場合、反応領域間の距離は特に臨界的ではないが、例えば2mm〜10mmである。反応領域の長さ(縦方向の長さ)は通常0.1mm〜10mmである。
【0021】反応領域に固定される捕捉試薬は、通常、抗原又は抗体であり、これらを多孔性担体に固定化する方法は当業界においてよく知られており、それらの既知の方法を用いればよい。例えば、リン酸緩衝生理食塩水に抗原又は抗体を溶解させ、多孔性担体に塗布する。塗布後、25℃にて18時間乾燥させる。固定化の後、多孔性担体が有する反応基をブロックするため、常用のブロッキング剤、例えばゼラチン、アルブミン等により多孔性担体を処理するのが好ましい。
【0022】多孔性担体の上流端に設けられるフィルターは、試料溶液中に不溶性物質が存在すればそれを除去することを主たる目的としており、従って、溶液中の不溶物を濾過・除去することができるものであれば、その材質には特に制限がない。例えば、セルロース膜、ガラス繊維濾紙、ニトロセルロース膜、布、ナイロン膜等を使用することができる。フィルターの寸法は、通常、多孔性担体(2)の幅より広い方が好ましく、例えばその幅より2mm〜5mm程度広くした方がよい。また、長さは10mm〜50mm程度が便利である。
【0023】好ましい態様においては、フィルターにはpH緩衝剤を含有せしめる。こうすることにより、フィルターを通過する試料溶液のpHをその後の抗原・抗体反応のために都合のよいpHに調整することができる。緩衝剤の種類及びpHは、分析試料の種類、そのpH、分析対象の種類、分析に用いる反応試薬(例えば抗原、抗体、標識物質等)により異るが、例えばTris緩衝剤、ジエタノール緩衝剤、リン酸緩衝剤、等、常用の緩衝剤を用いることができる。
【0024】フィルターに緩衝剤を付加するには、例えば緩衝液、 100mM〜1M濃度の緩衝液によりフィルターを含浸し、これを常法に従って乾燥すればよい。フィルター(1)と多孔性担体(2)との接着は、例えば物理的に接触させる、例えば機械的に押し付ける、等により行うことができる。
【0025】標識化試薬含有部材は標識された試薬を収容し、且つ試料溶液を適用した場合に該試料溶液中の分析対象と該標識された試薬との反応の場を提供するものである。この場合、標識された試薬は、標識化試薬含有部材に「固定化」されておらず、試料溶液が適用された場合に該溶液に溶解し、標識化試薬含有部材から「遊離」していなければならない。
【0026】従ってこの様な要件を満たすように、標識化試薬含有部材用材料への標識された試薬の適用条件及び標識化試薬含有部材用材料の種類を選択する必要がある。例えば、標識化された試薬の溶液を標識化試薬含有部材用の材料に適用し、これを凍結乾燥する場合、標識化試薬含有部材用の材料としてセルロース膜、ガラス繊維濾紙、ニトロセルロース膜、ナイロン膜等を使用することができ、セルロース膜が好ましい。
【0027】標識化試薬含有部材(3)の寸法は、前記フィルター(1)の幅と同じ幅を有し、その長さは10mm〜50mmが適当である。標識化試薬含有部材(3)と多孔性担体(2)との接着は、例えば、物理的に接触させることにより、例えば機械的に押し付けること、等により行うことができる。
【0028】本発明においては、分析試料として種々の溶液が用いられ、好ましくは生物由来の液体試料、例えば血液、血漿、血清、唾液、尿等が用いられる。これらに含有されており、本発明の装置により分析される分析対象としては、それに対して特異的に結合する物質が存在するものであればよく、例えばポリペプチド、蛋白質、複合蛋白質、多糖類、脂質、複合脂質、ホルモン類、核酸等が例示される。ここで、特異的に結合する物質とは抗原に対する抗体、及び抗体に対する抗原、並びに種々の生理活性物質に対するそのレセプター、等が例示される。
【0029】分析対象のさらに具体的な例としては、被検物質の例としては、卵胞刺激ホルモン、黄体刺激ホルモン、胎盤性ゴナドトロピン、甲状腺ホルモン、リポ蛋白、アポリポ蛋白、アルブミン、ヘモグロビン、プロゲステロン、エストラジオール、等が挙げられるがこれらに限定されるものではない。
【0030】本発明の装置は、特異的反応を用いる、種々の原理に基く測定に使用することができ、その最も典型的な例として、抗原・抗体反応を用いる、いわゆるサンドイッチ法、競合法等が挙げられる。
【0031】サンドイッチ法においては、標識された試薬として、分析対象とは結合するが捕捉試薬とは直接結合しない物質を用い、捕捉試薬として分析対象と結合する物質を用いる。
【0032】例えば、測定対象が抗原である場合、標識された試薬として測定対象に対する第一の抗体を用い、そして捕捉試薬として該測定対象に対する第二の抗体を用いる。この場合、第一の抗体及び第二の抗体は測定対象抗原上の異る抗原決定基を認識するものである。
【0033】この方法においては、測定対象抗原が標識された第一抗体と結合して免疫複合体を形成し、この免疫複合体は、試料溶液が多孔性担体中を移動するに従って移動し、第二抗体が固定されている反応領域に対した時、前記標識された第一抗体/分析対象抗原−免疫複合体中の分析対象抗原がその他方の抗原決定基により第二抗体と結合し、この結果、標識された第一抗体/分析対象抗原/固定された第二抗体−三元免疫複合体(いわゆるサンドイッチ)が反応領域において形成される。従って、このようにして固定(捕捉)された標識物質を検出することにより分析対象抗原の存否又は量を知ることができる。
【0034】サンドイッチ法の第二の態様として、測定対象が抗体である場合、標識された試薬として該測定対象抗体に対する抗体を用い、そして捕捉試薬として該測定対象抗体に対する抗原を用いることができる。また、これとは逆に標識された試薬として測定対象抗体に対応する抗原を用い、そして捕捉試薬として測定対象抗体に対する抗体を用いることもできる。
【0035】さらに、競争的方法においては、分析対象及び標識された試薬の再者が捕捉試薬に競争的に結合するように、標識された試薬及び捕捉試薬を選択することができる。
【0036】この具体例として、捕捉試薬として抗原を用い、分析対象及び標識された試薬は該抗原に競争的に結合する同一の又は異る抗体である。この結果、分析試料溶液中に存在する分析対象抗体と、標識化試薬含有部材中に収容されていた標識された抗体とは相互に結合することなく、試料溶液の移動と共に多孔性担体上の反応領域に輸送される。
【0037】そして、この反応領域に固定されている捕捉抗原との結合に関して前記分析対象抗体と標識された抗体とが競争し、捕捉固定された標識物質の量を測定することにより試料溶液中に存在した分析対象抗体の量を決定することができる。
【0038】また、上記の方法とは逆に、捕捉試薬とし抗体を用い、そして測定対象及び標識された試薬が該捕捉抗体に競争的に結合するように、捕捉物質及び標識された試薬を選択することもできる。
【0039】以上のごとく、本発明の装置においては、多孔性担体上の結合領域に、分析対象、分析原理等に応じて種々の捕捉試薬を固定化して用いるが、本発明の好ましい態様においては「ポジティブコントロール」としての追加の反応領域を、好ましくは前記の分析用反応領域よりも下流に設ける(図1において10)。
【0040】このポジティブコントロール用反応領域には、分析対象の不存在下でも標識された試薬を捕捉することができる物質、すなわち標識された試薬と直接結合する物質、を固定化する。この様な物質として、標識された物質がある動物からの抗体である場合、その動物の抗体に対する他の動物由来の抗体を用いることができる。例えば、標識された物質がマウス抗体である場合、ポジティブコントロール反応領域用捕捉試薬としてマウス抗体に対するウサギ由来の抗体を用いることができる。
【0041】本発明の標識物質としては、当業界において知られている常用の標識物質を用いることができ、またその検出手段としても対応する常用の手段を用いることができる。例えば、標識物質として、それ自体が色を有し、直接目視できる物質、それ自体発光性を有する物質、更なる反応により検出可能なシグナルを発生する物質等を用いることができる。
【0042】しかしながら、本発明の装置は、分析対象を極めて簡単に、且つ短時間に測定することができることを1つの特徴としており、この特徴を発揮するためには、標識物質として直接目視可能な物質、又はそれ自体発光性を有する物質を用いることができる。
【0043】直接目視可能な物質としては、例えば、着色粒子、コロイド状粒子、染料粒子(分散染料)等を挙げることができ、コロイド状金粒子、染料粒子(分散染料、染料ゾル)等が特に好ましい。また、それ自体発光性を有する物質としては蛍光発色団、例えばフルオレッセイン等を用いることができる。また放射性同位元素を用いることができる。
【0044】更なる反応により検出可能なシグナルを発生することができる物質としては、例えば酵素、酵素等を収容したリポゾーム等を用いることができる。酵素としては例えばカルカリホスファターゼ、ワサビパーオキシダーゼ、β−ガラクトシダーゼ等を用いることができ、これらの検出方法は当業界においてよく知られている。
【0045】上記の種々の標識物質はいずれも当業界において知られており、そしてそれらを反応試薬、例えば抗原、抗体等に結合させる(後者を標識する)方法も当業界においてよく知られている。
【0046】前記のごとく、本発明の装置により分析対象物を定量するためには、図1のCに示すように、複数の反応領域(ポジティブコントロール用反応領域のほかに)を設けるのが好ましい。また効率よく、精度よくまた広範囲にわたる量(濃度)の分析対象物を定量しようとする場合、反応領域が下流に位置するに従って多くの捕捉試薬を固定しておく必要がある。
【0047】この場合、例えば試料中の分析対象の量が非常に少ない場合、分析対象物と標識物質および捕捉試薬との反応効率によって、捕捉試薬が最も多く固定化された反応領域(最下流)においてのみ分析対象物が捕捉可能となり、シグナル(例えは発色)が得られ、従って1個のシグナル(発色)をもたらす。
【0048】しかし、分析対象の量が多くなればなるほど、捕捉試薬の量が少ない反応領域でも分析対象物が捕捉され、シグナル(発色)をもたらす。こうして、分析対象の量(濃度)に応じた数のシグナル(発色)が得られる。
【0049】本発明の他の態様においては、分析試料中の複数種類の分析対象に対応して複数の標識された試薬を標識化試薬含有領域に収容せしめ、それに対応して複数の反応領域を設けることができる。こうすることにより、1つの分析試料中に存在する複数の種類の分析対象を、1個の装置を用いる1回の操作により同時に測定することができる。
【0050】本発明の装置の他の態様においては、装置の小部分又は大部分をカバー部材により覆うことができる。この場合、カバーの少なくともフィルターに対応する部分に試料適用のための窓を設ける必要がある。さらに分析結果を目視する方式の装置においては、カバーの少なくとも反応領域に対応する部分には観察用の窓を設けるか、又は透明部材により構成するか、あるいはカバーが存在しないようにする必要がある。この構成により、分析に際して装置の上流端を全体的に分析用試料溶液中に浸漬するか、又は該上流端に分析用試料溶液を注びかけることにより極めて簡単に試料を適用することができる。
【0051】次に、このカバー付き装置の具体例を図4及び図5により説明する。図4はこの装置の構造を模式的に示すものであり、図5はこの装置を部材に分解して示すものである。この装置は、装置全体に強度を与え、且つ装置のカバーとして機能するZ形に曲げられた長い部材(Z形部材)(20)を有し、これは標識化試薬含有部材支持部(21)及び多孔性担体支持部(22)並びに垂直部(23)を有する。さらに、その下流端が曲げられ、多孔性担体固定部(24)が構成されている。このZ形部材はさらにその垂直部(23)に貫通孔(25)を有する。
【0052】多孔性担体(2)は、前記貫通孔(25)を通してZ部材(20)にそって配置され、そして多孔性担体固定部(24)により固定される。標識化試薬含有部材(3)は、前記標識化試薬含有部材支持部(22)と多孔性担体(2)との間に挿入される。また、フィルター1は多孔性担体(2)の上であって標識化試薬含有部材(3)に対応する位置に配置される。
【0053】Z形部材(20)の標識化試薬含有部材支持部(21)、標識化試薬含有部材(3)、多孔性担体(2)及びフィルター(1)は、留具(30)により機械的に押付けられ一体化される。こうしてフィルター(1)、多孔性担体(2)及び標識化試薬含有部材(3)が相互に接触する。
【0054】留具(30)は、その上面31に開口部、すなわち窓32を有し、この窓を通して試薬溶液がフィルター(1)に適用される。留具(30)はつめ(33)を有し、その曲った先端34部が標識化試薬含有部材支持部(21)を背部から抱え込むことにより関連各部材が一体化される。
【0055】この構造において、Z形部材(20)の材質は特に限定されないが、例えば合成樹脂板を用いるのが便利である。Z形部材が透明である場合、多孔性担体上に現われる測定結果は図4の矢印26及び27のいずれの方向からでも観察することができる。これに対して、Z形部材が不透明な材料から作られている場合、測定結果はカバーとしてのZ形部材が存在しないか又は窓を形成している側(図4における矢印27)から観察される。
【0056】留具(30)の材質も特に限定されず、例えば金属、合成樹脂板等が使用される。なお、1つの態様においては、標識化試薬含有部材支持部(21)の上面であって長手方向の縁部に2本の線状の凸部を形成し、この間に標識化試薬含有部材(3)を配列することにより該部材動きを防止し、同時に分析用試料溶液の横からの侵入を防止することもできる。また、標識化試薬含有部材支持部(21)に貫通孔を設けて、標識化試薬含有部材(3)に分析用試料溶液が入る場合に脱気を促進することもでき、またこの孔を通して、分析用試料溶液の一部が標識化試薬含有部材(3)に入るようにすることもできる。
【0057】次に、実施例により本発明をさらに具体的に説明する。
実施例1. hCG のイムノクロマトグラフィーアッセイa)金コロイド標識化マウス抗 hCG抗体の調製金コロイド標識化方法については、Journal of Immunoassay 1(1), 77-91, 1980に記載されている方法に準じて行うことが出来る。例えば、金コロイドG30(粒径30nm、Amersham International plc. から供給される。)20mlに0.2NのK2CO3 3mlを加えpH7に調製した。一方、2mM硼砂緩衝液pH9で透析したマウス抗hCG抗体(1mg/ml)を 100,000g、1時間遠心後、その上清2/3をとり2mM硼砂緩衝液pH9で40μg/mlに希釈した。
【0058】金コロイド液(pH7)20mlを攪拌しながら抗体溶液2mlを加え、2分間攪拌する。次いで1% PEG 20,000ml 、10% BSA(1N NaCl でpH9に調製されている)2mlを加える。この反応液を12,000gで遠心し得られた沈査を1% BSA、0.05% PEG 20,000 を含む20mMトリス塩酸緩衝液(pH8.2)に再浮遊させ、再度遠心した。
【0059】この操作を3回繰り返し最終的に得られた沈査を1% BSA、0.05% PEG 20,000 を含む20mMトリス塩酸緩衝液(pH8.2)で再浮遊させ、波長 520nmでの吸光度が6.0になるように調製する。得られた金コロイド標識化抗体液を5%BSA、0.05% PEC 20,000 、0.3M NaCl を含む20mMトリス塩酸緩衝液(pH8.2)で2倍希釈し、最終調製液とした。
【0060】b)染料ゾル標識化マウス抗 hCG抗体の調製染料ゾル標識化方法については、特開昭56−160655明細書に記載されている。例えば、ルミナスRed(BASF社から供給される) 2.5gを50mlの蒸留水に懸濁させ、45分間室温で攪拌する。これを 125g、30分間遠心後、沈査を50mlの蒸留水で再浮遊させた。この操作を3回繰り返し洗浄した。得られた沈査を25mlの蒸留水で再浮遊させた後、同レベルの量のガラスビーズ(直径3mm:4mm=1:2に混合したもの)を加え5日間振盪した。この染料ゾル液を回収し 300g、30分間遠心した後、 1,000g、30分間さらに遠心し下層部を採取した。
【0061】ついで波長 520nmの吸光度を5.0に調整した。一方、マウス抗 hCG抗体溶液を5mM NaCl(pH7に0.1Na2CO3で調整されている)で透析後1mg/mlに調整した。この抗体溶液0.1mlをルミナス Red液5mlに加え、室温で1時間反応させる。さらに30% BSA、0.01%チメロザールを含む5mM NaCl(pH7) で波長 520nmでの吸光度を8.0に調整した。
【0062】c)多孔性担体の調製マウス抗 hCG抗体を1mg/mlの濃度に10mMリン酸緩衝液生理食塩水(pH7.2)で調整する。ガラス繊維濾紙(GF/A、 Whatman社製、20cm×12cm)上にこの抗体溶液を直線状に塗布した。塗布はアクリル棒に抗体溶液をしみ込ませて、直線を引いた。さらにポジティブコントロールとしてウサギ抗マウス抗体を同様に抗 hCG抗体塗布線の下流側に塗布した。この多孔性抗体を25℃で18時間乾燥した。次に1%ゼラチン液に1時間、浸した後10mMリン酸緩衝液生理食塩水(pH7.2)で3回洗浄した。これを陰圧乾燥機で乾燥後、抗体の塗布線に垂直に5mm幅で切断し、5mm×12cmの多孔性担体を作製した。
【0063】d)標識化試薬含有部材の調製粘稠性濾紙(NO.60、Toyo Roshi社製)5mm×30mmに実施例1.a)又はb)項に記載の方法で調製した標識化試薬を75μl加え、凍結乾燥した。
【0064】e)フィルターの調製ガラス繊維濾紙 (GF/A、 Whatman社製)8mm×30mmに 200mMトリス塩酸緩衝液(pH10)をしみ込ませて凍結乾燥した。
【0065】f)定量分析用多孔性担体の調製マウス抗 hCG抗体溶液を2,1,0.5,0.25、及び 0.125mg/mlの各濃度に10mMリン酸緩衝液生理食塩水(pH7.2)で調整した。この抗体溶液を実施例1.c)項に記載の方法で上流側から下流側に向かって薄い濃度の抗体溶液から、段階状に塗布した。これを定量用多孔性担体とした。
【0066】g)hCG の測定実施例1.のa),c),d),e)に記載の方法で調製した多孔性担体、金コロイド標識化抗体含有パッドおよびフィルターを用いて、図1A及び図2に示す装置を組み立てた。図1は本発明の装置を示し、図2aおよびbは比較対照として用いた装置を示す。尚、各装置の金コロイド標識化抗体の量は同量とした。hCG 0, 10, 25, 50、又は 100IU/lをそれぞれ含む0.2% BSA−リン酸緩衝生理食塩水を試験試料とし、この各試験試料をフィルターへ適用した。経時的、可視的に観察しバンドの呈色が確認された時間と10分後の呈色バンドの強さを記録した。結果を表1に示す。
【0067】
【表1】

【0068】h)濾過膜の効果の確認尿を試験試料として用いた場合の本発明の装置の効果を確認するためにhCG(0, 25、又は50IU/l)を含んだ尿試料を準備し、本発明の装置へ適用した。対照として、フィルターを除いた同様な装置を用いた。観察は実施例1.g)項に記載の方法に準じた。観察された結果を以下の表2に示す。
【0069】
【表2】

【0070】i)フィルターへの緩衝液添加の効果の確認フィルターへのトリス塩酸緩衝液あるいはジエタノールアミン緩衝液添加の効果について検討した。尿を試験試料とする場合、一般的に尿のpHは5〜8(平均6)であり、特に酸性尿の場合はpH4になるといわれる。そこで尿のpHを4に調整し、本発明の装置へ適用した。また対照として緩衝液を含まないフィルターを用いた。観察された結果は次のとおりである。尚、 hCGは含まない尿を試料とした。結果を表3に示す。
【0071】
【表3】

【0072】j)hCG の定量分析免疫クロマトグラフィー法で定量分析を行うために実施例1.f)項に記載の方法で調製した多孔性担体を用いて本発明の装置を組み立てて、hCG(0, 10, 50,100, 500IU/l)試験試料を適用した。観察された結果を以下に示す。 hCGの濃度が増すに連れて、確認される呈色バンドの数が据えた。結果を表4に示す。
【0073】
【表4】

【0074】この結果で得られた呈色バンドの発色強度を数値で表せば検量線が得られる。例えば、TLCスキャナー(島津社製)を用いて波長 530nmの吸光度を求めて各ピークの高さを積算する。この結果を図示すれば検量線が得られる。結果を表5に示す。
【0075】
【表5】

【0076】実施例2.図1に示す本発明の装置と図4に示す市販の装置(商品A及び商品B)とを hCGの測定において比較した。市販の装置は図4に示すように、多孔性担体の一端に試料適用部位が存在し、その下流に抗hCG 標識化抗体が含浸されており、さらに下流に抗hCG 固定化抗体(反応領域)及びポジティブコントロール用反応領域を有する。hCG 0, 10, 25, 50, 100IU/lをそれぞれ含む、0.2% BSA−リン酸緩衝生理食塩水を試験試料とし、この試料を各装置の用法用量に従って適用した。経時的、可視的に観察しバンドの呈色が確認された時間と10分後のバンドの強さを記録した。結果を表6に示す。
【0077】
【表6】

上記のごとく、本発明の装置は従来の装置に比べて非常に鋭敏である。
【図面の簡単な説明】
【図1】この図のAは本発明の装置の1態様を横から見た略面であり、BはAの装置の平面図であり、そしてCは本発明の装置の、多数の反応領域を有する態様を示す。
【図2】この図のa及びbはいずれも従来技術の装置を模式的に示したものである。
【図3】本発明の装置の他の態様であって、図1に示す装置が、フィルターに対応する部分に窓を有する透明な不透水性カバーにより覆われている。
【図4】本発明の装置の一例を模式的に示すものである。
【図5】図4に示す装置を構成部材に分けて示す。
【図6】従来技術の装置を示す。
【符号の説明】
1…フィルター
2…多孔性担体
3…標識化試薬含有部材
4…反応領域
10…ポジティブコントロール用反応領域
11…不透水性透明カバー
12…試料適用のための窓
【0001】
【産業上の利用分野】本発明は、抗原・抗体反応を利用して被検物質を測定するための装置に関する。
【0002】
【従来の技術】医学診断薬の分野での液体試料中に含まれる微量物質の測定法として、種々の分析法が開発されているが、特に高感度測定法として抗原抗体反応を利用した免疫分析法が幅広く用いられている。臨床分野ではこの測定原理を応用した装置を用いて分析している。この免疫反応の原理は、例えば特開昭47-18597、同53-47518、臨床検査 vol.121、NO.1,977等に記載されている。
【0003】更に、医院や一般家庭でもこの免疫反応を利用した簡易測定の必要性も高まり、その目的のための簡易型測定装置の開発も進歩しつつある。これらの装置、方法の中で、例えば特開昭62−501034、同62−501989、同63−118657、同64-463などで開示されている方法、いわゆる「ステイック」法がある。一般にこの方法は個体支持体上に固定化された抗体と試験試料とを反応させた後、この個体支持体を取り出して洗浄し、標識試薬と反応させ検出可能なシグナルを得る。標識が酵素の場合は、さらに発色試薬と反応させる必要がある。もちろん標識試薬と試料中の被検物質とを反応させた後に個体支持体上の抗体と反応させることもできる。しかしいずれの方法も複数の操作手順を必要とし、しかも少なくとも1回の洗浄操作が必要である。
【0004】この点を補うために洗浄操作を省いた装置も考案された。例えば特開昭63−281053、特開平1−299464、同2−12061 、特表平2−500540等に記載されている方法で、いわゆる「膜アッセイ」である。この方法は多孔質膜に抗体を固定化し、この多孔質膜と吸収剤を組み合わせて、試験試料、標識化試薬を順次加えて検出可能なシグナルを得る方法である。この方法では洗浄操作が省かれたものの、まだ数回の操作が必要とされている。
【0005】そのため、操作手順をより簡略化した方法が望まれている。一方、例えば特開昭62-39770、特開平1−123149等には、凝集法を利用した装置が記載されているがこの方法には、複雑な操作手順が必要ないが検出可能なシグナルを得るためには30分から60分の反応時間を必要とし、かつ判定がむずかしい欠点を持つ。これらの欠点を補う装置および方法として、米国特許第 4,235,601及び同 4,361,537に記載されている免疫クロマトグラフィー装置、ならびに測定方法がある。
【0006】この装置および方法は、抗体が固定化されたセルロース濾紙担体に各試薬を予め塗布して置き、試験試料を所定の位置に加える。毛細管現象により濾紙担体上を試料が移動した後、所定の位置に結合した標識試薬を計測する方法であって、抗原抗体反応に不可欠であった洗浄操作、すなわち、未反応物質の除去工程を省略した装置である。その後この装置および方法を改良した多くの公報がある。
【0007】例えば特開昭60−133368には、抗体を固相化し、さらに標識化試薬を保持させた不溶性担体を毛細管へ充填、この毛細管を試験試料につけて試料を毛細管現象で移動させることで測定する装置が記載されている。又、特開昭61−145459には吸収性シートをキャリアーとした免疫クロマトグラフィー法が開示されている。これら吸収性キャリアーを担体とした装置は、特開昭63−159760、同63-96559等にも記載されている。これらの装置の多くは抗体を固相化したクロマトグラフ物質と標識化試薬および必要なら反応に預かるその他の試薬を一体化して、操作手順を極力省いたものである。
【0008】一方、これらの装置のキット化のためにはハウジングを施すのが好ましく、例えば特開昭63−269059、同63−501595、同64-59069等にはハウジングについての記載がある。又、例えば特開平1−503174には多孔質キャリアー上のあるゾーンに抗体を固相化しついで他のゾーンに移動可能な状態で標識化試薬を含ませて、さらに試料受容部をも設け、これをハウジングにより一体化させた装置が考案されている。これを用いることにより、何等複雑な操作手順をふむことなく敏速に、かつ簡便に試験試料中の被検物質を測定できるが、抗原抗体反応が毛細管現象の流体中で起こるために測定感度において十分な効果が得られない。
【0009】また特開平1−244370では試料受容部に標識試薬を含ませる装置が考案されている。この装置は液体試料中の被検物質と標識化試薬との結合反応をインキュベーションにより行うため高感度に測定することが出来るが、しかし、液体試料が血液や尿、とくに尿の場合、これに含まれる不溶物のための試料受容部位が目ずまりを起こし毛管流が停止することがある。このため濾過手段を設けることが好ましいが試料受容部の上部やクロマトグラフィー物質と試料受容部の間に設置してもその効果は十分ではない。そのため、検出までの時間や測定感度の点でさらに改良が必要とされる。
【0010】
【発明が解決しようとする課題】本発明は、分析試料中の分析対象物質(単に、分析対象と言う場合がある)を、抗原・抗体反応を用いて簡単に且つ短時間に測定することができる装置を提供しようとするものである。
【0011】
【課題を解決するための手段】上記の課題を解決するため、本発明は、フィルター、標識化試薬含有部材、及び1又は複数の反応領域を有する多孔性担体を有する免疫測定装置であって、該多孔性担体がその上流端において該フィルターと該標識化試薬含有部材とにより挟まれており、該反応領域が該フィルター及び該標識化試薬含有部材から離れてその下流に位置し、該標識化試薬含有部材が標識された試薬を含有しており、そして該反応領域に捕捉試薬が固定されていることを特徴とする、特異的反応を用いて分析対象を測定する測定装置を提供する。
【0012】
【作用】本発明の装置においては、多孔性担体の一端(上流端と称する)がフィルター及び標識化試薬含有部材により挟まれており、該多孔性担体の下流側には狭い領域に捕捉試薬が固定されている。この領域を反応領域と称する。今、分析対象(例えば抗原)を含有する試料溶液をフィルターに適用すれば、該溶液はフィルターを通過して多孔性担体に移行し、さらに前記標識化試薬部材に入る。この標識化試薬部材には標識された物質(例えば前記抗原に対する抗体)が含まれており、前記分析対象抗原と標識された抗体との免疫複合体が形成される。
【0013】十分量の被検試料液をフィルターに適用すればこの溶液は多孔性担体を毛細管現象により移動し、この際に前記の免疫複合体は該溶液により運搬され、この免疫複合体が前記多孔性フィルター上の反応領域に達すると、該領域に固定されている捕捉試薬(例えば、分析対象抗原に対する第二抗体)と反応し、前記免疫複合体は例えばサンドイッチ状複合体の形で捕捉試薬抗体に捕捉され、こうして捕捉固定された標識が検出される。
【0014】
【効果】本発明の装置を用いる場合、前記のごとく、免疫複合体が反応領域に捕捉濃縮されるので、それに伴って標識物質も濃縮され、分析対象を極めて高感度に、しかも非常に簡単な方法で測定することができる。
【0015】
【具体的な説明】本発明の装置の構造の一例を模式的に図1に示す。図1においてAは該装置の横から見た重層構造を示しており、Bはその平面図である。図中1はフィルターを示し、2は多孔性担体を示し、3は標識化試薬含有部材を示し、そして4は反応領域を示す。また10は場合によっては存在するポジティブコントロール用反応領域を示す。
【0016】多孔性担体(2)は、使用時においては通常、細長いテープ状の形状を有している。多孔性担体は、分析試料等の溶液を例えば毛細管現象等の作用により移行させるための媒体として機能するものであり、この様な作用をするものである限りその材質は特に制限されない。この様な材料として、例えばガラス繊維濾紙(例えば、GF/A、 Whatman製)、セルロース膜、ニトロセルロース膜、ナイロン膜等を用いることができる。
【0017】多孔性担体の寸法は特に制限はないが、使用時においては、例えば幅2mm〜10mm、長さ50mm〜 150mm、厚さ20μm〜1000μmのものが用いられる。多孔性担体として幅広いシートを用意しており、使用前にテープに切断して使用することもできる。
【0018】多孔性担体(2)には、前記フィルター(1)及び標識化試薬含有部材(3)より下流であって且つこれらから離れた位置に1個又は複数個の反応領域が設けられており、これらの反応領域には捕捉試薬が固定されている。なお、本発明において「上流」及び「下流」とは、試料溶液等をフィルターに適用した場合に該溶液が多孔性担体中を移行する場合の移動の方向を意味する。
【0019】多孔性担体(2)は1個又は複数個の反応領域を有し、1個の反応領域を有する場合には定性試験又は半定量試験に用いることができ、また複数個の反応領域を有する場合には定量試験に用いることができる。
【0020】1個の反応領域が存在する場合の該反応領域とフィルター(及び標識化試薬含有部材)との間の距離は特に臨界的ではないが5mm〜3cmであり、また複数の反応領域が存在する場合の最上流の反応領域とフィルター(及び標識化試薬含有部材)との間の距離も同様である。複数の反応領域が存在する場合、反応領域間の距離は特に臨界的ではないが、例えば2mm〜10mmである。反応領域の長さ(縦方向の長さ)は通常0.1mm〜10mmである。
【0021】反応領域に固定される捕捉試薬は、通常、抗原又は抗体であり、これらを多孔性担体に固定化する方法は当業界においてよく知られており、それらの既知の方法を用いればよい。例えば、リン酸緩衝生理食塩水に抗原又は抗体を溶解させ、多孔性担体に塗布する。塗布後、25℃にて18時間乾燥させる。固定化の後、多孔性担体が有する反応基をブロックするため、常用のブロッキング剤、例えばゼラチン、アルブミン等により多孔性担体を処理するのが好ましい。
【0022】多孔性担体の上流端に設けられるフィルターは、試料溶液中に不溶性物質が存在すればそれを除去することを主たる目的としており、従って、溶液中の不溶物を濾過・除去することができるものであれば、その材質には特に制限がない。例えば、セルロース膜、ガラス繊維濾紙、ニトロセルロース膜、布、ナイロン膜等を使用することができる。フィルターの寸法は、通常、多孔性担体(2)の幅より広い方が好ましく、例えばその幅より2mm〜5mm程度広くした方がよい。また、長さは10mm〜50mm程度が便利である。
【0023】好ましい態様においては、フィルターにはpH緩衝剤を含有せしめる。こうすることにより、フィルターを通過する試料溶液のpHをその後の抗原・抗体反応のために都合のよいpHに調整することができる。緩衝剤の種類及びpHは、分析試料の種類、そのpH、分析対象の種類、分析に用いる反応試薬(例えば抗原、抗体、標識物質等)により異るが、例えばTris緩衝剤、ジエタノール緩衝剤、リン酸緩衝剤、等、常用の緩衝剤を用いることができる。
【0024】フィルターに緩衝剤を付加するには、例えば緩衝液、 100mM〜1M濃度の緩衝液によりフィルターを含浸し、これを常法に従って乾燥すればよい。フィルター(1)と多孔性担体(2)との接着は、例えば物理的に接触させる、例えば機械的に押し付ける、等により行うことができる。
【0025】標識化試薬含有部材は標識された試薬を収容し、且つ試料溶液を適用した場合に該試料溶液中の分析対象と該標識された試薬との反応の場を提供するものである。この場合、標識された試薬は、標識化試薬含有部材に「固定化」されておらず、試料溶液が適用された場合に該溶液に溶解し、標識化試薬含有部材から「遊離」していなければならない。
【0026】従ってこの様な要件を満たすように、標識化試薬含有部材用材料への標識された試薬の適用条件及び標識化試薬含有部材用材料の種類を選択する必要がある。例えば、標識化された試薬の溶液を標識化試薬含有部材用の材料に適用し、これを凍結乾燥する場合、標識化試薬含有部材用の材料としてセルロース膜、ガラス繊維濾紙、ニトロセルロース膜、ナイロン膜等を使用することができ、セルロース膜が好ましい。
【0027】標識化試薬含有部材(3)の寸法は、前記フィルター(1)の幅と同じ幅を有し、その長さは10mm〜50mmが適当である。標識化試薬含有部材(3)と多孔性担体(2)との接着は、例えば、物理的に接触させることにより、例えば機械的に押し付けること、等により行うことができる。
【0028】本発明においては、分析試料として種々の溶液が用いられ、好ましくは生物由来の液体試料、例えば血液、血漿、血清、唾液、尿等が用いられる。これらに含有されており、本発明の装置により分析される分析対象としては、それに対して特異的に結合する物質が存在するものであればよく、例えばポリペプチド、蛋白質、複合蛋白質、多糖類、脂質、複合脂質、ホルモン類、核酸等が例示される。ここで、特異的に結合する物質とは抗原に対する抗体、及び抗体に対する抗原、並びに種々の生理活性物質に対するそのレセプター、等が例示される。
【0029】分析対象のさらに具体的な例としては、被検物質の例としては、卵胞刺激ホルモン、黄体刺激ホルモン、胎盤性ゴナドトロピン、甲状腺ホルモン、リポ蛋白、アポリポ蛋白、アルブミン、ヘモグロビン、プロゲステロン、エストラジオール、等が挙げられるがこれらに限定されるものではない。
【0030】本発明の装置は、特異的反応を用いる、種々の原理に基く測定に使用することができ、その最も典型的な例として、抗原・抗体反応を用いる、いわゆるサンドイッチ法、競合法等が挙げられる。
【0031】サンドイッチ法においては、標識された試薬として、分析対象とは結合するが捕捉試薬とは直接結合しない物質を用い、捕捉試薬として分析対象と結合する物質を用いる。
【0032】例えば、測定対象が抗原である場合、標識された試薬として測定対象に対する第一の抗体を用い、そして捕捉試薬として該測定対象に対する第二の抗体を用いる。この場合、第一の抗体及び第二の抗体は測定対象抗原上の異る抗原決定基を認識するものである。
【0033】この方法においては、測定対象抗原が標識された第一抗体と結合して免疫複合体を形成し、この免疫複合体は、試料溶液が多孔性担体中を移動するに従って移動し、第二抗体が固定されている反応領域に対した時、前記標識された第一抗体/分析対象抗原−免疫複合体中の分析対象抗原がその他方の抗原決定基により第二抗体と結合し、この結果、標識された第一抗体/分析対象抗原/固定された第二抗体−三元免疫複合体(いわゆるサンドイッチ)が反応領域において形成される。従って、このようにして固定(捕捉)された標識物質を検出することにより分析対象抗原の存否又は量を知ることができる。
【0034】サンドイッチ法の第二の態様として、測定対象が抗体である場合、標識された試薬として該測定対象抗体に対する抗体を用い、そして捕捉試薬として該測定対象抗体に対する抗原を用いることができる。また、これとは逆に標識された試薬として測定対象抗体に対応する抗原を用い、そして捕捉試薬として測定対象抗体に対する抗体を用いることもできる。
【0035】さらに、競争的方法においては、分析対象及び標識された試薬の再者が捕捉試薬に競争的に結合するように、標識された試薬及び捕捉試薬を選択することができる。
【0036】この具体例として、捕捉試薬として抗原を用い、分析対象及び標識された試薬は該抗原に競争的に結合する同一の又は異る抗体である。この結果、分析試料溶液中に存在する分析対象抗体と、標識化試薬含有部材中に収容されていた標識された抗体とは相互に結合することなく、試料溶液の移動と共に多孔性担体上の反応領域に輸送される。
【0037】そして、この反応領域に固定されている捕捉抗原との結合に関して前記分析対象抗体と標識された抗体とが競争し、捕捉固定された標識物質の量を測定することにより試料溶液中に存在した分析対象抗体の量を決定することができる。
【0038】また、上記の方法とは逆に、捕捉試薬とし抗体を用い、そして測定対象及び標識された試薬が該捕捉抗体に競争的に結合するように、捕捉物質及び標識された試薬を選択することもできる。
【0039】以上のごとく、本発明の装置においては、多孔性担体上の結合領域に、分析対象、分析原理等に応じて種々の捕捉試薬を固定化して用いるが、本発明の好ましい態様においては「ポジティブコントロール」としての追加の反応領域を、好ましくは前記の分析用反応領域よりも下流に設ける(図1において10)。
【0040】このポジティブコントロール用反応領域には、分析対象の不存在下でも標識された試薬を捕捉することができる物質、すなわち標識された試薬と直接結合する物質、を固定化する。この様な物質として、標識された物質がある動物からの抗体である場合、その動物の抗体に対する他の動物由来の抗体を用いることができる。例えば、標識された物質がマウス抗体である場合、ポジティブコントロール反応領域用捕捉試薬としてマウス抗体に対するウサギ由来の抗体を用いることができる。
【0041】本発明の標識物質としては、当業界において知られている常用の標識物質を用いることができ、またその検出手段としても対応する常用の手段を用いることができる。例えば、標識物質として、それ自体が色を有し、直接目視できる物質、それ自体発光性を有する物質、更なる反応により検出可能なシグナルを発生する物質等を用いることができる。
【0042】しかしながら、本発明の装置は、分析対象を極めて簡単に、且つ短時間に測定することができることを1つの特徴としており、この特徴を発揮するためには、標識物質として直接目視可能な物質、又はそれ自体発光性を有する物質を用いることができる。
【0043】直接目視可能な物質としては、例えば、着色粒子、コロイド状粒子、染料粒子(分散染料)等を挙げることができ、コロイド状金粒子、染料粒子(分散染料、染料ゾル)等が特に好ましい。また、それ自体発光性を有する物質としては蛍光発色団、例えばフルオレッセイン等を用いることができる。また放射性同位元素を用いることができる。
【0044】更なる反応により検出可能なシグナルを発生することができる物質としては、例えば酵素、酵素等を収容したリポゾーム等を用いることができる。酵素としては例えばカルカリホスファターゼ、ワサビパーオキシダーゼ、β−ガラクトシダーゼ等を用いることができ、これらの検出方法は当業界においてよく知られている。
【0045】上記の種々の標識物質はいずれも当業界において知られており、そしてそれらを反応試薬、例えば抗原、抗体等に結合させる(後者を標識する)方法も当業界においてよく知られている。
【0046】前記のごとく、本発明の装置により分析対象物を定量するためには、図1のCに示すように、複数の反応領域(ポジティブコントロール用反応領域のほかに)を設けるのが好ましい。また効率よく、精度よくまた広範囲にわたる量(濃度)の分析対象物を定量しようとする場合、反応領域が下流に位置するに従って多くの捕捉試薬を固定しておく必要がある。
【0047】この場合、例えば試料中の分析対象の量が非常に少ない場合、分析対象物と標識物質および捕捉試薬との反応効率によって、捕捉試薬が最も多く固定化された反応領域(最下流)においてのみ分析対象物が捕捉可能となり、シグナル(例えは発色)が得られ、従って1個のシグナル(発色)をもたらす。
【0048】しかし、分析対象の量が多くなればなるほど、捕捉試薬の量が少ない反応領域でも分析対象物が捕捉され、シグナル(発色)をもたらす。こうして、分析対象の量(濃度)に応じた数のシグナル(発色)が得られる。
【0049】本発明の他の態様においては、分析試料中の複数種類の分析対象に対応して複数の標識された試薬を標識化試薬含有領域に収容せしめ、それに対応して複数の反応領域を設けることができる。こうすることにより、1つの分析試料中に存在する複数の種類の分析対象を、1個の装置を用いる1回の操作により同時に測定することができる。
【0050】本発明の装置の他の態様においては、装置の小部分又は大部分をカバー部材により覆うことができる。この場合、カバーの少なくともフィルターに対応する部分に試料適用のための窓を設ける必要がある。さらに分析結果を目視する方式の装置においては、カバーの少なくとも反応領域に対応する部分には観察用の窓を設けるか、又は透明部材により構成するか、あるいはカバーが存在しないようにする必要がある。この構成により、分析に際して装置の上流端を全体的に分析用試料溶液中に浸漬するか、又は該上流端に分析用試料溶液を注びかけることにより極めて簡単に試料を適用することができる。
【0051】次に、このカバー付き装置の具体例を図4及び図5により説明する。図4はこの装置の構造を模式的に示すものであり、図5はこの装置を部材に分解して示すものである。この装置は、装置全体に強度を与え、且つ装置のカバーとして機能するZ形に曲げられた長い部材(Z形部材)(20)を有し、これは標識化試薬含有部材支持部(21)及び多孔性担体支持部(22)並びに垂直部(23)を有する。さらに、その下流端が曲げられ、多孔性担体固定部(24)が構成されている。このZ形部材はさらにその垂直部(23)に貫通孔(25)を有する。
【0052】多孔性担体(2)は、前記貫通孔(25)を通してZ部材(20)にそって配置され、そして多孔性担体固定部(24)により固定される。標識化試薬含有部材(3)は、前記標識化試薬含有部材支持部(22)と多孔性担体(2)との間に挿入される。また、フィルター1は多孔性担体(2)の上であって標識化試薬含有部材(3)に対応する位置に配置される。
【0053】Z形部材(20)の標識化試薬含有部材支持部(21)、標識化試薬含有部材(3)、多孔性担体(2)及びフィルター(1)は、留具(30)により機械的に押付けられ一体化される。こうしてフィルター(1)、多孔性担体(2)及び標識化試薬含有部材(3)が相互に接触する。
【0054】留具(30)は、その上面31に開口部、すなわち窓32を有し、この窓を通して試薬溶液がフィルター(1)に適用される。留具(30)はつめ(33)を有し、その曲った先端34部が標識化試薬含有部材支持部(21)を背部から抱え込むことにより関連各部材が一体化される。
【0055】この構造において、Z形部材(20)の材質は特に限定されないが、例えば合成樹脂板を用いるのが便利である。Z形部材が透明である場合、多孔性担体上に現われる測定結果は図4の矢印26及び27のいずれの方向からでも観察することができる。これに対して、Z形部材が不透明な材料から作られている場合、測定結果はカバーとしてのZ形部材が存在しないか又は窓を形成している側(図4における矢印27)から観察される。
【0056】留具(30)の材質も特に限定されず、例えば金属、合成樹脂板等が使用される。なお、1つの態様においては、標識化試薬含有部材支持部(21)の上面であって長手方向の縁部に2本の線状の凸部を形成し、この間に標識化試薬含有部材(3)を配列することにより該部材動きを防止し、同時に分析用試料溶液の横からの侵入を防止することもできる。また、標識化試薬含有部材支持部(21)に貫通孔を設けて、標識化試薬含有部材(3)に分析用試料溶液が入る場合に脱気を促進することもでき、またこの孔を通して、分析用試料溶液の一部が標識化試薬含有部材(3)に入るようにすることもできる。
【0057】次に、実施例により本発明をさらに具体的に説明する。
実施例1. hCG のイムノクロマトグラフィーアッセイa)金コロイド標識化マウス抗 hCG抗体の調製金コロイド標識化方法については、Journal of Immunoassay 1(1), 77-91, 1980に記載されている方法に準じて行うことが出来る。例えば、金コロイドG30(粒径30nm、Amersham International plc. から供給される。)20mlに0.2NのK2CO3 3mlを加えpH7に調製した。一方、2mM硼砂緩衝液pH9で透析したマウス抗hCG抗体(1mg/ml)を 100,000g、1時間遠心後、その上清2/3をとり2mM硼砂緩衝液pH9で40μg/mlに希釈した。
【0058】金コロイド液(pH7)20mlを攪拌しながら抗体溶液2mlを加え、2分間攪拌する。次いで1% PEG 20,000ml 、10% BSA(1N NaCl でpH9に調製されている)2mlを加える。この反応液を12,000gで遠心し得られた沈査を1% BSA、0.05% PEG 20,000 を含む20mMトリス塩酸緩衝液(pH8.2)に再浮遊させ、再度遠心した。
【0059】この操作を3回繰り返し最終的に得られた沈査を1% BSA、0.05% PEG 20,000 を含む20mMトリス塩酸緩衝液(pH8.2)で再浮遊させ、波長 520nmでの吸光度が6.0になるように調製する。得られた金コロイド標識化抗体液を5%BSA、0.05% PEC 20,000 、0.3M NaCl を含む20mMトリス塩酸緩衝液(pH8.2)で2倍希釈し、最終調製液とした。
【0060】b)染料ゾル標識化マウス抗 hCG抗体の調製染料ゾル標識化方法については、特開昭56−160655明細書に記載されている。例えば、ルミナスRed(BASF社から供給される) 2.5gを50mlの蒸留水に懸濁させ、45分間室温で攪拌する。これを 125g、30分間遠心後、沈査を50mlの蒸留水で再浮遊させた。この操作を3回繰り返し洗浄した。得られた沈査を25mlの蒸留水で再浮遊させた後、同レベルの量のガラスビーズ(直径3mm:4mm=1:2に混合したもの)を加え5日間振盪した。この染料ゾル液を回収し 300g、30分間遠心した後、 1,000g、30分間さらに遠心し下層部を採取した。
【0061】ついで波長 520nmの吸光度を5.0に調整した。一方、マウス抗 hCG抗体溶液を5mM NaCl(pH7に0.1Na2CO3で調整されている)で透析後1mg/mlに調整した。この抗体溶液0.1mlをルミナス Red液5mlに加え、室温で1時間反応させる。さらに30% BSA、0.01%チメロザールを含む5mM NaCl(pH7) で波長 520nmでの吸光度を8.0に調整した。
【0062】c)多孔性担体の調製マウス抗 hCG抗体を1mg/mlの濃度に10mMリン酸緩衝液生理食塩水(pH7.2)で調整する。ガラス繊維濾紙(GF/A、 Whatman社製、20cm×12cm)上にこの抗体溶液を直線状に塗布した。塗布はアクリル棒に抗体溶液をしみ込ませて、直線を引いた。さらにポジティブコントロールとしてウサギ抗マウス抗体を同様に抗 hCG抗体塗布線の下流側に塗布した。この多孔性抗体を25℃で18時間乾燥した。次に1%ゼラチン液に1時間、浸した後10mMリン酸緩衝液生理食塩水(pH7.2)で3回洗浄した。これを陰圧乾燥機で乾燥後、抗体の塗布線に垂直に5mm幅で切断し、5mm×12cmの多孔性担体を作製した。
【0063】d)標識化試薬含有部材の調製粘稠性濾紙(NO.60、Toyo Roshi社製)5mm×30mmに実施例1.a)又はb)項に記載の方法で調製した標識化試薬を75μl加え、凍結乾燥した。
【0064】e)フィルターの調製ガラス繊維濾紙 (GF/A、 Whatman社製)8mm×30mmに 200mMトリス塩酸緩衝液(pH10)をしみ込ませて凍結乾燥した。
【0065】f)定量分析用多孔性担体の調製マウス抗 hCG抗体溶液を2,1,0.5,0.25、及び 0.125mg/mlの各濃度に10mMリン酸緩衝液生理食塩水(pH7.2)で調整した。この抗体溶液を実施例1.c)項に記載の方法で上流側から下流側に向かって薄い濃度の抗体溶液から、段階状に塗布した。これを定量用多孔性担体とした。
【0066】g)hCG の測定実施例1.のa),c),d),e)に記載の方法で調製した多孔性担体、金コロイド標識化抗体含有パッドおよびフィルターを用いて、図1A及び図2に示す装置を組み立てた。図1は本発明の装置を示し、図2aおよびbは比較対照として用いた装置を示す。尚、各装置の金コロイド標識化抗体の量は同量とした。hCG 0, 10, 25, 50、又は 100IU/lをそれぞれ含む0.2% BSA−リン酸緩衝生理食塩水を試験試料とし、この各試験試料をフィルターへ適用した。経時的、可視的に観察しバンドの呈色が確認された時間と10分後の呈色バンドの強さを記録した。結果を表1に示す。
【0067】
【表1】

【0068】h)濾過膜の効果の確認尿を試験試料として用いた場合の本発明の装置の効果を確認するためにhCG(0, 25、又は50IU/l)を含んだ尿試料を準備し、本発明の装置へ適用した。対照として、フィルターを除いた同様な装置を用いた。観察は実施例1.g)項に記載の方法に準じた。観察された結果を以下の表2に示す。
【0069】
【表2】

【0070】i)フィルターへの緩衝液添加の効果の確認フィルターへのトリス塩酸緩衝液あるいはジエタノールアミン緩衝液添加の効果について検討した。尿を試験試料とする場合、一般的に尿のpHは5〜8(平均6)であり、特に酸性尿の場合はpH4になるといわれる。そこで尿のpHを4に調整し、本発明の装置へ適用した。また対照として緩衝液を含まないフィルターを用いた。観察された結果は次のとおりである。尚、 hCGは含まない尿を試料とした。結果を表3に示す。
【0071】
【表3】

【0072】j)hCG の定量分析免疫クロマトグラフィー法で定量分析を行うために実施例1.f)項に記載の方法で調製した多孔性担体を用いて本発明の装置を組み立てて、hCG(0, 10, 50,100, 500IU/l)試験試料を適用した。観察された結果を以下に示す。 hCGの濃度が増すに連れて、確認される呈色バンドの数が据えた。結果を表4に示す。
【0073】
【表4】

【0074】この結果で得られた呈色バンドの発色強度を数値で表せば検量線が得られる。例えば、TLCスキャナー(島津社製)を用いて波長 530nmの吸光度を求めて各ピークの高さを積算する。この結果を図示すれば検量線が得られる。結果を表5に示す。
【0075】
【表5】

【0076】実施例2.図1に示す本発明の装置と図4に示す市販の装置(商品A及び商品B)とを hCGの測定において比較した。市販の装置は図4に示すように、多孔性担体の一端に試料適用部位が存在し、その下流に抗hCG 標識化抗体が含浸されており、さらに下流に抗hCG 固定化抗体(反応領域)及びポジティブコントロール用反応領域を有する。hCG 0, 10, 25, 50, 100IU/lをそれぞれ含む、0.2% BSA−リン酸緩衝生理食塩水を試験試料とし、この試料を各装置の用法用量に従って適用した。経時的、可視的に観察しバンドの呈色が確認された時間と10分後のバンドの強さを記録した。結果を表6に示す。
【0077】
【表6】

上記のごとく、本発明の装置は従来の装置に比べて非常に鋭敏である。
【図面の簡単な説明】
【図1】この図のAは本発明の装置の1態様を横から見た略面であり、BはAの装置の平面図であり、そしてCは本発明の装置の、多数の反応領域を有する態様を示す。
【図2】この図のa及びbはいずれも従来技術の装置を模式的に示したものである。
【図3】本発明の装置の他の態様であって、図1に示す装置が、フィルターに対応する部分に窓を有する透明な不透水性カバーにより覆われている。
【図4】本発明の装置の一例を模式的に示すものである。
【図5】図4に示す装置を構成部材に分けて示す。
【図6】従来技術の装置を示す。
【符号の説明】
1…フィルター
2…多孔性担体
3…標識化試薬含有部材
4…反応領域
10…ポジティブコントロール用反応領域
11…不透水性透明カバー
12…試料適用のための窓
【特許請求の範囲】
【請求項1】 フィルター、標識化試薬含有部材、及び1又は複数の反応領域を有する多孔性担体を有する免疫測定装置であって、該多孔性担体がその上流端において該フィルターと該標識化試薬含有部材とにより挟まれており、該反応領域が該フィルター及び該標識化試薬含有部材から離れてその下流に位置し、該標識化試薬含有部材が標識された試薬を含有しており、そして該反応領域に捕捉試薬が固定されていることを特徴とする、特異的反応を用いて分析対象を測定する測定装置。
【請求項2】 前記標識された試薬が、前記分析対象とは結合するが前記捕捉試薬とは直接結合しない物質である、請求項1に記載の装置。
【請求項3】 前記測定対象が抗原であり、前記標識された試薬が測定対象抗原に対する第一の抗体であり、前記捕捉試薬が該測定対象に対する第二の抗体であり、そして該第一の抗体及び該第二の抗体は該測定対象抗原上の異る抗原決定基を認識するものである、請求項2に記載の装置。
【請求項4】 前記測定対象が抗体であり、前記標識された試薬が該測定対象抗体に対する抗体であり、そして前記捕捉試薬が該測定対象抗体に対する抗原である、請求項2に記載の装置。
【請求項5】 前記測定対象が抗体であり、前記標識された試薬が該測定対象抗体に対する抗原であり、そして前記捕捉試薬が該抗体に対する抗体である、請求項2に記載の装置。
【請求項6】 前記分析対象及び前記標識された試薬の両者が前記捕捉試薬に競争的に結合する物質である、請求項1に記載の装置。
【請求項7】 前記捕捉試薬が抗原であり、そして前記測定対象及び前記標識された試薬が該捕捉抗原に競争的に結合する同一の又は異る抗体である、請求項6に記載の装置。
【請求項8】 前記捕捉試薬が抗体であり、そして前記測定対象及び前記標識された試薬が該捕捉抗体に競争的に結合する抗原である、請求項6に記載の装置。
【請求項9】 前記反応領域が複数存在し、これらの反応領域に上流から下流に向けて増加する量の捕捉試薬が固定化されており、発色した反応領域の数により分析対象を定量できるようにした、請求項1に記載の装置。
【請求項10】 前記フィルターがpH緩衝剤を含有する、請求項1に記載の装置。
【請求項11】 装置の少なくとも部分が不透水性カバーで覆われており、該カバーは装置のフィルターに対応する部分に試料適用のための窓を用し、さらに装置の多孔性担体上の反応領域に対応する部分に観察用窓を有するか又は少なくともカバーのこの部分が透明部材により作られているか又はこの部分にカバーが存在しない、請求項1に記載の装置。
【請求項12】 前記多孔性担体がポジティブコントロール用反応領域を有する、請求項1に記載の装置。
【請求項13】 標識化試薬含有部材が、複数種類の分析対象に対応する複数種類の標識された試薬を収容しており、さらに多孔性部材が対応する複数の反応領域を有し、同時に複数の分析対象の測定が可能な、請求項1に記載の装置。
【請求項1】 フィルター、標識化試薬含有部材、及び1又は複数の反応領域を有する多孔性担体を有する免疫測定装置であって、該多孔性担体がその上流端において該フィルターと該標識化試薬含有部材とにより挟まれており、該反応領域が該フィルター及び該標識化試薬含有部材から離れてその下流に位置し、該標識化試薬含有部材が標識された試薬を含有しており、そして該反応領域に捕捉試薬が固定されていることを特徴とする、特異的反応を用いて分析対象を測定する測定装置。
【請求項2】 前記標識された試薬が、前記分析対象とは結合するが前記捕捉試薬とは直接結合しない物質である、請求項1に記載の装置。
【請求項3】 前記測定対象が抗原であり、前記標識された試薬が測定対象抗原に対する第一の抗体であり、前記捕捉試薬が該測定対象に対する第二の抗体であり、そして該第一の抗体及び該第二の抗体は該測定対象抗原上の異る抗原決定基を認識するものである、請求項2に記載の装置。
【請求項4】 前記測定対象が抗体であり、前記標識された試薬が該測定対象抗体に対する抗体であり、そして前記捕捉試薬が該測定対象抗体に対する抗原である、請求項2に記載の装置。
【請求項5】 前記測定対象が抗体であり、前記標識された試薬が該測定対象抗体に対する抗原であり、そして前記捕捉試薬が該抗体に対する抗体である、請求項2に記載の装置。
【請求項6】 前記分析対象及び前記標識された試薬の両者が前記捕捉試薬に競争的に結合する物質である、請求項1に記載の装置。
【請求項7】 前記捕捉試薬が抗原であり、そして前記測定対象及び前記標識された試薬が該捕捉抗原に競争的に結合する同一の又は異る抗体である、請求項6に記載の装置。
【請求項8】 前記捕捉試薬が抗体であり、そして前記測定対象及び前記標識された試薬が該捕捉抗体に競争的に結合する抗原である、請求項6に記載の装置。
【請求項9】 前記反応領域が複数存在し、これらの反応領域に上流から下流に向けて増加する量の捕捉試薬が固定化されており、発色した反応領域の数により分析対象を定量できるようにした、請求項1に記載の装置。
【請求項10】 前記フィルターがpH緩衝剤を含有する、請求項1に記載の装置。
【請求項11】 装置の少なくとも部分が不透水性カバーで覆われており、該カバーは装置のフィルターに対応する部分に試料適用のための窓を用し、さらに装置の多孔性担体上の反応領域に対応する部分に観察用窓を有するか又は少なくともカバーのこの部分が透明部材により作られているか又はこの部分にカバーが存在しない、請求項1に記載の装置。
【請求項12】 前記多孔性担体がポジティブコントロール用反応領域を有する、請求項1に記載の装置。
【請求項13】 標識化試薬含有部材が、複数種類の分析対象に対応する複数種類の標識された試薬を収容しており、さらに多孔性部材が対応する複数の反応領域を有し、同時に複数の分析対象の測定が可能な、請求項1に記載の装置。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開平5−5743
【公開日】平成5年(1993)1月14日
【国際特許分類】
【出願番号】特願平3−11161
【出願日】平成3年(1991)1月31日
【出願人】(000250100)湧永製薬株式会社 (51)
【公開日】平成5年(1993)1月14日
【国際特許分類】
【出願日】平成3年(1991)1月31日
【出願人】(000250100)湧永製薬株式会社 (51)
[ Back to top ]

