炎症又は感染の検出のための過分極13Cピルビン酸塩を含む磁気共鳴造影媒体の使用
本発明は過分極13C−物質を含む造影媒体を用いた炎症又は感染の13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、過分極13C−物質を含む造影媒体を用いた炎症又は感染の炭素−13(13C)磁気共鳴(MR)造影又は分光の方法に関する。本発明は、炎症又は感染を検出又は監視するための、MR造影によって次に造影するための過分極された炭素−13標識分子の応用に関する。
【背景技術】
【0002】
炎症は体組織に損傷を与える有害な因子に対する生物学的反応である。炎症は宿主の防御と組織傷害の間のバランスを取る作用である。炎症反応の鍵となるのは免疫系と血管組織である。免疫系は白血球と、生体が感染と戦うこと、有害な刺激を除去すること、及び損傷組織を修復することを助ける分子とからなっている。炎症過程の間、免疫系及び増大した血流は病原体を排除し、傷害を受けた組織を修復することを助ける。
【0003】
炎症には、感染又は傷害を受けた部位に栄養分及び免疫系の追加的な成分を搬入するために新たな血管を動員することが含まれる。炎症はしばしば外因性病原体(例えば細菌、ウイルス、真菌、寄生虫、プリオン及びウイロイド)の結果であるが、炎症反応の他の起因因子としては自己抗原、外傷、アレルゲン、及び刺激物がある。炎症がなければ創傷及び感染は治癒せず、組織の進行性破壊は生命体の死につながるであろう。炎症はしばしば、潜在的な疾患が存在し、生体がその疾患を排除しようとしていることを知らせている。感染は外来種による宿主生命体への定着であり、これはしばしば臨床的に明白な疾患をもたらす。外来種は通常、細菌のコロニー、真菌、ウイルス、寄生虫、プリオン、又はウイロイド等の顕微鏡的病原体である。炎症は感染を排除するために宿主生命体によって搭載されている機構である。炎症はまた自己抗原、損傷組織(例えば外傷)、アレルゲン、又は刺激物を排除するために起こることもある。
【0004】
しかし、炎症は調節を誤った場合又は制御なく放置された場合には、宿主に問題を生じることもあり、その中には自己免疫疾患、アレルギー、アテローム性動脈硬化症、炎症性及び退行性関節炎、喘息、慢性気管支炎、慢性閉塞性肺疾患(COPD)、及び多発性硬化症が含まれる。炎症が正常には生体によって厳しく規制されているのはこのためである。炎症は急性又は慢性のいずれかに分類することができる。急性炎症は有害な刺激に対する生体の最初の反応であり、血液から傷害組織への血漿及び白血球の移動の増大によって達成される。生化学的事象のカスケードが伝播し、局所血管系、免疫系、及び傷害組織内の種々の細胞が関与する炎症反応を成熟させる。慢性炎症として知られている長期的な炎症は、炎症の部位に存在する細胞の型を進行的に変化させ、炎症プロセスからの組織の崩壊及び治癒が同時に起こることによって特徴付けられる。
【0005】
炎症疾患及び感染疾患は分子レベル及び細胞レベルでの同様の機構を共有している。これらの疾患は免疫系の活性化をもたらし、臨床的に検出及び監視するのが困難なことが多い疾患プロセスである。現在のところ、炎症及び感染の造影による検出のための選択は限られており、治療に対するこれらの疾患の反応を検出し、監視するための良好な臨床的試験は存在しない。臨床医は、患者がどのように感じているかという主観的な方法、血液検査(白血球数、CRP等)等の二次的兆候、非特異的核医学造影、又は解剖学的造影(従来のMRI、超音波、コンピュータ断層撮影、及びX線写真)に基づく疾患の晩期解剖学的変化に頼らざるを得ない。例として、関節リウマチは老年人口の約1%が罹患するありふれた疾患であり、現在関節リウマチを検出し、又は監視するための良好な非侵襲的検査は存在しない。臨床医にはしばしば、疾患を診断するため及び患者がどのように治療に反応しているかを決定するために、主観的な方法しか残されていない。したがって、ヒト又はヒト以外の動物の身体においてインビボで非侵襲的に炎症及び感染を検出することには興味がある。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】国際公開第2009/133169号
【発明の概要】
【発明が解決しようとする課題】
【0007】
MR造影(MRI)、MR分光法(MRS)及びMR分光造影(MRSI)等のMR検出は炎症及び感染を検出するための価値あるツールとなる可能性があり、これらのツールは非侵襲的に、また患者及び医療関係者をX線等の有害な可能性がある放射線に曝すことなく患者の体及びその部分の画像を得ることを可能にするので、医師たちにとって特に魅力的なものになってきた。優れた軟組織コントラスト及び良好な空間的及び時間的解像度を備えたその高品質な画像のため、MRIは軟組織及び臓器の好ましい造影手法である。
【課題を解決するための手段】
【0008】
ところで、過分極13C−物質が13C−MRI、13C−MRS、又は13C−MRSIを用いたヒト又はヒト以外の動物の身体における炎症及び感染を検出するための薬剤として用い得るということが見出された。
【0009】
したがって、第1の態様において、本発明は過分極13−C物質を含む造影媒体を用いて炎症又は感染を検出するための13C−MR造影及び/又は13C−MR分光法及び/又は13C−MR分光造影の方法を提供する。そのような物質は、10秒より長く、好ましくは30秒より長く、さらにより好ましくは60秒より長い縦緩和時間定数(T1)を有する核を含むはずである。そのような、いわゆる「高T1薬剤」は、例えば国際公開第99/35508号に記載されている。或いは、候補物質のT1値は文献で見出されるか、候補物質のNMRスペクトル、例えば13C−標識された候補物質のT1を決定するための13C−NMRスペクトルを取得することによって決定し得る。
【発明を実施するための形態】
【0010】
好ましい過分極13C−物質はヒト及びヒト以外の動物の身体における代謝プロセスにおいて役割を果たす生体分子である。したがって、特に好ましい物質は内因性化合物、より好ましくはヒト又はヒト以外の動物の身体における代謝プロセスにおいて役割を果たす内因性化合物である。特に好ましい物質はアミノ酸(プロトン化又は脱プロトン化形における)、好ましくはアラニン、グリシン、グルタミン、グルタミン酸、システイン、アスパラギン及びアスパラギン酸、酢酸塩、ピルビン酸、ピルビン酸塩、シュウ酸塩、リンゴ酸塩、フマル酸塩、乳酸塩、乳酸、クエン酸塩、重炭酸塩、マロン酸塩、コハク酸塩、オキサロ酢酸塩、α−ケトグルタル酸塩、3−ヒドロキシ酪酸塩、イソクエン酸塩及び尿素から選択される。
【0011】
ピルビン酸塩は比較的高い濃度においてさえも極めて良好に人体に認容される内因性化合物である。クエン酸サイクルにおける前駆体として、ピルビン酸塩は人体内で重要な代謝的役割を果たす。ピルビン酸は種々の化合物に変換される。そのトランスアミノ化は酸化的脱カルボキシル化を経てアラニンを生じ、ピルビン酸塩はアセチル−CoA及び二酸化炭素(これはさらに重炭酸塩に変換される)に変換され、ピルビン酸塩の還元は乳酸塩及びそのオキサロ酢酸塩におけるカルボキシル化をもたらす。
【0012】
さらに、過分極13C−ピルビン酸塩の、その代謝産物である過分極13C−乳酸塩、過分極13C−重炭酸塩(13C1−ピルビン酸塩、13C1,2−ピルビン酸塩又は13C1,2,3−ピルビン酸塩の場合のみ)及び過分極13C−アラニンへの代謝的変換は、MRを用いて人体内の代謝プロセスを研究するために用いることができる。13C1−ピルビン酸塩はヒト全血中、37℃で約42sのT1緩和を有するが、過分極13C−ピルビン酸塩の過分極13C−乳酸塩、過分極13C−重炭酸塩及び過分極13C−アラニンへの変換は充分に速く、13C−ピルビン酸塩ペアレント化合物及びその代謝産物からの信号の検出は可能であることが見出された。アラニン、重炭酸塩及び乳酸塩の量は検査する組織の代謝状態に依存する。過分極13C−乳酸塩、過分極13C−重炭酸塩及び過分極13C−アラニンのMR信号強度はこれらの化合物の量及び検出の時に残っていた分極の程度に関連し、したがって過分極13C−ピルビン酸塩の過分極13C−乳酸塩、過分極13C−重炭酸塩及び過分極13C−アラニンへの変換を監視することによって、非侵襲的MRI、MRS、又はMRSIを用いたインビボでのヒト又はヒト以外の動物の身体における代謝プロセスの研究が可能である。
【0013】
種々のピルビン酸塩代謝産物から生じるMR信号の振幅は組織型によって変動することが見出された。アラニン、乳酸塩、重炭酸塩及びピルビン酸塩によって生じる独特の代謝ピークパターンは、検査する組織の代謝状態を表わす指紋として用いることができ、それにより健常組織と非健常組織との間の区別が可能になる。腫瘍造影のための過分極13C−ピルビン酸塩の使用(腫瘍組織が高い代謝活性を示す)は国際公開第2006/011810号に詳しく記載されている。さらに、心臓造影のための過分極13C−ピルビン酸塩の使用は国際公開第2006/054903号に記載されている。
【0014】
このように、好ましい実施形態では本発明は過分極13C−ピルビン酸塩を含む造影媒体を用いて炎症又は感染を検出するための13C−MR造影及び/又は13C−MR分光法及び/又は13C−MR分光造影の方法を提供する。
【0015】
本発明は、どのようにして炎症又は感染の部位を検出するかという課題を解決する。これは、診断及び検出することが困難な潜在的感染に特に重要である。本発明の方法によって疾患領域の解剖学的位置が同定される。さらに、本発明の方法によって炎症又は感染の部位を定量化することができ、疾患活性の代謝プロセスに関する情報を提供することができる。したがって、本方法は解剖学的造影に加えて代謝プロセスを特徴付けることができるという利益を含んでいる。分子プロセスの変化を検出することは、疾患を解剖学的に記述することよりも感度及び特異性が高い可能性がある。本発明の方法で用いる過分極炭素−13MRSIは、分子プロセスに対する感度を劇的に増大させる。本発明の主観的且つ定量的な造影方法によって疾患をより早く検出できる可能性があり、より良く治療に合わせられる可能性がある。これは薬剤の選択が困難で疾患の進行が監視困難な、喘息、慢性気管支炎、COPD、及び多発性硬化症等の炎症要素を有する疾患の治療において特に重要であり得る。さらに、本発明によって薬剤の開発を加速することを助けられる可能性もある。というのは、本発明の非侵襲的な方法が疾患活動性を測定するために利用可能である場合には、より少ない対象者数及びより短い時間しか必要としないからである。
【0016】
当技術の応用として、本発明者らは13C−ピルビン酸塩が炎症を検出するために用い得ることを示した。しかし、過分極し得る同位元素を用いて作成されるいかなる物質も、潜在的には炎症又は感染を検出又は監視するための候補となり得る。過分極MRI手法を用いて炎症又は感染を検出するための候補である他の物質としては、酸素、窒素、キセノン、ヘリウム、及びフッ素の同位元素を含む物質が挙げられる。
【0017】
用語「13C−ピルビン酸塩」は13C−ピルビン酸の塩を意味する。以下において用語ピルビン酸塩、13C−ピルビン酸塩及び13C1−ピルビン酸塩は互換的に用いられ、全て13C1−ピルビン酸塩を意味する。同様に用語ピルビン酸、13C−ピルビン酸及び13C1−ピルビン酸は互換的に用いられ、全て13C1−ピルビン酸を意味する。さらに、用語乳酸塩、13C−乳酸塩及び13C1−乳酸塩は互換的に用いられ、さらに特定しない限り、全て13C1−乳酸塩を意味する。
【0018】
用語「過分極」及び「分極」はこれ以降、互換的に用いられ、0.1%を超え、より好ましくは1%を超え、最も好ましくは10%を超える核分極レベルを意味する。
【0019】
分極レベルは例えば固体過分極13C−ピルビン酸塩、例えば13C−ピルビン酸塩の動的核分極(DNP)によって得られる固体過分極13C−ピルビン酸塩における固体状態13C−NMRの測定によって決定し得る。固体状態13C−NMR測定は、好ましくは低いフリップ角を用いた単純パルス獲得NMRシーケンスからなる。NMRスペクトルにおける過分極13C−ピルビン酸塩の信号強度を分極プロセスの前に取得したNMRスペクトルにおける13C−ピルビン酸塩の信号強度と比較する。次いで分極前後の信号強度の比から分極レベルを計算する。
【0020】
同様にして、溶解した過分極13C−ピルビン酸塩の分極レベルを液体状態NMR測定によって決定することができる。ここでも溶解した過分極13C−ピルビン酸塩の信号強度を分極前の溶解した13C−ピルビン酸塩の信号強度を比較する。次いで分極前後の13C−ピルビン酸塩の信号強度の比から分極レベルを計算する。
【0021】
用語「造影媒体」は、MR活性剤としての過分極13C−ピルビン酸塩等の過分極13C−物質を含むが、これに限らない液体組成物を意味する。本発明による造影媒体は、MR造影における造影媒体として、又はMR分光法及びMR分光造影におけるMR分光剤として用い得る。
【0022】
本発明の方法による造影媒体は、インビボMR造影、分光法及び/又は分光造影、即ち生きたヒト又はヒト以外の動物について実施されるMR造影、分光法及び/又は分光造影のための造影媒体として用い得る。さらに、本発明の方法による造影媒体は、インビトロMR造影、分光法及び/又は分光造影のため、例えば細胞培養物又はエクスビボ組織において炎症又は感染を検出及び監視するための造影媒体として用い得る。細胞培養物は、例えば血液、尿又は唾液等のヒト又はヒト以外の動物の身体から得られる試料から得た細胞から誘導し得る。一方エクスビボ組織は生検又は手術から得られる。
【0023】
本発明の方法で用いる過分極13C−ピルビン酸塩の同位体濃縮は、好ましくは75%以上、より好ましくは80%以上、特に好ましくは90%以上であり、90%を超える同位体濃縮が最も好ましい。理想的には、濃縮は100%である。本発明の方法で用いる13C−ピルビン酸塩は、C1位(13C1−ピルビン酸塩)、C2位(13C2−ピルビン酸塩)、C3位(13C3−ピルビン酸塩)、C1位及びC2位(13C1,2−ピルビン酸塩う)、C1位及びC3位(13C1,3−ピルビン酸塩)、C2位及びC3位(13C2,3−ピルビン酸塩)、又はC1位、C2位及びC3位(13C1,2,3−ピルビン酸塩)で同位体濃縮し得る。C1位での同位体濃縮が好ましい。13C1−ピルビン酸塩は、ヒト全血中、37℃で、他のC位で同位体濃縮された13C−ピルビン酸塩よりも高いT1緩和(約42s)を有するからである。
【0024】
NMR活性13C−核の過分極は、例えば参照により本明細書に組み込まれる国際公開第98/30918号、同第99/24080号及び同第99/35508号に記載された種々の方法によって実施することができ、過分極の方法は貴ガスからの分極転移、「ブルートフォース」、スピン凍結、パラ水素法及び動的核分極(DNP)である。
【0025】
過分極13C−ピルビン酸塩を得るには、13C−ピルビン酸塩を直接分極するか、13C−ピルビン酸を分極し、分極した13C−ピルビン酸を例えば塩基で中和して分極13C−ピルビン酸塩に変換することのいずれかが好ましい。
【0026】
過分極13C−ピルビン酸塩を得るための1つの適当な方法は過分極貴ガスからの分極転移であり、これは国際公開第98/30918号に記載されている。ノンゼロ核スピンを有する貴ガスは、円偏光を用いることによって過分極することができる。過分極貴ガス、好ましくはHe又はXe、又はそのようなガスの混合物は、13C−核の過分極に効果を与えるために用い得る。過分極ガスは気相でもよく、液体/溶媒に溶解してもよく、又は過分極ガスそれ自体が溶媒として働いてもよい。或いは、冷却された固体表面上にガスを凝縮させてこの形態で用いてもよく、昇華させてもよい。
【0027】
過分極ガスを13C−ピルビン酸塩又は13C−ピルビン酸と緊密に混合することが好ましい。したがって、室温で液体である13C−ピルビン酸を分極させる場合には、過分極ガスは好ましくは液体/溶媒に溶解するか、溶媒として働く。13Cピルビン酸塩を分極させる場合には、過分極ガスは好ましくは液体/溶媒に溶解し、これはまたピルビン酸塩を溶解させる。
【0028】
過分極13C−ピルビン酸塩を得るための別の適当な方法は、極低温及び高磁場における熱力学的平衡によって分極を13C−核に与えることである。NMR分光計の操作磁場及び温度に比べて、非常に高い磁場及び非常に低い温度を用いることによって、過分極がもたらされる(ブルートフォース)。用いる磁場強度はできるだけ高く、適切には1Tより高く、好ましくは5Tより高く、より好ましくは15T以上、特に好ましくは20T以上とする。温度は極めて低く、例えば4.2K以下、好ましくは1.5K以下、より好ましくは1.0K以下、特に好ましくは100mK以下とする。
【0029】
過分極13C−ピルビン酸塩を得るための別の適当な方法は、スピン凍結法である。この方法はスピン凍結分極による固体化合物又は系のスピン分極に及ぶ。系は次数3以上の対称軸を有するNi2+、ランタニド又はアクチニドイオン等の適当な結晶性常磁性材料でドープするか、これらと緊密に混合する。共鳴励起磁場は適用されないので、均一な磁場の必要はなく、装置はDNPに必要なものよりも単純である。プロセスは、磁場の方向に垂直な軸の周りに試料を物理的に回転させることによって行なわれる。この方法の前提条件は、常磁性種が高度に異方性のg−ファクターを有することである。試料回転の結果として、電子常磁性共鳴が核スピンと接触させられ、核スピン温度の低下をもたらす。試料回転は、核スピン分極が新たな平衡に達するまで行なわれる。
【0030】
好ましい実施形態では、過分極13C−ピルビン酸塩を得るために動的核分極(DNP)が用いられる。DNPにおいては、分極すべき化合物中のMR活性核の分極は、分極剤又はいわゆるDNP剤、不対電子を含む化合物によって影響される。DNPプロセスの間、通常はマイクロ波照射の形のエネルギーが供給され、最初はこれがDNP剤を励起することになる。基底状態への減衰の際に、DNP剤の不対電子から分極すべき化合物のNMR活性核への、例えば13C−ピルビン酸塩の13C核への分極の転移がある。一般にDNPプロセスにおいては、例えばDNPプロセスを液体ヘリウム中、約1T以上の磁場で実施することによって、中程度の又は高い磁場と極めて低い温度が用いられる。或いは、中程度の磁場と充分な分極促進が達成される任意の温度を利用してもよい。DNP手法は例えば国際公開第98/58272号及び同第01/96895号にさらに記載されており、それらの開示内容は援用によって本明細書の内容の一部をなす。
【0031】
化合物をDNP法によって分極するためには、分極すべき化合物とDNP剤との混合物を調製し(「試料」)、これを次に凍結して分極のためのDNPポーラライザーに挿入する。分極の後、凍結された固体過分極試料を、それを融解するか若しくはそれを適当な溶解媒体に溶解することによって迅速に液体状態に移す。溶解が好ましく、そのための凍結過分極試料の溶解プロセス及び適当なデバイスは、国際公開第02/37132号に詳細に記載されている。融解プロセス及び融解のための適当なデバイスは、例えば国際公開第02/36005号に記載されている。
【0032】
分極すべき化合物において高い分極レベルを得るためには、前記化合物とDNP剤とはDNPプロセスの間、緊密に接触している必要がある。凍結又は冷却される際に試料が結晶化する場合にはそうではない。結晶化を避けるためには、試料中にガラス形成剤が存在している必要があるか、若しくは凍結される際に結晶化せず、むしろガラスを形成する化合物を分極に選択する必要がある。
【0033】
前に述べたように、13C−ピルビン酸又は13C−ピルビン酸塩は過分極13C−ピルビン酸塩を得るための適切な出発原料である。
【0034】
同位体濃縮された13C−ピルビン酸塩は例えば13C−ピルビン酸ナトリウムとして市販されている。或いは、これはS.Anker,J.Biol.Chem 176,1948,133―1335に記載されているように合成してもよい。
【0035】
13C1−ピルビン酸の合成のためのいくつかの方法が当技術分野で知られている。簡潔には、Seebach et al.,Journal of Organic Chemistry,40(2),1975、231―237に、S,S−アセタールとしてのカルボニル含有出発原料、例えば1,3−ジチアン又は2−メチル−1,3−ジチアンの保護及び活性化を利用する合成経路が記載されている。ジチアンは金属化され、メチル含有化合物及び/又は13CO2と反応する。この参考文献に概要が記されている適当な同位体濃縮13C−成分を用いることによって、13C1−ピルビン酸塩、13C2−ピルビン酸塩又は13C1,2−ピルビン酸塩を得ることが可能である。続いてカルボニル官能基が文献に記載された従来の方法を用いることによって遊離される。別の合成経路は酢酸から出発し、これは最初に臭化アセチルに変換され、次いでCu13CNと反応する。得られたニトリルはアミドを経由してピルビン酸に変換される(例えばS.H.Anker et al.,J.Biol.Chem.176(1948),1333又はJ.E.Thirkettle,Chem Commun.(1997),1025を参照されたい)。さらに、13C−ピルビン酸は、市販の13C−ピルビン酸ナトリウムを例えば米国特許第6232497号に記載された方法又は国際公開第2006/038811に記載された方法によってプロトン化することによって得てもよい。
【0036】
DNPによる13C−ピルビン酸の過分極は、参照により本明細書に組み込まれる国際公開第2006/011809号に詳しく記載されている。簡潔には、13C−ピルビン酸は凍結された際にガラスを形成するので、DNPに直接用い得る。DNPの後、凍結過分極13C−ピルビン酸は溶解して中和する、即ち13C−ピルビン酸塩に変換する必要がある。変換のためには強塩基が必要である。さらに、13C−ピルビン酸は強酸であるので、DNP剤はこの強酸の中で安定であるものを選ぶ必要がある。好ましい塩基は水酸化ナトリウムであり、水酸化ナトリウムによる過分極13C−ピルビン酸の変換によって過分極13C−ピルビン酸ナトリウムが得られる。これはインビボMR造影、分光法、及び/又は分光造影、即ち生きたヒト又はヒト以外の動物について実施されるMR造影、分光法、及び/又は分光造影のために用いられる造影媒体のための好ましい13C−ピルビン酸塩である。
【0037】
或いは、13C−ピルビン酸塩、即ち13C−ピルビン酸の塩をDNPに用いることができる。参照により本明細書に組み込まれる国際公開第2007/111515号に詳しく記載されているように、好ましい塩はNH4+、K+、Rb+、Cs+、Ca2+、Sr2+及びBa2+、好ましくはNH4+、K+、Rb+又はCs+、より好ましくはK+、Rb+、Cs+、最も好ましくはCs+からなる群からの無機カチオンを含む13C−ピルビン酸塩である。これらの好ましい13C−ピルビン酸塩の合成も、国際公開第2007/111515号に開示されている。過分極13C−ピルビン酸塩をインビボMR造影及び/又は分光法のための造影媒体において用いる場合には、NH4+、K+、Rb+、Cs+、Ca2+、Sr2+及びBa2+からなる群からの無機カチオンを、Na+又はメグルミン等の生理学的に極めてよく認容可能なカチオンに交換することが好ましい。これは、カチオン交換カラムの使用等の当技術で知られた方法によって行なってよい。
【0038】
参照により本明細書に組み込まれる国際公開第2007/069909号に詳しく記載されているように、さらに好ましい塩は有機アミン又はアミノ化合物の13C−ピルビン酸塩、好ましくはTRIS−13C1−ピルビン酸塩又はメグルミン−13C1−ピルビン酸塩である。これらの好ましい13C−ピルビン酸塩の合成も、国際公開第2007/069909号に記載されている。
【0039】
本発明の方法で用いる過分極13C−ピルビン酸塩がDNPによって得られる場合には、13C−ピルビン酸又は13C−ピルビン酸塩及びDNP剤を含む分極すべき試料は、常磁性金属イオンをさらに含んでもよい。参照により本明細書に組み込まれる国際公開第2007/064226号に詳しく記載されているように、DNPによって分極すべき組成物中の常磁性金属イオンの存在によって13C−ピルビン酸/13C−ピルビン酸塩における分極レベルが増大することが見出された。
【0040】
前に述べたように、本発明の方法による造影媒体は、インビボMR造影、分光法、及び/又は分光造影、即ち生きたヒト又はヒト以外の動物について実施されるMR造影、分光法及び/又は分光造影のための造影媒体として用いられ得る。そのような造影媒体は、好ましくは13C−ピルビン酸塩等のMR活性剤13C−物質に加えて水性担体、好ましくは水/生理食塩液、緩衝液又は緩衝液の混合物等の生理学的に認容可能で、薬学的に許容される水性担体を含む。造影媒体は従来の薬学的に許容される担体、添加剤及び配合助剤をさらに含んでもよい。したがって、造影媒体は例えば安定剤、浸透圧調整剤、可溶化剤等、例えばヒト医学又は獣医学における診断用組成物のための従来のもの等の配合助剤を含んでよい。
【0041】
さらに、本発明の方法による造影媒体は、インビトロMR造影、分光法、及び/又は分光造影のため、例えば細胞培養物又はエクスビボ組織において炎症又は感染を検出するための造影媒体として用い得る。そのような造影媒体は、好ましくは13C−ピルビン酸塩等のMR活性剤13C−物質に加えてインビトロ細胞又は組織アッセイに適合して用いられる溶媒、例えばDMSO若しくはメタノール又は水性担体及び非水性溶媒を含む溶媒混合物、例えばDMSOと水若しくは緩衝溶液又はメタノールと水若しくは緩衝溶液の混合物を含む。当業者には明らかなように、薬学的に許容される担体、添加剤及び配合助剤はそのような造影媒体中に存在してもよいが、そのような目的のために要求されてはいない。
【0042】
過分極13C−ピルビン酸塩を例えば細胞培養物又はエクスビボ組織を用いたMR造影又は分光法のインビトロ方法で感染の検出のための造影剤として用いる場合には、細胞培養物又はエクスビボ組織に添加する過分極13C−ピルビン酸塩を含む造影媒体は13C−ピルビン酸塩が10mM〜100mM、より好ましくは20mM〜90mM、最も好ましくは13C−ピルビン酸塩が40〜80mMである。
【0043】
さらに、本発明の方法によって検出される炎症及び感染疾患の種類は様々であり得る。本方法は免疫系が活性化されているか変化している疾患の範囲を検出するために用い得る。これらの疾患は皮膚及び骨格系、消化系、筋肉系、リンパ系、内分泌系、神経系、心臓血管系、男性又は女性生殖系、及び泌尿器系等のいかなる体組織にも影響し得る。本方法は身体のいかなる部分に対する自己免疫疾患をも検出し得る。自己免疫成分を含む臨床疾患の非包括的なリストとしては、関節リウマチ、若年性特発性関節炎、全身性紅斑性狼瘡、強皮症、皮膚筋炎、心筋症、クローン病及び多発性硬化症が挙げられる。この方法は外傷後の治癒に対する炎症反応を検出するために用い得る。この方法はアテローム性動脈硬化症、変形性関節症、腱炎、滑液包炎、痛風性関節炎、COPD、喘息、及び慢性気管支炎等の炎症成分を有する慢性疾患を検出するために用い得る。この方法は皮膚、四肢、筋肉、結合組織、骨、関節、神経系、並びに頭部、頚部、胸部、及び腹部の内部器官を含む身体のいかなる部分の感染(例えば細菌、ウイルス、真菌、寄生虫、又は他の感染源)に対する反応における炎症をも検出し得る。炎症は移植において大きな役割を果たす。本方法は、固形臓器の急性及び慢性移植拒絶、移植後リンパ増殖性疾患及びグラフト対宿主疾患等の、移植の設定における免疫系の変化を検出し得る。
【0044】
本発明の方法は上述のこれらの種類の条件全ての検出を含む。好ましい実施形態は関節炎、より好ましくは関節リウマチを検出するための13C−MR造影、13C−MR分光法、及び/又は13C−MR分光造影の方法であり、過分極13C−物質、好ましくは過分極13C−ピルビン酸塩を含む造影媒体が用いられる。
【0045】
別の実施形態では、造影媒体は乳酸塩をさらに含む。したがって、本発明の方法による造影媒体は過分極13C−ピルビン酸塩に加えて非過分極乳酸塩(以下、乳酸塩という)を含む。適切には、乳酸塩は乳酸又は乳酸の塩、好ましくは乳酸リチウム又は乳酸ナトリウム、最も好ましくは乳酸ナトリウムの形で添加される。乳酸塩及び過分極13C−ピルビン酸塩を含む造影媒体及びそれらを用いるための方法は、参照により本明細書に組み込まれるWO2008/020765にさらに記載されている。
【0046】
炎症及び感染は、本発明の方法により、13C−ピルビン酸塩の信号及びその代謝産物である13C−乳酸塩の信号を経時的に追跡することによって検出することができる。生存できる、例えば非炎症性の細胞において、13C−ピルビン酸塩の信号は経時的に減衰する。13C−乳酸塩の信号は13C−ピルビン酸塩の13C−乳酸塩への代謝変換によって最初増加し、次いで主として緩和のためにゆっくりと減少する。炎症領域においてはピルビン酸塩の代謝は上方調節されており、13C−ピルビン酸塩の13C−乳酸塩への変換は増加する。過分極13C−ピルビン酸塩を含む造影媒体を用いて、13C−MR検出によって検出することができる13C−乳酸塩の産生の増加によってこの亢進した代謝活性を見ることができる。
【0047】
乳酸塩(本発明による造影媒体中に存在していようと、又は個別に添加/投与されようと)の添加によって、観察し得る13C−乳酸塩の量の増加及びそれによる13C−乳酸塩からのMR信号の増大がもたらされることがさらに見出された。
【0048】
用語「13C−MR検出」は、13C−MR造影若しくは13C−MR分光法又は13C−MR造影と13C−MR分光法の組み合わせ、即ち13C−MR分光造影を意味する。この用語はさらに、種々の時点における13C−MR分光造影を意味する。
【0049】
周波数と空間的に選択的な方法を組み合わせて関心体積をエンコードするMR造影シーケンスが適用され、13C−ピルビン酸塩の13C−MR信号が造影剤の添加(t=0)から約1分間又はT1緩和を経由する信号の減衰によって13C−MR信号が検出不能になるまでの時間にわたってMR造影又は分光造影によって追跡される。同じ時間の間、13C−乳酸塩の信号の出現、増加及び/又は減少が監視される。定量的評価を得るため、健常な細胞又は組織のMR造影、分光法、又は分光造影を行なってもよく、その結果(即ち所与の時間の間に形成された13C−乳酸塩の量又は速度)を比較することができる。
【0050】
過分極13C−ピルビン酸塩を例えば生きたヒト又はヒト以外の動物の身体におけるMR造影、分光法又は分光造影のインビボ法において炎症又は感染の検出のための造影剤として用いる場合には、過分極13C−ピルビン酸塩を含む造影媒体は、好ましくは前記生体に非経口的に、好ましくは静脈内に投与される。一般的には、検査される生体はMR磁石の中に置かれる。専用の13C−MR RFコイルが関心領域をカバーするように置かれる。造影媒体の用量及び濃度は、毒性及び投与経路等の要素の範囲に依存することになる。一般的には、造影媒体は体重kgあたり1mmol13C−ピルビン酸塩まで、好ましくは0.01〜0.5mmol/kg、より好ましくは0.1〜0.3mmol/kgの濃度で投与される。投与速度は好ましくは10ml/s未満、より好ましくは6ml/s未満、最も好ましくは5ml/s〜0.1ml/sである。投与後400s未満、好ましくは120s未満、より好ましくは投与後60s未満、特に好ましくは20〜50sで、周波数と空間的に選択的な方法を組み合わせて関心体積をエンコードするMR造影シーケンスが適用される。これにより13C−ピルビン酸塩、13C−乳酸塩及び/又は他の13C−標識代謝生成物の代謝画像がもたらされることになる。MRシーケンスを適用する正確な時間は、感染又は炎症を検出する関心体積に高度に依存する。
【0051】
関心体積のエンコーディングは、これだけに限らないが、例えばT.R.Brown et al.,Proc Natl Acad Sci USA 79、3523−3526(1982);A.A.Maudsley et al.,J Magn Res 51,147−152(1983);D.Mayer et al.,Magn Reson Med 56,932−937(2006);S.J.Kohler et al.,Magn Reson Med 58(1),65−9(2007);Y−F.Yen et al.,Magn Reson Med(Epub ahead of print)Mar 24(2009)に記載されているもの等のいわゆる分光造影シーケンスを用いることによって達成することができる。分光画像データには、その中の各要素が完全な13C−MRスペクトルを含むいくつかの体積要素が含まれる。13C−ピルビン酸塩及びその代謝物である13C−乳酸塩は13C−MRスペクトルにおいて独特の位置を有しており、それらの共鳴周波数はそれらを同定するために用いることができる。その共鳴周波数におけるスペクトルピークの積分は、それぞれ13C−ピルビン酸塩及び13C−乳酸塩の量に直接関連する。13C−ピルビン酸塩及び13C−乳酸塩の量が例えばL.Vanhamme et al.,J Magn Reson 129,35−43(1997)に記載されているようなスペクトルピーク積分解析若しくは時間領域近似ルーチン又は例えばS.B.Reeder et al.,J Magn Reson Imaging 26,1145−1152(2007)及びY.S.Levin et al.,Magn Reson Med 58(2),245−52(2007)に記載されているような最小二乗化学シフト分離法を用いて推定される場合には、13C−ピルビン酸塩及び13C−乳酸塩の画像を生成し、その中のカラーコーディング又はグレイコーディングによって13C−ピルビン酸塩及び13C−乳酸塩の測定された量を表わすことができる。
【0052】
分光造影法は全種類のMR核、例えば1H、31P、23Naを用いる代謝画像を生成することにおいてその価値を証明してきたが、分光画像を完全にエンコードするために必要な繰り返しの量が多いので、このアプローチは過分極13Cにはあまり適しないものになっている。全体のMRデータ取得の間、過分極13C−信号が利用可能であることを確実にするよう、注意を払わなくてはならない。これは、例えばL.Zhao et al.,J Magn Reson,B(113),179−183(1996)に記載されているようにRF−パルス励起フリップ角を低減するか、若しくは変動フリップ角を適用することによって、又は例えばP.E.Z.Larson et al.,J Magn Reson 194:121−127(2008)に記載されているように全フェーズエンコーディングステップにおいて適用されるマルチバンドRF励起デザインによって、達成することができる。マトリックスサイズが大きくなると、フェーズエンコーディングステップを多くし、走査時間を長くする必要がある。
【0053】
P.C.Lauterbur(Nature,242,190−191,(1973)及びP.Mansfield(J.Phys.C.6,L422−L426(1973))の先駆的な研究に基づく造影方法はデータ取得の間、読み出し勾配を適用するものであるが、これにより高い信号雑音比の画像、又はこれと等価の高い空間分解能の画像が可能になるであろう。しかし、その基本形におけるこれらの造影方法は13C−ピルビン酸塩と13C−乳酸塩についての個別の画像を生成することはできず、即ち特定の代謝産物の同定は可能でない。
【0054】
別の実施形態では、周波数情報をコードするためにマルチエコーを用いることになる造影シーケンスが用いられる。水と脂肪の1H−画像を個別に生成することができるシーケンスは、例えばG.Glover,J Magn Reson Imaging1,521−530(1991)及びS.B.Reeder et al.,Magn Reson Med 51,35−45(2004)に記載されている。検出すべき代謝産物、したがってそのMR周波数は知られているので、上の参考文献で議論されたアプローチは13C−ピルビン酸塩及び13C−乳酸塩の直接の画像を取得するために適用することができる。この手順により過分極13C−MR信号の使用がより効率的になり、分光造影に比べてより良い信号品質、より高い空間分解能及びより早い取得時間が得られる。
【0055】
好ましい実施形態では、本発明による方法には、過分極13C−ピルビン酸塩を含む造影媒体を予め投与したヒト又はヒト以外の動物の身体から、又は造影媒体を添加した細胞培養物又はエクスビボ組織から、直接の13C−MR画像又は13C−ピルビン酸塩及び13C−乳酸塩のスペクトルを取得するステップが含まれる。開示した方法では、感染又は炎症は13C−乳酸塩からの高い13C−信号強度又は13C−乳酸塩の生成速度の増大によって同定及び検出される。本発明による過分極13C−ピルビン酸塩造影は、炎症及び感染において乳酸への代謝が増大していることを示す。
【0056】
ピルビン酸塩の信号を補正するために、乳酸塩及びピルビン酸塩の画像を各個別の画像における最大値に正規化してもよい。次に、正規化された乳酸塩の画像にピルビン酸塩の画像の逆数、例えば画像中の最大のピルビン酸塩の信号からピクセル毎のピルビン酸塩レベルを差し引いたものを乗じる。最後のステップとして、上の操作で得られた中間結果に元の乳酸塩の画像を乗じる。或いは、それぞれの画像の各ピクセル中のピルビン酸塩及び乳酸塩のピーク強度をピルビン酸塩と乳酸塩との間の13C−ラベルのフラックスの動態モデルに合致させて、ラベルフラックス及びスピン格子緩和時間の速度定数を得ることができる。分極の喪失に対するマルチプルRFパルスの影響について補正を行なう必要があろう。
【0057】
本方法をインビボの炎症又は感染の検出のために用いる場合には、本発明の方法による炎症又は感染の検出において解剖学的及び/又は潅流情報が含まれてもよい。解剖学的情報は、例えば適当な造影剤を用いて、又は用いずにプロトンMR画像を取得することによって得られる。相対的な潅流は例えばOmniscan(商標)のようなMR造影剤を用いることによって決定することができる。同様に、造影剤を投与しない潅流測定のためのMR造影手法は当技術分野で知られている。好ましい実施形態では、定量的潅流を決定するために非代謝過分極13C−造影剤を用いる。適切な手法及び造影剤は例えば国際公開第02/23209号に記載されている。より好ましい実施形態では、定量的潅流を決定するために過分極13C−ピルビン酸塩が用いられる。
【0058】
別の好ましい実施形態では、過分極13C−ピルビン酸塩を含む造影媒体は繰り返し投与され、それにより長期的研究が可能になる。ピルビン酸塩の毒性が低いこととその好ましい安全性プロファイルにより、この化合物の繰り返し用量は患者によく認容される。
【0059】
本発明の方法で得られる結果は、例えば医師が検討中の患者に対する適切な処置を選択することを可能にする。さらなる好ましい実施形態では、本発明の方法は処置が成功したかどうかを決定するために用いられる。
【0060】
さらなる態様から見れば、本発明は炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−物質の使用を提供する。より好ましくは、本発明は炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−ピルビン酸塩の使用を提供する。好ましくは、造影媒体の製造のために用いられる過分極13C−ピルビン酸塩は、13C−ピルビン酸又は13C−ピルビン酸塩の動的核分極によって得られる。任意選択で、造影媒体の製造のために乳酸塩を13C−物質に添加してもよい。
【0061】
13C−ピルビン酸又は13C−ピルビン酸塩からの過分極13C−ピルビン酸塩の製造及び製造の好ましい実施形態、並びに過分極13C及び任意選択で乳酸塩を含む造影媒体の製造については、本出願の6〜10頁に詳しく記載されている。
【0062】
好ましい実施形態では、本発明は造影媒体を予め投与したヒト又はヒト以外の動物の身体から、又は造影媒体を添加した細胞培養物又はエクスビボ組織から、直接の13C−画像及び/又は13C−ピルビン酸塩及び13C−乳酸塩の13C−スペクトルを取得することによって炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−ピルビン酸塩及び任意選択による乳酸塩の使用を提供する。
【0063】
別の好ましい実施形態では、本発明はヒト又はヒト以外の動物の身体において炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における過分極13C−物質を含む造影媒体の使用を提供する。造影媒体は好ましくは、ヒト又はヒト以外の動物の身体に予め投与されている。
【図面の簡単な説明】
【0064】
【図1】関節炎の関節の代謝マップを示す図である。過分極[1−13C]ピルビン酸塩を注射した20秒後に、マップは関節炎の足において乳酸塩の産生が亢進していることを示している。A:T2重み付け解剖学的画像は、関節炎の右後足(矢印)において正常な左足に比べて組織が腫脹していることを示しており、次の代謝マップ上では尾(T)及び非分極13C−乳酸塩(L)の参照チューブに重ねられている。マップはB:[1−13C]ピルビン酸塩、C:[1−13C]乳酸塩、及びD:[1−13C]乳酸塩/[1−13C]ピルビン酸塩の比を示している。
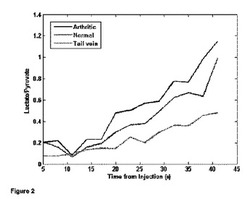
【図2】1匹のラットの関節炎の足(青)における[1−13C]乳酸塩の産生の亢進を正常な足(右)及び尾(緑)と比較した時間分解造影を示す図である。
【実施例】
【0065】
実施例1:関節炎の検出
6匹の幼若Sprague Dawleyラット(4〜5週齢、平均体重114g)に0.4μL/gの完全フロイントアジュバントを注射(ラット3匹には右膝、ラット3匹には右足首)することによって関節炎を誘導した。誘導の7日後に、励起及び信号受容の両方のために自己遮蔽グラジエント(40mT/m、150mT/m/ms)及び特注のデュアルチューン(1H/13C)直角位相コイル(φ=80mm)を備えたGE 3T スキャナーにより、13C MRSによって関節炎の関節を造影した。13C−1−ピルビン酸塩の100mM溶液0.5mLをDNP(15〜20%液体状態分極)によって過分極し、尾静脈から注射した。注射の20秒後に、FID CSIシーケンス(ボクセル=2.5×2.5×10mm、FOV=4×4cm)によって13C−1ピルビン酸塩及びその代謝産物の単一時点MRS解析を得た。2回目の過分極13C−ピルビン酸塩の注射の間、1D EPSIシーケンスによって時間分解造影を得た。関節におけるROI解析によってピルビン酸塩及び乳酸塩の平均信号強度を得て、正常及び関節炎の関節をT検定によって比較した。
【0066】
関節炎の関節は紅斑があり、腫脹していて(平均±SD=0.5±0.2mm厚みが大きい)、組織学的スコアは炎症について3/4(正常関節の0/4と比較)を有し、解剖学的MR画像において炎症のT2重み付け変化を示した。[1−13C]ピルビン酸塩及び代謝された[1−13C]乳酸塩は、FID CSI画像(図1A、B)上で、関節炎の関節において増加しているように思われ、関節における代謝産物の全13Cに対する比のROI解析によって有意差を有する傾向があった[関節炎のピルビン酸塩=0.34対正常=0.28、p<0.17;関節炎の乳酸塩=0.21対正常=0.16、p<0.12]。炎症組織における血流の増大が造影剤の送達の増大の原因かも知れないが、時間分解造影(図2)によって、また乳酸塩の全13Cに対する比(関節炎=0.62対正常=0.56、p<0.03)によって示されるように、乳酸塩への変換速度も関節炎の関節において増大していた。
【0067】
したがって、これらの結果によれば、過分極[1−13C]ピルビン酸塩造影は、関節炎に罹患した関節における乳酸塩への代謝の亢進を示す。乳酸塩産生の亢進は、関節炎の活動度のマーカーとして役立つであろう。
【符号の説明】
【0068】
A T2重み付け解剖学的画像
B [1−13C]ピルビン酸塩
C [1−13C]乳酸塩
D [1−13C]乳酸塩/[1−13C]ピルビン酸塩の比
L 非分極13C−乳酸塩
T 尾
【技術分野】
【0001】
本発明は、過分極13C−物質を含む造影媒体を用いた炎症又は感染の炭素−13(13C)磁気共鳴(MR)造影又は分光の方法に関する。本発明は、炎症又は感染を検出又は監視するための、MR造影によって次に造影するための過分極された炭素−13標識分子の応用に関する。
【背景技術】
【0002】
炎症は体組織に損傷を与える有害な因子に対する生物学的反応である。炎症は宿主の防御と組織傷害の間のバランスを取る作用である。炎症反応の鍵となるのは免疫系と血管組織である。免疫系は白血球と、生体が感染と戦うこと、有害な刺激を除去すること、及び損傷組織を修復することを助ける分子とからなっている。炎症過程の間、免疫系及び増大した血流は病原体を排除し、傷害を受けた組織を修復することを助ける。
【0003】
炎症には、感染又は傷害を受けた部位に栄養分及び免疫系の追加的な成分を搬入するために新たな血管を動員することが含まれる。炎症はしばしば外因性病原体(例えば細菌、ウイルス、真菌、寄生虫、プリオン及びウイロイド)の結果であるが、炎症反応の他の起因因子としては自己抗原、外傷、アレルゲン、及び刺激物がある。炎症がなければ創傷及び感染は治癒せず、組織の進行性破壊は生命体の死につながるであろう。炎症はしばしば、潜在的な疾患が存在し、生体がその疾患を排除しようとしていることを知らせている。感染は外来種による宿主生命体への定着であり、これはしばしば臨床的に明白な疾患をもたらす。外来種は通常、細菌のコロニー、真菌、ウイルス、寄生虫、プリオン、又はウイロイド等の顕微鏡的病原体である。炎症は感染を排除するために宿主生命体によって搭載されている機構である。炎症はまた自己抗原、損傷組織(例えば外傷)、アレルゲン、又は刺激物を排除するために起こることもある。
【0004】
しかし、炎症は調節を誤った場合又は制御なく放置された場合には、宿主に問題を生じることもあり、その中には自己免疫疾患、アレルギー、アテローム性動脈硬化症、炎症性及び退行性関節炎、喘息、慢性気管支炎、慢性閉塞性肺疾患(COPD)、及び多発性硬化症が含まれる。炎症が正常には生体によって厳しく規制されているのはこのためである。炎症は急性又は慢性のいずれかに分類することができる。急性炎症は有害な刺激に対する生体の最初の反応であり、血液から傷害組織への血漿及び白血球の移動の増大によって達成される。生化学的事象のカスケードが伝播し、局所血管系、免疫系、及び傷害組織内の種々の細胞が関与する炎症反応を成熟させる。慢性炎症として知られている長期的な炎症は、炎症の部位に存在する細胞の型を進行的に変化させ、炎症プロセスからの組織の崩壊及び治癒が同時に起こることによって特徴付けられる。
【0005】
炎症疾患及び感染疾患は分子レベル及び細胞レベルでの同様の機構を共有している。これらの疾患は免疫系の活性化をもたらし、臨床的に検出及び監視するのが困難なことが多い疾患プロセスである。現在のところ、炎症及び感染の造影による検出のための選択は限られており、治療に対するこれらの疾患の反応を検出し、監視するための良好な臨床的試験は存在しない。臨床医は、患者がどのように感じているかという主観的な方法、血液検査(白血球数、CRP等)等の二次的兆候、非特異的核医学造影、又は解剖学的造影(従来のMRI、超音波、コンピュータ断層撮影、及びX線写真)に基づく疾患の晩期解剖学的変化に頼らざるを得ない。例として、関節リウマチは老年人口の約1%が罹患するありふれた疾患であり、現在関節リウマチを検出し、又は監視するための良好な非侵襲的検査は存在しない。臨床医にはしばしば、疾患を診断するため及び患者がどのように治療に反応しているかを決定するために、主観的な方法しか残されていない。したがって、ヒト又はヒト以外の動物の身体においてインビボで非侵襲的に炎症及び感染を検出することには興味がある。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】国際公開第2009/133169号
【発明の概要】
【発明が解決しようとする課題】
【0007】
MR造影(MRI)、MR分光法(MRS)及びMR分光造影(MRSI)等のMR検出は炎症及び感染を検出するための価値あるツールとなる可能性があり、これらのツールは非侵襲的に、また患者及び医療関係者をX線等の有害な可能性がある放射線に曝すことなく患者の体及びその部分の画像を得ることを可能にするので、医師たちにとって特に魅力的なものになってきた。優れた軟組織コントラスト及び良好な空間的及び時間的解像度を備えたその高品質な画像のため、MRIは軟組織及び臓器の好ましい造影手法である。
【課題を解決するための手段】
【0008】
ところで、過分極13C−物質が13C−MRI、13C−MRS、又は13C−MRSIを用いたヒト又はヒト以外の動物の身体における炎症及び感染を検出するための薬剤として用い得るということが見出された。
【0009】
したがって、第1の態様において、本発明は過分極13−C物質を含む造影媒体を用いて炎症又は感染を検出するための13C−MR造影及び/又は13C−MR分光法及び/又は13C−MR分光造影の方法を提供する。そのような物質は、10秒より長く、好ましくは30秒より長く、さらにより好ましくは60秒より長い縦緩和時間定数(T1)を有する核を含むはずである。そのような、いわゆる「高T1薬剤」は、例えば国際公開第99/35508号に記載されている。或いは、候補物質のT1値は文献で見出されるか、候補物質のNMRスペクトル、例えば13C−標識された候補物質のT1を決定するための13C−NMRスペクトルを取得することによって決定し得る。
【発明を実施するための形態】
【0010】
好ましい過分極13C−物質はヒト及びヒト以外の動物の身体における代謝プロセスにおいて役割を果たす生体分子である。したがって、特に好ましい物質は内因性化合物、より好ましくはヒト又はヒト以外の動物の身体における代謝プロセスにおいて役割を果たす内因性化合物である。特に好ましい物質はアミノ酸(プロトン化又は脱プロトン化形における)、好ましくはアラニン、グリシン、グルタミン、グルタミン酸、システイン、アスパラギン及びアスパラギン酸、酢酸塩、ピルビン酸、ピルビン酸塩、シュウ酸塩、リンゴ酸塩、フマル酸塩、乳酸塩、乳酸、クエン酸塩、重炭酸塩、マロン酸塩、コハク酸塩、オキサロ酢酸塩、α−ケトグルタル酸塩、3−ヒドロキシ酪酸塩、イソクエン酸塩及び尿素から選択される。
【0011】
ピルビン酸塩は比較的高い濃度においてさえも極めて良好に人体に認容される内因性化合物である。クエン酸サイクルにおける前駆体として、ピルビン酸塩は人体内で重要な代謝的役割を果たす。ピルビン酸は種々の化合物に変換される。そのトランスアミノ化は酸化的脱カルボキシル化を経てアラニンを生じ、ピルビン酸塩はアセチル−CoA及び二酸化炭素(これはさらに重炭酸塩に変換される)に変換され、ピルビン酸塩の還元は乳酸塩及びそのオキサロ酢酸塩におけるカルボキシル化をもたらす。
【0012】
さらに、過分極13C−ピルビン酸塩の、その代謝産物である過分極13C−乳酸塩、過分極13C−重炭酸塩(13C1−ピルビン酸塩、13C1,2−ピルビン酸塩又は13C1,2,3−ピルビン酸塩の場合のみ)及び過分極13C−アラニンへの代謝的変換は、MRを用いて人体内の代謝プロセスを研究するために用いることができる。13C1−ピルビン酸塩はヒト全血中、37℃で約42sのT1緩和を有するが、過分極13C−ピルビン酸塩の過分極13C−乳酸塩、過分極13C−重炭酸塩及び過分極13C−アラニンへの変換は充分に速く、13C−ピルビン酸塩ペアレント化合物及びその代謝産物からの信号の検出は可能であることが見出された。アラニン、重炭酸塩及び乳酸塩の量は検査する組織の代謝状態に依存する。過分極13C−乳酸塩、過分極13C−重炭酸塩及び過分極13C−アラニンのMR信号強度はこれらの化合物の量及び検出の時に残っていた分極の程度に関連し、したがって過分極13C−ピルビン酸塩の過分極13C−乳酸塩、過分極13C−重炭酸塩及び過分極13C−アラニンへの変換を監視することによって、非侵襲的MRI、MRS、又はMRSIを用いたインビボでのヒト又はヒト以外の動物の身体における代謝プロセスの研究が可能である。
【0013】
種々のピルビン酸塩代謝産物から生じるMR信号の振幅は組織型によって変動することが見出された。アラニン、乳酸塩、重炭酸塩及びピルビン酸塩によって生じる独特の代謝ピークパターンは、検査する組織の代謝状態を表わす指紋として用いることができ、それにより健常組織と非健常組織との間の区別が可能になる。腫瘍造影のための過分極13C−ピルビン酸塩の使用(腫瘍組織が高い代謝活性を示す)は国際公開第2006/011810号に詳しく記載されている。さらに、心臓造影のための過分極13C−ピルビン酸塩の使用は国際公開第2006/054903号に記載されている。
【0014】
このように、好ましい実施形態では本発明は過分極13C−ピルビン酸塩を含む造影媒体を用いて炎症又は感染を検出するための13C−MR造影及び/又は13C−MR分光法及び/又は13C−MR分光造影の方法を提供する。
【0015】
本発明は、どのようにして炎症又は感染の部位を検出するかという課題を解決する。これは、診断及び検出することが困難な潜在的感染に特に重要である。本発明の方法によって疾患領域の解剖学的位置が同定される。さらに、本発明の方法によって炎症又は感染の部位を定量化することができ、疾患活性の代謝プロセスに関する情報を提供することができる。したがって、本方法は解剖学的造影に加えて代謝プロセスを特徴付けることができるという利益を含んでいる。分子プロセスの変化を検出することは、疾患を解剖学的に記述することよりも感度及び特異性が高い可能性がある。本発明の方法で用いる過分極炭素−13MRSIは、分子プロセスに対する感度を劇的に増大させる。本発明の主観的且つ定量的な造影方法によって疾患をより早く検出できる可能性があり、より良く治療に合わせられる可能性がある。これは薬剤の選択が困難で疾患の進行が監視困難な、喘息、慢性気管支炎、COPD、及び多発性硬化症等の炎症要素を有する疾患の治療において特に重要であり得る。さらに、本発明によって薬剤の開発を加速することを助けられる可能性もある。というのは、本発明の非侵襲的な方法が疾患活動性を測定するために利用可能である場合には、より少ない対象者数及びより短い時間しか必要としないからである。
【0016】
当技術の応用として、本発明者らは13C−ピルビン酸塩が炎症を検出するために用い得ることを示した。しかし、過分極し得る同位元素を用いて作成されるいかなる物質も、潜在的には炎症又は感染を検出又は監視するための候補となり得る。過分極MRI手法を用いて炎症又は感染を検出するための候補である他の物質としては、酸素、窒素、キセノン、ヘリウム、及びフッ素の同位元素を含む物質が挙げられる。
【0017】
用語「13C−ピルビン酸塩」は13C−ピルビン酸の塩を意味する。以下において用語ピルビン酸塩、13C−ピルビン酸塩及び13C1−ピルビン酸塩は互換的に用いられ、全て13C1−ピルビン酸塩を意味する。同様に用語ピルビン酸、13C−ピルビン酸及び13C1−ピルビン酸は互換的に用いられ、全て13C1−ピルビン酸を意味する。さらに、用語乳酸塩、13C−乳酸塩及び13C1−乳酸塩は互換的に用いられ、さらに特定しない限り、全て13C1−乳酸塩を意味する。
【0018】
用語「過分極」及び「分極」はこれ以降、互換的に用いられ、0.1%を超え、より好ましくは1%を超え、最も好ましくは10%を超える核分極レベルを意味する。
【0019】
分極レベルは例えば固体過分極13C−ピルビン酸塩、例えば13C−ピルビン酸塩の動的核分極(DNP)によって得られる固体過分極13C−ピルビン酸塩における固体状態13C−NMRの測定によって決定し得る。固体状態13C−NMR測定は、好ましくは低いフリップ角を用いた単純パルス獲得NMRシーケンスからなる。NMRスペクトルにおける過分極13C−ピルビン酸塩の信号強度を分極プロセスの前に取得したNMRスペクトルにおける13C−ピルビン酸塩の信号強度と比較する。次いで分極前後の信号強度の比から分極レベルを計算する。
【0020】
同様にして、溶解した過分極13C−ピルビン酸塩の分極レベルを液体状態NMR測定によって決定することができる。ここでも溶解した過分極13C−ピルビン酸塩の信号強度を分極前の溶解した13C−ピルビン酸塩の信号強度を比較する。次いで分極前後の13C−ピルビン酸塩の信号強度の比から分極レベルを計算する。
【0021】
用語「造影媒体」は、MR活性剤としての過分極13C−ピルビン酸塩等の過分極13C−物質を含むが、これに限らない液体組成物を意味する。本発明による造影媒体は、MR造影における造影媒体として、又はMR分光法及びMR分光造影におけるMR分光剤として用い得る。
【0022】
本発明の方法による造影媒体は、インビボMR造影、分光法及び/又は分光造影、即ち生きたヒト又はヒト以外の動物について実施されるMR造影、分光法及び/又は分光造影のための造影媒体として用い得る。さらに、本発明の方法による造影媒体は、インビトロMR造影、分光法及び/又は分光造影のため、例えば細胞培養物又はエクスビボ組織において炎症又は感染を検出及び監視するための造影媒体として用い得る。細胞培養物は、例えば血液、尿又は唾液等のヒト又はヒト以外の動物の身体から得られる試料から得た細胞から誘導し得る。一方エクスビボ組織は生検又は手術から得られる。
【0023】
本発明の方法で用いる過分極13C−ピルビン酸塩の同位体濃縮は、好ましくは75%以上、より好ましくは80%以上、特に好ましくは90%以上であり、90%を超える同位体濃縮が最も好ましい。理想的には、濃縮は100%である。本発明の方法で用いる13C−ピルビン酸塩は、C1位(13C1−ピルビン酸塩)、C2位(13C2−ピルビン酸塩)、C3位(13C3−ピルビン酸塩)、C1位及びC2位(13C1,2−ピルビン酸塩う)、C1位及びC3位(13C1,3−ピルビン酸塩)、C2位及びC3位(13C2,3−ピルビン酸塩)、又はC1位、C2位及びC3位(13C1,2,3−ピルビン酸塩)で同位体濃縮し得る。C1位での同位体濃縮が好ましい。13C1−ピルビン酸塩は、ヒト全血中、37℃で、他のC位で同位体濃縮された13C−ピルビン酸塩よりも高いT1緩和(約42s)を有するからである。
【0024】
NMR活性13C−核の過分極は、例えば参照により本明細書に組み込まれる国際公開第98/30918号、同第99/24080号及び同第99/35508号に記載された種々の方法によって実施することができ、過分極の方法は貴ガスからの分極転移、「ブルートフォース」、スピン凍結、パラ水素法及び動的核分極(DNP)である。
【0025】
過分極13C−ピルビン酸塩を得るには、13C−ピルビン酸塩を直接分極するか、13C−ピルビン酸を分極し、分極した13C−ピルビン酸を例えば塩基で中和して分極13C−ピルビン酸塩に変換することのいずれかが好ましい。
【0026】
過分極13C−ピルビン酸塩を得るための1つの適当な方法は過分極貴ガスからの分極転移であり、これは国際公開第98/30918号に記載されている。ノンゼロ核スピンを有する貴ガスは、円偏光を用いることによって過分極することができる。過分極貴ガス、好ましくはHe又はXe、又はそのようなガスの混合物は、13C−核の過分極に効果を与えるために用い得る。過分極ガスは気相でもよく、液体/溶媒に溶解してもよく、又は過分極ガスそれ自体が溶媒として働いてもよい。或いは、冷却された固体表面上にガスを凝縮させてこの形態で用いてもよく、昇華させてもよい。
【0027】
過分極ガスを13C−ピルビン酸塩又は13C−ピルビン酸と緊密に混合することが好ましい。したがって、室温で液体である13C−ピルビン酸を分極させる場合には、過分極ガスは好ましくは液体/溶媒に溶解するか、溶媒として働く。13Cピルビン酸塩を分極させる場合には、過分極ガスは好ましくは液体/溶媒に溶解し、これはまたピルビン酸塩を溶解させる。
【0028】
過分極13C−ピルビン酸塩を得るための別の適当な方法は、極低温及び高磁場における熱力学的平衡によって分極を13C−核に与えることである。NMR分光計の操作磁場及び温度に比べて、非常に高い磁場及び非常に低い温度を用いることによって、過分極がもたらされる(ブルートフォース)。用いる磁場強度はできるだけ高く、適切には1Tより高く、好ましくは5Tより高く、より好ましくは15T以上、特に好ましくは20T以上とする。温度は極めて低く、例えば4.2K以下、好ましくは1.5K以下、より好ましくは1.0K以下、特に好ましくは100mK以下とする。
【0029】
過分極13C−ピルビン酸塩を得るための別の適当な方法は、スピン凍結法である。この方法はスピン凍結分極による固体化合物又は系のスピン分極に及ぶ。系は次数3以上の対称軸を有するNi2+、ランタニド又はアクチニドイオン等の適当な結晶性常磁性材料でドープするか、これらと緊密に混合する。共鳴励起磁場は適用されないので、均一な磁場の必要はなく、装置はDNPに必要なものよりも単純である。プロセスは、磁場の方向に垂直な軸の周りに試料を物理的に回転させることによって行なわれる。この方法の前提条件は、常磁性種が高度に異方性のg−ファクターを有することである。試料回転の結果として、電子常磁性共鳴が核スピンと接触させられ、核スピン温度の低下をもたらす。試料回転は、核スピン分極が新たな平衡に達するまで行なわれる。
【0030】
好ましい実施形態では、過分極13C−ピルビン酸塩を得るために動的核分極(DNP)が用いられる。DNPにおいては、分極すべき化合物中のMR活性核の分極は、分極剤又はいわゆるDNP剤、不対電子を含む化合物によって影響される。DNPプロセスの間、通常はマイクロ波照射の形のエネルギーが供給され、最初はこれがDNP剤を励起することになる。基底状態への減衰の際に、DNP剤の不対電子から分極すべき化合物のNMR活性核への、例えば13C−ピルビン酸塩の13C核への分極の転移がある。一般にDNPプロセスにおいては、例えばDNPプロセスを液体ヘリウム中、約1T以上の磁場で実施することによって、中程度の又は高い磁場と極めて低い温度が用いられる。或いは、中程度の磁場と充分な分極促進が達成される任意の温度を利用してもよい。DNP手法は例えば国際公開第98/58272号及び同第01/96895号にさらに記載されており、それらの開示内容は援用によって本明細書の内容の一部をなす。
【0031】
化合物をDNP法によって分極するためには、分極すべき化合物とDNP剤との混合物を調製し(「試料」)、これを次に凍結して分極のためのDNPポーラライザーに挿入する。分極の後、凍結された固体過分極試料を、それを融解するか若しくはそれを適当な溶解媒体に溶解することによって迅速に液体状態に移す。溶解が好ましく、そのための凍結過分極試料の溶解プロセス及び適当なデバイスは、国際公開第02/37132号に詳細に記載されている。融解プロセス及び融解のための適当なデバイスは、例えば国際公開第02/36005号に記載されている。
【0032】
分極すべき化合物において高い分極レベルを得るためには、前記化合物とDNP剤とはDNPプロセスの間、緊密に接触している必要がある。凍結又は冷却される際に試料が結晶化する場合にはそうではない。結晶化を避けるためには、試料中にガラス形成剤が存在している必要があるか、若しくは凍結される際に結晶化せず、むしろガラスを形成する化合物を分極に選択する必要がある。
【0033】
前に述べたように、13C−ピルビン酸又は13C−ピルビン酸塩は過分極13C−ピルビン酸塩を得るための適切な出発原料である。
【0034】
同位体濃縮された13C−ピルビン酸塩は例えば13C−ピルビン酸ナトリウムとして市販されている。或いは、これはS.Anker,J.Biol.Chem 176,1948,133―1335に記載されているように合成してもよい。
【0035】
13C1−ピルビン酸の合成のためのいくつかの方法が当技術分野で知られている。簡潔には、Seebach et al.,Journal of Organic Chemistry,40(2),1975、231―237に、S,S−アセタールとしてのカルボニル含有出発原料、例えば1,3−ジチアン又は2−メチル−1,3−ジチアンの保護及び活性化を利用する合成経路が記載されている。ジチアンは金属化され、メチル含有化合物及び/又は13CO2と反応する。この参考文献に概要が記されている適当な同位体濃縮13C−成分を用いることによって、13C1−ピルビン酸塩、13C2−ピルビン酸塩又は13C1,2−ピルビン酸塩を得ることが可能である。続いてカルボニル官能基が文献に記載された従来の方法を用いることによって遊離される。別の合成経路は酢酸から出発し、これは最初に臭化アセチルに変換され、次いでCu13CNと反応する。得られたニトリルはアミドを経由してピルビン酸に変換される(例えばS.H.Anker et al.,J.Biol.Chem.176(1948),1333又はJ.E.Thirkettle,Chem Commun.(1997),1025を参照されたい)。さらに、13C−ピルビン酸は、市販の13C−ピルビン酸ナトリウムを例えば米国特許第6232497号に記載された方法又は国際公開第2006/038811に記載された方法によってプロトン化することによって得てもよい。
【0036】
DNPによる13C−ピルビン酸の過分極は、参照により本明細書に組み込まれる国際公開第2006/011809号に詳しく記載されている。簡潔には、13C−ピルビン酸は凍結された際にガラスを形成するので、DNPに直接用い得る。DNPの後、凍結過分極13C−ピルビン酸は溶解して中和する、即ち13C−ピルビン酸塩に変換する必要がある。変換のためには強塩基が必要である。さらに、13C−ピルビン酸は強酸であるので、DNP剤はこの強酸の中で安定であるものを選ぶ必要がある。好ましい塩基は水酸化ナトリウムであり、水酸化ナトリウムによる過分極13C−ピルビン酸の変換によって過分極13C−ピルビン酸ナトリウムが得られる。これはインビボMR造影、分光法、及び/又は分光造影、即ち生きたヒト又はヒト以外の動物について実施されるMR造影、分光法、及び/又は分光造影のために用いられる造影媒体のための好ましい13C−ピルビン酸塩である。
【0037】
或いは、13C−ピルビン酸塩、即ち13C−ピルビン酸の塩をDNPに用いることができる。参照により本明細書に組み込まれる国際公開第2007/111515号に詳しく記載されているように、好ましい塩はNH4+、K+、Rb+、Cs+、Ca2+、Sr2+及びBa2+、好ましくはNH4+、K+、Rb+又はCs+、より好ましくはK+、Rb+、Cs+、最も好ましくはCs+からなる群からの無機カチオンを含む13C−ピルビン酸塩である。これらの好ましい13C−ピルビン酸塩の合成も、国際公開第2007/111515号に開示されている。過分極13C−ピルビン酸塩をインビボMR造影及び/又は分光法のための造影媒体において用いる場合には、NH4+、K+、Rb+、Cs+、Ca2+、Sr2+及びBa2+からなる群からの無機カチオンを、Na+又はメグルミン等の生理学的に極めてよく認容可能なカチオンに交換することが好ましい。これは、カチオン交換カラムの使用等の当技術で知られた方法によって行なってよい。
【0038】
参照により本明細書に組み込まれる国際公開第2007/069909号に詳しく記載されているように、さらに好ましい塩は有機アミン又はアミノ化合物の13C−ピルビン酸塩、好ましくはTRIS−13C1−ピルビン酸塩又はメグルミン−13C1−ピルビン酸塩である。これらの好ましい13C−ピルビン酸塩の合成も、国際公開第2007/069909号に記載されている。
【0039】
本発明の方法で用いる過分極13C−ピルビン酸塩がDNPによって得られる場合には、13C−ピルビン酸又は13C−ピルビン酸塩及びDNP剤を含む分極すべき試料は、常磁性金属イオンをさらに含んでもよい。参照により本明細書に組み込まれる国際公開第2007/064226号に詳しく記載されているように、DNPによって分極すべき組成物中の常磁性金属イオンの存在によって13C−ピルビン酸/13C−ピルビン酸塩における分極レベルが増大することが見出された。
【0040】
前に述べたように、本発明の方法による造影媒体は、インビボMR造影、分光法、及び/又は分光造影、即ち生きたヒト又はヒト以外の動物について実施されるMR造影、分光法及び/又は分光造影のための造影媒体として用いられ得る。そのような造影媒体は、好ましくは13C−ピルビン酸塩等のMR活性剤13C−物質に加えて水性担体、好ましくは水/生理食塩液、緩衝液又は緩衝液の混合物等の生理学的に認容可能で、薬学的に許容される水性担体を含む。造影媒体は従来の薬学的に許容される担体、添加剤及び配合助剤をさらに含んでもよい。したがって、造影媒体は例えば安定剤、浸透圧調整剤、可溶化剤等、例えばヒト医学又は獣医学における診断用組成物のための従来のもの等の配合助剤を含んでよい。
【0041】
さらに、本発明の方法による造影媒体は、インビトロMR造影、分光法、及び/又は分光造影のため、例えば細胞培養物又はエクスビボ組織において炎症又は感染を検出するための造影媒体として用い得る。そのような造影媒体は、好ましくは13C−ピルビン酸塩等のMR活性剤13C−物質に加えてインビトロ細胞又は組織アッセイに適合して用いられる溶媒、例えばDMSO若しくはメタノール又は水性担体及び非水性溶媒を含む溶媒混合物、例えばDMSOと水若しくは緩衝溶液又はメタノールと水若しくは緩衝溶液の混合物を含む。当業者には明らかなように、薬学的に許容される担体、添加剤及び配合助剤はそのような造影媒体中に存在してもよいが、そのような目的のために要求されてはいない。
【0042】
過分極13C−ピルビン酸塩を例えば細胞培養物又はエクスビボ組織を用いたMR造影又は分光法のインビトロ方法で感染の検出のための造影剤として用いる場合には、細胞培養物又はエクスビボ組織に添加する過分極13C−ピルビン酸塩を含む造影媒体は13C−ピルビン酸塩が10mM〜100mM、より好ましくは20mM〜90mM、最も好ましくは13C−ピルビン酸塩が40〜80mMである。
【0043】
さらに、本発明の方法によって検出される炎症及び感染疾患の種類は様々であり得る。本方法は免疫系が活性化されているか変化している疾患の範囲を検出するために用い得る。これらの疾患は皮膚及び骨格系、消化系、筋肉系、リンパ系、内分泌系、神経系、心臓血管系、男性又は女性生殖系、及び泌尿器系等のいかなる体組織にも影響し得る。本方法は身体のいかなる部分に対する自己免疫疾患をも検出し得る。自己免疫成分を含む臨床疾患の非包括的なリストとしては、関節リウマチ、若年性特発性関節炎、全身性紅斑性狼瘡、強皮症、皮膚筋炎、心筋症、クローン病及び多発性硬化症が挙げられる。この方法は外傷後の治癒に対する炎症反応を検出するために用い得る。この方法はアテローム性動脈硬化症、変形性関節症、腱炎、滑液包炎、痛風性関節炎、COPD、喘息、及び慢性気管支炎等の炎症成分を有する慢性疾患を検出するために用い得る。この方法は皮膚、四肢、筋肉、結合組織、骨、関節、神経系、並びに頭部、頚部、胸部、及び腹部の内部器官を含む身体のいかなる部分の感染(例えば細菌、ウイルス、真菌、寄生虫、又は他の感染源)に対する反応における炎症をも検出し得る。炎症は移植において大きな役割を果たす。本方法は、固形臓器の急性及び慢性移植拒絶、移植後リンパ増殖性疾患及びグラフト対宿主疾患等の、移植の設定における免疫系の変化を検出し得る。
【0044】
本発明の方法は上述のこれらの種類の条件全ての検出を含む。好ましい実施形態は関節炎、より好ましくは関節リウマチを検出するための13C−MR造影、13C−MR分光法、及び/又は13C−MR分光造影の方法であり、過分極13C−物質、好ましくは過分極13C−ピルビン酸塩を含む造影媒体が用いられる。
【0045】
別の実施形態では、造影媒体は乳酸塩をさらに含む。したがって、本発明の方法による造影媒体は過分極13C−ピルビン酸塩に加えて非過分極乳酸塩(以下、乳酸塩という)を含む。適切には、乳酸塩は乳酸又は乳酸の塩、好ましくは乳酸リチウム又は乳酸ナトリウム、最も好ましくは乳酸ナトリウムの形で添加される。乳酸塩及び過分極13C−ピルビン酸塩を含む造影媒体及びそれらを用いるための方法は、参照により本明細書に組み込まれるWO2008/020765にさらに記載されている。
【0046】
炎症及び感染は、本発明の方法により、13C−ピルビン酸塩の信号及びその代謝産物である13C−乳酸塩の信号を経時的に追跡することによって検出することができる。生存できる、例えば非炎症性の細胞において、13C−ピルビン酸塩の信号は経時的に減衰する。13C−乳酸塩の信号は13C−ピルビン酸塩の13C−乳酸塩への代謝変換によって最初増加し、次いで主として緩和のためにゆっくりと減少する。炎症領域においてはピルビン酸塩の代謝は上方調節されており、13C−ピルビン酸塩の13C−乳酸塩への変換は増加する。過分極13C−ピルビン酸塩を含む造影媒体を用いて、13C−MR検出によって検出することができる13C−乳酸塩の産生の増加によってこの亢進した代謝活性を見ることができる。
【0047】
乳酸塩(本発明による造影媒体中に存在していようと、又は個別に添加/投与されようと)の添加によって、観察し得る13C−乳酸塩の量の増加及びそれによる13C−乳酸塩からのMR信号の増大がもたらされることがさらに見出された。
【0048】
用語「13C−MR検出」は、13C−MR造影若しくは13C−MR分光法又は13C−MR造影と13C−MR分光法の組み合わせ、即ち13C−MR分光造影を意味する。この用語はさらに、種々の時点における13C−MR分光造影を意味する。
【0049】
周波数と空間的に選択的な方法を組み合わせて関心体積をエンコードするMR造影シーケンスが適用され、13C−ピルビン酸塩の13C−MR信号が造影剤の添加(t=0)から約1分間又はT1緩和を経由する信号の減衰によって13C−MR信号が検出不能になるまでの時間にわたってMR造影又は分光造影によって追跡される。同じ時間の間、13C−乳酸塩の信号の出現、増加及び/又は減少が監視される。定量的評価を得るため、健常な細胞又は組織のMR造影、分光法、又は分光造影を行なってもよく、その結果(即ち所与の時間の間に形成された13C−乳酸塩の量又は速度)を比較することができる。
【0050】
過分極13C−ピルビン酸塩を例えば生きたヒト又はヒト以外の動物の身体におけるMR造影、分光法又は分光造影のインビボ法において炎症又は感染の検出のための造影剤として用いる場合には、過分極13C−ピルビン酸塩を含む造影媒体は、好ましくは前記生体に非経口的に、好ましくは静脈内に投与される。一般的には、検査される生体はMR磁石の中に置かれる。専用の13C−MR RFコイルが関心領域をカバーするように置かれる。造影媒体の用量及び濃度は、毒性及び投与経路等の要素の範囲に依存することになる。一般的には、造影媒体は体重kgあたり1mmol13C−ピルビン酸塩まで、好ましくは0.01〜0.5mmol/kg、より好ましくは0.1〜0.3mmol/kgの濃度で投与される。投与速度は好ましくは10ml/s未満、より好ましくは6ml/s未満、最も好ましくは5ml/s〜0.1ml/sである。投与後400s未満、好ましくは120s未満、より好ましくは投与後60s未満、特に好ましくは20〜50sで、周波数と空間的に選択的な方法を組み合わせて関心体積をエンコードするMR造影シーケンスが適用される。これにより13C−ピルビン酸塩、13C−乳酸塩及び/又は他の13C−標識代謝生成物の代謝画像がもたらされることになる。MRシーケンスを適用する正確な時間は、感染又は炎症を検出する関心体積に高度に依存する。
【0051】
関心体積のエンコーディングは、これだけに限らないが、例えばT.R.Brown et al.,Proc Natl Acad Sci USA 79、3523−3526(1982);A.A.Maudsley et al.,J Magn Res 51,147−152(1983);D.Mayer et al.,Magn Reson Med 56,932−937(2006);S.J.Kohler et al.,Magn Reson Med 58(1),65−9(2007);Y−F.Yen et al.,Magn Reson Med(Epub ahead of print)Mar 24(2009)に記載されているもの等のいわゆる分光造影シーケンスを用いることによって達成することができる。分光画像データには、その中の各要素が完全な13C−MRスペクトルを含むいくつかの体積要素が含まれる。13C−ピルビン酸塩及びその代謝物である13C−乳酸塩は13C−MRスペクトルにおいて独特の位置を有しており、それらの共鳴周波数はそれらを同定するために用いることができる。その共鳴周波数におけるスペクトルピークの積分は、それぞれ13C−ピルビン酸塩及び13C−乳酸塩の量に直接関連する。13C−ピルビン酸塩及び13C−乳酸塩の量が例えばL.Vanhamme et al.,J Magn Reson 129,35−43(1997)に記載されているようなスペクトルピーク積分解析若しくは時間領域近似ルーチン又は例えばS.B.Reeder et al.,J Magn Reson Imaging 26,1145−1152(2007)及びY.S.Levin et al.,Magn Reson Med 58(2),245−52(2007)に記載されているような最小二乗化学シフト分離法を用いて推定される場合には、13C−ピルビン酸塩及び13C−乳酸塩の画像を生成し、その中のカラーコーディング又はグレイコーディングによって13C−ピルビン酸塩及び13C−乳酸塩の測定された量を表わすことができる。
【0052】
分光造影法は全種類のMR核、例えば1H、31P、23Naを用いる代謝画像を生成することにおいてその価値を証明してきたが、分光画像を完全にエンコードするために必要な繰り返しの量が多いので、このアプローチは過分極13Cにはあまり適しないものになっている。全体のMRデータ取得の間、過分極13C−信号が利用可能であることを確実にするよう、注意を払わなくてはならない。これは、例えばL.Zhao et al.,J Magn Reson,B(113),179−183(1996)に記載されているようにRF−パルス励起フリップ角を低減するか、若しくは変動フリップ角を適用することによって、又は例えばP.E.Z.Larson et al.,J Magn Reson 194:121−127(2008)に記載されているように全フェーズエンコーディングステップにおいて適用されるマルチバンドRF励起デザインによって、達成することができる。マトリックスサイズが大きくなると、フェーズエンコーディングステップを多くし、走査時間を長くする必要がある。
【0053】
P.C.Lauterbur(Nature,242,190−191,(1973)及びP.Mansfield(J.Phys.C.6,L422−L426(1973))の先駆的な研究に基づく造影方法はデータ取得の間、読み出し勾配を適用するものであるが、これにより高い信号雑音比の画像、又はこれと等価の高い空間分解能の画像が可能になるであろう。しかし、その基本形におけるこれらの造影方法は13C−ピルビン酸塩と13C−乳酸塩についての個別の画像を生成することはできず、即ち特定の代謝産物の同定は可能でない。
【0054】
別の実施形態では、周波数情報をコードするためにマルチエコーを用いることになる造影シーケンスが用いられる。水と脂肪の1H−画像を個別に生成することができるシーケンスは、例えばG.Glover,J Magn Reson Imaging1,521−530(1991)及びS.B.Reeder et al.,Magn Reson Med 51,35−45(2004)に記載されている。検出すべき代謝産物、したがってそのMR周波数は知られているので、上の参考文献で議論されたアプローチは13C−ピルビン酸塩及び13C−乳酸塩の直接の画像を取得するために適用することができる。この手順により過分極13C−MR信号の使用がより効率的になり、分光造影に比べてより良い信号品質、より高い空間分解能及びより早い取得時間が得られる。
【0055】
好ましい実施形態では、本発明による方法には、過分極13C−ピルビン酸塩を含む造影媒体を予め投与したヒト又はヒト以外の動物の身体から、又は造影媒体を添加した細胞培養物又はエクスビボ組織から、直接の13C−MR画像又は13C−ピルビン酸塩及び13C−乳酸塩のスペクトルを取得するステップが含まれる。開示した方法では、感染又は炎症は13C−乳酸塩からの高い13C−信号強度又は13C−乳酸塩の生成速度の増大によって同定及び検出される。本発明による過分極13C−ピルビン酸塩造影は、炎症及び感染において乳酸への代謝が増大していることを示す。
【0056】
ピルビン酸塩の信号を補正するために、乳酸塩及びピルビン酸塩の画像を各個別の画像における最大値に正規化してもよい。次に、正規化された乳酸塩の画像にピルビン酸塩の画像の逆数、例えば画像中の最大のピルビン酸塩の信号からピクセル毎のピルビン酸塩レベルを差し引いたものを乗じる。最後のステップとして、上の操作で得られた中間結果に元の乳酸塩の画像を乗じる。或いは、それぞれの画像の各ピクセル中のピルビン酸塩及び乳酸塩のピーク強度をピルビン酸塩と乳酸塩との間の13C−ラベルのフラックスの動態モデルに合致させて、ラベルフラックス及びスピン格子緩和時間の速度定数を得ることができる。分極の喪失に対するマルチプルRFパルスの影響について補正を行なう必要があろう。
【0057】
本方法をインビボの炎症又は感染の検出のために用いる場合には、本発明の方法による炎症又は感染の検出において解剖学的及び/又は潅流情報が含まれてもよい。解剖学的情報は、例えば適当な造影剤を用いて、又は用いずにプロトンMR画像を取得することによって得られる。相対的な潅流は例えばOmniscan(商標)のようなMR造影剤を用いることによって決定することができる。同様に、造影剤を投与しない潅流測定のためのMR造影手法は当技術分野で知られている。好ましい実施形態では、定量的潅流を決定するために非代謝過分極13C−造影剤を用いる。適切な手法及び造影剤は例えば国際公開第02/23209号に記載されている。より好ましい実施形態では、定量的潅流を決定するために過分極13C−ピルビン酸塩が用いられる。
【0058】
別の好ましい実施形態では、過分極13C−ピルビン酸塩を含む造影媒体は繰り返し投与され、それにより長期的研究が可能になる。ピルビン酸塩の毒性が低いこととその好ましい安全性プロファイルにより、この化合物の繰り返し用量は患者によく認容される。
【0059】
本発明の方法で得られる結果は、例えば医師が検討中の患者に対する適切な処置を選択することを可能にする。さらなる好ましい実施形態では、本発明の方法は処置が成功したかどうかを決定するために用いられる。
【0060】
さらなる態様から見れば、本発明は炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−物質の使用を提供する。より好ましくは、本発明は炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−ピルビン酸塩の使用を提供する。好ましくは、造影媒体の製造のために用いられる過分極13C−ピルビン酸塩は、13C−ピルビン酸又は13C−ピルビン酸塩の動的核分極によって得られる。任意選択で、造影媒体の製造のために乳酸塩を13C−物質に添加してもよい。
【0061】
13C−ピルビン酸又は13C−ピルビン酸塩からの過分極13C−ピルビン酸塩の製造及び製造の好ましい実施形態、並びに過分極13C及び任意選択で乳酸塩を含む造影媒体の製造については、本出願の6〜10頁に詳しく記載されている。
【0062】
好ましい実施形態では、本発明は造影媒体を予め投与したヒト又はヒト以外の動物の身体から、又は造影媒体を添加した細胞培養物又はエクスビボ組織から、直接の13C−画像及び/又は13C−ピルビン酸塩及び13C−乳酸塩の13C−スペクトルを取得することによって炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−ピルビン酸塩及び任意選択による乳酸塩の使用を提供する。
【0063】
別の好ましい実施形態では、本発明はヒト又はヒト以外の動物の身体において炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における過分極13C−物質を含む造影媒体の使用を提供する。造影媒体は好ましくは、ヒト又はヒト以外の動物の身体に予め投与されている。
【図面の簡単な説明】
【0064】
【図1】関節炎の関節の代謝マップを示す図である。過分極[1−13C]ピルビン酸塩を注射した20秒後に、マップは関節炎の足において乳酸塩の産生が亢進していることを示している。A:T2重み付け解剖学的画像は、関節炎の右後足(矢印)において正常な左足に比べて組織が腫脹していることを示しており、次の代謝マップ上では尾(T)及び非分極13C−乳酸塩(L)の参照チューブに重ねられている。マップはB:[1−13C]ピルビン酸塩、C:[1−13C]乳酸塩、及びD:[1−13C]乳酸塩/[1−13C]ピルビン酸塩の比を示している。
【図2】1匹のラットの関節炎の足(青)における[1−13C]乳酸塩の産生の亢進を正常な足(右)及び尾(緑)と比較した時間分解造影を示す図である。
【実施例】
【0065】
実施例1:関節炎の検出
6匹の幼若Sprague Dawleyラット(4〜5週齢、平均体重114g)に0.4μL/gの完全フロイントアジュバントを注射(ラット3匹には右膝、ラット3匹には右足首)することによって関節炎を誘導した。誘導の7日後に、励起及び信号受容の両方のために自己遮蔽グラジエント(40mT/m、150mT/m/ms)及び特注のデュアルチューン(1H/13C)直角位相コイル(φ=80mm)を備えたGE 3T スキャナーにより、13C MRSによって関節炎の関節を造影した。13C−1−ピルビン酸塩の100mM溶液0.5mLをDNP(15〜20%液体状態分極)によって過分極し、尾静脈から注射した。注射の20秒後に、FID CSIシーケンス(ボクセル=2.5×2.5×10mm、FOV=4×4cm)によって13C−1ピルビン酸塩及びその代謝産物の単一時点MRS解析を得た。2回目の過分極13C−ピルビン酸塩の注射の間、1D EPSIシーケンスによって時間分解造影を得た。関節におけるROI解析によってピルビン酸塩及び乳酸塩の平均信号強度を得て、正常及び関節炎の関節をT検定によって比較した。
【0066】
関節炎の関節は紅斑があり、腫脹していて(平均±SD=0.5±0.2mm厚みが大きい)、組織学的スコアは炎症について3/4(正常関節の0/4と比較)を有し、解剖学的MR画像において炎症のT2重み付け変化を示した。[1−13C]ピルビン酸塩及び代謝された[1−13C]乳酸塩は、FID CSI画像(図1A、B)上で、関節炎の関節において増加しているように思われ、関節における代謝産物の全13Cに対する比のROI解析によって有意差を有する傾向があった[関節炎のピルビン酸塩=0.34対正常=0.28、p<0.17;関節炎の乳酸塩=0.21対正常=0.16、p<0.12]。炎症組織における血流の増大が造影剤の送達の増大の原因かも知れないが、時間分解造影(図2)によって、また乳酸塩の全13Cに対する比(関節炎=0.62対正常=0.56、p<0.03)によって示されるように、乳酸塩への変換速度も関節炎の関節において増大していた。
【0067】
したがって、これらの結果によれば、過分極[1−13C]ピルビン酸塩造影は、関節炎に罹患した関節における乳酸塩への代謝の亢進を示す。乳酸塩産生の亢進は、関節炎の活動度のマーカーとして役立つであろう。
【符号の説明】
【0068】
A T2重み付け解剖学的画像
B [1−13C]ピルビン酸塩
C [1−13C]乳酸塩
D [1−13C]乳酸塩/[1−13C]ピルビン酸塩の比
L 非分極13C−乳酸塩
T 尾
【特許請求の範囲】
【請求項1】
炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法であって、過分極13C−物質を含む造影媒体を用いる方法。
【請求項2】
過分極13C−物質が過分極13C−ピルビン酸塩である、請求項1記載の方法。
【請求項3】
造影媒体をヒト又はヒト以外の動物の身体に投与し、前記ヒト又はヒト以外の動物の身体における炎症又は感染を検出するために前記13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影を実施する、請求項1又は請求項2記載の方法。
【請求項4】
造影媒体を細胞培養物又はエクスビボ組織に添加し、前記細胞培養物又はエクスビボ組織における炎症又は感染を検出するために前記13C−MR造影及び/又は13C−MR分光法を実施する、請求項1又は請求項2記載の方法。
【請求項5】
13C−物質及びその代謝産物である13C−乳酸塩からの13C−信号強度を経時的に追跡する、請求項1乃至請求項4のいずれか1項記載の方法。
【請求項6】
13C−物質及び13C−乳酸塩からの13C−信号強度を造影媒体の投与/添加の時点から約1分間又はT1緩和を経由する信号の減衰によって13C−MR信号が検出不能になるまで追跡する、請求項5記載の方法。
【請求項7】
炎症又は感染を13C−乳酸塩からの高い13C−信号強度又は13C−乳酸塩の生成速度の増大によって検出する、請求項1乃至請求項6のいずれか1項記載の方法。
【請求項8】
前記造影媒体の投与/添加に先立って前記ヒト又はヒト以外の動物の身体に乳酸塩を投与する、請求項3記載の方法。
【請求項9】
前記造影媒体の添加に先立って前記細胞培養物又はエクスビボ組織に乳酸塩を添加する、請求項4記載の方法。
【請求項10】
過分極13C−ピルビン酸塩が13C−ピルビン酸又は13C−ピルビン酸塩の動的核分極によって得られる、請求項2乃至請求項9のいずれか1項記載の方法。
【請求項11】
炎症又は疾患を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−物質の使用。
【請求項12】
ヒト又はヒト以外の動物の身体において炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法であって、過分極13C−物質を含む造影媒体をヒト又はヒト以外の動物の身体に予め投与する方法。
【請求項13】
ヒト又はヒト以外の動物の身体において炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影方法における過分極13C−物質を含む造影媒体の使用。
【請求項1】
炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法であって、過分極13C−物質を含む造影媒体を用いる方法。
【請求項2】
過分極13C−物質が過分極13C−ピルビン酸塩である、請求項1記載の方法。
【請求項3】
造影媒体をヒト又はヒト以外の動物の身体に投与し、前記ヒト又はヒト以外の動物の身体における炎症又は感染を検出するために前記13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影を実施する、請求項1又は請求項2記載の方法。
【請求項4】
造影媒体を細胞培養物又はエクスビボ組織に添加し、前記細胞培養物又はエクスビボ組織における炎症又は感染を検出するために前記13C−MR造影及び/又は13C−MR分光法を実施する、請求項1又は請求項2記載の方法。
【請求項5】
13C−物質及びその代謝産物である13C−乳酸塩からの13C−信号強度を経時的に追跡する、請求項1乃至請求項4のいずれか1項記載の方法。
【請求項6】
13C−物質及び13C−乳酸塩からの13C−信号強度を造影媒体の投与/添加の時点から約1分間又はT1緩和を経由する信号の減衰によって13C−MR信号が検出不能になるまで追跡する、請求項5記載の方法。
【請求項7】
炎症又は感染を13C−乳酸塩からの高い13C−信号強度又は13C−乳酸塩の生成速度の増大によって検出する、請求項1乃至請求項6のいずれか1項記載の方法。
【請求項8】
前記造影媒体の投与/添加に先立って前記ヒト又はヒト以外の動物の身体に乳酸塩を投与する、請求項3記載の方法。
【請求項9】
前記造影媒体の添加に先立って前記細胞培養物又はエクスビボ組織に乳酸塩を添加する、請求項4記載の方法。
【請求項10】
過分極13C−ピルビン酸塩が13C−ピルビン酸又は13C−ピルビン酸塩の動的核分極によって得られる、請求項2乃至請求項9のいずれか1項記載の方法。
【請求項11】
炎症又は疾患を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法における使用のための造影媒体の製造のための過分極13C−物質の使用。
【請求項12】
ヒト又はヒト以外の動物の身体において炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影の方法であって、過分極13C−物質を含む造影媒体をヒト又はヒト以外の動物の身体に予め投与する方法。
【請求項13】
ヒト又はヒト以外の動物の身体において炎症又は感染を検出するための13C−MR造影、13C−MR分光法及び/又は13C−MR分光造影方法における過分極13C−物質を含む造影媒体の使用。
【図1】


【図2】




【図2】


【公表番号】特表2012−522549(P2012−522549A)
【公表日】平成24年9月27日(2012.9.27)
【国際特許分類】
【出願番号】特願2012−502586(P2012−502586)
【出願日】平成22年3月25日(2010.3.25)
【国際出願番号】PCT/EP2010/053912
【国際公開番号】WO2010/112397
【国際公開日】平成22年10月7日(2010.10.7)
【出願人】(305040710)ジーイー・ヘルスケア・リミテッド (99)
【出願人】(507098070)スタンフォード・ユニバーシティ ザ・ボード・オブ・トラスティーズ・オブ・ザ・ルランド・スタンフォード・ジュニア・ユニバーシティ (4)
【Fターム(参考)】
【公表日】平成24年9月27日(2012.9.27)
【国際特許分類】
【出願日】平成22年3月25日(2010.3.25)
【国際出願番号】PCT/EP2010/053912
【国際公開番号】WO2010/112397
【国際公開日】平成22年10月7日(2010.10.7)
【出願人】(305040710)ジーイー・ヘルスケア・リミテッド (99)
【出願人】(507098070)スタンフォード・ユニバーシティ ザ・ボード・オブ・トラスティーズ・オブ・ザ・ルランド・スタンフォード・ジュニア・ユニバーシティ (4)
【Fターム(参考)】
[ Back to top ]

