炎症性メディエータ産生抑制剤及びそれを含有する皮膚外用剤
【課題】経皮吸収性に優れ、副作用が少なく、且つ安全性の高い炎症性メディエータ産生抑制能及びそれを含有する皮膚外用剤の提供。
【解決手段】アルニカの植物体から抽出物を取得し、これを有効成分とする炎症性メディエータ(例えばIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるもの)の産生抑制剤を得、さらにこの炎症性メディエータ産生抑制剤を皮膚外用剤に配合して炎症性メディエータ産生抑制用皮膚外用剤とする。
【解決手段】アルニカの植物体から抽出物を取得し、これを有効成分とする炎症性メディエータ(例えばIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるもの)の産生抑制剤を得、さらにこの炎症性メディエータ産生抑制剤を皮膚外用剤に配合して炎症性メディエータ産生抑制用皮膚外用剤とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、炎症性メディエータ産生抑制剤及びそれを含有する皮膚外用剤に関する。詳しくは、本発明は、アルニカ抽出物を有効成分とし、経皮吸収性、安全性等に優れた炎症性メディエータ産生抑制剤及びそれを含有する皮膚外用剤に関する。
【背景技術】
【0002】
皮膚は生体の最外郭に位置し、化学物質や紫外線などの環境因子の刺激を常に受け、生体防御の最前線であるとともに生体防御反応の場となっている。炎症反応は、本来生体を防御するための反応であるが、その反応が過剰に進行した場合、紅斑(赤み)、血管透過性亢進(腫脹)、発熱(ほてり)を主徴とする症状が現れる。
【0003】
いわゆる、日焼けと呼ばれる紫外線を浴びた後に惹起される色素沈着は、表皮に存在するメラノサイトにおけるメラニン色素の合成促進がその本態であるが、このメラニン産生亢進も生体防御反応のひとつと考えられる。
【0004】
しかし、これらの反応が過剰になった場合、特に皮膚ではその反応が身体の浅部で惹起され症状が顕著に発現するために、医療上の問題ばかりでなく、外観への影響といった美容上の問題も含まれる。
【0005】
近年の研究で、炎症反応およびメラニン合成促進反応に、表皮細胞で産生されるIL−6(インターロイキン−6)、IL−1α(インターロイキン−1α)、プロスタグランジン、エンドセリンといった化学物質が深く関与することが明らかになってきている。特に、IL−6が紫外線照射によって表皮細胞から放出されると、皮膚にとどまらずIL−6の血中濃度が上昇し、抑鬱感、集中力の低下、形状認識障害などの全身作用(精神作用)への影響が現れることばかりでなく、例えばトライアスロン選手のランタイムがIL−6の増加に伴って悪化するといった運動能力への影響があることも明らかになった。
【0006】
従来は、炎症に対しては抗炎症作用を有する物質が、色素沈着に対してはメラニン合成を抑制する作用を有する物質が、全身作用については向精神薬的な物質が投与されてきた。また、運動能力の低下に関しては、筋肉増強剤などのドーピング違反となるような物質以外に適用されているものは無い。
【0007】
しかしながら、これまで開発されてきた上記の各有効性を示す物質は優れた効果を有するものの、目的とする作用以外に強い生理作用を併有する、また皮膚での局所投与ではその経皮吸収性の問題から期待した効果が得られない場合がある等の課題があることが知られている。さらに、上記の作用に対して網羅的に効果を発揮するものではないため、各作用に対して個々に対応する必要があった。
【0008】
一方、アルニカ抽出物が抗アレルギー作用や抗炎症作用を有することは知られており、化粧料等の外用剤へ配合して使用することが提案されている(特許文献1〜3)。しかしながら、アルニカ抽出物が特定の炎症性メディエータ産生抑制作用を有することは知られていなかった。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開平9−87189
【特許文献2】特開2006−348035
【特許文献3】特開2007−8847
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、経皮吸収性に優れ、副作用が少なく、且つ安全性の高い炎症性メディエータ産生抑制能及びそれを含有する皮膚外用剤を提供することを課題とする。
【課題を解決するための手段】
【0011】
本発明者らは、アルニカ抽出物が、IL−6、IL−1α、プロスタグランジン、及びエンドセリンといった炎症性メディエータの産生を抑制する作用に優れる、特にIL−6の産生を抑制する作用に優れること、並びにIL−6の産生を抑制することによって運動能力の低下予防効果が期待できること、同時に生体に対しては安全であることを見いだし、本発明を完成した。
【0012】
すなわち、本発明は、以下の(1)〜(2)に示す皮膚外用剤に関する。
(1)アルニカ抽出物を有効成分とする、炎症性メディエータ産生抑制剤。
(2)前記炎症性メディエータがIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるものである、(1)記載の炎症性メディエータ産生抑制剤。
(3)前記炎症性メディエータがIL−6であることを特徴とする、(1)記載の炎症性メディエータ産生抑制剤。
(4)(1)〜(3)のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、炎症性メディエータ産生抑制用皮膚外用剤。
(5)(1)〜(3)のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、運動能力低下予防剤。
【発明の効果】
【0013】
本発明によれば、アルニカ抽出物を有効成分とする炎症性メディエータ産生抑制剤は抗炎症作用に加え、メラニン合成抑制作用、向精神作用、運動能力の低下予防作用などに優れ、副作用が少なく、且つ経皮吸収性及び人体への安全性が高い。よって、炎症性メディエータ産生抑制用皮膚外用剤として有用である。
【図面の簡単な説明】
【0014】
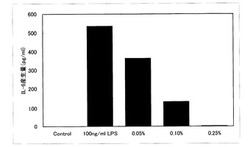
【図1】本発明の実施例1の結果を示すグラフである。
【図2】本発明の実施例2の結果を示すグラフである。
【図3】本発明の実施例3の結果を示すグラフである。
【図4】本発明の実施例4の結果を示すグラフである。
【図5】本発明の実施例5の結果を示すグラフである。
【図6】本発明の実施例6,7,比較例1の結果を示すグラフである。
【図7】本発明の実施例6,7,比較例1の結果を示すグラフである。
【発明を実施するための形態】
【0015】
(1)アルニカ抽出物
本発明に使用されるアルニカはキク科ウサギギク属に属する植物であり、使用する部位は特に限定されず花、根、葉、枝、茎など全草から抽出することができる。
抽出物は、乾燥した植物体を細切し、水、エタノール、プロピレングリコール、1,3−ブチレングリコール等の親水性有機溶剤、又はこれらの混合物に浸漬し、得られた液をろ過して得られる。溶剤の温度及び浸漬時間は特に制限されない。
このようにして得られるアルニカ抽出物の形態は、粉末状、ゲル状、ペースト状などいずれであってもよい。
【0016】
(2)炎症性メディエータ産生抑制剤
上記アルニカ抽出物は、そのまま炎症性メディエータ産生抑制剤として利用することができる。特に、前記炎症性メディエータとしてIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるものに対し、優れた産生抑制作用を有する。さらに、前記炎症性メディエータとしてIL−6に対し、優れた産生抑制作用を有する。そして、IL−6の産生により引き起こされるとされる抑鬱感、集中力の低下、形状認識障害などの全身作用(精神作用)への影響や、IL−6の増加に伴って悪化するとされる運動能力の低下を抑制又は予防する作用が期待される。
【0017】
(3)皮膚外用剤
本発明の炎症性メディエータ産生抑制剤はそのまま、あるいは皮膚外用剤へ配合して使用することができる。
皮膚外用剤中のアルニカ抽出物の配合量は、特に限定されるものではないが、乾燥固形物重量で、総量を基準として0.0001〜10.0重量%が好ましく、更に好ましくは0.0005〜5.0重量%、特に好ましくは0.01〜5重量%である。該配合量が0.0001重量%未満であると、本発明の効果が充分に得られず、一方10.0重量%を超えても、その増量に見合った効果の向上は認められない。
【0018】
本発明の皮膚外用剤は、例えばローション類、乳液類、クリーム類、軟膏類、パック類等の剤型とすることができる。
また、本発明の皮膚外用剤には、上記炎症性メディエータ産生抑制剤に加え、本発明の効果を損なわない範囲で必要に応じて医薬品類、医薬部外品類、化粧品類などの製剤に使用される成分や添加剤、例えば色素(着色剤)、防腐剤、界面活性剤、香料、顔料等を任意成分として適宜配合することができる。
【0019】
そのような任意成分としては、例えば、マカデミアナッツ油、アボガド油、トウモロコシ油、オリーブ油、ナタネ油、ゴマ油、ヒマシ油、サフラワー油、綿実油、ホホバ油、ヤシ油、パーム油、液状ラノリン、硬化ヤシ油、硬化油、モクロウ、硬化ヒマシ油、ミツロウ、キャンデリラロウ、カルナウバロウ、イボタロウ、ラノリン、還元ラノリン、硬質ラノリン、ホホバロウ、鉱物油(ミネラルオイル)等のオイル、ワックス類、流動パラフィン、スクワラン、プリスタン、オゾケライト、パラフィン、セレシン、ワセリン、マイクロクリスタリンワックス等の炭化水素類;
【0020】
イソオクタン酸セチル、ミリスチン酸イソプロピル、イソステアリン酸ヘキシルデシル、アジピン酸ジイソプロピル、セバチン酸ジ−2−エチルヘキシル、乳酸セチル、リンゴ酸ジイソステアリル、ジ−2−エチルヘキサン酸エチレングリコール、ジカプリン酸ネオペンチルグリコール、ジ−2−ヘプチルウンデカン酸グリセリン、トリ−2−エチルヘキサン酸グリセリン、トリ−2−エチルヘキサン酸トリメチロールプロパン、トリイソステアリン酸トリメチロールプロパン、テトラ−2−エチルヘキサン酸ペンタンエリトリット、水添ココグリセリル、ステアリン酸ポリグリセリル、パラオキシ安息香酸メチル(メチルパラベン)等のエステル類;
【0021】
ジメチルポリシロキサン、メチルフェニルポリシロキサン、ジフェニルポリシロキサン等の鎖状ポリシロキサン、オクタメチルシクロテトラシロキサン、デカメチルシクロペンタシロキサン、ドデカメチルシクロヘキサンシロキサン等の環状ポリシロキサン、アミノ変性ポリシロキサン、ポリエーテル変性ポリシロキサン、アルキル変性ポリシロキサン、フッ素変性ポリシロキサン等の変性ポリシロキサン等のシリコーン油等の油剤類;
【0022】
脂肪酸セッケン(ラウリン酸ナトリウム、パルミチン酸ナトリウム等)、ラウリル硫酸カリウム、アルキル硫酸トリエタノールアミンエーテル等のアニオン界面活性剤類、塩化ステアリルトリメチルアンモニウム、塩化ベンザルコニウム、ラウリルアミンオキサイド等のカチオン界面活性剤類、イミダゾリン系両性界面活性剤(2−ココイル−2−イミダゾリニウムヒドロキサイド−1−カルボキシエチロキシ2ナトリウム塩等)、ベタイン系界面活性剤(アルキルベタイン、アミドベタイン、スルホベタイン等)、アシルメチルタウリン等の両性界面活性剤類、ソルビタン脂肪酸エステル類(ソルビタンモノステアレート、セスキオレイン酸ソルビタン等)、グリセリン脂肪酸類(モノステアリン酸グリセリン等)、プロピレングリコール脂肪酸エステル類(モノステアリン酸プロピレングリコール等)、硬化ヒマシ油誘導体、グリセリンアルキルエーテル、ショ糖脂肪酸エステル、アルキルグルコシド等の非イオン界面活性剤類等の界面活性剤類;
【0023】
ポリエチレングリコール、1,3−ブチレングリコール、グリセリン等の多価アルコール類;
ステアリン酸等の高級脂肪酸類;
ピロリドンカルボン酸ナトリウム、乳酸、乳酸ナトリウム等の保湿成分類;
【0024】
グアガム、クインスシード、カラギーナン、ガラクタン、アラビアガム、ペクチン、マンナン、デンプン、カードラン、メチルセルロース、ヒドロキシエチルセルロース、カルボキシメチルセルロース、メチルヒドロキシプロピルセルロース、コンドロイチン硫酸、デルマタン硫酸、グリコーゲン、ヘパラン硫酸、ヒアルロン酸ナトリウム、トラガントガム、ケラタン硫酸、コンドロイチン、ムコイチン硫酸、ヒドロキシエチルグアガム、カルボキシメチルグアガム、デキストラン、ケラト硫酸、ローカストビーンガム、サクシノグルカン、カロニン酸、キチン、キトサン、カルボキシメチルキチン、寒天、ポリビニルアルコール、ポリビニルピロリドン、カルボキシビニルポリマー(カルボマー)、ポリアクリル酸ナトリウム等のポリアクリル酸及び/又はその塩、ポリエチレングリコール、ベントナイト、微粒子セルロースゲル等の増粘剤;
【0025】
表面を処理されていても良い、マイカ、タルク、カオリン、合成雲母、炭酸カルシウム、炭酸マグネシウム、無水ケイ酸(シリカ)、酸化アルミニウム、硫酸バリウム等の粉体類; 表面を処理されていても良い、ベンガラ、黄酸化鉄、黒酸化鉄、酸化コバルト、群青、紺青、酸化チタン、酸化亜鉛の無機顔料類;表面を処理されていても良い、雲母チタン、魚燐箔、オキシ塩化ビスマス等のパール剤類;レーキ化されていても良い赤色202号、赤色228号、赤色226号、黄色4号、青色404号、黄色5号、赤色505号、赤色230号、赤色223号、橙色201号、赤色213号、黄色204号、黄色203号、青色1号、緑色201号、紫色201号、赤色204号等の有機色素類;ポリエチレン末、ポリメタクリル酸メチル、ナイロン粉末、オルガノポリシロキサンエラストマー等の有機粉体類;
【0026】
パラアミノ安息香酸系紫外線吸収剤、アントラニル酸系紫外線吸収剤、サリチル酸系紫外線吸収剤、桂皮酸系紫外線吸収剤、ベンゾフェノン系紫外線吸収剤、糖系紫外線吸収剤、2−(2’−ヒドロキシ−5’−t−オクチルフェニル)ベンゾトリアゾール、4−メトキシ−4’−t−ブチルジベンゾイルメタン等の紫外線吸収剤類;
【0027】
エタノール、イソプロパノール等の低級アルコール類;
ビタミンA又はその誘導体、ビタミンB6塩酸塩、ビタミンB6トリパルミテート、ビタミンB6ジオクタノエート、ビタミンB2又はその誘導体、ビタミンB12、ビタミンB15又はその誘導体等のビタミンB類、α−トコフェロール、β−トコフェロール、γ−トコフェロール、ビタミンEアセテート等のビタミンE類、ビタミンD類、ビタミンH、パントテン酸、パンテチン、ピロロキノリンキノン等のビタミン類;などが好ましく例示できる。
【実施例】
【0028】
以下に、本発明を実施例に基づいてさらに詳しく説明する。ただし本発明はこれらの実施例に限定されるものではない。なお、以下の調製例及び実施例中%とあるのは、特に指定がない場合w/w%である。
【0029】
<製造例1>(アルニカ抽出液含有サンプルの製造)
市販アルニカ抽出液(丸善製薬社製;固形分(蒸発残量)=2.4%;溶媒=水:1,3−ブチレングリコール=50:50(重量比))を各試験に使用する細胞培養用培地で希釈して、以下のような0.25%,0.05%および0.01%アルニカ抽出液含有サンプルとした。
・0.25%アルニカ抽出液含有サンプル(アルニカ抽出物濃度;60μg/l)
・0.05%アルニカ抽出液含有サンプル(アルニカ抽出物濃度;12μg/l)
・0.01%アルニカ抽出液含有サンプル(アルニカ抽出物濃度;2.4μg/l)
【0030】
<実施例1>(アルニカのIL−6産生抑制効果)
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル(溶媒;1,3−ブチレングリコール)及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、該上清中のIL−6量(単位;pg/ml)をmouse IL-6 CytoSet kit(Biosourse)を用いて測定した。結果を表1及び図−1に示す。
【0031】
【表1】

【0032】
<実施例2>(アルニカのIL−1α産生抑制効果)
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、該上清中のIL−1α量(単位;pg/ml)をmouse IL-1α ELISA kit(Thermo Scientific)を用いて測定した。結果を表2及び図−2に示す。
【0033】
【表2】

【0034】
<実施例3>(アルニカのプロスタグランジン産生抑制効果)
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、該上清中のプロスタグランジン量(単位;pg/ml)をPGE ELISA kit(Thermo Scientific)を用いて測定した。結果を表3及び図−3に示す。
【0035】
【表3】

【0036】
<実施例4>(アルニカのエンドセリン産生抑制作用)
マウス由来マクロファージ細胞株RAW264.7を60mmディッシュ(Falcon)に5.0×104cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換6時間後、細胞を回収し、常法に従ってRNA抽出、逆転写酵素によるDNA合成およびリアルタイムPCR(使用機器;Real-time PCR Detector Chromo4;Bio Rad社製)
を実施し、エンドセリン遺伝子の発現量を測定した(単位;%)。結果を表4及び図−4に示す。
【0037】
【表4】

【0038】
<実施例5>(アルニカの細胞毒性)
製造例1と同様の方法で0.25%、0.05%及び0.01%アルニカ抽出液含有サンプルを製造した。
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、LDH測定キットで細胞破壊によって放出されたLDH量を、測定した。測定は以下の方法で行った(単位;吸光度(%))。結果を表5及び図−5に示した。
測定用試薬キット:宝酒造社製
測定波長:490nm
測定機器:Microplate Reader SH1000(Corona Electric社製)
【0039】
【表5】

【0040】
<実施例6−7,比較例1>(紫外線照射による紅斑およびIL−6産生に対する作用)
表6に示した皮膚外用剤を調製した。簡潔にはAの油相部の原料とBの水相部の原料をそれぞれ80℃に加熱した後、B相をA相へ混合し、乳化した。その後40℃まで冷却した後、C相を加え、攪拌混合する。その後、室温まで冷却し、皮膚外用剤を得た。
サンプルの塗布は、紫外線照射前3日間(朝・入浴後1日2回)、照射直後、照射日夜、照射後1週間(朝・入浴後1日2回)、サンプルを綿棒にとり適量を照射部位に塗布した。紫外線照射は大腿部内側の非露光部位に直径約8mmで16ヶ所に1.2MEDのUVBを照射した。
紫外線照射6時間後に局所麻酔下表皮層を摘出し、常法に従ってRNA抽出、逆転写酵素によるDNA合成およびリアルタイムPCRを実施し、実施例1と同様の方法でIL−6遺伝子の発現量を測定した。比較のため非照射部位及び照射部位(非塗布)の測定を行った。結果を表7及び図−6に示した。また、照射1日、3日および5日にノギスで紅斑の長径と短径を測定しその積を紅斑の相対面積(単位;mm2)とした。結果を表8及び図−7に示した。
【0041】
【表6】

【0042】
【表7】

【0043】
【表8】

【産業上の利用可能性】
【0044】
本発明によれば、アルニカ抽出物を有効成分とする炎症性メディエータ産生抑制剤は抗炎症作用に加え、メラニン合成抑制作用、向精神作用、運動能力の低下予防作用などに優れ、副作用が少なく、且つ経皮吸収性及び人体への安全性が高く、炎症性メディエータ産生抑制用皮膚外用剤として有用である。
【技術分野】
【0001】
本発明は、炎症性メディエータ産生抑制剤及びそれを含有する皮膚外用剤に関する。詳しくは、本発明は、アルニカ抽出物を有効成分とし、経皮吸収性、安全性等に優れた炎症性メディエータ産生抑制剤及びそれを含有する皮膚外用剤に関する。
【背景技術】
【0002】
皮膚は生体の最外郭に位置し、化学物質や紫外線などの環境因子の刺激を常に受け、生体防御の最前線であるとともに生体防御反応の場となっている。炎症反応は、本来生体を防御するための反応であるが、その反応が過剰に進行した場合、紅斑(赤み)、血管透過性亢進(腫脹)、発熱(ほてり)を主徴とする症状が現れる。
【0003】
いわゆる、日焼けと呼ばれる紫外線を浴びた後に惹起される色素沈着は、表皮に存在するメラノサイトにおけるメラニン色素の合成促進がその本態であるが、このメラニン産生亢進も生体防御反応のひとつと考えられる。
【0004】
しかし、これらの反応が過剰になった場合、特に皮膚ではその反応が身体の浅部で惹起され症状が顕著に発現するために、医療上の問題ばかりでなく、外観への影響といった美容上の問題も含まれる。
【0005】
近年の研究で、炎症反応およびメラニン合成促進反応に、表皮細胞で産生されるIL−6(インターロイキン−6)、IL−1α(インターロイキン−1α)、プロスタグランジン、エンドセリンといった化学物質が深く関与することが明らかになってきている。特に、IL−6が紫外線照射によって表皮細胞から放出されると、皮膚にとどまらずIL−6の血中濃度が上昇し、抑鬱感、集中力の低下、形状認識障害などの全身作用(精神作用)への影響が現れることばかりでなく、例えばトライアスロン選手のランタイムがIL−6の増加に伴って悪化するといった運動能力への影響があることも明らかになった。
【0006】
従来は、炎症に対しては抗炎症作用を有する物質が、色素沈着に対してはメラニン合成を抑制する作用を有する物質が、全身作用については向精神薬的な物質が投与されてきた。また、運動能力の低下に関しては、筋肉増強剤などのドーピング違反となるような物質以外に適用されているものは無い。
【0007】
しかしながら、これまで開発されてきた上記の各有効性を示す物質は優れた効果を有するものの、目的とする作用以外に強い生理作用を併有する、また皮膚での局所投与ではその経皮吸収性の問題から期待した効果が得られない場合がある等の課題があることが知られている。さらに、上記の作用に対して網羅的に効果を発揮するものではないため、各作用に対して個々に対応する必要があった。
【0008】
一方、アルニカ抽出物が抗アレルギー作用や抗炎症作用を有することは知られており、化粧料等の外用剤へ配合して使用することが提案されている(特許文献1〜3)。しかしながら、アルニカ抽出物が特定の炎症性メディエータ産生抑制作用を有することは知られていなかった。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開平9−87189
【特許文献2】特開2006−348035
【特許文献3】特開2007−8847
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、経皮吸収性に優れ、副作用が少なく、且つ安全性の高い炎症性メディエータ産生抑制能及びそれを含有する皮膚外用剤を提供することを課題とする。
【課題を解決するための手段】
【0011】
本発明者らは、アルニカ抽出物が、IL−6、IL−1α、プロスタグランジン、及びエンドセリンといった炎症性メディエータの産生を抑制する作用に優れる、特にIL−6の産生を抑制する作用に優れること、並びにIL−6の産生を抑制することによって運動能力の低下予防効果が期待できること、同時に生体に対しては安全であることを見いだし、本発明を完成した。
【0012】
すなわち、本発明は、以下の(1)〜(2)に示す皮膚外用剤に関する。
(1)アルニカ抽出物を有効成分とする、炎症性メディエータ産生抑制剤。
(2)前記炎症性メディエータがIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるものである、(1)記載の炎症性メディエータ産生抑制剤。
(3)前記炎症性メディエータがIL−6であることを特徴とする、(1)記載の炎症性メディエータ産生抑制剤。
(4)(1)〜(3)のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、炎症性メディエータ産生抑制用皮膚外用剤。
(5)(1)〜(3)のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、運動能力低下予防剤。
【発明の効果】
【0013】
本発明によれば、アルニカ抽出物を有効成分とする炎症性メディエータ産生抑制剤は抗炎症作用に加え、メラニン合成抑制作用、向精神作用、運動能力の低下予防作用などに優れ、副作用が少なく、且つ経皮吸収性及び人体への安全性が高い。よって、炎症性メディエータ産生抑制用皮膚外用剤として有用である。
【図面の簡単な説明】
【0014】
【図1】本発明の実施例1の結果を示すグラフである。
【図2】本発明の実施例2の結果を示すグラフである。
【図3】本発明の実施例3の結果を示すグラフである。
【図4】本発明の実施例4の結果を示すグラフである。
【図5】本発明の実施例5の結果を示すグラフである。
【図6】本発明の実施例6,7,比較例1の結果を示すグラフである。
【図7】本発明の実施例6,7,比較例1の結果を示すグラフである。
【発明を実施するための形態】
【0015】
(1)アルニカ抽出物
本発明に使用されるアルニカはキク科ウサギギク属に属する植物であり、使用する部位は特に限定されず花、根、葉、枝、茎など全草から抽出することができる。
抽出物は、乾燥した植物体を細切し、水、エタノール、プロピレングリコール、1,3−ブチレングリコール等の親水性有機溶剤、又はこれらの混合物に浸漬し、得られた液をろ過して得られる。溶剤の温度及び浸漬時間は特に制限されない。
このようにして得られるアルニカ抽出物の形態は、粉末状、ゲル状、ペースト状などいずれであってもよい。
【0016】
(2)炎症性メディエータ産生抑制剤
上記アルニカ抽出物は、そのまま炎症性メディエータ産生抑制剤として利用することができる。特に、前記炎症性メディエータとしてIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるものに対し、優れた産生抑制作用を有する。さらに、前記炎症性メディエータとしてIL−6に対し、優れた産生抑制作用を有する。そして、IL−6の産生により引き起こされるとされる抑鬱感、集中力の低下、形状認識障害などの全身作用(精神作用)への影響や、IL−6の増加に伴って悪化するとされる運動能力の低下を抑制又は予防する作用が期待される。
【0017】
(3)皮膚外用剤
本発明の炎症性メディエータ産生抑制剤はそのまま、あるいは皮膚外用剤へ配合して使用することができる。
皮膚外用剤中のアルニカ抽出物の配合量は、特に限定されるものではないが、乾燥固形物重量で、総量を基準として0.0001〜10.0重量%が好ましく、更に好ましくは0.0005〜5.0重量%、特に好ましくは0.01〜5重量%である。該配合量が0.0001重量%未満であると、本発明の効果が充分に得られず、一方10.0重量%を超えても、その増量に見合った効果の向上は認められない。
【0018】
本発明の皮膚外用剤は、例えばローション類、乳液類、クリーム類、軟膏類、パック類等の剤型とすることができる。
また、本発明の皮膚外用剤には、上記炎症性メディエータ産生抑制剤に加え、本発明の効果を損なわない範囲で必要に応じて医薬品類、医薬部外品類、化粧品類などの製剤に使用される成分や添加剤、例えば色素(着色剤)、防腐剤、界面活性剤、香料、顔料等を任意成分として適宜配合することができる。
【0019】
そのような任意成分としては、例えば、マカデミアナッツ油、アボガド油、トウモロコシ油、オリーブ油、ナタネ油、ゴマ油、ヒマシ油、サフラワー油、綿実油、ホホバ油、ヤシ油、パーム油、液状ラノリン、硬化ヤシ油、硬化油、モクロウ、硬化ヒマシ油、ミツロウ、キャンデリラロウ、カルナウバロウ、イボタロウ、ラノリン、還元ラノリン、硬質ラノリン、ホホバロウ、鉱物油(ミネラルオイル)等のオイル、ワックス類、流動パラフィン、スクワラン、プリスタン、オゾケライト、パラフィン、セレシン、ワセリン、マイクロクリスタリンワックス等の炭化水素類;
【0020】
イソオクタン酸セチル、ミリスチン酸イソプロピル、イソステアリン酸ヘキシルデシル、アジピン酸ジイソプロピル、セバチン酸ジ−2−エチルヘキシル、乳酸セチル、リンゴ酸ジイソステアリル、ジ−2−エチルヘキサン酸エチレングリコール、ジカプリン酸ネオペンチルグリコール、ジ−2−ヘプチルウンデカン酸グリセリン、トリ−2−エチルヘキサン酸グリセリン、トリ−2−エチルヘキサン酸トリメチロールプロパン、トリイソステアリン酸トリメチロールプロパン、テトラ−2−エチルヘキサン酸ペンタンエリトリット、水添ココグリセリル、ステアリン酸ポリグリセリル、パラオキシ安息香酸メチル(メチルパラベン)等のエステル類;
【0021】
ジメチルポリシロキサン、メチルフェニルポリシロキサン、ジフェニルポリシロキサン等の鎖状ポリシロキサン、オクタメチルシクロテトラシロキサン、デカメチルシクロペンタシロキサン、ドデカメチルシクロヘキサンシロキサン等の環状ポリシロキサン、アミノ変性ポリシロキサン、ポリエーテル変性ポリシロキサン、アルキル変性ポリシロキサン、フッ素変性ポリシロキサン等の変性ポリシロキサン等のシリコーン油等の油剤類;
【0022】
脂肪酸セッケン(ラウリン酸ナトリウム、パルミチン酸ナトリウム等)、ラウリル硫酸カリウム、アルキル硫酸トリエタノールアミンエーテル等のアニオン界面活性剤類、塩化ステアリルトリメチルアンモニウム、塩化ベンザルコニウム、ラウリルアミンオキサイド等のカチオン界面活性剤類、イミダゾリン系両性界面活性剤(2−ココイル−2−イミダゾリニウムヒドロキサイド−1−カルボキシエチロキシ2ナトリウム塩等)、ベタイン系界面活性剤(アルキルベタイン、アミドベタイン、スルホベタイン等)、アシルメチルタウリン等の両性界面活性剤類、ソルビタン脂肪酸エステル類(ソルビタンモノステアレート、セスキオレイン酸ソルビタン等)、グリセリン脂肪酸類(モノステアリン酸グリセリン等)、プロピレングリコール脂肪酸エステル類(モノステアリン酸プロピレングリコール等)、硬化ヒマシ油誘導体、グリセリンアルキルエーテル、ショ糖脂肪酸エステル、アルキルグルコシド等の非イオン界面活性剤類等の界面活性剤類;
【0023】
ポリエチレングリコール、1,3−ブチレングリコール、グリセリン等の多価アルコール類;
ステアリン酸等の高級脂肪酸類;
ピロリドンカルボン酸ナトリウム、乳酸、乳酸ナトリウム等の保湿成分類;
【0024】
グアガム、クインスシード、カラギーナン、ガラクタン、アラビアガム、ペクチン、マンナン、デンプン、カードラン、メチルセルロース、ヒドロキシエチルセルロース、カルボキシメチルセルロース、メチルヒドロキシプロピルセルロース、コンドロイチン硫酸、デルマタン硫酸、グリコーゲン、ヘパラン硫酸、ヒアルロン酸ナトリウム、トラガントガム、ケラタン硫酸、コンドロイチン、ムコイチン硫酸、ヒドロキシエチルグアガム、カルボキシメチルグアガム、デキストラン、ケラト硫酸、ローカストビーンガム、サクシノグルカン、カロニン酸、キチン、キトサン、カルボキシメチルキチン、寒天、ポリビニルアルコール、ポリビニルピロリドン、カルボキシビニルポリマー(カルボマー)、ポリアクリル酸ナトリウム等のポリアクリル酸及び/又はその塩、ポリエチレングリコール、ベントナイト、微粒子セルロースゲル等の増粘剤;
【0025】
表面を処理されていても良い、マイカ、タルク、カオリン、合成雲母、炭酸カルシウム、炭酸マグネシウム、無水ケイ酸(シリカ)、酸化アルミニウム、硫酸バリウム等の粉体類; 表面を処理されていても良い、ベンガラ、黄酸化鉄、黒酸化鉄、酸化コバルト、群青、紺青、酸化チタン、酸化亜鉛の無機顔料類;表面を処理されていても良い、雲母チタン、魚燐箔、オキシ塩化ビスマス等のパール剤類;レーキ化されていても良い赤色202号、赤色228号、赤色226号、黄色4号、青色404号、黄色5号、赤色505号、赤色230号、赤色223号、橙色201号、赤色213号、黄色204号、黄色203号、青色1号、緑色201号、紫色201号、赤色204号等の有機色素類;ポリエチレン末、ポリメタクリル酸メチル、ナイロン粉末、オルガノポリシロキサンエラストマー等の有機粉体類;
【0026】
パラアミノ安息香酸系紫外線吸収剤、アントラニル酸系紫外線吸収剤、サリチル酸系紫外線吸収剤、桂皮酸系紫外線吸収剤、ベンゾフェノン系紫外線吸収剤、糖系紫外線吸収剤、2−(2’−ヒドロキシ−5’−t−オクチルフェニル)ベンゾトリアゾール、4−メトキシ−4’−t−ブチルジベンゾイルメタン等の紫外線吸収剤類;
【0027】
エタノール、イソプロパノール等の低級アルコール類;
ビタミンA又はその誘導体、ビタミンB6塩酸塩、ビタミンB6トリパルミテート、ビタミンB6ジオクタノエート、ビタミンB2又はその誘導体、ビタミンB12、ビタミンB15又はその誘導体等のビタミンB類、α−トコフェロール、β−トコフェロール、γ−トコフェロール、ビタミンEアセテート等のビタミンE類、ビタミンD類、ビタミンH、パントテン酸、パンテチン、ピロロキノリンキノン等のビタミン類;などが好ましく例示できる。
【実施例】
【0028】
以下に、本発明を実施例に基づいてさらに詳しく説明する。ただし本発明はこれらの実施例に限定されるものではない。なお、以下の調製例及び実施例中%とあるのは、特に指定がない場合w/w%である。
【0029】
<製造例1>(アルニカ抽出液含有サンプルの製造)
市販アルニカ抽出液(丸善製薬社製;固形分(蒸発残量)=2.4%;溶媒=水:1,3−ブチレングリコール=50:50(重量比))を各試験に使用する細胞培養用培地で希釈して、以下のような0.25%,0.05%および0.01%アルニカ抽出液含有サンプルとした。
・0.25%アルニカ抽出液含有サンプル(アルニカ抽出物濃度;60μg/l)
・0.05%アルニカ抽出液含有サンプル(アルニカ抽出物濃度;12μg/l)
・0.01%アルニカ抽出液含有サンプル(アルニカ抽出物濃度;2.4μg/l)
【0030】
<実施例1>(アルニカのIL−6産生抑制効果)
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル(溶媒;1,3−ブチレングリコール)及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、該上清中のIL−6量(単位;pg/ml)をmouse IL-6 CytoSet kit(Biosourse)を用いて測定した。結果を表1及び図−1に示す。
【0031】
【表1】

【0032】
<実施例2>(アルニカのIL−1α産生抑制効果)
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、該上清中のIL−1α量(単位;pg/ml)をmouse IL-1α ELISA kit(Thermo Scientific)を用いて測定した。結果を表2及び図−2に示す。
【0033】
【表2】

【0034】
<実施例3>(アルニカのプロスタグランジン産生抑制効果)
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、該上清中のプロスタグランジン量(単位;pg/ml)をPGE ELISA kit(Thermo Scientific)を用いて測定した。結果を表3及び図−3に示す。
【0035】
【表3】

【0036】
<実施例4>(アルニカのエンドセリン産生抑制作用)
マウス由来マクロファージ細胞株RAW264.7を60mmディッシュ(Falcon)に5.0×104cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換6時間後、細胞を回収し、常法に従ってRNA抽出、逆転写酵素によるDNA合成およびリアルタイムPCR(使用機器;Real-time PCR Detector Chromo4;Bio Rad社製)
を実施し、エンドセリン遺伝子の発現量を測定した(単位;%)。結果を表4及び図−4に示す。
【0037】
【表4】

【0038】
<実施例5>(アルニカの細胞毒性)
製造例1と同様の方法で0.25%、0.05%及び0.01%アルニカ抽出液含有サンプルを製造した。
マウス由来マクロファージ細胞株RAW264.7を96ウェル培養プレート(Falcon)に5.0×103cells/wellになるように細胞を播種した。培地には10v/v%ウシ胎児血清及び1v/v%非必須アミノ酸溶液を含むMinimum Essential Medium Eagle(Sigma)を使用し、24時間培養した。細胞の状態を確認した後、培地を吸引除去し、0.25%、0.05%及び0.01%アルニカ抽出液含有サンプル及び100ng/mlLPS(リポサッカライド,Sigma)を含有する上記培地に培地を交換した。培地交換24時間後、培養上清を回収し、LDH測定キットで細胞破壊によって放出されたLDH量を、測定した。測定は以下の方法で行った(単位;吸光度(%))。結果を表5及び図−5に示した。
測定用試薬キット:宝酒造社製
測定波長:490nm
測定機器:Microplate Reader SH1000(Corona Electric社製)
【0039】
【表5】

【0040】
<実施例6−7,比較例1>(紫外線照射による紅斑およびIL−6産生に対する作用)
表6に示した皮膚外用剤を調製した。簡潔にはAの油相部の原料とBの水相部の原料をそれぞれ80℃に加熱した後、B相をA相へ混合し、乳化した。その後40℃まで冷却した後、C相を加え、攪拌混合する。その後、室温まで冷却し、皮膚外用剤を得た。
サンプルの塗布は、紫外線照射前3日間(朝・入浴後1日2回)、照射直後、照射日夜、照射後1週間(朝・入浴後1日2回)、サンプルを綿棒にとり適量を照射部位に塗布した。紫外線照射は大腿部内側の非露光部位に直径約8mmで16ヶ所に1.2MEDのUVBを照射した。
紫外線照射6時間後に局所麻酔下表皮層を摘出し、常法に従ってRNA抽出、逆転写酵素によるDNA合成およびリアルタイムPCRを実施し、実施例1と同様の方法でIL−6遺伝子の発現量を測定した。比較のため非照射部位及び照射部位(非塗布)の測定を行った。結果を表7及び図−6に示した。また、照射1日、3日および5日にノギスで紅斑の長径と短径を測定しその積を紅斑の相対面積(単位;mm2)とした。結果を表8及び図−7に示した。
【0041】
【表6】

【0042】
【表7】

【0043】
【表8】

【産業上の利用可能性】
【0044】
本発明によれば、アルニカ抽出物を有効成分とする炎症性メディエータ産生抑制剤は抗炎症作用に加え、メラニン合成抑制作用、向精神作用、運動能力の低下予防作用などに優れ、副作用が少なく、且つ経皮吸収性及び人体への安全性が高く、炎症性メディエータ産生抑制用皮膚外用剤として有用である。
【特許請求の範囲】
【請求項1】
アルニカ抽出物を有効成分とする、炎症性メディエータ産生抑制剤。
【請求項2】
前記炎症性メディエータがIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるものである、請求項1記載の炎症性メディエータ産生抑制剤。
【請求項3】
前記炎症性メディエータがIL−6であることを特徴とする、請求項1記載の炎症性メディエータ産生抑制剤。
【請求項4】
請求項1〜3のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、炎症性メディエータ産生抑制用皮膚外用剤。
【請求項5】
請求項1〜3のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、運動能力低下予防剤。
【請求項1】
アルニカ抽出物を有効成分とする、炎症性メディエータ産生抑制剤。
【請求項2】
前記炎症性メディエータがIL−6、IL−1α、プロスタグランジン、及びエンドセリンからなる群から選択されるものである、請求項1記載の炎症性メディエータ産生抑制剤。
【請求項3】
前記炎症性メディエータがIL−6であることを特徴とする、請求項1記載の炎症性メディエータ産生抑制剤。
【請求項4】
請求項1〜3のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、炎症性メディエータ産生抑制用皮膚外用剤。
【請求項5】
請求項1〜3のいずれかに記載の炎症性メディエータ産生抑制剤を含有することを特徴とする、運動能力低下予防剤。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2011−178705(P2011−178705A)
【公開日】平成23年9月15日(2011.9.15)
【国際特許分類】
【出願番号】特願2010−43563(P2010−43563)
【出願日】平成22年2月26日(2010.2.26)
【出願人】(504401994)株式会社セプテム総研 (11)
【Fターム(参考)】
【公開日】平成23年9月15日(2011.9.15)
【国際特許分類】
【出願日】平成22年2月26日(2010.2.26)
【出願人】(504401994)株式会社セプテム総研 (11)
【Fターム(参考)】
[ Back to top ]

