焼結体及びその製造方法
【課題】優れたリチウムイオン伝導性を備える焼結体及びその製造方法を提供する。
【解決手段】 Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなり、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有する焼結体である。前記焼結体は、Li化合物とLa化合物とZr化合物とを混合した混合原料を一次焼成し、粉末状の複合金属酸化物粉末を得る工程と、該複合金属酸化物粉末に対して、放電プラズマ焼結により二次焼成する工程とにより製造することができる。
【解決手段】 Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなり、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有する焼結体である。前記焼結体は、Li化合物とLa化合物とZr化合物とを混合した混合原料を一次焼成し、粉末状の複合金属酸化物粉末を得る工程と、該複合金属酸化物粉末に対して、放電プラズマ焼結により二次焼成する工程とにより製造することができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、焼結体及びその製造方法に関する。
【背景技術】
【0002】
近年、リチウムイオン二次電池において、リチウムイオンを伝導させるための媒体として、液状の電解液に代えてリチウムイオン伝導性を備える固体電解質が注目されている。
【0003】
前記リチウムイオン伝導性を備える固体電解質は、電解液の漏洩がなく、リチウムデンドライドの成長を抑制することにより、電池内部での短絡を防ぐことができる等の利点がある。
【0004】
前記リチウムイオン伝導性を備える固体電解質として、化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物からなる焼結体が知られている(例えば特許文献1及び2参照)。前記焼結体は、炭酸リチウムと水酸化ランタンと酸化ジルコニウムとを混合して一次焼成し、複合金属酸化物粉末を得た後に、該複合金属酸化物粉末をプレス成形することにより予備成形体を作製し、該予備成形体を坩堝に収容して、1125〜1230℃の範囲の温度で、30〜50時間の範囲の時間、二次焼成することにより製造することができる。前記製造方法により得られた焼結体は、化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物の理論密度(5.116g/cm3)に対して92%の相対密度を備えている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2010−45019号公報
【特許文献2】特開2011−51855号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、従来の製造方法で得られた焼結体は、十分なリチウムイオン伝導性を得ることができないという不都合がある。
【0007】
本発明は、かかる不都合を解消して、優れたリチウムイオン伝導性を備える焼結体及びその製造方法を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明者らは、前記従来の製造方法で得られた焼結体において、十分なリチウムイオン伝導性を得ることができない理由について鋭意検討した結果、100nm以上5μm以下の範囲の最大長を有する空隙が存在することにより、抵抗が大きくなることを知見した。
【0009】
前記焼結体において、前記空隙としては、前記予備成形体を構成する前記複合金属酸化物粉末の粒子間に存在した空隙が、二次焼成を行った後も、そのまま或いは圧縮された状態で残留したものと、二次焼成の際に、該予備成形体に含有されるリチウムが揮発し、気泡として生成したものとがある。
【0010】
前者の空隙は、前記二次焼成において、前記複合金属酸化物粉末の粒子間の焼結速度が遅いことにより、該粒子間に存在した空隙が消滅することなく、そのまま或いは圧縮された状態で結晶粒界に残留したものと考えられる。一方、後者の空隙は、緻密な焼結体を得ようとして、前記二次焼成において、前記予備成形体が高温下で長時間熱処理されることにより、該予備成形体に含有されるリチウムが揮発し、結晶粒内に気泡として生成したものであると考えられる。
【0011】
本発明は、前記知見に基づいてなされたものであり、前記目的を達成するために、Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなる焼結体であって、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有することを特徴とする。
【0012】
本発明の焼結体は、前記範囲の相対密度を備えるとともに、空隙が前記範囲の最大長を有することにより、優れたリチウムイオン伝導性を得ることができる。
【0013】
前記相対密度が94%未満の焼結体は、十分なリチウムイオン伝導性を得ることができない。前記相対密度が98%を超える焼結体は、製造が困難である。また、前記空隙が1nm未満の最大長を有する焼結体は、製造が困難である。前記空隙が100nm以上の最大長を有する焼結体は、十分なリチウムイオン伝導性を得ることができない。
【0014】
本発明の焼結体は、好ましくは基本組成が化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物からなる。
【0015】
また、本発明の焼結体は、前記Laの一部をSr,Baからなる群から選択される1種の金属に置換した焼結体であってもよく、前記Zrの一部を、Nb,Ta,Sb,Biからなる群から選択される1種の金属に置換した焼結体であってもよい。
【0016】
本発明の焼結体は、Li化合物とLa化合物とZr化合物とを混合した混合原料を一次焼成し、粉末状の複合金属酸化物粉末を得る工程と、該複合金属酸化物粉末に対して、放電プラズマ焼結により二次焼成する工程とにより、有利に製造することができる。
【0017】
本発明の製造方法では、まず、Li化合物とLa化合物とZr化合物とを混合して混合原料を得る。このとき、前記化学式の前記La又は前記Zrの一部を他の金属で置換した焼結体を得ようとする場合には、Li化合物とLa化合物とZr化合物とに加えて該他の金属を含有する化合物とを混合して混合原料を得る。
【0018】
次に、得られた混合原料を一次焼成することにより、Li,La及びZrを含有し、ガーネット型複合金属酸化物からなる粉末を得る。
【0019】
次に、得られた複合金属酸化物粉末に対して、放電プラズマ焼結による二次焼成により、前記焼結体を得る。前記放電プラズマ焼結(SPS:Spark Plasma Sintering)は、前記複合金属酸化物粉末に対して、加圧した状態で電流をパルス印加することにより、該複合金属酸化物粉末を焼成温度にまで加熱して焼成させるものである。
【0020】
本発明の製造方法では、前記放電プラズマ焼結による二次焼成により、前記複合金属酸化物粉末を自己発熱させて、焼成温度まで急速に昇温することができるとともに、焼成温度での焼成時間を短縮することができる。したがって、本発明の製造方法によれば、焼成温度までの昇温時間と、焼成温度での保持時間とを短縮することができる結果、前記複合金属酸化物粉末に含有されるリチウムの揮発を抑制することができる。
【0021】
さらに、本発明の製造方法では、前記放電プラズマ焼結による二次焼成において、前記複合金属酸化物粉末に対して、圧力を付与した状態で電流をパルス印加する。この結果、前記電流のパルス印加により、前記複合金属酸化物粉末の粒子間の焼結が促進されるとともに、前記圧力により、前記複合金属酸化物粉末の粒子間に存在した空隙を押しつぶすことができ、得られた焼結体の結晶粒界に生じる空隙の数を少なくするか、或いは、該空隙の最大長を小さくすることができる。さらに、前記複合金属酸化物粉末に含有されるリチウムが揮発して気泡が生成した場合であっても、該気泡を前記圧力により押しつぶし、該気泡による前記空隙の数を少なくするか、或いは、前記空隙の最大長を小さくすることができる。
【0022】
以上により、本発明の製造方法によれば、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有し、優れたリチウムイオン伝導性を備える焼結体を得ることができる。
【0023】
また、本発明の製造方法において、前記混合原料を一次焼成する際に、Al2O3,Al(OH)3,SiO2,ケイ酸の群から選択される1種以上の化合物を焼結助剤として用いることにより、さらに緻密な焼結体を得ることができる。
【図面の簡単な説明】
【0024】
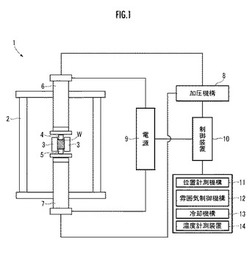
【図1】本実施形態の製造方法に用いる放電プラズマ焼結装置を示すシステム構成図。
【図2】実施例1で得られた試料の外観を示す画像。
【図3】実施例1で得られた試料の破断面を示すSEM画像。
【図4】実施例2で得られた試料の破断面を示すSEM画像。
【図5】実施例3で得られた試料の破断面を示すSEM画像。
【図6】比較例1で得られた試料の外観を示す画像。
【図7】比較例1で得られた試料の破断面を示すSEM画像。
【図8】比較例2で得られた試料の破断面を示すSEM画像。
【図9】実施例4で得られた試料の破断面を示すSEM画像。
【発明を実施するための形態】
【0025】
次に、添付の図面を参照しながら本発明の実施の形態についてさらに詳しく説明する。
【0026】
本実施形態の焼結体は、Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなる焼結体であり、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有するものである。
【0027】
本実施形態の焼結体は、基本組成が化学式Li7La3Zr2O12で表わされる焼結体であり、前記Laの一部をSr,Baからなる群から選択される1種の金属に置換してもよく、前記Zrの一部を、Nb,Ta,Sb,Biからなる群から選択される1種の金属に置換してもよい。
【0028】
本実施形態の焼結体は、前記範囲の相対密度を備えるとともに、空隙が前記範囲の最大長を有することにより、優れたリチウムイオン伝導性を得ることができる。
【0029】
本実施形態の焼結体は、例えば次の方法により製造することができる。まず、Li化合物とLa化合物とZr化合物とを、ボールミル、ミキサー等の粉砕・混合機器を用いて粉砕、混合し、得られた混合原料を、大気雰囲気下、850〜950℃の範囲の温度で、5〜7時間の範囲の時間、仮焼する。このとき、前記化学式の前記La又は前記Zrの一部を他の金属で置換した焼結体を得ようとする場合には、Li化合物とLa化合物とZr化合物とに加えて該他の金属を含有する化合物とを混合して混合原料を得る。
【0030】
また、このとき、前記混合原料における混合比の精度を向上するために、Li化合物、La化合物、Zr化合物のそれぞれを別々に脱水等の前処理を行った後に混合することにしてもよく、或いは前処理せずに混合することにしてもよい。
【0031】
前記Li化合物として、例えば、LiOH、水酸化リチウム水和物、Li2CO3、LiNO3、CH3COOLi等を挙げることができる。前記La化合物として、例えば、La2CO3、La(OH)3、La2(CO3)3、La(NO3)3、La(CHCOO)3等を挙げることができる。前記Zr化合物として、例えば、ZrO2、ZrO(NO3)2、ZrO(CHCOO)2、Zr(OH)2CO3・ZrO2を挙げることができる。
【0032】
また、前記化学式の前記Laの一部を置換する金属、又は前記Zrの一部を置換する金属の化合物として、例えば、酸化物、水酸化物,炭酸塩、硝酸塩等を挙げることができる。
【0033】
次に、仮焼した原料を、酸素を含有する雰囲気下、例えば大気雰囲気下で、1000〜1100℃の範囲の温度で、5〜7時間の範囲の時間、一次焼成することにより、Li,La及びZrを含有し、ガーネット型複合金属酸化物からなる粉末を得る。このとき、得られた複合金属酸化物粉末が1〜50μmの範囲の粒径を備えるように、該複合金属酸化物粉末をボールミル、ミキサー等の粉砕機器を用いて粉砕することにしてもよい。
【0034】
次に、得られた前記複合金属酸化物粉末を、放電プラズマ焼結(SPS:Spark Plasma Sintering)により二次焼成する。
【0035】
ここで、前記放電プラズマ焼結を行う放電プラズマ焼結装置について説明する。図1に示す放電プラズマ焼結装置1は、水冷式真空チャンバー2内に、焼結ダイ3と、互いに対向する一対のパンチ4,5と、パンチ4,5を通して電流をパルス印加する電極6,7とを備えており、粉末状の材料を焼結ダイ3に装入し、該材料をパンチ4,5で加圧した状態で、電流をパルス印加することにより、該材料を加熱し、焼成することができる。
【0036】
焼結ダイ3は、電気伝導性材料又は電気絶縁性材料からなるものを使用することができる。前記電気伝導性材料としては、黒鉛、グラッシーカーボン(登録商標)等の炭素材料、モリブデン、タングステン等の高融点金属等が挙げられる。前記電気絶縁材料としては、アルミナ、ジルコニア等が挙げられる。
【0037】
パンチ4,5は、電気伝導性材料からなり、それぞれ電極6,7に電気的かつ機械的に接続され、加圧機構8により駆動される。電極6,7は、電源9に電気的に接続されている。そして、加圧機構8及び電源9は、制御装置10により制御される。
【0038】
制御装置10は、パンチ4,5の位置を計測する位置計測機構11と、真空チャンバー2内の雰囲気を制御する雰囲気制御機構12と、真空チャンバー2を冷却する冷却機構13と、焼結ダイ3に取り付けられ、焼結ダイ3に装入された材料の温度を計測する熱電対(図示せず)に接続された温度計測機構14とを備えている。
【0039】
雰囲気制御機構12は、真空チャンバー2内の雰囲気を、真空雰囲気、アルゴン雰囲気、又は大気雰囲気とすることができる。真空チャンバー2内の雰囲気は、焼成の際には、焼結ダイ3の酸化を抑制するために、真空雰囲気又はアルゴン雰囲気とすることが好ましい。
【0040】
本実施形態では、放電プラズマ焼結装置1において、まず、前記複合金属酸化物粉末を焼結ダイ3に装入する(複合金属酸化物粉末W)。真空チャンバー2内を10〜100Paの範囲の圧力の真空雰囲気下にする。次に、焼結ダイ3に装入された複合金属酸化物粉末Wを、パンチ4,5で20〜50MPaの範囲の圧力で加圧した状態で、500〜20000Aの範囲の直流電流を200〜400Hzの範囲の周期でパルス印加する。このとき、前記熱電対により計測される温度が800℃以下では10〜100℃/分の範囲の昇温速度で昇温させ、800℃に達した以降は1〜20℃/分の範囲の昇温速度で昇温させる。そして、焼結ダイ3に装入された複合金属酸化物粉末Wを、前記範囲の圧力で加圧した状態で、1100〜1250℃の範囲の焼成温度で5〜30分の範囲の時間保持することにより、二次焼成を行い、焼結体を得る。
【0041】
次に、前記パルス印加及び前記加圧を停止し、冷却機構13により真空チャンバー2を冷却するか、又は自然放冷することにより、得られた焼結体を室温まで冷却することにより、本実施形態の焼結体を得ることができる。
【0042】
本実施形態の製造方法では、前記二次焼成において、前記放電プラズマ焼結を行うことにより、前記複合金属酸化物粉末を自己発熱させて、焼成温度まで急速に昇温することができるとともに、焼成温度での焼成時間を短縮することができる。したがって、本実施形態の製造方法によれば、焼成温度までの昇温時間と、焼成温度での保持時間とを短縮することができる結果、前記複合金属酸化物粉末に含有されるリチウムの揮発を抑制することができる。
【0043】
さらに、本実施形態の製造方法では、前記放電プラズマ焼結による二次焼成において、前記複合金属酸化物粉末に対して、圧力を付与した状態で電流をパルス印加する。この結果、前記電流のパルス印加により、前記複合金属酸化物粉末の粒子間の焼結が促進されるとともに、前記圧力により、該粒子間に存在した空隙を押しつぶすことができ、得られた焼結体の結晶粒界に生じる空隙の数を少なくするか、或いは、該空隙の最大長を小さくすることができる。さらに、前記複合金属酸化物粉末に含有されるリチウムが揮発して気泡が生成した場合であっても、該気泡を前記圧力により押しつぶし、該気泡による前記空隙の数を少なくするか、或いは、前記空隙の最大長を小さくすることができる。
【0044】
また、本実施形態の製造方法において、前記混合原料を一次焼成する際に、Al2O3,Al(OH)3等のAl含有化合物や、SiO2,ケイ酸等のSi含有化合物をを焼結助剤として用いることにより、さらに緻密な焼結体を得ることができる。
【0045】
次に、本発明の実施例を示す。
【0046】
〔実施例1〕
本実施例では、まず、水酸化リチウム一水和物(関東化学株式会社製)を、圧力500Paの真空雰囲気下、350℃の温度で6時間加熱し、脱水処理することにより、水酸化リチウム無水物を得た。また、酸化ランタン(関東化学株式会社製)を、大気雰囲気下、950℃の温度で24時間加熱することにより、脱水及び脱炭酸処理した。
【0047】
次に、得られた水酸化リチウム無水物と、脱水及び脱炭酸された酸化ランタンと、酸化ジルコニウム(関東化学株式会社製)とを、Li:La:Zr=7.7:3:2のモル比となるように調製して、遊星型ボールミル(商品名:premium line P-7、フリッチュジャパン株式会社製)を用いて、360rpmの回転数で3時間粉砕混合し、混合原料を得た。
【0048】
次に、前記混合原料をアルミナ製坩堝に収容し、大気雰囲気下、1050℃の温度で6時間保持して、一次焼成することにより、Li,La及びZrを含有し、ガーネット型複合金属酸化物からなる粉末を得た。
【0049】
前記一次焼成で得られた複合金属酸化物粉末について、X線回折装置(商品名:D8 ADVANCE、Bruker AXS社製)を用いて、X線回折測定を行ったところ、化学式Li7+xLa3Zr2O12+x/2(x=0〜0.3)で表わされ、正方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0050】
次に、得られた複合金属酸化物粉末について、放電プラズマ焼結装置1(商品名SPS−3.20S、SPSシンテックス株式会社製)を用いて、放電プラズマ焼結(SPS:Spark Plasma Sintering)により二次焼成した。まず、得られた複合金属酸化物粉末10gを、内径が20mmの黒鉛製焼結ダイ3に装入し(複合金属酸化物粉末W)、真空チャンバー2内を圧力20Paの真空雰囲気にした。次に、焼結ダイ3に装入された複合金属酸化物粉末Wを、パンチ4,5で20MPaの圧力で加圧した状態で、900〜1000Aの範囲の直流電流をパルス印加することにより、100℃/分の昇温速度で昇温させた。そして、800℃の温度に達した後、焼結ダイ3に装入された複合金属酸化物粉末Wを、前記加圧を継続した状態で、900〜1050Aの範囲の直流電流をパルス印加することにより、5℃/分の昇温速度で昇温させた後、1150℃の温度で10分間保持することにより、二次焼成を行い、焼結体を得た。
【0051】
前記パルス印加は、いずれも、300Hzの周期で、12回連続でパルス印加し2回分の時間休止することを1サイクルとして、繰り返し行った。
【0052】
次に、前記パルス印加及び前記加圧を停止し、自然放冷して、得られた焼結体を室温まで冷却し、本実施例の焼結体を得た。
【0053】
次に、本実施例で得られた焼結体を、ダイヤモンドカッタにて、700〜800μmの範囲の厚さに切断し、シリコンカーバイド製の耐水ペーパにて表面を研磨することにより、厚さ500μmの円盤状試料を作製した。
【0054】
図2に、本実施例で得られた試料の外観を示す画像を示す。図2から、本実施例で得られた試料は、透明性を備えることから、光を透過する性質を備えていることが明らかである。このことから、本実施例で得られた試料は、光を散乱させるような結晶粒界及び空隙が非常に少なく、高度に緻密化されているものと考えられる。
【0055】
次に、本実施例で得られた試料について、乾燥重量及び体積を測定することにより、実測密度を算出した。そして、得られた実測密度を基に、化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物の理論密度(5.116g/cm3)に対する相対密度を算出したところ、94%であった。結果を表1に示す。
【0056】
次に、本実施例で得られた試料について、X線回折装置(商品名:D8 ADVANCE、Bruker AXS社製)を用いて、X線回折測定を行ったところ、化学式Li7La3Zr2O12で表わされ、正方晶と立方晶との混晶であるガーネット型構造からなる複合金属酸化物であることが確認できた。
【0057】
次に、本実施例で得られた試料について、次のようにして、リチウムイオン伝導率を求めた。まず、本実施例で得られた試料の両面に、スパッタリング装置(商品名:JFC‐1600 オートファインコータ、日本電子株式会社製)を用いて、Auを300秒間スパッタリングして、該試料の両面に薄膜状電極を作製した。次に、接触抵抗を低減するために、前記薄膜状電極の表面にCuメッシュを貼付した後に、該電極を有する試料を2極セルに装着した。そして、前記2極セルについて、インピーダンス測定器(商品名:1287型、Solartron社製)を用いて、周波数を0.1Hz〜1MHzの範囲、電圧振幅を20mVとしたときの交流抵抗値を測定し、測定値からリチウムイオン電導率を算出したところ、1.0×10−4S/cmであった。結果を表1に示す。
【0058】
次に、本実施例で得られた試料について、メノウ製乳棒を用いて圧砕し、得られた破断面を走査型電子顕微鏡(SEM)にて観察した。得られた画像を図3に示す。図3から、本実施例の試料は、最大長が100nmを超える空隙は存在せず、高度に緻密化されていることが明らかである。
【0059】
〔実施例2〕
本実施例では、一次焼成により得られた複合金属酸化物粉末を、1170℃の温度で10分間保持して、放電プラズマ焼結による二次焼成を行った以外は、実施例1と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0060】
次に、本実施例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、95%であった。結果を表1に示す。
【0061】
次に、本実施例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0062】
次に、本実施例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、1.5×10−4S/cmであった。結果を表1に示す。
【0063】
次に、本実施例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図4に示す。図4から、本実施例の試料は、最大長が100nmを超える空隙は存在せず、高度に緻密化されていることが明らかである。
【0064】
〔実施例3〕
本実施例では、一次焼成により得られた複合金属酸化物粉末を、1200℃の温度で10分間保持して、放電プラズマ焼結による二次焼成を行った以外は、実施例1と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0065】
次に、本実施例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、97%であった。結果を表1に示す。
【0066】
次に、本実施例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0067】
次に、本実施例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、1.3×10−4S/cmであった。結果を表1に示す。
【0068】
次に、本実施例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図5に示す。図5から、本実施例の試料は、最大長が100nmを超える空隙は存在せず、高度に緻密化されていることが明らかである。
【0069】
〔比較例1〕
本比較例では、実施例1と全く同一にして一次焼成を行い、複合金属酸化物粉末を得た。
【0070】
次に、得られた複合金属酸化物粉末について、次のようにして、二次焼成を行った。まず、得られた複合金属酸化物粉末100gのうち10gを、ハンドプレス機の内径20mmのダイに装入し、255MPaの圧力で加圧することにより、予備成形体を作製した。
【0071】
次に、残りの複合金属酸化物粉末90gをアルミナ製坩堝に収容するとともに、該複合金属酸化物粉末に得られた予備成形体を埋入させた。
【0072】
次に、アルミナ製坩堝に収容された複合金属酸化物粉末を、大気雰囲気下、5℃/分の昇温速度で昇温させ、600℃の温度に達した後に1℃/分の昇温速度で昇温させ、1170℃の温度で12時間保持することにより、二次焼成を行い、焼結体を得た。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0073】
図6に、本比較例で得られた試料の外観を示す画像を示す。図6から、本比較例で得られた試料は、白色を呈しており、光を透過する性質を備えていないことが明らかである。このことから、本比較例で得られた試料は、焼結体の結晶粒界に多数の空隙が存在し、緻密化されていないものと考えられる。
【0074】
次に、本比較例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、79%であった。結果を表1に示す。
【0075】
次に、本実施例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、正方晶と立方晶の混晶であるガーネット型構造からなる複合金属酸化物であることが確認できた。
【0076】
次に、本比較例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、1.2×10−5S/cmであった。結果を表1に示す。
【0077】
次に、本比較例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図7に示す。図7から、本比較例の試料は、焼結が不十分で、最大長が100nmを超える空隙が多数存在し、緻密でないことが明らかである。
【0078】
〔比較例2〕
本比較例では、一次焼成により得られた複合金属酸化物粉末を、1170℃の温度で30時間保持して、二次焼成を行った以外は、比較例1と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0079】
次に、本比較例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、90%であった。結果を表1に示す。
【0080】
次に、本比較例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0081】
次に、本比較例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、7.4×10−5S/cmであった。結果を表1に示す。
【0082】
次に、本比較例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図8に示す。図8から、本比較例の試料は、結晶粒界に最大長が100nmを超える空隙は存在しないものの、長時間の焼結に伴ってLiが揮発したことにより生成したとみられる気泡状の空隙が結晶粒内に存在し、緻密でないことが明らかである。
【0083】
【表1】

【0084】
表1から、放電プラズマ焼結による二次焼成を行った実施例1〜3の試料は、放電プラズマ焼結を行っていない比較例1,2の試料と比較して、相対密度が大きく、緻密であることが明らかである。また、実施例1〜3の試料は、比較例1,2の試料と比較して、優れたイオン伝導性を備えることが明らかである。
【0085】
〔実施例4〕
本実施例では、Li化合物とLa化合物とZr化合物との混合原料に、焼結助剤として、二酸化ケイ素と水酸化アルミニウムと添加した以外は、実施例2と全く同一にして、一次焼成及び放電プラズマ焼結による二次焼成を行った。二酸化ケイ素及び水酸化アルミニウムは、生成されるLi7La3Zr2O121molに対して、Si及びAlがそれぞれ0.1mol%となるように添加した。
【0086】
次に、本実施例で得られた試料について、実施例2と全く同一にして、相対密度を算出したところ、98%であった。結果を表2に示す。
【0087】
次に、本実施例で得られた試料について、実施例2と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0088】
次に、本実施例で得られた試料について、実施例2と全く同一にして、リチウムイオン伝導率を求めたところ、1.8×10−4S/cmであった。結果を表2に示す。
【0089】
次に、本実施例で得られた試料について、実施例2と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図9に示す。図9から、本実施例の試料は、図3の実施例1の試料のSEM画像で観察された結晶粒界とみられる線が消失しており、実施例1と比較して、さらに緻密化されていることが明らかである。
【0090】
〔実施例5〕
本実施例では、一次焼成により得られた粉末状の複合金属酸化物粉末を、1170℃の温度で20分間保持して、放電プラズマ焼結による二次焼成を行った以外は、実施例4と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例2と全く同一にして、試料を作製した。
【0091】
次に、本実施例で得られた試料について、実施例2と全く同一にして、相対密度を算出したところ、96%であった。結果を表2に示す。
【0092】
次に、本実施例で得られた試料について、実施例2と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0093】
次に、本実施例で得られた試料について、実施例2と全く同一にして、リチウムイオン伝導率を求めたところ、2.4×10−4S/cmであった。結果を表2に示す。
【0094】
【表2】

【0095】
表2から、焼結助剤を用いて一次焼成を行った実施例4の試料は、焼結助剤を用いずに一次焼成を行った実施例2の試料と比較して、さらに相対密度が大きく、より優れたイオン伝導性を備えることが明らかである。
【0096】
また、表2から、焼結助剤を用いて一次焼成を行った後、1170℃の温度で20分間二次焼成を行った実施例5の試料は、焼結助剤を用いて一次焼成を行った後、1170℃の温度で10分間二次焼成を行った実施例4の試料と比較して、相対密度が僅かに小さいものの、さらに優れたイオン伝導性を備えることが明らかである。
【技術分野】
【0001】
本発明は、焼結体及びその製造方法に関する。
【背景技術】
【0002】
近年、リチウムイオン二次電池において、リチウムイオンを伝導させるための媒体として、液状の電解液に代えてリチウムイオン伝導性を備える固体電解質が注目されている。
【0003】
前記リチウムイオン伝導性を備える固体電解質は、電解液の漏洩がなく、リチウムデンドライドの成長を抑制することにより、電池内部での短絡を防ぐことができる等の利点がある。
【0004】
前記リチウムイオン伝導性を備える固体電解質として、化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物からなる焼結体が知られている(例えば特許文献1及び2参照)。前記焼結体は、炭酸リチウムと水酸化ランタンと酸化ジルコニウムとを混合して一次焼成し、複合金属酸化物粉末を得た後に、該複合金属酸化物粉末をプレス成形することにより予備成形体を作製し、該予備成形体を坩堝に収容して、1125〜1230℃の範囲の温度で、30〜50時間の範囲の時間、二次焼成することにより製造することができる。前記製造方法により得られた焼結体は、化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物の理論密度(5.116g/cm3)に対して92%の相対密度を備えている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2010−45019号公報
【特許文献2】特開2011−51855号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、従来の製造方法で得られた焼結体は、十分なリチウムイオン伝導性を得ることができないという不都合がある。
【0007】
本発明は、かかる不都合を解消して、優れたリチウムイオン伝導性を備える焼結体及びその製造方法を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明者らは、前記従来の製造方法で得られた焼結体において、十分なリチウムイオン伝導性を得ることができない理由について鋭意検討した結果、100nm以上5μm以下の範囲の最大長を有する空隙が存在することにより、抵抗が大きくなることを知見した。
【0009】
前記焼結体において、前記空隙としては、前記予備成形体を構成する前記複合金属酸化物粉末の粒子間に存在した空隙が、二次焼成を行った後も、そのまま或いは圧縮された状態で残留したものと、二次焼成の際に、該予備成形体に含有されるリチウムが揮発し、気泡として生成したものとがある。
【0010】
前者の空隙は、前記二次焼成において、前記複合金属酸化物粉末の粒子間の焼結速度が遅いことにより、該粒子間に存在した空隙が消滅することなく、そのまま或いは圧縮された状態で結晶粒界に残留したものと考えられる。一方、後者の空隙は、緻密な焼結体を得ようとして、前記二次焼成において、前記予備成形体が高温下で長時間熱処理されることにより、該予備成形体に含有されるリチウムが揮発し、結晶粒内に気泡として生成したものであると考えられる。
【0011】
本発明は、前記知見に基づいてなされたものであり、前記目的を達成するために、Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなる焼結体であって、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有することを特徴とする。
【0012】
本発明の焼結体は、前記範囲の相対密度を備えるとともに、空隙が前記範囲の最大長を有することにより、優れたリチウムイオン伝導性を得ることができる。
【0013】
前記相対密度が94%未満の焼結体は、十分なリチウムイオン伝導性を得ることができない。前記相対密度が98%を超える焼結体は、製造が困難である。また、前記空隙が1nm未満の最大長を有する焼結体は、製造が困難である。前記空隙が100nm以上の最大長を有する焼結体は、十分なリチウムイオン伝導性を得ることができない。
【0014】
本発明の焼結体は、好ましくは基本組成が化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物からなる。
【0015】
また、本発明の焼結体は、前記Laの一部をSr,Baからなる群から選択される1種の金属に置換した焼結体であってもよく、前記Zrの一部を、Nb,Ta,Sb,Biからなる群から選択される1種の金属に置換した焼結体であってもよい。
【0016】
本発明の焼結体は、Li化合物とLa化合物とZr化合物とを混合した混合原料を一次焼成し、粉末状の複合金属酸化物粉末を得る工程と、該複合金属酸化物粉末に対して、放電プラズマ焼結により二次焼成する工程とにより、有利に製造することができる。
【0017】
本発明の製造方法では、まず、Li化合物とLa化合物とZr化合物とを混合して混合原料を得る。このとき、前記化学式の前記La又は前記Zrの一部を他の金属で置換した焼結体を得ようとする場合には、Li化合物とLa化合物とZr化合物とに加えて該他の金属を含有する化合物とを混合して混合原料を得る。
【0018】
次に、得られた混合原料を一次焼成することにより、Li,La及びZrを含有し、ガーネット型複合金属酸化物からなる粉末を得る。
【0019】
次に、得られた複合金属酸化物粉末に対して、放電プラズマ焼結による二次焼成により、前記焼結体を得る。前記放電プラズマ焼結(SPS:Spark Plasma Sintering)は、前記複合金属酸化物粉末に対して、加圧した状態で電流をパルス印加することにより、該複合金属酸化物粉末を焼成温度にまで加熱して焼成させるものである。
【0020】
本発明の製造方法では、前記放電プラズマ焼結による二次焼成により、前記複合金属酸化物粉末を自己発熱させて、焼成温度まで急速に昇温することができるとともに、焼成温度での焼成時間を短縮することができる。したがって、本発明の製造方法によれば、焼成温度までの昇温時間と、焼成温度での保持時間とを短縮することができる結果、前記複合金属酸化物粉末に含有されるリチウムの揮発を抑制することができる。
【0021】
さらに、本発明の製造方法では、前記放電プラズマ焼結による二次焼成において、前記複合金属酸化物粉末に対して、圧力を付与した状態で電流をパルス印加する。この結果、前記電流のパルス印加により、前記複合金属酸化物粉末の粒子間の焼結が促進されるとともに、前記圧力により、前記複合金属酸化物粉末の粒子間に存在した空隙を押しつぶすことができ、得られた焼結体の結晶粒界に生じる空隙の数を少なくするか、或いは、該空隙の最大長を小さくすることができる。さらに、前記複合金属酸化物粉末に含有されるリチウムが揮発して気泡が生成した場合であっても、該気泡を前記圧力により押しつぶし、該気泡による前記空隙の数を少なくするか、或いは、前記空隙の最大長を小さくすることができる。
【0022】
以上により、本発明の製造方法によれば、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有し、優れたリチウムイオン伝導性を備える焼結体を得ることができる。
【0023】
また、本発明の製造方法において、前記混合原料を一次焼成する際に、Al2O3,Al(OH)3,SiO2,ケイ酸の群から選択される1種以上の化合物を焼結助剤として用いることにより、さらに緻密な焼結体を得ることができる。
【図面の簡単な説明】
【0024】
【図1】本実施形態の製造方法に用いる放電プラズマ焼結装置を示すシステム構成図。
【図2】実施例1で得られた試料の外観を示す画像。
【図3】実施例1で得られた試料の破断面を示すSEM画像。
【図4】実施例2で得られた試料の破断面を示すSEM画像。
【図5】実施例3で得られた試料の破断面を示すSEM画像。
【図6】比較例1で得られた試料の外観を示す画像。
【図7】比較例1で得られた試料の破断面を示すSEM画像。
【図8】比較例2で得られた試料の破断面を示すSEM画像。
【図9】実施例4で得られた試料の破断面を示すSEM画像。
【発明を実施するための形態】
【0025】
次に、添付の図面を参照しながら本発明の実施の形態についてさらに詳しく説明する。
【0026】
本実施形態の焼結体は、Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなる焼結体であり、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有するものである。
【0027】
本実施形態の焼結体は、基本組成が化学式Li7La3Zr2O12で表わされる焼結体であり、前記Laの一部をSr,Baからなる群から選択される1種の金属に置換してもよく、前記Zrの一部を、Nb,Ta,Sb,Biからなる群から選択される1種の金属に置換してもよい。
【0028】
本実施形態の焼結体は、前記範囲の相対密度を備えるとともに、空隙が前記範囲の最大長を有することにより、優れたリチウムイオン伝導性を得ることができる。
【0029】
本実施形態の焼結体は、例えば次の方法により製造することができる。まず、Li化合物とLa化合物とZr化合物とを、ボールミル、ミキサー等の粉砕・混合機器を用いて粉砕、混合し、得られた混合原料を、大気雰囲気下、850〜950℃の範囲の温度で、5〜7時間の範囲の時間、仮焼する。このとき、前記化学式の前記La又は前記Zrの一部を他の金属で置換した焼結体を得ようとする場合には、Li化合物とLa化合物とZr化合物とに加えて該他の金属を含有する化合物とを混合して混合原料を得る。
【0030】
また、このとき、前記混合原料における混合比の精度を向上するために、Li化合物、La化合物、Zr化合物のそれぞれを別々に脱水等の前処理を行った後に混合することにしてもよく、或いは前処理せずに混合することにしてもよい。
【0031】
前記Li化合物として、例えば、LiOH、水酸化リチウム水和物、Li2CO3、LiNO3、CH3COOLi等を挙げることができる。前記La化合物として、例えば、La2CO3、La(OH)3、La2(CO3)3、La(NO3)3、La(CHCOO)3等を挙げることができる。前記Zr化合物として、例えば、ZrO2、ZrO(NO3)2、ZrO(CHCOO)2、Zr(OH)2CO3・ZrO2を挙げることができる。
【0032】
また、前記化学式の前記Laの一部を置換する金属、又は前記Zrの一部を置換する金属の化合物として、例えば、酸化物、水酸化物,炭酸塩、硝酸塩等を挙げることができる。
【0033】
次に、仮焼した原料を、酸素を含有する雰囲気下、例えば大気雰囲気下で、1000〜1100℃の範囲の温度で、5〜7時間の範囲の時間、一次焼成することにより、Li,La及びZrを含有し、ガーネット型複合金属酸化物からなる粉末を得る。このとき、得られた複合金属酸化物粉末が1〜50μmの範囲の粒径を備えるように、該複合金属酸化物粉末をボールミル、ミキサー等の粉砕機器を用いて粉砕することにしてもよい。
【0034】
次に、得られた前記複合金属酸化物粉末を、放電プラズマ焼結(SPS:Spark Plasma Sintering)により二次焼成する。
【0035】
ここで、前記放電プラズマ焼結を行う放電プラズマ焼結装置について説明する。図1に示す放電プラズマ焼結装置1は、水冷式真空チャンバー2内に、焼結ダイ3と、互いに対向する一対のパンチ4,5と、パンチ4,5を通して電流をパルス印加する電極6,7とを備えており、粉末状の材料を焼結ダイ3に装入し、該材料をパンチ4,5で加圧した状態で、電流をパルス印加することにより、該材料を加熱し、焼成することができる。
【0036】
焼結ダイ3は、電気伝導性材料又は電気絶縁性材料からなるものを使用することができる。前記電気伝導性材料としては、黒鉛、グラッシーカーボン(登録商標)等の炭素材料、モリブデン、タングステン等の高融点金属等が挙げられる。前記電気絶縁材料としては、アルミナ、ジルコニア等が挙げられる。
【0037】
パンチ4,5は、電気伝導性材料からなり、それぞれ電極6,7に電気的かつ機械的に接続され、加圧機構8により駆動される。電極6,7は、電源9に電気的に接続されている。そして、加圧機構8及び電源9は、制御装置10により制御される。
【0038】
制御装置10は、パンチ4,5の位置を計測する位置計測機構11と、真空チャンバー2内の雰囲気を制御する雰囲気制御機構12と、真空チャンバー2を冷却する冷却機構13と、焼結ダイ3に取り付けられ、焼結ダイ3に装入された材料の温度を計測する熱電対(図示せず)に接続された温度計測機構14とを備えている。
【0039】
雰囲気制御機構12は、真空チャンバー2内の雰囲気を、真空雰囲気、アルゴン雰囲気、又は大気雰囲気とすることができる。真空チャンバー2内の雰囲気は、焼成の際には、焼結ダイ3の酸化を抑制するために、真空雰囲気又はアルゴン雰囲気とすることが好ましい。
【0040】
本実施形態では、放電プラズマ焼結装置1において、まず、前記複合金属酸化物粉末を焼結ダイ3に装入する(複合金属酸化物粉末W)。真空チャンバー2内を10〜100Paの範囲の圧力の真空雰囲気下にする。次に、焼結ダイ3に装入された複合金属酸化物粉末Wを、パンチ4,5で20〜50MPaの範囲の圧力で加圧した状態で、500〜20000Aの範囲の直流電流を200〜400Hzの範囲の周期でパルス印加する。このとき、前記熱電対により計測される温度が800℃以下では10〜100℃/分の範囲の昇温速度で昇温させ、800℃に達した以降は1〜20℃/分の範囲の昇温速度で昇温させる。そして、焼結ダイ3に装入された複合金属酸化物粉末Wを、前記範囲の圧力で加圧した状態で、1100〜1250℃の範囲の焼成温度で5〜30分の範囲の時間保持することにより、二次焼成を行い、焼結体を得る。
【0041】
次に、前記パルス印加及び前記加圧を停止し、冷却機構13により真空チャンバー2を冷却するか、又は自然放冷することにより、得られた焼結体を室温まで冷却することにより、本実施形態の焼結体を得ることができる。
【0042】
本実施形態の製造方法では、前記二次焼成において、前記放電プラズマ焼結を行うことにより、前記複合金属酸化物粉末を自己発熱させて、焼成温度まで急速に昇温することができるとともに、焼成温度での焼成時間を短縮することができる。したがって、本実施形態の製造方法によれば、焼成温度までの昇温時間と、焼成温度での保持時間とを短縮することができる結果、前記複合金属酸化物粉末に含有されるリチウムの揮発を抑制することができる。
【0043】
さらに、本実施形態の製造方法では、前記放電プラズマ焼結による二次焼成において、前記複合金属酸化物粉末に対して、圧力を付与した状態で電流をパルス印加する。この結果、前記電流のパルス印加により、前記複合金属酸化物粉末の粒子間の焼結が促進されるとともに、前記圧力により、該粒子間に存在した空隙を押しつぶすことができ、得られた焼結体の結晶粒界に生じる空隙の数を少なくするか、或いは、該空隙の最大長を小さくすることができる。さらに、前記複合金属酸化物粉末に含有されるリチウムが揮発して気泡が生成した場合であっても、該気泡を前記圧力により押しつぶし、該気泡による前記空隙の数を少なくするか、或いは、前記空隙の最大長を小さくすることができる。
【0044】
また、本実施形態の製造方法において、前記混合原料を一次焼成する際に、Al2O3,Al(OH)3等のAl含有化合物や、SiO2,ケイ酸等のSi含有化合物をを焼結助剤として用いることにより、さらに緻密な焼結体を得ることができる。
【0045】
次に、本発明の実施例を示す。
【0046】
〔実施例1〕
本実施例では、まず、水酸化リチウム一水和物(関東化学株式会社製)を、圧力500Paの真空雰囲気下、350℃の温度で6時間加熱し、脱水処理することにより、水酸化リチウム無水物を得た。また、酸化ランタン(関東化学株式会社製)を、大気雰囲気下、950℃の温度で24時間加熱することにより、脱水及び脱炭酸処理した。
【0047】
次に、得られた水酸化リチウム無水物と、脱水及び脱炭酸された酸化ランタンと、酸化ジルコニウム(関東化学株式会社製)とを、Li:La:Zr=7.7:3:2のモル比となるように調製して、遊星型ボールミル(商品名:premium line P-7、フリッチュジャパン株式会社製)を用いて、360rpmの回転数で3時間粉砕混合し、混合原料を得た。
【0048】
次に、前記混合原料をアルミナ製坩堝に収容し、大気雰囲気下、1050℃の温度で6時間保持して、一次焼成することにより、Li,La及びZrを含有し、ガーネット型複合金属酸化物からなる粉末を得た。
【0049】
前記一次焼成で得られた複合金属酸化物粉末について、X線回折装置(商品名:D8 ADVANCE、Bruker AXS社製)を用いて、X線回折測定を行ったところ、化学式Li7+xLa3Zr2O12+x/2(x=0〜0.3)で表わされ、正方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0050】
次に、得られた複合金属酸化物粉末について、放電プラズマ焼結装置1(商品名SPS−3.20S、SPSシンテックス株式会社製)を用いて、放電プラズマ焼結(SPS:Spark Plasma Sintering)により二次焼成した。まず、得られた複合金属酸化物粉末10gを、内径が20mmの黒鉛製焼結ダイ3に装入し(複合金属酸化物粉末W)、真空チャンバー2内を圧力20Paの真空雰囲気にした。次に、焼結ダイ3に装入された複合金属酸化物粉末Wを、パンチ4,5で20MPaの圧力で加圧した状態で、900〜1000Aの範囲の直流電流をパルス印加することにより、100℃/分の昇温速度で昇温させた。そして、800℃の温度に達した後、焼結ダイ3に装入された複合金属酸化物粉末Wを、前記加圧を継続した状態で、900〜1050Aの範囲の直流電流をパルス印加することにより、5℃/分の昇温速度で昇温させた後、1150℃の温度で10分間保持することにより、二次焼成を行い、焼結体を得た。
【0051】
前記パルス印加は、いずれも、300Hzの周期で、12回連続でパルス印加し2回分の時間休止することを1サイクルとして、繰り返し行った。
【0052】
次に、前記パルス印加及び前記加圧を停止し、自然放冷して、得られた焼結体を室温まで冷却し、本実施例の焼結体を得た。
【0053】
次に、本実施例で得られた焼結体を、ダイヤモンドカッタにて、700〜800μmの範囲の厚さに切断し、シリコンカーバイド製の耐水ペーパにて表面を研磨することにより、厚さ500μmの円盤状試料を作製した。
【0054】
図2に、本実施例で得られた試料の外観を示す画像を示す。図2から、本実施例で得られた試料は、透明性を備えることから、光を透過する性質を備えていることが明らかである。このことから、本実施例で得られた試料は、光を散乱させるような結晶粒界及び空隙が非常に少なく、高度に緻密化されているものと考えられる。
【0055】
次に、本実施例で得られた試料について、乾燥重量及び体積を測定することにより、実測密度を算出した。そして、得られた実測密度を基に、化学式Li7La3Zr2O12で表わされるガーネット型複合金属酸化物の理論密度(5.116g/cm3)に対する相対密度を算出したところ、94%であった。結果を表1に示す。
【0056】
次に、本実施例で得られた試料について、X線回折装置(商品名:D8 ADVANCE、Bruker AXS社製)を用いて、X線回折測定を行ったところ、化学式Li7La3Zr2O12で表わされ、正方晶と立方晶との混晶であるガーネット型構造からなる複合金属酸化物であることが確認できた。
【0057】
次に、本実施例で得られた試料について、次のようにして、リチウムイオン伝導率を求めた。まず、本実施例で得られた試料の両面に、スパッタリング装置(商品名:JFC‐1600 オートファインコータ、日本電子株式会社製)を用いて、Auを300秒間スパッタリングして、該試料の両面に薄膜状電極を作製した。次に、接触抵抗を低減するために、前記薄膜状電極の表面にCuメッシュを貼付した後に、該電極を有する試料を2極セルに装着した。そして、前記2極セルについて、インピーダンス測定器(商品名:1287型、Solartron社製)を用いて、周波数を0.1Hz〜1MHzの範囲、電圧振幅を20mVとしたときの交流抵抗値を測定し、測定値からリチウムイオン電導率を算出したところ、1.0×10−4S/cmであった。結果を表1に示す。
【0058】
次に、本実施例で得られた試料について、メノウ製乳棒を用いて圧砕し、得られた破断面を走査型電子顕微鏡(SEM)にて観察した。得られた画像を図3に示す。図3から、本実施例の試料は、最大長が100nmを超える空隙は存在せず、高度に緻密化されていることが明らかである。
【0059】
〔実施例2〕
本実施例では、一次焼成により得られた複合金属酸化物粉末を、1170℃の温度で10分間保持して、放電プラズマ焼結による二次焼成を行った以外は、実施例1と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0060】
次に、本実施例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、95%であった。結果を表1に示す。
【0061】
次に、本実施例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0062】
次に、本実施例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、1.5×10−4S/cmであった。結果を表1に示す。
【0063】
次に、本実施例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図4に示す。図4から、本実施例の試料は、最大長が100nmを超える空隙は存在せず、高度に緻密化されていることが明らかである。
【0064】
〔実施例3〕
本実施例では、一次焼成により得られた複合金属酸化物粉末を、1200℃の温度で10分間保持して、放電プラズマ焼結による二次焼成を行った以外は、実施例1と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0065】
次に、本実施例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、97%であった。結果を表1に示す。
【0066】
次に、本実施例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0067】
次に、本実施例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、1.3×10−4S/cmであった。結果を表1に示す。
【0068】
次に、本実施例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図5に示す。図5から、本実施例の試料は、最大長が100nmを超える空隙は存在せず、高度に緻密化されていることが明らかである。
【0069】
〔比較例1〕
本比較例では、実施例1と全く同一にして一次焼成を行い、複合金属酸化物粉末を得た。
【0070】
次に、得られた複合金属酸化物粉末について、次のようにして、二次焼成を行った。まず、得られた複合金属酸化物粉末100gのうち10gを、ハンドプレス機の内径20mmのダイに装入し、255MPaの圧力で加圧することにより、予備成形体を作製した。
【0071】
次に、残りの複合金属酸化物粉末90gをアルミナ製坩堝に収容するとともに、該複合金属酸化物粉末に得られた予備成形体を埋入させた。
【0072】
次に、アルミナ製坩堝に収容された複合金属酸化物粉末を、大気雰囲気下、5℃/分の昇温速度で昇温させ、600℃の温度に達した後に1℃/分の昇温速度で昇温させ、1170℃の温度で12時間保持することにより、二次焼成を行い、焼結体を得た。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0073】
図6に、本比較例で得られた試料の外観を示す画像を示す。図6から、本比較例で得られた試料は、白色を呈しており、光を透過する性質を備えていないことが明らかである。このことから、本比較例で得られた試料は、焼結体の結晶粒界に多数の空隙が存在し、緻密化されていないものと考えられる。
【0074】
次に、本比較例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、79%であった。結果を表1に示す。
【0075】
次に、本実施例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、正方晶と立方晶の混晶であるガーネット型構造からなる複合金属酸化物であることが確認できた。
【0076】
次に、本比較例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、1.2×10−5S/cmであった。結果を表1に示す。
【0077】
次に、本比較例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図7に示す。図7から、本比較例の試料は、焼結が不十分で、最大長が100nmを超える空隙が多数存在し、緻密でないことが明らかである。
【0078】
〔比較例2〕
本比較例では、一次焼成により得られた複合金属酸化物粉末を、1170℃の温度で30時間保持して、二次焼成を行った以外は、比較例1と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例1と全く同一にして、試料を作製した。
【0079】
次に、本比較例で得られた試料について、実施例1と全く同一にして、相対密度を算出したところ、90%であった。結果を表1に示す。
【0080】
次に、本比較例で得られた試料について、実施例1と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0081】
次に、本比較例で得られた試料について、実施例1と全く同一にして、リチウムイオン伝導率を求めたところ、7.4×10−5S/cmであった。結果を表1に示す。
【0082】
次に、本比較例で得られた試料について、実施例1と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図8に示す。図8から、本比較例の試料は、結晶粒界に最大長が100nmを超える空隙は存在しないものの、長時間の焼結に伴ってLiが揮発したことにより生成したとみられる気泡状の空隙が結晶粒内に存在し、緻密でないことが明らかである。
【0083】
【表1】

【0084】
表1から、放電プラズマ焼結による二次焼成を行った実施例1〜3の試料は、放電プラズマ焼結を行っていない比較例1,2の試料と比較して、相対密度が大きく、緻密であることが明らかである。また、実施例1〜3の試料は、比較例1,2の試料と比較して、優れたイオン伝導性を備えることが明らかである。
【0085】
〔実施例4〕
本実施例では、Li化合物とLa化合物とZr化合物との混合原料に、焼結助剤として、二酸化ケイ素と水酸化アルミニウムと添加した以外は、実施例2と全く同一にして、一次焼成及び放電プラズマ焼結による二次焼成を行った。二酸化ケイ素及び水酸化アルミニウムは、生成されるLi7La3Zr2O121molに対して、Si及びAlがそれぞれ0.1mol%となるように添加した。
【0086】
次に、本実施例で得られた試料について、実施例2と全く同一にして、相対密度を算出したところ、98%であった。結果を表2に示す。
【0087】
次に、本実施例で得られた試料について、実施例2と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0088】
次に、本実施例で得られた試料について、実施例2と全く同一にして、リチウムイオン伝導率を求めたところ、1.8×10−4S/cmであった。結果を表2に示す。
【0089】
次に、本実施例で得られた試料について、実施例2と全く同一にして、走査型電子顕微鏡にて観察した。得られた画像を図9に示す。図9から、本実施例の試料は、図3の実施例1の試料のSEM画像で観察された結晶粒界とみられる線が消失しており、実施例1と比較して、さらに緻密化されていることが明らかである。
【0090】
〔実施例5〕
本実施例では、一次焼成により得られた粉末状の複合金属酸化物粉末を、1170℃の温度で20分間保持して、放電プラズマ焼結による二次焼成を行った以外は、実施例4と全く同一にして、焼結体を作製した。そして、得られた焼結体から、実施例2と全く同一にして、試料を作製した。
【0091】
次に、本実施例で得られた試料について、実施例2と全く同一にして、相対密度を算出したところ、96%であった。結果を表2に示す。
【0092】
次に、本実施例で得られた試料について、実施例2と全く同一にして、X線回折測定を行ったところ、立方晶のガーネット型構造からなる複合金属酸化物であることが確認できた。
【0093】
次に、本実施例で得られた試料について、実施例2と全く同一にして、リチウムイオン伝導率を求めたところ、2.4×10−4S/cmであった。結果を表2に示す。
【0094】
【表2】

【0095】
表2から、焼結助剤を用いて一次焼成を行った実施例4の試料は、焼結助剤を用いずに一次焼成を行った実施例2の試料と比較して、さらに相対密度が大きく、より優れたイオン伝導性を備えることが明らかである。
【0096】
また、表2から、焼結助剤を用いて一次焼成を行った後、1170℃の温度で20分間二次焼成を行った実施例5の試料は、焼結助剤を用いて一次焼成を行った後、1170℃の温度で10分間二次焼成を行った実施例4の試料と比較して、相対密度が僅かに小さいものの、さらに優れたイオン伝導性を備えることが明らかである。
【特許請求の範囲】
【請求項1】
Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなる焼結体であり、
94〜98%の範囲の相対密度を備えるとともに、
空隙が1nm以上かつ100nm未満の範囲の最大長を有することを特徴とする焼結体。
【請求項2】
請求項1記載の焼結体において、
前記ガーネット型複合金属酸化物は、化学式Li7La3Zr2O12で表わされることを特徴とする焼結体。
【請求項3】
Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなり、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有する焼結体の製造方法であって、
Li化合物とLa化合物とZr化合物とを混合した混合原料を一次焼成し、粉末状の複合金属酸化物粉末を得る工程と、
該複合金属酸化物粉末に対して、放電プラズマ焼結により二次焼成する工程とを備えることを特徴とする焼結体の製造方法。
【請求項4】
請求項3記載の焼結体の製造方法において、
前記混合原料を一次焼成する際に、Al2O3,Al(OH)3,SiO2,ケイ酸からなる群から選択される1種以上の化合物を焼結助剤として用いることを特徴とする焼結体の製造方法。
【請求項1】
Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなる焼結体であり、
94〜98%の範囲の相対密度を備えるとともに、
空隙が1nm以上かつ100nm未満の範囲の最大長を有することを特徴とする焼結体。
【請求項2】
請求項1記載の焼結体において、
前記ガーネット型複合金属酸化物は、化学式Li7La3Zr2O12で表わされることを特徴とする焼結体。
【請求項3】
Li,La及びZrを含有し、リチウムイオン伝導性を備えるガーネット型複合金属酸化物からなり、94〜98%の範囲の相対密度を備えるとともに、空隙が1nm以上かつ100nm未満の範囲の最大長を有する焼結体の製造方法であって、
Li化合物とLa化合物とZr化合物とを混合した混合原料を一次焼成し、粉末状の複合金属酸化物粉末を得る工程と、
該複合金属酸化物粉末に対して、放電プラズマ焼結により二次焼成する工程とを備えることを特徴とする焼結体の製造方法。
【請求項4】
請求項3記載の焼結体の製造方法において、
前記混合原料を一次焼成する際に、Al2O3,Al(OH)3,SiO2,ケイ酸からなる群から選択される1種以上の化合物を焼結助剤として用いることを特徴とする焼結体の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2013−107779(P2013−107779A)
【公開日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願番号】特願2011−251616(P2011−251616)
【出願日】平成23年11月17日(2011.11.17)
【出願人】(000005326)本田技研工業株式会社 (23,863)
【Fターム(参考)】
【公開日】平成25年6月6日(2013.6.6)
【国際特許分類】
【出願日】平成23年11月17日(2011.11.17)
【出願人】(000005326)本田技研工業株式会社 (23,863)
【Fターム(参考)】
[ Back to top ]

