燃料電池用空気極触媒とその製造方法
【課題】金属や窒素を含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有する改質カーボンナノチューブを用いた、燃料電池の空気極触媒を提供する。
【解決手段】カーボンナノチューブからなる燃料電池用空気極触媒であって、該カーボンナノチューブは、側壁に側壁を貫通していてもよい細孔を有し、その細孔は0.1nm〜30nmの範囲の細孔径分布を有し、かつBET比表面積が100〜4,000m2/gである、燃料電池用空気極触媒。
【解決手段】カーボンナノチューブからなる燃料電池用空気極触媒であって、該カーボンナノチューブは、側壁に側壁を貫通していてもよい細孔を有し、その細孔は0.1nm〜30nmの範囲の細孔径分布を有し、かつBET比表面積が100〜4,000m2/gである、燃料電池用空気極触媒。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は燃料電池用空気極触媒とその製造方法に関する。
【背景技術】
【0002】
従来、燃料電池の正極(空気極)触媒として白金が使用されることが多い。一方、代替の非白金触媒として、ポリビニルコバルトフタロシアニン、鉄フタロシアニン、ポルフィリンなどを原料に高温で炭化した含窒素カーボン(カーボンアロイ)が、高い酸素還元特性を持つために注目されている。しかし、カーボンアロイは金属や窒素を含む炭素であり、構造が非常に複雑である。また、FeやCoなどの金属や、窒素ドーピングが活性を支配する因子と考えられているが、酸素還元の活性サイトが何であるのかはわかっていないので、活性サイトをより高密度化、高耐久化するための方針が立たず、その構造制御等が課題となっている。
【0003】
また、他の炭素系非白金触媒の研究では、コバルト/ポリピロール/カーボンという高い酸素還元活性を持つ複合触媒において、Co-N サイトが活性を持つと報告されている(Nature VOL443, 63−66 (2006))。また、炭素担持鉄系触媒の場合は、炭素細孔に固定されたFe-N4 構造が活性をもたらすと報告されている(Science VOL. 324, 71-74 (2009))。一方、カーボンナノチューブ(CNT)を用いた触媒では、N ドープにより電子密度が低くなった隣接の炭素が反応サイトであると説明された(Science VOL.323, 760-764 (2009))。いずれの場合も、活性の出現に窒素が重要な役割を持つと考えられており、触媒の作製プロセスには有毒なアンモニアガスや高価な窒素系金属錯体などが用いられている。
【先行技術文献】
【非特許文献】
【0004】
【非特許文献1】Nature VOL443, 63−66 (2006)
【非特許文献2】Science VOL. 324, 71-74 (2009)
【非特許文献3】Science VOL.323, 760-764 (2009)
【発明の概要】
【発明が解決しようとする課題】
【0005】
従来のカーボンナノチューブは、比表面積が小さく、触媒微粒子との相互作用が弱い等の難点がある。そこで、本発明者は、先般、比表面積が大きく(望ましくはカーボンブラックと同等以上)、触媒微粒子との相互作用が強く、さらには細孔を壁面に有するCNT表面処理法を見出すべく、種々の検討を行ない、そのようなCNTを実現し得る方法を見出した。そして、さらに得られた改質CNTの酸化還元特性を調べたところ、意外にも改質CNT自体が燃料電池の空気極触媒に好適であることを見出した。
【課題を解決するための手段】
【0006】
本発明は、上記の課題を解決するために、以下の発明を提供する。
(1)カーボンナノチューブからなる燃料電池用空気極触媒であって、該カーボンナノチューブは、側壁に側壁を貫通していてもよい細孔を有し、その細孔は0.1nm〜30nmの範囲の細孔径分布を有し、かつBET比表面積が100〜4,000m2/gである、燃料電池用空気極触媒。
(2)カーボンナノチューブが多層カーボンナノチューブである上記(1)に記載の燃料電池用空気極触媒。
(3)上記(1)または(2)に記載の燃料電池用空気極触媒を用いてなる燃料電池。
(4)表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱する燃料電池用空気触媒の製造方法。
(5)金属酸化物が酸化コバルト、酸化鉄、酸化バナジウム、酸化スズまたは酸化ニッケルであり、金属硝酸塩が硝酸コバルト、硝酸鉄、硝酸バナジウム、硝酸スズまたは硝酸ニッケルである、上記(4)に記載の燃料電池用空気極触媒の製造方法。
(6)表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去する請求項4または5に記載の燃料電池用空気極触媒の製造方法。
(7)表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去した後に、さらに不活性ガス中または真空中で、500〜3,000℃の温度で熱処理する上記(6)に記載の燃料電池用空気極触媒の製造方法。
(8)カーボンナノチューブが多層カーボンナノチューブである請求項4〜7のいずれかに記載の燃料電池用空気極触媒の製造方法。
(9)上記(4)〜(8)のいずれかに記載の燃料電池用空気極触媒の製造方法で作製した燃料電池用空気極触媒を用いてなる燃料電池。
【発明の効果】
【0007】
本発明によれば、金属や窒素を故意に含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有する改質CNTを用いた、燃料電池の空気極触媒を提供し得る。すなわち、本発明によれば、従来の空気極触媒に比較して、
1)窒素ドープのためにアンモニアガスなどを使った煩雑なプロセスの必要はなく、安定性が高く、電子伝導性の高い純炭素の触媒を実現し得る。
2)カーボンは通常Pt 触媒の担体として用いられているが、Pt の酸化機能によってカーボンがCO2 となって腐食されるという難点がある。一方、炭素触媒の場合は、Ptなどの金属触媒が存在しないため、高い耐久性を実現し得る。
【0008】
一般に、酸素の酸化還元活性を示す指標として、酸素還元の開始電位が用いられているが、電位が高いほど活性も高いといえる。酸性電解液において、白金 触媒の酸素還元の開始電位は通常0.9V 程度(vs.RHE)であるが、本発明においては、白金等を担持しないで、たとえば0.8V(vs.RHE)以上の値を得ることもできる。
【図面の簡単な説明】
【0009】
【図1】(A)は多層カーボンナノチューブ(MWCNT)にCoO微粒子を担持させた模式図であり、(B)はCoO微粒子が触媒となり、MWCNTを開孔すること示す模式図であり、(C)は前記(B)でMWCNTに生じた開孔にCo3O4微粒子が存在するMWCNT(Co3O4/MWCNT)を示す模式図であり、(D)は前記(C)のCo3O4/MWCNTを酸処理してCo3O4微粒子を除去して得られた有孔(欠陥)MWCNT(DMWCNT)を示す模式図である。
【図2】CoOが酸素(O2)による酸化でCo3O4を生成する酸化反応と、生成したCo3O4が炭素(C)による還元でCoOを生成する還元反応からなる酸化・還元サイクル反応の模式図である。
【図3】(a)はCoO微粒子を担持したMWCNTの透過型電子顕微鏡写真である。(b)は空気雰囲気中加熱処理してCo3O4/MWCNTとした試料の透過型電子顕微鏡写真である。
【図4】実施例1で得られたDMWCNTの透過型電子顕微鏡写真である。
【図5】図4の拡大透過型電子顕微鏡写真である。
【図6】実施例1によるMWCNTとDMWCNTのBET比表面積を示す。
【図7】実施例1によるMWCNTとDMWCNTの細孔分布を示すグラフである。
【図8】白金(Pt)を担持させたDMWCNTの透過型電子顕微鏡写真である。
【図9】実施例2で得られたDMWCNTの透過型電子顕微鏡写真である。
【図10】実施例3で得られたDMWCNTを用いて得られた燃料電池用空気極触媒のLSV特性を示す図である。
【図11】実施例4における燃料電池特性評価の結果を示す図である。
【発明を実施するための形態】
【0010】
本発明の燃料電池用空気極触媒は、表面が改質されたカーボンナノチューブからなり、表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱することにより得られる。本発明において用いられるカーボンナノチューブは、六員環配列構造を主体とする炭素環構造(グラフェン層、グラファイト層)の炭素壁を部分的に侵食した細孔、そして或いは、炭素壁を貫通した細孔を有する。
【0011】
以下に、その製造方法を説明する。本発明においては、表面に金属酸化物または金属硝酸塩微粒子を担持させたカーボンナノチューブを、たとえば酸素または空気中の、酸素を含む雰囲気中で100〜1,000℃程度の温度で加熱する。これにより、金属酸化物の2つの状態、すなわち酸化状態と還元状態がサイクルする金属酸化物とCNTの炭素の固相反応によりCNT表面に細孔(すなわち、欠陥と呼ぶこともできる)を作製するものである。このサイクル反応では、表面に金属酸化物微粒子を担持させたCNT炭素による金属酸化物の還元と酸素による酸化反応が繰り返されて炭素が削られることにより細孔が形成されて、すなわち、金属酸化物が炭素と酸素の反応触媒として作用することによって、表面が改質された新たな物性を持つCNTが得られる。
【0012】
本発明で使用される金属酸化物は、カーボンナノチューブの炭素の酸化反応と、炭素による還元で生成した金属酸化物の酸化反応が繰り返される金属酸化物であればよい。また金属酸化物に容易に変化する金属硝酸塩を用いることもできる。このような金属酸化物としては、酸化コバルト、酸化鉄、酸化バナジウム、酸化スズ、酸化ニッケル等が挙げられるが、酸化コバルトが好ましい。一方、金属硝酸塩としては、硝酸コバルト、硝酸鉄、硝酸バナジウム、硝酸スズ、硝酸ニッケル等が挙げられるが、硝酸コバルトが好ましい。
【0013】
金属酸化物が酸化コバルトの場合の反応模式図を図1に示し、その酸化・還元サイクル反応の反応式を図2に示す。図1(A)は、多層カーボンナノチューブ(MWCNT)にCoO微粒子を担持させた模式図であり、図1(B)はCoO微粒子が触媒となり、MWCNTを開孔すること示す模式図である。
【0014】
図1(C)は、(B)でMWCNTに生じた開孔にCo3O4微粒子が存在するMWCNT(Co3O4/MWCNT)を示し、(D)は、(C)のCo3O4/MWCNTを酸処理してCo3O4微粒子を除去することにより得られた、細孔を有する多層カーボンナノチューブ(DMWCNT)を示している。
【0015】
図2は、金属酸化物微粒子がCoO微粒子であり、CNTに担持させたCoO微粒子表面で起きる、酸素(O2)によるCoOの酸化反応とCNTの炭素(C)によるCo3O4の還元反応からなる酸化・還元サイクル反応を示している。
【0016】
この酸化・還元サイクル反応には、酸素の存在が必要であり、酸素を含む雰囲気中で加熱することにより、目的の反応を進行させることができる。酸素濃度を変えることによって、反応を制御することができ、改質の程度を調整できる。通常は、大気圧下に、空気雰囲気中で反応させればよい。反応温度は、100〜500℃、好ましくは200〜300℃である。反応温度が100℃より低いと反応に長時間を要し実際的でなく、500℃を超えるとCNTの消失が激しくなるので好ましくない。
【0017】
カーボンナノチューブとしては、単層カーボンナノチューブ、二層カーボンナノチューブや多層カーボンナノチューブが知られている。本発明で好適に用いられるCNTは、多層カーボンナノチューブ(MWCNT)であるが、それに限定されるものではない。CNTとして、竹様の節がみられる、いわゆるバンブー型CNTを用いることもできる。カーボンナノチューブは、所望により、これを前処理により精製して用いてもよい。CNTの精製は、熱処理または酸処理により行うことができる。CNTの純度が十分に高い場合には精製は不要であるが、表面のアモルファスカーボン等の炭素屑を除去したいときは、500〜600℃程度で熱処理することが好ましい。この加熱温度は500℃より低いとアモルファスカーボンが除去できず、600℃より高いとCNTが過度に酸化されてしまうおそれがある。
【0018】
また、カーボンナノチューブ製造時に含まれる金属触媒等の不純物を除去したい場合は、酸処理によってこれを除去することができる。酸としては硫酸や硝酸等の金属触媒を溶解する酸を用いることができるが、濃硫酸を使用するとCNTが過度に酸化されるおそれがあるので、濃硝酸に硫酸を混合したものなどを使用することが好ましい。
【0019】
カーボンナノチューブ表面に金属酸化物微粒子を担持させる方法は特に制限されない。例えば、酸化コバルトについては、次の手順に従えばよい。
【0020】
[酸化コバルトの担持]
必要に応じて熱処理及び/または酸処理したCNTに、メタノール、エタノール等の溶剤を加え、超音波洗浄機で分散撹拌する。さらにスターラーで撹拌後、混合溶液に塩化コバルトCoCl2・6H2O水溶液を加える。これに、メタノール、エタノール等の溶剤、1Mのテトラメチルアンモニウムハイドロオキサイド水溶液を加え、混合溶液をスターラーで撹拌し、ろ過し、メタノール、エタノール等の溶剤で洗浄し、約60℃の真空乾燥炉で乾燥させ塩化コバルト担持CNTを得た後、この塩化コバルト担持CNTを空気中、あるいは必要に応じてアルゴン(Ar)等の不活性気体雰囲気下に、100℃から300℃で加熱することにより酸化コバルト(CoO)微粒子を担持したCNTを得ることができる。また、Ar雰囲気下に100〜500℃程度で加熱することにより、酸化コバルトを作製することができる。
【0021】
[硝酸コバルトの担持]
硝酸コバルトCo(NO3)2・6H2Oとメタノール、エタノール等の溶剤を混合撹拌し、溶解させ、CNTを投入し、超音波洗浄機で分散させ、混合分散液を100℃に加熱し溶剤を蒸発させ、乾燥した試料を粉砕することにより硝酸コバルトCo(NO3)2・6H2Oを担持させたCNT粉末を得ることができる。
【0022】
カーボンナノチューブ表面に担持させる金属酸化物および金属硝酸塩微粒子の粒子サイズは特に制限されないが、担持後の粒子サイズは条件にもよるが0.5nm〜数nm程度である。処理条件によるが、酸素を含む雰囲気中で熱処理を行うことで、反応後の粒子サイズは1nm〜数十nm程度である。
【0023】
[細孔(欠陥)の形成]
金属酸化物や金属硝酸塩を担持したカーボンナノチューブを空気中で熱処理することにより細孔(欠陥)を導入することができる。 酸化コバルト、あるいは硝酸コバルトなどを担持したカーボンナノチューブを空気中で電気炉等を用いて比較的低温度で欠陥を導入できる。特に、硝酸コバルトを用いた場合は、200℃程度の低い温度で短時間の処理で、目的の細孔を有するカーボンナノチューブを得ることができる。
【0024】
反応後は、金属酸化物微粒子を酸処理により除去することができる。酸としては硫酸や硝酸等の金属酸化物を溶解する酸を用いることができる。
【0025】
酸処理後に、さらにアルゴン、窒素等の不活性ガス中または真空中で、500〜3,000℃程度の温度で熱処理して、細孔表面に形成された官能基を適宜に除去、制御することにより、燃料電池用空気極触媒にさらに好適な活性点を形成し得る。
【0026】
上記の方法によれば、カーボンナノチューブ骨格の結晶性を維持しながら、CNT表面に多数の欠陥(細孔)を形成することができる。この細孔は、六員環配列構造を主体とする炭素環構造(グラフェン層、グラファイト層)を有するCNTの炭素(壁)が部分的に失われて細孔(欠陥)を生じることにより形成されるものである。更に、この細孔は、CNTの炭素層(側壁)を部分的に、または完全に、貫通して形成されるものである。また、細孔の部分には酸素を含む官能基が形成される。
【0027】
上記の方法は、固体間で起きる固相反応を利用したものであり、細孔(欠陥)を生じさせる部分の制御が容易である。気相反応や液相反応では、CNTの全表面に均一に反応が起こるため制御しにくいが、固相反応を利用する本発明では、酸化物微粒子を担持したCNT表面部(局部)で反応を行うので制御が容易である。
【0028】
すなわち、CNTに担持させる金属酸化物或いは金属硝酸塩の微粒子サイズ、担持密度(濃度)及び反応雰囲気等の制御によって、細孔径、細孔の深さ、細孔の数や密度を変えることができ、様々な性質及び用途を持つDMWCNTを作り出すことができる。例えば、酸化還元サイクル反応の回数を増やすこと(反応時間を長くすること)によってCNTの壁の垂直方向に孔を開けることができ、さらにはその孔を利用して酸化物微粒子をCNTの内壁にも担持させて更に酸化還元サイクル反応を行うことによって内壁にも孔をあけることができる。また、金属酸化微粒子の担持密度を上げて、酸化還元サイクル反応を行えば金属酸化物微粒子と酸素の反応方向がCNTの壁と平行方向に制御され多層カーボンナノチューブ(MWCNT)の薄層化も可能である。
【0029】
本発明に用いられるCNTは、上記のように金属や窒素を含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有するが、製造過程で用いられる金属が残存していてもよく、さらには目的に応じて従来法により少量の金属や窒素を含有させることを制限するものではない。
【0030】
本発明に用いられるCNTは、カーボンナノチューブが側壁に細孔を有し、その細孔は0.1nm〜30nm、好ましくは0.1nm〜10nm、の範囲の細孔径分布を実質的に有する。そして、このカーボンナノチューブは、BET比表面積100〜4,000m2/g、実用的に好ましくは200〜1,500m2/gを有し、未改質のカーボンナノチューブに比して、著しい比表面積の増大をもたらし得る。
【0031】
本発明の燃料電池用空気極触媒は、上記の改質されたCNTを用いて、常法により燃料電池の空気極として使用され得、形状、大きさ等も特に制限されない。たとえば、燃料極を対極として、高分子電解質膜等の電解質を挟んだ構造のセルを形成し、セパレータがそのセルを挟んで配置され、このセルとセパレータが積み重ねられて、セルスタックを構成する。
【実施例】
【0032】
以下、実施例及び比較例を挙げて本発明を具体的に説明するが、これらは単なる例示であって、本発明はこれらに制限されるものではない。
【0033】
実施例1
1)MWCNTの精製前処理
多層カーボンナノチューブ(MWCNT,アルドリッチ(Aldrich)社製)を、500℃で1時間、大気中で加熱して精製した。精製したMWCNTを1g秤量した。秤量したMWCNTを、濃硝酸(和光純薬工業製 硝酸含量69%)を40mLと2M硫酸(和光純薬工業製 硫酸含量97%)を40mLとの混合溶液を蓄えた処理槽に投入した。オイルバスを使用し、処理槽中のMWCNTを含む混合分散液を、120℃で4時間、撹拌しながら沸騰させ加熱した。1時間冷却後、MWCNTを含む混合分散液を、400mLになるように超純水で希釈し、さらに3時間撹拌した。MWCNTを含む混合分散液をろ過して、ろ紙上に残されたMWCNTを、200mLの超純水を使用して2回洗浄し、乾燥させ粉砕した。以下、上記の酸溶液による処理を施した後のMWCNTを、精製前処理済MWCNTとして参照する。
2)酸化コバルトの担持
0.05482gの硝酸コバルト(II)・六水和物Co(NO3)2・6H2O(和光純薬工業製、純度99.5%)と100mLのエタノールをビーカーに入れ、2時間程度撹拌し溶解させた。精製前処理済MWCNT0.1mgを上記の溶液に投入し超音波洗浄機にて15分間処理し分散させた。分散液を100℃に加熱しエタノールを蒸発、乾燥させた試料を粉砕した。得られた粉末をAr雰囲気下、300℃で2時間加熱することによってコバルト酸化物微粒子をCNTに担持させた(CoO/MWCNT)。
3)細孔(欠陥)形成
CoO/MWCNT試料を適量取り、空気雰囲気中、250℃、6時間加熱処理した。加熱処理して得られた試料の透過電子顕微鏡(日立製 H8100)写真を図3に示す。図3からMWCNTの側壁を貫通した細孔ができており、チューブ内に酸化コバルト微粒子が侵入していることが判る。また、MWCNTの側壁を貫通しないで途中で留まっている酸化コバルトも認められる。貫通した、或いは貫通しない細孔の直径は、酸化コバルト微粒子のサイズに大略匹敵しており、0.1nm〜5nm程度である。
XRD分析は、空気中250℃で加熱後酸化コバルトの構造がCoOからCo3O4に変化したことを示した。Co3O4/MWCNT試料を40mLの2M H2SO4に投入し、3時間撹拌して酸処理することによりCo3O4を除去し、細孔を有するカーボンナノチューブ(DMWCNT)を得た。このDMWCNTの透過電子顕微鏡写真を図4に、その拡大図を図5に示す。図4から、カーボンナノチューブの側壁に5nmから10nmの側壁を貫通した細孔が生成していることが明らかである。図5から、カーボンナノチューブの側壁に側壁を貫通しない細孔(グラフェン層が10数層)が生成していることがわかる。また、DMWCNT及びMWCNTについてBET比表面積を測定した。その結果、図6に示す通りMWCNTのBET比表面積は106m2/gであるのに対し、DMWCNTのBET比表面積は152m2/gであった。また、その細孔分布は図7に示した通りに、未処理のMWCNTと比べて、直径が5nm程度の細孔にピークを持つ分布となった。
実施例2
1)MWCNTの精製前処理
多層カーボンナノチューブ(VGCF−X 昭和電工株式会社製)を1g計量し、実施例1と同様に精製前処理を行った。
【0034】
2)硝酸コバルトの担持
硝酸コバルト(II)六水和物(和光純薬工業製 純度99.5%)を0.0551g計量し、200mLビーカーに硝酸コバルトとエタノール100mL、撹拌子を入れてスターラーの上に置き、撹拌した。精製前処理したMWCNTを0.1g計量し、ビーカーに入れ、超音波洗浄機で15分撹拌した。温度100℃に加熱し、エタノールを蒸発させ、真空乾燥した後、乳鉢ですりつぶした。
3)細孔(欠陥)形成
硝酸コバルトを担持したMWCNTを坩堝に入れ、電気炉(KDF−75 デンケン製)に入れた。電気炉を10分で室温から250℃まで昇温し、250℃で25分保持し、10分で250℃から室温まで温度を下げて、Co3O4/MWCNT試料を得た。この試料(細孔MWCNT;DMWCNT)の透過電子顕微鏡写真を図9に示す。酸化物微粒子がDMWCNTのチューブ内に侵入した痕跡がはっきり見える。この痕跡は、カーボンナノチューブの側壁を貫通した細孔であり、細孔の直径は、ほぼ酸化物微粒子の直径に相当している。細孔の直径は、0.1nm〜10nm程度である。更に、酸化物微粒子がDMWCNTの側壁に留まっている場所があることもわかる。また、別の処理条件では、DMWCNTの側壁の厚さが薄くなっている、即ち、MWCNT側壁のグラフェン層を層に平行方向に削られる場合も判明した。
【0035】
100mLビーカーに2M硫酸40mLとCo3O4/MWCNT試料、撹拌子を入れ、超音波洗浄器で、15分間処理、撹拌した。更に4時間撹拌した後、ろ過、超純水洗浄を2回繰り返した。真空乾燥炉(DP33 ヤマト科学製)で温度60℃、気圧0.1MPaで一晩乾燥させた。乾燥後、乳鉢に入れ15分すりつぶした。
【0036】
酸化物微粒子を除去したDMWCNT及び細孔(欠陥)形成をしない精製前処理のみのMWCNTについて比表面積を測定した。その結果、MWCNTは264m2/gであるのに対して、本発明によるDMWCNTは374m2/gであった。
実施例3
カーボンナノチューブとして、気相法炭素繊維(「VGCF-XA」昭和電工株式会社製)を用いた。
(精製)
まず、カーボンナノチューブ1g を焼成装置に投入し、空気の雰囲気下、約500℃の温度で1時間焼成した。これを、濃硝酸40mL と2M 硫酸40mLの混酸に加え、120℃で4 時間還流した。還流後、室温で1 時間攪拌し、さらに超純水を加えて総量を400mLにしたものを3 時間攪拌した。攪拌した後、0.5μm径のPTFE膜でろ過し、超純水400mLで洗浄して、真空乾燥炉で温度60℃、気圧0.1MPa で一晩乾燥した。この乾燥の後、乳鉢ですりつぶすことで、精製したカーボンナノチューブを得た(このプロセスで、アモルファスカーボンやFe 触媒などの不純物を取り除き、また表面官能基が形成されることによって親水性が増し、コバルトの担持に有利と考えられる。)。
(硝酸コバルトの担持)
精製したカーボンナノチューブ0.1g、硝酸コバルト6 水和物0.0551g をエタノール100mLに溶かし、スターラーを回転数300rpm、加熱温度100℃に設定し、エタノールを蒸発させた後、真空乾燥炉で温度60℃、気圧0.1MPa で一晩乾燥した。乾燥した後、乳鉢ですりつぶすことで、硝酸コバルトを坦持したカーボンナノチューブを得た。
(酸化コバルトの形成)
硝酸コバルトを坦持したカーボンナノチューブを焼成装置に投入し、アルゴンガスの雰囲気下、300℃の温度で3 時間焼成することで、脱硝を行い、酸化コバルトを坦持したカーボンナノチューブを得た。
(カーボンナノチューブ上の欠陥の形成)
酸化コバルトを坦持したカーボンナノチューブを焼成装置に投入し、アルゴンガスと酸素ガスの比率が4:1 の雰囲気下、250℃の温度で1 時間焼成することで、カーボンとコバルトが固相反応を起こし、欠陥のあるカーボンナノチューブを得た。
(酸化コバルトの除去)
酸化コバルトがついた欠陥のあるカーボンナノチューブを2M硫酸40mL に溶かし、スターラーで4 時間攪拌する。攪拌した後、0.5μm径のPTFE膜でろ過し、超純水400mLで洗浄して、真空乾燥炉で温度60℃、気圧0.1MPa で一晩乾燥した。この乾燥の後、乳鉢ですりつぶすことで、酸化コバルトを除去した欠陥のあるカーボンナノチューブを得た。
(アルゴン処理)
カーボンナノチューブ(DMWCNT)を電気炉に投入し、アルゴンガスの雰囲気下、900℃の温度で1時間焼成することで、表面官能基の除去を行い、アルゴン処理したDMWCNTを得た。
(テスト電極の作製)
Ar処理後の欠陥のあるカーボンナノチューブを2.5mg秤量し、ナフィオン溶液(ALDRICH社製 5wt%)1mLとエタノール49mLを混合した分散溶液0.5mLに投入した。分散溶液を30分間超音波で攪拌し、カーボンナノチューブを十分に分散させた。事前に鏡面となるまで研磨したGC電極上に、マイクロシリンジを用いて試料溶液を10μL量り取り、GC電極上に滴下した後、室温でエタノールを蒸発させた後、乾燥炉において温度60℃で30分間、乾燥させた。LSV(リニアスイープボルタンメトリ)測定では、電解液に0.1M過塩素酸150mL、カウンターに白金メッシュ、参照電極にAg/AgClを使用した。
(電極のクリーニング及び酸素還元電流の測定)
セルを組み立てた後、溶液中にアルゴンガスを30分間流し、溶存ガスを追い出した。アルゴンガス置換後、CV(サイクリックボルタンメトリ)を-0.3から0.8Vの電位幅で、スキャン速度を50mV/s、サイクル数を20サイクルとしクリーニングを行った。クリーニング後、-0.3Vから0.8Vの電位幅で、スキャン速度を5mV/s、電極の回転数を3000rpmでLSV測定行った。その後、酸素ガスを30分間流し、溶液中に酸素を溶存させた。酸素ガスに置換後、-0.3Vから0.8Vの電位幅で、スキャン速度を5mV/s、電極の回転数を3000rpmでLSV測定行った。
(還元電流のバックグランドの測定)
再び溶液中にアルゴンガスを流し、溶存酸素ガスを追い出す。アルゴンガス置換後、0.05 から0.8V の電位幅で、スキャン速度を5mV/sのLSV測定を3 回行った。
(酸素還元電流の算出)
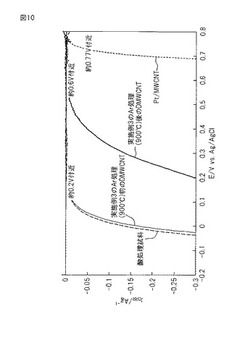
酸素雰囲気下で測定した酸素還元電流からアルゴンガス雰囲気下で測定した還元電流(バックグランド)を引いて、電流を算出した。得られたLSV 特性を図10に示す。
実施例4
(アノード電極作製)
0.9gのPt/C触媒(田中貴金属社製、70wt%)、25mLの純水、5.0gのナフィオン溶液(Aldrich社製、5wt%)、および25mLのイソプロピルアルコールを予備混合した後にスターラーにて1時間撹拌し、アノード触媒スラリーを得た。その後、面積5cm2のカーボンペーパー(東レ株式会社製)上に、アノード触媒スラリーをスプレー方式でPt/C触媒が1mg/cm2になるように均一に塗布し、80℃の真空下で乾燥させた。
(カソード電極作製)
0.3gの実施例3に記載のAr処理後の欠陥のあるカーボンナノチューブ、0.075gのカーボンブラック(Vulcan社製、XC−72)、870μlの純水、及び0.226gのナフィオン溶液(Aldrich社製、5wt%)を予備混合し、混錬器を用いて混錬し、カソード触媒スラリーを得た。その後、面積5cm2のカーボンペーパー(東レ株式会社製)上に、カソード触媒スラリーをバーコーターを用いて、カーボンナノチューブ触媒が2.5mg/cm2なるように均一に塗布し、80℃の真空下で乾燥させた。
(膜−電極接合体(MEA)の作製)
上記のアノード電極とカソード電極及び電解質膜(DuPont社製、Nafion(登録商標)212)を、アノード電極/電解質膜/カソード電極の順番に積層し、プレス装置を用いてこれに140℃で360秒間、0.1MPaの圧力を印加し接合体を得た。
(燃料電池特性評価)
得られたMEAの両側を溝つきセパレータで挟みこみ評価セルを作成し、そのセルを特性評価用燃料電池に組み込んだ。アノード側には純水素ガスを背圧300kPa、流量200mL/minで、カソード側には純酸素ガスを背圧300kPa、流量400mL/minで供給し、運転温度90℃、相対湿度100%で燃料電池を運転し、電池特性評価を行った。得られた結果を図11に示す。図11において、実線は電圧(V)を示し、破線は出力(mW/cm2)を示す。本発明の欠陥のあるカーボンナノチューブを触媒としてカソードに備えた燃料電池は、良好な発電性能を有することがわかった。
【産業上の利用可能性】
【0037】
本発明によれば、金属や窒素を含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有する改質CNTを用いた、燃料電池の空気極触媒を提供し得る。
【技術分野】
【0001】
本発明は燃料電池用空気極触媒とその製造方法に関する。
【背景技術】
【0002】
従来、燃料電池の正極(空気極)触媒として白金が使用されることが多い。一方、代替の非白金触媒として、ポリビニルコバルトフタロシアニン、鉄フタロシアニン、ポルフィリンなどを原料に高温で炭化した含窒素カーボン(カーボンアロイ)が、高い酸素還元特性を持つために注目されている。しかし、カーボンアロイは金属や窒素を含む炭素であり、構造が非常に複雑である。また、FeやCoなどの金属や、窒素ドーピングが活性を支配する因子と考えられているが、酸素還元の活性サイトが何であるのかはわかっていないので、活性サイトをより高密度化、高耐久化するための方針が立たず、その構造制御等が課題となっている。
【0003】
また、他の炭素系非白金触媒の研究では、コバルト/ポリピロール/カーボンという高い酸素還元活性を持つ複合触媒において、Co-N サイトが活性を持つと報告されている(Nature VOL443, 63−66 (2006))。また、炭素担持鉄系触媒の場合は、炭素細孔に固定されたFe-N4 構造が活性をもたらすと報告されている(Science VOL. 324, 71-74 (2009))。一方、カーボンナノチューブ(CNT)を用いた触媒では、N ドープにより電子密度が低くなった隣接の炭素が反応サイトであると説明された(Science VOL.323, 760-764 (2009))。いずれの場合も、活性の出現に窒素が重要な役割を持つと考えられており、触媒の作製プロセスには有毒なアンモニアガスや高価な窒素系金属錯体などが用いられている。
【先行技術文献】
【非特許文献】
【0004】
【非特許文献1】Nature VOL443, 63−66 (2006)
【非特許文献2】Science VOL. 324, 71-74 (2009)
【非特許文献3】Science VOL.323, 760-764 (2009)
【発明の概要】
【発明が解決しようとする課題】
【0005】
従来のカーボンナノチューブは、比表面積が小さく、触媒微粒子との相互作用が弱い等の難点がある。そこで、本発明者は、先般、比表面積が大きく(望ましくはカーボンブラックと同等以上)、触媒微粒子との相互作用が強く、さらには細孔を壁面に有するCNT表面処理法を見出すべく、種々の検討を行ない、そのようなCNTを実現し得る方法を見出した。そして、さらに得られた改質CNTの酸化還元特性を調べたところ、意外にも改質CNT自体が燃料電池の空気極触媒に好適であることを見出した。
【課題を解決するための手段】
【0006】
本発明は、上記の課題を解決するために、以下の発明を提供する。
(1)カーボンナノチューブからなる燃料電池用空気極触媒であって、該カーボンナノチューブは、側壁に側壁を貫通していてもよい細孔を有し、その細孔は0.1nm〜30nmの範囲の細孔径分布を有し、かつBET比表面積が100〜4,000m2/gである、燃料電池用空気極触媒。
(2)カーボンナノチューブが多層カーボンナノチューブである上記(1)に記載の燃料電池用空気極触媒。
(3)上記(1)または(2)に記載の燃料電池用空気極触媒を用いてなる燃料電池。
(4)表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱する燃料電池用空気触媒の製造方法。
(5)金属酸化物が酸化コバルト、酸化鉄、酸化バナジウム、酸化スズまたは酸化ニッケルであり、金属硝酸塩が硝酸コバルト、硝酸鉄、硝酸バナジウム、硝酸スズまたは硝酸ニッケルである、上記(4)に記載の燃料電池用空気極触媒の製造方法。
(6)表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去する請求項4または5に記載の燃料電池用空気極触媒の製造方法。
(7)表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去した後に、さらに不活性ガス中または真空中で、500〜3,000℃の温度で熱処理する上記(6)に記載の燃料電池用空気極触媒の製造方法。
(8)カーボンナノチューブが多層カーボンナノチューブである請求項4〜7のいずれかに記載の燃料電池用空気極触媒の製造方法。
(9)上記(4)〜(8)のいずれかに記載の燃料電池用空気極触媒の製造方法で作製した燃料電池用空気極触媒を用いてなる燃料電池。
【発明の効果】
【0007】
本発明によれば、金属や窒素を故意に含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有する改質CNTを用いた、燃料電池の空気極触媒を提供し得る。すなわち、本発明によれば、従来の空気極触媒に比較して、
1)窒素ドープのためにアンモニアガスなどを使った煩雑なプロセスの必要はなく、安定性が高く、電子伝導性の高い純炭素の触媒を実現し得る。
2)カーボンは通常Pt 触媒の担体として用いられているが、Pt の酸化機能によってカーボンがCO2 となって腐食されるという難点がある。一方、炭素触媒の場合は、Ptなどの金属触媒が存在しないため、高い耐久性を実現し得る。
【0008】
一般に、酸素の酸化還元活性を示す指標として、酸素還元の開始電位が用いられているが、電位が高いほど活性も高いといえる。酸性電解液において、白金 触媒の酸素還元の開始電位は通常0.9V 程度(vs.RHE)であるが、本発明においては、白金等を担持しないで、たとえば0.8V(vs.RHE)以上の値を得ることもできる。
【図面の簡単な説明】
【0009】
【図1】(A)は多層カーボンナノチューブ(MWCNT)にCoO微粒子を担持させた模式図であり、(B)はCoO微粒子が触媒となり、MWCNTを開孔すること示す模式図であり、(C)は前記(B)でMWCNTに生じた開孔にCo3O4微粒子が存在するMWCNT(Co3O4/MWCNT)を示す模式図であり、(D)は前記(C)のCo3O4/MWCNTを酸処理してCo3O4微粒子を除去して得られた有孔(欠陥)MWCNT(DMWCNT)を示す模式図である。
【図2】CoOが酸素(O2)による酸化でCo3O4を生成する酸化反応と、生成したCo3O4が炭素(C)による還元でCoOを生成する還元反応からなる酸化・還元サイクル反応の模式図である。
【図3】(a)はCoO微粒子を担持したMWCNTの透過型電子顕微鏡写真である。(b)は空気雰囲気中加熱処理してCo3O4/MWCNTとした試料の透過型電子顕微鏡写真である。
【図4】実施例1で得られたDMWCNTの透過型電子顕微鏡写真である。
【図5】図4の拡大透過型電子顕微鏡写真である。
【図6】実施例1によるMWCNTとDMWCNTのBET比表面積を示す。
【図7】実施例1によるMWCNTとDMWCNTの細孔分布を示すグラフである。
【図8】白金(Pt)を担持させたDMWCNTの透過型電子顕微鏡写真である。
【図9】実施例2で得られたDMWCNTの透過型電子顕微鏡写真である。
【図10】実施例3で得られたDMWCNTを用いて得られた燃料電池用空気極触媒のLSV特性を示す図である。
【図11】実施例4における燃料電池特性評価の結果を示す図である。
【発明を実施するための形態】
【0010】
本発明の燃料電池用空気極触媒は、表面が改質されたカーボンナノチューブからなり、表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱することにより得られる。本発明において用いられるカーボンナノチューブは、六員環配列構造を主体とする炭素環構造(グラフェン層、グラファイト層)の炭素壁を部分的に侵食した細孔、そして或いは、炭素壁を貫通した細孔を有する。
【0011】
以下に、その製造方法を説明する。本発明においては、表面に金属酸化物または金属硝酸塩微粒子を担持させたカーボンナノチューブを、たとえば酸素または空気中の、酸素を含む雰囲気中で100〜1,000℃程度の温度で加熱する。これにより、金属酸化物の2つの状態、すなわち酸化状態と還元状態がサイクルする金属酸化物とCNTの炭素の固相反応によりCNT表面に細孔(すなわち、欠陥と呼ぶこともできる)を作製するものである。このサイクル反応では、表面に金属酸化物微粒子を担持させたCNT炭素による金属酸化物の還元と酸素による酸化反応が繰り返されて炭素が削られることにより細孔が形成されて、すなわち、金属酸化物が炭素と酸素の反応触媒として作用することによって、表面が改質された新たな物性を持つCNTが得られる。
【0012】
本発明で使用される金属酸化物は、カーボンナノチューブの炭素の酸化反応と、炭素による還元で生成した金属酸化物の酸化反応が繰り返される金属酸化物であればよい。また金属酸化物に容易に変化する金属硝酸塩を用いることもできる。このような金属酸化物としては、酸化コバルト、酸化鉄、酸化バナジウム、酸化スズ、酸化ニッケル等が挙げられるが、酸化コバルトが好ましい。一方、金属硝酸塩としては、硝酸コバルト、硝酸鉄、硝酸バナジウム、硝酸スズ、硝酸ニッケル等が挙げられるが、硝酸コバルトが好ましい。
【0013】
金属酸化物が酸化コバルトの場合の反応模式図を図1に示し、その酸化・還元サイクル反応の反応式を図2に示す。図1(A)は、多層カーボンナノチューブ(MWCNT)にCoO微粒子を担持させた模式図であり、図1(B)はCoO微粒子が触媒となり、MWCNTを開孔すること示す模式図である。
【0014】
図1(C)は、(B)でMWCNTに生じた開孔にCo3O4微粒子が存在するMWCNT(Co3O4/MWCNT)を示し、(D)は、(C)のCo3O4/MWCNTを酸処理してCo3O4微粒子を除去することにより得られた、細孔を有する多層カーボンナノチューブ(DMWCNT)を示している。
【0015】
図2は、金属酸化物微粒子がCoO微粒子であり、CNTに担持させたCoO微粒子表面で起きる、酸素(O2)によるCoOの酸化反応とCNTの炭素(C)によるCo3O4の還元反応からなる酸化・還元サイクル反応を示している。
【0016】
この酸化・還元サイクル反応には、酸素の存在が必要であり、酸素を含む雰囲気中で加熱することにより、目的の反応を進行させることができる。酸素濃度を変えることによって、反応を制御することができ、改質の程度を調整できる。通常は、大気圧下に、空気雰囲気中で反応させればよい。反応温度は、100〜500℃、好ましくは200〜300℃である。反応温度が100℃より低いと反応に長時間を要し実際的でなく、500℃を超えるとCNTの消失が激しくなるので好ましくない。
【0017】
カーボンナノチューブとしては、単層カーボンナノチューブ、二層カーボンナノチューブや多層カーボンナノチューブが知られている。本発明で好適に用いられるCNTは、多層カーボンナノチューブ(MWCNT)であるが、それに限定されるものではない。CNTとして、竹様の節がみられる、いわゆるバンブー型CNTを用いることもできる。カーボンナノチューブは、所望により、これを前処理により精製して用いてもよい。CNTの精製は、熱処理または酸処理により行うことができる。CNTの純度が十分に高い場合には精製は不要であるが、表面のアモルファスカーボン等の炭素屑を除去したいときは、500〜600℃程度で熱処理することが好ましい。この加熱温度は500℃より低いとアモルファスカーボンが除去できず、600℃より高いとCNTが過度に酸化されてしまうおそれがある。
【0018】
また、カーボンナノチューブ製造時に含まれる金属触媒等の不純物を除去したい場合は、酸処理によってこれを除去することができる。酸としては硫酸や硝酸等の金属触媒を溶解する酸を用いることができるが、濃硫酸を使用するとCNTが過度に酸化されるおそれがあるので、濃硝酸に硫酸を混合したものなどを使用することが好ましい。
【0019】
カーボンナノチューブ表面に金属酸化物微粒子を担持させる方法は特に制限されない。例えば、酸化コバルトについては、次の手順に従えばよい。
【0020】
[酸化コバルトの担持]
必要に応じて熱処理及び/または酸処理したCNTに、メタノール、エタノール等の溶剤を加え、超音波洗浄機で分散撹拌する。さらにスターラーで撹拌後、混合溶液に塩化コバルトCoCl2・6H2O水溶液を加える。これに、メタノール、エタノール等の溶剤、1Mのテトラメチルアンモニウムハイドロオキサイド水溶液を加え、混合溶液をスターラーで撹拌し、ろ過し、メタノール、エタノール等の溶剤で洗浄し、約60℃の真空乾燥炉で乾燥させ塩化コバルト担持CNTを得た後、この塩化コバルト担持CNTを空気中、あるいは必要に応じてアルゴン(Ar)等の不活性気体雰囲気下に、100℃から300℃で加熱することにより酸化コバルト(CoO)微粒子を担持したCNTを得ることができる。また、Ar雰囲気下に100〜500℃程度で加熱することにより、酸化コバルトを作製することができる。
【0021】
[硝酸コバルトの担持]
硝酸コバルトCo(NO3)2・6H2Oとメタノール、エタノール等の溶剤を混合撹拌し、溶解させ、CNTを投入し、超音波洗浄機で分散させ、混合分散液を100℃に加熱し溶剤を蒸発させ、乾燥した試料を粉砕することにより硝酸コバルトCo(NO3)2・6H2Oを担持させたCNT粉末を得ることができる。
【0022】
カーボンナノチューブ表面に担持させる金属酸化物および金属硝酸塩微粒子の粒子サイズは特に制限されないが、担持後の粒子サイズは条件にもよるが0.5nm〜数nm程度である。処理条件によるが、酸素を含む雰囲気中で熱処理を行うことで、反応後の粒子サイズは1nm〜数十nm程度である。
【0023】
[細孔(欠陥)の形成]
金属酸化物や金属硝酸塩を担持したカーボンナノチューブを空気中で熱処理することにより細孔(欠陥)を導入することができる。 酸化コバルト、あるいは硝酸コバルトなどを担持したカーボンナノチューブを空気中で電気炉等を用いて比較的低温度で欠陥を導入できる。特に、硝酸コバルトを用いた場合は、200℃程度の低い温度で短時間の処理で、目的の細孔を有するカーボンナノチューブを得ることができる。
【0024】
反応後は、金属酸化物微粒子を酸処理により除去することができる。酸としては硫酸や硝酸等の金属酸化物を溶解する酸を用いることができる。
【0025】
酸処理後に、さらにアルゴン、窒素等の不活性ガス中または真空中で、500〜3,000℃程度の温度で熱処理して、細孔表面に形成された官能基を適宜に除去、制御することにより、燃料電池用空気極触媒にさらに好適な活性点を形成し得る。
【0026】
上記の方法によれば、カーボンナノチューブ骨格の結晶性を維持しながら、CNT表面に多数の欠陥(細孔)を形成することができる。この細孔は、六員環配列構造を主体とする炭素環構造(グラフェン層、グラファイト層)を有するCNTの炭素(壁)が部分的に失われて細孔(欠陥)を生じることにより形成されるものである。更に、この細孔は、CNTの炭素層(側壁)を部分的に、または完全に、貫通して形成されるものである。また、細孔の部分には酸素を含む官能基が形成される。
【0027】
上記の方法は、固体間で起きる固相反応を利用したものであり、細孔(欠陥)を生じさせる部分の制御が容易である。気相反応や液相反応では、CNTの全表面に均一に反応が起こるため制御しにくいが、固相反応を利用する本発明では、酸化物微粒子を担持したCNT表面部(局部)で反応を行うので制御が容易である。
【0028】
すなわち、CNTに担持させる金属酸化物或いは金属硝酸塩の微粒子サイズ、担持密度(濃度)及び反応雰囲気等の制御によって、細孔径、細孔の深さ、細孔の数や密度を変えることができ、様々な性質及び用途を持つDMWCNTを作り出すことができる。例えば、酸化還元サイクル反応の回数を増やすこと(反応時間を長くすること)によってCNTの壁の垂直方向に孔を開けることができ、さらにはその孔を利用して酸化物微粒子をCNTの内壁にも担持させて更に酸化還元サイクル反応を行うことによって内壁にも孔をあけることができる。また、金属酸化微粒子の担持密度を上げて、酸化還元サイクル反応を行えば金属酸化物微粒子と酸素の反応方向がCNTの壁と平行方向に制御され多層カーボンナノチューブ(MWCNT)の薄層化も可能である。
【0029】
本発明に用いられるCNTは、上記のように金属や窒素を含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有するが、製造過程で用いられる金属が残存していてもよく、さらには目的に応じて従来法により少量の金属や窒素を含有させることを制限するものではない。
【0030】
本発明に用いられるCNTは、カーボンナノチューブが側壁に細孔を有し、その細孔は0.1nm〜30nm、好ましくは0.1nm〜10nm、の範囲の細孔径分布を実質的に有する。そして、このカーボンナノチューブは、BET比表面積100〜4,000m2/g、実用的に好ましくは200〜1,500m2/gを有し、未改質のカーボンナノチューブに比して、著しい比表面積の増大をもたらし得る。
【0031】
本発明の燃料電池用空気極触媒は、上記の改質されたCNTを用いて、常法により燃料電池の空気極として使用され得、形状、大きさ等も特に制限されない。たとえば、燃料極を対極として、高分子電解質膜等の電解質を挟んだ構造のセルを形成し、セパレータがそのセルを挟んで配置され、このセルとセパレータが積み重ねられて、セルスタックを構成する。
【実施例】
【0032】
以下、実施例及び比較例を挙げて本発明を具体的に説明するが、これらは単なる例示であって、本発明はこれらに制限されるものではない。
【0033】
実施例1
1)MWCNTの精製前処理
多層カーボンナノチューブ(MWCNT,アルドリッチ(Aldrich)社製)を、500℃で1時間、大気中で加熱して精製した。精製したMWCNTを1g秤量した。秤量したMWCNTを、濃硝酸(和光純薬工業製 硝酸含量69%)を40mLと2M硫酸(和光純薬工業製 硫酸含量97%)を40mLとの混合溶液を蓄えた処理槽に投入した。オイルバスを使用し、処理槽中のMWCNTを含む混合分散液を、120℃で4時間、撹拌しながら沸騰させ加熱した。1時間冷却後、MWCNTを含む混合分散液を、400mLになるように超純水で希釈し、さらに3時間撹拌した。MWCNTを含む混合分散液をろ過して、ろ紙上に残されたMWCNTを、200mLの超純水を使用して2回洗浄し、乾燥させ粉砕した。以下、上記の酸溶液による処理を施した後のMWCNTを、精製前処理済MWCNTとして参照する。
2)酸化コバルトの担持
0.05482gの硝酸コバルト(II)・六水和物Co(NO3)2・6H2O(和光純薬工業製、純度99.5%)と100mLのエタノールをビーカーに入れ、2時間程度撹拌し溶解させた。精製前処理済MWCNT0.1mgを上記の溶液に投入し超音波洗浄機にて15分間処理し分散させた。分散液を100℃に加熱しエタノールを蒸発、乾燥させた試料を粉砕した。得られた粉末をAr雰囲気下、300℃で2時間加熱することによってコバルト酸化物微粒子をCNTに担持させた(CoO/MWCNT)。
3)細孔(欠陥)形成
CoO/MWCNT試料を適量取り、空気雰囲気中、250℃、6時間加熱処理した。加熱処理して得られた試料の透過電子顕微鏡(日立製 H8100)写真を図3に示す。図3からMWCNTの側壁を貫通した細孔ができており、チューブ内に酸化コバルト微粒子が侵入していることが判る。また、MWCNTの側壁を貫通しないで途中で留まっている酸化コバルトも認められる。貫通した、或いは貫通しない細孔の直径は、酸化コバルト微粒子のサイズに大略匹敵しており、0.1nm〜5nm程度である。
XRD分析は、空気中250℃で加熱後酸化コバルトの構造がCoOからCo3O4に変化したことを示した。Co3O4/MWCNT試料を40mLの2M H2SO4に投入し、3時間撹拌して酸処理することによりCo3O4を除去し、細孔を有するカーボンナノチューブ(DMWCNT)を得た。このDMWCNTの透過電子顕微鏡写真を図4に、その拡大図を図5に示す。図4から、カーボンナノチューブの側壁に5nmから10nmの側壁を貫通した細孔が生成していることが明らかである。図5から、カーボンナノチューブの側壁に側壁を貫通しない細孔(グラフェン層が10数層)が生成していることがわかる。また、DMWCNT及びMWCNTについてBET比表面積を測定した。その結果、図6に示す通りMWCNTのBET比表面積は106m2/gであるのに対し、DMWCNTのBET比表面積は152m2/gであった。また、その細孔分布は図7に示した通りに、未処理のMWCNTと比べて、直径が5nm程度の細孔にピークを持つ分布となった。
実施例2
1)MWCNTの精製前処理
多層カーボンナノチューブ(VGCF−X 昭和電工株式会社製)を1g計量し、実施例1と同様に精製前処理を行った。
【0034】
2)硝酸コバルトの担持
硝酸コバルト(II)六水和物(和光純薬工業製 純度99.5%)を0.0551g計量し、200mLビーカーに硝酸コバルトとエタノール100mL、撹拌子を入れてスターラーの上に置き、撹拌した。精製前処理したMWCNTを0.1g計量し、ビーカーに入れ、超音波洗浄機で15分撹拌した。温度100℃に加熱し、エタノールを蒸発させ、真空乾燥した後、乳鉢ですりつぶした。
3)細孔(欠陥)形成
硝酸コバルトを担持したMWCNTを坩堝に入れ、電気炉(KDF−75 デンケン製)に入れた。電気炉を10分で室温から250℃まで昇温し、250℃で25分保持し、10分で250℃から室温まで温度を下げて、Co3O4/MWCNT試料を得た。この試料(細孔MWCNT;DMWCNT)の透過電子顕微鏡写真を図9に示す。酸化物微粒子がDMWCNTのチューブ内に侵入した痕跡がはっきり見える。この痕跡は、カーボンナノチューブの側壁を貫通した細孔であり、細孔の直径は、ほぼ酸化物微粒子の直径に相当している。細孔の直径は、0.1nm〜10nm程度である。更に、酸化物微粒子がDMWCNTの側壁に留まっている場所があることもわかる。また、別の処理条件では、DMWCNTの側壁の厚さが薄くなっている、即ち、MWCNT側壁のグラフェン層を層に平行方向に削られる場合も判明した。
【0035】
100mLビーカーに2M硫酸40mLとCo3O4/MWCNT試料、撹拌子を入れ、超音波洗浄器で、15分間処理、撹拌した。更に4時間撹拌した後、ろ過、超純水洗浄を2回繰り返した。真空乾燥炉(DP33 ヤマト科学製)で温度60℃、気圧0.1MPaで一晩乾燥させた。乾燥後、乳鉢に入れ15分すりつぶした。
【0036】
酸化物微粒子を除去したDMWCNT及び細孔(欠陥)形成をしない精製前処理のみのMWCNTについて比表面積を測定した。その結果、MWCNTは264m2/gであるのに対して、本発明によるDMWCNTは374m2/gであった。
実施例3
カーボンナノチューブとして、気相法炭素繊維(「VGCF-XA」昭和電工株式会社製)を用いた。
(精製)
まず、カーボンナノチューブ1g を焼成装置に投入し、空気の雰囲気下、約500℃の温度で1時間焼成した。これを、濃硝酸40mL と2M 硫酸40mLの混酸に加え、120℃で4 時間還流した。還流後、室温で1 時間攪拌し、さらに超純水を加えて総量を400mLにしたものを3 時間攪拌した。攪拌した後、0.5μm径のPTFE膜でろ過し、超純水400mLで洗浄して、真空乾燥炉で温度60℃、気圧0.1MPa で一晩乾燥した。この乾燥の後、乳鉢ですりつぶすことで、精製したカーボンナノチューブを得た(このプロセスで、アモルファスカーボンやFe 触媒などの不純物を取り除き、また表面官能基が形成されることによって親水性が増し、コバルトの担持に有利と考えられる。)。
(硝酸コバルトの担持)
精製したカーボンナノチューブ0.1g、硝酸コバルト6 水和物0.0551g をエタノール100mLに溶かし、スターラーを回転数300rpm、加熱温度100℃に設定し、エタノールを蒸発させた後、真空乾燥炉で温度60℃、気圧0.1MPa で一晩乾燥した。乾燥した後、乳鉢ですりつぶすことで、硝酸コバルトを坦持したカーボンナノチューブを得た。
(酸化コバルトの形成)
硝酸コバルトを坦持したカーボンナノチューブを焼成装置に投入し、アルゴンガスの雰囲気下、300℃の温度で3 時間焼成することで、脱硝を行い、酸化コバルトを坦持したカーボンナノチューブを得た。
(カーボンナノチューブ上の欠陥の形成)
酸化コバルトを坦持したカーボンナノチューブを焼成装置に投入し、アルゴンガスと酸素ガスの比率が4:1 の雰囲気下、250℃の温度で1 時間焼成することで、カーボンとコバルトが固相反応を起こし、欠陥のあるカーボンナノチューブを得た。
(酸化コバルトの除去)
酸化コバルトがついた欠陥のあるカーボンナノチューブを2M硫酸40mL に溶かし、スターラーで4 時間攪拌する。攪拌した後、0.5μm径のPTFE膜でろ過し、超純水400mLで洗浄して、真空乾燥炉で温度60℃、気圧0.1MPa で一晩乾燥した。この乾燥の後、乳鉢ですりつぶすことで、酸化コバルトを除去した欠陥のあるカーボンナノチューブを得た。
(アルゴン処理)
カーボンナノチューブ(DMWCNT)を電気炉に投入し、アルゴンガスの雰囲気下、900℃の温度で1時間焼成することで、表面官能基の除去を行い、アルゴン処理したDMWCNTを得た。
(テスト電極の作製)
Ar処理後の欠陥のあるカーボンナノチューブを2.5mg秤量し、ナフィオン溶液(ALDRICH社製 5wt%)1mLとエタノール49mLを混合した分散溶液0.5mLに投入した。分散溶液を30分間超音波で攪拌し、カーボンナノチューブを十分に分散させた。事前に鏡面となるまで研磨したGC電極上に、マイクロシリンジを用いて試料溶液を10μL量り取り、GC電極上に滴下した後、室温でエタノールを蒸発させた後、乾燥炉において温度60℃で30分間、乾燥させた。LSV(リニアスイープボルタンメトリ)測定では、電解液に0.1M過塩素酸150mL、カウンターに白金メッシュ、参照電極にAg/AgClを使用した。
(電極のクリーニング及び酸素還元電流の測定)
セルを組み立てた後、溶液中にアルゴンガスを30分間流し、溶存ガスを追い出した。アルゴンガス置換後、CV(サイクリックボルタンメトリ)を-0.3から0.8Vの電位幅で、スキャン速度を50mV/s、サイクル数を20サイクルとしクリーニングを行った。クリーニング後、-0.3Vから0.8Vの電位幅で、スキャン速度を5mV/s、電極の回転数を3000rpmでLSV測定行った。その後、酸素ガスを30分間流し、溶液中に酸素を溶存させた。酸素ガスに置換後、-0.3Vから0.8Vの電位幅で、スキャン速度を5mV/s、電極の回転数を3000rpmでLSV測定行った。
(還元電流のバックグランドの測定)
再び溶液中にアルゴンガスを流し、溶存酸素ガスを追い出す。アルゴンガス置換後、0.05 から0.8V の電位幅で、スキャン速度を5mV/sのLSV測定を3 回行った。
(酸素還元電流の算出)
酸素雰囲気下で測定した酸素還元電流からアルゴンガス雰囲気下で測定した還元電流(バックグランド)を引いて、電流を算出した。得られたLSV 特性を図10に示す。
実施例4
(アノード電極作製)
0.9gのPt/C触媒(田中貴金属社製、70wt%)、25mLの純水、5.0gのナフィオン溶液(Aldrich社製、5wt%)、および25mLのイソプロピルアルコールを予備混合した後にスターラーにて1時間撹拌し、アノード触媒スラリーを得た。その後、面積5cm2のカーボンペーパー(東レ株式会社製)上に、アノード触媒スラリーをスプレー方式でPt/C触媒が1mg/cm2になるように均一に塗布し、80℃の真空下で乾燥させた。
(カソード電極作製)
0.3gの実施例3に記載のAr処理後の欠陥のあるカーボンナノチューブ、0.075gのカーボンブラック(Vulcan社製、XC−72)、870μlの純水、及び0.226gのナフィオン溶液(Aldrich社製、5wt%)を予備混合し、混錬器を用いて混錬し、カソード触媒スラリーを得た。その後、面積5cm2のカーボンペーパー(東レ株式会社製)上に、カソード触媒スラリーをバーコーターを用いて、カーボンナノチューブ触媒が2.5mg/cm2なるように均一に塗布し、80℃の真空下で乾燥させた。
(膜−電極接合体(MEA)の作製)
上記のアノード電極とカソード電極及び電解質膜(DuPont社製、Nafion(登録商標)212)を、アノード電極/電解質膜/カソード電極の順番に積層し、プレス装置を用いてこれに140℃で360秒間、0.1MPaの圧力を印加し接合体を得た。
(燃料電池特性評価)
得られたMEAの両側を溝つきセパレータで挟みこみ評価セルを作成し、そのセルを特性評価用燃料電池に組み込んだ。アノード側には純水素ガスを背圧300kPa、流量200mL/minで、カソード側には純酸素ガスを背圧300kPa、流量400mL/minで供給し、運転温度90℃、相対湿度100%で燃料電池を運転し、電池特性評価を行った。得られた結果を図11に示す。図11において、実線は電圧(V)を示し、破線は出力(mW/cm2)を示す。本発明の欠陥のあるカーボンナノチューブを触媒としてカソードに備えた燃料電池は、良好な発電性能を有することがわかった。
【産業上の利用可能性】
【0037】
本発明によれば、金属や窒素を含有させないでも、従来の「カーボンアロイ触媒」と同程度の酸化還元活性を有する改質CNTを用いた、燃料電池の空気極触媒を提供し得る。
【特許請求の範囲】
【請求項1】
カーボンナノチューブからなる燃料電池用空気極触媒であって、該カーボンナノチューブは、側壁に側壁を貫通していてもよい細孔を有し、その細孔は0.1nm〜30nmの範囲の細孔径分布を有し、かつBET比表面積が100〜4,000m2/gである、燃料電池用空気極触媒。
【請求項2】
カーボンナノチューブが多層カーボンナノチューブである請求項1に記載の燃料電池用空気極触媒。
【請求項3】
請求項1または2に記載の燃料電池用空気極触媒を用いてなる燃料電池。
【請求項4】
表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱する燃料電池用空気触媒の製造方法。
【請求項5】
金属酸化物が酸化コバルト、酸化鉄、酸化バナジウム、酸化スズまたは酸化ニッケルであり、金属硝酸塩が硝酸コバルト、硝酸鉄、硝酸バナジウム、硝酸スズまたは硝酸ニッケルである、請求項4に記載の燃料電池用空気極触媒の製造方法。
【請求項6】
表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去する請求項4または5に記載の燃料電池用空気極触媒の製造方法。
【請求項7】
表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去した後に、さらに不活性ガス中または真空中で、500〜3,000℃の温度で熱処理する請求項6に記載の燃料電池用空気極触媒の製造方法。
【請求項8】
カーボンナノチューブが多層カーボンナノチューブである請求項4〜7のいずれか1項に記載の燃料電池用空気極触媒の製造方法。
【請求項9】
請求項4〜8のいずれか1項に記載の燃料電池用空気極触媒の製造方法で作製した燃料電池用空気極触媒を用いてなる燃料電池。
【請求項1】
カーボンナノチューブからなる燃料電池用空気極触媒であって、該カーボンナノチューブは、側壁に側壁を貫通していてもよい細孔を有し、その細孔は0.1nm〜30nmの範囲の細孔径分布を有し、かつBET比表面積が100〜4,000m2/gである、燃料電池用空気極触媒。
【請求項2】
カーボンナノチューブが多層カーボンナノチューブである請求項1に記載の燃料電池用空気極触媒。
【請求項3】
請求項1または2に記載の燃料電池用空気極触媒を用いてなる燃料電池。
【請求項4】
表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱する燃料電池用空気触媒の製造方法。
【請求項5】
金属酸化物が酸化コバルト、酸化鉄、酸化バナジウム、酸化スズまたは酸化ニッケルであり、金属硝酸塩が硝酸コバルト、硝酸鉄、硝酸バナジウム、硝酸スズまたは硝酸ニッケルである、請求項4に記載の燃料電池用空気極触媒の製造方法。
【請求項6】
表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去する請求項4または5に記載の燃料電池用空気極触媒の製造方法。
【請求項7】
表面に金属酸化物又は金属硝酸塩の微粒子を担持させたカーボンナノチューブを、酸素を含む雰囲気中で100〜1,000℃の温度で加熱した後に、金属酸化物微粒子を酸処理により除去した後に、さらに不活性ガス中または真空中で、500〜3,000℃の温度で熱処理する請求項6に記載の燃料電池用空気極触媒の製造方法。
【請求項8】
カーボンナノチューブが多層カーボンナノチューブである請求項4〜7のいずれか1項に記載の燃料電池用空気極触媒の製造方法。
【請求項9】
請求項4〜8のいずれか1項に記載の燃料電池用空気極触媒の製造方法で作製した燃料電池用空気極触媒を用いてなる燃料電池。
【図1】


【図2】


【図6】


【図7】


【図10】


【図11】


【図3】


【図4】


【図5】


【図8】


【図9】




【図2】


【図6】


【図7】


【図10】


【図11】


【図3】


【図4】


【図5】


【図8】


【図9】


【公開番号】特開2012−164492(P2012−164492A)
【公開日】平成24年8月30日(2012.8.30)
【国際特許分類】
【出願番号】特願2011−23361(P2011−23361)
【出願日】平成23年2月4日(2011.2.4)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【出願人】(000002004)昭和電工株式会社 (3,251)
【Fターム(参考)】
【公開日】平成24年8月30日(2012.8.30)
【国際特許分類】
【出願日】平成23年2月4日(2011.2.4)
【出願人】(304021417)国立大学法人東京工業大学 (1,821)
【出願人】(000002004)昭和電工株式会社 (3,251)
【Fターム(参考)】
[ Back to top ]

